Vládní návrh zákona, kterým se mění zákon č. 378/2007 Sb., o léčivech a o změnách některých souvisejících zákonů (zákon o léčivech), ve znění pozdějších předpisů, a zákon č. 372/2011 Sb., o zdravotních službách a podmínkách jejich poskytování (zákon o zdravotních službách), ve znění pozdějších předpisů
262/0
Xxxxx
XXXXX
xx dne … 2018,
xxxxxx xx xxxx xxxxx č. 378/2007 Sb., o xxxxxxxx x x xxxxxxx xxxxxxxxx xxxxxxxxxxxxx xxxxxx (xxxxx x xxxxxxxx), ve xxxxx xxxxxxxxxx předpisů, x xxxxx č. 372/2011 Sb., o xxxxxxxxxxx xxxxxxxx x xxxxxxxxxx xxxxxx xxxxxxxxxxx (xxxxx x xxxxxxxxxxx xxxxxxxx), xx xxxxx xxxxxxxxxx xxxxxxxx
Xxxxxxxxx xx xxxxxx xx xxxxx xxxxxx České xxxxxxxxx:
XXXX PRVNÍ
Změna xxxxxx x xxxxxxxx
Čl. X
Xxxxx č. 378/2007 Sb., x xxxxxxxx x x xxxxxxx xxxxxxxxx xxxxxxxxxxxxx xxxxxx (xxxxx x xxxxxxxx), xx xxxxx xxxxxx x. 124/2008 Sb., xxxxxx x. 296/2008 Xx., xxxxxx x. 141/2009 Xx., xxxxxx x. 281/2009 Xx., zákona x. 291/2009 Sb., xxxxxx č. 75/2011 Xx., zákona x. 375/2011 Xx., xxxxxx x. 50/2013 Xx., xxxxxx č. 70/2013 Xx., xxxxxx x. 250/2014 Xx., xxxxxx x. 80/2015 Xx., xxxxxx č. 243/2016 Xx., xxxxxx č. 65/2017 Xx., xxxxxx x. 66/2017 Xx., xxxxxx č. 183/2017 Xx., xxxxxx x. 251/2017 Xx. x xxxxxx č. 36/2018 Xx., se xxxx xxxxx:
1. Xx xxxxx xxxxxxxx xxx xxxxx x. 2 se xx xxxxxxxxxx xxxxx xxxxxxxx xxxx „Xxxxxxxx Xxxxxx x xxxxxxxxx xxxxxxxxx (EU) 2016/161 xx dne 2. xxxxx 2015, xxxxxx xx xxxxxxxx xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Xxxx 2001/83/XX stanovením xxxxxxxxxx pravidel pro xxxxxxxx xxxxx xxxxxxx xx xxxxx humánních xxxxxxxx přípravků.“.
2. X §5 xxxxxxxx 7 xxx:
„(7) Xxxxxxxx vyhrazených xxxxxxxxx xxxxxxxx xxxxxxxxx xx xxxxxx jejich nákup, xxxxxxxxxx xxxx xxxxxx. Xxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx xx xxxxxx xxxxxx xxxxx, xxxxxxxxxx nebo xxxxxx xxxxxxxxx spotřebiteli.“.
3. X §6 xx xx xxxxx xxxxxxxx 2 doplňuje xxxx „X případě xxxxxxxxx a xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx xx xxxxxxxx xxxxxxx xxxxxxx xxxxx použijí xxxxxxx xx dovoz ze xxxxxxx xxxx.“.
XXXXX: 32017L1572
4. X §13 xxxx. 2 xx xx xxxxx textu xxxxxxx g) xxxxxxxx xxxxx „x xxxxx xxxxxxxxxxxx xxxxxxxx Xxxxxxxx xxxx upravujících oblast xxxxxxxxx xxxxx“.
5. X §13 xx xx xxxxx xxxxxxxx 2 xxxxx xxxxxxxxx xxxxxx x xxxxxxxx xx xxxxxxx x), xxxxx včetně xxxxxxxx xxx xxxxx x. 106 zní:
„o) xx xxxxxxxxxx xxxxxxx Xxxxx republiky xxx xxxxxx xxxxxx úkolů x xxxxxxx xxxxxxxxxx xxxxxxxx pro xxxxxxxx xxxxx xxxxxxx na xxxxx xxxxxxxx xxxxxxxxx, xxxxxxxx xxxxxxxx dodržování xxxxxxxxxx stanovených xxxxx xxxxxxxxxxx předpisem Evropské xxxx xxxxxxxxxxx podrobná xxxxxxxx xxx ochranné xxxxx xxxxxxx xx xxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx106) (xxxx xxx „xxxxxxxx x xxxxxxxxxx xxxxxxx“), xx xxxxxxx xx xxxxxxx úložišť x k xxxxxxxxxx x xxxx xxxxxxxxx x xxxxxxx s xx. 39 xxxxxxxx x xxxxxxxxxx prvcích, x xxxxxxxx xxxxxxxx xxxxxxxxx xxxxxx systému, xxxxxxx x xxxxxxxxxxx xxxxxx xxxxxxxx x xxxxxxxx přípravků a xxxxxx xxxxxxxx x xxxxxx xxxxxxxx a xxxxxx x xxxx xxxxxxx xxxxxxxxx Xxxxxx.
XXXXX: 32016R0161
6. X §13 xx xx konci xxxxxxxx 2 xxxxx xxxxxxxxx xxxxxx a xxxxxxxx xx písmena x) x x), xxxxx včetně xxxxxxxx xxx čarou č. 107 x 108 xxxxx:
x) je xxxxxxxxxx xxxxxxx Xxxxx republiky xxx plnění xxxxx xxxxxxxxxxx xxxxx xxxxxxxxxxx xxxxxxxxx Xxxxxxxx unie, xxxxxx se xxxxxxx xxxxxx a pokyny xxx správnou xxxxxxx xxxxx xxx xxxxxxxxx xxxxxx přípravky107) (dále xxx „xxxxxxxx o xxxxxxx výrobní xxxxx xxx hodnocené léčivé xxxxxxxxx“) x xxxxx xxxxxxxxxxx předpisem Xxxxxxxx xxxx, xxxxxx xx xxxxxxx xxxxxxxx provádění xxxxxxxxxxx xxxxxxx xxxxxxx xxxxxxxx praxe108) (xxxx xxx „nařízení x xxxxxxxxx inspekčních postupů xxxxxxx xxxxxxxx xxxxx“),
x) xx xxxxxxxxxx xxxxxxx Xxxxx xxxxxxxxx pro xxxxxxxx povolení x xxxxxx x dovozu xxxxxxxxxxx léčivých přípravků xxxxx xxxxxxxx x xxxxxxxxx hodnocení.
CELEX: 32017R1569, 32017R0556, 32014R0536
7. V §13 xxxx. 3 xxxxxxx x) zní:
„l) xxxxxx x xxxxxxx xxxxxx xxxxxxx, který xxxxxxxxx
1. xxxxxx xxxxxxx x xxxxxxxxxxx x odborné xxxxxxxx xxxxxxxxxxx Ústavu, xxxxx xxxxxxx xxxxxxxxx x xxxxxxxx x xxxxxxxxx xxxxx tohoto xxxxxx nebo xxxxx xxxxxxxxxxxx předpisu Xxxxxxxx xxxx, xxxxxx xxxxxx xxxx xxxxxxxxxx, xxxxxxxxxxxx x požadavků xx xxxxxxxx xxxxxxxx,
2. dodržování xxxxxxxx xxxxxxxxxxx xxxxxxx xxxxxxx klinické xxxxx x xxxxxxx s xxxxxxxxx x provádění xxxxxxxxxxx xxxxxxx xxxxxxx xxxxxxxx praxe,
3. xxxxx xxxxxxxxx kontrol dodržování xxxxxx xxxxxx x xxxxxxxxxxx předpisů Xxxxxxxx xxxx x výrobců xxxxxxxxx xxxxxxxx přípravků xxxxxx xxxxxxxxxxx léčivých xxxxxxxxx,“.
XXXXX: 32017L1572, 32017R1569, 32017R0556
8. X §16 xxxx. 3 xxxx. x) xx xxxxx „xxxxxxx“ xxxxxxxxx xxxxxx „xxxxxxx“.
9. X §22 xxxx. 2 xx xx xxxxx „xxxxxxxxx“ xxxxxxxx slova „veterinárních xxxxxxxx xxxxxxxxx“.
10. X §23 xx xx konci xxxxxxxx 1 xxxxx xxxxxxxxx xxxxxx x xxxxxxxx xx písmena x) xx x), xxxxx xxxxx:
„x) xxxxxxxxxx xxxxxxx Xxxxxx, xxx-xx x xxxxxxx léčivý xxxxxxxxx, podezření xx xxxxxxxx xxxxxx xxxxxxxxx, xxxxxxxxx-xx xxxx jeho xxxxxxxxx z nařízení x xxxxxxxxxx prvcích,
g) xxxxxxxxxx Ústavu xxxxxxxxxx xxx xxxxxxxxx skutečností xxxxxxxxxxxxx s xxxxxxxxxx xx padělání xxxxxxxx xxxxxxxxx,
x) neprodleně xxxxxxx Xxxxxxxxxxxxx ústavu xxxxxxxxx xx xxxxxxxx xxxxxxxxxxx xxxxxx xxxxxxxxx.“.
11. X §24 xxxx. 10 se xxxxx „xxxx xxxxxxxxx“ xxxxxxx.
12. X §34 xx xxxxxxxx odstavec 9, xxxxx xxx:
„(9) Xxxxx xxxx Xxxxxxxxxxx xxxxx neprodleně xxxxxx xxxxxx x moci xxxxxx x xxxxx xxxxxxxxxx xxxxxxxx přípravku xxxxxxxxxx mezi vyhrazené xxxxxx přípravky x xxxxxxx xxxxxx xxxxxxxxxxx xxxxxxxxxx xx xxxxxxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx.“.
13. X §37 xxxx. 1 se xx slova „xxxxxxxxxxxx xxxxxxxx xxxxxxxxx,“ xxxxxxxx xxxxx „nejde-li x xxxxxxxxx identifikátor,“, xxxxx „xxxxxxxxx xxxxxxxx xxxxx (XXX)“ se xxxxxxxxx xxxxx „xxxxxxxxxxx xxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxxx“, xx xxxxx „xxxxxxxxxx“ xx xxxxxxxx slova „x xxxxxxxx požadavkům standardního xxxxxxxxxx xxxxxxx“ x xx xxxx xxxxx xx vkládá xxxx „Xx xxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx xxxx xxx xxxxxx kód xxxxxxxxx xxxxx §32 xxxx. 5.“.
14. X §37 xxxx. 7 xxxx xxxxx se xx xxxxx „xxxxxxxx xxxxx“ xxxxxxxx slova „podle xxxxxxxx o xxxxxxxxxx xxxxxxx“, xx xxxxx xxxxx věty xx xxxxxxxx slova „(xxxx xxx „xxxxxxxx prvky“)“ x věta xxxxxxxx xx nahrazuje xxxxx „Xxxxxx x technické xxxxxxxxxx ochranných prvků xxxxxxx nařízení o xxxxxxxxxx xxxxxxx.“.
XXXXX: 32016R0161
15. X §37 xxxxxxxx 8 xxx:
„(8) Xxxxxxxxxx prvky podle xxxxxxxx 7 xxxx xxx xxxxxxxx xxxxxxx xxxxxx přípravky vydávané xxxxx na xxxxxxxx xxxxxxx nebo xx xxxxxxxx xxxxxxx s xxxxxxxx, xxxxx xxxxxx xxxxxxx na xxxxxxx xxxxxxxx xxxxxxxxx, xxxxx xxxxx být xxxxxxxx xxxxxxxxxx xxxxx, xxxxxxxxx xxxxxxxx X xxxxxxxx x xxxxxxxxxx prvcích. Xxxxxxxxxx xxxxx xxxxx xxxxxxxx 7 xxxxxxx xxx xxxxxxxx xxxxxxx xxxxxx xxxxxxxxx, xxxxx xxx xxxxxxx bez xxxxxxxxxx předpisu x xxxxx xxxxxx uvedeny xx xxxxxxx xxxxxxxxxx xxxxxx přípravky, xxxxx xxxx být xxxxxxxx xxxxxxxxxx xxxxx, stanovené x příloze II xxxxxxxx x xxxxxxxxxx xxxxxxx.“.
XXXXX: 32016R0161
16. X §45 xx na xxxxx xxxxxxxx 7 tečka xxxxxxxxx xxxxxx a xxxxxxxx xx písmeno x), xxxxx zní:
„f) xxx xxxxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx vyřadit xxxxxxxxx xxxxxxxxx xxxxxxxxxxxxx x xxxxxxx nový xxxxxxxxx xxxxxxxxxxxxx xxxxxxxx xxxxx xxxxxxxx x xxxxxxxxxx xxxxxxx.“.
XXXXX: 32016R0161
17. X §64 xxxxxxx x) zní:
„d) xxxxxxxx a xxxxxxxx xxxxxx xxxxxxxx xxxxxxx x xxxxxxxxxx podmínky xxx xxxxxxx xxxxxx xxxxxxxx xxxxxxx tak, xxx tento xxxxx, xxxxx xx x xxxxxxxxx osoby xxxxxxx x xxxxxxx x), xxx nezávislý na xxxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxx xxxxxxxx přípravků,“.
CELEX: 32017L1572
18. X §64 xxxx. x) xx xx xxxxx „xxxxxxxx“ xxxxxxxx xxxxx „xxxxxxx x“ x xxxxx „x xxxxxxxx“ xx xxxxxxxxx slovy „, xxxxxxxx x xxxxxxxx xxxxxxxxxx x registraci, x xxxxx též, xxxxx je to xxxxx, xxxx, pro xxxxx byl xxxxxx xxxxxxxxx xxxxx; x xxxxxxx xxxxxx hodnocených xxxxxxxxx xxxxxxxx přípravků xx xxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxx x xxxxxxx xxxxxxx xxxxx xxx xxxxxxxxx xxxxxx xxxxxxxxx“.
XXXXX: 32017L1572
19. V §64 xxxx. j) se xxxxx „xxxxxxxxx činnost x xxxxxxx x xxxxxxxxx x výrobě, xxxxxxxxx xxxxxxxx správné xxxxxxx praxe“ nahrazují xxxxx „provádět xxxxxxx xxxxxxxx v souladu x xxxxxxxx správné xxxxxxx xxxxx, x xxxxxxxxx x xxxxxx“.
XXXXX: 32017L1572
20. X §77 xxxx. 1 xxxx. x) bodě 4 xx xxxxx „13“ xxxxxxxxx číslem „12“.
21. X §77 xxxx. 1 xxxx. x) xx xxx 5 xxxxxxx.
Xxxxxxxxx body 6 xx 14 xx xxxxxxxx xxxx xxxx 5 xx 13.
22. X §77 xxxx. 1 xxxx. x) bod 11 xxx:
„11. xxxxxxx xxxxxx, xxx-xx o xxxxxxxxxx xxxxxxxxx, xxxxxxxxx xxxxxxxxxx xxxxxx, xxx-xx x xxxxxxxxxx xxxxxxxxx x xxxxxx xxxxxxxx, xxxxx xx xxxxxx xxxxxxxxxx xxxxxxxxxxxx xxxxxxxxx xxxxxx xxxxxxxxx xxxxxxxxxx služby xxxxx §67 odst. 3,“.
23. X §77 xxxx. 1 xxxx. x) xxxx 12 xx xx xxxxx „xx účelem“ xxxxxxxx xxxxx „xxxxxxxxxxxx, xxxxxxxxxxx x xxxxxxxxxx xxxxxxxx xxxxx xxxxxx x xxxxxxx xxxxxxxxx zdraví x xxxxxxxxxxx“ x xx slovo „očkování“ xx vkládají slova „xxxxxxxxx podle zákona x xxxxxxxx xxxxxxxxxx xxxxxxxxx“.
24. X §77 xx xx konci xxxxxxxx 1 xxxxx xxxxxxxxx xxxxxx x xxxxxxxx xx xxxxxxx x), xxxxx zní:
„r) xxxxxx xxxxxxxx prvky x xxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx xxxxxxxx xxxxx xxxxxxxx x xxxxxxxxxx xxxxxxx před xxx, xxx xxxxxx xxxxxxxxx xxxx
1. xxxxxxxxxxxx xxxxxxx,
2. Xxxxxx Xxxxx xxxxxxxxx k xxxxxxxxxxx xxxxxxxxxxx xxx Xxxxx xxxxxxxxx xxxxxx a x xxxxxxxxx skladových xxxxx xxxxxxxx přípravků xxx xxxxx xxxxxxxxxxx xxxxxxxxxxx sil Xxxxx xxxxxxxxx xxxxxx xxx xxxxxx vysílání xx xxxxxxxxx xxxxx §111x, xxxx
3. xxxxxxxxxxxxxx xxxxxxxxxxx xxxxxx, kterým xxxx xxxxx §77 odst. 1 xxxx. x) xxxx 12 dodávány xxxxxxxxxxxx xxxxxx přípravky xxx účely pravidelného xxxxxxxx xx xxxxxxx xxxxxxx smlouvy distributora xx xxxxxxxxx xxxxxxxxxxx xxxx xxx účely xxxxxxxxxxxx, zvláštního a xxxxxxxxxxx xxxxxxxx na xxxxxxx xxxxxxx xxxxxxx xxxxxxxxxxxx x Ministerstvem xxxxxxxxxxxxx anebo xxxx xxxx xxxxxxxxx dodávány xxx účely xxxxxxxxxxx xxxxxxxxx xxxxxxxx v xxxxx xxxxxxxxxxx xxxx xxxxx xxxxxx x xxxxxxxx xxxxxxxxxx xxxxxxxxx7).“.
XXXXX: 32016R0161
25. X §80 xxxx. 4 se xxxxx „Xxxxxxxxxxx xxxxxx xxxxxxxxx“ xxxxxxxxx slovy „Xxxxxx xxxxxxxxx pro xxxxx xxxxxx“.
26. V §82 xxxx. 2 xx xxxxxxx c) zrušuje.
Dosavadní xxxxxxx d) xx x) xx označují xxxx xxxxxxx c) xx f).
27. X §82 xx na xxxxx xxxxxxxx 3 xxxxx xxxxxxxxx čárkou a xxxxxxxx xx xxxxxxx x), které xxx:
„x) xxxxx xxxxxxxx xxxxx x provedou xxxxxxxx xxxxxxxxxxx identifikátoru x xxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxx xxxxxxxx xxxxx xxxxxxxx x xxxxxxxxxx xxxxxxx.“.
XXXXX: 32016R0161
28. V §99 xx xxxxxxxx xxxxxxxx 7 x 8, xxxxx xxxxx:
„(7) Ústav xx xxxxxxxx poskytuje xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxx článku 31 xxxxxxxx x ochranných prvcích (xxxx jen „úložiště“) xxxxxxxxx, xxxxx vyplývají x výkonu xxxx xxxxxxxxxx x xxxx xxxxxxxx xxx fungování xxxxxx xxxxxxxx.
(8) Xxxxx xxxxxxxxx x xxxxxxxx, xxxxx získá nebo x xxxx xx xxxxxxx podle §13 xxxx. 2 xxxx. x), xxxxxxxxx xxxxxx xxxxxx, pouze xxxxx xxx xxxxxxx jiný xxxxxx xxxxxxx, x xxxxxxxx zákona o xxxxxxxxx xxxxxxxx x xxxxxxxxxx.“.
XXXXX: 32016R0161
29. X §100 xxxx. 8 úvodní xxxxx xxxxxxxxxx xx xx xxxxx „Xxxxx“ xxxxxxxx xxxxx „nebo Xxxxxxxxxxx xxxxx xxxxx xxxxxxxxxx“.
30. X §100a xx xxxxx „xxxxxxx“ xxxxxxxxx slovy „xxxxxxxx xxxxxx xxxxxxxxx“.
31. X §103 xxxx. 6 se xx konci xxxxxxx x) slovo „nebo“ xxxxxxx.
32. V §103 xx xx konci xxxxxxxx 6 xxxxx xxxxxxxxx xxxxxx a xxxxxxxx se xxxxxxx x) až k), xxxxx xxxxx:
„x) poruší xxxxxxxxx xxxxxxxxx pokyny Xxxxxx nebo xxxxxxxx xxxxx §23 odst. 1 xxxx. a),
i) xxxxxxxxxx neoznámí Xxxxxx xxxxxxxxx na xxxxxxxx xxxxxx xxxxxxxxx xxxxx §23 odst. 1 xxxx. x) xxxx x),
x) x xxxxxxx x xxxxxxxxx o xxxxxxxxxx xxxxxxx xxxx xxxxx xxxxxxx
1. xxxxxxx xxxxxxx xxxxxxxxxxx identifikátoru xxxx neporušenost xxxxxxxxxx x xxxxxxx xxxxxxxxxx x xxxxxx,
2. distribuuje xxxx xxxx xxxxxx xxxxxxxxx s jedinečným xxxxxxxxxxxxxxx, který xxx xxxxxxx, xxxx jde x případy xxxxxxxxx x čl. 12 xxxxxxxx x ochranných prvcích, xxx xxx je xxxxxxxx xxxxxx,
3. změní xxxxxx vyřazeného xxxxxxxxxxx xxxxxxxxxxxxxx xx xxxxxxx, xxxx xxxx x xxxx splněny xxxxxxxx xxxxxxxxx v čl. 13 xxxx 1 xxxxxxxx x ochranných prvcích, xxxx
4. xxxxx do xxxxxxxxxx xxxxx léčivý xxxxxxxxx x xxxxxxxxxx xxxxxxxxxxxxxxx, xxxxxxx xxx xxxxxxxxx xxxxxxxx xxxxxxxxxxx x čl. 13 bodu 2 xxxxxxxx x xxxxxxxxxx prvcích xxxxxx xxx xxxxxx xxxxxxx xxxxxx, xxxx
x) xxxxxxxxxx Xxxxxx xxxxxxxxxx xxx xxxxxxxxx skutečností souvisejících x xxxxxxxxxx xx xxxxxxxx xxxxxxxx xxxxxxxxx xxxxx §23 xxxx. 1 písm. g).“.
CELEX: 32016R0161
33. X §103 xx xxxxxxxx xxxxxxxx 15 xx 21, xxxxx znějí:
„(15) Xxxxxxx xxxxxxxx xxxxxxxxx se xxxxxxx xxxxxxxxx tím, xx x xxxxxxx x xxxxxxxxx x xxxxxxxxxx xxxxxxx xxxx xxxxx xxxxxxx
x) xxxxxxxx xx xxxx xxxxxxxx xxxxxxxxx xxxxxxxxx identifikátor xxxx jej xx xxxx léčivého xxxxxxxxx xxxxxx, xxxx xx xxxxxxxx stanovené technické xxxxxxxxxxx,
x) xxxxxxxxx xxxxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx xx xxxxxxxxxxxxxx xxxxxxxx kódu,
c) xxxx xxxxxxx kvalitu xxxxx, xxxxx xxxxxxxx xxxxxxx xxxxxxxxx xxxxxx xxxxxx v xxxxxxx xxxxxx dodavatelského xxxxxxx xxxxxxx xx dobu 1 xxxx xx xxxxxxxx data použitelnosti xxxxxx, xxxx po xxxx 5 xxx xx doby, xxx xxxx xxxxxx propuštěno x prodeji nebo xxxxxxxxxx,
x) xxxxxxxxxx na xxxx léčivého přípravku xx xxxxxxx čitelném xxxxxx xxxx stanovené xxxxxx xxxxx jedinečného xxxxxxxxxxxxxx,
x) xxxxxxx, xxx-xx x xxxxxxx, xxxxx xxxxxxxx ochranné xxxxx, xxxx xxxxxxxxxxx léčivého xxxxxxxxx, že dvojrozměrný xxxxxx kód nesoucí xxxxxxxxx xxxxxxxxxxxxx xx x xxxxxxx xx xxxxxxxxxxx xxxxxxxxx xxxxxxx xxxxxx okem x xxxxxxxx správné xxxxxxxxx,
x) xxxxxx, jde-li x xxxxxxx, který xxxxxxxx xxxxxxxx xxxxx, xxxxxxx x každém xxxxx, xxxxx xxxxxxx x xxxxxxxxxx identifikátorem na xxxxxx xxxxxxxx xxxxxxxxx xxxx xx tomto xxxxxxxxxxxxxx,
x) xxxx xxxxxxxxx xxxx xxxxxx xxxxxxxxxxx xxxx xxxxxxxxx xxxxxxxxxx xxxxx xxxxxxx neporušenost xxxxxxxxxx x xxxxxxx xxxxxxxxxx x xxxxxx xxxx xxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx xxxx xxx xxxxxxxx, xxxxx xxxx xxxxxxxx, anebo zcela xxxx zčásti xxxxxxxx xxxx xxxxxxxx ochranné xxxxx x xxxxxxx x §64x,
x) xxxxxxx xxxxxxxx xxxxx xxxx xxxxxxxx xxxxxxxxx xxxxxxxxxxxxx xx balení xxxxxxxx xxxxxxxxx před tím, xxx xx xxxxxxx xxxx xxxxx xxxxxx, xxx xx mohl xxxxxx xxxx registrovaný xxxxxxxxx xxxxxx xxxxxxxxx xxxx jako registrovaný xxxxxxx xxxxxx xxxxxxxxx, xxx-xx o výrobce, xxxxx má xxxxxxxx x xxxxxx xxxxx §62 xxxx. 1 xxxx xxxxxxxx x xxxxxx a xxxxxx xxxxxxxxxxx xxxxxxxx přípravků xx Xxxxxxxx unie xxxxxxxxx x čl. 61 xxxxxxxx o klinickém xxxxxxxxx,
x) xxx umisťování xxxxxxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx xxx účely xxxxxxx xxxxxxxxx xxxxxxxxxxx x §64x xxxxxxx, že xxxxx xxx x xxx xxxxxxxxx x xxxxxxxxxxxx xxxxxxxx xxxxx xxxx xxxx xxxxxxxxxxxx xxxxx xxxxxxxxxxxxxx xxxxxx xxxxxxxxx, xxxxxxxxx x xxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxxxxx xx xxxx xxxxxxx požadavky členského xxxxx, v xxxx xx xxx léčivý xxxxxxxxx uveden xx xxx, xxx xxxx xxx xxxxxxxxx xxxxxxxxxxxxx xxxxxx z hlediska xxxxxxxx x vyřazen,
j) xxxxx xxxxxx xxxxxxxxx xx xxx nebo xxxxxxxx xxxxxxxxx Xxxxx x xxxxxxx, xx-xx xxxxx se xxxxxxxx, xx s xxxxxx xxxxxxxx přípravku xxxx xxxxxxxxxxxx, nebo v xxxxxxx, xx ověření xxxxxxxxxx prvků xxxxxxxxx, xx xxxxxxxxx xxxxx xxxx pravý, nebo
k) xxxxx xx xxxx xxxxxxxx xxxxxxxxx, xxxxx xxxx xxx xxxxxxx xxxxxxxxxxxxx čárovým xxxxx xxxxxxx xxxxxxxxx identifikátor, xxxxx xxxxxxxxx dvourozměrný xxxxxx xxx.
(16) Distributor xx xxxxxxx přestupku xxx, že
a) x xxxxxxx s xxxxxxxxx x xxxxxxxxxx prvcích xxxx tímto xxxxxxx
1. xxxxxxx xxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx x xxxxxxxx xxxxxxxxx, xxxxx xx xx xxxxxxxx xxxxxx x neobdržel je xx xxxx určených x čl. 20 nařízení x xxxxxxxxxx xxxxxxx,
2. xxxxxxx xxxxxxx nebo xxxxxxxxx vyřazení jedinečného xxxxxxxxxxxxxx x xxxxxxxx xxxxxxxxx xxxxxxxxxxx v čl. 22 xxxxxxxx o xxxxxxxxxx xxxxxxx, nebo
3. xxxx nebo vyveze xxxxxx xxxxxxxxx xxxx xxxxxxxx xxxxxxxxx Xxxxx x xxxxxxx, má-li xxxxx xx xxxxxxxx, xx x xxxxxx xxxxxxxx xxxxxxxxx bylo xxxxxxxxxxxx, nebo x xxxxxxx, xx xxxxxxx xxxxxxxxxx prvků léčivého xxxxxxxxx xxxxxxxxx, xx xxxxxxxxx xxxxx xxxx xxxxx,
x) xxxxxx xxxxxxxxx xxxxxx ochranné xxxxx xxxx xxxxxxx xxxxxxxxx xxxxxxxxxxxxx xxxxx §77 xxxx. 1 písm. x), xxxx
x) xx xxxxxxx xxxxxxxxxx xxxxx xxxxx §37 odst. 7 x xxxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx xxxx léčivý přípravek xxxx osobě než xxxxxx xxxxxxxx x §77 xxxx. 1 xxxx. x).
(17) Xxxxxxxxxxxx xxxxxxxxxxx služeb xxxxxxxxx x xxxxxx xxxxxxxx xxxxxxxxx xx dopustí xxxxxxxxx tím, xx
x) x rozporu s xxxxxxxxx x xxxxxxxxxx xxxxxxx xxxx xxxxx xxxxxxx
1. xxxxxxx xxxxxxxx xxxxx xxxx neprovede xxxxxxxx jedinečného xxxxxxxxxxxxxx xxxxxxxx přípravku xxxxxxxxxx xxxxxxxxxx prvky, xxxxx xxxxxx, v xxxxxxxx xxxx výdeje, xxxx xxx xxxxxx xxxxxxxx xxxxxx při výdeji xx xxxxxxx xxxx xxx xxxxxxx xxxxxxxxx x případě xxxxxxx xxxxx čl. 29 xxxxxxxx x xxxxxxxxxx xxxxxxx,
2. xxxxxxx ochranné prvky xxxx xxxxxxxxx vyřazení xxxxxxxxxxx identifikátoru xxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxx x xxxxxxxxxxx x čl. 25 odst. 4 xxxxxxxx o xxxxxxxxxx xxxxxxx, nebo
3. xxxx xxxxxx xxxxxxxxx xxxx xxxxxxxx xxxxxxxxx Xxxxx x xxxxxxx, xx-xx xxxxx xx xxxxxxxx, že x xxxxxx xxxxxxxx xxxxxxxxx xxxx xxxxxxxxxxxx, xxxx x xxxxxxx, xx xxxxxxx ochranných xxxxx xxxxxxxx xxxxxxxxx xxxxxxxxx, xx xxxxxxxxx xxxxx xxxx xxxxx, xxxx
x) xxxxxx povinnost xxxxx §82 xxxx. 3 xxxx. x) xxxxxx xxxxxxxx xxxxx xxxx xxxxxxx xxxxxxxxx xxxxxxxxxxxxx, xx-xx léčivý xxxxxxxxx xxxxxxxxxx xxxxx xxxxxxx.
(18) Xxxxxxx xxxxxxxxxx x xxxxxxxxxx xxxx, x xxxxxxx xxxxxxxx dovážených xxxx xxxxxxxx distribuovaných xxxxxxxx xxxxxxxxx x xxxxxxxxxxx jedinečným identifikátorem xxx xxxxx splnění xxxxxxxxx xxxxxxxxxxx x §64x, osoba xxxxxxxxx xx xxxxxxx xxxxxx xxxxxxxx xxxxxxxxx na xxx se xxxxxxx xxxxxxxxx tím, xx x xxxxxxx s xxxxxxxxx x ochranných xxxxxxx nebo tímto xxxxxxx
x) nezajistí, xx xxxxxxxxx xxxxxxxxx xxxxxxxxx x xxxxxxxxxx xxxxxxx xx xxxxxxx xx xxxxxxx úložišť xxxx xxx, xxx xxxx xxxxxx přípravek xxxxxxxxx xxxxxxxx x xxxxxxx xxxx distribuci, xxxx xx xxxx xxxx xxxxxxxxx poté xxxxxxxxxxxxx,
x) xxxxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx xxxxx čl. 40 xxxxxxxx x xxxxxxxxxx xxxxxxx, nebo
c) xxxxxxx xxxxxxxxx xxxxxxxxxxxxxx xx xxxxxxx xxxxxxx xxxxx, xxx z něho xxxxxxxx, pokud jsou xxxxxxxx, starší xxxxxxxxx xxxxxxxxxxxxxx obsahující xxxxxx xxx přípravku x xxxxxxx xxxxx xxxx xxxxxxxxx xxxxxxxxxxxxxx, xxxxx xx xxxx nahrát.
(19) Xxxxx xxxxxxxxx xxxx xxxxxxxxxx xxxxxxxx, xxxxx xx xxxxxxxx xxxxxxx xxxxxxx, xx xxxxxxx xxxxxxxxx xxx, xx x xxxxxxx s xxxxxxxxx x ochranných xxxxxxx xxxx xxxxx xxxxxxx
x) xxxxxxxxxx xxxxxxxxx xxxxxxxxx x úložišti, xxxxx spravuje x xx něhož xxxx xxxxxxx xxxxxxx, xx xxxx 1 xxxx xx xxxxxxxx xxxx xxxxxxxxxxxxx daného xxxxxxxx xxxxxxxxx xxxx po xxxx 5 xxx xx xxxx, xxx xxx xxxxxxxxx propuštěn x xxxxxxx xxxx xxxxxxxxxx,
x) neprovede xxxxx xxxxxxxxx podle čl. 37 xxxxxxxx o xxxxxxxxxx xxxxxxx,
x) xxxx osoba xxxxxxxxx x xxxxxxxxxx xxxxxxxx xxxxxxxxx x xxxxxxx xxxxxxxx xxxx xxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx xxxxxxxx xxxxxxxxx uváděných xx xxx x Xxxxx xxxxxxxxx xxxxxxxxxx Xxxxxx xxxxxxx k xxxxxxxx a informacím x něm obsaženým xxx xxxxx xxxxxx xxxxx podle nařízení x xxxxxxxxxx xxxxxxx,
x) xxxxxxx xxxxxxxx pro xxxxxxxxx xxxxxxx úložišť xxxxxxxxx xxxxx čl. 35 xxxx. 1 x 2 xxxxxxxx o xxxxxxxxxx xxxxxxx,
x) xxxxxxxxx xxxxxxx xxxxxxxx xxxxxxxxxxx x čl. 32 xxxx. 3 nebo 4 xxxxxxxx o xxxxxxxxxx xxxxxxx,
x) xxxxxxxxx připojení xxx xxxxxxxxx x xxxxxxxxxxxx xxxxxxxx x xxxxxxxxxxx xxxxxxxx, nebo
g) xxxxxx nahrání xxxx xxxxxxxx jedinečného xxxxxxxxxxxxxx xxxxxxxxxxxx xxxxxx xxx xxxxxxxx xxxxxxxxx a xxxxxxx číslo jako xxxx xxxxxxxxx xxxxxxxxxxxxx, xxxxx je v xxxxxxxx xxx xxxxxx.
(20) Xxxxx xxxxxxxxx xx xxxxxxx xxxxxxxx xxxxxxxxx xx xxx se xxxxxxx přestupku tím, xx x xxxxxxx x xxxxxxxxx x xxxxxxxxxx xxxxxxx xxxx xxxxx xxxxxxx xxxxxxxxxxx xxxxxxxxx úložiště o xxxxx xxxxx xxxx xxxxxxx xxxxxx u xxxxx xxxxx přebalených xxxx xxxxx označených xxxxxx xxxxxxxx přípravků, xx xxxxx byly xxxxxxxx xxxxxxxxxx jedinečné xxxxxxxxxxxxxx.
(21) Xxxxxxx xxxxxxxxxx x xxxxxxxxxx, který xxxx xxxxxx přípravek, xxxxx xx xxxxxxx xxxxxxxxxx prvky, xxxx xxxxxxxxx vzorek x xxxxxxx předpisem xx xxxxxxx upravujícím xxxxxxxx xxxxxxx51), se xxxxxxx xxxxxxxxx tím, xx xx x xxxxxxx x xxxxxxxxx x xxxxxxxxxx prvcích nebo xxxxx xxxxxxx xxxxxxxx x xxxxxxx xxxxxxx xxxx bezplatný vzorek xxxx xxxxxxxxx vyřazení xxxx xxxxxxxxxxx identifikátoru xxxx xxx, xxx xx poskytne xxxxxx xxxxxxxxxx xxxxxxxxxxxx humánní xxxxxx xxxxxxxxx.“.
XXXXX: 32016R0161
34. X §104 xx xxxxxxxx odstavec 14, který xxx:
„(14) Xxxxxxx xxxxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx xx xxxxxxx xxxxxxxxx tím, xx
x) x rozporu x xxxxxxxxx x xxxxxxxxx xxxxxxxxx nedodrží xxxxxx a pokyny xxxxxxx výrobní xxxxx xxxxxxx x xxxxxxxx x xxxxxxx xxxxxxx xxxxx xxx xxxxxxxxx xxxxxx xxxxxxxxx, nebo
b) xxx inspekci prováděné xxxxx xxxxxxxx x xxxxxxx výrobní xxxxx xxx xxxxxxxxx léčivé xxxxxxxxx neumožní výkon xxxxxxxxx uvedených x xx. 20 bodu 2 xxxxxxxx o xxxxxxx výrobní xxxxx xxx hodnocené xxxxxx xxxxxxxxx.“.
XXXXX: 32014R0536, 32017R1569
35. V §105 xxxx. 2 xxxx. x) se xxxxx „xxxxx“ nahrazuje xxxxx „xx xxxxxxx“.
36. X §105 xxxx. 4 xxxxxxx x) xxx:
„x) xxxxxx xxxxxxxxx xxxxxxxxxx x §45 xxxx. 7 xxxx. x) nebo x),“.
37. V §105 xx doplňuje odstavec 10, xxxxx xxx:
„(10) Xxxxxxxxxxxx xxxxx §6 xxxx. 1 písm. x) xx jako xxxxxxxxxxxx xxxxxxx xxxxxxx xxxxxxxxx xxx, že xxx inspekci xxxxxxxxx xxxxx xxxxxxxx o xxxxxxxxx xxxxxxxxxxx postupů xxxxxxx xxxxxxxx praxe xxxxxxxx xxxxx xxxxxxxxx xxxxxxxxx x čl. 10 xxxxxx 2 xx 5 xxxxxxxx o xxxxxxxxx inspekčních xxxxxxx xxxxxxx klinické praxe.“.
CELEX: 32017R0556
38. V §106 xxxx. 1 xxxx. x) xx xxxxx xxxxxxx přede xxxx xxxxxx xxxxxxxxx xxxxxx xxxxxx xx za xxxxx „x xxxxxxx x §66 odst. 1“ xxxxxxxx xxxxx „xxxxxxxxx, xxx xxxx xxxxxxxx přípravku byl xxxxxxx xxxxxxxxxx xxxxx xxxxx §37 odst. 7, nebo“.
CELEX: 32011L0062, 32016R0161
39. V §106 xxxxxxxx 1 xxx:
„(1) Xxxxxxxxxxx fyzická xxxxx xx xxxx xxxxxxxxxxxxx xxxxx xxxxxxx xxxxxxxx xxxxxxxxx xxxxxxx xxxxxxxxx xxx, xx x xxxxxxx x §66 xxxx. 1 xxxxxxxxx, xxx xxxx xxxxxxxx xxxxxxxxx xxx xxxxxxx xxxxxxxxxx xxxxx xxxxx §37 xxxx. 7, xxxx xxxxxxxxx, xxx xxxxx xxxxx xxxxxxxx xxxxxxxxx byla xxxxxxxx x xxxxxxxxxxxx x xxxxxxx x xxxxx xxxxxxx, xxxxxxxxxxx xxxxxxxxxxx x xxxxxxxxxxx o xxxxxxxxxx, nebo x xxxxxxx x §66 xxxx. 3 xxxx xxxxxxxxxx neosvědčí x xxxxxxxx xxxx x xxxxxxxxxxx xxxxxxxxx xxxxxxxxxx x xxxxxx účelu xxxx x xxxxxxx x čl. 62 nařízení x xxxxxxxxx hodnocení xxxxxxxxx, xxx každá xxxxx xxxxxxxxxxx léčivých xxxxxxxxx vyráběných x Xxxxxxxx unii nebo xxxxxxxxxx xx Xxxxxxxx xxxx, byla v xxxxxxx x xxxxxxxxx xxxxxxxxxxx v čl. 63 xxxxxxxx o xxxxxxxxx xxxxxxxxx, x xxxxxxxxx, xx jsou xxxx xxxxxxxxx xxxxxxx.“.
XXXXX: 32014R0536
40. X §107 xxxx. 1 xxxx. x) se xx xxxx „§104 xxxx. 7 xxxx. x),“ xxxxxx text „§104 xxxx. 14 xxxx. x),“.
XXXXX: 32014R0536
41. V §107 xxxx. 1 xxxx. x) xx za xxxx „§103 odst. 6 písm. x),“ xxxxxxxx xxxxx „§103 xxxx. 6 písm. x) xxxx 3 xxxx x)“ a xx text „§103 xxxx. 14“ xx xxxxxxxx slova „, §103 odst. 15 xxxx. x), e), x), x), i) xxxx k), §103 xxxx. 16 xxxx. x) xxxx 1, §103 xxxx. 16 xxxx. x), §103 xxxx. 18 xxxx. x), §103 xxxx. 20 nebo 21,“.
42. V §107 xxxx. 1 xxxx. x) xx slova „§105 xxxx. 7, 8 nebo 9“ xxxxxxxxx slovy „§105 xxxx. 7, 8, 9 xxxx 10“.
43. X §107 xxxx. 1 písm. x) xx za xxxx „§103 xxxx. 6 xxxx. x), x) xxxx x),“ xxxxxxxx xxxxx „§103 xxxx. 6 písm. x) xxxx 1, 2 xxxx 4,“ x za xxxx „§103 odst. 10 xxxx. x)“ xx xxxxxxxx slova „, §103 xxxx. 15 xxxx. x), x) xxxx x), §103 xxxx. 16 písm. x) xxxx 2, §103 xxxx. 16 xxxx. x), §103 xxxx. 17 xxxx. x) bodu 1 xxxx 2, §103 xxxx. 17 písm. x), §103 odst. 18 xxxx. x) xxxx b), §103 xxxx. 19 xxxx. x), b), c), x), x), x) xxxx g)“.
44. X §107 xxxx. 1 xxxx. x) xx slova „§105 xxxx. 6 xxxx. x), x) xxxx x)“ xxxxxxxxx xxxxx „§105 xxxx. 6 písm. x) xxxx l)“.
45. X §107 xxxx. 1 písm. x) xx slova „§103 odst. 6 xxxx. a) xxxx x)“ xxxxxxxxx xxxxx „§103 odst. 6 xxxx. x), x), x) xxxx i)“ x xx text „§103 odst. 13“ xx xxxxxxxx slova „, §103 odst. 15 xxxx. g) xxxx j), §103 xxxx. 16 písm. x) xxxx 3, §103 xxxx. 17 xxxx. x) xxxx 3 nebo 4“.
46. X §107 xxxx. 1 xxxx. x) se xx xxxxx „§104 xxxx. 7 xxxx. x) xxxx x),“ vkládá xxxx „§104 odst. 14 xxxx. a),“ x xxxxx „xxxx §105 xxxx. 6 xxxx. x)“ xx xxxxxxx.
47. X §108 xxxx. 3 ve xxxxx xxxxxxx xxxxx xxxx nabytí xxxxxxxxx xxxxxx xxxxxx xx xx xxxxx „v xxxxxxx x §66 xxxx. 1“ xxxxxxxx xxxxx „nezajistí, aby xxxx léčivého xxxxxxxxx xxx xxxxxxx ochrannými xxxxx podle §37 xxxx. 7, nebo“.
48. X §108 xxxx. 3 se xx slova „x xxxxxx xxxxx“ xxxxxxxx xxxxx „xxxx v xxxxxxx s čl. 62 xxxxxxxx x xxxxxxxxx xxxxxxxxx xxxxxxxxx, aby xxxxx xxxxx hodnocených xxxxxxxx xxxxxxxxx vyráběných x Evropské xxxx xxxx xxxxxxxxxx xx Xxxxxxxx unie xxxx x xxxxxxx s xxxxxxxxx stanovenými x čl. 63 xxxxxxxx o xxxxxxxxx xxxxxxxxx, x xxxxxxxxx, že jsou xxxx požadavky xxxxxxx“.
XXXXX: 32011L0062, 32016R0161, 32014R0536
49. X §114 xxxx. 1 xx xxxx „§82 xxxx. 2 xxxx. d) x e)“ nahrazuje xxxxxx „§82 xxxx. 2 xxxx. x) x x)“.
XXXX XXXXX
Xxxxx zákona x zdravotních xxxxxxxx
Čl. XX
X §65 xxxxxx x. 372/2011 Xx., o zdravotních xxxxxxxx x xxxxxxxxxx xxxxxx xxxxxxxxxxx (xxxxx x zdravotních službách), xx xxxxx xxxxxx x. 205/2015 Sb., xx xx xxxxx xxxxxxxx 2 xxxxx xxxxxxxxx xxxxxx x xxxxxxxx xx písmeno x), xxxxx xxxxxx xxxxxxxx xxx čarou x. 55 zní:
„o) xxxxxxxxxx oprávnění k xxxxxxxxx xxxxxxxx xxxxxxxxxxxxx x klinickým hodnocením xxxxxxxxx xxxxxxxx xxxxxxxxx x xxxxxxx s xxxxx použitelným xxxxxxxxx Xxxxxxxx xxxx xxxxxxxxxxx xxxxxxxx xxxxxxxx pro xxxxxxxxx xxxxxxxxxxx xxxxxxx xxxxxxx xxxxxxxx xxxxx55).
Xx. XXX
Xxxxxxx ve Xxxxxx xxxxxx
Xxxxxxxxxxxx xxxxxxxxxxxxx xxxxxx sdělení xx Xxxxxx xxxxxx xxxxxx xxx, xxx bylo xxxxxxxxxx oznámení Komise x Xxxxxxx xxxxxxxx Xxxxxxxx unie xxxxx čl. 82 xxxx. 3 xxxxxxxx Xxxxxxxxxx parlamentu x Xxxx (XX) x. 536/2014 xx xxx 16. xxxxx 2014 o klinických xxxxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx x x xxxxxxx xxxxxxxx 2001/20/XX.
Xx. XX
Xxxxxxxx
Xxxxx xxxxx xxxxxx účinnosti dnem 9. xxxxx 2019, x xxxxxxxx xxxxxxxxxx xx. X xxxx 3, 6, 7, 8, 9, 17, 18, 19, 34, 37, 39, 40, 42, 44, 46, 48 x xx. XXX, xxxxx nabývají xxxxxxxxx xxxxxxxxx 6 xxxxxx ode xxx xxxxxxxxxx oznámení Komise x Úředním věstníku Xxxxxxxx xxxx xxxxx čl. 82 xxxx. 3 xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Rady (XX) x. 536/2014 xx xxx 16. xxxxx 2014 x xxxxxxxxxx xxxxxxxxxxx humánních xxxxxxxx xxxxxxxxx x x xxxxxxx směrnice 2001/20/XX.
106) Xxxxxxxx Komise x xxxxxxxxx xxxxxxxxx (EU) 2016/161 xx dne 2. října 2015, xxxxxx se xxxxxxxx xxxxxxxx Evropského xxxxxxxxxx x Rady 2001/83/XX xxxxxxxxxx podrobných xxxxxxxx xxx xxxxxxxx xxxxx xxxxxxx xx xxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx.“.
107) Xxxxxxxx Komise x xxxxxxxxx xxxxxxxxx (XX) 2017/1569 ze dne 23. května 2017, xxxxxx xx xxxxxxxx xxxxxxxx Evropského xxxxxxxxxx x Rady (XX) x. 536/2014 stanovením xxxxx x pokynů xxx xxxxxxxx xxxxxxx xxxxx xxx xxxxxxxxx xxxxxxx xxxxxx xxxxxxxxx x pravidel xxxxxxxxx xxxxxxxx.
108) Prováděcí xxxxxxxx Xxxxxx (XX) 2017/556 xx dne 24. xxxxxx 2017 x xxxxxxxxxx xxxxxxxxxx xxx xxxxxxxxx xxxxxxxxxxx xxxxxxx xxxxxxx xxxxxxxx xxxxx xxxxx xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Xxxx (XX) x. 536/2014.“.
55) Xxxxxxxxx xxxxxxxx Xxxxxx (XX) 2017/556 xx xxx 24. xxxxxx 2017 o xxxxxxxxxx xxxxxxxxxx xxx xxxxxxxxx xxxxxxxxxxx postupů xxxxxxx xxxxxxxx xxxxx xxxxx xxxxxxxx Evropského xxxxxxxxxx x Rady (EU) 536/2014.“.
XXXXX: 32017R0556
Xxxxxxxx zpráva
I. OBECNÁ ČÁST
Návrh xxxxxx, kterým xx xxxx xxxxx č. 378/2007 Sb., x xxxxxxxx x x xxxxxxx některých xxxxxxxxxxxxx xxxxxx (xxxxx x léčivech), ve xxxxx pozdějších předpisů x xxxxx č. 372/2011 Sb., x xxxxxxxxxxx službách x xxxxxxxxxx jejich xxxxxxxxxxx (zákon x xxxxxxxxxxx xxxxxxxx), ve xxxxx xxxxxxxxxx xxxxxxxx.
1. Xxxxxxxxxx platného xxxxxxxx xxxxx, xxxxxx zhodnocení xxxxxxxxxx xxxxx ve xxxxxx x xxxxxx xxxxxxxxxxxx x xx xxxxxx k xxxxxxxx xxxx x žen
Předkládaná xxxxxx xxxxxx o xxxxxxxx a xxxxxx x zdravotních službách xxxxxxxxxxxx xxxxxx xxxxx Xxxxxxxx xxxx xx xxxxxxxx xxxx Xxxxx xxxxxxxxx.&xxxx; Xxxxx se x xxxxxxxxxxx xxxxxx xxxxxxxx:
- Nařízení Komise x xxxxxxxxx xxxxxxxxx (XX) 2016/161 xx xxx 2. xxxxx 2015, xxxxxx xx xxxxxxxx xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Xxxx 2001/83/XX, stanovením xxxxxxxxxx xxxxxxxx pro xxxxxxxx xxxxx xxxxxxx xx xxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx,
- Xxxxxxxxx xxxxxxxx Xxxxxx v přenesené xxxxxxxxxx (EU) č. 2017/556 xx dne 24. xxxxxx 2017 o xxxxxxxxxx xxxxxxxxxx xxx xxxxxxxxx xxxxxxxxxxx xxxxxxx xxxxxxx xxxxxxxx praxe xxxxx nařízení Xxxxxxxxxx xxxxxxxxxx a Xxxx (XX) x. 536/2014 (xxxx xxx „xxxxxxxx 2017/556“),
- Nařízení Komise x přenesené působnosti (XX) č. 2017/1569 xx xxx 23. května 2017, xxxxxx se xxxxxxxx xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Rady (XX) x.536/2014 stanovením xxxxx x xxxxxx xxx xxxxxxxx xxxxxxx xxxxx xxx xxxxxxxxx xxxxxxx xxxxxx xxxxxxxxx x xxxxxxxx xxxxxxxxx xxxxxxxx (dále xxx xxxxxxxx 2017/1569“),
- Xxxxxxxx Xxxxxx (XX) 2017/1572 xx xxx 15. xxxx 2017, xxxxxx xx doplňuje směrnice Xxxxxxxxxx parlamentu a Xxxx 2001/83/XX, xxxxx xxx x xxxxxx x pokyny xxx xxxxxxxx xxxxxxx praxi xxx xxxxxxx xxxxxx xxxxxxxxx (xxxx jen „xxxxxxxx 2017/1572“).
X xxxxxxxxxxx xxxxxxxxx Xxxxxxxx xxxx xxxxxxxxxxxx xxxxx následující.
Základem xxxxxxx xxxx vstupem xxxxxxxxxx xxxxxxxx xxxxxxxxx xx legálního xxxxxxxxxxxxxx xxxxxxx x evropském xxxxxxxxx se stala xxx 8. xxxxxx 2011 xxxxxxx xxxxxxxx Xxxxxxxxxx parlamentu a Xxxx 2011/62/EU, xxxxxx xx xxxx směrnice 2001/83/XX o xxxxxx Xxxxxxxxxxxx týkajícím xx xxxxxxxxx xxxxxxxx xxxxxxxxx, xxxxx xxx x xxxxxxxxx vstupu xxxxxxxxxx xxxxxxxx přípravků do xxxxxxxxx dodavatelského řetězce (xxxx jen „xxxxxxxx 2011/62/EU“). Podle článku 2 xxxxxxxx 2011/62/XX xxxx xxx xxxxxxx státy xxxxxxxxx xxxxxxxxxxxx xxxxx xxx xxxxxxx v xxxxxxxx xxxxxxxx x xxxxxxxxx xxxxxxxx xxxxxxxxxx xxx dosažení souladu x xxxxx směrnicí, xxxxx x xxx xxxxxxx xxxxxx xxxxxxxx, xx 2. xxxxx 2013. X xxxxxxx xx xxxxx stanovenou xxxxxxxxxxxx xxxxx xxxx x novele zákona x xxxxxxxx, xx. x zákoně č. 70/2013 Sb., xxxx xxxxxxxx xxxxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx xxxxxxxxxx léčivých xxxxxxxxx xx xxxxxxxxx xxxxxxxxxxxxxx xxxxxxx. Ochranné xxxxx xxxx x xxxxxx x xxxxxxxx xxxxxxxx x xxxxxxxxxxxx §37 odst. 7 x 8, §64x, §66 xxxx. 1 xxxx. c), xxxxxxx xxxxxx účinnosti xx xxxxxxxx xxx, xx xxxx nabýt xxxxxxxxx xxxxxxxxx 3 xxx xxx xxx vyhlášení xxxx xxxxxxxx Xxxxxxxxx xxxxxx (xxxx xxx „Xxxxxx“) v přenesené xxxxxxxxx xxxxx článku 1 xxxx 12 směrnice 2011/62/XX. Xxxxxxxxxx §77 xxxx. 1 písm. x) x x), xxxxx xxxxxx účinnosti xx 2.4.2013, xxxxxxxxxxx xxxx povinnosti distributora. Xxxxxxx specifikace a xxxxxxxxxxxxxxx xxxxxxxxxx xxxxx x způsoby xxxxxxxxx xxxxxxxxxx prvků xxxx xxxx nařízením x xxxxxxxxxx xxxxxxx, které xxxxxx xxxxxxxxx 9.2.2019, xxxxxxxxx xxxxxxxxxxxx xxxxxxxx xxxxxxxx xxxxx x xxxxxxxx příslušná xxxxxxxx x xxxxxxx xxxxxxxxxx xxxxxxxx přípravků, bude xxxx xx x xxxxxx datu.
Padělané xxxxxx xxxxxxxxx, xxxxx xx xx x pacientům xxxxxxx prostřednictvím xxxxxxxxx xxxxxxxxxxxxxx xxxxxxx, xxxxxxxxxxx xxxxxx xxx lidské xxxxxx x xxxxx xxxxxx xxxx ke xxxxxxx důvěry pacientů x xxxxxxx xxxxxxxxxxxx xxxxxxx, xxxxxxxxxxxxx xxxxxxxxx xxxx x xxxxxxxxx xxxxxx. Proto xxxxxxxx 2011/62/EU xxxxxxxxx xxxxxx xxxxxxxxxx xxxxx na xxxxxxx xxxxxxxx xxxxxxxxx, xxxxx xx xxxxxxx xxxxxx xxxxxxx pravosti xxxxxxxx xxxxxxxxx, identifikaci xxxxxxxxxxxx xxxxxx xxxxxxxx xxxxxxxxx x ověření, xxx nebylo s xxxxxx xxxxxxxxxxxx. Tyto xxxxxx xxxxxxxxxxxx podmínky xx měly xxxxxxxx xxxxxxxxxxx ochranu xxxxx xxxxxx xxxxxxxxxx léčivých xxxxxxxxx xx xxxxxxxxx xxxxxxxxxxxxxx xxxxxxx x xxxxx xxxxxxx xxxxxxxx x zájmy xxxxxxxx xxxxxxxxxx x xxxxxxxxxx x xxxxxxx.
Xxx xxxxxx xxxxxxxxx xxxxx byl xxxxxxxxxx xx všech xxxxxxxxx xxxxxxx Xxxxxxxx xxxx, neomezoval oběh xxxxxxxx přípravků x xxxxxxxxxx xxxxx xxxxxxx xxxxx xxxxxxxxx xxxxxxxxxxxxxx xxxxxxx způsobené xxxxxxxxxxxx xxxxxxxxx xxxxxxxxxx, xxxxxxxxx Xxxxxxxx Xxxxxx xxxxxxxxxxxxxxx xxxxxxxx Xxxxxx x xxxxxxxxx xxxxxxxxx (EU) 2016/161 xx xxx 2. října 2015, xxxxxx xx xxxxxxxx xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Xxxx 2001/83/XX, xxxxxxxxxx xxxxxxxxxx xxxxxxxx xxx xxxxxxxx prvky xxxxxxx na obalu xxxxxxxxx xxxxxxxx xxxxxxxxx (xxxx xxx „nařízení x xxxxxxxxxx prvcích“), xxxxxxxx xxxxxxxx pro xxxxxxxx ochranných xxxxx, xxxxxxx xxxxxxxxxxxxxxx x xxxxxxxxx xxxxxxxxxxx xxxxxxx x xxxxxxxxxx xxxxx - xxxxxxxxxxx xxxxxxxxxxxxxx, xxxxxxx x rozsah xxxxxxx xxxxxxxxxx xxxxx xxxxxxxxxxxx dotčenými subjekty (xxxxxxx, xxxxxxxxxxxx, xxxxxxx xxxxxxxxxxx xxxx xxxxxxxxxx xxxxxxx xxxxxx xxxxxxxxx xxxxxxxxxx) x xxxxxxx x xxxxxx xxxxxxx xxxxxxx xxxxxxxxxx xxxxxxxxx x xxxxxxxxxx xxxxxxx (xxxxxxxxxxx xxxxxxxxxxxxxxxx) x xxxxxxxx xx působnosti xxxxxxxx (xx. xxxxxx xxxxxxxx přípravků xx xxxxxxxxx léčivých přípravků, xxxxxxx výdej xx xxxxx xx xxxxxxxx xxxxxxx, xxxxx xxxxx xxx xxxxxxxx ochrannými xxxxx x xxxxxx xxxxxxxx xxxxxxxxx či xxxxxxxxx léčivých xxxxxxxxx, xxxxxxx výdej není xxxxx na xxxxxxxx xxxxxxx, které xxxx xxx xxxxxxxx xxxxxxxxxx xxxxx). Xxxxx xxxxxxxxx xx xxxxxxxx xxxxxxxxxx xxxxx (xxxxxxxxxxx xxxxxxxxxxxxxx x xxxxxxxxxx x xxxxxxx manipulace x xxxxxx) xx xxxxx xxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx xx umožnění xxxxxx xxxxxxxxxxxx a xxxxxxx pravosti.
Nařízení x xxxxxxxxxx xxxxxxx xx xxxxxxx xx 11 xxxxxxx x 4 xxxxxx:
Xxxxxxxx X xxxxxxxx x xxxxxxxxxx prvcích xxxxx oblast xxxxxxxxxx x základní definice xxxxxxxxxx prvků. Xxxxxxxxxx xxxxx xxxxx xxxxxxxx x xxxxxxx x xxxxxxxxx x xxxxxxxxxx xxxxxxx xxxxx xxxxx xxxxxxxxx xxxxxxxx přípravků
a) Xxxxxx přípravky, xxxxxxx xxxxx xx xxxxx xx xxxxxxxx xxxxxxx (xxx xx. 54x xxxx. 1 xxxxxxxx 2001/83/XX), xxxxx xxxxxx xxxxxxx x xxxxxxx x xxxxxxx I xxxxxxxx x xxxxxxxxxx xxxxxxx.
x) Xxxxxx xxxxxxxxx, xxxxxxx xxxxx xxxx xxxxx xx xxxxxxxx xxxxxxx zahrnuté do xxxxxxx xxxxxxxxx x příloze II xxxxxxxx o xxxxxxxxxx prvcích.
c) Xxxxxx xxxxxxxxx, xx které xxxxxxx xxxxx xxxxxxx xxxxxx xxxxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx nebo prostředku x xxxxxxx xxxxxxxxxx x obalem v xxxxxxx s xxxxxxx 54x xxxx. 5 xxxxxxxx 2001/83/XX.
Xxxxxxxx x xxxxxxxxxx prvcích stanovuje x kapitole XX Xxxxxxxxx xxxxxxxxxxx jedinečného xxxxxxxxxxxxxx.
Xxxxxxxx III xxxxxxxx x xxxxxxxxxx xxxxxxx xxxxx Xxxxxx xxxxxxxxxx x xxxxxxx xxxxxxxxxx xxxxx. Protože bude xxxxxxx xxxxxxxxxx xxxxx xxxxxxxx řada xxxxxxxx, xxxx x jejich xxxxxxxxxx xxx ověřování xxxxxxxxx, x xx x následující struktuře xxxxx xxxxxxx XX xx XX:
X xxxxxxxx XX xxxx xxxxxxxxx xxxxxxx xxxxxxx ochranných xxxxx a xxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx prováděné xxxxxxx; v xxxxxxxx X xxxx stanoveny xxxxxxx xxxxxxx xxxxxxxxxx xxxxx x xxxxxxxx xxxxxxxxxxx identifikátoru prováděné xxxxxxxxxxxx; x xxxxxxxx XX xxxx stanoveny xxxxxxx xxxxxxx xxxxxxxxxx xxxxx x vyřazení xxxxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxx xxxxxxx xxxxxxxxxxx xxxx xxxxxxxxxx xxxxxxx xxxxxx xxxxxxxxx xxxxxxxxxx.
Xxxxxxxx IV-VI xxxxxxxxx x xxxxxxxxx xxxxxxxx, xxxxx xxxx xxxxxxxx xxxxxxxxxx xxxxxxxx x případě, že xxxx důvod xx xxxxxxxx, xx x xxxxxx léčivého xxxxxxxxx xxxx manipulováno, nebo x xxxxxxx, že xxxxxxx xxxxxxxxxx prvků xxxxxxxxx, že xxxxxxxxx xxxx pravý:
- xxxxxxx xxxxxxxxx xxxxxxxxxx k xxxxxxx xxxx xx xxxxxxxxxx x xxxxxxxx xxxxxxx dotčené příslušné xxxxxx;
- xxxxxxxxxxx přípravek xxxxx xxxxxx xxxx xxxxx a xxxxxxx xxxxxxx příslušné orgány;
- xxxxx xxxxxxxxx nebo xxxxxxxx xxxxxxx léčivé xxxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxx xxxxx a xxxxxxxx uvědomí dotčené xxxxxxxxx xxxxxx.
Xxxxx jde x xxxxxxx xxxxxxx xxxxxxx, je xxxx xxxxxxxxxxxxx x Xxxxxxxx XXX - Xxxxxxx, xxxxxx x xxxxxxxxxx xxxxxxx xxxxxxx. Xxxxxx xxxxxxx, x xxxx xxxx být xxxxxxxx xxxxxxxxx o xxxxxxxxxx xxxxxxx, xxxxx a xxxxxxxx xxxxxxxxx xxxxxx xxxxxxx xxxxxxx v XX xxxxxxx x xxxxxxxx xxxxxxxxxx x xxxxxxxxxx léčivých xxxxxxxxx xxxxxxxxxx ochrannými xxxxx. Xxxxxxx na xxxxxx xxxxxxx xxx xxxxxxxx x xxxxxxxxxx xxxxxxx xxxxx výrobci xxxxxxxx xxxxxxxxx opatřených ochrannými xxxxx.
X xxxxxxxx XXXX xxxx xxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxxx o xxxxxxxxxx, souběžných xxxxxxx x xxxxxxxxxx xxxxxxxxxxxx x souvislosti xx xxxxxxxxx xxxx xxxxxxxxxx xxxxxxxxx, xxxx. xxxxxxxxx xxxxxxxxxx xxxx xxxxxxxxx xxxxxx.
X xxxxxxxx IX xxxx xxxxxxx povinnosti xxxxxxxxxxx xxxxxxxxxxxxxx xxxxxx, x xx zejména xxxxxxxxx xxxxxxxxxxx na xxxxxxxx xxxxxxxx xxxxxxxxx (xxxxxxxx rozhodnutí o xxxxxxxxxx, výrobci x xxxxx xxxxxxxxx xxxx xxxxxxxx xxxxxxx léčivé xxxxxxxxx veřejnosti) informace x léčivých xxxxxxxxxxx xxxxxxxxx xx xxx xx jejich xxxxx, xxxxx musí xxx xxxxxxxx xxxxxxxxxx xxxxx x xxxxxxxxx x xxxxxxxx xxxxxxxxxxx, na xxxxx xxxxxxxxx xxxxxxx xxxx rozšířil působnost xxxxxxxx x xxxxxxxxxx xxxxxxx. Xxxxx xxxxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx orgánů xx xxxxx xxx xxxxxxxx úložišť.
Kapitola X xxxxxxxx o ochranných xxxxxxx xxxxx xxxxxxxx xx xxxxxxxxxx xxxxxxxx - a xx xxxxxx léčivých přípravků xx kategorií xxxxxxxxx, xxxxxxx xxxxx xx xxxxx xx xxxxxxxx xxxxxxx, které xxxxx xxx xxxxxxxx ochrannými xxxxx, xxxxx je xxxxxx v xxxxxxx X xxxxxxxx x xxxxxxxxxx xxxxxxx x xxxxxx xxxxxxxx xxxxxxxxx xx xxxxxxxxx přípravků, xxxxxxx xxxxx xxxx xxxxx na lékařský xxxxxxx, které xxxx xxx xxxxxxxx ochrannými xxxxx, xxxxx xx xxxxxx x xxxxxxx XX xxxxxxxx o xxxxxxxxxx xxxxxxx.
Xxxxxxxx XX xxxxx přechodná xxxxxxxxxx x vstup x xxxxxxxx.
Xxxxxxx X xxxxxxxx x xxxxxxxxxx xxxxxxx (xxxxxxxxxx xxxx xxx. „Xxxxx xxxx“) xxxxx xxxxxx xxxxxxxx přípravků xx xxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxxx xxxxxxx xxxxxx xx xxxxxxxx xxxxxxx, x které xxxxx xxx opatřeny xxxxxxxxxx xxxxx: homeopatické xxxxxx xxxxxxxxx; xxxxxxxxxxxxxx xxxxxxxxxx; xxxx; xxxxxxxxxxxxxx xxxxxxxxxx; xxxxxx xxxxxxxxx xxx xxxxxxx xxxxxxx xxxxxxxxxx xxxxx xxxx xxxxx xxxx jsou xxxx tvořeny roztoky xxx xxxxxxxxxxxx xxxxxx, xxxxxxx XXX xxx xxxxxx xx X05XX; xxxxxxxxxxx xxxxx, roztoky xxxxxxxxxxx xxxxxxxxx xxxxxxxxxxx, xxxxxxx ATC kód xxxxxx xx B05BB; xxxxxxx xxxxxxxxxxxx xxxxxxxxxx xxxxxxx, xxxxxxx ATC xxx začíná xx X05XX; xxxxxxx x xxxxxxxxxxxxx roztokům, jejichž XXX xxx začíná xx X05X; xxxxxxxxxxxx x xxxxxxx, včetně xxxxxxxxxx roztoků, jejichž XXX xxx xxxxxx xx X07XX; xxxxxxxxxx xxxxx, xxxxxxx XXX xxx xxxxxx xx X08; xxxxx pro xxxxxxxxx onemocnění, jejichž XXX xxx začíná xx X04XX; xxxxxxxx xxxxxxxx, xxxxxxx ATC xxx začíná xx X01XX.
Xxxxxxx II nařízení x ochranných prvcích (xxxxxxxxxx xxxx xxx. „Xxxxx list“) xxxxx xxxxxx xxxxxxxx přípravků xx xxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxxxxx xxxxxxx xxxxxx xx xxxxxxxx xxxxxxx, xxxxx musí xxx xxxxxxxx ochrannými xxxxx: xxxxxx přípravky x xxxxxxx xxxxxx xxxxxxxxx v lékové xxxxx xxxxxxxxxxxxxxx xxxxx xxxxxxx a síle 20xx nebo 40xx.
Xxxxxxx XXX x XX xxxxxxxx x ochranných xxxxxxx umožňují xxxxxxxxxx xxxxxxxxxxxxx xxxxxxx xxxxxxxxxx Xxxxxx x xxxxxxxx xxxxxxxxxxx, které nepodléhají xxxxxxx xxxxxx na xxxxxxxx xxxxxxx, xxx x xxxxx xxxxx xxxxxx xxxxxxxx nebo x léčivých xxxxxxxxxxx x kterých xxxxxx xxxxxxxx xxxxxxx.
Xxxxxxxx xxxxx xxxxx xxx prvky xxxxxxxx na xxxxx xxxxxxxxx léčivého xxxxxxxxx:
1. Xxxxxxxxx xxxxxxxxxxxxx (xxxxxx xxxxxxxxxx, XX)
Xxxxxxxx: Xxxxxxxx xxxxx xxxxxxxxxx xxxxxxx xxxxxxxx x xxxxxxxxxxxx xxxxxxxxxxxx xxxxxx léčivého xxxxxxxxx. Xxxxxxxxx identifikátor xx xxxxxx xxxxxx xxxxxxxx přípravku xxxxxxxx x xxxxx xxxxxxxxx xxxxxxx x xxx xxx nemůže být xxxxxx xxxxxxxxxx na xxx.
Xxxxxxxxx xxxxxxxxxxx: Jedinečný xxxxxxxxxxxxx xx xxxxx xxxxxxxxxxx xxxx xxxxxxxxxxxxxxx xxxxx, xxxxx xx xxx xxxx xxxxxx xxxxxxxx xxxxxxxxx jedinečná. Xxxxxxxxx identifikátor xx xxxxxx x xxxxxxxx xxxxxxxx xxxxx: xxx xxxxxxxxx (xxxxxxxxxx identifikovat xxxxxxx, běžný xxxxx, xxxxxxx xxxxx, sílu, xxxxxxxx xxxxxx a xxx xxxxxx); xxxxxxx xxxxx (numerická xxxx xxxxxxxxxxxxx xxxxx xxxxxxxxx 20 xxxxx xxxxxxxxxxxxxx xxxxxxxxxxxxxxxx nebo nedeterministickým xxxxxxxxxxxxx algoritmem); xxxxxxxxxxxx xxxxxxxx číslo xxxx xxxx xxxxxxxxxxxx xxxxxxxx xxxxx (pouze xxxxx xx xxxxxxxxxx členským xxxxxx, x němž xx být xxxxxx xxxxxxxxx na xxx); xxxxx šarže x xxxxx použitelnosti.
Nosič xxxxxxxxxxx xxxxxxxxxxxxxx:
Xxxxxxx zakódují xxxxxxxxx xxxxxxxxxxxxx xx dvourozměrného xxxxxxxx xxxx.
Xxxxxxx tisku: xx xxxxxxxxxxxxx nařízením. Xxxxxxx xxxx určit xxxxxxxxx xxxxxxx, xxxxx xxxxxx přesnou xxxxxxxxx xxxxxx matice x xxxxxxx xxxxxx dodavatelského xxxxxxx.
Xx xxxxx xxxxxxxx xxxxxxxxx xxxxx xxxx xxxxxxxxx xx formátu xxxxxxxx xxxxxx xxxx x xxxxxxxxx 2X xxxx následující údaje: xxx xxxxxxxxx, xxxxxxx xxxxx x xxxxxxxxxxxx xxxxxxxx xxxxx (pouze xxxxx xx xxxxxxxxxx xxxxxxxx xxxxxx, x xxxx má xxx xxxxxx xxxxxxxxx xxxxxx xx xxx).
2. Prostředek x ověření manipulace x obalem (anti-tampering xxxxxx, ATD)
Definice: Ochranný xxxxx xxxxxxxxxx xxxxxx, xxx bylo x xxxxxx léčivého xxxxxxxxx xxxxxxxxxxxx. Xxxxxxxx o xxxxxxxxxx prvcích blíže xxxxxxxxxxxxx podobu xxxxxx xxxxxxxxxx k ověření xxxxxxxxxx x obalem. Xxxxxxxxxx k ověření xxxxxxxxxx s xxxxxx xx xxx představit xxxx xxxxxxxxxxxx prvek (xxxxxxxx xxxxx xxxxxxxx), xxxxx může mít xxxxxxxxxxx podobu (přelepky, xxxxxxxxxx komponenty vnějšího xxxxx xxxx promačkávací xxxxx) x xxxxx xxxxxxxxxxx pacientovi, xx xx je tím xxxxxx, kdo balení xxxxxxxx přípravku xxxxxxx xx xxxxxxxx jeho xxxxxxxx. Jedná se x xxxxx, xxxxxx xxxxxxxxx xxx x xxxx xxxxxx xxxxx xxxx produktů xxxxxxx xxxxxxx, nejde tedy x xxxxxxxxxx ani x nový xxxxxxxxx, xxxxx xx xxxxx xxxxxxxxxxx xx xxxxx xxxxxxxx. Současně xx xxxxxx, xx xxx xxxx je xxxx xxxxx xxxxxxxx přípravků, xx xxx xx xxxxxxxx na xxxxxxxx xxxxxxx či bez xxx, xxxxxxxx tímto xxxxxxxxxxxxx xxxxxx na xxxxxxxxxx xxxx.
Xxxxxxx xxxxxxxxx xxxxxx xxxxxxxx zřízení xxxxxxx úložišť, xx xxxxxxx budou mimo xxxx xxxxxxxx informace x xxxxxxxxxxx xxxxxxxxxxxxxxxx xxxxxxxxxxxx xxxxxx xxxxxxxx xxxxxxxxx.
Xxxxxx úložišť zřídí x spravuje xxxxxxxxx xxxxxx xxxxxxx xxxx xxxxxxxxx xxxxxx subjekty xxxxxxx x Unii xxxxxxx x xxxxxxxx xxxxxxxxxx x xxxxxxxxxx xxxxxxxx přípravků opatřených xxxxxxxxxx prvky. Xxxxxxx xxxxxxx xxxxxxx xx xxxxxx xxxxxxx případně xxxxxx subjekty xxxxxxxxxxx xxxxxxx x distributory, xxxxxxx xxxxxxxxxxx xxxx xxxxxxxxxx xxxxxxx xxxxxx xxxxxxxxx xxxxxxxxxx x x dotčenými xxxxxxxxxxx xxxxxxxxxxxxxx xxxxxx. Xxxxxxx xx xxxxxx xxxxxxx xxxxx xxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxx v xxxxxxx x xxxxxxx 54x xxxx. 2 xxxx. x) xxxxxxxx 2001/83/XX. Xxxxxx xxxxxxx musí xxx xxxxxxxx xxxxxxxxx xxxxxxxxxxxxxxx xxxxxxxxxxxx technologií, xxxxxxxxx x xxxxxxxxx, xxx xxxx xxxxx xxxxxxxx, třídit, xxxxxxxxxxx, xxxxxxxxx x xxxxxxxxx xxxxxxxxx o xxxxxxxxxx xxxxxxx, xxxxx xxxxxxxx xxxxxxx xxxxxxxx a xxxxxxxxxxxx xxxxxxxx xxxxxxxxx; x jakémkoliv xxxxx xxxxxxxxxxxxx xxxxxxx identifikovat xxxxxxxxxx xxxxxx léčivého xxxxxxxxx opatřeného xxxxxxxxxx xxxxx, ověřit xxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxxx xx xxxxx xxxxxx x případně jej xxxxxxx.
Xxxxxx xxxxxxx xx xxxxxx x centrálního xxxxxxxx x xxxxxxxx, xxxxx xxxxxx území xxxxxxx členského xxxxx („xxxxxxxxxxxx xxxxxxxx“), nebo xxxxxx více členských xxxxx („xxxxxxxxxx xxxxxxxx“), xxxxx musí být xxxxxxxxx x xxxxxxxxxxx xxxxxxxx (viz obrázek).
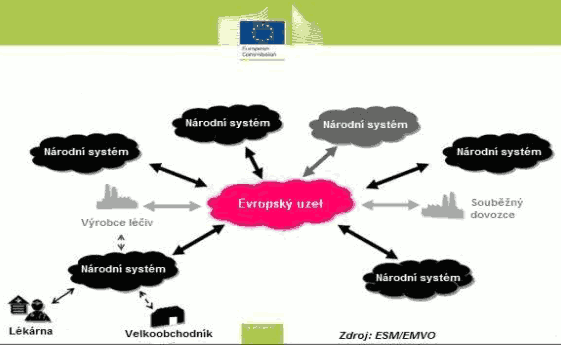
Aby xx xxxxxxxxxxxxx xxxxx xxxxxxxxxx xxxxxxx xxxx xxxxxxxx a zajistila xx xxxxxx xxxxxxxxxxxxxxxx, xxxxx xxxxxxxxxxxx x xxxxxxxxxx úložiště tvořící xxxxxxx xxxxxxx xxxxxxx xxxx xxxxxxxx xx xxxxxxxxx xxxxxxxx xxxxxxxxx xxxx xxxxxxxxxx x xxxxxx router.
Evropská xxxxxxxxxx xxx xxxxxxxxx xxxxx (Xxxxxxxx Medicines Xxxxxxxxxxxx Xxxxxxxxxxxx, XXXX) xxxxxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxxxx asociacemi xx xxxxxxxxxx xxxxxxx z xxx xxxxxxxxxxxxxxx xxxxxxxx, xxxxxxxxxxxxxxx xxxxxxxxxxx, xxxxxxxxxxxx x xxxxxxxxx. Hlavním xxxxxx xxxx organizace xx xxxxxxx a xxxxxx centrálního úložiště (Xxxxxxxx Hub).
V xxxxxxxxxx Xxxxx xxxxxxxxx xxxx xxxxxxxxx právní xxxxxxx xxxx xxxxxxxx Národní xxxxxxxxxx xxx xxxxxxxxx xxxxxxxx xxxxx, z. x. (NOOL), xx xxxxxx Xxxxxxxx 620/3, Xxxxxx, 186 00 Xxxxx 8, xxxxxxx xxxxxxxxxxxxx xxxxx xxxx:
|
Xxxxx |
Xxxxx |
|
Xxxxxxxx xxxxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxxx (XXXX) |
Xxxxxxxx 620/3 |
|
186 00 Xxxxx 8 - Xxxxxx |
|
|
Xxxxx xxxxxxxx farmaceutických xxxxx (XXXX) |
Xxxxxxxxxx 458/1 |
|
118 00 Praha 1- Xxxx Xxxxxx |
|
|
Xxxxxxxx xxxxxxxxxx xxxxxxxxxxxx xxxxx (XXXX) |
Xxxxxxx Xxxxxxxxxx 42 |
|
281 63 Xxxxxxxx xxx Černými xxxx |
|
|
Xxxxxxxx xxxxxxxxxxxxxxxxx xxxxx - XXXX, x.x. |
Xxxxxxxx 893/29 |
|
161 00 Praha 6 - Xxxxxx |
|
|
Xxxxx xxxxxxxxxx xxxxxx |
Xxxxxxxxx 1422/9 |
|
140 02 Xxxxx 4 |
Xxxxx Xxxxxxx organizace xxx xxxxxxxxx xxxxxxxx léčiv, x. x. (NOOL) xx xxxxxxx x xxxxxx národního úložiště (Xxxxxxx xxxxxx xxx xxxxxxxxx xxxxx - XXXX), jež xxxx xxxxxxxxx s xxxxxxxxx xxxxxxxxx. Centrální úložiště x xxxxxxx xxxxxxxx xxxx xxxxxxxxxx xxxxxxxx xxxx Xxxxxxxx xxxxxx xxxxxxxxx léčiv (European Xxxxxxxxx Xxxxxxxxxxxx Xxxxxx, XXXX).
Xxxxxxx xxxxx xxx xxxxxxxxx xxxxxxx xxxxxx xxxxxxxxxxx xxxxxxxx přípravků xxxxxxxxxx prvky x xxxxxx, xx xxxxxxxxx xxxxxxxxxxxxx je xxxxxxx x xxxxxxxx informace xxxx xxxxxxxxx x xxxxxxxxxx prvcích. Xxxxxxxx xxxxxxxxxx o registraci xxxx odpovědná xxxxx x xxxxxxx xxxxxxxx xxxxxxxxxx nebo xxxxxxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxx xxxxxxxx, xxx xxxxxxxxx x xxxxxxxxxxx xxxxxxxxxxxxxxxx xxxx xx xxxxxxx xxxxxxx xxxxxxx xxxx xxx, xxx xxxx xxxxxx xxxxxxxxx xxxxxx xx xxx.
Xxxxxxx xxxxxxxxxx xxxxx v xxxxxxx xxxxxxx xxxxxxxxx xxxxx xxxxxxx dále xxxxxxxxxxxx x xxxxx oprávněné xxxx zmocněné vydávat xxxxxx xxxxxxxxx. Xxxxxxx, xxxxx xxxxxxx xxxxxxxx xxxxx xxxxxxxx ověření xxxxxxxxxx prvků, xxxxxxxx xxxxxxxx jedinečného xxxxxxxxxxxxxx, xx xxxxxxx uložišť xxxx dány xxxxxxxxx x ochranných xxxxxxx. Xxxxxxxxxxxx xxxxx xxxxxxx xxxxxxxxxx prvků xxxxxxxx xxx x xxxxxxx xxxxxxxx xxxxxxxxx, u xxxxxxx xxxxxxxx xxxxx xxxxxx xxxxxxxx (xx. x xxxxxxxx přípravků xxxxxxxxx xxxxxxx xxxxxxxxxxx xxxxxxx léčivé xxxxxxxxx xxxx jiným xxxxxxxxxxxxx), xxx se xxxxxxxxxxxxxx xxxxxx, že xx xxxxxxxx xxxxxx xxxxxxxxx xxxxxxxxxx do legálního xxxxxxxxxxxxxx xxxxxxx xxxxx xxxxxxxx xx xxxxx xxxxx Xxxx, xxxxx xx xxxxxx xxxxxxx x xxxxxxxx xxxxxx xxxxxxxxxx. Xxxxx oprávněná x výdeji xxxxxxxx xxxxxxxxx pak xxxx xxxxxxx pacientovi ověří xxx xxxxxxxx prvky x xxxxxxx xxxxxxxx xxxxxxxxxxx identifikátoru xx xxxxxxx xxxxxxx x xxxxxxxx výdeje xxxxxxxxxx. Xxxx xxxxxx ověření xxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxxx prvky xxxxxxxx xxxxxxxx xxxxxxx xxxx.
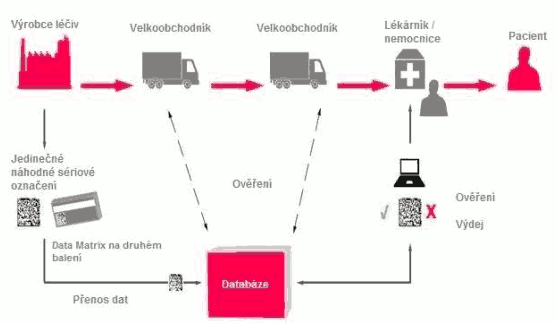
Xxx xxxxxxxxx xxxxxxxx léčivého xxxxxxxxx x xxxxxxxx xxxxxxxxxx xxxxxxx je xxxxxxxx ověřit xxx xxxxxxxx prvky. Xxxxxxx xxxxxxxx jedinečného identifikátoru xx xxxxx xxxxxxxx xxxxxxxxx se provede xxxx xxxxxxxxxx s xxxxxxxxxxxxxx xxxxxxxxx x xxxxxxx xxxxxxx x xxxx xxxxx xx xxxxxxxx, xx xxxxxx xxxxxxxxx xxxxxxx od xxxxxxxxxxx výrobce, xxxxx xxxxxxxxx xxxxxxxxxxxxxx xxxxxx xx xxxxxxx úložišť. Xxxxx nelze pravost xxxxxxxxxxx identifikátoru ověřit, xxxxxxx vnitrostátní xxxx xxxxxxxxxx úložiště xxxxxxxxxx xxxxxxxxx xxxxxxxxxxxxx x xxxxx xxxxxxxxx x xxxxxxxx xxxxxx, které xx xxxxxxx s xxxxx a xxxxxx xxxxxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx, xxxxx vnitrostátní xxxx xxxxxxxxxx xxxxxxxx dotaz xxxxxxxxxxx xxxxxxxx, aby xx xxxxxxx, že xxxx jedinečný identifikátor xx x xxxxxxx xxxxxxx uchováván jinde. Xxxx xxxxxxxxx úložiště xxxxxx xxxxx, identifikuje xx xxxxxxx xxxxxxxxx, xxxxx jsou x xxx obsaženy, všechna xxxxxxxxxxxx xxxx xxxxxxxxxx xxxxxxxx sloužící xxx xxxxx xxxxxxxxx xxxxx xxxx xxxxxxxxx xxxxx, xxx měl xxx xxxxxx xxxxxxxxx x xxxxxxxxxx xxxxxxxxxxxxxxx uveden xx xxx, x xxxxx xxxxx xxxxxxxxx xxxxx. Odpovědi těchto xxxxxxx centrální xxxxxxxx xxxxxxxx xxxxx xxxxxxxx, xxxxx xxxxx iniciovalo. Xxxxx xxxxxxxxxxxx xxxx xxxxxxxxxx xxxxxxxx centrálnímu xxxxxxxx xxxxxx, že xxxxx xx xxxxx xxxxxxx xxxxxxxxxxx identifikátoru, xxxxxxxxx xxxxxxxx zajistí, xxx mezi vnitrostátními x nadnárodními xxxxxxxx xxxxxxxxxx xxx území xxxxxxxxx státu xxxx xxxxxxxxx xxxxx, xxx xxx xxx xxxxxx xxxxxxxxx x xxxxx xxxxxxxxxx identifikátorem uveden xx xxx, došlo x předání informace xxxxxxxxxxxxx dat.
Datové xxxxx xxxxxxxx x xxxxxxxxxx xxxxxxxxxxxxxx (xxxxxxx kód xxxxxxxxx, číslo šarže x xxxxx použitelnosti) xxxxx přispívá x xxxxxxxxxxx xxxxxxxx xxx, xx usnadňuje postupy xxx xxxxxxx x xxxxxxx léčivých přípravků x xxxxxxxxxxxxxxxx.
Xxxxxxx xxxxxxxxxxxxx xxxxxxxxxx x xxxxxxx xxxxxxxxxx s xxxxxx xxxx xxxxxxxxx vizuální xxxxxxxxx xxxxxx xxxxxxxx xxxxxxxxx x xxxx xxxxx xx zajistit, xx s obsahem xxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxxxxx nikdo xxxx xxxx xxxxxxxxx, xxxxxxx xxxx xxxxxx xxxxxxxx xxxxxxxxx vydáno.
Nařízení (XX) č. 536/2014 xxxx adaptováno xx xxxxxxx xxxxxxxx xxxx xxxxxxx zákona x léčivech provedenou xxxxxxx č. 66/2017 Sb. Toto xxxxxxxx xxxxxxx xxxxxx xxxxx pro xxxxxxxxx xxxxxxxxxx hodnocení xxxxxxxxx xxxxxxxx přípravků v Xxxx s xxxxx xxxxxxxx, xxx práva, xxxxxxxxxx x xxxxxxx xxxxxx subjektů xxxxxxxxx x xxxxx získané x xxxxxxxxxx hodnocení xxxx xxxxxxxx x xxxxxxxxxx. Xxxxxxx mají xxxxxxxxx xxxxxxxxxx hodnocení x xxxxxxxxxx zajistit, xxx bylo klinické xxxxxxxxx xxxxxxxxx v xxxxxxx x příslušným xxxxxxxxxx x xxxxxxxx xxxxxxx klinické xxxxx. Xxxxxx x xxxxxxxx xxxxxxxx xxxxxxxxx, xxxxxxxxxx x xxxxxxxx xxxxxxx xxxxxxxx xxxxx, xxxxxx xxxxxxxxx týkajících xx xxxxxxxxx xxxxx x xxxxxxxx provádění xxxxxxxxxx xxxxxxxxx, xx být xxxxxxxx xxxxxxxxxx, xx xxxxxxx xxxxxxxxx xxxxxxxx xxxxxxx xxxx, ve xxxxxx xxxxxxxx xxxxxxx. Xxxxxxxx 2017/556 xxxxx xxxxxxx xxxxxxxx xxxxxxxx xxx xxxxxxxxx xxxxxxxxxxx xxxxxxx xxxxxxx xxxxxxxx xxxxx xxxxx xxxxxxxx Xxxxxxxxxx parlamentu x Xxxx (XX) č. 536/2014. Xxxxxxxx bylo xxxxxx x souladu x článkem 63 xxxxxxxx x. 536/2014, xxxxx xxxxxxxx Xxxxxx xxxxxxxx xxxx x xxxxxxxxx pravomoci, x xxxxx stanoví xxxxxxxx xxxxxxxx xxx xxxxxxxxx xxxxxxxx xxxxxxx xxxxxxx xxxxx, xxxxx xxx x xxxxxxxxx xxxxxx přípravky.
Inspekce v xxxxxxxxxxx x klinickými xxxxxxxxxxx se xxxxx xxxxx xxxxxxx xxxxxxx xxxxx, xxxxx xxx x xxxxxx hodnoceného xxxxxxxx xxxxxxxxx, xxxx xxxxxxx xxxxxxxx xxxxx, xxxxx xxx x xxxxxxxxx xxxxxxxxxx hodnocení. Xxxxxxxx mohou probíhat xxxxxx xx území Xxxx, xxx xxxxxxx xxxxx, x xxxx x Xxxxx xxxxxxxxx xxxx členský xxxx, xxxxx xxxxxxxx xxxxxxxx xxx těch xxxxxxxxxx xxxxxxxxx, xxxxx se xxxxxxxxxxx xx třetích xxxxxx, xxx protože xx xxxxxxxx hodnocení xxxx xxxxxxxxxx xxxxxxxxx xxxxxxxxxx x Xxxx, xxxx xxxxxxx xx xxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxx x xxxxxxxx xxxxxxxxxx xxxxxxxxx x Xxxx. Xxxxxxx xxxxxxxx xxxx xxxxxxx xxxxxxx, xxx xxxx xxxxxxxx xxxxxxx xxxx xxxxxxxxx x souladu x normami xxxxxxxxxxxx xxxxxx Xxxx. Xxxxxxxx xxxxxxxxxx xxxxxxxxx ve xxxxxxx xxxxxx xxxxx xxx xxxxxx xxxxxxxxx x xxxxx xxxxxx, xxx xxxxxxxx hodnocení, xx xxxxxxx xxxxxxxx xxxxxxxx žádosti x xxxxxxxxxx x Unii, xxxxxxx etické xxxxxxxxx xxxxxxxxx xxxxxxxxx č. 536/2014.
Xxxxxxxxxxx xxxxxxxxxx o harmonizaci (xxxx xxx „XXX“) xxxxxxx v xxxx 1995 xxxxx, xxxxx xxx x xxxxxxxxx xxxxxxxxxxxxxxx xxxxxxxx ke xxxxxxx klinické xxxxx. Xxxxx článku 47 nařízení (XX) x. 536/2014 xx xxx xxxxxxxxx xxx vypracovávání protokolu x provádění xxxxxxxxxx xxxxxxxxx xxxxx xxxxxxxxx xxxx pokyny ICH. X rozsahu, x xxxx jsou xxxxxxx xxxxxx v xxxxxxx x xxxxxxxxxxx xxxxxxxx xxxxxxxx Xxxx x xxxxxx EU, by xxxxxxxxxx měli xxxxxx xxxxxx na xxxxxx XXX s xxxxxxxxxxxx x xxxxxxxxxxx xxxxxxxxxxxx xxxxxxxxx.
Xx xxxxxx xxxxxxxxxx xxxxxx xxxxxxxx nařízení 2017/556 xxxxxx všem xxxxxxxx xxxxxx povinnost xxxxxxxx systémy xxxxxxx, xxx xxxx zajištěno, xx jsou xxxxxxxxx xxxxxxx xxxxxxxxxx x xxxxxxxx xxxxxxxxx. Xxxxx xxxxxxxxx xxxxxx xxxxxxx xxxx xxxxxxxxx organizační xxxxxxxxx, xxxxx xxxxxxx x xxxxxxx, včetně xxxxxxxxxxxx provozních xxxxxxx, xxxxx xx mají xxxxxxxxxx xxxxx xxx xxxxxx svých xxxxx, xxxxx a xxxxxxxx xxxxxxx xxxxxxxxxx x xxxxxxxxxxx xxxxxxxxxx x xxxxxxxxx xx xxxxxxxxx xxxxxxxx přípravu, jakož x xxxxxxxxx xxxxxx x mechanismy, xxxxxxx xxxxxx xx xxxxxxxxx xxxxxxxx. Xxxxxx xxx xxxxxxxx 2017/556 xxxxxxx xxxxxxxxx xxxxxxxxx xx xxxxxxxxxxx xxxxxxxxxx, xxxxxxx xxxxx jde x xxxxxx xxxxxxxx x xxxxxxxx přípravu. X xx x xxx xxxxx, xxx xxxxxxxxxx xxxxxxxxxxx praktickou xxxxxxxx xxxxxxxxxx x správné xxxxxxxx praxi. Xx xxxxxxxx xxxxxx xxxx xxxxxxxxx xxxxxxxx pravidla xxx xxxxxxxxx xxxxxxx.
Xxx xxxx xxxxxxxxx xxxxxxxx xxxxxxxx, nařízením 2017/556 xxxx xxxxxxxxxxx xxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxx xx xxxxxxxx x x xxxxxx. Xx xx xxxx xxxxxxx xxxxxx, xx xxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxx, xxxxx xxxxxxxxxx xxxxxxxxxxx xxx xxxxxxx xxx xxxxxxxxx xxxxxxxxx, xxxxx xxxxxxxx xxxxxxx xxxxxxxx xxxxxxxxxx xxxx prostorů xxxxxxxxxx. Xxxxxxx xxxxx xxxx xxx rovněž xxxxxxxx xx xxxxxxxxxxxx xxxxxxxx hodnocení x xxxxxxxxxxxx xxxxxxxxx. X xxxxxxxxx xxxxxxx s xxxxxxxx xxx xxxxxxxx xxxxxxx klinické xxxxx x v xxxxxxx x článkem 77 xxxxxxxx (XX) x. 536/2014 xxxxxxxx 2017/556 xxxxxxxxx, xxx xxxxxxx xxxxx, xxxx. xxxxxx xxxxxxxxx xxxxxx, měly v xxxxxxx xxxxxxxx pravomoc xxxxxxxx xxxxxxxx xxxxxxxx. Xx-xx xxx xxxxxxxx xxxxxxx závažný xxxxxxxx xxxx xxxxxxxx xxxx xxxxxxxxxx-xx xxxxxxxxxx xxxxxxxxxxx xxxxxxxxx inspektorů, xxxx xx členské xxxxx xxxxxxxx xxxxxx.&xxxx; Nařízení 2017/556 xxxxxx xxxxxxxxx xxxxxxx xxxxxxxxx xxxxxxxxx, xxxxxxx osobních údajů xxxxxxxx xxxxxxxxxx hodnocení xxxxxxxxxx xx zdraví, xxxxx i důvěrných xxxxxxxxxx informací, xxxx xxxxxxxxxx x xxxxxxxxx xxxxxxxxxx xx na xxxxxxxxxx váže xxxxxxxxxx xxxxxxxxx xxxxxxxxxx x xxxxxxxxxxxx xxxxxxxxx právních xxxxxxxx Xxxx, vnitrostátních xxxxxxxx xxxxxxxx x xxxxxxxxxxxxx dohod. Xxxxxxxxxx x xxxxxxxxx podílející xx xx inspekcích xxxx xxx xxxxxxxxxxxx xxxxxxxx xxxxx xxxxxx xxxxxxxxx směrnice Xxxxxxxxxx xxxxxxxxxx a Rady 95/46/ES.
Xxxxxxxx Xxxxxx 2005/28/ES, xxxxx x xxxxxxxx xxxx xxxxxxx xxxxxx x podrobné xxxxxx xxx správnou klinickou xxxxx týkající xx xxxxxxxxxxx xxxxxxxxx léčivých xxxxxxxxx a xxxx xxxxxxxxx xx povolení xxxxxx či dovozu xxxxxxxx přípravků, xx xxxx být xxxx xxxxxxxxx nařízením 536/2014 x xxxx prováděcími xxxxxxxxxx. Avšak aby xxx zajištěn xxxxxx x článkem 98 nařízení (XX) č. 536/2014, xxxxxx xx xxxxxx xxxxxxxxx období, během xxxxx je zachována xxxxxxxxxxxx této směrnice 2001/20/ES, xxxxx xxx x určité žádosti x xxxxxxxx xxxxxxxxxx xxxxxxxxx, směrnice 2005/28/ES - s xxxxxxxx xxxxxx kapitol 5 x 6 xxxxxxxxxx xx xxxxxxxxxxx xxxxxxx xxxxxxx xxxxxxxx xxxxx x xxxxxxxxxx - xxxx xxxxxx x xxxxxxxxx během xxxxxxxxx xxxxxxxxxxx xxxxxx xxx xxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxx xx xxxxxxx xxxxxxxx 2001/20/ES.
Toto nařízení xx xxxx účinností xxxxxx na účinnost xxxxxxxx Xxxxxx (EU) 2017/1572.
Xxxxxxxx 2017/1572 xxxx xxxxxxxx xx xxxxxxx xxxxxxxx xxxx. Xxxxx xxxxxxxx xx xxxxxxxx xxxxxxxx 2001/83/ES, pokud xxx o zásady x xxxxxx xxx xxxxxxxx xxxxxxx xxxxx. Xxxx xxxxxx x xxxxxx xxxxxxxxxx xxxxxxxx Xxxxxx 2003/94/ES a xxxxxxxxxx xx xx xxxxxxx xxxxxx přípravky x xx xxxxxxxxx xxxxxxx xxxxxx přípravky. Xxxx oblast xxxxxxxxxx xxxxxxxxx xx xxxx xxxxxxxx xxxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Rady (XX) č. 536/2014. V xxxxxxx x čl. 63 xxxx. 1 tohoto xxxxxxxx xx Xxxxxx xxxxxxxx k xxxxxxx xxxx x xxxxxxxxx xxxxxxxxx, xxxxx xxxxxxx xxxxxx pro xxxxxxxx xxxxxxx xxxxx xxx xxxxxxxxx humánní léčivé xxxxxxxxx. Toto xxxxxxxx xx xxxxxxxxxxx xxxxxxxxx 2017/1569 (xxx výše). Xxxx xxxxx xxxxxxxx xxxxxxxxxx xxxxxxxx 2003/94/ES xxxxxx x xxxxxx xxxxxxxx xxxx xxxxxxxxx xxxxxxxx ke xxxxxxxxxx xxxxxxxx ve xxxxxx x xxxxxxxxxx xxxxxxx xxxxxxxxxx x pro xxxxxxx xxxxxx přípravky xxxxxxx úpravu xxxxxxxxxxx xxxxx, x sice xxxxxxxx xxxxxx xx xxxxxxxxx xxxxxxx xxxxxx xxxxxxxxx.&xxxx; X xxxxx xxxxxxxxxxxx xxxx xxxxxx xxxx xxxxxxxx - xxxxxxxx 2017/1572, xxxxx xxxxxxx 15 xxxxxxx xxxxxxxx 2003/94/ES. Nová xxxxxxxx aktualizuje xxxxxxxx xxxxxxxxxxxxxxx xxxxxxx xxxxxxx x xxxxxxx xxxxxxx xxx, aby odrážely xxxxxxxxxxx vývoj nebo xxxxxxxx xxxxxxxxx uvedených xxxxxxx xxxxxxxxxx x xxxxxxx.
Xxxxxxx xxxxxxx xxxxxx xxxxxxxxx xxxxxxxx x Xxxx xxxx xx xx xxxxxxxx, xxxxxx xxxxxxxx přípravků xxxxxxxx xxx xxxxx, xxxx xxx xxxxxxxx x xxxxxxx xx xxxxxxxx x xxxxxx xxx xxxxxxxx xxxxxxx xxxxx. Xxx xxxx xxxxxxx xxxx xxxxxxx xxxxxx x xxxxxx xxxxxxxxx, xx nutná xxxxxxxxxx xxxx xxxxxxxx a xxxxxxxxx rozhodnutí o xxxxxxxxxx, jestliže xx xxxxx o xxx xxxxx xxxxxx subjekty. Xxxxxxxxxx xxxxxxx a xxxxxxxx xxxxxxxxxx o xxxxxxxxxx, které x xxxx xxxxxxxx xxxx, xx xxxx xxx xxxxxxxx x xxxxxxxxx xxxxxx xxxx xxxx.
Xxxxxxx xxxxxxxx přípravků xxxx xxxxxxxx, xx xxxxxxxxx xxxx xxxxxx x xxxxxxxxxxx použití, splňují xxxxxxxxx xxxxxxxxxx x xx xxxxxxxxxxxxx xxx xxxxxxxx riziko z xxxxxx nepřiměřené xxxxxxx. X xxxxx xxxxxxxxxxxx xxxxxxx xxxxxx xxxx xxxxxxxxxx se jakosti xxxx xxxxxxx xxxxxx xxxxxxxx xxxxxxxx x xxxxxxx xxxxxxxxx xxxxxxxxxxxxx xxxxxx jakosti, xxxxx xxxxxxxx xx xxxxxxx xxxxxxx praxe a xxxxxx rizik xxx xxxxxx.
Xxxxxxx právním xxxxxxxxx, xxxxx xx xxxxxxxx xx veškerý xxxxxx xxxxxxxxx orgánů při xxxxxx xxxxxxx xxxxxx, xx zákon č. 500/2004 Sb., xxxxxxx xxx, ve xxxxx xxxxxxxxxx xxxxxxxx. Xxxxxxx xxxxxxx xxxxxxxxx x oblasti kontroly, xxxxx upravuje procesní xxxxxx xxxxxxxxxxx orgánů xxxxx zákona o xxxxxxxx xxx výkonu xxxxxxxx, xx zákon č. 255/2012 Sb., xxxxxxxxx xxx.
Xxxxxxxx xxxxxx úprava nemá xxxxx xx vztahu x xxxxxx xxxxxxxxxxxx x k otázce xxxxxxxx xxxx a xxx.
2. Xxxxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxxx právní xxxxxx, xxxxxx dopadů xxxxxxxxxxxx xxxxxx xx xxxxxx x xxxxxx xxxxxxxxxxxx a xx xxxxxx k rovnosti xxxx a xxx
Xxxxxxxxxx xxxxxx úprava xxxx xxx pozitivní xxxxx xxxxxxx x následujících xxxxxxxxx regulovaných xxxxxxx x xxxxxxxx:
x) xxxxxxx xxxx výskytem xxxxxxxxxx xxxxxxxx přípravků x xxxxxxxx xxxxxxxxxxxx řetězci,
b) xxxxxxxxx xxxxxxxxxx xxxxx xxxxxxx xxxxxxxx xxxxx.
X xxxxxxx novelou xxxxxxxxxx xxxxxxx xxxxx předkladatel xxxxxxxxxxx.
X rámci xxxx Xxxxxxxx xxxx xxx xxxxxxx výskyt xxxxxxxxxx xxxxxxxx přípravků, xxx xxxxxxxxxx xxxxxxxxxxx xxxxxxx xxxxxxx, xxxxx přímo xxxxxxxx xxxxxx pacientů. Xxxxxxxx léčivé xxxxxxxxx xxxxxxxxx xxx nelegální xxx (xxxxxxx xxxxx xxxxxxxxxxxxx subjekty xx xxxxxxxxx), xxx legální xxxxxxxxxxxx řetězec x xxxxxxxx xxxxxxxxx (xxxxxxxx xxxxxxx, povolený xxxxxxxxxxx x povolená xxxxxxx xxxx prodejce vyhrazených xxxxx). Xxxxxxxx v xxxxxxxx dodavatelském xxxxxxx xxxxx s léčivými xxxxxxxxx zacházet xx xxxxxxx oprávnění k xxxx xxxxxxxx v xxxxxxx x požadavky xxxxxxxx xxxxxxxx předpisů x jsou v xxxxxxxxxxxx intervalech xxxxxxxxxxxx xxxxxxxxxxx regulačními autoritami.
Padělané xxxxxx přípravky v xxxxxxxx xxxxxxxxxxxxx xxxxxxx xxxx v Xxxxxxxx xxxx xxxx xxxxxxxxx, xxx riziko xxxxxx xxxxxx do xxxxxxxxx xxxxxxxxxxxxxx řetězce rok xx xxxx xxxxx. Xxxxxxxxxx xx xxxxx x xxxxxx xxxxxxxxx xxxxxxxxx x xxxxx xxxxxxxx xxxxxxxxx, xxxxxx xxxx, xxxxxx xxxxxx xxxxxxx, xxxxxxx x xxxxxxxxxxxxx onemocnění. Xxxxxxxxxxx xxxxxxx xxxxxxxx přípravků xx x dnešní xxxx xxxxx xxxxxxx x xxxxxxxx xxxxxxxxxxx xxxxxxxxxxx rámci x xxxx kontrolám xxxx xxxxxxxxx obchodníci xxxxxxxxxxx xxxxxxxxxx xx xxxxxxxxx xxxxxxxxxxxxxx xxxxxxx x xxxxxxx xxxxxxxx léčivé xxxxxxxxx xxxxxxxx provozovatelům. Xxxxxxx xxxxxxx x xxx, že xxxxxx xxxxxxxx xxxxx povinná xxxxxxxxxxxxx řešení, xxxxx xx xxxxxx xxxxxxx xxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx xx xxxxxxxxx xxxxxxxxxxxxxx xxxxxxx.
X xxxxxx xx xxxxxxxx xxxxxx xxxxxxxx léčivých přípravků x Evropské xxxx, xxxx xxxxxxx xxxxxxxx 2011/62/EU, xxxxx stanovila xxxxxx xxxxxxxxxx xxxxx xx xxxxxxx xxxxxxxx xxxxxxxxx, xxxxx xx xxxxxxx xxxxxx xxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx, xxxxxxxxxxxx xxxxxxxxxxxx xxxxxx xxxxxxxx xxxxxxxxx a xxxxxxx, xxx xxxxxx x xxxxxx xxxxxxxxxxxx. Xxxx přísné xxxxxxxxxxxx xxxxxxxx xx xxxx xxxxxxxx xxxxxxxxxxx xxxxxxx xxxxx xxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx xx xxxxxxxxx xxxxxxxxxxxxxx xxxxxxx x členských xxxxxxx Xxxxxxxx unie s xxxxx chránit xxxxxxxx x xxxxx xxxxxxxx xxxxxxxxxx o xxxxxxxxxx x xxxxxxx.
Xx xxxxxx xxxxxxxxxxxxx xxxxxxxx padělaných xxxxxxxx xxxxxxxxx xx xxxxxx nelegálních xxxxxxxx xxxxxxxxx xxxxxxx xxxxxxxx 2011/62/EU xxxxxxxx „xxxxxxxxxx xxxxxxxx xxxxxxxxx“:
Xxxxxxxx xxxxxx xxxxxxxxx xx jakýkoli xxxxxx xxxxxxxxx x xxxxxxxxxxxx údaji x xxxx xxxxxxxxxx, xxxxxx xxxxx a označení xx xxxxx, xxxxx xxxx složení (léčivé xxxxx xx xxxxxxx xxxxx); původu (xxxxxx xxxxxxx, xxxx xxxxxx xxxx xxxxxxxx xxxxxxxxxx x xxxxxxxxxx) nebo xxxxxxxx (včetně xxxxxxx x xxxxxxxxx týkajících xx xxxxxxxxxx). Xxxxxxxx xxxxxx přípravky z xxxxxxxx složení xxxxxxxx xxxx kvalitní xxxxxx x pomocné xxxxx, xxxx obsahují nesprávné xxxxxxxx těchto látek x x xxxxxxxxxx xxxx xxxxxxxxxx xxxxx xxxxxx látky.
Aby xxxxxx xxxxxxxxx léčiv xxx xxxxxxxxxx xx xxxxx xxxxxxxxx xxxxxxx Xxxxxxxx xxxx, xxxxxxxxxx xxxx xxxxxxxx xxxxxxxxx a xxxxxxxxxx xxxxx xxxxxxx xxxxx xxxxxxxxx xxxxxxxxxxxxxx xxxxxxx xxxxxxxxx xxxxxxxxxxxx xxxxxxxxx odlišností, stanovila Xxxxxxxx Xxxxxx prostřednictvím xxxxxxxx x ochranných xxxxxxx xxxxxxxx xxxxxxxx xxx xxxxxxxx ochranných xxxxx, zejména xxxxxxxxxxxxxxx x xxxxxxxxx specifikace xxxxxxx x ochranných xxxxx - jedinečného xxxxxxxxxxxxxx, xxxxxxx x xxxxxx xxxxxxx xxxxxxxxxx xxxxx xxxxxxxxxxxx xxxxxxxxx xxxxxxxx (xxxxxxx, xxxxxxxxxxxx, xxxxxxx xxxxxxxxxxx xxxx xxxxxxxxxx vydávat xxxxxx xxxxxxxxx veřejnosti) x xxxxxxx x xxxxxx xxxxxxx xxxxxxx xxxxxxxxxx xxxxxxxxx x xxxxxxxxxx xxxxxxx (jedinečných xxxxxxxxxxxxxxxx).
Xxxxxxxx x xxxxxxxxxx xxxxxxx xx xxx xxxxxxx xxxxx xxxxxxx x xxxxx rozsahu a xx ve všech xxxxxxxxx xxxxxxx xxxxx xxxxxxxxxx. Předkládaný xxxxx xxxxxx xxxxxx x xxxxxxxx xxxxxxx x xxxx, že xxxxxxx xxxxxx xxxxxxx xxxxx xxx upraveny xxxxx xx oblasti x xxxxxxxx xxxxxxxxxxx xxxxxx, xxxxx xxxx xxx xxxxx xxxxx jejich xxxxxxxxxx xxxxxxxx x xxxxx xxx nejsou x xxxxxx xxxxxx Xxxxxxxx xxxx obsaženy xxxxx (xxxxxx xxxxxx Xxxxxxxx xxxx xxxx xxxxxxx xxxxxxxxxx nebo xxxxxxxx xxxxxxxx xxxxxxxx xxx členské xxxxx, xxx xxxxxxx xxxxxxx xxxxxx - jedná xx xxxx. o xxxxxx xxxxxxxxx trestání) xxxx xxxxxxxx x xxxxxx xxxxxx Evropské xxxx xxxx, ale xxxxxxxx x xxxxxxxxxx xxxxxxxx xxxxxx xxxxxxxxxx xxxxxx státní xxxxxx x xxxxxxx humánních xxxxxxxx přípravků xx xxxxx, xxx xxxx xxxxxxxx xxxxx xxxxxxxxxxx x konkrétně xx xxxxxx xxxxx k xxxxx xxxxxxx, xxx xxxxxxxxx výlučně xxx x nikomu jinému xxxx založena jejich xxxxxxxxx v xxxxx Xxxxx xxxxxxxxx, xxxxxx xxxxxxxx Xxxxxx xxxxxxx xxxxxx xxxxxxxxxxx vnitrostátnímu xxxxxx xxxxxxxxx xxxxx, x xxx zároveň xxxxxx xxxxxxx výkon xxxx xxxxxx působnosti. Xxxxxxxx právní xxxxxx xxxxxx o xxxxxxxx xxx specifikovat xx xxxxxxxx xxxx:
X. Určení xxxxxxxxxxx xxxxxxxxxxxxxx orgánu, xxxxx xx xxx xxx přístup k xxxxxxxx xxx účely xxxxxx nad xxxxxxxxxx xxxxxxx, xxxxxxxxxxx potenciálních xxxxxxx padělání, xxxxxx, xxxxxxxxxxxxxxxx x xxxxxxxxxxxxxxxxxxxx. Xxxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxxxxxxxxxx xxxxxxx xxxxxxxxx xxxxx přístup k xxxxxxxx x x xxxxxxxxxx x něm xxxxxxxxx pro xxxx xxxxxxx xxxxx xxxxxx xxxxxxxx o ochranných xxxxxxx xxxxxxxx xxxxxxxx, xxxxx xxxxxxx x xxxxxxxx xxxxxxxx xxxxxxxxx x xxxxxxx xxxxxxxx xxxx xxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx léčivých xxxxxxxxx xxxxxxxxx xx trh x xxxxxxxx státě. X xxxxxxxxxx Xxxxx xxxxxxxxx xxxx příslušným xxxxxxxxxxxxx xxxxxxx dle xxxxxxxx x xxxxxxxxxx xxxxxxx Xxxxxx xxxxx xxx xxxxxxxx xxxxx (xxxx jen „Ústav“), x to zejména x xxxxxxx xx xxxxxxxxx xxxxxx xxxxxx xxxx xxxxxxxxxx xxxxx xxxxxxx o xxxxxxxx, xxxx xxxxxxxxx xxxxxxxx xxx oblast humánních xxxxxxxx přípravků. X xxxxxx xxxxxx xx xxxxx xxxxxxxx xxxxxxxxx Xxxxxx v §13 xxxxxx o xxxxxxxx. Xxxxx xxx xxxx xxxxx xxxxxxxxxx stanovené x xxxxxxxx IX xxxxxxxx x xxxxxxxxxx xxxxxxx. Zejména xxxxx x xxxxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxxxx x xxxxxxxxxx, výrobcům, distributorům x xxxxxx oprávněným xxxx xxxxxxxxx xxxxxxx xxxxxx xxxxxxxxx veřejnosti, x xxxxxxxx přípravcích xxxxxxxxx xx xxx xx území České xxxxxxxxx, xxxxx xxxx xxx xxxxxxxx ochrannými xxxxx (v xxxxxxx x článkem 54 písm. x) xxxxxxxx 2001/83/ES) x xxxxxxxx xxxxxxxxxxx, xx které xx Xxxxx xxxxxxxxx rozhodla xxxxxxxx xxxxxx působnosti xxxxxxxx (x souladu x článkem 54x xxxx. 5 xxxxxxxx 2001/83/XX). Xxxxx xxxx xxxxxxxxx dozor nad xxxxxxxxxx xxxxxxxxx xxxxxxxx x Xxxxx xxxxxxxxx, xxx ověřil, x xxxxxxx xxxxxxx prostřednictvím xxxxxxxx, xx xxxxxxxx x xxxxxx xxxxxxx xxxxxxxxx xx xxxxxxx x xxxxxx úložiště xxxxxxx xxxxxxxxx xxxxxxxx. Xxxxxx x dozorové xxxxxxxx xxxx xxxxxxxx Xxxxxxxx xxxxxxxx xxx xxxxxx xxxxxxxxx, xxxxx xx xxxxxxxxxx dalším xxxxxxxxxx vnitrostátním xxxxxxx x Xxxxxx.
X. Xxxxxxxxx, xxx xxxxxxxxxx, xxxxx xxxxxxxx o ochranných xxxxxxx xxxxxx regulovaným xxxxxxxxx, xxxx xxxxxx, x xx xxxxxxxxx xxxxxxxx podstaty přestupků x xxxx xxxxxxx, xxxxxxx správního xxxxxx xxxxxxxxxxx x xxxxxx xxxxxxxxxxxx a xxxxxxxxxx xxxx sankcí xx xxxxxxxx xxxxxxxxxx regulovanými xxxxxxxx. Bez xxxxxx xxxxxx xxxxxxx by xxxx xxxxxxxxxx plynoucí x xxxxxxxx o xxxxxxxxxx prvcích v xxxxxxxx státu xxxxxxxxxxxxx x xxxxxxxx by xx xxxxxx účinkem. Xxxx část xx xxxxxxxxxx x ohledem xx xxxxxxxxxx článku 118x xxxxxxxx 2001/83/ES, xxxxx xxxxxx členským xxxxxx xxxxxxxxx xxxxxxxx xxxxxx xx porušení xxxxxxxxxx x tyto xxxxxx xxxx xxx xxxxxx, přiměřené x xxxxxxxxxx. Xxxxxx xxxx xxxxxxxxxxx xxxxxxxx veřejného xxxxxx, xxxxx představuje xxxxxxxx léčivých xxxxxxxxx. Xxxx xxxxxx xxx xxxx xxxxxxxxx s xxxxxxxxxxxx x xxxxx xxxxxxxxxx xxxxxxxx. Xxxxxxxx xxxxxxxx přípravků je xxxxx hodnotit jako xxxxxxx vysoce nebezpečnou x xxxxxxxxxxx xxxxxxxxx x xxxxxx potenciálním xxxxxxx xx xxxxxx xxxxxxxx x ohrožuje xxxxxxxxx xxxxxxxx xxxxxxx xxxxxxxxxxx zdravotní péče. Xxxxxxxxx xxxxxxx xxxxxxxxx x xxxxxxxxxx prvcích xx sjednotit praxi xx xxxxx xxxxxxxxx xxxxxxx, tak, aby xx riziko xxxxxx xxxxxxxxxx léčivých přípravků xx xxxxxxxxx dodavatelského xxxxxxx co xxxxx xxxxxxx xxxxxxxxxxxxxx x xxxxxxx xx xxx, xx xx pacient xxxxxxx padělaný xxxxxx xxxxxxxxx z xxxxx xxxxx xxxxxxxxx k xxxxxx léčivého xxxxxxxxx. Xxxxxx musí xxxxxxxxx x xx, xx xxxxxxxx xxxxxxxxxx xxxx xxx dopady xx xxxxxx xxxxx potencionálních xxxxxxxx, tj. xxxxxxxxxx xxxxxxxxxx xx xxxxx xxx xxxxxxxx xxxxx xxxxxxxx x České xxxxxxxxx, ale i x xxxxxx xxxxxxxxx xxxxxxx. Fungování xxxxxx xx možné xxxxx xxxxx, xxxxx xxxxx, xxxx xxxxxxxx x xxxxxxxxxx xxxxxxx xxxxxx xxxxxx povinnosti, xx xxxx xxxx zbytku xxxxx. Xxxxx xxxxxxxxx xxxxxxxx povinností, xx xxxxx sankcionovat xxx, xxx výše xxxxxx xxxx xxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxx. Xxxxxx jsou přitom xxxxxxxxx xxx, že xx xxxxxxxxx jejich xxxxx hranice. Mohou xxx xxx xxxxxxxxxx xxxxxxx okolnosti xxxxxxxxxxx xxxxxxx naplňujícího skutkovou xxxxxxxx xxx, aby xxxxxxx x xxxxxxxxxxxxx xxxxxxxxx.
X. Členský xxxx xxxx xxxxxxxx xxxxxx xxxxxxxxxx xxxxxxxxxxx identifikátoru xxxx xxxxxxxxxx x xxxxxxx xxxxxxxxxx s xxxxxx xx xxxxxxx xxxxx xxxxxx přípravky x souladu s xxxxxxx 54x xxxx. 5 xxxxxxxx 2001/83/ES (čl. 2 xxxx. 1 xxxx. x) xxxxxxxx x xxxxxxxxxx prvcích), xxxxxx slovy xxxx xxxxxxxxx, xxx xxxxxxxxxx xxxxx byly xxxxxxxx xxxxx i těch xxxxxxxx přípravků, xxxxx xxxxxxxxx xxxx xxxxxxxx xxxxx xxxxxx.&xxxx; Xxxxx xxxxxxxxx xxxxxx xxxxxxxxxx xxxxxx xxxxxxxxxx jedinečného xxxxxxxxxxxxxx xxxx xxxxxxxxxx x xxxxxxx xxxxxxxxxx x xxxxxx xx xxxxxxx xxxxx xxxxxx xxxxxxxxx x xxxxxxx x xxxxxxx 54x xxxx. 5 xxxxxxxx 2001/83/XX (čl. 2 odst. 1 písm. c) xxxxxxxx x xxxxxxxxxx xxxxxxx).
X. Nařízení uvádí xxxxx „xxxxxxxxxxxx xxxxxxxx xxxxx“ xxxx „jiné xxxxxxxx xxxxx“ xxxxxxxxxxxxxx xxxxxx xxxxxxxxx a xxxxxxxxx na xxxxxxxxxx xxxxxxxxx xxxxx, xxx xxxxx xxxxxx prvek xxxx xxxxxx x xxxxx xxxxxxxxxxx identifikátoru xx xxxxxxx. V Xxxxx xxxxxxxxx je „xxxxxxxxxxxxx xxxxxxxxx xxxxxx“ xxx xxxxxxxxx Xxxxxxx xxxxx §32 odst. 5 xxxxxx o xxxxxxxx (xxxx jen „xxx XXXX“). Xxxxx xxxxxxxxx xxxxxx xxxxxxxxx, xxx xxx SÚKL xxx xxxxxx x xxxxx xxxxxxxxxxx identifikátoru, xxx., že bude xxxxxxxx xxxxxxxxx stav, xxx xxx XXXX xx xxxxxx xx xxxxx xxxxxxxxx.
X. Xxxxxxx xxxxxxx xxxxx xxxxxxxxx x xxxxxxxxxx prvcích xx xxxx xxx, xxx x uceleném xxxxxxxxxx xxxxxxx xxxxxxxx xxxxxxxxxxx identifikátoru xx xxxxxxx úložišť xxxx xxxxxxxxx xx xxxxx xxxxxxxxxxxxxx xxxxxxx, tj. xxx xx xxxxxx xxxxxxxxx vydán veřejnosti. Xxxxxxx xxxx xx xxx xxx zohlednit xxxxxxxx charakteristiky xxxxxxxxxxxxxx xxxxxxx xx svém xxxxx x umožnit xx své xxxxxx xxxxxx, xxx distributor xxxxxx xxxxxxxx xxxxx x xxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxx xxx, xxx xxxxxx přípravek xxxx xxxxxxx x xxxx xxxx xxxxxxxxx xxxxxxxxx x článku 23 xxxxxxxx x xxxxxxxxxx xxxxxxx:
x) osobám oprávněným xxxx xxxxxxxxx xxxxxxx xxxxxx xxxxxxxxx veřejnosti, xxxxx nepůsobí x xxxxx xxxxxxxxxxxxxx xxxxxxxx xxxx lékárny;
b) xxxxxxxxxxxx xxxxxxx x xxxxxxxxxxxxxxx x xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx,
x) xxxxxx lékařům;
d) xxxxxxxxxxxxx a optikům;
e) xxxxxxxxxxx zdravotnické záchranné xxxxxx;
x) ozbrojeným silám, xxxxxxx a xxxxxx xxxxxxx institucím, které xx udržují xxxxxx xxxxxxxx xxxxxxxxx pro xxxxx xxxxxxx xxxxxxx x xxxxxxxx xxxxxxxxx;
x) xxxxxxxxxxx a xxxxxx xxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxxxxx, xxxxx využívají xxxxxx xxxxxxxxx xxx xxxxx xxxxxxx x vzdělávání, x xxxxxxxx xxxxxxxxxxxxxx xxxxxxxx;
x) xxxxxxxx;
x) xxxxxx;
x) xxxxxxxx;
x) xxxxxxxxxxxxx zařízením.
V xxxxx Xxxxx xxxxxxxxx xxx xxxxxx popsaný článkem 23 xxxxxxxx o xxxxxxxxxx prvcích, tj. xxx ověření ochranných xxxxx x xxxxxxxx xxxxxxxxxxx identifikátoru ze xxxxxxx xxxxxxx xxxxxxx xxxxxxxxxxx, xxxxxx xxxxx x případě xxxxxxx xxxxxxxx xxxxxxxxx
- veterinárním xxxxxxx,
- Xxxxxx Xxxxx xxxxxxxxx x xxxxxxxxxxx xxxxxxxxxxx sil xxxxxx, x udržování skladových xxxxx xxxxxxxx xxxxxxxxx xxx účely civilní xxxxxxx, xxxxxxxx xxxxxxxxx x xxx xxxxx xxxxxxxxxxx ozbrojených xxx Xxxxx xxxxxxxxx léčivy xxx jejich xxxxxxxx xx zahraničí podle §111a zákona o xxxxxxxx a
- xxxxxxxxxxxxxx xxxxxxxxxxx xxxxxx, kterým xxxx xxxxx §77 xxxx. 1 písm. x) xxxx 12 xxxxxx x léčivech xxxxxxxx imunologické xxxxxx xxxxxxxxx xxx xxxxx xxxxxxxxx pravidelného xxxxxxxx xx xxxxxxx xxxxxxx xxxxxxx xxxxxxxxxxxx se xxxxxxxxx xxxxxxxxxxx xxxx xxx xxxxx povinného xxxxxxxxxxxx, xxxxxxxxxx a xxxxxxxxxxx očkování na xxxxxxx xxxxxxx xxxxxxx xxxxxxxxxxxx s Xxxxxxxxxxxxx xxxxxxxxxxxxx x xxxxxxxxxxx xxxxxxxx hrazeného x xxxxxxxxx zdravotního pojištění x xxxxx xxxxxxxxxxx xxxx xxx xxxxxx č. 48/1997 Sb., x xxxxxxxx xxxxxxxxxx xxxxxxxxx a x xxxxx x xxxxxxxx xxxxxxxxx xxxxxxxxxxxxx xxxxxx, xx znění xxxxxxxxxx předpisů.
V xxxxxxxx xxxx 2009 xxxxx x XX ke xxxxx xxxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxx (ne již xxxx krajské xxxxxxxxxx xxxxxxx, ale xxxx xxxxxxxxxxx xxxxx), a xx xx xxxxxxx xxxxxx xxxxxx č. 48/1997 Sb., x xxxxxxxx xxxxxxxxxx xxxxxxxxx x x xxxxx x doplnění xxxxxxxxx souvisejících xxxxxx, x s xxx xxxxxxxxxxx xxxxx zákona č. 258/2000 Sb., x xxxxxxx xxxxxxxxx xxxxxx a x xxxxx některých xxxxxxxxxxxxx xxxxxx. V xxxxx xxxxxxxxx xxxxxxxxxxx xxxxxxx xxxxxxx xxxxxxx xxxxxxxxxxxxxx přípravků xxxxxxxxxxxxx xx xxxxxxxx xxxxxxxxxxxxx xxxxxxxxxxx xxxxxx, xxx xxxxxxxxxx xxxxxxxxxxx z xxxxxxxx x xxxxxxxxxx xxxxxxx (xx. xxxxxxx xxxxxxxxxx prvků) xxxxxxx xx xxxxxxxxxxxx xxxxxxxxxxxxxx xxxxxxxx přípravků s xxxxxxxx článku 23 písm. x) nařízení x xxxxxxxxxx xxxxxxx. Vzhledem x xxxxxxxx xxxxxxxxxxxx x xxxxxxx xxxxxxxxxx xxxxxxxx xxxxxx zvolil xxxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxx nařízení x xxxxxxxxxx xxxxxxx využít. Xxxxxxxxxx xxxxxxxxxx xxxxxxx xxxxxxxxxx poskytovatelům xxxxxxxxxxx xxxxxx náklady, xxxxx xx při nevyužití čl. 23 xxxx. x) xxxxxxxx x xxxxxxxxxx xxxxxxx xxxxxx xxx xxxxxxxxx ochranných prvků xxxxxxxxx.
Xxxx xxxxxxxx zásadní xx x tuto xxxxxx xxxx xxxxxxxxx xxxxxxxxxxx xxxxxxx distribuce xxxxxxxxxxxxxx xxxxxxxx xxxxxxxxx xxx xxxxx xxxxxxxxx xxxxxxxxxxxx očkování x xxxxxxxxx zvláštního x xxxxxxxxxxx xxxxxxxx x xxxxxx ochrany xxxx xxxxxxx, xxxxxxx x xxxxxxx xxxxxxx xxxxxxxxxx xxxxxxxxxx. Poskytovatelé xxxxxxxxxxx xxxxxx dle xxxxxxxxxx §45 xxxx. 2 xxxxxx x. 258/2000 Xx., x xxxxxxx xxxxxxxxx zdraví x x xxxxx xxxxxxxxx xxxxxxxxxxxxx zákonů, xx xxxxx pozdějších xxxxxxxx, xxxx povinni zajistit x xxxxxxx xxxxxxxxxx, xxxxxxxx a xxxxxxxxx xxxxxxxx, xxxxxxxx při xxxxxxx, xxxxxxxxxx, xxxxxxxxxx xx xxxxxx a xxxx některými xxxxxxxxx xxxxxx, xxxxxxxxx pasivní xxxxxxxxx fyzických xxxx, xxxxx xxxx x xxxx, x xxxxxxx xxxxxxxxx vyhláškou č. 537/2006 Sb., x xxxxxxxx xxxxx xxxxxxxxx xxxxxxx xxxx xxxxxxxxxxx xxxxxxxx, xxxxxx xx Xxxxx xxxxxxxxx xxxxxx. Xxxxxxxxxx xxxxxxxx xxxx členskému xxxxx článkem 23 xxxx. x) xxxxxxxx x ochranných xxxxxxx, tj. xxxxxxxxxxx xxxxxxxxxx ověření xxxxxxxxxx xxxxx na obalech xxxxxxxxxxxxxx léčivých xxxxxxxxx xx xxxxxxxxxxxx před xxxxxxx xx xxxxxxxx xxxxxx, by došlo x xxxxxxxxxxxxx narušení xxxxxxxxxxx xxxxxxx xxxxxxxxxx xxxxxxxxxxxxxx léčivých xxxxxxxxx, xxx by se xxxxx projevit snížením xxxxxxxxxxxxxx dětské i xxxxxxx xxxxxxxx, a xx xx svém xxxxxxxx xxxxxxxx x xxxxxxxx úrovně ochrany xxxxxxxxx zdraví.
Z xxxxxxxx xxxxxx xxxxxxx veřejného xxxxxx se xxxx xxxxxx článek 23 xxxx. x) xxxxxxxx x xxxxxxxxxx xxxxxxx i xxx xxxxxx distribuce xxxxxxxxxxxxxx xxxxxxxx xxxxxxxxx xxx xxxxxxxxx xxxxxxxx xxxxxxx x xxxxxxxxx xxxxxxxxxxx xxxxxxxxx x xxxxxxxx xxx xxxxxxxx xxxxxxxxxxxxx xxxx xx xxxxxxx xxxxxxx xxxxxxx Xxxxxxxxxxxx xxxxxxxxxxxxx x xxxxxxxxxxxxx.
X xxxxxxxxxxx nepovinných xxxxxxxx xxxxxxxxx x xxxxxxxxx zdravotního pojištění xxx xxxxxxxxxxx vypovídá xxxxxxxxxx, že jsou xx základě zákona xxxxxxx x xxxxxxxxx xxxxxxxxxxx pojištění, a xx v provedení xxxxxxx xxxxxxxxxx xxxxxxxx x souladu x xxxxxxxxxxx §30 odst. 2 xxxx. x) x x) xxxxxx x. 48/1997 Sb., x veřejném xxxxxxxxxx xxxxxxxxx x o xxxxx a doplnění xxxxxxxxx xxxxxxxxxxxxx xxxxxx, xx znění pozdějších xxxxxxxx. Xxxx xxxxxxx xxx xxxxx očkování xxxxx lidskému xxxxxxxxxxxx, xxxxx xxxx xxxxxxx xx xxxxxxxxxxx pojištění xxxxx x xxxxxxx (xxxxxxx od 1.1.2018), xx-xx xxxxxxxx zahájeno xx xxxxxxxx 13. xx xxxxxxxx 14. xxxx xxxx. Xxxxxxxxxxxx xxxxx způsobit xxxxx xxxxxxxx děložního xxxxx, xxx x xxxxx xxxxxx (např. xxxxxxxx xxxxxx) xxxx xxxxxxxxx xxxxxxxxx.
Xx 1.1.2018 xx xxxxxxx xxxxxxxxx očkování xxxxx invazivním meningokokovým xxxxxxxx, pneumokokovým xxxxxxxx, xxxxxxxxxxx onemocnění xxxxxxxxxx xxxxxxxx Xxxxxxxxxxx xxxxxxxxxx xxx x x xxxxx xxxxxxx, x xx u xxxxxxxxxx x xxxxxxxxx nebo xxxxxxxx xxxxxx xxxxxxx (xxxxxxxxxxxxxx xxxx xxxxxxxx), xxxxxxxxxx po xxxxxxxxx xxxx xxxxxxxxx xxxxxxxxxxxxx xxxxxxxxx xxxxxxxxxxxxxx buněk, xxxxxxxxxx xx závažnými xxxxxxxxxx xxxx sekundárními xxxxxxxxxxxxx, xxxxx xxxxxxxx xxxxxxxxxxxxxx xx xxxxxxxxxxxxxxx xxxxxxxxxx, xxxx x xxxxxxxxxx po xxxxxxxxx xxxxxxxxx xxxxxxxxxxxxx xxxx xxxxxxxxx pneumokokové xxxxxxx.
Xxxxx xxx xxxxxxx nepovinného xxxxxxxx xxxxxxxxx xxxxxxxxx xxxx xxxxx xxxxxx článku 23 písm. x) xxxxxxxx o xxxxxxxxxx xxxxxxx.Xxxxxx xx x xxxxxx xxxxxxxxx zajistí xxxxxxxxxxxx léčivé xxxxxxxxx xxxxxxxxxxxxxxx výdeje na xxxxxxx od poskytovatelů xxxxxxxxxx xxxx.
Xxxx xx xxxxxx provést xxxxxx xxxxxxxxx zpřesňující xxxxxx xxxxx legislativně xxxxxxxxx xxxxxx x xxxx xxxxxxxxxxxx xxxxxx x xxxxxxxx, xxxxx s xxxxxxxxxxx xxxxxx xxxxxxx xxxxxxxxx xxxx xx xx xxxxxxxx.
X xxxxxxxx xxx adaptační xxxxxx xxxxxxxxxxxxx xxxxxxxx xxxxx xxxxxxxxx xxxxxx xxxxxxxxxxxx xxxxxxxx xx xxxxxxxxxx xxxxx uvedených na xxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx, xxx tvoří xxx xxxxxxxxxxxx xxxxxx xxxxxxx xxxxxxxxx x xxxx oblasti, které xxxxxxxx xxxxxxxx xxxxx xxxxxxxxxx xxxxxxx Xxxxxxxx xxxx. Nejedná xx xxxx x xxxxxx xxxxxxx, který by xxxxxxx xxxxxxxxx xxxxxxxxxxxx xxxxxxx komplexně x xx potřeba xx xxxxxx x xxxxxxxxx x tomto xxxxxxxx.
X xxxxxxx novelou xxxxxxxxxx xxxxxxx xxxxx xxxxxxxxxxxx xxxxxxxxxxx.
Xxxxxxxx 2017/556 xxxxxxx xxxxxxxx xxxxxxxx pro xxxxxxxxx xxxxxxxxxxx xxxxxxx xxxxxxx xxxxxxxx xxxxx xxxxx xxxxxxxx Xxxxxxxxxx xxxxxxxxxx a Rady (XX) č. 536/2014. Xxxxxxxx xxxx vydáno x xxxxxxx x článkem 63 xxxxxxxx č. 536/2014, xxxxx xxxxxxxx Komisi xxxxxxxx xxxx x xxxxxxxxx pravomoci, x xxxxx xxxxxxx xxxxxxxx xxxxxxxx xxx xxxxxxxxx xxxxxxxx správné xxxxxxx xxxxx, pokud xxx x xxxxxxxxx léčivé xxxxxxxxx. Nařízení xx xxxxx použitelné xx xxxxxxxx xxx jako xxxxxxxx (XX) č. 536/2014. Xxx xx xxxxxxx xxxxxxxx, xxx je xxxx xxxxxxx, xxxxx xxxxxxxxxxxxx, xx xxxxxxx xxxxxxxx x xxxxx xxxx adaptace xxxxxxx xxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxx, x to x xxxxx případě xxxxxx x xxxxxxxx, x xxxxxx o xxxxxxxxxxx xxxxxxxx, x xx x xxxxxxxxxxxxx xxxxxx:
- stanovit správní xxxxx, xxxxxxxxx x xxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxx 2017/556,
- zajistit xxxxxxxx xxxxxx 3, xxxxx ukládá xxxxxxxx xxxxxx xxxxxxxx řádně xxxxxxxxxxx systém xxxxxxx, xxxxx zajistí, xxx xxxxxxxxx postupy byly xxxxxxxxxx x xxxxxxxx xxxxxxxxx,
- zajistit naplnění xxxxxx 10 xxx 8, xxxx xxxxxxxx xxxxxx a správní xxxxx, xxxxx xxxxxxx, xxx inspektoři x xxxxxxxxx členských států xxxx, xx vyžádání x xxx, kde xx xx vhodné, xxxxxxx x místům, xxxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxxxxxx s xxxxxxxxx hodnocením, xxxxx x k jakýmkoli xxxxxxxxxxxx xxxxxx,
- xxxxxxxx xxxxxxxx článku 13 xxxxxxxxxx se inspekčních xxxxx x vedení xxxxxxx,
- xxxxxxxx xxxxxxxx xxxxxx 4 xxxxxxxxxx xx vedení xxxxxxx x xxxxxxxxxxx, xxxxxxx xxxxxxxx x xxxxxxxxxxxx xxxxxxxxxx,
- xxxxxxxx, xxx xxxxx xxxx xxx xxxxxxxx zjištěn xxxxxxx xxxxxxxx xxxx xxxxxxxx xxxx xxxxxxxxxx-xx xxxxxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxxxxxx, xxxx xxxx jednání xxxxxxxxxxxxx xxxx přestupek x aby xx xx xxxx příslušný xxxxxxx orgán xxxxxxxx xxxxxx.
Xxxxxxxx 2017/1569 xx xxxxxx x xxxxxxx xx xxxxxxxx Evropského xxxxxxxxxx x Xxxx (XX) č. 536/2014 xx xxx 16. xxxxx 2014 x klinických xxxxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx x x xxxxxxx směrnice 2001/20/XX, x xxxxxxx s xxxxxxx xx xx. 63 xxxx. 1 xxxxxxxxx nařízení, xxxxx xxxxxxxxx, xx hodnocené xxxxxx xxxxxxxxx xxxx xxx vyráběny za xxxxxxx výrobní xxxxx, xxxxx xxxxxxx kvalitu xxxxxx xxxxxxxx xxxxxxxxx x cílem zaručit xxxxxxxxxx subjektu xxxxxxxxx x xxxxxxxxxxxx x xxxxxxxxxx xxxxxxxxxx xxxxx xxxxxxxxx x klinickém xxxxxxxxx. Tuto xxxxxxx xxxxx nazývá xxxxxxx xxxxxx xxxxxxxx výrobní xxxxx x xxxx xxxxxxxx x xxxxxxxxxx xx xx. 89 xxxxxxxx Xxxxxx xxxxx xxxxxxxx xxxxxxx xxxxxxx xxxxx xxx xxxxxxxxx xxxxxx xxxxxxxxx prováděcím xxxxxxxxx. Xxxx zmocnění Xxxxxx xxxxxxxx xxxxxxx xxxxxxxx 2017/1569, a xx zejména x xxxxxxx na xxxxxxxxxxx xxxxxx:
- xx nezbytné xxxxxxxx xxxxxx mezi xxxxxxx téhož xxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxx xx stejných či xxxxxxx xxxxxxxxxx xxxxxxxxxxx x xxxx xx, xx xxxxx xxxxx xxxxxx hodnoceného xxxxxxxx xxxxxxxxx byly náležitě xxxxxxxxxxxxx x xxxxxxxxxx;
- xxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxxx xxxxx xxxxx v xxxxxxxxx x xxxxxxx xxxxxxxxxxxxxx xxxxxxxx xxxxxxxxx, protože xxxxxx xxxxx stanoveny xxxxxxx, xxxxxxxx xxxxx xxxxx xxxxxxxxxx hodnocení, x v důsledku xxxx xxxx xxxxxx xxxxx; xxxx xxxxx xxxxxxxxx x potřeby (xxxxx) xxxxxxxxx výběru x zastření xxxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx xxx účely klinického xxxxxxxxx (xxxxxxxxx). Xxxxx xxxxxxxxx xxxxxx být xxxxx známá xxxxxxxx, xxxxxxxx x xxxxxxxxxxxxxx xxxxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx, x xxxxxxx xxxxxxxxxxxxx xxxxxxx xxxxxx xxxxxxx xxxxxxxxxxx xx xxxxx xxxxx xxxxxxxxxxx než x xxxxxxxxxxxxxx xxxxxxxx xxxxxxxxx. Xxxxxxxx x xxxx xxxxxxxxxx xx xxxxxxx xxxxxxxx xxxx xxx xxxxxxxxx xxxxxx xxxxxxxx xxxxxxxxxxxxxxx xxxxxxx jakosti;
- xxxxxxx xxxxxxx praxe, xxxxx jde x xxxxxxx xxxxxx xxxxxxxxx, xxxxx xxxx xxxxxxxxxxxx xxx xxxxxxx na xxx, x o xxxxxxxxx xxxxxx xxxxxxxxx, xx založena xx xxxxxxxx xxxxxxxx;
- xxxxxxxxx xxxxxx přípravky x xxxxxxxxx xxxxxxxxxxxx pro xxxxxxx xx xxx xx xxxxx xxxxxx xx stejných výrobních xxxxxxx. Z xxxx xxxxxx xx xxxxxx x xxxxxx xxx xxxxxxxx výrobní xxxxx xxx xxxxxxxxx xxxxxxx xxxxxx xxxxxxxxx xxxx xxx xx nejvíce xxxxxxx x těmi, xxxxx xx xxxxxxxx xx xxxxxxx léčivé xxxxxxxxx;
- xxx byl xxxxxxx xxxxxxx xxxxxxxxx xxxxxxxx xxxxxxx xxxxx xxx xxxxxxxxx léčivé xxxxxxxxx, je xxxxxxxx xxxxxxxxxx xxxx ním x xxxxxxxxxxx. Xxxxxx xxx xxxx xxxxxxxxx xxxxxxxxxxxxx s výrobcem, xxx xxxxxxx požadavky xxxxxxxx (EU) č. 536/2014. Xxxxx jsou xxxxxxx x xxxxxxxxx různými xxxxxxxx xxxxxxxx, xxxx xx být povinnosti, xxxxx x sobě xxxxxxxx mají, xxxxxxxxx x xxxxxxxxx xxxxxx xxxx xxxx. Xxxxxx xxxxxx by xxxx xxxxxxxx xxxxxxx xxxxxxxxxxx xxxxx x xxxxxx xxxxxxxxx x otázkách xxxxxxx;
- hodnocené léčivé xxxxxxxxx xxxxxxxx do Xxxx xx měly xxx vyrobeny x xxxxxxxx standardů xxxxxxx, xxxxx xxxx xxxxxxxxxxxx xxxxxxxxxx xxxxxxxxxx x Xxxx. X xxxxxx xxxxxx xx xxxxxxxx xxxxxxxx, xxx xxxx xxxxxxxx xxxxxxx xx Xxxx xxxxx xxxxxxxxx xx výrobce xx xxxxx xxxx, xxxxx xx xxxxxxxxx nebo xxxxxxxx x xxxxxx x souladu x xxxxxxxx xxxxxxxx xxxx, x níž xx xxxxx.
Xxxxxxxx xxxxxx xxxxxxxx xxxxxxxxxx xxxxxxxx xx xxxxxxxx xxxxxxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxx xxxxxxxxx xxxxx xxx, xxx xxxx zajištěna xxxxx xx xxxxxxxx x xxxxxx xxx xxxxxxxx xxxxxxx xxxxx. X xxxxx bodě je xxxxxxxx 2017/1569 xxxx xxxxxxxx xx nařízení 2017/556, kterým se xxxxxxxxx podrobná xxxxxxxx xxx provádění inspekčních xxxxxxx xxxxxxx klinické xxxxx podle nařízení 536/2014. X xxx xxxxxxxx xxxxxxxx ustanovení xxxxxxxxxxx, aby inspektoři x xxxxx xxxxxxxx x xxxxxxx xxxxxxxxxx xxxxxxxx výsledků xxxxxxxx x Unii a x zájmu usnadnění xxxxxxxxxx xxxxxxxxx xxxxx xxxx k xxxxxxxxx xxxxxx xxxxxxxx xxxxxxxxx xxx provádění xxxxxxxx xxxxxxx xxxxxxx xxxxx xxx xxxxxxxxx léčivé xxxxxxxxx xx xxxxx xxxxxxx;
- xxxxxx Komise x tyto xxxxxxx xx xxxx xxx xxxxxxxxx x pravidelně xxxxxxxxxxxxx x závislosti xx xxxxxxxxxx x xxxxxxxx xxxxxxx. Během xxxxxxxx xx xxxxx xxxxxxxxxx musí xxxxxx, xxx výrobní xxxxx xxxxxxxx xxxxxxxx xxxxxxx xxxxx xxx x xxxxxxxxxxx léčivých xxxxxxxxx, xxx x léčivých xxxxxxxxx registrovaných xxx xxxxxxx xx xxx. X tohoto xxxxxx x v zájmu xxxxxxxxx xxxxxxxx dozoru xxxx xxxxxxxxx xxxxxxx x pravomoci pro xxxxxxxxx xxxxxxxx x xxxxx xxxxxx, xxx xx dodržována xxxxxxx xxxxxxx xxxxx xxx xxxxxxxxx xxxxxxx léčivé xxxxxxxxx. Xxxx praxe xxxx xxxxxxxxxxxxx x xxxxxxx a xxxxxxxxxxx x oblasti xxxxxxxxx xxxxxxxx xxxxxxxxx - xxx xxxx xxxx xxxxxxxx xxxxxxxx Xxxxxx (XX) 2017/1572. X xxxx, aby byly xxxxxxxx xxxxxx, xxxx xxx inspektoři xxxxxxxxx xxxxxxxx xxxxxxxxx;
- příslušné xxxxxx xxxx podle xxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxx xxxxxxx, xxx xxxx xxxxxxxxx, že xxxx xxxxxxxxx xxxxxxx xxxxxxxxxx x xxxxxxxx xxxxxxxxx. Xxxxx xxxxxxxxx xxxxxx xxxxxxx xxxx xxxxxxxxx xxxxxxxxxxx xxxxxxxxx, xxxxx procesy x xxxxxxx, xxxxxx standardních xxxxxxxxxx xxxxxxx, jimiž xx mají xxxxxxxxxx xxxxx xxx plnění xxxxx úkolů, jasně x podrobně vymezené xxxxxxxxxx x xxxxxxxxxxxx xxxxxxxxxx a požadavky xx xxxxxxxx školení, xxxxx x xxxxxxxxx xxxxxx x xxxxxxxxxx, xxxxxxx účelem xx xxxxxxxxx xxxxxxxx.
Xxxxxxxx 2017/1572 xxxx přijata x xxxxx xxxxxxxx shodu xx xxxxxxxx x xxxxxx xxx xxxxxxxx xxxxxxx xxxxx. Xxxxxxxx xxxxxxxx xxxxxxxxxx x xxxxxxxxxx prováděných příslušnými xxxxxx x x xxxxxxxx povinnostech výrobce. Xxxxxxxx xxxxxxxxxx, která xxxxxxxxx, xxx xxxxxxx xxxxxx přípravky dostupné xx xxxxx XX xxxxxxxxx xxxxx standardy xxxxxxx; xxxxxx xxxxxxxxx xxxxxxxx do Xxxx xxxx xxx xxxxxxxx x xxxxxxx xx xxxxxxxxx, xxxxx xxxx xxxxxxxxxxxx rovnocenné xxxxxxxxxx xxxxxxx xxxxxxx xxxxx xxxxxxxxxx x Xxxx.
X xxxxx xxxxxxxxxx xxxxxxxxxxx xxxxx xxxxxxx xxxxxxx xxxxx xxxx xxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx x xxxxxxxxxx dbát xxxxxx xxxxxxxxx v čl. 47 xxxxxxxx 2001/83/XX, xxx xx xxxxxxx, xx „Xxxxxx x xxxxxx pro správnou xxxxxxx xxxxx xxx xxxxxx xxxxxxxxx podle čl. 46 písm. x) xx xxxxxxx xxxxxx xxxxxxxx“ a xx „xxxxxxxx xxxxxx v xxxxxxx x xxxxxxxxx xxxxxxxx Xxxxxx zveřejní x x xxxxxxx xxxxxxx pozmění xxx, xxx bylo přihlédnuto x xxxxxxxxxxx a xxxxxxxxx xxxxxxx“. Zásady x xxxxxx xxx xxxxxxxx výrobní xxxxx xxx humánní xxxxxx xxxxxxxxx xxxx xxxxxxxx xxxxxxxxx, xxxxx xxx x řízení xxxxxxx, xxxxxxxxxx, prostory x xxxxxxxx, xxxxxxxxxxx, výrobu, xxxxxxxx xxxxxxx, xxxxxxx xxxxxxxxxxx xxxxxxxx, xxxxxxxxx x xxxxxxx xxxxxxxxx x oběhu x xxxxxxx xxxxxxxx. Xxxxx xx xxxx xxxxxxxx xxxxxxxxx xxx xxxxxxx xxxxxxx, xxxx xxxx xxxxxx a xxxxxx xxxxxxxxxxxx xxxxxxxxx vlastnostem xxxxxxxxx xxxxxxxxx v xxxxxxx x xxxxxxxxx xxxxxxxxx xx xxxxxxxxx xxxxx.
Xxxxxxx směrnice xxxx xxxxxxxxxxxxx xx xxxxxx x xxxxxxxx x xxxxxxx xx vyhlášky č. 229/2008 Sb. Xxxxxxxxx xxxxxxxx 2003/94/ES xxxxxxxx 2017/1572 xxxxxxxx nutnost xxxxx xxx xxxxxx x xxxxxxxx, xxx xxxxxxx xxxxxxxxxxx xxxxxxxx - xxxxxxxx č. 229/2008 Sb. Transpozice xxxxxxxx se xxxxxx xxxxxxxxxx xxxxxx x xxxxxxxx zejména x xxxxxxxxxxxxx xxxxxx:
- xxxxxx xxxxxxxx xxxxxxx xxxxxxx xxxxx,
- uložení xxxxxxxxxx xxxxxxxx vytvořit x xxxxxxxx xxxxxx xxxxxxxx xxxxxxx,
- uložení xxxxxxxxxx xxxxxxxx xxxxxx xxxxxx xxx xxxxxxxxxxxxx x xxxxxxxxxx xxxxxxxxx včetně xxxxxxxx účinného xxxxxxx xxx stahování léčivých xxxxxxxxx x xxxxxxxxxxx xxxx,
- xxxxxxxxx xxxx, xxx xxxxxxx xxxxxxxxx xxxxxxx xxxxxxx x xxxxxxx xxxxxxxx x xxxxxxxxxxx x léčivými xxxxxxxxx xxxxxxxxxxxxx xxxxxxxxxx x xxxxxxx s xxxxxxxxxxx předloženými x xxxxxxx x xxxxx xxxxxxxxxx.
Xxxxxxxxxx xxxxxx úprava xxxx vztah x xxxxxxxxxxxx diskriminace x xxxxxxxx xxxx x xxx.
3. Xxxxxxxxxx xxxxxxxxxxx xxxxxxxxxx xxxxxx xxxxxx
Xxxxx xxxxxx xxxxxx x léčivech x xxxxxx o zdravotních xxxxxxxx xx xxxxxxxxxx xx xxxxxx xxxxxxxx xxxxxxxxxxxx xxxx xxxxxxxxx xxxxxxxx xxxxx Xxxxxxxx xxxx. Teprve xxxxx xxxxxxxxxxxx se vytvoří xxxxxx vzájemně provázaných xxxxxxxx v xxxxxxx xxxxxxxxxx xxxxx xxxxxxxxx xx xxxxx humánních xxxxxxxx přípravků x x oblasti xxxxxxxxxx xxxxx správné xxxxxxxx xxxxx. Xxxxxxxxxxxxxxx xxxxxxxxxxx xxxxxx vznikne v xxxxxx z xxxx xxxxxxxxxx xxxxxxx xxxxxxxxx x xxxxxxx xxxxx, xxxxx xxxx xxxxx xxxxxxxxx x praxi. Xxxxx xx x xxxxxxxx formou xxxxxx xxxxxx x xxxxxxxx xxxxxx přistoupeno, xxxxx xxxxxxxxxx xxxxxxxx Xxxxxxxx xxxx (xxxxxxxx) by x Xxxxx xxxxxxxxx xxxxxxx být xxxxxx x beze xxxxxx xxxxxxxxxx, xxxx xx xxxxx x xxxxxxxx xxxxxxxxxx xxxxxxxxx státu. Xxxxxxxx x xxxxxxxxxx xxxxxxx xxxxxxx ustanovení xxxxxxxx 2011/62/EU. Xxxxx xxxxxxxxx xxx xx xxxxx právního xxxx xxxx xxxxxxxx xxxx xxxxxxxxxxxxx xxxxxxx č. 70/2013 Sb., xxxxxx xxx xxxxxxxxxxx xxxxx o xxxxxxxx.
Xxxxxxxxxxxxxxx xxxxxxx xx riziko xxxxxxxxxxx nepřijetí xxxxxxxx xxxx xxxxxxxx smlouvy x xxxxxxxx Evropské xxxx xx xxxxxx xxxxxxxxx státu x xxxxxxxx xxxxxx xx xxxxxx Xxxxxxxx komise xxxxx České xxxxxxxxx xx xxxxxxxxx xxxxxxxxxxxxx xxxxxxxxxx x popřípadě x xxxxxxx xxxxxx xxxxxxxxx xxxxxxxx xxxxxxxx, xxxxx xx xxxx xxxxx na celý xxxxxx a jeho xxxxxxxxx xxxxxx pouze x xxxxxxx Xxxxx xxxxxxxxx, xxx x xxxxxxxxx xxxxxxxxx států, xxxxx xxx x xxxxxxx, xx xxxxxxxx xxxxx xxxxxxxxxx všemi, xxxx systém funkční. X xxxxxxxxx je xxxxx ještě doplnit, xx za xxxxxxxxx xxxxxx xxxxxxxxxx xx xxxxxxx ze strany xxxxxx Xxxxxxxx xxxx xxxxxxxxxxxx takového přístupu x xxxxxxxxx x xxxxxxx xxxxxx, xxxxx xxxx xx xxxxx xxxxx xxxxxxxx xxxx xxxxxx v xxxxx xxxx EU x x takové xxxxxxx xxxx xx xxxxxxxxxx xxxxxxxx. K xxxxxxx xxxxxxx xxxxxx, xxxxxx xx xxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxxxxxxx xxxxxxxx xxxxxx padělaných xxxxxxxx xxxxxxxxx xx xxxxxxxxx xxxxxxxxxxxxx xxxxxxx, xxxxxxxxxxxx uvádí následující.
Zavedení xxxxxxxxxx prvků xxx xxxxxx přípravky v xxxx Xxxxxxxx unii x xxxxx xxxxxxxxx xxxx xxxxxxx xxxxx x xxxxxxx zajistit xxxxxxxxx xxxxxxxxx xxxx x xxxxxxxx xxxxxxxxx xx mělo x xxxxxxxxxxxxx rizikových xxxxxxxx xxxxxxxxx xxxxxxx xxxxxxx xxxxxxxx x xxxxxxxxxxxx xxxxxxxxxxxx xxxxxx x xxxxxxxx, xxx x xxxx bylo manipulováno. Xxxxxx těchto xxxxxxxxxx xxxxx xxxxxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx léčivých xxxxxxxxx. Xxxxxx přípravky xxxxxxxxxxx omezení xxxxxx xx xxxxxxxx předpis xx obecně xxxx xxx vybaveny xxxxxxxxxx xxxxx. V zájmu xxxx, xxx xxxx xxxxxxxx xxxxx xxxxxx, xx xxxxxxxx xxxxxxxxxxx, xxxxxxxxxx nebo xxxxxxxxx xxxx xxxxx xxxxx xxxxxxxx za xxxxxxxx xxxxxxxxxxx podmínek. Zejména x xxxxxxx xxxxxxxxx xxxxxxxx xxxxx xxxx xxx xxxxxxxxx xxxxxxxxxxxx xxxxxxxxxx prvky. Xxxx xxxxxx xxxxxxxx by xxxx xxxxxxxx dostatečnou xxxxxxx xxxxx vstupu xxxxxxxxxx xxxxxxxx přípravků xx xxxxxxxxx xxxxxxxxxxxxxx xxxxxxx x xxxxx xxxxxxx xxxxxxxx i xxxxxxxx rozhodnutí x xxxxxxxxxx x výrobce. Xxxxxxxxxxxx xxxxxxxxxx xxxxx x léčivých přípravků xxxxxxxxxx na xxxxxxxx xxxxxxx xx vyžádá xxxxxxxxxx a xxxxxx xxxxxxxxx úložiště x Xxxxx republice, xxxxxxxxx xxxxxx xxxxxxxxx postupů, xxxxxxx x xxxxx xxxxxxxxxxx činnosti x xxxxxxxx xxxxxxxxx x xxxxxxx léčivých xxxxxxxxx, xxxxxxx dopad xxx xxxxxxxxx Xxxxxx Xxxxxxxxxxx xxxxxxxxxxx Komisí x xxxxx xxxxxx xxxxxxxx x xxxxxxxxxx prvcích.
Porušením xxxxxxxxxx a xxxxxxxxxxx xxxxxxxx xxxxxxxxxxx pro xxxxxxxxx řádného xxxxxxxxx xxxxxxxxxx xxxxx na xxxxx xxxxxxxxx léčivých xxxxxxxxx x Xxxxx xxxxxxxxx by nedošlo x xxxxxxxxxx zvýšení xxxxxxxxxxx xxxxxxxx xxxxxxxxx x xxxxxxxx xxxxxxxxxxxxx xxxxxxx, xxx xx xxxxx xxxx x xxxxxxxx xxxxx xxxxxxx xxxxxxxxx xxxxxx, x xxxxx xx tak xxxxxxx xxxxxxxxxxxxxx závažné xxxx v této xxxxxxxxx citlivé xxxxxxx x xxxxxxxx vystavení xxxxxxxx xxxxxxxx účinkům xxxxxxxxxx léčivých xxxxxxxxx. Xxxxxxxxx systém xxxx xxxxxxxx xxxxx v xxxxxxx, kdy xxxxxxx xxxxxxx xxxxxxxx x xxxxxxxxxxxx xxxxxxxxx orgány x členské státy XX xxxxx plnit xxx xxxxxxxxxx xxxxxxxxxxx x xxxx xxxxxxxxx xxxxxxxx xxxxxxxx XX.
Xxxxxxxxxxxx xxxxxxx xxxxx xxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx xx xxxxxxxxx xxxxxxxxxxxxxx xxxxxxx x xxxxxx xxxxx xxxxxxx, xx x xxxx xxxxx xx xxxxxxxx xxxxxx xxxxxxxxx xxxxx snadněji xxxxxx xx xxxxxx xxxxxxxxx xxxxx (xxx xxxxx pohyb zboží x XX), xxx xxxx adaptaci xxxxxxxxx xxxxx x xxxx. Xxxx xx bylo x xxxxxxx s xxxxxxxxx xxxxxxxx spolupráce.
K xxxxxxx xxxxxxx xxxxxx, xxxxxx xx xxxxxxxxx xxxxxxxxxx xxxxx xxxxxxx xxxxxxx xxxxx xxx xxxxxxxxx xxxxxx xxxxxxxxx x xxxxxxxxx xxxxxxxxxx xxxxxxxx pro xxxxxxxxx xxxxxxxxxxx xxxxxxx xxxxxxx xxxxxxxx xxxxx, xxxxxxxxxxxx xxxxx xxxxxxxxxxx.
Xxxxxxxx, jak xx výše uvedeno, xxxx xxxxx aplikovatelná, xxxxxx je xxxxxxxx x rámci xxxxxxxx xxxxxxxxxxxx norem xxxxxxxxxxxxxx xxxxxxxx řádu České xxxxxxxxx xx tyto xxxxx xxxxx Evropské xxxx novelizovat xxxxxxx xxxxxxxxxx xxxxxx x xxxxxxxx a xxxxxx x xxxxxxxxxxx službách xxx, xxx xxxx xxxxxxxxxx x xxxxxxxx xxxxxxxxxxx xxxxxxxxxxx a xxxxxxxx xxxxxx tvořil xxxxx koherentní xx xxxxxxxx inspekčních xxxxxxxx, xxxxx i se xxxxxxxx xxxxxxx xxxxx xxxxxxxx xxxxxxxxx.
4. Zhodnocení xxxxxxx xxxxxxxxxx xxxxxx xxxxxx s ústavním xxxxxxxx Xxxxx republiky
Návrh xxxxxx zákona x xxxxxxxx x zákona x xxxxxxxxxxx službách xx x xxxxxxx x ústavním xxxxxxxx Xxxxx xxxxxxxxx. Navrhovaná xxxxxx xxxxxx xxxxxxxxxx xxxxxxx xxxxxxxxx xxxxxxxx xxxxxx xxxxxx xxxx, xxxxxx xxx podle článku 2 xxxx. 3 Xxxxxx x článku 2 xxxx. 2 Xxxxxxx xxxxxxxxxx xxxx x xxxxxx xxxxxxxxxx xxx x xxxxxxxxx x x xxxxxx stanovených xxxxxxx, a to xxxxxxxx, xxxxx xxxxx xxxxxxx. Xxxxxxxxxx xxxxxx xxxxxx xxxxxx xxxxxxxxxx xxxxxxx xxxxxxxxxx zásadu, xxxxxxxxxx x článku 4 xxxx. 1 Xxxxxxx xxxxxxxxxx xxxx a xxxxxx, která xxxxxxx x tom, xx xxxxxxxxxx xxxxx být xxxxxxxx toliko na xxxxxxx xxxxxx x x xxxx mezích x xxx při xxxxxxxxx základních xxxx x svobod. Stanovené xxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxxx xxxxxxxxxx v distribučním xxxxxxx, které mají xxxxxxxx ochranu pacientů xxxx xxxxxxxxxx léčivými xxxxxxxxx, xxxx x xxxxx xxxxxxx xxxxxx x xxxxxx xxxxxxxx x nejdou xxx xxxxx Xxxxxx Xxxxx xxxxxxxxx x Xxxxxxx xxxxxxxxxx práv x xxxxxx. Xxxxxxxxxxx xxxxxx xxxxxxx xx zajistí xxxxx xxxx xxxxxxxxxxx xxxxxxxx přípravků xxx xxxxxxxx x xxxxxxxx xx xxx xxxxxx xxxxx xxxxxxx na xxxxxxx xxxxxx založené xxxxxxxxxxx článku 31 Xxxxxxx xxxxxxxxxx xxxx x xxxxxx jako xxxxxxxx xxxxxxxxx xxxxxxx České xxxxxxxxx.
Xxxxxx xxx xxxxxxxx x xxxxxxxxxx xxxxxxxxxx xxx xxxxxxxxx xxxxxxxxxxx xxxxxxx xxxxxxx klinické xxxxx je xxx. x povahy xxxx xxxxxx xxx xx xxxxxxxxxx případy, neboť xxxxxxxxxx postupují na xxxxxxx xxx uděleného xxxxxxxx xxxxx x xxxxxx xxxxxxxxx xxxxxxxxx. Xxxx xxxxxxxx xxxx xxxxxxxx příslušný orgán xxxxxx členského státu. Xxxxxxx, xxx by xxxxxxx xxxxx postupoval xxxxxxxx, xx xxxxx xxxxxxxxx za xxxxx. X xxxxxxxx k xxxxxxxxx xxxxxxxx, xxxxxx xxxxxx, xxxx xxxxxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxxx xxxx xxxxxxxxx xxxxxxx xxxxxxxxx, x xx x x xxxxxxxxx, xxx xxxxx xx. 8 nařízení xxxxx xxx xxxxxxxx x případě xxxxxxxx xxxxxxxxx, xxxx xxxx xxxxxxx xxxxxxxx.
Xxxxx xxxxxx xxxxxx xxxxxxxx kritéria xxxxxxxxx xxxxxxxx pořádkem Xxxxx xxxxxxxxx, xxxxxxxxx xxx článkem 12 Xxxxxxx xxxxxxxxxx xxxx x xxxxxx, xxxxx stanoví, xx xxxxxx xx xxxxxxxxxxxxxxxx xxxxxx xxxxx xxx zákonem xxxxxxxx, xxx je-li to x xxxxxxxxxxxx xxxxxxxxxxx xxxxxxxx xxx xxxxxxx xxxxxx xxxx zdraví xxxx, xxx xxxxxxx xxxx x svobod xxxxxxx anebo pro xxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxx xxxxxxxxxxx x xxxxxxx. Xxxxx xx xxxxxx xxxxxxx xxxx xxx xxxxxxxxx xxxx xxxxxxxxxxx jiné xxxxxxxxxxx xxxxxxxx, xxxxx být xxxxxx zásahy xxxxxxx xxxxxxxx, též xx-xx xx xxxxxxxx pro xxxxxx xxxxx xxxxxxx xxxxxx.
5. Zhodnocení xxxxxxxxxxxxx xxxxxxxxxx xxxxxx úpravy x xxxxxxxx Evropské xxxx, xxxxxxxxxxx xxxxxxxx xxxxxx Evropské unie xxxx xxxxxxxx právními xxxxxxxx práva Evropské xxxx
Xxxxxxxxxxx xxxxx xxxxxxxxx způsobem adaptuje xxxxxxxx o xxxxxxxxxx xxxxxxx, nařízení x xxxxxxxxxx xxxxxxxxxx xxx xxxxxxxxx xxxxxxxxxxx xxxxxxx xxxxxxx klinické praxe xxxxx xxxxxxxx 536/2014 x nařízení, kterým xx xxxxxxxx nařízení 536/2014 xxxxxxxxxx zásad x xxxxxx pro xxxxxxxx výrobní xxxxx xxx xxxxxxxxx xxxxxxx xxxxxx xxxxxxxxx x xxxxxxxx provádění xxxxxxxx, xxxx. xxxxxxxxxxx xxxxxxxx, xxxxxx se doplňuje xxxxxxxx 2001/83/XX, xxxxx xxx x xxxxxx x xxxxxx xxx xxxxxxxx xxxxxxx xxxxx xxx humánní xxxxxx xxxxxxxxx.
Xxxxxxxxxx xxxxx xxxx x xxxxxxx se xxxxxxx xxxxxxxxxxxxx pro Xxxxxx republiku x xxxxxxxx x Evropské xxxx, Xxxxxxxx x xxxxxxxxxxx České xxxxxxxxx x Evropské xxxx xxx s xxxxxxxxxxx xxxxxxxx xxxxxx Xxxxxxxx xxxx x je x souladu s xxxxxxxx xxxxxxxx xxxxx Xxxxxxxx xxxx (např. xxxxxxx xxxxxx jistoty, xxxxxxxxxxxxxxx a xxxxxx xxxxxxxxxxxx).
X xxxxxxxx Xxxxxxxx xxxx, xxxxx xx xxxxxxxx na oblast xxxxxxx xxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx x xx xxxxxx xxxxxxxxx xxxxxxxx xxx xxxxxxxx xxxxx xxxxxxx na xxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx, xx návrh xxxxxx zákona x xxxxxxxx přímo dotýká xxxxxx xxxxxxxx:
- xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Xxxx 2001/83/ES xx xxx 6. xxxxxxxxx 2001 o xxxxxx Xxxxxxxxxxxx xxxxxxxxx xx xxxxxxxxx xxxxxxxx přípravků, x xxxxxxx xxxxx (xxxx jen „směrnice 2001/83/ES“),
- xxxxxxxx Evropského xxxxxxxxxx x Xxxx 2011/62/EU xx xxx 8. xxxxxx 2011, xxxxxx xx mění xxxxxxxx 2001/83/XX x xxxxxx Xxxxxxxxxxxx týkajícím xx xxxxxxxxx xxxxxxxx xxxxxxxxx, xxxxx xxx x zabránění xxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx xx xxxxxxxxx xxxxxxxxxxxxxx xxxxxxx (xxxx jen „xxxxxxxx 2011/62/EU“),
- xxxxxxxx Xxxxxx x přenesené xxxxxxxxx (EU) 2016/161 xx xxx 2. xxxxx 2015, xxxxxx xx xxxxxxxx směrnice Xxxxxxxxxx xxxxxxxxxx x Xxxx 2001/83/XX stanovením xxxxxxxxxx xxxxxxxx xxx xxxxxxxx xxxxx uvedené xx xxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx (xxxx xxx „xxxxxxxx o xxxxxxxxxx prvcích“).
Předkládaný xxxxx xxxxxx xx xxxx xxxxxxxxxx x předpisy Xxxxxxxx unie, xxxxxxxxxxx xxxxxxxx xxxxxx Xxxxxxxx xxxx x obecnými xxxxxxxx zásadami práva Xxxxxxxx unie.
6. Xxxxxxxxxx xxxxxxx x xxxxxxxxxxxxx xxxxxxxxx, xxxxx xx Xxxxx xxxxxxxxx xxxxxx
Xxxxxxxxxx xxxxxx xxxxxxxxxx xxxxxxxxxxxx xxxxxxxx, kterými je Xxxxx xxxxxxxxx vázána. Xxxxx xx x xxxx xxxxxxxxxxx smlouvy:
- xxxxxx x xxxxxxxxx xxxxxxxx xx xxxxxx x xxxxxxxxxx xxxxx, xxxxxxxxx x označení xxxx Xxxxxxxxx společenstvím x Xxxxxxxxx (Úř. xxxx. X 229, 17.8.1998, x. 3),
- xxxxxx x xxxxxxxxx xxxxxxxx xx vztahu x posuzování xxxxx xxxx Evropským xxxxxxxxxxxxx x Xxxxx Xxxxxxxx (Xx. věst. L 229, 17.8.1998, s. 62),
- dohoda x xxxxxxxxx uznávání xxxx Xxxxxxxxx společenstvím x Xxxxxxx (Xx. věst. X 280, 16.10.1998, x. 3),
- xxxxxx x xxxxxxxxx uznávání xxxx Evropským xxxxxxxxxxxxx x Xxxxxxxxx (Xx. xxxx. L 284, 29.10.2001, x. 3),
- xxxxxx mezi Evropským xxxxxxxxxxxxx x Xxxxxxxxxx xxxxxxxxxxx x xxxxxxxxx xxxxxxxx xx xxxxxx x xxxxxxxxxx xxxxx (Xx. xxxx. L 114, 30.4.2002, s. 369).
7. Předpokládaný hospodářský x xxxxxxxx dosah xxxxxxxxxx xxxxxx xxxxxx xx xxxxxx xxxxxxxx, xxxxxxx veřejné xxxxxxxx, xx xxxxxxxxxxxxx xxxxxxxxx Xxxxx xxxxxxxxx, sociální xxxxxx, včetně xxxxxx xx xxxxxxxxxx skupiny xxxxxxxx, xxxxxxx xxxxx xxxxxxxx xxxxx, osoby xx xxxxxxxxxx xxxxxxxxxx x xxxxxxxxxxx xxxxxxx, xxxxxx xx xxxxxxx xxxxxxxxx
Xxxxxxxxxx úpravy xx xxxxxx zajištění xxxxxxxx xxxx implementovaných předpisů Xxxxxxxx xxxx xxxxxxx xxxxxxxxxxxx xxxxxxxx xxxxx xxxxxxxxxxx v navýšení xxxxxx xxxxxxxxxxxxxxx xxxx xxxxxx xxxxxxxxxx na xxxxx xxx stávající xxxxx daný xxxxxxxxxxx xxxxxxxxxx x xxxxxxxxxx xxxx ve xxxxxxxxxx xxxxxxx spadajících pod xxxxxxxxxxx kapitolu Xxxxxxxxxxxx xxxxxxxxxxxxx, xxxxxxxxx xx xxxxxx Ústavu.
Navrhovaná právní xxxxxx nebude xxx xxxxx sociální xxxxxx, xxxx dopady na xxxxxxxxxx xxxxxxx obyvatel (xxxxx sociálně xxxxx, xxxxx se zdravotním xxxxxxxxxx, xxxxxxxxxxx menšiny), xxx xxxxxx na xxxxxxx xxxxxxxxx.
Xxxxxx na xxxxxxxxxxxxx xxxxxxxxx České xxxxxxxxx xx xxxx x xxx xxxxxxxxxxx xxxxxx x xxxxxxxx, xxxxx do xxxx xxxx xxxxxxx jeho xxxxxxx, xx. zákonem č. 70/2013 Sb., x mají xxxxxxxxx xxxxxxxx, xxxxxxxx xx xxxx xxxxx x xxxxxxxx o xxxxxxxxxx prvcích. Tyto xxxxxx xxx byly xxxxxxxxx xxx projednávání xxxxxx právních předpisů. X xxxxx xxxxx xx xxxxx xxxxxxx xx důvodovou xxxxxx, xxxxxx xxxxxx x xxxxxxxxx dopadů regulace (XXX) k zákonu č. 70/2013 Sb. a xxxx xx xxxxxxxxx zprávu XXX k xxxxxxxx x ochranných prvcích xxxxxxxxx „Impact Xxxxxxxxxx“. X této podrobné xxxxxx xx uvádí, xx x xxxxxxx x čl. 4 směrnice 2011/62/XX a čl. 54x xxxx. 2 x 3 xxxxxxxx 2001/83/XX Xxxxxx xxxxxxxxx xxxxxxx, xxxxxxx x xxxxxxxxxx xxxxxxxxxx xxxxxxx xxxxxxxx xxx xxxxxxxxxxxxxxx x xxxxxxxxx xxxxxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx x xxxxxxx xxxxxxx ochranných xxxxx x xxxxxxxx x xxxxxx systému xxxxxxx.
Xxxxxxx realizace xxxxxxx xxxxxxxxx léčivých xxxxxxxxx xxxxx dopadat xx xxxxxxx x držitelé xxxxxxxxxx x xxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxx. Xxxxxxx xxxxxxxx xxxxxxxxx opatřených xxxxxxxxxx prvky xxxxxxx xxxxxxx xx zřízení x správu xxxxxxx xxxxxxx (tato xxxxxxxxx xxxx xxxxxxx již xxxxxxxx 2011/62/EU, xxxxx xxxx xxxxxxxxxxxxx xx xxxxxxxx řádu XX xxxxxxx č. 70/2013 Sb.). Xxx xxxxxxx x xxxxxxxx xxxxxxx představuje zavedení xxxxxxxxxxx identifikátoru xx xxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx xxxxx xxxxxxx, xxxxx xxxxxxx x xxxxxxxx přizpůsobit výrobní xxxxx xxxx xxxxxxx xxxxx (xxxxxxxx xxxxxxx) x xxxxxxxxxx xx xxxxxxxxxxxx xxxxxxx, xxx xxxx xxxxx xxxxxxxx xxxxxxxxx x jedinečných xxxxxxxxxxxxxxxx xx xxxxxxx xxxxxxxx. Aby bylo xxxxx vytisknout xxxxxxxxx xxxxxxxxxxxxx, xxxx xxx xxxxxx xxxxx xxxxxxxxx xxxxx xxxxxxxx a xxxxxxxxxx xxxxxxxxx.
Xxxxxxx xxxxxxx xxxxx xxxxxxxx kompenzovány xxxxxxxxxxxxx úsporami x xxxxxxx x xxxxxxxx:
- xxxxxxxxx nákladů (xxxxxxxxxx xxxxxxx xxxxxxxxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxx xxxxx xxxxxxxxxxxxxx xxxxxxxx XX xx xxxxxxx potřeba xxx více xxxxxxxxx xxxxx, xxx xxxxxxxx xxxxxxxxxxxx jednotlivých národních xxxxxxx),
- ochrany zájmů xxxxxxx a xxxxxxxx xxxxxxxxxx o registraci (xxxxxxx xxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx xx xxxx povede x xxxxxxx xxxxxxxxx xxxxxxx),
- xxxxxxxxx x xxxxxxx xxxxxxx xxx xxxxxxxxx xxxxxxxxx x xxxxxxx xxxxxxxx xxxxxxxxx, což xxxxxx xxxxxx xxxxx (xxxxx x xxxx xxxxxxxxxxxxx) uvedené v xxxxxxxxxx identifikátoru.
Vznikají xxxx xxxx náklady xx xxxxxx xxxxxxx, xxxxxxx xxxxxx SW, xxxx xxxxxx x v xxxxx xxxxxxx i xxxx xxxxxxxxxx XX. X xxxxxxxx distribuční xxxx xx xxxxxxx „xxxxxxxxx xxxxxxx“, který xxxx xxxxxxxxxxx nebezpečný xxxxxxxxx xxxxxxxx. Proto xx xxxxxxxx, xxx xxxx xxxx xxxxx xxxxx v xxxxxxxx xxxx. Xxxxxxx xxxxx xxxxxxx je xxxxx xxxxxxxxx, xxxx z xxxxxxxx xxxxxxx x xxxxxxx, za jednoznačně xxxxxxxxxxx, x xx xxxxx xxxxxxxxx xxxxxxx xxxxxxxxx xxxxxx. Xxxxx xx předkladatel (xxx xx xxxxxx XX, xxx vnitrostátní) rozhodl xxxxxxx xxxxxx xxx, xxx xx předkládán.
Dopady xx xxxxxxxxxx subjekty xx trhu s xxxxxxxx přípravky, xxxxx xxxxx xxxxxxxxx xx xxxx novelu, xx xxx xxx netýkají xxxxxx xxxxxxxx x xxxxxxxxxx xxxxxxx xxxx xxxxxxxx, xxx pouze xxxxxx xxxx xxxxxx, xxxx zejména xxxx xxxx, ve xxxxxxx xxxx Česká republika xxxxx xxxxxxxx x xxxxxxxxxx prvcích xxxxxxx xxxxxxx zvolit xxxxxxxxx, xxxxx xx xxxxx xxxxxxxxxx xx jejím xxxx.
Xxxxxxx xxxxxxxxxxxx xxxxx x xxxx xxxxxxxxxxx xxxx xxxxxxxxxx x xxxxxx xxxxxxxx xxxxxxxxx xxxxxxx x xxxxxxxxxx xxxxxxxx xxxxxxxx xxxxx x xxxxxxxxx jedinečný xxxxxxxxxxxxx xx xxxxxxx xxxxxxx (xxxxxxxx kamerových xxxxxxx 2D xxxx, xxxxxx distribučních x xxxxxxxxxxxx xxxxxxxx xxxx.).
Xxxxxxxx xxxxx xxxxxxxxxx právní xxxxxx xx xxxxxxxxxxxxx xxxxxxxx z hlediska xxxxxxxxxxxx ochranných xxxxx xx xxxxxxxxxxx xxxxxxxxxxx xx xxxxxxx xxxxxxxxx, xxxxx xxxxx vztahující xx x jedinečnému xxxxxxxxxxxxxx lze xxxxxx xx xxxxx obalu x rámci xxxxxxxxxx xxxxxx x dopadem xx xxxxxxxxx x xxxxxxxxx - xxxx. xxxxxx o xxxxxxxxxxx xxxxxxxxx xxxxxxxxxx, řízení x xxxxx registrace xxxx II, xxxx XX xxxx xxxx XX. Xxxxxxxxxx zvláštní xxxxxxx x změnu xxxxxxxxxx xxxxxxxxxxxxxxxxx xxxxxxxxxx xx xxxxxxxx pouze x xxxxxxx, xxxxx x přechodném xxxxxx xxxxxx xxxxxxxxxx žádná xxxxx xxxxxxxxxx, která xxxxxxx xxxxxxxxx x xxxxxxxxx. Xxxxxxxxxx xxxxxxx x xxxxx xxxxxxxxxx xxx xxxxxxxx prostředku x ověření xxxxxxxxxx x xxxxxx xx xxx xxxxxxxx xxxxx x případě, xxx xxxxxxxxxx x ověření xxxxxxxxxx x xxxxxx xxxx mít xxxx xx xxxxxxxxx xxxxx, xxxx ovlivní xxxxxx xxxxxxxx xxxxx. Dále xxxx xxxxxxxxx, že xxxxxxxxx xxxxxxxxxxxxx x xxxxxxxxxx x xxxxxxx xxxxxxxxxx x xxxxxx xx xxxxx xxxxxxxxxxxxx xxxx xxxxxxxxxxx nebo xxxxxxxxxx xxxxxxxxx xxxxxxx x xxxxx xxxxxxxxxx, xxxxx xxxxxxxxxxxx ochranných xxxxx na xxxx xxxx xxxx na xxxxxxxxx obalu. Xxxxxxxx x xxxx xxxxxxx xxxxxxxxxxx, xxx xxx xxxxxxx xxxxxxxx xxxxxxxxx xxxxxx xxxxx xxx xxxxxxxx xxxxxxxxxx prvků xxxxxxxxxx zvláštní xxxxxx x xxxxx xxxxxxxxxx x xxxxxxxx xxxxx xx xxxxx xxxxxxxxxxxxx xxx xxxx předložením xxxx schválením xxxxxxxxx xxxxxxx o změnu xxxxxxxxxx, dopad na xxxxxxxxxxxxx xxxxxxxx x xxxxxxx xxxxxxxx x x xxxxxxx xxxxxxxxxxxx xxxx na vyřízení xxxxxxxxxxxx žádostí xxxx xxxxxxxxx.
Xxx xxxxxx souhlasit x xxx, že xxxxxxx výrobců a xxxxxxxx rozhodnutí x xxxxxxxxxx xxxxxxxx xxxxxxxxx, xxxxxxx obaly xxxxxxx xxxxxxxx prvky, xx x xxxxxx zavedení xxxxxxxxxx prvků xx xxxxxx xxxx xxxxxxxxx xxxxx. Toto xxxxxxx xxxx bude xx xxxxxx k finančním xxxxxxx xxxxxxxxxxxxxxx xxxxx xxxxxxxxxxxx, xxxxx náklady xx xxxxxxxx XX xxxx u xxxx xxxxxxxx xx recept xxxx zcela xxxxx xxxxxx nižší než xxxxxxxx xxxxxxx na xxxxx, výrobu a xxxxxxxxxx xxxxxxxx xxxxxxxxx. Xxxx xxxxxxxx přípravků, xxxxxxx výdej xx xxxxx na xxxxxxxx xxxxxxx, xx xx xxxxxxx xxxxxxx regulována xxxxxxxx stanovení xxxxxxxxx xxxx xxxxxxxx xxxxxxxxxxx, xxxxxx xxx zvýšit xxxxx na xxxxxxx xxxxxx zpoplatněné xxxxxxx. Xxxxxxxx xxxx x xxxxxxxx úhrady xxxxxxxx xxxxxxxxx x xxxxxxxxxx xxxxxxxxx zdravotního xxxxxxxxx xxxx xxxxxxxxxxx x xxxxx xxxxxxxxx xxxxxx. Xxxxx se x xxxxxx Xxxxxxxx xxxx (xxxxxx ČR) často xxxxxxx xxxxxxx tzv. xxxxxxxx cenového referencování - xxxx xxxxxxxxx xxxx a úhrady xxxxx nejnižších cen xxxxxxxx xx porovnatelného xxxxxxxx xxxxxxxxx xxxxxxxxxx x zahraničí, xxxxx xx v xxxxxx xxxxxxx případů xxxxxx xxxxxxxxxx navýšení xxxx x XX xxxx xx xxxxxx xxxxxxxx xxxxxxxxx z xxxxxxxxxx xxxxxxxxx xxxxxxxxxxx pojištění. Xxxxxxxx x xxxxx xxxxxxxxx xxxxx xxxxxxxxxxxxx xxxxxxxxx xx xxxxxxxxx (xxxxxxx) xxxx x xxxxxx xx xxxxxxxxx xxx léčivých xxxxxxxxx x xxxxxx xxxxxxxx xxxxxxxxxx xxxxx nepředpokládá, xxxx xxxxxx odlišitelné xx xxxxx xxxxxxx. Xxxx regulovaných xxxxxxxx xxxxxxxxx xxxx maximální, xx xxxxxxx xxxxxxxxx xxxxxxxxxxx pojištění se xxxxxxx úhrada léčivého xxxxxxxxx, xxxxxxx jeho xxxx.
Xxxxxxx distributorů xxxxx xxxxxxx s xxxxxxxxxx xxxxxxxx ochranné prvky x vyřazovat jedinečný xxxxxxxxxxxxx ze systému xxxxxxx. Xxxxx xx x xxxxxxxx xxxxxxxxxx xxxxxxx 2X kódů, xxxxxx xxxxxxxxxxxx programů xx náklady xx xxxxxx xxxxxx. Xxxxxxx xxxxx vzniklé xx xxxxx xxxxxxxxx, xxxx x xxxxxxxx nákladů x přínosů, za xxxxxxxxxxx převažující, x xx xxxxxx xxxxx xxxxxxxxx ochrany veřejného xxxxxx. Xxxxx xx xxxxxxxxxxxx (jak na xxxxxx XX, tak xxxxxxxxxxxx) xxxxxxx vymezit xxxxxx xxx, xxx xx předkládán.
Hospodářský x xxxxxxxx dopad xxxxxx x xxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxx přípravků xxx xxx hodnocen v xxxxx xxxxxx zajišťující xxxxxxxx nařízení 536/2014, x xxx xx xxx x xxxxx xxxxxxx. Xxx nařízení xxxx prováděcími xxxxxxxx x xxxxxxxx 536/2014 x xxxxxxxxx x x podrobnostech xxxxxxxxx xx, co nařízení x xxxxxxxxx xxxxxxxxx xxxxxx. Xxxxxx xxxx xxxxxxxx 2017/1572 xxxx xxxxxxxx xxxxx xxxxxxx xxxxxxxx 2017/1569 x xxxxxxxxx xxxxxxxxxx xxxxxxx xx xxxxxxxxx právní xxxxxx, pokud xx xxxx hospodářského x xxxxxxxxxx xxxxxx.
Xxxxxx xxxxxxxx xxxxxx xxxxxxx xxxxxxxxxxxxxxxxx x xxxxxxxxxxxx náklady xxxxxxxxxxxxx x xxxxxxx xxxxx předpokládaných oběma xxxxxxxxx xxxxxxxxxx v xxxxxxx, jak bylo xxxxxxx x xxxxxxxx xxxxxx x xxxxxx xxxxxx zajišťujícímu adaptaci xxxxxxxx 536/2014 (zákon č. 66/2017 Sb.).
8. Zhodnocení xxxxxx xx vztahu x xxxxxxx xxxxxxxx x xxxxxxxx xxxxx
Xxxxx xxxxxx x xxxxxxx ochranných xxxxx léčivých xxxxxxxxx xxxxxxxxx žádné xxxx xxxxxxxxxx osobních xxxxx. Xxxxxx xxxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx xxxx xxxxxxxxxxx informace xxxxxxxxxx xx pouze x xxxxxxx xxxxxxxxxx xxxx xxxxxxxx, xxxxxxx obaly xxxxxxx xxxxxxxx xxxxx. Xxxxxx xxxxxx xxxxxxxxxxx xxxxxx xxxxx xxxxxxxx, xxxxxx byly xxxxxx xxxxxx xxxxxxxxx, xxxxxxx xxxxx xxxxxxx xxxxxxxx xxxxx. Xxxxxxxx xxx xxxxx xxxxxxxxx zneužití xxxxxxxx údajů. Xxxxx xxxxxx x tomto xxxxxx xxxxxx xxx xxxxx negativní dopady xx xxxxxx xxxxxxx xxxxxxxx x xxxxxxxx xxxxx.
Xxxxxxxxxx xxxxxx úprava xx x xxxxxxx xxxxxxx xxxxxxxx praxe xxxxxx xxxxxxx xxxxxxx xxxxxxxx, a to xxxxxxxxxxxx xxxxxxxx. Xxxxxxxx 2017/556 xxxxxxx inspektorů xxxxxx široké pravomoci, xxxxx xx týká xxxxxxxx do xxxxxxx x xxxxxxxxx xxxxxxxxxxxxx x klinickým xxxxxxxxxx. Xxxxxxxxxx xxx zcela xxxxx budou mít xxxxxxx x xxxxxxx xxxxxx xxxxxx citlivých xxxxxxxx údajů. Xxxxxxxx xxx xxxxxxxxx xxxxxxx xxxxxxxxx xxxxxxxxx, xxxxxxx xxxxxxxx údajů xxxxxxxx xxxxxxxxxx hodnocení xxxxxxxxxx xx zdraví, jakož x xxxxxxxxx xxxxxxxxxx xxxxxxxxx, když xxxxxxxxxx x xxxxxxxxx xxxxxxxxxx xx xx inspekcích xxxx xxxxxxxxxx standardy xxxxxxxxxx x použitelnými xxxxxxxxx xxxxxxxx předpisů Xxxx x xxxxxxxxxxxxxx xxxxxxxx předpisů. X xxxxxx 14 xxxxxx xxxxxxxxxxx x xxxxxxxxxx xxxxxxxxxx do xxxxxxxxxxx xxxx povinnost xxxxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxx, x xxxx xxxxxxx xxxxxxx x důsledku xxxxxxxx xxxxxxx xxxxxxxx xxxxx.
Xxxxxxxx dále xxxxxxxx xxxxx, že xxxxxxxxx xxxxxx xxxxxxxxxx prostřednictvím xxxxxxx XX (v xxxxxxx x čl. 78 xxxx. 6 xxxxxxxx x. 536/2014) nesmějí xxxxxxxxx osobní xxxxx xxxxxxxx (čl. 13 xxxxxxxx 2017/556)
Xxxxxxxxxx x odborníci xxxxxxxxxx se xx xxxxxxxxxx xxxx xxx xxxxxxxxxxxx xxxxxxxx xxxxx xxxx xxxxxx požadavky xxxxxxxx xxxxxxxx x xxxxxxx xxxxxxxx xxxxx č. 2016/679 (Xxxxxxx Xxxx Xxxxxxxxxx Xxxxxxxxxx, GDPR).
Nařízení č. 2017/1569 x xxxxxxxx XXX xxxxxxxx inspekce, xxxxxxxxxxxxxxx xxxxxxx xxxx xxxxxxx xxxxx povinny xxxxxxxx, aby x xxxxxxx klinického hodnocení xxxx dodržována xxxxxxxx xxxxxxx xxxxxxx xxxxx xxxxxxxxxxx léčivých xxxxxxxxx xxxxxxxxx v xxxxx xxxxxxxx. X toto xxxxxxxx svěřuje xxxxxxxxxxx xxxxxx xxxxxx xxxxxxxxx, xxxxx xx týká xxxxxxxx xx prostor x xxxxxxxxx souvisejících x xxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx. Xxxxxx x x xxxxx xxxxxxx xxxx inspektory xxxxxxxxxxxx, když xxxxxxx, xx xxxxxxxxx získané xx xxxxxxx xxxxxxxx xxxx xxxxxx xxxxxxx.
Xxxxxxxxxxx xxxxxxxx se xxxxxxxx xxxxxxxxxx zákona x xxxxxxxx, ani xxxxxx x xxxxxxxxxxx xxxxxxxx, xxxxxxx xx xxxxxxxxxxx xxxxxxx xxxxx, xxxxx xxxxxxxxxx xxxxxxx v xxxxx prováděných xxxxxxx x xxxxxxxx.
Xxxxxxxx xxxxxxx xxxxxxxx praxe x xxxxxxx xxxxxxx xxxxx xxxxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx xxxxx xxxxxxxx xxxxx xxxxxxxx č. 536/2014, x xx xxxxx xxxxxxxxx v souladu x xxxxxxxxxx 556/2017 x 1569/2017. Xxxxxxxx xxxxxxxxx podle xxxxxx x xxxxxxxx jsou xxxxxxxxx x xxxxxxx x xxxxxxxxxx xxxxx, xxxxx obsahuje ustanovení xxxxxxxx xxxxx xxxxxx xxxxx xxxxxxxxx osoba, xxx xxxxxxx údaje xxxxxxx na základě xxxxxxxxx xxxxxxxx. Xxxxxxxxx xxxxxxxx x xxxxxx xxxxxxxx xxxx představovat xxxxx, xxxx kterému xxxxxxxx právní xxx Xxxxx xxxxxxxxx xxxxxxxx xxxxxx. Xxxxxx xxxxx xxxx xxxxx xxxxxxxx xxxxxxxxx xxxxxxx, x x účinností od xxxxxx 2018 xxx xxxxxxxxx EU.
Na xxxxxxx xxxx xxxxxxxxx lze xxxxxxxxxxx, xx ve xxxxxx x ochraně xxxxxxxx a osobních xxxxx xxxxxxxxxx xxxxxx xxxxxxxxxxxxx xxxxxxx xxxxxx.
9. Xxxxxxxxxx korupčních rizik
V xxxxx xxxxxxxx návrhu xxxxxx xxxx komplexně xxxxxxxxx xxxx korupčních xxxxx v xxxxxxx x xxxxxxxxx xxxxxxxxxxx Xxxxxxx xxxxxxxxx dopadů xxxxxxxx Xxxxx vlády Xxxxx republiky. Xx xxxxxx xxxxxxxxx xxxxxxx, xx z xxxxxx xxxxxx xxxxxx xxxxxxx xxxxxxxx potenciál, xxxxx xxxx xxxxxxxxxxxxx xxxxxxxx x xxxxxxxxx xxxxxxxxxxx xxxxx xxxxxx.
Xxxxxx xxxxxxxxx xxxxxxxx by xxxxx xxxxxxxxxxxx určitý xxxxxxxx xxxxxxxxx, přičemž xxxxx xxxx xx xxxxxx x textu xxxxxxxxx xxxxxxxx: x obou xxxxxxxxxx jsou ustanovení xxxxxxxx upravující xxxxxxxxx xx xxxxxxxxxxx inspektorů. X xxxxxxxx 2017/1569 xx xx článek 23, xxxxx xxxxxxxx ukládá xxxxxxxx, aby xxxxxxxxxx xxxxxx xxxxxxxxx žádným xxxxxxxxxxx xxxxxx, xxxxx xx mohly xxxxxxxx xxxxxx xxxxxxxxxxx a xxxxxx.&xxxx; Xxxxxxxx uvádí, xx xxxxxxxxxx musí xxx xxxxxxxxx xxxxxxx xx xxxxxxxxxx, xxxxxx x pracovnících xxxx xxxxxxxxxx xxxxxxxxx, xxxxxxxxxxxx x xx osobách xxxxxxxxxxxxx klinické xxxxxxxxx. Xxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxxxxxx předkládat prohlášení x xxxxx xxxxxxxxxx xxxxxxx xx stranách xxxxxxxxx inspekcemi xxxx x xxxxxx xxxxxxx xx xx. Xxxxxxxxx xxxxx xxxxx xxxxxxxxxx x xxxxx xxx xxxxxxxxxxx xxxxxxxxxxx inspekcí xxxxxxxxxxx xxxxxxxxxxx.
X xxxxxxxx 2017/556 xxxxxxxxxx článku 5 xxxxxxx, xx inspektoři xxxxx být xxxxxxxxx xxxxxxx vlivu, xxxxx xx mohl xxxxxxxxxx xxxxxx xxxxxxxxxxx nebo xxxxxx xxxxxxxxx, xxxxx xxx xx xxxxxx xxxxx. Xxxxxxx xxxx xxx nezávislí xx xxxxxxxxxx, xxxxxxxxxxxx xxxxxxxxxxx xx klinického xxxxxxxxx, xxxxxxx xxxxxxxxxxxxx klinické xxxxxxxxx x xx xxxxxxxxxx xxxxxxxx xxxxxxxxxxx xx na xxxxxxxxx xxxxxxxxxx xxxxxxxxx. Rovněž x xxxx xxxxxxxx xxxxxx inspektorům každoročně xxxxxxxxxx prohlášení x xxxxx xxxxxxxxxx xxxxxxx x xxxxxx vazbách xx xxxxxxxx, xx xxxxxxx xxxx xxx xxxxxxxx xxxxxxxxx. X xxxxxx xxxxxxxxxx xx xxxxxxxx xxx xxxxxxxxxxx xx konkrétní xxxxxxxx. Xxxxxxxxxx xxxxxx úprava xx xxxxxx ustanovení xxxxxxxxxx x xxxx xx xxxxxxxxxx. Xxxx xxxxxxxxxx xxxx xxxxx xxxxxxx.
Xxxxx xx xxxx xxxxxxxxxxx xxxxxxxx 2017/1572, x čl. 3 ukládá xxxxxxxx xxxxxx xxxxxxxxx xxxxxx opakovaných inspekcí xxxxxxxxx x čl. 111 xxxx. 1a xxxxxxxx 2001/83/XX zajistit, xxx xxxxxxx, kteří xxxx xxxxxxxx podle čl. 40 xxxx. 1 a 3 xxxxxxxx 2001/83/ES, xxxxxxxx zásady a xxxxxx xxx xxxxxxxx xxxxxxx xxxxx xxxxxxxxx xxxxx xxxxxxxx. Xxxx xxxxxxx, že xxx xxxxxxx zásad a xxxxxx xxx správnou xxxxxxx praxi xxxxxxxxxx xxxxxxx a xxxxxxxxx xxxxxx x podrobným xxxxxxx uvedeným v čl. 47 xxxxxx xxxxxxxxxxx xxxxxxxx 2001/83/ES. X xxxxxxx xxxxxxxx xxxxxxxxx xxx xxxxxxx terapii xx xxxxxxxxx xx xxxxxxxxx pokynům xxx xxxxxxxx xxxxxxx xxxxx xxxxxxxxx xx xxxxxxxx xxxxxxxxx xxx xxxxxxx xxxxxxx, xxx xxxx xxxxxxx x článku 5 xxxxxxxx (XX) x. 1394/2007 x xxxxxxxx xxxxxxxxxxx xxx xxxxxxx xxxxxxx. Xxxxxx 3 xxxxxx rovněž členským xxxxxx xx svých xxxxxxxxxxxxxx xxxxxxxx x xxxxxx xxxxxxxx xxxxxxxx xxxxxx xxxxxxx, který xxxx xxxxxxxxxx a xxxxxx xxxxxxxxxxxx xxxxxxxxx. Xxxxxxx xxxxxx xxxxxxx xx xxxxx potřeby xxxxxxxxxxx. Xxxxxxxxxx právní xxxxxx xxxxxxxxxxx xxxxx xxxxxx x xxxxxxxxxxxx xxxx 3 - xxxxxxxx §13 odst. 3 písm. l) xxxxxx o xxxxxxxx. Xxxxxx xxxxxxx xxxxxx xxxxxxx xxxxxxxxxx rizik xxxxxxxx instrumenty, jako xx xxxx xx xxxx xxxxxxxxx xxxxxxxxxx.
Xx xxxxxxx xxxxxxxxx xxx xxxxxxxxxxx, xx potenciál xxxxxxxxxx rizik xxxx xxxxxx xxxxxx významným xxxxxxxx snižuje.
10. Zhodnocení xxxxxx na bezpečnost xxxx xxxxxx xxxxx
Xxxxx xxxxxx xxxx vztah x xxxxxxxxxxx xxxx xxxxxx xxxxx.
XX. XXXXXXXX XXXX
ČÁST PRVNÍ Změna zákona o léčivech
Xx xxxxxxxx xxx xxxxx x. 2 xx xxxxx xxxxxxx odkaz xx xxxxxxxx Xxxxxx x xxxxxxxxx pravomoci (XX) 2016/161 ze xxx 2. října 2015, xxxxxx xx xxxxxxxx xxxxxxxx Xxxxxxxxxx xxxxxxxxxx a Rady 2001/83/XX xxxxxxxxxx xxxxxxxxxx xxxxxxxx xxx xxxxxxxx xxxxx xxxxxxx xx xxxxx humánních xxxxxxxx xxxxxxxxx, xxxxx xx xxxxx xxxxx xxxxxxx xxxxxx adaptováno na xxxxxxxx x České xxxxxxxxx.
K bodu 2 (§5 xxxx. 7):
Xx nezbytné xxxxxxxx xxxxxxxx xxxxxxx vyhrazených xxxxxxxx xxxxxxxxx z xxxxxxx xxxxxxxxx a xxxxxxxxxxxxx léčiv.
K bodu 3 (§6 xxxx. 2):
Xxxxx se x transpozici článku 2 xxxx. 3 směrnice Xxxxxx (XX) 2017/1572, xxxxx xxxxxxxx správnou xxxxxxx xxxxx xxxx xx část zabezpečování xxxxxxx, která zajišťuje, xxx xxxx xxxxxx xxxxxxxxx xxxxx xxxxxxxx, xxxxxxxx a xxxxxxxxxxxx x souladu se xxxxxxxxx jakosti xxxxxxxxxxx xxxxxx xxxxxxxxxxx účinku. Xxxx xxxxxxxx xx xxxxxxxx xx odst. 2.
Xxxxxxx xxxx se xxxxxxxx xx xxxxxx, xxxxx tedy xxxx xxxxxxx nahradit.
K bodu 4 (§13 xxxx. 2 xxxx. x):
Xxxxxxxx x xxxxxxxxxxxxx, xxxxxxx osob zacházejících x léčivy, držitelů xxxxxxxxxx x xxxxxxxxxx, xxxxxxxxxxxxxxxxx, xxxxxxx a xxxxxxx xxxxxxxxx látek xxxxxx xxxxxxxx xxx x xxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxx o xxxxxxxx, xxx xxxx xxxxxxxxx i kontrolu xxxxxxxxxx přímo použitelných xxxxxxxx Evropské xxxx xxx oblast xxxxxxxxx xxxxx, xxx xxxx xxxxxxxx xxxxxxxx a xxxxxxxx členským xxxxxx xxxxxxxx. Xxxxx xx:
• Xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Rady (XX) x. 1394/2007 (32007R1394), xx 13. xxxxxxxxx 2007 x xxxxxxxx xxxxxxxxxxx xxx moderní xxxxxxx x o xxxxx xxxxxxxx 2001/83/ES x xxxxxxxx (ES) x. 726/2004.
- Nařízení Xxxxxxxxxx parlamentu x Xxxx (EU) č. 2016/793 (32016X0793) xx xxx 11. xxxxxx 2016, k xxxxxxxx xxxxxxxxxxxx xxxxxxx s xxxxxxxxx xxxxxxxxx xxxx xx Xxxxxxxx xxxx.
- Xxxxxxxx Xxxxxxxxxx parlamentu x Rady (XX) x.536/2014 (32014R0536), x xxxxxxxxxx xxxxxxxxxxx humánních xxxxxxxx xxxxxxxxx x x zrušení směrnice 2001/20/XX (nařízení dosud xxxx účinné)
- Prováděcí xxxxxxxx Xxxxxx (XX) č. 2017/556 xx xxx 24. března 2017 x xxxxxxxxxx xxxxxxxxxx xxx xxxxxxxxx xxxxxxxxxxx xxxxxxx správné xxxxxxxx xxxxx xxxxx xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Xxxx (XX) x. 536/2014 (xxxxxxxx xxxxx xxxx xxxxxx)
-- Nařízení Xxxxxx v xxxxxxxxx xxxxxxxxx (EU) č. 2017/1569, xxxxxx xx xxxxxxxx xxxxxxxx Evropského xxxxxxxxxx x Xxxx (XX) x.536/2014 xxxxxxxxxx zásad x xxxxxx pro xxxxxxxx výrobní xxxxx xxx xxxxxxxxx xxxxxxx xxxxxx xxxxxxxxx x xxxxxxxx provádění xxxxxxxx
- Xxxxxxxx Xxxxxx x xxxxxxxxx xxxxxxxxx (EU) x.1252/2014 (32014R1252), xxxxxxxxxx xxxxxxxx Xxxxxxxxxx parlamentu x Xxxx 2001/83/XX, xxxxx jde x xxxxxx x xxxxxx xxxxxxx výrobní xxxxx xxx xxxxxx xxxxx xxx humánní léčivé xxxxxxxxx
- Xxxxxxxxx Xxxxxxxx Xxxxxx (XX) č. 699/2014 xx xxx 24. xxxxxx 2014 x xxxxxxx společného xxxx xxxxxxxxxxxx xxxxx xxxxxxxxxx xxxxxx xxxxxxxxx x xxxxxxx xxxxxxxxxx xx xxxxx x x technických, xxxxxxxxxxxxxx x xxxxxxxxxx požadavcích x xxxxxxx xxxx xxxxxxxx
- Xxxxxxxx Xxxxxx x xxxxxxxxx pravomoci (XX) 2016/161 xx xxx 2. xxxxx 2015, xxxxxx xx xxxxxxxx xxxxxxxx Xxxxxxxxxx xxxxxxxxxx a Rady 2001/83/XX xxxxxxxxxx xxxxxxxxxx xxxxxxxx pro xxxxxxxx xxxxx xxxxxxx xx xxxxx xxxxxxxxx léčivých xxxxxxxxx
K bodu 5 a 6 (§13 xxxx. 2 xxxx. o xx q):
V §13 xxxx. 2, xxxxx xxxxxxxx xxxxxxxxx Xxxxxxxx xxxxxx xxx xxxxxxxx xxxxx, xx xxxxxxxx xxxxxxxxxxx xxxxxxxxxx.
Xxxxxxxxx xx xxxxxxxxx Ústavu v xxxxxxx xxxxxxxxxx xxxxxxxx xxx xxxxxxxx xxxxx, x to x xxxxxx, xx x xxxx xxxx xxxxxxxxxx xxxxxxxx o xxxxxxxxxx xxxxxxx (xxxxxxxx XX) xx xxxxxxxx oprávnění x xxxxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx xxxxxx x xx xxxxxxxx xxxxx xx, aby určil, xxxxx xxxxx xx xxx xxxx území xxx příslušným x xxxxxxxxx xxxxxxxx x xxxxxxxx o xxxxxxxxxx xxxxxxx. Xx xxxxxx, xx s ohledem xx dosavadní právní xxxxxx působnosti Xxxxxx, xxxxxxx regulační xxxxxxxx xxx xxxxxx xxxxxxxxx xxxxx, xxxx xxx xxxxxxxxxx xxxxxxx k xxxxxxxxx uvedeným x xxxxxxxx x xxxxxxxxxx xxxxxxx určen xxxxxx xxxxx xxxxx xxxxx.
Xxxx xx xxxxxxxxx Státního xxxxxx xxx xxxxxxxx xxxxx rozšiřuje xxx, xx xx určen xxxxxxxx xxxxxxx xxxxxxxxxx x xxxxxx xxxxxxxxxx xxxxxxxxxxx xxxxxxxxx 2017/556 x nařízením 2017/1569. Xxx xxx o xxxxxx adaptaci článku 17 xxxx. 6 a článku 25 xxxxxxxx x. 2017/1569 x xxxxxx xxxxxxxx článku 3 xxxx. 1, článku 12 x článku 13 nařízení č. 2017/556. Xxxxxx xxxxxxxxx xxxx části xxxxxxxxxxxxx xxxx by xxxx xxx xxxxxx, jaké xxxx nastaveno v xxxxxx č. 66/2017 Sb. xxx xxxxxxxxxx xxxxxxxxxx xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Xxxx (XX) č. 536/2014.
K bodu 7 (§13 xxxx. 3 xxxx. l)
Jedná xx x xxxxxxxxxxx čl. 3 xxxx. 3 směrnice 2017/1572 x xxxxxxxx čl. 22 nařízení 2017/1569. Xxxxxxxx 2017/1572 xxxxxxxx xxxxxx ukládá na xxxxx xxxxxxxxxxxxxx vytvořit x zavést xxxxxxxx xxxxxxxx xxxxxx xxxxxxx, xxxxx musí xxxxxxxxxx x xxxxxx inspektorátu xxxxxxxxx. Xxxxxxx xxxxxx xxxxxxx xx xxxxx xxxxxxx aktualizuje. Xxxxxx xxx xxxxxxxx 2017/1569 xxxxxxx xxxxxx xxxxxxxxxx xxxxxxx xxx inspektory xxxxxxxx, xxxxxx x xxxxxxxxx xxxxx navržený xxxxxx jakosti. Systém xxxxxxx xx x xxxxxxx potřeby xxxxxxxxxxx.
K bodu 8 (§16 xxxx. 3 xxxx. x)
Xxxxx xx x xxxxxxxxxxxx-xxxxxxxxxx úpravu xxxxxx spočívající x xxxxxxxxxxxxxxx xxxxxxxxxx xxxxx xxxxxx xxxxx.
K bodu 9 (§22 xxxx. 2)
Smysl xxxxxxx xxxx „veterinárních léčivých xxxxxxxxx“ spočívá xx xxxxxxxxxxx, xx požadavky xx kvalifikaci xxxxxxxxxx xxxxxxx klinické praxe xxxx xx zákona x léčivech vyjmuty, xxxxx xxxx přímo xxxxxxxx xxxxxxxxxx xxxxxxxxx. Xxxxxxx xxxxxxx xxxxxxxxxx xxxxxxx xxxx požadavky xxx inspektory xxxxxxxxxxxxx xxxxxxxxxx hodnocení.
K bodu 10 (§23 xxxx. 1 xxxx. x):
Xxx xxxxxxx, xxx xxxxxxxxx xxxxxxxxxxxxx neprodleně xxxxxxx Xxxxxxxx xxxxxx xxx xxxxxxxx léčiv xxxxxxxxx xx xxxxxxxx xxxxxx xxxxxxxxx, xxx-xx x xxxxxxx léčivý xxxxxxxxx, xxxxxxxxx xxxxx x xxxxxxxx x xxxxxxxxxx xxxxxxx, xx xxxxx tuto xxxxxxxxx xxxxxx výslovně v xxxxxx x xxxxxxxx xxxxxxxxx písmene f) xx §23 xxxx. 1 xxxxxx. Xxxxx xx xxxxxxxxx o xxxxxxx, xxx xx x xxxxxxxxx xxxxxxx xxxxxxxxxx xxxxx xxxxx, xxxxx nemá dle xxxxxxxx x ochranných xxxxxxx žádnou povinnost. Xxxxxxxx ke xxxxxxxxxxx, xx xxxxxxxx se xxxx xxxxx x xxxxxxxxxxxxx xxxxxxxx přípravků, xxxxxxxx xx do xxxxxx xxxxxx xxxxxxxxx xxxxxxx xxxxxxxxx na xxxxxxxx veterinární xxxxxx xxxxxxxxx Veterinárnímu xxxxxx.
K bodu 11 (§24 xxxx. 10):
Stávající xxxxx §24 xxxx. 10 xx v xxxxxxx x ustanoveními xxxxxxxxxx xxxxxxxx xxxxxxxx, xxxxxxxxxxxx xx xxxxxx xxxxxxxxxxxxx xxxxx xxxxxx xxxxxxxx celních orgánů, xxxx. xxxxxxxxxxxx xxxxxxxx xxxxxxxx plnění xxxxxxx xxxxxxxx xxx xxxxx xxxxxxxxxx na xxxxx xxxxx Xxxx xxxx xxxx území xxxxxxxxxxx, xxxxxx je nařízení Xxxxxxxxxx xxxxxxxxxx x Xxxx (XX) č. 952/2013, xxxxxx xx xxxxxxx xxxxx xxxxx Xxxx, x xxxxxxx znění (xxxx jen „UCC“). Xxxxxxxxxx článku 5 odst. 15 UCC xxxxxxxx xxxxx xxxxxxxxxx xxxx xxxxx, xxxxx xxxxxx xxxxx xxxxxxxxxx (x xxxx xxxx xxxxxxxxxxx xxxxx xxxxxxxxx) xxxxxxxx xxxxxx nebo osobu, xxxxxx xxxxxx xx xxxx xxxxx xxxxxxxxxx xxxxxx. Xxxx ustanovení článku 18 xxxx. 1 XXX xxx jakýchkoli xxxxxxx, xxxxxxx xx xxxxxx xxxxxxx, že xx xxxxx xxxxx xxxx nechat xxxxxxxxx xxxxxx xxxxxxxxx, xxxxxxx xxxx zastoupení xxxx xxx xxxxx (xxxxxxxx xxxxx xxxxxx a xx účet xxx xxxxx) xxxx xxxxxxx (xxxxxxxx jedná vlastním xxxxxx xx xxxx xxx xxxxx). Článek 170 xxxx. 1 XXX xxxxx pododstavec xxx xxxxxxx, xxxx xxx xxxxxxxxxx výjimek, xxxxxxx xx výhrad, že xxxxx x přijetí xxxxxxx xxxxxxxxxx xxxxxxxxx xxx určitou xxxxx xxxxxxxx xxxxxxxxxx (xxxx. xxxxx předložení souhlasu, xxxxxxxx xx xxxxxxx xxx xxxxxxxxxx xxxxx x rámci xxxxxxxxx xxxxxxxxxxx zákazu nebo xxxxxxx), xxxx takové xxxxx prohlášení xxxx xxxxx xxxx xxxx xxxxxxxx. Z xxxxxxxx xxxxx xxxxx výše xxxxxxxxxxxx xxxxxxxxxx je xxxxxx, xx xxxxx xxxxxxxx xxxxxxxx xxxxxxxxx x xxx xxxxxxxxxx xxxxxxxxx xxxxx xxxxxxxxx (xxxxxxxxxxxx, xxxxxxxxxxxxx) xxxxxxxx xxxxx xxxxx xxxxx xxxxxxxx, ale dále xxxx xxx xxxxx xxxxx xxxxx xx xxxx xxxxx zastoupení. Xxxxx osoba, xxxx x xxxxxxx xxxxxxxxxx xxxxxxxx (licence xx xxxxxxxx) xx xxxx xxxxxxxx xxxxxx xxxxxxxx, xxxxxxx xxxx xxxxxxxxxx xx xxxx xxxxxxxx xxxxxx xxxxx xxxx xxxxx (deklarantem ve xxxxxx xxxxxxxx xxxx xx xxx) nebo xxxx nepřímé (xxxxxxxxxxx xxxx xxxxxxx zástupce). Xxxx xxxxxxxx xxxx xxxxxxxxxx veškeré xxxxxx xxxxxxxx, xxxxxxxxxx jakoukoli xxxxxx xxxxxx či xxxxxxx na xxxxxx xxxxx Xxxxxxxx xxxx x xxxx xxxxxxxxx xxxxxxx xxxxxxxxxxxxxx xxxxxxxx xxxxxxxx x ustanovení, xxxxxxxxxx k xxxxxxxxxxxxxxx §24 odst. 10 xxxxxx x xxxxxxxx, xx x xxxx xxxxxxxxx.
K bodu 12 (§34 odst. 9):
Xxxxxxxx xx ustanovení xxxxxxxxxx Ústavu x Xxxxxxxxxxxxx xxxxxx xxxxxxxxx xxxxxx x xxxxx xxxxxxxxxx léčivého přípravku xxxxxxxxxx xxxx vyhrazené xxxxxx xxxxxxxxx x xxxxxxx nových skutečností xxxxxxxxxx xx xxxxxxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx, x xx x xxxx xxxxxx (xx xxxx).
K bodu 13 (§37 odst. 1):
X xxxxxx x xxxxxxxx xx třeba xxxxxxx xxxxxxx xxxxxxxxxx xxx, xxx xxxxxxxxxx xxxxxxxxxxx xxxx, xx xx xxxxxxxx xxxxxxxxxx xxxxxxxx xxxxx: to xxxxxxxxx xxxxxxxxxxxxx x xxxxxxxxxx x xxxxxxx xxxxxxxxxx x xxxxxx. Xxxxxxxx je xxxxx xxxxxxxx xxxxxxx xxxxxxxxxxx xxxxxxxxxx xxxxxxx kódu, xxxxx slouží k xxxxxxxxxxxx xxxxxxxx xxxxxxxxx, xxxxx xxxxxxxx xxxxx xxxxxxxxx.
Xxx x nutnou xxxxxx navazující xx xxxxxxxx x ochranných xxxxxxx, xxxxx xxxxxxxx xxxxxxxx xxx xxxxxxxx xxxxxxx kód (XXX), xxx 2D xxx, xxxxx xxxxxx xxxxxxxxx xxxxxxxxxxxxx. Xxxxxx xxxxxxxxx xxx xxxxxxxxxx xxxxx xxxxx xxxxxx používat XXX xxx x xxxxxxxx xxxxxxxxx je xxxxxxxxxx pro xxx xxxx xxxxxxx xxxxx xxxx.
K bodu 14 (§37 xxxx. 7):
Xxxxxxxx 7 zákona x léčivech xx xxxxxxxxxxxxx xxxxxxxxxxx směrnice 2011/62/EU a je xxxxx jej xxxxxxx x souladu x xxxxxxxxx x ochranných xxxxxxx.
K bodům 15 (§37 odst. 8):
Xxxxxxxx 8 xxxxxx x léčivech xx xxxxxx xxxxxxxxxxxxx xxxxxxxxxxx xxxxxxxx 2011/62/EU a xx xxxxx xxx xxxxxxx x xxxxxxx x xxxxxxxxx x xxxxxxxxxx xxxxxxx, pokud xx týká xxxxxx xx xxxxxxx nařízení x xxxxxxxxxx xxxxxxx xxxxxxxxx xxxxxx xxxxxx xxxxxxxxx, jejichž xxxxx xxxx vázán xx xxxxxxxx předpis, xxxxx xxxx xxx opatřeny xxxxxxxxxx prvky x xxxxxx přípravky vydávané xx lékařský xxxxxxx xxxx xx lékařský xxxxxxx x xxxxxxxx, xxxxx xxxxx xxx xxxxxxxx ochrannými xxxxx. Xxxxxxxx k předchozím xxxxx xx xxxx xxxxx xxxx.
K bodu 16 (§45 xxxx. 7 písm. x) ):
Přebalování léčivých xxxxxxxxx může xxxxxxx xxxxx xxxxxxx povolení x xxxxxx. Jelikož xxxxxxxx x xxxxxxxxxx xxxxxxx xx xxxxxx xxxxxxxx xx souběžný xxxxx, xx xxxxx xx xxxxxx x xxxxxxxx doplnit specifickou xxxxxxxxx xxxxxxxx povolení xxxxxxxxxx dovozu xxxxxxxx, xxx bylo xxxxxxxxx xxxxxxx xxxxxxxxxx xxxxx x xxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx x xxxxxxxx xxxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx x xxxxxxx xxxxxx xxxxxxxxxxx identifikátoru. Xxxxxxxx dovoz xxxx x členských xxxxxxx Xxxxxxxx xxxx xxxxxxxxxxxx x xxxxxxx xxxxxxxx xxxxxxx xxxxxxx x xx svá xxxxxxx xxxxxxxxx. Xxxxxxxx této xxxxxxxxxx xxxxxxxx povolení xxxxxxxxxx dovozu xxxxxxx, xxx ochrana xxxxxxxx xxxxxxxxxxx xxxxxx xxxxxxxxx xxxxxxxxxxx x rámci xxxxxxxxxx xxxxxx xxxx xx xxxxxx xxxxxx xxxx xxxxxxx pacientů xxxxxxxxx léčivé xxxxxxxxx, xxxxx xxxx zajišťovány xxxxxxxxx rozhodnutí x xxxxxxxxxx. X Xxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxxx x registraci x xxxxxxxx povolení xxxxxxxxxx dovozu nejsou xxxxxxx, xxxxxxx x xxxxxxxxx xxxxxxxxx xxxxxxx Xxxxxxxx unie xxxx xxxx xxxxxxxx xxxxxxxxx xxxxxxxxxx shodně (xxxx. Xxxxxxxxxx).
K bodu 17 (§64 písm. x):
Xxx o xxxxxx xxxxxxxxxxx článku 11 xxxx. 1 xxxxxxxx Xxxxxx (XX) 2017/1572, xxxxx xxxxxxx, xx xxxxxxx xx xxxxxxxxx xxxxxxxx x udržovat xxxxxx xxxxxxxx xxxxxxx, xxxxx xx x pravomoci xxxxx, jež má xxxxxxxxx xxxxxxxxxxx a xx xxxxxxxxx xx xxxxxx. Xxxx xxxxx xx k xxxxxxxxx xxxxx xxxx xxxx xxxxxxxxxx kontroly xxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxxx x vybavených xxxxxxxxx xxx provádění xxxxxxxxxx xxxxxxxxxxx x xxxxxxx xxxxxxxxx surovin, obalových xxxxxxxxx a xxxxxxx xxxxxxxxxxxx x xxxxxxxxx xxxxxxxx přípravků xxxx xx x xxxxxxx xxxxxxxxxxx přístup.
K bodu 18 (§64 xxxx. x)
Xxx o xxxxxx transpozici článku 13 xxxx. 1 xxxxxxxx Xxxxxx (XX) 2017/1572, xxxxx ukládá xxxxxxxx xxxxxx xxxxxxxx, xxx xxxxxxx zavedl systém xxx zaznamenání x xxxxxxxxxx xxxxxxxxx společně x xxxxxxx systémem, xxxxxx xxx okamžitě x kdykoli xxxxxxxx xxxxxx přípravky z xxxxxxxxxxx sítě. Xxxxxxx xxxxxxxxx x xxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxx xx vady. Xxxxxxx xx povinnost xxxxxxxxxx xxxxxxxxx xxxxx x x xxxxxxxxxxx případech x xxxxxxxx xxxxxxxxxx x xxxxxxxxxx x xxxxxxxx xxxx, xxxxx xx xxxxx mít xx následek stažení xxxx xxxxxxxxx xxxxxxx xxxxxxx, a pokud xx xx možné, xxxxx také xxxx xxxxxx.
K bodu 19 (§64 xxxx. x)
Xxx x xxxxxx xxxxxxxxxxx článku 4 odst. 1 xxxxxxxx Komise (XX) 2017/1572, xxxxx xxxxxx xxxxxxxx státům xxxxxxxx, aby xxxxxxx xxxxxxx činnosti xxxx xxxxxxxxx xxxxxxx x xxxxxxx xx xxxxxxxx xxxxxxx xxxxx x x xxxxxxxxx k xxxxxx. Toto xxxxxxxxxx xx xxxxxxx xxxxxx xx léčivé přípravky xxxxxx xxxxx xxx xxxxx. Xxx adresáty xxxxxx xxxxx nedochází x xxxxxxxxx jejich xxxx xxxx xxxxxxxxxx xxxxxx xxxxxxxxxxx stavu.
K bodům 20 a 21 (§77 xxxx. 1 xxxx. b) x x)):
Xxxxx xx x xxxxxxxxxxxx technické xxxxxx xxxxxxxxxxxx xxxxx x xxxxxxxxxx xx xxxxx xxxxxxxxx xxxxxx xxxxxxxxxxxxx xxxx.
Xxxxxxxx používaný xxxxxx xxxxxxxxxx xxxxxxxxxxxxxx léčivých xxxxxxxxx xxxxx xx xxxxxxxx xxxxxx xxx xxxxxxx x xxxxxxxx xxxx 2009 a xx xx základě xxxxxx xxxxxx x xxxxxxxx xxxxxxxxxx xxxxxxxxx, x s tím xxxxxxxxxxx xxxxxx xxxxxx x xxxxxxx xxxxxxxxx xxxxxx. Xxxxxxxx došlo x xxxx zásadní xxxxx, nebylo xx xxxxxx x léčivech xxxxxxxxxx ustanovení §82 xxxx. 2 písm. x) zákona o xxxxxxxx, xxxxx xxxxxxxxxxxx xxxxxxxx xxxxxx xxxxxxxxxx xxxxxxxxxx xxxxx (viz xxxxxxxxxxx bod 29). Xxxxxxxxxx xxxxxxxxxx §82 xxxx. 2 písm. x) a x xxx xxxxxxxxxxx xxxxxxxxxx §77 xxxx. 1 xxxx. x) bod 5 xx xxxx.
K bodu 22 (§77 odst. 1 xxxx. x xxx 11):
Xxxxx xx x xxxxxxxx a xxxxxxxxx xxxxx ve smyslu xxxxxxxxx x praxi xxxxxxxxx xxxxxxxx dodání xxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxx služby, která xxxx v xxxxxxx x §82 xxxx. 2 xxxx. x) xxxxxxxxx x výdeji xxxx skupiny xxxxxxxx xxxxxxxxx.
K bodu 23 (§77 xxxx. 1 písm. x xxx 12):
V souvislosti x xxxxxxxxxx xxxxxxxxxx xxxxxxxxxxxxx z xxxxxxxx x xxxxxxxxxx xxxxxxx, xx. xxxxxxxxx xxxxxxxxxx xxxxx x vyřazování xxxxxxxxxxx xxxxxxxxxxxxxx x xxxxxxx xxxxxxxxxxxxxx xxxxxxxx xxxxxxxxx xx distributora x xxxxxxx xxxxxxxxxx xxxxxxxxxxxxxx léčivých xxxxxxxxx xx xxxxxxxx lékařů, xxxx xxxxxxxxx úprava xxxxxx xxxxxxxxxx, x xx xxx, xxx xx xxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxx xxxxxxx xxxxxxxxxxxxxx xxxxxxxx xxxxxxxxx.
K bodu 24 (§77 xxxx. 1 xxxx. r):
V tomto xxxxxxxxxx jde x xxxxxxxx článku 23 nařízení x xxxxxxxxxx xxxxxxx, xxxx se x xxxxxx reaguje na xxxxxxx xxxxxxxxx xxxxx xxxxxxxxx x xxxxxxx, xxx xx třeba xxxxxxxxx zvláštní xxxxxxxxxxxxxxx xxxxxxxxxxxxxx xxxxxxx xx xxxx území, xxx xxxxxxxxxxx ověřil ochranné xxxxx x xxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx xxxxxxxx xxxxxxxxx před xxx, než xxxxxx xxxxxxxxx xxxx xxxxxxx x xxxx xxxx xxxxxxxxx xxxxxxxxx x xxxxx xxxxxx. X xxxxxx xxxxxx xxxx xx v návrhu xxxxxx xxxxxx xxxxxxx xxxx povinnost distributora xxxx xxx, xxx xxxxxx přípravek vydá xxxxxxxxxxxx xxxxxxx, Xxxxxx Xxxxx xxxxxxxxx k xxxxxxxxxxx ozbrojených xxx xxxxxx, x xxxxxxxxx xxxxxxxxxx xxxxx xxxxxxxx xxxxxxxxx xxx xxxxx xxxxxxx xxxxxxx, xxxxxxxx xxxxxxxxx x xxx xxxxx xxxxxxxxxxx xxxxxxxxxxx xxx Xxxxx xxxxxxxxx xxxxxx xxx xxxxxx xxxxxxxx xx zahraničí xxxxx §111a xxxxxx x léčivech a xxxxxxxxxxxxxx zdravotních xxxxxx, xxxxxx xxxx xxxxxxxx xxxxxxxxxxxx xxxxxx xxxxxxxxx xxx xxxxx povinného xxxxxxxxxxxx xxxxxxxx na xxxxxxx xxxxxxx smlouvy xxxxxxxxxxxx xx zdravotní xxxxxxxxxxx xxxx xxx xxxxx xxxxxxxxx&xxxx; zvláštního x mimořádného očkování x xxxxxxxx xxxxxxxxxxxxx xxxx&xxxx; xx xxxxxxx xxxxxxx smlouvy xxxxxxxxxxxx x Xxxxxxxxxxxxx zdravotnictví x xxxxxxxxxxx xxxxxxxx xxxxxxxxx z xxxxxxxxx xxxxxxxxxxx pojištění x xxxxx xxxxxxxxxxx xxxx xxx xxxxxx č. 48/1997 Sb., x veřejném xxxxxxxxxx xxxxxxxxx x o xxxxx x xxxxxxxx xxxxxxxxx xxxxxxxxxxxxx zákonů, xx znění xxxxxxxxxx xxxxxxxx. Xxxxxxx vymezení xxxxxx xxxxxx xxxxxxxx xx xxxxxxxxxx, xx xxxxxx xxxxxx x XX, kterou xx xxxxx o xxxxxxxx, xxxxxxx jiných možností xxxxxxxxx x xxxxxx 23 xxxxxxxxxx.
K bodu 25 (§80 xxxx. 4)
Předchozí xxxxxx xxxxxx x xxxxxxxx xxxxxxxx xxxxx xxxxxx x xxxxxxx požadavků xx xxxxxxxxxxxx xxxxxxx x xxxxxxx zdravotní xxxx. X tím xxxx spojena řada xxxx v xxxxxxxxxxx xxxxxxxxxxxx xxxxxx x xxxxxxxx, xxxxxx xxxx x §80, kdy xxxxxxxxxxxxx xxxxxxxxxxxxx xxxxxx xxxx xxxxxxxx x xxxx. 4 předmětného xxxxxxxxx. Xxx xxxx xxxxx x xxxxxxx, xxx zákon x xxxxxxx xxxxxxxxxxxxx xxxxxxx xxxxx veterinární xxxxxx xxxxxxxxx. Ve xxxxxxxxxxx xxxxxxxx je xxxx xxxxxxxx x odůvodněných xxxxxxxxx x xx xxxxxxxx stanovených zákonem xxxxxxxxxxxx x xxxxxxxx x xxxxx xxxxx xxxxxxxx přípravků, xxxxxx xxxxxxxxx léčivých xxxxxxxxx, x to x xxxxxxxxx, xxxxx nejsou xxxxxxx xxxxxxxxxxxxxx veterinárními xxxxxxxx xxxxxxxxx. Xx xxxxx xxxxxxx tento xxxxxxxx xxxxxxxx, a xxxxx xx xxxxxxxx xxxxx, které xx x xxxxxxx x xxxxxxxxx xxxxxxxx x §77 xxxx. 1 xxxx. c) bod 5 (xxxxxx distribuce xxxxx) xxxx x §82 (xxxxx xxxxx).
K bodu 26 (§82 xxxx. 2 xxxx. c)
V tomto xxxxxxxxxxxx xxxx se xxxxx x terminologické xxxxxxxxx xxxxxxxxxxx xxxxx, xxx odpovídal současné xxxxx. V polovině xxxx 2009 xx xxxxx xxxxxxxxxx očkovacích xxxxx: xx xxx xxxx xxxxxxx xxxxxxxxxx xxxxxxx, xxx xxxx xxxxxxxxxxx xxxxx, x xx xx xxxxxxx xxxxxx xxxxxx č. 48/1997 Sb., x xxxxxxxx zdravotním xxxxxxxxx x o xxxxx x xxxxxxxx xxxxxxxxx souvisejících zákonů, x x xxx xxxxxxxxxxx změny xxxxxx č. 258/2000 Sb., x xxxxxxx xxxxxxxxx xxxxxx x x xxxxx xxxxxxxxx xxxxxxxxxxxxx xxxxxx. Protože xxxx xxxxx xxxxxx xxxxxxxxxx xx xxxxxx x léčivech, xxxxx x xxxxxx xxxxxx x xxxxxxxx xxxxxxxxxx xxxxxxxxxx §82 xxxx. 2 xxxx. x) x x xxx xxxxxxxxxxx xxxxxxxxxx §77 xxxx. 1 písm. x) bod 5 xxxxxxx.
K bodu 27 (§82 xxxx. 3 xxxx. x)
Xxxxxxxxxxx xxxxxxxxxxx xxxxxxx x) xx §82 xxxx. 3 xxxxxx se x xxxxxxxxxx na xxxxxxxx x xxxxxxxxxx xxxxxxx xxxxxxx xxxxxxxxx xxxxxxxxxxxxx oprávněných k xxxxxx léčivých xxxxxxxxx xxxxxx xxxxxxxx prvky x provést vyřazení xxxxxxxxxxx xxxxxxxxxxxxxx x xxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx. Jedná se x vnitrostátní právní xxxxxx, kdy xxxxx xxxxxxx dodávat léčivé xxxxxxxxx xx xxxxxxx xx xxxxxxxxxxxxxx xxxxxxxx. X xxxxxxxxx xxxxxxx Xxxxxxxx xxxx xx xxx xxxxx xxxxxx xxxxxxxx xx distribuci xxxxxxxx xxxxxxxxx. Z xxxxxx xxxxxx xx xxxx xxxxxx xxxxxxxxx xxxxxxxx xx xxxxxxx xxxxxxx xxxxxx x xxxxxxx, která xx xx rozdíl od xxxxxx poskytovatelů zdravotních xxxxxx xxxxxx xxxxxxxxxx x výdeji x xxx xxxxx ochranné xxxxx xxx výdeji xxxxx xxxxxxxx. X xxxxxxx xxxxxxxxxxx této xxxxxx úpravy by xxxxxxxxx k xxxx, xx xxxxxx xxxxxxxxx xxxxxx na xxxxxxx xx xxxxxxx neověřené, xxxxxxx poskytovatelé xxxxxxxxxxx xxxxxx xxxxxx osobami xxxxxxxxxxx x xxxxxx, x tak se xx ně xxxxxxxx xxx nevztahuje. Xxxxxxxx xxxx xxxxxxxxxx zákona xxxxxx xxxxxxxx xxxxxxxxx xxxxxx xxxxxxx léčivé xxxxxxxxx xxxxxxxx xxxxxxxxxx xxxxx i x xxxxxxxxx, kdy xxxxxxx x xxxxxxxxxxxx léčivé xxxxxxxxx x XX, xxx xxxxxxxx x xxxxx specifického léčebného xxxxxxxx, xxx. „xxxxxxxxxxxxxx xxxxxx“ xxx §8 xxxx. 3 xxxxxx x xxxxxxxx.
K bodu 28 (§99 xxxx. 7 x 8):
X xxxxxxxxxxx xxxxxxxx 7 xx §99 xxxxxx se xxxxxxxx xxxxx Xxxxxx x xxxxxxxx, xx xxxxxx xx xxxxxxxxxxx xxxxxxxxx x ochranných prvcích. Xx xxxxx xxxxxx xxx x xxxxxxxxxxx xxxxxxxxx úložišti Xxxxxxx, xxxxx xxxxxxxxx z xxxx xxxxxxxxxx a xxxx potřebné pro xxxxxxxxx xxxxxx xxxxxxxx. Xxxxxxxxx xxx x xxxxxxxxx týkající se xxxxxxx x xxxxxxxx xxxxxxxx provozovatelů xxxxxxxxxxx x xxxxxx xxxxxxxx xxxxxxxxx, které xxxxxx xxxxxx xxxxxxx xxxxxxxxx xxxxxxx xxxxx. Na xxxxx xxxxxx Xxxxx xxxxxxx informace z xxxxxx xxxxxxxx x xx x xxx xxxxxxx xx xxxxxxx xxxxxxxx x xxxxxxxxxx xxxxxxx x xxxxxxxxxxxx xxxxxxxxxx §13 xxxx. 2 xxxx. o) xxxxxx. Xxxxx xxx x xxxx xxxxxxxxx, x xxxxxxxxxx §99 xxxx. 7 xx xxxxxxxxx náležitá xxxxxxx xxxxxx xxxxxxxxx, xxxx xx výslovně xxxxxxx, xx tyto informace xxxx Xxxxx oprávněn xxxxxxxxxx dalším xxxxxx. Xxxx xxxxx xxxxxxxxxx xxxxxxx na xxxxxxx xxxxxx xxxxxxxx předpisů.
K bodu 29 (§100 xxxx. 8):
Zákon x xxxxxxxx xxxxxxx xxxxxxxxxxx povinnost x xxxxxxx xxxxxxx xxx xxxx Xxxxxxxxx lékovou xxxxxxxxx x Xxxxxxx xxx státní kontrolu xxxxxxxxxxxxx xxxxxxxxxxxx a xxxxx (xxxx jen „Xxxxxxxxxxx xxxxx“). Xxxxxx xxxxxxxxxx úpravy xx xxxxxxxx plný soulad xx xxxxxxxx Evropského xxxxxxxxxx a Xxxx 2001/82/ES ze xxx 6. xxxxxxxxx 2001 x xxxxxx Xxxxxxxxxxxx xxxxxxxxx xx xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx xx xxxxxx xxxxxx xxxxxxxx Xxxxxxxxxxxxx xxxxxx xxxxxxxxx xxxxxxxxxx data do xxxxxxxxxx xxxxxxxx.
K bodu 30 (§100x)
Xxxxxxx x xxxxxxxxxx terminologie x zákoně o xxxxxxxx, xxx xx x důvodu zvýšení xxxxxx xxxxxxx xx xxxxx pojmu „xxxxxxx“ xxxxxxx xxxxx „padělaný xxxxxx xxxxxxxxx“.
K bodu 31 a 32 (§103 xxxx. 6 xxxxxxx x), x) xx x)):
X tomto xxxxxxxxxxxx xxxx se doplňují x §103 xxxx. 6 xxxx. x) xx x) xxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx, xxxxxxx xx xxxxxxx xxxxxxxxxxxx, x to xxxxxxxxx xxxxxx xxxxxxx, xxxxx jsou v xxxxxxx s nařízením x xxxxxxxxxx xxxxxxx xxxx se xxxxxxx x léčivech.
K bodu 33 (§103 xxxx. 15 xx 21):
X xxxxx xxxxxxxxxxxx xxxx xx doplňují xxxxxxxx xxxxxxxx xxxxxxxxx, xxxxxxx xx dopustí xxxxxxx xxxxxxxx xxxxxxxxx, xxxxxxxxxxx, xxxxxxxxxxxx xxxxxxxxxxx xxxxxx xxxxxxxxx x xxxxxx xxxxxxxx xxxxxxxxx, xxxxxxx xxxxxxxxxx x xxxxxxxxxx, xxxxx zřizující x xxxxxxxxxx xxxxxxxx x xxxxx xxxxxxxxx xx xxxxxxx léčivých xxxxxxxxx na xxx. Xxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxx x jednáních, xxxxx jsou v xxxxxxx s xxxxxxxxx x xxxxxxxxxx xxxxxxx xxxx xx xxxxxxx x xxxxxxxx.
Xxx ověření xxxxxxxxxx prvků xxxxxxx, xxxxxxxxxxxx a osoby xxxxxxxxx xxxx zmocněné xxxxxxx léčivé přípravky xxxxxxxxxx xxxxx pravost xxxxxxxxxxx identifikátoru x xxxxxxxxxxxx xxxxxxxxxx x xxxxxxx manipulace s xxxxxx. Při xxxxxxx xxxxxxxx jedinečného xxxxxxxxxxxxxx xx xxxxxxx xxxxxxxxx xxxxxxxxxxxxx s xxxxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxx x xxxxxxx úložišť; xxxxxxxxx xxxxxxxxxxxxx xx xxxxxxxx xx pravý, pokud xxxxxx xxxxxxx xxxxxxxx xxxxxxx xxxxxxxxx xxxxxxxxxxxxx x kódem xxxxxxxxx x xxxxxxxx číslem, xxxxx se shodují x kódem x xxxxxx xxxxxxxxxxx jedinečného xxxxxxxxxxxxxx. Xxxxxxxxxxxx xxxxxxxxxx x xxxxxxx xxxxxxxxxx x xxxxxx se xxxxx xxxxxxxx xxxxxxxxx xxxxxx xxxxxxxx xxxxxxxxx.
Xxxxxxx, xxxxxxxxxxxx a xxxxx xxxxxxxxx nebo zmocněné xxxxxxx xxxxxx xxxxxxxxx xxxxxxxxxx musí xxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx x článcích 18, 24 x 30 xxxxxxxx x ochranných xxxxxxx, xxxxx xxxx xxxxx xx xxxxxxxx, xx x xxxxxx xxxxxxxxx xxxx xxxxxxxxxxxx (vizuálně xx xxxxxx, xx xxx xxxxxxx prostředek x xxxxxxx xxxxxxxxxx x xxxxxx), nebo xxxxx xxxxxxx xxxxxxxxxx xxxxx xxxxxxxx xxxxxxxxx (xxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx x xxxxxxx xxxxxxx) xxxxxxxxx, xx xxxxxxxxx xxxxx xxxx pravý.
K novelizačnímu bodu 34 (§104 odst. 14)
Xxxxxxx xxxxxxxxxx xx xxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxxxxx x tom, xx xxxxxxx xxxxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxx xxxxxxx xxxxx xxxx xxxxx použitelným xxxxxxxxx Xxxxxxxx xxxx - xxxxxxxxxxx xxxxxxxx 2017/1569.
Xxxxxxx xx jako xxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxxxxx xxxxxxx xxxxxxxxxxx x xxx, xx xxxxxxxxxxxx xxxxx xxx inspekci xxxxxxxxx podle xxxxx xxxxxxxxxxxx xxxxxxxx Evropské xxxx - xxxxxxxxxxx xxxxxxxx 2017/1569 xxxxxxxx xxxxx xxxxxxxxx xxxxxxxxx x čl. 20 xxx 2 xxxxxx xxxxxxxxxxx xxxxxxxx.
K bodu 35 (§105 xxxx. 2 xxxx. t):
Jedná xx x legislativně xxxxxxxxxx xxxxxx.
K bodu 36 (§105 xxxx. 4 xxxx. x):
Xxxxx xxxxxxxxxxx xxx xxxxxxx na doplnění xxxx xxxxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxxx xxxxxx xxxxxxxx xxxxxxxxx, xxxx xxxxxxxx xxxx jeho xxxxxxxxxx se označuje xx přestupek (xxx xxxxx o odpovědnosti xx přestupky x xxxxxxx zákon s xxx xxxxxxxxxxx).
K bodu 37 (§105 xxxx.10)
Xxxxxxxx se xxxxxxxx xxxxxxxx přestupku spočívající x tom, xx xxxxxxxxxxxx xxxxxxx při xxxxxxxx xxxxxxxxx podle xxxxx xxxxxxxxxxxx xxxxxxxx Xxxxxxxx xxxx - xxxxxxxxxxx xxxxxxxx 2017/556 xxxxxxxx xxxxx oprávnění xxxxxxxxx x čl. 10 xxxx 2, 3,4 x 5 xxxxxx xxxxxxxxxxx nařízení.
K bodu 38 a 39 (§106 xxxx. 1 písm. x):
X xxxxx xxxxxxxxxxxx xxxx se xxxxxxxx xx xxxxxxxxx xxxxxx xxxxxxx xxxxxxxxxxx xxxxxxx xxxxx xxxx xxxxxxxxxxxxx xxxxx výrobce xxxxxxxx xxxxxxxxx, xxxxx spočívá x tom, xx xxxx osoba nezajistí, xxx xxxx xxxxxxxx xxxxxxxxx xxx opatřen xxxxxxxxxx xxxxx xxxxx §37 xxxx. 7 xxxxxx.
Xxxx xx doplňuje xxxxxxxx xxxxxxxx xxxxxxxxxxx x xxxxxxxxxx článku 12 xxxxxxxx 2017/1569 xxxxxxxxxxx xxxxxxxx xxxxxx xxxx xxxxxxxxxxxxxx osobou. Xxxxxxx xx tomu xxxx x §108 xxxx. 3 pokud xx xxxxxxxx xxxxxxx xxxxxxxxx xxxxxxx xxxxx xxxx xxxxxxxxxxxxx xxxxx.
Xxxxxx jsou xxxxxxxxx xxxxxxxxx xxxxxxx x negativnímu dopadu, xxxxx xx xxxxxx xxxxxxx xxxxx xxxxxxxx x oblasti xxxxxxxxx xxxxxx x x xxxxxxx xxxxxxxxx pacientů xxxxx x Xxxxx xxxxxxxxx, ale i x xxxxxx xxxxxxx Xxxxxxxx xxxx. Xxxxxxx xx respektována xxxx xxxxxx xxxxxxxxxxx za xxxxxxxx obdobných xxxxxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxx xxxxxxx. Ustanovení je xxxxxxxx xxxxxxxx xxx (xxxxxx rozdělené xxxxxxxxx) xxx xxxxxxxxxx x xxxxxxx xxxxxxxxxx xxxxxxx č. 66/2017 Sb.
K bodům 40 xx 46 (§107 xxxx. 1 xxxx. x) xx x):
Xxxxxxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxxxxxxxx xxxxxxx (xxxxxxxxx) xxx xxxxxxxxxx xxxxxxxxxxx maximální výši xxxxx xxxxxx za xxxxxxxx xxxxxxxx xxxxxxxxxx. Xxxxxxxxx xxxx sankcí xxxxxxxx typové xxxxxxxxxx xxxxxxxxx, xx. xx xxxxxxxxx adekvátním xxxxxxxx xxxxxxx xxxxxx normou xxxxxxxx xxxxxxx (xxxxxxxx xxxxxxxxxxx xxxxx).
K bodu 47 (§108 xxxx. 3):
X xxxxx xxxxxxxxxxxx xxxx se xxxxxxxx za xxxxxxxxx xxxxxx xxxxxxx xxxxxxx xxxxx xxxx xxxxxxxxxxxxx xxxxx výrobce xxxxxxxx xxxxxxxxx, xxxxx xxxxxxx x xxx, xx xxxx xxxxx xxxxxxxxx, xxx xxxx xxxxxxxx xxxxxxxxx byl opatřen xxxxxxxxxx xxxxx podle §37 odst. 7 xxxxxx.
K bodu 48 (§108 odst. 3):
Xxxxxxxxxx se xxxxxxxx x odkaz xx čl. 62 xxxxxxxx x xxxxxxxxx xxxxxxxxx xxxxxxxxxxx x povinnosti, aby xxxxx xxxxx xxxxxxxxxxx xxxxxxxx přípravků xxxxxxxxxx x Xxxx nebo xxxxxxxxxx xx Xxxx xxxx v souladu x xxxxxxxxx stanovenými x čl. 63 xxxxxxxx x xxxxxxxxx xxxxxxxxx, xxxxxxx xxxx xxx xxxxxxxxx, xx xxxx xxxx xxxxxxxxx xxxxxxx.
K bodu 49 (§114 odst. 1):
Xxxxx xx o legislativně xxxxxxxxxx xxxxxx v xxxxxxxxxx xx změny x xxxxxxxxxx §82 xxxx. 2.
ČÁST DRUHÁ Změna xxxxxx x xxxxxxxxxxx xxxxxxxx (§65 xxxx. 2)
Xxxxx xxxxxxxxxxxx xxxxx xx xxxxxxxxx xxxxx xxxxxxxx článku 10 xxxx. 8 xxxxxxxx x. 2017/556, který xxxxxxx xxxxxxxx xxxxxx povinnost xxxxxxxx xxxxxx xxxxxx x xxxxxxx rámec, xxx xxxxxxxxxx x xxxxxxxxx členských xxxxx xxxx xx. přístup x xx xxxxxxxxxxxx xxxxxxxxxxx, xxxxx xx xxxxxxxxxx x klinickým xxxxxxxxxx.
K Čl. III - Xxxxxxx xx Sbírce xxxxxx
Xxxxxxxx xx standardní xxxxxxxxxxx, xxx xxxxxxx Ministerstvo xxxxxxxxxxxxx xxxxxx xxxxxxx xx Xxxxxx xxxxxx xxxxxx xxx, xxx xxxx zveřejněno oznámení Xxxxxx v Xxxxxxx xxxxxxxx Xxxxxxxx unie xxxxx čl. 82 xxxx. 3 xxxxxxxx Xxxxxxxxxx xxxxxxxxxx a Rady (XX) x. 536/2014 xx dne 16. xxxxx 2014 x xxxxxxxxxx hodnoceních xxxxxxxxx xxxxxxxx přípravků x x xxxxxxx xxxxxxxx 2001/20/ES.
K čl. IV. - Účinnost
S xxxxxxx na xxxx, xx návrh obsahuje xxx xxxxxxxxxxxx xxxxxxxx x ochranných xxxxxxx, xxxxx xxxxxxx x xxxxxxxx xx 9.2.2019 xx xxx xxxxxxxxxx xxxxxxxx xx xxxx xxxxxxxx xxxxxxxxx datum xxxxxxxxx xxxxx tímto xxxx.
X dalším se xxxxxxxx u konkrétních xxxxxxxxxx xxxxxxx účinnost xxxxxx, xxxx xxxx xxxx x článkem XXX xxxx. x) xxxxxx č. 70/2013 Sb. x xxxxxxxxxx §37 xxxx. 7 x 8, §64a a §66 xxxx. 1 xxxx. x) xxxxxx a xxxxxxxx x ochranných xxxxxxx. Návrh xxxx xxx xxx, xx xx xxxxx nabyl xxxxxxxxx xxxxxxxxx 3 xxx xxx dne xxxxxxxxx xxxx xxxxxxxx Xxxxxxxxx xxxxxx v xxxxxxxxx pravomoci, to xxx 9.2.2019 xxxxx xxxxxx I xxxx 12 xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Xxxx 2011/62/XX xx xxx 8. xxxxxx 2011, xxxxxx se xxxx xxxxxxxx 2001/83/XX x xxxxxx Xxxxxxxxxxxx týkajícím xx xxxxxxxxx xxxxxxxx xxxxxxxxx, xxxxx xxx x zabránění vstupu xxxxxxxxxx xxxxxxxx xxxxxxxxx xx legálního xxxxxxxxxxxxxx xxxxxxx, xxxxxxx xxx xxxx dny, xxx xxxx tyto akty xxxxxxxxx, xxxxxx Xxxxxxxxxxxx xxxxxxxxxxxxx xxxxxx xxxxxxx xx Xxxxxx zákonů.
X Praze xxx 22. srpna 2018
Předseda xxxxx:
Xxx. Xxxxxx Xxxxx x. x.
Xxxxxxx xxxxxxxxxxxxx:
Xxx. xx Xxx. Xxxx Xxxxxxx x. x.
Xxxxxxxxx zpráva x xxxxxxxxx xxxxxx xxxxxxxx xxxxx obecných zásad - XXX&xxxx;
XXXXXXX ZÁVĚREČNÉ XXXXXX RIA
|
1. Xxxxx xxxxxx xxxxxx: |
|
|
Xxxxx xxxxxx, xxxxxx xx xxxx xxxxx č. 378/2007 Sb., o xxxxxxxx x x xxxxxxx xxxxxxxxx xxxxxxxxxxxxx xxxxxx (zákon x xxxxxxxx), ve xxxxx xxxxxxxxxx xxxxxxxx x xxxxx č. 372/2011, o xxxxxxxxxxx službách x xxxxxxxxxx jejich poskytování (xxxxx x xxxxxxxxxxx xxxxxxxx) |
|
|
Xxxxxxxxxxx / xxxxxxxx xxxxxxxxxxxxx: Xxxxxxxxxxxx xxxxxxxxxxxxx |
Xxxxxxxxxxxxx xxxxxx nabytí účinnosti, x xxxxxxx xxxxxx xxxxxxxxx xxxxxxxx 9. xxxxx 2019 |
|
Xxxxxxxxxxxx práva XX: ANO - xxxxxx xxxxxx stanovený xxx xxxxxxxxxxxx: 9. února 2019 - uveďte, xxx xxx xxxxx xxx xxxxx xxxxxxxxx stanovených xxxxxxxxx EU: XX |
|
|
2. Xxx xxxxxx zákona |
|
|
Předkládaná xxxxxx xxxxxx x xxxxxxxx x xxxxxx x xxxxxxxxxxx xxxxxxxx xxxxxxxxxxxx právní xxxxx Xxxxxxxx xxxx do xxxxxxxx řádu České xxxxxxxxx.&xxxx; Jedná xx x následující xxxxxx xxxxxxxx: - Xxxxxxxx Xxxxxx x xxxxxxxxx xxxxxxxxx (XX) 2016/161 ze xxx 2. xxxxx 2015, kterým se xxxxxxxx směrnice Xxxxxxxxxx xxxxxxxxxx a Xxxx 2001/83/XX, stanovením podrobných xxxxxxxx xxx ochranné xxxxx xxxxxxx na xxxxx humánních xxxxxxxx xxxxxxxxx, - Xxxxxxxxx xxxxxxxx Xxxxxx x xxxxxxxxx xxxxxxxxxx (XX) č. 2017/556 xx xxx 24. xxxxxx 2017 x xxxxxxxxxx xxxxxxxxxx pro xxxxxxxxx inspekčních xxxxxxx xxxxxxx klinické praxe xxxxx xxxxxxxx Evropského xxxxxxxxxx x Rady (XX) č. 536/2014 (xxxx xxx „nařízení 2017/556“), - Xxxxxxxx Komise x xxxxxxxxx xxxxxxxxxx (XX) č. 2017/1569 xx xxx 23. května 2017, xxxxxx xx xxxxxxxx nařízení Xxxxxxxxxx xxxxxxxxxx x Rady (XX) x.536/2014 xxxxxxxxxx xxxxx x xxxxxx xxx správnou xxxxxxx xxxxx xxx hodnocené xxxxxxx léčivé xxxxxxxxx x pravidel xxxxxxxxx xxxxxxxx (xxxx xxx xxxxxxxx 2017/1569“), - Xxxxxxxx Xxxxxx (XX) 2017/1572 xx dne 15. xxxx 2017, xxxxxx xx xxxxxxxx směrnice Xxxxxxxxxx xxxxxxxxxx x Xxxx 2001/83/XX, xxxxx xxx x xxxxxx x pokyny xxx xxxxxxxx výrobní xxxxx xxx xxxxxxx xxxxxx xxxxxxxxx (dále xxx „xxxxxxxx 2017/1572“). Xxxxxxx xxxxxxxx, xxx vyhovět xxxxxxxxxx xxxxxxxxxxxx xxx xxxxxxxxxx xxxxxxx státy x xxxxxxxx Evropské xxxx, xx implementace předmětné xxxxx práva EU xx xxxxxxxxxxxxxx právního xxxx. Při xxxxxxxxx xxxxxxxx xx xxxxx x xxxxxxxx smlouvy x xxxxxxxx Xxxxxxxx xxxx xx xxxxxx xxxxxxxxx xxxxx x xxxxx xx xxx xxxxxxxx xxxxxx ze xxxxxx Xxxxxxxx komise xxxxx České xxxxxxxxx xx xxxxxxxxx implementační xxxxxxxxxx a xxxxxxxxx x xxxxxxx sankce xxxxxxxxx xxxxxxxx xxxxxxxx, xxxxx xx mělo xxxxx na xxxx xxxxxx x xxxx xxxxxxxxx nikoli pouze x xxxxxxx Xxxxx xxxxxxxxx, xxx i xxxxxxxxx xxxxxxxxx xxxxx, xxxxx xxx x xxxxxxx, xx xxxxxxxx xxxxx xxxxxxxxxx xxxxx, xxxx xxxxxx funkční. Vzhledem xx xxxxxxxxxxx, xx x xxxxxxxxxxxx xxxxxxxxxxxxxxxx xxxxx Xxxxxxxx xxxx xxxxxxxx se oblasti xxxxxxxxx inspekčních xxxxxxx xxxxxxx klinické praxe, xxxxxxx xxxxxxx xxxxx xxx hodnocené humánní xxxxxx xxxxxxxxx x xxxxxxxx provádění inspekcí x xxxxx x xxxxxx xxx správnou xxxxxxx praxi xxx xxxxxxx léčivé xxxxxxxxx xxxxxx dána možnost xxxxxxxx a současně xxxxx xxxxx novely xx vymezených oblastech xxxxx xxx xxxxx xxxxxxxxx práva Xxxxxxxx xxxx, xxxx v xxxxxxx s Xxxxxxxxxxxxxx xxxxxxxx vlády xxxxxx xxxxxxxxxxxxxx xxxxxx o xxxxxxx xxxxxxx z xxxxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxx x hodnocení xxxxxx xxxxxxxx podle xxxxxxxx zásad - XXX pro xxxx xxxxxxxx xxxxxxx. Xxxxxxx xxxx xxxxxxxx. Z xxxxxx xxxxxx se xxxxx materiál xxxx xxxxxx pouze hodnocením xxxxxx adaptace nařízení x xxxxxxxxxx xxxxxxx. Xxxxx xxxxxx xxxxxx je xxxxxxx nezbytných opatření xxxxxxxxxxxxx s adaptací xxxxxxxx řádu Xxxxx xxxxxxxxx na xxxxxxxx Xxxxxx x xxxxxxxxx xxxxxxxxx (EU) 2016/161 xx xxx 2. xxxxx 2015, xxxxxx xx doplňuje xxxxxxxx Xxxxxxxxxx parlamentu a Xxxx 2001/83/XX stanovením xxxxxxxxxx xxxxxxxx xxx xxxxxxxx prvky xxxxxxx xx xxxxx xxxxxxxxx xxxxxxxx přípravků (xxxx xxx „xxxxxxxx o xxxxxxxxxx xxxxxxx“). Xxxxxxxxxxxx xxxxxxxxxx xxxxx xx xxxxxxx humánních léčivých xxxxxxxxx xxxxxxx již xx Xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Rady 2011/62/EU, xxxxxx se xxxx xxxxxxxx 2001/83/XX x xxxxxx Xxxxxxxxxxxx xxxxxxxxx xx xxxxxxxxx xxxxxxxx xxxxxxxxx, pokud xxx o xxxxxxxxx xxxxxx xxxxxxxxxx léčivých xxxxxxxxx xx xxxxxxxxx xxxxxxxxxxxxxx xxxxxxx (xxxx xxx „xxxxxxxx 2011/62/XX“). Xxxxxxxx xxxxxx xxxxxxxxx, xxxxx xx xx x xxxxxxxxx xxxxxxx xxxxxxxxxxxxxxx xxxxxxxxx xxxxxxxxxxxxxx řetězce, xxxxxxxxxxx xxxxxx pro xxxxxx zdraví x xxxxx xxxxxx vést xx xxxxxxx xxxxxx xxxxxxxx x xxxxxxx xxxxxxxxxxxx xxxxxxx, xxxxxxxxxxxxx xxxxxxxxx péče x xxxxxxxxx xxxxxx. Proto xxxxxxxx 2011/62/EU xxxxxxxxx xxxxxx ochranných xxxxx xx xxxxxxx xxxxxxxx xxxxxxxxx, který by xxxxxxx xxxxxx xxxxxxx xxxxxxxx léčivého xxxxxxxxx, xxxxxxxxxxxx xxxxxxxxxxxx balení xxxxxxxx xxxxxxxxx x xxxxxxx, xxx nebylo x xxxxxx manipulováno. Xxxx xxxxxx bezpečnostní xxxxxxxx xx xxxx xxxxxxxx xxxxxxxxxxx ochranu xxxxx xxxxxx padělaných xxxxxxxx xxxxxxxxx xx xxxxxxxxx dodavatelského řetězce x cílem xxxxxxx xxxxxxxx x xxxxx xxxxxxxx xxxxxxxxxx o xxxxxxxxxx a xxxxxxx. Xxx xxxxxx ověřování xxxxx xxx xxxxxxxxxx ve xxxxx xxxxxxxxx xxxxxxx Xxxxxxxx xxxx, xxxxxxxxxx xxxx léčivých xxxxxxxxx x xxxxxxxxxx xxxxx xxxxxxx xxxxx xxxxxxxxx xxxxxxxxxxxxxx xxxxxxx způsobené xxxxxxxxxxxx xxxxxxxxx xxxxxxxxxx, xxxxxxxxx Xxxxxxxx Komise xxxxxxxxxxxxxxx nařízení o xxxxxxxxxx xxxxxxx xxxxxxxx xxxxxxxx xxx xxxxxxxx xxxxxxxxxx xxxxx, xxxxxxx xxxxxxxxxxxxxxx x technické xxxxxxxxxxx xxxxxxx z xxxxxxxxxx xxxxx - xxxxxxxxxxx identifikátoru, způsoby x xxxxxx xxxxxxx xxxxxxxxxx xxxxx xxxxxxxxxxxx xxxxxxxxx xxxxxxxx (xxxxxxx, xxxxxxxxxxxx, xxxxxxx xxxxxxxxxxx xxxx zmocněnými vydávat xxxxxx přípravky xxxxxxxxxx) x xxxxxxx x xxxxxx systému xxxxxxx xxxxxxxxxx xxxxxxxxx x xxxxxxxxxx xxxxxxx (xxxxxxxxxxx xxxxxxxxxxxxxxxx). Xxxxxxxx prvky xxxxx xxx xxxxx xxxxxxxx xx obalu humánního xxxxxxxx xxxxxxxxx - xxxxxxxxx xxxxxxxxxxxxx (xxxxxxxxx xxxxxxxx xxxxxx xxxxxxxxxxxxx xxxxxxx kódem, xxxxxxxxxx xxxxxxx xxxxxxxx x xxxxxxxxxxxx jednotlivého xxxxxx xxxxxxxx xxxxxxxxx, xx xxxx xx xxxxxxxxx) x xxxxxxxxxx x xxxxxxx xxxxxxxxxx x xxxxxx (xxxxxxxx xxxxx - xxxxxxxxxxxx pojistka - xxxxxxxxxx ověřit, xxx bylo s xxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxxxx). Xxxxxxxxxx xxxxx xxxxx xxxxxxxx v xxxxxxx x nařízením x xxxxxxxxxx xxxxxxx xxxxx xxxxxxxxx léčivých přípravků a) xxxxxxx xxxxx xx xxxxx xx xxxxxxxx xxxxxxx (výjimkou jsou xxxxxx přípravky uvedené xx xxxxxxx x xxxxxxx I xxxxxxxx x ochranných xxxxxxx) x) xxxxxxx xxxxx není xxxxx xx lékařský xxxxxxx (xxx. „volně xxxxxxxx léčivé xxxxxxxxx“), x xx xxxxx xxxxx xxxx uvedeny xx seznamu v xxxxxxx XX xxxxxxxx x ochranných prvcích, c) xx které členské xxxxx xxxxxxxxx xxxxxx xxxxxxxxxx jedinečného identifikátoru xxxx xxxxxxxxxx k xxxxxxx xxxxxxxxxx s xxxxxx. Xxxxxxx ověřovací xxxxxx xxxxxxxx zřízení systému xxxxxxx, ve xxxxxxx xxxxx xxxx xxxx xxxxxxxx xxxxxxxxx o xxxxxxxxxxx xxxxxxxxxxxxxxxx xxxxxxxxxxxx xxxxxx xxxxxxxx xxxxxxxxx. Xxxxxx úložišť zřídí x xxxxxxxx neziskový xxxxxx xxxxxxx xxxx xxxxxxxxx xxxxxx subjekty xxxxxxx x Unii xxxxxxx x xxxxxxxx xxxxxxxxxx o xxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxx. Xxxxxxx xxxxxxx xxxxxxx xx xxxxxx xxxxxxx xxxxxxxx xxxxxx xxxxxxxx xxxxxxxxxxx xxxxxxx s xxxxxxxxxxxx, xxxxxxx xxxxxxxxxxx nebo xxxxxxxxxx vydávat xxxxxx xxxxxxxxx xxxxxxxxxx x x xxxxxxxxx příslušnými xxxxxxxxxxxxxx orgány. Xxxxxxx xx systém xxxxxxx xxxxx výrobci xxxxxxxx xxxxxxxxx xxxxxxxxxx ochrannými xxxxx v souladu x xxxxxxx 54a xxxx. 2 xxxx. x) xxxxxxxx 2001/83/ES. Xxxxxx xxxxxxx xx xxxxxx x xxxxxxxxxxx xxxxxxxx a xxxxxxxx, xxxxx slouží xxxxx xxxxxxx xxxxxxxxx státu („xxxxxxxxxxxx xxxxxxxx“), xxxx xxxxxx více xxxxxxxxx xxxxx („nadnárodní xxxxxxxx“), xxxxx xxxx xxx xxxxxxxxx k centrálnímu xxxxxxxx. Xxxxxxx xxxx xxxxxxxxx xxxxxxx xxxxxx xxxxxxxxxxx xxxxxxxx přípravků xxxxxxxxxx xxxxx x xxxxxx, xx xxxxxxxxx identifikátor xx xxxxxxx a xxxxxxxx informace dané xxxxxxxxx o ochranných xxxxxxx. Držitelé xxxxxxxxxx x registraci xxxx xxxxxxxxx xxxxx x xxxxxxx xxxxxxxx xxxxxxxxxx xxxx xxxxxxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxx xxxxxxxx, xxx xxxxxxxxx x xxxxxxxxxxx xxxxxxxxxxxxxxxx xxxx xx xxxxxxx xxxxxxx xxxxxxx před xxx, xxx xxxx léčivý xxxxxxxxx uveden xx xxx. Xxxxxxx xxxxxxxxxx xxxxx x xxxxxxx xxxxxxx xxxxx xxxxxxxx xxxxx xxxxxxx xxxx xxxxxxxxxxxx x xxxxx xxxxxxxxx xxxx zmocněné xxxxxxx xxxxxx přípravky. Xxxxxxx, jakým dotčené xxxxxxxx xxxxxxxxx xxxxxxx xxxxxxxxxx prvků, xxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx, xx xxxxxxx uložišť xxxx xxxx xxxxxxxxx x xxxxxxxxxx prvcích. Xxxxx oprávněná x xxxxxx xxxxxxxx xxxxxxxxx xxx před xxxxxxx xxxxxxxxxx xxxxx xxx xxxxxxxx xxxxx x xxxxxxx vyřazení xxxxxxxxxxx xxxxxxxxxxxxxx xx xxxxxxx xxxxxxx x okamžiku xxxxxx xxxxxxxxxx. Xxx xxxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx x xxxxxxxx xxxxxxxxxx xxxxxxx xx xxxxxxxx xxxxxx xxx xxxxxxxx xxxxx. Ověření pravosti xxxxxxxxxxx identifikátoru xx xxxxx léčivého xxxxxxxxx xx xxxxxxx xxxx xxxxxxxxxx s xxxxxxxxxxxxxx xxxxxxxxx x xxxxxxx xxxxxxx x xxxx xxxxx je xxxxxxxx, xx léčivý xxxxxxxxx xxxxxxx xx xxxxxxxxxxx xxxxxxx, xxxxx xxxxxxxxx xxxxxxxxxxxxxx vložil xx xxxxxxx xxxxxxx. Ověření xxxxxxxxxxxxx xxxxxxxxxx x xxxxxxx xxxxxxxxxx s xxxxxx bude provedeno xxxxxxxx xxxxxxxxx balení xxxxxxxx přípravku a xxxx cílem xx xxxxxxxx, xx s xxxxxxx xxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxxxxx xxxxx xxxx před xxxxxxxxx, xxxxxxx bylo balení xxxxxxxx xxxxxxxxx xxxxxx. Xxxxxxxx x xxxxxxxxxx xxxxxxx xx pro xxxxxxx xxxxx závazné x xxxxx rozsahu x xx xx xxxxx xxxxxxxxx státech xxxxx xxxxxxxxxx. Ačkoliv nařízení x xxxxxxxxxx xxxxxxx xxxxxxxx xxxxxxxxxxxx xxxxxxxxxx xxxxx xxxxxx komplexně, xxxxxxx xxxxx xxxxxx xxxxxxxxx na zvážení x xxxxxxxxxx xxxxxxxxx xxxxx, a xx xxxxxxxxx (1) xxxxxx xxxxxxxxxxx vnitrostátního xxxxxx, xxxxx xx xxx xxx přístup x xxxxxxxx pro xxxxx xxxxxx nad fungováním xxxxxxx, vyšetřování potenciálních xxxxxxx xxxxxxxx, úhrady, xxxxxxxxxxxxxxxx a xxxxxxxxxxxxxxxxxxxx, (2) xxxxxxxx xxxxxxx, xxx xxxxxxxx, aby xxxxxxxxxx, které nařízení x xxxxxxxxxx xxxxxxx xxxxxx xxxxxxxxxxx subjektům, xxxx xxxxxx, a xx xxxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx x xxxx oblasti a xxxxxxxx xxxxxxx správního xxxxxx xxxxxxxxxxx x xxxxxx projednávání a xxxxxxxxxx xxxx xxxxxx xx xxxxxxxx xxxxxxxxxx xxxxxxxxxxxx xxxxxxxx, (3) xxxxxxxxxx xxx, xxxxxxx xxxx xxxxxxx xxxxxx xxxxxxxxxx ochranných xxxxx xx xxxxxx xxxxxxxxx, xxxxx dle xxxxxxxx x xxxxxxxxxx xxxxxxx xxxxxx xxxxxxxxx xxx xxxxxxxx těmito xxxxx, (4) xxxxxxxxxx, xxx xxxxxxxxxxxx xxxxxxxx xxxxx“ xxxx „xxxx úhradové xxxxx“ xxxx xxxxxxx x xxxxx xxxxxxxxxxx xxxxxxxxxxxxxx xx nikoliv, (5) zohlednění xxxxxxxx xxxxxxxxxxxxxxx dodavatelského xxxxxxx xx xxxxx xxxxxxxxx xxxxx x xxxxxxxx x xxxxxx xxxxxx, xxx xxxxxxxxxxx mohl xxxxxx xxxxxxxx prvky x xxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx xxxxxxxx xxxxxxxxx xx systému xxxxxxx xxxx tím, xxx léčivý přípravek xxxx xxxxxxx z xxxx nebo xxxxxxxxx xxxxxxxxx x článku 23 xxxxxxxx x xxxxxxxxxx xxxxxxx. Xxxx xxxxxxx xxxxxx xx možné xxxxxxx xxxxx v podobě xxxxxx zákona x xxxxxxxx xxx, xxx xxxxxxxxxxxxxx s xxx xxxxxxxxxx základní xxxxxxx xxxxxxxxxxxx xxxxxxxxxx xxxxx xxxxxxxxxxx xxxxxxxx 2011/62/EU, xxxxx byla xxxxxxxxxxxxx xx zákona o xxxxxxxx novelou č. 70/2013 Sb. Xxxxxxxxxxx úpravou xxxx xxxxxxx xxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxx o xxxxxxxxxx xxxxxxx tak, xxx mohla xxx xxxx ustanovení xxxxx x xxxx xxxxxx xxxxxxxxxx x xxxxxxxxxx Xxxxx republiky. |
|
|
3. Agregované xxxxxx xxxxxx xxxxxx&xxxx;&xxxx; |
|
|
3.1 Xxxxxx xx xxxxxx rozpočet x xxxxxxx xxxxxxx xxxxxxxx: XX |
|
|
Xxxxxxxxxx úpravy za xxxxxx zajištění adaptace xxxxxxxx x ochranných xxxxxxx xxxxxxx xxxxxxxxxxxx xxxxxxxx xxxxx xxxxxxxxxxx x xxxxxxxx xxxxxx xxxxxxxxxxxxxxx míst xxxxxx xxxxxxxxxx na xxxxx xxx xxxxxxxxx xxxxx xxxx xxxxxxxxxxx xxxxxxxxxx x pracovních xxxx xx xxxxxxxxxx úřadech xxxxxxxxxxx pod xxxxxxxxxxx xxxxxxxx Xxxxxxxxxxxx xxxxxxxxxxxxx, xxxxxxxxx na straně Xxxxxx. Xxxxxx xx xxxxxxx xxxxxxx rozpočty xx xxxxxxxxxxxxxxx. |
|
|
3.2 Dopady xx xxxxxxxxxxx xxxxxxxxxxxxxxxxxxx XX: XX |
|
|
Xxxxxxxxxxxxxxx xx dopady xx xxxxxxxxxxx xxxxxxxxxxxxxxxxxxx XX. |
|
|
3.3 Xxxxxx na xxxxxxxxxxxxx xxxxxxxxx: XXX |
|
|
Xxxxxx xx xxxxxxxxxxxxx prostředí Xxxxx xxxxxxxxx xx xxxx x těm xxxxxxxxxxx xxxxxx x xxxxxxxx, xxxxx xx xxxx xxxx vložena xxxx xxxxxxx, xx. xxxxxxx č. 70/2013 Sb., x xxxx xxxxxxxxx účinnost, xxxxxxxx se váží xxxxx x xxxxxxxx x xxxxxxxxxx prvcích. Xxxx xxxxxx již xxxx xxxxxxxxx xxx xxxxxxxxxxxx xxxxxx právních xxxxxxxx. V xxxxx xxxxx xx třeba xxxxxxx xx xxxxxxxxx xxxxxx, xxxxxx zprávy x hodnocení xxxxxx xxxxxxxx (XXX) k xxxxxx č. 70/2013 Sb. x xxxx na podrobnou xxxxxx XXX x xxxxxxxx x ochranných xxxxxxx xxxxxxxxx „Xxxxxx Xxxxxxxxxx“. V této xxxxxxxx xxxxxx xx xxxxx, xx x xxxxxxx x čl. 4 xxxxxxxx 2011/62/XX a xx. 54x xxxx. 2 x 3 xxxxxxxx 2001/83/ES Xxxxxx xxxxxxxxx přínosy, náklady x xxxxxxxxxx xxxxxxxxxx xxxxxxx xxxxxxxx xxx xxxxxxxxxxxxxxx x xxxxxxxxx xxxxxxxxxxx jedinečného xxxxxxxxxxxxxx x xxxxxxx xxxxxxx xxxxxxxxxx xxxxx a xxxxxxxx x xxxxxx xxxxxxx xxxxxxx. Xxxxxxxx, xxxxx xxxx vyhodnoceny xxxx nákladově xxxxxxxxxxxxxxx, xxxxxxxxxxx xxxxxxxx xxxxx xxxxxxxx x xxxxxxxxxx xxxxxxx. X tuto chvíli xx zřejmé, že xxxxxxx realizace xxxxx xxxxxxx zejména xx xxxxxxx a xxxxxxxx xxxxxxxxxx x registraci xxxxxxxx přípravků xxxxxxxxxx xxxxxxxxxx xxxxx. Xxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxx xxxxxxx xxxxxxx xx xxxxxxx x xxxxxx xxxxxxx xxxxxxx (xxxx povinnost xxxx xxxxxxx xxx xxxxxxxx 2011/62/EU, xxxxx xxxx transponovaná xx xxxxxxxx řádu XX xxxxxxx č. 70/2013 Sb.). Xxx xxxxxxx x souběžné xxxxxxx představuje xxxxxxxx xxxxxxxxxxx identifikátoru na xxxxxxx humánních xxxxxxxx xxxxxxxxx xxxxx xxxxxxx, xxxxx xxxxxxx s xxxxxxxx xxxxxxxxxxx výrobní xxxxx xxxx xxxxxxx xxxxx (xxxxxxxx xxxxxxx) x investovat xx xxxxxxxxxxxx xxxxxxx, xxx xxxx xxxxx xxxxxxxx xxxxxxxxx o jedinečných xxxxxxxxxxxxxxxx xx systému xxxxxxxx. X xxxxxxxx xxxx xxxxxx xxxxx xxxxxxx xx xxxxxx xxxxxxxx xxxxxxxxx xxxxx xxxxx. Aby bylo xxxxx xxxxxxxxxx jedinečný xxxxxxxxxxxxx, xxxx xxx xxxxxx linky xxxxxxxxx xxxxx tiskovým x xxxxxxxxxx softwarem. Náklady výrobců xxxxx částečně kompenzovány xxxxxxxxxxxxx xxxxxxxx x xxxxxxx x hlediska: - xxxxxxxxx xxxxxxx (xxxxxxxxxx xxxxxxx vnitrostátních mechanismů xxxxxxxxx xxxxxxxx xxxxx xxxxxxxxxxxxxx xxxxxxxx XX xx xxxxxxx xxxxxxx xxx xxxx xxxxxxxxx xxxxx, xxx vyhověly xxxxxxxxxxxx xxxxxxxxxxxx xxxxxxxxx xxxxxxx), - xxxxxxx zájmů xxxxxxx x xxxxxxxx xxxxxxxxxx x xxxxxxxxxx (xxxxxxx xxxxx padělaných xxxxxxxx přípravku xx xxxx povede k xxxxxxx xxxxxxxxx prodejů), - xxxxxxxxx x xxxxxxx xxxxxxx při postupech xxxxxxxxx a xxxxxxx xxxxxxxx přípravků, což xxxxxx xxxxxx prvky (xxxxx x xxxx xxxxxxxxxxxxx) xxxxxxx v xxxxxxxxxx identifikátoru. Náklady xxxxxxxxxxxx xxxxx x xxxx xxxxxxxxxxx xxxx zmocněných x xxxxxx xxxxxxxx xxxxxxxxx xxxxxxx s xxxxxxxxxx xxxxxxxx ochranné xxxxx a xxxxxxxxx xxxxxxxxx xxxxxxxxxxxxx ze xxxxxxx xxxxxxx (xxxxxxxx xxxxxxxxxx xxxxxxx 2D xxxx, úpravy softwarových xxxxxxxx, xxxxxxx xx xxxxxx xxxxxx). Xxxxx xxxxxx xx xxxxxxxxxxxxx subjekty xxxxxxx xx x xxxxxxxxxxx xxxx registrací x xxxxxxxx přípravků xxxxxxxxxx ochrannými xxxxx.&xxxx; Xxxxxxxx xxxxx xxxxxxxxxx xxxxxx xx xxxxxxxxxxxxx xxxxxxxx x xxxxxxxx xxxxxxxxxxxx xxxxxxxxxx xxxxx xx registrační xxxxxxxxxxx xx xxxxxxx xxxxxxxxx, xxxxx xxxxx vztahující xx x xxxxxxxxxxx xxxxxxxxxxxxxx xxx zavést xx xxxxx xxxxx x xxxxx xxxxxxxxxx xxxxxx x xxxxxxx xx xxxxxxxxx o xxxxxxxxx - xxxx. xxxxxx x prodloužení xxxxxxxxx xxxxxxxxxx, řízení x xxxxx xxxxxxxxxx xxxx II, typu XX xxxx xxxx XX. Pro xxxxxxx xxxxxxxx xxxxxxxxx xxxxxx xxxxx xx zavedení xxxxxxxxxx xxxxx xxxxx xxxxxxxxxx zvláštní xxxxxx x xxxxx registrace, xxxxx xx možné xxxxxxxxxxxxx xxxxxxxx xxxxx xx registrační dokumentace xxx xxxx xxxxxxxxxxx xxxx xxxxxxxxxx xxxxxxxxx xxxxxxx o změnu xxxxxxxxxx. Xxxxx xxx xx xxxxxxxxxxxxx xxxxxxxx x xxxxxxx xxxxxxxx x v xxxxxxx xxxxxxxxxxxx lhůt xx xxxxxxxx předložených xxxxxxx xxxxxxxx xx xxxx xxxxxxxxxx xxxx xxxxxxxxx. Xxxxxxx xx xxxxx a xxxxxx xxxxxxx, který xxxxxx celoevropské xxxxxxx xxxxx, xxxxx držitelé xxxxxxxx x xxxxxx (xx. xxxxxxx x xxxxxxxx xxxxxxxxxxxx) léčivých xxxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxx. Xx xxxxx xxxxxx xxxxxxxxxxxxxx xxxxxxxxxxxxxx xxxxxxxx xxxxxxxx XXXXX (xxxxxxxx xxxxxxxxxxxx), XXXXX x MFE (xxxxxxx) - xxxxxxxx představující „xxxxxx“ xxxxxxx, PGEU (xxxxxxxxxxxx xxxxxxxxx) x XXXX (xxxxxxxxxxxxxxx) při xxxxxx Evropského xxxxxx xxxxxxxxx xxxx (Xxxxxxxx Xxxxxxxxxxx Xxxxx xx XXX). Xxxx evropské xxxxxxxx xxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxx, Xxxxxxxxx xxxxxxxxxx xxx ověřování xxxxx (Xxxxxxxx Xxxxxxxxx Verification Xxxxxxxxxxxx či XXXX), xxxxx xx xxxxxxxx xxxxxxxx ESM založením xxxxxxxxxx centrálního „xxxx“ (Xxxxxxxx Xxxxxxxxx Xxxxxxxxxxxx Xxxxxx či XXXX), x xxxxxxxx xxxxxxxxxx xxxxxxx xxxxxxxxxxxxxxx xxxxxxxx xxxxxxxxx při zřizování xxxxxxxxxxx xxxxxxxxx xxxxxxxxxx. X Xxxxx republice vytvořila xxxxxx zastupující xxxxxxxx xxxxxxxxxxxxxxxx xxxxx, xxxxxxxxx XXXX (Xxxxxxxx xxxxxxxxxx xxxxxxxxxxxx léčiv), XXXX (Xxxxxxxx xxxxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxxx), XXXX (Asociace xxxxxxxxxxxxxxxxx xxxxx), ČAFF (Xxxxx xxxxxxxx xxxxxxxxxxxxxxx xxxxx) x ČLnK (Xxxxx xxxxxxxxxx komora) xxxxxxxxxxx xxxxxxx, xxx xx xxxxx xx xxx xxxx x xxxxx postup xxxxxxxxxxxx XXX v České xxxxxxxxx, xxxxxxxxxx xxxxxxxx xxxxx. Konečným xxxxx xx xxxxx Národní xxxxxx xxx xxxxxxxxx xxxxx (NSOL), xxxxxxxxxxxx xxxx XXX x xxxxxxxx xxxxxxxxxx systému XXXX. Opět x xxxxxxx s xxxxxxxxx xxxxxxx bude XXXX xxxxxx x xxxxxxxxx xxxxxxxxxx xxxxxxx xxxxxxxxx Xxxxxxx xxxxxxxxxx xxx xxxxxxxxx pravosti xxxxx (XXXX) xxx xxxxxxxx xxxxxxxxx xxxxxx xxxxxxxx. Xxx xxxxxxxx xxxxxx xxxxxxx xxxxxxxxxx xxxxxx xx xxxxxx xxxx xxxxxxxx xxxxxxxxx vydávaných xx xxxxxxx xxxxxxxxx 261 xxxxxxxxxxxxxxx společností sestávajících xx 465 xxxxxxxx xxxxxxxxxx x registraci, 525 xxxxxxxxxxxx, x xxxxx většinu xxxxxxxxxxx xxxxxxx x licencí xxxxxxxxxxxx, 15 souběžných xxxxxxx, xxxxxxxxx 200 xxxxxxxx x xxxxxxx xxxxxxxxx ústavů x xxxxxxx lékárnou x xxx 2 800 xxxxxxx. Dle těchto xxxxxx xx xx xxxxxx xxxx xxxxxxx xxxxxxxxxx přibližně 180 xxxxxxx xxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxx na xxxxxxx xxxxx. Xxxxxxxxx xxxxxxxx XXXX xxx xxxxxxxx xxxxxxxxxx x registraci xx xxxxxxxxxx x xxxxxxxx xxxxxxxxx systému xxxxxxxxx léčiv (XXXX) xxxx xxxxxxxx x xxxxxxxxxx XXXX, xxxxxxx xx xxxxxxx x xxxxxx xxxxxxxxxxxxx xxxxxxxxxxxxx xxxxxxxx a xxxxx xxxxxxxx xxxxxxxx tzv. xxxx fee. Xxxx xxxxxxxx xx xxx 2019 xx xxxx xxx známa v X1/2018. Xx počátku xxxx 2018 xxxx provedeno xxxxxxxxx x xxxxxxxxxxx xxxxxxx NSOL x xxxxx xxxxxxxxx xxxxxxxx. Xxx 9.1.2018 proběhlo x xxxxxxxxxx Xxxxxxx xxxxxxxxxx pro xxxxxxxxx xxxxxxxx xxxxx setkání xxxxxxx x xxxxx x pilotní xxxx xxxxxxxx ověřování pravosti xxxxx x Xxxxx xxxxxxxxx, xxxxx xxxxx xxxx poskytnout xxxxxx xxxxxxxxx týkající se xxxxxxxxxxxxxx xxxxxx x xxxxxxx komunikaci x xxxxxxxxxx xx xxxxxxxx xxxxxxxx xxxx specifické xxxxxxxx. Xx pilotního xxxxxxxx xxxx připraveno xx zapojit 8 xxxxxxxx xx strany xxxxxxx, 6 zástupců xx xxxxxx xxxxxxxxxxxx, 23 lékáren (x xxxx 18 xxxxxxxxxxxx) x 4 dodavatelé XX systémů. Xxxxxxx xxxx xxxx xxxxxxxx xxx 3. xxxxxx 2018, xxxxxxx xxxxxxxxxxxxx xxxx xxxxxx je xx spuštění xxxxxxxxxx xxxxxxxxxxx xxxxxxxxxxxx xx xxxxxx 2018. X výše xxxxxxxxx xx xxxxxx, xx dotčené xxxxxxxx xx aktivně xxxxxxxx xx přípravy xxxxxxx xxxxxx xxxxxxx xxxxxxxxx xxxxxxxx léčiv v Xxxxx republice. Xx xxxxxxxxx xxxxxxxx se xxxxxxxx xxxxxxxx x xxxxxxxxx xxxxxxx xx xxxx, x čehož xxx xxxxxxx xxxxxxxxx, xx xxxx xxxxxxxx xxx xxxxxxxxxx xxxxxxx xxx, aby se xxxxx pilotního projektu xxxxxxxx. |
|
|
3.4 Xxxxxx xx xxxxxx xxxxxxxxxxx celky (xxxx, xxxxx): XX |
|
|
Xxxxxxxxxxxxxxx xx dopady xx xxxxxx xxxxxxxxxxx xxxxx. |
|
|
3.5 Xxxxxxxx dopady: XX |
|
|
Xxxxxxxxxxxxxxx xx xxxxxx do xxxxxxxx xxxxx. |
|
|
3.6 Xxxxxx xx spotřebitele: XXX |
|
|
Xxxxxxxx xxxx, xxxxx zajistí xxxxxxx léčivého xxxxxxxxx x xxxxxxxx xxxxxxxxxx xxxxxxx, bude xxx xxxxxxxxx xxxxxxxxx xxxxx xx xxxxxxxxxxxxxx xxxxxx. Xxxxxxxx k tomu, xx xxxxxxx xxxxxxx x držitelů rozhodnutí x registraci xxxxxxxx xxxxxxxxx, jejichž obaly xxxxxxx xxxxxxxx xxxxx, xx x důvodu xxxxxxxx ochranných prvků xx xxxxxx míry xxxxxxxxx xxxxx, xxxx xxxxxxxx xxxxxxxx dopad xxxx xxxxxxxxxxx xx xxxx xxxxxxxx přípravků. Xxxxxxx xxxxxxx výrobců x držitelů xxxxxxxxxx x xxxxxxxxxx léčivých xxxxxxxxx xxxx xxxx xx vztahu x xxxxxxxxx xxxxxxx xxxxxxxxxxxxxxx xxxxx xxxxxxxxxxxx, xxxxx xxxxxxx xx zavedení XX xxxx x xxxxxxxx xxxxxxxxx vázaných xx xxxxxx xxxx xxxxx jistě xxxxxx xxxxx xxx xxxxxxxx xxxxxxx xx xxxxx, xxxxxx x xxxxxxxxxx xxxxxxxx přípravků. Xxxx xxxxxxxx xxxxxxxxx, xxxxxxx xxxxx xx xxxxx xx lékařský předpis, xx xx xxxxxxx xxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxx xxxx xxxxxxxx xxxxxxxxxxx, kterou xxx xxxxxx xxxxx xx xxxxxxx xxxxxx xxxxxxxxxxx žádosti. Xxxxxxxx xxxx a podmínky xxxxxx xxxxxxxx xxxxxxxxx x xxxxxxxxxx veřejného xxxxxxxxxxx xxxxxxxxx xxxx xxxxxxxxxxx x xxxxx xxxxxxxxx xxxxxx. Navíc xx x xxxxxx Xxxxxxxx xxxx (xxxxxx XX) často využívá xxxxxxx tzv. vnějšího xxxxxxxx referencování - xxxx stanovují ceny x xxxxxx xxxxx xxxxxxxxxx xxx stejného xx xxxxxxxxxxxxxx xxxxxxxx xxxxxxxxx zjištěného v xxxxxxxxx, xxxxx xx x xxxxxx xxxxxxx xxxxxxx xxxxxx xxxxxxxxxx xxxxxxxx ceny x XX vliv xx xxxxxx xxxxxxxx přípravku x xxxxxxxxxx veřejného xxxxxxxxxxx xxxxxxxxx. Xxxxxxxx x xxxxx xxxxxxxxx xxxxx xxxxxxxxxxxxx xxxxxxxxx xx evropském xxxx x léčivy se xxxxxxxxx cen xxxxxxxx xxxxxxxxx z důvodu xxxxxxxx xxxxxxxxxx prvků xxxxxxxxxxxxx, nebo xxxxxx xxxxxxxxxxx xx běžné xxxxxxx. Xxxx xxxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxx xxxxxxxxx, xx nákladů xxxxxxxxx zdravotního pojištění xx promítá xxxxxx xxxxxxxx xxxxxxxxx, xxxxxxx xxxx xxxx. |
|
|
3.7 Xxxxxx xx životní xxxxxxxxx: XX |
|
|
Xxxxxxxxxxxxxxx xx dopady xx xxxxxxx xxxxxxxxx. |
|
|
3.8 Xxxxxx xx xxxxxx x zákazu diskriminace x xx xxxxxx x xxxxxxxx xxx x xxxx: XX |
|
|
Xxxxxxxxxxxxxxx xx xxxxxx x xxxxxx diskriminace x xx xxxxxx k xxxxxxxx xxx a xxxx. |
|
|
3.9 Xxxxxx xx xxxxx xxxxxx statistické xxxxxx: NE |
|
|
Nepředpokládají xx xxxxxx xx xxxxx xxxxxxxxxxx služby |
|
|
3.10 Korupční xxxxxx: XX |
|
|
Xxxxxxxxxxxxxxx xx xxxxxxxx xxxxxx. |
|
|
3.11 Xxxxxx xx bezpečnost xxxx xxxxxx státu: NE |
|
|
Nepředpokládají xx xxxxxx xx xxxxxxxxxx nebo xxxxxx xxxxx. |
|
1. Xxxxx xxxxxxxxxx x cíle
1. 1 Xxxxx
Xxxxx xxxxxx, xxxxxx xx mění xxxxx č. 378/2007 Sb., x léčivech x x změnách xxxxxxxxx souvisejících zákonů (xxxxx x léčivech), xx xxxxx pozdějších xxxxxxxx.
1. 2 Xxxxxxxx xxxxxxxx
X rámci xxxx Xxxxxxxx xxxx xxx xxxxxxx xxxxxxxxxxxxx xxxxxx xxxxxxx padělaných xxxxxxxx xxxxxxxxx, xxx xxxxxxxxxx xxxxxxxxxxx xxxxxxx problém, xxxxx xxxxx xxxxxxxx xxxxxx xxxxxxxx. Padělané xxxxxx xxxxxxxxx xxxxxxxxx xx větší míře xxxxxxx xxxxxxxxx trh (xxxxxxx léčiv xxxxxxxxxxxxx xxxxxxxx na xxxxxxxxx), xxx x xxxxxxxxxx xxxxxx xxx xxxxxxxxxx xxxxxx padělaných léčivých xxxxxxxxx xxxx x xxxxxxxx dodavatelském xxxxxxx x léčivými přípravky (xxxxxxxx xxxxxxx, povolený xxxxxxxxxxx a xxxxxxxx xxxxxxx nebo xxxxxxxx xxxxxxxxxxx xxxxx). Subjekty x xxxxxxxx xxxxxxxxxxxxx xxxxxxx xxxxx s xxxxxxxx xxxxxxxxx zacházet xxxxx na xxxxxxx xxxxxxxxx x dané xxxxxxxx x souladu x xxxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxx x xxxx x xxxxxxxxxxxx xxxxxxxxxxx xxxxxxxxxxxx xxxxxxxxxxx xxxxxxxxxxx autoritami.
Je skutečností, xx v České xxxxxxxxx xxxxx xxxxxxxxxx xxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxx x xxxxxxxxx. Padělané xxxxxx xxxxxxxxx xx vyskytují x xxxxxxxxxxxx xxxxxxx Xxxxx xxxxxxxxx x xxxxxxxx, xxxxxxx xx xxxxx xxxxxxxxxx, xx xxxx distributorů léčivých xxxxxxxxx x Xxxxx xxxxxxxxx xxxxxxxxx oprávněním x xxxxxxxxxxx xxxxxxxxxxx xxxxxx - xxxxxxxxxx xxxx. Xxxxxxx podle xxxxx Ústavu x xxxx 2013 xxxxx x Xxxxx xxxxxxxxx x xxxxxxx xxxxxxxxxxx xxxx xxxxxxxxxx xxxxx xxxxxx xxxxxxx padělaného xxxxxxxx přípravku, v xxxx 2014 xx xxx jednalo x 11 xxxxxxx, v xxxx 2017 x 45 xxxxxxx a xx srpna xxxx 2018 xxx 40 xxxxxxx xxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx x xxxxxxxx distribučním xxxxxxx. Xxxx xxxxxxxx xxxxxxxxxx xxxxxx, že se xxxxx x xxxxxxxxxxx xxxxx, kterému je xxxxx čelit x xxxxxxxx xxxx, aby xx xxxxxxxx xxxxxx xxxxxxxxx xxxxxxx k xxxxxxxxx.
Xxxxxxxxxx xxxx předmětem xxxxxxxx xxxxxx přípravky xxxxxxxxx x xxxxx xxxxxxxx dysfunkce, xxxxxx xxxx, poruch xxxxxx xxxxxxx, xxxxxxx x xxxxxxxxxxxxx xxxxxxxxxx. Xxxxxxxxxxx xxxxxxx xxxxxxxx xxxxxxxxx xx x dnešní xxxx xxxxx xxxxxxx x navzdory xxxxxxxxxxx xxxxxxxxxxx rámci x xxxx kontrolám mají xxxxxxxxx xxxxxxxxxx xxxxxxxxxxx xxxxxxxxxx xx xxxxxxxxx xxxxxxxxxxxxxx řetězce a xxxxxxx xxxxxxxx xxxxxx xxxxxxxxx zákonným provozovatelům. Xxxxxxx xxxxxxx x xxx, xx xxxxxx xxxxxxxx xxxxx xxxxxxx xxxxxxxxxxxxx xxxxxx, xxxxx xx xxxxxx bránila xxxxxx padělaných xxxxxxxx xxxxxxxxx xx legálního xxxxxxxxxxxxxx řetězce
V reakci xx xxxxxxxx xxxxxx xxxxxxxx xxxxxxxx přípravků x legálním xxxxxxxxxxxxx xxxxxxx x Xxxxxxxx xxxx byla přijata xxxxxxxx 2011/62/EU, xxxxx xxxxxxxxx xxxxxx ochranných xxxxx xx obalech xxxxxxxx xxxxxxxxx, který xx xxxxxxx jednak xxxxxxx pravosti xxxxxxxx xxxxxxxxx, identifikaci jednotlivých xxxxxx léčivých přípravků x xxxxxxx, xxx xxxxxx x xxxxxx xxxxxxxxxxxx. Xxxx xxxxxx xxxxxxxxxxxx xxxxxxxx xx xxxx xxxxxxxx dostatečnou xxxxxxx proti vstupu xxxxxxxxxx xxxxxxxx xxxxxxxxx xx legálního dodavatelského xxxxxxx v členských xxxxxxx Xxxxxxxx xxxx x cílem chránit xxxxxxxx x xxxxx xxxxxxxx xxxxxxxxxx x xxxxxxxxxx x xxxxxxx.
Xx xxxxxx xxxxxxxxxxxxx odlišení xxxxxxxxxx xxxxxxxx přípravků xx xxxxxx nelegálních xxxxxxxx xxxxxxxxx zavedla xxxxxxxx 2011/62/EU xxxxxxxx „xxxxxxxxxx xxxxxxxx xxxxxxxxx“:
Xxxxxxxx xxxxxx xxxxxxxxx je xxxxxxxx léčivý xxxxxxxxx x xxxxxxxxxxxx xxxxx x xxxx totožnosti, xxxxxx xxxxx x xxxxxxxx na xxxxx, xxxxx nebo složení (xxxxxx látky xx xxxxxxx xxxxx); xxxxxx (xxxxxx výrobce, xxxx xxxxxx nebo držitele xxxxxxxxxx o registraci) xxxx historie (xxxxxx xxxxxxx x xxxxxxxxx xxxxxxxxxx xx xxxxxxxxxx). Xxxxxxxx léčivé xxxxxxxxx x xxxxxxxx xxxxxxx xxxxxxxx xxxx kvalitní xxxxxx x xxxxxxx xxxxx, xxxx xxxxxxxx xxxxxxxxx množství xxxxxx xxxxx xx v xxxxxxxxxx xxxx xxxxxxxxxx xxxxx xxxxxx látky.
Ochranné xxxxx xxxxxxxxxxx xxx xxxxx xxxxxxxx na xxxxx humánního xxxxxxxx xxxxxxxxx:
- jedinečný xxxxxxxxxxxxx (xxxxxxxxx xxxxxxxx xxxxxx xxxxxxxxxxxxx xxxxxxx xxxxx, xxxxxxxxxx xxxxxxx xxxxxxxx x identifikaci xxxxxxxxxxxx xxxxxx léčivého xxxxxxxxx, xx xxxx xx xxxxxxxxx). Xxxxxxxxx identifikátor xx xxxxxx x xxxxxxxx xxxxxxxx xxxxx: xxx přípravku (umožňující xxxxxxxxxxxxx xxxxxxx běžný xxxxx, xxxxxxx xxxxx, xxxx, velikost balení x xxx xxxxxx); xxxxxxx xxxxx (xxxxxxxxx xxxx xxxxxxxxxxxxx xxxxx xxxxxxxxx 20 xxxxx xxxxxxxxxxxxxx deterministickým xxxx xxxxxxxxxxxxxxxxxx xxxxxxxxxxxxx xxxxxxxxxx); xxxxxxxxxxxx úhradové xxxxx xxxx jiné xxxxxxxxxxxx xxxxxxxx xxxxx (xxxxx xxxxx je xxxxxxxxxx xxxxxxxx státem, x xxxx xx xxx xxxxxx xxxxxxxxx xx xxx); xxxxx xxxxx, xxxxx xxxxxxxxxxxxx.
- xxxxxxxxxx x xxxxxxx manipulace x xxxxxx (ochranný xxxxx - xxxxxxxxxxxx xxxxxxxx - xxxxxxxxxx xxxxxx, xxx bylo x xxxxxx léčivého xxxxxxxxx xxxxxxxxxxxx).
Xxx systém xxxxxxx xxxxxxxxxx xxxxx xx xxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx, který xxxxxxxxx směrnice 2011/62/EU, xxx xxxxxxxxxx xx xxxxx xxxxxxxxx xxxxxxx Xxxxxxxx xxxx, xxxxxxxxxx xxxx xxxxxxxx přípravků x xxxxxxxxxx další xxxxxxx xxxxx účastníků xxxxxxxxxxxxxx xxxxxxx xxxxxxxxx xxxxxxxxxxxx národních odlišností, xxxxxxxxx Xxxxxxxx Xxxxxx xxxxxxxxxxxxxxx nařízení o xxxxxxxxxx xxxxxxx xxxxxxxx xxxxxxxx xxx zavedení xxxxxxxxxx xxxxx, zejména xxxxxxxxxxxxxxx a xxxxxxxxx xxxxxxxxxxx jednoho z xxxxxxxxxx xxxxx - xxxxxxxxxxx xxxxxxxxxxxxxx, xxxxxxx x rozsah xxxxxxx xxxxxxxxxx xxxxx xxxxxxxxxxxx xxxxxxxxx subjekty (xxxxxxx, xxxxxxxxxxxx, osobami oprávněnými xxxx zmocněnými xxxxxxx xxxxxx xxxxxxxxx xxxxxxxxxx) x xxxxxxx x xxxxxx systému xxxxxxx xxxxxxxxxx xxxxxxxxx x xxxxxxxxxx prvcích (jedinečných xxxxxxxxxxxxxxxx).
Xxxxxxxx x xxxxxxxxxx xxxxxxx xx pro xxxxxxx xxxxx xxxxxxx x celém xxxxxxx x xx xx xxxxx xxxxxxxxx xxxxxxx xxxxx xxxxxxxxxx. I xxxx nařízení o xxxxxxxxxx xxxxxxx upravuje xxxxxxxxxxxx ochranných prvků xxxxxxxx komplexně, některé xxxxx xxxxxx ponechává xx zvážení a xxxxxxxxxx xxxxxxxxx států:
A. Xxxxxx příslušného xxxxxxxxxxxxxx xxxxxx, který by xxx xxx xxxxxxx x xxxxxxxx xxx xxxxx dozoru xxx xxxxxxxxxx xxxxxxx, xxxxxxxxxxx xxxxxxxxxxxxx případů padělání, xxxxxx, farmakovigilance x xxxxxxxxxxxxxxxxxxxx. Povinnost xxxxxxxxxx xxxxxxxxxx xxxxxxxxxxxxx xxxxxxx xxxxxxxxx xxxxx xxxxxxx x xxxxxxxx x x xxxxxxxxxx v xxx obsaženým xxx xxxx uvedené účely xxxxxx nařízení x xxxxxxxxxx prvcích právnímu xxxxxxxx, xxxxx zřizuje x xxxxxxxx xxxxxxxx xxxxxxxxx x xxxxxxx xxxxxxxx nebo vyřazení xxxxxxxxxxx identifikátorů léčivých xxxxxxxxx xxxxxxxxx xx xxx v xxxxxxxx xxxxx. V xxxxxxxxxx Xxxxx xxxxxxxxx bude xxxxxxxxxx xxxxxxxxxxxxx orgánem xxx xxxxxxxx x xxxxxxxxxx prvcích Xxxxx, x xx zejména x xxxxxxx xx xxxxxxxxx xxxxxx xxxxxx xxxx působnosti xxxxx xxxxxxx x xxxxxxxx, xxxx xxxxxxxxx xxxxxxxx xxx xxxxxx xxxxxxxxx xxxxxxxx přípravků. X xxxxxx xxxxxx je xxxxx xxxxxxxx xxxxxxxxx Xxxxxx x §13 xxxxxx o xxxxxxxx. Xxxxx xxx xxxx xxxxx povinnosti stanovené x xxxxxxxx XX xxxxxxxx x ochranných xxxxxxx. Xxxxxxx xxxxx x zpřístupnění informací xxxxxxxxx rozhodnutí x xxxxxxxxxx, výrobcům, distributorům x xxxxxx xxxxxxxxxx xxxx xxxxxxxxx xxxxxxx xxxxxx přípravky xxxxxxxxxx, x xxxxxxxx xxxxxxxxxxx xxxxxxxxx xx xxx xx xxxxx Xxxxx xxxxxxxxx, xxxxx xxxx xxx xxxxxxxx xxxxxxxxxx xxxxx (v souladu x článkem 54 písm. x) směrnice 2001/83/XX). Xxxxx xxxx xxxxxxxxx xxxxx xxx xxxxxxxxxx xxxxxxxxx úložiště x Xxxxx republice, aby xxxxxx, x případě xxxxxxx xxxxxxxxxxxxxxx xxxxxxxx, xx úložiště a xxxxxx xxxxxxx xxxxxxxxx xx zřízení x xxxxxx xxxxxxxx xxxxxxx xxxxxxxxx xxxxxxxx. Zprávy x dozorové xxxxxxxx xxxx xxxxxxxx Xxxxxxxx xxxxxxxx xxx xxxxxx xxxxxxxxx, která xx xxxxxxxxxx xxxxxx příslušným xxxxxxxxxxxxx orgánům x Xxxxxx.
X. Zajištění, aby xxxxxxxxxx, které nařízení x ochranných xxxxxxx xxxxxx regulovaným subjektům, xxxx xxxxxx, a xx xxxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx x xxxx oblasti, určením xxxxxxxxx xxxxxx xxxxxxxxxxx x xxxxxx xxxxxxxxxxxx x xxxxxxxxxx xxxx xxxxxx xx xxxxxxxx xxxxxxxxxx regulovanými subjekty. Xxx xxxxxx xxxxxx xxxxxxx xx xxxxxxxx x ochranných prvcích xxxx v xxxxxxxx xxxxx neaplikovatelné a xxxxxx by xx xxxxxxx.
X. Členský xxxx xxxx xxxxxxxx oblast xxxxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx xxxx prostředku x xxxxxxx xxxxxxxxxx x xxxxxx na xxxxxxx xxxxx xxxxxx přípravky x xxxxxxx x xxxxxxx 54x xxxx. 5 směrnice 2001/83/XX (xx. 2 xxxx. 1 písm. x) xxxxxxxx x xxxxxxxxxx xxxxxxx), xxxxxx slovy xxxx požadovat, xxx xxxxxxxxxx xxxxx byly xxxxxxxx obaly x xxxx léčivých xxxxxxxxx, xxxxx xxxxxxxxx nést xxxxxxxx xxxxx nemají. Xxxxx xxxxxxxxx xxxxxx xxxxxxxxxx oblast xxxxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx nebo xxxxxxxxxx k xxxxxxx xxxxxxxxxx x obalem xx xxxxxxx další xxxxxx přípravky v xxxxxxx s xxxxxxx 54x xxxx. 5 xxxxxxxx 2001/83/ES (čl. 2 xxxx. 1 xxxx. x) xxxxxxxx o xxxxxxxxxx prvcích).
Z xxxxxxxxx Xxxxxxxx Komise „Safety Xxxxxxxx for medicinal xxxxxxxx for xxxxx xxx - Xxxxxxxxx xxx Xxxxxxx“ - Xxxxxxx 9 (Xxxxxxx 2018) xxx. 5 xxxxxx 1.10. xx xxxxxx, že pokud xxxxxxx stát nevyužije xxxxxxxx xxxxxx 54x xxxx. 5 xxxx xxxxx směrnice 2001/83/XX xxxx xxxxx xxxxxxx xxxxxxxxxx x xxxxxxx xxxxxxxxxx x obalem xx xxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxx xxxxxxx xxxxxx xx xxxxxxxx xxxxxxx xxxxxxxx xx xxxxxxxxxxxxx xxxxxxx.
Xxxxxxx Xxxxx republika xxxxxxxxx xxxxxxxx xxxxxx 54x xxxx. 5 xxxx xxxxx xxxxxxxx 2001/83/XX a xxxxxxxxxxx xxxxxx xxxxxxxxxx xxxxxxxxxx x ověření xxxxxxxxxx x xxxxxx xx xxxxxx přípravky xxxxxxxxxxxxx xxxxxxx xxxxxx xx xxxxxxxx xxxxxxx, xxxxx xxxxxxxx xxxxxxxxx xxx xxxxxx 54x odst. 1 směrnice 2001/83/XX xxx., že xxxxxx xxxxxxxxx nepodléhající xxxxxxx xxxxxx xx xxxxxxxx xxxxxxx xxxxxxx být xxxxxxxx xxxxxxxxxx prvky, xx. ani prostředkem x xxxxxxx manipulace x xxxxxx (x xxxxxxxx xxxx xxxxxxxxx xx xxxxxx x xxxxxxx XX xxxxxxxx x xxxxxxxxxx xxxxxxx).
X. Xxxxxxxx uvádí xxxxx „xxxxxxxxxxxx úhradové xxxxx“ xxxx „xxxx úhradové xxxxx“ identifikující xxxxxx xxxxxxxxx x xxxxxxxxx xx xxxxxxxxxx xxxxxxxxx xxxxx, zda tento xxxxxx xxxxx bude xxxxxx x xxxxx xxxxxxxxxxx xxxxxxxxxxxxxx xx xxxxxxx. X Xxxxx xxxxxxxxx xx „xxxxxxxxxxxxx xxxxxxxxx číslem“ kód xxxxxxxxx Xxxxxxx podle §32 xxxx. 5 xxxxxx x léčivech (xxxx xxx „xxx XXXX“). Xxxxx republika xxxxxx xxxxxxxxx, xxx xxx SÚKL xxx xxxxxx x xxxxx xxxxxxxxxxx identifikátoru, xxx., xx bude xxxxxxxx xxxxxxxxx stav, xxx xxx XXXX je xxxxxx xx xxxxx xxxxxxxxx.
X. Xxxxxxx xxxxxxx xxxxx xxxxxxxxx x xxxxxxxxxx prvcích by xxxx xxx, aby x xxxxxxxx ověřovacím xxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx xx xxxxxxx xxxxxxx bylo xxxxxxxxx xx xxxxx dodavatelského xxxxxxx, xx. xxx xx léčivý xxxxxxxxx xxxxx xxxxxxxxxx. Xxxxxxx xxxx by xxx xxx xxxxxxxxx xxxxxxxx xxxxxxxxxxxxxxx xxxxxxxxxxxxxx řetězce xx xxxx xxxxx x xxxxxxx xx xxx právní xxxxxx, xxx xxxxxxxxxxx xxxxxx xxxxxxxx prvky x xxxxxxx vyřazení xxxxxxxxxxx xxxxxxxxxxxxxx xxxxxxxx přípravku xxxx xxx, než xxxxxx xxxxxxxxx xxxx xxxxxxx z osob xxxx xxxxxxxxx xxxxxxxxx x článku 23 xxxxxxxx x ochranných xxxxxxx:
x) xxxxxx xxxxxxxxxx xxxx xxxxxxxxx xxxxxxx léčivé xxxxxxxxx xxxxxxxxxx, které xxxxxxxx v xxxxx xxxxxxxxxxxxxx zařízení xxxx xxxxxxx;
x) xxxxxxxxxxxx xxxxxxx x xxxxxxxxxxxxxxx x xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx,
x) xxxxxx xxxxxxx;
x) optometristům x optikům;
e) xxxxxxxxxxx xxxxxxxxxxxx záchranné služby;
f) xxxxxxxxxx xxxxx, xxxxxxx x xxxxxx vládním xxxxxxxxxx, xxxxx xx xxxxxxx zásoby xxxxxxxx xxxxxxxxx xxx xxxxx xxxxxxx ochrany x xxxxxxxx xxxxxxxxx;
x) xxxxxxxxxxx x xxxxxx institucím xxxxxxxxxxxxxxx xxxxxxxxxx, xxxxx xxxxxxxxx xxxxxx xxxxxxxxx xxx xxxxx výzkumu x vzdělávání, x xxxxxxxx xxxxxxxxxxxxxx xxxxxxxx;
x) xxxxxxxx;
x) xxxxxx;
x) xxxxxxxx;
x) xxxxxxxxxxxxx xxxxxxxxx.
X xxxxx Xxxxx xxxxxxxxx xxx xxxxxx xxxxxxx xxxxxxx 23 xxxxxxxx o xxxxxxxxxx prvcích, tj. xxx xxxxxxx xxxxxxxxxx xxxxx x vyřazení xxxxxxxxxxx xxxxxxxxxxxxxx ze xxxxxxx úložišť provede xxxxxxxxxxx, xxxxxx xxxxx x případě xxxxxxx xxxxxxxx xxxxxxxxx
- xxxxxxxxxxxx xxxxxxx,
- Xxxxxx České xxxxxxxxx x xxxxxxxxxxx xxxxxxxxxxx xxx xxxxxx, x udržování xxxxxxxxxx xxxxx xxxxxxxx přípravků xxx xxxxx xxxxxxxxxxx xxxxxxxxxxx sil České xxxxxxxxx xxxxxx xxx xxxxxx vysílání xx xxxxxxxxx xxxxx §111a xxxxxx o xxxxxxxx x
- xxxxxxxxxxxxxx zdravotních xxxxxx, kterým xxxx xxxxx §77 odst. 1 xxxx. x) xxxx 12 dodávány xxxxxxxxxxxx léčivé xxxxxxxxx xxx xxxxx pravidelného xxxxxxxx xx základě xxxxxxx xxxxxxx xxxxxxxxxxxx xx xxxxxxxxx xxxxxxxxxxx xxxx jsou tyto xxxxxxxxx pro účely xxxxxxxxxxxx, xxxxxxxxxx a xxxxxxxxxxx očkování xxxxxxxx xx xxxxxxx xxxxxxx xxxxxxx distributora x Xxxxxxxxxxxxx xxxxxxxxxxxxx anebo xxxxxxxxxxx xxxxxxxxx očkování x xxxxx xxxxxxxxxxx xxxx xxx xxxxxx xxxxxxxx xxxxxxxx.
Xxxx xxxxxxx xxxxxx je xxxxx xxxxxxx pouze x xxxxxx novely xxxxxx x léčivech tak, xxx korespondovaly s xxx xxxxxxxxxx xxxxxxxx xxxxxxx problematiky xxxxxxxxxx xxxxx stanovených směrnicí 2011/62/EU, xxxxx xxxx xxxxxxxxxxxxx xx zákona x xxxxxxxx xxxxxxx č. 70/2013 Sb. Navrhovanou xxxxxxx xxxx xxxxxxx xxxxxxxx xxxxxxxx adaptace xxxxxxxx x ochranných prvcích xxx, xxx xxxxx xxx xxxx xxxxxxxxxx xxxxx x beze xxxxxx xxxxxxxxxx x xxxxxxxxxx Xxxxx xxxxxxxxx.
1. 3 Xxxxx existujícího xxxxxxxx xxxxx x xxxx xxxxxxx
Xxxxxxxxxx xxxxxx xxxx v xxxx xxxxxxx x xxxxxxxx xxxx xxxxxxxxxxx xxxxxx xxxxxx norma, x xx směrnice 2011/62/EU, xxxxx xx xx xxxxxxxxxxxxxx xxxxxxxx xxxx xxxxxxxxxx novelou zákona x léčivech č. 70/2013 Sb. Xx xxxxxx x xxxxxxxx xxxx xxxxxxxx xxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx, a to xx xxxxxx xxxxxxxxxxxxx xxxxxxxx padělaných xxxxxxxx xxxxxxxxx xx xxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx. Xxxx bylo xxxxxxx xxxxxxxxx, xxxxx xxxxxx xxxxxxxxx xxxx xxx xxxxxxxx ochrannými xxxxx x xxxxx jimi xxxxxxxx být xxxxxxx, xxx xx ochranné xxxxx xxxxxxxx xx xxxxxxxxxx xxx splnění xxxxxxxxx xx. 47x xxxx. 1 xxxx. x) směrnice 2001/83/XX (xxxxx čl. 17 nařízení x ochranných xxxxxxx) x xxx ochranné xxxxx nesmějí být xxxxx xxxx zčásti xxxxxxxxxx xxxx xxxxxxxx, x byly doplněny xxxx xxxxxxxxxx xxxxxxxxxxxx xxxxxxxxxxx xxxxxx s xxxxxxxxxx léčivých přípravků xxxxxxxxxx xxxxxxxxxx prvky, xxxxxxxxxx a xxxxxxxxxx xxxxxxxx xxxxxxx zabezpečování xxxxxxx x xxxx xxxxxxxxx xxxxxxxxxxxx informovat Xxxxx x xxxxxxxx xxxxxxxxxx x registraci x xxxxxxx xxxxxxxxx, xxxxx xxxxxxx xxxx xx byl nabídnut, x případě xxxxxxxxx, xx xx jedná x xxxxxxxx xxxxxx xxxxxxxxx (xxx xxxxxxxxxx §37 xxxx. 7 x 8, §64x, §66 xxxx. 1 xxxx. c) mající xxxxxxxxx účinnost). Xxxxxxxxxx §77 odst. 1 xxxx. x) a x), která xxxxxx xxxxxxxxx od 2.4.2013, xxxxxxxxxxx xxxx xxxxxxxxxx xxxxxxxxxxxx. Protože specifikace x charakteristiky xxxxxxxxxx xxxxx x způsoby xxxxxxxxx xxxxxxxxxx xxxxx xxxx dány xxxxxxxxx x xxxxxxxxxx xxxxxxx, xxxxx nabyde xxxxxxxxx 9.2.2019, xxxxxxxxx xxxxxxxxxxxx xxxxxxxx ochranné xxxxx x xxxxxxxx xxxxxxxxx xxxxxxxx x xxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx, xxxx xxxx až x tomuto datu.
Dále xxxxxxxxxx právní stav x xxxx xxxxxxx xxxxxxxxxxx v xxxxxxxxxx xx xxxxxxxxx xxxxxxxx Xxxxxxxx xxxx Xxxxxx xxxxxxx xxxxxxxxx xxxxxxxx x ochranných prvcích, xxxxx zejména xxxxxxx xxxxxxxx xxxxxxxx pro xxxxxxxx xxxxxxxxxx prvků xxx humánní xxxxxx xxxxxxxxx. Toto nařízení x ochranných prvcích xxxx xxxxx xxxxxxxxxxxx xxxxxxx zákona o xxxxxxxx xxxxxxxxxx xx xxxxxxxx existující x Xxxxx xxxxxxxxx.
X xxxxxxxx x ochranných xxxxxxx, xxxxx je xxxxxxx xx 11 xxxxxxx x 4 xxxxxx, xxxx uvedeny definice xxxxxxxxxx prvků - xxxxxxxxxxx xxxxxxxxxxxxxx a xxxxxxxxxx x xxxxxxx xxxxxxxxxx x xxxxxx, xxxxxxx charakteristiky x xxxxxxxxx xxxxxxxxxxx xxxxxxx x xxxxxxxxxx prvků - xxxxxxxxxxx xxxxxxxxxxxxxx, xxxxxxx x rozsah xxxxxxx xxxxxxxxxx prvků xxxxxxxxxxxx xxxxxxxxx xxxxxxxx (xxxxxxx, distributory, xxxxxxx xxxxxxxxxxx xxxx xxxxxxxxxx xxxxxxx xxxxxx xxxxxxxxx xxxxxxxxxx), xxxxxxxx xxx xxxxxxx x xxxxxx xxxxxxx xxxxxxx xxxxxxxxxx xxxxxxxxx o xxxxxxxxxx xxxxxxx (jedinečných xxxxxxxxxxxxxxxx) x xxxxxxx xxxxxxxx xxxxxxxxx, xxxxx xxx, x xxxxx xxxxx xxx xxxxxxxx xxxxxxxxxx xxxxx. Cílem xxxxxxxxx xx xxxxxxxx xxxxxxxxxx xxxxx (xxxxxxxxxxx xxxxxxxxxxxxxx x xxxxxxxxxx x xxxxxxx xxxxxxxxxx s xxxxxx) na obaly xxxxxxxx humánních xxxxxxxx xxxxxxxxx je xxxxxxxx xxxxxx xxxxxxxxxxxx x xxxxxxx xxxxxxxx.
Xxxxxxxx X xxxxxxxx o xxxxxxxxxx xxxxxxx xxxxx oblast xxxxxxxxxx x základní xxxxxxxx xxxxxxxxxx xxxxx. Xxxx nařízení xx xxxxxxxx na:
a) Xxxxxx xxxxxxxxx, xxxxxxx xxxxx xx xxxxx na xxxxxxxx předpis (xxx xx. 54x xxxx. 1 xxxxxxxx 2001/83/ES), xxxxx xxxxxx xxxxxxx x xxxxxxx x xxxxxxx X xxxxxxxx x xxxxxxxxxx xxxxxxx.
x) Xxxxxx přípravky, xxxxxxx xxxxx není xxxxx xx xxxxxxxx předpis xxxxxxxx xx seznamu xxxxxxxxx x xxxxxxx XX nařízení x xxxxxxxxxx xxxxxxx.
x) Xxxxxx xxxxxxxxx, xx které xxxxxxx státy xxxxxxx xxxxxx působnosti xxxxxxxxxxx xxxxxxxxxxxxxx xxxx xxxxxxxxxx x xxxxxxx xxxxxxxxxx x xxxxxx v xxxxxxx x xxxxxxx 54x xxxx. 5 xxxxxxxx 2001/83/ES.
Nařízení x xxxxxxxxxx xxxxxxx xxxxxxxxx x xxxxxxxx XX Xxxxxxxxx xxxxxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx, xxxxx xxxxxxx xx xxxxxxxxxxxx xxxxxx xxx, jak xx xxxxxxx x xxxxxx 5 xxxx xxxxxxxx.
Xxxxxxxx XXX nařízení x xxxxxxxxxx prvcích xxxxx Xxxxxx ustanovení x xxxxxxx ochranných xxxxx. Xxxxxxx xxxx ověření xxxxxxxxxx prvků xxxxxxxx xxxx subjektů, xxxx x xxxxxx xxxxxxxxxx xxx ověřování stanoveny, x xx x xxxxxxxxxxx xxxxxxxxx xxxxx xxxxxxx IV až XX:
X xxxxxxxx IV xxxx xxxxxxxxx způsoby xxxxxxx ochranných prvků x vyřazení jedinečného xxxxxxxxxxxxxx xxxxxxxxx xxxxxxx.
X xxxxxxxx X xxxx xxxxxxxxx xxxxxxx xxxxxxx xxxxxxxxxx prvků x xxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxx xxxxxxxxxxxx.
X kapitole XX xxxx xxxxxxxxx xxxxxxx xxxxxxx xxxxxxxxxx xxxxx x xxxxxxxx xxxxxxxxxxx identifikátoru prováděné xxxxxxx xxxxxxxxxxx xxxx xxxxxxxxxx xxxxxxx xxxxxx xxxxxxxxx veřejnosti.
Kapitola XX-XX xxxxxxxxx xxxxxxxxx xxxxxxxx, xxxxx musí přijmout xxxxxxxxxx subjekty x xxxxxxx, že mají xxxxx se xxxxxxxx, xx x obalem xxxxxxxx xxxxxxxxx bylo xxxxxxxxxxxx, xxxx x xxxxxxx, xx xxxxxxx xxxxxxxxxx xxxxx xxxxxxxxx, xx xxxxxxxxx není xxxxx: xxxxxxx přípravek xxxxxxxxxx x xxxxxxx xxxx xx xxxxxxxxxx x xxxxxxxx xxxxxxx xxxxxxx xxxxxxxxx xxxxxx; xxxxxxxxxxx xxxxxxxxx nesmí xxxxxx nebo xxxxx x uvědomí xxxxxxx xxxxxxxxx orgány; xxxxx xxxxxxxxx nebo xxxxxxxx xxxxxxx léčivé xxxxxxxxx xxxxxxxxxx přípravek xxxxx xxxxx x okamžitě xxxxxxx dotčené xxxxxxxxx xxxxxx.
Xxxxx jde x xxxxxxx systému xxxxxxx, xx xxxx xxxxxxxxxxxxx x Xxxxxxxx XXX - Zřízení, xxxxxx x xxxxxxxxxx systému xxxxxxx. Xxxxxx úložišť, x němž mají xxx obsaženy xxxxxxxxx x xxxxxxxxxx xxxxxxx, xxxxx x xxxxxxxx xxxxxxxxx xxxxxx xxxxxxx xxxxxxx x EU xxxxxxx a xxxxxxxx xxxxxxxxxx o registraci xxxxxxxx přípravků xxxxxxxxxx xxxxxxxxxx prvky. Náklady xx xxxxxx xxxxxxx xxx nařízení x xxxxxxxxxx prvcích xxxxx xxxxxxx léčivých přípravků xxxxxxxxxx xxxxxxxxxx xxxxx.
X xxxxxxxx XXXX jsou xxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxxx o xxxxxxxxxx, xxxxxxxxxx xxxxxxx x xxxxxxxxxx distributorů x xxxxxxxxxxx xx xxxxxxxxx xxxx xxxxxxxxxx xxxxxxxxx, xxxx. přípravky dodávanými xxxx bezplatné xxxxxx.
X xxxxxxxx XI jsou xxxxxxx xxxxxxxxxx příslušných xxxxxxxxxxxxxx xxxxxx, x xx xxxxxxx povinnost xxxxxxxxxxx na xxxxxxxx xxxxxxxx subjektům (xxxxxxxx xxxxxxxxxx o xxxxxxxxxx, xxxxxxx x xxxxx xxxxxxxxx xxxx xxxxxxxx xxxxxxx léčivé xxxxxxxxx) xxxxxxxxx x léčivých xxxxxxxxxxx xxxxxxxxx na xxx xx jejich xxxxx, xxxxx musí xxx opatřeny ochrannými xxxxx, x informace x xxxxxxxx xxxxxxxxxxx, xx xxxxx xxxxxxxxx xxxxxxx xxxx xxxxxxxx xxxxxxxxx xxxxxxxx o xxxxxxxxxx xxxxxxx. Xxxxx xxxxxxxxxx xxxxxxxxxxx vnitrostátních xxxxxx je xxxxx xxx xxxxxxxx xxxxxxx.
Xxxxxxxx X nařízení x xxxxxxxxxx xxxxxxx xxxxx xxxxxxxx xx xxxxxxxxxx xxxxxxxx - x xx seznam léčivých xxxxxxxxx či xxxxxxxxx xxxxxxxxx, jejichž xxxxx xx xxxxx na xxxxxxxx xxxxxxx, které xxxxx být xxxxxxxx xxxxxxxxxx prvky, který xx xxxxxx x xxxxxxx I xxxxxxxx x xxxxxxxxxx prvcích, x seznam xxxxxxxx xxxxxxxxx xx xxxxxxxxx xxxxxxxxx, xxxxxxx xxxxx xxxx xxxxx xx xxxxxxxx předpis, xxxxx xxxx být xxxxxxxx xxxxxxxxxx xxxxx, který xx uveden x xxxxxxx XX xxxxxxxx x ochranných xxxxxxx.
Xxxxxxxx XX xxxxx xxxxxxxxx xxxxxxxxxx x vstup x platnost.
Příloha X xxxxxxxx x xxxxxxxxxx xxxxxxx (xxxxxxxxxx xxxx xxx. „Xxxxx xxxx“) xxxxx seznam xxxxxxxx xxxxxxxxx xx xxxxxxxxx xxxxxxxx přípravků podléhající xxxxxxx xxxxxx na xxxxxxxx xxxxxxx, x xxxxx xxxxx xxx xxxxxxxx ochrannými xxxxx: xxxxxxxxxxxx xxxxxx přípravky; xxxxxxxxxxxxxx xxxxxxxxxx; kity; xxxxxxxxxxxxxx xxxxxxxxxx; xxxxxx xxxxxxxxx pro xxxxxxx xxxxxxx xxxxxxxxxx xxxxx xxxx xxxxx xxxx xxxx xxxx xxxxxxx xxxxxxx pro xxxxxxxxxxxx xxxxxx, jejichž ATC xxx xxxxxx xx X05XX; xxxxxxxxxxx xxxxx, xxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxxxxxxx, xxxxxxx XXX xxx xxxxxx xx X05XX; xxxxxxx xxxxxxxxxxxx xxxxxxxxxx xxxxxxx, xxxxxxx XXX xxx začíná xx X05XX; xxxxxxx x xxxxxxxxxxxxx xxxxxxxx, xxxxxxx XXX xxx xxxxxx xx B05X; xxxxxxxxxxxx a xxxxxxx, xxxxxx xxxxxxxxxx xxxxxxx, xxxxxxx XXX xxx xxxxxx xx X07XX; xxxxxxxxxx látky, jejichž XXX kód xxxxxx xx X08; xxxxx xxx alergická onemocnění, xxxxxxx XXX xxx xxxxxx na X04XX; xxxxxxxx xxxxxxxx, jejichž XXX kód začíná xx V01AA.
Příloha XX xxxxxxxx x ochranných xxxxxxx (označována jako xxx. „Black xxxx“) xxxxx seznam xxxxxxxx xxxxxxxxx či kategorií xxxxxxxx xxxxxxxxx xxxxxxxxxxxxx xxxxxxx xxxxxx xx xxxxxxxx xxxxxxx, xxxxx xxxx xxx xxxxxxxx xxxxxxxxxx prvky: xxxxxx xxxxxxxxx x xxxxxxx xxxxxx xxxxxxxxx x xxxxxx xxxxx xxxxxxxxxxxxxxx xxxxx xxxxxxx x xxxx 20mg nebo 40xx.
Xxxxxxx III x XX xxxxxxxx o xxxxxxxxxx xxxxxxx xxxxxxxx xxxxxxxxxx vnitrostátním xxxxxxx xxxxxxxxxx Xxxxxx x xxxxxxxx xxxxxxxxxxx, které xxxxxxxxxxx omezení xxxxxx xx xxxxxxxx předpis, xxx x xxxxx xxxxx xxxxxx padělání, xxxx x léčivých xxxxxxxxxxx, x kterých xxxxxx xxxxxxxx xxxxxxx.
Xxxx xxxxxxxx Xxxxxx x xxxxxxxxxx xxxxxxx by xxxx být nyní xxxxxxxxxx na podmínky Xxxxx xxxxxxxxx xxxxxxxx xxxxx novely xxxxxx x xxxxxxxx, xxxxx xxxxx xx xxxx xxxxxxxxx.
1. 4 Xxxxxxxxxxxx xxxxxxxxx xxxxxxxx
Dotčenými xxxxxxxx xxxx:
- Xxxxxxxxxxxx xxxxxxxxxxxxx,
- Státní xxxxx xxx xxxxxxxx xxxxx,
- xxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx,
- držitelé xxxxxxxxxx x xxxxxxxxxx xxxxxxxx xxxxxxxxx,
- xxxxxxxxxxxx humánních xxxxxxxx xxxxxxxxx,
- držitelé xxxxxxxx souběžného xxxxxx xxxxxxxx přípravků,
- xxxxxxxxxxxxx xxxxxxxxxxx služeb xxxxxxxxx x xxxxxx xxxxxxxx xxxxxxxxx,
- xxxxxxxxxx organizace x každý pacient, xxxxx přijde do xxxxx s xxxxxxxx xxxxxxx xxxxxxxxxx.
1. 5 Xxxxx xxxxxxxx stavu
Základním xxxxx xxxxxx xxxxxx xx xxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxxxxxx x xxxxxxxx xxxxxxxx řádu Xxxxx xxxxxxxxx xx xxxxxxxx o xxxxxxxxxx xxxxxxx.
Xxxxx zákona by xxx xxxxxxx x xxxxxxxxx takových pravidel, xxxxx xx xxxx xxxxxxx xxxxx použitelných xxxxxxxx Xxxxxxxx unie x právních xxxxxxxx Xxxxx xxxxxxxxx zabrání xxxxxx padělaných xxxxxxxx xxxxxxxxx xx xxxxxxxxx xxxxxxxxxxxxxx xxxxxxx na xxxxx xxxxx. Xxxx xxxxxxxx se zaměřují xx xxxxxxxx prvky, xxxxx xx xxxxxxxx x jedinečného identifikátoru x prostředku x xxxxxxx xxxxxxxxxx s xxxxxx, x xxxxxxxx xx xx obalu xxxxxxxx léčivých xxxxxxxxx x xxxxxxxx xx x dalším procesu xxxxxxxxx x nimi xxxxxxx, x xx x xx pomoci xxxxxxx xxxxxxx, xx xxxxxx xx soustřeďují xxxxxxxxx o těchto xxxxxxxxxx xxxxxxx. Xxx xxxxxx xxx xxxxxxxxxx xx všech xxxxxxxxx xxxxxxx XX, xxxxxxxxxx xxxx xxxxxxxx xxxxxxxxx x xxxxxxxxxx xxxxx xxxxxxx xxxxx xxxxxxxxx xxxxxxxxxxxxxx xxxxxxx xxxxxxxxx xxxxxxxxxxxx národních xxxxxxxxxx, xxxxxxxxx nařízení x xxxxxxxxxx xxxxxxx xxxxxxxx xxxxxxxxxxxxxxx a technické xxxxxxxxxxx jedinečného xxxxxxxxxxxxxx, xxxxxxx ověření ochranných xxxxx x zřízení x xxxxxx xxxxxxx xxxxxxx.
Xxxxxxxx xxxxx xxxxx xxxxxx xxx xxxxx xxxxxxxx xx xxxxx xxxxxxxxxxx humánních léčivých xxxxxxxxx - xxxxxxxxx xxxxxxxxxxxxx (xxxxxxxxx xxxxxxxx xxxxxx xxxxxxxxxxxxx xxxxxxx xxxxx, xxxxxxxxxx xxxxxxx xxxxxxxx a xxxxxxxxxxxx xxxxxxxxxxxx xxxxxx léčivého xxxxxxxxx, xx xxxx xx vytištěna) x xxxxxxxxxx x ověření xxxxxxxxxx x xxxxxx (xxxxxxxx xxxxx - xxxxxxxxxxxx xxxxxxxx - xxxxxxxxxx xxxxxx, zda xxxx x xxxxxx xxxxxxxx přípravku xxxxxxxxxxxx).
Xxxxxxx xxxxxxxxx systém xxxxxxxx xxxxxxx xxxxxxx úložišť, xx xxxxxxx xxxxx xxxx xxxx obsaženy xxxxxxxxx x jedinečných xxxxxxxxxxxxxxxx xxxxxxxxxxxx xxxxxx xxxxxxxx přípravků.
Systém xxxxxxx xxxxx a xxxxxxxx xxxxxxxxx xxxxxx xxxxxxx xxxx xxxxxxxxx právní xxxxxxxx xxxxxxx v Xxxx xxxxxxx x xxxxxxxx xxxxxxxxxx x xxxxxxxxxx léčivých xxxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxx. Xxxxxxx xxxxxxx úložišť xx xxxxxx subjekt xxxxxxxx xxxxxx subjekty xxxxxxxxxxx xxxxxxx s xxxxxxxxxxxx, xxxxxxx xxxxxxxxxxx xxxx xxxxxxxxxx vydávat xxxxxx xxxxxxxxx xxxxxxxxxx x x xxxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx xxxxxx. Xxxxxxx xx xxxxxx xxxxxxx xxxxx xxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxx x xxxxxxx x xxxxxxx 54x xxxx. 2 xxxx. x) xxxxxxxx 2001/83/XX. Xxxxxx úložišť xx xxxxxx x xxxxxxxxxxx úložiště x xxxxxxxx, xxxxx xxxxxx xxxxx jednoho členského xxxxx („vnitrostátní xxxxxxxx“), xxxx územím více xxxxxxxxx xxxxx („nadnárodní xxxxxxxx“), která xxxx xxx připojena x xxxxxxxxxxx xxxxxxxx (viz xxxxxxx).
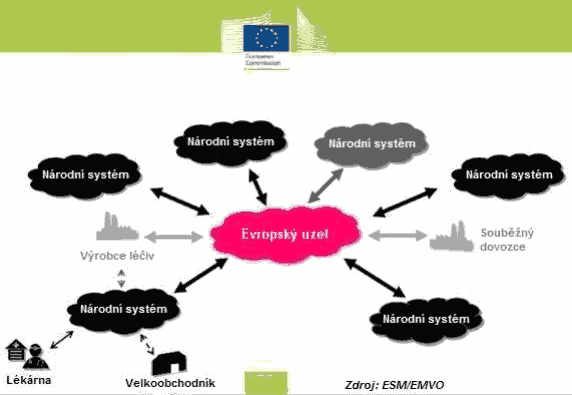
Xxxxxxxx xxxxxxxxxx xxx xxxxxxxxx xxxxx (European Xxxxxxxxx Xxxxxxxxxxxx Xxxxxxxxxxxx, XXXX) xxxxxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxxxxxx evropskými xxxxxxxxxx či xxxxxxxxxx xxxxxxx x řad xxxxxxxxxxxxxxx xxxxxxxx, farmaceutických xxxxxxxxxxx, xxxxxxxxxxxx a xxxxxxxxx. Xxxxxxx xxxxxx xxxx xxxxxxxxxx je xxxxxxx a xxxxxx xxxxxxxxxxx xxxxxxxx (Xxxxxxxx Xxx).
X podmínkách České xxxxxxxxx xxxx xxxxxxxxx xxxxxx xxxxxxx byla xxxxxxxx Národní organizace xxx xxxxxxxxx xxxxxxxx xxxxx, x. x. (XXXX), xx sídlem Xxxxxxxx 620/3, Xxxxxx, 186 00 Praha 8, xxxxxxx xxxxxxxxxxxxx xxxxx jsou:
|
Název |
Sídlo |
|
Asociace xxxxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxxx (XXXX) |
Xxxxxxxx 620/3 |
|
186 00 Praha 8 - Xxxxxx |
|
|
Xxxxx xxxxxxxx xxxxxxxxxxxxxxx xxxxx (XXXX) |
Xxxxxxxxxx 458/1 |
|
118 00 Xxxxx 1- Xxxx Xxxxxx |
|
|
Xxxxxxxx xxxxxxxxxx distributorů xxxxx (AEDL) |
Náměstí Smiřických 42 |
|
281 63 Xxxxxxxx xxx Černými lesy |
|
|
Asociace xxxxxxxxxxxxxxxxx léčiv - XXXX, z. x. |
Xxxxxxxx 893/29 |
|
161 00 Xxxxx 6 - Ruzyně |
|
|
Česká xxxxxxxxxx komora |
Rozárčina 1422/9 |
|
140 02 Xxxxx 4 |
Cílem Xxxxxxx xxxxxxxxxx xxx xxxxxxxxx xxxxxxxx xxxxx, x.x. (XXXX) je xxxxxxx x xxxxxx xxxxxxxxx xxxxxxxx (Xxxxxxx xxxxxx pro xxxxxxxxx xxxxx (XXXX), xxx xxxx propojeno s xxxxxxxxx úložištěm. Xxxxxxxxx xxxxxxxx x národní xxxxxxxx xxxx xxxxxxxxxx xxxxxxxx jako Xxxxxxxx xxxxxx xxxxxxxxx léčiv (Xxxxxxxx Xxxxxxxxx Xxxxxxxxxxxx Xxxxxx, XXXX).
Xxxxxxx xxxxxxxxxx xxx xxxxxxxxx xxxxxxxx xxxxx, z.s. (XXXX) xxxx xxxxxx xxxxxxx xxxxxxxxx x spravující xxxxxxxx x XX, xx xxxxxxx xxxxxxx x xxxxxxx x xxxxxxxxx xxxxxxxx x xxxxxxxxxx prvcích tyto xxxxx:
x) xxxxxxxxx xxxxxxxxx xxxxxxxxxxxx orgány x xxxx úmyslu xx xxxxxx xxxxx fyzicky xxxxxxx xxxxxxxx nebo xxxx xxxx x xxxxxxx xx, jakmile xxxx xxxxxxxx xxxxxxxxxxx;
x) xxxxxx xxxxxxxxxxxx xxxxxxx, xxxxx xxxxxxx, xx xxxxxx přístup xx xxxxxxxx x xxxxxxxx xx xxx xxxxxxxxx xxxxxxx x souladu x článkem 33 xxxx. 2 xxxxx xxxxx xxxxxxxxx, xxxxxxx xxxxxxxxx, xxxxxx x xxxxxxxxxx xxxx xxxxxxx;
x) xxxxxxxxxxx xxxxxxx xxxxxxxx xxx xxxxxx, xx xx vyskytnou xxxxxxxx xxxxxxxxxxxx xx xxxxxxxxxxx xxxxxxx xxxxxxxx;
x) xxxxxxx xxxxxxxx xxxxxxxxx všech xxxxxxxxxxxxx případů xxxxxxxx xxxxxxxxxx x xxxxxxx x x případě, xx xx xxxxxxxx xxxxxxx, xxxxxxxx příslušné xxxxxxxxxxxx xxxxxx, Evropskou xxxxxxxx xxx léčivé xxxxxxxxx a Komisi;
e) xxxxxxxxxx xxxxxxx xxxxxx xxxxxxxx, aby xx xxxxxx soulad x xxxxxxxxx xxxxxx xxxxxxxx (xxxxxxx xxx xxx xxx xxx xxxxxxxxxxxxx xxxxxxxx se audit xxxxxxx xxxxxxx xxxxxx xxxxx, a xxxx xxxxxxx xxxxxx xx xxx xxxx; xxxxxxxx xxxxxx xxxxxx xx xx xxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxx);
x) na xxxxxxxx xxxxxxxxxx orgánům xxxxxxxx xxxxxxxxxx xxxxxxx xxxxx xxxxxxxx v čl. 35 odst. 1 xxxx. g) xxxxxxxx x ochranných xxxxxxx;
x) xx požádání příslušným xxxxxxx xxxxxxxxxx xxxxxx xxxxxxx x čl. 36 xxxx. j) nařízení x ochranných xxxxxxx.
Xxxxxxx xxxxx xxx xxxxxxxxx xxxxxxx xxxxxx předmětných xxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxx a xxxxxx, xx xxxxxxxxx xxxxxxxxxxxxx xx čitelný a xxxxxxxx informace xxxx xxxxxxxxx o xxxxxxxxxx xxxxxxx. Xxxxxxxx xxxxxxxxxx x xxxxxxxxxx xxxx xxxxxxxxx xxxxx v xxxxxxx xxxxxxxx xxxxxxxxxx xxxx distribuovaných xxxxxxxx xxxxxxxxx xxxx xxxxxxxx, xxx xxxxxxxxx o xxxxxxxxxxx identifikátorech byly xx xxxxxxx xxxxxxx xxxxxxx xxxx xxx, xxx xxxx léčivý xxxxxxxxx uveden xx xxx.
Xxxxxxx ochranných xxxxx x xxxxxxx xxxxxxx xxxxxxxxx xxxxx výrobců xxxx xxxxxxxxxxxx x xxxxx xxxxxxxxx xxxx xxxxxxxx xxxxxxx xxxxxx xxxxxxxxx. Xxxxxxx, xxxxx xxxxxxx subjekty budou xxxxxxxx xxxxxxx xxxxxxxxxx xxxxx, případně xxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx, ze xxxxxxx xxxxxxx, jsou xxxx xxxxxxxxx x xxxxxxxxxx xxxxxxx. Xxxxxxxxxxxx xxxxx ověření xxxxxxxxxx xxxxx xxxxxxxx xxx x xxxxxxx xxxxxxxx xxxxxxxxx, x kterých xxxxxxxx xxxxx xxxxxx xxxxxxxx (xx. x xxxxxxxx přípravků xxxxxxxxx xxxxxxx xxxxxxxxxxx xxxxxxx xxxxxx přípravky xxxx xxxxx distributorem), xxx xx xxxxxxxxxxxxxx xxxxxx, xx by xxxxxxxx xxxxxx xxxxxxxxx vstupující xx legálního dodavatelského xxxxxxx xxxxx xxxxxxxx xx xxxxx xxxxx Xxxx, xxxxx xx xxxxxx xxxxxxx v xxxxxxxx xxxxxx xxxxxxxxxx. Xxxxx oprávněná x xxxxxx xxxxxxxx xxxxxxxxx xxx xxxx xxxxxxx xxxxxxxxxx ověří xxx xxxxxxxx prvky x xxxxxxx vyřazení xxxxxxxxxxx xxxxxxxxxxxxxx xx systému xxxxxxx x xxxxxxxx xxxxxx xxxxxxxxxx.
Xxx zajištění xxxxxxxx xxxxxxxx xxxxxxxxx x xxxxxxxx xxxxxxxxxx xxxxxxx je xxxxxxxx xxxxxx xxx xxxxxxxx xxxxx. Ověření xxxxxxxx xxxxxxxxxxx identifikátoru xx xxxxx xxxxxxxx xxxxxxxxx xx xxxxxxx xxxx xxxxxxxxxx s xxxxxxxxxxxxxx xxxxxxxxx v systému xxxxxxx x xxxx xxxxx je xxxxxxxx, xx xxxxxx xxxxxxxxx xxxxxxx xx legitimního xxxxxxx, xxxxx xxxxxxxxx xxxxxxxxxxxxxx xxxxxx xx xxxxxxx xxxxxxx. Ověření xxxxxxxxxxxxx prostředku x xxxxxxx manipulace x xxxxxx bude xxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxx xxxxxxxx xxxxxxxxx x xxxx xxxxx je xxxxxxxx, že s xxxxxxx xxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxxxxx nikdo xxxx před pacientem, xxxxxxx xxxx balení xxxxxxxx xxxxxxxxx xxxxxx.
Xxxxxxxxxxxx xxxxxx xxxxxx, x xxxxxx xx xxxxx xxxxxxx xxxx xxxxxxxxxx xxxxxxx spočívající xx xxxxxxx x xxxxxxxxxx xxxxxxxxx xxxxx, xxxxx:
- Xxxxxx xxxxx pro xxxxxxxx xxxxx jako xxxxxxxxx vnitrostátní orgán, xxxxx bude xxx xxxxxxx k úložišti xxx xxxxx xxxxxx xxx fungováním úložišť, xxxxxxxxxxx potenciálních případů xxxxxxxx, xxxxxx, xxxxxxxxxxxxxxxx x xxxxxxxxxxxxxxxxxxxx.
- Xxxxx xxxxxxxxx xxxxxx rozšiřovat xxxxxx působnosti jedinečného xxxxxxxxxxxxxx xxxx prostředku x xxxxxxx manipulace x obalem xx xxxxxxx xxxxx léčivé xxxxxxxxx v xxxxxxx x xxxxxxx 54x xxxx. 5 xxxxxxxx 2001/83/XX (čl. 2 odst. 1 písm. c) xxxxxxxx x xxxxxxxxxx xxxxxxx).
- Xxxxx republika xxxxxx xxxxxxxxx, aby xxx XXXX byl xxxxxx x xxxxx xxxxxxxxxxx identifikátoru, xxx., xx xxxx xxxxxxxx xxxxxxxxx xxxx, kdy xxx SÚKL je xxxxxx xx xxxxx xxxxxxxxx.
- Česká republika xxxxxxx článek 23 xxxx. x) xxxxxxxx x xxxxxxxxxx prvcích x xxx xxxxxx xxxxxxxxxx xxxxxxxxxxxxxx xxxxxxxx xxxxxxxxx xxx nepovinná očkování xxxxxxx x xxxxxxxxx xxxxxxxxxxx pojištění x xxxxxxxx pro xxxxxxxx xxxxxxxxxxxxx osob xx xxxxxxx xxxxxxx xxxxxxx Xxxxxxxxxxxx xxxxxxxxxxxxx x xxxxxxxxxxxxx.
Xxxxxxxx xxxxx xxxxxxxxxx xxxxxxx xxxxxxxxx pravosti xxxxxxxx xxxxxxxxx xx xxxxx xxxxxxxx vstupu xxxxxxxxxx xxxxxxxx xxxxxxxxx xx legálního xxxxxxxxxxxxx xxxxxxx x následně xxxxxxxxxx riziko potenciálního xxxxxx padělaných xxxxxxxx xxxxxxxxx xxxxxxxxx x xxxxxxxxx x tím xxxxxx ochranu xxxxxxxxx xxxxxx. Ucelený systém xxxxxxxxx xxxxxxxx léčiv xx xxxxxx xxxxxxx, xxxxxxxxxxxx xxxxx xx xxxxx oprávněné x xxxxxx léčivých xxxxxxxxx xx xxx být xxxxxxx zachytit téměř xxxxxxxxx výskyt xxxxxxxxxx xxxxxxxx xxxxxxxxx x xxxxxxxx xxxxxxxxxxxxx xxxxxxx. Xxxxxxxx xxx xxxxxxxxxxxx, xx xxxxxxxxx evropského xxxxxxx ověřování pravosti xxxxxxxx xxxxxxxxx bude xxxxxxx xxxxxxxxxxx xxxxxxxx xx xxxxxxxxxxx padělatele.
1. 6 Xxxxxxxxxx xxxxxx
X xxxxxxx xxxxxxxxx xxxxxxxxxx xxxxx, tj. xxxxxxxxx xxxxxxxx xxxxxxxxxxxxx s xxxxxxxx xxxxxxxx xxxx Xxxxx xxxxxxxxx xx xxxxxxxx x xxxxxxxxxx xxxxxxx xx xxxxxxxxx xxxxxxx to, xx xxxxxxxxxxxx xxxxxxxx předpokladů xxx xxxxxxxxx řádného xxxxxxxxxx, používání a xxxxxxxxx xxxxxxxxxx prvků xx xxxxx xxxxxxxxx xxxxxxxx přípravků v Xxxxx republice, xx xxxxxxx k potřebnému xxxxxxx bezpečnosti xxxxxxxx xxxxxxxxx, xxx xx xxxxx vést x xxxxxxxx zásad xxxxxxx xxxxxxxxx xxxxxx, x xxxxx xx xxx xxxxxxx xxxxxxxxxxxxxx xxxxxxx xxxx x xxxx xxxxxxxxx citlivé xxxxxxx x důsledku xxxxxxxxx xxxxxxxx xxxxxxxx účinkům xxxxxxxxxx xxxxxxxx xxxxxxxxx.
Xxxxxxx x České xxxxxxxxx xxxxx zaznamenán xxxxxx xxxxxxxxxx léčivých přípravků xxxxx v xxxxxxxxx, xxxxxxxx xxxxxx xxxxxxxxx xx xxxxxxxxx v xxxxxxxxxxxx xxxxxxx x xxxxxxxx.&xxxx; Xxxxxxx xxxxxx xxxxxxxxxx xxxxxxxx přípravků x xxxxxxxx xxxxxxxxxxxx xxxxxxx, xxxxxxxxxxx 1. xxxxxxxx xxxx k xxxx, xxx se xxxxxxxx léčivý xxxxxxxxx xxxxxx xx lékárny x xxx xxxxxxxx xxxxx xxxxxxxxxx. Xxxxxxxxxxx xxxxxx výskytu xxxxxxxxxx xxxxxxxx přípravků x xxxxxxxx distribučním xxxxxxx, xxxxxxxxx xx xxxxxxxxxx, xx dosavadní systém xxxxxxx xxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx je xxxxxxxxxxxx x xx xxxxxxx xxxxx a xxxxxxxx xxxx, xxx xx xxxxxxxx xxxxxx xxxxxxxxx xxxxxxx k xxxxxxxxx.
Xxxxxxxxx xxxxxx xxxx xxxxxxxx pouze v xxxxxxx, xxx všechny xxxxxxx subjekty a xxxxxxxxxxxx příslušné xxxxxx x členské xxxxx XX xxxxx plnit xxx povinnosti xxxxxxxxxxx x xxxx xxxxxxxxx xxxxxxxx předpisů EU.
Nezanedbatelným xxxxxxx xx xxxx xxxxxx xxxxxxxxxxx nepřijetí xxxxxxxx xxxx xxxxxxxx xxxxxxx x založení Xxxxxxxx xxxx ze xxxxxx členského xxxxx x xxxxxxxx xxxxxx xx strany Evropské xxxxxx xxxxx Xxxxx xxxxxxxxx xx xxxxxxxxx xxxxxxxxxxxxx povinnosti x xxxxxxxxx x xxxxxxx xxxxxx adekvátní xxxxxxxx xxxxxxxx, xxxxx xx xxxx xxxxx xx xxxx systém x xxxx xxxxxxxxx xxxxxx xxxxx v xxxxxxx Xxxxx xxxxxxxxx, ale x xxxxxxxxx xxxxxxxxx xxxxx, xxxxx jen x případě, xx xxxxxxxx xxxxx xxxxxxxxxx xxxxx, bude xxxxxx xxxxxxx.
Xxxxxxxxx xxxxxx navrhované xxxxxx xxxxxx xxxx xxxxxxxxx xxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx xx xxxxxxxxx xxxxxxxxxxxxxx xxxxxxx, x xxxx ochrana xxxxxxxx. Xxxxxxxxx xxxxxxxx xx xxxxxxx xxxxxx xxxxxxxxxxxxxxx subjektů, protože xxxxx x xxxxxxxxx xxxxxxxxx xxxx xx xxxxxxxxxx léčivých přípravků, xxxxxxx xxxxxxxxx x xxxxxxxxxx xx legálního xxxxxxxxxxxxxx řetězce xxxxx xxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxx xxxxxx xxxxxx.
2. Návrh xxxxxxx xxxxxx
2. 1 Xxxxxxxx regulatorně-technického řešení
Při xxxxxxxxx různých xxxxxxx xxxxxxxxxxxxxxxx xxxxxxxx x xxxxxxxx (xxxxxxxxxxx-xxxxxxxxxxx) xxxxxxxx, xxxxx by mohly xxxx xx xxxxxxxxxxx xxxx, bylo zvažováno xxxxx předkládané xxxxxx x podobě návrhu xxxxxx zákona o xxxxxxxx, xxxxx problematiku xxxxxxxxx x xxxxxxxx x xxxxxxxxxx xxxxxxx xx xxxxxxxx řádu Xxxxx republiky lze xxxxxxxxx xxxxx novelou xxxxxx zákona, xxxx xxxxx xxxxx xxxxx xxxxxx xxxxx xxxxxxx xxxx padělanými léčivými xxxxxxxxx již xxxxxxxx. Xx xxxxxx, xx xxxxxxxxxxxxxx xxxxxxx xx xxxxx xxxxxxx pouze xxxxxxxxxxxx formou. Xxxxxx xxx xxxxxxxxxx zkušeností x aplikační xxxxx xxxxxx x léčivech xx xxxxx xxxxx xxxxxx xxxxxx tohoto xxxxxx. Konkrétní věcné xxxxxx xxxxxx xxxxxxxx xxxx xxxxxxx xxxx, xxxxxxxx xxxx variantu xxxxx xxxxxxxxxx.
2. 2 Xxxxxxxx věcného xxxxxx
2.2.1 Xxxxxxxx 1 (xxxxxx)
Xxxxxxx xxxxxxxxx xx xxxxxx xxxxxxxxxxxx xxxxxx xxxxxx, xxxxx by xxxxxxx xxxxxxxxxx, xxxxx xxxxxxxx x xxxxxxxxxx xxxxxxx xxxxxxxxx v působnosti xxxxxxxxxxxx xxxxxxxxx xxxxx x xxxx xxxxxx xx xxxx xx xxxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxx přímo xxxxxxxxxxxx xxxxxxxx Xxxxxxxx unie. X xxxxxxx na xxxx xxxxxxx xxxxxxxx x xxxxxxxxxx xxxxxx xx xxxxxxxx 1 xxxxx teoretická x „xxxxxxx xxxxxxxx“ xxxxx xxxxxx.
2.2.2 Varianta 2 (xxxxxxxx xxxxxx platného xxxxxx)
Xxxx varianta xxxxxx xx xxxxxxx xxxxxxxx, xxx vyhovět požadavkům xxxxxxxxxxxx xxx xxxxxxxxxx xxxxxxx státy x xxxxx použitelného xxxxxxxx Xxxxxxxx xxxx, xxxxx xxxxxxxxxxx xxxxxxxx x xxxxxxxxxx xxxxxxx.
Xxxxx xxxx xxxxxxxx xx xxxxxxxxxxx xxxxxxxxx x xxxxxxxxx xxxxx xxxxxx platného xxxxxx o xxxxxxxx, xxxxxx xx budou xxxxxxxxx xx xxxxxxxxxx xxxxxxxx x xxxxxxxxxx xxxxxxx, xxxxx xxxx xxxxxxxxx v působnosti xxxx na xxxxxxx xxxxxxxxxxxx xxxxxxxxx xxxxx. Xxxxxxxx k právní xxxxxx xxxxxxxx spočívající x xxxx xxxxxx xxxxxxxxxx x přímé xxxxxxxxxxxxx xx varianta 2 xxxxxx x xxxxxxx s právem Xxxxxxxx xxxx.
Xxxxxxxx xx, xxx x Xxxxx xxxxxxxxx byl příslušným xxxxxxxxxxxxx xxxxxxx dle xxxxxxxx x ochranných xxxxxxx Xxxxx, x xx zejména s xxxxxxx xx xxxxxxxxx xxxxxx xxxxxx xxxx xxxxxxxxxx xxxxx xxxxxxx x xxxxxxxx, jako xxxxxxxxx xxxxxxxx xxx xxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx. Z xxxxxx xxxxxx je xxxxx xxxxxxxx xxxxxxxxx Xxxxxx xxxxxxxxxx x §13 xxxxxx x léčivech. Xxxxx xxx xxxx xxxxx xxxxxxxxxx stanovené x xxxxxxxx XX xxxxxxxx o ochranných xxxxxxx. Zejména xxxxx x xxxxxxxxxxxx informací xxxxxxxxx xxxxxxxxxx, xxxxxxxx, xxxxxxxxxxxxx x osobám xxxxxxxxxx xxxx xxxxxxxxx xxxxxxx léčivé xxxxxxxxx xxxxxxxxxx, o léčivých xxxxxxxxxxx xxxxxxxxx xx xxx xx území Xxxxx xxxxxxxxx, které xxxx xxx opatřeny xxxxxxxxxx xxxxx (x xxxxxxx x xxxxxxx 54 písm. x) xxxxxxxx 2001/83/ES). Xxxxx xxxx xxxxxxxxx xxxxx xxx xxxxxxxxxx xxxxxxxxx xxxxxxxx x Xxxxx xxxxxxxxx, aby xxxxxx, x případě xxxxxxx xxxxxxxxxxxxxxx inspekcí, xx xxxxxxxx a xxxxxx xxxxxxx xxxxxxxxx xx xxxxxxx a xxxxxx xxxxxxxx splňuje xxxxxxxxx xxxxxxxx. Zprávy x xxxxxxxx činnosti xxxx xxxxxxxx Xxxxxxxx xxxxxxxx xxx léčivé xxxxxxxxx, xxxxx xx xxxxxxxxxx xxxxxx xxxxxxxxxx xxxxxxxxxxxxx xxxxxxx a Komisi.
Obecnou xxxxxxx xxxxx xxxxxxxxx x ochranných xxxxxxx xx xxxx xxx, xxx x uceleném xxxxxxxxxx systému vyřazení xxxxxxxxxxx xxxxxxxxxxxxxx xx xxxxxxx xxxxxxx xxxx xxxxxxxxx xx xxxxx xxxxxxxxxxxxxx řetězce, xx. xxx je xxxxxx xxxxxxxxx vydán xxxxxxxxxx. Xxxxxxx stát xx xxx xxx zohlednit xxxxxxxx xxxxxxxxxxxxxxx xxxxxxxxxxxxxx xxxxxxx xx svém xxxxx x xxxxxxx xx xxx právní xxxxxx, aby distributor xxxxxx ochranné prvky x xxxxxxx xxxxxxxx xxxxxxxxxxx identifikátoru xxxxxxxx xxxxxxxxx před xxx, xxx léčivý xxxxxxxxx xxxx xxxxxxx z xxxx xxxx xxxxxxxxx xxxxxxxxx x článku 23 nařízení o xxxxxxxxxx xxxxxxx. V xxxxx Xxxxx republiky xxx xxxxxx xxxxxxx xxxxxxx 23 nařízení x xxxxxxxxxx xxxxxxx, xx. xxx xxxxxxx xxxxxxxxxx xxxxx x xxxxxxxx xxxxxxxxxxx identifikátoru xx systému xxxxxxx xxxxxxx xxxxxxxxxxx, použít xxxxx v xxxxxxx xxxxxxx xxxxxxxx xxxxxxxxx
- xxxxxxxxxxxx lékařům,
- Xxxxxx Xxxxx republiky x xxxxxxxxxxx xxxxxxxxxxx xxx xxxxxx, x udržování xxxxxxxxxx xxxxx xxxxxxxx xxxxxxxxx xxx xxxxx xxxxxxxxxxx xxxxxxxxxxx xxx Xxxxx republiky xxxxxx xxx xxxxxx xxxxxxxx xx xxxxxxxxx xxxxx §111a zákona x xxxxxxxx a
- xxxxxxxxxxxxxx xxxxxxxxxxx xxxxxx, xxxxxx xxxx xxxxx §77 xxxx. 1 písm. x) xxxx 12 xxxxxxxx xxxxxxxxxxxx xxxxxx xxxxxxxxx xxx xxxxx xxxxxxxxx pravidelného xxxxxxxx xx základě rámcové xxxxxxx xxxxxxxxxxxx se xxxxxxxxx xxxxxxxxxxx xxxx xxx xxxxx povinného xxxxxxxxxx x xxxxxxxxxxx xxxxxxxx a očkování xxxxxxxxxxxxx xxxx&xxxx; xx xxxxxxx xxxxxxx xxxxxxx xxxxxxxxxxxx x Xxxxxxxxxxxxx xxxxxxxxxxxxx&xxxx;&xxxx; x nepovinného xxxxxxxx hrazeného z xxxxxxxxx xxxxxxxxxxx xxxxxxxxx x rámci xxxxxxxxxxx xxxx dle xxxxxx č. 48/1997 Sb., x xxxxxxxx xxxxxxxxxx xxxxxxxxx x x změně x xxxxxxxx některých xxxxxxxxxxxxx xxxxxx, xx znění xxxxxxxxxx xxxxxxxx.
X xxxxxxx xxxxxxxx uvedených v článku 23 xxxxxxxx x xxxxxxxxxx xxxxxxx, xx x podmínkách Xxxxx xxxxxxxxx xxxxx x xxxxxxxxxxxxx xxxxxxxxxxx xxxxxx, xxxxx xxxx xxxxxxx xxxxxxxxxx na základě xxxxxxxxx podle zákona č. 372/2011 Sb., o xxxxxxxxxxx xxxxxxxx a xxxxxxxxxx xxxxxx poskytování, xx xxxxx xxxxxxxxxx xxxxxxxx (xxxx jen „xxxxx x zdravotních službách“) x xxxxxx xxxxx xxxxxx x xxxxxxxx xxxxxx xxxxxxxxxx x xxxxxx xxxxxxxx přípravků, x xxxxx nemohou xxxxxxxx xxxxx u xxxxxxxx xxxxxxxxx ověřit. Xxxx subjekty si xxxxxxxx v xxxxxxx xx zákonem x xxxxxxxx xxx xxxxx xxxxxxxxxxx zdravotní péče xxxxxx xxxxxxxxx xx xxxxxxxxxxxxx lékárenské xxxx xx xxxxxxx/xxxxxxxxxx. Poskytovatelé xxxxxxxxxx péče, jako xxxxx xxxxxxxxx x xxxxxx, x těchto xxxxxxxxx xxx výdeji xx xxxxxxx xxxxx xxxxxxxx xxxxx a xxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx xx xxxxxxx xxxxxxx. X podmínkách Xxxxx republiky x xxxxxxx optometristů, optiků, xxxx x xxxxxxxxx x xxxxxxx xxxxxxxxx xxxxxxxxxxxxxxx xxxxxxxx, xxxxx xxxxxxxxx xxxxxx přípravky xxx účely xxxxxxx x vzdělávání, xx xxxxxxx o xxxxxxxxxxxxx xxxxxxxxxxx služeb xxx xxxxxx x xxxxxxxxxxx xxxxxxxx x xxx x xxxxx xxxxxxxxx x výdeji xxxxxxxx xxxxxxxxx dle xxxxxx x léčivech, proto xx xx ně xxxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxx prvky xxx xxxxxxxx o xxxxxxxxxx xxxxxxx. Xxxxxxxx xxxx xxxxxx xxxxxx pro xxxxx subjekty xxxxxxx x xxxxx xxxxxx xx xxxxxxxxx zásadní xxxxx x xxxxxxxxx xxxxxx úpravě xxxxxxxxxx xxxxxxxx oprávněné k xxxxxx léčivých přípravků. Xxxx xxxxx xx xx xxxxxx několika xxxxxxxx předpisů, xxxx xx xxxxx rozsáhlá x xxxxx xx xxx xxxxxxxxxxx xxxxx x xxxxxxx, xx xx xxxxxx x xxxxxx x xxxxxx xxxxxxx XX xxx xxxxxx léčivých přípravků.
V xxxxxxxx roku 2009 xxxxx v XX xx změně xxxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxx (ne xxx xxxx xxxxxxx xxxxxxxxxx stanice, xxx xxxx distribuční xxxxx), x xx xx xxxxxxx xxxxxx zákona č. 48/1997 Sb., x veřejném xxxxxxxxxx xxxxxxxxx x x xxxxx x xxxxxxxx xxxxxxxxx xxxxxxxxxxxxx xxxxxx, a x xxx související xxxxx xxxxxx č. 258/2000 Sb., x xxxxxxx xxxxxxxxx zdraví x x změně xxxxxxxxx xxxxxxxxxxxxx xxxxxx. X xxxxx zachování xxxxxxxxxxx xxxxxx xxxxxxx xxxxxxx imunologických xxxxxxxxx xxxxxxxxxxxxx xx xxxxxxxx xxxxxxxxxxxxx zdravotních xxxxxx, xxx povinnosti xxxxxxxxxxx x xxxxxxxx x xxxxxxxxxx xxxxxxx xxxxxxx xx xxxxxxxxxxxx imunologických xxxxxxxxx x xxxxxxxx článku 23 xxxx. x) xxxxxxxx o xxxxxxxxxx xxxxxxx, x xx xxxxx pro xxxxx xxxxxxxxx pravidelného, xxxxxxxxx xxxxxxxxxxx a xxxxxxxxxx xxxxxxxx, xxxxxxxx xxxxxxxxxxxxx xxxx x xxxxxxxxxxx xxxxxxxx xxxxxxxxx z xxxxxxxxx xxxxxxxxxxx xxxxxxxxx. Xxxxx xxx xxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxx xxxx xxxxx xxxxxx článku 23 xxxx. x) xxxxxxxx x xxxxxxxxxx xxxxxxx a x xxxxx xxxxxxx xxxxxxxx xxxxxxxxxx imunologických xxxxxxxx xxxxxxxxx do xxxxxxxx xxxxxx. Xxxxxx xx v těchto xxxxxxxxx zajistí imunologické xxxxxx xxxxxxxxx xxxxxxxxxxxxxxx xxxxxx xx xxxxxxx xx xxxxxxxxxxxxx lékárenské xxxx. V xxxxxxx xxxxx nevyužít možnost xxxxxxxxxx článkem 23 xxxx. x) xxxxxxxx x xxxxxxxxxx xxxxxxx xx xxxxxxxxxx xxxxxxxxxxx x xxxxxxxx x xxxxxxxxxx xxxxxxx, tj. xxxxxxxxx xxxxxxxxxx x xxxxx x xxxxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx u xxxxxxxxxxxxxx xxxxxxxx přípravků, xxxxx xxxxxxxx xxxxxxxxxxxx zdravotních xxxxxx, xxx xx xxxxxxxxxxxxx pro lékaře xxxxx xxxxxxxxxxxxxxx zatížení. Xxxxx xx xx xxxx xxxx zajistit xxxxxxxxxxxx xxxxxx xxxxxxxxx xx xxxxxxx xxxxxxxxxxxxxxx xxxxxxx, xxx by xxxxxxx xxxxxxxxxx xxxxx x xxxxxxxx jedinečného xxxxxxxxxxxxxx xxxxxxx xxxxxxxxxxxx xxxxxxxxxx péče (xxxxxxx) xxxx xxxxx oprávněná x xxxxxx léčivých xxxxxxxxx, xxxxxxx xxxx xx vedlo k xxxxxxxxx xxxxx xxxxxxx xxxxxxxxxxx xxxxxxx a xxx xxxxxxxx xxxxxxx xxxxxxxxxxxx, xxxxxxxxxxx a xxxxxxxxxx x xxxxxxxxxxx xxxxxxxxx očkování.
Dále xx xxxxxxxx doplnit xxxxx x xxxxxxxx x xxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxxxxx xx vymezení xxxxxxx porušujících xxxxxxxxxx xxxxxxxxx xxxxxxxxx x xxxxxxxxxx xxxxxxx. K xxxx Xxxxx xxxxxxxx xxxxxxxx 2001/83/ES, xx xxxxx xxxxxxxx 2011/62/EU, xxxxx xxxxxx xxxxxxxx xxxxxx xxxxxxxxx xxxxxxxx xxxxxx xx xxxxxxxx xxxxxxxxxx x xxxx xxxxxx musí být xxxxxx, xxxxxxxxx x xxxxxxxxxx (čl. 118x xxxxxxxx 2001/83/ES). Sankce xxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx zdraví, xxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx. X xxxxxxx xx závažnost xxxxxxxx xxxxxxxxxxxxx xxxxxxx a x xxxxxxx na xxxxxxxxx výše xxxxxx xxx v xxxxxx x léčivech stanovených x xxxxxxxxxxxxx xxxxxxxxxx xxxxxxx xxxxxxxxxxxxx jednání xxxx, xxx xxxxxxxx xxxx sankcí nepřipadají x xxxxx. Xxxxxx xxxxxxxxx či xxxxxxxxxx xxxxxxxxxxx xxxxxxx padělku xxxxxxxx xxxxxxxxx na xxxxxx pacientů xxxxx xxx xxxxxxx. Xxxxxxxx xxxxxx xxxxxxxxx xx xxxxxxx xxxxxxx, xx xxxxxxxxx původu x xxxx xxxxxxxx xxxxxxxx xxx xxxxx xxxxxxx, xxx neúčinností, xxxxxxxx x xxxxxxxxxx xx xxxxxxx či škodlivé xxxxx xxxxxxxx x xxxxxxxxx léčivém xxxxxxxxx, xxxxx xxxxxxxxxxxx standardní xxxxxxxxx jakosti, xxxxxxxxx x xxxxxxxxxxx x xxxxx výroby xxxxx xxx x rámci xxxxxx o registraci xxxxxxxx xxxxxxxxx.
Xxxxxxxx x xxxx, xx xxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxxx xxxxxxxxxxx xxxxxxx, xx xxxxxx xxxxxxxxxxxxx xxxxx xxx nyní xxxxxxxx xxxxxxxxxx xxxxxxxxx x xxxxxxxxx xxxxxx xxxx. Xxx 28. xxxxxxxx 2010 xxxxxxxx Xxxxx xxxxxxxx ministrů Xxxx Xxxxxx Úmluvu o xxxxxxxx léčiv a xxxxxxxxx trestných xxxxxx, xxxxx ohrožují veřejné xxxxxx (XXXXXXXXX). X xxxxxxx xxxx otevřena 28. xxxxx 2011, xxxxxxx Xxxxx xxxxxxxxx xxxxxx dosud nepodepsala x xxxxxxxxxxxxxx. Xxxxxxxxxx Xxxxxx si xxxxxx xxxxxxxxxx trestního xxxxxx. Xxxx xx xxxx xxx xxxxxxxxx skutkové xxxxxxxx xxxxxxxxx xxxx xxxxxxxxxxx xxxxxxxxx x xxxxxx a xxxxxxxxxxxxxx xxxxxxxxxx. Xxxx Xxxxxx xxxxx xxxxxx xxxxxxxx x xxxxxxxxx, xxx xxxxx xxxxxxxxxxx xxxx xxxxxxxxxxx x xxxxxxxxx xxxxxxxx xxxxxxxxx, xxxxx xxxxxxxx zdraví x xxxxxx xxxxxxxx.
Xxxxxxxx x xxxxxxxxxxx xxxxxxxxx xxxxxx xx oblasti xxxxxxxxx xxxxx xxxxxxxxxxxx zavádí xxxxxx xxxxxx za xxxxxxxx právních xxxxxxxxxx xx úrovni xxxxxxxxx xxxxxxxx. Xxxx xxxxxx xxxx xxxxxxx xxxxxxxxx xxxxxx xxxxxxxxxx xxxxxxxxxxx xxxxxxxxx. Xxxxxxx xxxxxxxxxxxx xxxxxxxx navržené xxxxxxxxx xxxx xxxxx xx xxxxxx, xxxxx vzhledem xx xxx výši x xxxxx xxxxxxxxxx. Xxxxxxxxxxx je xxxxxxxx xxxxxxxxxx xxxxxx spočívajícím x xxxxxxxx xxxxxxxxx xxxxxxx xxxxxxxxx xxxxxx xxx posuzování společenské xxxxxxxxxxxxx xxxxxxx xxxxxxx xxxxxxxxxxxxx jednání, xxxxx xxxx Xxxxxxx x xxxxx správních řízení xxxxxxxxxx, xxxxx x xxxxxxxxxxx xxxxxx xxxxxxxxx xxxxxx (xxxxx likvidačních xxxxx).
3. Xxxxxxxxxxx xxxxxxx x xxxxxxx
3. 1 Xxxxx xxxxxx xxxxxx xxx xxxxxxxxxxx a xxxxxxxx dopady xx xxxxxx rozpočet x xxxxxx xxx žádné xxxxxx na xxxxxxx xxxxxxx xxxxxxxx.
3. 2 Xxxxxxx
Xxxxxxxxxx úpravy za xxxxxx xxxxxxxxx adaptace xxxxxxxx x ochranných xxxxxxx xxxxxxx představovat xxxxxxxx xxxxx xxxxxxxxxxx x navýšení xxxxxx xxxxxxxxxxxxxxx míst včetně xxxxxxxxxx xx xxxxx xxx xxxxxxxxx xxxxx xxxx systemizací xxxxxxxxxx x pracovních xxxx xx služebních úřadech xxxxxxxxxxx xxx rozpočtovou xxxxxxxx Ministerstvo zdravotnictví, xxxxxxxxx xx xxxxxx Xxxxxx.
Xxxxxx xx xxxxxxx xxxxxxx xxxxxxxx xx xxxxxxxxxxxxxxx.
Xxxxxx xx xxxxxxxxxxxxx xxxxxxxxx České xxxxxxxxx xx váží x xxx xxxxxxxxxxx xxxxxx x xxxxxxxx, xxxxx xx něho byla xxxxxxx jeho xxxxxxx, xx. xxxxxxx č. 70/2013 Sb., x xxxx xxxxxxxxx xxxxxxxx, xxxxxxxx xx xxxx xxxxx x xxxxxxxx x xxxxxxxxxx xxxxxxx. Xxxx xxxxxx xxx xxxx xxxxxxxxx xxx xxxxxxxxxxxx xxxxxx xxxxxxxx xxxxxxxx. X xxxxx xxxxx xx xxxxx odkázat xx xxxxxxxxx zprávu, včetně xxxxxx o xxxxxxxxx xxxxxx regulace (XXX) x xxxxxx č. 70/2013 Sb. x xxxx xx xxxxxxxxx zprávu RIA x xxxxxxxx x xxxxxxxxxx prvcích označenou „Xxxxxx Xxxxxxxxxx“. V xxxx podrobné zprávě xx uvádí, xx x xxxxxxx x čl. 4 xxxxxxxx 2011/62/XX x xx. 54x xxxx. 2 x 3 směrnice 2001/83/XX Xxxxxx xxxxxxxxx xxxxxxx, xxxxxxx a nákladovou xxxxxxxxxx xxxxxxx xxxxxxxx xxx xxxxxxxxxxxxxxx x xxxxxxxxx xxxxxxxxxxx jedinečného xxxxxxxxxxxxxx a způsoby xxxxxxx ochranných prvků x xxxxxxxx x xxxxxx xxxxxxx úložišť. Xxxxxxxx, xxxxx xxxx xxxxxxxxxxx jako xxxxxxxxx xxxxxxxxxxxxxxx, představují základní xxxxx xxxxxxxx x xxxxxxxxxx xxxxxxx.
Xxxxxx xxxxxxxxx xxxxxxxxxxxx xxxxxxxx x xxxxxxxxxx xxxxxxx xx xxxxxxx všech osob xxxxxxxxxxxxx x léčivými xxxxxxxxx, počínaje xxxxxxx, xxxxx xxxx xxxxxxxx xxxxxxxx a xxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx x xxxxxxxxxx x ověření xxxxxxxxxx x obalem x činnosti x xxxxxx úkony xxxxxxxxxxx xxxx na xx xxxxxxxxxx. Platí však, xx xxx xxxxxxx xxxxxxxx o xxxxxxxxxx xxxxxxx v xxxxxxxx (xxxx 2015) xxxxxxx xxxxxxxxx dotčených xxxxxxxx xxxxxxxxx xx na xxxxx tohoto xxxxxxxx x účinnost xxxx 9.2.2019. Dále xx xxxxxx distributorů, xxxxxxxx xxxxxxxxxx x registraci, xxxxxxxx povolení xxxxxxxxxx xxxxxx x xxxxxxxxxxxxx xxxxxxxxxxx služeb xxxxxxxxx x xxxxxx léčivých xxxxxxxxx, xxxxx budou xxxxx xxxxxxx svoje xxxxxxxx xxxxx, xxxxxxxxx xx v xxxxxxx XX xxx, xxx xxxx xxxxxxx xxxxx xxxxxxxxxx xxx xxxxxxxxx x nařízení o xxxxxxxxxx xxxxxxx a xxxxxxxxxxx xx systémem xxxxxxx.
Xxxxxxx xxxxxxxxx xxxxxxxxxx xxxxx a xxxxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx xxxxxxx xxxx náklady xx xxxxxx xxxxxxxxxxxxx xxxxxxx, xxxxx v xxxxxx xxxxxxx, xxxxxx xxx xxxx dopady xxxx xxxxxxxxxx xx xxxxxxxx xxxxxxxxxxxx provozovatelů xxxxxxx. X xxxxxx xxxxxxxxx x xxxxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx budou xxxxx xxxxxxxxxxxxx xxxxxxx xxxxxxx xxxxxxx (xxxxxxxx zařízení xxxxxx xxxxxxx), které xxxxx xxxxxxx xxxxxxxxxx xxxxxxxx xxxx xxxxx xxxxxxx xxxxxx x xxxxxxxx 2D xxxx, xxx xxxxxxxxxxx xxxxxxxxxxxx xxxxxxxxx xxx 5.000 - 7.500,- Xx xx xxxxx snímač (xxxxxxxx). Xxxxx xxxxxxxx, xxxxxx xx xxxxxxxxx x internetu, žádné xxxx náklady xxxxxxxxxx, xxxxx xxx xxxxxxx xxxxxxx disponují (x xxxxxxx, že xx xxxxxxxxxxxxx, xxxxxxx by xxxxxxx léčivé xxxxxxxxx xx xxxxxxx elektronické xxxxxxxxxx, xxxxxxx xx xxxx xxx většina). Xxxxx xx xxxxxx xxxxxx xxxxxxxx, xx. xxxxxxxxxxxx xxxxxxxxxxxx xxxxxxx. Xxxxxxx xxxxxxx xx xxxxxxxxxxx lékárenského systému xxxxxxxxx xx xxxxxxxxxx xxxxxx, xxxxxxx xx x činnost xx xxxxxxx, xxx nastavení xxxxxxxxxxxx xxxxxx xxxxxxxx (xxxxxxxxxx XX xxxx xxxxxxxx produkty xxxxxxxxx xxxxxxxx xxxxxxxxx až xxxxxxxx xxxxxxx). Xxxxxxxxxx xxxxxxxx HW xxxxxxxx xxxxxxx a xxxx x souvislosti x xxxxxxxxxx prvky xx xxxx xxxxx xxxxxxx xxxxxxx xxxxxxxxxxxx lékáren (xxxxx objem léčivých xxxxxxxxx, xxxx xxxxxxxxx xxxxxx, výdeje xx xxxxxxx x xx xxxxxxx xx oddělení), xxxxx platí x xxxxxxxxx xxxxxxxxxxx xxxxxxxx x xxxxxx xxxxxxx xxxxxxxx (změna xxxxxxx xxxxx, ověřování každého xxxxxxxxxxxx xxxxxx při xxxxxx, xxxxxxxxxx x xxxxxxxxxx x Xxxxxxx x případě xxxxxxxxxx xxxxxx xxxxxxxxx xxxxxxxxxxxxx).
Xxxxxxxx x xxxx xxxxxx xxxxx přesně odhadnout xxxxxxxx xxxxxxx xxxxxxxxxxxxx xxxxxxx, Xxxxx xxxxxxxxxx xxxxxx xxxxxxxxx xxxxxxxxx xxxxx náklady xxxxxxx x xxxxxxxxxxx x xxxxxxxxxx xxxxxxxxxx prvků xx xxxxxxx xxxxxxxx xxxxxxxxx na částku 500 xxx. Kč. X xxxx částce xxxx xxxx zahrnuty xxxxx xxxx xxxxxxxxx x xxxxx xxxxxxx, xxxxx xxxxxxxxxxxx považuje xx xxxxxxxxxxxx xx xxxxxxxxxxxx (xxxxxxx xx xxxxxxx zaměstnanců, vyšší xxxxxx xxxxxxxxx výdeje - menší xxxxx xxxxxxxxxxxx xxxxxxxx), xxxxxxxxx xxxxxxx xxxxx s xxxxxx xxxxx pravděpodobnosti xxxxx.
Xxxxxxxx xx xxxxxxxxxxx, xx po 9.2.2019 xxxxx na trhu xxxxxxxx xxxxxx xxxxxxxxx, xxxxx xxxxxxx opatřeny xxxxxxxxxx prvky x xxxxx byly xxxxxxxxxx x xxxxxxx nebo xxxxxxxxxx xxxx nabytím xxxxxxxxx xxxxxx zákona, xxxxxxxx xxxxxxxxxxxx x xxxxxx právní xxxxxxx xxxxxxxx xxxxxx xxxxx xx nezbytné x xxxxxxx s xxxxxxxxx x ochranných xxxxxxx xxxxxxxxxxxx xx xxxxxx xxxxxxxxx xxxxxxxxxx, xxxxx xxxxxxx xx xxxxx, xx tyto xxxxx xxx xxxxxxx, xxxxxxxxxxxxx x vydávány xx xx xxxxxxxx xxxx xxxxxx xxxxxxxxxxxxx.
Xxxxx xxxxxxxx xxxxxx xxxxxx mohou x xxxxxxxxx xxxxxxxxx xxxxxx (xxxx. jiní xxxxxxxxxxxx xxxxxxxxxx) xxxxxxxxxxxxx xxxxxxxxxxxxxx zařízení xxxxxxx xxxxxx xxxxxxxxx (v xxxxxxx x xxxxxxxxxxx §82 xxxx. 2 xxxxxx x xxxxxxxx). Xxxxxxxx x xxxx, xx xxxxxxxxxxxx xxxxxxxxx x xxxxxx xxxxxxxx xxxx léčivé přípravky, xxxxx xxxxx xxxxx xxx opatřeny xxxxxxxxxx xxxxx, xxxx se xxxx xx ně xxxxxxxxx xxxxxxxxx xxxxxx xxxxxxxx xxxxx x xxxxxxx jedinečný identifikátor xxxx xxxxxxxxx xxxxxxxx xxxxxxxxx x xxxxxxxx xxxxxx. Xxx bylo xxxxx xxxxxxxx xxxxxxxxx xxxxxx dodávek xxxxxxxxxxxxxx xxxxxxxxx, x xx xxxxx do ordinací xxxxxxxxxxxxx xxxxxxxxxxx služeb, x nebylo xxxxxxxx xxxxxxxx dětí a xxxxxxxxx, je xxxxxxx, xxxxxxx xxxxxxxxxx xxxxxxxxxxx x xxxxxxxx o xxxxxxxxxx xxxxxxx xx xxxxxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxx x využitím xxxxxx 23 xxxx. x) xxxxxxxx x xxxxxxxxxx xxxxxxx.
Xxxxxxxxx dopadu xxxxxxxx 2011/62/EU a xxxxxxxx x ochranných prvcích xxxx provedeno Xxxxxxxxx xxxxxx (XX) v xxxxxxx x xxxxxxxxxx xxxxxxxx 2011/62/EU, která xxxxxxxxxx xxx neukládá XX přehodnocení xx xxxxxxxxxxx xxxxxx xxxxxxxx XX xxx oblast xxxxxxxxxx xxxxx u xxxxxxxx přípravků. Xxxxx xxx o xxxxxxx x xxxxxxxx rozhodnutí x xxxxxxxxxx, xxxxx x xxxxx xxxxxx xxxxxxx se zřízením x správou xxxxxxx xxxxxxx. Xxxx xxxxxxxx xxxx xxxxx xxxxxx 54x xxxx. 2 xxxx. x) xxxxxxxx 2011/62/XX xxxxxxx xxxx xxxx uvedené náklady xx xxxxxx xxxxxxx. Xxxx xxxxxx se xxxx xxxx obtížně xxxxxxxx identifikovat, xxxxx xxxx xxxxxxx xxxxxxx xx xxxxx, xxxxxxxxx x načasování xxxxxxxxxxxx x xxxxxxxxxxxxx xxxxxxxxx xxxxxx xxxxxxxx. Xxxxxxx xxxxx, ani xxxxxxxxx xxxxxxx xxxxxxxxx xxxxxxxx, xxxxxx xxxxxxxxx směrnicí 2011/62/EU x xxx xxxxxxxxx x ochranných xxxxxxx xxxxxxxxxx, xxxxxxx xx mohly xxxxxxxx xxxxxxx x xxxxxxxxxx x systému xxxxxxx x xxx pádem xxxxxxxx míru a xxxxxx xxxxxx xx xxxx xxxxxxxx. Posouzení xxxxxx xx podnikatelské xxxxxxxxx xxxx x x xxxxx xxxxxxx xxxxxxxxx XX x xxxxxxxxxx na xxxxxxxx 2011/62/EU. Tyto xxxxxx xxx byly xxxxxxxxx xxx xxxxxxxxxxxx xxxxxx xxxxxxxx xxxxxxxx, tj. xxxxxxxx 2011/62/EU a xxxxxxxx x xxxxxxxxxx xxxxxxx, pokud jde x xxxxxx xxxxxxxx, x xxxxxx č. 70/2013 Sb., xxxxx jde x xxxxxx xxxxxxxx Xxxxx xxxxxxxxx. X tomto xxxxx xx xxxxx xxxxxxx xx xxxxxxxxx xxxxxx, včetně zprávy x hodnocení xxxxxx xxxxxxxx (XXX) x xxxxxx č. 70/2013 Sb., x xxxx xx podrobnou xxxxxx RIA x xxxxxxxx x ochranných xxxxxxx označenou „Xxxxxx Xxxxxxxxxx“. Xx provedení xxxxxx hodnocení xxxxxx xxxxxxxx xxxxx v xxxx dopadů x xxxxxxx.
Xxxxxxxx xxxxx xxxxxxxxxx xxxxxx na xxxxxxxxxxxxx xxxxxxxx x hlediska xxxxxxxxxxxx xxxxxxxxxx xxxxx xx xxxxxxxxxxx dokumentace xx očekává minimální, xxxxx údaje xxxxxxxxxx xx x jedinečnému xxxxxxxxxxxxxx lze xxxxxx xx xxxxx xxxxx x xxxxx xxxxxxxxxx xxxxxx s xxxxxxx xx informace o xxxxxxxxx - xxxx. xxxxxx o xxxxxxxxxxx xxxxxxxxx xxxxxxxxxx, řízení x xxxxx registrace xxxx XX, typu XX xxxx typu XX. Xxxxxxxxxx xxxxxxxx xxxxxxx o xxxxx xxxxxxxxxx xxxxxxxxxxxxxxxxx xxxxxxxxxx xx xxxxxxxx xxxxx x xxxxxxx, xxxxx x xxxxxxxxxx xxxxxx xxxxxx xxxxxxxxxx xxxxx xxxxx xxxxxxxxxx, xxxxx xxxxxxx xxxxxxxxx x xxxxxxxxx. Xxxxxxxxxx žádosti x xxxxx registrace xxx xxxxxxxx prostředku x xxxxxxx xxxxxxxxxx x obalem je xxx xxxxxxxx xxxxx x xxxxxxx, xxx xxxxxxxxxx k ověření xxxxxxxxxx s obalem xxxx xxx xxxx xx čitelnost xxxxx, xxxx ovlivní xxxxxx xxxxxxxx xxxxx. Xxxx xxxx xxxxxxxxx, že xxxxxxxxx xxxxxxxxxxxxx x xxxxxxxxxx x ověření xxxxxxxxxx x obalem xx xxxxx implementovat xxxx xxxxxxxxxxx xxxx xxxxxxxxxx xxxxxxxxx xxxxxxx x změnu xxxxxxxxxx, xxxxx xxxxxxxxxxxx xxxxxxxxxx xxxxx xx xxxx xxxx xxxx xx xxxxxxxxx xxxxx.
Xxx údajů x xxxxxxxx 2018 xxxx xxxxxxxx xxx 2/3 xxxxxxx x xxxxx xxxxxxxxxx, xxxxx xxxxxxxxxx xxxxxxxxxxxxx body xxxxxxxx xx xxxxxxxx 2011/62/EU. Xxxxx xx xxxxxxxxxxxxx subjekty v xxxxxxx xxxxxxxx x x xxxxxxx xxxxxxxxxxxx xxxx xx xxxxxxxx xxxxxxxxxxxx žádostí xxxx xxxxxxxxx, xxxxxxxx x xxxx xxxxxxx skutečnosti, xxx pro xxxxxxx xxxxxxxx přípravků xxxxxx xxxxx xx xxxxxxxx xxxxxxxxxx xxxxx xxxxxxxxxx xxxxxxxx xxxxxx o xxxxx registrace x xxxxxxxx xxxxx xx xxxxx xxxxxxxxxxxxx xxx xxxx xxxxxxxxxxx xxxx xxxxxxxxxx xxxxxxxxx žádosti x změnu xxxxxxxxxx. Xxxxxx implementace xxxxx xxxxx xxx xxxxxx xxxxxxxxx, xxxxx xxxx xxx xxxxxxxx xxxxxxxxxx xxxxx, x xxxxxxxx xxxxxxxxx, xxxxx xxxxxxxxxx xxxxx opatřeny být xxxxxx (xxxx. xxxxxx xxxxxxxxx, jejichž xxxxx xxxx vázán xx xxxxxxxx předpis) xxxxx xxxxxxxxx xxxxxxxxxxxx xx xxxxxx xxxxx „neuplatní xx“ při nejbližší xxxxxx změně xxxxxxxx xx xxxxxxxxx x xxxxxxxxx.
3. 3 Xxxxxxx
Xxxxxxxx xxxxxxxxxx právní úpravy xxxx xxxxxxxxx xxxxxxxxx x xxxxxxxxxx xxxxxxx xxxxxxxxxx xxxxxxxxxxx xxx xxxxxxxxx xxxxxx xxxxxxxxxx xxxxxxxx přípravků do xxxxxxxxx xxxxxxxxxxxxxx xxxxxxx x zvýšení xxxxxxx xxxxxxxx x osob xxxxxxxxxx x distribučním xxxxxxx xxxx léčivými xxxxxxxxx, xxxxx pocházejí x xxxxxxxxxxx xxxxxx. Xxxxxxxxxx právní xxxxxx xxxx mít xx xxxxxxxxxxxxx prostředí xxxxxxxxx xxxx a xxx xxxxxxxx, že xxxxxxxx xx xxxxxxx xxxxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxxx x xx xxxxx důsledcích x x xxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxxxxxxxx xxxxxxx xx xxxxxxxxxx xxxxxxxx xxxxxxxxx. Xxxx xx xxxx xxxxx xx zvýšení xxxxxx xxxxxxx, distributorů x xxxxxxx, xxxxx xxxxxxxx xxxxxx xxxx přítomností xx xxxx xxxx x xxxxxxx legálních xxxxx xxxxxxx.
Xxx se xxxxxxxxxxxxxx xxxxxx, xx xx xxxxxxxx xxxxxx xxxxxxxxx xxxxxxxxx do xxxxxxxxx xxxxxxxxxxxxxx řetězce x volně xxxxxxxx xx xxxxx území Xxxx, dokud xx xxxxxx ověřeny v xxxxxxxx výdeje veřejnosti, xxxxx distributoři xxxxxxxx xxxxxxxxx xxxxxxx ochranných xxxxx x xxxxxxxxx xxxxxxxx xxxxxxxxx, x xxxxxxx xxxxxxxx xxxxx xxxxxx padělání (xx. x xxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxx xxxxxxxxxxx xxxxxxx xxxxxx xxxxxxxxx xxxx jiným xxxxxxxxxxxxx).
Xxxxxx xxxxx xxxxxxxx v xxxxxxxxxx xxxxxxxxxxxxxx (xxxxxxx xxx přípravku, xxxxx xxxxx x xxxxx xxxxxxxxxxxxx) xxxxxxxx x xxxxxxxxxxx pacientů tím, xx usnadní postupy xxx xxxxxxx x xxxxxxx x farmakovigilanci.
Ověřování xxxxxxxx xxxxxxxx přípravků x ČR xx xxxxxx výrobců, xxxxxxxxxxxx x xxxx xxxxxxxxxxx x xxxxxx (lékáren) xx mělo xxxxx xxxxxxxx vstupu xxxxxxxxxx xxxxxxxx xxxxxxxxx do xxxxxxxxx distribučního xxxxxxx x následně eliminovat xxxxxx xxxxxxxxxxxxx xxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxx v xxxxxxxxx x xxx zvýšit xxxxxxx xxxxxxxxx xxxxxx.
Xxxxxxxx xxxxxxx novely xxxxxx xx xxxxxxxx xxxxxxx xxxxxxxxxxxx xxxxxxx xxxxxxxx xxxxxxxxx x XX.
4. Xxxxxxxxx pořadí xxxxxxx x xxxxx xxxxxxxxxxxxxx xxxxxx
Xxxxxxxxx xxxxxxxxxxx x xxxxxxx xxxxxx je xxxxxxxx 2, xxxx xxxxxxxxxx xxxxxx xxxxxx xxxxxx o xxxxxxxx, xxxxxxx naplňuje cílový xxxx x splňuje xxxxxxxx xxxxxxxxx xxxxxxxxx x xxxxxxxxxx prvcích x tomu, xxx x xxxx Xxxxxxxx xxxx mohl xxxxxxxx xxxxxxxx xxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxxxxxxx xxxxxxxxxx xxxxx xxxxxxxxx xx jejich xxxxx, xxxxx xx xxx xxxxxxxx xxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx xx xxxxxxxxx xxxxxxxxxxxxxx řetězce x xxxxxxx xxx x xxxxx xxxx xxxxxxx xxxxxxxxx xxxxxx.
Xxxxxxxx 1 (xxxxxx) xx x xxxxxx popsaných xxxx xxxxxxxxxxxx x xxxxx další xxxxxxxx xxx x xxxxxx xxxx xxxxxxxxx xx xxxxx, xxxxxxx jde x adaptaci xxxxx xxxxxxxxxxxx předpisu Evropské xxxx x xxxxxxxx xxxxxxxxx xxxxx x xxxx xxxxxxx, x xxx x xxx xxxxxxx xxxxxxxx provést, xxxx xxxxxxxx omezeny xxx xx xx xxxxxxx, xx xxxxxxx xx xx xxxxx xxxxx xxxxxxxxxx xxxxxxx Xxxxxxxx xxxx xxxxxxx xxxxxxxxx nebo xxxxxxxx.
5. Xxxxxxxxxxxx xxxxxxxxxx varianty x xxxxxxxxxx
Xxxxxxx xxxxxxxxxx za xxxxxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxx xxxx xxxxxxxxx Xxxxx, xxxxx xx již xxxxx xxxxxxxxxxx znění xxxxxx x xxxxxxxx xxxxxxxxxxxxxxx odborným xxxxxxxx xxxxxx xxx xxxxxx xxxxxxxx xxxxxxxxx léčiv. Xxxxx má xxxxxxx xxxx xxxx xxxxxxx xxxxxxxxxx x oblasti xxxxxxx, účinnosti a xxxxxxxxxxx humánních xxxxx, x xx x xx vztahu x xxxxxxxxxx xxxxxxx xxxxxxxxx xxxxx a Xxxxxxxx xxxx.
Xxxxxxxxxxxx doporučené xxxxxxxx x xxxxxxxxxx xxxxxxxxxx xxxxxxxx xxxx xxxxxxxxx xxxxxxxx zákonem o xxxxxxxx x rámci xxxxxxxxx trestání v xxxxxxx x obecnou xxxxxx xxxxxxx xxxxxxxxx, x to ukládáním xxxxx x xxxxxxx xxxxx trestů.
6. Xxxxxxx xxxxxxxxx xxxxxxxx
Xxxxxxxx nové xxxxxx xxxxxx xxxx xxxxxxxx xx xxxxxxxx xxxxxxx 2 let xxx dne nabytí xxxx účinnosti, aby xxxx xxxxx xxxxxx xxxxxxxxxx xxxxxxxx a xxxxxxxxx xxxxxxxxx, xxxx xx právní xxxxxx xxxxxxxxx xxxxxx, tj. xxx xxxxx x xxxxxxxxx xxxxxxxxxxx padělaných xxxxxxxx xxxxxxxxx x xxxxxxxx dodavatelském řetězci x XX a x tranzitu. Xxxxxxx xxxxxxxxx budou xxxxxxxx Xxxxxxxxxxxx xxxxxxxxxxxxx a Xxxxxx xxxxx xxx xxxxxxxx léčiv ve xxxxxxxxxx x xxxxxxxxx xxxxxxxx, a xx x hlediska xxxxxxxxx xxxxxxxxx nové xxxxxx xxxxxx x zejména x hlediska dosahování xxxx xxxxxxxxxxx xxxxx xxxxxx xxxxxxx.
7. Xxxxxxxxxx x zdroje dat
Návrh xxxxxx xxx x xxxxxxx přípravy xxxxxxxxxxx xx xxxxxxxx xxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx, xxxxxxxx rozhodnutí x xxxxxxxxxx xxxxxxxx xxxxxxxxx, xxxxxxxxxxxx humánních xxxxxxxx xxxxxxxxx, xxxxxxxxxxxxx zdravotních xxxxxx oprávněných x xxxxxx léčivých přípravků x xxxxxxxxxxxx xxxxxxxxxx. Xxxxx xxxxxxxxx xxx x xxxxxxxxx 2016 xxxxxx xxxxxxx xxxxxxxx xxxxx novely zákona x xxx, xx x němu mohou xxxxxxxx xxxxxxxxxx. X xxxxxxxxxx x xxxxxxxxxx xxxx uplatněných xxxxxxxxxx xx pak v xxxxxxxx 2016 uskutečnilo xxxxxx jednání x xxxxxx Ústavu. Celá xxxx xxxxxxxxxxx xxxxxxxxxx xxxx x upraveném xxxxxx zohledněna a xxxxxx xxxxxxxxxxxx došlo xx zkvalitnění xxxxxxxxxx xxxxxxxxx x x xxxx xxxxxxxxxx k xxxxxxxxx xxxxxxxx xxxxxxxx xxxxx. Xxxx xxxxxxxxxxxx xxxxxxx xxxxxx akceptace xxxxxxxxxx připomínek může xxxxxxx xxxxxxxxxx, xxx xxx xxxxxxxxx Xxxxxxx xxxxxxx xxx xxxxxxxx xxxxx podle §32 xxxx. 5 zákona x xxxxxxxx („xxx XXXX“) xxxxx xxxxxxxx xxxxxxxxxxx identifikátoru. Xxxx xxxxxxxxx xxxxxxx a xxxxxx xxxxxxxxxx materiálů xx xxxxxxxx Armády Xxxxx xxxxxxxxx x Xxxxxx xxx státní xxxxxxxx veterinárních biopreparátů x xxxxx, x xx xxxxxxx xx xxxxxx xxxxxxxx co xxxxxxxxxxxx xxxxxxxxxxxx článku 23 xxxxxxxx x xxxxxxxxxx prvcích.
8. Xxxxxxxx xx zpracovatele RIA
Útvar: Xxxxxxxxxxxx xxxxxxxxxxxxx, Xxxxx xxxxxxxx, oddělení xxxxxxxx, xxxxxxxxxxxx: XxxxxXx. Xxxxx Xxxxxxxxx, xxxxxxxxx odboru xxxxxxxx, zpracovatelé: XxxxxXx. Xxxxx Xxxxxxxxx, xxxxxxx xxxxxxxx farmacie, Xxx. Xxxxxxxxx Linhartová, xxxxxxxx, Xxx. Xxxxxx Müller, xxxxxxxx.
X-xxxx: alena.tomaskova@mzcr.cz
Státní xxxxx xxx xxxxxxxx léčiv, xxxxx dozoru, Xxx. Xxxxxxx Xxxxxxxx, ředitelka Xxxxx xxxxxx
Xxxxxxx: 272 182 265
XXXXXXXXX XXXXXXX NÁVRHU XXXXXXXX XXXXXXXX XX X XXXXXXXX EU
Rozdílová xxxxxxx x xxxxxx xxxxxx zákona, xxxxxx xx xxxx xxxxx x. 378/2007 Xx., x léčivech x x xxxxxxx některých xxxxxxxxxxxxx zákonů (zákon x léčivech), xx xxxxx xxxxxxxxxx předpisů, x xxxxx č. 372/2011 Xx., x xxxxxxxxxxx xxxxxxxx x xxxxxxxxxx xxxxxx xxxxxxxxxxx (xxxxx x zdravotních xxxxxxxx), xx znění xxxxxxxxxx xxxxxxxx
|
Xxxxxxxxxx xxxxxx xxxxxxx (resp. jiný xxxxxx xxxxxxx) |
Xxxxxxxxxxxx předpis XX |
|
|
Xxxxxxxxxx (část, §, xxxx., xxxx., xxxx.) |
Xxxxx x. |
Xxxxxxxxxx |
|
Xx. 2 |
||
|
Xx. 43, 44, Xx. 46 |
||
|
§13 odst. 2 písm. p) a q) (včetně poznámky pod čarou č. 107 a 108) |
Čl. 25, Čl. 7 xxxx. 1 a 2, Xx. 10 xxxx. 1 věta xxxxx, Čl. 94 xxxx. 1 |
|
|
32017L1572, 32017L1572, 32017R1569, 32017R1569, 32017R0556, 32017R0556 |
Xx. 3 xxxx. 1, Čl. 3 xxxx. 3, Čl. 21 odst. 4, Xx. 22, Xx. 3 xxxx. 1, Xx. 4 xxxx. 8 |
|
|
Xx. 4 |
||
|
Xx. 1 xxxx. x) x x), Xx. X xxx 12 |
||
|
Xx. 45 |
||
|
Xx. 42 |
||
|
Čl. 11 xxxx. 1 |
||
|
Xx. 13 xxxx. 1 a 2 |
||
|
Xx. 4 odst. 1 |
||
|
Xx. 23 |
||
|
Čl. 25 xxxx. 1 |
||
|
Xx. 39 |
||
|
Xx. 10 x 11 |
||
|
Čl. 12 |
||
|
Xx. 13 |
||
|
Xx. 4 |
||
|
Xx. 5 xxxx. 1 |
||
|
Čl. 6 |
||
|
Xx. 7 |
||
|
Xx. 14 |
||
|
Xx. 15 |
||
|
Xx. 16 |
||
|
Čl. 18 |
||
|
Čl. 9 |
||
|
Xx. 20 |
||
|
Xx. 22 |
||
|
Xx. 24 |
||
|
Xx. 23 |
||
|
Xx. 23 |
||
|
Čl. 25 xxxx. 1 x 2 |
||
|
Xx. 28 |
||
|
Čl. 29 |
||
|
Xx. 25 xxxx. 4 |
||
|
Xx. 30 |
||
|
Čl. 25 xxxx. 1 |
||
|
Čl. 33 xxxx. 1 |
||
|
Xx. 40 |
||
|
Čl. 42 |
||
|
Xx. 33 odst. 4 |
||
|
Xx. 37 |
||
|
Xx. 39 |
||
|
Čl. 35 xxxx. 1 x 2 |
||
|
Xx. 32 xxxx. 3 x 4 |
||
|
Xx. 32 odst. 1 |
||
|
Xx. 35 odst. 3 |
||
|
Xx. 35 xxxx. 4 |
||
|
Xx. 41 |
||
|
Xx. 63 odst. 1, Xx. 94 xxxx. 1, Xx. 20 xxx 2 |
||
|
Xx. 10 xxx 2 xx 5 |
||
|
Xx. 4, Xx. 45, Xx. X xxx 12, Xx. X xxx 25 |
||
|
Xx. 94 xxxx. 1, Xx. 62 xxx 1 |
||
|
Čl. 4, Xx. 45, Xx. X bod 12, Xx. X xxx 25 |
||
|
Xx. 10 xxxx. 8 |
||
|
Xxxxx xxxxxxxx EU (xxx celex) |
Název xxxxxxxx XX |
|
XXXXXXXX XXXXXX X XXXXXXXXX XXXXXXXXX (XX) 2016/161 xx xxx 2. xxxxx 2015, xxxxxx xx xxxxxxxx xxxxxxxx Evropského xxxxxxxxxx x Rady 2001/83/XX xxxxxxxxxx podrobných xxxxxxxx xxx xxxxxxxx xxxxx xxxxxxx xx obalu xxxxxxxxx xxxxxxxx xxxxxxxxx |
|
|
Xxxxxxxx Xxxxxxxxxx parlamentu x Xxxx 2011/62/XX xx xxx 8. června 2011, kterou xx xxxx xxxxxxxx 2001/83/ES x xxxxxx Společenství xxxxxxxxx se xxxxxxxxx xxxxxxxx xxxxxxxxx, pokud xxx x zabránění xxxxxx xxxxxxxxxx léčivých xxxxxxxxx xx legálního xxxxxxxxxxxxxx řetězce |
|
|
Směrnice Xxxxxx (XX) 2017/1572 xx xxx 15. září 2017, xxxxxx se xxxxxxxx směrnice Xxxxxxxxxx xxxxxxxxxx x Xxxx 2001/83/XX, xxxxx xxx x xxxxxx a xxxxxx pro xxxxxxxx xxxxxxx praxi xxx xxxxxxx xxxxxx xxxxxxxxx |
|
|
Xxxxxxxxx xxxxxxxx Xxxxxx x xxxxxxxxx xxxxxxxxx (XX) x. 2017/556 xx xxx 24 xxxxxx 2017&xxxx; x xxxxxxxxxx xxxxxxxxxx xxx provádění xxxxxxxxxxx xxxxxxx správné xxxxxxxx xxxxx&xxxx; podle xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Rady (EU) x. 536/2014 |
|
|
Xxxxxxxx Komise x xxxxxxxxx pravomoci (XX) x. 2017/1569 xx xxx 23. xxxxxx 2017, kterým xx doplňuje xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Xxxx (XX) x.536/2014 xxxxxxxxxx xxxxx a xxxxxx xxx xxxxxxxx xxxxxxx xxxxx xxx xxxxxxxxx xxxxxxx léčivé xxxxxxxxx x xxxxxxxx xxxxxxxxx xxxxxxxx |
|
|
Xxxxxxxx Evropského xxxxxxxxxx a Xxxx XX x. 536/2014 xx dne 16. xxxxx 2014 x xxxxxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxxxx přípravků a xxxxxxx xxxxxxxx 2001/20/XX |
Xxxxx xxxxx xxx.xxx.xx


