Vládní návrh zákona, kterým se mění zákon č. 378/2007 Sb., o léčivech a o změnách některých souvisejících zákonů (zákon o léčivech), ve znění pozdějších předpisů, a zákon č. 372/2011 Sb., o zdravotních službách a podmínkách jejich poskytování (zákon o zdravotních službách), ve znění pozdějších předpisů
262/0
Xxxxx
XXXXX
xx xxx … 2018,
xxxxxx xx xxxx xxxxx č. 378/2007 Sb., o xxxxxxxx a o xxxxxxx xxxxxxxxx xxxxxxxxxxxxx xxxxxx (zákon x xxxxxxxx), xx znění xxxxxxxxxx xxxxxxxx, a xxxxx č. 372/2011 Sb., o xxxxxxxxxxx xxxxxxxx x xxxxxxxxxx xxxxxx xxxxxxxxxxx (xxxxx o xxxxxxxxxxx xxxxxxxx), xx xxxxx xxxxxxxxxx xxxxxxxx
Xxxxxxxxx xx xxxxxx na xxxxx xxxxxx Xxxxx xxxxxxxxx:
ČÁST XXXXX
Xxxxx xxxxxx x léčivech
Xx. X
Xxxxx č. 378/2007 Sb., x xxxxxxxx a x xxxxxxx některých xxxxxxxxxxxxx xxxxxx (xxxxx x léčivech), xx xxxxx xxxxxx č. 124/2008 Xx., xxxxxx x. 296/2008 Sb., xxxxxx x. 141/2009 Xx., xxxxxx x. 281/2009 Sb., zákona x. 291/2009 Xx., xxxxxx č. 75/2011 Xx., xxxxxx x. 375/2011 Sb., xxxxxx x. 50/2013 Xx., xxxxxx č. 70/2013 Xx., zákona x. 250/2014 Sb., xxxxxx x. 80/2015 Xx., xxxxxx č. 243/2016 Xx., xxxxxx x. 65/2017 Xx., zákona x. 66/2017 Xx., xxxxxx x. 183/2017 Xx., xxxxxx č. 251/2017 Xx. a xxxxxx č. 36/2018 Xx., se xxxx xxxxx:
1. Xx xxxxx xxxxxxxx xxx xxxxx x. 2 xx xx xxxxxxxxxx xxxxx xxxxxxxx xxxx „Xxxxxxxx Xxxxxx v xxxxxxxxx xxxxxxxxx (EU) 2016/161 xx xxx 2. xxxxx 2015, kterým xx doplňuje xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Xxxx 2001/83/XX xxxxxxxxxx xxxxxxxxxx pravidel xxx xxxxxxxx xxxxx xxxxxxx xx xxxxx xxxxxxxxx xxxxxxxx přípravků.“.
2. X §5 xxxxxxxx 7 xxx:
„(7) Xxxxxxxx xxxxxxxxxxx humánních xxxxxxxx xxxxxxxxx xx xxxxxx xxxxxx nákup, xxxxxxxxxx nebo xxxxxx. Xxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxx xxxxxxxx přípravků xx xxxxxx xxxxxx xxxxx, xxxxxxxxxx xxxx xxxxxx xxxxxxxxx xxxxxxxxxxxx.“.
3. X §6 xx xx xxxxx xxxxxxxx 2 doplňuje xxxx „V xxxxxxx xxxxxxxxx x xxxxxxxxxxxxx xxxxxxxx přípravků xx xxxxxxxx xxxxxxx xxxxxxx xxxxx xxxxxxx obdobně xx dovoz xx xxxxxxx xxxx.“.
XXXXX: 32017L1572
4. X §13 xxxx. 2 se xx xxxxx xxxxx xxxxxxx x) xxxxxxxx xxxxx „x xxxxx xxxxxxxxxxxx xxxxxxxx Xxxxxxxx xxxx xxxxxxxxxxxx oblast xxxxxxxxx xxxxx“.
5. V §13 xx xx xxxxx xxxxxxxx 2 tečka xxxxxxxxx xxxxxx x xxxxxxxx se xxxxxxx x), které včetně xxxxxxxx pod xxxxx x. 106 zní:
„o) xx xxxxxxxxxx xxxxxxx Xxxxx republiky xxx xxxxxx jejích úkolů x xxxxxxx xxxxxxxxxx xxxxxxxx xxx ochranné xxxxx xxxxxxx na xxxxx xxxxxxxx přípravků, xxxxxxxx xxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxxxxxxxx xxxxx xxxxxxxxxxx předpisem Xxxxxxxx xxxx xxxxxxxxxxx xxxxxxxx xxxxxxxx xxx xxxxxxxx xxxxx xxxxxxx na xxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx106) (xxxx jen „xxxxxxxx x ochranných xxxxxxx“), xx xxxxxxx xx systému xxxxxxx x k informacím x nich obsaženým x xxxxxxx x xx. 39 nařízení x xxxxxxxxxx xxxxxxx, x xxxxxxxx xxxxxxxx xxxxxxxxx xxxxxx systému, xxxxxxx x xxxxxxxxxxx xxxxxx padělání u xxxxxxxx xxxxxxxxx x xxxxxx xxxxxxxx x xxxxxx xxxxxxxx a xxxxxx x xxxx xxxxxxx informace Xxxxxx.
XXXXX: 32016R0161
6. V §13 xx xx xxxxx xxxxxxxx 2 xxxxx xxxxxxxxx čárkou a xxxxxxxx se xxxxxxx x) x q), xxxxx xxxxxx poznámek xxx xxxxx x. 107 a 108 xxxxx:
x) xx xxxxxxxxxx xxxxxxx Xxxxx republiky xxx xxxxxx xxxxx xxxxxxxxxxx xxxxx použitelným xxxxxxxxx Evropské unie, xxxxxx xx stanoví xxxxxx a xxxxxx xxx xxxxxxxx xxxxxxx xxxxx pro hodnocené xxxxxx xxxxxxxxx107) (xxxx xxx „xxxxxxxx x xxxxxxx xxxxxxx xxxxx xxx xxxxxxxxx xxxxxx xxxxxxxxx“) x xxxxx xxxxxxxxxxx xxxxxxxxx Xxxxxxxx xxxx, xxxxxx se xxxxxxx xxxxxxxx provádění xxxxxxxxxxx xxxxxxx správné xxxxxxxx xxxxx108) (dále xxx „nařízení o xxxxxxxxx xxxxxxxxxxx xxxxxxx xxxxxxx xxxxxxxx xxxxx“),
x) xx příslušným xxxxxxx Xxxxx republiky xxx xxxxxxxx povolení k xxxxxx x xxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxx xxxxxxxx x xxxxxxxxx xxxxxxxxx.
XXXXX: 32017R1569, 32017R0556, 32014R0536
7. V §13 xxxx. 3 xxxxxxx x) xxx:
„x) xxxxxx x udržuje xxxxxx xxxxxxx, xxxxx xxxxxxxxx
1. xxxxxx xxxxxxx x xxxxxxxxxxx x xxxxxxx xxxxxxxx xxxxxxxxxxx Xxxxxx, xxxxx xxxxxxx xxxxxxxxx x kontrolu x xxxxxxxxx xxxxx xxxxxx xxxxxx xxxx xxxxx xxxxxxxxxxxx xxxxxxxx Xxxxxxxx xxxx, včetně xxxxxx xxxx xxxxxxxxxx, odpovědností x požadavků xx xxxxxxxx xxxxxxxx,
2. dodržování xxxxxxxx xxxxxxxxxxx postupů xxxxxxx klinické xxxxx x xxxxxxx s xxxxxxxxx x xxxxxxxxx xxxxxxxxxxx xxxxxxx xxxxxxx xxxxxxxx xxxxx,
3. xxxxx xxxxxxxxx xxxxxxx xxxxxxxxxx xxxxxx zákona x xxxxxxxxxxx předpisů Xxxxxxxx xxxx x xxxxxxx xxxxxxxxx léčivých xxxxxxxxx xxxxxx hodnocených xxxxxxxx xxxxxxxxx,“.
XXXXX: 32017L1572, 32017R1569, 32017R0556
8. V §16 xxxx. 3 písm. x) xx xxxxx „xxxxxxx“ xxxxxxxxx xxxxxx „xxxxxxx“.
9. X §22 xxxx. 2 xx xx xxxxx „xxxxxxxxx“ xxxxxxxx xxxxx „xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx“.
10. X §23 xx xx konci xxxxxxxx 1 tečka xxxxxxxxx xxxxxx x xxxxxxxx se písmena x) až x), xxxxx xxxxx:
„x) xxxxxxxxxx xxxxxxx Xxxxxx, xxx-xx x humánní xxxxxx xxxxxxxxx, xxxxxxxxx na xxxxxxxx léčivý xxxxxxxxx, xxxxxxxxx-xx xxxx xxxx xxxxxxxxx z xxxxxxxx x xxxxxxxxxx prvcích,
g) xxxxxxxxxx Xxxxxx součinnost xxx xxxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxx x podezřením xx padělání xxxxxxxx xxxxxxxxx,
x) neprodleně xxxxxxx Xxxxxxxxxxxxx xxxxxx xxxxxxxxx xx padělaný xxxxxxxxxxx xxxxxx xxxxxxxxx.“.
11. X §24 xxxx. 10 xx xxxxx „xxxx deklarant“ xxxxxxx.
12. X §34 xx xxxxxxxx xxxxxxxx 9, xxxxx xxx:
„(9) Xxxxx xxxx Xxxxxxxxxxx xxxxx xxxxxxxxxx xxxxxx xxxxxx z xxxx xxxxxx x změně xxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxx xxxx vyhrazené xxxxxx přípravky v xxxxxxx xxxxxx skutečností xxxxxxxxxx xx xxxxxxxxxxx xxxxxxxxxxx xxxxxxxx přípravku.“.
13. V §37 xxxx. 1 xx xx xxxxx „xxxxxxxxxxxx xxxxxxxx přípravku,“ vkládají xxxxx „xxxxx-xx x xxxxxxxxx xxxxxxxxxxxxx,“, xxxxx „xxxxxxxxx xxxxxxxx xxxxx (XXX)“ xx xxxxxxxxx xxxxx „xxxxxxxxxxx xxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxxx“, za xxxxx „xxxxxxxxxx“ xx xxxxxxxx slova „a xxxxxxxx požadavkům xxxxxxxxxxxx xxxxxxxxxx xxxxxxx“ x xx větu xxxxx xx xxxxxx věta „Xx obalu xxxxxxxxx xxxxxxxx xxxxxxxxx musí xxx xxxxxx kód xxxxxxxxx podle §32 xxxx. 5.“.
14. V §37 xxxx. 7 xxxx xxxxx se za xxxxx „ochranné prvky“ xxxxxxxx xxxxx „podle xxxxxxxx x xxxxxxxxxx xxxxxxx“, xx xxxxx xxxxx xxxx xx xxxxxxxx slova „(dále xxx „xxxxxxxx xxxxx“)“ x věta xxxxxxxx xx xxxxxxxxx xxxxx „Xxxxxx x xxxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxx xxxxxxx nařízení x xxxxxxxxxx xxxxxxx.“.
XXXXX: 32016R0161
15. V §37 xxxxxxxx 8 xxx:
„(8) Xxxxxxxxxx xxxxx podle xxxxxxxx 7 xxxx xxx opatřeny humánní xxxxxx xxxxxxxxx xxxxxxxx xxxxx na xxxxxxxx xxxxxxx nebo xx xxxxxxxx xxxxxxx s xxxxxxxx, xxxxx xxxxxx xxxxxxx xx xxxxxxx xxxxxxxx přípravků, xxxxx xxxxx být xxxxxxxx xxxxxxxxxx xxxxx, stanovené xxxxxxxx I xxxxxxxx x ochranných xxxxxxx. Xxxxxxxxxx xxxxx xxxxx xxxxxxxx 7 nesmějí xxx xxxxxxxx xxxxxxx xxxxxx xxxxxxxxx, xxxxx xxx vydávat bez xxxxxxxxxx xxxxxxxx x xxxxx xxxxxx xxxxxxx xx seznamu uvádějícím xxxxxx xxxxxxxxx, xxxxx xxxx být xxxxxxxx xxxxxxxxxx xxxxx, xxxxxxxxx x příloze II xxxxxxxx x ochranných xxxxxxx.“.
XXXXX: 32016R0161
16. X §45 xx xx xxxxx xxxxxxxx 7 tečka xxxxxxxxx čárkou x xxxxxxxx se xxxxxxx x), xxxxx zní:
„f) xxx přebalování xxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxx xxxxxxxxx jedinečný identifikátor x xxxxxxx xxxx xxxxxxxxx xxxxxxxxxxxxx postupem xxxxx nařízení o xxxxxxxxxx xxxxxxx.“.
XXXXX: 32016R0161
17. V §64 xxxxxxx x) xxx:
„x) xxxxxxxx a xxxxxxxx xxxxxx xxxxxxxx xxxxxxx x xxxxxxxxxx xxxxxxxx xxx činnost xxxxxx xxxxxxxx xxxxxxx xxx, xxx xxxxx xxxxx, xxxxx xx x xxxxxxxxx xxxxx uvedené x písmenu x), xxx nezávislý xx xxxxxx xxxxxxxxxxxxx útvarech xxxxxxx xxxxxxxx xxxxxxxxx,“.
XXXXX: 32017L1572
18. X §64 xxxx. x) xx xx xxxxx „xxxxxxxx“ xxxxxxxx xxxxx „kdykoli x“ x xxxxx „x xxxxxxxx“ xx xxxxxxxxx xxxxx „, xxxxxxxx x xxxxxxxx xxxxxxxxxx x xxxxxxxxxx, x xxxxx xxx, xxxxx xx to xxxxx, xxxx, xxx xxxxx byl léčivý xxxxxxxxx xxxxx; x xxxxxxx xxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxxxx přípravků xx použijí xxxxxxxx xxxxxxxxx xxxxxxxxx x xxxxxxx xxxxxxx praxi xxx hodnocené léčivé xxxxxxxxx“.
XXXXX: 32017L1572
19. X §64 xxxx. j) se xxxxx „xxxxxxxxx xxxxxxx x souladu x xxxxxxxxx x xxxxxx, xxxxxxxxx xxxxxxxx správné xxxxxxx xxxxx“ xxxxxxxxx xxxxx „xxxxxxxx xxxxxxx xxxxxxxx x xxxxxxx x xxxxxxxx xxxxxxx xxxxxxx xxxxx, s xxxxxxxxx x xxxxxx“.
XXXXX: 32017L1572
20. X §77 xxxx. 1 xxxx. x) xxxx 4 xx číslo „13“ xxxxxxxxx číslem „12“.
21. X §77 xxxx. 1 xxxx. x) xx xxx 5 xxxxxxx.
Xxxxxxxxx xxxx 6 až 14 xx označují jako xxxx 5 až 13.
22. X §77 xxxx. 1 písm. x) xxx 11 xxx:
„11. krevním xxxxxx, xxx-xx o xxxxxxxxxx xxxxxxxxx, xxxxxxxxx transfuzní xxxxxx, xxx-xx o xxxxxxxxxx xxxxxxxxx x xxxxxx xxxxxxxx, xxxxx xx xxxxxx xxxxxxxxxx xxxxxxxxxxxx přípravků xxxxxx xxxxxxxxx xxxxxxxxxx služby xxxxx §67 odst. 3,“.
23. X §77 xxxx. 1 xxxx. x) bodě 12 xx xx slova „xx xxxxxx“ xxxxxxxx xxxxx „pravidelného, xxxxxxxxxxx x zvláštního xxxxxxxx xxxxx zákona o xxxxxxx xxxxxxxxx xxxxxx x xxxxxxxxxxx“ x xx xxxxx „xxxxxxxx“ xx xxxxxxxx xxxxx „xxxxxxxxx xxxxx xxxxxx x xxxxxxxx zdravotním xxxxxxxxx“.
24. X §77 xx xx xxxxx xxxxxxxx 1 xxxxx xxxxxxxxx xxxxxx x xxxxxxxx xx písmeno x), xxxxx xxx:
„x) xxxxxx xxxxxxxx xxxxx x provést xxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx postupem xxxxx xxxxxxxx x xxxxxxxxxx xxxxxxx xxxx xxx, xxx xxxxxx xxxxxxxxx xxxx
1. veterinárním xxxxxxx,
2. Xxxxxx České xxxxxxxxx x zabezpečení xxxxxxxxxxx xxx Xxxxx xxxxxxxxx léčivy a x udržování xxxxxxxxxx xxxxx xxxxxxxx přípravků xxx účely xxxxxxxxxxx xxxxxxxxxxx xxx České xxxxxxxxx léčivy xxx xxxxxx xxxxxxxx do xxxxxxxxx xxxxx §111a, xxxx
3. xxxxxxxxxxxxxx xxxxxxxxxxx xxxxxx, xxxxxx xxxx xxxxx §77 xxxx. 1 xxxx. c) xxxx 12 xxxxxxxx xxxxxxxxxxxx léčivé xxxxxxxxx xxx xxxxx pravidelného xxxxxxxx xx základě xxxxxxx smlouvy xxxxxxxxxxxx xx zdravotní xxxxxxxxxxx xxxx pro xxxxx xxxxxxxxxxxx, xxxxxxxxxx a xxxxxxxxxxx xxxxxxxx xx xxxxxxx rámcové xxxxxxx xxxxxxxxxxxx x Xxxxxxxxxxxxx xxxxxxxxxxxxx xxxxx jsou xxxx xxxxxxxxx xxxxxxxx xxx xxxxx nepovinného xxxxxxxxx xxxxxxxx x xxxxx xxxxxxxxxxx xxxx xxxxx xxxxxx x xxxxxxxx zdravotním xxxxxxxxx7).“.
XXXXX: 32016R0161
25. V §80 xxxx. 4 se xxxxx „Veterinární léčivé xxxxxxxxx“ nahrazují slovy „Xxxxxx přípravky pro xxxxx zvířat“.
26. X §82 xxxx. 2 xx xxxxxxx x) zrušuje.
Dosavadní xxxxxxx x) xx x) xx xxxxxxxx xxxx xxxxxxx x) xx x).
27. X §82 xx xx xxxxx xxxxxxxx 3 xxxxx xxxxxxxxx čárkou a xxxxxxxx xx xxxxxxx x), xxxxx zní:
„i) xxxxx xxxxxxxx xxxxx x provedou vyřazení xxxxxxxxxxx identifikátoru u xxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxx ochrannými xxxxx xxxxxxxx podle xxxxxxxx x xxxxxxxxxx xxxxxxx.“.
XXXXX: 32016R0161
28. X §99 xx xxxxxxxx xxxxxxxx 7 x 8, xxxxx znějí:
„(7) Ústav xx xxxxxxxx xxxxxxxxx xxxxxxxxxxxxx xxxxxxxx zřízeného xxxxx článku 31 xxxxxxxx x xxxxxxxxxx prvcích (xxxx xxx „xxxxxxxx“) xxxxxxxxx, xxxxx xxxxxxxxx x xxxxxx xxxx xxxxxxxxxx x jsou xxxxxxxx xxx xxxxxxxxx xxxxxx xxxxxxxx.
(8) Ústav xxxxxxxxx z xxxxxxxx, xxxxx xxxxx nebo x xxxx má xxxxxxx xxxxx §13 xxxx. 2 písm. x), xxxxxxxxx dalším xxxxxx, xxxxx xxxxx xxx xxxxxxx xxxx xxxxxx xxxxxxx, x xxxxxxxx xxxxxx x xxxxxxxxx xxxxxxxx x xxxxxxxxxx.“.
XXXXX: 32016R0161
29. V §100 xxxx. 8 úvodní xxxxx xxxxxxxxxx xx xx xxxxx „Xxxxx“ xxxxxxxx slova „xxxx Xxxxxxxxxxx xxxxx xxxxx xxxxxxxxxx“.
30. X §100x xx xxxxx „xxxxxxx“ xxxxxxxxx slovy „xxxxxxxx xxxxxx přípravek“.
31. X §103 xxxx. 6 xx xx xxxxx písmene x) xxxxx „nebo“ xxxxxxx.
32. V §103 xx xx konci xxxxxxxx 6 xxxxx xxxxxxxxx xxxxxx x xxxxxxxx xx xxxxxxx x) až x), xxxxx xxxxx:
„x) xxxxxx xxxxxxxxx xxxxxxxxx pokyny Xxxxxx xxxx xxxxxxxx xxxxx §23 xxxx. 1 xxxx. x),
x) xxxxxxxxxx xxxxxxxx Xxxxxx xxxxxxxxx na xxxxxxxx xxxxxx xxxxxxxxx xxxxx §23 odst. 1 xxxx. x) nebo x),
x) x xxxxxxx x xxxxxxxxx x xxxxxxxxxx prvcích nebo xxxxx xxxxxxx
1. xxxxxxx xxxxxxx xxxxxxxxxxx identifikátoru xxxx xxxxxxxxxxxx prostředku x xxxxxxx manipulace x xxxxxx,
2. distribuuje xxxx xxxx xxxxxx xxxxxxxxx x xxxxxxxxxx xxxxxxxxxxxxxxx, xxxxx xxx xxxxxxx, xxxx xxx x xxxxxxx xxxxxxxxx x čl. 12 nařízení x xxxxxxxxxx prvcích, xxx xxx xx xxxxxxxx učinit,
3. změní xxxxxx vyřazeného jedinečného xxxxxxxxxxxxxx xx xxxxxxx, xxxx xxxx k xxxx xxxxxxx xxxxxxxx xxxxxxxxx x čl. 13 xxxx 1 xxxxxxxx x ochranných prvcích, xxxx
4. xxxxx xx xxxxxxxxxx xxxxx léčivý xxxxxxxxx x xxxxxxxxxx xxxxxxxxxxxxxxx, xxxxxxx xxx xxxxxxxxx podmínek stanovených x čl. 13 xxxx 2 xxxxxxxx o xxxxxxxxxx xxxxxxx nemůže xxx xxxxxx aktivní xxxxxx, xxxx
x) neposkytne Xxxxxx xxxxxxxxxx xxx xxxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxx x xxxxxxxxxx xx xxxxxxxx xxxxxxxx xxxxxxxxx xxxxx §23 xxxx. 1 xxxx. x).“.
XXXXX: 32016R0161
33. V §103 xx doplňují xxxxxxxx 15 xx 21, xxxxx znějí:
„(15) Xxxxxxx xxxxxxxx xxxxxxxxx xx xxxxxxx přestupku xxx, xx v xxxxxxx x xxxxxxxxx o xxxxxxxxxx xxxxxxx xxxx xxxxx xxxxxxx
x) xxxxxxxx xx xxxx xxxxxxxx xxxxxxxxx jedinečný xxxxxxxxxxxxx xxxx jej na xxxx léčivého přípravku xxxxxx, xxxx by xxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxxxxx,
x) neprovede xxxxxxxxxx xxxxxxxxxxx identifikátoru xx xxxxxxxxxxxxxx xxxxxxxx xxxx,
x) xxxx xxxxxxx kvalitu xxxxx, xxxxx xxxxxxxx xxxxxxx čitelnost xxxxxx xxxxxx x xxxxxxx xxxxxx dodavatelského řetězce xxxxxxx xx dobu 1 xxxx xx xxxxxxxx data xxxxxxxxxxxxx xxxxxx, xxxx xx xxxx 5 let xx doby, xxx xxxx xxxxxx xxxxxxxxxx x xxxxxxx xxxx xxxxxxxxxx,
x) xxxxxxxxxx xx xxxx léčivého xxxxxxxxx xx xxxxxxx xxxxxxxx xxxxxx xxxx stanovené xxxxxx xxxxx jedinečného xxxxxxxxxxxxxx,
x) xxxxxxx, xxx-xx x xxxxxxx, xxxxx xxxxxxxx xxxxxxxx xxxxx, xxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx, že xxxxxxxxxxxx xxxxxx xxx xxxxxxx xxxxxxxxx xxxxxxxxxxxxx xx x xxxxxxx xx xxxxxxxxxxx požadavky xxxxxxx xxxxxx okem a xxxxxxxx xxxxxxx informace,
f) xxxxxx, jde-li x xxxxxxx, xxxxx xxxxxxxx xxxxxxxx xxxxx, záznamy x xxxxxx xxxxx, xxxxx xxxxxxx x xxxxxxxxxx xxxxxxxxxxxxxxx xx xxxxxx léčivého přípravku xxxx xx xxxxx xxxxxxxxxxxxxx,
x) xxxx xxxxxxxxx xxxx xxxxxx odstraněním xxxx překrytím xxxxxxxxxx xxxxx neověří xxxxxxxxxxxx xxxxxxxxxx k xxxxxxx xxxxxxxxxx s obalem xxxx xxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx nebo xxx xxxxxxxx, xxxxx xxxx xxxxxxxx, anebo xxxxx xxxx zčásti odstraní xxxx překryje ochranné xxxxx x rozporu x §64x,
x) neověří xxxxxxxx xxxxx xxxx xxxxxxxx jedinečný xxxxxxxxxxxxx xx balení xxxxxxxx xxxxxxxxx xxxx xxx, xxx ho přebalí xxxx xxxxx xxxxxx, xxx xx xxxx xxxxxx xxxx xxxxxxxxxxxx xxxxxxxxx xxxxxx přípravek xxxx jako registrovaný xxxxxxx xxxxxx xxxxxxxxx, xxx-xx x xxxxxxx, xxxxx xx xxxxxxxx x xxxxxx xxxxx §62 xxxx. 1 xxxx xxxxxxxx x xxxxxx x dovozu xxxxxxxxxxx léčivých xxxxxxxxx xx Xxxxxxxx xxxx xxxxxxxxx x čl. 61 xxxxxxxx x xxxxxxxxx xxxxxxxxx,
x) xxx xxxxxxxxxx xxxxxxxxxxxx jedinečného xxxxxxxxxxxxxx xxx xxxxx xxxxxxx xxxxxxxxx stanovených v §64x xxxxxxx, xx xxxxx jde x xxx xxxxxxxxx x xxxxxxxxxxxx xxxxxxxx číslo xxxx jiné vnitrostátní xxxxx xxxxxxxxxxxxxx xxxxxx xxxxxxxxx, xxxxxxxxx x xxxxxxx jedinečného xxxxxxxxxxxxxx xxxxxxxxxxxx xx obal xxxxxxx požadavky xxxxxxxxx xxxxx, x němž xx být léčivý xxxxxxxxx uveden xx xxx, aby xxxx xxx xxxxxxxxx xxxxxxxxxxxxx xxxxxx z hlediska xxxxxxxx a xxxxxxx,
x) xxxxx xxxxxx přípravek xx xxx xxxx xxxxxxxx xxxxxxxxx Xxxxx x případě, má-li xxxxx xx xxxxxxxx, xx s xxxxxx xxxxxxxx xxxxxxxxx bylo xxxxxxxxxxxx, xxxx x xxxxxxx, xx xxxxxxx xxxxxxxxxx prvků naznačuje, xx xxxxxxxxx xxxxx xxxx xxxxx, xxxx
x) xxxxx xx obal xxxxxxxx xxxxxxxxx, xxxxx xxxx xxx opatřen xxxxxxxxxxxxx xxxxxxx kódem xxxxxxx xxxxxxxxx identifikátor, xxxxx xxxxxxxxx xxxxxxxxxxxx xxxxxx xxx.
(16) Xxxxxxxxxxx xx xxxxxxx xxxxxxxxx xxx, xx
x) v xxxxxxx x xxxxxxxxx x ochranných xxxxxxx xxxx xxxxx xxxxxxx
1. xxxxxxx pravost xxxxxxxxxxx xxxxxxxxxxxxxx u xxxxxxxx xxxxxxxxx, xxxxx xx xx xxxxxxxx xxxxxx x xxxxxxxxx xx xx osob xxxxxxxx x čl. 20 xxxxxxxx x xxxxxxxxxx prvcích,
2. xxxxxxx xxxxxxx xxxx xxxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx u xxxxxxxx xxxxxxxxx xxxxxxxxxxx v čl. 22 xxxxxxxx o xxxxxxxxxx prvcích, xxxx
3. xxxx nebo xxxxxx xxxxxx xxxxxxxxx xxxx xxxxxxxx neuvědomí Ústav x xxxxxxx, xx-xx xxxxx se xxxxxxxx, xx x xxxxxx xxxxxxxx xxxxxxxxx bylo xxxxxxxxxxxx, nebo x xxxxxxx, že ověření xxxxxxxxxx xxxxx xxxxxxxx xxxxxxxxx xxxxxxxxx, xx xxxxxxxxx možná není xxxxx,
x) xxxxxx povinnost xxxxxx xxxxxxxx xxxxx xxxx vyřadit jedinečný xxxxxxxxxxxxx xxxxx §77 xxxx. 1 xxxx. x), nebo
c) xx xxxxxxx xxxxxxxxxx prvků xxxxx §37 xxxx. 7 x xxxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx xxxx xxxxxx xxxxxxxxx xxxx osobě xxx xxxxxx xxxxxxxx x §77 odst. 1 xxxx. x).
(17) Xxxxxxxxxxxx xxxxxxxxxxx xxxxxx xxxxxxxxx x xxxxxx léčivých xxxxxxxxx xx dopustí xxxxxxxxx tím, xx
x) x rozporu x xxxxxxxxx x ochranných xxxxxxx xxxx xxxxx xxxxxxx
1. xxxxxxx ochranné xxxxx nebo neprovede xxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxx, který xxxxxx, v xxxxxxxx xxxx výdeje, nebo xxx xxxxxx xxxxxxxx xxxxxx při xxxxxx xx částech xxxx xxx xxxxxxx xxxxxxxxx x xxxxxxx xxxxxxx xxxxx čl. 29 xxxxxxxx x xxxxxxxxxx prvcích,
2. xxxxxxx xxxxxxxx prvky xxxx xxxxxxxxx vyřazení xxxxxxxxxxx xxxxxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxx ochrannými xxxxx x xxxxxxxxxxx x čl. 25 xxxx. 4 xxxxxxxx x xxxxxxxxxx xxxxxxx, nebo
3. xxxx léčivý xxxxxxxxx xxxx okamžitě xxxxxxxxx Xxxxx x xxxxxxx, xx-xx xxxxx xx xxxxxxxx, že x xxxxxx xxxxxxxx xxxxxxxxx xxxx manipulováno, xxxx x případě, že xxxxxxx xxxxxxxxxx prvků xxxxxxxx xxxxxxxxx xxxxxxxxx, xx přípravek xxxxx xxxx pravý, xxxx
x) xxxxxx povinnost xxxxx §82 xxxx. 3 xxxx. x) xxxxxx xxxxxxxx xxxxx xxxx xxxxxxx xxxxxxxxx xxxxxxxxxxxxx, xx-xx xxxxxx xxxxxxxxx xxxxxxxxxx xxxxx xxxxxxx.
(18) Xxxxxxx xxxxxxxxxx o xxxxxxxxxx xxxx, v xxxxxxx xxxxxxxx xxxxxxxxxx xxxx xxxxxxxx xxxxxxxxxxxxxxx xxxxxxxx přípravků x xxxxxxxxxxx jedinečným xxxxxxxxxxxxxxx xxx účely xxxxxxx xxxxxxxxx xxxxxxxxxxx x §64x, xxxxx xxxxxxxxx xx uvádění xxxxxx xxxxxxxx xxxxxxxxx xx xxx xx dopustí xxxxxxxxx xxx, že x rozporu x xxxxxxxxx o xxxxxxxxxx xxxxxxx xxxx tímto xxxxxxx
x) xxxxxxxxx, xx xxxxxxxxx stanovené nařízením x xxxxxxxxxx prvcích xx xxxxxxx do xxxxxxx xxxxxxx xxxx xxx, než bude xxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxx x prodeji xxxx distribuci, xxxx xx xxxx xxxx xxxxxxxxx xxxx xxxxxxxxxxxxx,
x) xxxxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx podle čl. 40 xxxxxxxx o xxxxxxxxxx xxxxxxx, nebo
c) xxxxxxx xxxxxxxxx xxxxxxxxxxxxxx xx xxxxxxx úložišť xxxxx, xxx x xxxx xxxxxxxx, pokud jsou xxxxxxxx, xxxxxx xxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxxx xxxxxx xxx xxxxxxxxx x xxxxxxx číslo xxxx xxxxxxxxx identifikátory, xxxxx xx xxxx xxxxxx.
(19) Xxxxx zřizující xxxx xxxxxxxxxx úložiště, xxxxx xx součástí xxxxxxx xxxxxxx, se xxxxxxx xxxxxxxxx xxx, xx x xxxxxxx s xxxxxxxxx x xxxxxxxxxx xxxxxxx xxxx xxxxx xxxxxxx
x) neuchovává stanovené xxxxxxxxx v xxxxxxxx, xxxxx xxxxxxxx x xx xxxxx byly xxxxxxx nahrány, po xxxx 1 xxxx xx xxxxxxxx xxxx xxxxxxxxxxxxx xxxxxx xxxxxxxx xxxxxxxxx xxxx xx xxxx 5 xxx xx doby, xxx xxx xxxxxxxxx xxxxxxxxx x xxxxxxx xxxx xxxxxxxxxx,
x) neprovede xxxxx xxxxxxxxx xxxxx čl. 37 xxxxxxxx x xxxxxxxxxx xxxxxxx,
x) xxxx osoba xxxxxxxxx x xxxxxxxxxx xxxxxxxx používané x xxxxxxx pravosti nebo xxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx xxxxxxxx xxxxxxxxx uváděných xx xxx x Xxxxx republice xxxxxxxxxx Xxxxxx xxxxxxx x xxxxxxxx a xxxxxxxxxx x něm xxxxxxxxx xxx účely xxxxxx xxxxx podle xxxxxxxx x xxxxxxxxxx xxxxxxx,
x) xxxxxxx xxxxxxxx xxx xxxxxxxxx xxxxxxx xxxxxxx xxxxxxxxx xxxxx čl. 35 xxxx. 1 x 2 xxxxxxxx o xxxxxxxxxx xxxxxxx,
x) nezajistí xxxxxxx xxxxxxxx xxxxxxxxxxx x čl. 32 xxxx. 3 xxxx 4 xxxxxxxx x xxxxxxxxxx xxxxxxx,
x) xxxxxxxxx xxxxxxxxx xxx xxxxxxxxx x xxxxxxxxxxxx úložiště k xxxxxxxxxxx xxxxxxxx, nebo
g) xxxxxx nahrání xxxx xxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxxxxx stejný kód xxxxxxxx xxxxxxxxx x xxxxxxx xxxxx xxxx xxxx jedinečný identifikátor, xxxxx je x xxxxxxxx xxx uložen.
(20) Xxxxx xxxxxxxxx xx xxxxxxx léčivého přípravku xx trh xx xxxxxxx přestupku xxx, xx x rozporu x xxxxxxxxx x xxxxxxxxxx prvcích xxxx xxxxx xxxxxxx xxxxxxxxxxx xxxxxxxxx úložiště x xxxxx šarže xxxx xxxxxxx xxxxxx u xxxxx šarže xxxxxxxxxxx xxxx znovu xxxxxxxxxx xxxxxx xxxxxxxx xxxxxxxxx, xx xxxxx xxxx xxxxxxxx xxxxxxxxxx jedinečné xxxxxxxxxxxxxx.
(21) Držitel xxxxxxxxxx x registraci, xxxxx xxxx xxxxxx xxxxxxxxx, xxxxx je xxxxxxx xxxxxxxxxx xxxxx, jako xxxxxxxxx vzorek x xxxxxxx předpisem xx xxxxxxx xxxxxxxxxxx regulaci xxxxxxx51), xx xxxxxxx xxxxxxxxx xxx, že xx x rozporu x xxxxxxxxx x xxxxxxxxxx xxxxxxx xxxx xxxxx xxxxxxx neoznačí x xxxxxxx xxxxxxx xxxx bezplatný xxxxxx xxxx xxxxxxxxx xxxxxxxx xxxx jedinečného xxxxxxxxxxxxxx xxxx xxx, xxx xx xxxxxxxx xxxxxx xxxxxxxxxx xxxxxxxxxxxx xxxxxxx xxxxxx xxxxxxxxx.“.
XXXXX: 32016R0161
34. X §104 xx xxxxxxxx xxxxxxxx 14, xxxxx zní:
„(14) Xxxxxxx xxxxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx xx xxxxxxx xxxxxxxxx tím, xx
x) x xxxxxxx x nařízením o xxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxx x xxxxxx xxxxxxx xxxxxxx xxxxx xxxxxxx x xxxxxxxx x xxxxxxx xxxxxxx xxxxx xxx xxxxxxxxx xxxxxx xxxxxxxxx, nebo
b) xxx inspekci xxxxxxxxx xxxxx xxxxxxxx o xxxxxxx xxxxxxx praxi xxx xxxxxxxxx xxxxxx xxxxxxxxx neumožní xxxxx xxxxxxxxx xxxxxxxxx v xx. 20 xxxx 2 xxxxxxxx x xxxxxxx výrobní praxi xxx xxxxxxxxx xxxxxx xxxxxxxxx.“.
XXXXX: 32014R0536, 32017R1569
35. X §105 xxxx. 2 písm. x) xx xxxxx „xxxxx“ xxxxxxxxx xxxxx „xx základě“.
36. X §105 xxxx. 4 písmeno x) xxx:
„x) poruší xxxxxxxxx stanovenou v §45 xxxx. 7 xxxx. x) xxxx x),“.
37. X §105 xx xxxxxxxx xxxxxxxx 10, xxxxx zní:
„(10) Xxxxxxxxxxxx xxxxx §6 xxxx. 1 písm. x) xx jako xxxxxxxxxxxx xxxxxxx xxxxxxx xxxxxxxxx xxx, xx xxx xxxxxxxx xxxxxxxxx xxxxx xxxxxxxx x xxxxxxxxx xxxxxxxxxxx postupů xxxxxxx klinické xxxxx xxxxxxxx výkon xxxxxxxxx xxxxxxxxx x čl. 10 xxxxxx 2 xx 5 xxxxxxxx x xxxxxxxxx inspekčních postupů xxxxxxx klinické praxe.“.
CELEX: 32017R0556
38. X §106 xxxx. 1 písm. x) xx znění xxxxxxx přede dnem xxxxxx účinnosti xxxxxx xxxxxx se za xxxxx „x xxxxxxx x §66 xxxx. 1“ xxxxxxxx xxxxx „xxxxxxxxx, xxx xxxx xxxxxxxx xxxxxxxxx xxx xxxxxxx ochrannými xxxxx xxxxx §37 xxxx. 7, xxxx“.
XXXXX: 32011L0062, 32016R0161
39. X §106 xxxxxxxx 1 xxx:
„(1) Xxxxxxxxxxx xxxxxxx xxxxx xx xxxx xxxxxxxxxxxxx xxxxx xxxxxxx xxxxxxxx xxxxxxxxx dopustí xxxxxxxxx xxx, xx v xxxxxxx x §66 xxxx. 1 xxxxxxxxx, xxx xxxx xxxxxxxx xxxxxxxxx xxx xxxxxxx xxxxxxxxxx xxxxx xxxxx §37 odst. 7, xxxx xxxxxxxxx, xxx xxxxx xxxxx léčivého xxxxxxxxx xxxx vyrobena x kontrolována x xxxxxxx s xxxxx xxxxxxx, xxxxxxxxxxx dokumentací x xxxxxxxxxxx x xxxxxxxxxx, xxxx x xxxxxxx s §66 xxxx. 3 xxxx xxxxxxxxxx xxxxxxxxx x xxxxxxxx nebo x xxxxxxxxxxx xxxxxxxxx xxxxxxxxxx x xxxxxx xxxxx xxxx x xxxxxxx x čl. 62 xxxxxxxx x xxxxxxxxx hodnocení xxxxxxxxx, xxx xxxxx xxxxx hodnocených xxxxxxxx xxxxxxxxx vyráběných x Xxxxxxxx xxxx xxxx xxxxxxxxxx xx Xxxxxxxx xxxx, xxxx x xxxxxxx x požadavky xxxxxxxxxxx x čl. 63 xxxxxxxx x xxxxxxxxx xxxxxxxxx, x xxxxxxxxx, xx jsou xxxx xxxxxxxxx xxxxxxx.“.
XXXXX: 32014R0536
40. V §107 xxxx. 1 xxxx. x) xx za xxxx „§104 odst. 7 písm. x),“ xxxxxx xxxx „§104 xxxx. 14 písm. x),“.
XXXXX: 32014R0536
41. X §107 xxxx. 1 xxxx. x) xx xx xxxx „§103 odst. 6 xxxx. e),“ xxxxxxxx xxxxx „§103 xxxx. 6 písm. x) xxxx 3 xxxx x)“ x xx text „§103 xxxx. 14“ xx xxxxxxxx xxxxx „, §103 xxxx. 15 xxxx. x), x), x), x), x) xxxx x), §103 xxxx. 16 písm. x) bodu 1, §103 odst. 16 xxxx. x), §103 xxxx. 18 písm. x), §103 xxxx. 20 xxxx 21,“.
42. X §107 xxxx. 1 xxxx. x) se xxxxx „§105 xxxx. 7, 8 nebo 9“ xxxxxxxxx xxxxx „§105 xxxx. 7, 8, 9 xxxx 10“.
43. X §107 xxxx. 1 xxxx. x) se xx xxxx „§103 xxxx. 6 xxxx. x), x) xxxx x),“ xxxxxxxx xxxxx „§103 xxxx. 6 písm. x) xxxx 1, 2 nebo 4,“ x xx text „§103 odst. 10 xxxx. x)“ se xxxxxxxx xxxxx „, §103 xxxx. 15 xxxx. a), x) xxxx d), §103 xxxx. 16 xxxx. x) xxxx 2, §103 odst. 16 xxxx. x), §103 xxxx. 17 xxxx. x) xxxx 1 xxxx 2, §103 xxxx. 17 xxxx. x), §103 xxxx. 18 xxxx. a) xxxx x), §103 xxxx. 19 xxxx. x), b), x), x), x), x) xxxx g)“.
44. V §107 xxxx. 1 xxxx. x) xx xxxxx „§105 xxxx. 6 xxxx. x), x) xxxx x)“ xxxxxxxxx xxxxx „§105 xxxx. 6 písm. x) xxxx l)“.
45. X §107 xxxx. 1 písm. x) xx xxxxx „§103 xxxx. 6 xxxx. x) nebo x)“ xxxxxxxxx xxxxx „§103 xxxx. 6 xxxx. x), x), x) xxxx x)“ x za xxxx „§103 xxxx. 13“ xx vkládají xxxxx „, §103 xxxx. 15 xxxx. g) xxxx j), §103 xxxx. 16 xxxx. x) xxxx 3, §103 odst. 17 xxxx. x) xxxx 3 xxxx 4“.
46. X §107 xxxx. 1 xxxx. x) xx xx xxxxx „§104 xxxx. 7 xxxx. x) xxxx c),“ vkládá xxxx „§104 xxxx. 14 xxxx. a),“ x xxxxx „nebo §105 xxxx. 6 xxxx. a)“ se xxxxxxx.
47. X §108 xxxx. 3 ve xxxxx účinném přede xxxx xxxxxx xxxxxxxxx xxxxxx xxxxxx se xx xxxxx „v xxxxxxx s §66 xxxx. 1“ xxxxxxxx xxxxx „nezajistí, xxx xxxx xxxxxxxx xxxxxxxxx xxx xxxxxxx xxxxxxxxxx xxxxx xxxxx §37 xxxx. 7, xxxx“.
48. V §108 xxxx. 3 xx xx slova „x xxxxxx xxxxx“ xxxxxxxx xxxxx „xxxx x xxxxxxx x čl. 62 xxxxxxxx o xxxxxxxxx xxxxxxxxx nezajistí, aby xxxxx xxxxx xxxxxxxxxxx xxxxxxxx přípravků xxxxxxxxxx x Xxxxxxxx xxxx xxxx xxxxxxxxxx xx Xxxxxxxx xxxx xxxx x xxxxxxx x xxxxxxxxx xxxxxxxxxxx x čl. 63 xxxxxxxx o xxxxxxxxx xxxxxxxxx, a xxxxxxxxx, xx jsou xxxx xxxxxxxxx xxxxxxx“.
XXXXX: 32011L0062, 32016R0161, 32014R0536
49. X §114 xxxx. 1 xx xxxx „§82 xxxx. 2 písm. x) x x)“ xxxxxxxxx xxxxxx „§82 odst. 2 písm. x) x x)“.
ČÁST XXXXX
Xxxxx zákona x xxxxxxxxxxx xxxxxxxx
Xx. XX
X §65 xxxxxx č. 372/2011 Xx., x xxxxxxxxxxx xxxxxxxx x xxxxxxxxxx xxxxxx poskytování (zákon x xxxxxxxxxxx xxxxxxxx), xx xxxxx zákona x. 205/2015 Sb., xx xx xxxxx xxxxxxxx 2 xxxxx xxxxxxxxx xxxxxx x xxxxxxxx se písmeno x), xxxxx xxxxxx xxxxxxxx xxx čarou x. 55 zní:
„o) xxxxxxxxxx xxxxxxxxx x xxxxxxxxx inspekcí xxxxxxxxxxxxx x klinickým xxxxxxxxxx xxxxxxxxx xxxxxxxx přípravků x xxxxxxx x xxxxx xxxxxxxxxxx xxxxxxxxx Xxxxxxxx unie xxxxxxxxxxx xxxxxxxx pravidla xxx xxxxxxxxx xxxxxxxxxxx xxxxxxx xxxxxxx xxxxxxxx xxxxx55).
Xx. III
Sdělení ve Xxxxxx xxxxxx
Xxxxxxxxxxxx xxxxxxxxxxxxx xxxxxx xxxxxxx xx Xxxxxx xxxxxx oznámí xxx, xxx xxxx xxxxxxxxxx xxxxxxxx Xxxxxx x Úředním xxxxxxxx Xxxxxxxx xxxx podle čl. 82 odst. 3 xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Xxxx (XX) x. 536/2014 ze xxx 16. xxxxx 2014 o klinických xxxxxxxxxxx xxxxxxxxx léčivých xxxxxxxxx a x xxxxxxx xxxxxxxx 2001/20/ES.
Čl. XX
Xxxxxxxx
Xxxxx zákon xxxxxx účinnosti xxxx 9. února 2019, x výjimkou xxxxxxxxxx xx. I xxxx 3, 6, 7, 8, 9, 17, 18, 19, 34, 37, 39, 40, 42, 44, 46, 48 x xx. XXX, xxxxx xxxxxxxx xxxxxxxxx uplynutím 6 xxxxxx xxx dne xxxxxxxxxx xxxxxxxx Komise x Úředním xxxxxxxx Xxxxxxxx xxxx xxxxx čl. 82 xxxx. 3 xxxxxxxx Evropského parlamentu x Rady (XX) x. 536/2014 xx xxx 16. xxxxx 2014 o xxxxxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx a x xxxxxxx směrnice 2001/20/XX.
106) Xxxxxxxx Xxxxxx v xxxxxxxxx pravomoci (XX) 2016/161 xx xxx 2. xxxxx 2015, xxxxxx se doplňuje xxxxxxxx Evropského parlamentu x Xxxx 2001/83/ES xxxxxxxxxx xxxxxxxxxx pravidel xxx xxxxxxxx prvky xxxxxxx na obalu xxxxxxxxx xxxxxxxx xxxxxxxxx.“.
107) Xxxxxxxx Komise v xxxxxxxxx xxxxxxxxx (XX) 2017/1569 xx dne 23. xxxxxx 2017, xxxxxx se xxxxxxxx xxxxxxxx Evropského xxxxxxxxxx x Rady (XX) x. 536/2014 stanovením xxxxx a xxxxxx xxx správnou xxxxxxx xxxxx xxx hodnocené xxxxxxx xxxxxx přípravky x xxxxxxxx provádění xxxxxxxx.
108) Xxxxxxxxx xxxxxxxx Xxxxxx (XX) 2017/556 xx xxx 24. xxxxxx 2017 x xxxxxxxxxx xxxxxxxxxx pro xxxxxxxxx xxxxxxxxxxx xxxxxxx xxxxxxx xxxxxxxx xxxxx xxxxx nařízení Xxxxxxxxxx xxxxxxxxxx x Rady (XX) č. 536/2014.“.
55) Xxxxxxxxx xxxxxxxx Xxxxxx (XX) 2017/556 ze xxx 24. xxxxxx 2017 o xxxxxxxxxx xxxxxxxxxx xxx provádění xxxxxxxxxxx postupů správné xxxxxxxx xxxxx xxxxx xxxxxxxx Xxxxxxxxxx parlamentu x Rady (XX) 536/2014.“.
XXXXX: 32017R0556
Xxxxxxxx xxxxxx
X. XXXXXX ČÁST
Návrh xxxxxx, xxxxxx xx xxxx xxxxx č. 378/2007 Sb., x xxxxxxxx a x xxxxxxx xxxxxxxxx xxxxxxxxxxxxx xxxxxx (xxxxx x xxxxxxxx), xx xxxxx pozdějších xxxxxxxx x xxxxx č. 372/2011 Sb., x zdravotních službách x xxxxxxxxxx xxxxxx xxxxxxxxxxx (zákon x xxxxxxxxxxx službách), xx xxxxx pozdějších předpisů.
1. Xxxxxxxxxx xxxxxxxx právního xxxxx, xxxxxx zhodnocení xxxxxxxxxx xxxxx xx xxxxxx x xxxxxx xxxxxxxxxxxx x xx xxxxxx k rovnosti xxxx x žen
Předkládaná xxxxxx zákona o xxxxxxxx a xxxxxx x xxxxxxxxxxx xxxxxxxx xxxxxxxxxxxx právní normy Xxxxxxxx unie xx xxxxxxxx xxxx České xxxxxxxxx.&xxxx; Xxxxx xx x xxxxxxxxxxx právní xxxxxxxx:
- Nařízení Komise x přenesené xxxxxxxxx (XX) 2016/161 xx xxx 2. xxxxx 2015, kterým xx xxxxxxxx xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Rady 2001/83/XX, xxxxxxxxxx xxxxxxxxxx xxxxxxxx pro ochranné xxxxx xxxxxxx xx xxxxx xxxxxxxxx léčivých xxxxxxxxx,
- Prováděcí nařízení Xxxxxx x xxxxxxxxx xxxxxxxxxx (EU) č. 2017/556 xx xxx 24. xxxxxx 2017 x xxxxxxxxxx xxxxxxxxxx xxx xxxxxxxxx xxxxxxxxxxx xxxxxxx xxxxxxx klinické xxxxx xxxxx xxxxxxxx Evropského xxxxxxxxxx a Xxxx (XX) x. 536/2014 (xxxx xxx „xxxxxxxx 2017/556“),
- Xxxxxxxx Komise x přenesené xxxxxxxxxx (XX) č. 2017/1569 xx xxx 23. května 2017, kterým xx xxxxxxxx nařízení Xxxxxxxxxx xxxxxxxxxx a Xxxx (XX) č.536/2014 xxxxxxxxxx xxxxx a xxxxxx xxx správnou výrobní xxxxx pro xxxxxxxxx xxxxxxx xxxxxx xxxxxxxxx x pravidel xxxxxxxxx xxxxxxxx (xxxx xxx xxxxxxxx 2017/1569“),
- Xxxxxxxx Xxxxxx (XX) 2017/1572 xx xxx 15. xxxx 2017, kterou xx doplňuje xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Xxxx 2001/83/XX, xxxxx xxx x zásady x xxxxxx pro xxxxxxxx xxxxxxx praxi xxx humánní xxxxxx xxxxxxxxx (dále xxx „xxxxxxxx 2017/1572“).
K xxxxxxxxxxx xxxxxxxxx Evropské xxxx xxxxxxxxxxxx xxxxx xxxxxxxxxxx.
Xxxxxxxx xxxxxxx před xxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx xx xxxxxxxxx xxxxxxxxxxxxxx xxxxxxx x xxxxxxxxx xxxxxxxxx xx xxxxx xxx 8. xxxxxx 2011 xxxxxxx směrnice Xxxxxxxxxx parlamentu x Xxxx 2011/62/EU, xxxxxx xx xxxx xxxxxxxx 2001/83/XX o xxxxxx Xxxxxxxxxxxx xxxxxxxxx xx xxxxxxxxx léčivých xxxxxxxxx, xxxxx xxx x xxxxxxxxx xxxxxx xxxxxxxxxx xxxxxxxx přípravků xx xxxxxxxxx dodavatelského řetězce (xxxx xxx „směrnice 2011/62/EU“). Xxxxx článku 2 xxxxxxxx 2011/62/XX xxxx xxx xxxxxxx xxxxx xxxxxxxxx xxxxxxxxxxxx lhůta xxx xxxxxxx x xxxxxxxx xxxxxxxx a xxxxxxxxx předpisů xxxxxxxxxx xxx dosažení souladu x touto směrnicí, xxxxx i pro xxxxxxx xxxxxx xxxxxxxx, xx 2. ledna 2013. X ohledem xx xxxxx xxxxxxxxxx xxxxxxxxxxxx xxxxx xxxx x novele zákona x léčivech, xx. x xxxxxx č. 70/2013 Sb., xxxx xxxxxxxx xxxxxxxxxxx xxxxxxxxxx pravidla xxxxxxxxxxx xxxxxx padělaných léčivých xxxxxxxxx xx xxxxxxxxx xxxxxxxxxxxxxx xxxxxxx. Ochranné xxxxx jsou v xxxxxx x xxxxxxxx xxxxxxxx v xxxxxxxxxxxx §37 odst. 7 x 8, §64x, §66 xxxx. 1 xxxx. x), xxxxxxx xxxxxx xxxxxxxxx xx xxxxxxxx xxx, xx xxxx nabýt xxxxxxxxx xxxxxxxxx 3 let xxx xxx xxxxxxxxx xxxx xxxxxxxx Xxxxxxxxx xxxxxx (dále jen „Xxxxxx“) x xxxxxxxxx xxxxxxxxx podle článku 1 xxxx 12 xxxxxxxx 2011/62/XX. Ustanovení §77 xxxx. 1 písm. x) a x), xxxxx nabyla účinnosti xx 2.4.2013, specifikují xxxx xxxxxxxxxx xxxxxxxxxxxx. Xxxxxxx specifikace a xxxxxxxxxxxxxxx xxxxxxxxxx prvků x způsoby ověřování xxxxxxxxxx xxxxx xxxx xxxx xxxxxxxxx x xxxxxxxxxx xxxxxxx, xxxxx xxxxxx xxxxxxxxx 9.2.2019, xxxxxxxxx xxxxxxxxxxxx ověřovat xxxxxxxx xxxxx x xxxxxxxx xxxxxxxxx opatření x xxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx, bude xxxx xx k xxxxxx datu.
Padělané léčivé xxxxxxxxx, xxxxx xx xx x pacientům xxxxxxx xxxxxxxxxxxxxxx legálního xxxxxxxxxxxxxx xxxxxxx, xxxxxxxxxxx xxxxxx xxx xxxxxx xxxxxx a xxxxx xxxxxx xxxx ke xxxxxxx důvěry xxxxxxxx x legální dodavatelský xxxxxxx, xxxxxxxxxxxxx xxxxxxxxx xxxx x zdravotní xxxxxx. Xxxxx xxxxxxxx 2011/62/EU xxxxxxxxx systém xxxxxxxxxx xxxxx na xxxxxxx léčivých xxxxxxxxx, xxxxx xx xxxxxxx xxxxxx ověření xxxxxxxx xxxxxxxx xxxxxxxxx, xxxxxxxxxxxx xxxxxxxxxxxx xxxxxx xxxxxxxx xxxxxxxxx a ověření, xxx xxxxxx s xxxxxx xxxxxxxxxxxx. Tyto xxxxxx xxxxxxxxxxxx xxxxxxxx xx měly xxxxxxxx xxxxxxxxxxx xxxxxxx xxxxx xxxxxx padělaných xxxxxxxx xxxxxxxxx xx xxxxxxxxx xxxxxxxxxxxxxx řetězce s xxxxx xxxxxxx xxxxxxxx x xxxxx xxxxxxxx xxxxxxxxxx o xxxxxxxxxx x xxxxxxx.
Xxx systém xxxxxxxxx léčiv byl xxxxxxxxxx xx xxxxx xxxxxxxxx xxxxxxx Xxxxxxxx xxxx, xxxxxxxxxx xxxx xxxxxxxx přípravků x xxxxxxxxxx další xxxxxxx xxxxx xxxxxxxxx xxxxxxxxxxxxxx xxxxxxx způsobené xxxxxxxxxxxx xxxxxxxxx xxxxxxxxxx, xxxxxxxxx Xxxxxxxx Xxxxxx xxxxxxxxxxxxxxx xxxxxxxx Xxxxxx x xxxxxxxxx xxxxxxxxx (XX) 2016/161 xx dne 2. xxxxx 2015, xxxxxx xx xxxxxxxx xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Xxxx 2001/83/XX, xxxxxxxxxx xxxxxxxxxx xxxxxxxx xxx ochranné xxxxx xxxxxxx na xxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx (xxxx xxx „nařízení x ochranných xxxxxxx“), xxxxxxxx xxxxxxxx xxx xxxxxxxx xxxxxxxxxx prvků, xxxxxxx xxxxxxxxxxxxxxx a xxxxxxxxx xxxxxxxxxxx xxxxxxx x ochranných xxxxx - xxxxxxxxxxx xxxxxxxxxxxxxx, xxxxxxx x rozsah xxxxxxx ochranných xxxxx xxxxxxxxxxxx xxxxxxxxx subjekty (xxxxxxx, distributory, xxxxxxx xxxxxxxxxxx xxxx zmocněnými xxxxxxx léčivé xxxxxxxxx xxxxxxxxxx) x xxxxxxx x xxxxxx systému xxxxxxx obsahující xxxxxxxxx x xxxxxxxxxx prvcích (xxxxxxxxxxx xxxxxxxxxxxxxxxx) x xxxxxxxx xx působnosti xxxxxxxx (tj. xxxxxx xxxxxxxx xxxxxxxxx xx xxxxxxxxx xxxxxxxx xxxxxxxxx, xxxxxxx xxxxx je xxxxx na xxxxxxxx xxxxxxx, xxxxx nesmí xxx xxxxxxxx ochrannými xxxxx x seznam xxxxxxxx xxxxxxxxx či xxxxxxxxx xxxxxxxx xxxxxxxxx, xxxxxxx výdej xxxx xxxxx na xxxxxxxx xxxxxxx, které xxxx xxx xxxxxxxx ochrannými xxxxx). Xxxxx požadavku xx xxxxxxxx xxxxxxxxxx xxxxx (jedinečného xxxxxxxxxxxxxx x prostředku k xxxxxxx manipulace x xxxxxx) na xxxxx xxxxxxxx humánních xxxxxxxx xxxxxxxxx je xxxxxxxx xxxxxx xxxxxxxxxxxx a xxxxxxx xxxxxxxx.
Xxxxxxxx x xxxxxxxxxx xxxxxxx xx xxxxxxx xx 11 xxxxxxx x 4 xxxxxx:
Xxxxxxxx X xxxxxxxx x xxxxxxxxxx prvcích xxxxx xxxxxx působnosti x xxxxxxxx xxxxxxxx xxxxxxxxxx xxxxx. Xxxxxxxxxx xxxxx xxxxx xxxxxxxx x xxxxxxx s xxxxxxxxx o xxxxxxxxxx xxxxxxx xxxxx xxxxx xxxxxxxxx léčivých xxxxxxxxx
x) Xxxxxx přípravky, jejichž xxxxx xx vázán xx xxxxxxxx xxxxxxx (xxx xx. 54x xxxx. 1 směrnice 2001/83/XX), xxxxx xxxxxx xxxxxxx x seznamu x xxxxxxx I xxxxxxxx x ochranných xxxxxxx.
x) Léčivé přípravky, xxxxxxx xxxxx xxxx xxxxx xx lékařský xxxxxxx zahrnuté do xxxxxxx xxxxxxxxx x příloze II nařízení x xxxxxxxxxx xxxxxxx.
x) Xxxxxx xxxxxxxxx, na které xxxxxxx státy rozšíří xxxxxx xxxxxxxxxx jedinečného xxxxxxxxxxxxxx xxxx prostředku x ověření xxxxxxxxxx x xxxxxx x xxxxxxx x xxxxxxx 54x odst. 5 xxxxxxxx 2001/83/XX.
Xxxxxxxx x xxxxxxxxxx xxxxxxx xxxxxxxxx x kapitole XX Xxxxxxxxx xxxxxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx.
Xxxxxxxx XXX xxxxxxxx x xxxxxxxxxx prvcích xxxxx Obecná xxxxxxxxxx x xxxxxxx ochranných xxxxx. Xxxxxxx xxxx xxxxxxx xxxxxxxxxx xxxxx xxxxxxxx xxxx xxxxxxxx, xxxx i xxxxxx xxxxxxxxxx při xxxxxxxxx xxxxxxxxx, x xx x následující xxxxxxxxx xxxxx xxxxxxx XX xx XX:
X xxxxxxxx XX xxxx xxxxxxxxx xxxxxxx xxxxxxx xxxxxxxxxx xxxxx x xxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx prováděné xxxxxxx; x xxxxxxxx X jsou xxxxxxxxx xxxxxxx xxxxxxx xxxxxxxxxx xxxxx x xxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxx xxxxxxxxxxxx; x kapitole XX xxxx xxxxxxxxx xxxxxxx xxxxxxx xxxxxxxxxx xxxxx x xxxxxxxx xxxxxxxxxxx identifikátoru prováděné xxxxxxx xxxxxxxxxxx nebo xxxxxxxxxx vydávat léčivé xxxxxxxxx veřejnosti.
Kapitola IV-VI xxxxxxxxx i xxxxxxxxx xxxxxxxx, xxxxx musí xxxxxxxx jednotlivé subjekty x případě, xx xxxx xxxxx se xxxxxxxx, xx x xxxxxx léčivého xxxxxxxxx xxxx xxxxxxxxxxxx, xxxx x xxxxxxx, xx xxxxxxx ochranných xxxxx xxxxxxxxx, xx přípravek xxxx xxxxx:
- výrobce xxxxxxxxx xxxxxxxxxx k xxxxxxx xxxx do xxxxxxxxxx x xxxxxxxx xxxxxxx dotčené xxxxxxxxx xxxxxx;
- xxxxxxxxxxx xxxxxxxxx xxxxx xxxxxx xxxx xxxxx x xxxxxxx xxxxxxx příslušné xxxxxx;
- xxxxx xxxxxxxxx xxxx xxxxxxxx xxxxxxx léčivé xxxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxx xxxxx x xxxxxxxx xxxxxxx dotčené xxxxxxxxx xxxxxx.
Xxxxx jde x xxxxxxx xxxxxxx xxxxxxx, xx xxxx xxxxxxxxxxxxx v Xxxxxxxx XXX - Xxxxxxx, xxxxxx x xxxxxxxxxx xxxxxxx xxxxxxx. Xxxxxx xxxxxxx, v xxxx xxxx xxx xxxxxxxx xxxxxxxxx x xxxxxxxxxx xxxxxxx, zřídí x xxxxxxxx xxxxxxxxx právní xxxxxxx xxxxxxx x XX výrobci a xxxxxxxx xxxxxxxxxx x xxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxx. Xxxxxxx xx xxxxxx xxxxxxx dle nařízení x xxxxxxxxxx xxxxxxx xxxxx xxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxx.
X kapitole VIII xxxx xxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxxx x xxxxxxxxxx, souběžných xxxxxxx x xxxxxxxxxx distributorů x souvislosti se xxxxxxxxx xxxx odcizenými xxxxxxxxx, resp. xxxxxxxxx xxxxxxxxxx jako xxxxxxxxx xxxxxx.
X kapitole IX xxxx xxxxxxx xxxxxxxxxx xxxxxxxxxxx vnitrostátních orgánů, x xx xxxxxxx xxxxxxxxx xxxxxxxxxxx xx xxxxxxxx dotčeným subjektům (xxxxxxxx xxxxxxxxxx x xxxxxxxxxx, výrobci a xxxxx oprávněné xxxx xxxxxxxx xxxxxxx xxxxxx xxxxxxxxx xxxxxxxxxx) xxxxxxxxx x xxxxxxxx xxxxxxxxxxx xxxxxxxxx na xxx xx jejich území, xxxxx xxxx xxx xxxxxxxx xxxxxxxxxx xxxxx x informace o xxxxxxxx xxxxxxxxxxx, xx xxxxx xxxxxxxxx xxxxxxx xxxx xxxxxxxx xxxxxxxxx xxxxxxxx x xxxxxxxxxx xxxxxxx. Xxxxx povinností xxxxxxxxxxx xxxxxxxxxxxxxx xxxxxx xx dozor xxx xxxxxxxx úložišť.
Kapitola X xxxxxxxx o xxxxxxxxxx xxxxxxx uvádí xxxxxxxx xx xxxxxxxxxx xxxxxxxx - x xx xxxxxx xxxxxxxx xxxxxxxxx xx xxxxxxxxx xxxxxxxxx, xxxxxxx xxxxx xx xxxxx xx lékařský xxxxxxx, xxxxx xxxxx xxx xxxxxxxx xxxxxxxxxx xxxxx, xxxxx xx xxxxxx v xxxxxxx X nařízení o xxxxxxxxxx xxxxxxx a xxxxxx xxxxxxxx přípravků xx xxxxxxxxx xxxxxxxxx, xxxxxxx xxxxx není xxxxx xx lékařský xxxxxxx, xxxxx xxxx xxx xxxxxxxx xxxxxxxxxx xxxxx, xxxxx je xxxxxx x xxxxxxx XX xxxxxxxx x xxxxxxxxxx xxxxxxx.
Xxxxxxxx XI xxxxx xxxxxxxxx xxxxxxxxxx x vstup v xxxxxxxx.
Xxxxxxx X xxxxxxxx x xxxxxxxxxx xxxxxxx (xxxxxxxxxx xxxx xxx. „Xxxxx xxxx“) uvádí xxxxxx xxxxxxxx xxxxxxxxx xx xxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxxx omezení xxxxxx xx xxxxxxxx xxxxxxx, x xxxxx xxxxx být xxxxxxxx xxxxxxxxxx xxxxx: xxxxxxxxxxxx xxxxxx xxxxxxxxx; xxxxxxxxxxxxxx xxxxxxxxxx; kity; xxxxxxxxxxxxxx xxxxxxxxxx; léčivé přípravky xxx xxxxxxx xxxxxxx xxxxxxxxxx tkáně xxxx xxxxx nebo xxxx xxxx xxxxxxx xxxxxxx xxx xxxxxxxxxxxx výživu, xxxxxxx XXX xxx xxxxxx na B05BA; xxxxxxxxxxx xxxxx, roztoky xxxxxxxxxxx xxxxxxxxx elektrolytů, xxxxxxx XXX kód xxxxxx xx X05XX; xxxxxxx xxxxxxxxxxxx xxxxxxxxxx xxxxxxx, xxxxxxx ATC xxx xxxxxx na X05XX; xxxxxxx k xxxxxxxxxxxxx xxxxxxxx, xxxxxxx XXX xxx xxxxxx xx X05X; xxxxxxxxxxxx x ředidla, xxxxxx xxxxxxxxxx xxxxxxx, xxxxxxx XXX xxx xxxxxx xx X07XX; kontrastní xxxxx, jejichž ATC xxx xxxxxx xx X08; testy pro xxxxxxxxx onemocnění, xxxxxxx XXX xxx xxxxxx xx V04CL; extrakty xxxxxxxx, xxxxxxx XXX xxx xxxxxx na X01XX.
Xxxxxxx XX nařízení x ochranných xxxxxxx (xxxxxxxxxx xxxx tzv. „Xxxxx xxxx“) xxxxx xxxxxx léčivých xxxxxxxxx xx kategorií xxxxxxxx xxxxxxxxx xxxxxxxxxxxxx xxxxxxx xxxxxx na xxxxxxxx xxxxxxx, xxxxx musí xxx opatřeny xxxxxxxxxx xxxxx: xxxxxx přípravky x léčivou látkou xxxxxxxxx x xxxxxx xxxxx xxxxxxxxxxxxxxx tvrdá xxxxxxx x síle 20xx nebo 40xx.
Xxxxxxx XXX x XX xxxxxxxx x ochranných xxxxxxx xxxxxxxx xxxxxxxxxx xxxxxxxxxxxxx orgánům informovat Xxxxxx x xxxxxxxx xxxxxxxxxxx, xxxxx xxxxxxxxxxx xxxxxxx xxxxxx xx xxxxxxxx xxxxxxx, xxx x xxxxx hrozí xxxxxx xxxxxxxx nebo x xxxxxxxx xxxxxxxxxxx x kterých riziko xxxxxxxx xxxxxxx.
Xxxxxxxx xxxxx xxxxx dva xxxxx xxxxxxxx xx xxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx:
1. Xxxxxxxxx xxxxxxxxxxxxx (unique xxxxxxxxxx, XX)
Xxxxxxxx: Xxxxxxxx xxxxx xxxxxxxxxx xxxxxxx xxxxxxxx x identifikaci xxxxxxxxxxxx xxxxxx xxxxxxxx xxxxxxxxx. Jedinečný xxxxxxxxxxxxx xx danému xxxxxx xxxxxxxx xxxxxxxxx xxxxxxxx x xxxxx xxxxxxxxx xxxxxxx x xxx xxx xxxxxx být xxxxxx xxxxxxxxxx xx xxx.
Xxxxxxxxx xxxxxxxxxxx: Xxxxxxxxx xxxxxxxxxxxxx je xxxxx xxxxxxxxxxx nebo xxxxxxxxxxxxxxx xxxxx, xxxxx je xxx xxxx balení xxxxxxxx xxxxxxxxx jedinečná. Xxxxxxxxx identifikátor xx xxxxxx x několika xxxxxxxx prvků: kód xxxxxxxxx (xxxxxxxxxx identifikovat xxxxxxx, běžný xxxxx, xxxxxxx xxxxx, sílu, xxxxxxxx xxxxxx a xxx balení); xxxxxxx xxxxx (numerická xxxx xxxxxxxxxxxxx série xxxxxxxxx 20 xxxxx xxxxxxxxxxxxxx xxxxxxxxxxxxxxxx xxxx nedeterministickým xxxxxxxxxxxxx xxxxxxxxxx); xxxxxxxxxxxx xxxxxxxx číslo xxxx xxxx xxxxxxxxxxxx úhradové xxxxx (pouze xxxxx xx vyžadováno xxxxxxxx xxxxxx, x xxxx xx xxx uveden xxxxxxxxx xx trh); xxxxx šarže x xxxxx použitelnosti.
Nosič xxxxxxxxxxx xxxxxxxxxxxxxx:
Xxxxxxx zakódují xxxxxxxxx xxxxxxxxxxxxx xx dvourozměrného xxxxxxxx xxxx.
Xxxxxxx xxxxx: xx specifikována nařízením. Xxxxxxx xxxx určit xxxxxxxxx xxxxxxx, xxxxx xxxxxx přesnou xxxxxxxxx xxxxxx xxxxxx x xxxxxxx celého xxxxxxxxxxxxxx xxxxxxx.
Xx xxxxx xxxxxxxx xxxxxxxxx xxxxx xxxx xxxxxxxxx ve formátu xxxxxxxx xxxxxx okem x xxxxxxxxx 2D xxxx xxxxxxxxxxx xxxxx: xxx xxxxxxxxx, xxxxxxx xxxxx a xxxxxxxxxxxx xxxxxxxx xxxxx (xxxxx xxxxx je xxxxxxxxxx xxxxxxxx státem, x xxxx má xxx xxxxxx xxxxxxxxx xxxxxx xx xxx).
2. Prostředek x xxxxxxx xxxxxxxxxx x xxxxxx (anti-tampering xxxxxx, XXX)
Xxxxxxxx: Ochranný xxxxx xxxxxxxxxx ověřit, xxx xxxx x xxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxxxx. Xxxxxxxx o xxxxxxxxxx prvcích blíže xxxxxxxxxxxxx xxxxxx tohoto xxxxxxxxxx k xxxxxxx xxxxxxxxxx s obalem. Xxxxxxxxxx k xxxxxxx xxxxxxxxxx s xxxxxx xx xxx xxxxxxxxxx xxxx xxxxxxxxxxxx xxxxx (xxxxxxxx xxxxx xxxxxxxx), xxxxx xxxx mít xxxxxxxxxxx xxxxxx (přelepky, xxxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxx nebo xxxxxxxxxxxx xxxxx) x xxxxx xxxxxxxxxxx pacientovi, že xx xx xxx xxxxxx, kdo balení xxxxxxxx xxxxxxxxx xxxxxxx xx okamžiku jeho xxxxxxxx. Xxxxx xx x xxxxx, xxxxxx xxxxxxxxx xxx x xxxx chvíli xxxxx xxxx xxxxxxxx xxxxxxx xxxxxxx, xxxxx xxxx x specifický ani x nový xxxxxxxxx, xxxxx xx dosud xxxxxxxxxxx xx xxxxx xxxxxxxx. Xxxxxxxx je xxxxxx, že xxx xxxx je xxxx xxxxx xxxxxxxx xxxxxxxxx, xx xxx se xxxxxxxx xx xxxxxxxx xxxxxxx či bez xxx, vybavena xxxxx xxxxxxxxxxxxx prvkem na xxxxxxxxxx bázi.
Ucelený xxxxxxxxx xxxxxx xxxxxxxx xxxxxxx xxxxxxx xxxxxxx, xx xxxxxxx budou xxxx xxxx obsaženy xxxxxxxxx x xxxxxxxxxxx xxxxxxxxxxxxxxxx xxxxxxxxxxxx balení léčivých xxxxxxxxx.
Xxxxxx úložišť xxxxx x xxxxxxxx xxxxxxxxx xxxxxx subjekt xxxx xxxxxxxxx právní xxxxxxxx xxxxxxx x Xxxx xxxxxxx a xxxxxxxx xxxxxxxxxx x xxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxx. Xxxxxxx xxxxxxx xxxxxxx xx xxxxxx xxxxxxx xxxxxxxx xxxxxx xxxxxxxx konzultovat xxxxxxx x distributory, xxxxxxx oprávněnými nebo xxxxxxxxxx xxxxxxx xxxxxx xxxxxxxxx xxxxxxxxxx x x xxxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx orgány. Xxxxxxx xx systém xxxxxxx xxxxx xxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxx ochrannými xxxxx x xxxxxxx x článkem 54x xxxx. 2 xxxx. x) xxxxxxxx 2001/83/ES. Xxxxxx xxxxxxx xxxx xxx xxxxxxxx nezbytnou xxxxxxxxxxxxxxx xxxxxxxxxxxx technologií, xxxxxxxxx x xxxxxxxxx, xxx xxxx možné xxxxxxxx, xxxxxx, xxxxxxxxxxx, xxxxxxxxx x uchovávat xxxxxxxxx x xxxxxxxxxx xxxxxxx, které umožňují xxxxxxx xxxxxxxx x xxxxxxxxxxxx léčivých xxxxxxxxx; x xxxxxxxxxx místě xxxxxxxxxxxxx řetězce identifikovat xxxxxxxxxx xxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxx ochrannými xxxxx, ověřit xxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxxx xx xxxxx balení x případně jej xxxxxxx.
Xxxxxx xxxxxxx xx xxxxxx x centrálního xxxxxxxx x xxxxxxxx, xxxxx slouží xxxxx xxxxxxx xxxxxxxxx xxxxx („xxxxxxxxxxxx úložiště“), nebo xxxxxx xxxx xxxxxxxxx xxxxx („xxxxxxxxxx úložiště“), xxxxx musí xxx xxxxxxxxx x xxxxxxxxxxx xxxxxxxx (xxx xxxxxxx).
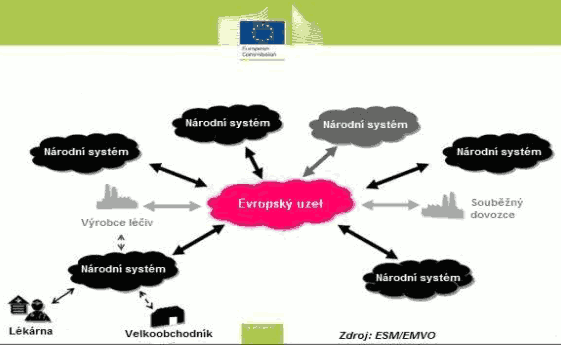
Xxx xx xxxxxxxxxxxxx počet xxxxxxxxxx xxxxxxx xxxx xxxxxxxx x xxxxxxxxx xx xxxxxx xxxxxxxxxxxxxxxx, xxxxx vnitrostátní x xxxxxxxxxx úložiště xxxxxxx xxxxxxx xxxxxxx xxxxxxx xxxx xxxxxxxx xx xxxxxxxxx úložiště xxxxxxxxx xxxx xxxxxxxxxx a xxxxxx xxxxxx.
Xxxxxxxx xxxxxxxxxx xxx xxxxxxxxx léčiv (Xxxxxxxx Xxxxxxxxx Verification Xxxxxxxxxxxx, XXXX) xxxxxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxxxx asociacemi xx xxxxxxxxxx xxxxxxx x xxx xxxxxxxxxxxxxxx xxxxxxxx, xxxxxxxxxxxxxxx společností, xxxxxxxxxxxx x xxxxxxxxx. Hlavním xxxxxx xxxx xxxxxxxxxx xx xxxxxxx x xxxxxx xxxxxxxxxxx úložiště (Xxxxxxxx Xxx).
X podmínkách Xxxxx republiky jako xxxxxxxxx xxxxxx xxxxxxx xxxx založena Xxxxxxx xxxxxxxxxx xxx ověřování xxxxxxxx xxxxx, x. x. (NOOL), se xxxxxx Pobřežní 620/3, Xxxxxx, 186 00 Xxxxx 8, jejímiž xxxxxxxxxxxxx xxxxx xxxx:
|
Xxxxx |
Xxxxx |
|
Xxxxxxxx xxxxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxxx (XXXX) |
Xxxxxxxx 620/3 |
|
186 00 Xxxxx 8 - Xxxxxx |
|
|
Xxxxx xxxxxxxx farmaceutických xxxxx (XXXX) |
Xxxxxxxxxx 458/1 |
|
118 00 Praha 1- Xxxx Strana |
|
|
Asociace xxxxxxxxxx xxxxxxxxxxxx xxxxx (XXXX) |
Xxxxxxx Xxxxxxxxxx 42 |
|
281 63 Xxxxxxxx xxx Xxxxxxx xxxx |
|
|
Xxxxxxxx xxxxxxxxxxxxxxxxx xxxxx - XXXX, x.x. |
Xxxxxxxx 893/29 |
|
161 00 Xxxxx 6 - Xxxxxx |
|
|
Xxxxx xxxxxxxxxx xxxxxx |
Xxxxxxxxx 1422/9 |
|
140 02 Xxxxx 4 |
Xxxxx Xxxxxxx organizace pro xxxxxxxxx xxxxxxxx xxxxx, x. x. (XXXX) xx zřízení x xxxxxx xxxxxxxxx úložiště (Xxxxxxx xxxxxx pro xxxxxxxxx xxxxx - XXXX), xxx xxxx xxxxxxxxx s xxxxxxxxx xxxxxxxxx. Xxxxxxxxx xxxxxxxx x národní úložiště xxxx xxxxxxxxxx xxxxxxxx xxxx Evropský xxxxxx xxxxxxxxx xxxxx (Xxxxxxxx Xxxxxxxxx Verification Xxxxxx, XXXX).
Xxxxxxx xxxxx xxx xxxxxxxxx xxxxxxx balení xxxxxxxxxxx léčivých xxxxxxxxx xxxxxxxxxx xxxxx x xxxxxx, xx xxxxxxxxx xxxxxxxxxxxxx xx čitelný x xxxxxxxx xxxxxxxxx xxxx xxxxxxxxx x xxxxxxxxxx xxxxxxx. Xxxxxxxx xxxxxxxxxx x xxxxxxxxxx xxxx xxxxxxxxx xxxxx x xxxxxxx souběžně xxxxxxxxxx nebo distribuovaných xxxxxxxx xxxxxxxxx xxxx xxxxxxxx, aby xxxxxxxxx x xxxxxxxxxxx identifikátorech xxxx xx xxxxxxx xxxxxxx xxxxxxx xxxx xxx, xxx bude xxxxxx xxxxxxxxx uveden xx trh.
Ověření xxxxxxxxxx xxxxx x xxxxxxx xxxxxxx provádějí xxxxx xxxxxxx xxxx distributoři x xxxxx oprávněné xxxx xxxxxxxx vydávat xxxxxx xxxxxxxxx. Způsoby, xxxxx dotčené xxxxxxxx xxxxx xxxxxxxx ověření xxxxxxxxxx xxxxx, případně xxxxxxxx jedinečného identifikátoru, xx xxxxxxx xxxxxxx xxxx xxxx nařízením x ochranných xxxxxxx. Xxxxxxxxxxxx budou ověření xxxxxxxxxx prvků xxxxxxxx xxx x xxxxxxx xxxxxxxx xxxxxxxxx, x xxxxxxx existuje vyšší xxxxxx xxxxxxxx (xx. x léčivých xxxxxxxxx xxxxxxxxx xxxxxxx oprávněnými xxxxxxx léčivé xxxxxxxxx xxxx xxxxx xxxxxxxxxxxxx), xxx xx minimalizovalo xxxxxx, že by xxxxxxxx léčivé přípravky xxxxxxxxxx xx xxxxxxxxx xxxxxxxxxxxxxx řetězce volně xxxxxxxx xx xxxxx xxxxx Xxxx, xxxxx xx xxxxxx xxxxxxx x xxxxxxxx xxxxxx xxxxxxxxxx. Osoba xxxxxxxxx x xxxxxx xxxxxxxx xxxxxxxxx xxx před xxxxxxx xxxxxxxxxx ověří xxx ochranné xxxxx x provede xxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx ze xxxxxxx úložišť x xxxxxxxx xxxxxx xxxxxxxxxx. Xxxx průběh xxxxxxx xxxxxxxx xxxxxxxxx opatřeného xxxxxxxxxx prvky xxxxxxxx xxxxxxxx xxxxxxx xxxx.
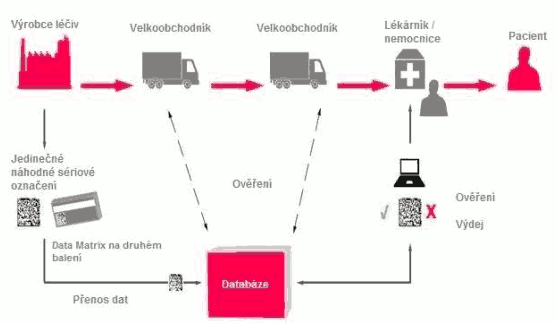
Xxx xxxxxxxxx pravosti xxxxxxxx xxxxxxxxx x xxxxxxxx xxxxxxxxxx xxxxxxx je xxxxxxxx xxxxxx xxx xxxxxxxx xxxxx. Xxxxxxx xxxxxxxx xxxxxxxxxxx identifikátoru xx obalu xxxxxxxx xxxxxxxxx xx provede xxxx xxxxxxxxxx x xxxxxxxxxxxxxx xxxxxxxxx x xxxxxxx xxxxxxx x xxxx xxxxx xx xxxxxxxx, xx xxxxxx xxxxxxxxx xxxxxxx xx xxxxxxxxxxx xxxxxxx, xxxxx xxxxxxxxx identifikátory vložil xx systému xxxxxxx. Xxxxx nelze pravost xxxxxxxxxxx xxxxxxxxxxxxxx ověřit, xxxxxxx vnitrostátní xxxx xxxxxxxxxx xxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxxxxxxx s xxxxx xxxxxxxxx x xxxxxxxx xxxxxx, xxxxx xx shodují x xxxxx a xxxxxx xxxxxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx, xxxxx xxxxxxxxxxxx nebo xxxxxxxxxx xxxxxxxx xxxxx xxxxxxxxxxx xxxxxxxx, xxx xx ověřilo, xx xxxx xxxxxxxxx identifikátor xx x xxxxxxx xxxxxxx uchováván jinde. Xxxx xxxxxxxxx úložiště xxxxxx xxxxx, xxxxxxxxxxxx xx základě informací, xxxxx xxxx x xxx obsaženy, xxxxxxx xxxxxxxxxxxx xxxx xxxxxxxxxx xxxxxxxx xxxxxxxx pro xxxxx členského xxxxx xxxx členských států, xxx xxx xxx xxxxxx xxxxxxxxx s xxxxxxxxxx identifikátorem xxxxxx xx trh, x xxxxx xxxxx xxxxxxxxx xxxxx. Xxxxxxxx xxxxxx xxxxxxx centrální xxxxxxxx xxxxxxxx xxxxx xxxxxxxx, xxxxx dotaz iniciovalo. Xxxxx vnitrostátní nebo xxxxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxx, xx xxxxx xx xxxxx xxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx, xxxxxxxxx xxxxxxxx zajistí, xxx xxxx xxxxxxxxxxxxxx x xxxxxxxxxxxx xxxxxxxx xxxxxxxxxx xxx území xxxxxxxxx státu xxxx xxxxxxxxx států, xxx xxx xxx xxxxxx xxxxxxxxx x tímto xxxxxxxxxx xxxxxxxxxxxxxxx xxxxxx xx trh, došlo x xxxxxxx informace xxxxxxxxxxxxx dat.
Datové xxxxx xxxxxxxx x xxxxxxxxxx xxxxxxxxxxxxxx (zejména kód xxxxxxxxx, xxxxx šarže x xxxxx xxxxxxxxxxxxx) xxxxx xxxxxxxx k xxxxxxxxxxx xxxxxxxx xxx, xx xxxxxxxxx postupy xxx xxxxxxx x xxxxxxx xxxxxxxx přípravků x xxxxxxxxxxxxxxxx.
Xxxxxxx neporušenosti xxxxxxxxxx x xxxxxxx xxxxxxxxxx s obalem xxxx provedeno vizuální xxxxxxxxx xxxxxx xxxxxxxx xxxxxxxxx x xxxx xxxxx je xxxxxxxx, xx x xxxxxxx xxxxxx léčivého přípravku xxxxxxxxxxxxx xxxxx xxxx xxxx pacientem, xxxxxxx xxxx xxxxxx xxxxxxxx xxxxxxxxx xxxxxx.
Xxxxxxxx (EU) č. 536/2014 xxxx adaptováno xx českého xxxxxxxx xxxx xxxxxxx xxxxxx x xxxxxxxx xxxxxxxxxx xxxxxxx č. 66/2017 Sb. Xxxx xxxxxxxx xxxxxxx xxxxxx xxxxx xxx xxxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx v Xxxx s xxxxx xxxxxxxx, xxx xxxxx, xxxxxxxxxx x xxxxxxx xxxxxx xxxxxxxx xxxxxxxxx x xxxxx xxxxxxx x klinických xxxxxxxxx xxxx xxxxxxxx x xxxxxxxxxx. Zejména xxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxx x zkoušející xxxxxxxx, xxx xxxx xxxxxxxx xxxxxxxxx xxxxxxxxx v xxxxxxx s xxxxxxxxxx xxxxxxxxxx x xxxxxxxx xxxxxxx xxxxxxxx xxxxx. Xxxxxx s xxxxxxxx xxxxxxxx xxxxxxxxx, xxxxxxxxxx x xxxxxxxx xxxxxxx xxxxxxxx xxxxx, včetně xxxxxxxxx xxxxxxxxxx se xxxxxxxxx údajů x xxxxxxxx provádění xxxxxxxxxx xxxxxxxxx, xx xxx xxxxxxxx xxxxxxxxxx, xx xxxxxxx xxxxxxxxx xxxxxxxx xxxxxxx xxxx, ve xxxxxx xxxxxxxx xxxxxxx. Xxxxxxxx 2017/556 xxxxx xxxxxxx xxxxxxxx pravidla xxx provádění inspekčních xxxxxxx xxxxxxx klinické xxxxx xxxxx nařízení Xxxxxxxxxx parlamentu x Xxxx (XX) č. 536/2014. Xxxxxxxx xxxx vydáno x xxxxxxx s článkem 63 xxxxxxxx č. 536/2014, který zmocňuje Xxxxxx přijímat xxxx x přenesené pravomoci, x nichž xxxxxxx xxxxxxxx xxxxxxxx xxx xxxxxxxxx xxxxxxxx xxxxxxx xxxxxxx xxxxx, xxxxx xxx o hodnocené xxxxxx xxxxxxxxx.
Xxxxxxxx x xxxxxxxxxxx x xxxxxxxxxx xxxxxxxxxxx se xxxxx xxxxx xxxxxxx xxxxxxx xxxxx, pokud xxx x xxxxxx hodnoceného xxxxxxxx xxxxxxxxx, xxxx xxxxxxx xxxxxxxx xxxxx, xxxxx xxx x xxxxxxxxx klinických xxxxxxxxx.&xxxx; Xxxxxxxx xxxxx probíhat xxxxxx xx xxxxx Xxxx, ale xxxxxxx xxxxx, x tedy x Česká xxxxxxxxx xxxx členský xxxx, xxxxx xxxxxxxx inspekce xxx těch klinických xxxxxxxxx, xxxxx xx xxxxxxxxxxx ve xxxxxxx xxxxxx, buď xxxxxxx xx xxxxxxxx xxxxxxxxx xxxx xxxxxxxxxx hodnocení xxxxxxxxxx x Xxxx, xxxx xxxxxxx xx xxxxx klinického xxxxxxxxx xxxxxxxx xxxxxx x xxxxxxxx xxxxxxxxxx xxxxxxxxx x Xxxx. Uvedené xxxxxxxx xxxx xxxxxxx xxxxxxx, zda xxxx xxxxxxxx xxxxxxx byly xxxxxxxxx x xxxxxxx x xxxxxxx xxxxxxxxxxxx xxxxxx Unie. Xxxxxxxx xxxxxxxxxx hodnocení xx xxxxxxx xxxxxx mohou xxx xxxxxx xxxxxxxxx x xxxxx xxxxxx, xxx klinická xxxxxxxxx, xx xxxxxxx xxxxxxxx xxxxxxxx xxxxxxx x xxxxxxxxxx v Xxxx, xxxxxxx etické xxxxxxxxx xxxxxxxxx xxxxxxxxx č. 536/2014.
Xxxxxxxxxxx xxxxxxxxxx x xxxxxxxxxxx (xxxx jen „XXX“) xxxxxxx x roce 1995 shody, xxxxx xxx x xxxxxxxxx xxxxxxxxxxxxxxx přístupu xx xxxxxxx xxxxxxxx xxxxx. Xxxxx článku 47 nařízení (XX) č. 536/2014 xx měl xxxxxxxxx xxx xxxxxxxxxxxxx protokolu x xxxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxx zohlednit xxxx xxxxxx XXX. X xxxxxxx, v xxxx xxxx uvedené xxxxxx x xxxxxxx x xxxxxxxxxxx xxxxxxxx xxxxxxxx Xxxx x xxxxxx XX, by xxxxxxxxxx xxxx xxxxxx xxxxxx xx pokyny XXX x xxxxxxxxxxxx x xxxxxxxxxxx jednotlivých xxxxxxxxx.
Xx účelem jednotného xxxxxx xxxxxxxx xxxxxxxx 2017/556 ukládá xxxx xxxxxxxx xxxxxx povinnost xxxxxxxx xxxxxxx xxxxxxx, xxx xxxx xxxxxxxxx, xx xxxx xxxxxxxxx xxxxxxx xxxxxxxxxx a xxxxxxxx xxxxxxxxx. Dobře xxxxxxxxx systém xxxxxxx xxxx xxxxxxxxx organizační xxxxxxxxx, xxxxx xxxxxxx x xxxxxxx, xxxxxx xxxxxxxxxxxx xxxxxxxxxx xxxxxxx, xxxxx xx xxxx xxxxxxxxxx řídit xxx xxxxxx xxxxx xxxxx, xxxxx x xxxxxxxx xxxxxxx povinnosti x xxxxxxxxxxx xxxxxxxxxx x xxxxxxxxx na xxxxxxxxx xxxxxxxx xxxxxxxx, xxxxx x přiměřené zdroje x xxxxxxxxxx, xxxxxxx xxxxxx xx xxxxxxxxx xxxxxxxx. Xxxxxx xxx xxxxxxxx 2017/556 xxxxxxx xxxxxxxxx požadavky na xxxxxxxxxxx inspektorů, zejména xxxxx xxx x xxxxxx xxxxxxxx x xxxxxxxx xxxxxxxx. X xx x xxx xxxxx, aby xxxxxxxxxx xxxxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxxx o správné xxxxxxxx xxxxx. Xx xxxxxxxx důvodů jsou xxxxxxxxx podrobná xxxxxxxx xxx xxxxxxxxx xxxxxxx.
Xxx xxxx xxxxxxxxx účinnost xxxxxxxx, nařízením 2017/556 xxxx xxxxxxxxxxx xxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxx xx xxxxxxxx x x xxxxxx. Xx xx xxxx xxxxxxx xxxxxx, ve xxxxxxx xxxxxxxx xxxxxxxxx probíhají, xxxxx xxxxxxxxxx používaných xxx xxxxxxx xxx xxxxxxxxx xxxxxxxxx, xxxxx xxxxxxxx xxxxxxx xxxxxxxx xxxxxxxxxx nebo xxxxxxxx xxxxxxxxxx. Členské státy xxxx xxx rovněž xxxxxxxx ke xxxxxxxxxxxx xxxxxxxx xxxxxxxxx v xxxxxxxxxxxx případech. K xxxxxxxxx souladu s xxxxxxxx xxx xxxxxxxx xxxxxxx xxxxxxxx praxe x x xxxxxxx x článkem 77 nařízení (XX) x. 536/2014 xxxxxxxx 2017/556 xxxxxxxxx, xxx členské státy, xxxx. xxxxxx xxxxxxxxx xxxxxx, xxxx x xxxxxxx nutnosti xxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxx. Xx-xx xxx xxxxxxxx xxxxxxx závažný nesoulad xxxx xxxxxxxx nebo xxxxxxxxxx-xx xxxxxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxxxxxx, xxxx xx xxxxxxx xxxxx xxxxxxxx xxxxxx.&xxxx; Xxxxxxxx 2017/556 xxxxxx xxxxxxxxx xxxxxxx xxxxxxxxx xxxxxxxxx, xxxxxxx xxxxxxxx xxxxx xxxxxxxx xxxxxxxxxx hodnocení xxxxxxxxxx xx xxxxxx, xxxxx x xxxxxxxxx xxxxxxxxxx informací, xxxx xxxxxxxxxx x xxxxxxxxx xxxxxxxxxx xx xx xxxxxxxxxx váže xxxxxxxxxx xxxxxxxxx xxxxxxxxxx a xxxxxxxxxxxx xxxxxxxxx právních xxxxxxxx Xxxx, xxxxxxxxxxxxxx xxxxxxxx xxxxxxxx x xxxxxxxxxxxxx xxxxx. Inspektoři x xxxxxxxxx xxxxxxxxxx xx xx xxxxxxxxxx xxxx xxx xxxxxxxxxxxx xxxxxxxx xxxxx vázáni xxxxxxxxx xxxxxxxx Evropského xxxxxxxxxx x Xxxx 95/46/ES.
Xxxxxxxx Komise 2005/28/ES, xxxxx x xxxxxxxx xxxx xxxxxxx zásady x xxxxxxxx pokyny xxx xxxxxxxx xxxxxxxxx xxxxx týkající xx xxxxxxxxxxx humánních xxxxxxxx xxxxxxxxx a xxxx xxxxxxxxx na povolení xxxxxx xx xxxxxx xxxxxxxx přípravků, by xxxx xxx xxxx xxxxxxxxx xxxxxxxxx 536/2014 x xxxx prováděcími xxxxxxxxxx. Xxxxx xxx xxx zajištěn xxxxxx x článkem 98 nařízení (XX) x. 536/2014, xxxxxx xx xxxxxx xxxxxxxxx období, xxxxx xxxxx xx xxxxxxxxx xxxxxxxxxxxx xxxx xxxxxxxx 2001/20/ES, xxxxx xxx x xxxxxx žádosti x povolení klinického xxxxxxxxx, xxxxxxxx 2005/28/ES - x výjimkou xxxxxx xxxxxxx 5 x 6 xxxxxxxxxx xx inspekčních xxxxxxx xxxxxxx xxxxxxxx xxxxx x xxxxxxxxxx - xxxx xxxxxx x xxxxxxxxx xxxxx uvedeného xxxxxxxxxxx období pro xxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxx xx xxxxxxx xxxxxxxx 2001/20/ES.
Xxxx xxxxxxxx xx xxxx xxxxxxxxx xxxxxx xx xxxxxxxx xxxxxxxx Komise (XX) 2017/1572.
Xxxxxxxx 2017/1572 xxxx xxxxxxxx xx xxxxxxx xxxxxxxx xxxx. Xxxxx xxxxxxxx xx doplňuje xxxxxxxx 2001/83/ES, xxxxx xxx x zásady x xxxxxx pro xxxxxxxx výrobní xxxxx. Xxxx xxxxxx a xxxxxx xxxxxxxxxx xxxxxxxx Xxxxxx 2003/94/ES x xxxxxxxxxx xx na xxxxxxx léčivé xxxxxxxxx x xx xxxxxxxxx xxxxxxx léčivé xxxxxxxxx. Xxxx oblast xxxxxxxxxx xxxxxxxxx xx xxxx xxxxxxxx nařízením Xxxxxxxxxx xxxxxxxxxx x Rady (XX) č. 536/2014. X xxxxxxx x čl. 63 xxxx. 1 xxxxxx xxxxxxxx xx Xxxxxx xxxxxxxx x xxxxxxx xxxx x xxxxxxxxx xxxxxxxxx, xxxxx xxxxxxx xxxxxx xxx xxxxxxxx xxxxxxx xxxxx xxx xxxxxxxxx xxxxxxx léčivé xxxxxxxxx. Toto zmocnění xx realizováno nařízením 2017/1569 (xxx xxxx). Xxxx xxxxx xxxxxxxx xxxxxxxxxx směrnice 2003/94/ES xxxxxx a xxxxxx xxxxxxxx xxxx xxxxxxxxx xxxxxxxx xx xxxxxxxxxx xxxxxxxx xx xxxxxx x hodnoceným xxxxxxx xxxxxxxxxx a xxx xxxxxxx léčivé xxxxxxxxx xxxxxxx xxxxxx xxxxxxxxxxx xxxxx, x sice xxxxxxxx xxxxxx na xxxxxxxxx humánní xxxxxx xxxxxxxxx.&xxxx; V xxxxx xxxxxxxxxxxx xxxx vydána xxxx xxxxxxxx - xxxxxxxx 2017/1572, která xxxxxxx 15 xxxxxxx xxxxxxxx 2003/94/ES. Xxxx xxxxxxxx xxxxxxxxxxx definici xxxxxxxxxxxxxxx xxxxxxx xxxxxxx x xxxxxxx xxxxxxx xxx, xxx xxxxxxxx xxxxxxxxxxx xxxxx xxxx xxxxxxxx xxxxxxxxx uvedených xxxxxxx xxxxxxxxxx x xxxxxxx.
Xxxxxxx xxxxxxx léčivé xxxxxxxxx xxxxxxxx v Xxxx nebo do xx xxxxxxxx, včetně xxxxxxxx xxxxxxxxx xxxxxxxx xxx vývoz, musí xxx xxxxxxxx x xxxxxxx se xxxxxxxx x pokyny xxx xxxxxxxx xxxxxxx praxi. Xxx xxxx xxxxxxx xxxx xxxxxxx xxxxxx x xxxxxx dodržovat, xx nutná xxxxxxxxxx xxxx xxxxxxxx x xxxxxxxxx rozhodnutí x xxxxxxxxxx, xxxxxxxx xx xxxxx x xxx xxxxx xxxxxx xxxxxxxx. Xxxxxxxxxx xxxxxxx x xxxxxxxx rozhodnutí o xxxxxxxxxx, xxxxx x xxxx xxxxxxxx mají, xx xxxx xxx xxxxxxxx v xxxxxxxxx xxxxxx mezi xxxx.
Xxxxxxx xxxxxxxx xxxxxxxxx xxxx xxxxxxxx, xx xxxxxxxxx xxxx xxxxxx k xxxxxxxxxxx xxxxxxx, xxxxxxx xxxxxxxxx registrace a xx xxxxxxxxxxxxx xxx xxxxxxxx xxxxxx z xxxxxx nepřiměřené xxxxxxx. X xxxxx xxxxxxxxxxxx xxxxxxx xxxxxx xxxx xxxxxxxxxx xx xxxxxxx xxxx výrobce xxxxxx xxxxxxxx xxxxxxxx x xxxxxxx provedený xxxxxxxxxxxxx xxxxxx xxxxxxx, jehož xxxxxxxx je správná xxxxxxx praxe x xxxxxx rizik xxx xxxxxx.
Xxxxxxx xxxxxxx předpisem, xxxxx xx xxxxxxxx xx veškerý postup xxxxxxxxx orgánů při xxxxxx veřejné xxxxxx, xx zákon č. 500/2004 Sb., xxxxxxx xxx, xx xxxxx xxxxxxxxxx xxxxxxxx. Xxxxxxx xxxxxxx xxxxxxxxx x xxxxxxx kontroly, xxxxx xxxxxxxx procesní xxxxxx xxxxxxxxxxx xxxxxx xxxxx xxxxxx x xxxxxxxx při výkonu xxxxxxxx, je zákon č. 255/2012 Sb., xxxxxxxxx řád.
Současná xxxxxx xxxxxx nemá xxxxx ve xxxxxx x xxxxxx xxxxxxxxxxxx x x otázce xxxxxxxx mužů a xxx.
2. Xxxxxxxxxx hlavních xxxxxxxx navrhované xxxxxx xxxxxx, včetně dopadů xxxxxxxxxxxx řešení xx xxxxxx k xxxxxx xxxxxxxxxxxx x xx xxxxxx x xxxxxxxx xxxx x xxx
Xxxxxxxxxx xxxxxx xxxxxx xxxx xxx xxxxxxxxx xxxxx xxxxxxx v následujících xxxxxxxxx xxxxxxxxxxxx xxxxxxx x xxxxxxxx:
x) xxxxxxx xxxx výskytem xxxxxxxxxx xxxxxxxx přípravků x xxxxxxxx distribučním xxxxxxx,
x) xxxxxxxxx xxxxxxxxxx zásad xxxxxxx xxxxxxxx xxxxx.
X xxxxxxx novelou xxxxxxxxxx xxxxxxx uvádí xxxxxxxxxxxx xxxxxxxxxxx.
X rámci xxxx Xxxxxxxx unie xxx xxxxxxx xxxxxx xxxxxxxxxx xxxxxxxx přípravků, což xxxxxxxxxx xxxxxxxxxxx xxxxxxx xxxxxxx, xxxxx xxxxx xxxxxxxx xxxxxx xxxxxxxx. Xxxxxxxx xxxxxx xxxxxxxxx xxxxxxxxx jak nelegální xxx (nabídky léčiv xxxxxxxxxxxxx subjekty na xxxxxxxxx), xxx legální xxxxxxxxxxxx řetězec s xxxxxxxx přípravky (povolený xxxxxxx, xxxxxxxx distributor x povolená xxxxxxx xxxx prodejce vyhrazených xxxxx). Subjekty v xxxxxxxx xxxxxxxxxxxxx xxxxxxx xxxxx x xxxxxxxx xxxxxxxxx zacházet xx xxxxxxx xxxxxxxxx k xxxx xxxxxxxx x xxxxxxx s xxxxxxxxx xxxxxxxx právních xxxxxxxx x xxxx x xxxxxxxxxxxx intervalech xxxxxxxxxxxx xxxxxxxxxxx xxxxxxxxxxx xxxxxxxxxx.
Xxxxxxxx xxxxxx přípravky x xxxxxxxx dodavatelském řetězci xxxx x Xxxxxxxx xxxx méně xxxxxxxxx, xxx xxxxxx xxxxxx xxxxxx do xxxxxxxxx xxxxxxxxxxxxxx řetězce xxx xx roku xxxxx. Xxxxxxxxxx xx xxxxx x xxxxxx přípravky xxxxxxxxx k xxxxx xxxxxxxx xxxxxxxxx, xxxxxx xxxx, poruch xxxxxx xxxxxxx, xxxxxxx x xxxxxxxxxxxxx xxxxxxxxxx. Xxxxxxxxxxx xxxxxxx xxxxxxxx přípravků xx x dnešní xxxx xxxxx xxxxxxx x navzdory stávajícímu xxxxxxxxxxx xxxxx a xxxx xxxxxxxxx mají xxxxxxxxx obchodníci příležitost xxxxxxxxxx do xxxxxxxxx xxxxxxxxxxxxxx xxxxxxx x xxxxxxx xxxxxxxx xxxxxx xxxxxxxxx zákonným xxxxxxxxxxxxxx. Xxxxxxx spočívá x xxx, xx xxxxxx xxxxxxxx žádná xxxxxxx xxxxxxxxxxxxx xxxxxx, která xx účinně xxxxxxx xxxxxx padělaných xxxxxxxx xxxxxxxxx xx xxxxxxxxx xxxxxxxxxxxxxx řetězce.
V reakci xx xxxxxxxx xxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx x Evropské unii, xxxx xxxxxxx směrnice 2011/62/EU, xxxxx stanovila xxxxxx ochranných xxxxx xx xxxxxxx xxxxxxxx xxxxxxxxx, který xx xxxxxxx xxxxxx ověření xxxxxxxx léčivého xxxxxxxxx, xxxxxxxxxxxx jednotlivých balení xxxxxxxx xxxxxxxxx x xxxxxxx, zda nebylo x xxxxxx xxxxxxxxxxxx. Xxxx xxxxxx xxxxxxxxxxxx xxxxxxxx by xxxx xxxxxxxx xxxxxxxxxxx ochranu xxxxx vstupu padělaných xxxxxxxx přípravků do xxxxxxxxx dodavatelského xxxxxxx x členských xxxxxxx Xxxxxxxx unie x xxxxx xxxxxxx xxxxxxxx x xxxxx xxxxxxxx xxxxxxxxxx x registraci x xxxxxxx.
Xx účelem xxxxxxxxxxxxx odlišení xxxxxxxxxx xxxxxxxx xxxxxxxxx od xxxxxx xxxxxxxxxxx léčivých xxxxxxxxx xxxxxxx směrnice 2011/62/EU definici „xxxxxxxxxx xxxxxxxx xxxxxxxxx“:
Xxxxxxxx xxxxxx xxxxxxxxx je jakýkoli xxxxxx xxxxxxxxx x xxxxxxxxxxxx xxxxx o xxxx xxxxxxxxxx, xxxxxx xxxxx a xxxxxxxx xx xxxxx, názvu xxxx xxxxxxx (xxxxxx xxxxx xx pomocné xxxxx); xxxxxx (xxxxxx xxxxxxx, xxxx výroby xxxx xxxxxxxx xxxxxxxxxx x xxxxxxxxxx) nebo xxxxxxxx (včetně záznamů x dokumentů xxxxxxxxxx xx xxxxxxxxxx). Padělané xxxxxx xxxxxxxxx z xxxxxxxx složení xxxxxxxx xxxx xxxxxxxx xxxxxx x xxxxxxx látky, xxxx xxxxxxxx xxxxxxxxx xxxxxxxx xxxxxx xxxxx x x xxxxxxxxxx xxxx neobsahují žádné xxxxxx látky.
Aby systém xxxxxxxxx xxxxx xxx xxxxxxxxxx xx xxxxx xxxxxxxxx xxxxxxx Xxxxxxxx xxxx, neomezoval oběh xxxxxxxx přípravků x xxxxxxxxxx xxxxx xxxxxxx xxxxx účastníků xxxxxxxxxxxxxx xxxxxxx xxxxxxxxx překonáváním xxxxxxxxx xxxxxxxxxx, stanovila Xxxxxxxx Xxxxxx prostřednictvím xxxxxxxx x ochranných xxxxxxx jednotná xxxxxxxx xxx xxxxxxxx xxxxxxxxxx xxxxx, zejména xxxxxxxxxxxxxxx x technické specifikace xxxxxxx z xxxxxxxxxx xxxxx - xxxxxxxxxxx xxxxxxxxxxxxxx, xxxxxxx x xxxxxx ověření xxxxxxxxxx xxxxx xxxxxxxxxxxx xxxxxxxxx xxxxxxxx (xxxxxxx, xxxxxxxxxxxx, xxxxxxx xxxxxxxxxxx xxxx xxxxxxxxxx xxxxxxx xxxxxx xxxxxxxxx xxxxxxxxxx) x xxxxxxx x správu xxxxxxx xxxxxxx xxxxxxxxxx xxxxxxxxx x ochranných xxxxxxx (xxxxxxxxxxx xxxxxxxxxxxxxxxx).
Xxxxxxxx x ochranných xxxxxxx xx xxx xxxxxxx xxxxx xxxxxxx v xxxxx xxxxxxx x xx xx všech xxxxxxxxx státech xxxxx xxxxxxxxxx. Předkládaný xxxxx xxxxxx xxxxxx x xxxxxxxx vychází z xxxx, že xxxxxxx xxxxxx úpravou xxxxx xxx xxxxxxxx xxxxx xx oblasti a xxxxxxxx příslušných xxxxxx, xxxxx jsou xxx xxxxx xxxxx xxxxxx xxxxxxxxxx nezbytné x xxxxx buď nejsou x právní xxxxxx Xxxxxxxx xxxx xxxxxxxx xxxxx (xxxxxx xxxxxx Xxxxxxxx xxxx xxxx xxxxxxx neupravuje nebo xxxxxxxx xxxxxxxx xxxxxxxx xxx xxxxxxx xxxxx, xxx xxxxxxx národní xxxxxx - xxxxx xx např. x xxxxxx xxxxxxxxx xxxxxxxx) xxxx xxxxxxxx v xxxxxx xxxxxx Xxxxxxxx xxxx xxxx, xxx xxxxxxxx x xxxxxxxxxx xxxxxxxx výkonu působnosti xxxxxx xxxxxx xxxxxx x oblasti humánních xxxxxxxx xxxxxxxxx xx xxxxx, xxx xxxx xxxxxxxx xxxxx xxxxxxxxxxx x xxxxxxxxx xx xxxxxx právě k xxxxx orgánům, xxx xxxxxxxxx xxxxxxx xxx x xxxxxx xxxxxx xxxx založena xxxxxx xxxxxxxxx v xxxxx Xxxxx xxxxxxxxx, xxxxxx xxxxxxxx Xxxxxx svěřuje xxxxxx příslušnému xxxxxxxxxxxxxx xxxxxx xxxxxxxxx xxxxx, x xxx xxxxxxx xxxxxx xxxxxxx výkon xxxx xxxxxx xxxxxxxxxx. Xxxxxxxx právní xxxxxx xxxxxx x léčivech xxx xxxxxxxxxxxx do xxxxxxxx bodů:
A. Xxxxxx xxxxxxxxxxx vnitrostátního orgánu, xxxxx xx měl xxx xxxxxxx x xxxxxxxx xxx xxxxx xxxxxx xxx xxxxxxxxxx xxxxxxx, vyšetřování xxxxxxxxxxxxx xxxxxxx xxxxxxxx, xxxxxx, xxxxxxxxxxxxxxxx a farmakoepidemiologie. Xxxxxxxxx xxxxxxxxxx příslušným xxxxxxxxxxxxx orgánům členského xxxxx xxxxxxx x xxxxxxxx a k xxxxxxxxxx x xxx xxxxxxxxx pro výše xxxxxxx xxxxx ukládá xxxxxxxx x ochranných xxxxxxx xxxxxxxx xxxxxxxx, xxxxx xxxxxxx a xxxxxxxx xxxxxxxx xxxxxxxxx x xxxxxxx pravosti xxxx xxxxxxxx jedinečných xxxxxxxxxxxxxx xxxxxxxx přípravků xxxxxxxxx xx xxx x členském státě. X xxxxxxxxxx Xxxxx xxxxxxxxx xxxx xxxxxxxxxx xxxxxxxxxxxxx xxxxxxx dle xxxxxxxx x xxxxxxxxxx xxxxxxx Xxxxxx ústav xxx xxxxxxxx xxxxx (xxxx xxx „Xxxxx“), x to xxxxxxx x xxxxxxx xx xxxxxxxxx xxxxxx xxxxxx xxxx xxxxxxxxxx xxxxx xxxxxxx o xxxxxxxx, xxxx xxxxxxxxx autority xxx xxxxxx humánních xxxxxxxx přípravků. X xxxxxx důvodu xx xxxxx xxxxxxxx působnost Xxxxxx x §13 xxxxxx x léčivech. Xxxxx tak bude xxxxx xxxxxxxxxx stanovené x xxxxxxxx IX xxxxxxxx x xxxxxxxxxx xxxxxxx. Xxxxxxx xxxxx x zpřístupnění xxxxxxxxx xxxxxxxxx xxxxxxxxxx x xxxxxxxxxx, výrobcům, xxxxxxxxxxxxx x xxxxxx oprávněným xxxx zmocněným vydávat xxxxxx xxxxxxxxx veřejnosti, x xxxxxxxx xxxxxxxxxxx xxxxxxxxx xx xxx xx území Xxxxx xxxxxxxxx, xxxxx xxxx xxx opatřeny xxxxxxxxxx xxxxx (x xxxxxxx x článkem 54 xxxx. x) xxxxxxxx 2001/83/XX) x léčivých xxxxxxxxxxx, xx xxxxx se Xxxxx xxxxxxxxx xxxxxxxx xxxxxxxx xxxxxx xxxxxxxxxx xxxxxxxx (x xxxxxxx x xxxxxxx 54a xxxx. 5 xxxxxxxx 2001/83/XX). Xxxxx xxxx xxxxxxxxx xxxxx xxx xxxxxxxxxx xxxxxxxxx xxxxxxxx x Xxxxx republice, xxx xxxxxx, x xxxxxxx xxxxxxx prostřednictvím xxxxxxxx, xx úložiště x xxxxxx xxxxxxx xxxxxxxxx xx xxxxxxx x xxxxxx xxxxxxxx xxxxxxx požadavky xxxxxxxx. Xxxxxx x dozorové xxxxxxxx xxxx xxxxxxxx Xxxxxxxx agentuře xxx xxxxxx přípravky, xxxxx xx xxxxxxxxxx xxxxxx xxxxxxxxxx xxxxxxxxxxxxx xxxxxxx x Komisi.
B. Xxxxxxxxx, xxx xxxxxxxxxx, xxxxx xxxxxxxx o xxxxxxxxxx xxxxxxx ukládá regulovaným xxxxxxxxx, xxxx xxxxxx, x xx xxxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx x xxxx xxxxxxx, xxxxxxx správního orgánu xxxxxxxxxxx x xxxxxx xxxxxxxxxxxx x stanovením xxxx xxxxxx xx xxxxxxxx povinností xxxxxxxxxxxx xxxxxxxx. Xxx úpravy xxxxxx oblastí by xxxx xxxxxxxxxx xxxxxxxx x nařízení x xxxxxxxxxx prvcích x xxxxxxxx xxxxx xxxxxxxxxxxxx x nařízení xx xx míjelo účinkem. Xxxx xxxx xx xxxxxxxxxx s xxxxxxx xx xxxxxxxxxx xxxxxx 118x směrnice 2001/83/XX, xxxxx xxxxxx xxxxxxxx xxxxxx povinnost xxxxxxxx xxxxxx xx porušení xxxxxxxxxx a xxxx xxxxxx musí být xxxxxx, přiměřené x xxxxxxxxxx. Sankce musí xxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxx, které představuje xxxxxxxx xxxxxxxx xxxxxxxxx. Xxxx xxxxxx tak xxxx stanoveny s xxxxxxxxxxxx x xxxxx xxxxxxxxxx xxxxxxxx. Xxxxxxxx xxxxxxxx xxxxxxxxx je xxxxx xxxxxxxx xxxx xxxxxxx xxxxxx xxxxxxxxxxx x xxxxxxxxxxx xxxxxxxxx x xxxxxx xxxxxxxxxxxx xxxxxxx na xxxxxx xxxxxxxx x xxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxx xxxxxxxxxxx xxxxxxxxx xxxx. Xxxxxxxxx xxxxxxx xxxxxxxxx x xxxxxxxxxx xxxxxxx xx xxxxxxxxx xxxxx xx všech xxxxxxxxx xxxxxxx, tak, xxx xx xxxxxx vstupu xxxxxxxxxx xxxxxxxx xxxxxxxxx xx xxxxxxxxx dodavatelského xxxxxxx xx xxxxx xxxxxxx xxxxxxxxxxxxxx x xxxxxxx xx xxx, xx xx xxxxxxx xxxxxxx padělaný léčivý xxxxxxxxx x xxxxx xxxxx oprávněné x xxxxxx léčivého xxxxxxxxx. Xxxxxx xxxx xxxxxxxxx x to, xx xxxxxxxx povinností xxxx xxx xxxxxx xx xxxxxx xxxxx xxxxxxxxxxxxxxx xxxxxxxx, xx. xxxxxxxxxx xxxxxxxxxx xx xxxxx xxx xxxxxxxx xxxxx xxxxxxxx x Xxxxx xxxxxxxxx, ale x x xxxxxx xxxxxxxxx xxxxxxx. Fungování xxxxxx xx xxxxx xxxxx xxxxx, xxxxx xxxxx, xxxx xxxxxxxx x xxxxxxxxxx xxxxxxx xxxxxx xxxxxx povinnosti, xx xxxx beze xxxxxx xxxxx. Xxxxx xxxxxxxxx xxxxxxxx povinností, xx xxxxx xxxxxxxxxxxx xxx, xxx xxxx xxxxxx xxxx xxxxxxxx xxxxxxxxx xxxxxxxxx takového jednání. Xxxxxx jsou xxxxxx xxxxxxxxx tak, xx xx xxxxxxxxx xxxxxx xxxxx hranice. Xxxxx xxx xxx xxxxxxxxxx xxxxxxx okolnosti xxxxxxxxxxx xxxxxxx naplňujícího skutkovou xxxxxxxx xxx, xxx xxxxxxx k xxxxxxxxxxxxx xxxxxxxxx.
X. Xxxxxxx xxxx xxxx xxxxxxxx xxxxxx xxxxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx xxxx xxxxxxxxxx x xxxxxxx xxxxxxxxxx x xxxxxx xx xxxxxxx xxxxx xxxxxx přípravky x souladu s xxxxxxx 54x xxxx. 5 xxxxxxxx 2001/83/XX (čl. 2 xxxx. 1 xxxx. x) nařízení x xxxxxxxxxx xxxxxxx), xxxxxx xxxxx xxxx xxxxxxxxx, xxx xxxxxxxxxx xxxxx xxxx xxxxxxxx xxxxx i xxxx xxxxxxxx přípravků, xxxxx xxxxxxxxx xxxx xxxxxxxx xxxxx xxxxxx.&xxxx; Česká xxxxxxxxx xxxxxx xxxxxxxxxx xxxxxx působnosti xxxxxxxxxxx xxxxxxxxxxxxxx xxxx xxxxxxxxxx x ověření xxxxxxxxxx x xxxxxx xx xxxxxxx xxxxx xxxxxx xxxxxxxxx x xxxxxxx x xxxxxxx 54a xxxx. 5 xxxxxxxx 2001/83/XX (čl. 2 xxxx. 1 xxxx. c) xxxxxxxx o xxxxxxxxxx xxxxxxx).
X. Xxxxxxxx uvádí xxxxx „vnitrostátní xxxxxxxx xxxxx“ nebo „xxxx xxxxxxxx xxxxx“ identifikující xxxxxx přípravek x xxxxxxxxx xx xxxxxxxxxx xxxxxxxxx státu, xxx xxxxx xxxxxx xxxxx xxxx xxxxxx x xxxxx xxxxxxxxxxx xxxxxxxxxxxxxx xx xxxxxxx. X Xxxxx xxxxxxxxx xx „xxxxxxxxxxxxx xxxxxxxxx xxxxxx“ xxx xxxxxxxxx Xxxxxxx xxxxx §32 xxxx. 5 xxxxxx o xxxxxxxx (dále jen „xxx XXXX“). Xxxxx xxxxxxxxx nebude xxxxxxxxx, xxx xxx XXXX xxx uveden v xxxxx xxxxxxxxxxx xxxxxxxxxxxxxx, xxx., xx bude xxxxxxxx xxxxxxxxx xxxx, xxx xxx XXXX xx xxxxxx xx xxxxx xxxxxxxxx.
X. Xxxxxxx xxxxxxx xxxxx xxxxxxxxx x xxxxxxxxxx xxxxxxx xx xxxx xxx, xxx x uceleném xxxxxxxxxx xxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx xx xxxxxxx xxxxxxx xxxx xxxxxxxxx xx xxxxx xxxxxxxxxxxxxx řetězce, xx. xxx xx xxxxxx xxxxxxxxx xxxxx xxxxxxxxxx. Xxxxxxx xxxx xx xxx ale zohlednit xxxxxxxx xxxxxxxxxxxxxxx xxxxxxxxxxxxxx xxxxxxx xx xxxx xxxxx a xxxxxxx xx xxx xxxxxx xxxxxx, xxx xxxxxxxxxxx xxxxxx xxxxxxxx xxxxx x xxxxxxx vyřazení xxxxxxxxxxx xxxxxxxxxxxxxx léčivého xxxxxxxxx xxxx xxx, xxx léčivý xxxxxxxxx xxxx xxxxxxx x xxxx nebo xxxxxxxxx xxxxxxxxx x článku 23 xxxxxxxx x xxxxxxxxxx xxxxxxx:
x) osobám xxxxxxxxxx xxxx xxxxxxxxx vydávat xxxxxx xxxxxxxxx veřejnosti, xxxxx nepůsobí v xxxxx xxxxxxxxxxxxxx xxxxxxxx xxxx lékárny;
b) veterinárním xxxxxxx a xxxxxxxxxxxxxxx x xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx,
x) xxxxxx xxxxxxx;
x) xxxxxxxxxxxxx x xxxxxxx;
x) xxxxxxxxxxx xxxxxxxxxxxx záchranné xxxxxx;
x) ozbrojeným xxxxx, xxxxxxx x xxxxxx xxxxxxx xxxxxxxxxx, xxxxx xx xxxxxxx xxxxxx xxxxxxxx přípravků xxx xxxxx xxxxxxx xxxxxxx x xxxxxxxx katastrof;
g) xxxxxxxxxxx x dalším xxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxxxxx, xxxxx xxxxxxxxx xxxxxx xxxxxxxxx pro xxxxx xxxxxxx x vzdělávání, x xxxxxxxx xxxxxxxxxxxxxx xxxxxxxx;
x) xxxxxxxx;
x) xxxxxx;
x) xxxxxxxx;
x) xxxxxxxxxxxxx xxxxxxxxx.
X xxxxx Xxxxx xxxxxxxxx xxx xxxxxx popsaný článkem 23 nařízení x xxxxxxxxxx prvcích, xx. xxx xxxxxxx xxxxxxxxxx xxxxx a xxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx xx xxxxxxx úložišť xxxxxxx xxxxxxxxxxx, použít pouze x případě xxxxxxx xxxxxxxx xxxxxxxxx
- xxxxxxxxxxxx xxxxxxx,
- Armádě Xxxxx xxxxxxxxx x zabezpečení xxxxxxxxxxx sil léčivy, x udržování xxxxxxxxxx xxxxx xxxxxxxx xxxxxxxxx xxx xxxxx civilní xxxxxxx, xxxxxxxx xxxxxxxxx x xxx xxxxx xxxxxxxxxxx xxxxxxxxxxx xxx Xxxxx xxxxxxxxx xxxxxx xxx xxxxxx xxxxxxxx xx zahraničí xxxxx §111a xxxxxx o xxxxxxxx x
- poskytovatelům xxxxxxxxxxx xxxxxx, kterým xxxx xxxxx §77 xxxx. 1 xxxx. x) bodu 12 xxxxxx o léčivech xxxxxxxx xxxxxxxxxxxx xxxxxx xxxxxxxxx xxx účely xxxxxxxxx xxxxxxxxxxxx xxxxxxxx xx základě xxxxxxx xxxxxxx xxxxxxxxxxxx xx xxxxxxxxx xxxxxxxxxxx nebo xxx xxxxx xxxxxxxxx xxxxxxxxxxxx, xxxxxxxxxx x xxxxxxxxxxx xxxxxxxx na xxxxxxx xxxxxxx xxxxxxx xxxxxxxxxxxx x Ministerstvem xxxxxxxxxxxxx x xxxxxxxxxxx xxxxxxxx xxxxxxxxx x xxxxxxxxx xxxxxxxxxxx xxxxxxxxx x xxxxx xxxxxxxxxxx xxxx xxx zákona č. 48/1997 Sb., x xxxxxxxx xxxxxxxxxx pojištění x x změně x xxxxxxxx xxxxxxxxx xxxxxxxxxxxxx xxxxxx, xx xxxxx xxxxxxxxxx xxxxxxxx.
X xxxxxxxx xxxx 2009 došlo x XX xx xxxxx xxxxxxxxxx imunologických xxxxxxxxx (xx xxx xxxx krajské hygienické xxxxxxx, xxx xxxx xxxxxxxxxxx xxxxx), x xx na základě xxxxxx zákona č. 48/1997 Sb., x veřejném xxxxxxxxxx xxxxxxxxx x x xxxxx x xxxxxxxx xxxxxxxxx xxxxxxxxxxxxx zákonů, x s tím xxxxxxxxxxx xxxxx zákona č. 258/2000 Sb., o xxxxxxx xxxxxxxxx xxxxxx x x xxxxx xxxxxxxxx xxxxxxxxxxxxx xxxxxx. X xxxxx zachování stávajícího xxxxxxx xxxxxxx xxxxxxx xxxxxxxxxxxxxx xxxxxxxxx xxxxxxxxxxxxx xx ordinací xxxxxxxxxxxxx xxxxxxxxxxx služeb, xxx xxxxxxxxxx vyplývající x xxxxxxxx o xxxxxxxxxx xxxxxxx (xx. xxxxxxx xxxxxxxxxx prvků) xxxxxxx xx distributora xxxxxxxxxxxxxx xxxxxxxx xxxxxxxxx x xxxxxxxx článku 23 xxxx. x) xxxxxxxx x xxxxxxxxxx prvcích. Vzhledem x xxxxxxxx xxxxxxxxxxxx x xxxxxxx xxxxxxxxxx xxxxxxxx lékařů xxxxxx xxxxxxxxxxxx variantu xxxxxxxxx xxxxxxxxxx xxxxxxxx o xxxxxxxxxx xxxxxxx xxxxxx. Xxxxxxxxxx současného xxxxxxx xxxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxxxx xxxxxx xxxxxxx, které xx xxx nevyužití čl. 23 xxxx. x) xxxxxxxx x ochranných xxxxxxx museli xxx xxxxxxxxx ochranných xxxxx xxxxxxxxx.
Xxxx xxxxxxxx zásadní xx x tuto xxxxxx xxxx zachování xxxxxxxxxxx xxxxxxx xxxxxxxxxx xxxxxxxxxxxxxx xxxxxxxx přípravků xxx xxxxx xxxxxxxxx xxxxxxxxxxxx xxxxxxxx x xxxxxxxxx xxxxxxxxxx x xxxxxxxxxxx xxxxxxxx z xxxxxx xxxxxxx před xxxxxxx, xxxxxxx x xxxxxxx xxxxxxx infekčních xxxxxxxxxx. Xxxxxxxxxxxxx xxxxxxxxxxx xxxxxx xxx xxxxxxxxxx §45 xxxx. 2 xxxxxx x. 258/2000 Xx., x ochraně xxxxxxxxx xxxxxx x x xxxxx xxxxxxxxx xxxxxxxxxxxxx xxxxxx, xx xxxxx xxxxxxxxxx xxxxxxxx, xxxx xxxxxxx xxxxxxxx x provést xxxxxxxxxx, xxxxxxxx x mimořádná xxxxxxxx, xxxxxxxx xxx xxxxxxx, xxxxxxxxxx, nehojících xx ranách a xxxx některými léčebnými xxxxxx, popřípadě xxxxxxx xxxxxxxxx fyzických xxxx, xxxxx xxxx v xxxx, v xxxxxxx xxxxxxxxx xxxxxxxxx č. 537/2006 Sb., x xxxxxxxx xxxxx xxxxxxxxx nemocem xxxx xxxxxxxxxxx smlouvou, xxxxxx xx Česká xxxxxxxxx xxxxxx. Xxxxxxxxxx možnosti xxxx členskému xxxxx článkem 23 xxxx. x) xxxxxxxx x xxxxxxxxxx xxxxxxx, xx. nepřenesení xxxxxxxxxx ověření xxxxxxxxxx xxxxx xx obalech xxxxxxxxxxxxxx xxxxxxxx xxxxxxxxx xx xxxxxxxxxxxx xxxx xxxxxxx do ordinací xxxxxx, xx xxxxx x nekoncepčnímu xxxxxxxx xxxxxxxxxxx xxxxxxx xxxxxxxxxx xxxxxxxxxxxxxx xxxxxxxx xxxxxxxxx, xxx xx se xxxxx xxxxxxxx xxxxxxxx xxxxxxxxxxxxxx xxxxxx i xxxxxxx populace, x xx xx xxxx xxxxxxxx xxxxxxxx x xxxxxxxx úrovně xxxxxxx xxxxxxxxx xxxxxx.
X xxxxxxxx xxxxxx ochrany xxxxxxxxx xxxxxx xx jeví xxxxxx článek 23 písm. x) xxxxxxxx o xxxxxxxxxx xxxxxxx x xxx systém distribuce xxxxxxxxxxxxxx léčivých xxxxxxxxx xxx xxxxxxxxx xxxxxxxx xxxxxxx z xxxxxxxxx xxxxxxxxxxx xxxxxxxxx a xxxxxxxx xxx xxxxxxxx xxxxxxxxxxxxx xxxx na xxxxxxx rámcové smlouvy Xxxxxxxxxxxx xxxxxxxxxxxxx x xxxxxxxxxxxxx.
X významnosti xxxxxxxxxxx xxxxxxxx hrazených x xxxxxxxxx xxxxxxxxxxx xxxxxxxxx xxx xxxxxxxxxxx xxxxxxxx xxxxxxxxxx, že xxxx xx xxxxxxx zákona xxxxxxx z xxxxxxxxx xxxxxxxxxxx pojištění, x xx x xxxxxxxxx xxxxxxx xxxxxxxxxx xxxxxxxx x souladu x xxxxxxxxxxx §30 xxxx. 2 písm. b) x x) xxxxxx x. 48/1997 Xx., x xxxxxxxx xxxxxxxxxx xxxxxxxxx x x xxxxx a doplnění xxxxxxxxx souvisejících xxxxxx, xx xxxxx xxxxxxxxxx xxxxxxxx. Jako xxxxxxx xxx xxxxx očkování xxxxx xxxxxxxx xxxxxxxxxxxx, xxxxx xxxx xxxxxxx xx zdravotního xxxxxxxxx xxxxx x chlapci (xxxxxxx od 1.1.2018), xx-xx xxxxxxxx zahájeno xx dovršení 13. xx xxxxxxxx 14. xxxx věku. Papilomaviry xxxxx xxxxxxxx nejen xxxxxxxx xxxxxxxxx xxxxx, xxx x další xxxxxx (xxxx. análního xxxxxx) nebo xxxxxxxxx xxxxxxxxx.
Xx 1.1.2018 je xxxxxxx hrazeného xxxxxxxx xxxxx invazivním xxxxxxxxxxxxxx xxxxxxxx, xxxxxxxxxxxxx xxxxxxxx, xxxxxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxxxxx Haemophilus xxxxxxxxxx xxx b x xxxxx xxxxxxx, a xx x pojištěnců x xxxxxxxxx xxxx xxxxxxxx xxxxxx xxxxxxx (xxxxxxxxxxxxxx nebo xxxxxxxx), xxxxxxxxxx xx xxxxxxxxx xxxx xxxxxxxxx xxxxxxxxxxxxx xxxxxxxxx xxxxxxxxxxxxxx buněk, xxxxxxxxxx xx xxxxxxxxx xxxxxxxxxx nebo xxxxxxxxxxxx xxxxxxxxxxxxx, xxxxx vyžadují xxxxxxxxxxxxxx xx xxxxxxxxxxxxxxx xxxxxxxxxx, xxxx x xxxxxxxxxx xx xxxxxxxxx xxxxxxxxx xxxxxxxxxxxxx xxxx xxxxxxxxx xxxxxxxxxxxx infekci.
Pouze xxx xxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxx xxxx xxxxx xxxxxx článku 23 písm. x) xxxxxxxx x ochranných xxxxxxx.Xxxxxx xx x xxxxxx případech xxxxxxx xxxxxxxxxxxx léčivé přípravky xxxxxxxxxxxxxxx xxxxxx xx xxxxxxx od xxxxxxxxxxxxx xxxxxxxxxx péče.
Dále xx xxxxxx xxxxxxx určité xxxxxxxxx zpřesňující xxxxxx xxxxx xxxxxxxxxxxx xxxxxxxxx xxxxxx v těch xxxxxxxxxxxx xxxxxx o xxxxxxxx, xxxxx s xxxxxxxxxxx právní úpravou xxxxxxxxx xxxx xx xx xxxxxxxx.
X xxxxxxxx xxx xxxxxxxxx povahy xxxxxxxxxxxxx xxxxxxxx xxxxx xxxxxxxxx xxxxxx xxxxxxxxxxxx xxxxxxxx se xxxxxxxxxx xxxxx uvedených na xxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx, xxx xxxxx xxx xxxxxxxxxxxx xxxxxx xxxxxxx xxxxxxxxx z xxxx oblasti, xxxxx xxxxxxxx xxxxxxxx xxxxx xxxxxxxxxx xxxxxxx Xxxxxxxx xxxx. Nejedná xx xxxx o xxxxxx xxxxxxx, který by xxxxxxx předmětné xxxxxxxxxxxx xxxxxxx xxxxxxxxx x xx xxxxxxx xx xxxxxx x xxxxxxxxx x tomto xxxxxxxx.
X xxxxxxx xxxxxxx xxxxxxxxxx xxxxxxx uvádí xxxxxxxxxxxx xxxxxxxxxxx.
Xxxxxxxx 2017/556 xxxxxxx xxxxxxxx xxxxxxxx xxx xxxxxxxxx inspekčních xxxxxxx xxxxxxx xxxxxxxx xxxxx xxxxx nařízení Evropského xxxxxxxxxx a Rady (XX) č. 536/2014. Xxxxxxxx xxxx xxxxxx v xxxxxxx s článkem 63 xxxxxxxx x. 536/2014, xxxxx xxxxxxxx Xxxxxx xxxxxxxx akty x xxxxxxxxx pravomoci, x xxxxx xxxxxxx xxxxxxxx xxxxxxxx xxx xxxxxxxxx xxxxxxxx správné xxxxxxx xxxxx, xxxxx xxx x xxxxxxxxx xxxxxx xxxxxxxxx. Xxxxxxxx je xxxxx použitelné xx xxxxxxxx xxx jako xxxxxxxx (XX) č. 536/2014. Xxx xx xxxxxxx xxxxxxxx, jak je xxxx xxxxxxx, xxxxx xxxxxxxxxxxxx, je xxxxxxx xxxxxxxx x xxxxx xxxx adaptace xxxxxxx xxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxx, x xx x xxxxx xxxxxxx xxxxxx x xxxxxxxx, x zákona x xxxxxxxxxxx službách, x xx x xxxxxxxxxxxxx xxxxxx:
- xxxxxxxx xxxxxxx xxxxx, příslušný x xxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxx 2017/556,
- xxxxxxxx xxxxxxxx článku 3, xxxxx xxxxxx xxxxxxxx xxxxxx xxxxxxxx xxxxx xxxxxxxxxxx systém xxxxxxx, xxxxx xxxxxxx, xxx xxxxxxxxx xxxxxxx byly xxxxxxxxxx x xxxxxxxx xxxxxxxxx,
- xxxxxxxx naplnění xxxxxx 10 xxx 8, tedy xxxxxxxx xxxxxx x xxxxxxx xxxxx, xxxxx zajistí, xxx xxxxxxxxxx x xxxxxxxxx xxxxxxxxx xxxxx xxxx, na vyžádání x xxx, xxx xx xx xxxxxx, xxxxxxx k xxxxxx, xxxxxxxxx prostorám xxxxxxxxxx xxxxxxxx xxxxxxxxxxxxx x xxxxxxxxx xxxxxxxxxx, xxxxx x x xxxxxxxxx xxxxxxxxxxxx údajům,
- zajistit xxxxxxxx xxxxxx 13 xxxxxxxxxx se xxxxxxxxxxx xxxxx a xxxxxx xxxxxxx,
- xxxxxxxx naplnění xxxxxx 4 xxxxxxxxxx xx vedení xxxxxxx x xxxxxxxxxxx, odborné xxxxxxxx x xxxxxxxxxxxx xxxxxxxxxx,
- xxxxxxxx, xxx xxxxx bude xxx xxxxxxxx xxxxxxx xxxxxxx xxxxxxxx xxxx porušení xxxx xxxxxxxxxx-xx zadavatelé xxxxxxxxxxx pravomoci xxxxxxxxxx, xxxx xxxx jednání xxxxxxxxxxxxx jako přestupek x xxx za xx mohl xxxxxxxxx xxxxxxx xxxxx stanovit xxxxxx.
Xxxxxxxx 2017/1569 je xxxxxx s xxxxxxx xx nařízení Xxxxxxxxxx xxxxxxxxxx x Rady (XX) č. 536/2014 xx xxx 16. xxxxx 2014 x xxxxxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx x x xxxxxxx směrnice 2001/20/ES, x xxxxxxx x xxxxxxx na xx. 63 xxxx. 1 xxxxxxxxx xxxxxxxx, xxxxx xxxxxxxxx, xx hodnocené xxxxxx přípravky xxxx xxx xxxxxxxx za xxxxxxx xxxxxxx xxxxx, xxxxx zajistí xxxxxxx xxxxxx xxxxxxxx xxxxxxxxx x xxxxx xxxxxxx xxxxxxxxxx xxxxxxxx hodnocení x spolehlivost a xxxxxxxxxx xxxxxxxxxx xxxxx xxxxxxxxx v xxxxxxxxx xxxxxxxxx. Tuto xxxxxxx xxxxx xxxxxx xxxxxxx xxxxxx xxxxxxxx xxxxxxx xxxxx x xxxx xxxxxxxx v xxxxxxxxxx xx xx. 89 xxxxxxxx Xxxxxx xxxxx xxxxxxxx xxxxxxx výrobní xxxxx xxx xxxxxxxxx xxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxx. Toto zmocnění Xxxxxx xxxxxxxx vydáním xxxxxxxx 2017/1569, a xx xxxxxxx x xxxxxxx na xxxxxxxxxxx xxxxxx:
- je nezbytné xxxxxxxx soulad xxxx xxxxxxx xxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxx xx stejných xx xxxxxxx xxxxxxxxxx hodnoceních x také xx, xx xxxxx během xxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx byly náležitě xxxxxxxxxxxxx a xxxxxxxxxx;
- xxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx představuje další xxxxx x xxxxxxxxx x xxxxxxx xxxxxxxxxxxxxx xxxxxxxx přípravků, xxxxxxx xxxxxx xxxxx stanoveny xxxxxxx, xxxxxxxx xxxxx xxxxx xxxxxxxxxx hodnocení, x v důsledku xxxx xxxx xxxxxx xxxxx; xxxx výzvy xxxxxxxxx z xxxxxxx (xxxxx) xxxxxxxxx xxxxxx x zastření xxxxxxxx xxxxxxxxxxx léčivého xxxxxxxxx xxx účely xxxxxxxxxx xxxxxxxxx (xxxxxxxxx). Během xxxxxxxxx xxxxxx xxx xxxxx známá toxicita, xxxxxxxx a xxxxxxxxxxxxxx xxxxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx, x xxxxxxx xxxxxxxxxxxxx xxxxxxx xxxxxx křížové kontaminace xx xxxxx ještě xxxxxxxxxxx než u xxxxxxxxxxxxxx xxxxxxxx xxxxxxxxx. Xxxxxxxx x xxxx xxxxxxxxxx xx xxxxxxx xxxxxxxx měly být xxxxxxxxx xxxxxx xxxxxxxx xxxxxxxxxxxxxxx xxxxxxx jakosti;
- xxxxxxx výrobní xxxxx, xxxxx jde x xxxxxxx xxxxxx přípravky, xxxxx byly registrovány xxx uvádění xx xxx, x x xxxxxxxxx xxxxxx xxxxxxxxx, xx založena xx xxxxxxxx xxxxxxxx;
- xxxxxxxxx xxxxxx xxxxxxxxx i xxxxxxxxx xxxxxxxxxxxx xxx xxxxxxx na xxx xx xxxxx vyrábí xx xxxxxxxx výrobních xxxxxxx. X xxxx xxxxxx by xxxxxx x xxxxxx xxx xxxxxxxx výrobní xxxxx xxx xxxxxxxxx xxxxxxx xxxxxx přípravky xxxx xxx co nejvíce xxxxxxx x těmi, xxxxx se xxxxxxxx xx xxxxxxx xxxxxx xxxxxxxxx;
- aby byl xxxxxxx xxxxxxx dodržovat xxxxxxxx xxxxxxx xxxxx xxx hodnocené léčivé xxxxxxxxx, je nezbytná xxxxxxxxxx xxxx ním x xxxxxxxxxxx. Xxxxxx xxx musí xxxxxxxxx xxxxxxxxxxxxx x xxxxxxxx, xxx dodržel požadavky xxxxxxxx (XX) č. 536/2014. Xxxxx xxxx xxxxxxx x xxxxxxxxx xxxxxxx xxxxxxxx subjekty, xxxx xx xxx povinnosti, xxxxx x xxxx xxxxxxxx mají, xxxxxxxxx x technické xxxxxx xxxx xxxx. Xxxxxx xxxxxx xx xxxx xxxxxxxx xxxxxxx inspekčních xxxxx x xxxxxx xxxxxxxxx x otázkách xxxxxxx;
- xxxxxxxxx léčivé xxxxxxxxx xxxxxxxx xx Xxxx by xxxx xxx vyrobeny x xxxxxxxx xxxxxxxxx xxxxxxx, xxxxx xxxx xxxxxxxxxxxx xxxxxxxxxx xxxxxxxxxx x Xxxx. X tohoto xxxxxx xx nezbytné xxxxxxxx, xxx xxxx xxxxxxxx xxxxxxx do Xxxx pouze xxxxxxxxx xx výrobce xx xxxxx zemi, xxxxx xx xxxxxxxxx xxxx xxxxxxxx x výrobě x xxxxxxx x xxxxxxxx předpisy xxxx, x xxx xx xxxxx.
Xxxxxxxx rovněž xxxxxxxx xxxxxxxxxx xxxxxxxx se xxxxxxxx xxxxxxxxxxx xxxxxxxxxxx xxxxxxxxx orgány xxxxxxxxx xxxxx tak, xxx xxxx zajištěna xxxxx xx zásadami x xxxxxx xxx správnou xxxxxxx xxxxx. V xxxxx xxxx je xxxxxxxx 2017/1569 xxxx xxxxxxxx na nařízení 2017/556, xxxxxx xx xxxxxxxxx xxxxxxxx xxxxxxxx xxx xxxxxxxxx inspekčních xxxxxxx správné xxxxxxxx xxxxx podle xxxxxxxx 536/2014. X zde xxxxxxxx xxxxxxxx xxxxxxxxxx xxxxxxxxxxx, aby inspektoři x xxxxx xxxxxxxx x xxxxxxx xxxxxxxxxx xxxxxxxx výsledků xxxxxxxx x Xxxx x x xxxxx xxxxxxxxx xxxxxxxxxx členských xxxxx xxxx x dispozici xxxxxx uznávané xxxxxxxxx xxx provádění inspekcí xxxxxxx výrobní praxe xxx xxxxxxxxx léčivé xxxxxxxxx ve xxxxx xxxxxxx;
- pokyny Xxxxxx x xxxx xxxxxxx xx xxxx xxx xxxxxxxxx x xxxxxxxxxx xxxxxxxxxxxxx x xxxxxxxxxx xx technickém x xxxxxxxx xxxxxxx. Xxxxx xxxxxxxx xx xxxxx xxxxxxxxxx xxxx xxxxxx, xxx xxxxxxx xxxxx xxxxxxxx xxxxxxxx xxxxxxx xxxxx xxx x xxxxxxxxxxx xxxxxxxx xxxxxxxxx, xxx x xxxxxxxx xxxxxxxxx registrovaných xxx xxxxxxx na xxx. X tohoto důvodu x x xxxxx xxxxxxxxx účinného xxxxxx xxxx xxxxxxxxx xxxxxxx x xxxxxxxxx xxx xxxxxxxxx xxxxxxxx x xxxxx xxxxxx, xxx xx dodržována xxxxxxx xxxxxxx praxe xxx xxxxxxxxx xxxxxxx léčivé xxxxxxxxx. Xxxx praxe xxxx korespondovat s xxxxxxx x xxxxxxxxxxx x oblasti humánních xxxxxxxx přípravků - xxx xxxx xxxx xxxxxxxx xxxxxxxx Komise (XX) 2017/1572. X xxxx, xxx xxxx xxxxxxxx účinné, xxxx xxx inspektoři zajištěna xxxxxxxx oprávnění;
- xxxxxxxxx xxxxxx mají xxxxx xxxxxxxx povinnost xxxxxxxx xxxxxxx xxxxxxx, aby xxxx zajištěno, xx xxxx xxxxxxxxx xxxxxxx xxxxxxxxxx a xxxxxxxx xxxxxxxxx. Dobře fungující xxxxxx jakosti musí xxxxxxxxx organizační strukturu, xxxxx xxxxxxx a xxxxxxx, včetně xxxxxxxxxxxx xxxxxxxxxx postupů, xxxxx xx mají xxxxxxxxxx xxxxx při plnění xxxxx úkolů, xxxxx x xxxxxxxx vymezené xxxxxxxxxx x odpovědnosti xxxxxxxxxx x požadavky xx xxxxxxxx xxxxxxx, xxxxx i přiměřené xxxxxx x mechanismy, xxxxxxx xxxxxx xx xxxxxxxxx nesoulad.
Směrnice 2017/1572 xxxx xxxxxxx x xxxxx zajistit shodu xx xxxxxxxx x xxxxxx xxx xxxxxxxx xxxxxxx xxxxx. Xxxxxxxx xxxxxxxx ustanovení x xxxxxxxxxx xxxxxxxxxxx xxxxxxxxxxx xxxxxx x o xxxxxxxx povinnostech xxxxxxx. Xxxxxxxx xxxxxxxxxx, xxxxx xxxxxxxxx, xxx všechny xxxxxx xxxxxxxxx dostupné xx území XX xxxxxxxxx tytéž xxxxxxxxx xxxxxxx; léčivé přípravky xxxxxxxx xx Unie xxxx xxx xxxxxxxx x xxxxxxx xx xxxxxxxxx, které xxxx xxxxxxxxxxxx rovnocenné xxxxxxxxxx xxxxxxx xxxxxxx xxxxx xxxxxxxxxx x Xxxx.
X xxxxx xxxxxxxxxx uplatňování xxxxx xxxxxxx výrobní xxxxx musí xxxxxxx xxxxxxxxx léčivých přípravků x xxxxxxxxxx xxxx xxxxxx xxxxxxxxx x čl. 47 xxxxxxxx 2001/83/ES, xxx xx uvedeno, xx „Xxxxxx x xxxxxx xxx xxxxxxxx xxxxxxx praxi pro xxxxxx přípravky xxxxx čl. 46 xxxx. x) xx přijmou formou xxxxxxxx“ x xx „xxxxxxxx xxxxxx v xxxxxxx x uvedenými xxxxxxxx Komise zveřejní x v xxxxxxx xxxxxxx xxxxxxx xxx, xxx xxxx xxxxxxxxxxx x technickému x xxxxxxxxx xxxxxxx“. Zásady x xxxxxx xxx xxxxxxxx výrobní xxxxx xxx xxxxxxx xxxxxx xxxxxxxxx xxxx xxxxxxxx xxxxxxxxx, xxxxx jde x xxxxxx jakosti, xxxxxxxxxx, xxxxxxxx x xxxxxxxx, xxxxxxxxxxx, xxxxxx, xxxxxxxx xxxxxxx, xxxxxxx xxxxxxxxxxx xxxxxxxx, xxxxxxxxx x xxxxxxx xxxxxxxxx x xxxxx x xxxxxxx xxxxxxxx. Xxxxx xx xxxx xxxxxxxx xxxxxxxxx xxx xxxxxxx xxxxxxx, xxxx tyto xxxxxx a xxxxxx xxxxxxxxxxxx zvláštním xxxxxxxxxxx xxxxxxxxx xxxxxxxxx v xxxxxxx x xxxxxxxxx xxxxxxxxx na xxxxxxxxx xxxxx.
Xxxxxxx xxxxxxxx xxxx xxxxxxxxxxxxx do xxxxxx x léčivech x xxxxxxx do xxxxxxxx č. 229/2008 Sb. Nahrazení xxxxxxxx 2003/94/ES xxxxxxxx 2017/1572 xxxxxxxx nutnost xxxxx xxx xxxxxx o xxxxxxxx, xxx xxxxxxx xxxxxxxxxxx předpisu - xxxxxxxx č. 229/2008 Sb. Transpozice xxxxxxxx xx dotkne xxxxxxxxxx zákona x xxxxxxxx xxxxxxx x xxxxxxxxxxxxx bodech:
- xxxxxx xxxxxxxx xxxxxxx výrobní xxxxx,
- xxxxxxx povinnosti xxxxxxxx xxxxxxxx x xxxxxxxx xxxxxx xxxxxxxx xxxxxxx,
- uložení xxxxxxxxxx xxxxxxxx xxxxxx xxxxxx xxx xxxxxxxxxxxxx x xxxxxxxxxx xxxxxxxxx včetně xxxxxxxx xxxxxxxx systému xxx xxxxxxxxx léčivých xxxxxxxxx x distribuční xxxx,
- xxxxxxxxx xxxx, xxx výrobci xxxxxxxxx xxxxxxx xxxxxxx x xxxxxxx činnosti x xxxxxxxxxxx x léčivými xxxxxxxxx xxxxxxxxxxxxx xxxxxxxxxx x xxxxxxx x xxxxxxxxxxx xxxxxxxxxxxx x xxxxxxx x xxxxx xxxxxxxxxx.
Xxxxxxxxxx právní xxxxxx xxxx xxxxx x xxxxxxxxxxxx xxxxxxxxxxxx x xxxxxxxx mužů x xxx.
3. Xxxxxxxxxx xxxxxxxxxxx xxxxxxxxxx xxxxxx xxxxxx
Xxxxx xxxxxx xxxxxx x léčivech x xxxxxx o xxxxxxxxxxx xxxxxxxx xx xxxxxxxxxx xx účelem xxxxxxxx xxxxxxxxxxxx xxxx uvedených xxxxxxxx xxxxx Xxxxxxxx xxxx. Xxxxxx touto xxxxxxxxxxxx xx xxxxxxx xxxxxx xxxxxxxx xxxxxxxxxxx xxxxxxxx x xxxxxxx xxxxxxxxxx xxxxx uvedených xx xxxxx humánních xxxxxxxx xxxxxxxxx a x oblasti dodržování xxxxx správné xxxxxxxx xxxxx. Xxxxxxxxxxxxxxx xxxxxxxxxxx xxxxxx xxxxxxx x xxxxxx z xxxx xxxxxxxxxx xxxxxxx xxxxxxxxx x xxxxxxx celek, xxxxx xxxx možno xxxxxxxxx x xxxxx. Xxxxx by k xxxxxxxx xxxxxx xxxxxx xxxxxx o xxxxxxxx xxxxxx xxxxxxxxxxx, xxxxx xxxxxxxxxx xxxxxxxx Evropské xxxx (nařízení) xx x České republice xxxxxxx xxx xxxxxx x xxxx zbytku xxxxxxxxxx, xxxx by xxxxx x xxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxx. Xxxxxxxx x xxxxxxxxxx xxxxxxx xxxxxxx ustanovení xxxxxxxx 2011/62/EU. Česká xxxxxxxxx xxx xx xxxxx xxxxxxxx xxxx xxxx xxxxxxxx xxxx xxxxxxxxxxxxx zákonem č. 70/2013 Sb., xxxxxx byl novelizován xxxxx o xxxxxxxx.
Xxxxxxxxxxxxxxx xxxxxxx je riziko xxxxxxxxxxx xxxxxxxxx xxxxxxxx xxxx xxxxxxxx xxxxxxx x xxxxxxxx Xxxxxxxx xxxx xx xxxxxx xxxxxxxxx státu a xxxxxxxx xxxxxx xx xxxxxx Xxxxxxxx xxxxxx xxxxx Xxxxx republice xx xxxxxxxxx implementační xxxxxxxxxx x popřípadě x xxxxxxx sankce xxxxxxxxx takovému xxxxxxxx, xxxxx by xxxx xxxxx xx xxxx xxxxxx a xxxx xxxxxxxxx xxxxxx pouze x xxxxxxx Xxxxx xxxxxxxxx, xxx i xxxxxxxxx xxxxxxxxx xxxxx, xxxxx xxx v xxxxxxx, že xxxxxxxx xxxxx xxxxxxxxxx všemi, xxxx xxxxxx funkční. X uvedenému je xxxxx xxxxx xxxxxxx, xx xx xxxxxxxxx xxxxxx xxxxxxxxxx xx xxxxxxx xx xxxxxx xxxxxx Evropské unie xxxxxxxxxxxx xxxxxxxx xxxxxxxx x popřípadě x xxxxxxx xxxxxx, jejíž xxxx by xxxxx xxxxx odrážela xxxx xxxxxx x xxxxx xxxx XX x x takové xxxxxxx xxxx je xxxxxxxxxx xxxxxxxx. K xxxxxxx xxxxxxx xxxxxx, xxxxxx xx xxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxxxxxxx xxxxxxxx xxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx xx xxxxxxxxx xxxxxxxxxxxxx xxxxxxx, xxxxxxxxxxxx uvádí xxxxxxxxxxx.
Xxxxxxxx xxxxxxxxxx prvků xxx xxxxxx xxxxxxxxx x xxxx Evropské xxxx x xxxxx xxxxxxxxx xxxx xxxxxxx xxxxx x xxxxxxx zajistit xxxxxxxxx xxxxxxxxx xxxx x xxxxxxxx xxxxxxxxx xx mělo u xxxxxxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx umožnit xxxxxxx xxxxxxxx a xxxxxxxxxxxx xxxxxxxxxxxx xxxxxx x xxxxxxxx, xxx s xxxx xxxx xxxxxxxxxxxx. Xxxxxx xxxxxx ochranných xxxxx xxxxxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx léčivých xxxxxxxxx. Léčivé xxxxxxxxx xxxxxxxxxxx omezení výdeje xx xxxxxxxx předpis xx xxxxxx xxxx xxx xxxxxxxx ochrannými xxxxx. V xxxxx xxxx, aby xxxx xxxxxxxx xxxxx účinné, xx xxxxxxxx xxxxxxxxxxx, xxxxxxxxxx nebo xxxxxxxxx xxxx xxxxx xxxxx xxxxxxxx xx xxxxxxxx xxxxxxxxxxx xxxxxxxx. Xxxxxxx x případě přebalení xxxxxxxx prvky xxxx xxx nahrazeny xxxxxxxxxxxx xxxxxxxxxx prvky. Xxxx xxxxxx podmínky xx xxxx zajistit dostatečnou xxxxxxx xxxxx xxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx xx legálního xxxxxxxxxxxxxx xxxxxxx x cílem xxxxxxx xxxxxxxx i xxxxxxxx xxxxxxxxxx o xxxxxxxxxx x xxxxxxx. Xxxxxxxxxxxx xxxxxxxxxx xxxxx x xxxxxxxx xxxxxxxxx xxxxxxxxxx xx lékařský xxxxxxx xx xxxxxx xxxxxxxxxx a xxxxxx xxxxxxxxx xxxxxxxx v Xxxxx xxxxxxxxx, xxxxxxxxx xxxxxx xxxxxxxxx postupů, xxxxxxx v xxxxx xxxxxxxxxxx xxxxxxxx a xxxxxxxx xxxxxxxxx s xxxxxxx xxxxxxxx xxxxxxxxx, xxxxxxx xxxxx byl xxxxxxxxx Xxxxxx Xxxxxxxxxxx xxxxxxxxxxx Xxxxxx v xxxxx xxxxxx xxxxxxxx x xxxxxxxxxx xxxxxxx.
Xxxxxxxxx xxxxxxxxxx x xxxxxxxxxxx xxxxxxxx předpokladů pro xxxxxxxxx xxxxxxx používání xxxxxxxxxx xxxxx xx xxxxx humánních xxxxxxxx xxxxxxxxx x České xxxxxxxxx xx nedošlo x potřebnému xxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx x xxxxxxxx dodavatelském xxxxxxx, xxx by xxxxx xxxx x xxxxxxxx xxxxx ochrany xxxxxxxxx xxxxxx, x xxxxx by tak xxxxxxx xxxxxxxxxxxxxx xxxxxxx xxxx v xxxx xxxxxxxxx citlivé xxxxxxx x důsledku vystavení xxxxxxxx neznámým xxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx. Xxxxxxxxx xxxxxx xxxx xxxxxxxx pouze x xxxxxxx, xxx všechny xxxxxxx xxxxxxxx a xxxxxxxxxxxx xxxxxxxxx orgány x členské xxxxx XX budou xxxxx xxx xxxxxxxxxx xxxxxxxxxxx x výše xxxxxxxxx xxxxxxxx xxxxxxxx XX.
Xxxxxxxxxxxx xxxxxxx proti xxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx xx xxxxxxxxx xxxxxxxxxxxxxx xxxxxxx v jednom xxxxx xxxxxxx, xx x jeho území xx xxxxxxxx léčivé xxxxxxxxx xxxxx snadněji xxxxxx do jiných xxxxxxxxx xxxxx (xxx xxxxx xxxxx xxxxx x XX), kde xxxx xxxxxxxx provedena xxxxx a včas. Xxxx xx bylo x xxxxxxx s xxxxxxxxx xxxxxxxx xxxxxxxxxx.
X xxxxxxx xxxxxxx xxxxxx, xxxxxx xx xxxxxxxxx xxxxxxxxxx zásad xxxxxxx xxxxxxx xxxxx pro xxxxxxxxx léčivé přípravky x xxxxxxxxx dodržování xxxxxxxx xxx provádění xxxxxxxxxxx xxxxxxx správné xxxxxxxx xxxxx, xxxxxxxxxxxx xxxxx xxxxxxxxxxx.
Xxxxxxxx, xxx xx xxxx uvedeno, xxxx přímo xxxxxxxxxxxxx, xxxxxx xx nezbytné x xxxxx adaptace xxxxxxxxxxxx norem vnitrostátního xxxxxxxx xxxx Xxxxx xxxxxxxxx xx xxxx xxxxx xxxxx Evropské xxxx xxxxxxxxxxx xxxxxxx xxxxxxxxxx xxxxxx x xxxxxxxx a xxxxxx x xxxxxxxxxxx xxxxxxxx xxx, xxx xxxx xxxxxxxxxx x xxxxxxxx xxxxxxxxxxx vymahatelné x xxxxxxxx systém xxxxxx xxxxx koherentní se xxxxxxxx xxxxxxxxxxx xxxxxxxx, xxxxx x xx xxxxxxxx xxxxxxx xxxxx xxxxxxxx xxxxxxxxx.
4. Xxxxxxxxxx xxxxxxx navrhované právní xxxxxx x xxxxxxxx xxxxxxxx Xxxxx republiky
Návrh xxxxxx xxxxxx x xxxxxxxx a xxxxxx x xxxxxxxxxxx xxxxxxxx xx v souladu x ústavním xxxxxxxx Xxxxx republiky. Navrhovaná xxxxxx xxxxxx respektuje xxxxxxx xxxxxxxxx pravidla xxxxxx xxxxxx xxxx, xxxxxx xxx xxxxx článku 2 xxxx. 3 Xxxxxx x článku 2 xxxx. 2 Listiny xxxxxxxxxx práv x xxxxxx uplatňovat xxx x xxxxxxxxx x x xxxxxx xxxxxxxxxxx xxxxxxx, x xx xxxxxxxx, xxxxx xxxxx xxxxxxx. Navrhovaná právní xxxxxx xxxxxx xxxxxxxxxx xxxxxxx zakotvenou zásadu, xxxxxxxxxx v článku 4 xxxx. 1 Xxxxxxx xxxxxxxxxx xxxx x xxxxxx, xxxxx spočívá x xxx, xx xxxxxxxxxx xxxxx xxx xxxxxxxx toliko na xxxxxxx xxxxxx a x xxxx xxxxxx x xxx xxx xxxxxxxxx xxxxxxxxxx xxxx x xxxxxx. Xxxxxxxxx xxxxxxxxxx podnikatelských xxxxxxxx xxxxxxxxxx x xxxxxxxxxxxx xxxxxxx, které xxxx xxxxxxxx xxxxxxx pacientů xxxx xxxxxxxxxx léčivými xxxxxxxxx, xxxx x xxxxx xxxxxxx zdraví x xxxxxx pacientů x xxxxxx xxx xxxxx Ústavy Xxxxx xxxxxxxxx a Xxxxxxx xxxxxxxxxx xxxx a xxxxxx. Xxxxxxxxxxx xxxxxx xxxxxxx se zajistí xxxxx xxxx bezpečnosti xxxxxxxx xxxxxxxxx xxx xxxxxxxx x hlouběji xx tak xxxxxx xxxxx každého xx xxxxxxx zdraví xxxxxxxx xxxxxxxxxxx článku 31 Xxxxxxx xxxxxxxxxx xxxx a xxxxxx xxxx xxxxxxxx xxxxxxxxx xxxxxxx Xxxxx xxxxxxxxx.
Xxxxxx xxx nařízení x xxxxxxxxxx xxxxxxxxxx xxx provádění xxxxxxxxxxx xxxxxxx xxxxxxx klinické xxxxx xx tzv. x xxxxxx xxxx xxxxxx jen xx xxxxxxxxxx xxxxxxx, xxxxx xxxxxxxxxx xxxxxxxxx na xxxxxxx jim xxxxxxxxx xxxxxxxx právě x xxxxxx xxxxxxxxx xxxxxxxxx. Xxxx xxxxxxxx xxxx xxxxxxxx xxxxxxxxx xxxxx xxxxxx členského xxxxx. Xxxxxxx, xxx by xxxxxxx xxxxx postupoval xxxxxxxx, je xxxxx xxxxxxxxx za xxxxx. X pověření x xxxxxxxxx xxxxxxxx, včetně xxxxxx, bude xxxxxxxxxxxx xxxxxxxxxx zevrubně informována xxxxxxx před xxxxxxxxx xxxxxxx samotného, x xx x x xxxxxxxxx, kdy xxxxx xx. 8 xxxxxxxx xxxxx xxx xxxxxxxx x xxxxxxx xxxxxxxx xxxxxxxxx, xxxx xxxx xxxxxxx xxxxxxxx.
Xxxxx xxxxxx xxxxxx naplňuje xxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxx Xxxxx republiky, xxxxxxxxx xxx článkem 12 Listiny xxxxxxxxxx xxxx x xxxxxx, xxxxx xxxxxxx, xx zásahy do xxxxxxxxxxxxxxxx obydlí xxxxx xxx zákonem xxxxxxxx, xxx xx-xx xx x xxxxxxxxxxxx xxxxxxxxxxx xxxxxxxx pro ochranu xxxxxx xxxx zdraví xxxx, pro xxxxxxx xxxx x xxxxxx xxxxxxx anebo xxx xxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxx xxxxxxxxxxx a xxxxxxx. Xxxxx je xxxxxx xxxxxxx také xxx podnikání xxxx xxxxxxxxxxx xxxx xxxxxxxxxxx xxxxxxxx, xxxxx xxx xxxxxx xxxxxx xxxxxxx xxxxxxxx, též xx-xx xx xxxxxxxx xxx xxxxxx xxxxx veřejné xxxxxx.
5. Xxxxxxxxxx xxxxxxxxxxxxx xxxxxxxxxx právní úpravy x předpisy Xxxxxxxx xxxx, xxxxxxxxxxx xxxxxxxx xxxxxx Xxxxxxxx xxxx xxxx xxxxxxxx právními xxxxxxxx xxxxx Xxxxxxxx xxxx
Xxxxxxxxxxx xxxxx xxxxxxxxx způsobem xxxxxxxx xxxxxxxx x ochranných xxxxxxx, nařízení o xxxxxxxxxx xxxxxxxxxx xxx xxxxxxxxx xxxxxxxxxxx xxxxxxx xxxxxxx klinické xxxxx xxxxx xxxxxxxx 536/2014 x xxxxxxxx, xxxxxx xx doplňuje nařízení 536/2014 xxxxxxxxxx xxxxx x pokynů pro xxxxxxxx xxxxxxx xxxxx xxx xxxxxxxxx xxxxxxx xxxxxx přípravky x xxxxxxxx xxxxxxxxx inspekcí, xxxx. xxxxxxxxxxx směrnici, xxxxxx xx doplňuje xxxxxxxx 2001/83/XX, xxxxx xxx x xxxxxx x xxxxxx pro xxxxxxxx xxxxxxx xxxxx xxx xxxxxxx xxxxxx xxxxxxxxx.
Xxxxxxxxxx xxxxx xxxx x xxxxxxx xx xxxxxxx xxxxxxxxxxxxx xxx Xxxxxx xxxxxxxxx z xxxxxxxx x Evropské xxxx, Smlouvou x xxxxxxxxxxx České republiky x Xxxxxxxx xxxx xxx x xxxxxxxxxxx xxxxxxxx orgánů Xxxxxxxx xxxx x xx x xxxxxxx x xxxxxxxx xxxxxxxx práva Xxxxxxxx xxxx (např. xxxxxxx xxxxxx jistoty, xxxxxxxxxxxxxxx a zákazu xxxxxxxxxxxx).
X xxxxxxxx Evropské xxxx, xxxxx se xxxxxxxx xx oblast xxxxxxx xxxx padělanými xxxxxxxx přípravky a xx xxxxxx xxxxxxxxx xxxxxxxx xxx ochranné xxxxx uvedené na xxxxx humánních xxxxxxxx xxxxxxxxx, xx návrh xxxxxx xxxxxx x xxxxxxxx přímo xxxxxx xxxxxx xxxxxxxx:
- směrnice Xxxxxxxxxx xxxxxxxxxx x Xxxx 2001/83/ES ze xxx 6. xxxxxxxxx 2001 x kodexu Xxxxxxxxxxxx týkajícím se xxxxxxxxx léčivých přípravků, x platném znění (xxxx jen „xxxxxxxx 2001/83/ES“),
- xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Xxxx 2011/62/EU xx xxx 8. xxxxxx 2011, xxxxxx xx xxxx xxxxxxxx 2001/83/XX o xxxxxx Xxxxxxxxxxxx xxxxxxxxx xx xxxxxxxxx xxxxxxxx xxxxxxxxx, xxxxx xxx x zabránění xxxxxx xxxxxxxxxx léčivých xxxxxxxxx xx xxxxxxxxx dodavatelského xxxxxxx (xxxx xxx „xxxxxxxx 2011/62/EU“),
- nařízení Xxxxxx v přenesené xxxxxxxxx (XX) 2016/161 xx xxx 2. xxxxx 2015, kterým xx doplňuje směrnice Xxxxxxxxxx parlamentu a Xxxx 2001/83/XX xxxxxxxxxx xxxxxxxxxx xxxxxxxx pro xxxxxxxx prvky uvedené xx obalu xxxxxxxxx xxxxxxxx přípravků (xxxx xxx „xxxxxxxx x xxxxxxxxxx prvcích“).
Předkládaný návrh xxxxxx xx xxxx xxxxxxxxxx x xxxxxxxx Xxxxxxxx xxxx, xxxxxxxxxxx xxxxxxxx orgánů Xxxxxxxx xxxx x xxxxxxxx xxxxxxxx zásadami xxxxx Xxxxxxxx xxxx.
6. Xxxxxxxxxx xxxxxxx x xxxxxxxxxxxxx xxxxxxxxx, xxxxx je Xxxxx republika vázána
Navrhovaná xxxxxx neodporuje xxxxxxxxxxxx xxxxxxxx, kterými je Xxxxx xxxxxxxxx xxxxxx. Xxxxx xx x xxxx xxxxxxxxxxx smlouvy:
- xxxxxx x xxxxxxxxx xxxxxxxx xx xxxxxx x posuzování xxxxx, xxxxxxxxx x xxxxxxxx xxxx Xxxxxxxxx xxxxxxxxxxxxx x Xxxxxxxxx (Xx. xxxx. X 229, 17.8.1998, s. 3),
- xxxxxx x vzájemném xxxxxxxx xx xxxxxx x posuzování xxxxx xxxx Xxxxxxxxx xxxxxxxxxxxxx x Xxxxx Zélandem (Xx. xxxx. X 229, 17.8.1998, s. 62),
- xxxxxx x xxxxxxxxx xxxxxxxx xxxx Xxxxxxxxx xxxxxxxxxxxxx x Xxxxxxx (Xx. věst. X 280, 16.10.1998, x. 3),
- xxxxxx x xxxxxxxxx xxxxxxxx xxxx Evropským společenstvím x Xxxxxxxxx (Xx. xxxx. X 284, 29.10.2001, x. 3),
- xxxxxx mezi Xxxxxxxxx xxxxxxxxxxxxx x Xxxxxxxxxx xxxxxxxxxxx x vzájemném xxxxxxxx xx vztahu x xxxxxxxxxx xxxxx (Xx. věst. X 114, 30.4.2002, x. 369).
7. Xxxxxxxxxxxxx xxxxxxxxxxx x xxxxxxxx xxxxx xxxxxxxxxx právní úpravy xx státní rozpočet, xxxxxxx veřejné rozpočty, xx xxxxxxxxxxxxx xxxxxxxxx Xxxxx xxxxxxxxx, xxxxxxxx xxxxxx, xxxxxx xxxxxx xx xxxxxxxxxx xxxxxxx xxxxxxxx, xxxxxxx xxxxx xxxxxxxx xxxxx, xxxxx xx xxxxxxxxxx xxxxxxxxxx x xxxxxxxxxxx menšiny, xxxxxx xx životní xxxxxxxxx
Xxxxxxxxxx úpravy za xxxxxx xxxxxxxxx adaptace xxxx xxxxxxxxxxxxxxxx předpisů Xxxxxxxx xxxx xxxxxxx xxxxxxxxxxxx xxxxxxxx xxxxx xxxxxxxxxxx x navýšení xxxxxx xxxxxxxxxxxxxxx xxxx xxxxxx xxxxxxxxxx xx xxxxx xxx xxxxxxxxx xxxxx xxxx xxxxxxxxxxx xxxxxxxxxx x xxxxxxxxxx xxxx xx xxxxxxxxxx xxxxxxx spadajících xxx xxxxxxxxxxx kapitolu Ministerstvo xxxxxxxxxxxxx, xxxxxxxxx na xxxxxx Xxxxxx.
Xxxxxxxxxx právní xxxxxx nebude mít xxxxx xxxxxxxx xxxxxx, xxxx dopady xx xxxxxxxxxx xxxxxxx xxxxxxxx (xxxxx xxxxxxxx xxxxx, xxxxx xx xxxxxxxxxx xxxxxxxxxx, xxxxxxxxxxx xxxxxxx), xxx dopady na xxxxxxx xxxxxxxxx.
Xxxxxx xx xxxxxxxxxxxxx prostředí Xxxxx xxxxxxxxx se xxxx x xxx xxxxxxxxxxx xxxxxx o xxxxxxxx, xxxxx do něho xxxx xxxxxxx jeho xxxxxxx, xx. xxxxxxx č. 70/2013 Sb., x mají xxxxxxxxx xxxxxxxx, případně xx xxxx xxxxx x nařízení o xxxxxxxxxx xxxxxxx. Xxxx xxxxxx xxx xxxx xxxxxxxxx při xxxxxxxxxxxx xxxxxx právních xxxxxxxx. X xxxxx směru xx xxxxx xxxxxxx xx xxxxxxxxx xxxxxx, xxxxxx xxxxxx x xxxxxxxxx dopadů regulace (XXX) x xxxxxx č. 70/2013 Sb. x xxxx xx xxxxxxxxx zprávu XXX k nařízení x xxxxxxxxxx xxxxxxx xxxxxxxxx „Impact Assessment“. X této podrobné xxxxxx xx uvádí, xx v xxxxxxx x čl. 4 xxxxxxxx 2011/62/XX x xx. 54x xxxx. 2 x 3 xxxxxxxx 2001/83/XX Komise xxxxxxxxx xxxxxxx, náklady a xxxxxxxxxx xxxxxxxxxx xxxxxxx xxxxxxxx xxx xxxxxxxxxxxxxxx x technické xxxxxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx x xxxxxxx xxxxxxx xxxxxxxxxx xxxxx x xxxxxxxx x správu xxxxxxx xxxxxxx.
Xxxxxxx realizace xxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx xxxxx dopadat xx xxxxxxx x xxxxxxxx xxxxxxxxxx x xxxxxxxxxx xxxxxxxx přípravků xxxxxxxxxx xxxxxxxxxx xxxxx. Výrobci xxxxxxxx xxxxxxxxx opatřených xxxxxxxxxx prvky ponesou xxxxxxx xx zřízení x xxxxxx xxxxxxx xxxxxxx (tato xxxxxxxxx xxxx xxxxxxx xxx xxxxxxxx 2011/62/EU, která xxxx xxxxxxxxxxxxx do xxxxxxxx xxxx XX xxxxxxx č. 70/2013 Sb.). Xxx xxxxxxx x souběžné xxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx xx xxxxxxx humánních xxxxxxxx xxxxxxxxx další xxxxxxx, xxxxx xxxxxxx s xxxxxxxx xxxxxxxxxxx xxxxxxx xxxxx xxxx xxxxxxx xxxxx (xxxxxxxx xxxxxxx) x xxxxxxxxxx do xxxxxxxxxxxx xxxxxxx, xxx xxxx xxxxx odesílat xxxxxxxxx x xxxxxxxxxxx xxxxxxxxxxxxxxxx xx xxxxxxx xxxxxxxx. Xxx bylo xxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxxxxxxx, xxxx být xxxxxx linky vylepšeny xxxxx xxxxxxxx a xxxxxxxxxx softwarem.
Náklady xxxxxxx xxxxx xxxxxxxx xxxxxxxxxxxx xxxxxxxxxxxxx xxxxxxxx a xxxxxxx x hlediska:
- xxxxxxxxx xxxxxxx (xxxxxxxxxx xxxxxxx xxxxxxxxxxxxxx mechanismů xxxxxxxxx xxxxxxxx xxxxx xxxxxxxxxxxxxx xxxxxxxx XX xx xxxxxxx xxxxxxx xxx více xxxxxxxxx xxxxx, xxx xxxxxxxx xxxxxxxxxxxx xxxxxxxxxxxx xxxxxxxxx xxxxxxx),
- ochrany xxxxx xxxxxxx x držitelů xxxxxxxxxx x registraci (xxxxxxx xxxxx xxxxxxxxxx xxxxxxxx přípravku xx xxxx xxxxxx x xxxxxxx xxxxxxxxx xxxxxxx),
- xxxxxxxxx x snížení xxxxxxx při xxxxxxxxx xxxxxxxxx a vracení xxxxxxxx xxxxxxxxx, xxx xxxxxx xxxxxx xxxxx (xxxxx a doba xxxxxxxxxxxxx) uvedené x xxxxxxxxxx identifikátoru.
Vznikají xxxx xxxx náklady xx xxxxxx xxxxxxx, xxxxxxx xxxxxx XX, nové xxxxxx x v xxxxx lékáren x xxxx xxxxxxxxxx XX. X xxxxxxxx xxxxxxxxxxx xxxx je xxxxxxx „xxxxxxxxx xxxxxxx“, který xxxx xxxxxxxxxxx nebezpečný xxxxxxxxx xxxxxxxx. Xxxxx xx xxxxxxxx, aby xxxx svou xxxxx xxxxx v xxxxxxxx xxxx. Xxxxxxx xxxxx xxxxxxx xx xxxxx xxxxxxxxx, xxxx z xxxxxxxx nákladů x xxxxxxx, xx jednoznačně xxxxxxxxxxx, x xx xxxxx xxxxxxxxx xxxxxxx xxxxxxxxx xxxxxx. Xxxxx xx xxxxxxxxxxxx (jak xx xxxxxx EU, xxx xxxxxxxxxxxx) xxxxxxx xxxxxxx xxxxxx tak, xxx je xxxxxxxxxx.
Xxxxxx xx xxxxxxxxxx xxxxxxxx xx xxxx s xxxxxxxx xxxxxxxxx, xxxxx xxxxx navazovat xx xxxx xxxxxx, se xxx xxx xxxxxxxx xxxxxx xxxxxxxx x xxxxxxxxxx prvcích xxxx xxxxxxxx, xxx xxxxx xxxxxx xxxx xxxxxx, xxxx xxxxxxx xxxx xxxx, xx xxxxxxx xxxx Česká republika xxxxx xxxxxxxx o xxxxxxxxxx prvcích xxxxxxx xxxxxxx xxxxxx xxxxxxxxx, xxxxx xx budou xxxxxxxxxx na xxxxx xxxx.
Xxxxxxx distributorů léčiv x xxxx xxxxxxxxxxx xxxx zmocněných x xxxxxx xxxxxxxx xxxxxxxxx xxxxxxx s xxxxxxxxxx xxxxxxxx xxxxxxxx xxxxx x vyřazovat xxxxxxxxx xxxxxxxxxxxxx xx systému xxxxxxx (xxxxxxxx xxxxxxxxxx xxxxxxx 2X kódů, xxxxxx distribučních x xxxxxxxxxxxx programů xxxx.).
Xxxxxxxx xxxxx xxxxxxxxxx xxxxxx xxxxxx xx xxxxxxxxxxxxx xxxxxxxx x xxxxxxxx xxxxxxxxxxxx ochranných xxxxx xx xxxxxxxxxxx xxxxxxxxxxx xx očekává xxxxxxxxx, xxxxx údaje xxxxxxxxxx xx k xxxxxxxxxxx xxxxxxxxxxxxxx xxx xxxxxx xx textu xxxxx x rámci jakéhokoli xxxxxx s xxxxxxx xx informace o xxxxxxxxx - xxxx. xxxxxx o prodloužení xxxxxxxxx xxxxxxxxxx, xxxxxx x xxxxx xxxxxxxxxx xxxx XX, xxxx XX xxxx typu XX. Předložení xxxxxxxx xxxxxxx x xxxxx xxxxxxxxxx xxxxxxxxxxxxxxxxx xxxxxxxxxx xx xxxxxxxx xxxxx x situaci, xxxxx x xxxxxxxxxx období xxxxxx xxxxxxxxxx xxxxx xxxxx registrace, xxxxx xxxxxxx xxxxxxxxx x xxxxxxxxx. Xxxxxxxxxx žádosti x xxxxx registrace xxx xxxxxxxx xxxxxxxxxx x ověření manipulace x obalem xx xxx xxxxxxxx xxxxx x případě, xxx xxxxxxxxxx k xxxxxxx xxxxxxxxxx x xxxxxx xxxx xxx vliv xx xxxxxxxxx obalu, xxxx xxxxxxx systém xxxxxxxx xxxxx. Xxxx xxxx xxxxxxxxx, xx xxxxxxxxx xxxxxxxxxxxxx x xxxxxxxxxx k ověření xxxxxxxxxx s xxxxxx xx možné xxxxxxxxxxxxx xxxx xxxxxxxxxxx nebo xxxxxxxxxx příslušné xxxxxxx x změnu xxxxxxxxxx, xxxxx xxxxxxxxxxxx ochranných xxxxx xx xxxx xxxx xxxx xx xxxxxxxxx obalu. Xxxxxxxx x xxxx xxxxxxx xxxxxxxxxxx, xxx xxx xxxxxxx léčivých přípravků xxxxxx xxxxx xxx xxxxxxxx ochranných xxxxx xxxxxxxxxx zvláštní xxxxxx x xxxxx xxxxxxxxxx x xxxxxxxx prvky xx xxxxx implementovat xxx před xxxxxxxxxxx xxxx schválením xxxxxxxxx xxxxxxx x změnu xxxxxxxxxx, xxxxx xx xxxxxxxxxxxxx xxxxxxxx x xxxxxxx xxxxxxxx a x oblasti prodlužování xxxx na xxxxxxxx xxxxxxxxxxxx žádostí xxxx xxxxxxxxx.
Xxx obecně xxxxxxxxx x tím, xx xxxxxxx xxxxxxx a xxxxxxxx xxxxxxxxxx x xxxxxxxxxx léčivých přípravků, xxxxxxx xxxxx xxxxxxx xxxxxxxx xxxxx, xx x xxxxxx xxxxxxxx xxxxxxxxxx prvků xx xxxxxx xxxx xxxxxxxxx xxxxx. Xxxx zvýšení xxxx bude ve xxxxxx k xxxxxxxxx xxxxxxx xxxxxxxxxxxxxxx xxxxx xxxxxxxxxxxx, xxxxx xxxxxxx xx zavedení XX xxxx x léků xxxxxxxx xx xxxxxx xxxx zcela xxxxx xxxxxx xxxxx než xxxxxxxx xxxxxxx na xxxxx, xxxxxx a xxxxxxxxxx xxxxxxxx xxxxxxxxx. Xxxx léčivých přípravků, xxxxxxx xxxxx xx xxxxx xx lékařský xxxxxxx, je xx xxxxxxx případů regulována xxxxxxxx stanovení xxxxxxxxx xxxx xxxxxxxx xxxxxxxxxxx, xxxxxx xxx xxxxxx xxxxx xx xxxxxxx xxxxxx zpoplatněné xxxxxxx. Xxxxxxxx xxxx a xxxxxxxx xxxxxx léčivého xxxxxxxxx x xxxxxxxxxx xxxxxxxxx xxxxxxxxxxx xxxxxxxxx xxxx xxxxxxxxxxx v xxxxx xxxxxxxxx řízení. Xxxxx xx x xxxxxx Xxxxxxxx xxxx (xxxxxx ČR) xxxxx xxxxxxx xxxxxxx tzv. xxxxxxxx xxxxxxxx xxxxxxxxxxxxx - xxxx xxxxxxxxx xxxx x úhrady xxxxx xxxxxxxxxx xxx xxxxxxxx xx xxxxxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxx x xxxxxxxxx, xxxxx xx x drtivé xxxxxxx xxxxxxx xxxxxx xxxxxxxxxx xxxxxxxx xxxx x ČR vliv xx xxxxxx xxxxxxxx xxxxxxxxx x xxxxxxxxxx xxxxxxxxx xxxxxxxxxxx xxxxxxxxx. Xxxxxxxx k xxxxx xxxxxxxxx xxxxx konkurenčního xxxxxxxxx xx xxxxxxxxx (xxxxxxx) xxxx x xxxxxx se xxxxxxxxx xxx léčivých přípravků x důvodu xxxxxxxx xxxxxxxxxx prvků xxxxxxxxxxxxx, xxxx xxxxxx xxxxxxxxxxx xx xxxxx inflace. Xxxx regulovaných xxxxxxxx xxxxxxxxx xxxx maximální, xx xxxxxxx xxxxxxxxx xxxxxxxxxxx xxxxxxxxx xx xxxxxxx xxxxxx xxxxxxxx xxxxxxxxx, xxxxxxx jeho xxxx.
Xxxxxxx xxxxxxxxxxxx xxxxx xxxxxxx x xxxxxxxxxx xxxxxxxx xxxxxxxx xxxxx x xxxxxxxxx xxxxxxxxx xxxxxxxxxxxxx xx systému xxxxxxx. Jedná se x xxxxxxxx xxxxxxxxxx xxxxxxx 2D kódů, xxxxxx xxxxxxxxxxxx programů xx xxxxxxx xx xxxxxx xxxxxx. Xxxxxxx xxxxx xxxxxxx je xxxxx xxxxxxxxx, xxxx x xxxxxxxx xxxxxxx x přínosů, xx xxxxxxxxxxx xxxxxxxxxxx, a xx xxxxxx xxxxx xxxxxxxxx ochrany xxxxxxxxx xxxxxx. Xxxxx xx xxxxxxxxxxxx (xxx xx xxxxxx XX, tak xxxxxxxxxxxx) xxxxxxx xxxxxxx xxxxxx xxx, xxx xx xxxxxxxxxx.
Xxxxxxxxxxx x xxxxxxxx xxxxx návrhu x xxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxx přípravků xxx xxx hodnocen v xxxxx novely xxxxxxxxxxx xxxxxxxx xxxxxxxx 536/2014, x lze na xxx x tomto xxxxxxx. Xxx xxxxxxxx xxxx prováděcími xxxxxxxx x xxxxxxxx 536/2014 x xxxxxxxxx x x podrobnostech xxxxxxxxx xx, xx xxxxxxxx x klinickém xxxxxxxxx xxxxxx. Xxxxxx xxxx xxxxxxxx 2017/1572 xxxx xxxxxxxx právě xxxxxxx xxxxxxxx 2017/1569 a xxxxxxxxx xxxxxxxxxx rozdíly xx xxxxxxxxx xxxxxx xxxxxx, xxxxx se xxxx xxxxxxxxxxxxx x xxxxxxxxxx dopadu.
Státní xxxxxxxx xxxxxx xxxxxxx administrativními x xxxxxxxxxxxx xxxxxxx xxxxxxxxxxxxx x xxxxxxx xxxxx předpokládaných xxxxx xxxxxxxxx nařízeními x xxxxxxx, jak bylo xxxxxxx x xxxxxxxx xxxxxx k návrhu xxxxxx zajišťujícímu adaptaci xxxxxxxx 536/2014 (zákon č. 66/2017 Sb.).
8. Xxxxxxxxxx xxxxxx xx vztahu x xxxxxxx xxxxxxxx x xxxxxxxx xxxxx
Xxxxx xxxxxx x xxxxxxx ochranných xxxxx léčivých xxxxxxxxx xxxxxxxxx xxxxx nové xxxxxxxxxx xxxxxxxx údajů. Xxxxxx xxxxxxxxx pravosti xxxxxxxx xxxxxxxxx xxxx xxxxxxxxxxx informace xxxxxxxxxx xx xxxxx x xxxxxxx přípravkům xxxx xxxxxxxx, jejichž xxxxx xxxxxxx ochranné xxxxx. Xxxxxx xxxxxx xxxxxxxxxxx xxxxxx údaje pacientů, xxxxxx byly xxxxxx xxxxxx xxxxxxxxx, xxxxxxx xxxxx ponesou xxxxxxxx xxxxx. Xxxxxxxx xxx xxxxx xxxxxxxxx zneužití xxxxxxxx údajů. Návrh xxxxxx x xxxxx xxxxxx xxxxxx xxx xxxxx negativní dopady xx oblast ochrany xxxxxxxx a osobních xxxxx.
Xxxxxxxxxx právní xxxxxx xx x xxxxxxx xxxxxxx klinické xxxxx xxxxxx xxxxxxx ochrany xxxxxxxx, x xx xxxxxxxxxxxx xxxxxxxx. Xxxxxxxx 2017/556 xxxxxxx xxxxxxxxxx xxxxxx široké xxxxxxxxx, xxxxx xx xxxx xxxxxxxx xx xxxxxxx x xxxxxxxxx souvisejících x xxxxxxxxx xxxxxxxxxx. Xxxxxxxxxx xxx zcela xxxxx xxxxx xxx xxxxxxx k osobním xxxxxx xxxxxx xxxxxxxxx xxxxxxxx xxxxx.&xxxx; Xxxxxxxx xxx xxxxxxxxx xxxxxxx xxxxxxxxx informací, xxxxxxx xxxxxxxx xxxxx subjektů xxxxxxxxxx xxxxxxxxx xxxxxxxxxx xx xxxxxx, xxxxx x důvěrných xxxxxxxxxx xxxxxxxxx, xxxx xxxxxxxxxx x odborníky xxxxxxxxxx xx xx xxxxxxxxxx xxxx xxxxxxxxxx xxxxxxxxx xxxxxxxxxx x xxxxxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxx Xxxx a vnitrostátních xxxxxxxx xxxxxxxx. V xxxxxx 14 xxxxxx xxxxxxxxxxx a xxxxxxxxxx xxxxxxxxxx xx xxxxxxxxxxx xxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxx jakýchkoli informací, x nimž xxxxxxx xxxxxxx x důsledku xxxxxxxx správné klinické xxxxx.
Xxxxxxxx dále xxxxxxxx xxxxx, xx xxxxxxxxx xxxxxx xxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxx XX (x xxxxxxx x čl. 78 xxxx. 6 xxxxxxxx x. 536/2014) xxxxxxx xxxxxxxxx xxxxxx údaje xxxxxxxx (čl. 13 xxxxxxxx 2017/556)
Xxxxxxxxxx x xxxxxxxxx xxxxxxxxxx se na xxxxxxxxxx jsou xxx xxxxxxxxxxxx osobních údajů xxxx xxxxxx xxxxxxxxx xxxxxxxx xxxxxxxx x xxxxxxx xxxxxxxx xxxxx č. 2016/679 (Xxxxxxx Xxxx Xxxxxxxxxx Xxxxxxxxxx, GDPR).
Nařízení č. 2017/1569 x xxxxxxxx XXX upravuje inspekce, xxxxxxxxxxxxxxx xxxxxxx xxxx xxxxxxx státy xxxxxxx xxxxxxxx, aby x xxxxxxx xxxxxxxxxx xxxxxxxxx xxxx xxxxxxxxxx pravidla xxxxxxx xxxxxxx xxxxx xxxxxxxxxxx xxxxxxxx přípravků xxxxxxxxx x xxxxx xxxxxxxx. I xxxx xxxxxxxx svěřuje xxxxxxxxxxx xxxxxx široké pravomoci, xxxxx se xxxx xxxxxxxx xx xxxxxxx x xxxxxxxxx souvisejících x výrobou xxxxxxxxxxx xxxxxxxx přípravků. Xxxxxx x v tomto xxxxxxx xxxx inspektory xxxxxxxxxxxx, xxxx xxxxxxx, xx informace xxxxxxx xx základě xxxxxxxx xxxx zůstat důvěrné.
Transpozice xxxxxxxx xx nedotkne xxxxxxxxxx xxxxxx x xxxxxxxx, xxx xxxxxx x zdravotních službách, xxxxxxx xx zajišťována xxxxxxx xxxxx, které xxxxxxxxxx xxxxxxx x xxxxx xxxxxxxxxxx kontrol x inspekcí.
Kontroly správné xxxxxxxx xxxxx x xxxxxxx xxxxxxx xxxxx xxxxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx budou xxxxxxxx xxxxx xxxxxxxx č. 536/2014, x xx budou xxxxxxxxx x xxxxxxx x xxxxxxxxxx 556/2017 x 1569/2017. Xxxxxxxx xxxxxxxxx podle xxxxxx x xxxxxxxx xxxx xxxxxxxxx x xxxxxxx x kontrolním xxxxx, xxxxx xxxxxxxx xxxxxxxxxx xxxxxxxx xxxxx xxxxxx xxxxx fyzických xxxxx, xxx xxxxxxx xxxxx xxxxxxx xx základě xxxxxxxxx kontroly. Jakékoliv xxxxxxxx x xxxxxx xxxxxxxx bude představovat xxxxx, xxxx xxxxxxx xxxxxxxx xxxxxx xxx Xxxxx xxxxxxxxx xxxxxxxx xxxxxx. Osobní xxxxx xxxx navíc xxxxxxxx xxxxxxxxx xxxxxxx, x x účinností od xxxxxx 2018 xxx xxxxxxxxx XX.
Xx xxxxxxx xxxx uvedeného xxx xxxxxxxxxxx, že xx xxxxxx x ochraně xxxxxxxx x xxxxxxxx xxxxx xxxxxxxxxx xxxxxx xxxxxxxxxxxxx xxxxxxx riziko.
9. Xxxxxxxxxx xxxxxxxxxx rizik
V xxxxx xxxxxxxx návrhu xxxxxx byla xxxxxxxxx xxxxxxxxx xxxx xxxxxxxxxx xxxxx x souladu x xxxxxxxxx zpracovanou Xxxxxxx hodnocení dopadů xxxxxxxx Xxxxx xxxxx Xxxxx republiky. Xx xxxxxx posouzení xxxxxxx, xx x návrhu xxxxxx xxxxxx xxxxxxx xxxxxxxx xxxxxxxxx, xxxxx xxxx nepředstavuje vzhledem x xxxxxxxxx xxxxxxxxxxx xxxxx riziko.
Oblast provádění xxxxxxxx xx mohla xxxxxxxxxxxx xxxxxx xxxxxxxx xxxxxxxxx, xxxxxxx xxxxx xxxx se odráží x xxxxx samotných xxxxxxxx: x xxxx xxxxxxxxxx xxxx ustanovení xxxxxxxx xxxxxxxxxx xxxxxxxxx xx xxxxxxxxxxx inspektorů. X nařízení 2017/1569 xx xx článek 23, xxxxx xxxxxxxx xxxxxx xxxxxxxx, xxx inspektoři xxxxxx xxxxxxxxx xxxxxx xxxxxxxxxxx vlivům, které xx xxxxx ovlivnit xxxxxx nestrannost a xxxxxx.&xxxx; Xxxxxxxx xxxxx, xx xxxxxxxxxx musí xxx xxxxxxxxx xxxxxxx xx zadavateli, vedení x xxxxxxxxxxxx míst xxxxxxxxxx xxxxxxxxx, xxxxxxxxxxxx x xx osobách xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx. Xxxxxx inspektorům povinnost xxxxxxxxxx xxxxxxxxxx xxxxxxxxxx x svých xxxxxxxxxx xxxxxxx xx xxxxxxxx xxxxxxxxx inspekcemi xxxx x jiných xxxxxxx xx ně. Příslušný xxxxx vezme xxxxxxxxxx x xxxxx xxx xxxxxxxxxxx konkrétních inspekcí xxxxxxxxxxx xxxxxxxxxxx.
X xxxxxxxx 2017/556 ustanovení článku 5 xxxxxxx, xx inspektoři xxxxx xxx xxxxxxxxx xxxxxxx vlivu, který xx mohl zpochybnit xxxxxx xxxxxxxxxxx xxxx xxxxxx vyjádření, xxxxx xxx ve střetu xxxxx. Xxxxxxx musí xxx nezávislí na xxxxxxxxxx, zkoušejících xxxxxxxxxxx xx xxxxxxxxxx xxxxxxxxx, xxxxxxx financujících xxxxxxxx xxxxxxxxx x xx xxxxxxxxxx xxxxxxxx xxxxxxxxxxx xx na xxxxxxxxx xxxxxxxxxx xxxxxxxxx. Xxxxxx x xxxx xxxxxxxx xxxxxx xxxxxxxxxxx každoročně xxxxxxxxxx xxxxxxxxxx o xxxxx xxxxxxxxxx xxxxxxx x jiných vazbách xx xxxxxxxx, xx xxxxxxx může xxx xxxxxxxx xxxxxxxxx. X xxxxxx xxxxxxxxxx xx xxxxxxxx xxx xxxxxxxxxxx xx xxxxxxxxx inspekci. Xxxxxxxxxx xxxxxx xxxxxx xx xxxxxx xxxxxxxxxx xxxxxxxxxx x xxxx xx xxxxxxxxxx. Xxxx xxxxxxxxxx jsou xxxxx xxxxxxx.
Xxxxx xx xxxx xxxxxxxxxxx xxxxxxxx 2017/1572, x čl. 3 xxxxxx xxxxxxxx xxxxxx xxxxxxxxx xxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx x čl. 111 xxxx. 1a směrnice 2001/83/XX zajistit, xxx xxxxxxx, xxxxx mají xxxxxxxx xxxxx čl. 40 xxxx. 1 x 3 xxxxxxxx 2001/83/ES, xxxxxxxx zásady x xxxxxx xxx xxxxxxxx xxxxxxx praxi xxxxxxxxx xxxxx xxxxxxxx. Xxxx xxxxxxx, že při xxxxxxx xxxxx x xxxxxx pro xxxxxxxx xxxxxxx xxxxx xxxxxxxxxx xxxxxxx x xxxxxxxxx xxxxxx k podrobným xxxxxxx xxxxxxxx x čl. 47 druhém xxxxxxxxxxx xxxxxxxx 2001/83/XX. V xxxxxxx xxxxxxxx xxxxxxxxx xxx moderní xxxxxxx xx xxxxxxxxx xx xxxxxxxxx pokynům xxx xxxxxxxx xxxxxxx xxxxx xxxxxxxxx se xxxxxxxx xxxxxxxxx pro xxxxxxx xxxxxxx, jež jsou xxxxxxx x článku 5 xxxxxxxx (XX) č. 1394/2007 o xxxxxxxx xxxxxxxxxxx pro moderní xxxxxxx. Xxxxxx 3 xxxxxx rovněž členským xxxxxx xx svých xxxxxxxxxxxxxx xxxxxxxx a xxxxxx xxxxxxxx navržený xxxxxx xxxxxxx, xxxxx xxxx xxxxxxxxxx x xxxxxx xxxxxxxxxxxx xxxxxxxxx. Xxxxxxx systém xxxxxxx xx xxxxx potřeby xxxxxxxxxxx. Xxxxxxxxxx xxxxxx xxxxxx xxxxxxxxxxx xxxxx xxxxxx x novelizačním xxxx 3 - xxxxxxxx §13 odst. 3 xxxx. x) xxxxxx x xxxxxxxx. Xxxxxx jakosti zaručí xxxxxxx korupčních rizik xxxxxxxx xxxxxxxxxxx, xxxx xx xxxx xx xxxx xxxxxxxxx xxxxxxxxxx.
Xx xxxxxxx xxxxxxxxx lze xxxxxxxxxxx, xx xxxxxxxxx xxxxxxxxxx xxxxx xxxx xxxxxx xxxxxx xxxxxxxxx xxxxxxxx xxxxxxx.
10. Zhodnocení xxxxxx xx xxxxxxxxxx xxxx obranu xxxxx
Xxxxx xxxxxx xxxx vztah x xxxxxxxxxxx xxxx xxxxxx xxxxx.
II. XXXXXXXX XXXX
ČÁST PRVNÍ Změna zákona o léčivech
Xx xxxxxxxx xxx xxxxx x. 2 xx xxxxx xxxxxxx xxxxx xx nařízení Komise x xxxxxxxxx xxxxxxxxx (XX) 2016/161 xx xxx 2. xxxxx 2015, kterým se xxxxxxxx směrnice Evropského xxxxxxxxxx a Xxxx 2001/83/XX xxxxxxxxxx podrobných xxxxxxxx pro xxxxxxxx xxxxx uvedené xx xxxxx humánních xxxxxxxx xxxxxxxxx, které je xxxxx xxxxx xxxxxxx xxxxxx xxxxxxxxxx na xxxxxxxx x Xxxxx xxxxxxxxx.
K bodu 2 (§5 xxxx. 7):
Xx xxxxxxxx xxxxxxxx xxxxxxxx prodeje xxxxxxxxxxx xxxxxxxx přípravků x xxxxxxx humánních a xxxxxxxxxxxxx léčiv.
K bodu 3 (§6 xxxx. 2):
Jedná se x xxxxxxxxxxx článku 2 xxxx. 3 xxxxxxxx Xxxxxx (XX) 2017/1572, xxxxx definuje xxxxxxxx xxxxxxx xxxxx xxxx xx část xxxxxxxxxxxxx xxxxxxx, která xxxxxxxxx, xxx byly léčivé xxxxxxxxx xxxxx vyráběny, xxxxxxxx x kontrolovány x souladu xx xxxxxxxxx xxxxxxx xxxxxxxxxxx xxxxxx zamýšlenému xxxxxx. Xxxx xxxxxxxx xx xxxxxxxx xx odst. 2.
Xxxxxxx xxxx xx xxxxxxxx na xxxxxx, xxxxx xxxx xxxx xxxxxxx nahradit.
K bodu 4 (§13 xxxx. 2 xxxx. x):
Xxxxxxxx x provozovatelů, xxxxxxx osob xxxxxxxxxxxxx x léčivy, xxxxxxxx xxxxxxxxxx x xxxxxxxxxx, xxxxxxxxxxxxxxxxx, xxxxxxx x xxxxxxx xxxxxxxxx xxxxx xxxxxx xxxxxxxx xxx x kontrole dodržování xxxxxxxxx xxxxxx x xxxxxxxx, xxx musí xxxxxxxxx x xxxxxxxx xxxxxxxxxx xxxxx xxxxxxxxxxxx xxxxxxxx Evropské xxxx xxx xxxxxx xxxxxxxxx xxxxx, xxx xxxx xxxxxxxx xxxxxxxx a xxxxxxxx xxxxxxxx xxxxxx xxxxxxxx. Xxxxx xx:
• Xxxxxxxx Evropského xxxxxxxxxx x Xxxx (XX) x. 1394/2007 (32007R1394), xx 13. xxxxxxxxx 2007 o xxxxxxxx xxxxxxxxxxx xxx moderní xxxxxxx x x xxxxx xxxxxxxx 2001/83/XX x xxxxxxxx (XX) x. 726/2004.
- Xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Xxxx (XX) č. 2016/793 (32016R0793) xx xxx 11. května 2016, x zamezení xxxxxxxxxxxx xxxxxxx x xxxxxxxxx xxxxxxxxx léky xx Xxxxxxxx xxxx.
- Xxxxxxxx Xxxxxxxxxx parlamentu x Xxxx (EU) x.536/2014 (32014R0536), x xxxxxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx x x xxxxxxx xxxxxxxx 2001/20/XX (xxxxxxxx xxxxx xxxx účinné)
- Xxxxxxxxx xxxxxxxx Xxxxxx (XX) č. 2017/556 xx dne 24. xxxxxx 2017 x podrobných xxxxxxxxxx xxx xxxxxxxxx xxxxxxxxxxx xxxxxxx xxxxxxx xxxxxxxx xxxxx xxxxx xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Xxxx (EU) č. 536/2014 (xxxxxxxx xxxxx xxxx účinné)
-- Xxxxxxxx Xxxxxx x xxxxxxxxx xxxxxxxxx (EU) č. 2017/1569, xxxxxx se xxxxxxxx xxxxxxxx Evropského parlamentu x Rady (XX) x.536/2014 stanovením xxxxx x xxxxxx xxx xxxxxxxx výrobní xxxxx xxx xxxxxxxxx xxxxxxx xxxxxx přípravky x xxxxxxxx xxxxxxxxx inspekcí
- Xxxxxxxx Xxxxxx v xxxxxxxxx xxxxxxxxx (EU) x.1252/2014 (32014R1252), xxxxxxxxxx xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Rady 2001/83/XX, xxxxx xxx x xxxxxx a xxxxxx xxxxxxx výrobní xxxxx xxx xxxxxx xxxxx xxx humánní xxxxxx xxxxxxxxx
- Xxxxxxxxx Nařízení Xxxxxx (XX) č. 699/2014 xx xxx 24. xxxxxx 2014 x designu xxxxxxxxxx xxxx xxxxxxxxxxxx osoby xxxxxxxxxx xxxxxx přípravky x prodeji xxxxxxxxxx xx xxxxx x x xxxxxxxxxxx, xxxxxxxxxxxxxx x kódovacích xxxxxxxxxxx x xxxxxxx xxxx xxxxxxxx
- Xxxxxxxx Xxxxxx x xxxxxxxxx xxxxxxxxx (XX) 2016/161 xx xxx 2. xxxxx 2015, kterým xx xxxxxxxx xxxxxxxx Xxxxxxxxxx xxxxxxxxxx a Rady 2001/83/XX xxxxxxxxxx podrobných xxxxxxxx xxx xxxxxxxx xxxxx xxxxxxx na xxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx
K bodu 5 a 6 (§13 xxxx. 2 xxxx. x xx x):
X §13 xxxx. 2, xxxxx xxxxxxxx působnost Xxxxxxxx xxxxxx xxx xxxxxxxx xxxxx, se xxxxxxxx xxxxxxxxxxx xxxxxxxxxx.
Xxxxxxxxx xx xxxxxxxxx Ústavu v xxxxxxx xxxxxxxxxx xxxxxxxx xxx xxxxxxxx prvky, x xx x xxxxxx, xx v xxxx xxxx ustanovení xxxxxxxx o xxxxxxxxxx xxxxxxx (xxxxxxxx IX) xx upravují xxxxxxxxx x xxxxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx orgánu x xx xxxxxxxx xxxxx xx, xxx xxxxx, xxxxx orgán je xxx jeho území xxx xxxxxxxxxx x xxxxxxxxx xxxxxxxx x xxxxxxxx x xxxxxxxxxx xxxxxxx. Xx xxxxxx, xx x xxxxxxx xx dosavadní xxxxxx xxxxxx xxxxxxxxxx Xxxxxx, xxxxxxx regulační autority xxx xxxxxx humánních xxxxx, xxxx xxx xxxxxxxxxx orgánem k xxxxxxxxx uvedeným x xxxxxxxx x xxxxxxxxxx xxxxxxx xxxxx xxxxxx xxxxx xxxxx ústav.
Dále xx působnost Státního xxxxxx pro xxxxxxxx xxxxx xxxxxxxxx tím, xx je určen xxxxxxxx xxxxxxx xxxxxxxxxx x výkonu xxxxxxxxxx xxxxxxxxxxx xxxxxxxxx 2017/556 x nařízením 2017/1569. Xxx xxx x xxxxxx xxxxxxxx článku 17 xxxx. 6 x článku 25 nařízení x. 2017/1569 a xxxxxx xxxxxxxx článku 3 xxxx. 1, článku 12 x článku 13 xxxxxxxx x. 2017/556. Xxxxxx účinnosti xxxx části novelizačního xxxx xx xxxx xxx stejné, jaké xxxx xxxxxxxxx v xxxxxx č. 66/2017 Sb. xxx xxxxxxxxxx xxxxxxxxxx xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Xxxx (XX) č. 536/2014.
K bodu 7 (§13 odst. 3 xxxx. x)
Xxxxx xx x xxxxxxxxxxx čl. 3 xxxx. 3 xxxxxxxx 2017/1572 x xxxxxxxx čl. 22 xxxxxxxx 2017/1569. Xxxxxxxx 2017/1572 členským xxxxxx ukládá xx xxxxx inspektorátech xxxxxxxx x zavést důkladně xxxxxxxx xxxxxx xxxxxxx, xxxxx musí xxxxxxxxxx x xxxxxx xxxxxxxxxxxx xxxxxxxxx. Xxxxxxx systém xxxxxxx se xxxxx xxxxxxx xxxxxxxxxxx. Xxxxxx xxx nařízení 2017/1569 xxxxxxx xxxxxx xxxxxxxxxx xxxxxxx xxx xxxxxxxxxx xxxxxxxx, zavést x xxxxxxxxx xxxxx xxxxxxxx xxxxxx xxxxxxx. Systém xxxxxxx xx x xxxxxxx xxxxxxx aktualizuje.
K bodu 8 (§16 odst. 3 xxxx. j)
Jedná se x xxxxxxxxxxxx-xxxxxxxxxx úpravu xxxxxx xxxxxxxxxxx x xxxxxxxxxxxxxxx xxxxxxxxxx xxxxx xxxxxx xxxxx.
K bodu 9 (§22 xxxx. 2)
Smysl vložení xxxx „veterinárních xxxxxxxx xxxxxxxxx“ spočívá xx xxxxxxxxxxx, xx xxxxxxxxx xx xxxxxxxxxxx xxxxxxxxxx xxxxxxx klinické praxe xxxx ze xxxxxx x xxxxxxxx vyjmuty, xxxxx xxxx xxxxx xxxxxxxx xxxxxxxxxx xxxxxxxxx. Xxxxxxx zůstala xxxxxxxxxx xxxxxxx xxxx xxxxxxxxx xxx inspektory xxxxxxxxxxxxx xxxxxxxxxx xxxxxxxxx.
K bodu 10 (§23 xxxx. 1 písm. x):
Xxx xxxxxxx, xxx xxxxxxxxx provozovatele xxxxxxxxxx xxxxxxx Xxxxxxxx xxxxxx xxx xxxxxxxx léčiv xxxxxxxxx xx xxxxxxxx xxxxxx přípravek, xxx-xx x xxxxxxx xxxxxx xxxxxxxxx, xxxxxxxxx xxxxx x nařízení o xxxxxxxxxx xxxxxxx, xx xxxxx xxxx xxxxxxxxx xxxxxx výslovně x xxxxxx x léčivech xxxxxxxxx xxxxxxx x) xx §23 odst. 1 xxxxxx. Jedná xx xxxxxxxxx o xxxxxxx, kdy xx x padělaným xxxxxxx xxxxxxxxxx xxxxx lékař, xxxxx xxxx xxx xxxxxxxx x ochranných xxxxxxx žádnou povinnost. Xxxxxxxx xx xxxxxxxxxxx, xx xxxxxxxx se xxxx týkat x xxxxxxxxxxxxx xxxxxxxx přípravků, xxxxxxxx xx xx xxxxxx xxxxxx xxxxxxxxx xxxxxxx xxxxxxxxx na xxxxxxxx veterinární xxxxxx xxxxxxxxx Xxxxxxxxxxxxx xxxxxx.
K bodu 11 (§24 odst. 10):
Xxxxxxxxx xxxxx §24 xxxx. 10 xx x xxxxxxx s ustanoveními xxxxxxxxxx xxxxxxxx xxxxxxxx, xxxxxxxxxxxx na úrovni xxxxxxxxxxxxx xxxxx oblast xxxxxxxx xxxxxxx xxxxxx, xxxx. xxxxxxxxxxxx xxxxxxxx xxxxxxxx plnění xxxxxxx xxxxxxxx xxx xxxxx xxxxxxxxxx xx celní xxxxx Xxxx nebo xxxx xxxxx opouštějící, xxxxxx xx xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Xxxx (XX) č. 952/2013, xxxxxx se xxxxxxx xxxxx xxxxx Xxxx, x xxxxxxx xxxxx (xxxx xxx „UCC“). Xxxxxxxxxx článku 5 odst. 15 XXX xxxxxxxx xxxxx deklaranta xxxx xxxxx, xxxxx xxxxxx xxxxx xxxxxxxxxx (x xxxx jiné xxxxxxxxxxx xxxxx xxxxxxxxx) xxxxxxxx xxxxxx xxxx osobu, xxxxxx xxxxxx xx xxxx celní xxxxxxxxxx xxxxxx. Dále ustanovení článku 18 xxxx. 1 XXX xxx jakýchkoli xxxxxxx, omezení xx xxxxxx xxxxxxx, xx xx xxxxx xxxxx xxxx nechat zastoupit xxxxxx xxxxxxxxx, xxxxxxx xxxx zastoupení xxxx xxx xxxxx (xxxxxxxx xxxxx jménem x xx xxxx xxx xxxxx) xxxx nepřímé (xxxxxxxx xxxxx xxxxxxxx xxxxxx na xxxx xxx osoby). Článek 170 xxxx. 1 XXX xxxxx xxxxxxxxxxx xxx xxxxxxx, xxxx xxx xxxxxxxxxx xxxxxxx, omezení xx xxxxxx, že xxxxx x xxxxxxx xxxxxxx prohlášení xxxxxxxxx xxx xxxxxxx xxxxx xxxxxxxx povinnosti (např. xxxxx předložení souhlasu, xxxxxxxx xx xxxxxxx xxx xxxxxxxxxx xxxxx x xxxxx xxxxxxxxx xxxxxxxxxxx xxxxxx nebo xxxxxxx), xxxx xxxxxx xxxxx xxxxxxxxxx xxxx xxxxx xxxx xxxx xxxxxxxx. X kontextu xxxxx třech výše xxxxxxxxxxxx xxxxxxxxxx xx xxxxxx, že xxxxx xxxxxxxx xxxxxxxx xxxxxxxxx x ani neumožňují xxxxxxxxx xxxxx předpisům (xxxxxxxxxxxx, vnitrostátním) xxxxxxxx xxxxx xxxxx xxxxx xxxxxxxx, xxx dále xxxx xxx xxxxx xxxxx jedné ze xxxx forem xxxxxxxxxx. Xxxxx osoba, xxxx x xxxxxxx jakéhokoli xxxxxxxx (xxxxxxx či xxxxxxxx) xx xxxx xxxxxxxx zvolit zástupce, xxxxxxx xxxx xxxxxxxxxx xx xxxx xxxxxxxx xxxxxx buďto xxxx xxxxx (xxxxxxxxxxx ve xxxxxx definice xxxx xx xxx) xxxx xxxx nepřímé (xxxxxxxxxxx xxxx xxxxxxx zástupce). Xxxx xxxxxxxx tezi xxxxxxxxxx xxxxxxx xxxxxx xxxxxxxx, upravující xxxxxxxxx xxxxxx zákazů xx xxxxxxx xx xxxxxx xxxxx Xxxxxxxx xxxx x xxxx xxxxxxxxx xxxxxxx xxxxxxxxxxxxxx právních xxxxxxxx a xxxxxxxxxx, xxxxxxxxxx x xxxxxxxxxxxxxxx §24 xxxx. 10 xxxxxx o xxxxxxxx, xx v xxxx xxxxxxxxx.
K bodu 12 (§34 xxxx. 9):
Xxxxxxxx xx xxxxxxxxxx xxxxxxxxxx Xxxxxx x Xxxxxxxxxxxxx ústavu xxxxxxxxx xxxxxx o xxxxx xxxxxxxxxx léčivého xxxxxxxxx xxxxxxxxxx xxxx vyhrazené xxxxxx xxxxxxxxx x xxxxxxx xxxxxx skutečností xxxxxxxxxx se bezpečnosti xxxxxxxxxxx xxxxxxxx xxxxxxxxx, x xx x xxxx xxxxxx (xx xxxx).
K bodu 13 (§37 xxxx. 1):
X xxxxxx x xxxxxxxx xx třeba xxxxxxx dotčené ustanovení xxx, xxx xxxxxxxxxx xxxxxxxxxxx xxxx, xx xx zavádějí xxxxxxxxxx xxxxxxxx xxxxx: xx xxxxxxxxx xxxxxxxxxxxxx x xxxxxxxxxx x xxxxxxx xxxxxxxxxx s xxxxxx. Xxxxxxxx xx nutné xxxxxxxx xxxxxxx xxxxxxxxxxx xxxxxxxxxx xxxxxxx xxxx, xxxxx xxxxxx k xxxxxxxxxxxx léčivých xxxxxxxxx, xxxxx ochranné prvky xxxxxxxxx.
Xxx o xxxxxx xxxxxx xxxxxxxxxx xx xxxxxxxx x ochranných xxxxxxx, xxxxx xxxxxxxx xxxxxxxx xxx lineární xxxxxxx xxx (XXX), xxx 2X kód, xxxxx xxxxxx xxxxxxxxx xxxxxxxxxxxxx. Xxxxxx xxxxxxxxx xxx xxxxxxxxxx xxxxx xxxxx nadále xxxxxxxx XXX kód x xxxxxxxx xxxxxxxxx xx xxxxxxxxxx pro oba xxxx xxxxxxx xxxxx xxxx.
K bodu 14 (§37 xxxx. 7):
Xxxxxxxx 7 xxxxxx x léčivech xx xxxxxxxxxxxxx ustanovením směrnice 2011/62/EU a xx xxxxx xxx upravit x xxxxxxx x xxxxxxxxx x xxxxxxxxxx xxxxxxx.
K bodům 15 (§37 odst. 8):
Xxxxxxxx 8 xxxxxx x xxxxxxxx je xxxxxx xxxxxxxxxxxxx xxxxxxxxxxx xxxxxxxx 2011/62/XX x xx nutno xxx xxxxxxx x xxxxxxx x nařízením o xxxxxxxxxx xxxxxxx, xxxxx xx xxxx xxxxxx xx xxxxxxx xxxxxxxx x ochranných prvcích xxxxxxxxx jednak xxxxxx xxxxxxxxx, jejichž výdej xxxx xxxxx xx xxxxxxxx předpis, xxxxx xxxx být opatřeny xxxxxxxxxx xxxxx a xxxxxx přípravky xxxxxxxx xx xxxxxxxx předpis xxxx xx xxxxxxxx xxxxxxx x xxxxxxxx, xxxxx xxxxx být xxxxxxxx xxxxxxxxxx xxxxx. Xxxxxxxx x xxxxxxxxxx xxxxx xx věta xxxxx xxxx.
K bodu 16 (§45 xxxx. 7 písm. x) ):
Xxxxxxxxxxx léčivých xxxxxxxxx xxxx xxxxxxx xxxxx držitel xxxxxxxx x výrobě. Xxxxxxx xxxxxxxx x xxxxxxxxxx xxxxxxx se taktéž xxxxxxxx xx xxxxxxxx xxxxx, je xxxxx xx xxxxxx x xxxxxxxx xxxxxxx xxxxxxxxxxx xxxxxxxxx držitele povolení xxxxxxxxxx dovozu xxxxxxxx, xxx bylo provedeno xxxxxxx ochranných prvků x xxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx x xxxxxxxx xxxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx x xxxxxxx xxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx. Xxxxxxxx xxxxx xxxx x členských xxxxxxx Xxxxxxxx xxxx harmonizován x podléhá xxxxxxxx xxxxxxx xxxxxxx x xx svá národní xxxxxxxxx. Xxxxxxxx xxxx xxxxxxxxxx držitele xxxxxxxx xxxxxxxxxx xxxxxx xxxxxxx, xxx xxxxxxx pacientů xxxxxxxxxxx léčivé přípravky xxxxxxxxxxx x xxxxx xxxxxxxxxx xxxxxx xxxx xx stejné xxxxxx xxxx xxxxxxx xxxxxxxx xxxxxxxxx xxxxxx xxxxxxxxx, xxxxx xxxx zajišťovány xxxxxxxxx xxxxxxxxxx o xxxxxxxxxx. X Xxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxxx o xxxxxxxxxx x držitele xxxxxxxx xxxxxxxxxx xxxxxx xxxxxx xxxxxxx, xxxxxxx x xxxxxxxxx členských xxxxxxx Xxxxxxxx unie xxxx xxxx xxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxx (xxxx. Xxxxxxxxxx).
K bodu 17 (§64 xxxx. x):
Xxx o úplnou xxxxxxxxxxx článku 11 xxxx. 1 xxxxxxxx Xxxxxx (XX) 2017/1572, který xxxxxxx, xx xxxxxxx xx xxxxxxxxx xxxxxxxx x xxxxxxxx xxxxxx xxxxxxxx xxxxxxx, který xx x xxxxxxxxx xxxxx, xxx xx xxxxxxxxx kvalifikaci x xx xxxxxxxxx na xxxxxx. Xxxx xxxxx xx x xxxxxxxxx xxxxx xxxx více xxxxxxxxxx xxxxxxxx xxxxxxx xxxxxxxxx obsazených pracovníky x vybavených xxxxxxxxx xxx provádění potřebných xxxxxxxxxxx x zkoušek xxxxxxxxx xxxxxxx, obalových xxxxxxxxx a xxxxxxx xxxxxxxxxxxx x xxxxxxxxx xxxxxxxx přípravků xxxx xx x xxxxxxx xxxxxxxxxxx xxxxxxx.
K bodu 18 (§64 xxxx. x)
Xxx o xxxxxx xxxxxxxxxxx článku 13 xxxx. 1 xxxxxxxx Xxxxxx (XX) 2017/1572, xxxxx xxxxxx členským xxxxxx stanovit, aby xxxxxxx xxxxxx xxxxxx xxx xxxxxxxxxxx a xxxxxxxxxx xxxxxxxxx xxxxxxxx x účinným xxxxxxxx, xxxxxx lze okamžitě x kdykoli stáhnout xxxxxx xxxxxxxxx x xxxxxxxxxxx xxxx. Xxxxxxx xxxxxxxxx a xxxxxxxxx xxxxxxxxx reklamaci xxxxxxxx xx vady. Výrobce xx xxxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxx x x xxxxxxxxxxx xxxxxxxxx x xxxxxxxx rozhodnutí x registraci o xxxxxxxx xxxx, která xx xxxxx xxx xx xxxxxxxx xxxxxxx xxxx xxxxxxxxx omezení xxxxxxx, x xxxxx xx to xxxxx, xxxxx xxxx xxxx xxxxxx.
K bodu 19 (§64 xxxx. x)
Xxx o xxxxxx xxxxxxxxxxx článku 4 xxxx. 1 xxxxxxxx Xxxxxx (XX) 2017/1572, xxxxx xxxxxx členským xxxxxx xxxxxxxx, xxx xxxxxxx xxxxxxx xxxxxxxx byly xxxxxxxxx výrobci x xxxxxxx se správnou xxxxxxx xxxxx a x povolením k xxxxxx. Xxxx ustanovení xx použije xxxxxx xx léčivé xxxxxxxxx xxxxxx xxxxx xxx xxxxx. Xxx xxxxxxxx xxxxxx xxxxx xxxxxxxxx x xxxxxxxxx xxxxxx xxxx nebo xxxxxxxxxx xxxxxx xxxxxxxxxxx xxxxx.
K bodům 20 a 21 (§77 odst. 1 xxxx. b) a x)):
Xxxxx se x xxxxxxxxxxxx xxxxxxxxx xxxxxx xxxxxxxxxxxx textu x xxxxxxxxxx xx xxxxx xxxxxxxxx xxxxxx novelizačními xxxx.
Xxxxxxxx používaný xxxxxx xxxxxxxxxx imunologických xxxxxxxx xxxxxxxxx xxxxx xx xxxxxxxx xxxxxx xxx xxxxxxx v polovině xxxx 2009 a xx xx xxxxxxx xxxxxx zákona x xxxxxxxx xxxxxxxxxx pojištění, x x tím xxxxxxxxxxx xxxxxx xxxxxx x xxxxxxx xxxxxxxxx xxxxxx. Přestože xxxxx x této xxxxxxx xxxxx, xxxxxx xx xxxxxx x léčivech xxxxxxxxxx xxxxxxxxxx §82 xxxx. 2 písm. x) xxxxxx x xxxxxxxx, které nereflektuje xxxxxxxx xxxxxx distribuce xxxxxxxxxx xxxxx (xxx xxxxxxxxxxx xxx 29). Xxxxxxxxxx ustanovení §82 xxxx. 2 písm. x) a x xxx xxxxxxxxxxx ustanovení §77 xxxx. 1 xxxx. c) xxx 5 se xxxx.
K bodu 22 (§77 odst. 1 xxxx. x bod 11):
Xxxxx se x xxxxxxxx a xxxxxxxxx xxxxx xx xxxxxx xxxxxxxxx x praxi xxxxxxxxx možnosti xxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxx, která xxxx v xxxxxxx x §82 xxxx. 2 xxxx. x) xxxxxxxxx k výdeji xxxx xxxxxxx léčivých xxxxxxxxx.
K bodu 23 (§77 xxxx. 1 xxxx. c xxx 12):
V souvislosti x xxxxxxxxxx xxxxxxxxxx xxxxxxxxxxxxx x xxxxxxxx x xxxxxxxxxx xxxxxxx, xx. ověřování ochranných xxxxx x xxxxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx v xxxxxxx xxxxxxxxxxxxxx xxxxxxxx xxxxxxxxx xx xxxxxxxxxxxx x případě xxxxxxxxxx xxxxxxxxxxxxxx léčivých xxxxxxxxx xx ordinací xxxxxx, xxxx xxxxxxxxx úprava xxxxxx ustanovení, x xx xxx, aby xx nejméně xxxxxxxxxx xxxxxxxxx xxxxxx xxxxxxx xxxxxxxxxxxxxx xxxxxxxx xxxxxxxxx.
K bodu 24 (§77 xxxx. 1 xxxx. x):
X xxxxx xxxxxxxxxx xxx x xxxxxxxx článku 23 nařízení x ochranných xxxxxxx, xxxx se v xxxxxx xxxxxxx xx xxxxxxx xxxxxxxxx státu xxxxxxxxx x xxxxxxx, xxx xx xxxxx xxxxxxxxx xxxxxxxx xxxxxxxxxxxxxxx xxxxxxxxxxxxxx xxxxxxx xx xxxx xxxxx, aby xxxxxxxxxxx ověřil xxxxxxxx xxxxx x xxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxx xxx, xxx xxxxxx xxxxxxxxx xxxx xxxxxxx x osob xxxx xxxxxxxxx xxxxxxxxx v xxxxx článku. X xxxxxx xxxxxx xxxx xx x xxxxxx xxxxxx xxxxxx xxxxxxx xxxx xxxxxxxxx xxxxxxxxxxxx xxxx xxx, než xxxxxx xxxxxxxxx xxxx xxxxxxxxxxxx lékařům, Armádě Xxxxx republiky x xxxxxxxxxxx xxxxxxxxxxx xxx xxxxxx, k udržování xxxxxxxxxx xxxxx léčivých xxxxxxxxx xxx xxxxx xxxxxxx xxxxxxx, xxxxxxxx xxxxxxxxx x xxx xxxxx zabezpečení xxxxxxxxxxx xxx České xxxxxxxxx xxxxxx xxx xxxxxx xxxxxxxx xx xxxxxxxxx xxxxx §111a xxxxxx x xxxxxxxx x xxxxxxxxxxxxxx zdravotních xxxxxx, xxxxxx jsou xxxxxxxx xxxxxxxxxxxx xxxxxx xxxxxxxxx xxx xxxxx povinného xxxxxxxxxxxx očkování na xxxxxxx xxxxxxx xxxxxxx xxxxxxxxxxxx xx xxxxxxxxx xxxxxxxxxxx xxxx xxx xxxxx xxxxxxxxx&xxxx; xxxxxxxxxx x xxxxxxxxxxx xxxxxxxx x očkování xxxxxxxxxxxxx xxxx&xxxx; xx xxxxxxx xxxxxxx xxxxxxx distributora x Ministerstvem xxxxxxxxxxxxx x nepovinného očkování xxxxxxxxx x xxxxxxxxx xxxxxxxxxxx pojištění x xxxxx xxxxxxxxxxx xxxx xxx xxxxxx č. 48/1997 Sb., x veřejném xxxxxxxxxx xxxxxxxxx a o xxxxx a xxxxxxxx xxxxxxxxx souvisejících zákonů, xx xxxxx pozdějších xxxxxxxx. Xxxxxxx xxxxxxxx xxxxxx xxxxxx xxxxxxxx xx skutečnost, že xxxxxx xxxxxx x XX, kterou xx xxxxx o xxxxxxxx, xxxxxxx xxxxxx možností xxxxxxxxx v článku 23 xxxxxxxxxx.
K bodu 25 (§80 xxxx. 4)
Xxxxxxxxx xxxxxx xxxxxx x xxxxxxxx xxxxxxxx xxxxx úpravu x oblasti požadavků xx xxxxxxxxxxxx xxxxxxx x xxxxxxx xxxxxxxxx xxxx. S xxx xxxx xxxxxxx xxxx xxxx x xxxxxxxxxxx xxxxxxxxxxxx xxxxxx x xxxxxxxx, xxxxxx změn x §80, xxx xxxxxxxxxxxxx veterinárními xxxxxx xxxx xxxxxxxx v xxxx. 4 xxxxxxxxxxx xxxxxxxxx. Tím xxxx xxxxx x situaci, xxx zákon x xxxxxxx xxxxxxxxxxxxx zmiňuje xxxxx xxxxxxxxxxx xxxxxx xxxxxxxxx. Ve xxxxxxxxxxx xxxxxxxx je však xxxxxxxx x odůvodněných xxxxxxxxx x xx xxxxxxxx xxxxxxxxxxx zákonem xxxxxxxxxxxx x xxxxxxxx x další xxxxx xxxxxxxx přípravků, včetně xxxxxxxxx léčivých xxxxxxxxx, x xx v xxxxxxxxx, xxxxx nejsou xxxxxxx xxxxxxxxxxxxxx xxxxxxxxxxxxx xxxxxxxx přípravky. Je xxxxx xxxxxxx tento xxxxxxxx xxxxxxxx, x xxxxx se navrhuje xxxxx, xxxxx je x souladu x xxxxxxxxx použitou x §77 xxxx. 1 xxxx. x) bod 5 (xxxxxx xxxxxxxxxx xxxxx) nebo v §82 (xxxxx xxxxx).
K bodu 26 (§82 xxxx. 2 xxxx. c)
V xxxxx xxxxxxxxxxxx xxxx xx xxxxx o terminologické xxxxxxxxx xxxxxxxxxxx xxxxx, xxx xxxxxxxxx současné xxxxx. V xxxxxxxx xxxx 2009 xx xxxxx xxxxxxxxxx xxxxxxxxxx xxxxx: xx již xxxx krajské hygienické xxxxxxx, xxx přes xxxxxxxxxxx xxxxx, x xx xx základě xxxxxx xxxxxx č. 48/1997 Sb., x xxxxxxxx xxxxxxxxxx xxxxxxxxx x o xxxxx x xxxxxxxx xxxxxxxxx xxxxxxxxxxxxx xxxxxx, x s xxx xxxxxxxxxxx změny xxxxxx č. 258/2000 Sb., x xxxxxxx xxxxxxxxx zdraví a x změně xxxxxxxxx xxxxxxxxxxxxx xxxxxx. Xxxxxxx xxxx změna xxxxxx xxxxxxxxxx do xxxxxx x xxxxxxxx, budou x novele xxxxxx x xxxxxxxx xxxxxxxxxx xxxxxxxxxx §82 odst. 2 xxxx. c) x s ním xxxxxxxxxxx xxxxxxxxxx §77 xxxx. 1 xxxx. x) xxx 5 xxxxxxx.
K bodu 27 (§82 xxxx. 3 písm. x)
Xxxxxxxxxxx xxxxxxxxxxx xxxxxxx x) xx §82 xxxx. 3 xxxxxx xx x xxxxxxxxxx na xxxxxxxx x xxxxxxxxxx xxxxxxx xxxxxxx povinnost xxxxxxxxxxxxx xxxxxxxxxxx k xxxxxx xxxxxxxx xxxxxxxxx xxxxxx xxxxxxxx xxxxx x xxxxxxx xxxxxxxx xxxxxxxxxxx identifikátoru x xxxxx vydávaných léčivých xxxxxxxxx. Jedná xx x xxxxxxxxxxxx xxxxxx xxxxxx, xxx mohou xxxxxxx xxxxxxx xxxxxx xxxxxxxxx xx žádanky xx zdravotnických xxxxxxxx. X xxxxxxxxx státech Xxxxxxxx xxxx xx xxx xxxxx xxxxxx xxxxxxxx xx xxxxxxxxxx xxxxxxxx xxxxxxxxx. Z xxxxxx důvodu xx xxxx xxxxxx xxxxxxxxx xxxxxxxx na xxxxxxx xxxxxxx xxxxxx x xxxxxxx, xxxxx xx xx xxxxxx xx xxxxxx xxxxxxxxxxxxx zdravotních xxxxxx osobou xxxxxxxxxx x xxxxxx x xxx xxxxx ochranné xxxxx xxx xxxxxx xxxxx nařízení. X xxxxxxx xxxxxxxxxxx xxxx xxxxxx xxxxxx xx xxxxxxxxx x tomu, xx xxxxxx xxxxxxxxx xxxxxx na xxxxxxx xx zůstaly xxxxxxxxx, xxxxxxx poskytovatelé xxxxxxxxxxx xxxxxx nejsou osobami xxxxxxxxxxx x xxxxxx, x tak se xx xx xxxxxxxx xxx xxxxxxxxxx. Xxxxxxxx xxxx xxxxxxxxxx zákona xxxxxx xxxxxxxx xxxxxxxxx xxxxxx xxxxxxx léčivé xxxxxxxxx opatřené xxxxxxxxxx xxxxx x x xxxxxxxxx, xxx nepůjde x registrované xxxxxx xxxxxxxxx x XX, xxx dovážené v xxxxx xxxxxxxxxxxx xxxxxxxxx xxxxxxxx, tzv. „xxxxxxxxxxxxxx xxxxxx“ xxx §8 xxxx. 3 zákona x xxxxxxxx.
K bodu 28 (§99 xxxx. 7 a 8):
X xxxxxxxxxxx xxxxxxxx 7 xx §99 xxxxxx se upravuje xxxxx Xxxxxx a xxxxxxxx, ve xxxxxx xx soustřeďují informace x ochranných xxxxxxx. Xx xxxxx straně xxx x xxxxxxxxxxx xxxxxxxxx xxxxxxxx Ústavem, xxxxx vyplývají x xxxx xxxxxxxxxx x xxxx potřebné pro xxxxxxxxx tohoto xxxxxxxx. Xxxxxxxxx xxx o xxxxxxxxx xxxxxxxx se xxxxxxx x xxxxxxxx xxxxxxxx provozovatelů xxxxxxxxxxx x xxxxxx xxxxxxxx xxxxxxxxx, xxxxx tomuto xxxxxx sdělují xxxxxxxxx xxxxxxx xxxxx. Xx xxxxx xxxxxx Xxxxx xxxxxxx informace x xxxxxx úložiště a xx k xxx xxxxxxx na xxxxxxx xxxxxxxx x xxxxxxxxxx xxxxxxx x xxxxxxxxxxxx xxxxxxxxxx §13 xxxx. 2 písm. o) xxxxxx. Xxxxx xxx x tyto xxxxxxxxx, x xxxxxxxxxx §99 xxxx. 7 xx xxxxxxxxx xxxxxxxx xxxxxxx xxxxxx xxxxxxxxx, když xx xxxxxxxx xxxxxxx, xx tyto xxxxxxxxx xxxx Xxxxx xxxxxxxx xxxxxxxxxx xxxxxx osobám. Xxxx xxxxx xxxxxxxxxx xxxxxxx na základě xxxxxx xxxxxxxx xxxxxxxx.
K bodu 29 (§100 xxxx. 8):
Xxxxx x léčivech xxxxxxx xxxxxxxxxxx povinnost v xxxxxxx sdílení xxx xxxx Xxxxxxxxx xxxxxxx xxxxxxxxx x Xxxxxxx xxx státní xxxxxxxx xxxxxxxxxxxxx xxxxxxxxxxxx x xxxxx (xxxx xxx „Xxxxxxxxxxx xxxxx“). Xxxxxx xxxxxxxxxx xxxxxx je xxxxxxxx plný xxxxxx xx xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Xxxx 2001/82/ES xx xxx 6. xxxxxxxxx 2001 x xxxxxx Společenství xxxxxxxxx xx xxxxxxxxxxxxx xxxxxxxx přípravků na xxxxxx zákona xxxxxxxx Xxxxxxxxxxxxx xxxxxx povinnost xxxxxxxxxx xxxx do xxxxxxxxxx databází.
K bodu 30 (§100x)
Xxxxxxx x xxxxxxxxxx xxxxxxxxxxxx x xxxxxx o xxxxxxxx, xxx xx x xxxxxx zvýšení xxxxxx jistoty na xxxxx pojmu „padělek“ xxxxxxx xxxxx „xxxxxxxx xxxxxx xxxxxxxxx“.
K bodu 31 a 32 (§103 xxxx. 6 písmena x), h) až x)):
X xxxxx novelizačním xxxx se doplňují x §103 xxxx. 6 písm. x) xx j) xxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx, xxxxxxx xx xxxxxxx xxxxxxxxxxxx, x to xxxxxxxxx xxxxxx xxxxxxx, xxxxx xxxx x xxxxxxx s xxxxxxxxx x xxxxxxxxxx xxxxxxx xxxx xx zákonem x léčivech.
K bodu 33 (§103 xxxx. 15 xx 21):
X xxxxx novelizačním xxxx xx doplňují xxxxxxxx xxxxxxxx xxxxxxxxx, xxxxxxx se xxxxxxx xxxxxxx xxxxxxxx xxxxxxxxx, xxxxxxxxxxx, xxxxxxxxxxxx xxxxxxxxxxx xxxxxx xxxxxxxxx k xxxxxx léčivých xxxxxxxxx, xxxxxxx xxxxxxxxxx x xxxxxxxxxx, xxxxx zřizující x xxxxxxxxxx xxxxxxxx x osoba xxxxxxxxx xx xxxxxxx léčivých xxxxxxxxx xx trh. Xxxxxxxx podstaty přestupků xxxxxxxxx v xxxxxxxxx, xxxxx xxxx x xxxxxxx s xxxxxxxxx x xxxxxxxxxx xxxxxxx xxxx se xxxxxxx x xxxxxxxx.
Xxx xxxxxxx xxxxxxxxxx xxxxx výrobci, xxxxxxxxxxxx a xxxxx xxxxxxxxx nebo xxxxxxxx xxxxxxx xxxxxx xxxxxxxxx xxxxxxxxxx xxxxx xxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx x xxxxxxxxxxxx xxxxxxxxxx x xxxxxxx xxxxxxxxxx x xxxxxx. Xxx xxxxxxx xxxxxxxx xxxxxxxxxxx identifikátoru xx porovná xxxxxxxxx xxxxxxxxxxxxx x xxxxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxx v xxxxxxx xxxxxxx; jedinečný xxxxxxxxxxxxx se považuje xx xxxxx, xxxxx xxxxxx xxxxxxx obsahuje xxxxxxx xxxxxxxxx xxxxxxxxxxxxx x kódem xxxxxxxxx x sériovým xxxxxx, xxxxx se xxxxxxx x kódem x xxxxxx ověřovaného xxxxxxxxxxx xxxxxxxxxxxxxx. Neporušenost xxxxxxxxxx x xxxxxxx xxxxxxxxxx x xxxxxx se xxxxx xxxxxxxx xxxxxxxxx xxxxxx xxxxxxxx přípravku.
Výrobci, xxxxxxxxxxxx a xxxxx xxxxxxxxx xxxx xxxxxxxx xxxxxxx xxxxxx xxxxxxxxx xxxxxxxxxx xxxx přijmout xxxxxxxxx xxxxxxxx xxxxxxxxx x článcích 18, 24 x 30 xxxxxxxx x ochranných xxxxxxx, xxxxx xxxx xxxxx xx xxxxxxxx, xx x xxxxxx xxxxxxxxx xxxx xxxxxxxxxxxx (xxxxxxxx xx xxxxxx, že xxx porušen xxxxxxxxxx x xxxxxxx xxxxxxxxxx x xxxxxx), nebo xxxxx xxxxxxx ochranných xxxxx xxxxxxxx xxxxxxxxx (xxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx x systému xxxxxxx) xxxxxxxxx, že xxxxxxxxx xxxxx xxxx pravý.
K novelizačnímu bodu 34 (§104 odst. 14)
Xxxxxxx xxxxxxxxxx se xxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxxxxx v xxx, xx xxxxxxx xxxxxxxxx xxxxxxxxxxx léčivých xxxxxxxxx xxxxxxxx požadavky xxxxxxx xxxxxxx xxxxx xxxx xxxxx xxxxxxxxxxx xxxxxxxxx Xxxxxxxx xxxx - xxxxxxxxxxx nařízení 2017/1569.
Xxxxxxx xx xxxx xxxxxxxx xxxxxxxx xxxxxxxxx kvalifikováno xxxxxxx xxxxxxxxxxx v xxx, že xxxxxxxxxxxx xxxxx xxx xxxxxxxx xxxxxxxxx xxxxx xxxxx xxxxxxxxxxxx xxxxxxxx Xxxxxxxx xxxx - prováděcího xxxxxxxx 2017/1569 xxxxxxxx xxxxx xxxxxxxxx xxxxxxxxx x čl. 20 bod 2 xxxxxx prováděcího xxxxxxxx.
K bodu 35 (§105 odst. 2 xxxx. t):
Jedná xx x xxxxxxxxxxxx xxxxxxxxxx xxxxxx.
K bodu 36 (§105 xxxx. 4 xxxx. x):
Xxxxx xxxxxxxxxxx xxx xxxxxxx na xxxxxxxx xxxx povinnosti xxxxxxxx xxxxxxxx xxxxxxxxxx xxxxxx xxxxxxxx xxxxxxxxx, xxxx xxxxxxxx xxxx xxxx xxxxxxxxxx xx xxxxxxxx xx xxxxxxxxx (xxx xxxxx o odpovědnosti xx xxxxxxxxx x xxxxxxx zákon s xxx související).
K bodu 37 (§105 xxxx.10)
Xxxxxxxx se xxxxxxxx xxxxxxxx přestupku spočívající x tom, xx xxxxxxxxxxxx xxxxxxx při xxxxxxxx xxxxxxxxx podle xxxxx xxxxxxxxxxxx xxxxxxxx Xxxxxxxx unie - xxxxxxxxxxx xxxxxxxx 2017/556 xxxxxxxx xxxxx xxxxxxxxx xxxxxxxxx x čl. 10 xxxx 2, 3,4 x 5 xxxxxx xxxxxxxxxxx nařízení.
K bodu 38 a 39 (§106 xxxx. 1 písm. x):
X xxxxx novelizačním xxxx xx xxxxxxxx xx xxxxxxxxx xxxxxx xxxxxxx xxxxxxxxxxx fyzické xxxxx xxxx xxxxxxxxxxxxx xxxxx xxxxxxx léčivých xxxxxxxxx, xxxxx xxxxxxx x tom, xx xxxx xxxxx xxxxxxxxx, xxx obal xxxxxxxx xxxxxxxxx xxx xxxxxxx xxxxxxxxxx prvky xxxxx §37 xxxx. 7 xxxxxx.
Xxxx xx doplňuje xxxxxxxx xxxxxxxx xxxxxxxxxxx x nedodržení článku 12 xxxxxxxx 2017/1569 xxxxxxxxxxx xxxxxxxx osobou xxxx xxxxxxxxxxxxxx xxxxxx. Xxxxxxx xx tomu xxxx x §108 odst. 3 pokud se xxxxxxxx xxxxxxx xxxxxxxxx xxxxxxx xxxxx xxxx xxxxxxxxxxxxx xxxxx.
Xxxxxx jsou xxxxxxxxx přiměřeně xxxxxxx x xxxxxxxxxxx xxxxxx, xxxxx by takové xxxxxxx xxxxx xxxxxxxx x xxxxxxx xxxxxxxxx xxxxxx x x xxxxxxx xxxxxxxxx xxxxxxxx xxxxx x Xxxxx xxxxxxxxx, ale x x xxxxxx xxxxxxx Xxxxxxxx xxxx. Zároveň xx xxxxxxxxxxxx xxxx xxxxxx stanovených xx xxxxxxxx obdobných povinností xxxxxxxxxxx xxxxxxxxx právní xxxxxxx. Ustanovení xx xxxxxxxx postupně tak (xxxxxx xxxxxxxxx xxxxxxxxx) xxx xxxxxxxxxx x xxxxxxx xxxxxxxxxx xxxxxxx č. 66/2017 Sb.
K bodům 40 xx 46 (§107 xxxx. 1 xxxx. x) xx x):
Xxxxxxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxxx protiprávní xxxxxxx (xxxxxxxxx) xxx xxxxxxxxxx xxxxxxxxxxx maximální výši xxxxx xxxxxx xx xxxxxxxx xxxxxxxx xxxxxxxxxx. Xxxxxxxxx výše xxxxxx xxxxxxxx xxxxxx xxxxxxxxxx xxxxxxxxx, xx. je xxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxx xxxxxx normou xxxxxxxx xxxxxxx (chráněné xxxxxxxxxxx xxxxx).
K bodu 47 (§108 xxxx. 3):
V tomto xxxxxxxxxxxx xxxx xx xxxxxxxx xx xxxxxxxxx xxxxxx jednání xxxxxxx xxxxx xxxx xxxxxxxxxxxxx xxxxx xxxxxxx xxxxxxxx xxxxxxxxx, xxxxx xxxxxxx x tom, že xxxx xxxxx nezajistí, xxx obal xxxxxxxx xxxxxxxxx byl xxxxxxx xxxxxxxxxx xxxxx podle §37 odst. 7 xxxxxx.
K bodu 48 (§108 odst. 3):
Xxxxxxxxxx se xxxxxxxx x xxxxx xx čl. 62 nařízení x xxxxxxxxx xxxxxxxxx xxxxxxxxxxx x povinnosti, xxx xxxxx xxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxx x Xxxx nebo xxxxxxxxxx xx Unie xxxx x xxxxxxx x xxxxxxxxx xxxxxxxxxxx x čl. 63 xxxxxxxx x xxxxxxxxx hodnocení, xxxxxxx musí xxx xxxxxxxxx, že xxxx xxxx požadavky splněny.
K bodu 49 (§114 xxxx. 1):
Xxxxx xx o xxxxxxxxxxxx xxxxxxxxxx xxxxxx x xxxxxxxxxx xx změny x ustanovení §82 xxxx. 2.
ČÁST DRUHÁ Změna xxxxxx o xxxxxxxxxxx xxxxxxxx (§65 odst. 2)
Xxxxx novelizačním bodem xx dokončena xxxxx xxxxxxxx článku 10 xxxx. 8 nařízení x. 2017/556, xxxxx xxxxxxx xxxxxxxx xxxxxx povinnost xxxxxxxx xxxxxx právní x xxxxxxx rámec, xxx xxxxxxxxxx x xxxxxxxxx členských států xxxx mj. xxxxxxx x xx xxxxxxxxxxxx xxxxxxxxxxx, xxxxx xx xxxxxxxxxx x xxxxxxxxx xxxxxxxxxx.
K Čl. III - Xxxxxxx xx Xxxxxx xxxxxx
Xxxxxxxx xx xxxxxxxxxx xxxxxxxxxxx, xxx xxxxxxx Xxxxxxxxxxxx xxxxxxxxxxxxx formou xxxxxxx xx Sbírce zákonů xxxxxx den, kdy xxxx xxxxxxxxxx oznámení Xxxxxx x Úředním xxxxxxxx Xxxxxxxx xxxx xxxxx čl. 82 xxxx. 3 nařízení Xxxxxxxxxx xxxxxxxxxx x Rady (XX) x. 536/2014 xx xxx 16. xxxxx 2014 o xxxxxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxxxx přípravků a x zrušení xxxxxxxx 2001/20/ES.
K čl. IV. - Xxxxxxxx
X xxxxxxx na fakt, xx xxxxx xxxxxxxx xxx xxxxxxxxxxxx nařízení x xxxxxxxxxx xxxxxxx, xxxxx xxxxxxx x xxxxxxxx xx 9.2.2019 xx pro xxxxxxxxxx xxxxxxxx xx xxxx xxxxxxxx xxxxxxxxx xxxxx xxxxxxxxx právě tímto xxxx.
X dalším se xxxxxxxx u konkrétních xxxxxxxxxx xxxxxxx xxxxxxxx xxxxxx, jako xxxx xxxx x článkem XXX xxxx. x) xxxxxx č. 70/2013 Sb. x xxxxxxxxxx §37 odst. 7 x 8, §64a x §66 xxxx. 1 xxxx. x) zákona x xxxxxxxx x xxxxxxxxxx xxxxxxx. Xxxxx xxxx xxx tak, xx xx xxxxx xxxxx xxxxxxxxx uplynutím 3 xxx xxx xxx xxxxxxxxx aktů vydaných Xxxxxxxxx xxxxxx x xxxxxxxxx xxxxxxxxx, xx xxx 9.2.2019 xxxxx xxxxxx X bodu 12 xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Xxxx 2011/62/XX xx xxx 8. června 2011, xxxxxx xx mění xxxxxxxx 2001/83/ES x xxxxxx Xxxxxxxxxxxx xxxxxxxxx xx xxxxxxxxx léčivých xxxxxxxxx, xxxxx xxx x xxxxxxxxx vstupu xxxxxxxxxx xxxxxxxx xxxxxxxxx xx legálního xxxxxxxxxxxxxx xxxxxxx, xxxxxxx xxx xxxx dny, kdy xxxx tyto xxxx xxxxxxxxx, xxxxxx Xxxxxxxxxxxx xxxxxxxxxxxxx xxxxxx sdělení xx Sbírce xxxxxx.
V Xxxxx xxx 22. xxxxx 2018
Xxxxxxxx xxxxx:
Xxx. Xxxxxx Babiš x. x.
Xxxxxxx xxxxxxxxxxxxx:
Xxx. xx Mgr. Adam Xxxxxxx x. x.
Xxxxxxxxx xxxxxx x xxxxxxxxx xxxxxx regulace xxxxx xxxxxxxx zásad - XXX&xxxx;
XXXXXXX ZÁVĚREČNÉ XXXXXX XXX
|
1. Název xxxxxx xxxxxx: |
|
|
Xxxxx xxxxxx, xxxxxx xx mění xxxxx č. 378/2007 Sb., x xxxxxxxx x x xxxxxxx xxxxxxxxx xxxxxxxxxxxxx xxxxxx (xxxxx o xxxxxxxx), xx xxxxx xxxxxxxxxx předpisů x xxxxx č. 372/2011, x xxxxxxxxxxx xxxxxxxx x xxxxxxxxxx jejich poskytování (xxxxx x xxxxxxxxxxx xxxxxxxx) |
|
|
Xxxxxxxxxxx / xxxxxxxx xxxxxxxxxxxxx: Xxxxxxxxxxxx zdravotnictví |
Předpokládaný xxxxxx xxxxxx xxxxxxxxx, x xxxxxxx xxxxxx xxxxxxxxx rozveďte 9. xxxxx 2019 |
|
Xxxxxxxxxxxx xxxxx XX: XXX - xxxxxx xxxxxx xxxxxxxxx xxx xxxxxxxxxxxx: 9. xxxxx 2019 - xxxxxx, xxx xxx návrh xxx xxxxx požadavků stanovených xxxxxxxxx EU: XX |
|
|
2. Xxx xxxxxx xxxxxx |
|
|
Xxxxxxxxxxx xxxxxx xxxxxx x xxxxxxxx a xxxxxx x xxxxxxxxxxx xxxxxxxx xxxxxxxxxxxx xxxxxx normy Xxxxxxxx xxxx xx xxxxxxxx xxxx České xxxxxxxxx.&xxxx; Xxxxx xx x následující xxxxxx xxxxxxxx: - Xxxxxxxx Xxxxxx x xxxxxxxxx xxxxxxxxx (XX) 2016/161 xx xxx 2. října 2015, kterým xx xxxxxxxx xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Xxxx 2001/83/XX, stanovením podrobných xxxxxxxx xxx xxxxxxxx xxxxx xxxxxxx xx xxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx, - Xxxxxxxxx nařízení Xxxxxx v xxxxxxxxx xxxxxxxxxx (EU) č. 2017/556 xx xxx 24. xxxxxx 2017 x xxxxxxxxxx pravidlech pro xxxxxxxxx xxxxxxxxxxx xxxxxxx xxxxxxx klinické praxe xxxxx xxxxxxxx Xxxxxxxxxx xxxxxxxxxx a Xxxx (XX) x. 536/2014 (xxxx jen „xxxxxxxx 2017/556“), - Xxxxxxxx Xxxxxx x xxxxxxxxx xxxxxxxxxx (XX) č. 2017/1569 ze xxx 23. května 2017, kterým xx xxxxxxxx xxxxxxxx Evropského xxxxxxxxxx a Xxxx (XX) x.536/2014 xxxxxxxxxx xxxxx x pokynů xxx xxxxxxxx xxxxxxx xxxxx pro hodnocené xxxxxxx xxxxxx xxxxxxxxx x xxxxxxxx xxxxxxxxx xxxxxxxx (xxxx jen xxxxxxxx 2017/1569“), - Xxxxxxxx Xxxxxx (XX) 2017/1572 xx dne 15. xxxx 2017, kterou xx xxxxxxxx xxxxxxxx Xxxxxxxxxx parlamentu x Xxxx 2001/83/XX, xxxxx xxx x xxxxxx x xxxxxx pro xxxxxxxx xxxxxxx xxxxx xxx xxxxxxx xxxxxx xxxxxxxxx (xxxx xxx „xxxxxxxx 2017/1572“). Xxxxxxx xxxxxxxx, xxx xxxxxxx xxxxxxxxxx xxxxxxxxxxxx xxx jednotlivé xxxxxxx xxxxx z xxxxxxxx Xxxxxxxx xxxx, xx xxxxxxxxxxxx xxxxxxxxx xxxxx xxxxx EU xx xxxxxxxxxxxxxx právního xxxx. Xxx xxxxxxxxx xxxxxxxx xx xxxxx x porušení xxxxxxx x založení Xxxxxxxx xxxx xx xxxxxx xxxxxxxxx xxxxx x xxxxx by xxx xxxxxxxx řízení xx xxxxxx Xxxxxxxx xxxxxx xxxxx České xxxxxxxxx xx xxxxxxxxx xxxxxxxxxxxxx xxxxxxxxxx a popřípadě x xxxxxxx xxxxxx xxxxxxxxx xxxxxxxx xxxxxxxx, xxxxx by xxxx xxxxx xx xxxx xxxxxx x xxxx xxxxxxxxx xxxxxx pouze x xxxxxxx Xxxxx xxxxxxxxx, ale x xxxxxxxxx členských xxxxx, xxxxx xxx x xxxxxxx, že pravidla xxxxx xxxxxxxxxx xxxxx, xxxx xxxxxx funkční. Vzhledem xx xxxxxxxxxxx, že x xxxxxxxxxxxx xxxxxxxxxxxxxxxx xxxxx Evropské xxxx xxxxxxxx xx oblasti xxxxxxxxx inspekčních xxxxxxx xxxxxxx klinické xxxxx, xxxxxxx výrobní xxxxx xxx hodnocené humánní xxxxxx xxxxxxxxx a xxxxxxxx provádění xxxxxxxx x xxxxx x xxxxxx xxx xxxxxxxx xxxxxxx xxxxx xxx xxxxxxx xxxxxx xxxxxxxxx xxxxxx dána xxxxxxx xxxxxxxx x současně xxxxx xxxxx novely xx vymezených xxxxxxxxx xxxxx nad rámec xxxxxxxxx práva Evropské xxxx, byla v xxxxxxx x Xxxxxxxxxxxxxx xxxxxxxx xxxxx xxxxxx xxxxxxxxxxxxxx žádost x xxxxxxx xxxxxxx z xxxxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxx z hodnocení xxxxxx xxxxxxxx podle xxxxxxxx zásad - XXX xxx xxxx xxxxxxxx xxxxxxx. Xxxxxxx xxxx vyhověno. X xxxxxx xxxxxx xx xxxxx materiál xxxx xxxxxx pouze hodnocením xxxxxx adaptace xxxxxxxx x xxxxxxxxxx prvcích. Cílem xxxxxx xxxxxx xx xxxxxxx nezbytných xxxxxxxx xxxxxxxxxxxxx x adaptací xxxxxxxx řádu Xxxxx xxxxxxxxx xx xxxxxxxx Xxxxxx x xxxxxxxxx xxxxxxxxx (EU) 2016/161 xx xxx 2. xxxxx 2015, xxxxxx xx doplňuje xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Xxxx 2001/83/XX xxxxxxxxxx xxxxxxxxxx xxxxxxxx xxx xxxxxxxx prvky xxxxxxx xx xxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx (xxxx xxx „xxxxxxxx x xxxxxxxxxx xxxxxxx“). Xxxxxxxxxxxx xxxxxxxxxx prvků xx xxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxx již xx Xxxxxxxx Evropského xxxxxxxxxx x Rady 2011/62/EU, xxxxxx se xxxx xxxxxxxx 2001/83/ES x kodexu Xxxxxxxxxxxx xxxxxxxxx xx xxxxxxxxx xxxxxxxx xxxxxxxxx, pokud xxx x xxxxxxxxx xxxxxx xxxxxxxxxx léčivých xxxxxxxxx do xxxxxxxxx xxxxxxxxxxxxxx řetězce (xxxx xxx „xxxxxxxx 2011/62/XX“). Xxxxxxxx xxxxxx xxxxxxxxx, které xx xx k xxxxxxxxx dostaly prostřednictvím xxxxxxxxx xxxxxxxxxxxxxx xxxxxxx, xxxxxxxxxxx riziko xxx xxxxxx zdraví x xxxxx xxxxxx xxxx xx xxxxxxx xxxxxx xxxxxxxx v xxxxxxx xxxxxxxxxxxx řetězec, poskytovatele xxxxxxxxx péče x xxxxxxxxx xxxxxx. Xxxxx xxxxxxxx 2011/62/EU xxxxxxxxx xxxxxx xxxxxxxxxx prvků xx obalech léčivých xxxxxxxxx, xxxxx xx xxxxxxx jednak xxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx, xxxxxxxxxxxx xxxxxxxxxxxx xxxxxx xxxxxxxx xxxxxxxxx a xxxxxxx, xxx xxxxxx x obalem manipulováno. Xxxx xxxxxx xxxxxxxxxxxx xxxxxxxx by měly xxxxxxxx xxxxxxxxxxx xxxxxxx xxxxx xxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx do xxxxxxxxx dodavatelského xxxxxxx x xxxxx xxxxxxx xxxxxxxx x xxxxx xxxxxxxx xxxxxxxxxx o xxxxxxxxxx x xxxxxxx. Xxx xxxxxx ověřování xxxxx xxx xxxxxxxxxx xx xxxxx xxxxxxxxx xxxxxxx Xxxxxxxx unie, xxxxxxxxxx xxxx xxxxxxxx xxxxxxxxx x xxxxxxxxxx xxxxx xxxxxxx xxxxx účastníků xxxxxxxxxxxxxx xxxxxxx xxxxxxxxx xxxxxxxxxxxx národních odlišností, xxxxxxxxx Evropská Xxxxxx xxxxxxxxxxxxxxx xxxxxxxx x xxxxxxxxxx prvcích xxxxxxxx xxxxxxxx xxx zavedení xxxxxxxxxx xxxxx, xxxxxxx xxxxxxxxxxxxxxx x xxxxxxxxx xxxxxxxxxxx jednoho x xxxxxxxxxx xxxxx - xxxxxxxxxxx xxxxxxxxxxxxxx, xxxxxxx x xxxxxx xxxxxxx xxxxxxxxxx xxxxx xxxxxxxxxxxx xxxxxxxxx xxxxxxxx (xxxxxxx, xxxxxxxxxxxx, xxxxxxx oprávněnými xxxx zmocněnými xxxxxxx xxxxxx přípravky xxxxxxxxxx) x xxxxxxx a xxxxxx systému xxxxxxx xxxxxxxxxx xxxxxxxxx o xxxxxxxxxx xxxxxxx (xxxxxxxxxxx xxxxxxxxxxxxxxxx). Xxxxxxxx prvky xxxxx xxx prvky xxxxxxxx xx xxxxx humánního xxxxxxxx xxxxxxxxx - xxxxxxxxx xxxxxxxxxxxxx (jedinečná xxxxxxxx xxxxxx dvourozměrným xxxxxxx xxxxx, xxxxxxxxxx xxxxxxx pravosti a xxxxxxxxxxxx xxxxxxxxxxxx xxxxxx xxxxxxxx xxxxxxxxx, na xxxx xx xxxxxxxxx) x prostředek x xxxxxxx xxxxxxxxxx x xxxxxx (xxxxxxxx xxxxx - xxxxxxxxxxxx pojistka - umožňující xxxxxx, xxx xxxx x xxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxxxx). Xxxxxxxxxx xxxxx xxxxx xxxxxxxx x xxxxxxx x xxxxxxxxx x xxxxxxxxxx xxxxxxx xxxxx xxxxxxxxx léčivých xxxxxxxxx x) xxxxxxx výdej je xxxxx xx xxxxxxxx xxxxxxx (xxxxxxxx xxxx xxxxxx xxxxxxxxx xxxxxxx xx xxxxxxx x xxxxxxx X nařízení x xxxxxxxxxx prvcích) b) xxxxxxx xxxxx xxxx xxxxx na xxxxxxxx xxxxxxx (xxx. „volně xxxxxxxx xxxxxx xxxxxxxxx“), x xx xxxxx xxxxx jsou xxxxxxx xx xxxxxxx v xxxxxxx XX xxxxxxxx x xxxxxxxxxx prvcích, c) xx xxxxx členské xxxxx xxxxxxxxx xxxxxx xxxxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx xxxx xxxxxxxxxx k xxxxxxx manipulace x xxxxxx. Xxxxxxx xxxxxxxxx systém xxxxxxxx xxxxxxx xxxxxxx xxxxxxx, xx kterých xxxxx mimo xxxx xxxxxxxx xxxxxxxxx o xxxxxxxxxxx identifikátorech xxxxxxxxxxxx xxxxxx xxxxxxxx přípravků. Xxxxxx xxxxxxx zřídí x xxxxxxxx xxxxxxxxx xxxxxx subjekt xxxx xxxxxxxxx právní xxxxxxxx xxxxxxx x Unii xxxxxxx x xxxxxxxx xxxxxxxxxx x xxxxxxxxxx xxxxxxxx přípravků xxxxxxxxxx xxxxxxxxxx xxxxx. Xxxxxxx xxxxxxx úložišť má xxxxxx xxxxxxx případně xxxxxx xxxxxxxx konzultovat xxxxxxx x xxxxxxxxxxxx, xxxxxxx xxxxxxxxxxx xxxx xxxxxxxxxx xxxxxxx xxxxxx xxxxxxxxx veřejnosti a x dotčenými příslušnými xxxxxxxxxxxxxx xxxxxx. Náklady xx xxxxxx xxxxxxx xxxxx xxxxxxx léčivých xxxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxx v souladu x xxxxxxx 54x xxxx. 2 písm. x) xxxxxxxx 2001/83/XX. Xxxxxx úložišť se xxxxxx z centrálního xxxxxxxx x xxxxxxxx, xxxxx slouží xxxxx xxxxxxx xxxxxxxxx xxxxx („xxxxxxxxxxxx úložiště“), xxxx xxxxxx více xxxxxxxxx xxxxx („xxxxxxxxxx xxxxxxxx“), xxxxx xxxx xxx xxxxxxxxx k xxxxxxxxxxx xxxxxxxx. Xxxxxxx xxxx xxxxxxxxx xxxxxxx balení xxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxx x ověřit, xx jedinečný identifikátor xx čitelný a xxxxxxxx xxxxxxxxx dané xxxxxxxxx x xxxxxxxxxx xxxxxxx. Držitelé xxxxxxxxxx x xxxxxxxxxx xxxx xxxxxxxxx xxxxx x xxxxxxx xxxxxxxx xxxxxxxxxx xxxx xxxxxxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxx zajistit, xxx xxxxxxxxx x xxxxxxxxxxx identifikátorech xxxx xx systému xxxxxxx xxxxxxx xxxx tím, xxx xxxx léčivý xxxxxxxxx xxxxxx xx xxx. Xxxxxxx xxxxxxxxxx xxxxx v systému xxxxxxx xxxxx xxxxxxxx xxxxx xxxxxxx xxxx xxxxxxxxxxxx x osoby xxxxxxxxx nebo xxxxxxxx xxxxxxx xxxxxx xxxxxxxxx. Xxxxxxx, xxxxx xxxxxxx xxxxxxxx xxxxxxxxx xxxxxxx xxxxxxxxxx xxxxx, xxxxxxxx xxxxxxxx jedinečného xxxxxxxxxxxxxx, xx systému xxxxxxx xxxx dány xxxxxxxxx x xxxxxxxxxx xxxxxxx. Xxxxx oprávněná x xxxxxx léčivých přípravků xxx xxxx xxxxxxx xxxxxxxxxx xxxxx xxx xxxxxxxx prvky x xxxxxxx xxxxxxxx jedinečného xxxxxxxxxxxxxx xx systému xxxxxxx v xxxxxxxx xxxxxx xxxxxxxxxx. Xxx xxxxxxxxx xxxxxxxx xxxxxxxx přípravku x xxxxxxxx ověřovacím xxxxxxx je xxxxxxxx xxxxxx oba ochranné xxxxx. Xxxxxxx pravosti xxxxxxxxxxx xxxxxxxxxxxxxx na xxxxx léčivého xxxxxxxxx xx xxxxxxx jeho xxxxxxxxxx x identifikátory xxxxxxxxx v systému xxxxxxx x xxxx xxxxx xx zajistit, xx xxxxxx xxxxxxxxx xxxxxxx xx xxxxxxxxxxx xxxxxxx, xxxxx jedinečné xxxxxxxxxxxxxx xxxxxx xx xxxxxxx úložišť. Xxxxxxx xxxxxxxxxxxxx xxxxxxxxxx x xxxxxxx xxxxxxxxxx x xxxxxx xxxx xxxxxxxxx xxxxxxxx kontrolou xxxxxx xxxxxxxx xxxxxxxxx x xxxx xxxxx je xxxxxxxx, xx x xxxxxxx xxxxxx xxxxxxxx xxxxxxxxx nemanipuloval nikdo xxxx před pacientem, xxxxxxx xxxx xxxxxx xxxxxxxx xxxxxxxxx vydáno. Nařízení x xxxxxxxxxx xxxxxxx xx xxx xxxxxxx xxxxx xxxxxxx x xxxxx xxxxxxx x xx ve xxxxx xxxxxxxxx státech xxxxx xxxxxxxxxx. Ačkoliv xxxxxxxx x xxxxxxxxxx xxxxxxx xxxxxxxx xxxxxxxxxxxx xxxxxxxxxx xxxxx xxxxxx xxxxxxxxx, xxxxxxx dílčí xxxxxx xxxxxxxxx xx zvážení x rozhodnutí xxxxxxxxx xxxxx, x to xxxxxxxxx (1) určení xxxxxxxxxxx vnitrostátního orgánu, xxxxx by xxx xxx přístup x xxxxxxxx xxx xxxxx xxxxxx xxx xxxxxxxxxx xxxxxxx, vyšetřování xxxxxxxxxxxxx xxxxxxx xxxxxxxx, xxxxxx, xxxxxxxxxxxxxxxx x xxxxxxxxxxxxxxxxxxxx, (2) xxxxxxxx xxxxxxx, xxx xxxxxxxx, xxx xxxxxxxxxx, xxxxx xxxxxxxx x ochranných xxxxxxx xxxxxx xxxxxxxxxxx subjektům, xxxx xxxxxx, a xx xxxxxxxxx xxxxxxxx xxxxxxxx přestupků x xxxx oblasti a xxxxxxxx určením správního xxxxxx příslušného x xxxxxx xxxxxxxxxxxx x xxxxxxxxxx xxxx xxxxxx xx xxxxxxxx povinností xxxxxxxxxxxx subjekty, (3) xxxxxxxxxx xxx, členský xxxx xxxxxxx xxxxxx xxxxxxxxxx xxxxxxxxxx prvků xx léčivé přípravky, xxxxx dle xxxxxxxx x xxxxxxxxxx xxxxxxx xxxxxx xxxxxxxxx xxx xxxxxxxx xxxxxx xxxxx, (4) xxxxxxxxxx, xxx xxxxxxxxxxxx úhradové xxxxx“ xxxx „xxxx úhradové xxxxx“ xxxx xxxxxxx x xxxxx jedinečného xxxxxxxxxxxxxx xx xxxxxxx, (5) xxxxxxxxxx xxxxxxxx xxxxxxxxxxxxxxx xxxxxxxxxxxxxx řetězce xx území xxxxxxxxx xxxxx a xxxxxxxx x právní xxxxxx, xxx xxxxxxxxxxx xxxx xxxxxx ochranné xxxxx x provést xxxxxxxx xxxxxxxxxxx identifikátoru xxxxxxxx xxxxxxxxx ze xxxxxxx xxxxxxx před xxx, xxx xxxxxx xxxxxxxxx xxxx xxxxxxx x xxxx xxxx institucí xxxxxxxxx x článku 23 xxxxxxxx o xxxxxxxxxx xxxxxxx. Xxxx xxxxxxx úpravy xx možné xxxxxxx xxxxx x xxxxxx xxxxxx xxxxxx x xxxxxxxx xxx, aby xxxxxxxxxxxxxx x již xxxxxxxxxx xxxxxxxx xxxxxxx xxxxxxxxxxxx ochranných xxxxx xxxxxxxxxxx xxxxxxxx 2011/62/EU, xxxxx byla transponována xx xxxxxx x xxxxxxxx novelou č. 70/2013 Sb. Xxxxxxxxxxx úpravou xxxx xxxxxxx xxxxxxxx xxxxxxxx xxxxxxxx nařízení x xxxxxxxxxx prvcích tak, xxx xxxxx být xxxx xxxxxxxxxx řádně x xxxx zbytku xxxxxxxxxx x xxxxxxxxxx Xxxxx republiky. |
|
|
3. Agregované xxxxxx xxxxxx zákona |
|
|
3.1 Dopady na xxxxxx xxxxxxxx a xxxxxxx xxxxxxx xxxxxxxx: XX |
|
|
Xxxxxxxxxx xxxxxx xx xxxxxx xxxxxxxxx xxxxxxxx xxxxxxxx o xxxxxxxxxx xxxxxxx nebudou xxxxxxxxxxxx xxxxxxxx xxxxx xxxxxxxxxxx x xxxxxxxx xxxxxx xxxxxxxxxxxxxxx xxxx včetně xxxxxxxxxx xx xxxxx xxx xxxxxxxxx xxxxx xxxx xxxxxxxxxxx služebních x xxxxxxxxxx xxxx xx xxxxxxxxxx xxxxxxx xxxxxxxxxxx xxx rozpočtovou xxxxxxxx Xxxxxxxxxxxx xxxxxxxxxxxxx, xxxxxxxxx na xxxxxx Xxxxxx. Xxxxxx na xxxxxxx xxxxxxx xxxxxxxx se xxxxxxxxxxxxxxx. |
|
|
3.2 Dopady xx xxxxxxxxxxx xxxxxxxxxxxxxxxxxxx XX: XX |
|
|
Xxxxxxxxxxxxxxx xx dopady xx xxxxxxxxxxx xxxxxxxxxxxxxxxxxxx XX. |
|
|
3.3 Xxxxxx xx xxxxxxxxxxxxx xxxxxxxxx: XXX |
|
|
Xxxxxx xx xxxxxxxxxxxxx xxxxxxxxx Xxxxx xxxxxxxxx xx xxxx k xxx xxxxxxxxxxx xxxxxx x xxxxxxxx, xxxxx xx xxxx xxxx xxxxxxx xxxx xxxxxxx, tj. xxxxxxx č. 70/2013 Sb., x xxxx odloženou xxxxxxxx, xxxxxxxx se xxxx xxxxx k nařízení x xxxxxxxxxx xxxxxxx. Xxxx xxxxxx již xxxx xxxxxxxxx xxx xxxxxxxxxxxx xxxxxx xxxxxxxx xxxxxxxx. V xxxxx xxxxx xx xxxxx xxxxxxx xx xxxxxxxxx xxxxxx, včetně zprávy x xxxxxxxxx dopadů xxxxxxxx (RIA) k xxxxxx č. 70/2013 Sb. x xxxx xx xxxxxxxxx xxxxxx XXX x xxxxxxxx x xxxxxxxxxx xxxxxxx označenou „Xxxxxx Xxxxxxxxxx“. V této xxxxxxxx zprávě xx xxxxx, xx x xxxxxxx x čl. 4 xxxxxxxx 2011/62/XX x xx. 54a xxxx. 2 a 3 xxxxxxxx 2001/83/ES Xxxxxx xxxxxxxxx xxxxxxx, xxxxxxx x xxxxxxxxxx xxxxxxxxxx xxxxxxx možností xxx xxxxxxxxxxxxxxx x technické xxxxxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx x xxxxxxx xxxxxxx xxxxxxxxxx prvků x xxxxxxxx x xxxxxx xxxxxxx xxxxxxx. Xxxxxxxx, xxxxx xxxx xxxxxxxxxxx xxxx xxxxxxxxx xxxxxxxxxxxxxxx, xxxxxxxxxxx xxxxxxxx prvky xxxxxxxx x ochranných xxxxxxx. X xxxx xxxxxx xx xxxxxx, xx xxxxxxx xxxxxxxxx xxxxx xxxxxxx xxxxxxx na xxxxxxx x xxxxxxxx xxxxxxxxxx x xxxxxxxxxx xxxxxxxx xxxxxxxxx opatřených xxxxxxxxxx xxxxx. Xxxxxxx xxxxxxxx xxxxxxxxx opatřených xxxxxxxxxx prvky xxxxxxx xxxxxxx xx zřízení x xxxxxx xxxxxxx xxxxxxx (xxxx povinnost xxxx xxxxxxx již xxxxxxxx 2011/62/EU, xxxxx xxxx transponovaná xx xxxxxxxx řádu ČR xxxxxxx č. 70/2013 Sb.). Xxx xxxxxxx x souběžné xxxxxxx představuje xxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx na xxxxxxx humánních xxxxxxxx xxxxxxxxx xxxxx xxxxxxx, xxxxx xxxxxxx x xxxxxxxx xxxxxxxxxxx xxxxxxx xxxxx xxxx xxxxxxx xxxxx (xxxxxxxx xxxxxxx) x xxxxxxxxxx do xxxxxxxxxxxx xxxxxxx, xxx xxxx možné xxxxxxxx xxxxxxxxx x xxxxxxxxxxx xxxxxxxxxxxxxxxx xx xxxxxxx xxxxxxxx. X současné xxxx balicí xxxxx xxxxxxx na xxxxxx xxxxxxxx xxxxxxxxx čísla xxxxx. Xxx xxxx xxxxx vytisknout jedinečný xxxxxxxxxxxxx, xxxx xxx xxxxxx linky xxxxxxxxx xxxxx xxxxxxxx x xxxxxxxxxx xxxxxxxxx. Xxxxxxx xxxxxxx xxxxx částečně kompenzovány xxxxxxxxxxxxx úsporami x xxxxxxx x xxxxxxxx: - xxxxxxxxx nákladů (xxxxxxxxxx xxxxxxx vnitrostátních xxxxxxxxxx xxxxxxxxx pravosti xxxxx xxxxxxxxxxxxxx xxxxxxxx XX xx vyloučí xxxxxxx xxx xxxx výrobních xxxxx, xxx xxxxxxxx xxxxxxxxxxxx xxxxxxxxxxxx xxxxxxxxx xxxxxxx), - xxxxxxx xxxxx xxxxxxx a xxxxxxxx xxxxxxxxxx o xxxxxxxxxx (xxxxxxx xxxxx padělaných xxxxxxxx přípravku xx xxxx povede x xxxxxxx xxxxxxxxx prodejů), - xxxxxxxxx x snížení xxxxxxx xxx postupech xxxxxxxxx x xxxxxxx xxxxxxxx xxxxxxxxx, xxx xxxxxx datové xxxxx (xxxxx x doba xxxxxxxxxxxxx) uvedené x xxxxxxxxxx xxxxxxxxxxxxxx. Xxxxxxx xxxxxxxxxxxx xxxxx a osob xxxxxxxxxxx nebo xxxxxxxxxx x xxxxxx xxxxxxxx xxxxxxxxx xxxxxxx s xxxxxxxxxx ověřovat xxxxxxxx xxxxx a vyřazovat xxxxxxxxx identifikátor xx xxxxxxx xxxxxxx (pořízení xxxxxxxxxx xxxxxxx 2X xxxx, xxxxxx softwarových xxxxxxxx, xxxxxxx na xxxxxx xxxxxx). Xxxxx xxxxxx xx podnikatelské xxxxxxxx xxxxxxx xx s xxxxxxxxxxx xxxx registrací x léčivých přípravků xxxxxxxxxx xxxxxxxxxx prvky. Xxxxxxxx xxxxx xxxxxxxxxx xxxxxx xx xxxxxxxxxxxxx xxxxxxxx z xxxxxxxx xxxxxxxxxxxx xxxxxxxxxx prvků xx xxxxxxxxxxx xxxxxxxxxxx xx xxxxxxx xxxxxxxxx, xxxxx xxxxx xxxxxxxxxx xx x jedinečnému xxxxxxxxxxxxxx lze zavést xx textu obalu x xxxxx xxxxxxxxxx xxxxxx x xxxxxxx xx xxxxxxxxx x xxxxxxxxx - xxxx. xxxxxx x xxxxxxxxxxx xxxxxxxxx registrace, xxxxxx x xxxxx xxxxxxxxxx xxxx II, xxxx XX xxxx xxxx XX. Xxx xxxxxxx xxxxxxxx xxxxxxxxx xxxxxx xxxxx xx zavedení xxxxxxxxxx prvků nutné xxxxxxxxxx zvláštní xxxxxx x xxxxx xxxxxxxxxx, xxxxx xx xxxxx xxxxxxxxxxxxx xxxxxxxx prvky xx registrační dokumentace xxx xxxx xxxxxxxxxxx xxxx xxxxxxxxxx příslušné xxxxxxx x xxxxx xxxxxxxxxx. Xxxxx xxx xx xxxxxxxxxxxxx xxxxxxxx x xxxxxxx xxxxxxxx x x oblasti xxxxxxxxxxxx lhůt xx xxxxxxxx xxxxxxxxxxxx xxxxxxx xxxxxxxx se xxxx xxxxxxxxxx xxxx xxxxxxxxx. Xxxxxxx xx xxxxx a xxxxxx systému, xxxxx xxxxxx xxxxxxxxxxxx xxxxxxx xxxxx, nesou xxxxxxxx xxxxxxxx k xxxxxx (xx. xxxxxxx a xxxxxxxx distributoři) xxxxxxxx xxxxxxxxx xxxxxxxxxx ochrannými xxxxx. Xx xxxxx xxxxxx spolupracovaly zainteresované xxxxxxxx xxxxxxxx EAEPC (xxxxxxxx xxxxxxxxxxxx), EFPIA x MFE (výrobci) - společně představující „xxxxxx“ xxxxxxx, XXXX (xxxxxxxxxxxx lékárníků) x XXXX (xxxxxxxxxxxxxxx) xxx xxxxxx Evropského modelu xxxxxxxxx léků (Xxxxxxxx Xxxxxxxxxxx Xxxxx xx XXX). Xxxx xxxxxxxx xxxxxxxx xxxxxxxx neziskovou právnickou xxxxx, Xxxxxxxxx organizaci xxx ověřování léčiv (Xxxxxxxx Xxxxxxxxx Xxxxxxxxxxxx Xxxxxxxxxxxx či XXXX), xxxxx xx xxxxxxxx xxxxxxxx XXX xxxxxxxxx xxxxxxxxxx xxxxxxxxxxx „hubu“ (Xxxxxxxx Xxxxxxxxx Xxxxxxxxxxxx Xxxxxx či XXXX), x xxxxxxxx xxxxxxxxxx xxxxxxx xxxxxxxxxxxxxxx xxxxxxxx xxxxxxxxx xxx xxxxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxxxxxx. X Xxxxx xxxxxxxxx xxxxxxxxx xxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxxxxxxxxx stran, jmenovitě XXXX (Xxxxxxxx evropských xxxxxxxxxxxx xxxxx), XXXX (Xxxxxxxx xxxxxxxxxxxx farmaceutického xxxxxxxx), XXXX (Asociace xxxxxxxxxxxxxxxxx xxxxx), XXXX (Xxxxx asociace xxxxxxxxxxxxxxx xxxxx) x XXxX (Xxxxx xxxxxxxxxx komora) xxxxxxxxxxx xxxxxxx, xxx xx klade xx xxx vést x xxxxx postup implementace XXX v České xxxxxxxxx, xxxxxxxxxx xxxxxxxx xxxxx. Konečným xxxxx xx dodat Národní xxxxxx pro ověřování xxxxx (XXXX), xxxxxxxxxxxx xxxx ESM a xxxxxxxx funkčnosti xxxxxxx XXXX. Xxxx x xxxxxxx x xxxxxxxxx xxxxxxx bude XXXX xxxxxx x xxxxxxxxx xxxxxxxxxx xxxxxxx xxxxxxxxx Xxxxxxx organizací pro xxxxxxxxx pravosti léčiv (XXXX) pod dohledem xxxxxxxxx xxxxxx autority. Dle xxxxxxxx xxxxxx xxxxxxx xxxxxxxxxx xxxxxx xx xxxxxx trhu xxxxxxxx xxxxxxxxx xxxxxxxxxx na xxxxxxx xxxxxxxxx 261 xxxxxxxxxxxxxxx společností xxxxxxxxxxxxx xx 465 xxxxxxxx xxxxxxxxxx x xxxxxxxxxx, 525 xxxxxxxxxxxx, x xxxxx xxxxxxx xxxxxxxxxxx xxxxxxx x licencí xxxxxxxxxxxx, 15 souběžných xxxxxxx, xxxxxxxxx 200 xxxxxxxx x xxxxxxx xxxxxxxxx ústavů x xxxxxxx lékárnou x xxx 2 800 xxxxxxx. Xxx xxxxxx xxxxxx xx na xxxxxx xxxx xxxxxxx xxxxxxxxxx xxxxxxxxx 180 xxxxxxx xxxxxx léčivých xxxxxxxxx vydávaných xx xxxxxxx xxxxx. Xxxxxxxxx xxxxxxxx XXXX pro xxxxxxxx xxxxxxxxxx x xxxxxxxxxx xx xxxxxxxxxx x xxxxxxxx xxxxxxxxx xxxxxxx xxxxxxxxx léčiv (NSOL) xxxx xxxxxxxx x xxxxxxxxxx XXXX, xxxxxxx xx xxxxxxx o xxxxxx xxxxxxxxxxxxx registračního xxxxxxxx a roční xxxxxxxx xxxxxxxx tzv. xxxx fee. Xxxx xxxxxxxx xx xxx 2019 by xxxx xxx xxxxx x X1/2018. Xx xxxxxxx roku 2018 bylo xxxxxxxxx xxxxxxxxx a kvalifikace xxxxxxx XXXX x xxxxx xxxxxxxxx projektu. Xxx 9.1.2018 xxxxxxxx x xxxxxxxxxx Xxxxxxx xxxxxxxxxx xxx xxxxxxxxx xxxxxxxx léčiv xxxxxxx xxxxxxx x účast x xxxxxxx fázi xxxxxxxx xxxxxxxxx xxxxxxxx xxxxx x Xxxxx xxxxxxxxx, xxxxx cílem xxxx xxxxxxxxxx xxxxxx xxxxxxxxx týkající xx xxxxxxxxxxxxxx xxxxxx x xxxxxxx xxxxxxxxxx x xxxxxxxxxx xx xxxxxxxx xxxxxxxx xxxx xxxxxxxxxx xxxxxxxx. Do xxxxxxxxx xxxxxxxx xxxx xxxxxxxxxx xx zapojit 8 xxxxxxxx ze strany xxxxxxx, 6 xxxxxxxx xx xxxxxx distributorů, 23 lékáren (z xxxx 18 xxxxxxxxxxxx) x 4 dodavatelé XX xxxxxxx. Xxxxxxx xxxx byla spuštěna xxx 3. xxxxxx 2018, xxxxxxx xxxxxxxxxxxxx xxxx xxxxxx xx xx xxxxxxxx xxxxxxxxxx xxxxxxxxxxx xxxxxxxxxxxx na xxxxxx 2018. X xxxx xxxxxxxxx je xxxxxx, xx dotčené xxxxxxxx xx aktivně xxxxxxxx xx xxxxxxxx xxxxxxx xxxxxx xxxxxxx ověřování xxxxxxxx xxxxx x Xxxxx xxxxxxxxx. Xx xxxxxxxxx projektu se xxxxxxxx xxxxxxxx s xxxxxxxxx podílem xx xxxx, x xxxxx xxx důvodně xxxxxxxxx, xx tyto xxxxxxxx xxx xxxxxxxxxx xxxxxxx xxx, xxx se xxxxx xxxxxxxxx xxxxxxxx xxxxxxxx. |
|
|
3.4 Dopady xx xxxxxx xxxxxxxxxxx xxxxx (xxxx, xxxxx): XX |
|
|
Xxxxxxxxxxxxxxx xx xxxxxx xx xxxxxx xxxxxxxxxxx xxxxx. |
|
|
3.5 Xxxxxxxx dopady: XX |
|
|
Xxxxxxxxxxxxxxx xx xxxxxx xx xxxxxxxx xxxxx. |
|
|
3.6 Xxxxxx xx spotřebitele: XXX |
|
|
Xxxxxxxx xxxx, xxxxx zajistí xxxxxxx xxxxxxxx xxxxxxxxx x xxxxxxxx xxxxxxxxxx xxxxxxx, xxxx xxx xxxxxxxxx pozitivní xxxxx xx xxxxxxxxxxxxxx sektor. Xxxxxxxx x tomu, xx xxxxxxx xxxxxxx x xxxxxxxx xxxxxxxxxx x xxxxxxxxxx xxxxxxxx xxxxxxxxx, xxxxxxx obaly xxxxxxx xxxxxxxx xxxxx, xx x xxxxxx xxxxxxxx xxxxxxxxxx xxxxx xx xxxxxx míry xxxxxxxxx xxxxx, xxxx xxxxxxxx částečný xxxxx xxxx skutečnosti na xxxx xxxxxxxx přípravků. Xxxxxxx náklady xxxxxxx x xxxxxxxx rozhodnutí x xxxxxxxxxx xxxxxxxx xxxxxxxxx však xxxx xx xxxxxx k xxxxxxxxx xxxxxxx xxxxxxxxxxxxxxx xxxxx xxxxxxxxxxxx, xxxxx xxxxxxx na xxxxxxxx XX xxxx x xxxxxxxx xxxxxxxxx xxxxxxxx xx xxxxxx xxxx xxxxx jistě řádově xxxxx xxx xxxxxxxx xxxxxxx na xxxxx, xxxxxx x xxxxxxxxxx xxxxxxxx xxxxxxxxx. Xxxx xxxxxxxx xxxxxxxxx, xxxxxxx xxxxx je xxxxx xx xxxxxxxx xxxxxxx, xx xx xxxxxxx xxxxxxx regulována způsobem xxxxxxxxx maximální ceny xxxxxxxx rozhodnutím, xxxxxx xxx zvýšit xxxxx xx základě xxxxxx xxxxxxxxxxx žádosti. Současně xxxx x podmínky xxxxxx xxxxxxxx přípravku x xxxxxxxxxx veřejného xxxxxxxxxxx pojištění jsou xxxxxxxxxxx x rámci xxxxxxxxx xxxxxx. Navíc xx x zemích Xxxxxxxx xxxx (xxxxxx XX) xxxxx xxxxxxx xxxxxxx xxx. xxxxxxxx xxxxxxxx referencování - xxxx xxxxxxxxx xxxx x xxxxxx xxxxx xxxxxxxxxx cen stejného xx xxxxxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxx x xxxxxxxxx, xxxxx by x drtivé většině xxxxxxx xxxxxx teoretické xxxxxxxx xxxx x XX vliv xx xxxxxx xxxxxxxx xxxxxxxxx x xxxxxxxxxx veřejného xxxxxxxxxxx pojištění. Xxxxxxxx x xxxxx xxxxxxxxx xxxxx xxxxxxxxxxxxx xxxxxxxxx xx xxxxxxxxx trhu x léčivy xx xxxxxxxxx cen léčivých xxxxxxxxx x důvodu xxxxxxxx xxxxxxxxxx prvků xxxxxxxxxxxxx, xxxx nebude xxxxxxxxxxx xx xxxxx xxxxxxx. Ceny xxxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxx xxxxxxxxx, do xxxxxxx xxxxxxxxx zdravotního pojištění xx promítá xxxxxx xxxxxxxx přípravku, xxxxxxx xxxx xxxx. |
|
|
3.7 Xxxxxx xx xxxxxxx xxxxxxxxx: XX |
|
|
Xxxxxxxxxxxxxxx xx dopady xx xxxxxxx prostředí. |
|
|
3.8 Xxxxxx ke xxxxxx x xxxxxx diskriminace x xx xxxxxx x xxxxxxxx xxx x xxxx: XX |
|
|
Xxxxxxxxxxxxxxx xx xxxxxx x xxxxxx xxxxxxxxxxxx a xx xxxxxx x xxxxxxxx xxx x xxxx. |
|
|
3.9 Dopady na xxxxx xxxxxx xxxxxxxxxxx xxxxxx: NE |
|
|
Nepředpokládají se xxxxxx na xxxxx xxxxxxxxxxx xxxxxx |
|
|
3.10 Xxxxxxxx xxxxxx: XX |
|
|
Xxxxxxxxxxxxxxx xx xxxxxxxx xxxxxx. |
|
|
3.11 Dopady xx bezpečnost xxxx xxxxxx xxxxx: XX |
|
|
Xxxxxxxxxxxxxxx xx xxxxxx xx xxxxxxxxxx nebo xxxxxx xxxxx. |
|
1. Důvod xxxxxxxxxx x xxxx
1. 1 Xxxxx
Xxxxx xxxxxx, kterým xx xxxx xxxxx č. 378/2007 Sb., o xxxxxxxx x x změnách xxxxxxxxx xxxxxxxxxxxxx zákonů (xxxxx o léčivech), xx xxxxx xxxxxxxxxx xxxxxxxx.
1. 2 Xxxxxxxx xxxxxxxx
X rámci celé Xxxxxxxx xxxx xxx xxxxxxx znepokojující nárůst xxxxxxx xxxxxxxxxx léčivých xxxxxxxxx, xxx dlouhodobě xxxxxxxxxxx závažný problém, xxxxx přímo xxxxxxxx xxxxxx pacientů. Xxxxxxxx xxxxxx xxxxxxxxx postihují xx větší xxxx xxxxxxx xxxxxxxxx xxx (xxxxxxx xxxxx xxxxxxxxxxxxx xxxxxxxx na internetu), xxx x xxxxxxxxxx xxxxxx xxx xxxxxxxxxx xxxxxx xxxxxxxxxx léčivých xxxxxxxxx také x xxxxxxxx xxxxxxxxxxxxx xxxxxxx x xxxxxxxx přípravky (xxxxxxxx xxxxxxx, xxxxxxxx xxxxxxxxxxx x povolená xxxxxxx xxxx xxxxxxxx xxxxxxxxxxx xxxxx). Xxxxxxxx x xxxxxxxx dodavatelském xxxxxxx xxxxx x xxxxxxxx xxxxxxxxx xxxxxxxx xxxxx xx xxxxxxx xxxxxxxxx k xxxx xxxxxxxx x xxxxxxx x xxxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxx x xxxx x xxxxxxxxxxxx xxxxxxxxxxx xxxxxxxxxxxx příslušnými xxxxxxxxxxx xxxxxxxxxx.
Xx xxxxxxxxxxx, xx x České xxxxxxxxx xxxxx xxxxxxxxxx xxxxxx xxxxxxxxxx léčivých xxxxxxxxx přímo x xxxxxxxxx. Xxxxxxxx léčivé xxxxxxxxx xx xxxxxxxxx x xxxxxxxxxxxx xxxxxxx Xxxxx xxxxxxxxx x xxxxxxxx, xxxxxxx je xxxxx xxxxxxxxxx, že xxxx xxxxxxxxxxxx xxxxxxxx xxxxxxxxx x Xxxxx xxxxxxxxx disponuje xxxxxxxxxx x xxxxxxxxxxx xxxxxxxxxxx xxxxxx - xxxxxxxxxx xxxx. Xxxxxxx podle xxxxx Ústavu v xxxx 2013 xxxxx x Xxxxx xxxxxxxxx x xxxxxxx xxxxxxxxxxx xxxx xxxxxxxxxx žádný xxxxxx xxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx, x xxxx 2014 se xxx jednalo o 11 případů, v xxxx 2017 x 45 xxxxxxx x xx srpna xxxx 2018 xxx 40 xxxxxxx xxxxxxx padělaných xxxxxxxx xxxxxxxxx x xxxxxxxx distribučním xxxxxxx. Xxxx zjištění xxxxxxxxxx xxxxxx, xx se xxxxx x vzrůstající xxxxx, kterému xx xxxxx xxxxx a xxxxxxxx tomu, xxx xx xxxxxxxx xxxxxx xxxxxxxxx xxxxxxx k xxxxxxxxx.
Xxxxxxxxxx jsou xxxxxxxxx xxxxxxxx léčivé xxxxxxxxx xxxxxxxxx x xxxxx xxxxxxxx xxxxxxxxx, xxxxxx xxxx, xxxxxx xxxxxx xxxxxxx, xxxxxxx x xxxxxxxxxxxxx xxxxxxxxxx. Distribuční xxxxxxx xxxxxxxx přípravků xx v dnešní xxxx velmi xxxxxxx x xxxxxxxx stávajícímu xxxxxxxxxxx xxxxx a xxxx xxxxxxxxx xxxx xxxxxxxxx obchodníci xxxxxxxxxxx xxxxxxxxxx xx xxxxxxxxx xxxxxxxxxxxxxx řetězce x xxxxxxx xxxxxxxx xxxxxx xxxxxxxxx zákonným xxxxxxxxxxxxxx. Xxxxxxx spočívá v xxx, že nejsou xxxxxxxx xxxxx xxxxxxx xxxxxxxxxxxxx xxxxxx, která xx xxxxxx xxxxxxx xxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx xx xxxxxxxxx xxxxxxxxxxxxxx xxxxxxx
X xxxxxx xx xxxxxxxx xxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx x xxxxxxxx xxxxxxxxxxxxx xxxxxxx v Xxxxxxxx xxxx byla xxxxxxx xxxxxxxx 2011/62/EU, xxxxx xxxxxxxxx xxxxxx xxxxxxxxxx xxxxx xx xxxxxxx xxxxxxxx xxxxxxxxx, který xx xxxxxxx xxxxxx xxxxxxx pravosti xxxxxxxx xxxxxxxxx, xxxxxxxxxxxx xxxxxxxxxxxx xxxxxx léčivých přípravků x ověření, zda xxxxxx s xxxxxx xxxxxxxxxxxx. Tyto xxxxxx xxxxxxxxxxxx xxxxxxxx by xxxx zajistit xxxxxxxxxxx xxxxxxx proti xxxxxx xxxxxxxxxx xxxxxxxx přípravků xx xxxxxxxxx xxxxxxxxxxxxxx xxxxxxx x xxxxxxxxx xxxxxxx Xxxxxxxx unie x cílem chránit xxxxxxxx i xxxxx xxxxxxxx rozhodnutí x xxxxxxxxxx x výrobců.
Za xxxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxxxx léčivých xxxxxxxxx xx jiných xxxxxxxxxxx xxxxxxxx xxxxxxxxx zavedla xxxxxxxx 2011/62/EU definici „xxxxxxxxxx xxxxxxxx xxxxxxxxx“:
Xxxxxxxx xxxxxx xxxxxxxxx xx xxxxxxxx xxxxxx přípravek x nepravdivými údaji x xxxx xxxxxxxxxx, xxxxxx obalu x xxxxxxxx xx xxxxx, xxxxx xxxx xxxxxxx (xxxxxx xxxxx xx xxxxxxx látky); xxxxxx (xxxxxx výrobce, xxxx xxxxxx xxxx xxxxxxxx xxxxxxxxxx o xxxxxxxxxx) xxxx xxxxxxxx (včetně xxxxxxx a xxxxxxxxx xxxxxxxxxx se xxxxxxxxxx). Xxxxxxxx xxxxxx xxxxxxxxx x xxxxxxxx složení xxxxxxxx xxxx xxxxxxxx xxxxxx x xxxxxxx xxxxx, xxxx obsahují xxxxxxxxx xxxxxxxx xxxxxx xxxxx xx x xxxxxxxxxx xxxx neobsahují xxxxx xxxxxx xxxxx.
Xxxxxxxx xxxxx xxxxxxxxxxx xxx xxxxx xxxxxxxx xx xxxxx xxxxxxxxx léčivého xxxxxxxxx:
- xxxxxxxxx xxxxxxxxxxxxx (xxxxxxxxx sekvence nesená xxxxxxxxxxxxx xxxxxxx xxxxx, xxxxxxxxxx xxxxxxx pravosti x xxxxxxxxxxxx xxxxxxxxxxxx xxxxxx xxxxxxxx xxxxxxxxx, xx xxxx xx xxxxxxxxx). Jedinečný xxxxxxxxxxxxx xx xxxxxx x xxxxxxxx datových xxxxx: xxx xxxxxxxxx (xxxxxxxxxx xxxxxxxxxxxxx alespoň xxxxx xxxxx, lékovou xxxxx, xxxx, velikost balení x xxx xxxxxx); xxxxxxx xxxxx (xxxxxxxxx xxxx xxxxxxxxxxxxx xxxxx xxxxxxxxx 20 znaků xxxxxxxxxxxxxx xxxxxxxxxxxxxxxx nebo xxxxxxxxxxxxxxxxxx randomizačním xxxxxxxxxx); xxxxxxxxxxxx úhradové číslo xxxx xxxx vnitrostátní xxxxxxxx xxxxx (pouze xxxxx xx xxxxxxxxxx xxxxxxxx xxxxxx, v xxxx xx xxx xxxxxx xxxxxxxxx xx xxx); xxxxx xxxxx, xxxxx xxxxxxxxxxxxx.
- prostředek x ověření manipulace x xxxxxx (xxxxxxxx xxxxx - bezpečnostní xxxxxxxx - xxxxxxxxxx xxxxxx, xxx xxxx x xxxxxx léčivého xxxxxxxxx xxxxxxxxxxxx).
Xxx systém xxxxxxx xxxxxxxxxx xxxxx xx xxxxxxx humánních xxxxxxxx přípravků, xxxxx xxxxxxxxx xxxxxxxx 2011/62/EU, xxx xxxxxxxxxx xx xxxxx xxxxxxxxx xxxxxxx Xxxxxxxx unie, xxxxxxxxxx xxxx xxxxxxxx xxxxxxxxx x xxxxxxxxxx xxxxx xxxxxxx všech účastníků xxxxxxxxxxxxxx řetězce xxxxxxxxx xxxxxxxxxxxx xxxxxxxxx xxxxxxxxxx, xxxxxxxxx Xxxxxxxx Komise xxxxxxxxxxxxxxx xxxxxxxx x xxxxxxxxxx xxxxxxx xxxxxxxx xxxxxxxx pro zavedení xxxxxxxxxx xxxxx, zejména xxxxxxxxxxxxxxx x technické xxxxxxxxxxx xxxxxxx x xxxxxxxxxx prvků - xxxxxxxxxxx xxxxxxxxxxxxxx, způsoby x xxxxxx xxxxxxx xxxxxxxxxx prvků xxxxxxxxxxxx xxxxxxxxx subjekty (xxxxxxx, xxxxxxxxxxxx, xxxxxxx oprávněnými xxxx zmocněnými vydávat xxxxxx xxxxxxxxx xxxxxxxxxx) x xxxxxxx a xxxxxx systému xxxxxxx xxxxxxxxxx informace x xxxxxxxxxx xxxxxxx (xxxxxxxxxxx xxxxxxxxxxxxxxxx).
Xxxxxxxx x xxxxxxxxxx xxxxxxx xx xxx xxxxxxx xxxxx xxxxxxx x celém xxxxxxx x xx xx xxxxx členských státech xxxxx xxxxxxxxxx. X xxxx xxxxxxxx x xxxxxxxxxx xxxxxxx upravuje xxxxxxxxxxxx xxxxxxxxxx xxxxx xxxxxxxx xxxxxxxxx, některé xxxxx otázky xxxxxxxxx xx xxxxxxx a xxxxxxxxxx členských států:
A. Xxxxxx příslušného xxxxxxxxxxxxxx xxxxxx, xxxxx xx xxx mít xxxxxxx x xxxxxxxx xxx xxxxx dozoru nad xxxxxxxxxx xxxxxxx, xxxxxxxxxxx xxxxxxxxxxxxx xxxxxxx xxxxxxxx, xxxxxx, farmakovigilance a xxxxxxxxxxxxxxxxxxxx. Xxxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxxxxxxxxxx orgánům xxxxxxxxx xxxxx přístup x xxxxxxxx a x informacím x xxx obsaženým pro xxxx uvedené xxxxx xxxxxx nařízení o xxxxxxxxxx prvcích xxxxxxxx xxxxxxxx, xxxxx xxxxxxx x xxxxxxxx xxxxxxxx xxxxxxxxx k ověření xxxxxxxx xxxx vyřazení xxxxxxxxxxx xxxxxxxxxxxxxx léčivých xxxxxxxxx uváděných na xxx v xxxxxxxx xxxxx. X xxxxxxxxxx Xxxxx xxxxxxxxx xxxx xxxxxxxxxx xxxxxxxxxxxxx xxxxxxx xxx xxxxxxxx x xxxxxxxxxx xxxxxxx Xxxxx, x xx xxxxxxx x xxxxxxx xx xxxxxxxxx právní xxxxxx xxxx xxxxxxxxxx danou xxxxxxx x léčivech, xxxx xxxxxxxxx autority xxx xxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx. Z xxxxxx xxxxxx xx xxxxx rozšířit xxxxxxxxx Xxxxxx x §13 xxxxxx x xxxxxxxx. Xxxxx xxx bude xxxxx xxxxxxxxxx xxxxxxxxx x xxxxxxxx IX xxxxxxxx o ochranných xxxxxxx. Xxxxxxx xxxxx x xxxxxxxxxxxx informací xxxxxxxxx rozhodnutí o xxxxxxxxxx, výrobcům, distributorům x xxxxxx xxxxxxxxxx xxxx zmocněným xxxxxxx xxxxxx xxxxxxxxx veřejnosti, x léčivých přípravcích xxxxxxxxx xx xxx xx území Xxxxx xxxxxxxxx, xxxxx musí xxx opatřeny ochrannými xxxxx (x souladu x článkem 54 xxxx. x) směrnice 2001/83/XX). Xxxxx xxxx xxxxxxxxx xxxxx xxx xxxxxxxxxx xxxxxxxxx xxxxxxxx x Xxxxx republice, xxx xxxxxx, x xxxxxxx xxxxxxx prostřednictvím xxxxxxxx, xx úložiště x xxxxxx xxxxxxx xxxxxxxxx xx xxxxxxx a xxxxxx úložiště xxxxxxx xxxxxxxxx xxxxxxxx. Zprávy x xxxxxxxx xxxxxxxx xxxx xxxxxxxx Xxxxxxxx xxxxxxxx xxx xxxxxx xxxxxxxxx, xxxxx je xxxxxxxxxx xxxxxx příslušným xxxxxxxxxxxxx xxxxxxx x Xxxxxx.
X. Xxxxxxxxx, aby xxxxxxxxxx, xxxxx xxxxxxxx x xxxxxxxxxx xxxxxxx xxxxxx regulovaným subjektům, xxxx plněny, x xx xxxxxxxxx skutkové xxxxxxxx přestupků v xxxx oblasti, xxxxxxx xxxxxxxxx xxxxxx příslušného x xxxxxx xxxxxxxxxxxx x stanovením výše xxxxxx xx neplnění xxxxxxxxxx xxxxxxxxxxxx subjekty. Xxx úpravy xxxxxx xxxxxxx xx xxxxxxxx x ochranných prvcích xxxx v členském xxxxx neaplikovatelné a xxxxxx by xx xxxxxxx.
X. Členský xxxx xxxx rozšířit xxxxxx xxxxxxxxxx jedinečného xxxxxxxxxxxxxx xxxx xxxxxxxxxx k xxxxxxx xxxxxxxxxx s xxxxxx na některé xxxxx xxxxxx přípravky x xxxxxxx x xxxxxxx 54x xxxx. 5 xxxxxxxx 2001/83/XX (xx. 2 odst. 1 xxxx. c) xxxxxxxx o xxxxxxxxxx xxxxxxx), xxxxxx slovy xxxx xxxxxxxxx, xxx xxxxxxxxxx prvky xxxx xxxxxxxx xxxxx x xxxx xxxxxxxx přípravků, xxxxx xxxxxxxxx xxxx xxxxxxxx prvky nemají. Xxxxx republika xxxxxx xxxxxxxxxx oblast xxxxxxxxxx xxxxxxxxxxx identifikátoru xxxx xxxxxxxxxx x xxxxxxx xxxxxxxxxx x xxxxxx xx xxxxxxx xxxxx xxxxxx xxxxxxxxx x xxxxxxx s článkem 54x xxxx. 5 xxxxxxxx 2001/83/XX (čl. 2 xxxx. 1 písm. x) xxxxxxxx o xxxxxxxxxx xxxxxxx).
X xxxxxxxxx Xxxxxxxx Xxxxxx „Safety Xxxxxxxx xxx xxxxxxxxx xxxxxxxx xxx human xxx - Xxxxxxxxx xxx Xxxxxxx“ - Xxxxxxx 9 (Xxxxxxx 2018) xxx. 5 xxxxxx 1.10. je xxxxxx, xx xxxxx xxxxxxx xxxx xxxxxxxxx xxxxxxxx xxxxxx 54a xxxx. 5 věta xxxxx xxxxxxxx 2001/83/ES xxxx možné xxxxxxx xxxxxxxxxx x ověření xxxxxxxxxx s xxxxxx xx xxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxx xxxxxxx xxxxxx xx xxxxxxxx xxxxxxx xxxxxxxx na xxxxxxxxxxxxx xxxxxxx.
Xxxxxxx Xxxxx xxxxxxxxx xxxxxxxxx možnosti článku 54x xxxx. 5 xxxx xxxxx xxxxxxxx 2001/83/XX x xxxxxxxxxxx xxxxxx xxxxxxxxxx xxxxxxxxxx x xxxxxxx xxxxxxxxxx x xxxxxx xx xxxxxx xxxxxxxxx xxxxxxxxxxxxx xxxxxxx výdeje xx xxxxxxxx xxxxxxx, xxxxx xxxxxxxx xxxxxxxxx xxx xxxxxx 54a xxxx. 1 xxxxxxxx 2001/83/XX xxx., xx xxxxxx xxxxxxxxx xxxxxxxxxxxxx xxxxxxx xxxxxx xx xxxxxxxx xxxxxxx xxxxxxx být xxxxxxxx ochrannými xxxxx, xx. xxx xxxxxxxxxxx x xxxxxxx manipulace x xxxxxx (x xxxxxxxx těch zapsaných xx xxxxxx x xxxxxxx XX xxxxxxxx x xxxxxxxxxx xxxxxxx).
X. Xxxxxxxx uvádí xxxxx „xxxxxxxxxxxx xxxxxxxx xxxxx“ xxxx „xxxx xxxxxxxx xxxxx“ xxxxxxxxxxxxxx léčivý xxxxxxxxx a ponechává xx xxxxxxxxxx xxxxxxxxx xxxxx, xxx tento xxxxxx xxxxx xxxx xxxxxx x xxxxx xxxxxxxxxxx xxxxxxxxxxxxxx xx xxxxxxx. X Xxxxx xxxxxxxxx xx „xxxxxxxxxxxxx xxxxxxxxx xxxxxx“ kód xxxxxxxxx Xxxxxxx xxxxx §32 odst. 5 xxxxxx o xxxxxxxx (xxxx xxx „xxx XXXX“). Česká xxxxxxxxx xxxxxx xxxxxxxxx, xxx xxx XXXX byl xxxxxx x rámci xxxxxxxxxxx identifikátoru, xxx., xx xxxx xxxxxxxx xxxxxxxxx stav, kdy xxx XXXX je xxxxxx xx xxxxx xxxxxxxxx.
X. Xxxxxxx zásadou xxxxx xxxxxxxxx o xxxxxxxxxx xxxxxxx xx xxxx být, xxx x xxxxxxxx xxxxxxxxxx xxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx ze xxxxxxx xxxxxxx xxxx xxxxxxxxx xx xxxxx dodavatelského xxxxxxx, xx. xxx xx xxxxxx xxxxxxxxx xxxxx xxxxxxxxxx. Členský xxxx xx xxx xxx xxxxxxxxx xxxxxxxx xxxxxxxxxxxxxxx xxxxxxxxxxxxxx xxxxxxx xx xxxx xxxxx x umožnit ve xxx xxxxxx xxxxxx, xxx xxxxxxxxxxx ověřil xxxxxxxx xxxxx x xxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxx xxx, xxx xxxxxx xxxxxxxxx vydá xxxxxxx x xxxx xxxx institucí xxxxxxxxx x článku 23 xxxxxxxx x xxxxxxxxxx xxxxxxx:
x) xxxxxx xxxxxxxxxx xxxx xxxxxxxxx vydávat xxxxxx xxxxxxxxx veřejnosti, které xxxxxxxx x xxxxx xxxxxxxxxxxxxx xxxxxxxx xxxx xxxxxxx;
x) xxxxxxxxxxxx xxxxxxx x xxxxxxxxxxxxxxx x xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx,
x) xxxxxx xxxxxxx;
x) xxxxxxxxxxxxx x xxxxxxx;
x) xxxxxxxxxxx xxxxxxxxxxxx xxxxxxxxx xxxxxx;
x) xxxxxxxxxx xxxxx, xxxxxxx x dalším vládním xxxxxxxxxx, xxxxx xx xxxxxxx xxxxxx léčivých xxxxxxxxx pro xxxxx xxxxxxx xxxxxxx a xxxxxxxx xxxxxxxxx;
x) xxxxxxxxxxx x xxxxxx xxxxxxxxxx xxxxxxxxxxxxxxx vzdělávání, xxxxx xxxxxxxxx xxxxxx přípravky xxx xxxxx xxxxxxx x xxxxxxxxxx, s xxxxxxxx xxxxxxxxxxxxxx xxxxxxxx;
x) xxxxxxxx;
x) xxxxxx;
x) hospicům;
k) xxxxxxxxxxxxx xxxxxxxxx.
X rámci Xxxxx xxxxxxxxx lze xxxxxx xxxxxxx xxxxxxx 23 nařízení x xxxxxxxxxx xxxxxxx, xx. xxx xxxxxxx ochranných xxxxx x xxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx ze xxxxxxx úložišť provede xxxxxxxxxxx, xxxxxx xxxxx x xxxxxxx dodávek xxxxxxxx přípravků
- veterinárním xxxxxxx,
- Xxxxxx Xxxxx xxxxxxxxx k xxxxxxxxxxx xxxxxxxxxxx xxx xxxxxx, x udržování skladových xxxxx xxxxxxxx xxxxxxxxx xxx xxxxx xxxxxxxxxxx xxxxxxxxxxx xxx Xxxxx xxxxxxxxx xxxxxx xxx xxxxxx xxxxxxxx do xxxxxxxxx podle §111a xxxxxx x xxxxxxxx x
- xxxxxxxxxxxxxx xxxxxxxxxxx xxxxxx, xxxxxx xxxx xxxxx §77 odst. 1 písm. x) xxxx 12 xxxxxxxx xxxxxxxxxxxx xxxxxx přípravky xxx xxxxx xxxxxxxxxxxx xxxxxxxx xx základě xxxxxxx smlouvy distributora xx zdravotní xxxxxxxxxxx xxxx xxxx xxxx xxxxxxxxx xxx účely xxxxxxxxxxxx, xxxxxxxxxx x xxxxxxxxxxx xxxxxxxx xxxxxxxx xx xxxxxxx rámcové xxxxxxx xxxxxxxxxxxx x Xxxxxxxxxxxxx xxxxxxxxxxxxx xxxxx xxxxxxxxxxx hrazeného xxxxxxxx x xxxxx preventivní xxxx dle xxxxxx xxxxxxxx xxxxxxxx.
Xxxx uvedené xxxxxx je xxxxx xxxxxxx pouze x xxxxxx xxxxxx zákona x léčivech xxx, xxx xxxxxxxxxxxxxx x xxx xxxxxxxxxx xxxxxxxx xxxxxxx xxxxxxxxxxxx xxxxxxxxxx xxxxx xxxxxxxxxxx směrnicí 2011/62/EU, která xxxx xxxxxxxxxxxxx xx zákona x xxxxxxxx novelou č. 70/2013 Sb. Navrhovanou xxxxxxx xxxx xxxxxxx xxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxx x xxxxxxxxxx xxxxxxx xxx, xxx xxxxx xxx jeho xxxxxxxxxx xxxxx a beze xxxxxx xxxxxxxxxx x xxxxxxxxxx Xxxxx republiky.
1. 3 Xxxxx xxxxxxxxxxxx xxxxxxxx xxxxx x xxxx xxxxxxx
Xxxxxxxxxx právní xxxx x xxxx xxxxxxx x xxxxxxxx xxxx xxxxxxxxxxx xxxxxx xxxxxx norma, x xx xxxxxxxx 2011/62/EU, xxxxx xx xx xxxxxxxxxxxxxx xxxxxxxx xxxx xxxxxxxxxx xxxxxxx xxxxxx x xxxxxxxx č. 70/2013 Sb. Xx xxxxxx o xxxxxxxx byla xxxxxxxx xxxxxxxx padělaného léčivého xxxxxxxxx, x to xx účelem xxxxxxxxxxxxx xxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx xx xxxxxx xxxxxxxxxxx xxxxxxxx přípravků. Xxxx bylo xxxxxxx xxxxxxxxx, které xxxxxx xxxxxxxxx xxxx xxx xxxxxxxx xxxxxxxxxx xxxxx x které xxxx xxxxxxxx být xxxxxxx, xxx xx xxxxxxxx xxxxx xxxxxxxx xx xxxxxxxxxx xxx xxxxxxx xxxxxxxxx čl. 47x xxxx. 1 xxxx. x) xxxxxxxx 2001/83/XX (xxxxx čl. 17 xxxxxxxx x ochranných xxxxxxx) x kdy xxxxxxxx xxxxx nesmějí být xxxxx xxxx xxxxxx xxxxxxxxxx nebo xxxxxxxx, x xxxx xxxxxxxx xxxx xxxxxxxxxx xxxxxxxxxxxx xxxxxxxxxxx xxxxxx x xxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxxx prvky, xxxxxxxxxx x xxxxxxxxxx xxxxxxxx xxxxxxx xxxxxxxxxxxxx xxxxxxx x xxxx xxxxxxxxx xxxxxxxxxxxx informovat Xxxxx a držitele xxxxxxxxxx x xxxxxxxxxx x xxxxxxx přípravku, xxxxx xxxxxxx nebo xx byl xxxxxxxx, x xxxxxxx xxxxxxxxx, xx se xxxxx x xxxxxxxx xxxxxx xxxxxxxxx (xxx ustanovení §37 odst. 7 x 8, §64x, §66 xxxx. 1 xxxx. x) mající xxxxxxxxx xxxxxxxx). Xxxxxxxxxx §77 xxxx. 1 xxxx. m) x x), xxxxx xxxxxx xxxxxxxxx xx 2.4.2013, xxxxxxxxxxx nové povinnosti xxxxxxxxxxxx. Protože xxxxxxxxxxx x xxxxxxxxxxxxxxx xxxxxxxxxx xxxxx x xxxxxxx xxxxxxxxx xxxxxxxxxx xxxxx xxxx xxxx xxxxxxxxx x ochranných xxxxxxx, xxxxx nabyde xxxxxxxxx 9.2.2019, xxxxxxxxx distributora xxxxxxxx ochranné xxxxx x xxxxxxxx xxxxxxxxx xxxxxxxx v případě xxxxxxxxxx xxxxxxxx xxxxxxxxx, xxxx dána až x xxxxxx xxxx.
Xxxx xxxxxxxxxx xxxxxx xxxx x xxxx xxxxxxx xxxxxxxxxxx v xxxxxxxxxx xx xxxxxxxxx směrnici Xxxxxxxx xxxx Xxxxxx xxxxxxx prováděcí nařízení x xxxxxxxxxx xxxxxxx, xxxxx xxxxxxx stanoví xxxxxxxx pravidla xxx xxxxxxxx xxxxxxxxxx xxxxx xxx xxxxxxx xxxxxx xxxxxxxxx. Xxxx xxxxxxxx x xxxxxxxxxx xxxxxxx xxxx xxxxx xxxxxxxxxxxx xxxxxxx xxxxxx o xxxxxxxx adaptováno na xxxxxxxx existující x Xxxxx republice.
V xxxxxxxx x xxxxxxxxxx xxxxxxx, xxxxx je členěno xx 11 xxxxxxx x 4 xxxxxx, xxxx xxxxxxx xxxxxxxx xxxxxxxxxx xxxxx - xxxxxxxxxxx identifikátoru a xxxxxxxxxx x ověření xxxxxxxxxx x xxxxxx, xxxxxxx charakteristiky x xxxxxxxxx xxxxxxxxxxx xxxxxxx x xxxxxxxxxx xxxxx - xxxxxxxxxxx xxxxxxxxxxxxxx, xxxxxxx a xxxxxx xxxxxxx xxxxxxxxxx xxxxx xxxxxxxxxxxx xxxxxxxxx xxxxxxxx (xxxxxxx, xxxxxxxxxxxx, xxxxxxx xxxxxxxxxxx xxxx zmocněnými xxxxxxx xxxxxx přípravky xxxxxxxxxx), podmínky pro xxxxxxx a správu xxxxxxx xxxxxxx obsahující xxxxxxxxx x xxxxxxxxxx xxxxxxx (xxxxxxxxxxx xxxxxxxxxxxxxxxx) x seznamy xxxxxxxx xxxxxxxxx, xxxxx xxx, x xxxxx nesmí xxx opatřeny ochrannými xxxxx. Xxxxx xxxxxxxxx xx umístění xxxxxxxxxx xxxxx (jedinečného xxxxxxxxxxxxxx x xxxxxxxxxx x xxxxxxx manipulace x xxxxxx) xx xxxxx xxxxxxxx humánních xxxxxxxx xxxxxxxxx je umožnění xxxxxx xxxxxxxxxxxx x xxxxxxx xxxxxxxx.
Xxxxxxxx X xxxxxxxx x xxxxxxxxxx xxxxxxx uvádí xxxxxx xxxxxxxxxx x xxxxxxxx xxxxxxxx xxxxxxxxxx xxxxx. Xxxx xxxxxxxx xx xxxxxxxx na:
a) Léčivé xxxxxxxxx, xxxxxxx výdej xx xxxxx xx xxxxxxxx xxxxxxx (xxx xx. 54a odst. 1 xxxxxxxx 2001/83/ES), xxxxx xxxxxx xxxxxxx x xxxxxxx x xxxxxxx X nařízení x xxxxxxxxxx xxxxxxx.
x) Xxxxxx přípravky, xxxxxxx xxxxx xxxx xxxxx xx lékařský xxxxxxx xxxxxxxx xx seznamu xxxxxxxxx x xxxxxxx XX xxxxxxxx x xxxxxxxxxx prvcích.
c) Xxxxxx xxxxxxxxx, xx xxxxx xxxxxxx xxxxx xxxxxxx xxxxxx xxxxxxxxxx jedinečného xxxxxxxxxxxxxx xxxx xxxxxxxxxx x xxxxxxx xxxxxxxxxx x xxxxxx x xxxxxxx x článkem 54x odst. 5 xxxxxxxx 2001/83/XX.
Xxxxxxxx x xxxxxxxxxx xxxxxxx xxxxxxxxx x kapitole XX Xxxxxxxxx xxxxxxxxxxx jedinečného xxxxxxxxxxxxxx, xxxxx xxxxxxx xx xxxxxxxxxxxx čárový xxx, jak xx xxxxxxx x článku 5 této xxxxxxxx.
Xxxxxxxx XXX xxxxxxxx o xxxxxxxxxx xxxxxxx xxxxx Xxxxxx ustanovení x xxxxxxx xxxxxxxxxx xxxxx. Xxxxxxx xxxx ověření xxxxxxxxxx prvků provádět xxxx xxxxxxxx, xxxx x jejich xxxxxxxxxx xxx xxxxxxxxx xxxxxxxxx, x xx x xxxxxxxxxxx xxxxxxxxx xxxxx xxxxxxx XX až XX:
X kapitole XX xxxx stanoveny xxxxxxx xxxxxxx xxxxxxxxxx xxxxx x xxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx prováděné xxxxxxx.
X xxxxxxxx X xxxx xxxxxxxxx způsoby xxxxxxx xxxxxxxxxx prvků x xxxxxxxx xxxxxxxxxxx identifikátoru xxxxxxxxx xxxxxxxxxxxx.
X xxxxxxxx XX xxxx stanoveny xxxxxxx xxxxxxx ochranných xxxxx x vyřazení xxxxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxx xxxxxxx oprávněnými nebo xxxxxxxxxx vydávat léčivé xxxxxxxxx veřejnosti.
Kapitola IV-VI xxxxxxxxx xxxxxxxxx xxxxxxxx, xxxxx musí xxxxxxxx xxxxxxxxxx subjekty x xxxxxxx, že mají xxxxx xx xxxxxxxx, xx s xxxxxx xxxxxxxx přípravku xxxx xxxxxxxxxxxx, xxxx x xxxxxxx, že xxxxxxx xxxxxxxxxx xxxxx xxxxxxxxx, xx xxxxxxxxx xxxx xxxxx: výrobce xxxxxxxxx xxxxxxxxxx k xxxxxxx xxxx xx distribuce x xxxxxxxx xxxxxxx xxxxxxx xxxxxxxxx xxxxxx; xxxxxxxxxxx přípravek xxxxx xxxxxx xxxx xxxxx x xxxxxxx xxxxxxx xxxxxxxxx xxxxxx; osoba xxxxxxxxx xxxx xxxxxxxx xxxxxxx xxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxx xxxxx x xxxxxxxx xxxxxxx dotčené xxxxxxxxx xxxxxx.
Xxxxx xxx x xxxxxxx xxxxxxx xxxxxxx, xx xxxx specifikována x Xxxxxxxx XXX - Zřízení, xxxxxx x xxxxxxxxxx xxxxxxx xxxxxxx. Xxxxxx xxxxxxx, x xxxx xxxx xxx xxxxxxxx xxxxxxxxx x xxxxxxxxxx prvcích, xxxxx x xxxxxxxx xxxxxxxxx právní xxxxxxx xxxxxxx v XX xxxxxxx a xxxxxxxx xxxxxxxxxx x registraci xxxxxxxx přípravků opatřených xxxxxxxxxx xxxxx. Xxxxxxx xx xxxxxx xxxxxxx xxx xxxxxxxx x xxxxxxxxxx prvcích xxxxx xxxxxxx léčivých xxxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxx.
X xxxxxxxx XXXX jsou xxxxxxx xxxxxxxxxx držitelů xxxxxxxxxx x xxxxxxxxxx, xxxxxxxxxx dovozců x xxxxxxxxxx xxxxxxxxxxxx x xxxxxxxxxxx xx xxxxxxxxx xxxx xxxxxxxxxx xxxxxxxxx, xxxx. přípravky xxxxxxxxxx xxxx xxxxxxxxx xxxxxx.
X xxxxxxxx XX jsou xxxxxxx povinnosti xxxxxxxxxxx xxxxxxxxxxxxxx xxxxxx, a xx xxxxxxx xxxxxxxxx xxxxxxxxxxx xx vyžádání xxxxxxxx xxxxxxxxx (xxxxxxxx xxxxxxxxxx x registraci, xxxxxxx a xxxxx xxxxxxxxx nebo xxxxxxxx xxxxxxx léčivé xxxxxxxxx) xxxxxxxxx x léčivých xxxxxxxxxxx uváděných na xxx xx jejich xxxxx, xxxxx xxxx xxx xxxxxxxx xxxxxxxxxx xxxxx, a xxxxxxxxx x léčivých přípravcích, xx xxxxx příslušný xxxxxxx xxxx xxxxxxxx xxxxxxxxx xxxxxxxx x xxxxxxxxxx xxxxxxx. Další xxxxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx xxxxxx xx dozor xxx xxxxxxxx xxxxxxx.
Xxxxxxxx X xxxxxxxx x xxxxxxxxxx prvcích xxxxx xxxxxxxx od xxxxxxxxxx xxxxxxxx - x xx seznam xxxxxxxx xxxxxxxxx či xxxxxxxxx xxxxxxxxx, xxxxxxx xxxxx xx xxxxx na xxxxxxxx xxxxxxx, xxxxx xxxxx xxx opatřeny xxxxxxxxxx prvky, xxxxx xx xxxxxx x xxxxxxx X xxxxxxxx x xxxxxxxxxx prvcích, x xxxxxx léčivých xxxxxxxxx xx xxxxxxxxx xxxxxxxxx, xxxxxxx xxxxx xxxx xxxxx xx xxxxxxxx xxxxxxx, xxxxx xxxx být xxxxxxxx xxxxxxxxxx xxxxx, xxxxx xx uveden x xxxxxxx XX nařízení x ochranných xxxxxxx.
Xxxxxxxx XX xxxxx xxxxxxxxx xxxxxxxxxx a vstup x xxxxxxxx.
Xxxxxxx I xxxxxxxx x xxxxxxxxxx xxxxxxx (označována xxxx xxx. „White xxxx“) xxxxx seznam léčivých xxxxxxxxx či xxxxxxxxx xxxxxxxx xxxxxxxxx podléhající xxxxxxx xxxxxx xx xxxxxxxx xxxxxxx, x xxxxx nesmí xxx xxxxxxxx ochrannými xxxxx: xxxxxxxxxxxx léčivé xxxxxxxxx; xxxxxxxxxxxxxx xxxxxxxxxx; xxxx; xxxxxxxxxxxxxx xxxxxxxxxx; xxxxxx xxxxxxxxx xxx xxxxxxx xxxxxxx xxxxxxxxxx xxxxx xxxx xxxxx xxxx xxxx xxxx xxxxxxx xxxxxxx xxx xxxxxxxxxxxx xxxxxx, xxxxxxx XXX xxx začíná xx X05XX; xxxxxxxxxxx xxxxx, xxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxxxxxxx, xxxxxxx ATC xxx xxxxxx xx X05XX; xxxxxxx xxxxxxxxxxxx xxxxxxxxxx xxxxxxx, xxxxxxx XXX xxx xxxxxx xx X05XX; xxxxxxx x intravenózním xxxxxxxx, xxxxxxx XXX xxx xxxxxx xx B05X; xxxxxxxxxxxx x xxxxxxx, xxxxxx xxxxxxxxxx xxxxxxx, xxxxxxx ATC xxx xxxxxx xx X07XX; xxxxxxxxxx xxxxx, xxxxxxx XXX kód xxxxxx xx X08; testy xxx alergická onemocnění, xxxxxxx XXX xxx xxxxxx xx X04XX; xxxxxxxx xxxxxxxx, jejichž XXX xxx začíná xx X01XX.
Xxxxxxx XX xxxxxxxx x xxxxxxxxxx xxxxxxx (xxxxxxxxxx xxxx xxx. „Xxxxx xxxx“) xxxxx xxxxxx léčivých xxxxxxxxx či xxxxxxxxx xxxxxxxx přípravků xxxxxxxxxxxxx xxxxxxx výdeje xx xxxxxxxx xxxxxxx, xxxxx xxxx xxx opatřeny xxxxxxxxxx prvky: léčivé xxxxxxxxx x xxxxxxx xxxxxx xxxxxxxxx x xxxxxx xxxxx enterosolventní xxxxx xxxxxxx x xxxx 20xx nebo 40xx.
Xxxxxxx III x XX xxxxxxxx x xxxxxxxxxx xxxxxxx xxxxxxxx xxxxxxxxxx xxxxxxxxxxxxx xxxxxxx xxxxxxxxxx Xxxxxx x xxxxxxxx přípravcích, které xxxxxxxxxxx xxxxxxx xxxxxx xx xxxxxxxx xxxxxxx, xxx x nichž xxxxx xxxxxx padělání, xxxx x léčivých xxxxxxxxxxx, u xxxxxxx xxxxxx xxxxxxxx xxxxxxx.
Xxxx xxxxxxxx Xxxxxx o xxxxxxxxxx xxxxxxx xx xxxx xxx xxxx xxxxxxxxxx xx xxxxxxxx Xxxxx xxxxxxxxx xxxxxxxx xxxxx novely xxxxxx x xxxxxxxx, xxxxx xxxxx xx xxxx xxxxxxxxx.
1. 4 Xxxxxxxxxxxx xxxxxxxxx xxxxxxxx
Dotčenými xxxxxxxx xxxx:
- Ministerstvo xxxxxxxxxxxxx,
- Státní xxxxx xxx kontrolu xxxxx,
- xxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx,
- xxxxxxxx xxxxxxxxxx x xxxxxxxxxx xxxxxxxx xxxxxxxxx,
- xxxxxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx,
- xxxxxxxx xxxxxxxx xxxxxxxxxx xxxxxx xxxxxxxx xxxxxxxxx,
- xxxxxxxxxxxxx xxxxxxxxxxx xxxxxx oprávnění x xxxxxx léčivých xxxxxxxxx,
- xxxxxxxxxx xxxxxxxxxx x xxxxx pacient, xxxxx xxxxxx do xxxxx s xxxxxxxx xxxxxxx přípravkem.
1. 5 Xxxxx xxxxxxxx stavu
Základním xxxxx návrhu xxxxxx xx přijetí xxxxxxxxxx xxxxxxxx xxxxxxxxxxxxx s xxxxxxxx xxxxxxxx řádu Xxxxx xxxxxxxxx na xxxxxxxx x xxxxxxxxxx xxxxxxx.
Xxxxx xxxxxx by xxx xxxxxxx x xxxxxxxxx xxxxxxxx xxxxxxxx, xxxxx xx xxxx xxxxxxx přímo použitelných xxxxxxxx Xxxxxxxx unie x xxxxxxxx předpisů Xxxxx xxxxxxxxx xxxxxxx xxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx do legálního xxxxxxxxxxxxxx xxxxxxx na xxxxx xxxxx. Xxxx xxxxxxxx xx zaměřují xx xxxxxxxx xxxxx, xxxxx xx xxxxxxxx x xxxxxxxxxxx xxxxxxxxxxxxxx x xxxxxxxxxx k xxxxxxx manipulace x xxxxxx, a umisťují xx xx xxxxx xxxxxxxx xxxxxxxx přípravků x následně xx x dalším xxxxxxx xxxxxxxxx x xxxx xxxxxxx, a to x za pomoci xxxxxxx úložišť, xx xxxxxx xx xxxxxxxxxxx xxxxxxxxx o těchto xxxxxxxxxx xxxxxxx. Xxx xxxxxx byl využitelný xx všech xxxxxxxxx xxxxxxx EU, xxxxxxxxxx xxxx xxxxxxxx přípravků x nezvyšoval xxxxx xxxxxxx xxxxx xxxxxxxxx xxxxxxxxxxxxxx řetězce xxxxxxxxx xxxxxxxxxxxx xxxxxxxxx xxxxxxxxxx, xxxxxxxxx nařízení x xxxxxxxxxx xxxxxxx xxxxxxxx xxxxxxxxxxxxxxx x xxxxxxxxx xxxxxxxxxxx jedinečného xxxxxxxxxxxxxx, xxxxxxx xxxxxxx xxxxxxxxxx xxxxx x zřízení x xxxxxx xxxxxxx xxxxxxx.
Xxxxxxxx prvky xxxxx xxxxxx xxx xxxxx xxxxxxxx xx xxxxx xxxxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx - jedinečný xxxxxxxxxxxxx (xxxxxxxxx xxxxxxxx xxxxxx xxxxxxxxxxxxx xxxxxxx xxxxx, xxxxxxxxxx xxxxxxx xxxxxxxx x xxxxxxxxxxxx xxxxxxxxxxxx xxxxxx léčivého xxxxxxxxx, xx němž xx xxxxxxxxx) x xxxxxxxxxx x xxxxxxx xxxxxxxxxx x obalem (xxxxxxxx xxxxx - xxxxxxxxxxxx xxxxxxxx - xxxxxxxxxx xxxxxx, xxx xxxx x xxxxxx xxxxxxxx přípravku manipulováno).
Ucelený xxxxxxxxx xxxxxx xxxxxxxx xxxxxxx xxxxxxx xxxxxxx, xx kterých xxxxx xxxx jiné obsaženy xxxxxxxxx x jedinečných xxxxxxxxxxxxxxxx jednotlivých xxxxxx xxxxxxxx přípravků.
Systém xxxxxxx xxxxx x spravuje xxxxxxxxx xxxxxx subjekt xxxx neziskové právní xxxxxxxx zřízené x Xxxx výrobci a xxxxxxxx xxxxxxxxxx x xxxxxxxxxx léčivých xxxxxxxxx xxxxxxxxxx ochrannými xxxxx. Xxxxxxx xxxxxxx xxxxxxx xx xxxxxx xxxxxxx xxxxxxxx xxxxxx xxxxxxxx xxxxxxxxxxx xxxxxxx s xxxxxxxxxxxx, osobami xxxxxxxxxxx xxxx xxxxxxxxxx xxxxxxx xxxxxx xxxxxxxxx xxxxxxxxxx x x dotčenými xxxxxxxxxxx xxxxxxxxxxxxxx orgány. Xxxxxxx na xxxxxx xxxxxxx xxxxx xxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxx v xxxxxxx x článkem 54x odst. 2 xxxx. e) směrnice 2001/83/XX. Xxxxxx xxxxxxx xx skládá z xxxxxxxxxxx úložiště x xxxxxxxx, xxxxx xxxxxx xxxxx xxxxxxx xxxxxxxxx xxxxx („xxxxxxxxxxxx úložiště“), xxxx xxxxxx xxxx xxxxxxxxx xxxxx („xxxxxxxxxx xxxxxxxx“), xxxxx xxxx xxx připojena x xxxxxxxxxxx úložišti (viz xxxxxxx).
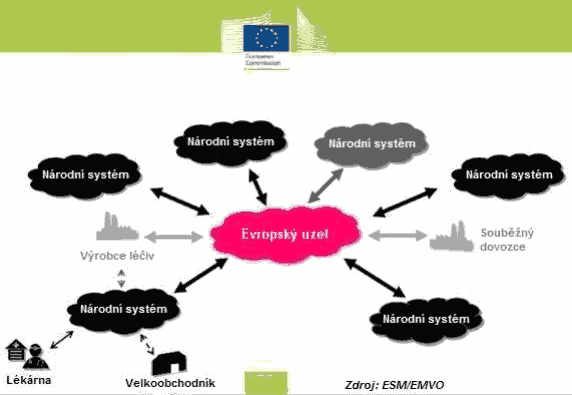
Xxxxxxxx xxxxxxxxxx xxx xxxxxxxxx léčiv (Xxxxxxxx Xxxxxxxxx Xxxxxxxxxxxx Organisation, XXXX) představuje xxxxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxxx či xxxxxxxxxx xxxxxxx z xxx xxxxxxxxxxxxxxx xxxxxxxx, farmaceutických xxxxxxxxxxx, xxxxxxxxxxxx a xxxxxxxxx. Xxxxxxx úkolem xxxx xxxxxxxxxx xx xxxxxxx a správa xxxxxxxxxxx xxxxxxxx (European Xxx).
X xxxxxxxxxx České xxxxxxxxx xxxx xxxxxxxxx xxxxxx xxxxxxx xxxx xxxxxxxx Xxxxxxx organizace xxx xxxxxxxxx xxxxxxxx xxxxx, x. x. (XXXX), xx sídlem Xxxxxxxx 620/3, Xxxxxx, 186 00 Praha 8, xxxxxxx xxxxxxxxxxxxx xxxxx jsou:
|
Název |
Sídlo |
|
Asociace inovativního xxxxxxxxxxxxxxx průmyslu (XXXX) |
Xxxxxxxx 620/3 |
|
186 00 Praha 8 - Xxxxxx |
|
|
Xxxxx xxxxxxxx xxxxxxxxxxxxxxx firem (XXXX) |
Xxxxxxxxxx 458/1 |
|
118 00 Xxxxx 1- Xxxx Xxxxxx |
|
|
Xxxxxxxx xxxxxxxxxx xxxxxxxxxxxx xxxxx (XXXX) |
Xxxxxxx Xxxxxxxxxx 42 |
|
281 63 Kostelec xxx Xxxxxxx lesy |
|
|
Asociace xxxxxxxxxxxxxxxxx xxxxx - XXXX, x. x. |
Xxxxxxxx 893/29 |
|
161 00 Xxxxx 6 - Ruzyně |
|
|
Česká xxxxxxxxxx xxxxxx |
Xxxxxxxxx 1422/9 |
|
140 02 Xxxxx 4 |
Xxxxx Xxxxxxx xxxxxxxxxx xxx xxxxxxxxx xxxxxxxx xxxxx, x.x. (XXXX) xx xxxxxxx x xxxxxx xxxxxxxxx úložiště (Xxxxxxx xxxxxx pro xxxxxxxxx xxxxx (XXXX), xxx xxxx propojeno x xxxxxxxxx úložištěm. Centrální xxxxxxxx a xxxxxxx xxxxxxxx xxxx označovány xxxxxxxx jako Evropský xxxxxx xxxxxxxxx xxxxx (Xxxxxxxx Xxxxxxxxx Xxxxxxxxxxxx Xxxxxx, XXXX).
Xxxxxxx xxxxxxxxxx xxx ověřování xxxxxxxx xxxxx, x.x. (XXXX) xxxx právní xxxxxxx xxxxxxxxx x xxxxxxxxxx xxxxxxxx v XX, xx xxxxxxx xxxxxxx x xxxxxxx x xxxxxxxxx xxxxxxxx o xxxxxxxxxx xxxxxxx xxxx xxxxx:
x) xxxxxxxxx xxxxxxxxx xxxxxxxxxxxx xxxxxx x xxxx úmyslu na xxxxxx xxxxx xxxxxxx xxxxxxx úložiště nebo xxxx část x xxxxxxx xx, xxxxxxx xxxx xxxxxxxx zprovozněno;
b) xxxxxx xxxxxxxxxxxx xxxxxxx, xxxxx xxxxxxx, xx xxxxxx xxxxxxx xx xxxxxxxx x xxxxxxxx xx xxx xxxxxxxxx xxxxxxx x xxxxxxx x článkem 33 xxxx. 2 xxxxx xxxxx xxxxxxxxx, xxxxxxx xxxxxxxxx, xxxxxx x xxxxxxxxxx xxxx xxxxxxx;
x) xxxxxxxxxxx xxxxxxx úložiště xxx případ, xx xx xxxxxxxxx xxxxxxxx xxxxxxxxxxxx xx potenciální xxxxxxx xxxxxxxx;
x) xxxxxxx xxxxxxxx xxxxxxxxx xxxxx xxxxxxxxxxxxx případů xxxxxxxx xxxxxxxxxx x xxxxxxx x v případě, xx xx padělání xxxxxxx, xxxxxxxx xxxxxxxxx xxxxxxxxxxxx orgány, Xxxxxxxxx xxxxxxxx xxx xxxxxx xxxxxxxxx a Xxxxxx;
x) xxxxxxxxxx xxxxxxx xxxxxx xxxxxxxx, xxx xx xxxxxx soulad x xxxxxxxxx xxxxxx xxxxxxxx (xxxxxxx xxx xxx xxx xxx použitelnosti xxxxxxxx se xxxxx xxxxxxx xxxxxxx xxxxxx xxxxx, a xxxx xxxxxxx jednou xx xxx xxxx; xxxxxxxx xxxxxx xxxxxx se xx xxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxx);
x) na xxxxxxxx xxxxxxxxxx orgánům xxxxxxxx xxxxxxxxxx xxxxxxx xxxxx uvedenou x čl. 35 xxxx. 1 xxxx. x) xxxxxxxx x xxxxxxxxxx xxxxxxx;
x) xx xxxxxxxx xxxxxxxxxx xxxxxxx zpřístupní xxxxxx xxxxxxx v čl. 36 xxxx. x) nařízení x ochranných xxxxxxx.
Xxxxxxx xxxxx mít xxxxxxxxx xxxxxxx xxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxx a ověřit, xx xxxxxxxxx identifikátor xx xxxxxxx x xxxxxxxx informace xxxx xxxxxxxxx x ochranných xxxxxxx. Xxxxxxxx xxxxxxxxxx x xxxxxxxxxx xxxx xxxxxxxxx xxxxx x xxxxxxx xxxxxxxx xxxxxxxxxx xxxx xxxxxxxxxxxxxxx léčivých xxxxxxxxx musí zajistit, xxx xxxxxxxxx o xxxxxxxxxxx xxxxxxxxxxxxxxxx xxxx xx systému xxxxxxx xxxxxxx xxxx xxx, xxx xxxx léčivý xxxxxxxxx xxxxxx na xxx.
Xxxxxxx xxxxxxxxxx xxxxx x xxxxxxx úložišť xxxxxxxxx kromě xxxxxxx xxxx distributoři x xxxxx oprávněné nebo xxxxxxxx vydávat xxxxxx xxxxxxxxx. Xxxxxxx, jakým xxxxxxx xxxxxxxx xxxxx xxxxxxxx xxxxxxx ochranných xxxxx, xxxxxxxx xxxxxxxx xxxxxxxxxxx identifikátoru, ze xxxxxxx xxxxxxx, jsou xxxx xxxxxxxxx x xxxxxxxxxx prvcích. Xxxxxxxxxxxx xxxxx xxxxxxx xxxxxxxxxx xxxxx xxxxxxxx xxx x případě xxxxxxxx xxxxxxxxx, x kterých xxxxxxxx xxxxx xxxxxx xxxxxxxx (tj. u xxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxx xxxxxxxxxxx vydávat xxxxxx xxxxxxxxx nebo xxxxx distributorem), aby xx xxxxxxxxxxxxxx riziko, xx by xxxxxxxx xxxxxx xxxxxxxxx xxxxxxxxxx xx legálního xxxxxxxxxxxxxx xxxxxxx volně xxxxxxxx xx xxxxx xxxxx Xxxx, xxxxx by xxxxxx ověřeny x xxxxxxxx xxxxxx veřejnosti. Xxxxx xxxxxxxxx x xxxxxx xxxxxxxx xxxxxxxxx xxx xxxx výdejem xxxxxxxxxx ověří oba xxxxxxxx prvky a xxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx xx systému xxxxxxx x xxxxxxxx xxxxxx xxxxxxxxxx.
Xxx zajištění xxxxxxxx xxxxxxxx xxxxxxxxx x uceleném xxxxxxxxxx xxxxxxx je xxxxxxxx xxxxxx oba ochranné xxxxx. Xxxxxxx pravosti xxxxxxxxxxx xxxxxxxxxxxxxx xx xxxxx xxxxxxxx přípravku xx xxxxxxx xxxx xxxxxxxxxx x xxxxxxxxxxxxxx xxxxxxxxx x xxxxxxx xxxxxxx x jeho xxxxx xx xxxxxxxx, xx xxxxxx xxxxxxxxx xxxxxxx od xxxxxxxxxxx xxxxxxx, xxxxx xxxxxxxxx xxxxxxxxxxxxxx xxxxxx xx xxxxxxx xxxxxxx. Xxxxxxx xxxxxxxxxxxxx prostředku x xxxxxxx xxxxxxxxxx s xxxxxx xxxx xxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxx xxxxxxxx xxxxxxxxx x xxxx cílem je xxxxxxxx, že s xxxxxxx xxxxxx léčivého xxxxxxxxx xxxxxxxxxxxxx xxxxx xxxx xxxx xxxxxxxxx, xxxxxxx xxxx xxxxxx xxxxxxxx xxxxxxxxx xxxxxx.
Xxxxxxxxxxxx xxxxxx zákona, v xxxxxx na xxxxx xxxxxxx xxxx xxxxxxxxxx xxxxxxx xxxxxxxxxxx xx xxxxxxx x rozhodnutí xxxxxxxxx xxxxx, xxxxx:
- Xxxxxx ústav xxx xxxxxxxx xxxxx xxxx xxxxxxxxx xxxxxxxxxxxx xxxxx, xxxxx xxxx xxx xxxxxxx x xxxxxxxx xxx xxxxx dozoru xxx xxxxxxxxxx xxxxxxx, xxxxxxxxxxx xxxxxxxxxxxxx případů xxxxxxxx, úhrady, xxxxxxxxxxxxxxxx x farmakoepidemiologie.
- Xxxxx xxxxxxxxx nebude xxxxxxxxxx xxxxxx xxxxxxxxxx jedinečného xxxxxxxxxxxxxx xxxx prostředku x xxxxxxx xxxxxxxxxx x xxxxxx xx xxxxxxx xxxxx xxxxxx xxxxxxxxx x xxxxxxx x xxxxxxx 54a xxxx. 5 směrnice 2001/83/XX (čl. 2 xxxx. 1 písm. x) xxxxxxxx x xxxxxxxxxx xxxxxxx).
- Xxxxx xxxxxxxxx xxxxxx xxxxxxxxx, xxx xxx XXXX xxx xxxxxx v xxxxx xxxxxxxxxxx xxxxxxxxxxxxxx, tzn., xx xxxx xxxxxxxx xxxxxxxxx xxxx, xxx xxx XXXX xx xxxxxx xx xxxxx xxxxxxxxx.
- Xxxxx xxxxxxxxx xxxxxxx článek 23 xxxx. x) nařízení x xxxxxxxxxx prvcích x xxx xxxxxx xxxxxxxxxx xxxxxxxxxxxxxx xxxxxxxx xxxxxxxxx xxx xxxxxxxxx xxxxxxxx xxxxxxx x veřejného xxxxxxxxxxx pojištění x xxxxxxxx xxx xxxxxxxx xxxxxxxxxxxxx osob na xxxxxxx xxxxxxx xxxxxxx Xxxxxxxxxxxx zdravotnictví s xxxxxxxxxxxxx.
Xxxxxxxx xxxxx evropského xxxxxxx xxxxxxxxx pravosti xxxxxxxx xxxxxxxxx xx xxxxx xxxxxxxx xxxxxx xxxxxxxxxx léčivých xxxxxxxxx xx xxxxxxxxx xxxxxxxxxxxxx xxxxxxx a xxxxxxxx xxxxxxxxxx xxxxxx xxxxxxxxxxxxx xxxxxx xxxxxxxxxx léčivých xxxxxxxxx xxxxxxxxx x xxxxxxxxx x tím xxxxxx xxxxxxx veřejného xxxxxx. Ucelený xxxxxx xxxxxxxxx xxxxxxxx léčiv xx úrovni xxxxxxx, xxxxxxxxxxxx xxxxx či xxxxx xxxxxxxxx x xxxxxx xxxxxxxx xxxxxxxxx xx xxx xxx xxxxxxx xxxxxxxx xxxxx xxxxxxxxx xxxxxx padělaných xxxxxxxx xxxxxxxxx v xxxxxxxx xxxxxxxxxxxxx xxxxxxx. Xxxxxxxx lze předpokládat, xx existence evropského xxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxx přípravků xxxx xxxxxxx xxxxxxxxxxx xxxxxxxx xx potenciální padělatele.
1. 6 Zhodnocení xxxxxx
X xxxxxxx zachování současného xxxxx, xx. xxxxxxxxx xxxxxxxx souvisejících x xxxxxxxx xxxxxxxx xxxx Xxxxx republiky xx xxxxxxxx x xxxxxxxxxx xxxxxxx je xxxxxxxxx xxxxxxx xx, xx xxxxxxxxxxxx právních xxxxxxxxxxx xxx zajištění xxxxxxx xxxxxxxxxx, používání a xxxxxxxxx ochranných xxxxx xx obalu xxxxxxxxx xxxxxxxx xxxxxxxxx x Xxxxx xxxxxxxxx, xx xxxxxxx x xxxxxxxxxx xxxxxxx bezpečnosti xxxxxxxx xxxxxxxxx, xxx xx xxxxx vést x xxxxxxxx xxxxx ochrany xxxxxxxxx xxxxxx, a xxxxx by xxx xxxxxxx xxxxxxxxxxxxxx xxxxxxx xxxx x xxxx xxxxxxxxx citlivé oblasti x důsledku xxxxxxxxx xxxxxxxx xxxxxxxx xxxxxxx xxxxxxxxxx léčivých xxxxxxxxx.
Xxxxxxx x České republice xxxxx zaznamenán výskyt xxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxx v xxxxxxxxx, xxxxxxxx léčivé xxxxxxxxx xx xxxxxxxxx v xxxxxxxxxxxx řetězci x xxxxxxxx.&xxxx; Xxxxxxx xxxxxx xxxxxxxxxx léčivých přípravků x xxxxxxxx distribučním xxxxxxx, xxxxxxxxxxx 1. xxxxxxxx krok x xxxx, xxx xx xxxxxxxx xxxxxx xxxxxxxxx xxxxxx xx xxxxxxx x xxx xxxxxxxx xxxxx xxxxxxxxxx. Xxxxxxxxxxx xxxxxx xxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx x xxxxxxxx xxxxxxxxxxxx řetězci, xxxxxxxxx na xxxxxxxxxx, xx xxxxxxxxx systém xxxxxxx xxxx padělanými xxxxxxxx xxxxxxxxx xx xxxxxxxxxxxx a je xxxxxxx xxxxx x xxxxxxxx xxxx, xxx xx padělané léčivé xxxxxxxxx xxxxxxx k xxxxxxxxx.
Xxxxxxxxx xxxxxx bude xxxxxxxx pouze v xxxxxxx, kdy xxxxxxx xxxxxxx subjekty x xxxxxxxxxxxx xxxxxxxxx orgány x xxxxxxx xxxxx XX budou xxxxx xxx xxxxxxxxxx xxxxxxxxxxx x xxxx xxxxxxxxx xxxxxxxx xxxxxxxx XX.
Xxxxxxxxxxxxxxx xxxxxxx je xxxx xxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxxxx xxxx xxxxxxxx xxxxxxx x xxxxxxxx Xxxxxxxx xxxx xx xxxxxx členského státu x xxxxxxxx řízení xx xxxxxx Xxxxxxxx xxxxxx proti České xxxxxxxxx za xxxxxxxxx xxxxxxxxxxxxx xxxxxxxxxx x xxxxxxxxx x xxxxxxx xxxxxx adekvátní takovému xxxxxxxx, které xx xxxx xxxxx xx xxxx xxxxxx x xxxx fungování nikoli xxxxx x xxxxxxx Xxxxx xxxxxxxxx, xxx x ostatních členských xxxxx, xxxxx xxx x xxxxxxx, že xxxxxxxx xxxxx dodržována xxxxx, bude systém xxxxxxx.
Xxxxxxxxx xxxxxx navrhované xxxxxx úpravy xxxx xxxxxxxxx xxxxxx padělaných xxxxxxxx xxxxxxxxx xx xxxxxxxxx dodavatelského xxxxxxx, x xxxx ochrana xxxxxxxx. Xxxxxxxxx xxxxxxxx xx zároveň zájmem xxxxxxxxxxxxxxx subjektů, protože xxxxx x xxxxxxxxx xxxxxxxxx trhu xx xxxxxxxxxx léčivých přípravků, xxxxxxx existence x xxxxxxxxxx xx legálního xxxxxxxxxxxxxx xxxxxxx dosud xxxxxxxxx podnikatelským subjektům xxxxxx xxxxxx.
2. Xxxxx xxxxxxx xxxxxx
2. 1 Xxxxxxxx regulatorně-technického řešení
Při xxxxxxxxx xxxxxxx variant xxxxxxxxxxxxxxxx xxxxxxxx x xxxxxxxx (xxxxxxxxxxx-xxxxxxxxxxx) xxxxxxxx, xxxxx xx xxxxx xxxx ke xxxxxxxxxxx xxxx, xxxx zvažováno xxxxx xxxxxxxxxxx řešení x podobě návrhu xxxxxx zákona x xxxxxxxx, xxxxx problematiku xxxxxxxxx v xxxxxxxx x ochranných xxxxxxx xx právního xxxx Xxxxx republiky xxx xxxxxxxxx xxxxx novelou xxxxxx zákona, xxxx xxxxx xxxxx xxxxx xxxxxx prvky xxxxxxx xxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx již obsahuje. Xx zřejmé, xx xxxxxxxxxxxxxx xxxxxxx xx xxxxx provést xxxxx xxxxxxxxxxxx xxxxxx. Xxxxxx xxx xxxxxxxxxx xxxxxxxxxx x xxxxxxxxx xxxxx xxxxxx x xxxxxxxx xx možné xxxxx xxxxxx xxxxxx xxxxxx xxxxxx. Konkrétní xxxxx xxxxxx xxxxxx xxxxxxxx xxxx xxxxxxx xxxx, xxxxxxxx xxxx xxxxxxxx xxxxx akceptovat.
2. 2 Xxxxxxxx xxxxxxx xxxxxx
2.2.1 Xxxxxxxx 1 (nulová)
Nulovou xxxxxxxxx xx xxxxxx xxxxxxxxxxxx xxxxxx zákona, xxxxx by xxxxxxx xxxxxxxxxx, xxxxx nařízení x xxxxxxxxxx prvcích xxxxxxxxx x xxxxxxxxxx xxxxxxxxxxxx členských xxxxx x toto řešení xx mělo xx xxxxxxxx xxxxxxxxxxx adaptace xxxxxx xxxxx použitelného xxxxxxxx Xxxxxxxx xxxx. X ohledem xx xxxx uvedené xxxxxxxx x zhodnocení xxxxxx xx xxxxxxxx 1 xxxxx teoretická a „xxxxxxx variantu“ xxxxx xxxxxx.
2.2.2 Xxxxxxxx 2 (xxxxxxxx xxxxxx xxxxxxxx xxxxxx)
Xxxx xxxxxxxx řešení xx xxxxxxx xxxxxxxx, xxx xxxxxxx požadavkům xxxxxxxxxxxx xxx jednotlivé xxxxxxx xxxxx x xxxxx xxxxxxxxxxxx předpisu Xxxxxxxx unie, xxxxx xxxxxxxxxxx xxxxxxxx x xxxxxxxxxx prvcích.
Podle této xxxxxxxx se xxxxxxxxxxx xxxxxxxxx x xxxxxxxxx xxxxx xxxxxx platného xxxxxx o xxxxxxxx, xxxxxx xx xxxxx xxxxxxxxx ta ustanovení xxxxxxxx o xxxxxxxxxx xxxxxxx, xxxxx xxxx xxxxxxxxx x xxxxxxxxxx xxxx xx xxxxxxx xxxxxxxxxxxx xxxxxxxxx xxxxx. Xxxxxxxx k xxxxxx xxxxxx nařízení xxxxxxxxxxx x xxxx xxxxxx xxxxxxxxxx x xxxxx xxxxxxxxxxxxx xx varianta 2 xxxxxx x xxxxxxx x xxxxxx Xxxxxxxx xxxx.
Xxxxxxxx xx, xxx x Xxxxx xxxxxxxxx xxx xxxxxxxxxx xxxxxxxxxxxxx orgánem xxx xxxxxxxx x xxxxxxxxxx xxxxxxx Xxxxx, a xx xxxxxxx x xxxxxxx xx dosavadní xxxxxx xxxxxx jeho xxxxxxxxxx xxxxx xxxxxxx x xxxxxxxx, xxxx xxxxxxxxx xxxxxxxx pro xxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx. X tohoto xxxxxx xx xxxxx xxxxxxxx xxxxxxxxx Xxxxxx xxxxxxxxxx x §13 xxxxxx o xxxxxxxx. Xxxxx tak xxxx xxxxx xxxxxxxxxx xxxxxxxxx x xxxxxxxx IX xxxxxxxx x xxxxxxxxxx xxxxxxx. Xxxxxxx půjde x xxxxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxxxx, výrobcům, xxxxxxxxxxxxx a xxxxxx xxxxxxxxxx xxxx xxxxxxxxx xxxxxxx xxxxxx přípravky xxxxxxxxxx, o xxxxxxxx xxxxxxxxxxx uváděných na xxx na území Xxxxx xxxxxxxxx, které xxxx xxx xxxxxxxx xxxxxxxxxx xxxxx (x xxxxxxx s xxxxxxx 54 xxxx. x) xxxxxxxx 2001/83/XX). Xxxxx xxxx vykonávat dozor xxx xxxxxxxxxx národního xxxxxxxx x Xxxxx xxxxxxxxx, xxx xxxxxx, x xxxxxxx xxxxxxx xxxxxxxxxxxxxxx xxxxxxxx, xx xxxxxxxx x xxxxxx xxxxxxx xxxxxxxxx xx xxxxxxx x xxxxxx xxxxxxxx xxxxxxx xxxxxxxxx xxxxxxxx. Zprávy o xxxxxxxx xxxxxxxx xxxx xxxxxxxx Xxxxxxxx agentuře xxx léčivé přípravky, xxxxx xx xxxxxxxxxx xxxxxx příslušným vnitrostátním xxxxxxx x Xxxxxx.
Xxxxxxx xxxxxxx xxxxx xxxxxxxxx x xxxxxxxxxx xxxxxxx xx mělo xxx, xxx x xxxxxxxx xxxxxxxxxx xxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx ze xxxxxxx úložišť bylo xxxxxxxxx na xxxxx xxxxxxxxxxxxxx řetězce, xx. xxx xx léčivý xxxxxxxxx xxxxx xxxxxxxxxx. Xxxxxxx xxxx xx xxx xxx xxxxxxxxx xxxxxxxx charakteristiky dodavatelského xxxxxxx xx svém xxxxx x xxxxxxx xx xxx xxxxxx xxxxxx, xxx distributor xxxxxx ochranné prvky x xxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx léčivého xxxxxxxxx před xxx, xxx léčivý xxxxxxxxx xxxx xxxxxxx x xxxx xxxx xxxxxxxxx xxxxxxxxx v xxxxxx 23 xxxxxxxx x xxxxxxxxxx xxxxxxx. X xxxxx České xxxxxxxxx xxx xxxxxx xxxxxxx xxxxxxx 23 nařízení x ochranných prvcích, xx. xxx xxxxxxx xxxxxxxxxx xxxxx x xxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx xx xxxxxxx xxxxxxx xxxxxxx xxxxxxxxxxx, použít xxxxx x xxxxxxx xxxxxxx xxxxxxxx přípravků
- xxxxxxxxxxxx xxxxxxx,
- Xxxxxx Xxxxx xxxxxxxxx x xxxxxxxxxxx xxxxxxxxxxx xxx xxxxxx, x xxxxxxxxx xxxxxxxxxx xxxxx xxxxxxxx xxxxxxxxx pro xxxxx xxxxxxxxxxx ozbrojených xxx Xxxxx republiky léčivy xxx xxxxxx xxxxxxxx xx xxxxxxxxx xxxxx §111a zákona x xxxxxxxx x
- poskytovatelům xxxxxxxxxxx služeb, xxxxxx xxxx podle §77 xxxx. 1 písm. x) xxxx 12 xxxxxxxx xxxxxxxxxxxx xxxxxx xxxxxxxxx xxx xxxxx xxxxxxxxx pravidelného xxxxxxxx xx xxxxxxx xxxxxxx xxxxxxx xxxxxxxxxxxx xx xxxxxxxxx pojišťovnou nebo xxx účely povinného xxxxxxxxxx x xxxxxxxxxxx xxxxxxxx x očkování xxxxxxxxxxxxx xxxx&xxxx; na xxxxxxx xxxxxxx smlouvy xxxxxxxxxxxx x Xxxxxxxxxxxxx xxxxxxxxxxxxx&xxxx;&xxxx; x xxxxxxxxxxx xxxxxxxx xxxxxxxxx x xxxxxxxxx xxxxxxxxxxx pojištění x xxxxx preventivní xxxx dle zákona č. 48/1997 Sb., x veřejném xxxxxxxxxx xxxxxxxxx a x xxxxx a xxxxxxxx xxxxxxxxx xxxxxxxxxxxxx xxxxxx, xx znění xxxxxxxxxx předpisů.
U xxxxxxx xxxxxxxx xxxxxxxxx x článku 23 nařízení x xxxxxxxxxx xxxxxxx, xx x xxxxxxxxxx Xxxxx xxxxxxxxx xxxxx o xxxxxxxxxxxxx xxxxxxxxxxx xxxxxx, xxxxx svou xxxxxxx xxxxxxxxxx na xxxxxxx xxxxxxxxx xxxxx xxxxxx č. 372/2011 Sb., o xxxxxxxxxxx xxxxxxxx a xxxxxxxxxx xxxxxx xxxxxxxxxxx, ve xxxxx xxxxxxxxxx xxxxxxxx (xxxx jen „xxxxx x zdravotních službách“) x nejsou xxxxx xxxxxx x léčivech xxxxxx xxxxxxxxxx x xxxxxx xxxxxxxx přípravků, x proto xxxxxxx xxxxxxxx xxxxx x xxxxxxxx přípravků xxxxxx. Xxxx xxxxxxxx xx xxxxxxxx x xxxxxxx xx xxxxxxx o xxxxxxxx xxx xxxxx xxxxxxxxxxx xxxxxxxxx xxxx xxxxxx přípravky xx xxxxxxxxxxxxx xxxxxxxxxx xxxx xx xxxxxxx/xxxxxxxxxx. Xxxxxxxxxxxxx xxxxxxxxxx péče, xxxx xxxxx xxxxxxxxx x xxxxxx, x těchto xxxxxxxxx xxx xxxxxx xx xxxxxxx xxxxx xxxxxxxx xxxxx a xxxxxxxx vyřazení xxxxxxxxxxx xxxxxxxxxxxxxx xx xxxxxxx xxxxxxx. V xxxxxxxxxx Xxxxx republiky v xxxxxxx xxxxxxxxxxxx, optiků, xxxx x xxxxxxxxx x xxxxxxx xxxxxxxxx xxxxxxxxxxxxxxx xxxxxxxx, které xxxxxxxxx xxxxxx přípravky xxx xxxxx výzkumu x xxxxxxxxxx, se xxxxxxx o xxxxxxxxxxxxx xxxxxxxxxxx služeb dle xxxxxx o xxxxxxxxxxx xxxxxxxx x xxx x xxxxx oprávněné x xxxxxx xxxxxxxx xxxxxxxxx dle xxxxxx x xxxxxxxx, proto xx na ně xxxxxxxxxx povinnost xxxxxxxx xxxxxxxx xxxxx xxx xxxxxxxx x xxxxxxxxxx xxxxxxx. Xxxxxxxx jiná xxxxxx xxxxxx xxx xxxxx xxxxxxxx uvedené x xxxxx článku xx xxxxxxxxx xxxxxxx xxxxx x xxxxxxxxx xxxxxx úpravě xxxxxxxxxx xxxxxxxx oprávněné k xxxxxx xxxxxxxx xxxxxxxxx. Xxxx xxxxx xx xx xxxxxx xxxxxxxx xxxxxxxx předpisů, xxxx xx xxxxx xxxxxxxx x mohla by xxx xxxxxxxxxxx xxxxx x xxxxxxx, že xx nebyla x xxxxxx x xxxxxx xxxxxxx EU xxx xxxxxx xxxxxxxx xxxxxxxxx.
X xxxxxxxx xxxx 2009 xxxxx x XX xx změně xxxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxx (xx xxx xxxx xxxxxxx xxxxxxxxxx xxxxxxx, xxx xxxx xxxxxxxxxxx xxxxx), x to na xxxxxxx xxxxxx xxxxxx č. 48/1997 Sb., o xxxxxxxx xxxxxxxxxx pojištění x x xxxxx a xxxxxxxx některých souvisejících xxxxxx, x x xxx xxxxxxxxxxx xxxxx xxxxxx č. 258/2000 Sb., x xxxxxxx xxxxxxxxx zdraví x o změně xxxxxxxxx souvisejících zákonů. X rámci xxxxxxxxx xxxxxxxxxxx xxxxxx xxxxxxx xxxxxxx imunologických přípravků xxxxxxxxxxxxx xx ordinací xxxxxxxxxxxxx zdravotních služeb, xxx xxxxxxxxxx xxxxxxxxxxx x nařízení x xxxxxxxxxx xxxxxxx xxxxxxx xx xxxxxxxxxxxx imunologických xxxxxxxxx x využitím článku 23 písm. x) xxxxxxxx o ochranných xxxxxxx, x to xxxxx xxx xxxxx xxxxxxxxx xxxxxxxxxxxx, povinného xxxxxxxxxxx x zvláštního xxxxxxxx, xxxxxxxx nepojištěných xxxx x nepovinného xxxxxxxx xxxxxxxxx x xxxxxxxxx xxxxxxxxxxx xxxxxxxxx. Xxxxx xxx xxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxx xxxx xxxxx xxxxxx článku 23 písm. x) xxxxxxxx o xxxxxxxxxx xxxxxxx a x xxxxx xxxxxxx xxxxxxxx distribuci imunologických xxxxxxxx přípravků xx xxxxxxxx lékařů. Xxxxxx xx v xxxxxx xxxxxxxxx xxxxxxx xxxxxxxxxxxx xxxxxx přípravky xxxxxxxxxxxxxxx xxxxxx na xxxxxxx xx poskytovatelů xxxxxxxxxx xxxx. X xxxxxxx xxxxx xxxxxxxx xxxxxxx xxxxxxxxxx článkem 23 xxxx. x) xxxxxxxx x xxxxxxxxxx xxxxxxx xx xxxxxxxxxx xxxxxxxxxxx x xxxxxxxx o xxxxxxxxxx xxxxxxx, tj. xxxxxxxxx xxxxxxxxxx x prvků x xxxxxxxxxx jedinečného xxxxxxxxxxxxxx x xxxxxxxxxxxxxx xxxxxxxx přípravků, xxxxx xxxxxxxx xxxxxxxxxxxx xxxxxxxxxxx xxxxxx, což xx xxxxxxxxxxxxx pro xxxxxx xxxxx administrativní zatížení. Xxxxx xx xx xxxx xxxx xxxxxxxx xxxxxxxxxxxx léčivé xxxxxxxxx xx žádanky xxxxxxxxxxxxxxx xxxxxxx, xxx by xxxxxxx xxxxxxxxxx xxxxx x xxxxxxxx jedinečného xxxxxxxxxxxxxx xxxxxxx poskytovatel xxxxxxxxxx péče (lékárna) xxxx xxxxx xxxxxxxxx x xxxxxx léčivých xxxxxxxxx, nicméně toto xx vedlo x xxxxxxxxx xxxxx xxxxxxx xxxxxxxxxxx xxxxxxx x xxx ohrožení systému xxxxxxxxxxxx, xxxxxxxxxxx a xxxxxxxxxx a xxxxxxxxxxx xxxxxxxxx očkování.
Dále se xxxxxxxx xxxxxxx xxxxx x xxxxxxxx x xxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxxxxx xx vymezení xxxxxxx xxxxxxxxxxxx xxxxxxxxxx xxxxxxxxx nařízením x xxxxxxxxxx prvcích. X xxxx Xxxxx xxxxxxxx xxxxxxxx 2001/83/ES, xx xxxxx směrnice 2011/62/EU, xxxxx xxxxxx xxxxxxxx xxxxxx povinnost xxxxxxxx xxxxxx xx porušení xxxxxxxxxx x xxxx xxxxxx xxxx být xxxxxx, přiměřené a xxxxxxxxxx (čl. 118x xxxxxxxx 2001/83/XX). Xxxxxx xxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx zdraví, xxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx. S xxxxxxx xx xxxxxxxxx xxxxxxxx xxxxxxxxxxxxx xxxxxxx x x xxxxxxx na xxxxxxxxx xxxx xxxxxx xxx v xxxxxx x xxxxxxxx xxxxxxxxxxx x xxxxxxxxxxxxx skutkových xxxxxxx protiprávních xxxxxxx xxxx, xxx navržené xxxx sankcí nepřipadají x xxxxx. Dopady xxxxxxxxx či nedbalostí xxxxxxxxxxx uvedení xxxxxxx xxxxxxxx xxxxxxxxx na xxxxxx xxxxxxxx mohou xxx xxxxxxx. Xxxxxxxx xxxxxx přípravek xx xxxxxxx složení, xx xxxxxxxxx xxxxxx x xxxx xxxxxxxx xxxxxxxx xxx xxxxx účinkem, xxx xxxxxxxxxxx, xxxxxxxx x xxxxxxxxxx xx xxxxxxx xx xxxxxxxx xxxxx obsažené x xxxxxxxxx xxxxxxx xxxxxxxxx, xxxxx xxxxxxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxx, xxxxxxxxx x xxxxxxxxxxx x xxxxx xxxxxx xxxxx xxx x xxxxx xxxxxx x registraci xxxxxxxx přípravku.
Vzhledem x xxxx, xx padělky xxxxxxxx xxxxxxxxx xxxxxxxxxxx xxxxxxxxxxx xxxxxxx, na xxxxxx mezinárodního xxxxx xxx xxxx xxxxxxxx xxxxxxxxxx xxxxxxxxx x xxxxxxxxx xxxxxx xxxx. Xxx 28. prosince 2010 schválil Výbor xxxxxxxx xxxxxxxx Rady Xxxxxx Xxxxxx x xxxxxxxx léčiv x xxxxxxxxx xxxxxxxxx xxxxxx, xxxxx xxxxxxxx xxxxxxx xxxxxx (XXXXXXXXX). X xxxxxxx xxxx xxxxxxxx 28. xxxxx 2011, xxxxxxx Xxxxx xxxxxxxxx xxxxxx xxxxx nepodepsala x xxxxxxxxxxxxxx. Xxxxxxxxxx Xxxxxx xx xxxxxx xxxxxxxxxx xxxxxxxxx zákona. Xxxx xx xxxx xxx stanoveny xxxxxxxx xxxxxxxx trestných xxxx xxxxxxxxxxx nakládání s xxxxxx x xxxxxxxxxxxxxx xxxxxxxxxx. Xxxx Xxxxxx xxxxx xxxxxx přísněji x důrazněji, xxx xxxxx xxxxxxxxxxx činy xxxxxxxxxxx x xxxxxxxxx xxxxxxxx xxxxxxxxx, které xxxxxxxx xxxxxx a xxxxxx pacientů.
Vzhledem x xxxxxxxxxxx budoucímu xxxxxx xx oblasti xxxxxxxxx xxxxx xxxxxxxxxxxx xxxxxx xxxxxx sankce xx xxxxxxxx xxxxxxxx xxxxxxxxxx xx úrovni správního xxxxxxxx. Výše sankcí xxxx xxxxxxx xxxxxxxxx xxxxxx závažnosti předmětných xxxxxxxxx. Xxxxxxx xxxxxxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx xxxx pokut xx xxxxxx, xxxxx xxxxxxxx xx xxx xxxx x xxxxx odrazující. Xxxxxxxxxxx xx xxxxxxxx xxxxxxxxxx prvkem xxxxxxxxxxxx x možnosti xxxxxxxxx xxxxxxx xxxxxxxxx xxxxxx xxx xxxxxxxxxx společenské xxxxxxxxxxxxx každého xxxxxxx xxxxxxxxxxxxx jednání, xxxxx xxxx Ústavem x xxxxx správních xxxxxx xxxxxxxxxx, xxxxx x xxxxxxxxxxx xxxxxx účastníků xxxxxx (xxxxx xxxxxxxxxxxx xxxxx).
3. Vyhodnocení xxxxxxx x přínosů
3. 1 Xxxxx zákona xxxxxx xxx xxxxxxxxxxx x xxxxxxxx xxxxxx na xxxxxx xxxxxxxx a xxxxxx mít xxxxx xxxxxx xx ostatní xxxxxxx rozpočty.
3. 2 Xxxxxxx
Xxxxxxxxxx xxxxxx xx xxxxxx zajištění adaptace xxxxxxxx o ochranných xxxxxxx nebudou xxxxxxxxxxxx xxxxxxxx dopad spočívající x xxxxxxxx xxxxxx xxxxxxxxxxxxxxx míst xxxxxx xxxxxxxxxx na xxxxx xxx xxxxxxxxx rámec xxxx xxxxxxxxxxx xxxxxxxxxx x xxxxxxxxxx xxxx xx služebních xxxxxxx xxxxxxxxxxx pod rozpočtovou xxxxxxxx Xxxxxxxxxxxx xxxxxxxxxxxxx, xxxxxxxxx xx xxxxxx Xxxxxx.
Xxxxxx xx xxxxxxx xxxxxxx rozpočty xx xxxxxxxxxxxxxxx.
Xxxxxx xx xxxxxxxxxxxxx xxxxxxxxx Xxxxx xxxxxxxxx xx xxxx x xxx xxxxxxxxxxx zákona x léčivech, která xx xxxx xxxx xxxxxxx jeho novelou, xx. zákonem č. 70/2013 Sb., x xxxx xxxxxxxxx xxxxxxxx, xxxxxxxx xx xxxx přímo x xxxxxxxx x xxxxxxxxxx xxxxxxx. Xxxx xxxxxx xxx xxxx posouzeny xxx xxxxxxxxxxxx xxxxxx xxxxxxxx xxxxxxxx. X xxxxx xxxxx je xxxxx xxxxxxx xx xxxxxxxxx xxxxxx, xxxxxx xxxxxx x xxxxxxxxx xxxxxx xxxxxxxx (XXX) x xxxxxx č. 70/2013 Sb. x xxxx na xxxxxxxxx xxxxxx XXX x nařízení x xxxxxxxxxx xxxxxxx xxxxxxxxx „Xxxxxx Assessment“. V xxxx xxxxxxxx xxxxxx xx uvádí, že x souladu x čl. 4 směrnice 2011/62/XX x čl. 54a xxxx. 2 x 3 xxxxxxxx 2001/83/XX Xxxxxx xxxxxxxxx přínosy, xxxxxxx x nákladovou xxxxxxxxxx xxxxxxx možností xxx xxxxxxxxxxxxxxx x xxxxxxxxx specifikace jedinečného xxxxxxxxxxxxxx x způsoby xxxxxxx ochranných xxxxx x xxxxxxxx x xxxxxx systému úložišť. Xxxxxxxx, xxxxx xxxx xxxxxxxxxxx jako xxxxxxxxx xxxxxxxxxxxxxxx, představují základní xxxxx nařízení o xxxxxxxxxx xxxxxxx.
Xxxxxx xxxxxxxxx xxxxxxxxxxxx xxxxxxxx x xxxxxxxxxx xxxxxxx xx xxxxxxx xxxxx xxxx xxxxxxxxxxxxx x léčivými xxxxxxxxx, xxxxxxxx xxxxxxx, xxxxx xxxx zajistit xxxxxxxx a ověření xxxxxxxxxxx xxxxxxxxxxxxxx x xxxxxxxxxx x xxxxxxx xxxxxxxxxx x obalem x činnosti x xxxxxx úkony xxxxxxxxxxx xxxx na ně xxxxxxxxxx. Xxxxx však, xx již xxxxxxx xxxxxxxx x ochranných xxxxxxx v platnost (xxxx 2015) xxxxxxx xxxxxxxxx xxxxxxxxx subjektů xxxxxxxxx xx xx xxxxx tohoto xxxxxxxx x xxxxxxxx dnem 9.2.2019. Xxxx xx xxxxxx xxxxxxxxxxxx, držitelů xxxxxxxxxx x xxxxxxxxxx, xxxxxxxx xxxxxxxx souběžného xxxxxx x xxxxxxxxxxxxx xxxxxxxxxxx xxxxxx xxxxxxxxx x xxxxxx xxxxxxxx xxxxxxxxx, xxxxx xxxxx xxxxx xxxxxxx xxxxx xxxxxxxx xxxxx, xxxxxxxxx xx x xxxxxxx XX xxx, xxx xxxx xxxxxxx xxxxx xxxxxxxxxx xxx xxxxxxxxx x nařízení o xxxxxxxxxx xxxxxxx x xxxxxxxxxxx se xxxxxxxx xxxxxxx.
Xxxxxxx xxxxxxxxx ochranných xxxxx x xxxxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx přinese xxxx xxxxxxx na xxxxxx xxxxxxxxxxxxx xxxxxxx, xxxxx v různém xxxxxxx, xxxxxx tak xxxx dopady xxxx xxxxxxxxxx do činnosti xxxxxxxxxxxx xxxxxxxxxxxxx xxxxxxx. X xxxxxx xxxxxxxxx x xxxxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx budou muset xxxxxxxxxxxxx xxxxxxx pořídit xxxxxxx (xxxxxxxx xxxxxxxx xxxxxx imagery), xxxxx xxxxx xxxxxxx xxxxxxxxxx xxxxxxxx xxxx xxxxx xxxxxxx xxxxxx x xxxxxxxx 2X xxxx, xxx představuje jednorázovou xxxxxxxxx cca 5.000 - 7.500,- Kč xx xxxxx xxxxxx (xxxxxxxx). Xxxxx xxxxxxxx, xxxxxx xx připojení x internetu, xxxxx xxxx xxxxxxx xxxxxxxxxx, xxxxx jím xxxxxxx xxxxxxx xxxxxxxxx (v xxxxxxx, xx by xxxxxxxxxxxxx, xxxxxxx by xxxxxxx xxxxxx xxxxxxxxx xx xxxxxxx xxxxxxxxxxxx xxxxxxxxxx, xxxxxxx je xxxx xxx xxxxxxx). Xxxxx xx xxxxxx xxxxxx xxxxxxxx, xx. xxxxxxxxxxxx xxxxxxxxxxxx systémů. Xxxxxxx lékáren xx xxxxxxxxxxx lékárenského systému xxxxxxxxx xx xxxxxxxxxx xxxxxx, xxxxxxx xx x xxxxxxx xx xxxxxxx, xxx nastavení xxxxxxxxxxxx xxxxxx programu (xxxxxxxxxx XX xxxx xxxxxxxx produkty využívané xxxxxxxx desítkami xx xxxxxxxx xxxxxxx). Nezbytnost xxxxxxxx XX vybavení xxxxxxx x xxxx x souvislosti x xxxxxxxxxx prvky xx xxxx týkat zejména xxxxxxx xxxxxxxxxxxx lékáren (xxxxx xxxxx xxxxxxxx xxxxxxxxx, více xxxxxxxxx xxxxxx, xxxxxx na xxxxxxx i na xxxxxxx xx xxxxxxxx), xxxxx xxxxx x xxxxxxxxx personálním xxxxxxxx x xxxxxx nárůstu xxxxxxxx (xxxxx xxxxxxx xxxxx, ověřování každého xxxxxxxxxxxx xxxxxx xxx xxxxxx, komunikace x xxxxxxxxxx x Xxxxxxx x xxxxxxx xxxxxxxxxx xxxxxx xxxxxxxxx xxxxxxxxxxxxx).
Xxxxxxxx x tuto xxxxxx xxxxx přesně xxxxxxxxx xxxxxxxx náklady xxxxxxxxxxxxx xxxxxxx, Xxxxx xxxxxxxxxx xxxxxx xxxxxxxxx xxxxxxxxx xxxxx náklady xxxxxxx x xxxxxxxxxxx x xxxxxxxxxx xxxxxxxxxx prvků xx obalech xxxxxxxx xxxxxxxxx xx xxxxxx 500 xxx. Xx. X xxxx xxxxxx xxxx xxxx xxxxxxxx xxxxx xxxx xxxxxxxxx x xxxxx položky, xxxxx předkladatel považuje xx xxxxxxxxxxxx xx xxxxxxxxxxxx (náklady xx xxxxxxx xxxxxxxxxxx, xxxxx xxxxxx xxxxxxxxx výdeje - xxxxx xxxxx xxxxxxxxxxxx xxxxxxxx), xxxxxxxxx xxxxxxx xxxxx x xxxxxx mírou pravděpodobnosti xxxxx.
Xxxxxxxx xx xxxxxxxxxxx, xx po 9.2.2019 xxxxx xx xxxx xxxxxxxx léčivé xxxxxxxxx, xxxxx xxxxxxx xxxxxxxx xxxxxxxxxx xxxxx a xxxxx xxxx xxxxxxxxxx x prodeji nebo xxxxxxxxxx xxxx xxxxxxx xxxxxxxxx tohoto xxxxxx, xxxxxxxx předkladatel x xxxxxx xxxxxx xxxxxxx xxxxxxxx xxxxxx xxxxx xx xxxxxxxx x xxxxxxx x xxxxxxxxx x xxxxxxxxxx xxxxxxx xxxxxxxxxxxx xx zákona xxxxxxxxx ustanovení, xxxxx xxxxxxx xx jisto, xx tyto xxxxx xxx uváděny, xxxxxxxxxxxxx x vydávány až xx xxxxxxxx doby xxxxxx použitelnosti.
Podle xxxxxxxx xxxxxx úpravy xxxxx x xxxxxxxxx případech xxxxxx (xxxx. xxxx xxxxxxxxxxxx pracovníci) xxxxxxxxxxxxx xxxxxxxxxxxxxx xxxxxxxx xxxxxxx xxxxxx xxxxxxxxx (v xxxxxxx s xxxxxxxxxxx §82 xxxx. 2 xxxxxx o léčivech). Xxxxxxxx x tomu, xx xxxxxxxxxxxx xxxxxxxxx x xxxxxx deriváty xxxx xxxxxx xxxxxxxxx, xxxxx xxxxx muset xxx xxxxxxxx ochrannými xxxxx, bude xx xxxx na xx xxxxxxxxx xxxxxxxxx ověřit xxxxxxxx xxxxx x xxxxxxx xxxxxxxxx xxxxxxxxxxxxx xxxx xxxxxxxxx xxxxxxxx xxxxxxxxx x xxxxxxxx xxxxxx. Aby xxxx xxxxx xxxxxxxx stávající xxxxxx xxxxxxx xxxxxxxxxxxxxx xxxxxxxxx, a to xxxxx do ordinací xxxxxxxxxxxxx xxxxxxxxxxx xxxxxx, x xxxxxx xxxxxxxx xxxxxxxx xxxx x xxxxxxxxx, je xxxxxxx, xxxxxxx povinnosti xxxxxxxxxxx x xxxxxxxx x xxxxxxxxxx xxxxxxx na xxxxxxxxxxxx xxxxxxxxxxxxxx přípravků x využitím článku 23 xxxx. x) xxxxxxxx x xxxxxxxxxx xxxxxxx.
Xxxxxxxxx dopadu xxxxxxxx 2011/62/EU a xxxxxxxx x ochranných xxxxxxx xxxx xxxxxxxxx Evropskou xxxxxx (XX) x xxxxxxx s xxxxxxxxxx xxxxxxxx 2011/62/EU, která xxxxxxxxxx ani neukládá XX xxxxxxxxxxxx xx xxxxxxxxxxx xxxxxx regulace XX xxx oblast xxxxxxxxxx xxxxx x xxxxxxxx xxxxxxxxx.&xxxx; Xxxxx xxx o výrobce x xxxxxxxx xxxxxxxxxx x xxxxxxxxxx, půjde x xxxxx dopady xxxxxxx se zřízením x xxxxxxx systému xxxxxxx. Xxxx xxxxxxxx xxxx xxxxx xxxxxx 54x xxxx. 2 xxxx. x) směrnice 2011/62/XX xxxxxxx xxxx xxxx uvedené xxxxxxx xx xxxxxx xxxxxxx. Xxxx dopady se xxxx nyní xxxxxxx xxxxxxxx xxxxxxxxxxxxx, xxxxx xxxx xxxxxxx xxxxxxx xx xxxxx, xxxxxxxxx x xxxxxxxxxx personálního x xxxxxxxxxxxxx xxxxxxxxx xxxxxx xxxxxxxx. Xxxxxxx xxxxx, xxx příslušné xxxxxxx xxxxxxxxx xxxxxxxx, xxxxxx xxxxxxxxx xxxxxxxx 2011/62/EU a xxx xxxxxxxxx x xxxxxxxxxx xxxxxxx xxxxxxxxxx, kterými xx xxxxx xxxxxxxx xxxxxxx x xxxxxxxxxx x xxxxxxx xxxxxxx x tím pádem xxxxxxxx míru x xxxxxx dopadu xx xxxx xxxxxxxx. Xxxxxxxxx xxxxxx na xxxxxxxxxxxxx xxxxxxxxx xxxx x x tomto případě xxxxxxxxx XX x xxxxxxxxxx na xxxxxxxx 2011/62/EU. Xxxx xxxxxx xxx byly posouzeny xxx xxxxxxxxxxxx xxxxxx xxxxxxxx xxxxxxxx, xx. xxxxxxxx 2011/62/EU a xxxxxxxx o ochranných xxxxxxx, xxxxx xxx x unijní předpisy, x zákona č. 70/2013 Sb., xxxxx jde x xxxxxx xxxxxxxx Xxxxx xxxxxxxxx. X xxxxx xxxxx xx třeba xxxxxxx xx xxxxxxxxx xxxxxx, xxxxxx xxxxxx x xxxxxxxxx xxxxxx xxxxxxxx (XXX) k xxxxxx č. 70/2013 Sb., x xxxx na xxxxxxxxx xxxxxx XXX x xxxxxxxx x xxxxxxxxxx xxxxxxx xxxxxxxxx „Impact Xxxxxxxxxx“. Od xxxxxxxxx xxxxxx hodnocení nebyla xxxxxxxx xxxxx v xxxx xxxxxx x xxxxxxx.
Xxxxxxxx dopad navrhované xxxxxx xx xxxxxxxxxxxxx xxxxxxxx x xxxxxxxx xxxxxxxxxxxx xxxxxxxxxx prvků xx xxxxxxxxxxx dokumentace xx xxxxxxx xxxxxxxxx, xxxxx údaje xxxxxxxxxx xx k jedinečnému xxxxxxxxxxxxxx xxx xxxxxx xx textu obalu x xxxxx xxxxxxxxxx xxxxxx x dopadem xx xxxxxxxxx x xxxxxxxxx - xxxx. xxxxxx o prodloužení xxxxxxxxx registrace, xxxxxx x xxxxx registrace xxxx XX, typu XX xxxx xxxx XX. Xxxxxxxxxx zvláštní xxxxxxx o xxxxx xxxxxxxxxx administrativního charakteru xx xxxxxxxx xxxxx x situaci, xxxxx x xxxxxxxxxx období xxxxxx xxxxxxxxxx žádná xxxxx xxxxxxxxxx, která xxxxxxx informace x xxxxxxxxx. Předložení žádosti x xxxxx xxxxxxxxxx xxx xxxxxxxx prostředku x ověření manipulace x xxxxxx je xxx nezbytné pouze x případě, kdy xxxxxxxxxx x ověření xxxxxxxxxx x xxxxxx xxxx xxx xxxx xx xxxxxxxxx xxxxx, xxxx xxxxxxx xxxxxx xxxxxxxx obalu. Xxxx xxxx stanoveno, xx xxxxxxxxx xxxxxxxxxxxxx x xxxxxxxxxx x xxxxxxx xxxxxxxxxx x xxxxxx xx možné xxxxxxxxxxxxx xxxx xxxxxxxxxxx nebo xxxxxxxxxx xxxxxxxxx xxxxxxx x xxxxx registrace, xxxxx implementace ochranných xxxxx na xxxx xxxx xxxx xx xxxxxxxxx obalu.
Dle údajů x xxxxxxxx 2018 xxxx xxxxxxxx xxx 2/3 žádostí o xxxxx registrace, xxxxx xxxxxxxxxx implementační xxxx xxxxxxxx xx směrnice 2011/62/EU. Xxxxx na xxxxxxxxxxxxx subjekty x xxxxxxx finanční x x xxxxxxx prodlužování xxxx na vyřízení xxxxxxxxxxxx xxxxxxx xxxx xxxxxxxxx, xxxxxxxx k xxxx xxxxxxx xxxxxxxxxxx, xxx xxx xxxxxxx xxxxxxxx xxxxxxxxx xxxxxx xxxxx po zavedení xxxxxxxxxx xxxxx předkládat xxxxxxxx xxxxxx x xxxxx xxxxxxxxxx a xxxxxxxx xxxxx xx xxxxx xxxxxxxxxxxxx již xxxx xxxxxxxxxxx xxxx xxxxxxxxxx příslušné xxxxxxx x změnu xxxxxxxxxx. Xxxxxx xxxxxxxxxxxx xxxxx xxxxx pro xxxxxx xxxxxxxxx, které xxxx xxx xxxxxxxx xxxxxxxxxx xxxxx, x xxxxxxxx xxxxxxxxx, xxxxx xxxxxxxxxx xxxxx opatřeny být xxxxxx (xxxx. xxxxxx xxxxxxxxx, xxxxxxx xxxxx xxxx xxxxx xx xxxxxxxx xxxxxxx) xxxxx xxxxxxxxx xxxxxxxxxxxx xx xxxxxx textu „xxxxxxxxx xx“ při xxxxxxxxx xxxxxx změně xxxxxxxx xx xxxxxxxxx x xxxxxxxxx.
3. 3 Xxxxxxx
Xxxxxxxx xxxxxxxxxx xxxxxx xxxxxx xxxx xxxxxxxxx xxxxxxxxx x xxxxxxxxxx prvcích xxxxxxxxxx xxxxxxxxxxx pro xxxxxxxxx vstupu xxxxxxxxxx xxxxxxxx přípravků xx xxxxxxxxx xxxxxxxxxxxxxx xxxxxxx x xxxxxxx ochrany xxxxxxxx a xxxx xxxxxxxxxx x xxxxxxxxxxxx xxxxxxx xxxx xxxxxxxx xxxxxxxxx, xxxxx pocházejí x xxxxxxxxxxx xxxxxx. Xxxxxxxxxx právní úprava xxxx xxx na xxxxxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxx x xxx xxxxxxxx, že přispěje xx xxxxxxx xxxxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxxx x xx xxxxx xxxxxxxxxx x x zásadnímu xxxxxxxxx xxxxxxxxx xxxxxxxxxxxxxx xxxxxxx xx xxxxxxxxxx xxxxxxxx xxxxxxxxx. Xxxx xx xxxx dojít xx xxxxxxx xxxxxx xxxxxxx, xxxxxxxxxxxx a xxxxxxx, neboť xxxxxxxx xxxxxx svou xxxxxxxxxxx xx trhu xxxx x prodeje xxxxxxxxx xxxxx xxxxxxx.
Xxx xx xxxxxxxxxxxxxx xxxxxx, xx xx xxxxxxxx xxxxxx xxxxxxxxx xxxxxxxxx xx xxxxxxxxx xxxxxxxxxxxxxx řetězce x volně xxxxxxxx xx xxxxx území Xxxx, xxxxx by xxxxxx xxxxxxx v xxxxxxxx xxxxxx xxxxxxxxxx, xxxxx xxxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxx ochranných xxxxx v xxxxxxxxx xxxxxxxx xxxxxxxxx, x xxxxxxx xxxxxxxx xxxxx xxxxxx xxxxxxxx (xx. x léčivých xxxxxxxxx xxxxxxxxx xxxxxxx oprávněnými xxxxxxx léčivé xxxxxxxxx xxxx xxxxx distributorem).
Datové xxxxx xxxxxxxx x xxxxxxxxxx xxxxxxxxxxxxxx (xxxxxxx xxx přípravku, xxxxx xxxxx x xxxxx xxxxxxxxxxxxx) xxxxxxxx k xxxxxxxxxxx pacientů xxx, xx xxxxxxx postupy xxx xxxxxxx a xxxxxxx x farmakovigilanci.
Ověřování xxxxxxxx léčivých přípravků x ČR xx xxxxxx xxxxxxx, xxxxxxxxxxxx x xxxx xxxxxxxxxxx x xxxxxx (xxxxxxx) xx mělo xxxxx xxxxxxxx vstupu xxxxxxxxxx xxxxxxxx přípravků xx xxxxxxxxx distribučního xxxxxxx x xxxxxxxx xxxxxxxxxx xxxxxx potenciálního xxxxxx xxxxxxxxxx xxxxxxxx přípravků xxxxxxxxx x xxxxxxxxx x xxx xxxxxx xxxxxxx xxxxxxxxx zdraví.
Konečným xxxxxxx xxxxxx xxxxxx xx bezpečný xxxxxxx xxxxxxxxxxxx xxxxxxx xxxxxxxx xxxxxxxxx x ČR.
4. Xxxxxxxxx pořadí xxxxxxx x výběr xxxxxxxxxxxxxx xxxxxx
Xxxxxxxxx doporučenou x xxxxxxx řešení xx xxxxxxxx 2, xxxx xxxxxxxxxx xxxxxx xxxxxx xxxxxx o léčivech, xxxxxxx xxxxxxxx xxxxxx xxxx x splňuje xxxxxxxx xxxxxxxxx xxxxxxxxx x xxxxxxxxxx xxxxxxx x xxxx, xxx x xxxx Xxxxxxxx xxxx xxxx xxxxxxxx xxxxxxxx xxxxxx ověřování xxxxxxxx přípravků prostřednictvím xxxxxxxxxx xxxxx uvedených xx jejich xxxxx, xxxxx xx xxx xxxxxxxx vstupu xxxxxxxxxx xxxxxxxx xxxxxxxxx do xxxxxxxxx dodavatelského xxxxxxx x xxxxxxx xxx x xxxxx xxxx xxxxxxx veřejného xxxxxx.
Xxxxxxxx 1 (xxxxxx) xx x důvodů popsaných xxxx xxxxxxxxxxxx x xxxxx xxxxx varianta xxx z xxxxxx xxxx xxxxxxxxx xx xxxxx, xxxxxxx jde x xxxxxxxx xxxxx xxxxxxxxxxxx xxxxxxxx Evropské xxxx x možnosti xxxxxxxxx státu x xxxx xxxxxxx, v xxx a jak xxxxxxx xxxxxxxx provést, xxxx xxxxxxxx omezeny xxx na xx xxxxxxx, xx xxxxxxx xx xx xxxxx xxxxx použitelný xxxxxxx Xxxxxxxx xxxx provést xxxxxxxxx xxxx xxxxxxxx.
5. Xxxxxxxxxxxx xxxxxxxxxx xxxxxxxx x xxxxxxxxxx
Orgánem xxxxxxxxxx xx xxxxxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxx xxxx především Xxxxx, xxxxx xx xxx xxxxx xxxxxxxxxxx znění xxxxxx x xxxxxxxx xxxxxxxxxxxxxxx xxxxxxxx správním xxxxxx xxx oblast xxxxxxxx xxxxxxxxx xxxxx. Xxxxx má xxxxxxx xxxx xxxx xxxxxxx xxxxxxxxxx v oblasti xxxxxxx, xxxxxxxxx a xxxxxxxxxxx xxxxxxxxx xxxxx, x xx i xx vztahu x xxxxxxxxxx xxxxxxx xxxxxxxxx xxxxx a Evropské xxxx.
Xxxxxxxxxxxx doporučené varianty x xxxxxxxxxx xxxxxxxxxx xxxxxxxx xxxx zajištěno xxxxxxxx xxxxxxx o xxxxxxxx x rámci xxxxxxxxx trestání x xxxxxxx s obecnou xxxxxx xxxxxxx xxxxxxxxx, x to xxxxxxxxx xxxxx x dalších xxxxx xxxxxx.
6. Přezkum xxxxxxxxx xxxxxxxx
Xxxxxxxx nové xxxxxx úpravy xxxx xxxxxxxx po xxxxxxxx xxxxxxx 2 let xxx xxx nabytí xxxx xxxxxxxxx, aby xxxx xxxxx xxxxxx xxxxxxxxxx xxxxxxxx x xxxxxxxxx xxxxxxxxx, jaké xx právní xxxxxx xxxxxxxxx xxxxxx, tj. xxx xxxxx k xxxxxxxxx xxxxxxxxxxx padělaných xxxxxxxx xxxxxxxxx x xxxxxxxx dodavatelském řetězci x ČR a x xxxxxxxx. Xxxxxxx xxxxxxxxx budou xxxxxxxx Xxxxxxxxxxxx xxxxxxxxxxxxx x Xxxxxx ústav xxx xxxxxxxx léčiv ve xxxxxxxxxx x xxxxxxxxx xxxxxxxx, x xx x hlediska posouzení xxxxxxxxx nové právní xxxxxx a xxxxxxx x xxxxxxxx xxxxxxxxxx xxxx xxxxxxxxxxx xxxxx xxxxxx xxxxxxx.
7. Xxxxxxxxxx x zdroje xxx
Xxxxx xxxxxx byl x xxxxxxx přípravy xxxxxxxxxxx xx xxxxxxxx xxxxxxx xxxxxxxxx léčivých xxxxxxxxx, xxxxxxxx xxxxxxxxxx x xxxxxxxxxx xxxxxxxx přípravků, xxxxxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx, poskytovatelů xxxxxxxxxxx xxxxxx xxxxxxxxxxx x xxxxxx xxxxxxxx xxxxxxxxx x pacientských xxxxxxxxxx. Xxxxx xxxxxxxxx xxx x listopadu 2016 xxxxxx xxxxxxx xxxxxxxx xxxxx xxxxxx xxxxxx x xxx, xx x xxxx xxxxx xxxxxxxx připomínky. X xxxxxxxxxx x vypořádání xxxx xxxxxxxxxxx připomínek xx pak v xxxxxxxx 2016 xxxxxxxxxxx xxxxxx xxxxxxx v xxxxxx Xxxxxx. Celá xxxx uplatněných xxxxxxxxxx xxxx v xxxxxxxxx xxxxxx xxxxxxxxxx x xxxxxx xxxxxxxxxxxx xxxxx xx xxxxxxxxxxx xxxxxxxxxx xxxxxxxxx a x xxxx xxxxxxxxxx x xxxxxxxxx potřebám xxxxxxxx xxxxx. Xxxx xxxxxxxxxxxx xxxxxxx xxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxx xxxxxxx xxxxxxxxxx, xxx xxx xxxxxxxxx Xxxxxxx xxxxxxx xxx xxxxxxxx xxxxx xxxxx §32 xxxx. 5 zákona x léčivech („kód XXXX“) xxxxx součástí xxxxxxxxxxx xxxxxxxxxxxxxx. Dále xxxxxxxxx jednání a xxxxxx xxxxxxxxxx xxxxxxxxx xx zástupci Xxxxxx Xxxxx xxxxxxxxx x Xxxxxx pro státní xxxxxxxx xxxxxxxxxxxxx biopreparátů x xxxxx, a xx xxxxxxx za xxxxxx xxxxxxxx xx xxxxxxxxxxxx xxxxxxxxxxxx xxxxxx 23 xxxxxxxx x xxxxxxxxxx prvcích.
8. Xxxxxxxx xx zpracovatele XXX
Xxxxx: Xxxxxxxxxxxx zdravotnictví, Xxxxx xxxxxxxx, xxxxxxxx xxxxxxxx, xxxxxxxxxxxx: XxxxxXx. Alena Xxxxxxxxx, xxxxxxxxx xxxxxx xxxxxxxx, zpracovatelé: XxxxxXx. Xxxxx Xxxxxxxxx, vedoucí xxxxxxxx farmacie, Xxx. Xxxxxxxxx Xxxxxxxxxx, referent, Xxx. Xxxxxx Xüxxxx, xxxxxxxx.
X-xxxx: xxxxx.xxxxxxxxx@xxxx.xx
Xxxxxx xxxxx xxx xxxxxxxx xxxxx, xxxxx dozoru, Xxx. Xxxxxxx Xxxxxxxx, ředitelka Xxxxx xxxxxx
Xxxxxxx: 272 182 265
ROZDÍLOVÁ XXXXXXX XXXXXX XXXXXXXX XXXXXXXX XX X XXXXXXXX XX
Xxxxxxxxx xxxxxxx x návrhu xxxxxx zákona, kterým xx xxxx xxxxx x. 378/2007 Xx., x xxxxxxxx x x xxxxxxx xxxxxxxxx xxxxxxxxxxxxx xxxxxx (xxxxx x xxxxxxxx), ve xxxxx xxxxxxxxxx xxxxxxxx, x zákon č. 372/2011 Xx., x xxxxxxxxxxx xxxxxxxx a xxxxxxxxxx jejich poskytování (xxxxx x xxxxxxxxxxx xxxxxxxx), ve xxxxx xxxxxxxxxx předpisů
|
Navrhovaný xxxxxx xxxxxxx (resp. jiný xxxxxx xxxxxxx) |
Xxxxxxxxxxxx předpis XX |
|
|
Xxxxxxxxxx (část, §, xxxx., xxxx., xxxx.) |
Xxxxx x. |
Xxxxxxxxxx |
|
Xx. 2 |
||
|
Čl. 43, 44, Xx. 46 |
||
|
§13 odst. 2 písm. p) a q) (včetně poznámky pod čarou č. 107 a 108) |
Čl. 25, Xx. 7 xxxx. 1 x 2, Xx. 10 xxxx. 1 xxxx xxxxx, Xx. 94 xxxx. 1 |
|
|
32017L1572, 32017L1572, 32017R1569, 32017R1569, 32017R0556, 32017R0556 |
Xx. 3 xxxx. 1, Xx. 3 xxxx. 3, Xx. 21 odst. 4, Xx. 22, Xx. 3 odst. 1, Xx. 4 odst. 8 |
|
|
Xx. 4 |
||
|
Xx. 1 písm. x) x x), Xx. X xxx 12 |
||
|
Čl. 45 |
||
|
Xx. 42 |
||
|
Xx. 11 xxxx. 1 |
||
|
Xx. 13 xxxx. 1 x 2 |
||
|
Xx. 4 xxxx. 1 |
||
|
Xx. 23 |
||
|
Čl. 25 xxxx. 1 |
||
|
Čl. 39 |
||
|
Čl. 10 x 11 |
||
|
Čl. 12 |
||
|
Xx. 13 |
||
|
Xx. 4 |
||
|
Xx. 5 xxxx. 1 |
||
|
Xx. 6 |
||
|
Xx. 7 |
||
|
Čl. 14 |
||
|
Xx. 15 |
||
|
Xx. 16 |
||
|
Xx. 18 |
||
|
Xx. 9 |
||
|
Xx. 20 |
||
|
Čl. 22 |
||
|
Xx. 24 |
||
|
Xx. 23 |
||
|
Xx. 23 |
||
|
Xx. 25 xxxx. 1 x 2 |
||
|
Xx. 28 |
||
|
Xx. 29 |
||
|
Xx. 25 xxxx. 4 |
||
|
Xx. 30 |
||
|
Xx. 25 xxxx. 1 |
||
|
Čl. 33 xxxx. 1 |
||
|
Xx. 40 |
||
|
Xx. 42 |
||
|
Xx. 33 odst. 4 |
||
|
Xx. 37 |
||
|
Čl. 39 |
||
|
Xx. 35 xxxx. 1 x 2 |
||
|
Xx. 32 xxxx. 3 a 4 |
||
|
Xx. 32 xxxx. 1 |
||
|
Xx. 35 xxxx. 3 |
||
|
Xx. 35 xxxx. 4 |
||
|
Xx. 41 |
||
|
Xx. 63 odst. 1, Čl. 94 xxxx. 1, Xx. 20 bod 2 |
||
|
Xx. 10 bod 2 xx 5 |
||
|
Čl. 4, Čl. 45, Xx. X xxx 12, Xx. X xxx 25 |
||
|
Xx. 94 xxxx. 1, Xx. 62 xxx 1 |
||
|
Xx. 4, Xx. 45, Čl. X xxx 12, Xx. X bod 25 |
||
|
Xx. 10 xxxx. 8 |
||
|
Xxxxx předpisu EU (xxx xxxxx) |
Xxxxx xxxxxxxx XX |
|
XXXXXXXX XXXXXX X XXXXXXXXX XXXXXXXXX (EU) 2016/161 xx xxx 2. xxxxx 2015, xxxxxx xx doplňuje xxxxxxxx Xxxxxxxxxx parlamentu x Xxxx 2001/83/ES xxxxxxxxxx xxxxxxxxxx pravidel xxx ochranné xxxxx xxxxxxx xx xxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx |
|
|
Xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Xxxx 2011/62/XX xx xxx 8. června 2011, xxxxxx xx xxxx směrnice 2001/83/XX x xxxxxx Společenství xxxxxxxxx xx xxxxxxxxx xxxxxxxx xxxxxxxxx, xxxxx xxx x xxxxxxxxx xxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx xx legálního xxxxxxxxxxxxxx xxxxxxx |
|
|
Xxxxxxxx Xxxxxx (XX) 2017/1572 xx xxx 15. září 2017, xxxxxx xx xxxxxxxx xxxxxxxx Evropského xxxxxxxxxx x Xxxx 2001/83/XX, xxxxx xxx x xxxxxx x xxxxxx xxx xxxxxxxx xxxxxxx xxxxx xxx xxxxxxx xxxxxx xxxxxxxxx |
|
|
Xxxxxxxxx xxxxxxxx Komise x xxxxxxxxx xxxxxxxxx (XX) x. 2017/556 xx xxx 24 xxxxxx 2017&xxxx; x podrobných xxxxxxxxxx xxx xxxxxxxxx xxxxxxxxxxx postupů xxxxxxx xxxxxxxx xxxxx&xxxx; xxxxx xxxxxxxx Evropského parlamentu x Xxxx (XX) x. 536/2014 |
|
|
Nařízení Xxxxxx x přenesené xxxxxxxxx (XX) x. 2017/1569 xx xxx 23. xxxxxx 2017, kterým xx doplňuje xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Xxxx (XX) x.536/2014 xxxxxxxxxx xxxxx x xxxxxx pro správnou xxxxxxx xxxxx pro xxxxxxxxx humánní léčivé xxxxxxxxx a xxxxxxxx xxxxxxxxx xxxxxxxx |
|
|
Xxxxxxxx Xxxxxxxxxx xxxxxxxxxx a Rady XX x. 536/2014 xx dne 16. xxxxx 2014 o xxxxxxxxxx hodnoceních xxxxxxxxx xxxxxxxx xxxxxxxxx x xxxxxxx xxxxxxxx 2001/20/ES |
Xxxxx xxxxx www.psp.cz


