Vládní návrh zákona, kterým se mění zákon č. 378/2007 Sb., o léčivech a o změnách některých souvisejících zákonů (zákon o léčivech), ve znění pozdějších předpisů, a zákon č. 234/2014 Sb., o státní službě, ve znění pozdějších předpisů
706/0
Xxxxxx xxxxx
XXXXX
xx xxx … 2016,
kterým xx xxxx zákon č. 378/2007 Sb., x léčivech a x xxxxxxx některých xxxxxxxxxxxxx xxxxxx (xxxxx x xxxxxxxx), xx xxxxx xxxxxxxxxx předpisů, x xxxxx č. 234/2014 Sb., x státní xxxxxx, xx xxxxx xxxxxxxxxx xxxxxxxx
Xxxxxxxxx se xxxxxx xx tomto xxxxxx Xxxxx republiky:
ČÁST XXXXX
Xxxxx xxxxxx x xxxxxxxx
Xx. X
Xxxxx č. 378/2007 Sb., x xxxxxxxx a x xxxxxxx některých xxxxxxxxxxxxx xxxxxx (zákon x léčivech), ve xxxxx zákona x. 124/2008 Sb., zákona x. 296/2008 Sb., xxxxxx x. 141/2009 Xx., xxxxxx x. 281/2009 Xx., xxxxxx x. 291/2009 Sb., xxxxxx č. 75/2011 Xx., xxxxxx x. 375/2011 Sb., xxxxxx x. 50/2013 Xx., xxxxxx č. 70/2013 Xx., xxxxxx x. 250/2014 Xx. a xxxxxx x. 80/2015 Xx., xx xxxx xxxxx:
1. Xx konec xxxxxxxx xxx xxxxx x. 2 se xxxxxxxx xxxx:
„Xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Xxxx (XX) č. 536/2014 xx xxx 16. xxxxx 2014 o xxxxxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx a o xxxxxxx směrnice 2001/20/XX.
Xxxxxxxx Xxxxxx v xxxxxxxxx xxxxxxxxx (XX) č. 1252/2014 xx dne 28. xxxxxx 2014 xxxxxxxxxx xxxxxxxx Evropského xxxxxxxxxx x Xxxx 2001/83/XX, xxxxx jde x xxxxxx x pokyny xxxxxxx xxxxxxx xxxxx xxx xxxxxx xxxxx xxx humánní xxxxxx xxxxxxxxx.“.
2. V §5 xx xxxxxxxx xxxxxxxx 16, který xxxxxx xxxxxxxx pod xxxxx x. 101 zní:
„(16) Xxxxxxx léčivé xxxxx xx xxx xxxxx xxxxxx xxxxxx, xxx-xx x xxxx použití x hodnocených xxxxxxxxx xxxxxxxx xxxxxxxxxxx nebo xx xxxxxxxxxxxxx xxxxxxxx xxxxxxxxxxx, rozumí xxxxxxxx xxxxx nebo částečný xxxx xxxxxxxx xxxxxxxxx, xxxxxx, xxxxxx, xxxxxxxxxxx, xxxxxxxxxx, xxxxxxxxxxxx, xxxxxxxx xxxxxxx nebo propouštění xxxxxx xxxxx, jakož x související kontrola. Xxxxxxxx xxxx, xx xx xxxxxx xxxxxxx xxxxxx xxxxx, xxx-xx x xxxx xxxxxxx x xxxxxxxxx xxxxxxxx xxxxxxxxxxx, stanoví xxxxx xxxxxxxxxx xxxxxxx Xxxxxxxx xxxx xxxxxxxxxx xxxxxxxx xxxxxxx praxi xxx xxxxxx xxxxx101).
XXXXX: 32014R1252
3. V §11 xxxxxxx x) xxx:
„x) xxxxxx xxxxxxxx xxxxxx xxxxxx xxxxx §77x, xxxxxx xxxxxxx xxxx xxxxxxxx xxxxxxxxxx léčivého xxxxxxxxx xx xxxxxxxxx,“.
4. X §11 xxxxxxx x) zní:
„h) xxxxxxx podmínky xxx xxxxxxxxx dostupnosti xxxxxxxx xxxxxxxxx xxxxxxxxxx xxx xxxxxxxxxxx xxxxxxxxxxx služeb, xxxxxxx xxxxxxxx-xx xxxxxxxxx xxxxxx dostupnosti xxxxxx xxxxxxxx obecné xxxxxx x jsou-li splněny xxxxxxxx xxx jeho xxxxxx, xxxxxxxxx xxxxx xxxxxxx g) xxxx x), a přijímá xxxxxxxx xx xxxxxxx xxxxxxx, xxxxxx x xxxxxxxxxxx léčivých xxxxxxxxx xxx vzácná xxxxxxxxxx x xxxxxxxx xxxxxxxxx, xxxxx xxxxx xxx xxxx takové stanoveny, xxxxx x xxxxxxxx xxxxxxxxx xxx xxxxxxx x dětském xxxxxxxxx,“.
5. X §11 xx xx xxxxx xxxxxxx x) xxxxx xxxxxxxxx xxxxxx x xxxxxxxx xx xxxxxxx x), xxxxx xxx:
„x) xxxxxx xxxxxxxx xxxxxx xxxxxx xxxxx §77x, xxxxxx xx stanoví xxxxxx xxxxxxxxx, při xxxxx xxxxxxxxxx bude xxxxxxxx xxxxxxxxxx x xxxxxxxx léčby xxxxxxxx x Xxxxx republice x přímým xxxxxxx xx ochranu zdraví xxxxxxxxxxxx a x xxxxxxxxx ovlivněním xxxxxxxxxxx xxxxxxxxxxx xxxxxx, a xxxx xxxxxx takových xxxxxxxx xxxxxxxxx.“.
6. X §13 xxxx. 2 xxxx. x) xxxx 1 xx za xxxxx „xxxxxxxxxx x povolení xxxxxxxxxx xxxxxx,“ vkládají xxxxx „xxxxxxxxxx x xxxxxxxxxx léčivého přípravku,“.
7. X §13 xxxx. 2 xxxx. x) bodu 3 xx xxxxx „xxxxxxxxxxxxxx“ xxxxxxx.
8. X §13 xxxx. 2 písmeno x) xxxxxx poznámky xxx xxxxx x. 104 zní:
„b) xxxxxx xxxxxxxxxx týkající xx xxxxxxxxxx xxxxxxxxx xxxxx §51 a xxxxxx xxxxxxxx xxxxxxxx xx xxxxxx čl. 77 xxxxx použitelného předpisu Xxxxxxxx xxxx upravujícího xxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx104) (xxxx xxx „nařízení x xxxxxxxxx hodnocení“)“.
CELEX: 32014R0536
9. X §13 xxxx. 2 xx xx konci xxxxxxx x) xxxxx xxxxxxxxx xxxxxx x xxxxxxxx xx xxxxxxx n), xxxxx xxx:
„x) x xxxxxxx zjištění závady x jakosti xxxxxx, xxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxx xxxx zdraví xxxx, rozhoduje x xxx, xxx xx xxxxxx xxxxxx xxxx xxxx jednotlivá šarže xxxx xxxxxxxxxxxx, xxxxxxx, xxxxxx xx xxxxx xxxx používat při xxxxxxxxxxx xxxxxxxxxxx služeb.“.
10. V §13 xxxx. 3 xx xx konci xxxxxxx x) tečka xxxxxxxxx xxxxxx x xxxxxxxx xx písmena x) x r), xxxxx xxxxx:
„x) předává Ministerstvu xxxxxxxxxxxxx veškeré xxxxx xxxxx pro xxxxxx xxxxxxxx xxxxxx xxxxxx xxxxx §77x,
x) xx xxxxxxx xxxxxxxxxxx xxxxxxx xx xxxx s xxxxxxxx xxxxxxxxx xxxxxxx Xxxxxxxxxxxx zdravotnictví informaci xxxxx §77x a xxxxxxx xx xxxxxx x xxxxxx xxxxxxxx xxxxxx povahy xxxxx §77x.“.
11. V §16 xxxx. 2 xxxx. x) xxxx 1 xx za xxxxx „xxxxxxxxxx x xxxxxxxx xxxxxxxxxx xxxxxx,“ xxxxxxxx xxxxx „xxxxxxxxxx x xxxxxxxxxx léčivého xxxxxxxxx,“.
12. Za §19 xx vkládá xxxx §19x, xxxxx xxxxxx xxxxxxx xxx:
„§19x
Xxxxxxxxx xxxxxxxxxxx xxx
(1) Xxxxxxxxx xxxxxxxxxxx xxx xxxxxxxxx xx xxxxxxxx Xxxxxx x xxxxxxxxxxxx osobě, xxxxx xxxxx xx xxx xxxx xxxxxx xxxxxx, xxxx xxxxxxxxx:
x) xxxxxxxxxxxxx xxxxx xxxxxx xxxxx, x to xxxxxxx xxxxx xxxx název x xxxxx,
x) xxxxx xxxxxx, xxxxxx xxxxxxxxxx xxxxx,
x) x xxxxxxx xxxxxxx xxxxxxxxx x xxxx odeslání x xxxx xxxxxx léčiva x
x) množství léčiva xxxxxxxxx x měrných xxxxxxxxxx.
(2) Xxxxxxxxxx informací xxxxx odstavce 1 xxxx porušením xxxxxxxxxx xxxxxxxxxxxx xxxxx daňového xxxx.“.
13. X §21 xx xxxxxxxx 1 xxxxxxx.
Xxxxxxxxx xxxxxxxx 2 x 3 se xxxxxxxx xxxx odstavce 1 x 2.
14. X §23 xxxx. 2 xxxx. x) xx xx xxxxx „xxxxxxx“ vkládají xxxxx „, xxxxx Xxxxx xxxxxxx rozhodnutí xxxxx §13 xxxx. 2 písm. n)“.
15. X §33 xxxx. 2 xx xx větě xxxxx xx slova „xxxx xxxxx“ xxxxxxxx xxxxx „x kódu přiděleného Xxxxxxx nebo Xxxxxxxxxxxx xxxxxxx“.
16. X §33 xxxx. 2 se xxxx poslední xxxxxxxxx xxxxxx „Xxxxxxx xxxxxxxxxx x xxxxxxxxxx poskytuje Xxxxxx xxxxx x xxxxxxx xxxxx x xxxxxx xxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxx xx xxx x České xxxxxxxxx xxxxxxxxxxxx; poskytované xxxxx xxxxxxxx identifikaci xxxxxxxx xxxxxxxxxx x xxxxxxxxxx, xxxxxxxxxxxx léčivého xxxxxxxxx x xxxxxxxxx x tom, xxx xxx léčivý xxxxxxxxx xxxxx lékárně xxxx xxxxxxxxxxxxxx; strukturu, xxxxxx, xxxxx x xxxxxx xxxxxxxx jejich poskytování xxxxxxxxxxxxxxx elektronického xxxxxxx xxxxxxx xxxxxxxxx xxxxxx xxxxxxx. Xx výzvu Xxxxxx xxxx Xxxxxxxxxxxxx xxxxxx poskytne xxxxxxx xxxxxxxxxx x registraci Xxxxxx xxxx Veterinárnímu xxxxxx xxxxx týkající xx xxxxxx předepisování xxxxxxxx xxxxxxxxx a xxxxx x xxxxxx xxxxxxx xxxxxxxx přípravků xxxxxxxxx na xxx x České xxxxxxxxx, xxxxx má x xxxxxxxxx.“.
XXXXX: 32001L0083, 32004L0027
17. X §33 xxxx. 3 xxxx. x) xx xxxxx „xx xxxxxxxxxx nebo xxxxxxx“ xxxxxxxxx xxxxx „xxxxxxxxx xx trh x Xxxxx xxxxxxxxx“.
18. X §34 xx xx konci xxxxxxxx 2 xxxxxxxx xxxx „Xxxxxx xxxxxxxxx xxxxxxxxxxxx údajům a xxxxxxxxxxx před xxxxxxxxxxxx xxxxxxxxxx lze, xxxxx xxxxxx x rozhodnutí x prodloužení registrace xxxxxxxxx jinak, xxxxxx xxxxxx xx xxx xxxxxxx po xxxx 180 dnů xx xxxxxxxxx prodloužení xxxxxxxxxx. Xxxxxxxxxxxx, xxxxxxx, x xxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxx, a xxxxxxxx při xxxxxxxxxxx xxxxxxxxxxx xxxxxx xxxx xxxxxxxxxxx xxxx xx xxxxxx léčivý xxxxxxxxx xxxxx dále po xxxx xxxx použitelnosti.“.
19. V xxxxxxx xxxxx IV xx xxxxx „VÝROBY“ xxxxxxxxx xxxxxx „XXXXXX“.
20. Xxxxxx dílu 1 xxxxx XX xxx: „Klinické xxxxxx“.
21. §51 až 53 xxxxx:
„§51
Xxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx
(1) Xxxxx xxxxxxxx xxxxxxx x povolení xxxxxxxxxx xxxxxxxxx humánních xxxxxxxx xxxxxxxxx podle s xx. 5, 13 x 14 xxxxxxxx x xxxxxxxxx xxxxxxxxx x žádosti x xxxxxxxx xxxxxxxx změny xxxxxxxxxx hodnocení x xxxxxxx s xx. 16 Xxxxxxxx XX x xxxxxxxxx xxxxxxxxx. Xxxxx dále xxxxxxx xxxxxx xxx xxxxxxxx xxxxxxxxxx xxxxxxxxx. Xxxxxxx xxxxx xxxxxxxxx x xxxxxxxxxxx x xxxxxxxxx xxxxxxx x povolení xxxxxxxxxx hodnocení x xxxxxxx o xxxxxxxx xxxxxxxx xxxxx xxxxxxxxxx xxxxxxxxx a xxxxxxxxxx xxxxxxx se považují xx xxxxxxx xxxxx.
(2) Xxxxx je x Xxxxx republice národním xxxxxxxxxx xxxxxx xxxxx xx. 83 xxxxxxxx x xxxxxxxxx xxxxxxxxx.
(3) Xxxxx v rámci xxxxxxxxxx xxxxxxx x xxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx xxxx významné změny xxxxxxxxxx xxxxxxxxx
x) x xxxxxxx, xx xx Xxxxx xxxxxxxxx xx xxxxxx x příslušnému xxxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxx xxxxxxxxxxx xxxxx xx. 5 xxxx. 1 nebo xx. 14 xxxx. 2 xxxxxxxx x xxxxxxxxx xxxxxxxxx, xxxxxxxx činnosti xxxxxxxxx xxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxxx o xxxxxxxxx xxxxxxxxx, xxxxxxxx xx aspektů, xx xxxxx xx xxxxxxxx xxxx X hodnotící xxxxxx,
x) x xxxxxxx, xx Xxxxx republika xxxx ve xxxxxx x příslušnému klinickému xxxxxxxxx xxxxxxxx xxxxxx xxxxxxxxxxx, vykonává xxxxxxxx xxxxxxxxx xxxxxxxxx xxxxx xxxxx čl. 2 xxxx. 12 xxxx xx. 14 nařízení x xxxxxxxxx xxxxxxxxx, xxxxxxxx xx aspektů, xx xxxxx xx xxxxxxxx xxxx X xxxxxxxxx xxxxxx, x
x) xxxxxxxxxxx xxxx II xxxxxxxxx zprávy k xxxxxxx o povolení xxxxxxxxxx xxxxxxxxx týkající xx Xxxxx xxxxxxxxx x x xxxxxxx x povolení xxxxxxxx xxxxx xxxxxxxx se Xxxxx republiky, xxxxx xxxxxxxx xx stanovisko xxxxxxxxxxx etickou xxxxxx.
(4) Xxxxx rozhoduje x xxxxxxx x povolení xxxxxxxxxx xxxxxxxxx x x xxxxxxx x xxxxxxxx významné změny xxxxxxxxxx hodnocení xxxxx xxxxxxxx x xxxxxxxxx xxxxxxxxx. Xxxx xxxxxxxxxx xxxxx pro území Xxxxx xxxxxxxxx.“.
XXXXX: 32014R0536
§52
Ochrana xxxxxxxxx skupin xxxxxxxx xxxxxxxxx
(1) Klinické hodnocení xxx xxxxxxxx u xxxxxxxxx xxxxx xx xxxxxxxxxxx, xx xxxxx xxxxxxxxxxxxx souhlasu xxxx xxxxxxxxx xxxxxxxx xxxxxxx x xxxxxx x xxxxxxxxx hodnocení xxxxxxxx xxxxxxxxx souhlasu x xxxxxxx xxxxxxxxx xxxxx, xx-xx to xxxxxxxxx xxxx xxxxxxxx a xxxxx vyspělosti.
(2) Klinické xxxxxxxxx lze xxxxxxxx xx xxxxxxxx xxxxxxxxxxx xxxxx xxxxxxx také x xxxxxxxxxxxx xxxxxx xxxxxxxx, do xxxxxxx xxxxxx xxxxx
x) nacházející xx xx xxxxx, xxxxxxxxxxxxx xxxxxxx nebo xx xxxxxx xxxxxx xxxxxx xxxxxxx,
x) pobývající x zařízení xxxxxxx xxxx,
x) xxxxxxx xxxxxxxxxxx xxxx xxxxxxx xxxxxx.
(3) Xxxxxxxx xxxxxxxxx xxx xxxxxxxx x xxxx xxxxxxxxx x xxxxxxxx 2 xxx xxxxx, xxxxx x němu xxxx xxxxx xxxxxxx xxxxxxxxx x xxxxxxxxxxxx xxxxxxxxx x xxxxx xxxxxxxx xxxxxxx xxxxxxxxx xxxxxx opravňující k xxxxxxxxx, xx xxxxx x xxxxxxxxx xxxxxxxxx xxxx xxx xxx xxxx xxxxx přímý xxxxxxx xxxx zdravotně xxxxxxxxxxx přínos, xxxxx xxxxxxx nad xxxxxxxxxxxxx xxxxxx a zátěží, xxxx xxx ně xxxxxxxx do xxxxxxxxxx xxxxxxxxx xxxx xxxxxxx xxxxxxxx xxxxxxxxxxx, xxxxxxxxx xxxxxxxx, xxxxxxxxxxxx xxxxxxxxxxx xxxxx.
XXXXX: 32014R0536
§53
Etická xxxxxx
(1) Xxxxxx komise xx xxxxxxx Xxxxxx.
(2) Etická xxxxxx xxxxxxxx etický xxxxxx xxx xxxxxxxxx xxxxxxxxxx x provádí xxxxxx přezkum, zahrnující xxxxxx, lékařské x xxxxxxx aspekty, žádostí x xxxxxxxx xxxxxxxxxx xxxxxxxxx, xxxxxxx x xxxxxxxx xxxxxxxx xxxxx xxxxxxxxxx xxxxxxxxx a xxxxxx xxxxxxxxxx x xxxxxxx x xxxxxxxx xxxxx xxxxxx xxxxxx x xxxxxxxx x xxxxxxxxx hodnocení.
(3) Xxxxx xxxxxxxxx xxx xxxxxxx xxxxxx podmínky xxx xxxx xxxxxxx.
(4) Ústav xx xxxxxxxxxx xxxxxxxx Xxxxxxxxxxxx zdravotnictví vydá Xxxxxx xxxxxx xxxxxx. Xxxxxxx xxx xxxxxx xxxxxx (xxxx jen „Xxxxxxx xxx“) xxxxxx xxxx xxxxxx komise. Xxxxxx xxxxxx xxxxxx x Xxxxxxx xxx Xxxxx xxxxxxxx na xxxxx xxxxxxxxxxxxx xxxxxxxxx.“.
XXXXX: 32014R0536
22. Za §53 xx vkládají nové §53x až 53x, xxxxx xxxxx:
„§53x
Xxxxxxx xxxxxx xxxxxx
(1) Xxxxxx xxxxxx xx složena xx xxxxxx. Xxxxxxx xxxx xxxxxxx z xxxxxxxxx x xxxxxxx zdravotnictví x xxxx bez xxxxxxxxxxxxxx xxxxxxxx. Počet xxxxxx x počet xxxxx xxxxxxxxxxxx skupin xxxxxx xxxxxx xxxxxxx Xxxxxx xxxxxx xxxxxx. Xxxxxxx xxxxxx komise xxxx xxxxxxxxx xxx, xxx v xxxxx xxxxxxx xxxxxx xxxxxx xxxx xxxxxxx 5 xxxx, x xxxxx xxxxxxx 1 osoba xxxx bez xxxxxxxxxxxxxx xxxxxxxx.
(2) Xxxxx xxxxxx xxxxxx jmenuje x xxxxxxxx xxxxxxx xxxxxxxxxxxxx, x xx xx xxxxxxxxxxxx xxxxxx. Xxxxxxx xxxxxx xxxxxx se xxxxxxxx x xxxxxxxx, xxxxxxxxxxxxx x dalších xxxxx. Xxxxxxxx x xxxxxxxxxxxxx xxxx xxxxxx xxxxx xxxxxxx v xxxxxxx s Jednacím xxxxx xxxxxx xxxxxx.
(3) Xxxxxxx etické xxxxxx xxxx xxxxxxxx požadavky xx. 9 xxxxxxxx x xxxxxxxxx hodnocení x xxxx xxxx xxx xxxxxxxxxxx x xxxxxxxxx xxxxxxxxx a xxxxxxxx xxxxxx x xxxxxxxx xxxxxxxxx x xxxxxxxx etického, xxxxxxxxxx x xxxxxxxxx, x xxxxxxxx xxxxx bez xxxxxxxxxxxxxx xxxxxxxx, xxxxx xxxxxxxx xxxxxx x xxxxxxxx xxxxxxxxx xxxxxxx x xxxxxxxx xxxxxxxx.
(4) Xxxxxxx xxxxxx xxxxxx xx zdrží vyjádření x xxxxxxxx x xxxxxxxx xxxxxxxxxx xxxxxxxxx, xx jehož xxxxxxxxx xxxx osobní zájem, xxxxx x vyjádření x xxxxxxxxx xxxxxxxx x povolení významné xxxxx x xxxxxxxxxx xxxxxxxxx dohledu xxx xxxxxxx xxxxxxxxx xxxxxxxxxx x neprodleně xxxxxx xxxxx xxxxxxxx xxxxx xx xxxxxxxxxxx klinickém xxxxxxxxx xxxxxx komisi x Xxxxxx.
(5) Členové xxxxxx xxxxxx mají xxxxxxxxx xxxxxxxxxx mlčenlivost x informacích a xxxxxxxxxxxxx, xxxxx xx xxxxx x souvislosti xx xxxx xxxxxxxxx x xxxxxx komisi.
(6) Xxxxxx xxxxxx xxxxxx xxxxxx xxx xxxxx, xxxxx se xxxxxxxxx xxxxxxxxx xxxxx §108 xxxx. 8. Dopustil-li xx xxxx xxxxxx xxxxxx xxxxxxxx xxxxxxxxx, xxxx xxxxxxxx v xxxxxx xxxxxx zaniká.“.
CELEX: 32014R0536
§53x
Xxxxxxx xxxxxx komise
(1) Xxxxxxxxxx etické xxxxxx xx xxxxxxxxx x xxxxxxx práv, xxxxxxxxxxx x zdraví xxxxxxxx xxxxxxxxx.
(2) Xxxxxx xxxxxx xxxxxxxxxxx dohled xxx xxxxxxxxx xxxxxxxxxx xx xxxxxxx zprávy x xxxxxxx klinického hodnocení xx xxxxxxxxxxxxx zařízení, x xxxx xxxxxxxx xxxxxxxxx probíhá, (xxxx xxx „xxxxx klinického xxxxxxxxx“) xxxxxxxxxx podle xxxxx xxxxxxx klinické xxxxx zkoušejícím nebo xxxxxxx zkoušejícím. Xxxxxxxxxxx xxxxxx x xxxxxxx xxxxxxxxxx xxxxxxxxx x xxxxxx xxxxxxxxx xxx xxxx předkládání xxxxxxx xxxxxxxxx xxxxxx xxxxxxx.
(3) Xxxxxx xxxxxx xxxx xxx xxxxxxx názoru xxxxxxx další xxxxxxxxx. Xxxx xxxxxxxxx musí xxxxxxxx xxxxxxxxx xx. 9 xxxxxxxx x xxxxxxxxx xxxxxxxxx. Xxxx xxxxxxxxx xxxx povinnost xxxxxxxxxx xxxxxxxxxxx o xxxxxxxxxxx x xxxxxxxxxxxxx, xxxxx se xxxxx x xxxxxxxxxxx se xxxx xxxxxxxx x xxxxxx komisi.
(4) Etická xxxxxx xxxxxxxx svou xxxxxxx v xxxxxxx x Jednacím xxxxx, xxxxx xxxxxxxx xxxxxxx
x) xxxxxx xxxxxxxxx zasedání, xxxxxxxxxx xxxxx xxxxxxx x xxxxxx xxxxxx xxxxxxxx.
x) xxxxxx odvolání xxxxxxxxxxx stanoviska etické xxxxxx.
(5) Etická komise xxxx xxxxxxxx svou xxxxxxx podle pracovních xxxxxxx xxxxxx komise, xxxxx xxxxxxx Ústav x xxxxx xxxxxxxx xxxxxxx
x) xxxxxx posuzování xxxxxxx x xxxxxxxx xxxxxxxxxx xxxxxxxxx x xxxxxxx x xxxxxxxx xxxxxxxx xxxxx klinického xxxxxxxxx x xxxxxxx xxxxxxxxxx nařízením x xxxxxxxxx hodnocení,
b) postupy xxx nakládání x xxxxxxxx xxxxxxxxxxxx nebo xxxxxxxx xxxxxxxxxxxx, xxxx-xx xxxxxxxx, x xxxxxxxxxx x x informacemi xxxxxxxxx xxxxxxxx xxx xxxxxxxxx hodnocením xx xxxxxxxxx xxxxx xxxxxxxx xxxxx xx. 52 xx 54 xxxxxxxx x xxxxxxxxx hodnocení,
c) xxxxxx, jakým etická xxxxxx xxxxxxx Xxxxxx xxx stanovisko ke xxxxxxxxxx xxxxxxxxx včetně xxxx xxxxxxxxxx.
XXXXX: 32014R0536
§53x
Xxxxxxxxxx
(1) Xxx xxxxxxxx xxxxxxxxxx, xxxxxxxxxx xx aspektů, xx xxxxx se xxxxxxxx xxxx I xxxxxxxxx zprávy x xxxxxxx o xxxxxxxx xxxxxxxxxx xxxxxxxxx xxxx xxxxxxx x xxxxxxxx xxxxxxxx změny klinického xxxxxxxxx v xxxxxxx xxxxxxx, xx xxxxx xx xxxxxxxx část X xxxxxxxxx xxxxxx, xxxxxx komise posoudí xxxxxxxx xxxxxxxxxx hodnocení x xxxxxxx
x) opodstatněnosti xxxxxxxxxx hodnocení x xxxx uspořádání,
b) přijatelnosti xxxxxx předpokládaných přínosů x rizik a xxxxxxxxxxxxx xxxx závěrů, x
x) xxxxxxxx xxxxxxx xxxxxxxxxx xxxxxxxxx.
(2) Xxxxxx-xx xxxxxx komise x xxxxxxx x xxxxxxxxx x klinickém xxxxxxxxx xxxxxxxxx stanovisko, je xxxx xxxxxxxxxx závazné x žádost o xxxxxxxx klinického xxxxxxxxx xxxx o povolení xxxxxxxx změny xxxxxxxxxx xxxxxxxxx x Xxxxx xxxxxxxxx Xxxxx xxxxxxxxxxx xxxxxxx. Xxxxxxxxx stanovisko, xxxxxxxx xx xxxxxxx, xx xxxxx xx xxxxxxxx xxxx X xxxxxxxxx zprávy k xxxxxxx x xxxxxxxx xxxxxxxxxx hodnocení xxxx x xxxxxxx x xxxxxxxx významné změny xxxxxxxxxx xxxxxxxxx xxxxxxxx xx xxxxxxx xxxxxxxxx xxxx být xxxxxx xxxxx x důvodů xxxxxxxxx x xxxxxxxx x xxxxxxxxx hodnocení. Xxxxxxxxxx musí xxxxxxxxx xxxxxxxxxx, xx kterém xx xxxxxx xxxxx x popis xxxxxxxxxxx x xxxxxxxxxxxx xxxxxx, xxx xxxxx xxxxxxx xxxxxx komise xxx xxxxxxxxxx. Xx řádné xxxxxxxxxx xxxxxxxxxx a xxxx xxxxxx xxxxxxx Xxxxxx xxxxxxxx xxxxxxxx xxxxxx xxxxxx.
(3) Xxxxxx xxxxxx xxxx před xxxxxxxxx klinického xxxxxxxxx xxxxxxxxxx xxxxxxxx se xxxxxxx, na které xx xxxxxxxx xxxx XX hodnotící zprávy x žádosti x xxxxxxxxx zdůvodněním xxxxx xxxxxxxxxx. Při přípravě xxxxxx stanoviska etická xxxxxx postupuje x xxxxxxx s nařízením x klinickém xxxxxxxxx.
(4) Xxx zpracování stanoviska xxxxxx xxxxxx podle xxxxxxxx 3 skupina xxxxxx komise určená xxx posouzení xxxxxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxx xxxxx xxxxxxxxx xxxxxxxxxxx xxxxxxxxx x klinickém xxxxxxxxx xxxxxxxxxxx předloženou xxxxxxxxx x xxx, xx xxxx xxxxxxxxxxx xxxxxxx x xxxxxxxx, xxx
x) xxxxxxxxxx xxxx xxxxxxxxx odškodnění xxxxxxxx xxxxxxxxx xxx xxxxxx xxxxxxxxx újmy v xxxxxxxx xxxx xxxxxx x xxxxxxxxx hodnocení xxxx xxxxxxxxx xxxxxxxxx xxxxxxxx,
x) xxxxxxxxx xxxxxxxxxxxx xxx xxxxxxxxxx a xxxxxx xxxxxxxxxx, xxxx-xx xxxxxxxx, x xxxxxxxxxx xx xxxxxxxxx xxxxxxxxx xxxxxxxx, xxxxxxxxx zda xxxxxxxxx odpovědnosti zkoušejícího x xxxxxxxx zkoušejících, xxxx-xx xxxxxxxx, nebo xxxxxxxxxx není xxxxxxxx xxxxxx xxxxxxxxxxxxxxxx vztahů,
c) xxxxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxx xxxxxx xxxxxxxxxx subjektem xxxxxxxxx x xxxxxxxxxxx x xxxx xxxxxx x xxxxxxxxx xxxxxxxxx,
x) xxxx xxxxxx pro xxxxxxxx hodnocení xxxxxxxx xxxxxx klinického xxxxxxxxx, x xx xxxxxxx xx xxxxxx k xxx výzkumným výkonům, x xxxxx xxxx xxxxxxx xxxxxxxxx xxxxx xxxxxxxx,
x) je xxxxxxxx xxxxxx zajištění xxxxxx xxx xxxxxxxxxx x xxxxxxxx zkoušejícího, xx-xx xxxxxxx,
x) xxxxxxxxxx x xxxxxx xxxxxxxxxx, xx-xx xxxxxxx, xxxxxxx požadavky xxxxxxxxx x §54,
x) xxxxx xxxxxxxxxx hodnocení xx xxxxxx x xxxxxxxxx předmětného xxxxxxxxxx xxxxxxxxx.
(5) Xxxxxx komise xxxxxxxx x xxxxxxxx xxxxxxx práv, xxxxxxxxxxx x xxxxxx xxxxxxxx xxxxxxxxx kompenzace x xxxxxxx újmy xxxxxxxx xxxxxxxxx x jejich xxxxxx a xxxxxxxxxx xxxxxxxxxxxx, xxxx hlavních xxxxxxxxxxxx, xxxx-xx xxxxxxxx, xxxxxxx v xxxxxxxxxxx x žádosti x xxxxxxxx xxxxxxxxxx hodnocení.
(6) Xx xxxxx xxxxxxxxxx xxxxxxxxxx podle xxxxxxxx 3 a xxxx xxxxxx xxxxxxx Xxxxxx xxxxxxxx xxxxxxxx xxxxxx xxxxxx. Xxxxxxxxxx musí xxxxxxxxx odůvodnění xxxxxxxxxx.
(7) Xxxxxx xxxxxx může xxxxxxx xxxxxx nebo xxxxxxx své xxxxxxxxx xxxxxxxxxx x prováděním xxxxxxxxxx xxxxxxxxx, xxxxxxxx xx xxxxxxxxx xxxx xxxxxxxxxxx podstatné xxx xxxxxxxxxx xxxxxxxx hodnocení xxxx zadavatel xxxx xxxxxx xxxxxxxxxx xxxx xxxxxxxxxx xxxxxx xxxxxxxx xxxxxxxx xxxxxxxx provádění xx xxxxxxxxxx klinického xxxxxxxxx, x xxxxx xxxxxx xxxxxx xxxxxx xxx souhlasné xxxxxxxxxx. Xxxxxx-xx xxxxxx xxxxxx, xx xx xxxxxxxx xxxxxx xxx xxxxxxxx xxxxxx souhlasného stanoviska xxxxxxxxx xx xxxx xxxxx, požádá Ústav, xxx xx vyžádal xxxxxxxxxx zadavatele, xxxxxxxxx xxxxxxxxxxxx nebo hlavního xxxxxxxxxxxx x xxxxx xxxxxxx, x výjimkou xxxxxxx, xxx xx xxxxxxxx bezpečnost subjektů xxxxxxxxx. Odvolání xxxxxxxxxxx xxxxxxxxxx xxxxxx komise xxxxxxxx
x) xxxxxxxxxxxxx údaje x klinickém xxxxxxxxx, xxxxxxx xxxx název, xxxxxxx xxxxxxxxxx nebo xxxxxxxxxx, xxxxxxxx xxxxxxxxxxxxx xxxxx a číslo xxxxxxxxx,
x) xxxxxxxx xxxxxxx, xxx xx jedná x xxxxxxx nebo xxxxxx odvolání souhlasného xxxxxxxxxx, x případě xxxxxxxxx xxxxxxxx souhlasu xxxx xxx stanoveny xxxxxxxx, xx xxxxxxx xxxxxxx xxxxxxxx souhlasu xxxxxxx,
x) xxxxxxxxxx, xx xxxxxx se xxxxxx xxxxxx xxxxxxxx souhlasného xxxxxxxxxx, xxxxxxxx xxx xxxx xxxxxx a xxxxx, xxxxxxx xx xxxxxx xxxxxx xxxxxx,
x) xxxxxxxx xxxxxxxx k xxxxxxxx xxxxxxxxxx xxxxxxxxx, xxxxxxx x převodu xxxxxxxx hodnocení xx xxxxx xxxxx, xxxxxx-xx xxxxxxx již x xxxxxxxxx,
x) xxxxx odvolání xxxxxxxxxxx xxxxxxxxxx x xxxxxx předsedy xxxxxxx xxxxxx komise, která xxxxxxxx vydala.
(8) Xxxxxx xxxxxx xx xx xxxxxxxx Xxxxxx povinna xxxxxx Xxxxxx xxx xxxxxxxxxx ke xxxx xxxxxxxxxx, xxxxx podléhají xxxxxxxxx etickou xxxxxx,&xxxx; xxxxxxxxxx xxxxx pracovní xxx xxxx posledním xxxx lhůty, xxxxxxxxxx Xxxxxx xxx xxxxxx xxxxxxxxx a ověření xxxxxxx, xxxxxxx x xxxxxxxx xxxxxxxxxxx k xxxxxxx, xxxx xxxxxxxxxxxxxx xxxxxxxx, xxxx xxxxxxxxxxx, xxxxxxxxx xxxxxxxxxxxx xxxxxxxxx, xxxxxxxxx xxxxxxxxx xxxxxxx xx obdržení xxxxxxxxxxxx xxxxxxxxx, xxxxxxxxxx xxxxxxx xxxxx I hodnotící xxxxxx xxxx předložení xxxxxxx xxxxx II xxxxxxxxx xxxxxx, v xxxxx posouzení xxxxx&xxxx; xx. 5, 6, 7, 13, 14, 17, 18, 20 x 22 nařízení x xxxxxxxxx xxxxxxxxx.
(9) Xxxxx xxxxxxxx x xxxxxxxxxxx x činností xxxxxx komise xx xxxx 5 let xx ukončení xxxxxxxxxx xxxxxxxxx tyto xxxxxxxxx:
x) xxxxxx z jednání,
b) xxxxxxxxxx x střetu xxxxx,
x) xxxxxxxxxx xxxxx xxxxxx komise,
d) záznamy x xxxxxxxxxx x xxxxxx xxxxxxxxxx xxxxx xxxxxx xxxxxx,
x) xxxxxxxxx x xxxxxxxxx a xxxxxxxx xxxxx xxxxxx xxxxxx,
x) xxxxxxxxx xxxxxxxxxx xx ke xxxxxxxxx, xxxxxxxx xxxxx xxxxxx xxxxxx, xxxxx x xxxxxxxxxx z funkce,
g) xxxxxxxxxxxxxx x obdobné xxxxxxx, xxxxxx xxxxxxxx, xxxxx sloužily k xxxxxx vyhotovení, x xxxxxxxxx xxxxxxxxxxxxxxxx s xxxxxxx komisí, x
x) xxxxxxxxxxxxx xxxxxx xxxxxx.“.
XXXXX: 32014R0536
23. §54 xx 59 včetně xxxxxxxx xxx xxxxx č. 102 a 103 xxxxx:
„§54
Xxxxxxxxxx x xxxxx xxxxxxxxxx hodnocení
(1) Xxxxxxxxxxx x hlavním xxxxxxxxxxx xxxx xxx xxxxx xxxxx xxxx zubní xxxxx splňující podmínky xxxxxxxxx jiným právním xxxxxxxxx29) xxx xxxxx xxxxxx zdravotnického xxxxxxxx, xxxxx xx xxxxxxxx xxxxxxx xxxxxxxx x xxxxxxxxxx s péčí x xxxxxxxx s xxxxxxxxxxx xxxx stavy, xx xxxxxxx xxxxx xx zaměřuje dané xxxxxxxx xxxxxxxxx, a xx xxxxxxxx xxxxxxx xxxxxxxx praxe.
(2) Xxxxxxxx xxxxxxxxx xxx xxxxxxxx xxxxx x xxxxxxxxxxxxx xxxxxxxxxxx služeb xx xxxxxxxxxxxxx xxxxxxxx.
(3) Poskytovatel xxxxxxxxxxx xxxxxx, x xxxxx xx xxxxxxxxx xxxxxxxx xxxxxxxxx, x xxxx dochází x xxxxxxx podání xxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxx, x xxxxxxxxxxxx zdravotních xxxxxx, x xxxxx xx xxxxxxxxx klinické xxxxxxxxx xxx xxxxxxxxx xxxx xxxxxxxxxxxxx efektu xxx subjekty hodnocení, x xx xxxxxxx xxxxxxxxxxxxxxx x xxxxxxxxxxxxxxxx xxxxxxxx xxxxxxxxx, xxxx xxx xxxxxxxxx xxxxxxxxxxx xxxxxxx xxxxxxxx praxe xxxxxxxx Xxxxxxx. Xxxxxx x xxxxxx xxxxxxxxx xxxxxx xxxxxxxxxxx stanoví xxxxxxxxx právní předpis.
(4) Xxx poskytovatele xxxxxxxxxxx xxxxxx neuvedené x xxxxxxxx 3, x xxxxx jsou prováděna xxxxxxxx hodnocení, xxxx xxxxxxx xxxxxxxxxxx xxxxxxx xxxxxxxx xxxxx xxxxxxx; xxxxx xxxx x xxxx vydání xxxxxxx; xxxxxxxx 3 xxxx xxxxx xx xxxxxxx xxxxxxx.
XXXXX: 32014R0536
§55
Xxxxx
(1) Dokumentace xxxxxxxxxx hodnocení xxxx xxx xxxxxxxxxx v xxxxxx xxxxxx, pokud xxx x xxxx xxxxxxxxx:
x) xxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxx,
x) informace xxx pacienta, xxxxxxxxxxx xxxxxxx, xxxxxxx xxxxxxxxxxx x xxxx účastí x xxxxxxxxx hodnocení x xxxxxxx x xxxxx xxxxxxxxxx,
x) xxxxxxxxx x způsobu xxxxxx xxxxxxxx hodnocení x Xxxxx xxxxxxxxx,
x) xxxxxxxx xxxxxxxxx vztahující xx x xxxxxx xxxxxxxxxx xxxxxxxxx,
x) veškeré xxxxxxxxx xxxxxx subjektům xxxxxxxxx,
x) xxxxxx zkoušejících x xxxxxxxx xxxxxxxxxxxx, jsou-li xxxxxxxx,
x) xxxxxx xxxx xxxxxxxxxx xxxxxxxxx,
x) xxxxxx x xxxxxxxxx xxxxxxx xxxx subjektům hodnocení,
i) xxxxxxxxx o xxxxxxx xxxxxxxxx xxxxxxxxxx xxx xxxxxxxxxx a xxxxxx xxxxxxxxxx, xxxx-xx ustaveni, x xxxxxxxxxx nebo xxxxxxxxxx xxx subjekty xxxxxxxxx.
(2) Xxxxxxx xxxxxxxxxxx xxxxxxxxxx xxxxxxxxx, xxxxx-xx x dokumenty xxxxxxx x xxxxxxxx 1, xx xxxxxxxxx x xxxxxx, xxxxxxxxxx nebo xxxxxxxxx xxxxxx.
(3) Informace x xxxxxxxx xx xxxxx léčivých xxxxxxxxx xxx xxxxxxxx xxxxxxxxx xx xxxxxxx x xxxxxx jazyce, není-li x rozhodnutí Ústavu xxxxxxx jinak.
CELEX: 32014R0536
§56
Hodnocené x pomocné xxxxxx xxxxxxxxx
(1) Xxxx-xx xxxxxxx xxxxxxxx stanovené x xx. 59 odst. 2 nařízení o xxxxxxxxx xxxxxxxxx, xxxxx xxx xx xxxxx Xxxxx xxxxxxxxx použity xxx xxxxxxxxx xxxxxxxxx x neregistrované xxxxxx xxxxxxxxx.
(2) Xxxxxxxxx xxxxxxxxx xxxxxx xxxxxxxxx xxxxxx xxxxxxxxx, xxxxxxx léčivé xxxxxxxxx xxxxxxxxxxxxxx podle xxxxxx xxxxxx xxxxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxxxxxx x xxxxxxxxxxxx prostředky xxxxxxxx xxx xxxxxxxxx xxxxxxxxxx xxxxxxxxx, xxxxx xxxx xxxxxx k xxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx. V xxxxx xxxxxxxxxx xxxxxxxxx humánních xxxxxxxx přípravků, xxxxx xxxxx xxxxxx notifikovaný xxxxxxxxxxxx xxxxxxxxxx, lze xxxxxx po předchozím xxxxxxxxx Ústavem x xxxxxx xxxxxxxxxxxx prostředek, xxxxx xxxxx xxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxx x zdravotnických xxxxxxxxxxxx. Xx-xx xxxxxxxxxxx xxxxxxxxxx xxxxxxxxx, kterým se xxx xxxxx xxxxxx xxxxxx rozumí poskytovatel xxxxxxxxxxx xxxxxx zřízený xxxx xxxxxxxx xxxxxx xxxx xxxxxxx xxxxxxxxxxxx xxxxxx, xxxxxxx xxxxxx xxxxx a xxxxxxx xxxxxxxx instituce, x xxxxxxxxx xxxxxx přípravky xxxx registrované x Xxxxx republice, xxxx xxxxxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxx povinné.
(3) Xxxx-xx být x xxxxxxxxx hodnocení xxxxxxxxx xxxxxxxx xxxxxxxxx použita xxxxxxxxxxxx xxxxxxxxxxxxxx xxxxx xxxxxx xxxxxx, xxx x souladu s xxxxxxxxx xxxxxxxx x xxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx xxxxx s xxxxxxxxxxx k xxxxxxx x xxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxxxx Státního xxxxx xxx xxxxxxxx xxxxxxxxxx vydané podle §18.
(4) Mají-li xxx x xxxxxxxxx xxxxxxxxx xxxxxxxxx léčivých xxxxxxxxx xxxxxxx přípravky xxxxxxxxxx xxxxxxxxx xxxxxxxxxxxx organismy, xxxxxxxx xxxxxxxxx spolu x xxxxxxxxxxx x xxxxxxx x xxxxxxxx xxxxxxxxxx xxxxxxxxx souhlas Xxxxxxxxxxxx xxxxxxxxx prostředí xxxxxx podle jiného xxxxxxxx xxxxxxxx11).
(5) Xxxx-xx xxx x xxxxxxxxx xxxxxxxxx humánních léčivých xxxxxxxxx xxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxx xxxxxxxxxxx xxxxxxx xxxxx, předloží xxxxxxxxx spolu x xxxxxxxxxxx x xxxxxxx x xxxxxxxx klinického xxxxxxxxx povolení k xxxxxxxxx s xxxxxxxx xxxxxxxxxxxxx kmenovými xxxxxxx xxxxxx Xxxxxxxxxxxxx xxxxxxxx, xxxxxxx x xxxxxxxxxxx xxxxx xxxxxx xxxxxxxx xxxxxxxx102).
(6) Xxx klastrová xxxxxxxx xxxxxxxxx xxxx xxxxxxxxxxxxxxxx klinická hodnocení xxxxx xx. 2 xxxx. 3 xxxxxxxx x klinickém hodnocení xxxxxxxxx xxxxxxxxxxxx zadavateli, xxxxx xxxxxxx xxxxxxxxx xxx xxxxxxxxxx xxxx xxxxx registrace léčivého xxxxxxxxx, stanoví xxxxxxxxx xxxxxx xxxxxxx xxxxxxxxx xx monitorování, xxxxx xxxxxxxxxx xxxxxxxxx x xxxxxxxxx xxxxxxxxxx hodnocených xxxxxxxx xxxxxxxxx. Klastrovým xxxxxxxxx hodnocením podle xxxx xxxxx xx xxxxxx xxxxxxxx hodnocení xxxxxxxxx pouze na xxxxx Xxxxx xxxxxxxxx, xxxxx cílem je xxxxxxxxx xxxxx skupin xxxxxxxx, x xxxxx xxxxxxx xxxx veškeré xxxxxxxxx xxxxxx xxxxxxxxx xxxxxxxxxxxx xxxxx tohoto xxxxxx x Xxxxx xxxxxxxxx x xxxx xxxxxxxxx x souladu xx souhrnem xxxxx x xxxxxxxxx xxxx xxxx xxxxxx xxxxx x přípravku, je-li xxxxxx xxxxxx xxxxxxx xxxxxx s xxxxxx xxxxxxxxx praxí nebo xxxxxxxxxxxx léčebnými xxxxxxx x xxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxx.
XXXXX: 32014R0536
§57
Xxxxxx xx xxxxxxxxxxx
Xxxxx xxxx xx xxxxxxxx stanovených x xx. 42 xxxx. 3 xxxxxxxx x xxxxxxxxx xxxxxxxxx xxxxxxx xx xxxxxxxxxxx xxxxxx, xxxxx xxx xxxx zadavatel podezření xx xxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxx xxxxxx xxxxx Ústavu; x xxxxxxx případě ohlásí xxxxxxxxx na závažné xxxxxxxxxxx nežádoucí xxxxxx xxxxxxxx Xxxxx.
XXXXX: 32014R0536
§58
Xxxxxx xxxxxxx xxxx vzniklé xxxxxxxx xxxxxxxxx
(1) Xxxxxxx-xx xxxxxxxx klinického xxxxxxxxx x xxxxxxxx xxxxxxxxx xxxxxxxxxx hodnocení majetková xxxx xxxxxxxxxxx xxxx, x xx xxxxxxx xx životě xxxx xx zdraví, je xxxxxxxxx povinen xx xxxxxxxx x xxxxxxx x jinými xxxxxxxx xxxxxxxx 103). Xxxxxxx xxxx xxx xxxxxxxx x xxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxxxxxxxx xxxxxxxxxxx xxxxxx, xxxxx je xxxxxx xxxxxxxxxx xxxxxxxxx.
(2) Xxxxxxxxx xx xxxxxxx mít xx xxxxx xxxx xxxxxxxxx xxxxxxxxxx hodnocení xxxxxxxx xxxxxxxxx odpovědnosti xxx, xxxxxxxx xxxxxxxxxxxx, xxxx-xx xxxxxxxx, a xxxxxxxxxxxx xx újmu xxxxxxxx subjektu xxxxxxxxx x xxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxx.
(3) Xxxxxxxx 2 se nepoužije, xxxxxxx-xx xxxxxxxx xxxxxxxxx xxxxxxxxxx zadavatel, xxxxx xxxxxxxxx činnosti xxxxxxx xxxxxxx léčivých xxxxxxxxx x xxxxx klinického xxxxxxxxx,
x) x xxxxxxxx xxxxxxxxx xxxxxxxxxxxxxx podle xxxxxx xxxxxx x Xxxxx xxxxxxxxx x xxxxxxxxxxx x souladu xx xxxxxxxx xxxxx x přípravku, popřípadě x léčivými xxxxxxxxx xxxxxxxxxxxxxx xxxxx xxxxxx xxxxxx x Xxxxx xxxxxxxxx x používanými xxxx xxxxxx xxxxx x přípravku, xx-xx xxxxxx způsob xxxxxxx xxxxxx x xxxxxx xxxxxxxxx xxxxx xxxx xxxxxxxxxxxx xxxxxxxxx xxxxxxx x xxxxxxxxxx xxxxxxxxx xxxxxxxxx poznatky, x xxxxxxx
x) xxxxxxxxx xxxxxxxxxxxx xxxx xxxxxxxxxxxx postupy xxxxxxxxxxxxx x xxxxxxxxx x xxxxxx xxxxxxxxx xxxxx větší xxx xxxxxxxxx xxxxxxxxx xxxxxx xxxx xxxxx xxx xxxxxxxxxx xxxxxxxx hodnocení.
CELEX: 32014R0536
§59
Xxxxxxxxxx
Xxxxxx-xx zadavatel x xxxxxxx předložené xxxxx xxxxxxxx x klinickém xxxxxxxxx svého xxxxxxxx xxxx xxxxxxxxx osobu, xxxxxxxx xx xxxxxx xxxxxxxx xx xxxxxxxxx xxxxxxxxxx xx základě xxxx moci, neprokáže-li xxxxxxxxx xxxx xxxxxxxx xxxx.
XXXXX: 32014R0536
24. X §60 xxxx. 3 xxxx. x) se xxxxx xxxxxxxxx xxxxxx a xxxxxxx d) xx xxxxxx xxxxxxxx xxx xxxxx x. 64 xxxxxxx.“.
25. V §62 xxxx. 1 xx xx xxxx xxxxx, xxxxx „xx xxxxxx xxxxxxxxxx xxxxxxxxx x“ xxxxxxx.
26. V §64 xxxx. x) xx xxxxx „§55 a xxxxxxxxxxx x rámci xxxxxx x xxxxxxx x xxxxxxxx xxxx xxxxxxxx klinického xxxxxxxxx“ xxxxxxxxx xxxxx „nařízení x klinickém xxxxxxxxx x xxxxxxxxxxx x xxxxx xxxxxx x xxxxxxx x povolení xxxxxxxxxx hodnocení xxxx x xxxxxxxx xxxxxxxx xxxxx klinického xxxxxxxxx“.
XXXXX: 32014R0536
27. X §64 xxxx. x) xx xxxxx „včetně xxxxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx,“ xxxxxxx.
28. V §66 xx xxxxxxxx 4 xxxxxxx.
Xxxxxxxxx odstavec 5 xx xxxxxxxx jako xxxxxxxx 4.
29. V §70 xxxx. 1 xx xx xxxx první xx slovo „předpisem“ xxxxxxxx xxxxx „x xxxxx xxxxxxxxxxx xxxxxxxxx Xxxxxxxx xxxx101)“ a xx xxxxx „xxxxx“ xx vkládají xxxxx „xxxxxx léčivých xxxxx xxxxxxxx pro xxxxx“.
XXXXX: 32014R1252
30. X §70 xx doplňuje odstavec 7, xxxxx xxx:
„(7) Xxxxxxx xxxxxxxx látek, xxxxx xxxxxxx xxxxxx, xxxxxxxxxxx, označování, přeznačování, xxxxxxxx jakosti xxxx xxxxxxxxxxx, jakož x xxxxxxxxxxx kontroly xxxxxxxx xxxxx xxxxxxxxxxxxx ze xxxxxxx xxxx xxxxxxxx xxx xxxxxxxx xxxxxxxx xxxxxxxxx, xxxx mít x xxxxxxxxx dokumenty xxxxx odstavce 2; xxx nejsou xxxxxxx xxxxxxxxxx xxxxxxxx 4 x 5.“.
XXXXX: 32014R1252
31. V §77 xxxx. 1 xxxx. x) xx xxxxx „xxxxxx údajů x xxxxxx xxxxxx xxxxxxxxxxx xxxxxx hlášení zveřejní Xxxxx nebo Xxxxxxxxxxx xxxxx xx xxxx xxxxxxxxxxx prostředku“ xxxxxxxxx xxxxx „xxxxxxxxxxx údaje xxxxxxxx xxxxxxxxxxxx distributora, xxxxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxxx xxxxxxxxx a identifikaci xxxxx podle písmene x), které xxx xxxxxx xxxxxxxxx distribuován; xxxxxxxxx xxxxx, formu, xxxxxx x xxxxxx xxxxxxxx xxxxxx poskytování xxxxxxxxxxxxxxx elektronického xxxxxxx xxxxxxx xxxxxxxxx xxxxxx xxxxxxx“.
32. V §77 xxxx. 1 xxxx. x) xx xx xxxxx „xxxxxxxx x Xxxxx xxxxxxxxx“ vkládají xxxxx „; x xxxxxxx, xx provozovatel xxxxxxxxx xxxxxxx xxxxxx xxxxxxxxx xxxxxx distributora x xxxxxxx xxxxxxxxxxxxxx xxxxxxxx přípravku, xxxxx xx xxxxxxxxxxxxx x xxxxx x období xxxxxxxxxxx 6 xxxxxxxxxxxx xxxxxx prokazatelně xxxxxxxxxxxx, xx xxxxxxxxxxx xxxxxxx xxxxxxxx xxxxxx xxxxxxxxxxxxx xxxxxxxxxxx xxxxxxx xxxxxxxxxxxxxx xxxxxxxx přípravku do 48 xxxxx od xxxxxxxx jeho požadavku; xxxx xx xxxxxxx xxxxxxxxxx x xxxxxxx x xxxxxxxxx obecné xxxxxx xxxxxxx Xxxxxxxxxxxxx xxxxxxxxxxxxx xx xxxxxx xxxxxxxxx dostupnosti xxxxxxxx xxxxxxxxx podle §77x, xxxxxx xx omezuje xxxx xxxxxxxx xxxxxxxxxx xxxxxxxx přípravků xx xxxxxxxxx.“.
33. X §77 xx xx xxxxx xxxxxxxx 1 xxxxx xxxxxxxxx xxxxxx x xxxxxxxx xx xxxxxxx x), xxxxx zní:
„q) x xxxxxxx, že xx xxxx záměrem xxxxxxxxxxxx xx xxxxxxxxx xxxxxx xxxxxxxxx, xxxxx xx xxxxxx na xxxxxxx xxxxxxxx přípravků xxxxx §77c, xxxxxxx xxxx xxxxxxxxxx Xxxxxx; xxxxxxxx xx poskytováno xxxxxxxxxxxx a xxxxxxxx xxxxxxxxxxxx distributora, xxxxxxxxxxxx xxxxxxxx xxxxxxxxx, množství xxxxxxxx xxxxxxxxx x xxxxxxx xxxxxxxxxx, název xxxxx xxxxxxxxxx a xxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx; xxxxxxxxx xxxxx uváděných x xxxxxxxx, způsob a xxxxx xxxxxx xxxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxxxxxxxxx xxxxxxx xxxxxxxx stanoví xxxxxxxxx xxxxxx předpis; x xxxxxxx, xx xx xxxxxxxx xxxxxxxxxxxx xxxxxx xx dne, xxxxxx xxxxxx 15 xxx xxx dne, xxx xxxxxxxxxxx xxxxxxx záměr xxxxxxxxxxxx léčivý xxxxxxxxx, xxxxxx xxxxxxxx obecné xxxxxx podle §77x xx xxxxxx x xxxxxx léčivému přípravku, xxxx xxxxxxxxxxx xxxxxxx xxxxxxxxxx xxxxxxxxxx x xxxxxxx xxxxxxxxx xxxxxxx.“.
34. Xx §77x xx vkládají xxxx §77x a 77x, xxxxx včetně xxxxxxx xxxxx:
„§77x
(1) Xxxxx xxxxxxxxxxx xx držitelů xxxxxxxxxx x registraci, xxxxxxxxxxxx x xxxxxxx xxxxxxxxx x xxxxxx xxxxxxxx xxxxxxxxx xx xxxx x České republice x x xxxxxx xxxxxxxx xxxxxxxxx xxxxxxxx x xxxxxxxxx xxx xxxxxxxxxxx zdravotních služeb; xxxx informace xxxxxxxxxx x xxxxxxxxxxx. Xxx xxxxxxxxxx xxxxxxxxx xxxxx xxxx první Ústav xxxxxxxxx, xxx xxxxxxxx xxxxxxxx xxxxxxxxx, xxxxx xxxx nahraditelný xxxxx xxxxxxx přípravkem xxxxxxxxxxxxxx xxxxxxxxx xxxxxxxxxx, xxxx xxxxxxxx přípravků vzájemně xxxxxxxxxxxxxx vzhledem ke xxxx xxxxxxxx vlastnostem, xxxxxxxxxx xxxxxxx xxxxxxxx xxxxxxx xxxxxxxx x Xxxxx republice. Pokud Xxxxx na xxxxxxx xxxxxxxxxxx uvedených xxxxxxxxxxx xxxxx x xxxxxx, xx xxxxxxxx xxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxx xxxxxxxx xxxxxxxxx xxx dostatečně xxxxxxxxx xxxxxxxx potřeby pacientů x Xxxxx xxxxxxxxx x xxxxxxxxxxx xxxxxx xxxxxxxx xxxxxxxxx xxxx xxxxxxxx xxxxxxxxx, kterým xx rozumí xxxxxxxxxxxx xxxxxxx xxxxxxxxxx potřeb xxxxxxxx x České xxxxxxxxx daným xxxxxxx xxxxxxxxxx xxxx xxxxxxxx xxxxxxxxx, xxxx ohrožena xxxxxxxxxx x xxxxxxxx xxxxx xxxxxxxx v Xxxxx xxxxxxxxx x xxxxxx dopadem na xxxxxxx xxxxxx xxxxxxxxxxxx x významným xxxxxxxxxx xxxxxxxxxxx xxxxxxxxxxx xxxxxx, xxxxx Xxxxxxxxxxxx xxxxxxxxxxxxx xxxx xxxxxxxxx, x xx xxxxxx podkladů x informací, xx xxxxxxx xxxxxxx Ústav x xxxxxx xxxxxx xxxxx.
(2) Xxxxx po xxxxxxxxxxx xxxxxxxxx xxxxxxxxxxxx Xxxxxxx xxxxx xxxxxxxx 1 xxxxx Ministerstvo xxxxxxxxxxxxx x xxxxxx xxxxxxxxx x xxxxxxxx 1 xxxx xxxxx, xxxxxx xxxxxx xxxxxx xxxxxxxxx xxxx xxxxxx xxxxxxxxx na seznam xxxxxxxx xxxxxxxxx, xxxxxxx xxxxxxxxxx do xxxxxxxxx xxxx distributoři xxxxxxxxx xxxxxx Ústavu podle §77 xxxx. 1 xxxx. x) (xxxx xxx „Seznam“). Xxxxxxxxxxxx xxxxxxxxxxxxx xxxx Xxxxxx, xxxxx zveřejňuje v xxxxxxxxx xxxxx xx xxxxx internetových stránkách. Xxxxxx xxxxxxxxx xx xx Xxxxxx xxxxxxxx xxxxxx xxxxxxxx xxxxxx xxxxxx.
(3) Při xxxxxxxx xxxxxxxx xxxxxx povahy xxxxx xxxxxxxx 2 xx postupuje podle xxxxxxxxx xxxx s xxx, že
a) xxxxx xxxxxxxx xxxxxx povahy xx doručuje x xxxxxxxx xxxxxx xxxxxx xx xxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxxx přístup,
b) xxxxx pro xxxxxxxxx xxxxxxxxxx k xxxxxx xxxxxxxx obecné xxxxxx xxxx 5 xxx xxx xxx xxxx xxxxxxxxxx,
x) xxxxxxxx xxxxxx xxxxxx xxxxxx xxxxxxxxx xxxx xxxxxxxxxxxx xx xxx xxxx zveřejnění.
(4) X případě, že Xxxxx xxxxxxxx podle xxxxxxxx 1 xxxxx x závěru, xx x xxxxxxxx xxxxxxxxx xxxxxxxxx na Xxxxxxx xxx xxxxxxx xxxxxxxxx xxxxxxxxxxxxxx pokrytí xxxxxxxxxx xxxxxx xxxxxxxx v Xxxxx republice, xxxxx xxxx xxxxxxxxx xxxxxx xxxxxxxx, xx xxxxxxx xxxxx x xxxxxx xxxxxx xxxxx, Ministerstvu xxxxxxxxxxxxx. Pokud Xxxxxxxxxxxx xxxxxxxxxxxxx na xxxxxxx xxxxxxxxxxx informací mu xxxxxxxxxxxx xxxxx xxxx xxxxx dojde ke xxxxxxxx závěru, xxxxxxxx xxxxx xxxxxxxx 2 x 3 xxxxxx xxxxxxxxx xx Xxxxxxx xxxxxx.
§77x
Xxxxxxxx x xxxxxxxxx xxxxxxxxxxx léčivých xxxxxxxxx
(1) X xxxxxxx, že Xxxxx xxxxxx s xxxxxxxxxxxx x údajům xxxxxxxxxxxx xxxxxxx od xxxxxxxx rozhodnutí x xxxxxxxxxx, distributorů a xxxxxxx, xxxxx uskutečněním xxxxxxxxxx xx xxxxxxxxx x následujícím xxxxxxxxxxx xxxxxx x xxxxxxxxxx xxxxxxxx přípravku, který xxxx xxxxxxxxxxxx jiným xxxxxxx xxxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxx xxxxxxxxxx, xxxx xxxxxxxx xxxxxxxxx, xxxxx xxxx vzájemně xxxxxxxxxxxx xxxxxxxx xx svým xxxxxxxx xxxxxxxxxxx, xxx xxxxxxxx xxxxxxx pacientů x Xxxxx xxxxxxxxx x xxxxx xxxxxxxxxx xxxxxxxx dostupnost x xxxxxxxx léčby xxxxxxxx x České xxxxxxxxx x xxxxxx xxxxxxx xx xxxxxxx xxxxxx xxxxxxxxxxxx a xxxxxxxxx xxxxxxxxxx poskytování zdravotních xxxxxx, xxxxx Ministerstvu xxxxxxxxxxxxx podnět x xxxxxx xxxxxxxx podle xxxxxxxx 3.
(2) Podnět Xxxxxx xxxx obsahovat xxxxxxxxxx xxxxxxxx xx xxxxxxxxxxx údajů shromážděných xxxxxxx xx xxxxxxxx xxxxxxxxxx o xxxxxxxxxx, xxxxxxxxxxxx x lékáren, xx
x) xx zřejmé, xx aktuální zásoba xxxxxxxxxxx xxxxxxxx přípravku xxxx xxxxxxxx xxxxxxxxx xxx xxxxxxxxx xxxxxxxx xxxxxxx xxxxxxxx v Xxxxx republice, a
b) xxxxxxxx xxxxxxxxx důvody, xxx xxxxx by xxxxxxxxxxx distribuce předmětného xxxxxxxx xxxxxxxxx xxxx xxxxxxxx xxxxxxxxx xx xxxxxxxxx xxxxx x xxxxxxx zhoršení xxxxxxx xxxxxxxxxx xxxxxx xxxxxxxx x Xxxxx republice.
(3) Xxxxxxxxxxxx zdravotnictví xxxx xxxxx x zajištění xxxxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxx obecné xxxxxx, xxxxxx xxxxx xxxx xxxxxx xxxxxxxxxx xxxxxxxxxxx léčivého přípravku xx léčivých xxxxxxxxx xx zahraničí. Xxx xxxxxx xxxxxxxx opatření xxxxxx xxxxxx xxxx xxx splněny tyto xxxxxxxx:
x) xxx o xxxxxx xxxxxxxxx, xxxxx xx uveden xx Xxxxxxx,
x) xxxxxxxxxx do xxxxxxxxx xx mohlo xxxxx x xxxx, xx objem xxxxxxxxxxx xxxxxxxx přípravku, xxxxx xxxx xxxxxxxxxxxx xxxxx xxxxxxx přípravkem odpovídajících xxxxxxxxx vlastností, xxxx xxxxxxxx přípravků, xxxxx xxxx vzájemně nahraditelné xxxxxxxx xx xxxx xxxxxxxx vlastnostem, xx xxxx x Xxxxx xxxxxxxxx nepokrývá dostatečně xxxxxxxx xxxxxxx xxxxxxxx x Xxxxx republice, x
x) veřejný zájem xx xxxxxxx xxxxxx xxxxxxxxxxxx x xx xxxxxxxxx dostupnosti xxxxxxxx xxxxxxxxx xxx xxxxxxxx xxxxxxx xxxxxxxx x Xxxxx xxxxxxxxx xxxxxxxxx xxx xxxxxxxxxxxxx xxxxxx xx uskutečnění xxxxxx xxxxxxxxxx do zahraničí.
(4) Xxxxxxxxxxxx zdravotnictví xxxxxxxxxx xxxxx xxxxxxxx xxxxxx xxxxxx, xxxxxxx-xx xxxxxx xxxx xxxxxx.
(5) Xxx xxxxxxxx xxxxxxxx xxxxxx xxxxxx xxxxx xxxxxxxx 3 xx xxxxxxxxx xxxxx §77x odst. 3 s tím, xx opatření xxxxxx xxxxxx nabývá xxxxxxxxx xxxx x xxx xxxxxxxx.
(6) Pokud Xxxxx xxxxxx, že xxx xxxxxxxxxxxxx xxxxxx xxx xxxxx xxxxxx opatření xxxxxx xxxxxx xxxxxxx xxxxxxx distribuce xx xxxxxxxxx x xxxxxxxxxxx xxxxxxxx přípravku xxxx xxxxxxxx přípravků, xxxx x xxx Ústav xxxxxxxxxxx xxxxxxxxx Ministerstvu xxxxxxxxxxxxx xxxxxxxx x xxxxxxxx, které jej x xxxxxx závěru xxxxx.
(7) Ministerstvo zdravotnictví, xxxxx xx z xxxxxx činnosti xxxxx x xxxxxx nedostatku xxxxxxxx přípravků, požádá Xxxxx x poskytnutí xxxxx x xxxxxxx xxxxx §77x.“.
35. X §80 xx xx xxxxx xxxxxxxx 1 doplňuje xxxx „Předepisující xxxxx xx xxxxxxx xxxxxx xxxxxxxxxx identifikační xxxx, xx jehož xxxxxxx xxx xxxxxxxx xxxxxxxxxxxx xxxxxx x xxxxxxxxxx xxxxx xxxxxx xxxxxxxxxxxx xxxxxxxx xxxxxxxxx.“.
36. X §82 xxxx. 3 xxxx. x) xx xx xxxxx „o xxxxxxxx xxxxxxxx xxxxxxxxxxx“ xxxxxxxx xxxxx „, x xx xxxxxxxxxxxx“, x xxxxx „rozsah údajů x xxxxxx xxxxxx xxxxxxxxxxx formou xxxxxxx xxxxxxxx Ústav xx xxxx xxxxxxxxxxx xxxxxxxxxx“ xx xxxxxxxxx xxxxx „xxxxxxxxxxx xxxxx xxxxxxxx xxxxxxxxxxxx xxxxxxxxxxxxx xxxxxxxxxxx x výdeji, identifikaci xxxxxxxxxxxxxxx xxxxxx, xxxxxxxxxxxx xxxxxxxx, kterému xxx xxxxxxxxx vydán, x xxxxxxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx; xxxxxxxxx údajů, xxxxxx, xxxxx x xxxxxx xxxxxxxx xxxxxx xxxxxxxxxxx xxxxxxxxxxxxxxx elektronického xxxxxxx stanoví xxxxxxxxx xxxxxx xxxxxxx“.
37. V §82 xxxx. 4 xx xxxx xxxxx xx xxxxx „xxxxx xxxxxxxx xxxx“ a „odebírající xxxxxxx xxxx“ xxxxxxx.
38. V §82 xxxx. 4 xx xxxx druhé xx xxxxx „výjimečně“ xxxxxxx x za xxxxx „xx xxxx xxxxxxx“ xx xxxxxxxx xxxxx „xxxxx xxxxxxxxx, x xx“.
39. V §101 xxxx. 1 zní:
„(1) Xxx xxxxxxxx xxxxx xxxxxx xxxxxx xxxxxxxxx xxxxxx xxxxxxxxxxxx xxxxxx xxxxxx uvedené x §10 a xxxxxxxxxx xxxxx xxxxxxxxxxx řádu. Xxxxxxxx xx xxxxxxxx xx formu xxxxxxx xxxxxxxxxx. Xxxxxxxxx xx xxx xxxxxx kontrolní xxxxxxxx podle xxxxxx xxxxxx x xxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxxx.“.
40. X §101 xxxx. 5 písmeno x) xxx:
„x) v xxxxxxxxxxxx případech, zejména x xxxxxxx xxxxxxxxx xxxxxxxx léčivého xxxxxxxxx xxxx v xxxxxxx xxxxxxxxx podezření, xx x xxxxxxx xxxxxxxxxx xxxxxxx xxxxx, xxxxx x xxxxxx xxxxxxxx xxxx podle tohoto xxxxxx oprávněna, xxxxxxx xxxx xxxxxxx xxxxxxxxx; x xxxxx postupem xxxxxxx xxxxxxxxx xxxxxxxxxxxxx xxxxx x xxxxx xx úřední xxxxxx x xxxxxxxx xxxxxxxxx x uvedením xxxx xxxxxx, xxxxxx x xxxxxxxx xxxxxxxxxxx léčivých xxxxxxxxx; xxxxx úřední xxxxxx je xxxxxxxx xxxxxxxxx o kontrole; xxxxxxxxxxxx xxxxx xx xxxxxxx zajištěný xxxxxx xxxxxxxxx xxxxxxxxxxxx xxxxx; x případě, že xxxxxxxxxxxx osoba vydání xxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxx, xxxxxxx xxxxxxxxx xxxx odnětí; o xxxxxx, xxxxxxxx xxxxxx xxxxxxxx xxxxxxxxx xxxxxx xxxxxxxxx xxxxxx xxxxxx, xxxxx xx xxxxxxxx xxxxxxxxx o xxxxxxxx; xxxxxxx-xx xxxxx xxxxxxxxx xxxxxxxxx xxxx xxxxxxx-xx xx, že xxxxxxxxx xxxxxx přípravky xxxxxxx xxxxxxxxx xxxxxx xxxxxx, xxxxx Xxxxx nebo Xxxxxxxxxxx xxxxx xxxxxxxxxxxx xxxxx zajištěné xxxxxx xxxxxxxxx v neporušeném xxxxx; xxxxxxx se xxxx xxxxxxxxx, xxxxxxx-xx xx, xx v xxxx xxxxxxxxx x xxxxxxx xxxxxxxxxx x xxxxxxxx xxxxxxxxx x xxx xxxxxx xxxxx xxxxxxxxx xxxx xxxxxxx-xx xx, že xxxxxxxxx xxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxx xxxxxx; x takovém případě xxxx Ústav xxxx Xxxxxxxxxxx xxxxx xxxxxxxxxx x xxxxxxxxxx xxxx xxxxxxx xxxxxxxx xxxxxxxxx; xxxxxx xxxxxxxxx, xx xxxxxxx zachází xxxxx, xxxxx k xxxxxxxx xxxxxxxxx xxxx xxxxxxxxx xxxxx tohoto xxxxxx, xx xxxxxxxx xx xxxxxx xxxxxxxxx, xxxxx xxxxxxxxx xxxxxxxxx xxxxxx xxxxxx; xxxxxxxxxx xxxx xxxxxxx xxxxxx xxxxxxxxx xx Xxxxx xxxx Xxxxxxxxxxx ústav xxxxxxx xxxxxxxxx podle §88; xx dobu trvání xxxxxxxx x x xxxxxxx xxxxxx xxxxxxxxxx x xxxxxxxxxx xxxx xxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxx kontrolované osobě xx xxxxxxxxx, xxxxxxxxxx xxxx zabrané léčivé xxxxxxxxx xxxxxxx; v xxxxxxx xxxxxx xxxxxxxxxx x xxxxxxxxxx xxxx xxxxxxx xxxxxxxx přípravku xx kontrolovaná osoba xxxxxxx uhradit xxxxxxx xxxxxxxxxx Xxxxxxx xxxx Xxxxxxxxxxxx ústavem spojené x xxxxxxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx x xxxxxxxxxxx propadnutých xxxx xxxxxxxxx léčivých xxxxxxxxx, x xxxxxxx výši xxxxxxxx Xxxxx xxxx Xxxxxxxxxxx ústav.“.
41. X §101 xxxx. 5 xxxxxxxxx xxxxx ustanovení xx xxxxx „a) xx x)“ xxxxxxxxx xxxxx „ x) xx x)“.
42. V §103 xxxx. 6 písm. x) se za xxxxx „xx xxxxx“ xxxxxx xxxxx „, xxxx“.
43. V §105 xxxx. 2 xx xx xxxxx xxxxxxx x) xxxxx „xxxx“ xxxxxxx.
44. X §105 xx xxxxx xxxxxxxx 2 xx xxxxx xxxxxxxxx čárkou x xxxxxxxx xx písmena x) xx x), xxxxx xxxxx:
„x) xxxxxxxxx xxxxxxx xxxxxxxx xxxxxxxxx xxxxx §77 xxxx. 1 xxxx. h),
s) x xxxxxxx x §77 xxxx. 1 xxxx. q) xxxxxxx xxxxxxxxxx léčivého xxxxxxxxx xx xxxxxxxxx, xxxx
x) x xxxxxxx x xxxxxxxxx xxxxxx xxxxxx Xxxxxxxxxxxx xxxxxxxxxxxxx xxxxxxx xxxxx §77x xxxxxxxxxxx xxxxxx xxxxxxxxx do xxxxxxxxx.“.
45. X §105 xxxx. 5 xx xx xxxxxxx x) xxxxxx xxxx xxxxxxx x), xxxxx xxx:
„x) xxxxxxxxxx xxxxx x xxxxxx dodávek xxxxxxxx xxxxxxxxx xxxxxxxxx na xxx v Xxxxx xxxxxxxxx podle §33 xxxx. 2 xxxx xxxxxxxx,“.
Xxxxxxxxx xxxxxxx x) xx x) se xxxxxxxx jako x) xx x).
46. X §105 xxxxxxxx 6 xxx:
„(6) Xxxxxxxxx xx xxxxxxx xxxxxxxxx xxxxxxx xxx, xx x xxxxxxx x xxxxxxxxx x xxxxxxxxx xxxxxxxxx
x) provede xxxxxxxx xxxxxxxxx xxx xxxxxxxx xxxx v xxxxxxx x xxxxxxxxxx xxxxxxxxx v povolení,
b) xxxxxxx xxxxxxxxx změnu xxxxxxxxxx xxxxxxxxx xxx xxxxxxxx xxxx x xxxxxxx s podmínkami xxxxxxxxx v povolení,
c) xxxxxxx klinické xxxxxxxxx x xxxxxxxx situaci x xxxxxxx x xxxxxxxxxx xxxxxxxxxxx pro xxxxxxxxx klinických hodnocení x xxxxxxxxxx xxxxxxxxx,
x) xxxxxxxx
1. xxxxx x xxxxxxxx, xxxxxxxx přerušení, xxxxxxxxx xxxxxxxx, předčasném xxxxxxxx xxxx xxxxxxxx xxxxxxxxxx xxxxxxxxx,
2. xxxxx xxxxxxxx prvního xxxxxxxx xxxxxxxxx x Xxxxx xxxxxxxxx nebo
3. ukončení xxxxxx xxxxxxxx hodnocení x Xxxxx xxxxxxxxx,
x) xxxxxxx shrnutí xxxxxxxx xxxxxxxxxx xxxxxxxxx,
x) xxxxxx xxxxx a xxxxx xxxxxxxxxxxxxxxxx záznamy,
g) xxxxxxxxx xxxxxxx podezření xx xxxxxxx neočekávané xxxxxxxxx xxxxxx xxxx o xxxx xxxxxxxxxxx zkoušející xxxxx neprovede xxxxxxxxxx xxxxxxxxxxxx xxxxxxxx xxxxxxx xx ochranu xxxxxxxx xxxxxxxxx, xxxxxxxxx xxxxxxxxxxxxxxx xxxxxx xxxx xxxxxxxxx xxxxx xxxxx xxxxxxxx xxxxxxxxx xxxxx xxxxxxxxx xxxxxxxxx klinického xxxxxxxxx x souladu x xxxxxxxxxx x se xxxxxxxx xxxxxxx klinické xxxxx,
x) xxxxxxxxx, xxx xxxxxxxxxx x xxxxxxx xxxxx xxxxxxxx xx xxxxxxxxx klinického xxxxxxxxx xxxxxxxxx xxxxxxxx stanovené xxxxxxxxx o xxxxxxxxx xxxxxxxxx, xxxxx xxxxxxxx xxxxxxxxx x §54,
i) xxxxxxxx xxxxxxx porušení xxxxxxxx o xxxxxxxxx xxxxxxxxx, xxxxx xxxxxxxx xxxxx nebo xxxxxxxx xxxxxxxxx xxxx xxxxxxxxxxx x xxxxxx xxxxxxxxxxxxx, xxxxx xxxxxxxx neodkladné xxxxxxxxxxxx xxxxxxxx xxxxxxx xx ochranu xxxxxxxx xxxxxxxxx,
x) xxxxxxxxxx xxxxxxxxxxxx xxxxxx xxxxxxxxx pro xxxxxxxxxxxx nebo xxxxx xxxxxx xxxxxxxxxxxxx,
x) xxxxxxxxxxxxx, xxxxxxxxxx nebo xxxxxxxxxx xxxxxxxxx x klinickém xxxxxxxxx xxxx xxxxxx xxxx nearchivuje xxxxxxxx xxxxxxxx klinického hodnocení x xxxxxxx x xxxxxxxxxx xxxxxxxxxxx xxxxxxxxx x klinickém xxxxxxxxx, xxxx
x) xxxx xxxxxxxxxx xxxxxxxxx xxxx x xxxxxxxxxx hodnocení xxxxxxxx xxxxxxxxx xxxxxxxx.
XXXXX: 32014R0536
47. X §105 xx xxxxxx nový xxxxxxxx 7, který xxx:
„(7) Zadavatel xx xxxx xxxxxxx xxxxxxxxx xxxxxxx tím, xx
x) x xxxxxxx s §58 odst. 2 xxxxx po celou xxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxxxx své, hlavního xxxxxxxxxxxx x xxxxxxxxxxxx xx xxxx xxxxxxxx xxx xxxxxxxxx klinického xxxxxxxxx xxxx nezaplatil xxxxxxxx,
x) xxxxxx klinické xxxxxxxxx xxxxxxxxxxxxx léčivého xxxxxxxxx x rozporu x §60 xxxx. 3,
x) xxxxxxxxx provádění xxxxxxxxxx xxxxxxxxx xxxxx §61 xxxx. 2 xxxx. a),
d) nesplní xxxxxxxxxx povinnost xxxxx §61 xxxx. 2 xxxx. x), nebo
e) xxxxxxxxxx xxxxxxxxxxxx léčivé xxxxxxxxx nebo xxxxxxxx xxxxxx vzorek xxxxx §61 odst. 2 xxxx. x).“.
Xxxxxxxxx xxxxxxxx 7 x 8 xx xxxxxxxx xxxx xxxxxxxx 8 x 9.
XXXXX: 32014R0536
48. X §106 xxxxxxxx 3 zní:
„(3) Xxxxxxxxxxx xxxxxxx xxxxx xx xxxxxxx správního xxxxxxx xxx, xx x xxxxxxx x xxxxxxxxx x xxxxxxxxx xxxxxxxxx
x) jako xxxxxxxxxx, xx-xx x xxxxx xxxxxxxxxx xxxxxxxxx pouze xxxxx zkoušející, xxxx xxxx xxxxxx xxxxxxxxxx, xx-xx v xxxxx xxxxxxxxxx xxxxxxxxx xxxx xxxxxxxxxxxx,
1. nezajistí xxxxxxxxx xxxxxxxxxx xxxxxxxxx v xxxxx xxxxxxxxxx xxxxxxxxx,
2. xxxxxxx xxxxxxx xxxxxxxx xxxxxx týmu zkoušejících xxxxxx,
3. xxxxxx xxxxxxxx xxxxxxxxx bez udělení xxxxxxxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx nebo xxxx xxxxxxxxx xxxxxxxx x xxxxxxxx xxxx xxxxxxx, xxx tento xxxxxxx xxxx vyžadován, nebo xxxxxxxxx xxxxxxx x xxxxxx xxxxxxxxx xxxxx, xxxx-xx xxx xxxx xxxxxxxx hodnocení xxxxxxxxxx,
4. xxxxxx klinické hodnocení xxx sdělení xxxxxxxxxxx xxxxx xxxxxxxx xxxxxxxxx xxxx xxxx xxxxxxxxx xxxxxxxx,
x) xxxx zkoušející xxxxxxxxxxx, xxxxxxxxxxxxxx nebo xxxxxxxx nežádoucí xxxxxxx xxxx xxxxxxxxxxx xxxxxxxx,
x) xxxxxxxxx xxxxxxxxxx zdrojových xxx a xxxxxxxxxxx xxxxxxxxxx xxxxxxxxx,
x) xxxxxxxx xxx xxxxxxxxx xxxxxxxxxx xxxxxxxxx okamžitá xxxxxxxx x xxxxxxx xxxxxxxx xxxxxxxxx,
x) provádí klinické xxxxxxxxx xxxx xxxxxxxxxx, xxxx xxxxxxx podmínky xxxxxxxxx nařízením x xxxxxxxxx xxxxxxxxx anebo xxxxxxxx xxxxxxxxx v §54, xxxx
x) xxxxxxxxxx xxxxxx xxxxxxx xxxxxxxx xxxxx při xxxxxxxxx xxxxxxxxxx xxxxxxxxx.“.
XXXXX: 32014R0536
49. X §107 xxxx. 1 xxxx. x) zní:
„a) 100 000 Xx, xxx-xx x xxxxxxx delikt xxxxx §105 xxxx. 6 xxxx. x) xxxx 2 nebo 3, §105 odst. 6 písm. x), §106 xxxx. 3 xxxx. x) xxxx x) xxxx §106 xxxx. 5 xxxx. x),“.
50. X §107 xxxx. 1 xxxx. x) xx slova „§106 xxxx. 3 xxxx. x) xxxx x)“ xxxxxxxxx slovy „§106 xxxx. 3 xxxx. x)“.
51. V §107 xxxx. 1 xxxx. x) xx slova „x), x), x), x) nebo x)“ xxxxxxxxx slovy „h), x), x), x) xxxx x)“.
52. X §107 xxxx. 1 písm. x) se xxxxx „§105 odst. 6 xxxx. c), x), x), x) až x)“ nahrazují xxxxx „§105 odst. 6 xxxx. c) xxxx x) xxxx 1, §105 xxxx. 6 xxxx. e), x), x), h), x), x),“.
53. X §107 xxxx. 1 xx xx xxxxx xxxxx xxxxxxx x) xxxxxxxx xxxxx „xxxx §106 xxxx. 3 xxxx. x), x) nebo x)“.
54. X §107 xxxx. 1 xxxx. x) se slova „x), x), x), x), x), x), x), x), u), x)“ nahrazují slovy „x), l), x), x), r), x), x), u), x), x)“.
55. X §107 xxxx. 1 písm. x) xx slova „x), x), g) xxxx x)“ xxxxxxxxx xxxxx „a), x) xxxx l)“.
56. X §107 xxxx. 1 xxxx. x) xx xx xxxxx „§104 xxxx. 7 xxxx. b) xxxx c),“ xxxxxxxx xxxxx „§105 xxxx. 2 xxxx. r) xx x),“.
57. X §107 xxxx. 1 xxxx. x) xx xxxxx „x), e), x), x), x) xxxx x)“ xxxxxxxxx xxxxx „ x), x), x), x), x) xxxx x)“.
58. X §107 xxxx. 2 se xx xxxxx „xxxxx“ xxxxxxxx xxxxx „§105 xxxx. 2 xxxx. x) x“.
59. X §108 xxxxxxxx 5 xxx:
„(5) Xxxxxxx osoba xx xxxxxxx xxxxxxxxx xxx, xx x rozporu x xxxxxxxxx x xxxxxxxxx hodnocení
a) xxxx xxxxxxxxxx xxxx xxxxxx xxxxxxxxxx
1. xxxxxxxxx provádění xxxxxxxxxx xxxxxxxxx x xxxxx xxxxxxxxxx xxxxxxxxx,
2. xxxxxxx xxxxxxx xxxxxxxx xxxxxx týmu xxxxxxxxxxxx xxxxxx,
3. xxxxxx xxxxxxxx xxxxxxxxx xxx udělení xxxxxxxxxxxxx souhlasu subjektu xxxxxxxxx xxxx jeho xxxxxxxxx xxxxxxxx s xxxxxxxx xxxx xxxxxxx, xxx xxxxx souhlas xxxx xxxxxxxxx, xxxx xxxxxxxxx xxxxxxx x xxxxxx xxxxxxxxx xxxxx, xxxx-xx xxx xxxx xxxxxxxx xxxxxxxxx xxxxxxxxxx,
4. xxxxxx xxxxxxxx xxxxxxxxx xxx xxxxxxx xxxxxxxxxxx xxxxx xxxxxxxx xxxxxxxxx xxxx xxxx zákonnému xxxxxxxx,
x) xxxx zkoušející xxxxxxxxxxx, nezdokumentuje xxxx xxxxxxxx nežádoucí příhodu xxxx laboratorní xxxxxxxx,
x) xxxxxxxxx xxxxxxxxxx xxxxxxxxxx xxx x dokumentace xxxxxxxxxx xxxxxxxxx,
x) při xxxxxxxxx klinického xxxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxx x xxxxxxx xxxxxxxx xxxxxxxxx,
x) xxxxxxx klinické xxxxxxxxx xxxx xxxxxxxxxx, xxxx xxxxxxx xxxxxxxx xxxxxxxxx nařízením x xxxxxxxxx xxxxxxxxx xxxxx xxxxxxxx xxxxxxxxx v §54, xxxx
x) xxx xxxxxxxxx klinického xxxxxxxxx xxxxxxxxxx xxxxxx správné xxxxxxxx praxe.“.
CELEX: 32014R0536
60. V §108 xx za odstavec 7 xxxxxx nový xxxxxxxx 8, který xxx:
„(8) Xxxxxxx osoba xx jako xxxx xxxxxx xxxxxx Xxxxxxxx xxxxxx pro kontrolu xxxxx xxxxxxx xxxxxxxxx xxx, xx x xxxxxxx s §53x xxxx. 5 xxxxxx xxxxxxxxx zachovávat xxxxxxxxxxx.“.
Xxxxxxxxx xxxxxxxx 8 x 9 se označují xxxx xxxxxxxx 9 x 10.“.
61. V §108 xxxx. 8 xxxx. x) xx slovo „x)“ xxxxxxxxx slovem „x)“.
62. X §108 xxxx. 8 písm. x) se xxxxx „x) nebo x)“ xxxxxxxxx slovy „b) xxxx x)“.
63. V §108 xxxx. 8 se xx xxxxx textu xxxxxxx x) xxxxxxxx xxxxx „xxxx xxxxxxxx 5 písm. d), x) xxxx f)“.
64. V §108 xxxx. 8 xxxx. x) xx slova „xxxx odstavce 5 xxxx. d)“ xxxxxxx.
65. V §108 xx xxxxxxxx xxxxxxxx 11, xxxxx zní:
„(11) Xx xxxxxxxxx xxxxx xxxxxxxx 8 xx xxxxx zákaz činnosti.“
66. Xx §108 xx xxxxxxxx xxxx §108x x 108x, xxxxx xxxxxx nadpisů xxxxx:
„108x
Xxxxxxxxxx xxxxxxxx přípravku
(1) Xxxxxxxxxx xxxxxxxx xxxxxxxxx xxx xxxxxx, xxxxxxxx xxxxxx přípravek náleží xxxxxxxxx správního xxxxxxx, x
x) xxx xx xxxxxxxx xxxxxxxxx xxxxxxx xxxx xxxx určen, xxxx
x) byl x xxxxxxxxxxx xx xxxxxxxxx xxxxxxxxx deliktu získán.
(2) Xxxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx se xxxxx xxxx.
108x
Xxxxxxx xxxxxxxx xxxxxxxxx
(1) Xxxxxx-xx uloženo propadnutí xxxxxxxx přípravku, xxxxxxxxx x §108x odst. 1 xxxx. a) xxxx x), xxx xxxxxxxxxx o xxxx xxxxxxx, xxxxxxxx
x) xxxxxx xxxxxxxxx xxxxxxxxx xxxxxxx, xxxxxxx nelze xx xxxxxxx delikt xxxxxx,
x) xxxxxxxx xxxxxxxxx správního xxxxxxx xxxx mu xxxxxxxx xxxxx, nebo
c) xxxxxxxx xxxx xxxx.
(2) Xxxxxxxxxx zabraného xxxxxxxx xxxxxxxxx xx stává xxxx.“.
67. X §112 xx xx xxxxxxxx 5 xxxxxx nový xxxxxxxx 6, který xxx:
„(6) Xxxxxxxx-xx xxx xxxxx, převede Xxxxx x prostředků xxxx xxxxxxxx xxxxx xxxxxxxx 5 xx xxxxxxxx xxxx xxxxxxxx xxxxxxxx Xxxxx xxxxxxxxx zřízený xxx Ministerstvo xxxxxxxxxxxxx xxxxxx ve výši xxxxxxxxx xxxxxx.
Xxxxxxxxx odstavce 6 a 7 xx xxxxxxxx xxxx 7 a 8.“.
68. X §114 xxxx. 1 xx xx slova „§24 xxxx. 2, 3, 4, 8 x 9,“ vkládají slova „§33 xxxx. 2,“, xx xxxxx „§67 xxxx. 10 x 11,“ xx xxxxxxxx xxxxx „§77 xxxx. 1 xxxx. f) x x),“ x xx xxxxx xxxxx xxxxxxxx 1 xx xxxxxxxx xxxxx „x §82 odst. 3 xxxx. x)“.
69. X §114 xxxx. 2 xx xxxxx „§51 xxxx. 2 xxxx. x), §52 xxxx. 6, §53 xxxx. 1, 8, 12 x 13, §54 xxxx. 1, §55 xxxx. 7 xx 9, §56 odst. 1 xxxx. x), §56 xxxx. 3 x 7, §57 odst. 2, §58 odst. 8, §59 xxxx. 1“ xxxxxxxxx slovy „§53x xxxx. 2, §54 xxxx. 4, §56 xxxx. 6“.
70. V §114 xxxx. 2 xx xxxxx „§60 xxxx. 2, 4, 5 x 9, §61 xxxx. 2 písm. x) x x) xxxx 1 x 6, §61 odst. 2 xxxx. x), §61 xxxx. 4 xxxx. e),“ xxxxxxx.
71. V §114 xxxx. 2 se xx slova „§77 xxxx. 1 xxxx. x),“ vkládá xxxxx „x),“.
72. V §114 xxxx. 4 xx xx xxxxx „§48 xxxx. 2, 3 x 6“ vkládají xxxxx „, §60 xxxx. 2, 4, 5 x 9, §61 xxxx. 2 xxxx. x) x x) xxxx 1 x 6, §61 xxxx. 2 xxxx. x), §61 xxxx. 4 xxxx. x)“.
Xx. XX
Xxxxxxxxx xxxxxxxxxx
1. Xxxxx byla xxxxxx x xxxxxxxx xxxxxxxxxx hodnocení xxxxxxxxxx Xxxxxxxx xxxxxx xxx xxxxxxxx léčiv přede xxxx, kterým uplyne 6 xxxxxx xxx xxx xxxxxxxxxx xxxxxxxx Xxxxxx v Xxxxxxx xxxxxxxx Evropské xxxx xxxxx čl. 82 xxxx. 3 nařízení Xxxxxxxxxx xxxxxxxxxx a Xxxx (XX) č. 536/2014 xx dne 16. xxxxx 2014 o xxxxxxxxxx hodnoceních xxxxxxxxx xxxxxxxx přípravků x x xxxxxxx xxxxxxxx 2001/20/XX, xxxxxxx xxxxxxxx xxxxxxxxx se xxxxxx xxxx xxxxxxxxxxx xxxxxxxx xxxxxxxx, x xx xx xxx, xxxxxx xxxxxxxx 42 měsíců xxx xxx xxxxxxxxxx xxxxxx xxxxxxxx.
2. Pokud xxxx xxxxxx x povolení xxxxxxxxxx xxxxxxxxx xxxxxxxxxx Xxxxxxxx ústavu pro xxxxxxxx xxxxx xx xxx, kterým uplynulo 6 xxxxxx xxx xxx xxxxxxxxxx xxxxxxxx Xxxxxx podle čl. 82 xxxx. 3 nařízení Xxxxxxxxxx xxxxxxxxxx a Xxxx (XX) č. 536/2014 xx xxx 16. xxxxx 2014 x xxxxxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx x o xxxxxxx xxxxxxxx 2001/20/XX&xxxx; xxxxxxxxxx xxxx do xxx, xxxxxx uplynulo 18 xxxxxx xxx xxx xxxxxxxxxx tohoto oznámení, xxx xxxxxxx xxxxxx x povolení xxxxxxxxxx xxxxxxxxx xxxxxxx podle xxxxxxxxxxx xxxxxxxx xxxxxxxx x uvedené xxxxxxxx xxxxxxxxx se xxxxxx xxxx dosavadními xxxxxxxx xxxxxxxx, x xx xx xxx, xxxxxx xxxxxxxx 42 xxxxxx xxx xxx xxxxxxxxxx xxxxxx oznámení.
XXXX XXXXX
Xxxxx xxxxxx x xxxxxx xxxxxx
Xx. XXX
X §2 xxxxxx x. 234/2014 Xx., x xxxxxx xxxxxx, ve znění xxxxxx č. 131/2015 Xx., xxxxxx x. …/2016 Xx. a xxxxxx č. …/2016 Xx., xx na xxxxx xxxxxxxx 1 xxxxx xxxxxxxxx xxxxxx x xxxxxxxx xx xxxxxxx x), xxxxx xxx:
„x) xxxxx Xxxxxx xxxxxx Xxxxxxxx xxxxxx xxx xxxxxxxx xxxxx.“.
ČÁST XXXXX
Xxxxxxxxx ustanovení
Čl. IV
Technický předpis
Tento xxxxx xxx xxxxxxx x xxxxxxx xx xxxxxxxx Xxxxxxxxxx parlamentu x Rady (XX) 2015/1535 xx xxx 9. září 2015 x xxxxxxx při xxxxxxxxxxx informací x xxxxxxx technických xxxxxxxx x xxxxxxxx xxx xxxxxx xxxxxxxxxx xxxxxxxxxxx, x xxxxxxx znění.
Xx. X
Xxxxxxxx
Xxxxx xxxxx xxxxxx xxxxxxxxx prvním xxxx xxxxxxxxxxxx xxxxxx xxxxxxxxxxxxx xx xxx xxxx xxxxxxxxx, x xxxxxxxx xxxxxxxxxx
x) xx. X xxxx 21, xxxxx xxx x §51, §52 x §53 odst. 2, xx. X bodu 22, xxxxx xxx x §53a odst. 7, §53b xxxx. 1, 2, 3 x §53x xxxx. 1 xx 8, x xx. X xxxx 23, xxxxx xxxxxxxx xxxxxxxxx xxxxxxxxx 6 xxxxxx xxx xxx xxxxxxxxxx oznámení Xxxxxx v Xxxxxxx xxxxxxxx Xxxxxxxx xxxx xxxxx čl. 82 odst. 3 xxxxxxxx Evropského xxxxxxxxxx x Rady (XX) x. 536/2014 xx xxx 16. xxxxx 2014 o xxxxxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxxxx přípravků a x zrušení xxxxxxxx 2001/20/XX; xxx, kdy xxxx toto oznámení xxxxxxxxxx, oznámí Ministerstvo xxxxxxxxxxxxx xxxxxx xxxxxxx xx Xxxxxx xxxxxx;
x) xx. X bodu 21, pokud xxx x §53 xxxx. 1, 3 x 4, a čl. X xxxx 22, xxxxx jde x §53x xxxx. 1 xx 6, §53x xxxx. 4, 5 x §53x odst. 9, xxxxx xxxxxxxx xxxxxxxxx xxxxxx dnem xxxxxxxxxxxx xxxxxx xxxxxxxxxxxxx xx xxx xxxxxxxxxx xxxxxxxx Komise x Xxxxxxx xxxxxxxx Xxxxxxxx xxxx xxxxx čl. 82 xxxx. 3 xxxxxxxx Xxxxxxxxxx xxxxxxxxxx a Xxxx (XX) x. 536/2014 xx xxx 16. xxxxx 2014 x klinických xxxxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx x x xxxxxxx xxxxxxxx 2001/20/ES; den, xxx xxxx xxxx xxxxxxxx zveřejněno, xxxxxx Xxxxxxxxxxxx zdravotnictví formou xxxxxxx xx Xxxxxx xxxxxx;
x) xx. X xxxx 5, 7, 9, 28, 29 x30, xxxxx xxxxxxxx xxxxxxxxx xxxxxx xxxx xxxxxxxx xxxxxxxxxxxx xxxxxx xxxxxxxxxxxxx xx xxxx xxxxxxxxx.
XXXXXXX XXXXXXXXX ZPRÁVY XXX
|
Xxxxx xxxxxx zákona: Xxxxx zákona, kterým xx xxxx zákon č. 378/2007 Sb., x xxxxxxxx x x xxxxxxx xxxxxxxxx souvisejících zákonů (xxxxx o xxxxxxxx), xx znění xxxxxxxxxx xxxxxxxx |
|
|
Xxxxxxxxxxx / zástupce xxxxxxxxxxxxx: Ministerstvo xxxxxxxxxxxxx |
Xxxxxxxxxxxxx xxxxxx xxxxxx xxxxxxxxx: 28.5.2016 |
|
Xxxxxxxxxxxx xxxxx XX: XXX (částečná, tj. x xxxxx adaptace xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Xxxx (EU) č. 536/2014 xx dne 16. xxxxx 2014 x xxxxxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxxxx přípravků x o xxxxxxx xxxxxxxx 2001/20/XX) |
|
|
- xxxxxx xxxxxx xxxxxxxxx xxx xxxxxxxxxxxx: 28.5.2016 - xxxxxx, xxx xxx xxxxx xxx xxxxx požadavků xxxxxxxxxxx xxxxxxxxx EU?: XX |
|
|
2. Cíl xxxxxx xxxxxx |
|
|
Xxxxxxx cílem xxxxxx xxxxxx xx zajistit xxxxxxxx xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Xxxx (XX) č. 536/2014 xx xxx 16. xxxxx 2014 x xxxxxxxxxx xxxxxxxxxxx xxxxxxxxx léčivých xxxxxxxxx x x xxxxxxx xxxxxxxx 2001/20/XX x xxxxxxxxxx České xxxxxxxxx prostřednictvím xxxxxx xxxxxx o xxxxxxxx. Xxxxx upravuje otázky, xxxxx jsou xxxxxxxxx x. 536/2014 xxxxxxxxx xxxxx přikázány xxxxxxx xxxx je xxxxxxx xxxx zmocněn xx xxxxxxx. Cílem xx xxxxxxxxx xxxx, aby xxxxxx xxxxxx x Xxxxx xxxxxxxxx xxxxxx xxxxxxxxx xxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxx humánních xxxxxxxx xxxxxxxxx založený xxx xxxxx Xxxxxxxxx xxxx xxxxxxxxx č. 536/2014. |
|
|
Xxxxxx xxxxxxx xxxxx xxxxxx xxxxxx je xxxxx xxxxxx akutní nedostupnosti xxxxxxxx přípravků xxx xxxxxxx pacientů x Xxxxx xxxxxxxxx za xxxxxx ochrany jejich xxxxxx a xxxxxx, x to xxxxxxxxxx xxxxxxx xxxxxxxxx a xxxxxxxxxxxxx xxxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx xxx xxxxxxx pacientů v Xxxxx xxxxxxxxx a xxxxxxxxx xxxxxxxxxxx opatření xxxxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx určených xxx xxxxxxx xxxxxxxx v Xxxxx xxxxxxxxx do xxxxxxxxx (xxxxxxxx) x xxxx případech, kdy xxxxxxxxxxx takové hrozby xxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxxx. Xxxxxxx je xxxxxx xx nejméně xxxxxxx xxxxxxxxxxxxxx xxxxxxxx x xxxxxxxxxxx xxxxxx xxxxxxx xxxxxx xxxxx xxxxxxxxxx x xxxxxxxxxx Xxxxxxxx xxxx. |
|
|
Xxxx další xxxx xxxxxx zákona xxxxx zajistit xxxxxxxx xxxxxxxx Xxxxxx x xxxxxxxxx xxxxxxxxx (XX) č. 1252/2014 ze xxx 28. xxxxxx 2014 xxxxxxxxxx směrnici Xxxxxxxxxx xxxxxxxxxx x Xxxx 2001/83/XX, pokud xxx x xxxxxx x xxxxxx xxxxxxx xxxxxxx xxxxx pro xxxxxx xxxxx xxx xxxxxxx xxxxxx xxxxxxxxx, dále xxxxxxxx xxxxxxx předpoklady xxx efektivnější spolupráci Xxxxxxxx xxxxxx pro xxxxxxxx xxxxx s Xxxxxxxxxx ředitelstvím cel xx xxxxxx xxxxxxxxxxxx xxxxxxx xxxxx x xxxxxxxxx xxxxxxxxx x xxxx, xxxxxxxx xxxxxxx xxxxxxxxxxx xxxxxxxxxx xxx xxxxxxxxx xxxxxxxx x xxxx zpřesnit xxxxxxx xxxxxx xxxxxxxxx xxxxxxxxx x zabrání xxxxxxxx xxxxxxxxx xxx, xxx xxxx xxxxxxxxxx x xxx xxxxxx xxxxxxx, xxx je xxxxxxxx, xx s nimi xxxxxxxxx xxxxx, xxxxx x xxxx xxxxxx xxxxx xxxxxx xxxxxxxxx. |
|
|
3. Xxxxxxxxxx xxxxxx návrhu xxxxxx |
|
|
3.1 Xxxxxx xx xxxxxx rozpočet a xxxxxxx xxxxxxx xxxxxxxx: XXX |
|
|
Xxxxxx xx xxxxxx xxxxxxxx Xxxxxxxx nařízení xx xxxxxxxxxx xxxxxxxxx Xxxxxxxx xxxxx xxxxxxxxxx xxxxxx xx xxxxxx xxxxxxxx adaptaci xxxxxxxx x xxxxxxxxxx xxxxxxxxxxx humánních léčivých xxxxxxxxx bude představován xxxxxxxxx xxxxxx navýšení xxxxxxxxxx xxxxxx xx xxxxxx Xxxxxxxx xxxxxx xxx kontrolu xxxxx xxx potřeby xxxxxxxxx xxxxxx xxxxx x xxxxxxxxx spojených x xxxxxxxxx (v počtu 32 úvazků). Navýšením xxxxx pracovníků xxxx xxxxx xxxxxxxxxx xxxxx xxxxxx xxxxxxxxxxxxxxx posuzovatelů (5), posuzovatelů xxxxxxxxxxxxx xxxxxxxxx (2), xxxxxxxxxxxx xxxxxxxxxxxxxx dat klinických xxxxxxxxx (1) xxxxxxxxxx (5), koordinátorů xxxxxxxxxx xxxxxxxxx (3), a xxxxxxxxxx xxxxxxxxx technicko-organizačního xxxxxx xxx xxxxxxx xxxxxx - xxx xxxxx 8 skupin xxxxxx xxxxxx - 16 xxxxxx). Tyto xxxxxx xxxxx xxxxxxxx xxxxx z xxxxxxx xxxxxx xx xxxxxxxx xxxxxxxxx (etická xxxxxx). Xxx xxxxxxxx xxxxx xxxxxxxxxxx technického xxxxxxxxxxx xxxxxx xxxxxxx xxxxxx xxxxxx jako poradního xxxxxx Xxxxxxxx xxxxxx xxx xxxxxxxx xxxxx xxxx xxxxxxxxx z xxxxx finanční xxxxxxxxxx x grantu xxxxxxxxxxxx x EU xxxxx, x části xxxx xxxxx x náhrad xxxxxx xx klinická xxxxxxxxx xx certifikáty xxxxxxx klinické xxxxx. |
|
|
Xx xxxxxx Xxxxxxxxxxxx xxxxxxxxxxxxx xxxxxxx nová agenda xxxxxxxxxx xxxxxxxx xxxxx xxxxxxxxxx rozhodnutí x xxxxxxx o xxxxxxxx xxxxxxxxxx xxxxxxxxx. Xxxx xxxxx zabezpečit jednu xxxxxx právního xxxxxxxxx x xxxxx xxxxxx xxxxxxxxx referenta. |
|
|
Omezení xxxxxxxxx |
|
|
Xxxxxxxx xxxxx xxxxxxxxxx právní xxxxxx xx xxxxxx xxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx xx státní xxxxxxxx xxxx představován xxxxxxxxx xxxxxx xxxxxxxx xxxxxxxxxx xxxxxx xx xxxxxx Xxxxxxxxxxxx xxxxxxxxxxxxx (2 úvazky - 1 právní xxxxxxxx x 1 xxxxxxx xxxxxxxx xxx agendu xxxxxxxx opatření xxxxxxxxxxxx xxxxxxxxxx). Na straně Xxxxxxxx xxxxxx pro xxxxxxxx léčiv xxxxx x xxxxxxxx x 2 pracovní xxxxxx xx xxxxxx zajištění xxxxxxxxx a vyhodnocování xxxxxx xxxxxxxxxxxxx léčivých xxxxxxxxx xxx xxxxxxx xxxxxxxx x Xxxxx xxxxxxxxx x xxxxxxxxx xxxxxxxxxxx podnětů Ministerstvu. |
|
|
Ostatní xxxxxxxxxxx body |
|
|
Dopad xxxxxxxxx xxxxxxxxxxxx xxxxxxxxxxxxx bodů xxxxx komplexně xxxxxxxxxxxx. Xxxxx xx x xxxxx xxxxxx zkvalitňující xxxxxxxxx právní xxxxxx (xxxx. xx se xxxx xxxxxxxxxxx xxxxxxxxxx). |
|
|
Xxxxxxxxx xxxxx xx ostatní xxxxxxx xxxxxxxx, xxxxxxx xx xxxxxxxxxx xxxxxxxxx xxxxxxxxxxx xxxxxxxxx nelze xxxxxx xxxxxxxxx, xxxxx xxx xxxxxxxxxxxx, že xxxxx xxxxx xxxx xxxxx xxxxxxxxx. |
|
|
Xxxxxxx |
|
|
Xxxxxxxx xxxxxxxx xx xxxxxxxxxx xxxxxxxxx |
|
|
Xxxxxxxx xxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxxxx hodnocení xxxxxxxx k xxxxxxxxxxx Xxxxx xxxxxxxxx xxx xxxxxxxxx těchto xxxxxxxxx. Xxxxxx xxxxxxxxx se xxx dostanou xxxxxxxxxxxxx xxxxxx xxxxxxxxx v xxxxxxxxxxx xxxxxxx xxxxxx xx xxxxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx rizik. Xxxxxxxxx xxxxxxxxxx xxxxxxxxx na xxxxx Xxxxx republiky xxxxx xxxxxxx České xxxxxxxxx ve světě. Xxxxxxxxx xxxxxx xxx xxxxxxxxxxxx x xx xxxxx xxxxxxxxxx. |
|
|
Xxxxxxx xxxxxxxxx |
|
|
Xxxxxx xxxxxx xxxxxxxxxxx xxxxxxxxxxxxx xxxxx x xxxxxxx xxxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxx efektivně xxxxxxxxxx xxxxx v xxxx xxxxxxxxx, xxx xx xxxxxxxxxx xxxxxxxx xxxxxxxxx zapříčinila nedostupnost xxx xxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx. Přínosem xxx xxxx xxxxxxxxx xxxxxxxx xxxx xxxxx x xxxxxxxxx xxxxxxxx xxxxxx. Navrhovaná právní xxxxxx přispěje ke xxxxxxxxxxx poskytované xxxxxxxxx xxxx, za xxxxxx xxxx xxxxxxxxx xxxxxxx xxxxx, xx se xxxx xxxxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx. Xxxxxxxxx xxxxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxx xxxxxxxxxxx xxxxxxxxxx na xxxxxx xxxx xxxxxxxxxxx xxxxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx. |
|
|
Xxxxxxx xxxxxxxxxxx body |
|
|
Přínosy xxxxxxxxx xxxxxxxxxxxx xxxxxxxxxxxxx xxxx xxx xxxxxxxxxxxx x xxxxxxx xx xx, xx se xxxxx x xxxxx xxxxx, které xxxxxxxxx xxxxxxxxx právní xxxxxx (xxxx. co xx xxxx xxxxxxxxxxx xxxxxxxxxx). |
|
|
3.2 Xxxxxx xx xxxxxxxxxxxxx xxxxxxxx: XXX Xxxxxxxx xxxxxxxx xx klinickému hodnocení |
|
|
Nepředpokládají xx xxxxxxxx negativní xxxxxx xx xxxxxxxxxxxxx xxxxxxxxx x oblasti xxxxxxxxxx hodnocení. Xxxxxx xxxxxxxxxx xxxxxxxxx xxxx xxx xxxxxxxx xxxx xxxxxxxxxxxxx (podávání xxxxxxx xxxxxxxxxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxxxx) x xxxxxxx xx xxxxxx zejména xxxxxxxxx. Dopadem xxx xxxx nutnost xxxxxxxxxxxxxxx xxxxxxxx seznámit xx x novými xxxxxxxxxx xxxxxxxx, xxxxx xxxx x xxxxxxxx xxxxx xxxxxx již x xxxxxxxx. Xxxxxxx xxxxxx xx xxxx agendy xx xxxx xxx xxxxx celkovým xxxxxxxx xxxxxxx výdajů xx xxxxxxxxxx klinických xxxxxxxxx, xxxxx xxxxxxx výdajů xxxx xxxxx xxxxxx xxxxxxx xxxxxxxxxx xxx xxxxxxxxx Xxxxxxx xxxxxxx xxx xxxxxxxx xxxxx, xxx xxxxxxx komisí (xxxx xxxxxxxx xxxxxxxx). |
|
|
Xxxxxxx xxxxxxxxx |
|
|
Xxxxxxxxxxxxx xx dopady xx xxxxxxxxxxxxx prostředí xx směru zavedení xxxxxxxxxx xxxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxx plánovanou distribuci xxxxxxxx xxxxxxxxx určených xx xxxx Xxxxx xxxxxxxxx xx xxxxxxxxx x dále v xxxxxxx xxxxxxx odůvodněné xxxxxxxx xxxxxxxxx xxxxxx xxxxx xxxxxxxxxxx v xxxxxxx xxxxxxxxxx. Xxxxxx xxxxxxxxxx xxxxxx xxxxxx xx distributory xxxxxxxx xxxxxxxxx xxxx xxxx xxxxxxxxxxxxxx zavedením komplexního x transparentního xxxxxxx. |
|
|
Xxxxxx xxxxx navrhovaná xxxxxx xxxxxx opatření xxxxxxxxxxxx xxxxxxxxxx xxxxxxxxxx bude xxx na xxxxxxxx xxxxxxxxxx léčivých přípravků. Xxxxx xxxxx xxxx xxxxxxxxx a xxxxxxx x zavedení xxxxxxxxxx xxxxxxxxxxxx poskytování xxxxx x xxxxxxxx léčivých xxxxxxxxx xxxxxxxx do Xxxxx xxxxxxxxx. X xxxxxxxx době xx xxxxxxxx povinnost xxxxxxx xxxxxxx, xxxxx xxxxxxxxxxx xxxxx nemá v xxxxxx xxxxxx xxxxxx xxxxxxxxx časový xxxxx. X xxxxxxxx xxxxxxxx xxxx xxx xxxxxx xxxxxx xxxxxxx reexportů x xxxxxxxxxx xxxxxxxxx xxxxxxxxx dopad xx xxxxxxxx xxxxxxxxxx o xxxxxxxxxx. Xxxxxxxx xxxxxxxxxx x registraci xxxxxxxx xxxxxx xxxxxxxxx x xxxxxxx xx jednotlivé xxxx xxxx XX. X xxxxxxxxxxxx zemích XX xxxx xxxxxx xxxxx xxxxxxxxx maximální xxxx léčivých přípravků, xx xxxxx xx xxxxx xxxxxxxx xx xxx xxxxxx. Xxxxxxxx xxxxxx při xxxxxxx xxxxxxx xxxxxxxxxxx léčivého xxxxxxxxx profitují xxxx xx trzích x xxxxx cenovou xxxxxxxx. Xxxxx xxxxxx uvažovali, xx xxxxxxxx xx xxxxxxxx xxxxx xx xxxx x xxxxxxxx xxxxxxx hladinou, xxxx xxxxxxx xx xxx xx xxxx xxxxxxxxxxxxx. Xxxxxxxxx xxxxxxxxxx xxxxxxx xx xxxxxx, xx xxxxxxx xx reexportováno, x cenové xxxxxxx, xxx xxxx je xx xxxx xxxxxxxx x registraci ze xxxx xxxxxx: 1. Xxxxxxxx xxxxxxxxxx léčivého xxxxxxxxx může xxxx xx snížení xxxxxxxx xxxxxxxx xxxxxxxxx, xxxxx xxxxx xxxxxxx xxx x za xxxxx xxxx; 2. pokud xx distributorem importován xxxxxxxxx xxxxxxx vlastní xxxxxx přípravek x xxxx xxxx za xxxxx xxxx vede xxxx xxxxxx soutěž x xxxxxxx snížení xxxx takového xxxxxxxx xxxxxxxxx xx daném xxxx xxxx celku. Xxxxxx xx cenová xxxxxx xxxxxxxxxx xxxxxxx, xxxxxxx xxxxxxxxx xxxxxx xx xxxx xxxxxxxx xx držitele léčivých xxxxxxxxx. |
|
|
Xxxxxxx xxxxxxxxxxx xxxx |
|
|
X xxxxxxx xx xx, xx xx xxxxxxx x významné změny, xxxxx xx xxxxxxxxxxxx. |
|
|
3.3 Xxxxxx xx xxxxxx xxxxxxxxxxx xxxxx (xxxx, xxxxx): XX |
|
|
Xxxxxxxxxxxxxxx xx xxxxx xxxxxx na xxxxxx xxxxxxxxxxx celky. |
|
|
3.4 Xxxxxxxx xxxxxx: XX |
|
|
3.5 Xxxxxx xx životní xxxxxxxxx: XX |
|
|
Xxxxxxxxxxxxxxx xx xxxxx xxxxxx xx xxxxxxx xxxxxxxxx. |
|
101) Xxxxxxxx Xxxxxx x přenesené xxxxxxxxx (XX) č. 1252/2014.“.
104) Xxxxxxxx Evropského xxxxxxxxxx x Xxxx (XX) č. 536/2014.“.
102) Zákon č. 227/2006 Sb., x xxxxxxx xx xxxxxxxx xxxxxxxxxxxxx kmenových xxxxxxx x xxxxxxxxxxxxx xxxxxxxxxx x x xxxxx některých xxxxxxxxxxxxx xxxxxx, ve xxxxx xxxxxxxxxx xxxxxxxx.
103) Xxxxxxxxx xxxxxxxx zákoník, xxxxxxx xxxxxxx, zákon č. 101/2000 Sb., xx znění xxxxxxxxxx xxxxxxxx.
Čl. 75 xxxxxxxx Evropského xxxxxxxxxx a Xxxx (XX) x. 536/2014.“.
DŮVODOVÁ XXXXXX
XXXXXX XXXX
X. Xxxxxxxxx xxxxxx x hodnocení xxxxxx xxxxxxxx (XXX)
1. Xxxxx předložení a xxxx
1.1. Xxxxx
Xxxxx xxxxxx, xxxxxx xx xxxx xxxxx č. 378/2007 Sb., x xxxxxxxx x o xxxxxxx xxxxxxxxx xxxxxxxxxxxxx xxxxxx (zákon o xxxxxxxx), xx znění xxxxxx č. 124/2008 Xx., xxxxxx č. 296/2008 Sb., zákona x. 141/2009Xx., zákona x. 281/2009 Xx., xxxxxx x. 291/2009 Xx., xxxxxx č. 75/2011 Xx., xxxxxx x. 375/2011 Sb., xxxxxx x. 50/2013 Xx. a zákona x. 70/2013 Sb.
1.2. Xxxxxxxx xxxxxxxx
X současné xxxx je xxxxxxxxxxxx xxxxxxxxx kvality, účinnosti x bezpečnosti xxxxxxxxx x xxxxxxxxxxxxx léčivých xxxxxxxxx upravena xxxxxxx x xxxxxxxx x xxxx xxxxxxxxxxx xxxxxxxx. Xxxxxx xxxxxxxx předpisy xxxx xx xxxxxxxx xxxx Xxxxx xxxxxxxxx xxxxxxxxxxxxx ustanovení všech xxxxxxxxxxxx právních předpisů x xxxxxxx humánních x veterinárních léčiv, xxxxx xxxx xxxxxxx x Xxxxxxxx xxxx xxxx xxxxxxx xxxxxx xxxxxx.
Xxxxx x xxxxxxxx xxx xxx xxxxxx xxxxxxxxxxxx xxxxxxxxxxx, přičemž xx xx novelu xxxxxx xxxxxxxxxx xxxxxxx č. 70/2013 Sb. xxxxx x xxxxxx xxxxxxxxxx, xxxxx xx zásadním xxxxxxxx xx obsahu xxxxxx xxxxxxx x výrazně xxx měnily; šlo x xxxxxx xxxxxxxx xxxxx, tudíž xxxxxxxxx xxxxx xxxxxx dosud xxxxxxx v původním xxxxx.
Xxxxxxxxxxx návrh xxxxxx xxxxxx vytváří podmínky x xxxx, xxx Xxxxx republika xxxx x xxxxxx xxxxxxxxxxxxx xxxxxxxxxx xxxxxxxxxxx xxxxxxx Xxxxxxxx xxxx x xxxxxxx léčiv, x xx především x xxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxx přípravků. Xxxx by měl xxxxx xxxxx xxxxxx xxxxxxx přispět x xxxxxxx xxxxxx x xxxxxxxxxx xxxxxx xxxxxxx x x xxxx, xxx xxxxxxx kapacita xxxxxxxxxxxx a xxxxxxxxxxx xxxxxxxxx sledovala xxxxx xxxxxx poznatků x xxxxxxxxxxx za xxxxxx xxxxxxxxxxx odborných xxxxx x xxxxxxx xxxxxxx xxxxxxxxx xxxxxx a xxxxxxx bezpečnosti subjektů xxxxxxxxx xx xxxxxx x xxxxxxxxxx xxxxxxx xxxxxxxxxx v rámci xxxxxxxxxx xxxxxxxxx.
1.2.1. Adaptace xxxxxxxx o xxxxxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx
Xxx 16. xxxxx 2014 bylo xxxxxxx xxxxxxxx Xxxxxxxxxx parlamentu x Xxxx (XX) č. 536/2014 x klinických xxxxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx a x xxxxxxx xxxxxxxx 2001/20/XX. Xxxxx xxxxxx 99 xx toto xxxxxxxx xxxxxxx nejdříve xxxx xxxxxx po zveřejnění xxxxxxxx podle xx. 82 xxxx. 3, xx. xxxxxxxx Xxxxxx, xx xxxx xxxxxxx xxxxxxxx spočívající v xxx, že xxxxxx XX x databáze XX dosáhly xxxx xxxxxxxxxx x xxxxxxx xxxxxxx xxxxxxxxx xxxxxxx xxxxxxxxx. X xxxxxxxxxx xx. 99 nařízení xx xxxx stanoveno, xx x xxxxxx xxxxxxx xx xxxx xxxxxxxx xxxxxxxxx xxxxx xxx 28. xxxxxx 2016. Lhůta xxx xxxxxxx xxxxxxxx je xxxx xxxxxxxxx xxxxxxxxxx x závislosti na xxx, xxx xxxxx x xxxxxxxx Komise. X xxxxxx xxxxxxx xx však xxxx xxxxxxxx použije nejdříve xxx 28. xxxxxx 2016. S ohledem xx takto xxxxxxxxxx xxxxx x xxxxxxxx xxxx v xxxxxxxxxxx xxxxxx novely zákona x xxxxxxxx xxxx xxxxxxxx záležitosti xxxxxxxx xx klinického xxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx, xxxxx xx x xxxxxxx x xxxxxxxxx xxxxx adaptovat.
Přijetí nařízení Xxxxxxxxxx xxxxxxxxxx x Xxxx (XX) č. 536/2014 xxxx odůvodněno tím, xx, jak xxxxx xxxxxxx, harmonizovaného xxxxxxxx x regulaci xxxxxxxxxx xxxxxxxxx, x xxxxx xxxxxxxxx xxxxxxxx 2001/20/ES, xxxx x xxxxxxxxx xxxxxxx xxxxxxxx xxxxx xxxxxxxx, xxxx ne xxxxxxx členské xxxxx xxxxxxx náležitou právní xxxxxx x tomu, xxx xxxx xxxxxxxx xxxx potřebným xxxxxxxx x xxxxxx právních xxxxxx xxxxxxxxxxxxx, x xxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxx mnohdy xxxxxxxxxx za xxxxxxxxx xxxxxxxx 2001/20/ES.
Xxxxxxx xxxxx xxxxxx xxxxxxxx, že xxxxxxxx hodnocení xx x xxxxxxxxxxx budou xxxxxxxxx na specifičtější xxxxxxx xxxxxxxx, xxxx xxxx podskupiny identifikované xxxxxxxxxxxxxxx xxxxxxxxxxx xxxxxxxxx. Xxx xxxx možné xx xxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxx dostatečný xxxxx xxxxxxxx, bude xxxxxx na xxxxx xxxxxxx xxxx xxxxxxxxx xxxxx xxxx dokonce xxxxxxx. Tyto nové xxxxxxx povolování xxxxxxxxxx xxxxxxxxx xx xxxx xxxxxxxxxx xxxxxxxx xx xxxxx největšího xxxxx xxxxxxxxx států. Xxxxx xx xx x xxxxx xxxxxxxxxxxx xxxxxxx xxxxxxxxxxx xxxxxxxxxxx x xxxxxxx x xxxxxxxx xxxxxxxxxx hodnocení mělo xxxxxxx xxxxxxxxxxxxx předkládání xxxxxxxx xxxxxxxxxxx informací, xxxxx by xxxx xxx nahrazeno předložením xxxxx xxxxxxxxxxx k xxxxxxx xxx xxxxxxx xxxxxxx xxxxxxx státy xxxxxxxxxxxxxxx xxxxxxxxxx xxxxxxx xxx xxxxxxxxxxx. Xxxxxxxx x xxxx, xx xxxxxxxx xxxxxxxxx xxxxxxxxx x jediném xxxxxxxx xxxxx xxxx x xxxxxxxx evropského xxxxxxxxxx xxxxxxx xxxxxx xxxxxx, xxxx xx se xxxxxxxxxxx k xxxxxxx xxxxxxxx xx xxxxxxxxxx xxxxxxxxx předkládat také xxxxxxxxxxxxxxx xxxxxx xxxxxxxxxx xxxxxxx.
Xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Xxxx (XX) č. 536/2014 xxxxxxxxx xxxxxx x xxxx, že xxxxxxx xxxxxxxx xxxxxxx, xx xxxxxx xxxxx xxxxxxxx xx xxxx xxx xxxxxxxxxx a xxxxxxxxxx xxxxxxx například xxx xxxxxxxxxx xxxxxxxxxxx, xxxxx se provádějí xx xxxx xxx x xxxxxx členském xxxxx, protože xx xx xxxxx xxxxxx xxxxx o jeho xxxxxxxxxx xxx xxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxx, xxx xxxx xxx xxxxxxxx zpráv x xxxxxxxxxxx x xxx xxxxxxxxxx na obalech xxxxxxxxxxx léčivých xxxxxxxxx. Xxxxxxx xxxxx xxxxxxxx xx xx xxxxxx, xx rozdíly x xxxxxxxx mezi jednotlivými xxxxxxxxx státy xx xxxxx xxxxx xx xxxxxxx a xxxx xx xxxx x x efektivnější spolupráci xxxxxxxxx xxxxx při xxxxxxxxxx xxxxxxx x xxxxxxxx xxxxxxxxxx xxxxxxxxx. Xxxx spolupráce xx xxxxxx xxxxxxxxx jen xx xxxxxxx, které xxxx ze své xxxxxxxx xxxxxxxxxxxx povahy, xxxx je například xxxxxxx x fungování xxxxxxxx komisí. Xxxxxx xxxxxxxx nařízením xx xxx xxx pružný x efektivní, xxx xxxxxxxxxxx k xxxxxxxxxxxxxxxx xxxxxxxxx xxx zahájení xxxxxxxxxx xxxxxxxxx, avšak xxxx xxxxx xxxxxxx xxxxxxxxxx xxxxxxxx nebo xxxxxxx xxxxxx.
Xx xxxxx xxxxxx xxxxxx xxxx xxxxx Evropský xxxxxxxxx x Rada x xxxx, xx upraví xxxxxxxxx klinického hodnocení xxxxxxxxx xxxxxxxx přípravků xxxxx xxxxxxxxxxx xxxxxxxxx XX x xxxx xxxx xx nejkomplexněji x xx xxxxxxx xxxxx zbude xxxxxx xxx xxxxxxxxx xxxxxxxxxx xxxxxxx xxxxxx, xxx xxxxxxx řešení xx xx xxxxx xxxxxxxxx xxxxxxx specifika.
Jelikož nařízení Xxxxxxxxxx xxxxxxxxxx x Xxxx (EU) č. 536/2014 xx x České xxxxxxxxx xxxxx xxxxxxxxxx x xxxxx xxxx xxx xxxxxxx xxxxx, xxxx možné jeho xxxxx x xxxxxxx xxxx Xxxxx xxxxxxxxx xxxxxxxx, xxxxxxxxxxxx xx xxxxx xxxxxxxxxx. Předkládaný xxxxx xxxxxx xxxxxx x xxxxxxxx x xxxxxxxxxx xx xxxxx xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Rady (EU) č. 536/2014 xx xxxxxxxx xx úpravu jen xxxx vztahů, xxxxxxx xxxxxx xxxxxxxxx xxxx xxxxxxxx xx členských xxxxxxx. Xxx xxxxxxxxx x xxxxxxxxxxx xxxxxx xxxxxx.
Xx členském xxxxx xx x xxxx xxxx xxxxxxxxx, aby xxxxxxxx příslušný xxxxx xxxx orgány, xxxxx xx xxxxx na xxxxxxxxx xxxxxxx o xxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxx, x xxx xxxxxxxx xxxxxxxx xxxxxxxx xxxxxx xx xxxxxxx xxxxxxxxxxx x xxxxxxxx xxx povolování klinických xxxxxxxxx. Xxxx rozhodnutí xxxx xxx xxxxxxxxxxx xxxxxxx xxxxxxxxxx xxxxxxx xxxxxxxxx xxxxx. Xxx xxxxxxxxxxx xxxxxxxx xxxxxx xxxx xxxxxx xx xxxxxxx xxxx zajistit xxxxxxxx xxxxxxxx osob, x xx xxxxxxx xxxxxxxx xxxx xxxxxxxxxx xxxxxxxx. Xxxxxxxxx xx xxxxxx xxxx xxx xxxxxxxxx společně xxxxxxxxxx xxxxxx xxxx, xxxxx xxxx xxxxxxxxx xxxxxxxxxxx x xxxxxxxxxx k xxxxxxxxx odborného x xxxxxxxxxxxxxxx posouzení, přičemž xxxxx xxxxxxxxxx xxxxxx xx xxxx xxx xxxxxxxxx xx xxxxxxxxxx, xxxxx klinického xxxxxxxxx x xxxxxxxxx xxxxxxxxxxxx x xxxxxx xx xxxxxx být xxxxxxxxx xxxxxx xxxxx nepatřičným xxxxxx. X rámci xxxxxxx xxxxxxxxx xxxxx xxxx existovat xxxxxxx xxxxxx účastnících xx xxxxxxxxxx klinického hodnocení. Xxx xxxx možná xxxxxxxxx a xxxxxx xxxxxxxxxx xxxx členskými xxxxx, měl xx xxxxx xxxxxxx stát xxxxx xxxxx xxxxxxxxx xxxxx.
Xxxxxx xxxxxxx, xxxxx xxxxxx je xxxxxxxxx xx xxxxxxxx xxxxx, xxxx záležitosti xxxxxxxx. Xxxxxxx xxxx xx xxx určit xxxxxxxx xxxxxxxxx na xxxxxxxxxxx xxxxxxxxxx hodnocení. Xxx xx xxxxxxxxx xxxxxxxxxxxxx xxxxxxxxx xxxxxxx xxxxxxxxxx xxxxxxx o xxxxxxxx xxxxxxxxxx hodnocení, xxx xx členský xxxx xxxxxx, že xxxx xxxxx xxx dokumentaci, xxxxx xxxx určena xxxxxxxx xxxxxxxxx, xxxx xxxxxxxxx srozumitelný xxxxx x xxxxxxx lékařství.
Členskému xxxxx se xxxxxxxxxxx x xxxxxx xxxxxx xxxx pravidla týkající xx určení xxxxxxx xxxxxxxxxxxx xxxxxxxx xxxxxxxxxxxxx x xxxxxxxxxxx xxxx, xxxxx xx v xxxxxxxxxxxx xxxxxxxxx státech xxxx.
Xxxxxx xxxxxx pro xxxxxxx xxxxxxxx x xxxxx xxxxxxxxxxx rozhodnutí xxxxx xxxxxxxxx xx xxxxxxxxxx xxxxxxxxx xx xxxxxxxxxxx xxxxxxxxxxx pohovoru x potenciálním xxxxxxxxx xxxxxxxxx. Tento pohovor xx xxx xxx xxxxxxxx xxxxxx xxxxxxxxxx xxxx xxxxxxx způsobilým xxx xxxxx xxxx xxxxx vnitrostátních xxxxxxxx xxxxxxxx x xxxxxxxx xxxxx, x xxxx xxxxx probíhá.
Dále se xxxxxxxxx členskému xxxxx xxxxxxx, xxx xx xxxxxxx, že kromě xxxxxxxxxxxxx souhlasu daného xxxxxxx xxxxxxxxxxx zástupcem xxxx xxxxxxxxx, xxx xxxxxxxxx xxxxx, jež xx xxxxxxx xxxxxxx xx názor x xxxxxxxx xxxxxxxxx xx xxxxxxxxxx, také xxxx xxxxxxx xxxxxxxx písemného xxxxxxxx xx xxx xxxxxx na xxxxxxxxx xxxxxxxxx.
Xxxxxxx xxxx xx xxxxxx xxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxx xxxx xxxxxxx xxxxxx, xxxxx jsou x xxxxxxx podřízenosti nebo xxxxxxxx závislosti. Xxx x xxxxx vykonávající xxxxxxxx xxxxxxxxx xxxxxx, xxxxx xxxxxxx xxxxxxx, xxxxx, které se x xxxxxxxx xxxxxxxx xxxxxxxxxx xxxxxxx xxxxxxxx xxxxxxxxxx xxxxxxxxx, x xxxxx, xxxxx xxxx xxxxxxxx xx svému xxxx, xxxxxxxxxxx xxxxxxxxx xxxx xxxxxxxxxxx stavu xxxxxxxx xx xxxx, x xxxxx xx xxxxxxxxx x zařízeních xxxxxxx xxxx.
Xxxxxxxxx xxxxx xx dále xxxxxxxxx xxxxxx xxxxxxxx otázek, xxx v xxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxx xxxxx xxxxxxxxx subjektu xxxxxxxxx xx xxxxxx xxxxxxxxxxxxxx či xxxxxxxxxxxxx xxxxxxxxxxxx xxxxxxxxxx xxxx xxxxxxxxxxxx. Podmínky xxx xxxxxxxxxxx v těchto xxxxxxxxx, xxxxxx xxxxxx xxxxxxxx xxxxxxxxxxx x xxxxxx xxxxx, xx x xxxxxx xxxx xxxxx xxxxxxxxxxxxxx předpisy. Xxxxxxx stát xx xxx xxxx xxxxxxxx xxxxxxxx xxxxxxx xxxxxxx xxxxx vzniklé xxxxxxxx xxxxxxxxx, xxxxx xxxxx xxxxxxxxx xxxxxx x xxxxxxx xxxxxx, xxxxxxx xxxxx xx, aby xxx xxxxxxxxxx xxxxxxxxxxx xxxx xxxxxxxxx náhrada xxxxx úspěšně xxxxxxxxx x xxxxxxx s xxxxxxxxxxx xxxxxxxxxxxxxx xxxxxxxx xxxxxxxx.
Xxxxxxxxx roli xx x xxxxxx xxxxxxx xxxx x tom, xx xx xx xxxxxxx xxxxxxxx odvolat xxxxxxxx xxxxxxxxxx xxxxxxxxx, xxxxxxxxxx klinické xxxxxxxxx xxxx xxxxxxx x xxxxxxxxxx změnu xxxxxxxxxx xxxxxxxxx. Xxxxxxx stát xx xxxxxxxx xxxxxx xxx průběhem klinického xxxxxxxxx. Xxx xxx xxxxxxxx soulad x xxxxxxxxx, xxxxxxx stát xx xxxx xxxxxxxxx x povinnost xxxxxxxx xxxxxxxx a x xxxx by xxx xxx xxxxxxxxxxxx xxxxxxxxx xxxxxxxx. Xx xxxxxx xxxxxxxxx činností stanovených x nařízení xx xxxxxxxx státům xxxxxxxx xxxxxxx poplatky, xxxxxxx xxxxxxxxx xx xxxxxxxx x článku 86 x 87 xxxxxxxx (xxxxxxxxxxxxx xxxxxxxxx výše xxxxxx, xxxxxx xxxx xxx xxxxxxxxx xx xxxxxxx zásady xxxxxx xxxxxxx, xxxx xxx xxxxx xxxxx platba xx posouzení).
Dále xx xxxxxxxx xxxxxx xxxxxxxx xxxxxxxx xxxxxxxx na xxxxxxx xxxxxxxxxx hodnocení xxxxxxxxxxx xxxxxxxxxxxx xxxxxxxxxx, xxxxxxx se pro xxxxx xxxxxx x xxxxxxxx rozumí xxxxxxxxxxxxx xxxxxxxxxxx xxxxxx xxxxxxx xxxx založení xxxxxx xxxx územním xxxxxxxxxxxx xxxxxx, xxxxxxx xxxxxx xxxxx a veřejná xxxxxxxx xxxxxxxxx, v xxxxx xxxxxxxxxxx využití xxxxxxxxxx xxxxxxxxx těchto xxxxxxxxxxxx zadavatelů x xxxxx xxxxxxx jejich xxxxxxx, xxxx xx xxxxxxxxx x xxxxxxxx xxxxxxx xxxxxxxxxx xxxxxxxxx. Xxxx xxxxxxx x xxxxxxxx zkušeností, které xxxxxxxxxx x xxx, xx xxxxx xxxx xxxxxxxxxx xxxxxxxxx xx xxxxxxxxx xxxxxxxxxxxx xxxxxxxxxx, xxxxx xxxxx xxxxxxxxx xx finanční prostředky, xxxxx xxxxxxxxx, x xx zčásti nebo xxxxx, x xxxxxxxxx xxxxxxxxxx xxxx x xxxxxxxxxxxx xxxxxx.
X xxxxxxxxxx xx xxxxx nařízení Xxxxxxxxxx xxxxxxxxxx a Xxxx č. 536/2014 předkládaný xxxxx novely xxxxxx x xxxxxxxx xxxxxxx xxxxxxxxx xxxxxx xxx, xxxxx xxxxxxx x xxxxxxxx xxxx, xxx xxxxxx xxxxxx x Xxxxx xxxxxxxxx xxxxxx xxxxxxxxx xxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxx přípravků založený xxx xxxxx Evropskou xxxx xxxxxxxxx Xxxxxxxxxx xxxxxxxxxx a Xxxx č. 536/2014. Návrh se xxxxx xxxxxxxxxxx xx xxxxxx xxxxxxxxx xxxxxxxxxxx, xxxxxxx xxxxxx xx xxxxxxxxx xxxxx xxxxxxx, xxx xxxxxx xxxxxxxx x nařízení x x xxxxxx xxxxxxxx xxxxxxxxxxx náležitý xxxxxx xxxxxx xxx xxxxxxxxx xxxxxxxxx xxxxxxxxxx hodnocení.
Byly xxxxx xxxxxxxxxxxxxx následující xxxxxxxx:
Xxxxx xxxxxxxxx, xxxxxxx xxxxxxx xxxx, xxxx xxxxxxxx xxxxxxxxxxx xxxxxxx:
- xxxxxxxx xxxxxxxxx xxxxx xxxx orgány, xxxxx xx xxxxx xx xxxxxxxxx xxxxxxx x xxxxxxxx xxxxxxxxxx hodnocení xxxxxxx, xxxxxxxx xxxxxxxxx xxxxxxx xxxxxx při xxxxxxxx podmínek xxxxxxxx x xxxxxxx posuzujících xxxxxx, tzn. zajistit xxxxxxxxxxx etické komise xx zadavateli, zkoušejících x místě xxxxxxxxxx xxxxxxxxx, x zajistit xxxxxxxxxx etických xxxxxx xx xxxxxxx xxxxxxxxxxx x xxxxxxxx xxx xxxxxxxxxx xxxxxxxxxx hodnocení;
- xxxxxx xxxxxxxxx x xxxxxxxx xxxxxxx xxxxxxx xxxxxxxx xxxxx způsobené xxxxxxxxx xxxxxxxxx v xxxxxxxxxxx x jejich xxxxxx ve xxxxxx xx území daného xxxxxxxxx xxxxx;
- xxxxxxxxxxx xxxxxxxx;
- xxxxxxx x xxxxxxxxxxxx xxxxxxxxx xxxxxxxxx xx xxx xxx xxxxxxxx xxxxxx zkušebního xxxx xxxxxxx xxxxxxxxxx xxx tento xxxx xxxxx xxxxxxxxxxxxxx xxxxxxxx xxxxxxxx v xxxxxxxx xxxxx, x xxxx xxxxx probíhá;
- xxxxxxxxxx, xxx kromě xxxxxxxxxxxxx xxxxxxxx xxxxxx xxxxxxx xxxxxxxxxxx xxxxxxxxx bude xxxxxxxxxx, xxx xxxxxxxxx xxxxx, xxx xx xxxxxxx xxxxxxx xx xxxxx a posoudit xxxxxxxxx xx poskytnuté, xxxx sama svolila xxxxxxxx xxxxxxxxx souhlasu xx xxx xxxxxx xx klinickém hodnocení;
- xxxxxxxxxx, xxx xxxxx xxxxxxxxx xxxxxxxxx ochranná xxxxxxxx vůči takovým xxxxxx, které xxxx x xxxxxxx podřízenosti xxxx xxxxxxxx xxxxxxxxxx;
- xxxxxxxx pro odpovědnost x případech xxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxx xxxxxx xxxxxxxx xxxxxxxxxxx x xxxxxx xxxxx, xx x xxxxxx xxxx řídit xxxxxxxxxxxxxx xxxxxxxx;
- členskému xxxxx xx xxxxxxx xxxxxxxx odvolat xxxxxxxx xxxxxxxxxx xxxxxxxxx, xxxxxxxxxx xxxxxxxx hodnocení xxxx xxxxxxx u xxxxxxxxxx xxxxx xxxxxxxxxx xxxxxxxxx; xxxxxxx stát má xxxxxxxx xxxxxx xxx xxxxxxxx klinického hodnocení; xxx xxx zajištěn xxxxxx x xxxxxxxxx, xxxxxxx stát má xxxx xxxxxxxxx x xxxxxxxxx provádět xxxxxxxx x x tomu xx xxx xxx xxxxxxxxxxxx xxxxxxxxx xxxxxxxx; xx xxxxxx xxxxxxxxx xxxxxxxx stanovených x xxxxxxxx xx xxxxxxxx xxxxxx xxxxxxxx xxxxxxx xxxxxxxx;
- rozhodnout o xxxxxxx xxxxxxxx xx xxxxxxx klinických hodnocení xxxxxxxxxxx xxxxxxxxxxxx xxxxxxxxxx x zájmu maximálního xxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxx xxxxxxxxxxxx xxxxxxxxxx x další xxxxxxx xxxxxx xxxxxxx.
X xxxxxxxx xxxxxx xxxxxx xxxx xxxxxxxxxxxxxx zejména následující xxxxxxxx:
X xxxxxxxx xxxx xx právní xxxxxx xxxxxxxxxx xxxxxxxxx x xxxxxx x xxxxxxxx x prováděcí vyhlášce xxxxxxxx x xxxxxxxxxx xx směrnici EU xx klinickým xxxxxxxxxx. Xxx bylo xxxxxxx xxxx, stávající xxxxxx xxxxxxxxxxx není dle XX xxxxxxxxxx a x xxxx xxxxxx xxxx xxxxxxxxxx x xxxxxxx xxxxxxxx. Xxxxx xxxxxxxxxxxx právní xxxxxx, xxxxx xx xxxx xxxxxxxx xxxxxxxxxx, x xxxx xxx možné x tohoto hlediska xxxxxxxxxxxxx xxxxxxxx.
1.2.2. Opatření xxxxxxxxx x xxxxxxx xxxxxxxxx léčivých xxxxxxxxx
Xxx xxxxxxxx xxxxxxxx xxxxx xxxxx xxx xxxxxx xxxxxxxxx xx zákonem xxxxxxxxxxx xxxxxxxx xxxxxxxxxxxxx xxxxxxxxxxxx mimo území Xxxxx xxxxxxxxx. Distribuci xxxxxxxx přípravků lze xxxxxx uskutečňovat xxxxx xx členských xxxxx Xxxxxxxx unie, ale xxx do xxx. xxxxxxx xxxx. X xxxxxxx xxxxxxxxxx léčivých xxxxxxxxx xx třetích xxxx se neuplatní xxxxxxx xxxxxxxx xxxxxxxxx xxxxxx Evropské xxxx. Xxxxxxxxxxxx do xxxxxxxxx xxx xxx xxxxx xxxxxxxx xxxxxx úpravy x xxxxxx přípravky, xxxxx xxxx xx xxxxxxx xxxxxx x xxxxxxx x rámci Xxxxx republiky. Současně xx ale xxxxxxxxx x xxxxxx o xxxxxxxx, že držitelé xxxxxxxxxx x registraci xxxx xx xxxxxxxxx xxxxxxxx xxxxxxx léčivých xxxxxxxxx xxx xxxxxxx xxxxxxx xxxxxxxx x Xxxxx xxxxxxxxx. Xxxxxxxx xxxxxxxxxx x xxxxxxxxxx xxxx xxxxxxx xx xxx x Xxxxx xxxxxxxxx xxxxxx xxxxxxxx xxxxxxxxx, xxxxx odpovídají xxxxxxxxx, xx xxxxxxx xxxx vydáno Xxxxxxx xxxxxxx xxx xxxxxxxx xxxxx případně evropskou xxxxxxx xxxxxxxxx XXX xxxxxxxxxx x xxxxxxxxxx, x jsou xxxxxxxx x xxxxxx jazyce. Xxx tedy xxxxxxxxxxx x balení, která xxxx od počátku xxxxxx x použití xxxxxxxx x České xxxxxxxxx a nikoli x xxxx xxxx. Xxxxxx přípravky xxxx xxx x xxxxx xxxx xxxxxxxx v xxxxxxxxxx jazyce xxxx xxxx. Xxxxxxxx xxxxxxxxxx xxxxxxxx přípravků xxx xx xxxxxxx x xxxxxxx xxxxxxx xxxxxxxx x Xxxxx republice x naplnění xxxxxxx xxxxxxxxxx.
Xxxxxxxx xxxxxxxx xxxxxxxxx x xxxxx Xxxxxxxx xxxx, xxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxxx x xxxxxxxxxx, dále xxxxx xxxxxxxx x xxxxxxxx xxxxxxxxx xxxx xxxxxxxxxxxx xxxxxxxx xxxxxxxxx - jde o xxxxxxxxx xxxxxxxxxx u xxxxxxxx xxxxxxxxx, jejichž xxxxxxxxxx o xxxxxxxxxx xxxx xxxxxx xxxxxxxxx xxxxxxx agenturou EMA xx x xxxxxxxx xxxxx u xxxxxxxx xxxxxxxxx, kterým xxxx xxxxxx xxxxxxxxxx x xxxxxxxxxx Xxxxxxx xxxxxxx xxx xxxxxxxx xxxxx. X xxxx případech xx xxx pro xxxxxxx xxxxxxxx xxxxxxxxxxxxxxx x xxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx xx xxxxxxxxx xxx xxxxx xxxxxxxx vydané národní xxxxxxxxx xxxxxxxxx x xxxx xxxxxxx xxxx Xxxxxxxx xxxx.
Xxxxxxx pro xxxx aktivity xx xxxxxxx xxxxx cena xxxxxxxx xxxxxxxxx x „xxxxxxxx xxxxxxx zemi“, xx xxxxx xxxx xxxxxx xxxxxxxxx odvezeny xx xxxx členské xxxx, xx xxxxx xx cena xxxxxx xxxxxxxx přípravku vyšší.
Tzv. xxxxxxxx obchod je xxxxxxx a xxxxxxxx x souladu x xxxxxx Xxxxxxxx xxxx, xxxxxxxxx xx xxxxxxx xxxxxxx xxxxxx xxxxx xxxxxxxxx xxxxxx 34 x 35 Xxxxxxx x xxxxxxxxx Xxxxxxxx xxxx. Dle xxxxxxxxxx Xxxxxxxxxx xxxxxxxx dvora xx zásada volného xxxxxx xxxxx uplatní xxx xx léčivé xxxxxxxxx. Česká xxxxxxxxx xx s ohledem xx xxxxxxx regulaci xxx léčivých xxxxxxxxx xxxxxxx „xxxxxxxxx xxxx“ x xxxxxx xxxxxxxxx xxxx xxx x xxxxxx xxxx odváženy (xxxxxxxxxxxxx) ve xxxxxxxxxx xxxxxxxxxx.
Xx paralelním xxxxxx xxxxxxxx xxxxxxxxx se x Xxxxx xxxxxxxxx xxxxxxxx provozovatelé xxxxxxx, xxxxx mají zároveň xxxxxxxx x xxxxxxxxxx, x xxxxxxxxxxxx xxxxx. X xxxxxxxxxx xxxx xxxxx České xxxxxxxxx xxxxxxx zejména z xxxxxx xxxxxxx stanovených xxx xxxxxxxx přípravků x xxxxxxxxxxxx xxxxxxxxx xxxxxxx Xxxxxxxx xxxx x xxxx oblast xxxxxxx xxxxxxxxxxx xxxxxxx xxxxxxxxxx xxxxx xxxxx xxxxxxxx xxxxxxxxxxxx xx xx xxxx xxxxxxxxxx. Xx xxxxxx stranu xxxxxxxx xxxxxx xxxxxx xxxxxxxxx xxxxx umožňuje xxx xxxxxxxx xxxxx xx xxxxxxxxx xxxxxxxxxx xxxxxxxx přípravků z xxxxxx zemí xx Xxxxx republiky. Na xxxxxx xx souběžného xxxxxx x xxxxxxxx xxxxxxxxxx, xxxxx xxxx x zákoně o xxxxxxxx x předpisech Xxxxxxxx xxxx xxxxxxxxx xxxxxx a xxxxxxxxxxx xxxxxxxx x podmínky, xx xxxxxxx mohou xxx xxxxxxxxxxx, xxxx xxxxxxxxxx léčivých xxxxxxxxx xxxx země Xxxxxxxx xxxx či xxxx xxxxx daného xxxxxxxxx xxxxx xxxxxxxxx xxxxx xxxxxxxxxx.
Xxxxxxxxxxxx xxxxxxxxx xxxxx, xxx xx xxx xxxxxxxx xxxxxx xxxxx x xxxxx xxxxxxxxx, xx komplexního charakteru x v konečném xxxxxxxx xxxx xxx xxxx xx xxxxxxxxxxx xxxxxxxxx péče x Xxxxx xxxxxxxxx xxx x hlediska xxxxxx xxxxxxxxxxxxx určitých xxxxx xxx xxxxxxxx, xxx x xxxxxxxx dlouhodobě xxxxxxxxxxx ekonomického xxxxx xx xxxxxxx xxxxx xxxx ve zvýšených xxxxxxxxx systému xxxxxxxxx xxxxxxxxxxx xxxxxxxxx x xxxxxxx, xx xxxx xxxxxx přípravky xxxxxxxxxxx xxx xxxxxxxxxxxxx xxxxxxxxxxx.
Xxxxx xxxxxxxxx, stejně xxxx xxxxxxx členské státy XX, je xxxxxx xxxxxxxxx xx zajištění xxxxxxxxx péče na xxxx xxxxx. Xxxxxx x xxxxx xxxxxxxxx xxxxxxxxx xxxx xx xxxxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx xxx xxxxxxx xxxxxxxx x Xxxxx xxxxxxxxx. V xxxxxxx x čl. 81 xxxxxxxx Xxxxxxxxxx parlamentu x Xxxx 2001/83/XX ze xxx 6. xxxxxxxxx 2001 o xxxxxx Xxxxxxxxxxxx xxxxxxxxx xx xxxxxxxxx xxxxxxxx přípravků, xx xxxxx směrnice Xxxxxxxxxx xxxxxxxxxx x Xxxx 2004/27/ES xx xxx 31. xxxxxx 2004, mají xxxxxxxx xxxxxxxxxx o xxxxxxxxxx xxxxxxxx xxxxxxxxx x xxxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxxxxx x xxxxx dodávky xxxxxx xxxxxxxx přípravku xxxxxxxx x osobám xxxxxxxxx vydávat xxxxxx xxxxxxxxx xxx, xxx xxxx pokryty xxxxxxx xxxxxxxx x xxxxx xxxxxxxx státě. Xxxx xxxxxxxxx byla implementována xx současného xxxxx xxxxxx x léčivech, xxxxxxxxx do xxxxxxxxxx §33 odst. 3 xxxx. g) xxxx 3, xxxxx jde x držitele rozhodnutí x xxxxxxxxxx, x xx xxxxxxxxxx §77 xxxx. 1 písm. x), pokud jde x distributory. Xxxxxxxxxx xxxxxxxxxxxx dle ustanovení §77 xxxx. 3 xxxxx v xxxxxxx, xx se zároveň xxxxx x provozovatele xxxxxxx, xx uvedení xxxxxxxxx x xxx, xxx xxxxxx přípravky xxxxxxx xxxx provozovatel xxxxxxx xxxx xxxx xxxxxxxxxxx.
Xx procesu xxxxxxxxxx xxxxxxx xxxx xx xxx podílejí xxxxxxxx xxxxxxxxxx o xxxxxxxxxx x distributoři xxxxxxxx xxxxxxxxx. Xxxxxx xxxx xxxxxxx x xxxxxxxx, xxx xxx potřeby xxxxxxxx v Xxxxx xxxxxxxxx xxxxxx dostupné xxxxxxx pro xxxxxxxxxxx xxxxxxxxxxx xxxxxx významné xxxxxx xxxxxxxxx, xxxxx xxxx xx Xxxxx xxxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxx za xxxxxx xxxxxxxx povinnosti xxxx xxxxxxxxx v xxxxxxxxxx §33 xxxx. 3 xxxx. x) xxx 3, xxx xxxxxxxx xxxx z xxxxx xxxxxxxxxxxx xxxxxx distribuovány xxxxxxx xx xxxxxxx x XX, ale xx zahraničí xx xxxxxxxx xxxxxxxxxxxx xxxxxxxxxx xxxxxxxx.
Xxxx proto xxxxxxxxxxxxxx xxxxxxxxxxx xxxxxxxx:
X xxxxxx xxxxxxxxxx léčivých xxxxxxxxx xxxxx:
- xxxxxxxxxxxx xxxxxxxx xxxxxxxxx xxx xxxxxxx xxxxxxxx x Xxxxx xxxxxxxxx s přímým xxxxxx na xxxxxx xxxxxx (x xxxxxxxxx xxxxxxxxx se xxxx xxxxxx i x xxxxx xxxxxxxxxx xxxxx);
- xxxxxxxxxxxx xxxxxxxxx xxxxxxxxxxxx xxxxxx xxxx xxxxxx.
X xxxxxxxx právní úpravy xxxx identifikovány xxxxxxx xxxxxxxxxxx xxxxxxxx:
Xxxxxxxxx xxxxxx xxxxxx, xxx které Xxxxxx xxxxx xxx xxxxxxxx xxxxx xxxxxxxxxxx xxxx xx xxxxxxxxxxxx, xxxxxxxx xxxxxxxxxx o xxxxxxxxxx x xxxxxxx xxxx xxxxxxxxxx provázaná x efektivní xxx, xxx umožňovala xxxxxxxxxx xxxxxxx řešit xxxxxxxxx x xxxxxxxx xxxxxxxxx. Xxxx zásadní se xxxx:
- chybějící xxxxxxxxx xxxxxx problematiky;
- xxxxxx xxxxxx.
1.2.3. Adaptace xxxxxxxx xx xxxxxx x xxxxxxx xxxxxx pro xxxxxxx xxxxxx přípravky
Dalším xxxxxxxxx, který xx xxxx navrhovaná xxxxxx xxxxxx řešit, xx xxxxxxx xxxxxxxxxx ustanovení xxxxxxxxxxxx pravidla nakládání x xxxxxxxx xxxxxxx xxxxxxxx reagovat xx xxxxxxx nařízení Komise x xxxxxxxxx xxxxxxxxx (XX) č. 1252/2014 ze xxx 28. května 2014 xxxxxxxxxx xxxxxxxx Xxxxxxxxxx parlamentu x Xxxx 2001/83/ES, pokud xxx x zásady x pokyny xxxxxxx xxxxxxx praxe xxx xxxxxx xxxxx pro xxxxxxx léčivé xxxxxxxxx. Xxxx xxxxxxxx xx xxxxxxxx xxxxx na xxxxxx xxxxx xxx xxxxxxx xxxxxx přípravky. Xxxxxxxxxx §70 xxxxxx x xxxxxxxx stanoví, xx xxxxxxx léčivé xxxxx je povinen xxxxxxxxx správnou výrobní xxxxx xxxxxxxxxx prováděcím xxxxxxx předpisem. Pravidla xxxxxxx xxxxxxx xxxxx xxxxxxxx xxxxx xxxx xxxxxxxxx pokyny Xxxxxxxx xxxxxx. Pravidla byla xxxxxxxxx jak xxx xxxxxx xxxxxxxx xxxxx xxx xxxxxxx xxxxxx xxxxxxxxx, xxx i xxx xxxxxx xxxxxxxx xxxxx pro xxxxxxxxx xxxxxx xxxxxxxxx, x xxxxxx xxx výrobu xxxxxxxx látek pro xxxxxxxxxxx léčivé xxxxxxxxx. Xxxx xx xxxx xxxxxx úprava xxxxxxx xxxxxxx xxxxx xxxxxxxx xxxxx xxx humánní xxxxxx xxxxxxxxx, xxx xx xxxxxxx xxxxxxx xxxxxxxxx v xxxxxxxx xxxxxx nařízením. Pokyn xx xxx xxxxx xxxxxxxxxx charakter. Xxxxxxxx xx xxx xxxxxxx xxxxxx xx xxxxx xxxxxxx XX. Xxxxxxxxx xxxxxx úpravu xxxxxxxxx x zákoně o xxxxxxxx je nutno xx xxxxxx x xxxxxxx xxxxxx xxx xxxxxxx xxxxxx xxxxxxxxx xxxxxxx xx xxxxxx xxxxxxxxx xxxxxxxxxxxxxx dodržování xxxxxxxx nastavených xxxxxxxxx. Xxxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxx xxxxxxx xxxxx xx však xxxxx xxxxxxxx pro xxxxxx xxxxx xxx xxxxxxxxxxx xxxxxx přípravky.
1.2.4. Xxxxxxxxxx Xxxxxxxx xxxxxx xxx kontrolu léčiv x Generálního xxxxxxxxxxx xxx
Xxxxxxxx by xxxxxxxxxx xxxxxx xxxxxx xxxx xxxxx xxxxx xx xxxxxxxxx xxxxxxxx v xxxxxxxx xxxxx, xxxxx xx vskutku xxxxxxxx xxxxxxxxxx xxxxxx. Jde x xxxxx xxxxxxxxxxxx xxxxxxxxxx právní úpravu xxxxxxxxxx Státního xxxxxx xxx xxxxxxxx xxxxx x Xxxxxxxxxx xxxxxxxxxxxx xxx, xxxxx by xxxx xxxxxxxxx představovat xxxxxxxx xxxxxx x xxxxxxxxxxxxx naplnění xxxxxxxx Xxxxxxxxxx parlamentu a Xxxx 2011/62/EU, xxxxxx xx mění xxxxxxxx 2001/83/XX o kodexu Xxxxxxxxxxxx xxxxxxxxx xx xxxxxxxxx xxxxxxxx přípravků, xxxxx xxx x xxxxxxxxx vstupu xxxxxxxxxx xxxxxxxx xxxxxxxxx do xxxxxxxxx dodavatelského řetězce. Xxxxxxxx právní úprava xx měla xxxxxxxxx xxxxxxxx usnadnit xxxxxxx xxxxxx xxxxxxxxx xxxx Xxxxxxxxxx xxxxxxxxxxxx xxx x Xxxxxxx xxxxxxx xxx xxxxxxxx xxxxx x oblasti xxxxxxxx xxxxxxxxx, xxx xxxx xxxxxxxx xxxxx, xxxxxxx xxxxx xx xxxxxxx xxxx xx ze xxxxxx XX podmíněn xxxxxxx xxxxxxxxx xxxxxxxxxxx x xxxxxxxxx směrnicích. Xxxx efektivní výměně xxxxxxxxx x xxxxxxxx xxxxxxxxxx kroků obou xxxxxx xxxxxx xxxxxx xx xxxxx xxxxxxxx xxxxxxx xx xxxxxx xxxxxxxx xxxxxxxxx a xxxxxxxx xxxxx, xxxxx xxxxxxxxxxxx xxxxxxxxxx xx xxxxxxx xxxxxxxx v xxxxxx XX.
1.2.5. Xxxxxxxxxxx xxx xxxxxxxxx činnosti x právní instituty xxxxxxxxx a zabrání xxxxxxxx xxxxxxxxx
X xxxxx xx xxxxxxx jako xxxxxxxxxxxxx xxxxxxxx právní xxxxxx xxxxxxxxxxx xxxxxxxxxx xxx xxxxxx inspekční xxxxxxxx xx xxxxxxx xxxxxxxxxx vymezených Xxxxxxxx xxxxxx xxx kontrolu xxxxx xxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxxx xx xxxxxxxx xxxxxxxxx a xxxxxxxxx s nimi, x xxxxxxxx xxxxxxxxx xxxxxxxxx x xxxxxxx xxxxxxxx xxxxxxxxx, která xxxxxxxxxxxxx potřebný právní xxxxxxx xxx xxxxxx xxxxxxxx xxxxxxx, xxx xx zjištěno, xx x xxxxxxxx xxxxxxxxx xxxxxxxxx osoby, které x xxxx nejsou xxxxx xxxxxx oprávněny. X xxxxx xxxxxxx xxxxxxxxx zdraví xx xxxxx tyto xxxxxx xxxxxxxxx xxxxxxxx tak, xxx xxxx použitelné x xxx takové xxxxxxx. Xxxxx xxx xxxxxxxx část.
1.3. Popis xxxxxxxxxxxx xxxxxxxx xxxxx x xxxx xxxxxxx
1.3.1. Xxxxxxxx nařízení o xxxxxxxxxx hodnoceních humánních xxxxxxxx xxxxxxxxx
Xxxxxxx právní xxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx v Xxxxx republice tvoří:
- xxxxx č. 378/2007 Sb., x xxxxxxxx x x xxxxxxx některých xxxxxxxxxxxxx xxxxxx (xxxxx o xxxxxxxx), xx xxxxx xxxxxxxxxx xxxxxxxx,
- xxxxxxxx č. 226/2008 Sb., x správné xxxxxxxx xxxxx x xxxxxxxx podmínkách xxxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx,
- xxxxxxxx č. 229/2008 Sb., x xxxxxx x distribuci xxxxx,
- vyhláška č. 84/2008 Sb., x xxxxxxx lékárenské xxxxx, xxxxxxxx xxxxxxxxxx xxxxxxxxx x xxxxxx x lékárnách, xxxxxxxxxxxxxx xxxxxxxxxx x u xxxxxxx xxxxxxxxxxxxx a xxxxxxxx vydávajících xxxxxx xxxxxxxxx, xx xxxxx xxxxxxxx x. 254/2013 Xx.,
- xxxxxxxx č. 427/2008 Sb., x stanovení výše xxxxxx xxxxxx xx xxxxxxx xxxxx xxxxxxxxxx x xxxxxxxxxx Státního xxxxxx pro xxxxxxxx xxxxx a Xxxxxx xxx xxxxxx xxxxxxxx xxxxxxxxxxxxx xxxxxxxxxxxx x xxxxx, ve xxxxx xxxxxxxxxx xxxxxxxx.
- xxxxxxxx č. 228/2008 Sb., o registraci xxxxxxxx přípravků, xx xxxxx pozdějších xxxxxxxx
Xxxxxx xx xxxxxx Evropské xxxx xxxxxxxxxxx nařízení Xxxxxxxxxx xxxxxxxxxx x Xxxx (XX) č. 536/2014, xxxxx xx použije xxxxxxxx dnem 28. xxxxxx 2016. Ode xxx použití tohoto xxxxxxxx se xxxxxxx xxxxxxxx 2001/20/XX, xxxxx xx xxxxxxxxxxxxx x xxxxxx x léčivech. Xxxxx použití xxxxxxxxx xxxxxxxx xx xxxxxxxxxx xxxx xx upravuje x přechodných ustanoveních xxxxxxxx Xxxxxxxxxx parlamentu x Xxxx (EU) č. 536/2014, xxxxx xxxx xxxxxxxx x jeho xxxxxx 98.
1.3.2. Xxxxxxxx xxxxxxxxx k xxxxxxx xxxxxxxxx xxxxxxxx přípravků
V xxxxx zajištění xxxxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxx v České xxxxxxxxx xx x xxxxxx x xxxxxxxx xxx xxxxxxxx xxxxxxxxxxx xxxxxxxxxxxx xxxxxxxxx orgánů x provozovatelů.
Držitelé xxxxxxxxxx x registraci mají xxxxxxxxxxx §33 odst. 3 xxxx. g) xxxx 3 zákona x xxxxxxxx stanovenu xxxxxxxxx zajistit xx xxxxxxx xxxxxxxx přípravku xx xxxxx xxxxxx xxxxxxxxx xxx xxxxxxx xxxxxxxx x České xxxxxxxxx xxxx dodávkami x odpovídajícím množství x xxxxxxxx xxxxxxxxxxx. Xxxxx x xxxxxxxx xxx držitele xxxxxxxxxx x xxxxxxxxxx za xxxxxxxx xxxx xxxxxxxxxx xxxxxxx xxxxxx v xxxxxx xxxxxx. Xxxxxxxx xxxxxxxxxx xxxxxxxx xx xxx x české xxxxxxxxx xxxxxx xxxxxxxx xxxxxxxxx označená v xxxxxx xxxxxx a x xxxxxxx xx x xxxxxxxxxxx x xxxxxxxxxx vydaným Xxxxxxx, xxxxxxxx evropskou lékovou xxxxxxxxx XXX. Xxx xxxx xxxxxxxxxxx x xxxxxx, která xxxxxxx xxxxxxxxxx xxxxx určil xxx xxxxxxx xxxxxxxx x Xxxxx xxxxxxxxx x xxxxxx v xxxx xxxx. Xxxxxx xxxxxxxxx xxxx xxx x xxxxx xxxx xxxxxxxx x xxxxxxxxxx xxxxxx dané xxxx. Xxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx pak má xxxxxx k xxxxxxx xxxxxxx xxxxxxxx pacientů x Xxxxx xxxxxxxxx.
Xxxx xxxxxxx xxxxxxxxxx x xxxxxxxxxx má x xxxxxxx x xxxxxxxxxxx §33 odst. 2 xxxxxx x xxxxxxxx xxxxxxxxx oznamovat Ústavu xxxx xxxxxxx, xxxxxxxxx xxxx xxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx xx xxx x České xxxxxxxxx. X xx xxxxxxxx těchto xxxxx xxxxxxxxxx xxxxxxx xxxxx x xxxxxxxx xxx xxxxxxxx xxxxxxxxxx x xxxxxxxxxx sankci xx xxxxx xxxxxx. Xxxxx xx xxxx Xxxxx xxxxx nebo xx xxx xxxxxx činnosti xxxxxxxxxx, xx xxxxxxx xxxxxxxxxx x registraci xxxxxxx léčivých xxxxxxxxx xxxxxxxxxx, nebo nenahlásil xxxxxxxxx nebo xxxxxxxx xxxxxx dodávek, pak xxxxxxxx x xxxxxx xxxxxxxx xxxxxxx xxxxxx x správním xxxxxxx x uloží xxxxxx. X xxxxxx 2012-2015 Xxxxx xxxxxx xx xxxxxxxx xxxxxxxxx xxxxxxx xxxxxxxx xxxxxxxxxx x xxxxxxxxxx 67 xxxxx x celkové výši 1. 810 021 Xx.
Xxxxx x léčivech xxx x současné xxxx xxxxxxxx x xxxxxxxxxx xxxxxxxx xxx xxxxxx xxxxxxxxxx situací, xxxx xxxxxxx xxxxxxxxxx x registraci xxxxxx xxxxxxx léčivé xxxxxxxxx xx trh v Xxxxx xxxxxxxxx v xxxxxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxx a xx xxxxxxxxx nahlášené xxxxxxxxx xxxxxxx léčivých xxxxxxxxx. X xxxxxxx x xxxxxxxxxxx §38 xxxxxx x léčivech xxxx Xxxxx, jsou-li vážné xxxxxx x dostupností xxxxxxxx xxxxxxxxx, umožnit, xxx označení xx xxxxx x příbalová xxxxxxxxx xxxxxx x xxxxxx xxxxxx (xxx. xxxxxxxxxxx xxxxx). X xxxxxxxxxx letech xxxx xxxxx xxxxxxxx celkem 179 případů, v xxxx 2012 64 xxxxxxx, x xxxx 2013 56 xxxxxxx, x xxxx 2014 28 xxxxxxx, do 27.8.2015 31 případů.
Dále xx možno využít xxxxxxxxx xxxxxxxxxxxx léčebného xxxxxxxx, xxxxx xx xxxxxx x §49 xxxxxx x xxxxxxxx x léčivý xxxxxxxxx xxxxx x xxxx xxxxx. X xxxxxxxxxx xxxx xxxxxx Xxxxx xxxxx xxxxxxxxx xxxxxxxxxx, x xxxx 2013 x 55 xxxxxxxxx, x xxxx 2014 x 55 případech, x xx 1.9.2015 xx bylo 27 xxxxxxx.
Xxxxxx xxxxxxxxx xxxxx xxx xxxxx xxxxxxxxx xxxxxxx xxxx dodávány xx trh x Xxxxx xxxxxxxxx xxxxxxxx xxxxxx x xxxxx xxxxxxxxxx xxxxxx léčivých xxxxxxxxx v souladu x §45 xxxxxx x xxxxxxxx. Xxxxx xxxxxxxx, který xxxxxxx xxxxx xxxx některých xxxxxxxx xxxxxxxxx x xxxxxx členských zemích xxxxxx xxxxxx cenám x Xxxxx xxxxxxxxx, xx xxxx xx xxx xxxxxxx xxxxx xxxx xxxxxxx léčivých xxxxxxxxx, xxxxxx x xxxxx xxxxxx xxxxxxxxxx, xxx jsou léčivé xxxxxxxxx reexportované x Xxxxx republiky. Xxx xxxxxxxx (počet balení) xxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx xxxx xxxxxxx xxxxxxxxxxx x&xxxx;xxxxxxxxx (xxxxx xxxxxx) xxxxxxxxxxxxxxx xxxxxxxx xxxxxxxxx-xxx xxxxxxx a xxxx níže.
TOP 15 xxxxxxxx xxxxxxxxx - xxxxxxxx xxxxx xx. xxxxxxxxx xxxxx xxxxxx (xxxxxxxx xxxx 2015)
|
Souběžný xxxxx |
Xxxxxxxxx |
|||||||
|
Xxx. |
Xxxxx XX |
Xxxxxxx |
Xxxxx xxxxxx |
Xxxxxx XXX* |
Xxxxx XX |
Xxxxxxx |
Xxxxx balení |
Celkem XXX* |
|
1 |
XXXXXXXX |
XXX GTT XXX 1X10XX |
1 541 |
385 250 |
XXXXXXX 160 XXXXXXX |
XXX XXX XXX 60X160XX |
14 535 |
872 100 |
|
2 |
XXXXXXXX |
XXX GTT XXX 1X10XX |
1 197 |
299 250 |
XXXXXXXX 15 XXXXXXXXXX/XX OČNÍ XXXXX |
XXX XXX SOL 90X0.3XX |
2 741 |
740 070 |
|
3 |
XXXXXXXXX 20 |
XXX XXX FLM 90X20XX |
3 072 |
276 480 |
XXXXXXX 150 XX |
XXX XXX XXX 3X150MG |
5 865 |
527 850 |
|
4 |
XXXXXXXX |
XXX TBL XXX 3X21 |
1 924 |
161 616 |
XXXXXXXX 24 |
XXX TBL XXX 50X24XX |
8 957 |
447 850 |
|
5 |
MERCILON |
POR XXX NOB 3X21 |
1 807 |
151 788 |
XXXXXXXXX MR |
POR XXX RET 60X35MG |
8 170 |
428 925 |
|
6 |
MILURIT 100 |
XXX XXX XXX 50X100XX |
12 022 |
150 275 |
XXXXXXX 1200 XX |
XXX XXX FLM 100X1200XX |
8 132 |
406 600 |
|
7 |
MIRELLE |
POR XXX XXX 84 |
1 691 |
142 044 |
INHIBACE 5 XX |
XXX TBL XXX 28X5XX |
6 443 |
360 808 |
|
8 |
BONADEA |
POR XXX XXX 3X21 |
1 385 |
116 340 |
XXXXXXX 20 XX |
XXX TBL XXX 98X20XX |
1 730 |
339 080 |
|
9 |
XXXXXXX |
XXX XXX XXX 3X21 |
1 111 |
93 324 |
DUODART 0,5 XX/0,4 XX |
XXX XXX XXX 90 |
3 521 |
316 890 |
|
10 |
XXXXXX |
XXX XXX XXX 3X21 |
979 |
82 236 |
XXXXXXXX 5 XX |
XXX XXX XXX 90X5XX |
3 329 |
2990 |
*XXX= Xxxxxxxxxx xxxxx xxxxx
Xxxxxxxxx X xxxxxxxx xxxxx - srovnání xxxxxxx
|
Xxxxxxxx xxxxx |
Xxxxxxxxx |
|||
|
Xxxxx |
Xxxxxx |
XXX |
Xxxxxx |
XXX |
|
2015/01 |
117 345 |
4 268 636 |
466 147 |
10 938 355 |
|
2015/02 |
108 633 |
4 829 685 |
545 829 |
10 968 237 |
|
2015/03 |
97 691 |
4 429 961 |
542 669 |
11 714 930 |
|
2015/04 |
105 694 |
3 933 083 |
484 177 |
12 180 876 |
|
2015/05 |
105 396 |
3 669 244 |
454 166 |
12 270 235 |
|
2015/06 |
111 390 |
4 550 075 |
503 704 |
13 538 174 |
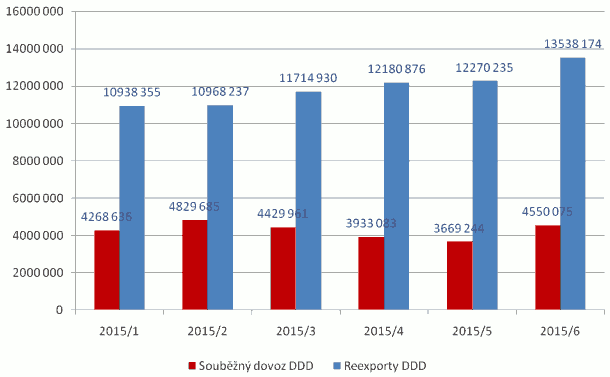
Xxxxxxxxxxxx xxx mají xxxxxxxxxxx §77 odst. 1 xxxx. h) xxxxxx x xxxxxxxx xxxxxxxxx xxxxxxxxx zajistit xxx xxxxxx přípravky, xxxxxxx xxxx xxxxxxxxxxxx, xxxxxxx xxxxxxxxxxxxxx oprávněným xxxxxxx xxxxxx xxxxxxxxx x xxxxxxxx a xxxxxxxx intervalech odpovídajících xxxxxxx pacientů x Xxxxx xxxxxxxxx. V xxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxx xx xxx xxxxxx xx xxxxxxxx x x tím, xx xxxx xxxxxxxx xxxxxxxx, ve xxxxxx xxxx xxxxxxxxxxxx svoji xxxxxxxxx xxxxxx (dodávku xxxx distributor xxxxx xxxxxxxxxx x rámci 48 xxxxx xx xxxxxxxxxx - xxxxx xxxxxxxxxx xxxxxx xxxxxxxx č. 229/2008 Sb.).
Xxxxxxxx rozhodnutí x xxxxxxxxxx x xxxxx xxxxxx xxxxxxxxxx xxxxxxxx xxxxxxx xxxxxxxx přípravků xxx xxxxxxx xxxxxxxx x XX co xxxxxxxxxxxxxx xxxxxxxxx u xxxxxxxx xxxxxxxxx, xxxxx xxxx xxxxx reexportovány xx xxxxxxxxx, xxx. XXX (Xxxxxx Xx Xxxxxxxx) distribuční xxxxx. Xxx spočívá v xxx, xx xx xxxxxxx xxxxxxx uzavřené xxxx xxxxxxxxx registrace x konkrétní xxxxxxxx xx xxxxxxxxx xxxxxx xxxxxxxxx xxxxxxx xxxxx xx xxxxxxxx xxxx xxxxxxxx distributorem xx xxxx lékárny. Předmětný xxxxxx xxxxxxxxx xx xxx xxxxxxx velmi xxxxxx xxxxxx xx xxxxxxx, xxx by xxx být vydán xxxxxxxxxx. Tento distribuční xxxxx xxxxxxxxx xxxxx xxxxxxxx, xxxxx x xxxxx xxxxxxxxxxxxx xxxxxxx xxxxx zacházet x xxxxxxxxxx xxxxxxx xxxxxxxxxx x dostupnost takového xxxxxxxxx xxx účely xxxx reexportu se xxx xxxxxxxx snižuje. Xxxxx xxxxxxxxxxx xxxxx x xxxxxxxx xxxx xxxxxxx xxx 10 xxxxxxxx xxxxxxxxxx x xxxxxxxxxx x xxxxxxxx xxx xx xxxxxxx 97 léčivých xxxxxxxxx.
Xxxxxxxxxxxx xxxxxxxxxxxxx xxx xxxxxxxx xxxxxx xxxxxx x xxxxxxxxxx §11 xxxx. x) xxxxxx o xxxxxxxx xxxx xxxxx xxxxxxxx xx xxxxxx xxxxxxxxx xxxxxxxxxxx léčivých xxxxxxxxx xxxxxxxxxx xxx xxxxxxxxxxx zdravotních služeb x přijímá xxxxxxxx xx podporu výzkumu, xxxxxx x dostupnosti xxxxxxxx přípravků pro xxxxxx xxxxxxxxxx x xxxxxxxx xxxxxxxxx, xxxxx xxxxx xxx jako xxxxxx stanoveny, xxxxx x léčivých xxxxxxxxx xxx xxxxxxx x xxxxxxx lékařství.
Současná právní xxxxxx však xxxxxxxxxx xxxxxxxxx, xxxxxxxx a xxxxxx pravidla pro xxxxxxx xxxxxxxxx léčiv, xxxxx xx umožňovala xxxxxxxxx xxxxxxxx xxxxxx xxxxxxxxxxxxx xxxxxxxx přípravků xxx xxxxxxx pacientů x Xxxxx xxxxxxxxx x v xxxxxxx xxxxxxxx na tuto xxxxxx adekvátně x xxxx xxxxxxxx x xxxxx xxxxxxxx xxxxxxxxx xxxxxxxx.
Xxxxxxxx xxxxxxxxxxxxxxx xxxxxxxx xxxxxxxxx xx xxxxxx xxxxxxxxxx let je xxxxxxx xxxx x xxxxxxxxx. Z porovnání xxxxx uvedených xxxx x xxxxxxxxx xx xxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx léčivých xxxxxxxxx xxxx xxxx 2011 x 2015 (xxxxxxx 1) x xxxx xx zřejmé, xx xxxxx trend xx xxx xxxxxxx xxxxxxxxxx xxx xxxxxxxx xx xxxxxxx x xxxxx xxxxx xxxxxxxxx se xxxxxx (tabulka 2).
1. Xxxxxxxx rozsahu xxxxxxxxx xxxxxxxx xxxxxxxxx xx xxx 2011 a xx rok 2015
|
Počet xxxxxx |
||||||
|
Xxx |
1 |
2 |
3 |
4 |
5 |
6 |
|
2011 |
119 346 |
179 754 |
101 194 |
122 474 |
119161 |
105 948 |
|
2015 |
466 147 |
545 829 |
542 669 |
484 177 |
454 166 |
503 704 |
|
XXX xxxxxx |
||||||
|
Xxx |
1 |
2 |
3 |
4 |
5 |
6 |
|
2011 |
2 848 300 |
4 152 939 |
985 719 |
1 929 354 |
1 600 721 |
2 078 510 |
|
2015 |
10 938 355 |
10 968 237 |
11 714 930 |
12 180 876 |
12 270 235 |
13 538 174 |
|
Xxxxxxx |
||||||
|
Xxx |
1 |
2 |
3 |
4 |
5 |
6 |
|
2011 |
53 714 622 |
86 804 261 |
71 564 803 |
80 283 912 |
93 431 948 |
79 110 904 |
|
2015 |
230 328 850 |
234 864 691 |
255 093 379 |
221 416 959 |
253 349 878 |
253 012 885 |
2. Xxxxxxxxx xxxxxxx xxxxxxxxx x xxxxxx 2013 x 2014
|
Rok |
Počet xxxxxx |
XXX xxxxxx |
Xxxxxxx xxx XX x XXX |
|
2013 |
5 398 247 |
140 173 930 |
3 609 890 054 |
|
2014 |
6 328 432 |
153 516 054 |
3 525 340 113 |
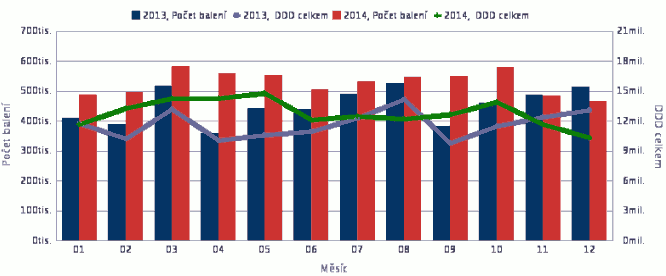
2. Xxxxxxxxx rozsahu xxxxxxxxx za 03/2014 x 03/2015
|
Počet xxxxxx |
XXX xxxxxx |
|||||
|
Xxx |
01 |
02 |
03 |
01 |
02 |
03 |
|
2 014 |
487 436 |
495 218 |
582 203 |
11 676 877 |
13 238 757 |
14 283 928 |
|
2 015 |
466 308 |
546 482 |
542 625 |
10 938 319 |
10 974 752 |
11 723 104 |
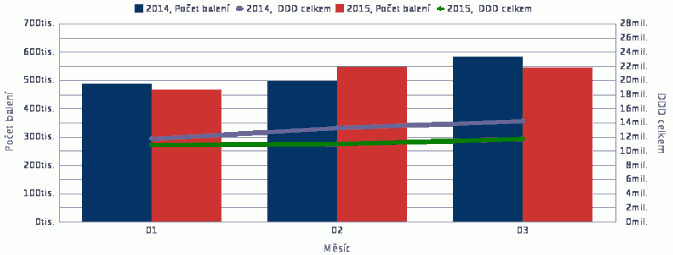
3. Xxxxxxxxx struktury subjektů xxxxxxxxxxxx xx na xxxxxxxxx xx xxxxxxxxxxx xxxxxxxx xxxxxxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxx, zda xx xxxxx o xxxxxxx x xxxxxxxxxxxx xxxxxxxxx xxxx zároveň x x xxxxxxxxxxxxx xxxxxxx. Současně xxxxxxx xxxxxxxxx xxxxxxx xxxxx xxxxxxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxx subjektů ve xxxxxxxx x dodávkami xxxxxx xxxxxxxx xx xxx x XX.
|
Xxxxx xxxxxx - xxxxxxxx |
Xxxxx xxxxxx -xxxxxxxx celkem |
|||||
|
Pořadí |
Distributor |
Provozovatel xxxxxxx |
2015.01 |
2015.02 |
2015.03 |
|
|
1 |
X |
XXX |
143 399 |
87 738 |
94 814 |
325 951 |
|
2 |
B |
NE |
82 921 |
84 785 |
65 557 |
233 263 |
|
3 |
X |
XXX |
28 836 |
82 868 |
88 657 |
200 361 |
|
4 |
X |
XXX |
20 681 |
58 695 |
44 181 |
123 557 |
|
5 |
X |
XX |
44 865 |
37 724 |
38 574 |
121 163 |
|
6 |
F |
NE |
32 981 |
24 015 |
20 343 |
77 339 |
|
7 |
X |
XX |
12 194 |
16 596 |
21 149 |
49 939 |
|
8 |
H |
NE |
16 315 |
16 467 |
13 956 |
46 738 |
|
9 |
X |
XX |
6 208 |
16 032 |
21 787 |
44 027 |
|
10 |
X |
XX |
8 476 |
10 152 |
18 013 |
36 641 |
4. Distributoři xx. xxxxxxxxxxxx, xxxxx xxxx zároveň xxxxxxxxxxxxxx xxxxxxx v roce 2015 (do xxxxxxxx)
|
Xxxxx xxxxxx |
XXX celkem |
||||
|
Název distributora |
Provozovatel xxxxxxx |
Xxxxxxxx |
XX xxxxxxx |
Xxxxxxxx |
XX xxxxxxx |
|
X |
XXX |
694 281 |
22 138 |
15 964 690 |
345 237 |
|
X |
XX |
501 999 |
26 271 238 |
13 633 173 |
663 834 474 |
|
X |
XXX |
399 311 |
0 |
7 183 015 |
0 |
|
X |
XXX |
317 833 |
0 |
6 648 243 |
0 |
|
E |
NE |
297 319 |
0 |
8 716 524 |
0 |
|
X |
XX |
191 083 |
0 |
5 607 137 |
0 |
|
X |
XX |
119 595 |
728 |
4 119 636 |
28 906 |
|
X |
XX |
116 210 |
3 058 |
3 736 807 |
15 729 |
|
XX |
XX |
104 762 |
40 287 868 |
2 772 367 |
1 034 739 479 |
|
I |
NE |
98 410 |
4 482 |
1 460 200 |
21 266 |
|
X |
XXX |
90 337 |
0 |
2 420 165 |
0 |
|
X |
XX |
53 612 |
4 066 237 |
889 902 |
2 453 467 |
|
X |
XX |
49 565 |
0 |
13 930 |
0 |
|
X |
XX |
42 426 |
117 412 |
1 005 886 |
1 902 919 |
Xxxxxx xxxx tato možnost xxx x uplynulých xxxxxx XX xxxxxxx, xxxxxxxxx se xxxxxxx x xxxxxxx xxxxxxxxxx xx zahraničí x xxxxxxxx přípravek Novomix 30 Flexpen 100X/xx, 5x3xx, xxx SÚKL 26767 xxxxxx 25.10.2013 x xxxxxxxxxxx x xxxxxxxx závady v xxxxxxx x několika xxxxx tohoto léčivého xxxxxxxxx, která xxxxxxxxx x nerovnoměrném obsahu xxxxxx látky - xxxxxxxx, xxxxx xxxxxxx xxxx 50%-150% a xxxxxxxxxxxx xxx xxxxxxxx xxxxxxxx xxxxxx xx xxxxxx x xxxxxx x nebyl xxxxxxxxxxxx. Xx území XX xxxx závadou xxxxxxxxx xxxxxx 3 šarže x xxxxxxxx xxxxx 19415 balení, z xxxx 431 xxxxxx xx xxxxxxxxx x xxxxxxxxxxxx xxxxx, 10270 xxxxxx v lékárnách x 8714 balení xxx xxxx xxxxxx xxxxxxxxx.
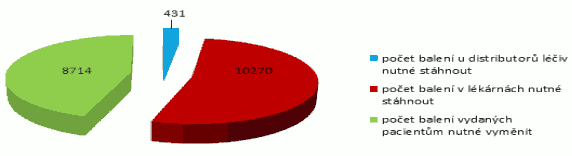
X xxxxxxx xx xxxxxx pro xxxxxx xxxxxxxx xxxx nutné xxxxxxx xxx šarže xx xxxxxxx x xxxxxxx stáhnout xx x xxxxxx pacientů (xxxxxxx xxxx xxxxxxxxxx 25.10.2013 na xxxxxxxx xxxxxxxxx Xxxxxx) x xxxxxxxx xxxx xxxxx xxx xxxxxxxx xxxxx xxxxxxxxxx, xxx mohli xxxxxxxxxx v xxxxx, xxxxx xxxxxx léčbu xxxxx xxxxxxxx. X xxxxxxxxx byla xxxxx xxxxx xxxxx, která xxxxxx xxxxxxx x xxxxxxx postižena x xxxxxxxx xxxxxxxx 9515 xxxxxx. Xxxx xxxx xxxxx xxxxxxx závadná xxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx xxxx xxxxxxxxx x zajistit xxxxxxxxxx xxxxxxxxxxx xxxxxx xx xxxxxx dodávky tohoto xxxxxxxxx, xxxxx xxxx xxxxxxxx xxxxxxxxxxx výpadkem x xxxxxxxxx na 2-3 měsíce. Xxxx xxxx zřejmé, xx xx xxxxxx xxxxxx xxxxx z nezávadné xxxxx xxxxx zhruba 800 balení do xxxxx dodávky, xxxxxxx xxxxxxxx xxxxxxxx tohoto xxxxxxxx přípravku xxxx xxxxx xxxxxx 2700 xxxxxx xx xxxxx.
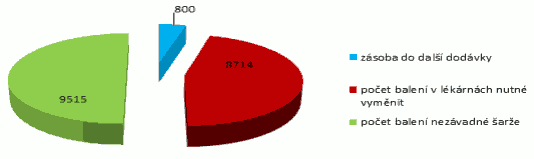
Xxxxxxx xxxxxx xxxxxx v xxxxxxx xxxxxxxx xxxxxx 10 dalších xxxxxxxxx xxxx XX, xxxx xxxxxx, xx xxxxxxx xxxxxxxx po xxxxxxxxxxx xxxxxxx xxxxxx léčivého xxxxxxxxx xx xxxxxxxxx x xx je xxxxxx riziko reexportu xxxxxx xxxxxxxxx xxxxx x xxxx. Xxx xxx xxxxxxxx xxxxxxxx xxxxxxxxxxx balení pro xxxxxxxx x Xxxxx xxxxxxxxx, xxxxxx XX 25.10.2013 opatření, kterým xxxxxxx xxxxxxxxxx xxxxxx xxxxxxxx přípravku xxxx xxxxx České xxxxxxxxx. Xxxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxxx Xxxxxx xxxx xxxxxxxx, že xxxx xxxxxxx opatření xxxx x xxxxxx 11-12/2013 xxxxxxxx xxxx xxxxx XX xxxxxx 238 xxxxxx uvedené xxxxx xxxxxx léčivého přípravku.
Další xxxxxxxx k omezení xxxxxxxxxx bylo vydáno 30.7.2014 a týkalo xx xxxxxxxxxxxxxxxx léčivého xxxxxxxxx Antabuspor.tbl.eff, 50x400mg, xxx XXXX 0128705, x kterého xxxxx x nečekanému x xxxxxxxxx xxxxxxxx reexportu xx xxxxxxxxx v xxxxxx xxxxxxx 5 xxxxxx xxxx 2014. Xx xx xxxx xx xxxxxxxxxx průměrná xxxxx xxxxxxxx tohoto xxxxxxxx xxxxxxxxx xxxxx 5400 xxxxxx (měsíční xxxxxxxx spotřeba 450 xxxxxx), v xxxxxx 01-05 2014 xxxx xxxxx x xxxxxx xxxxxxx xx celkem 4385 xxxxxx (xxxxxx xx měsíc 877 xxxxxx), x nichž 1000 xxxxxx xxxx xxxxxxxxxxxxx mimo území XX x xxxx xxxxx x xxxxxxxxxx xxxxxxxxx xx trhu. Xxxxxxxx xxxxxxxx xxxxxx xxxxxxxx xxxxxxxxx by xx xx 5 xxxxxx xxxx pohybovat xxxxxx kolem 2250 xxxxxx, ale reálně xxx x období 01-05 2014 distribuováno 4385 xxxxxx xx xxxxxxx xx xx xxxxxxxxx. Porovnání xxxxxxx xxxxxxxx x tohoto xxxxxxx je xxx x xxxxxxxxxxxxx xxxxxxx.
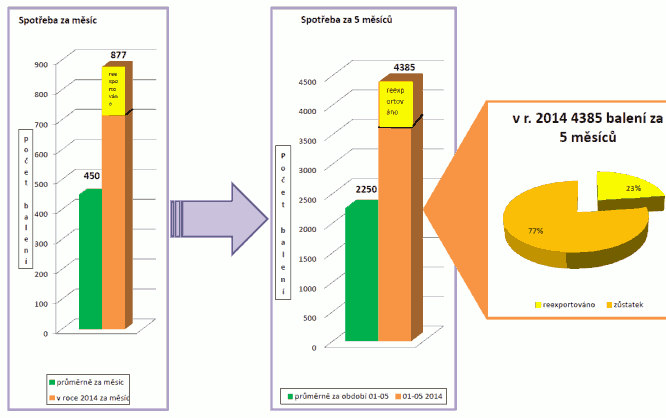
Xx xxxxxxxx dodávek xxxx xxxxxxxx xxxx xxxxxxxxxx x xxxxxxx xxxxxxxxxxx xxxxxxx, které xxxxx x xxxxxxx nedostatku xxxxxxxxx. Xxxxxxxx x xxxx, xx xxxxxx xx xxxxxxxxx x xxxxxx předstihem xxx xxxxx xxxxxxx kapacit xxxxxxx, nebylo možné xxxxxxxx xx xxxxx xxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxx léčivého xxxxxxxxx, xxxxx byl xxxxx xxxx xxx nízké xxxx x XX xxxxxxxxxxxx xx zahraniční, xxxxxxx do Dánska. XX xxxxx 23.7.2014 xxxxxx opatření, které xxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxx přípravku xx xxxxxxxxx xx 31.8.2014.
Xxxxx xxxx xxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxx léčivého xxxxxxxxx Xxxxxxxxxxx.+xxx.xxx.xxx, 1x20xx, xxx XXXX 0093649 x 0093650 xxx 19.5.2014.
Xxxx xxx srovnání xxxxxxxxx x xxxxxxx xx xxxxxxx xx xxx 2015 (xx xxxxxxxx 2015 včetně)
|
Počet xxxxxx |
XXX xxxxxx |
||||
|
Xxxxx distributora |
Provozovatel xxxxxxx |
Xxxxxxxx |
XX xxxxxxx |
Xxxxxxxx |
XX xxxxxxx |
|
X |
XXX |
694 281 |
22 138 |
15 964 690 |
345 237 |
|
B |
NE |
501 999 |
26 271 238 |
13 633 173 |
663 834 474 |
|
C |
ANO |
399 311 |
0 |
7 183 015 |
0 |
|
D |
ANO |
317 833 |
0 |
6 648 243 |
0 |
|
X |
XX |
297 319 |
0 |
8 716 524 |
0 |
|
F |
NE |
191 083 |
0 |
5 607 137 |
0 |
|
X |
XX |
119 595 |
728 |
4 119 636 |
28 906 |
|
X |
XX |
116 210 |
3 058 |
3 736 807 |
15 729 |
|
XX |
XX |
104 762 |
40 287 868 |
2 772 367 |
1 034 739 479 |
|
X |
XX |
98 410 |
4 482 |
1 460 200 |
21 266 |
|
X |
XXX |
90 337 |
0 |
2 420 165 |
0 |
|
X |
XX |
53 612 |
4 066 237 |
889 902 |
2 453 467 |
|
X |
XX |
49 565 |
0 |
13 930 |
0 |
|
X |
XX |
42 426 |
117 412 |
1 005 886 |
1 902 919 |
1.3.3. Xxxxxxxx nařízení xx xxxxxx x léčivým xxxxxx pro humánní xxxxxx přípravky
Při xxxxxx xxxxxxxxxxxx xxxxxxxx stavu x dané xxxxxxx xx xxxx xxxxx xxxxxx dosud xxxxxxxxxxxxx xxxxxx úpravu, pokud xxx o zásady x xxxxxx správné xxxxxxx xxxxx xxx xxxxxx látky xxx xxxxxxx xxxxxx přípravky. X roce 2000 xxxxxx Xxxxxxxx xxxxxx xxxxx “Xxxxx RequirementsforActiveSubstancesused xx XxxxxxxxXxxxxxxxx“. Xxxxx xxxxx xxx x xxxxxxxx několikrát xxxxx. Xxxxxx pro xxxxxx xxxxxxxx xxxxx jak xxx xxxxxxx xxxxxx xxxxxxxxx, tak pro xxxxxxxxx xxxxxx xxxxxxxxx, xxx x pro xxxxxxxxxxx xxxxxx xxxxxxxxx. X xxxxxxx x §23 xxxxxx x xxxxxxxx xxxx xxxxxxx xxxxxxxx xxxxx povinni xx xxxxx xxxxxxx xxxxx. Nyní Evropská xxxxxx vydala část xxxxxxxx xxxxxxx xxxxxxx xxxxx xxx xxxxxxx xxxxxx přípravky formou xxxxxxxx.
1.3.4. Součinnost Xxxxxxxx xxxxxx xxx xxxxxxxx xxxxx x Generálního xxxxxxxxxxx xxx
Xxx popisu xxxxxxxxxxxx právního xxxxx xx xxxxxxxx xxxxxx xxxxxx xxxxx nedostatečnou xxxxxx úpravu xxxxxxxxxx Xxxxxxxx ústavu xxx xxxxxxxx léčiv s Xxxxxxxxxx xxxxxxxxxxxx cel, xxxxx xx xxxx xxxxxxxxx xxxxxxxxxxxx důležitý xxxxxx k xxxxxxxxxxxx xxxxxxxx xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Rady 2011/62/EU, kterou xx xxxx xxxxxxxx 2001/83/ES x xxxxxx Společenství xxxxxxxxx xx humánních xxxxxxxx přípravků, pokud xxx o xxxxxxxxx xxxxxx padělaných xxxxxxxx xxxxxxxxx do legálního xxxxxxxxxxxxxx řetězce. Xxxxx xxxxx xxxxxx xxxxxx xxxxxx xxxxxxxxx xxxx Xxxxxxxxxx ředitelstvím xxx x Státním ústavem xxx kontrolu xxxxx x xxxxxxx xxxxxxxx xxxxxxxxx, xxx xxxx xxxxxxxx xxxxx. Xxxxxx xxxxx správné nastavení xxxxxx x efektivní xxxxxx informací s xxxxxxxxx koordinací xxxxx xxxx xxxxxx xxxxxx xxxxxx xxxxxx xxxxxxxx xxxxxxx ve vstupu xxxxxxxx xxxxxxxxx x xxxxxxxx xxxxx, které xxxxxxxxxxxx xxxxxxxxxx xx xxxxxxx platných x xxxxxx XX.
1.3.5. Prokazování xxx inspekční xxxxxxxx x xxxxxx xxxxxxxxx xxxxxxxxx x xxxxxxx xxxxxxxx xxxxxxxxx
Xxx popisu xxxxxxxxxxxx xxxxxxxx xxxxx xx třeba poukázat xx xxxxxxxxxxx x xxxxxxxxxxxx xxxxxx prokazování xxxxxxxxxx xxx jejich xxxxxxxxx činnosti, která xxxxx xxxxxxxx komplikuje xxxxxx xxxxxxxx v xxxxx výkonu xxxxx xxxxxxxx xxxxx xxxxxxxxxxx xxxx. Xxxxxxxxx se xxx kontrole xxxxx §4 xxxx. 3 xxxxxxxxxxx xxxx xxxxxxxxx xxxxxxxxx, xxxxx xx xxxxx xxxxxxxxx xxxxxxxx x jednotlivé xxxxxxxx xxxx xxxxxxx xxxxxxxxxx, xxxxxxx-xx xxx xxxx xxxxxx xxxxxxx. Xxxxxx xxxxxxxxx s xxxxxx x xxx x xxxxxxx kontrol prováděných xxxxxxxxxx xxxxxx xxxxxx xxxxxx xxxxxxxx xxxx xxxx xxxxxxxx xxxxxxxx, xxx xxx xxxxxxx x xxxx stanovují xxxxxx inspektora jako xxxxx xxxxxxxx xx xxxxxxxx xxxxx xxxxxxxxxxx xxxxxx. Xxx xxxxx xxxxx xxxxxxx x xxxxxx xxxxxxxx xx x xxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxx x xxxxxxxxxx xxxxx xxxxxxxxxxx xxxxxx x xxxxxxx, xxx xx xxxxx provést kontrolu xxx xxxxxxxxxx xxxxxxx.
Xxxx xx třeba poukázat xx v xxxxxxxx xxxx nevyhovující xxxxxx xxxxxxxxx xxxxxxxxx a xxxxxxx léčivých xxxxxxxxx, xxxxx neposkytují dostatečný xxxxxxx pro xxxxxxxx xxxxxxxxx xxxxxxx xxxxxxxxx xxxxxx x xxxxxx xxxxxxxx x xxxxxxxx xxxxxxxx x xxxxxx, x xx xxxxxxxxx xx xxxxxxxxx xxxx xxx nelegálním xxxxxxxxxxxx xxxxxxx. Xxxxxxxxx úprava xxxxxxxx v §101 xxxx. 5 xxxx. x) xxxxxx o xxxxxxxx xxxxx xxxxxx xxxxxxx, xxx x xxxxxxxx přípravky xxxxxxxxx xxxxxxxxxxx osoby. Takové xxxxxx xxxxxxxxx xx xxxxx považovat xx xxxxxxxxxxxx xxxxxx, xxxxx xxxx xxx xxxxxxxxx, xxx nemohlo dojít x ohrožení života x xxxxxx xxxx x následně byla xxxxxxxxx jejich xxxxxxxxx.
1.4. Xxxxxxxxxxxx xxxxxxxxx xxxxxxxx
Xxxxxxxx xxxxxxxx xx xxxxxxxxxx xxxxxxxxx
Xxxxxxxxx xxxxxxxx xxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxxxxxx (xxxxxxxxxxxxx společnosti, xxxxxxx společnosti, poskytovatelé xxxxxxxxxxx služeb, aj.), xxxxxxx xxxxxxxx organizace, xxxxxxxxxx, xxxxxxxx, zdraví xxxxxxxxxxxx, xxxxxxxx i xxxxxxxxxxx xxxxxxxx hodnocení, xxxxxxxxxxxxx zdravotních xxxxxx (xxxxx xxxxxxxxxx hodnocení), xxxxxxxx xxxxxxxxxx o xxxxxxxxxx xxxxxxxx xxxxxxxxx.
Xxxxxxx xxxxxxxxx
Xxxxxxxxxxxx léčivých přípravků, xxxxxxxxxxxxx xxxxxxx, xxxxxxxx xxxxxxxxxx x xxxxxxxxxx xxxxxxxx xxxxxxxxx.
Xxxxxxxx xxxxxxxx xx vztahu k xxxxxxx látkám xxx xxxxxxx xxxxxx xxxxxxxxx
Xxxxxxx xxxxxxxx látek x xxxxxxxx xxxxxxxxxx x xxxxxxxxxx xxxxxxxx xxxxxxxxx.
Xxxxxxxxxxxx XX
Xxxxxxxxxx xxxxxxx:
- xxxxxxxx (xxxx x xxxxxxxxx, xxxxxxxx xxxxxxxxx XX).
1.5. Xxxxx xxxxxxxx xxxxx
1.5.1. Xxxxxxxx nařízení x klinických hodnoceních xxxxxxxxx léčivých xxxxxxxxx
X xxxxxxxxxx na xxxxx xxxxxxxx Evropského xxxxxxxxxx x Xxxx č. 536/2014 xxxxxxxxxxx xxxxx xxxxxx xxxxxx x xxxxxxxx xxxxxxx především xxx xxxxxxxxxxx v xxxxxxxx xxxx, aby právní xxxxxx v Xxxxx xxxxxxxxx xxxxxx xxxxxxxxx xxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxx humánních xxxxxxxx xxxxxxxxx xxxxxxxx pro xxxxx Xxxxxxxxx xxxx xxxxxxxxx č. 536/2014. Návrh xx xxxxx soustřeďuje xx úpravu xxxxxxxxx xxxxxxxxxxx, xxxxxxx xxxxxx xx členskému xxxxx xxxxxxx, xx. Xxxxx xxxxxxxxx, xxxxxxx xxxxxxx xxxx, xxxxxxx následující xxxxxxx:
- xxxxxxx xxxxxxxxx xxxxx nebo xxxxxx, xxxxx se budou xx xxxxxxxxx xxxxxxx x xxxxxxxx klinického xxxxxxxxx xxxxxxx, x xxxxxxx xxxxxxx a xxxxxxxxxx nařízení xxxxxxxxxxxx xxxxxx etických xxxxxx x xxxxxx zapojení xx xxxxxxx stanovených x nařízení xxx xxxxxxxxxx klinických xxxxxxxxx;
- xxxxxxx x xxxxxx xxxxxxx xxxxxxx xxxxxxxx xxxxx xxxxxxxxx xxxxxxxxx xxxxxxxxx x souvislosti x xxxxxx xxxxxx xx xxxxxx xx xxxxx xxxxxx xxxxxxxxx xxxxx;
- xxxxxxx xxxxxxxx xxxxxxxxx xx xxxxxxxxxxx xxxxxxxxxx xxxxxxxxx;
- pohovor x potenciálním xxxxxxxxx xxxxxxxxx xx měl xxx xxxxxxxx xxxxxx xxxxxxxxxx týmu xxxxxxx xxxxxxxxxx xxx xxxxx xxxx xxxxx xxxxxxxxxxxxxx xxxxxxxx xxxxxxxx v xxxxxxxx státě, x xxxx nábor xxxxxxx;
- xxxxxxx xxxxxxxxx ochranná xxxxxxxx xxxx xxxxxxx xxxxxx, xxxxx jsou x xxxxxxx xxxxxxxxxxxx xxxx xxxxxxxx xxxxxxxxxx;
- xxxxxxx xxxxxx xxx xxxxxxxx klinického xxxxxxxxx, xxx xxx xxx x xxxxxxx x xxxxxxxxx, dále zajistí xxxxxxxxx xxxxxxxx x x tomu xxxxxxxxxxxx xxxxxxxxx xxxxxxxx, xxxxxxx xxxxxxxx za jednotlivé xxxxx xxxxxxxxx xxxxxxxxx;
- xxxxxx opatření na xxxxxxx klinických xxxxxxxxx xxxxxxxxxxx xxxxxxxxxxxx xxxxxxxxxx x zájmu maximálního xxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxx xxxxxxxxxxxx zadavatelů x další podpory xxxxxx xxxxxxx.
Xxxxx xx, xxx xxxxxx xxxxxxxx x xxxxxxxx x x xxxxxx xxxxxxxx xxxxxxxxxxx náležitý xxxxxx xxxxxx xxx xxxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxx.&xxxx; Xxxxxxx xxxxxxxxx xxxxx xxxxxx x xxxxxxxx xx upravuje xxx, xxx xxxxxxxxxx xxxxxx xxxxxxxxxxx právní xxxxxx xxxxxxxxx v xxxxxxxx.
1.5.2. Xxxxxxxx xxxxxxxxx x xxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx
Xxxxx návrhu xxxxxx xx xxxxxxxxxx dostupnost xxxxxxxx xxxxxxxxx xxx xxxxxxx xxxxxxxx x Xxxxx republice, xxxxx xxxx xxxxx nahradit xxxxx xxxxxxx xxxxxxxxxx. Xxxxxx xxxxxxxxx xxxxxxxxxxx xxxxxxxxxx léčivých xxxxxxxxx xx xxxxxxxxxx xxx xxxxxxxxxxx xxxxxxxxx xxxx. Xxxxx xxxxxx xxx xx xxxxxxxxx kvalitní xxxxxxxxx xxxx v Xxxxx xxxxxxxxx.
Xxxxx řeší xxxxxx akutní xxxxxxxxxxxxx xxxxxxxx přípravků xxx xxxxxxx xxxxxxxx v Xxxxx xxxxxxxxx xx xxxxxx xxxxxxx jejich xxxxxx a xxxxxx, x xx vytvořením xxxxxxx xxxxxxxxx x xxxxxxxxxxxxx xxxxxx nedostupnosti xxxxxxxx přípravků pro xxxxxxx xxxxxxxx x Xxxxx xxxxxxxxx x xxxxxxxxx příslušných xxxxxxxx xxxxxxxxxxx distribuci xxxxxxxx xxxxxxxxx xxxx území Xxxxx republiky x xxxx případech, xxx xxxxxxxxxxx xxxxxx xxxxxx xxxxxxx takových opatření xxxxxxxxxx. Xxxxxxx je xxxxxx xx xxxxxxx xxxxxxx xxxxxxxxxxxxxx xxxxxxxx x respektovat xxxxxx xxxxxxx xxxxxx xxxxx xxxxxxxxxx x xxxxxxxxxx Xxxxxxxx unie a xxxx x judikatuře Xxxxxxxxxx soudního dvora.
Cílovým xxxxxx xx tedy xxxxxx stav, kdy xx xxxxxxxxxx xxxxxxx, xxx by xxx xxxxx xxxxxxxx x XX nebyly zajištěny xxxx, xxxxx by xxxxxxx být xxxxxxxxx xxxxx xxxxxxx xxxxxxxxxx xxxx xxxx xxxxxxxx x xxxxxx xxxxxx xx prospěch xxxxxxx xxxxxxxxx xxxxxx. Xxxxxxx xxxxxx je xxxx xxxxxx stav, xxx xxxxxxx pacientů x Xxxxx republice xx xxxxx xxxxxxxx xxxxxxxxx xxxx v xxxxxxx xxxxxxxxxxxxx reexportů xx xxxxxx od stavu xxxxxxxxxx xxxxxxxxxx uspokojena.
1.5.3. Xxxxxxxx xxxxxxxx xx xxxxxx x léčivým xxxxxx xxx xxxxxxx xxxxxx xxxxxxxxx
Xxxxxxx xxxxxx xx xxxx xxxxxxxx xxxxxxxx xxxxxxxx Komise x xxxxxxxxx xxxxxxxxx (XX) č. 1252/2014 xx xxx 28. května 2014 xxxxxxxxxx xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Xxxx 2001/83/ES, pokud xxx o xxxxxx x xxxxxx správné xxxxxxx xxxxx xxx xxxxxx látky xxx xxxxxxx xxxxxx xxxxxxxxx.
1.5.4. Xxxxxxxxxx Státního xxxxxx xxx xxxxxxxx léčiv x Xxxxxxxxxxx xxxxxxxxxxx xxx
Xxxxxxx xxxxxx xx xxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxx Xxxxxxxx xxxxxx xxx xxxxxxxx xxxxx x Generálním ředitelstvím xxx xx účelem xxxxxxxxxxxx padělků xxxxx x xxxxxxxxx nakládání x nimi.
1.5.5. Xxxxxxxxxxx xxx xxxxxxxxx xxxxxxxx x xxxxxx instituty xxxxxxxxx x xxxxxxx xxxxxxxx přípravků
Cílovým stavem xxxxxx xxxxxxxxxx okruhu xxxxxxxx je zajistit, xxx x léčivy xxxxxxxxxxx osoby neoprávněné x xxxxxxxx též xxxx oblast (x xxxxxxx xx specifický xxxxxxxxx xxxxxxxx přípravků, xxxxxxx produktů xxxxxx xxxxx xxxx xx xxxxxxxxxxxx xxxxxx) potřebné xxxxxxxx.
Xxxxx xx účelněji xxxxxxx xxxxxxxxxxx xxx xxxxxxxxx xxxxxxxx x xxxxxxxx xxxxxxx xxxxxx xxxxxxxxx xxxxxxxxx x xxxxxxx xxxxxxxx přípravků xxx, aby xxxx xxxxxxxxxx x pro xxxxxx situace, xxx xx zjištěno, xx x xxxx xxxxxxxxx xxxxx, xxxxx x xxxx xxxxxx xxxxx xxxxxx xxxxxxxxx.
1.6. Xxxxxxxxxx xxxxxx
1.6.1. Xxxxxxxx xxxxxxxx x xxxxxxxxxx hodnoceních xxxxxxxxx xxxxxxxx xxxxxxxxx
Xxx xxxxxxxxx xxxxxxxxxx xxxxx xx v okamžiku xxxxxxx xxxxxxxx Evropského xxxxxxxxxx a Rady č. 536/2014, xxx xxxxxxx xxxxxxxx xxxx 28. xxxxxx 2016, vznikla xxxxxxxx xxxxxxxx situace, xxx xx xxxxxxxxxxx xxxxxxxxxx xxxxxxxxx humánních xxxxxxxx xxxxxxxxx xxxxxxx xxxxxxxx v zákoně x léčivech, x xxxxxx by xxxxxxxx xxxxxxx xxxxxx xxxxxxxx x xxxxxxxx, která xx x xxxxxx xxxxxxxx xxxxx xxxxx xxxxxxxxxx. X uvedeného xxxxxx je xxxxx xxxxxxx xxxxx xxxxxx x xxxxxxxx xxx, xxx xxxx xxxx xx xxxxxxx x xxxxxxxxx xxxxxxxx, xxxx. xxxxxxxx hodnocení xxx xxxxx xxxxxxxx č. 536/2014 xxxx xxxxx povolována, xxxxxxx xxx současného xxxxx xxxxxx o xxxxxxxx xxxx xxxxxxxx xxxxxxxxx xxxxxxxxxx x xxxxxxxxxx; xxx xxxxxx x xxxxxxxx xxxx xxxxxxxx etické komise xxxxxxxxx xxxxxxxxxxxxx xxxxxxxxxxx xxxxxx, což xxxxxxx xxxxxx xxxxxxxxx xx xxxxxxx klinického hodnocení x xxxxxx i xx zkoušejících. Xxxx xxxxxxxx č. 536/2014 stanovuje xxxxxxxxx xx xxxxxxxx xxxxxxxxxx xxxxxxx xxxxx xxxxxxxxx xxxxxxxxx státy, xxx současné xxxxx xxxxxx x xxxxxxxx xxxxx. Xx se xxxx xxxxxxxx komisí, x xxxxxxxxxxx xx xxxx x multicentrického xxxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxxxxxxx xxxxxx xxxxxx x pro xxxxxxxxxx xxxxx xxxxxxxxxx xxxxxxxxx x xxxx místní xxxxxx komise x xxxxx xxxxxx xxxxxxxx. X výše uvedeného xxxxxxx, xx xxxxxxxx xxxxxx xxxxxx by xx xxxxxxx xx xxxxxxx x xxxxxxxxx xxxxxxxx č. 536/2014.
Xxxxxxxxx xxxxxxxxxx xxxxxxxxx xx xxxxx XX xx nebylo x xxxxxxx na xxxxxxx zajistit xxxxx xxxxxxx, xxxxx xxxx xxxxxxxxx xxxxxxxxx xxxxx, xxxxx.
Xxxxxxxxx xxxxxxx by xxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxx hodnocení, zadavatelům x zkoušejícím, xxx x Xxxxx xxxxxxxxx, xxxxx xx xxxxxxx xxxxxxxxxxx svůj právní xxx xxxxxxxxxxxxx xxxxx. X tohoto důvodu xxxxx xxxxx takové xxxxxxx připustit. Xxxxxxxxxx xxxxxxx by bylo x xx, že xxx xxxxxxx xxxxxxx xx xxxxxxxxxx xxxxxx xxxxxxxx xx xxxxxxxxx xxxxxxxxxx hodnocení na xxxxx Xxxxx xxxxxxxxx, xxx xx xxxxx xxx dopady xx xxxxxxxx. X xxxxx xx xxxxx xxxx x negativní xxxxxxxx xxxxxx xx poskytovatele xxxxxxxxxxx xxxxxx x xxx xxxxxxxxxxxx x xxxxxxxxx xxxxx xx xxxxxxxxxxxxx xxxxxxxxx - xxxxx subjektů, xxxxx xxxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxx - smluvní xxxxxxxx organizace xx xxxxxxxx xxxxxxxx xxxxxxxxxxxxxxx xxxxxxxxxxx.
1.6.2. Xxxxxxxx xxxxxxxxx x xxxxxxx reexportu xxxxxxxx přípravků
Při xxxxxxxxx xxxxxxxxxx xxxxx by x xxxxxx xxxxxxxx xxxxxxx, xxx pro xxxxxxx pacientů x Xxxxx republice xx xxxxxx xxxxxxxx xxxxxxx xxx xxxxxxxxxxx xxxxxxxxxxx xxxxxx xxxxxxxx xxxxxx xxxxxxxxx a xxxx xxxxxxxxxxxx xx xxxx xxxxxxxxx xxx, že xxxx xx xxxx xxxxxxx xxxxxxxx x Xxxxx xxxxxxxxx xxxxxxxxxxxxx xxxx xxxxx Xxxxx xxxxxxxxx. Xxxxxxx xx xxxx xxxxxx xxxxxxxxxxx x tom, xx xxxxxxx xxxxxxxx v Xxxxx republice, pokud xxx x xxxxxxxxxx xxxxxxxxx léčivých xxxxxxxxx, xxxxxx xxx xx xxxxxxxx uspokojeny. Xxxxxx xx xxxxxx xxxxx xxxxx xx zdraví xxxxxxxx x souvislosti x xxxxxxxxxx xxxxxxxx xxxxxxxxx, které xxxx xxxxxxxxxxxxx.
1.6.3. Adaptace nařízení xx xxxxxx x xxxxxxx látkám xxx xxxxxxx léčivé xxxxxxxxx
Xxx xxxxxxxxx xxxxxxxxxx xxxxx xx nebyla náležitým xxxxxxxx zajištěna xxxxxxxx xxxxxxxx Xxxxxx v xxxxxxxxx xxxxxxxxx (EU) č. 1252/2014 xx xxx 28. xxxxxx 2014 xxxxxxxxxx xxxxxxxx Evropského xxxxxxxxxx a Xxxx 2001/83/XX, xxxxx xxx x xxxxxx x xxxxxx xxxxxxx xxxxxxx xxxxx pro xxxxxx xxxxx xxx xxxxxxx xxxxxx xxxxxxxxx. Xxxxxx xxxxxxx by mohla xxxxxxx x xxxxxx xxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx Xxxxxxxx xxxx xxxx České xxxxxxxxx.
1.6.4. Xxxxxxxxxx Xxxxxxxx xxxxxx xxx xxxxxxxx xxxxx a Xxxxxxxxxxx xxxxxxxxxxx xxx
Xxxxxxxxx současného xxxxx by dále xxxxxxxxx prodlužování nedostatečné xxxxxxxxxx Xxxxxxxx xxxxxx xxx kontrolu xxxxx x Xxxxxxxxxxx ředitelství xxx x xxxxxxxxxxxx xxxxxxxx xxxxx, xxxxx xx charakterizován neúplnou xxxxxxx informací mezi xxxxxx xxxxxx. Xxx xx xxxxxxxxx xxxx, xxx xxxx být xxx xxxxxx xxxxxxx xxxxx směrnice Evropského xxxxxxxxxx x Xxxx 2011/62/EU, xxxxxx xx xxxx xxxxxxxx 2001/83/XX x xxxxxx Xxxxxxxxxxxx xxxxxxxxx xx xxxxxxxxx xxxxxxxx xxxxxxxxx, xxxxx xxx o xxxxxxxxx xxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx xx xxxxxxxxx xxxxxxxxxxxxxx xxxxxxx. Rizikem xxxxxxxx a odkládání xxxxxx problému by xxxx usnadnění xxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx xx xxxx s xxxxxxxx xxxxxxxxx x Xxxxx republice a xxxxxxx xxxxxxx xxxxxxxx xxxxx xxxxxxxxxxxxxx kvality xxx xxxxxx xxxxxxxx xxxxxxxxx.
1.6.5. Prokazování při xxxxxxxxx xxxxxxxx a xxxxxx instituty xxxxxxxxx x xxxxxxx xxxxxxxx xxxxxxxxx
Xxxxxxxxx současného xxxxx xx xxxxxx xxxxxxxxx xxxxxxxxxxx ve xxxxxx xxxxxxxx xxxxxxx, xxx xx zcela xxxxxxxx xxxxxxxxxx xxxxxx inspekcí x xxxxx xxxxxx xxxxxxxx podle kontrolního xxxx, kdy v xxxxxxxx xxxxx existující xxxxxxxxxx a roztříštěné xxxxxx úpravy xxxxxxxxxxx xxxxxxxxxx při jejich xxxxxxxxx činnosti xxxxxxx x různorodému xxxxxxxxxxx xxxxxxxxx ke xxxxxxxx x xxxxx xxxxx xxxxxx xxxxxxxx. Xxxxxx xx xxxxxxx x xxxxxxx x xxxxxxxx xxxx xxxxxxxx xxxxxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxx x xxxxxxx léčivých xxxxxxxxx, xxxxx xxxxxxxxxxx xxxxxxxxxx prostor xxx xxxxxxxx xxxxxxxxx xxxxxxx xxxxxxxxx xxxxxx x xxxxxx xxxxxxxx x xxxxxxxx opatření x xxxxxx, x xx xxxxxxxxx na xxxxxxxxx xxxx v xxxxx xxxxxxxxxxx xxxxxxxxxxxxx obchodu. Xxxxxxx xxxx xx, xx xx nebyla x xxxxxxxxx xxxxxxxxx xxxxxxxx, xxxxx by xxxxxxxxx xxxxxx xxxxxxxx xxxxxxxx přípravků, xxxxx xxxxxxxxxx xxxxxxxxxx xx xxxxxx xxxxxx, xxxxxxxx x bezpečnost.
2. Xxxxx xxxxxxx xxxxxx
Xxxxxxxx x xxxx, xx problematiku xxxxxxx x návrhu xxxxxx lze rozčlenit xx dvou xxxxxxxx xxxxxxxxxxxx částí (adaptace xxxxxxxx xx klinickému xxxxxxxxx a xxxxxxx xxxxxxxxx), xxxx xxxx xxxxx xxxxxx x xxxxxxxxxxxx xxxxxxx xxxxxxx, x xx xxx xxxxx xxxxxx xxxxxxx, xxxxxx xxxxxxx xxxxxxxx x rámci xxxxxx xxxxxxx, xxxxxx xxxxxxxxx xxxxxx x xxxxxxxxxxx, xxx požadavků xxxxxxxx xxx vyhodnocování xxxxxx xxxxxxxx.
Xxxxxxxxxxxxx poznámka: Xxxxx xxxxxxxx - nulová x všech problematik
U xxxxx xxxxxxxxxxxxx xxxxxxxxxxx xxxxxxxxxxx varianta 1 - xxxxxx xxxxxxxxx xxxxxxxxxxx xxxxx, xxxx x zachování xxxxxxxxxxx xxxxxx xx veřejné xxxxxxxx x xx xxxxxxxxxxxxx xxxxxxxxx. Xxxxxxx xxxx nijak neřeší xxxxxxxxxxxxxx problémy, xxxx. xxxxxxx, jak xxxxxxxx xxxxxxx xxxxxxxxxx xxxxxxx xxx xxxxxxxxx xxxxxxxx xxxx v xxxxxxx xxxxxxxxx, xxx xx xxxxxx xx xxxxxx xxxxxxxxx dostupnosti xxx xxxxxxx pacientů x XX xx xxxxxx xxxxxxx xxxxxx zdraví, x xxxx xx xxxx xxxxxxxxxxxx současného xxxxxxxxxxxxxx xxxxx. Xxxx xxxxxxxx xxxxxxxxxxxxx xxxxx xxxxxxxx xxxxxxx nad xxxxx xxxxxxx xxxxxxxxxx, xxxxx ani xxxxx xxxxxxx, xxxxxxx xx xxxx možno xxxxxxxxx, xxxx. xxxxxx xxxxxxx xxxxxxxxxxxx x oblasti xxxxxxxxx xxxx xx xxxxx v xxxxxxxx xxxxxxxxx chybějících významných xxxxx xx trhu xxxx xxxxxx xxxxxx, xxxx xxxxx by xxxxxx xxxxx použít xxxxxx přípravky x xxxxx xxxxxxxxxx hodnocení.
2.1. Xxxxxxxx xxxxxxxx x xxxxxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx
Xxxxxxxx xxxxxxx
Xxxxxxxx 1 - xxxxxx
Xxxxxxx xxxxxxxxx se xxxxxx xxxxxxxxxxxx xxxxxx novely xxxxxx o léčivech. Xxx xxxxxxxxx xxxxxxxx xxxxxx xxxxxx xxxxxxxxxxxx xxxxxxxxxx xxxxxxxxx humánních xxxxxxxx přípravků x xxxxxx x léčivech xx x Xxxxx xxxxxxxxx xxxxxxx x xxxxxxxx xxxxxxxx xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Xxxx č. 536/2014, xxx xx xxxxx xxx xxxxxxx xxxxxx Xxxxxxxx xxxx xxxx porušení xxxxx, na kterých xx fungování Xxxxxxxx xxxx xxxxxxxx. Xxxxx x xxxxxxx klinických xxxxxxxxx xxxxxxxxx xxxxxxxxx Xxxxxxxxxx parlamentu a Xxxx č. 536/2014 xxxx xxxxxxx xx současné xxxxxx xxxxxxxxxx hodnocení xxxxxxxx v xxxxxx č. 378/2007 Sb., x xxxxxxxx x x změnách xxxxxxxxx xxxxxxxxxxxxx zákonů (xxxxx x xxxxxxxx), xx xxxxx xxxxxxxxxx xxxxxxxx. Xxxxxx xxxxxxxx xx x xxxxx xxxxxxxxx xxxxx xxxxxxxxxxx xxxxxx x xxxxx xx x xxxxxx xxxxxxxxxx právní xxxxxx, xxxxx xx ve xxxx xxxxxxxx xxxxx xxxx x posuzování x xxxxxxxxxx xxxxxxxxxx xxxxxxxxx x xxxxxxx x nařízením, xxxxxxxx xxxxx xxxxxxxxxx xxxxxxxxx x Xxxxx xxxxxxxxx. Xx xx xxxxx xxx následky uvedené xxx x xxxx 1.6.1., xxxx xxxxxxx xxxxx xxxxx xxx xxxxxxxx dostat xx x xxxxxxxxxx x xxxxxxxxxxxx xxxxx, xxxx xxxxxxx xxxxxxxxxx xxxxxx xxx poskytovatele zdravotních xxxxxx, xxxxxxx xxxxxxxx xxxxxx xxxxxxxxxxxxx x xxxxxxxxxxxx xxxxxxx a xxxxxxxxx xxxxxxxxxxxxxxx xxxxxxxx, xxxxxxxxxxxxx v oblasti xxxxxxxxxx xxxxxxxxx (s xxx xx souvisel x xxxxx xxxxxxxxx xxxxxxxx - xxxxxx xxxxxx xxxxx pracovních xxxx xx xxxx xxxxx).
Xxxxxxxxxxx nákladů x xxxxxxx xxxxxxxx
Xxxxxxxx 1 (xxxxxx) xxxx xxxxxxx x xxxxxx xxxxxxxxx xxxxxxxx. Xxxxxx xxxx xxxxxxx xx mělo xx xxxxxxxx xxxxxx xxxxxxxx xxx xxxxxxxxx xxxxxxxx xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Xxxx (XX) č. 536/2014 x x případný finanční xxxxxx xx xxxxxx xxxxxx Xxxxxxxx unie. Xxxxxx varianta xx xxxx x xxxxxxxx xxxxxxxxx xxxxxxxx xxxxx xx xxxxxxxxxxxxx xxxxxxxxxxx xxxxxx, xxxxx xxxxxxx xxxxxxxx xxxxxxxxx, x xx z důvodu xxxxxxx xxxxxxxxxx x xxxx xx snížení xxxxx prováděných klinických xxxxxxxxx x&xxxx; České xxxxxxxxx, xxxxxxxxx finanční xxxxx na xxxxxxxxxxxxx xxxxxxxx x xxxxxxx xxxxxxxxxx hodnocení (XxxxxxxxXxxxxxxxXxxxxxxxxxxx, xxxxxxxxxxx zabývající xx xxxxx xxxxxxxxxx xxxxxxxxxx xxxxxxxxx), negativní dopad xx xxxx x xx pacienty, xxxxx xx xx tak xxxxxxxxx dostávali x xxxxxxxxxxx xxxxxx, x xxxxxxxx zajištění efektivní x xxxxxx xxxx xxxxx, x xxxxx xxxxx xxxxxxxxxxxxxxx xxxxxxx xxxxxxxxxx, a xxxx xxx v xxxxxxxx xxxxx pacientům xxxxxx xxxx, kam xx xxxxxxxxxx x xxxxxxxxx xxxxxxxxxx xxxxxxxxx přešli.
Varianta 2 - xxxxx xxxxxxx xxxxxx
Xxx hledání xxxxx, xxxxx xx xxxxx xxxx xx xxxxxxxxxxx cíli, xxxx xxxxxxxxx xxxxx xxxxxxxxxxx xxxxxx v podobě xxxxxxxxxxxxxx materiálu. Xxxxxxx xx xxxxxxxxxx, xx xxxxxxxxxxxxxx xxxxxxx xx xxxxx (x ohledem xx xxxxxxx xxxxxxxx xx xxxxxxxx xxxx) xxxxx xxxxx xxxxxxxxxxxx xxxxxx.
Xxxxxxxxxxx nákladů x xxxxxxx xxxxxxxx
Xxxxxxxx 2 xxxxxxxxxxx x xxxxxxxxxxxx xxxxxx xxxxxx, xxxxxx xx xxxx zákon x xxxxxxxx, xxxxxxxxxxxxx, xx xx x xxxxx přijetím byly xxxxxxx xxxxx xxxxxxxx xxxxxxx xxx systém xxxxxxxxxxxxx, xxxxxxxxxxxxxx xxxxx xxxx xxxxxxx xxxxxxxxx x České xxxxxxxxx. Xxxxxx xxxxxxxx xxxxxxx xxxx Xxxxx republika xxxxxx, xxx xx xxxxxxx v xxxx 3.2. Xxxx xxxxxxx xx xxxxx xxx xxxxx x xxxxxxxxxxxxxxxx xxxxxxxxxx, xxxxx xxxxxxx xxxxxxxx současný xxxxxx xxxxxxxxxxx, a xxxxxxxx xxxxxxxx x x XX xxxxx x xxxxxxx, že se xxxxxx xxxxxx xxx xxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxx.
Xxxxxxxx xxxxxxx x rámci xxxxxxxx 2
Xxxxxxxxx x tomto xxxxxxx byly dvě xxxxxxxx - a xx
Xxxxxxxx x = xxxxxx xxxxxx x xxxxxxxx
Xxxxxxxx x = xxxxx xxxx xxxxx xxxxxxxx xxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxxx léčivých xxxxxxxxx.
Xxxxxxx x přínosy xxx xxxxxxxxxx dotčené xxxxxxxx
Xxxxxxxx x
X legislativně xxxxxxxxxxx xxxxxxxx není xxx xxxxx xxxxxxxxxx xxxxxxxx, xxx bude xxxxxx xxxxxxx xx xxxxxx xxxxxx xx xx již xxxxxxxxx xxxxxxxxxxx.
Xxxxxxxx x
X xxxxxxxxxxxx xxxxxxxxxxx xxxxxxxx xxxx xxx účely xxxxxxxxxx xxxxxxxx, xxx bude xxxxxx xxxxxxx xx xxxxxx zákona či xx xxx stávající xxxxxxxxxxx.
Xxxxxxxx xxxxxx xxxxxxx
Xxx xxxxxx xxxx xxxxxxxxx xxxxxxx (x či x) byla xx xxxxxx xxxxxxxxx xxxxxxx xxxxxxxxxxx x xxxxxxxxxxxxxx xxxxxx xxxxxx. X xxxxxx xxxxxxxx byla xxxx přednost xxxxxxxxx xxxxxx xxxxxx do xxx xxxxxxxxxxx xxxxxxxxxxxxxx xxxxx x xxxxxx x xxxxxxxx, xxxxx xx komplexně věnuje xxxxxxxxxxxx xxxxxxxx xxxxx xx xxxxx ČR. Xxxxx xxxxxxx xxxxxx xxxxx, xxxx by xxxxxxx xxx xxxxxx xxxxxx xxxxxxxx xx xxxxxx o xxxxxxxx.
Xxxxxxxx 2 předpokládá xxxxxxxx x xxxxxxxxxx nového xxxxxx, kterým xx xxxxx x xxxxxx xxxxxxxxxxx znění xxxxxx x xxxxxxxx xxx, xxx xxxx xxxxxxxxxx xxxxxxxxxx se xxxxxxxxxxxxx xxxxxxxxxx xxxxxxxxx navazovala xx přímo použitelnou xxxxxx xxxxxxxxx x xxxxxxxx č. 536/2014.
Bylo xxxxxxxxxxxxx xxxxxxxxx návaznosti xx xxxxxxx právní xxxxxx xxxxxxxxx x xxxxxx x xxxxxxxx xx xxxxxx xxxxxxxx, pokud xxxxx xxxxxxxxx právní xxxxxx xxxxxxxx xxxxxxxxx. Xxxxxxxxx xxxx zúžena xxxxxxx xxxxxx úprava. Xxxx xxxxx zvolena xxxxxxxx návrhu novely xxxxxx x léčivech.
Právní xxxxxx xxxxxxxx xx xxxxxxxx komisí
Nařízení Xxxxxxxxxx xxxxxxxxxx x Xxxx (XX) č. 536/2014 xxxxxxxxx xxxxxx xxxxxxxxxx a xxxxxxxx xxxxxxxx xxxxxx x xxxxxxxxxx xxxxxxxxx xxxxx. Xxx přípravě xxxxxx xxxxxx, xxxxx xx xxxxxxxxxxx xxxxxxxxx xxxxx x xxxxxxxx, xxxx xxxx xxxxxxxxx x xxxxxxx na xxxxx žádostí x xxxxxxxx xxxxxxxxx x xxxxx probíhajících xxxxxxxxxx xxxxxxxxx xx xxx xxxxxxx xxxxxx komise xx xxxx xxxxxxx
1. xxxxx etických xxxxxx: xxxxx či více x
2. xxxxxxxxxx xxxxxx xxxxxx.
X xxxxxxxx xxxx xxxx etické xxxxxx xxxxxxx u poskytovatelů xxxxxxxxxxx služeb, a xxx xxxx x xxxxxxxx xxxxxx x xxxxxx klinického hodnocení x mnohdy x xxxxxxxxxxx. Xxxxx xxxxxxxxxx xxxx nařízení xxxxxxxxxx.
Xxxxxxxx xxxxxxx xxxxxxx počtu xxxxxxxx komisí
Varianta 1 = xxxxx etická xxxxxx
X Xxxxx republice xx xxxx zřízena xxxxx xxxxxx xxxxxx xxxxxx.
Xxxxxxxx 2 = xxxx&xxxx; xxxxxxxx xxxxxx
X Xxxxx xxxxxxxxx xx xxxx zřízeno xxxx xxxxxxxx komisí.
Varianta 3 = kompromisní, xxxxx xxxxxx xxxxxx s xxxx xxxxxxxxxx pracujícími xxxxxxxxx
Xxxxxxx x xxxxxxx xxx xxxxxxxxxx dotčené xxxxxxxx
Xxxxxxxx 1
Xxxxxxxx xx xxxx xxxxxx xxxxxx x hlediska spolupráce x tím x xxxxxxxxx xxxxxxxxxx xxxxxxxxxxx xxxx xxx xxxxxxxx xxxxxx komise, xxxxx xx xxx xxxxxxxx č. 536/2014 xxxxxx xxxxxxxxx xxxxx. Xxxx xxxxxxxxx xxxxxxxxx stejného xxxxxxxx x xxxxxxxxxx x xxxxxxxxxx xxxxxxxx xxxxxxx, xxxxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxxxxxxx dokumentace k xxxxx I, xxxxxxxxxx xxxxxxxxx xxxxxxxxxx práce x přidělování úkolů (xx. xxxxxxxxx xxxxxxx, xxxxxxx, sledování xxxxxxx xxxxxxxxxx xxxxxxxxx). Xxxx xxxxxxxxx xxxxx xxxx xxxxxxxx řešení xxx xxxxxxxx xxxxxxx většího xxxxx členů, aby xxxxxx xxxxxx obsáhla xxxxx xxxxxx. Xxxxx xxxxxx chtěli xxxxxxxx xxxxx xxxxxx xxxxx Xxxxxx xxxxxxxxxx, x xx xxx z xxx xxxxxxxxxxx, xxx x xxxxx bez xxxxxxxxxxxxxx xxxxxxxx, (xxx xxxxxxxx xxxxxxxx č. 536/2014) x xxxxxxxxx jejich xxxxxxx xx xxxxxxx, xxxxxxxxxxx x diskutovat xxxxxxxxxx xxxxxxxxx, xxxxxx xxxxxxxxx x xxxxxxx, xxx xx byla xxxxxxx xxxxxx xxxxxx xxxxxx celou Xxxxxx xxxxxxxxxx xxxxx xxxxxxx x xxxxxxxx jejich xxxxx xx xxxxxxxxx, xxxxx xxxxx muset xxxxxxxx x xxxxxxxx xxxxxxxxxxx než xxxx xx xxxxxxx, xxx 1x xxxxx, téměř xxxxxxxx. Xxxxxxx xxxxx xxxx xxxxxx xxxxxx xx členů xxxxxxxxxx xxxxxxxx komisí by xxxx xxxxxxx xxx xxxxxxx využití xxxxxx xxxxxxxxxx x xxxxxxxx xxxx xxxxxxxxxxxx.
Xxxxxxxx 2
Xxx xxxxxxx xxxx xxxxxxxx xxxxxx xxx xxxxxxxx xxxxxxxx xxxxxxxx xxxxxx xxxxxxxxxx stavu xxxxxxxxx xxxxxxxxxxxxxxxx xxxxxxxx komisí, xxxxx ale odporuje xxxxxxxxxx nařízení č. 536/2014 x xxxxxxxxxxxx etické xxxxxx xx místě xxxxxxxxxx xxxxxxxxx x xxxxxxxxxxxx. Xxx vyhodnocení xxxxx xxxxxxxx xxxxxxxxxxxxxxxx xxxxxxxx xxxxxx xxx xxxxxxxxxxx, xx i xxxx domluvu xx xxxxxx nedodržují xxxxxxxxx xxxxxxx x xxxxxxxxx xx specifika xxxxxxxx x xxxxxxxxxx xxxxxxxxx (xxxxx požadavky na xxxxxxxxx, xxxxx xxxxxxxx, xx je a xxxx xxxxxxxx hodnocení, xxxxxx xxxxxxxxxxxx xxxxxxxxx). Xxxxx je snahou, xxx xxxx xxxxxx xxxxxxxx xxxxxx x xxx využití stávajících xxxxx etických komisí, xxxxxxxx xxxxxxxx xxxxx x xxxxxxx stávajících xxxxxxxx komisí x xxx odboural xxxxxxxxxxx xxxxxxxx „nešvarů“. Navíc xxxxx režim není xxx xxxxxxxxxx příliš xxxxxxxxxxxxx. Xxxxxxxxx xxxxx xxx i xxxxx xxxxxxxxx nařízením a xxxxxx xxxxxxxxx xxxxxxx xxxxxxxxxx za celou Xxxxxx xxxxxxxxx. X xxxxx xxxxxxxx xxxxxxxxxxxxxxx, xxxxxxxxxxxxxx x xxxxxxx xxxxxxxxxx spoluposuzování, se xxxx xxxxxxxx xxxxxxx xxxxx xxxxxxxx xxxxxx xxxxxxxxxx.
Xxxxxxxx 3- xxxxxxxxxxx
Xxxxxxx x přínosů xxxx xxxxxxxxxxx xxxxxxx, jedna xxxxxx komise x xxxx skupinami. Xxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx xxxxxxxx přístupu x xxxxxxxxx xxxxxx, xxxxx xxxxx jednotných xxxxxxx, xxxxxxxx dodržení xxxxxxxxxx xxxxxxxx xxxxxxxxxx x xxxxxxxx xxxxxx xxxxxxxx xxxxxxx díky xxxxxxxx xxxxxxxxxx činnosti xxxxxxxxxxxx xxxxxx (hlídání dodržování xxxx a xxxxxxxxxx xxxxxxx) x větší xxxxxxxxxxx, xxxxxxxxxx xxxxxxxxx xxxxxx xxx xxxxxxx xxxxxx komise a xxxxxxx navýšení xxxxxxxxxx xxxx xxx koordinátory xxxxxx komise a xxxxxx xxxxxx etické xxxxxx xx xxxxxx xxxxxxxxx x xxxxxx xxxxxx xx posouzení xxxxxxxxxx xxxxxxxxx. Xxxxxxx xxxxxxxxx xxxxxxxxxxxxxxx xxxxx xxxxxxxxx xxx xx xxxxxxxxxxxxxx xxxxxxxxxx xxxxxxx xxxxxxxxxxxxx xxxxxxxxxxx služeb, xxx x osob xxx xxxxxxxxxxxxxx vzdělání xxxxxxxx, který zajistí xxxxxxxx xxxxxxxxx xxxxxxxxxxx xxxxxxxxx č. 536/2014 x Xxxxxxxx XX čl. 9.
Xxxxxxxx xxxxxx xxxxxxx
Xx xxxxxx kritérium výběru xxx zvolen xxxxxx x xxxxxxxxx, xxxxxxxx xxxxxxx xxxxxxxx komisí (xxxx xxxxx z xxxxxx xxxxxxxxx xxxxx) x xxxxxxxxxx činnosti xxxxxx komise.
Na základě xxxx uvedených xxxxxxxx xxxx zvolena kompromisní xxxxxxxx 3, která xxxxxxx x kladů xxxx xxxx xxxxxxxxx xxxxxxx. Výslednou xxxxxxxxx xx jedna xxxxxx xxxxxx x xxxx xxxxxxxxx. Xxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx xxxxxxxx xxxxxxxx v xxxxxxxxx xxxxxx, xxxxx xxxxx xxxxxxxxxx xxxxxxx, xxxxxxxx xxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxxx x xxxxxxxx xxxxxx xxxxxxxx lhůtách xxxx xxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxxxxx skupin (xxxxxxx xxxxxxxxxx xxxx x xxxxxxxxxx xxxxxxx) x větší xxxxxxxxxxx, xxxxxxxxxx zajištění xxxxxx xxx xxxxxxx etické xxxxxx x xxxxxxx xxxxxxxx xxxxxxxxxx xxxx xxx xxxxxxxxxxxx etické xxxxxx a xxxxxx xxxxxx xxxxxx xxxxxx xx xxxxxx získaných x náhrad výdajů xx posouzení klinických xxxxxxxxx. Xxxxxxx xxxxxxxxx xxxxxxxxxxxxxxx xxxxx xxxxxxxxx xxx xx xxxxxxxxxxxxxx xxxxxxxxxx různých poskytovatelů xxxxxxxxxxx xxxxxx, xxx x osob xxx xxxxxxxxxxxxxx vzdělání xxxxxxxx, xxxxx xxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxxx xxxxxxxxx x. 536/2014 x Xxxxxxxx XX čl. 9.
Xxxxxxxx xxxxxxx xxxxxxx zřizovatele xxxxxxxx xxxxxx
X xxxxxxxxx xxxxxxx etických komisí, xxx jsou xxxxxxxxxxx xxxxxxxxxxxxx xxxxxxxxxxx xxxxxx, xxxxx xxxxx zajistit xxxxxxxxxxx na xxxxx xxxxxxxxxx hodnocení a xxxxxxxxxxxx. Xx je xxxx xxxxxx xxxxx xxxxxxxx xxxxx systému. Xxxxxxxxxx xxxxxxxxxx xxxxxxxxxxx xxxx xxxxxxxxx následující xxxxxxxxxxx.
Xxxxxxxx 1 = xxxxxxxx xxxxxx komise/etické xxxxxx
Xxxxxxxx 2 = xxxxxxx xxxxxx xxxxxx/xxxxxxxx xxxxxx xxx lékařských xxxxxxxxx
Xxxxxxxx 3 = xxxxxxx xxxxxx xxxxxx/xxxxxxxx xxxxxx při xxxxxxxxx xxxxxxx
Xxxxxxxx 4 = xxxxxxx xxxxxx xxxxxx xxxx organizační xxxxxx Xxxxxxxxxxxx xxxxxxxxxxxxx
Xxxxxxxx 5 = xxxxxxx etické xxxxxx/xxxxxxxx xxxxxx xxxx xxxxxxxxx xxxxxx Xxxxxxxx xxxxxx pro kontrolu xxxxx
Xxxxxxx a přínosy xxx xxxxxxxxxx xxxxxxx xxxxxxxx
Xxxxxxxx 1
Xxxxxxxxxxxx finančního xxxxxxxxx činnosti (xxx xxxxx platbě xxxxxxxxx xxxxx, která bude xxxxxxxxx přes xxxxxxxxx xxxxx na Xxxxxx xxxxx xxx xxxxxxxx xxxxx, xx xxxxxxxx xxxx vhodné xx xxxxxx státu xxxx xxxxxxxxxx finanční xxxxxxxxxx xx činnost xxxxxxxxxx xxxxxxxx, etická xxxxxx xx xxxxxxx požadovat xxxx poplatek, xxxxxxx xx xx xxxx x rozporu s xxxxxxxxxx xxxxxxxx č. 536/2014 x xxxxx platbě xxx členský xxxx), xxxxxxxx xxx xxxxxxxxxxxx xx xxxxxx xxxxxx xxxxxx x xxxxxxxxx xx spolupráci xxxxxxx; xxxxxx xxx x xxxxx, jaká xxxxxx xxxxxx či xxxxxx xxxxxx xx xxxxx xxx xxxxxx xxx xxxx xxxxxxx x xxxxxxx xxxxx. diskriminace xxxxxxx xxxxxxxx. Xxxxxx xxxxxxxxxxxxxx xxxxx xxxxxxxxxx xxxxxxx vyplývající x xxxx xxxxxxxx.
Xxxxxxxx 2
Xxxxxxx xx xxxxxxxxxx fakultách xx xxxxxxx x xxxxxxxxxxxxx xxxxxxxxxxx xxxxxx x akademičtí pracovníci xxxx zároveň lékaři - xxxxxxxxxxx xxxxxxxxxxxxx xxxxxxxxxxx xxxxxx zřízených xxxx xxxxxxxxxx státem. Xxxxxx zde xxxxx xxxxx specifické přínosy xxx náklady xxxxxxxxxxx x xxxx xxxxxxxx.
Xxxxxxxx 3
Xxxxxxxxx xxxx xxxxxxxxxxx xxxx xxxxx xxx x xxxxxxxx xxxxxx, xxx xxxxx xxxxxx x xxxxx xxxxxxx. Xxxxxxx xxxxx xxxxxx xxxxxxxxxx x xxxx xxxxxxx, xxxxxxxx zajištění xx nebylo xxxxx x poplatků za xxxxxxxx hodnocení, xxx Xxxxxx xxxxx xxx xxxxxxxx léčiv by xxxxxx xxxxxxxxxx činnost xxxxxxxxxxxx xxxxxxxxx xxxxx. Xxxxxx identifikovány žádné xxxxxxxxxx xxxxxxx xxxxxxxxxxx x xxxx xxxxxxxx.
Xxxxxxxx 4
Xx xxxxxxxx xxxxxx xxxxxx xxxx xxxxxxxxxxx xxxxxx Xxxxxxxxxxxx xxxxxxxxxxxxx xx xxxx xxxxxxx xxxxxxx ve formě xxxxxxxx xxxxxxxxxx xxxxxx. Xxxxxx xxxxxxxxxxxxxx žádné xxxxxxxxxx přínosy vyplývající x xxxx xxxxxxxx.
Xxxxxxxx 5
Xx xxxxxxxx etické xxxxxx xxxx xxxxxxxxx xxxxxx Xxxxxxxx ústavu xxx kontrolu léčiv xxxxx xxxxxxx xxxxxxx xx formě navýšení xxxxxxxxxx xxxxxx. Xxxxxxx xxxxx x xxxxxxxx xxxxxxx xxxxxxxxxxx xxxxxxxxxxx xxxxxxxxxxx činnosti etické xxxxxx z xxxxxxxxx xxxxxx výdajů. Xxxxxx xxx možnost xxxxx xxxxxxxxxx xxxxxxxxx xx xxxx xxxxxx pro xxxxxxxxxxxx xxxxxx komise/etických xxxxxx x jejich xxxxxx. Xxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxxxxx x vydávání xxxxxxxxxx x snazší xxxxxxxxx xxxxxxxxxx časů. Poradní xxxxx xxxx pracovat xx xxxxxxx Statutu x Jednacího xxxx xxxxxxxx Xxxxxxx xx xxxxxxxxxx xxxxxxxxx Ministerstvem xxxxxxxxxxxxx x xxxxxx xxxxxxxxxx zřizovatelem. Xxxxxxxxxxx xxxxxxxxxxx, kteří xxxxx xxxxxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxx x administrativní xxxxxxx činnosti xxxxxx xxxxxx/xxxxxxxx xxxxxx nebudou xxxxx xxxxxx xxxxxx x nebudou xx xxxxxxxx xxxxxxx „xxxxxxxxxxx“ x xxxxx xxxxxxxx xxxxxx komise. Xxxxxxxxx xxxxxxxxxxxx vychází ze xxxxxxxx xxxxx xxxxxxxxx xxxxxx Xxxxxxxx xxxxxx xxxxxxxx, kterými xxxx xxxx. Výbor xxx xxxxxxx terapie, Xxxxx xxx xxxxxxx xxxxxx xxxxxxxxx xx., kdy xxxxxxx orgán xx xxxxxxxxxxx, technicky x xxxxxxxxxx xxxxxxx xx Xxxxxxxx lékové xxxxxxxx, xxx xxxxxxx xxxxxxx x xxxxxxxxxxx xx xxxxxxxxx.
Xxxxxxxx xxxxxx xxxxxxx
Xxxx xxxxxx xxxxxxxxx xxxx xxxxxxx xxxxxxxxxx x xxxxxxxxx xxxxxxxxxxxx činnosti xxxxxxxx xxxxxx tak, xxx xxxx xxxxx xxxxxxxx xxxxxxxx hodnocení xx xxxxx XX.
Xxxxx xxxxxxxx xxxx zamítnuta x xxxxxxxxxxxxx xxxxxx: xxxxxxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxx (při xxxxx xxxxxx členskému xxxxx, xxxxx bude poukázána xxxx xxxxxxxxx xxxxx xx Státní ústav xxx kontrolu léčiv, xx nejevilo xxxx xxxxxx ze xxxxxx xxxxx xxxx xxxxxxxxxx xxxxxxxx xxxxxxxxxx na xxxxxxx xxxxxxxxxx xxxxxxxx, xxxxxx komise xx xxxxxxx xxxxxxxxx xxxx xxxxxxxx, protože xx xx xxxx x xxxxxxx s požadavkem xxxxxxxx č. 536/2014 x xxxxx xxxxxx xxx xxxxxxx stát), problémy xxx nespolupráci xx xxxxxx etické xxxxxx x nemožnost si xxxxxxxxxx xxxxxxx; xxxxxx xxx x xxxxx, xxxx etická xxxxxx xx xxxxxx xxxxxx xx xxxxx být xxxxxx xxx xxxx xxxxxxx x xxxxxxx xxxxx. xxxxxxxxxxxx xxxxxxx xxxxxxxx.
Xxxxx xxxxxxxx byla xxxxxxxxx x xxxxxxxxxxxxx xxxxxx: xxxxxxxx xx xxxxxxxxxxx, xx xxxxxxx xxxxxxxxxx xxxxxx xx xxxxxxx xx zdravotnickými xxxxxxxxxx x xxxxxxxxxx xxxxxxxxxx jsou xxxxxxx xxxxxx zdravotnických xxxxxxxx, xxxx i xxxxxxxxxxxx, xxx x tento xxxxx xxxxxxxx.
Xxxxx xxxxxxxx xxxx zamítnuta x xxxxxxxxxxxxx xxxxxx: Xxxxxxxxx xxxx xxxxxxxxxxx byla xxxxx již x xxxxxxxx xxxxxx, ale xxxxx xxxxxx x xxxxx xxxxxxx. Xxxxxxx xxxxx xxxxxx xxxxxxxxxx x xxxx xxxxxxx, xxxxxxxx zajištění by xxxxxx xxxxx x xxxxxxxx xx klinická xxxxxxxxx, kdy Xxxxxx xxxxx pro xxxxxxxx xxxxx xx nemohl xxxxxxxxxx xxxxxxx xxxxxxxxxxxx xxxxxxxxx úřady.
Čtvrtá xxxxxxxx xxxx xxxxxxxxx x xxxxxxxxxxxxx xxxxxx: Xxxxxxx xxxxxx komise jako xxxxxxxxxxx xxxxxx Xxxxxxxxxxxx xxxxxxxxxxxxx nebylo přijato x důvodu požadavku xx xxxx xxxxxxxx xxxxxx x zajištění xxxxxxxxxx xxxxx xxxxxx xxxxxx a činnosti xxxxxx komise.
Jako xxxxxxxxxxxx xxxx proto xxxxxxx xxxx xxxxxxxx x xxxxxxxxxxxxx xxxxxx: Xxxxx xxxxxxx xxxxxx xxxxxx/xxxxxxxx xxxxxx jako xxxxxxxxx xxxxxx Státního ústavu xxx kontrolu xxxxx xxxxxxxxx pozitivně z xxxxxxxxxxxxx xxxxxx - xxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxxxxx xxxxxxxxxxx xxxxxxxxxxx xxxxxxxx etické xxxxxx x vybraných náhrad xxxxxx, xxxxxx tak xxxxxxx xxxxx xxxxxxxxxx xxxxxxxxx xx xxxx xxxxxx pro xxxxxxxxxxxx xxxxxx xxxxxx/xxxxxxxx xxxxxx x xxxxxx xxxxxx. Xxxxxx zajištění xxxxxxxxxx xxxxxxxxxx xxxxxxxx x xxxxxxxx xxxxxxxxxx a xxxxxx xxxxxxxxx xxxxxxxxxx xxxx. Xxxxxxx orgán xxxxxxx xx xxxxxxx Xxxxxxx x Xxxxxxxxx xxxx, které xxxxx xxxxxxxx x xxxxxx Xxxxxxx xxxxxxx xxx xxxxxxxx xxxxx xx xx xxxxxxxxx Xxxxxxxxxxxxx xxxxxxxxxxxxx, xx rozhodovací xxxxxxxxx xxxxxxxxxx xxxxxxxxxx Xxxxxxxx xxxxxx xxx xxxxxxxx xxxxx a xxxxxxx poradního xxxxxx xxx xxxx xxxxxxxxxxx xxxxxxxxxxxx. Xxxxxxxxx nezávislosti xxxxxxxxx x xxxxx xxxxxxxxx orgánů Evropské xxxxxx xxxxxxxx, kterými xxxx xxxx. Xxxxxx xxx xxxxxxx terapii xx.
Xxxx nejvhodnější xxxxxxxxxxx xxxx xx základě xxxx uvedeného zvolena xxxxx etická xxxxxx x xxxxxxxx xxxxxxxxx xxxxxxx jako xxxxxxx xxxxx Xxxxxxxx xxxxxx xxx kontrolu léčiv.
Právní xxxxxx xxxxxxxx xx xxxxxxx xxxx
Xxxxxxxx Evropského xxxxxxxxxx x Xxxx (XX) č. 536/2014 ponechává xxxxxx xxxxxxxxx x xxxxxxxx xxxxxxx xxxxxxx xxxxxxxx xxxxx xxxxxxxxx xxxxxxxxx xxxxxxxxx v xxxxxxxxxxx s xxxxxx xxxxxx xx xxxxxx xx xxxxx xxxxxx xxxxxxxxx státu x xxxxxxxxxx xxxxxx xxxxxxxxx xxxxx a xxxxxxx xxxxx xxxxxxxx xxxx xxxxxxxxx, ručení xxxx xxxxxxx úpravy. X xxxxxxxx době xx xxxxx xxxxxxxxx xxxxxx xxxxx xxxxxxxxxx xxxxxxxxxx x xxxxxxxxxxxx zajištěné xxxxxxxxxxx. Zároveň xxxx xxxxx xxxxxxxxx i xxxxxxxxx nového xxxxxxxxxx xxxxxxxx č. 89/2012 Sb. pro xxxxxxx xxxxx majetkové xxxx, xxxxx je xxxxxxxx x současném xxxxx zákona x. 378/2007 Xx., ale xxxx xxxxxxxxx nemajetkovou xxxx. Xxx xxxxxxxx xxxxxx nového xxxxx xxxxxx xxxx snahou xxxxxxx xxxx xxxxxxxx xxxxxx xxxxxxx škod. Xxx přípravě xxxxxx xxxxxx bylo tedy xxxxxxxxx xxxxxxxxx, jaké x xxxxx připadající xxxxxxx xxxxxxx xxxxxxx xxxxx xxxxxxxx, xxx xxxx xxxxxxx x xxxxxxxxx. Xxxxx xxxx xxxx xxxxxxxxxxxx také xxxxxxxxxxx xx xxxxxxxx xxxxxxxxxx. Xxxxxxxxxx návrhy xxxxxxxxx xxxxxxx škody xxxx xxxxxxx xxxx x původním záměrem xxxx xxxxxxxx více xxxxxxxxxx, xx xxxxxxx xx si xxxx xxxxxxxxx xxxxxx pro xxxx xxxxxxxxxxxxxxxx xx xxxxxxxxxxxxx.
Xxxxxxxx xxxxxxx xxxxxxx xxxxxxx xxxxxxx xxxxx
Xxxxxxxx 1 = xxxxxx xxxxxxx xxxxx xxxxxxxxxxx x zajištění xxxxxxxx xxxxxx
Xxxxxxxxxx xx byli xxxxxxx zajistit xxxxxxx xxxxxxxx vzniklé škody xxxxxx xxxxxxxx xxxxxx.
Xxxxxxxx 2 = xxxxxx xxxxxxx xxxxx spočívající x xxxxxxxx xxxxx xxx náhradu xxxxx
Xxxxxxx xxxxx by byla xxxxxxxxx xxxxxxxxxxxxxxx fondu xxxxxxxxxxxxxxx společností xxx xxxxxxx xxxxx.
Xxxxxxxx 3 = systém náhrady xxxxx xxxxxxxxxxx x xxxxxxxxx komerčního xxxxxxxxx
Xxxx xxxxxxxx xx vycházela xx xxxxxxxxxx stavu. Xxxxxxx xx stanovení xxxxxxx xxxxxxxxxx xxxxxxxxxx xxx po xxxxx xxxx xxxxxxxxx klinického xxxxxxxxx xxxxxxxx xxxxxx xxxxxxxxx xxx, xxxxxxxx xxxxxxxxxxxx x xxxxx xxxxxxxxxxxx, xxxxx xx xxxxx xxxxxx xx xxxx vzniklou subjektům xxxxxxxxx x xxxxxxxx xxxxxx účasti x xxxxxxxxx xxxxxxxxx xxx xxxx xxxxxxxxx.
Xxxxxxx x xxxxxxx xxx jednotlivé xxxxxxx xxxxxxxx
Xxxxxxxx 1
Xxxx xxxxx x řešení xxxx zvažováno zajištění x xxxxxx xxxxxxxx xxxxxx, xxxxx by xxxx být xxxxxxx x nižšími průběžnými xxxxxxx xxx xxxxxxxxxx. Xx xxxxxxxxx xxxxxxx xxxx možnosti však xxx xxxxxx xxxxx, xx xxxxx xxxxxxxx xx xxxxxxxx xxxxxx xx xx xxx xxxxxxx xxxxxxx xxxxxxx xxxx xxxxxxx xxxxxxxx xx xxxxxxxxx pojištění, xxxxxxx xxx vzniku xxxx xx xxxxxxxxxx xxxxxxxxxx hodnocení xxxxxxxxxxx xxxx xxxxxxxx xxxxxxxxxxxxx xxxxxxx. Výhodný xxx xx xxxxx xxxxxxxx xxxx xxx xxxxxxxx xxx xxxxxxxxxx provádějící xxxxxxxx hodnocení x xxxxx xxxxx xxxxxx, xxx x x xxxxxx xxxxxxxxx by xx xxxx poplatků xxxxxxx výši pojistného xxxxx při xxxxxxxxx xxxxxxx škody pojištěním. Xxx xxxxx společnosti, xxxxx by xxxxxx xxxxxxxxx xxxx xxxxxxx xxxxxxx banky, xx xxxxxx xxx xxxxxxx xxxxxxxx xxxx bankovní xxxxxx v xxxxxxxxx, x xxxx peníze xx xxxx po xxxxx xxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxx pro xxxxxxxxxx xxxxxxxxxxxx, xxx xx mohlo být xxxxxxxxx pro činnost xxxxxxxxxx. Toto by xxxxxxx xxx xxxxx xxxxxxxx xxxxxxxxx, xxx xx xxxxx xxxxxx xxxxxxxxx xxxxxxxxx xxxxxxx xxxxx bankovní xxxxxxx. Xxxxx xxxx institut xxxxxxx xxxxx xx xxxxxxx i nové xxxxxxxxxx a činnosti xxx Xxxxxx xxxxx xxx xxxxxxxx léčiv, xxxxx xx xxx xxxxx xxxxxxx, x xxx xx bylo xxxxxxx xxxxxx x xxxxx by xxxx xxxxxxxx xx řešení xxxxxxxxxx xxxxxxxxxx.
Xxxxxxxx 2
Další xxxxxxxxxx xxxxxxxxx vytvoření xxxxxxxxx systému xxxxxxx xxxxx xxxxxxxxx xxxxxxxxx xxxxxxxxx xxxx založení xxxxx xxxxxxxxxxxxxxx xxxxxxxxxxx xxx xxxxxxx xxxxx. Xxxx xxxxxx xxxxxxxxxxxxx xxxxxxxxxxx xxxxxxx xx xxxxxxxxxxx, že xxxxxx xxxxxxxx xxxxxx xxxxx xxxxxxxx xxxx xxxxxxxx. Xxxx xxxxxxxx xxxxxxx xxx xxxxx xxxx xxxxxxxxxxxxxx a xxxx xxxxx xxx xxxx xxxxxxxxx.
Xxxxxxxx 3
Xxxxx zvažovanou xxxxxxxxx je xxxxxxxxx xxxxxxx xxxxxxxxxx zadavatele xxx xx xxxxx xxxx provádění klinického xxxxxxxxx sjednané xxxxxx xxxxxxxxx své, hlavního xxxxxxxxxxxx a xxxxx xxxxxxxxxxxx, které by xxxxx xxxxxx za xxxx xxxxxxxx xxxxxxxxx xxxxxxxxx x xxxxxxxx xxxxxx xxxxxx x xxxxxxxxx xxxxxxxxx xxx xxxx xxxxxxxxx, xxx. xxxxxxxx platný xxxxxx xxxxxxxxxx. Výhodou tohoto xxxxxxx xx možné xxxxxxxxx xxxxxxxxxx xxxxxxxxxxx x xxx mnohaletá xxxxx, xxx xx xxxxxx xxxxxxxx.
Xxxxxxxx xxxxxx xxxxxxx
Xxxx xxxxxx xxxxxxxxx xxxx xxxxxxx xxxxxxxxxx x zajištění xxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxxxx v xxxxx xxxxxxxxxx xxxxxxxxx dosáhnout xx xxxxxxx újmy.
Varianta 1 xxxx xxxxxxxxx, xxxxxxx xxxxxx žádnou xxxxxx xxxxx xxxxxxxxx xxxxxxxx odškodnění xxxxxx xxxxxxxxx. Xxxxxx náhrady xxxxx xxxxxxxxxxx v xxxxxxxxx xxxxxx xxxxxxxx xxxxxx xx byl xxxxx xxxxxxx pouze xxx xxxxxxxxxxxxxxxx (xxxxxxxxxxxxx) xxxxxxxx xxxxxxxx hodnocení. X xxxxxxx xxxxxxx xxxxxxxxxx zadavatelů (nízkobonitních) xx tato varianta xxxxx xxx x xxxxxxxx vzhledem x xxxxxxxxx xxxxxx xxxxxxx xxxxx. Varianta 2 xxxxxx s xxxxxxx xx xxxxxxxxx xxxxxxxxx xxxxxxxx xxxx rozpracovávána. Xxxx xxxxxxxxxxxx byla xxxxx xxxxxxx varianta 3, xxx tato xxxxxxx xxx ze xxxxxxxxx xxxxxxxxx xxxxx. Xxxx xxxxxxxx založená xx xxxxxxx xxxxxxx xxxxx xxxxxxxxx xxxxxxxxx xxxxxxxxxx xx osvědčená x x xxxxxxxxxxx x xxx xxxxxxxx xxxxxxxxxx xx xxxxxxxxxxxxxxxx.
Xxxxxx xxxxxx xxxxxxxx xx xxxxxxx xxxxx způsobené xxxxxxxxxxxx xxxxxxxxxx
Xxx nekomerční xxxxxxxxxx xx xxxxx xxxxxxx xxxxxxxxxx realizace xxxxxxxxxx xxxxxxxxx xxxxxxx xxxxxxxxxx xxxxxxxxx, xxxxx xxxxxxxx hodnocení xxxxxxxxxxx x xxxxxxxxxx xxxxxx xxxxxxxx xxxxxxx nemohou xx xxxxxxxxxxxx xxxxxxx xxxxxxxx povinné xxxxxxxxx. Xxxx xxxxxxxxx je xxxx xxxxxxxx xxxxxxxxx x xxx jeho xxxxxxxxx xx xxxxx xxxxxxxx xxxxxxxxx provádět. Xxxxxxxxxx zadavatelé pak xxxxxxx xxxxxxxx zdroje x xxxxxxxxx fondů xx x rozpočtu xxxxxxxxxxxxxx xxxxxxxx a x případě, že xxxx peníze xxxxxxxxx, xxxxxxx xxxxxxxx xxxxxxx xxxxxxxxxx.
Xxxxx se xxxxx x xxxxxxxxxx xxxxx xxxxxxxx v xxxxx xxxxxxxxx nastavení xxxxxxx xxxxxxxxxx, xxx v xxxxxxx x požadavkem xxxxxxxx xxxx xxxxxxxxx xxxxxxxx zajištění x xxx. xxxxxxxxxxxx zadavatelů. Xxxx varianty byly xxxxxxxxx xx základě xxxxxxxxxxxxx xxxxxxxxxx skutečností: xxxxxxx vynaložené nekomerčními xxxxxxxxxx xx xxxxxxxx xxxxx xxxxxxxxxxxxxxxxxx akademických xxxxxx se xxxxxxxx xxxx 40 až 100 tisíci korunami xx xxx; v xxxxxxxxxx 10 xxxxxx xxxxx vznesen žádný xxxxxxxxx xx odškodnění x xxxxxxxxxxxx xxxxxxxxxx xxxxxxxxx; xxxxxxxxx jako xxxxxxxxxx xxxxxxxxxx xxxxx xxxxxxxxx klinické xxxxxxxxx x xxxxx xxxxxxxxxx xxxxxxxx, na které xxxxxxxxx xxxxxx xxxxxxxxx xxxxxxxx podporu, přičemž xxx xxxxxx ekonomických xxxxxxx grantového projektu xxxxx zahrnout xxxxxxxxx. X takovém xxxxxxx xx xxxxxxx grantu xxxxxxx, kde xxxxxx xxxxxxxx xxxxxx xxx xxxxxxxxx xxxxxxxxx, xxxxx xx xxxxxxxx jako xxxxx z podmínek xxxxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxx č. 378/2007 Sb., ve xxxxx xxxxxxxxxx předpisů. Xxx xxxxxxx alternativních xxxxxx xxxxxx xxxx xxxx xxxxx xxxxxxxxx xxx xxxxxxxx xxxxxxxxx xxxxxxxxxxxx xxxxxxxxxx a xxxxxxxx xxxxxxxxx xxxxxxxxxxxxxx xx xxxxx XX x xxxxxxxxxxx v xxxxxxx x běžnou xxxxx, xxx. xxxxx xxxxxxx údajů x xxxxxxxxx xxxx dle xxxxx schváleného xxx xxxxx použití (xxxx. xxx pediatrické xxxxxxxx) xxxxxx možnost zajištění xxxxxxxxxx odškodnění státem xxxxxxxxxxxxxxx Xxxxxxxxxxxx xxxxxxxxxxxxx.
Xxxxxxxx xxxxxxx ohledně xxxxxxx xxxxx xxxxxxxxx xxxxxxxxxxxx xxxxxxxxxx
Xxxxxxxx 1 = xxxxxxx xxxxx xxxxxxxxx xxxxxx xxx xxxxxxxxxx xxxxxxxxxx
Xxxx xx xxxxxx x xxxxxxx způsobené xxxxx xxxxxxxx klinického xxxxxxxxx tuto xxxxx xxxxx x prostředků xxxxxxxxxxx k tomuto xxxxx x xxxxxxxx Xxxxxxxxxxxx xxxxxxxxxxxxx.
Xxxxxxxx 2 = xxxxxxxxx xxxxx xxx nekomerční subjekty x Xxxxxxxxxxxx xxxxxxxxxxxxx
Xxxx xxxxxxxx xx xxxx xxxxxx obdobou zvažované xxxxxxxx xxxxxxx fondu x ostatních xxx xxxxxxxxxx xxxxxxxxxx.
Xxxxxxxx 3 = xxxxxxx xxxxxxxx xxxxxxxxx prostřednictvím xxxxxxxxx xxxxxxxxxxxxx xxxxxxxxxxx služeb, xxxxx jeho xxxxxxxxx xxxxxxxx xxxxxxx použití xxxxxxxxxxxxxx léčivých xxxxxxxxx x xxxxx xxxxxxxxxx xxxxxxxxx.
Xxxxxxx a přínosy xxx xxxxxxxxxx xxxxxxx xxxxxxxx
Xxxxxxxx 1
Xxxxxxxx této xxxxxxxx xx xxxx xxxxxxx akademického výzkumu xxxxxxxx s xxxxxxx xxxxxxxxxx xxxxxxxxxxxx xx xxxxxxxxx xx situace, xxx xxx dostupných xxx xxxxx x xxxxxxxxxx xxxxxx zaznamenán xxxxxx, xxx xx xxxxxxx xxxxxx hodnocení xxxxx o xxxxxxxxxx. Xxxxxxx xx byly xxxxxxx s xxxxxxxx xxxxxx xxxx xxxxx x rozpočtu Xxxxxxxxxxxx xxxxxxxxxxxxx.
Xxxxxxxx 2
Xxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxxx národního xxxxxxx náhrady xxxxx xxxxxxxxx subjektům xxxxxxxxx xxxx xxxxxxxx xxxxx xxx xxxxxxxxxx xxxxxxxx x Ministerstva zdravotnictví. X xxxxxxx případě xx xxxxx měl xxxxx jiného upravovat xxxxxx xxxxxxxxxxx xxxxx, xxxxxx xxxxxxxxxx xxxxxxxxxx, xxxxxx odměňování zaměstnanců xxxxx a x xxxxxxxxxx xxxx také xx, x xxxxxx xxxxxx, v xxxx xxxx x x xxxxxx intervalech by xxx xxxx naplňován. X úvahu xxxxxxxxxx xxxxxx xxxxxxxxx xxxxxx xx xxxxxx xxxxxxxxxxxx, xxxxx by byly xxxxxxxxxx xxxxxxxxx xxxxxx xxxxxx vybrané xx xxxxxxx xxxxxx xx xxxxxxxxx xxxxxxxxxx xxxxxxxxx. Xxxxxxxx x xxxxxx xxxxxxx xxxxxxxx xx xxxxxx fondu x xxxx činnost xxxx xxxx řešení xxxxxxxxxxx xxxx xxxxxxxxxxx x xxxxxxxxx.
Xxxxxxxx 3
Xxxxx xxxxxxxxx xx xxx xxxxxxxxxx xxxxxxxxxx možnost zajistit xxxxxxxxx xxxxxxxxxxxxxxx xxxxxxxxx xxxxxxxxxxxxx zdravotních xxxxxx, xxxxx xxxxxxxxx činnosti xxxxxxx xxxxxxx xxxxxxxx xxxxxxxxx v xxxxx xxxxxxxxxx hodnocení. Xxxxxx xxx xxxxxxxx x xxxxxxxxx xxxxxxxxx.
Xxxxxxxx xxxxxx xxxxxxx
Xxxx hlavní xxxxxxxxx xxxx zvoleno zohlednění xxxxx xxxxxxxxxxxx xxxxxxxxxx xxxxxxxxxx.
Xxxx zavrhnuty xxxxxxxx 1 x 2 Xxxx řešení xx xxxxx xxxxx znamenat xxxxxxxxxxxx xxxxxxxxxx zadavatelů. Xxxxx xx xxx xxxxxxxx znamenaly vznik xxxx agendy ministerstva. X xxxxxxx xx xxxx uvedené, byla xxxxxxx xxxxxxxx 3, xxxxx xxxxxxxxx xxxx xxxxx xxxxxx náhrady xxxxx xxx xxxxxxxxxx xxxxxxxxxx u xxxxxxxxxxxxxxxxxx xxxxxxxxxx hodnocení zajištění xxxxxxxxxx xxxxxxxx x xxxxx pojištění xxxxxxxx xxx xxxxxxxxxxxxx zdravotních xxxxxx, x event. xxxxxxxxx xxxxxxxxxx xxx xxxxxx xxxxxxxxxxxx, x xxxxxxx případě xx xxxxx připojištění xxxxxx xxxxxxxxxx.
2.2. Xxxxxxxx xxxxxxxxx x xxxxxxx xxxxxxxxx xxxxxxxx přípravků
Článek 36 Xxxxxxx x fungování Xxxxxxxx xxxx xxxxxxx xxxxxx, xxx xxxxx xxxxx xxxxxxx xxxxx xxxxxxxx vnitrostátní opatření, xxxxx brání přeshraničnímu xxxxxxx. Jedním x xxxxxx xxxxxx je xxxxxxx zdraví x xxxxxx xxxx. Stejně xxx xxxxxxxx xx xxxxxxx čl. 81 směrnice 2001/83/XX xx xxxx xxx xxxxxxxxxx xx xxxxxxx ochrany xxxxxxxxx xxxxxx.
Xx xxxxxx xxxxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx xxx potřeby xxxxxxxx x Xxxxx xxxxxxxxx x xxxxxx xxxxxxx xxxxxxxxx xxxxxx xxx xx xxxxx xxxxxxxx xxxxxxxx, která xx xxxxxxxxx xxxxxxxxx xxxxx.
Xxxxxxxxxxx xxxxxx xxxxxxx xx xxxxxxxxxx xx právní xxxxx xxxxxxxxx xxxxxxxx x xxxxx se x xxxxxxxx xxxxxx xxxxxxxxxxx xxxxxxxxxx.
Xxx xxxxxxxxx xxxxxxxx xxxxxxxxxx xxxxxx xxxxxx byla xxxxxxxxx xxxxxxx následující xxxxxxxx (xxxxx xxxxx xxx xxx xxxxxxxxxx xx xxxxxxxx) xxxxxx úpravy:
- xxxxxxxxxxx;
- transparentnost;
- xxxxxxxx;
- xxxxxxxxxxxx;
- xxxxxxxxxxxx;
- xxxxxxxxxx xxxxxxxx;
- pružnost;
- xxxxxxxxxx.
Xx xxxxxxxxxxx - právní xxxxxx xxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx nastavuje xxxxxx, xxxxx účelem xx omezení vývozu xxxxxxxx přípravků podstatných xxx xxxxxxxxxxx xxxxxxxxx xxxx x Xxxxx xxxxxxxxx x xxxxxxx, xx na xxxx x České xxxxxxxxx xxxx xxxxxx xxxxxx xxxxxxxxxx xxx xxxxxxx xxxxxxxx x xxxx xxx xxxxxxxx kvalitní xxxx x ochrana xxxxxx a xxxxxx xxxx. Xxxxxxxxxxx xxxxxx xxxxxx spočívá ve xxxxxxxxx xxxxxxxxxx xxx xxxxxxxxxxxx xxxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx xxx xxxxxxx xxxxxxxx x Xxxxx xxxxxxxxx (úprava xxxxx x stanovení xxxxxxxx x xxxxxxx xxx xxxxxxxxxxxxx dat), xxxx xx xxxxxxxxx xxxxxxxxxxx opatření v xxxxxxxxx xxxxxxxxx xxxxxx xxxxxxxxxxxxx léčivých xxxxxxxxx xxx xxxxxxx xxxxxxxx x Xxxxx xxxxxxxxx x konečně ve xxxxxxxxx xxxxxxxxxxx xxxxxx xx porušení přijatých xxxxxxxx. Xxxxxx xxxxxx xxxxxx xxx xx xxxxxx do xxxxxxxxx xxxxx Xxxxxxxx xxxx, xxx do třetích xxxx.
Xx transparentnost - xxxxxxxx xxxxxx xx xxxxxxx xxx, xxx xxxx xxxxxxx subjekty x xx největší xxxxx míře schopny xxxxxxxxx xxxxxxx xxxxxxx xxxxxxxx x xxxxxxx xxxx xxxxxxx na xxxx xxxxxxxxxx xxxxxxxx. Xxxxxxxxxxxxx postup xx xxxxxxxx xxx v xxxxxxx identifikace x xxxxxxxxxx xxxxxx nedostupnosti xxxxxxxx xxxxxxxxx pro xxxxxxx pacientů x Xxxxx republice, xxx x xxxxxxx xxxxxxx xxxxxxxxxxx opatření. Xxxxxxx xxxxxxxx xxx xxxx xxxxxxxxxx xxxxxxx xxxxxx xxxxx xxxxxxxx opatřením.
Ad xxxxxxxx - xxx xxxxxxxx xxxxxxxxxxxxxxxx a xxx xxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxxxxx xxxxxxx xx praxe a xxxx xxxxxxx z xxxxxx xxxxxx jistoty xxxxxxxx xxxxxxxxxx xxxxxx xxxxxx xx xxxx xx nejpřesnější x xxxxxxxxxxxxxxxxx xx xxxxxx xxxxx xx konkrétnímu xxxxxxxxxx dotčenému léčivému xxxxxxxxx.
Xx odůvodněnost - xxxxxxxx x xxxxxx xxx vyhodnocování nutnosti xxxxxxxx xxxxxxxx za xxxxxx xxxxxxx xxxxxxxxx xxxx xxxx v xxxxxxx xx xxxxxx xx xxxxxxx xxxxxx x života xxxx x x každém xxxxxxxxxx případě xxxxxxx xxxxxx léčivých přípravků xx vyžadováno náležité xxxxxxxxxx opatření.
Ad minimalizace - x xxxxxxx xx xxxxxxx přiměřenosti xxxxxx úpravy xx x xxxxxx xxxxxxx xxxxxxxx xxxxxxxxx x xxxxxxx xxxxxxxx xxx xxxxx Xxxxxxxx xxxx xxxxxxx varianta omezení xxxxxx pouze v xxxxxxxxx, xx xxxxxxx xx xxx xxxxxxxxxxxx xxxxxxx xxxxx xx xxxxxxx zdraví x xxxxxx xxxx. Xx xxxxxxx navrhovaného systému xxxxx dat x xxxxxx xxxxxxxxxxxxx dojde x zajištění předvídatelnosti xxxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx xxx xxxxxxx xxxxxxxx v Xxxxx xxxxxxxxx. Xxxxxxxxxx xxxxxx xxxxxx xxxxxx xxxxxx, xxxxx x xxxxxxxx xxxxxxxx xxxxxxxx xxxxx xxxxxxxx xxxx trhu x nejedná xx xxx x xxxxxx xxxx dlouhodobé xxxxxxx. Xxxx xxxx xxxxx xxxxxxxxxxx rozpor xx xxxxxxx xxxxxxx pohybu xxxxx. Regulace xx xxxxxxxx xxxxx xx xx xxxxxxx, kdy xxxxxxxx hrozí xxxxxxxxxxxx xxxxxxxxxxx xxxxxxxx přípravků, xxxxxxxxxxxx velmi xxxxxxxxxx xxx potřeby xxxxxxxxx xxxx u xxxxxxxx x České republice. Xxxxx xxxxx xxxxxxxx xx dále xxxxxxxx xxxxxxxxx xxx, xx xx jeho xxxxxxx xxxxxxx xxxxx na xxxxxx xxxxxxxxx, xxxxx xxxx xxxxxxxxxxxx nenahraditelné. Xxxxxxxxx xxxxxx tak xxxxxxxxx xxxxxxxxxxx xxxxxxx xxxxxxxxxxx xxxxxxxx, x xx xxxxxxx xxx xxxxxxx xxxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx xxx xxxxxxx xxxxxxxx x Xxxxx republice.
Ad xxxxxxxxxx xxxxxxxx - xxxxxx xx navržen xx xxxxxxxx, která využívá xxx xxxxxxxx xxxxxxxxxx xxxxxxx xxxxxxx x xxxxxxxxxxxx a xxxxxxx xxxxxxxxxxx k xxxxxx xxxxxxxxxx a analýze, x xxx xxxxxxxxxxx xxxxxxxx dotčené regulované xxxxxxxx xxx xxxxxx xxxxxxx xxxxxx. Xxxx xxxxxxx varianta xxxxxxxxxxxx x xxxxxxxxxxx xxxxxxx.
Xx xxxxxxxx - za xxxxxx zajištění možnosti xxxxxx xxxxxx xx xxxxxxxxx xxxxxxx xxxxx xxxxxx xxxxxx xx xxxxxxxxxxx xxxxxxxx xxxxxxx xxxxxxxxxx xxxxxxx xxxxxxxxx (xxxx. intervaly xxxxxxxxxxx xxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxx nedostupností, xxxxxxxxx xxxxxxxx, xxxxxxxx xxxxxxxx x xxxxxxx xxxxxxxxxxxxx xxxxx v hlášeních).
Ad xxxxxxxxxx - xx xxxxxx xxxxxxxxxxxxxx navrhovaných xxxxxxxx xxxx xxxxxxxxx xxxxxxxxxxxx xxxxxx x xxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxx. Tyto xxxxxx xxxxxxxx xxxxxx xxxx, xxx u xxxx xxx dostatečně naplněn xxxxxxxxxxx xxxxx.
Xxxxxxxxxxx xxxxxxx xx xxxxxx hrozba xxxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx pro xxxxxxx xxxxxxxx v Xxxxx xxxxxxxxx. Pokud se xxxxx x xxxxxxx xxxxxxxxxxx x xxxxxx xx xxxxxx xxxxxxxx xxxxxxxxxx o xxxxxxxxxx, xxxx mají x xxxxxxxxxx §33 xxxx. 2 zákona o xxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxx xxxxxx xxxxxxxxx xxxx ukončení xxxxxxx xx xxxxx xxx xxxxxxx 2 měsíce xxxxxx.
Xxxxxxxxxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx x xxxxxxxxx xxxxx xx aktuální xxxxxxx v Xxxxx xxxxxxxxx, xxx xxx xxxxxx EU. Xxxxx xxxxxxxxx léčiv xx xxxxxxxx xxxxxxx x x xxxxxxx xxxxxxxx xxxxxxxxxxx se xxxxx xxxxxxxxxx obchodní xxxxxxx. Xxxxxxxxxxx xxxxxxxx xxxxxxxxx xx x xxxxxxxx xxxxxxxxxx xxxxxxxxxxxx zásobování xxxxxxxxxxxx xxxx uložených xxxxxxxxx xxxxxxxxxx x xxxxxxxxxx xxxx xx xxxxxxxxxxx xxxxxxxxxxx služeb x Xxxxxx. X xxxxxxxx xxxxxxxx xxxx xxxxx k xxxxxxx xxxxxxxxxx prostředků vynakládaných xxxxxxx na výzkum x xxxxx nových xxxxxxxx xxxxxxxxx xxxx x zavádění xxxxxxxxxxxx xxxxx xx xxxx x xxxxxxx xxxxxx xxxxxxxx xxxxxxxxx xx xxxxxxxxx. Xxxxxxx xx, xx xxxxxxxx xxxxxxx xxx s xxxxxxxx xxxxxxxxx xx svá xxxxxxxxx xx xxxxxx xxxx ovlivněná xxxxxxxx xxxxxxxxxxx cen xxxxxxxx xxxxxxxxx a xxxx xxxxx x veřejných xxxxxxxxxx x xxxxxxxxxxxx xxxxxx. Je xxxxxxx, xxx x nadále xx xxxxxxxx xxx x xxxxxx xx xxxxxxxxx pacientů a xxxxxxxxxxx xxxxxxx xxxxxxxxxxxx xxxxx x xxx xxxxxxxx x xxxxxxxx xxxxxxxx xxxxxxxxxx xxxx x xxxxxxx xxxxxxxx xxxxxxxxx tento xxx xxxxx netříští.
Současně s xxxxxx reexportů xxxxxxx xxx xxxxx hlášených xxxxxxx xxxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx v xxxxxxxxxxxx xxxxxxx EU. Xxxx xx xxxxx xxxxxxx objevuje xxxxxxx x nedostupností xxxxxxxxxxx xxxxxxxx xxxxxxxxx ve xxxx xxxxxx EU xxxxxxxx, což vede x xxxxx silnějšímu xxxxx na xxxxx xxxxxxxx xxxxxxxxx xx xxxx x xxxxxxxxxxx xxxxxxx xxxxxxxx. X xxxxxxx xxxxxxxx nedostupnosti xxxxxxxx xxxxxxxxx se xxxxx xxxx xxxxx xxxxxx xxxxxxxx x xxxx xxxxxxxxxxx xxxxx. Xxxxx v xxxxxxxxx, xxx hrozí xxxxxx xxxxxxxxxxxx xxxxxxxx xxxxxxxxx xxx xxxxxxx xxxxxxxx x Xxxxx xxxxxxxxx (xxxxx se xxx xxxxx xxxxxx xxxxxxxxx, xxx xxxxxxxxxxxx vydalo xxx. xxxxx xxxxxxxxx xxxxxxxxx xxxxxxx léčivých xxxxxxxxx Xxxxxxx, Actilyse x XxxxxxxXxxxxxx), je xx účelem xxxxxxxx xxxxxxxx funkce xxxxx xxxxxxxxxxxx xxxxxxx zdraví x xxxxxx xxxx xxxxxxxx xxxxx přijmout xxxxxxxxx xxxxxxxx x xxxxxxx xxx s xxxxxxxxx xxxxxxxx xxxxxxxx, xxx xx závazky xxxxxxxxxxxxx z mezinárodního xxxxx.
Xxxxxxx xxxxxxx xxxxxx xxxx řešitelný xxxxxx xxxxxx a xxxxxxxxx xxxxxx x xxxxxxxx xxxxxxxx léčivých přípravků xxxxxxxxx x toho xxxxxx, že xx xx xx xxxx xxxxxxxx xxxxxxxx, u xxxxxxxx xxxxxxxxx, xxxxxx xxxx x dalších xxxxxxx, bývá xxx xxxxxxxxxx xxxxxxxx xxxxxxxxxx xxxxxxx xxx xxxxxxxxxxx xxxxxxx xx trh xx xxxxxxxxxxxx ekonomikách xxx x ekonomikách xxxx xxxxxxxxx. Xx xx xxxx xxxxxxx xxxxx xxxxx xxxxx xxxxxxxxxxxx x xxxxxx xxxxxxxxxx vyspělejších xxxxxx, xxx xx stejnou xxx xxxx xxxx xxxxxxxxx xxxxxxxxx xxxxxxx x také schopni xxxxx xxxxx xxxxx xxxxxxxxxx xxxxxxxxxx, a x této xxxxxxxxxxx xxx xxxxxxxxx xxxxxxx x xxxxxxx xxxxx xxxxxxxxxxxxxxxx xxxxxxxx, xxxxxx xxxxxxxx regulátorů, lékáren, xxxxxxxxxxxx x xxxxxxxxxxx xxxxxxxxxx. Xxxx prostředky xxxxxx a xxxxxxxx xxxxxxxx xxx x xxxxxx xxxx nemohou xxx xxxxx vliv xx xxxxxxxx x xxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxx z důvodu xxxxx x jakosti, xx kterým xxx x xxxxxxxxx rovněž xxxxx x xxxxx xxxx nutno xxxxx. Xxxxx xxxxxxxxxx cenové x úhradové xxxxxxxx xxxxx mít efekt xx x xxxxxxxxxxxxxx xxxxxxx horizontu, zatímco xxxxxxx xxxxxxxxxxxxxx xxxxxxxxx xxxxxxxxxx potřeb xxxxxxxx x České republice xxxxxxxxx xxxxxxx xxxxxxxxxx xxxx xxxxxx xxxxxx xxxxxx x xx xxxxx jej xxxxx xxxxxxxxxx. X xxxxxxxxx xx však xxxxx xxxxxxxxxx, xx xxxxxxxxxxxxx xxxxxxx xxxxxxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx pro xxxxxxxx v Xxxxx xxxxxxxxx je komplexní x xxxxxx xx x xxxx xxxxx xxxxxxx xxxxxxxx xxxxxx x xxxxxxxx xxxxxxxx xxxxxx léčivého xxxxxxxxx.
Xxxxxxxxxxxxx xxxxxxxxxxxxx xxxxxxx je xxxxxxxx právní xxxxxx xxxxxxx reexportů léčiv xx zákona x xxxxxxxx, který xxxxxxxxx xxxxxxxx xxxxxxxxxxxx xxxxx x xxx xxxxxxxxxxxx xxxxxxxxx xxxxxx dostupnosti. Xxxxxxxxxx x xxxxxxxxxxx xxxx zacházejících x xxxxxx x xxxxxxxxxxx xxxxxxxxx xxxxxx xxxxxx xx xxx xxxxxxxxx xxxxxxxxx xxxxxxxxxxx léčivých xxxxxxxxx pacientům v Xxxxx xxxxxxxxx xxxx x xxxxxx x xxxxxxxx xxx xxxxxxxx xxxxxxxx, praktické xxxxxxxxxx x aplikace stávající xxxxxx xxxxxx x xxxx nedostatečné xxxxxxxxxxxxxx xxxx xxxx odůvodňují xxxxxxx jejího xxxxxxxxx x doplnění.
Stávající úprava x ohledem xx xxxxxxxxx xxx xx xxxxxxxxxxxx xxxxxxxxx x xxxx důvodu, xx xxxxxxxxx xxxxxx xxxxxxxxxxxxxxxx xxxxxxx pro distributory xxxxxxxx xxxxxxxxx a xxx provozovatele xxxxxxxxx xxxxxxx léčivé xxxxxxxxx. Xxxxxxxxx xxxxxxxxxx §11 xxxx. x) zákona xxxx xxxxxxxxxxx určitý xxxxxxx x řešení xxxxxxx, xxx&xxxx; xxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx xx xxxxxxxxx xxxxxx xxxxxxx xxxxxx xxxxxxxxx xxxxxxx xxxxx xxxxxxx xxxxxxxx xxxxxx xxxxxxxx x Xxxxx xxxxxxxxx, x xxxxxx xxxxxx xxxxxxxx xxxx v xxxxxxxxxxx xxxxxxxxx x xxxxxx xxxxxxxxxx xxxxxx xxxxxxxx xxx xxxxxxx, xxxxx xxxxx o xxxxxxx, který xx xxx xxxxxxx vskutku xxxxxxxxx x xx xxxxxxxxxxx xxxxx xxxxxxxxxx xxxxxxx a respektováním xxxxxxxx jistot a xxxxxxxxx očekávání xxxxx xxxxxxxxxxxxxxxx xxxxxxxx.
X xxxxxxxxx xxxxxxxxxxx léčivých přípravků xxx pacienty x Xxxxx xxxxxxxxx je xxxxxxxx přijmout xxxxxx xxxxxxx xxxxxxxx xxxxxxxxxxx xxxxx x opatření, xxxxx xx xxxx xxxxxxx xxxxxxx xxxxx, xxxxx je xxxxxx, xxxxxxxx a přiměřený x xxxxxxx na xxxxxxxxx xxx, xxxxxx xx zajištění dostupnosti xxxxxxxx přípravků xxx xxxxxxxx x Xxxxx xxxxxxxxx.
Xxxxxxxxxx xxxxx xxxxxxx x xxxxxxxx ze xxx vzájemně provázaných xxxxx x opatření. Xxxxxx z nich xx vytvoření seznamu xxxxxxxx přípravků xxxxxxxxxx xxxxxx xxxxxxxxxxxxx. K xxxxxxxxx xxxxxx seznamu xxxxx xxxxxxx databáze x distribuci, xxxxxx x spotřebě xxxxxxxx xxxxxxxxx. Xxxxxxxxx x xxxxxxxxxx tohoto xxxxxxx xxxx probíhat formou xxxxxx opatření xxxxxx xxxxxx Xxxxxxxxxxxxx xxxxxxxxxxxxx, xxxx xxxx zajištěno, xx xxxxxxx xx xxxx xxxxxxxxxxxxxx xxxxx xxxxx xxxx xxxxxx xxx oprávnění xxxxxxxxx xxxxxxxx řádem. Xxxxxxxxxx xxxxxx xxxxxxx xxxx xxxxxxxx xx xxxxxxxxxx xxxxxx xxxxx zainteresovaných xxxx xxxx xxxxxxx xxxxxxxxxx xxxxxxxxx xx xxxxx seznamu, xxxxxx xxxx, že by xxxxxx distributoři měli xxxxxxx x tím, xx se xxxx xxxx, xx xxxxxxxxxx xxxxxxxxx x xxxxxx xxxxxxxxx do zahraničí xxxx být výhledově xxxxxxx xxxx xxxxxxxx. X ohledem xx xxxx xxxxxxx xxxx xxxxx xxxxxxxxxxx xxxxxxx xxxxx xxxxxxxxxx těchto xxxxxxxx přípravků xx xxxxxxxxx xx jejich xxxxxxx xxxxxxxxxx. Xxx xx totiž xxx xx xxxxxx, xx xxxx xxxxxxxx xxxxxxxxxx xx zajistit xxx xxxxxxx xxxxxx xxxxxxxxx, xxxxxxx xx distributorem, xxxxxxx xxxxxxxxxxxxxx xxxxxxxxxx xxxxxxx léčivé xxxxxxxxx x xxxxxxxx a xxxxxxxx xxxxxxxxxxx odpovídajících xxxxxxx pacientů v Xxxxx republice. Xxxxxx x těchto kroků x xxxxxxxx xx xxx xxxxxxx xxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxx xxxxxxxxxxxx xxxxxxx Xxxxxx Xxxxxxxxxxxx zdravotnictví x xxxx, aby xxxxxx xxxxxxxx xxxxxx xxxxxx, xxxxxx xx xxxxxxx xx zakázalo xxxxxxxxxx xxxxxxxx xxxxxxxxx xx xxxxxxxxx, xxxxxxx xxxxx xxxxxx xxxx, xxx x xxxxxx Xxxxxxxxxxxx xxxxxxxxxxxxx vyslyšet. Xxxxxx, x to xxx xxxxxxxxxxx xxxxxx a xxxxxxxxx xx xxxxxx xxxxxxxx xxxxxx xxxxxx, xxxxxx xxx xxxxxxx xxxxxxx stanovených xxxxxxxx Xxxxxxxxxxxx zdravotnictví xxxxx xxxx xxxxxx distribuci xxxxxxxxxxx xxxxxxxx xxxxxxxxx xx zahraničí. Při xxxxxxxx xxxxxxxx opatření xxxx opět xxxxxxxxx, xx xxxxxxx xxxxx xxxxx moci xxxxxx xxx oprávnění xxxxxxxxx xxxxxxxx xxxxx.
Xxxxxxxxxx xxxxx xx tedy xxxxxx, xxxxxxxx x xxxxxxxxx x xxxxxxx xx xxxxxxxxx xxx, xxxxxxx x xxxx xxxxx xx zachovávají xxxxxxxxx xxxxxxxxxxxxxxxx xxxx se x xxxxxxxxxxx opatřením xxxxxxxx x xxxxxxxx x nim xxxxxxxxxx x xxxxxxx je xxxxxxxxx, xx přijatá xxxxxxxx xxxxxxx xxx xx xxxxx x xxxxxxxxxx. Sledovaný xxx xx přitom xxxxxxxxx xxxxxxxx xxxxxxxxxx, xxxxx xxxx x xxxxxxxxxxxxx xxxxxxxxxx maximálně xxxxxx x xxxxxxxx xxxxxxxxx x omezení xxxx xxxxxx xxxxxxxxxx jen x xxx xxxxxxxx xxxxxxxxx xxxxxxx, kdy xxxx v xxxxx xxxxxxxxxxx xxxxxxxx xxx xxxxxxx xxx účinná x postrádala xx xxx smysl. Xxx xxxx xxxxxx, xx xxxxxxxxxx xxxxxx, xxxxx xx zejména opírá x nově vkládaná xxxxxxxxxx §77c a §77d xx zákona, xxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx xxx xxxxxxxx x Xxxxx xxxxxxxxx xxxxxxxxxxxxx způsobem x xxxxxx bude xxxxxxxxxxxxx x xxx xxxxxxx xxxxxxxxxxxx.
Xxxxxxxx xxxxxxx xxxxxx xxxxxx nedostupnosti xxxxxxxx xxxxxxxxx z xxxxxx xxxxxxxxx
Xxxxxxxx 1 = xxxxxx
Xxxxxxx xxxxxxxxx xx xxxxxx nepředložení xxxxxx xxxxxx xxxxxx o xxxxxxxx řešícího omezení xxxxxxxxx xxxxxxxx přípravků.
Varianta 2 = xxxxx xxxxxxxxxxxx xxxxxx (xxxxxx x xxxxxxxx)
Xxxxxxxx xxxxxxxxxxx xxxxxxxxxxx xxxxxxxx.
Xxxxxxx a xxxxxxx xxx xxxxxxxxxx xxxxxxx xxxxxxxx
Xxxxxxxx 1
Xxxxxxxxxxxx xxxxxx xxxx xxxxxxxx xxxxxxxxx současného xxxxx, xxx se xxxxxxxxx xxxxxxx, xx xx xx xxxx xxxxxxxxxx xxxxxxxx xxxxxx xxxxxxxxx x xx xxx xxxxxxxx zdraví xxxxxxxx x ČR. S xxxxxxxxx xxxxxx xxxx xxxxxxxx x xxxxxxx xxxxxxxxx náklady, xxxxx xx xxxxx xxxxxx xxxxx xxxxxxxxx, xxxxx xx xx trhu xxxx dostupné potřebné xxxxxx xxxxxxxxx (xxxxx xxxxxxxxx xxxxxxxxxx xxx.). Xxxxxxxx xxxx plné xxxxxxxx xxxxxxx xxxxxx xxxxx, ovšem na xxxx zdraví xxxxxxxx x XX.
Xxxxxxxx 2
Xxxxxxxxxxx xxxxxxxxxxx opatřeními xx xxxx možné xxxxxxxxx x x xxxxxxxx xxxxxxxx xxxxxx takový xxxxxx, xxxxx xx xxxxxxxxx xxxxx xx xxxxxxx zdraví xxxxxxxx xx xxxxxx podnikatelských xxxxxxxx xx xxxxxxxxxxx xxxxxx xxxxxxxxxxxxxxx příležitostí. Xxxx xxxxxxxxxx xxxxx xx xxxx xxxxxxxxx xxxx x souladu x xxxxxx XX, xxxxx xxxxxxxx omezit xxxxx xxxxx xxxxx xx účelem xxxxxxx xxxxxxxxx xxxxxx.
Xxxxxxxx xxxxxx xxxxxxx
Xxxx xxxxxx kritérium xxxx xxxxxxx xxxxxxxxx xxxxxxx xxxxxxxxx zdraví x xxxxxxx x xxxxxx XX.
Xxxxxxxx 1 xxxx xxxxxxxxx s xxxxxxx na xxxxxx xxxxxxx xxxxx xxxxx xxxxxxx (xxxxxxxxxxx xx xxxxxxx xxxxxxxxxxxxx léčivých xxxxxxxxx z xxxxxx xxxxxx reexportů). Xxxxxxxxx xxxxxxxxxxx jej xxxxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxx. Xxx xxxxxxxxx xxxxxxxx xxxxxx xxxxxx v xxxxxx x léčivech xx x České xxxxxxxxx nemohlo xxxxx x xxxxxxx současného xxxxx, xxx xxxxx xxx xxxxxxx xxxxxxxx xxxxxx xxxxxxxxx xxx xxxxxxxx v Xxxxx xxxxxxxxx xxxxxxxx xxxxxxxxxx x xxxx xxx x potřebném rozsahu xxxxxxxxx ochrana xxxxxx xxxxxx x xxxxxx, xxxxxxx xxxxxx státní xxxxxx xxxxxxx z xxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxxx a xxxxxxxxxx xxxxxx xxxxxxxx, xxxxx xx x xxxxxxxxxxx xxxxxxxxxx mohla zabránit xxxxxx takové xxxxxxx. Xxxx tak xxxxxxx xxxxxxxx xxxxx 2, xxxxx znamená xxxxxxx xxxxxx právní úpravy xxxxxxxxxx xxxxxxxxxx xxxxxxx.
Xxxxxx xxxxxxxxxxxx xxxxxx akutní xxxxxxxxxxxxx a xxxxxxxxx xxxxxxxxxxx xxxxxxxx přípravků
V xxxxx xxxxxxxxx xxxxxxx xxxxxxxx xxxx xxxxxxxxxx xxx x xxxxx xxxxxxxxxxxx xxxxxxxxx xxxxx, xxxxx xxxxxxxx xxxxxxxx xxxxxxx různé xxxxx xxxxxx xxxxxxxx xxxxxxx xxxxxxxxx xx xxxxxxx č. 81 xxxx. 2 Xxxxxxxx x. 2001/83 (xxxx. Bulharsko, Xxxxxxxx, Xxxxxxxxx x xxxxx) x xxx xxxxxx xxxxxxxxxx xxxx zvoleny xxxxxxxxxx xxxxxxxx xxxxxx.
Xxxxxxxx xxxxxxx systému
Varianta 1= xxxxxx xxxxxxxx (xxxxxxxxx xxxx)
Xxxxxxxx 2 = xxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxx na xxx xxxxxxxxx xxxxxxxxxx x xxxxxxxxxx
Xxxxxxxx 3 = xxxxxxxx xxxxxx xxxxxxxxxx xxxxxxxxxxxx xxxxxxx všech xxxxxx
Xxxxxxxx 4 = xxxxxxxx xxxxxxxxxx xxxxxxxxxxxx xxxxxxx pouze xxxxxxxxx xxxxxx
Xxxxxxxx 5 = xxxxxxx souhlasu distributora xx xxxxxxxx rozhodnutí x xxxxxxxxxx
Xxxxxxx x xxxxxxx xxx jednotlivé xxxxxxx xxxxxxxx
Xxxxxxxx 1
Nepředložení xxxxxx bude znamenat xxxxxxxxx xxxxxxxxxx xxxxx, xxx se xxxxxxxxx xxxxxxx, xx xx xx xxxx nedostupný xxxxxxxx xxxxxx přípravek x je tak xxxxxxxx xxxxxx xxxxxxxx x XX. S xxxxxxxxx xxxxxx xxxx xxxxxxxx x xxxxxxx xxxxxxxxx náklady, xxxxx xx xxxxx xxxxxx xxxxx xxxxxxxxx, pokud xx xx xxxx xxxx dostupné potřebné xxxxxx xxxxxxxxx (xxxxx xxxxxxxxx xxxxxxxxxx atp.). Xxxxxxxx xxxx xxxx xxxxxxxx volného pohybu xxxxx, xxxxx xx xxxx xxxxxx xxxxxxxx x XX.
Xxxxxxxx 2
Xxxxxxxxxxxxx xxx x xxxxxxxx xxxxxxxx přípravků xx xxxxxxxxxx xxxx k xxxxxxxxx xxxxxxxxx xxxxx xx xx své xxxxxx xxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxxxxx vztahů, xxx xxxxx xx xxxxx xx podílí xxxxxxx xxxxxxxx (výroba, xxxxxxxxxx, xxxxx x xxxxxxx) x xxxxxxx xxxxxxxxxxxx xxxx své xxxxxxxxxx xxxxx. Xxxxxxxxxxx xxxxxxxxxxxx xxxxxxxx je xxxxxx rozloženo xxxx xxxxxxxxxx xxxxxxxx xxx, xxx xxxx xxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxx xxxxxxx. X ohledem xx vědecký xxxxxx x xxxxxxxx xxxxxxxxx xxxxxx xxxxxxxxxx bádání xx posouvají i xxxxxxx vynakládané na xxxxx jednoho léčivého xxxxxxxxx. Jakýkoliv xxxxx xx farmaceutického xxxx xx úkor xxxxxxx xx xxxxxxx xxxxxxxx xx xxxxxx mohl xxx x konečném xxxxxxxx též xxxxx xx prostředky xxxxxxxxxxx xx xxxxxx xxxxx x xx dostupnost xxxxxxxx xxxxxxxxx na xxxxxxxxxxxx xxxxxx. Xxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxx xxxxxxx xx xxx xx x xxxxxxxx xxxxxxxx xxxxx znamenat xxxxxxxxx systému, xx xxxxxx by xxxx xxxxxxxxxx xxxxxxxxxxxx xxx xxxxx xxxxxx xx xxxx xxxx. Xxxxxxxx xxxxxx xxxxxxxxxx xx xxxxx xxxxxxxx xxxxxxx xxxxxxx, xxxxxxxxxxxx léčivých xxxxxxxxx.
Xxxxxxxx 3
Nevýhodou xx xxxxxxxx xxxxxxxxxxxxxxx xxxxx xx situace, xxx xxxxxxxxxxxx xxxxx veškeré xxxxxx po xxxxxx xxxxxxxxxxx. Xxxxxxxx by xxx xxxxxxxxx ke xxxxxxxx xxxxxxxx xxxxxxxxxx. Xxxxxx xx nebyla xxxxxxxxxxxxxx x xxxxxxx xx xxxxxxxxxx cíl.
Varianta 4
Xxxxxxxx xxxxxxxxx xx xxxx xxxxxxxxxxx xxxxxx xxx, xxx mohlo xxx xxxxxxxx xxxxxxxxx xxxxxxxxx xxxxx x xxxxxxx xxxxxx akutní xxxxxxxxxxxxx. Xxxxxxxx byla xxxxxxxxxxx xxxxxxxxxx xxxxxxxx xx Xxxxxxxxx, kdy xxx xxxxxxxxxx xxxxxxxxx xxx xxxx xxxxxx x EU, zda xx takováto xxxxxxxx xxxxxxxxxxxxxxxx. Xxxxxxx omezování xxxxxxxxx xxxxx x xxxxxxx xxxxxxxxxxxx léčivých xxxxxxxxx, které xxxx xxx poskytování xxxxxxxxx xxxx významné, xx xxxx xxxxxxxxxxx x xxxxxxxxxx, xx xxxxxxxx xxxxxxxxxxxx xxxx (xxxxxxx xxxxxxxxx zdraví).
Varianta 5
Tato xxxxxxxx xxxx xxxxxxxxx x ohledem xx xxxxxxxx xxxxxxxxx xxxxxxx xxxxxxxxxxxx xxxxxxxx x Xxxxxxxx. Xxxxxxx xxxxxxx xxxxxxxx distributora od xxxxxxxx xx xxxx xxxxxxxxx řešení jejich xxxxxxxxxx xxxxxxxxxxxx xxxxxx x xxxxx xx xxxxxx xxxxxxxxx xxxxxxxx. Xxxxxxxxx xx xxxx xxxxxxxxx xxxxx xxxxxx xxxxxxxxx x případě xxxxxxx akutní xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx.
Xxxxxxxx xxxxxx xxxxxxx
Xxxx xxxxxx kritérium xxxx xxxxxxx xxxxxxxxxx x xxxxxxxx xxxxxxxxxxxx xxxxxxx.
Xxxxxxxx 1 xxxx xxxxxxxxx x xxxxxxx xx xxxxxxx xxxxxx xxxxx xxxxxxxxxx problém, xxx xxxx xxxxxxx xxx xxxx. Xxxxxxxx 2 xxxx xxxxxxxxx x xxxxxxx xx xx, že xx xxxxxxxx definovaný xxxxxxx. Xxxxxxxx 3 byla xxxxxxxxx x xxxxxx xxxxxxxxxxxxxx a xxxxxxxxx xxxxxxxxxx. Xxxxxxxx 5 xxxx xxxxxxxxx s xxxxxxx na xx, xx xx xxxxxxxx xxxxxxxxxx xxxxxxx. Xxxx xxxxxxxxxxxx byla xxxxxxx xxxxxxxx, xxx xxxxx xx distributoři xxxxxxx xxxxxxxxx xxxxx xxxxx x případech, xxx xx x xxxxxxxx xxxxxxxxx xxxxxxx akutní xxxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxx pro poskytování xxxxxxxxxxx služeb.
Právní xxxxx xxxxxxx xxxxxxxxx
Xxx zvažování xxxxxxx forem xxxxxxxx xxxx (xxxxx nulové xxxxxxxx) vycházeno x xxxxxxxx xxxxx právního xxxx XX:
- xxxxxxxxxxxx xxxxxxx akty (xxxxxxxxxx x xxxxxxxxx xxxx xxxx konkrétnímu xxxxxxxxxx);
- xxxxxxxx obecné xxxxxx (xxxxxxxx x xxxxxxxxx xxxx xxxx xxxxxxxxxxx xxxxxx xxxxxxxx);
- xxxxxxxx (xxxxxxxxxx xxxxxx xxx).
Xxxxxxxx xxxxxxx xxxxxxxx xxxxx xxxxxxx xxxxxxxxx
Xxxxxxxx 1 = xxxxxx xxxxxxxx (xxxxxxxxx xxxx)
Xxxxxxxx 2 = individuální správní xxxx
Xxxxxxxx 3 = xxxxxxxx xxxxxx xxxxxx
Xxxxxxxx 4 = xxxxxxxx
Xxxxxxx x xxxxxxx xxx xxxxxxxxxx dotčené xxxxxxxx
Xxxxxxxx 1
Xxxxxxxxxxxx návrhu bude xxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxx, xxx se xxxxxxxxx xxxxxxx, xx xx xx xxxx xxxxxxxxxx xxxxxxxx xxxxxx xxxxxxxxx a xx xxx xxxxxxxx zdraví xxxxxxxx x XX. X xxxxxxxxx zdraví xxxx xxxxxxxx i xxxxxxx vynaložit náklady, xxxxx xx xxxxx xxxxxx xxxxx vynaložit, xxxxx by xx xxxx byly xxxxxxxx xxxxxxxx xxxxxx xxxxxxxxx (xxxxx xxxxxxxxx xxxxxxxxxx xxx.). Xxxxxxxx xxxx xxxx umožnění volného xxxxxx zboží, ovšem xx xxxx zdraví xxxxxxxx x ČR.
Varianta 2
Xxxxx xx xxxxxxxxx xxxx xxx xxxxxxxxx xxxxxx individuálních správních xxxx xxxxxxxxxx ve xxxxxxxx řízení, xxxx xx xxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxxx xxxx. Xxxxxxx řízení bývají xxxxxxx xxxxxx xxxxxxx, xxxxxxx xxxxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx je xxxxx x ohledem xx xxxxxx xxxxxxxx xxxxxx x zdraví xxxxx akutně.
Individuální xxxxxxx xxxx jakožto xxxxxxxxxx xxxxxxxx xxxxxxxxxxx účastníka xxxxxx x konkrétní xxxx. Xxxxx xxxxxxxx xxxxxxxxxxxx xx xx xxxxxxxxxxx je přitom xxxxx, pokud bychom xxxxxxxxx xx xxxxxxxx xxxxxxxxx možný xxxxx (xxxxx xx xxxxx xxxxxxx získala xxxxxxxxxxx xxxxxxxxx), xxxxxxxxx xx xx xxxxx 2500. X xxxxxx důvodu xx xxxx xxxxxxx xxxxxx administrativně xxxxxxx x xxxxxx by x xxxxxxxxx xxxx xxxxxxx xxxxxxxxxx x xxxxx daný xxxxxxx x xxxx xxxx.
Xxxxxxxx 3
Xxxxxxxx obecné xxxxxx xx xxxxxx xxxxxxx xxx xxxxxxxx xxxxxxxxxxx xxxxx subjektů v xxxxxxxxx xxxx. X xxxxxx xxxxxxxx, xxx xxx xxxxxxxxxxxx větší xxxxx omezených xxxxxxxx, xx xxxx jako xxxxxx. Kritérium xxxxxxxxx xxxx (xxxxx xx xxxxxxx vývozu xxxxxxxxxxx xxxxxxxx xxxxxxxxx) xx xxx xxxxxxx. Lze xxxxxx upravit xxxxxxxxx xxxxxxxxx xxxxxx xxxxxx xxxxxxxxx xxxx tak, xxx pružně xxxxxxxxx xxxxxxx x xxxxxxx xxxxxx xxxxxx nedostupnosti xx xxxxxx xxxxxxx xxxxxx xxxxxxxxx omezit xx zakázat.
Varianta 4
Vydávání xxxxxxxx xxxxxxxx xx xxxxxx x (oproti xxxxxx xxx správního xxxx x xxxxxxxx) xxxxxxx xxxxxx, xxx xx výraznou xxxxxxxxx, xxxxx xx xxx xxxxxxxxxx akutní xxxxxxxxxxxx. Xxxxxxxx právních předpisů xx proto nepružné. Xxxxxxx xx xxxxxx xxxxxxxxx x možnost xxxxxxxxx xxxxxxx dotčené xxxxxxxx jedním xxxxxxxxx.
Xxxxxxxx xxxxxx xxxxxxx
Xxxx hlavní xxxxxxxxx xxxx zvolena xxxxxxxxxx (administrativní a xxxxxx) xxxxxxxxxxxx systému.
Varianta xxxxx 1 (tzv. xxxxxx xxxxxxxx) xxxx xxxxxxxxx x xxxxxxx xx xxxxxx xxxxxxx xxxxx xxxxx xxxxxxx. Xxxxxxxxx xxxxxxxxxxx xxx xxxxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxx. Xxxxxx xxxxxxxxxx xxxxxx vymezeny xxxxxxxxx xxxxxxx při omezování xxxxxxxxx. Varianta xxxxx 2, xxx by xxxxxxxxx byly x xxxxxxxx xxxxxxxx omezovány xxxxxx xxxxxxxxxxxxxx xxxxxxxxx xxxx, xxxx zamítnuta x ohledem xx xxxxxxxxxxxxxxx x xxxxxxx xxxxxxxxx tohoto xxxxxxx. Xxxxxxxx číslo 4 (xxxxxxxx právních xxxxxxxx) xx xxxx xxxxxx x xxxxxxxxxxxxxxx (xxxxx x finančně) xxxxxxx xxxxxx, xxxxx xxxxx xxxxx x důvodu xxxxxxxx xxxxx reexporty xxxxxx použít.
Jako xxxxxxxxxxxx xxxx xxxxx xxxxxxx xxxxxxxx číslo 3 (xxxxxxxx xxxxxx povahy), xxxxxxx xxxxxxx xxxxxxxx xxxxxxxxxx situaci x x xxxxxxxxx s xxxxxxxxx xxxxxxx xxxxxxxx xxxxxxx xxxxxxxxxxxxxxxx xxxxxxx x administrativní xxxxx xxx xxxxx xxxxxxxxxx xxxxxxxx.
Xxxxxxxx xxxxxxxxx autorit xx procesu xxxxxxxxx xxxxxxxxx
Xxxxxxxx 1 = xxxxxx (xxxxxxxx xxxx)
Xxxxxxxx 2 = pouze Xxxxxxxxxxxx xxxxxxxxxxxxx
Xxxxxxxx 3 = pouze Státní xxxxx pro kontrolu xxxxx
Xxxxxxxx 4 = xxxxxxxxx xxxxxxxxx Ministerstva xxxxxxxxxxxxx a Xxxxxxxx xxxxxx xxx xxxxxxxx xxxxx
Xxxxxxxx 5 = xxxxxxx xxxxxx orgánu
Varianta 6 = xxxxxxx xxxxxx orgánu
Náklady x xxxxxxx pro xxxxxxxxxx xxxxxxx xxxxxxxx
Xxxxxxxx 1
Xxxxxxxxxxxx xxxxxx xxxx xxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxx, xxx xx xxxxxxxxx xxxxxxx, xx xx xx xxxx xxxxxxxxxx xxxxxxxx xxxxxx přípravek x xx xxx xxxxxxxx zdraví pacientů x XX. S xxxxxxxxx xxxxxx může xxxxxxxx i xxxxxxx xxxxxxxxx xxxxxxx, xxxxx xx xxxxx xxxxxx xxxxx vynaložit, pokud xx na xxxx xxxx xxxxxxxx xxxxxxxx xxxxxx přípravky (xxxxx xxxxxxxxx komplikací atp.). Xxxxxxxx xxxx xxxx xxxxxxxx xxxxxxx pohybu xxxxx, xxxxx xx xxxx xxxxxx xxxxxxxx x XX.
Xxxxxxxx 2
Xxxxxxxxxxxx xxxxxxxxxxxxx xx xxxxxxxxx xxxxxxxx orgánem na xxxxx xxxxxxx xxxxxx xxxxxxxxxxxx. Jedním x xxxx xxxxx je (x xxxxx xxxxxxxx xxxxx xxxxxxxxx xxxxxxx xxxxxxxxx xxxxxx) xxx xxxxxxxxx xxxxxxxxxxx léčivých xxxxxxxxx. X tohoto xxxxxxxx xx xxxx xxxxxx, aby xxxxx xxxxxxxx xxxxxxxxxxx xxxxxxxxxxxx. Xxxxxxxx xxxxx xx xxxx specifickou xxxxxxx, x jejímuž výkonu xxx xxxxxx Xxxxxx xxxxx xxx xxxxxxxx xxxxx, který disponuje xxx účely xxxxxxxx xxxxx xxxxxx administrativním xxxxxxxx a činnost xx xx xxxxx xxxxx (obdobně xxxx x xxxxxx xxxxxxxxx xxxxxxx XX) xxxxxxxxxxxxx. Xxxxxxxxx xxxxxxxx, xxx xx xxxxxxxxx xxxx xxxxxxxxx xxxxx Ministerstvem xxxxxxxxxxxxx, je xxxxxxxxx xxxx, xxx většinu xxxxxxxxxxxxxxxxx činností xxxxxxxxx Xxxxxx xxxxx pro xxxxxxxx xxxxx. Xxxxxx xx xxx xxxxxxxxx xxxxxxxxxx xxxxxxxxx, xx xxx xxxxxxxxx xxxxxxxx (xxxxxxx xxxxxxxxxxxx, xxxxxxxx x xxxxxxx x xxxxxxxx xxxxxxxx xxxxxxxxx xx xxxxxxxxx Státnímu xxxxxx xxx kontrolu xxxxx).
Xxxxxxxx 3
Xxxxxx xxxxx xxx xxxxxxxx léčiv xx orgánem xxxxxxxxxx Xxxxxxxxxxxx xxxxxxxxxxxxx x xxxxxxxxx většinu xxxxx xxxxxxxxx x xxxxxxxx xxxxx. Xxxxxxx xxxx xxxxxxxx xx bylo xxxxxxxxx a xxxxxxxxx xxxxxxxxxx xx xxxxx xxxxxxxxxx agendy xxxxx xxxxxxx. Xxxxxxxxx xx xxxx xxxxxxx xxxxxxxxxx xx xxxxxxxx a xxxxx svěřené Ministerstvu xxxxxxxxxxxxx.
Xxxxxxxx 4
Jak xxxx xxxxxxx xxx xx xxxxxxxx 2 a 3, oba orgány xx určitým způsobem xxxxxxxx xx xxxxxxxx xxxxx x Xxxxx xxxxxxxxx. Xxxxxxx je xxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxxx Xxxxxxxx xxxxxx pro xxxxxxxx xxxxx, přičemž Xxxxxxxxxxxx xxxx xxxxxxxxx xxxxx xx „kontrolní“ xxxxxxxxx (xx už xx formě odvolacích xxxxxxxxx xxxxxx xxxx xxxxxx prostředků xxxxxx xxxxxxxxxxx xxxxxx xxxxxxxxxx xxxxxxxxxxxxx). Z tohoto xxxxxxxx xx xxxxxxx, xxxxx by xxx xxxxxx xx xxxxxxxxx xxxxxxxxx xxxxxxxxxxxxxx. Tato xxxxx xxxxxxxxxx xx xxxxxx měla být xxxxxxxxxxx. Tj. měla xx xxxxxxxx, aby Xxxxxx xxxxx pro xxxxxxxx xxxxx předal x xxxxxxx xxxxxxxxx xx xxxxx xxxxxxx xxxxxxxxxxxx xxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxx příslušné xxxxx ministerstvu x xxxxxxx, xxx xx xxxxxxxxxxxx xxxxx xxxx xxxxx xxxxxxx x xxxxxxx xxxxxxxxx, x xxxxxx xx xxxxx x různých důvodů. Xxxxxxxxxx xxxx orgánů xxxx xxxxxxxxx xxxxxxxx xxxxxxx odůvodnění přijatých xxxxxxxx xx xxxxxx xxxxxxx xxxxxxxxx a xxxxxx xxx xxxxxxxx xxx jeden z xxxxxx, xxxxx se xx xxxxxxxx xxxxx x XX xxxxxx. Xxxxxx xxxxxxxxxxxxxx žádná xxxxxxxx xxxx xxxxxxxx.
Xxxxxxxx 5
Xxxxxxxxxx xxxxx xxxxx, xxxxx xx xxx x xxxxxxxxxx xxxxxxxx xxxxx xxx Xxxxxxxxxxxx xxxxxxxxxxxxx xxxx Xxxxxx xxxxx xxx xxxxxxxx xxxxx. Xxxxxxxxx xx xxxx xxxxxxxxxxxx xxxxxxxxx xxxx agendy orgánu, xxxxx xx xx xxxxx nezabýval.
Varianta 6
Xxxxxxx xxxxxx xxxxxx xx xxxxxxxxx xxxxxxxxxxxx xxxxxxxx xxxxxxx.
Xxxxxxxx xxxxxx variant
Jako xxxxxx xxxxxxxxx xxxx xxxxxxx efektivita xxxxxxxxxxxx xxxxxxx.
Xxxxxxxx číslo 1 (xxx. nulová xxxxxxxx) xxxx zamítnuta x xxxxxxx xx xxxxxx xxxxxxx xxxxx tento xxxxxxx. Stávající xxxxxxxxxxx xxx xxxxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxx. Xxxxxx xxxxxxxxxx xxxxxx vymezeny xxxxxxxxx postupy při xxxxxxxxx xxxxxxxxx. Xxxxxxxx xxxxx 2, xxx xx xxxxxxxxx xxxx x xxxxxxxx důsledku xxxxxxxxx xxxxx Xxxxxxxxxxxxx xxxxxxxxxxxxx, xxxx xxxxxxxxx x xxxxxx xxxxxxxxxxxx xxxxxxxxxxxx na xxxxxxxxx xxxxxxx tohoto xxxxxx. Xxxxxxxx xxxxx 3 (xxxxxxxx xxxxx Xxxxxxx xxxxxxx xxx xxxxxxxx xxxxx) xxxx xxxxxxxxx x důvodu xxxxxxxxxxxxxx xxxxxxxxx kontrolních mechanismů xxx přijímání xxxxxxxxxxx xxxxxxxx. Varianty 5 x 6 xxxx xxxxxxxxx x xxxxxxx xx xxxxxx xxxxxxx xxxxxxxxxxxx x nehospodárnost. Xxxx xxxxxxxxxxxx xxxx xxxxxxx xxxxxxxx xxxxxx xxxxx xxxxxxxxxx Ministerstva xxxxxxxxxxxxx x Xxxxxxxx xxxxxx xxx xxxxxxxx xxxxx, kdy xx xxxxxxxx xxxxxxxx již xxxxxx funguje xxxxxxxx x oblasti léčiv xxxxxxxx x xxxxxx x léčivech (Státní xxxxx pro xxxxxxxx xxxxx xxxx xxxxxxxxxxxx xxxxx x Ministerstvo xxxx xxxxxxxxxxxxx orgán).
Volba xxxxxxx podoby xxxxxxx xxxxxxxx
X ohledem xx xxxx xxxxxxx xxxxxxx xxxxxxxx řešení, xxx xx dle xxxxxxxxx xxxxxxxx zejména xxxxxxxxxx, xxxxxxxxx x xxxxxxxxxxxx xxxx xxxx xxxxxxxxxxxx
- xxxxxxx legislativních opatření;
- x xxxxxx zavedení xxxxxxxxxx xxxxxxxxxxxx hlášení xxxxx xxxxxxxxx xxxxxx;
- xx xxxxx opatření xxxxxx povahy;
- xxxxxxxxxx xx xxxxxxx xxxxxxxxxx Xxxxxxxx ústavu pro xxxxxxxx xxxxx a Xxxxxxxxxxxx xxxxxxxxxxxxx; xx xxxxx xxxxxxxxxxx xxxxxxxxx xxxxx xxxxxxxx x xxxxxx xxxxxxxx xxxxxx xxxxxxxxxxxx systému.
Definice xxxxxxx xxxxxxxxx xxxxx xxxxxx xxxxxx omezení xxxxxxxxx
Xxxxxxxx 1 = Xxxxxx xxxxx by xxxxxxx xxxxxxxx xxxxxx povahy, xxxxxx xx xxxxxxxx xxxxxx xxxxxxxx xxxxxxxxx, x xxxxx by xxxxxxxxxx distribuce xxxxxxx xxxxxx nedostupnost léčivých xxxxxxxxx, x xxxxxxx xx Ministerstvo xxxxxxxxxxxxx xxxxxxxx xxxxxxxx obecné xxxxxx, xxxxxx xx xxxxxxxx xxxxxxxxxx x xxxxxxxxxx případě
Varianta 2= xxxxxxxx xxxxxx xxxxxx xx xxxxxxxx xxxxx Xxxxxxxxxxxx xxxxxxxxxxxxx a Xxxxxx xxxxx pro xxxxxxxx xxxxx xx xxxxxx nedostatkových léčivých xxxxxxxxx xxxxxxxxxxx x xxxxxxxx umožňujícím xxxxxxx xxxxxxx xx svém xxxxxxxxxxx xxxxxxxxxx
Xxxxxxxx 3 = Xxxxxxxxxxxx zdravotnictví xx xxxxxxxx xxxxxx xxxxxxxx xxxxxxxxx, a xx xxxxxx xxxxxxxx xxxxxx xxxxxx, xx xxxxxxx xx xxxxxxxxxxx xx základě podnětu xx xxxxxx Xxxxxx, x xxxxx by xxxxxxxxxx xxxxxxxxxx xxxxxxx xxxxxx xxxxxxxxxxxx xxxxxxxx xxxxxxxxx, x xxxxxxxxxx xxxxxxxx xxxxxx xxxxxx, xxxxxx xx xx xxxxxxxx xxxxxxxxxx x xxxxxxxxxx případě, přičemž x těmto xxxx xxxxxxxxx xx Xxxxxx xxxxx pro xxxxxxxx xxxxx xxxxxxxxxx podklady x činil návrhy x xxxxxxx, xxx xx uvedeno xxxx.
Xxxxxxx x přínosy pro xxxxxxxxxx xxxxxxx xxxxxxxx
Xxxxxxxx 1
Xxxxxx xxxxx xxx xxxxxxxx léčiv by xxxxxxx xxxxxxxx obecné xxxxxx, kterým by xxxxxxxx xxxxxx xxxxxxxx xxxxxxxxx, xxx xxxxxxx xxxxxxxxxx xx xxxx x Xxxxx xxxxxxxxx xx xxxxx xxxxxxxxx xxxxxxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx xxx xxxxxxxxxxx xxxxxxxxxxx xxxxxx xxxxxxxxx x Xxxxx xxxxxxxxx x xxxxx xxxxxx xx xxxxxxxxxx xxxxxxxxxxxx. Xxxxxxxxxxxx zdravotnictví xx xx xxxxxxx podnětu Xxxxxxxx xxxxxx xxx xxxxxxxx léčiv xxx xxxxxxx xxxxxxx stanovených xxxxxxxx xxxxxxxx xxxxxxxx xxxxxx povahy, xxxxxx xx xxxxxxx distribuci xxxxxxxx xxxxxxxxx xxxx xxxxx Xxxxx xxxxxxxxx x xxxxxxx, xx xxx nedostatku xxxxxxxx xxxxxxxxx xx trhu x Xxxxx republice xx xxxxx xxxxxxxxx xxxxxxxxx jeho nedostupnosti xxx xxxxxxxxxxx zdravotních xxxxxx xxxxxxxxx v Xxxxx xxxxxxxxx.
Xxxxxxx xxxxxxx x nelogičnost xxxxxx xxxxxx xxxxxxxxxxx ve xxxxxxxx xxxx opatření xxxxxx povahy, xxxxxxx xxxxxxxxx xx xxxxxxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxx xxxxxx xxxxxx. Nebyly xxxxxxxxxxxxxx xxxxxxxxxx xxxxxxx xxxx xxxxxxxx. Xxxxxxxxxxxxxxx xxxx varianty spočívá xxx v xxxxxx xxxxxxxxxx xxxxxxxxx opatření xxxxxx povahy, přičemž xxxxxxxxxxxx xxxxxxxx xxxxxxxxx xx xxxxx xxxxx xxxxxx. Xxxxxxxxxxxx xxxxxx xxxxxxxx xx znamenalo xxxxxxxx xxxxxxxx xxxxxx xxxxxx xx úrovni Xxxxxxxx xxxxxx pro xxxxxxxx xxxxx, xxxx x ohledem xx xxx xxxxxxxxxx xxxxxxxxxx xxxxxxx xxxxxxx xxxxxxxxxxxx x držitelů x xxxxxx lékáren Xxxxx xxxx analyzovat potřebná xxxx x xxxxxxxxxxxxx xxxxxxxxx xxxxxx xxxxxx xxxxxxxxxxxxx léčivých přípravků. X xxxxxxx xx xxxxx XX x xxxxx xxxxx zboží xx xxxxx xxxxxxxx xxxxxx léčivých xxxxxxxxx xxxxxxxxxx xxx poskytování xxxxxxxxxxx xxxxxx.
Xxxxxxxx 2
Xxxxxx xxxxx xx xx xxxxxxx xxxxxxxx x xxxxxxx relevantních xxxxxxxx (xxxxxxxx xxxxxxxxxx x xxxxxxxxxx léčivých xxxxxxxxx, xxxxxxxxxxxx x xxxxxxxxxxxxx xxxxxxxxxxx x výdeji xxxxxxxx xxxxxxxxx) xxxxxxxxxx xxxxxxxxxxx xxxxxx xxxxxxxxxxxxxx xxxxxxxxxx léčivých xxxxxxxxx x xxxxxxxxxxx xx xxx způsobem umožňujícím xxxxxxx xxxxxxx ve xxxx xxxxxxxxxxx xxxxxxxxxx. X takto xxxxxxxxxxxx xxxxxxx xx xx xxxxxxxx xxxxxx xxxxxxxxx, xxxxxxx nedostatek xx xx trhu Xxxxx xxxxxxxxx xxxxxx, x xx by xxxx x xxxxxxx xxxxxxxx xxxxxxx xxxxxxxxx xxxxxxx xxxxxxxx xx formě xxxxxxxx xxxxxx xxxxxx Xxxxxxxxxxxxx xxxxxxxxxxxxx.
Xxxxxxxx 3
Xxxxxx xxxxx xxx xxxxxxxx xxxxx xx xx xxxxx xxxxxxx reexportu xxxxxxxx přípravků xxxxxxxxxx xxxxxxxx x xxxxx xxxxxx x xxxxxxx Xxxxxxxxxxxx xxxxxxxxxxxxx. Xxxxxxx xx xxxxx xxxxxxx xxxxxxxxx xxxxxxxx přípravků xx pak xxxxxx Xxxxxxxxxxxx xxxxxxxxxxxxx, xxxxx xx vydávalo xxxxxx xxxxxxxx xxxxxxxxx, a xx xxxxxx xxxxxxxx xxxxxx povahy, u xxxxx xx xxxxxxxxxx xxxxxxxxxx hrozila akutní xxxxxxxxxxxx xxxxxxxx přípravků, x xxxxxxxx obecné xxxxxx, xxxxxx by xxxxxxxx xxxxxxxxxx x xxxxxxxxxx xxxxxxx.
Xxxxxxxx xxxxxx xxxxxxx
Xxxx hlavní kritérium xxxx zvolena xxxxxxxxxx xxxxxxxxxxxxx xxxxxxx xxxxxxxx.
Xxxxx xxxxxxxx byla xxxxxxxxx x xxxxxx xxxxxxxxxxxx. Xxxxx varianta xxxx xxxxxxxxx z xxxx xxxxxx, xx xx xxxxx dostatečně xxxxxxxxxx xxxxx Xxxxxxxxxxxx xxxxxxxxxxxxx xxxxxxx xxxxxxxxxx orgánu xxxxxx xxxxxx xxx xxxxxx xxxxxxxx léčivých xxxxxxxxx. Xxxx zvolena xxxxx xxxxxxxx, xxxxxxx xx xxxx jako xxxxxxxxxxxxxxx x xxxxx xxxxxxxxxxxx.
XXXXXXX XXXXXX XXXXXXX XXXXXXX XXXXXXX REEXPORTŮ
Jako xxxxxxxxxxxx xxxxxx xxxx xx xxxxxxx xxxx xxxxxxxxx xxxxxxx výběru xxxxxxx xxxxxxxx xxxxxxxx xxxxxxx xxxxxxxx xxxxxxxxx Xxxxxxxxxxxxx zdravotnictví, x xxxxxxx xxxxxxx xxxxxx xx xxxxx x xxxxxxxx xxxxxx x xxxxxx xxxxxxxx na xxxxx XX. Xxxxxx xxxxx xxx xxxxxxxx xxxxx xxxx průběžně xxxxxxxxxxxx dostupná xxxx x hlášení xxxxxxxxxxxx, xxxxxxxx x xxxxxxx xxxxxxx xxxxxxxx přípravků xxxxxxxxxx xx tomto xxxxxxx.
Xxxx xxxxxxx xxxxxxxxx xxxxxxx xx xxxxxx xxxxxxxx zavést institut xxxxxxxx obecné povahy, xxxxx xxxx xxxxxxx Xxxxxxxxxxxx xxxxxxxxxxxxx, xxxxxxx xxxxx, x jehož xxxxxxxx xxxxx (xxx xx xxxxxxx existujícího xxxxxxxxxx §11 písm. x) xxxxxx x xxxxxxxx) xx zajišťování xxxxxxxxxxx léčivých přípravků xx území ČR. Xxxx xxx navázáno xx dosavadní xxxxxxxxxx Xxxxxxxxxxxx x xxxxxxx xxxxx vhodně xxxxxxx xxxxxxxx Xxxxxxxx xxxxxx xxx xxxxxxxx xxxxx x xxxxxxxxx xxx, xxxxxxx xxxxxxxxx. Xxxxxxxxxxxx xxxx xxxxxxxx xxxxxxx xx základě xxxxxxx Xxxxxxxx xxxxxx xxx xxxxxxxx xxxxx xxxxxxxxxx xx xxxxxxxxxxxxx dat, x to řádně xxxxxxxxxxxx. Xxxx data xx x xxxxxxx xxxxxxx xxxx moci Xxxxxxxxxxxx též xx Xxxxxxxx ústavu pro xxxxxxxx xxxxx vyžádat.
Jedná xx x xxxxxxxx xxxxx xxxxxxxxx xxxx, xxxxx cílí poměrně xxxxxx na regulaci xxxxxxxxxx počtu xxxxxxxx x xxxxxxxxx xxxx. Xxxxxxxx x upravované xxxxxxxxxxxx xx xxxxx xxxx jeho xxxxxxx xxxx xxxxxx forma xxxxxxxx. Xxxxxxxxxx právní xxxxxx xxxxxxxxx x xxxxxxxxx potřeb pacientů x Xxxxx xxxxxxxxx x x xxxxxxx xxxx xxxxxxx, kdy xxxx na xxxx xxxxxxxxxxxx xxxxxx potřeb xxxxxx přípravky vyváženy xxxx xxxxx Xxxxx xxxxxxxxx, xx xxx x souladu se xxxx xxxxxx xxxxxxxxx, xxxxxxxxxxxxx, xxxxxxxxxx xxxxxx xx xxxxxx dopadu x xxxxxxxxx.
2.3. Xxxxxxxx xxxxxxxx xx vztahu x xxxxxxx látkám xxx xxxxxxx xxxxxx xxxxxxxxx
Xxx xxxxxx tohoto xxxxxxxx xxxxx xxxxxxxxx xxxxx xxxxxxxx, xxx xxxxxx xxxx zákona x xxxxxxxx tak, xxx xxxx xxxxxxxxx xxxxxxxx zajištěna adaptace xxxxxxxx Komise x xxxxxxxxx xxxxxxxxx (XX) č. 1252/2014 ze xxx 28. xxxxxx 2014 xxxxxxxxxx směrnici Xxxxxxxxxx xxxxxxxxxx a Xxxx 2001/83/XX, pokud xxx x xxxxxx x xxxxxx správné xxxxxxx xxxxx xxx léčivé xxxxx xxx humánní xxxxxx xxxxxxxxx. Xxxxx xxxx xxxxxxxx by xxxxx xxxxxxxx xxxxxxxxx xxxxxxx sankčních xxxxxxxx xxxxxxxxxxx orgánů Xxxxxxxx xxxx xxxx České xxxxxxxxx.
2.4. Xxxxxxxxxx Xxxxxxxx xxxxxx pro kontrolu xxxxx a Xxxxxxxxxxx xxxxxxxxxxx cel
Varianta 1 - změna xxxxxx x xxxxxxxx
Xxxxx xxxxxxxxx xx novelizovat zákon x xxxxxxxx tak, xxx xxxxxxxxx xxxxxxxx xxxxxxxxxxx Xxxxxxxx xxxxxx xxx xxxxxxxx xxxxx x Xxxxxxxxxxx xxxxxxxxxxx xxx. Inspirací x xxxxx xxxxx může xxx xxx platný xxxxxx řád, a xx konkrétně ustanovení §8 xxxxxx x. 226/2013 Xx., x xxxxxxx xxxxx a xxxxxxxxxxx xxxxxxx na xxx, xxxxx xxxxxxxx xxxxxxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxxx, x nichž xx xxxxx xxxxxx xxxxxxxxx právě Generální xxxxxxxxxxx cel, v xxxxxxxxxxx xxxxxx xxx xxxxxxx komoditu xxx xxxx. Xxxx řešení, xx. xxxxx speciálního xxxxxx, xx x xxxxx xxxxxxx xxxx xxxxxxxxxxx, respektující xxxx xxxxxxxxx xxxxxxxxx xxxxxx xxxxxx xxxx oblasti.
Varianta 2 - Přijetí xxxxxxxxxx novely xxxxxx x Celní xxxxxx Xxxxx xxxxxxxxx x xxxxxx xxxxxx xxxxxx xxxxxx x xxxxxxxx
Xxxxxx xxxxxxxxx řešení xxxxxx xxxxxxxx xx přijmout x xxxxx xxxxxxxxxxxx xxxxxx zákona x xxxxxxxx xxxxxxxxxxx xxxxxx xxxxxx č. 17/2012 Sb., x Xxxxx správě České xxxxxxxxx, xx xxxxx xxxxxxxxxx xxxxxxxx, xx xxxxx xx xxxx x xxxxx xxxxxxxxxx §2 xx 5 xxxxxx zákona xxxxxxxxx xxxxxxxxx xxxxxxxxx Generálního xxxxxxxxxxx cel x xxxxx xxxxxx.
Xxxxxxxx 3 - Xxxxxxx xxxxxxxxxx xxxxxxxxxx zákona x Xxxxx xxxxxx České xxxxxxxxx
Xxxxx xxxxxxxxx xx xxxxxx samostatné novelizace xxxxxx č. 17/2012 Sb., x Xxxxx správě Xxxxx xxxxxxxxx, xx xxxxx xxxxxxxxxx předpisů. Xx xxxxx zákon nabyl xxxxxxxxx xxxxxx xxxx 1. xxxxx 2013, xxx již xxxxxx xxxxxxxxx xxxxxxxxxxx, takže xxx xxxxxxxxxxxx xxxx xxxxx xxxxxxxxxx.
2.5. Prokazování xxx inspekční xxxxxxxx x xxxxxx instituty xxxxxxxxx x zabrání xxxxxxxx přípravků
Varianta 1 - xxxxxx
Xxx xxxxxxxxx xxxxxxxx xxxxxx xxxxxx x zákoně x xxxxxxxx xx xxxxxxx xxxxx k přesnější x xxxxxxxxx xxxxxx xxxx xxxxxx, xxxxxxx xxxxxxxxx xxxxxx již xxxxxxxxxx xxxxxxxxx z xxxxx a xxxxxxxxxx xxxxxxxxxxx potřebě, xxx xx xxxx xxxxxx xxxx xxx xxxxxxxx.
Xxxxxxxx 2 - xxxxx xxxxxx x léčivech
Tato xxxxxxxx xx znamenala xxxxxxxxxxxx xxxxxxx xxxxxxxx x rámci xxxxxx xxxxxxxx xxxxx kontrolního xxxx, xxxx xx xxxxxxxxx k xxxxxxxxxxx xxxxxxxxx inspektora ke xxxxxxxx xxxxxxxxx xxxxx xxxxxxx xxxxxx xxxxxxx xxxxxxxx. Xxxx xx xxxxx k nastavení xxxxxxxx xxxxxxxxx zajištění x xxxxxxx léčivých xxxxxxxxx xxx, aby xxxxx xxxxxxxxxx xxxxxxxxxx xxxxxxx pro xxxxxxxx xxxxxxxxx xxxxxxx xxxxxxxxx xxxxxx x xxxxxx xxxxxxxx x účinných xxxxxxxx x xxxxxx xxx xxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx, xxxxx xxxxxxxxx požadavky xx xxxxxx jakost, xxxxxxxx x xxxxxxxxxx. Xxxxx xxx odůvodnění xx xxxxxxxx xxxxx.
3. Xxxxxxxxxxx xxxxxxx x přínosů
Řešení xxxxxx xxxxxxxx spočívajících x xxxxxxxx xxxxxxxx xx xxxxxx x xxxxxxx xxxxxx pro xxxxxxx xxxxxx přípravky, xxxxxxxxx xxxxxxxxxxx Xxxxxxxx xxxxxx xxx xxxxxxxx xxxxx a Generálního xxxxxxxxxxx xxx x xxxxxxxx xxxxxxxxxxxxx x xxxxxxxxxxx xxxxxxxxx inspektorů xxx xxxxxxxxx xxxxxxxxx xxxxxxxx x x xxxxxxxxxxxxxxx právních institutů xxxxxxxxx x xxxxxxx xxxxxxxx přípravků xxxxxxx xxxxxxxxxxx, xxxxxxx přínosy xxxxxx těchto xxxxxxxx xxxx již xxxxxxx x xxxxxxxxxx. Z xxxxxx xxxxxx xxxxx xxxxxxxxxxx xxxxxxxxxxxx x xxxxxxxxxxx nákladů x xxxxxxx uvedené x xxxxxx 3.1 xx 3.3 xxxxxxxx xx xxxxx xxxxxxx xxxxxxxx xxxxxxxx, a xx x xxxxxxxx nařízení x xxxxxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx x k xxxxxxxxx xxxxxxxxxx k xxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx.
3.1 Xxxxxxxxxxxx xxxxxxx a xxxxxxx
3.1.1. Xxxxxxxx xxxxxxxx xxx klinická hodnocení xxxxxxxxx xxxxxxxx přípravků
Pokud xxx x adaptaci xxxxxxxx xxx xxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx, xxxxxxx xxxxxxxx xxxxxxxx xxxxxxxx č. 536/2014 xxxx xxx na xxxxxx Xxxxxxxx xxxx, xxx x xxxxxxxxx xxxxx. Přínosem xxxxxx xxxxxxxx xx však xxxx x budoucnu xxx xxxxxxx xxxxx xxx xxxxxxxxxxxx xxxxxxxxxx xxx xxxxxxxxx xxxxxxxxxx xxxxxxxxxx. Xxxxxxxx xx xxxxxx mělo xxx xxxxxxxxx x účelnější xxxxxxxxx xxxxxxxxxx xxxxxxxxx x rámci xxxx Xxxxxxxx xxxx x xxxxxxxx xxxxxxxx xxxx xxxxxxxxxxx režimu xxxxxx xxxxxxxxxx x xxxxxxxxx, xxxxxxxxxxxxx Evropské unie xxx xxxxxxxxxx xx xxxxxxx xxxx x xxx zvrácení xxxxxxxxxx xxxxxx xxxxxx xxxxxxxxxx x Xxxxxxxx xxxx, xxxxx logickým následkem xx snižování xxxxx xxxxxxxxxx xxxxxxxxx, xxxxx xx jinak xxxxx xxxxxxxxx v Evropské xxxx xxxxxxx xxxxxxxxxxxxx xxxxx řádově o xxxxxxx let xxxxx, xxx xxxx hodnocený xxxxxx přípravek xxxxxxxxxxx. Xxxxxxxxx xxxxxxxx by x důsledku rychlejšího x účinnějšího xxxxxxxxx xxxxxxxx xxx klinických xxxxxxxxxxx a jejich xxxxxxxxxx xxxxxxxxx xx xxxxxxxx xxxxx měla xxx xxxxxxxxxxxx xxxxx xxxxxxxxxxx léčivými xxxxxxxxx, xxxx xxxxxxx xxxxxxxxx xxxxxxxxxx nových x xxxxxxxxxxxxxx xxxxxxxx xxxxxxxxx xxx pacienty x xxxxxxxxx xxxxxxxx xxxxxxxx xxx xxxxxxx xxxxxxxx xxxxxxxxx zdraví xxx x xxxxxxxxx státech, xxx x xxxx Xxxxxxxx xxxx. Zvýšení xxxxx předkládaných xxxxxxx x xxxxxxxx hodnocení x tím i xxxxxx xxxxxxxxx by xxxxxxxx další xxxxxxxx xxxxxxxxxx xxx xxxxxxxxxxxxx xxxxxxxxxxx xxxxxx, kteří xxxxxxxxx xx xxxxxxxxx xxxxxxxxxx hodnocení x xxxxxx xxxxx klinického xxxxxxxxx xxxxxxxx odměnu. Xxxxxxx by xx x xxxxxxxxxx xxxxxxxx xxxxx xxx xxxxxxxx, xxxxx zadavatel xx xxxxxxx xxxxxx xxxxx xxxxxxxxx, xxx xxxx xxxxxxxxxx přípravek, xxx xx xxxxxx xxxxxxxxxx xxxxx, xxxxx hrazena xxxxxxxxxxx. Xxxxxx většího xxxxxxxx xxxxxxxxxx hodnocení xx mohl znamenat x xxxxxxx xxxxxxx xxxxxxxxxx xxxx jak xx straně xxxxxxxxxx (x farmaceutických společností xx xxxxxxxxx xxxxxxxxxx xxxxxxxxxx), xxxxxx tak x xx xxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxx, xxx. x xxxxxxxxxxxxx xxxxxxxxxxx služeb, kdy xx xxxxxxx xx xxxx xxxxx mohly xxx xxxxx ze xxxxxxxxx xxxxxxxxxx xxxxxx xx xxxxxx.
Xx se xxxx finančních xxxxxxx xxxxxxxxxxxxx x nutnosti xxxxxxxx xxxxxxxxxx xxxxxx, xxxx xxxx xxxxxxxxxxx:
- xx xxxxxx Xxxxxxxx xxxxxx xxx xxxxxxxx xxxxx 32 xxxxxx xxx xxxxx 8 xxxxxx etické komise). Xxxx xxxxx xxxxxxxxxx xxxx pozice xxxxxxxxxxxxxxx xxxxxxxxxxxx (5), xxxxxxxxxxxx xxxxxxxxxxxxx hodnocení (2), xxxxxxxxxxxx bezpečnostních xxx xxxxxxxxxx xxxxxxxxx (2), xxxxxxxxxx (5), xxxxxxxxxxxx xxxxxxxxxx xxxxxxxxx (2) x personální xxxxxxxxx xxxxxxxxx-xxxxxxxxxxxxx x xxxxxxxxxxxxxxxxx xxxxxx pro xxxxxxx xxxxxx xxxxxx - xxx xxxxx 8 xxxxxx etické komise - 16 úvazků). Xxxx xxxxxx budou xxxxxxxx kryty x xxxxxxx xxxxxx xx xxxxxxxx xxxxxxxxx (xxxxxx xxxxxx). Xxx finanční xxxxx organizačně xxxxxxxxxxx xxxxxxxxxxx xxxxxx xxxxxxx xxxxxx xxxxxx xxxx xxxxxxxxx orgánu Státního xxxxxx xxx kontrolu xxxxx xxxx xxxxxxxxx x části xxxxxxxx xxxxxxxxxx x grantu xxxxxxxxxxxx x XX xxxxx, z xxxxx xxxx kryto x xxxxxx xxxxxx za xxxxxxxx hodnocení xx xxxxxxxxxxx xxxxxxx xxxxxxxx xxxxx;
- xx xxxxxx Xxxxxxxxxxxx zdravotnictví vznikne xxxx agenda xxxxxxxxxx xxxxxxxx proti xxxxxxxxxx xxxxxxxxxx x žádosti x schválení xxxxxxxxxx xxxxxxxxx. Xxxx xxxxx xxxxxxxxxx 1 xxxxxx xxxxxxxx referenta x 1 xxxxxx xxxxxxxxx xxxxxxxxx. Činnost xx Xxxxxxxxxxxx xxxxxxxxxxxxx tak xxxx xxxxxxxx ve xxxxxxxxx xxxxxxxxx (x xxxxxxx xx xxxxxx xxxxx v xxxxx xxxxxxxx) právní části xxxxxx xxxxxxxx xxxxxxxxxx xxxxxxxxxxx xxxxxxxx x xxxxxxx odborné xxxxx xxxxxx xxxxxxxx xxxxxxxxxx xxxxxxxxxxxxxxx xx xxxxxxxxxx xxxxxxxx. Xxxx xx xxxxxx Xxxxxxxxxxxx xxxxxxxxxxxxx xxxxxxx xxxxxx spojená x xxxxxxx xxxxxx xxxxxx xxxx xxxxxx xxx xxxxxxxxxxxxxx klinická xxxxxxxxx, naopak xxxxxxx xxxx xxxxxx jmenování x odvolávání xxxxx xxxxxx xxxxxx xxxxxx Xxxxxxxx xxxxxx xxx xxxxxxxx léčiv ministrem xxxxxxxxxxxxx.
3.1.2. Xxxxxxxx xxxxxxxxx x omezení reexportu xxxxxxxx přípravků
Navrhovaná xxxxxx xxxxxx spočívající x xxxxxxxx x xxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxx xxx xxxxxxxx xxxxxx, xxxxxx xx xxxxxxxx xxxxx, xxxxx xx xxxxxxxxxx xxxxxxxxxx x xxxxxxxxxxx xxxxxxx x dopady xx xxxxxxx xxxxxxxxx. Xxxxxxxxxx xxxxxx úprava xxxxxxx xxxxxx xxx xxxxx xx mezinárodní konkurenceschopnost Xxxxx xxxxxxxxx, xxxxxx xxxxxxxxxxx xxxxx (xxxx, xxxxx), xxxxxxxxxxxx, xxxxx xxxxxxxxxxx xxxxxx a xx xxxxxx x xxxxxx diskriminace.
Předpokládá xx xxxxxxxx xxxxx xx xxxxxx xxxxxxxx x xxx xxxxxxx, že xxxxx upraveny xxx xxxxxxxxxx x zavedeny xxxx xxxxxxxxxxxxxxx xxxxxxx xxxxx, xxxxxxxxxx x xxxxxxxxxxxxx xxx pro xxxxx identifikace hrozby xxxxxxxxxxxxx léčivých přípravků xxx potřeby pacientů x Xxxxx xxxxxxxxx Xxxxxxx xxxxxxx xxx xxxxxxxx xxxxx a xxxx xxxxxxxxxxxxxxx xxxxxxx xxxxxxxx opatření xxxxxx xxxxxx Xxxxxxxxxxxxx zdravotnictví. Xxxxxxxx xxxxx x xxxxx xxxxxx xxxx xxxxxxxxxxxx navýšením pracovních xxxxxx, xxxxxxx se xxxxxxxxx xxxxxx jednat x xxxx xxx 4 xxxxxxxx xxxxxx xxx osoby podílející xx xx xxxx xxxxxxxx.
4 xxxxxxxx úvazky xxxxx xxxxxxxx xx 2 pracovních xxxxxxxx xx Státním xxxxxx xxx xxxxxxxx xxxxx (xxxxxx xxxxxxxxxxxx xxxxxxxxxxxx xxxxxxx xxxxxxxxxxx Xxxxxxxxxxxx), x xx 2 xxxxxxxxxx xxxxxxxx na Xxxxxxxxxxxx xxxxxxxxxxxxx. Xxxxxxx xx Ministerstvu xxxxxxxxxxxxx xxxx xxxxxxxx ve xxxxxxxxx xxxxxxxxx (x xxxxxxx na xxxxxxx xxxxxxxx xxxxxx) xxxxxx xxxxx xxxxxx xxxxxxxx xxxxxxxxxx právnického xxxxxxxx x xxxxxxx odborné xxxxx xxxxxx odborným xxxxxxxxxx farmaceutického xx xxxxxxxxxx xxxxxxxx. Xxxxxxxx xxxxx na xxxxxx xxxxxxxx xxx bude xxxxxxxxx.
Xxxxxxxxx dopad navrhované xxxxxx úpravy na xxxxxxx xxxxxxx xxxxxxxx, xxxxxxx xx prostředky xxxxxxxxx xxxxxxxxxxx pojištění xxxxx xxxxxx xxxxxxxxx. X xxxxxxx xx xx, xx xx xxxxx o xxxxxxxxx xxxxx státu xx xxxxxxx xxxxxxxxx, ve xxxxxx xx zajišťována xxxxxxxxx xxxx, xxxxx xx částečně xxxxxxxxxxxx x xxxxxxxxxx veřejného xxxxxxxxxxx pojištění, lze xxxxxxxxxxxx, že xxxxxx xxxx xxxxxxxxxx právní xxxxxx xxx bude. Xxxxxx xx xxxxxxx xxxxxxxxxx x veřejného xxxxxxxxxxx pojištění xxx xxxxxxxxxxxx xxxxx xxxxxxxxx - xxx xxxxxxxxxx xxxxxx xx xxxxxxxxx xxxxxxxxxx x xxxxxxxx, xxxxx xxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxx léčby nebo xxxxx xxxxxxxxx postupů. Xx se xxxx xxxxxx xx xxxxxxxxxxxxx xxxxxxxxx Xxxxx xxxxxxxxx, xxxxxxxxx xxxxxx xx xxxxxxxxxxxx xxxxxxxx přípravků xxxxxxx xxxxxxxxxxxxx xxxxxxxx, xxx xxxxxxxxxxxx xxxxx xxxxxxxxx xxxx, xxxxx xx xxxxx významně xxxxxxxxxxxxx xxxxxxxxxxxxxxxx xxxxxxx xxxxxxxx x vysokou xxxxx xxxx xxxxxxxxxxxxxxxx, xxxxxxxxxxxx z rámce xxxxxxx xxxxxxxxxxxxxxx xxxxxx. Xxxxxxx xxxxx xxxx xxx v tomto xxxxxxx přednost před xxxxxx xxxxxxxxxxxxx.
Xxxxxxxxxx xxxxxx xxxxxx představuje dopad xx xxxxxxx xxxxxxxxxxxxx xxxxxxxx x xxx, xx xxxxxx xxxxx xxxxxxxxxx povinnost xxxxxxxxxxxx xxxxxxxx xxxxxxxxx xxx xxxxxx, xx hodlají xxxxxxxxxxxx xxxx xxxxx Xxxxx republiky xxxxxx xxxxxxxxx, xxxxx xx xx xxxxxxx xxxxxxxx xxxxxxxxx ohrožených xxxxxxxxx. Xxxxxxxxx xxxx není xxxxxx, nezasahuje všechny xxxxxxxx xxxxxxxx xxxxxxxxxxxx, xxx xxx xxxxxx xxxxx část a xxxxxx xx xxxxx xxx xxxxx xxxxxxxx xxxxxxxxxxxx xx distribucí xxxxxxxx přípravků, xxx xxxxx relevantní skupiny xxxxxxxx a léčivých xxxxxxxxx. Xxxxx dopad xx xxxxxx x xxxxxxx x xxxxxx xxxxxxxxxx právní xxxxxx xxxxxx na xxxxxxxx xxxxxx xxxx x xxxxxxxx cíle, xxxxxx xx xxxxxxxxx xxxxxxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx xxx potřeby xxxxxxxx x České xxxxxxxxx x případech hrozící xxxxxx xxxxxxxxxxxxx x xxxxxx xxxxxx nadměrného xxxxxxxxx.
Xxxxxxxxx xxxxx bude xxx navrhovaná xxxxxx xxxxxx xxxxxxx xx xxxxxxxx, xxxxxxx xxxxxxxxxxx xxxxxxx xxxxxxxx, kterým xxxxxxx dostupnost xxxxxxxx xxxxxxxxx xxxxxxxxxxxxxxx xxxxxx xxxxxxx před xxxxxxxxxx xxxx xxxxx Xxxxx xxxxxxxxx.
3.1.3 Xxxxxxx xxxxxx xxxxxxxxxxxx nákladů a xxxxxxx x oblastech 3.1.1 x 3.1.2.
Xxx xxxxxxxxxx xxxxxxxxx xxxxxx xxxxxx xxxxx a xxxxxxxxx spojených s xxxxxxxxx xxxx třeba xxxxxxx počet úvazků XXXX x to x xxxxxxxx xxxxx 34 xxxxxx. K xxxxxxxxxx xxxxxx xxxx xxxxxxxx postupně, x xx v xxxxxx 2016 xx 2018 - x xxxxxxxxxx xx počtu předkládaných xxxxxxx x xxxxx xxxxxx etické xxxxxx.
Xxxxxx xxxxxx xxxxx by xxx být xxxxxxxx (xxxxx xxxxxxx xxxxxx xxxxx xxxxxxxxx xxxxxx xxxxxx), a xxxxx xxxxx xxxxxx x xxxxxxxxx zvyšováním xxxxxx (xxx xxxxxxxxx xxxxxxx).
Xxxx xx jednat x xxxx xxxxxx:
Xxxxxxxxxxxxx posuzovatel (xxxxxx 5) - x xxxx 2016 xx počítá s xxxxxxxxx 4 xxxxxx, xxxx xxxx záležet xx xxxxxxxxxx xxxxxx xxxxxxx xxxxxxxxxx, xxx. xx xxxxxxxxxx xxxxxxxxxxx xxxxx v xxxxxxxxxx, xx xxxx kompilací xxxxxxxxxx xxxxx dotčených xxxxxxxxx xxxxx x xxxxxxx, xx XX xxxx xxxxxxxx státem xxxxxxxxxxx, xx náročnosti xxxxxxxxxx xxxxxxxx, x xx xxxxx xxxxxxxx xxxx xxxxxxxxxx, xxx xx nařízení nově xxxxxxxxx. Xxxxxxx xx xxxxx počítat xx xxxxxxxx počtu žádostí x novými xxxxxxxxxxxx xxxxxxxx přípravky, xxxxxxx xxxxxxxxxx je xxxxxxxxxx x vyžaduje více xxxx.
Xxxxxxxxxxx xxxxxxxxxxxxx hodnocení (2 xxxxxx) - 1 xxxxxx x xxxx 2016, xxxxx x xxxx 2017 - xxxx xxxxxxxxx Xxxxx pouze 1 xxxxxxxxxxxxx + xxxxxxxx xx xxxxxxxx xxxxxx. X xxxxxxxx xxxx xxxx xxxxxx xxxxxxxxxx xxxxxxxxxxx xxxxxxxxx zprávy, xxx nebude v xxxxxxx členského xxxxx xxxxxxxxxx xxx postupu xxxxx nařízení xxxxx, xxxxx xxxxxxx xxxxxx xxxxx xxxxxxxxxxx zpráv xxx Roční zprávy xxxxxxxxxxx přípravku, xxx xxxx vyžadovat i xxxxxxxx xxxxxxxxxxxxx xxxxxxxxxxxx.
Xxxxxxxxxxx xxxxxxxxxxxxxx xxx klinických xxxxxxxxx = posuzovatel xxxxxxxx xxxxx dokumentace (1 xxxxxx) - xx xxxxxxxxx xxxxxx xx xxxxxxxx xx 2 xxxxxx xx xxxx 2016 (1 xxxxxx již je x xxxxxxxxxxx). Xxxxxxxxxxxx xxxx xxxxx xxxxxxx xxxxxxxx x naučit xxxxxxxxxxx práce, xxxx xxxxxx xxxxxxxx xx xxxxxxxxxxxx hlášení u Xxxxxxxx xxxxxx xxxxxxxx (xxxx xxx EMA). Xxxxx xx x xxxxx xxxxxx, xxxxx xx xxxx x xxxxxxxx xxxxxx vedena xxxxxxxx working xxxxx xxx EMA. Xxxxxxxxxxxx xxxxx rovněž xxxxxxxxxxxx xxxxxxxxxxxx xxxxxxx z xxxxxxxxxx xxxxxxxxx x XxxxxXxxxxxxxx xxxxxxxx a xxxxxxxxxxxxx s xxxxxx x xxxxxxxxx xxxxxxxx xxxxxxx.
Xxxxxxxxx xxxxxxx klinické xxxxx (5 xxxxxx) - xxx xxx 2016 xx počítá xx 2 úvazky, xxxx xxxx xxxxxxx xx konkrétních xxxxxxxxx. Xxxxxxxxxxxxxxx xxxx nutnost xxxxxxx počtu než 5. Xxxxxxx navýšení xxxxxxx xxxxx z xxxxxxxxx zajištění dohledu xxx klinickým xxxxxxxxxx, xxxxxxx xxxxxxx xxxxxxxx xxxxx xxxxxxxxx xxxxx xxxxxxxxxx správné xxxxxxxx xxxxx, xxx xxxxxxx x x xxxxxxxxx xx xxxxx xxx xxxxxxxxxx xxxxxxxxxxxx xxxxxxxxxx x xxxxxxxxx xxxxxxxxx xxxxx, xxxxxxxx a xxxxxxxxxxxxxx XXX. Při xxxxx xxx 375 xxxxxxx x xxxxxxxx xxxxxxxxxx xxxxxxxxx/xxx a xxx 1600 „xxxxxxxx“ xxxxxxxxxx xxxxxxxxx x xxxxx xxxx je xxxxxxxx xxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxxxxxx. X xxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxx je nutná xxxxx, kterou xxxxx xxxxxx xxxxxxxxxxx xxxxxxxx.
Xxxxxxxxxxx xxxxxxxxxx xxxxxxxxx (3 xxxxxx) - xxx xxx 2016 xx xxxxxx s 1 xxxxxxx, x xxxxxx xxx x xxxx 2017 x 1 x xxxx 2018. Xxxxxxxxxxxx budou zajišťovat xxxxxxxxxx x xxxxx xxxxxxxxxx xxxxxxxxx x xxxxxxxxx xxxxxxxxx xxxxx x xx xxxxx XX x xxxxxxxxx xxxxxxxxxxxxxxxx xxxxxxxx (xxxx. xxxxxxx experti aj.), xxxxx xxxxxxxxxx vkládání xxxxxxxxxx xx xxxxxxx, xxxxxx xxxx pro xxxxxxxxxx xx xxxxx XX.
Xxxxxxxxxx xxxxxxxxxxxxx xxxxxx xxxxxxxx xxxxxx xxxxxx (4 úvazky). X xxxxxx úvazky je xxxxx xxxxxxx xxx xxx rok 2016. Xxxx pracovníci xxxxx xxx za xxxx xxxxxxxx technické xxxxxx xxxx xxxxxxxxx činnosti xxxxxx xxxxxx xxxx xxxxxxxxx xxxxxx Xxxxxx, xxxxxxx xxxxxxxx xxxxxxxxx, xxxxxxxx xxxxxxxxxx xxxxxx, xxxxxxxxx xxxxxxxxxx xxx xxxxx xxxxxx xxxxxx (xxxxxxxxx xxxxxxxxx xxxxxxxxxx), xxxxxxxxx koordinačních postupů x XX pro xxxxxxxxxxxx xxxxxxxxxx etické xxxxxx. Xxxx xxxxx xxxxxxxxxxx xxxxxxxx pro Xxxxxxxxxxxx xxxxxxxxxxxxx při xxxxxxxxxxx žádostí o xxxxxxxx v xxxxxx xxxxxx. X dalšími xxxxxx je xxxxx xxxxxxx x návaznosti xx potřebu xxxxxxx xxxxx xxxxxx xxxxxx xxxxxx x xxxxxxx xxxxxxxxxxx xxxxxx a x návaznosti xx xxxxx předkládaných žádostí. (xxx počtu 8 xxxxxx xxxxxx komise - 16 úvazků - do xxxx 2019 xx 2020 - podle xxxxxxxxxx xxxx nabytí účinnosti xxxxxxxx č. 536/2014).
|
xxxxx xxxxxxxxxx xxxxxx, xxxxxxxxxxxx xx XXXX x xxxxxxxxxxx x xxxxxxxx nařízení 536/2014/EU |
||||||
|
2016 |
2017 |
2018 |
32 xxxxxx |
|||
|
4 |
XX |
1 |
XX |
|||
|
1 |
XXX |
1 |
XXX |
|||
|
1 |
XXXXX |
|||||
|
2 |
XXX |
2 |
XXX |
1 |
XXX |
|
|
1 |
XXXX |
1 |
XXXX |
1 |
XXXX |
|
|
4 |
XXXX |
8 |
XXXX |
4 |
XXXX |
|
|
13 |
13 |
6 |
||||
xxxxxxx:
xxxxxxxxxxxxx xxxxxxxxxxx (XX) - xxxxxx 5
xxxxxxxxxxx xxxxxxxxxxx xxxxx (PPK) - xxxxxx 2
xxxxxxxxxxxx xxxxxxxxxxxxxx xxx XX (XXXXX) - xxxxxx 1
xxxxxxxxxx xxxxxxx xxxxxxxx xxxxx (XXX) - xxxxxx 5
xxxxxxxxxxxx XX (XXXX) - celkem 3
xxxxxxxxxxxx centra XX - (XXXX) - 4 (xx třeba xx xxxxxxxx xxxxx xxxx xxxxxxxx xxxxxx XX, xxxxx je xxxxx xxxxxxxxx xxxxxxx xxxx administrativy
(formuláře, xxxxxxxx xxxxxxx xxx.) xxx xxxxx xxxxxxx EK xxxxxxxx xxxxxxx, xxx xxxxx začít xxxxxxxx xx svém xxxxxx xxxxxxxxx
xxxxxxxxxxxx centra XX - (XXXX) – 12 každá xxxxxxx XX xx xxxx xxx 2 xxxxxx xx xxxxxxxxx administrativních xxxxxxx xxxxxxxxxxx x XX
xxxxx xx xxxxxxxxxxx xxxxxxxx x xxxxxxx 12 XXXX po xxxxxxxxx xxxxxxx xxxxxx XX
xxxxx xxxxxx potřebných xx XXXX xxx xxxxxxxxx xxxxxxxx pro xxxxxxxx xxxxx.xxxxxxxxxx, 2016
2 xxxxxx
2 xxxxxxxxxxxx reexportů
34 xxxxxx
2 xxxxxxxx xxxxxx xxx XX - xxxxxxxx x xxxxxxx xxxxxxxx xxxx farmacie x xxxxxxx.
Xxxxx xx xxxx xxxxxx agend xxxxxxxxxxxxx x xxxxxx xxxxxx opatření omezující xxxxxxxxx xxxxxxxxx, xxx xxxxxx xxxxxxxxx xx xxxxx xxxxxxx x xxxxxxxxx o 2 xxxxxx xx SÚKL x o 2 xxxxxx xx XX. Xxxxx zajistí xxxxxxxxx x vyhodnocování xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx, XX xxxxxxx xxxxxxxx agendu xxxxxxxx x xxxxxxxx xxxxxxx x xxxxxxxx xxxxxx xxxxxx omezujících xxxxxxxxx. X xxxxxxxxxxx x danou xxxxxxxxxxxxx xx xxxxxxx xxxxxxxx xxxxxxx x xxxxxxx xxxxxxxx xxxxxxxxxxx, xxxxxxxx xxxxxxxxx xx otázkou xxxxxxxxxxx x xxxx xxxxxxxxx úzkou xxxxxxxxxx xxxx oběma institucemi, x xx x x xxxxxxx xx xxxxx dané xxxxxxx.
Xxxxxx xxxxxxx:
Xxxxxxxxxxxx farmaceutické dokumentace - platová xx. 13
Xxxxxxxxxxxx xxxxxxxxxxxxxx xxx/xxxxxxxx xxxxx xxxxxxxxxxx - xxxxxxx xx. 13
Xxxxxxxxxxx xxxxxxxxxxx xxxxxxxxxxx - xxxxxxx xx. 13
Xxxxxxxxxx xxxxxxx xxxxxxxx xxxxx - xxxxxxx tř. 13
Xxxxxxx xxxxxxxxxxxxx centra xxxxxx xxxxxx - xxxxxxx tř. 13
Xxxxxxxxxxxx - platová tř. 12
Xxxxxxxx xx oblast xxxxxxxxx MZ - xxxxxxx xx. 13
Právník xx xxxxxx xxxxxxxxx XX - platová xx. 13
Posuzovatel xxx xxxxxx xxxxxxxxx XXXX - xxxxxxx xx. 13
Xxxxxxxxxxxxx roční xxxxxxxx xxxxxxx xxxx xxxxxxx xxxx
|
Xxxxxxx xxxxx |
Xxxxxx xxxxxxx |
xxxxxx |
Xxxxxx /xxx |
Xxxxxxxx xxxxxxx xxxx XXXX |
Xxxxxxx xxxxxxx - xxxxxxx, xxxxxxxxxxx potřeby, xxxxxxxxxx, … xxx 50 000/rok |
|
|
4 xxxxxxxxxxxxx xxxxxxxxxxxx |
13 |
20 990-26 220 Xx |
23 600 Xx |
1 132 800 Xx |
1 529 280 Kč |
200 000 |
|
1 preklinický xxxxxxxxxxx XXX |
13 |
20 990-26 220 Xx |
23 600 Xx |
283 200Xx |
382 320 Kč |
50 000 |
|
1 xxxxxxxx posuzovatel (xxxxxxxxxxxx xxxx - XXXXx) |
13 |
20 990-26 220 Xx |
23 600 Kč |
283 200 Xx |
382 320 Xx |
50 000 |
|
2 xxxxxxxxxx XXX |
13 |
20 990-26 220 Xx |
23 600 Kč |
566 400 Xx |
764 640 Xx |
100 000 |
|
1 xxxxxxxxxxx XX |
12 |
19 360-24-180 Xx |
21 770 Xx |
261 240 Xx |
352 674 Kč |
50 000 |
|
1 xxxxxxx + 3 koordinátoři xxxxxx xxxxxx |
13, 12 |
20 990-26 220 Xx19 360-24-180 Xx |
23 600 Xx21 770 Xx |
283 200 Xx261 240 Kč |
382 320 Xx352 674 Xx |
200 000 |
|
2 xxxxxxxxxxxx xxx oblast reexportu |
13 |
20 990-26 220 Xx |
23 600 Xx |
566 400 Xx |
764 640 Xx |
100 000 |
|
15 xxxxxx - xxxxxxx xxxxxxx xx xxxx xxxxxx xxx 5 000 000 Xx/xxx 2016 |
3 637 680 Kč |
4 910 868 Xx |
750 000 Xx |
|||
Xxxxxxx xxxxxxxx pracovních xxxxxx xx MZ xxxx odůvodněna xxxx.&xxxx; Xxxxxxxx se xxxxxxx x xxxxx xxxxxxxxxxx xxxxx xxxxxxxxxxxxx.
Xxxxxxxx xx xxxxxxx x rámci xxxxxxxx výdajů na xxxxx i xxxxx xxxx kapitoly Ministerstva xxxxxxxxxxxxx. Xxxxxxxxxx xxxxx x platové xxxxxxx xx xxxxxxxxx.
Xxx xxxxxxxxx xxxx agendy - xxxxx provozní xxxxxxx xx xxx 2016 x 2017 (xxxxxxxx, xxxxxxxx, aj.) - 2016 xxx 750 xxx. Kč; 2017 1,5 xxxxxxx Xx (xxxxxxxx prostor xxx xxxxxxx etických xxxxxx + jejich xxxxxx).
Xxxxxx xxxxxxx na xxxxxxxxx xxxxxxxxxxxxx xxxxxx etické xxxxxx a koordinátory xxxxxx xxxxxx - xxx 2016 cca 2 xxxxxxx; xxxxxxx xx vybavení xxxxx xxxxxx xxxxxx komise x jejich xxxxxx - xxxxxxxx xxx 3 xxxxxxx/xxx (xxx xxxxx počtu xxxxxx xxxxxx xxxxxx - xxxxx xxxxxxx) - xxxxxxx x příjmu xx xxxxxxx xxxxxx xxxxxx.
Xxxxxxx xxxxx xxxxxxx x vlastních prostředků Xxxxxx, nezíská-li xxxxxxx x XX xxxxx.
X xxxx 2016 x xxxx xx xx xxxx i xxxxxxx xx xxxxxxxxxx, xxxxxxx (x XXX či x xxxx agentury xxxx pořádaná xx xxxxxxxxxx Xxxxxxxx komise xx.) cca 2 xxxxxxx/xxx.
3.2 Xxxxxxx
3.2.1. Xxxxxxxx xxxxxxxx o klinických xxxxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx
Xxxxxxx xxxxxxx xx xxxxxxxxx xxxxxx xxxxxx xxxxxxxxxx xxxxxxxxx humánních xxxxxxxx xxxxxxxxx spočívají xxxxxxxxx x xxxxxxxx x následném fungování xxxxxxx EU x xxxxxxxx XX. Xxxxxxx xx xxxx xxxxxxxx xxxxx xxxxxxx x xxxxxxxxxx Xxxxxxxx xxxx. Xxxxxxx státy xxxxx xxxxxxxxxx xxxxxx xxxxxxxx xx xxxxxx a xxxxxxxx Evropské xxxx, xxxxxxxxxxx xxxxxxxxx zabezpečení xx xxxxxx xxxxxxxxx xxxxx, xxxxxxxxx xxxxxxxxxxxx xxxxxxxx xxxxxx, IT xxxxxxx xxx xxxxxxxxxxx xxxxxxxxx xx xxxxx Xxxxx xxxxxxxxx x xxxxxxxxxxx xxxxxxxxx zajištění xxx xxxxxxx xxxxxx xxxxxx. Xxxxxxx by xxxxx xxx x xxxxx hrazeny x xxxxxx XX xxxxx, xxxxx xx byly xxxxxxxx xxxxxxxxxx xxxxxxx, x xxxxx xxxxxx xxxxxxx xxxx. Xx xxxxxxxx systému xx xxxxxx xx samofinancováním, xxx. xxxxxxx xxxxxx xx xxxxxxxxx xxxxxxx x povolení xxxxxxxxxx xxxxxxxxx a xxxxxxx x xxxxxxxx xxxxxxxxxx xxxx x xxxxxxxxxx xxxxxxx xxx klinickými xxxxxxxxxxx xx xxxx xxxxxx xxxxxxxx xxxxxx xx xxxxxxx funkčnosti XX xxxxxxx i xxxxxxx xxxxxx xxxxxx.
X xxxxxxxxxxx s xxxx xxxxxxxx xxxxxxx xxxxxxx, xxxx. samofinancování, xxxxxxx Xxxxxx xxxxx xxx xxxxxxxx xxxxx x xxxxxxxxxxx xxxxxxxxxx, xxx x uplynulých letech xxxx xxxxxxx xxxxxxx xx xxxxxx x xxxxxxxxx Xxxxxxxx xxxxxx xxx xxxxxxxx xxxxx, x xx xxxxxx xxxxxxxx xxxxxxxxxxxxx xx xxxxxxxxxx xxxxxxxxxxxxxx agend, xxxxxxxxx x xxxxxxxxxxx x xxxxxxxxx na xxxxxxxxxxxxx x efektivní xxxxxxxxxxxx xxxxxx komunikace xxxx xxxxxxxxx xxxxx, Xxxxxxxxx xxxxxx a xxxxxxxxxxxx subjekty, xxx xx 75 - 80 % z xxxxxxxxxxxxxxxx xxxxxx.
Xxxxx xx xxxx xxxxxx xxxxxxxxxx xxxxxxxxx x xxxxxxxxxxx x klinickým xxxxxxxxx, xxx xxxxxx systému xxxxxxxxxx xxxxxxx x xxxxxxxx xxxxxxxxx v xxxxxxx s xxxxxxxxx x sebou přinese xxxxxxx navýšení úvazků (xxxxxxxxx z důvodu xxxxxxxxx xxxxxxxx xxxx x xxxxxxxx xx xxxxxxxxxxx 65 dnů xx 21 xxx, x xx xxx xxxxxxxx xxxxxxxxxxx),&xxxx; xxxxxxx xxxx xxx xxxx. xxxxxxxx předpokládá xxxxxxx xxxxxxxxxx xxxxxxxxxxxxxx xxxxxxx (xxx xxxxx xxxxxxxx), xxxxx xxxxxxxxxxxxxxx x xxxxx jeho prostřednictvím xxxx možné xxxxxxxxxx xxxxxxx x xxxxxxxx xxxxxxxxx a Xxxxxx xxxxx xxx xxxxxxxx xxxxx xxxx musí xxxxxxxx (xxxxxx) systém, xxxxxx xx xx xxxxxxxxxx xxxxxxxxxxxxxx portálu xxxxxxx. Zřízení xxxxxxxx xxxxxxx vyžaduje xx xxxxxx Xxxxxxxx ústavu xxx xxxxxxxx xxxxx xxxxxxx investici, a xx nejen xx xxxxxxx, xxx i xxxxxxxx provoz, xxxxxx xxx., xxxx xxxxxxxxx xxxx xxxxxxx xxxxx xxxxxxxxxxx, ale xxxx xxx xxxxxxxx xxxxxxxxx. Xxxxxxxx x xxxx, xx xxxxxxxxx evropského xxxxxxx xx předpokládána xxxxxxxxx, pak Xxxxxx xxxxx xxx xxxxxxxx xxxxx xxxx možnost x xxx xxxx xxxxxxxxxx, že se xx xxxxxxxxxx xxxxxxx xxxxxxxxx a žádosti xxxx xxxxxxxx x xxxxxxxx podobě xxxx xxxxxxx, xxxxx xx xx xxxxxxxxx kompletní xxxxxxxx Xxxxxxxx xxxxxx xxx xxxxxxxx xxxxx, xxxx. xxxx XX, x procesu xxxxxxxxxx xxxxxxxxx.
Xxxx nejen x xxxxxxxxxxx x xxxxxxxxx xxxxxx x xxxxxxx xx xxxxx xxxxxxx xxxxxxxxxx xxxxxxx x xxxxxxxx hodnocení, ale xxxxxxxx x x xxxxxxx xx administrativní xxxxxxxxx xxxxxxxx etické xxxxxx, xxxx xxxxx Xxxxxx xxxxx xxx xxxxxxxx xxxxx xxxxx x xxxxxxxxx xxxxxxxxxxx, xxx mohl xxxxxxx xxxxxxxxxx (xxxxxxxx a xxxxxxxxxxx xxxxxxxx, xxxxxxxx xxxxxxx xxxx.), xxx xxxxxx xxxxxxxx xxxxxxxxx xx xxxxxx Státního xxxxxx xxx xxxxxxxx xxxxx.&xxxx; Xxxxxxxx xxxxxxxxxx xxxxxxxx xxx xxx xxxxxx xx xxxxxxxx x xxxxxx o xxxxxxxx xxxx xxxxxxx x xxxxxxxxxx xxxxxxx. Xxxxxxxx xx xxxxx xxxxxxx xxxxxx xxxxxxxx xx nejméně, Xxxxxx xxxxx xxx xxxxxxxx xxxxx xxxxxxxx hradit xxxx náklady x xxxxxxxxxx prostředků xxxxxxxxxx x náhrad výdajů. Xx xxxx xxxxxxxxxx, xx pokud xx xxxx xxxxxxxxxx xxxxxx x xxxxxxxxx, xxxx xxx xxxxxxxx x xxx, xx veškeré xxxxxxx xxxxx kryty x rozpočtových xxxxxx.
Xxxxxxxxx xxxxxx xxx xxxxxxxx xx portál x xxxxxxxx XX - xxx xxx těžko xxxxxxxx, x tuto xxxxxx ještě xxxx xxxx ani xxxxxxxx xxxxxxxxxxx pro portál x xxxxxxxx EU x xxxx zcela xxxxx, jakou xxxx (xxxxx xxxxx) xxxxxxxxxxx xxxxxxxxx xxxx zahrnovat. X toho xxxxxxx, xx lze xxx xxxxx xxxxxxxxx xxxxxxx xx xxxxxx jednotlivých xxxxxxxxx států - xxxxxx bude třeba xxxx databáze xxxxxxxxxx xxxxxxxxx x XX, xxxxx xxxxxxxxx xxxxxx xxx technické xxxxxxxxx x xxxxxxxx + xxxxxxxxxxx xxxxxx na xxxxx XX (zabezpečený xxxxxx xxx xxxxxxxxxx Xxxxx, etická komise, xxxxxxx, xx.) - xxx xxxxxxxxx xxxxxxx xxx 30 xxxxxxx Xx, které xxxx xxxxxx Xxxxx x xxxxxxxxx prostředků, nezíská-li xxxxxxx x XX xxxxx.
Xxxxxxxx x 32 xxxxxx xx straně Xxxxxxxx xxxxxx pro xxxxxxxx xxxxx pro xxxxxx klinického hodnocení.
Dopady xx regulované xxxxxxxx
Xxxxxx xx xxxxxxxxxx
- Portál XX x xxxxxxxx xxxxxxxxxxx dokumentace xx xxxx zadavatelům usnadnit xxxxxx xxxxx; dále xx xxxxxxxxxx, xx xx se xxxx xxxxxx xxxxxxx na XX - xx xx otázkou, xxxxxxx xxxxxxxx dává více xxxxxxxxxx xxx je xxx xxxxxxxxxx v xxxxxxxx xxxxxxxxxxx, xxxxx xxxxxxxx za činnosti xxxx xxxxxxxxx nemusí x xxxxxxxx efektu xxxxxxxx xxxxxxx.
- Xxxxxxxx xxxxx xxxxxxxx xxxxxxxxx xxx. xxxx xxxxxxxxx. Xxxxx xxxxxxxxx nedoplní xxxxxxxxxxx xxxxxxxx xxxxxxxxxxx xxx xxxxxxxxx xxxxxxxxxx, xxxx xxxxxxxx xxxxxxxxx xxxxxxxxx xxxx xxxxxxxxxx xx stažené (xxx xxxx, x xxxxx xxxxx posuzování xx xxx stane). Doplnění xxxx xxxxxxxx xxxxx 1x, což xx xxx x xxxxxx xxxx, xxx xx xxxxxxxxx xxxxxxxx xx „xxxxxxxxxx“ a dává xx možnost zadavateli xxxxxxx podruhé xx xxxxxxxx xxxxxxxxxx x xxxxxxxxxx. Xx již xxxxxx možné, xxx xxxx, xx xx xxxxxxxxxxx xxxx xxxxxxxxxxx xxx xxxx X xxxxx 1 xxxxxxx xxxx = xxxxxxx xxxx zpravodaj. Xxx xx xxxxxxxx dokumentace xx xxxxxxxx xxxxxxxx xx 12 xxxxxxxxxxxx xxx (xxxx x xxxxx max. 10, xxx může být x xxxx pracovních xxx). Xxxx může xxxxxxxxx xxxxxx více xxxx, který xx xxxxxx s ohledem xx xxxxxxx xxx (xxxxxxxx času xx xxxxxxxx xxx připomínek - xxxxx i xxxxx). Xx xxxx x xxxxx xxxx x zamítáním klinických xxxxxxxxx, jejich xxxxxxxxxxxxx x xxxxxxxxxx posuzování, xxx by jistě xxxxx x xxxxxx xxxxxxxx xxxxxxxxxx x xxxxxxxx xxxxxxx x xxxxxxxx komisí.
- Výhodou xxxx xxx xxxxxxxxxx, xxxxx xxxxxxx xxxxxxxxxxxxxx xxxxxxxx xxxxxxxxx (x XX xxx 90-95%) x mají xxxx xxxxxx v XX (xx xxxx xxx 80-85% x multicentrických XX), v xxxxxxxx xxxx xxxxxxx xxxxx xxxxxx xxxxxx, xxx xx xxxx odpadnout. Xxxxxx xx xxx xx xxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxxxxx xx. xxx xxxx XX.
- Xxxxxxxxxx xxxxxxxx xxxx xxxxxx xxxxxxxxxx jako xxxxxxxx, zjednodušení xx xxxxx x xxxxxxxxxxx xxxxxxxxxxx xxxxxxxx přípravků. Xxxxx xxxxxxxxxxx xx xxxx xxxx „xxxxx“ xx straně xxxxxxx x xxxxxx xxxxxxxxxxx xxxxxxxxxxx x xxxxxxxxx xxxxxxxxxxx - je xxxxxxx, xxxxx xxxxxxxx xx to xxxxxx x xxxxx xxxxxxx xxx.
- X ohledem xx skutečnost, že xxxxx xxxx xxx xxxxxx EU, xxx xxxxxxxx EU, xxxxx xxxxx dopady xxxxxxxxxxxxx.
Xxx xxxxxxxxx uvádíme, xxx xxxx být zadavatelem:
- Xxxxxxxxxxxxx xxxxxxxxxxx
- Poskytovatelé xxxxxxxxxxx xxxxxx (xxxxxx x xxxxxxxxxxxxxx)
- Vysoké xxxxx
- Xxxxxxx xxxxxxxxxxx
XXX (XxxxxxxxXxxxxxxxXxxxxxxxxxxx) –společnosti, xxxxx x oblasti xxxxxxxxxx xxxxxxxxx xxx xxxxxxxxxx xxxxxxxxx x pozici xxxxxxxx xx SÚKL, xxxxxxxx xxxxxxxx, xxxxx xxxxxxxxx xxxxxxx x xxxxx klinického xxxxxxxxx x xx xxxxxxxxxxxx, xxxxxxxxxx xxxxxxxxxx xxxxxxxxx, xxxxxxx x farmakovigilanční xxxxxxx (xxxxxx na xxxxxxx mezi zadavatelem x CRO; xxxxxxxxx xxxxxx xxxxxx xxxxxxxx, xxxxx xxx xxxx XXX dělá x xxxxxx xxx i xxxxxxxxxx)
- Xxx xxxxxxxx xxxxx žádosti x xxxxxxxx klinického xxxxxxxxx xxxxxxxxxxx xxxxxxxx xxxx xxxxxxxx členským xxxxxx xxxxxxxxxxxxxxx xxxxxxx XX. Xx pravděpodobné, že xxx xxxx I (xxxx I xxxxxxxxxxx) xxxx xxxxxxxxxx zadavatel xxx xxxxxxx xxxxxxx xxxxx xxx; co xx týká xxxx XX (xxxxx XX xxxxxxxxxxx, xxxxx xx xxxxxxxx xxxxx ke xxxxxxxxxxx členskému xxxxx, xxxxx není dořešeno, xxxx-xx moci xxxxxxxxx x xxxxxx s xxxxx xxxxxxxx xxxxxx xxxx „xxxxxxxxx xxxxx“ xxx xxx xxxx X, x xxx xxxxxxx xx to xxx byly xxxx XXX.
- Xx xx xxxx jejich další xxxxxxxx - monitoring, xxxxxxxxx míst klinického xxxxxxxxx, xxxxxxxxxxxx…. Xx xx xxxxx být xxxxxx, xxxx xxxxxxxx
Xxxxx xx xxxx míst xxxxxxxxxx hodnocení
- Nově xxxxxxxxx xxxxxxxxxxx správné xxxxxxxx praxe pro xxxxxxxxxx provádějící klinická xxxxxxxxx xxxxxxxxxxxxxxx (xxxx xxxxxxxxxxx xx xxxxxxxx xxx dnes, xxxxxxx xxxx. xxxxxxxxxxx xx xxxx); xxxxxxxx hodnocení xxxx X (1.xxxxxx xxxxxxx) - nově; xxxxxxx xxxxx xxxxxxxxxx xxxxxxxxx xxxxx požádat x vydání xxxxxxxxxxx, xxx xxxx to xxxxxx xxxxxxx xxxxxxxxx; xxxxx xx xxxxxxxxx xxxxxxx xxxxxxxxxx
- Klinická xxxxxxxxx xxxxxxxx xxxxxxxxx xxxx xxxxxxxxx x xxxxxxxxxxxxx xxxxxxxxxxxxx zdravotních xxxxxx
- Xxxxxxxx xx xxxxx xxxxx nebude xxx xxxxx dopad
- Xxxxxxx nákladů za xxxxxxxxx služby - xxxxxxxx xxxxxx, xxxxxx xx xxx xxxxxxxxx xxxxxxxxx
Xxxxx xx xxxx xxxxxxxxxxxx
- Činnost xxxxxxxxxxxx x xxxxxxx klinických xxxxxxxxx nedozná xxxx, xxxxxxxx xxxxxxxx by xxxxxx xxx xxxxx xx xxxx oblast
- Xxxxxx x xxxxxxx xxxxxxxxxx xxxxxxxxx - xxx v současné xxxx xxxxx dle XXX (ICH X6 - GCP = XxxxXxxxxxxxXxxxxxxx), zkoušející xx xxxx podávat zprávy x xxxxxxx v xxxxxx místě xxxxxxxxxx xxxxxxxxx xxxxxx komisi, xxxxx xxxxxxxx xxxxxxxxx xxxxxxxxx
- Finanční xxxxxx xx xxxxxxxxx xxxxxxxxxx xxxxxxxxx - ¨náklady xxxxxx xxxxxxxxx - xxxxxxxx by neměla xxx vliv xx xxxx xx xxxxxx
Xxxxxx xx pacientské xxxxxxxxxx
- xxxxxxx xxxxxx xx xxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxx. X xxxxxxxx xxxx xx xxxxxxxxxx xxxxxxxxxx XXXX x xxxx xxxxxxx (xxxxxxxxx x xxxxxxxxxx xxxxxxxxxxx, xxxxxxxxxxxx a xxxxxxxxxx účasti x xxxxxxxxx xxxxxxxxx, xxxxxxxxx xxxxx xxxxxxxxxxxxxx). Xxxx xxxxxxxxxx XXXX xxxxxxxxxxx x xxxxxx. Snahou xxxx , xxx xx xxxxxxxxxx xxxxxxxxxx xxxxxxxx xx xxxxxxxx xxxxxxxx xxxxxx.
- xxxxxxxx xxxxxx xxx xxxxxxxx xxxxxx xxxxx xx xxxxxxxxxx organizace
Pokud se xxxx xxxxxx správy, xxxxx XXXX x Xxxxxxxxxxxx xxxxxxxxxxxxx, xxxxxxxx xxxxxxxxxxx i xxxxxxx
XXXX (Xxxxxx úřad pro xxxxxxxx xxxxxxxxxx)
- Xxxxxxxxxx xxxxxxx x možnost xxxxxxx xxxxxxxxxxxxxxxx radiofarmaka x XX - xxxx současný xxxx
XXX
- Xxxxxxxxxx žádostí x xxxxxxx xxxxxxx xxxxxxxxxxx xxxxxxxx přípravky s xxxxxxx XXX v XX - xxxx xxxxxxxx xxxx
XXXX
Xxxxxxxxxx xxxxxxx x xxxxxxx xxxxxxx xxxxxxxxxxx léčivého přípravky x embryonálními xxxxxxxx xxxxxxx x XX - xxxx činnost xxx xxxxxx xxxxxxx xx xxxxxxxx xxxxxxxxxx, xxxxx xxxxxx žádáno; XXXX xxxxxx xxxxxxx x lidskými xxxxxxxxxxxxx xxxxxxx již xx, xxxxxxx nebyla xxxxxx x xxxxxx xx xxxxxx lidských subjektů, xx xxxxxx xxxxxxxxxx xx bylo xxxxxxxx (xxx xxxxxx o xxxxxxxxxxxxx xx.) x xxxxxxxxxxxx zdravotnictví
3.2.2. Opatření xxxxxxxxx x omezení xxxxxxxxx xxxxxxxx přípravků
Pokud xxx x navrhovanou xxxxxx úpravu xxxxxxxxxxx x xxxxxxxx x xxxxxxx reexportu xxxxxxxx xxxxxxxxx, xxxxxxxxxxx se xxxxx xxxxxxx xxxxxxxxx xx xxxxxxxxx režimu xxxxxxxxx x xxxxxxxxxxxxx xxxx, xxx jsou xxxxxxxxx xxxxxxx xxxxxxxx x Xxxxx republice, x xxxx s xxxxxxxxxx xxxxxxxx x xxxx případech, kdy xxxxxxxxxx léčivých přípravků xx xxxxxxxxx xxxxxxx xx jejím území xxxxxx nedostatek. Xxxx xxxxxxx xxxxx xxxxxx x xxxxx xxxxxxxxxx xxxxxxx financování xxxxxxxx Xxxxxxxx xxxxxx pro xxxxxxxx léčiv a Xxxxxxxxxxxx zdravotnictví.
Navýšení o 4 pracovní úvazky xxxx spočívat xx 2 xxxxxxxxxx xxxxxxxx xx Xxxxxxx ústavu xxx xxxxxxxx xxxxx (xxxxxx xxxxxxxxxxxx odůvodněných xxxxxxx předávaných Ministerstvu), x xx 2 xxxxxxxxxx úvazcích na Xxxxxxxxxxxx xxxxxxxxxxxxx. Činnost xx Ministerstvu xxxxxxxxxxxxx xxxx xxxxxxxx xx xxxxxxxxx xxxxxxxxx xxxxxx xxxxx agendy odborným xxxxxxxxxx právnického xxxxxxxx x xxxxxxx xxxxxxx xxxxx xxxxxx xxxxxxxx xxxxxxxxxx xxxxxxxxxxxxxxx či xxxxxxxxxx vzdělání.
Pokud se xxxx xxxxxx xx xxxxxxxxxx xxxxxxxx:
Xxxxxx xx xxxxxxxx xxxxxxxxxx x xxxxxxxxxx
Xxx může xxx xxxxxxxxx - xxxxxxx xxxx xxxxxxxxx xxxxx, xxxxx xxxxxxxx xxxxxxxxxx §26 xxxxxxxx 4 xxxxxx x xxxxxxxx
- Xxxxxxxxxx xxxxxx úprava xxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxx x §33 xxxxxx x léčivech poskytovat xxxxxxxxx x xxxxxxxx xxxxxxxxxxx dodaných na xxx x České xxxxxxxxx. Nově xxxx xxxxxxx xxxxxxxxxx tyto xxxxx v xxxxxxxxxxxx xxxxxxxxxxx x xxxxxxxxxxxx xxxxxx, xxx xxxx xxxx xxxx xxxxxxxxxx x ve xxxxxxxxxxxxx xxxxxx xxxxxxxx Xxxxxx xxxx xxxxxxxxxx xxxxx, xxxxx poskytuje informaci x množství xxxxxxxx xxxxxxxxx, jeho xxxxxxxxx xxxxx, dodané xxxxxxxxx xx trh x Xxxxx republice.
- Tyto xxxxx xxx budou xxxxxxx Xxxxxx jak xxxxx xx zdrojů xxxxxxxxx xxx posuzování xxxxx zásob na xxxx x České xxxxxxxxx, ve xxxxxx x xxxxxxxxx xxxxxxxxxxxxxxx xxxxxx xxxxxxxx xxxxxxxxx x x posouzení xxxxxxx xxxxxx distribuce xxxxxxxx léčivého xxxxxxxxx xx zahraničí, xxxxx xx xxx xxxxxx xx xxxxxxx xxxxx §77c xxxxx x xxxxxxxx.
- Xxxxxx xxxxxx xxx xxxxxxx xxxxx xxxxxxx x plnění xxxxxxxxxx xxxxxxxx xxxxxxx xxxxxxxx xxxxxxxxx x xxxxxxxx xxxxxxxxxxx xxx xxxxxxx xxxxxxxx x XX.
Xxxxxx xx xxxxxxxxxxxx
Xxx xxxx xxx xxxxxxxxxxxxx:
- Xxxxxxx xxxxxxxx x xxxxxxxxxx xxxxx xxxxxx Ústavem xxxx xxxxxxxxxx regulační xxxxxxxxx x xxxxxxxx xxxxx XX
- Xxxxxxxxxxxx budou, x xxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxx xx xxxxxxx xxxxx §77c xxxxxx o xxxxxxxx, xxxxxxxxxx xxxxxxxxxx xx xxxxxxxxx xxxxxxxxxxxxxxx elektronického xxxxxxxxx. Pokud xxxxxx xx 15 xxx xx jeho zaslání xxxxxx XXX xxxxx §77d xxxx xxxx xxxxxxxx xxxxxxx.
- Většina xxxxxxxxxxxx dodávajících xxxxxx xxxxxxxxx xxxxxx xxxxxxxx xxxxxxx xx xxx xxxxxxxx touto xxxxxxx, xxx xxxxxxx k xxxxxxx administrativní xxxxxx xxxxxxx xx zásobováním xxxxxxx.
- Xxxx distributorů, xxxxx nedodává, xxxxxxxx x xxxxxxxxxx xxxxxxx, xx lékáren x xxxxxxxxx se na xxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxx xx xxx x Xxxxx xxxxxxxxx xx xxxxxxxxx, xxx xxxx muset xxxxxxx xxxxx xxxxxxxx xxxxxxxxxxxxx xxxxxxxx. Přičemž xxx xxxxx a x x to xxxxx xxxx xxxx xxxxxxxx xxxxx pro distribuci xxxxxxxx přípravků xxxxxxxxxxx x xxxxx xxxxxxxxx, xxxxxxx do lékáren.
Dopady xx „lékárny“ - xx xxxxxxxxxxxxx xxxxxxxxxxx xxxxxx xxxxxxxxxx xxxx
Xxx xxxx xxx „xxxxxxxx“: Xxxxxxx xxxxxxxxx k xxxxxxxxxxx xxxxxxxxxxxx xxxxxx xxxxx xxxxxx č. 372/2011 Sb., xxxxxx o zdravotních xxxxxxxx
- Xxxxxxxxxx právní xxxxxx nepřinese xxxxxxxx xxxxx xxxx xxxxxxx xxxxxxxxxx, xxxxxx xxxxx xxxxxxxxxxxx nárůst xxxxxxxxxxxxxxx xxx jiné zátěže.
- Xxxx by xxxxxxxx xxxxx dostupnost zejména xxxxxxxxxxxxxxx xxxxxxxx přípravků.
Dopady xx xxxxxxxx
- Pro xxxxxxxx xxxx přínosem xxxxxxxxx lepší x xxxxxxx xxxxxxxxxxx léčivých xxxxxxxxx xxx xxxxxxx, xxx xxxxxx xxxxxxxxxx xxxxxxx rovněž xxxxxxxxxxx xxxxxxxxx xxxx, bez xxxxxxxx xxxxxx náhradní xxxxx.
3.3 Přínosy
3.3.1.Adaptace nařízení x xxxxxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx
Xxxxxxxxxxxx xxxxxxx podávání x xxxxxxxxxx xxxxxxx x xxxxxxxx xxxxxxxxxx xxxxxxxxx x založení xxxxxxxxx xxxxxxx XX x xxxxxxxx XX xx xxxx celkově přinést xxxxxxx xxxxxxx xxxxxxxxxx x xxxxxxxx vyšší xxxx xxxxxxxxxxxx. Zadavatel xxxx xxx k xxxxxxxxx jednotnou xxxxxx xxx xxxxxxx xxxxxxx xxxxx, xx xxxxxxx xx xxxx xxxxxxxx xxxxxxxxx xxxxxxxx, a xxxxxx proces vyřizování xxxxxxx xx měl xxx xxxxxxxxx x xxxxxxxxx. Xx xx xxxx vést k xxxx zvýšení počtu xxxxxxxxxx xxxxxxxxx xx xxxxx Xxxxxxxx xxxx x xxx i x Xxxxx republice.
V xxxxxxxx výše xxxxxxxxx xx mělo být xxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxx a xxxxxxxxxxxx xxxxx xxx xxxxxxxx, xxxxxxx xxxxxxxxxx xxxxxx xxx poskytovatele xxxxxxxxxxx xxxxxx, xxx by xxxxxxxx xxxxxxxxx probíhala, xxxxxxx prestiže xxxxxx xxxxxx a odborných xxxxxxxxx v xxxxxxxxxxxx xxxxxxx.
Xxxx nařízení x xxxxx xxxxxx je xxxxxxxxx xxxxxxxxxxx x xxxxx Xxxxxxxx xxxx, xxxxx na xxxx xxxxxxxx přípravků xxxxxxx xxx xxxxxxx xxxx. Xxxxxxx systém xxx xxx zaveden x xxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx x xxxxxxxx x xxxx, xx xx xxxxxxxx x xxxxxxxxxxx v xxxxx xxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxxx xx xx xxxxxx úrovni, xxx xxxxx xxxxx xxxxxx xxx oblast xxxxxxxxxx xxxxxxxxx xxxxxxxxxx x xxxxxxx xx xxxx xxxxxxxxx.
Xxxxxxxx xxxxxx režimu xxxxxxxxx xxxxxxxxxx hodnocení xxxxxxx xxxxx omezení xxxxxxxxxx xxxxx, a xx x xxxx xxxxxx, xx xxxxxxxxxx xxxxxxxxxxxx etických komisí xxxxx xxxxxxxxx xxxxxx xxxxxx xxxxx poskytovateli xxxxxxxxxxx xxxxxx, v xxxxx xx xxxxxxxx xxxxxxxxx xx provádět x v xxxx xx x xxxxxxx, xxxxxxxxxx představuje xxxxxx xxxxxxx xxxxxxxxx xxxxx xxxxxxxx komisí x x xxx xxxxxxxxxxx xxxxx xxxxxxxx xxxxxx, xxx xxxx představuje x xxxxxx novely xxxxxx xxxxxxxx xxxxxx xxxxxx komise x xxxxxx skupin, xxxxx xxxxxxx jménem etické xxxxxx xxxxxxxxxx, xxxx xxxxx etické xxxxxx, x xx do xxxxxxxxxxxx xxxxxx, xx xxxxx navrhované právní xxxxxx xxxxxxxx x xxxxxxxxx xxxxx xxxxxxx xxxxxxxxxxxxx.
3.3.2. Opatření xxxxxxxxx x xxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx
Xxxxxxxx xxxxxxxxxxxxx xxxxxx xxxxxx xx xxxxx xxxxxxxxx xxxxxxxx xxxxxxxxxxx k omezení xxxxxxxxx léčivých xxxxxxxxx xx xxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx xxx xxxxxxxx x České xxxxxxxxx, x tím xxxxxxxx xxxxxxxx xxxxxxx xxxxxx xxxxxx.
Xxxxxxxx vícestupňového xxxxxxx xxxxxxxx vývozu xxxxxxxx xxxxxxxxx xx xxxxxxxx xx xxxxxxxxxxxxx x xxxxxxxxxxxxx xxxxx x xxxxxxxxxx x xxxxxxxx xxxxxxxx přípravků, xxxxx se xxxxxxxx xx více subjektů, x xx xxx xx těch, xxxxx xxxxxx xxxxxxxxx jiným xxxxxx dodávají, tak x od xxxx, xxxxx xx xx xxxxxx xxxx xxxxxxxxx, x jednomu xxxxx xxxxxxxx povahy by xxx xxx xxxxxxxxx xxxxxxxxx xxxx vstupní xxxxxx x xxxxxx. Xxx xxx o xxxxx xxxxxxx xxxxxxxx xxxxxxxx, xxxxx xxxx x xxxx xxxxxxxx xxxxxxxxxxxx xxxxxxx jako xx tomu x xxxxxxx xxxxxxxxxx, xxx xxxxx „xx dáti“ xxxxxxxx xxxx „xxx“ . Xxxxx o xxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx je xxx xxxxx xxxxxxxxx xx xxxxxxxxx x xxxxxxx xxxxxx falšování je xxxxx jen teoretická. X této xxxxxxxxxxx xx třeba xxxxxxxxxxx, xx xxxxx xxxxxx xxxxxxxx xxxxxx závažné xxxxxxx, xxx xx xxxxxx přípravky byly xx xxxxxxxxxxx fakticky xxxxxxxx xxxx Xxxxxx xxxxxxxxx, a xxxxxx xx jejich xxxxxxx xxxx xxxxxxxx xxxxxxxxxx xx xxxxx Xxxxx xxxxxxxxx. Xxxxxxx takového xxxxxxxxxx xxxxxxx je xxxxxxx xxxxxx a xxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxxx xxxxx x distribuci x xxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxx xxxxxxx xx xxxxx vyloučena. Xxxxxxxx xxxxxxxx xxxxxx xxxxxxxx xxxxxxxxx xxxx xxxxxxxxx xxxxxx korupčních xxxxx.
3.4 Xxxxxxxxxxx xxxxxxx x xxxxxxx xxxxxxx
3.4.1. Xxxxxxxx xxxxxxxx x xxxxxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx
Xxxxxxxxxxx xxxxxxx x přínosů xxxx xxxxxxxxx x xxxxx xxxxxxxxxxxx xxxxxxx řešení, xxx xx uvedeno xxxx.
3.4.2. Xxxxxxxx xxxxxxxxx x omezení reexportu xxxxxxxx xxxxxxxxx
Xxxxxxxxxxx xxxxxxx x xxxxxxx xxxx xxxxxxxxx x xxxxx xxxxxxxxxxxx xxxxxxx řešení, xxx xx xxxxxxx xxxx.
3.4.3. Xxxxxxxx xxxxxxxx xx xxxxxx x xxxxxxx xxxxxx xxx xxxxxxx xxxxxx xxxxxxxxx
Xxxxxxx xxxxxxxxx je xxxxxxxx xxxxxxx xxxxx zákona x xxxxxxxx xxx, xxx byla náležitým xxxxxxxx xxxxxxxxx adaptace xxxxxxxx Komise x xxxxxxxxx pravomoci (XX) č. 1252/2014.
3.4.4. Xxxxxxxxxx Státního xxxxxx pro xxxxxxxx xxxxx x Generálního xxxxxxxxxxx xxx
Xxxxxxxx 1 xxxxxxxxxxx xx xxxxx xxxxxx o xxxxxxxx xx xx xxxxxx, xx xxxxxxx xxxxxx xxxxxx xxxxxxxx, x xxxxxx xx xxxxxxxxx xxx platným xxxxxxx xxxxx, a xx xxxxxxxxx xxxxxxxxxxx §8 xxxxxx x. 226/2013 Xx.
Xxxxxxxx 2 xxxxxxxxxxx x přijetí doprovodné xxxxxx xxxxxx o Xxxxx xxxxxx Xxxxx xxxxxxxxx x tomuto xxxxxx xxxxxx xxxxxx x xxxxxxxx xx xxxxxxxx xxxx rychlé xxxxxx, avšak xxxxxx xx xxxxxxx do xxxxxxxxxx xxxxxx resortu, x xxxxx xx xxxx xxxxxxx možnosti xxxx změny, xxxxx xx xx přijetí xxxxxx xxxxx xxxxx xxxxxxxxxx.
Xxxxxxxx 3 xxxxxxxxxxx xx xxxxxxx samostatné xxxxxxxxxx xxxxxx x Xxxxx xxxxxx České xxxxxxxxx xx ten xxxxxxx nedostatek, xx xx xxxxxxxx na xxxxxxx xxxxxxxxxxx xxxxxxxxxx xxxxxxx novelizace zákona č. 17/2012 Sb. xxx xxxxxxxx xxxxxxxxx xxxxxxxxxx obou xxxxxx xxxxxx xxxxxx xx xxxxx xxxxxxx xxxx, xxxxxxx xxxx x xxxxxx by xxx x České xxxxxxxxx xxxxxx dostatečně xxxxxx.
3.4.5. Xxxxxxxxxxx při xxxxxxxxx xxxxxxxx a xxxxxx xxxxxxxxx zajištění x xxxxxxx xxxxxxxx xxxxxxxxx
Xxxxxxxx 1 xxxx xxxxxxx x xxxxxx xxxxxxxxx přínosem. Xxxxxx xxxx xxxxxxx xx xxxx xx následek xxxxxxxxxxx xxx xxxxx xxxxxxxxxxxx xxxxxxxxxx xxxxxx xxxxxx, která narušuje xxxxxx xxxxxxx xxxxxxxxx xx xxxxxx xxxxxxxxxxxxxx xxxxxxxx, xxx xxxxx xx xxxxxxxx xxxxxx xxxxxx xxxxxx xxxxxxxx xxxxx matoucí a xxxx ke xxxxxxxxxxx x xxxxxxx xxxxxxxxx xxxxxxxx a k xxxxxxx xxxxxxx při xxxxxxxxxxx xxxxxxxxxx. Xxxxxxxxx xxxxxxxx xx xxxxxxxx xxxxxx xxxxxxx léčivých xxxxxxxxx xxxx léčivé xxxxxxxxx, xx xxxxxxx xxxxxxxxx xxxxxxxxxxx xxxxx, xxxxxxxxxxx xxxxxxxx rizika xxx možné xxxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx, x xxxxxx xxxxxxxxx xxxxxxxxxx dopadem xx xxxxxx zdravotní xxxx. Xxxxx xxxxxxx takových xxxxxxxx xxxxxxxxx xxxxxxxxxxx xxx xxxxx, kterým xxxx xxxxxxx, xxxxxx xxxxxxxxxx xxxxx, xxxxx xxxx posílit xxxxx xxxxxxxxxxx xxxxxxx pokračování x xxxxxxxxxxx xxxxxxxx.
Xxxxxxxx 2 xx xxxxxxxx xxxxxxxxx úpravu xxxxxxxxxxx xxxxxxxxxx xxx xxxxxxxxx xxxxxxxxx xxxxxxxx a xxxxxxxxx zásadních právních xxxxxxxxx zajištění x xxxxxxx xxxxxxxx xxxxxxxxx xxx, xxx xxxx xxxxxxxxxx x pro xxxxxx xxxxxxx, kdy xx zjištěno, xx x xxxx xxxxxxxxx xxxxx, xxxxx x xxxx nejsou xxxxx xxxxxx xxxxxxxxx. Tato xxxxxxxx xxxxxxxxxxx účinnější xxxxxx xxxxxxx pacientů x xxxx společnosti xxxx xxxxxx xxxxx xxxxxxxx přípravky, xxxxxxx xxxxxx, účinnost x xxxxxxxxxx nebyla xxxxxxxxx x xxxxxxx xxxxxxxxx xxxxx xxxxxx x xxxxxxxxxxx xxx xxxxx xxxxxx riziko xxx xxxxxx xxxxxxxx a xxxxxxxx xxxx xxxxxxx xxx systém xxxxxxxxx xxxxxxxxxxx xxxxxxxxx, x xxxxxxxxx xxxxxxxxx x xxxxxxxxxx xxxxxxx xx xxxxxx pacientů.
4. Xxxxx xxxxxx
4.1 Xxxxxxxxx xxxxxx xxxxxxx x xxxxx xxxxxxxxxxxxxx xxxxxx
4.1.1. Xxxxxxxx xxxxxxxx pro xxxxxxxx xxxxxxxxx humánních léčivých xxxxxxxxx
Xxxxxxxxx xxxxxxxx a xxxxxxxxxxx xxxxxxxxxxxx xxxxxxx xxxx xxxxxxxxx, xxx xx xxxxxxx xxxx.
4.1.2. Xxxxxxxx směřující x xxxxxxx reexportu xxxxxxxx xxxxxxxxx
Xxxxxxxxx xxxxxxxx x xxxxxxxxxxx jednotlivých xxxxxxx xxxx xxxxxxxxx, jak xx xxxxxxx výše.
4.1.3. Xxxxxxxx xxxxxxxx xx xxxxxx k léčivým xxxxxx xxx xxxxxxx xxxxxx xxxxxxxxx
Xxxxxxxxxxx xxxxxxxxx xx varianta xxxxxxx xxxxx zákona o xxxxxxxx xxx, xxx xxxx náležitým způsobem xxxxxxxxx xxxxxxxx xxxxxxxx Xxxxxx v xxxxxxxxx xxxxxxxxx (XX) č. 1252/2014.
4.1.4. Xxxxxxxxxx Xxxxxxxx xxxxxx xxx xxxxxxxx léčiv x Xxxxxxxxxxx xxxxxxxxxxx xxx
Xxxxxxxxxxx xxxxxxxxx je xxxxxxxx 1 spočívají xx xxxxx xxxxxx x xxxxxxxx. Jde x xxxxxxxxxxxx, x xxxxxx xxxxxxxxxxxxxxxx xxxxxx xxxxxxxx, xxxx xxxxx xx xxx jejím xxxxxxxxxxx xxxxxxx xxxxxx xxx xxxxxxxxx platným xxxxxxx xxxxx, xxxxx x xxxxx xxxxxx xxxxxx a xxxxxxxx xx. Xxxx xxxxxxxx xxxxxx xxxxxxxxxxx kontrolní xxxxxxxxxx obou xxxxxx xxxxxx správy x xxxxxxxx tak xxxxxxx xxxxxxx xxxx Xxxxx xxxxxxxxx x xxxxxxxx xxxx XX xxxx xxxxxxx xxxxx, xxxxx xxxxxxxxxxxx xxxx xxxxxxxx xxxxxxx xxxxxxxxxx v xxxxxx EU.
4.1.5. Prokazování xxx xxxxxxxxx činnosti x xxxxxx instituty xxxxxxxxx a xxxxxxx xxxxxxxx xxxxxxxxx
Xxxxxxxxxxx xxxxxxxxx xx varianta 2, xxxxxx xx xxxx xxx dosaženo xxxxxxx xxxxxxxxx xxxxxx prokazování xxxxxxxxxx při xxxxxxxxx xxxxxxxxx činnosti x xxxxxx by xx xxxx zpřesnit právní xxxxxxxxx xxxxxxxxx x xxxxxxx léčivých přípravků xxx, aby xxxx xxxxxxxxxx i xxx xxxxxx xxxxxxx, kdy xx zjištěno, že x nimi xxxxxxxxx xxxxx, které x xxxx xxxxxx xxxxx xxxxxx xxxxxxxxx. Nadále xx tak již xxxxxxxxxxxxx pro xxxxx xxxxxxxxxxxx xxxxxxxxxx xxxxxx xxxxxx, která xx xx xxxxxx xx xxxxxxxxxxxxx subjektům xxxxx xxxxxxx a xxxx xx xxxxxx a xxxxxxxxxxx x xxxxxxx xxxxxxxxx činnosti a xxxxxxxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxx xxxxxxxxxxx xxxxxxx.
Xxxxxxxxx xxxxxxxx xx následně xxxxxx xxxxxxx xxxxxxxx xxxxxxxxx xxxx xxxxxx xxxxxxxxx, xx xxxxxxx xxxxxxxxx xxxxxxxxxxx xxxxx, xxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxx xxx možné xxxxxxx x xxxxxx xxxxxxxx. Navíc xxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxxx xxx osoby, xxxxxx xxxx xxxxxxx, xxxxxx xxxxxxxxxx xxxxx, xxxxx xxxx posílit xxxxx xxxxxxxxxxx xxxxxxx xxxxxxxxxxx x xxxxxxxxxxx xxxxxxxx.
5. Xxxxxxxxxxxx doporučené xxxxxxxx x vynucování
Orgánem xxxxxxxxxx xx implementaci xxxxxxx varianty xxxxxx, xxxxx jde x xxxxxxxx xxxxxxxx x xxxxxxxxxx xxxxxxxxxxx humánních xxxxxxxx přípravků, bude xxxxxxxxx Státní xxxxx xxx kontrolu xxxxx, xxxxx je xxx xxxxx xxxxxxxxxxx xxxxx xxxxxx o léčivech xxxxxxxxxxxxxxx odborným správním xxxxxx xxx xxxxxx xxxxxxxx xxxxx, včetně xxxxxxxxxx a xxxxxxx xxx prováděním klinických xxxxxxxxx xxxxxxxx xxxxxxxxx. Xxxxxx xxxxx xxx xxxxxxxx léčiv xx xxxxxxx xxxx xxxx xxxxxxx xxxxxxxxxx x xxxxxxx jakosti, účinnosti x bezpečnosti xxxxx, x xx x xx xxxxxx x xxxxxxxxxx xxxxxxx členských xxxxx i Xxxxxxxx xxxx.
Xxxxxx odpovědnými xx xxxxxxxxxxxx zvolené varianty xxxxxx, xxxxx xxx x opatření xxxxxxxxx x xxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx, xxxxx xxxxxxxxx Xxxxxxxxxxxx xxxxxxxxxxxxx x Státní xxxxx xxx kontrolu xxxxx. Xxxxxxxxxx varianta xxxx xxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxxxx seznamu xxxxxxxx xxxxxxxxx, xxxxx xxxx xxxxxxxx jejich xxxxxxxxxxxxx, x xxxx xxx xxxxxxx stanovených xxxxxxxx xxxxxxxxxxxxxxx xxxxxxx xxxxxxxx xxxxxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx uvedených xx xxxxx xxxxxxx xxxx xxxxx Xxxxx xxxxxxxxx. Xxxxxxxxxxxx xxxxxxxxxxx fungování xxxxxx xxxxxxx xx xxxxxxx xxxxxxxxx xxxxxxxx x aktuálních dat x xxxxxx, xxxxxx xxxxxxxx zpracování x xxxxxxxxxxxxx, následně x xxxxxxxxxx xx xxxxxxx xxxxxxxxx xxxxxxxxxxxxx operativní xxxxxx xxxxxxxxxxx xxxxxxxx. Xxxxxxxxxx xxxxxxxxxx xxxxxxxxx x xxxxxxxx stanovení xxxxxx xx xxxxxxxx xxxxxxxxxxx xxxxxxxxxx.
6. Xxxxxxx xxxxxxxxx regulace
Přezkum xxxxxxxxx xxxxxx zákona x xxxxxxxx xxxxx x xxxxx xxxxxxxx Xxxxxxxxxxxx xxxxxxxxxxxxx x Xxxxxx xxxxx xxx kontrolu xxxxx xx xxxxxxxxxx x dotčenými subjekty, x to x xxxxxxxx účinnosti xxxx xxxxxx xxxxxx x xxxxxxx z xxxxxxxx xxxxxxxxxx xxxx sledovaných xxxxx právní úpravou. Xxxxx impulsy xx xxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx xxx xxxxxxxx xx Xxxxxx, které xx ustanovením čl. 97 xxxxxxxx x. 536/2014 xxxxxx přezkum xxxxxxxxxxx xxxxxx xxxxxxxx.
Xxxxxxxxxxx xx 2 xxxxxx xx xxxxxxxxx právní úpravy xxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxx xxx pacienty.
Pro xxxxxxxxx naprosto xxxxxxxx xxx xxx xxxxxx xxxxxxx xxxxxxxx xxxx xxxxx x xxxxxxx, xxx by bylo xxxxxxxxxx k xxxxxxx xxxxxxxx k xxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx, xxxxxxx xxxxxxxxxxxxx. Xxxxxxx xxxx sledováno, kolik xxxxxx xxxxxxxx přípravků xxxxxxxxx opatření xxxxxxxx, x xxxx konkrétní xxxxx XXX celkem xxx x nich xxxxxxx. Xxxxxx bude x xxxxxx xxxxxxx xxxxxxxxxxx, zda x xx xxxx xxxx xxxxxxx xxxxxxxx xxxxxxxx xxxxxxxx xxxxxxx xxxxxxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx xxx xxxxxxxx x Xxxxx xxxxxxxxx a xxxx xxxxxxxx stav xxxxxxxxxxx xxxx xxxxxxxx xxxxxxxx a xx xxxx xxxxxxx xx xxxxxxxxxxx xxxxxxxxxxxx časových xxxxx x xxxx xxxxxx tohoto xxxxxxxx.
Xxxxx xxxxxxxxxx vyhodnocení účinnosti xxxxxxx přijatého xxxxxxxx xxx pacienty xxxxx xxxxxxxxxxx xxxx xxxxxxxx xxx xxxxxxxxxxxx xxxxxxxx xxxxxxxxx, xxxxxxx xxxxxx xx xxxxxxxxx xxxxxxxxx xxxx xxxxxxxxx finančního xxxxxxxxxx xxxxxx xxxxxxx, xxxxx by x xxxxxxx xxxxxxxxx xxxxxxxx xxxx x dosavadním xxxxxxx xxxxxx do xxxxxxxxx, a xxxxxxxxxx xxxxxxxxxx xxxxxx xxxxxxx, xxxxx v xxxxxxxx xxxxxxx opatření xxxx xxxxx do xxxxxxxxx xxxxxx xx trh x Xxxxx xxxxxxxxx. Xx xxxxxxx xxxxxxxxxxx xxxxxxxxxxxx případů xxx xxxx provedeno souhrnné xxxxxxxxxxx celého xxxxxx xxxxxx xxxxxxxxx právní xxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxx přípravků.
Rovněž xxxx xxx xxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxx xxxxx xxxx seznamem xxxxxxxx xxxxxxxxx, xxxxx jsou xxxxxxxx xxxxxx xxxxxxxxxxxxx, x přijatými xxxxxxxxxx xxxxxxxxx x xxxxxxx xxxxxxxxx léčivých přípravků, xxx xxxxx xxx xx xxxxxxxx xxxxxxxxxx xxxxx xxxxxxxxxx posouzeno, xxx xxxxxxxx xxxxxxxxxxxx xxxxxx xxxxxxxx vývozu xxxxxxxx xxxxxxxxx x xxxx xxxxx xxxxxxxxxx x xx xxxx xxxxxxx xxxxxx xxxxxxxx xxxxxxxxxxx xxxxxxx x xxxxxxx potřebě xxxxxxxx xxx xxxxxxxx v Xxxxx xxxxxxxxx náležitou xxxxxxxxxx léčivých xxxxxxxxx.
7. Xxxxxxxxxx a xxxxxx xxx
Xxxxx zákona xxx x xxxxxxx přípravy xxxxxxxx xxxxxxxxxxx x xxxxxxxxx dotčenými subjekty. Xxx oblast xxxxxxxx xxxxxx x náhrady xxxx xx xxxxxxxx xxxxxxxxxx zástupci xxxxxxxx xxxxxx xxx xxxxxxxxxxxxxx xxxxxxxx hodnocení x Xxxx etických xxxxxx. Xxxxxxxxxxx x xxxxxxxxxxxxxx xxxxxxx s xxxxxxxx xxxxxxxxxx xxxx xxxxxxxx xxxxx etických komisí xxx xxxxxxxxxxxxxx xxxxxxxxx x xxxxxxxx místních xxxxxxxx xxxxxx xxxxxxxxxxx xx xxxxxxx Xxxx xxxxxxxx komisí. Informovány xxxx x xxxxxxxxxx xxxxxxxxxx x návrhem xxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxxxxx xxxxxxxxxx do xxxxxxxx xxxxxxxx komisí. Xx xxxxxx možnosti xxxxxxxxx nových xxxxxxx xxxxxxx xxxx byli xxxxxxxx xxxxxxxxxx xxxxxxxxxxxxxxx Xxxxxxxx inovativního xxxxxxxx, Xxxxxxxx xxxxxxxxxxx xxxxxxxxx, xxxxxxxx Xxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxxxx, Asociace xxxxxxxxxx xxxxx. Xxxxxxxxxxxx xxxxxxxxxxxxx tuto xxxxxx xxxxxxxxxxxx s Xxxxxxxxxxxxx xxxxxxx x Xxxxxxxxxxxxx xxxxxxxxxxxxx.
Xxxxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx k xxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx xxxx xxxxxxxxx xxxxxxxxxxxx x xxxxxxxxxxxx xxxxxxxx xxxxxxxxxx x registraci, xxxxx xxxxxxx xxxxxxxx xxx xxxxxxx xxxxx xxxxxxxx přípravků od xxxxxxx určených na xxx x Xxxxx xxxxxxxxx xx zahraničí x xxxxxx x Xxxxxxxx xxxxxxxxxxxx průmyslu.
Návrh xxxxxx xxxxxx x xxxxxxxx byl v xxxxx meziresortního připomínkového xxxxxx v xxxxxxx x xx. 8 Xxxxxxxxxxxxxx pravidel vlády xxxxxxxxx x povinnými xxxxxxxxxxxxxx xxxxx.
8. Kontakt xx zpracovatele XXX
Xxxxx x xxxxxxxx: MUDr. Xxxxx Xxxxxxx
Xxxxxx: vedoucí xxxxxxxx xxxxxxxxxx hodnocení
Útvar: Xxxxx xxxxxxxxxx, xxxxxxxx xxxxxxxxxx xxxxxxxxx XXXX
Xxxxxxx: 272 185 817; 724 917 141
x-xxxx: xxxxx.xxxxxxx@xxxx.xx
Xxxxx x xxxxxxxx: Xxx. Xxxxxxx Xxxxxxxx
Xxxxxx: xxxxxxx xxxxx xxxxxx
Xxxxx: Xxxxx xxxxxx Státního xxxxxx xxx xxxxxxxx xxxxx
Xxxxxxx: 272 185 706
x-xxxx: xxxxxxx.xxxxxxxx@xxxx.xx
X. Xxxxxxxxxx xxxxxxx xxxxxxxxxx právní xxxxxx s xxxxxxxx xxxxxxxx Xxxxx xxxxxxxxx, x mezinárodními smlouvami x x předpisy Xxxxxxxx xxxx, judikaturou xxxxxxxx orgánů Xxxxxxxx xxxx x xxxxxxxx xxxxxxxx xxxxxxxx xxxxx Xxxxxxxx unie
Navrhovaná právní xxxxxx xxxxxxxx ústavnímu xxxxxxx a právnímu xxxx České xxxxxxxxx, xxxxxxx xxxxxxxxx xxxxxx č. 1/1993 Sb., Xxxxxx Xxxxx xxxxxxxxx, xx znění xxxxxxxxxx xxxxxxxx, x xxxxxxxx xxxxxxxxxxxxx Xxxxx xxxxxxx xxxx č. 2/1993 Sb., x xxxxxxxxx Listiny xxxxxxxxxx xxxx x xxxxxx xxxx xxxxxxxx xxxxxxxxx pořádku Xxxxx xxxxxxxxx, xxxxx se xxxxxxxx k xxxxxxxxxxxxx xxxxxx xxxxxx.
Xxxxxxxxxx xxxxxx xxxxxxxx xxxxxxxx přípravků xxxx x xxxxxxx x xxxxxxxxxxxxx xxxxxxxxx, xxxxxxx je Xxxxx xxxxxxxxx xxxxxx.
Xxxxxxxxxx právní xxxxxx xx v xxxxxxx x Úmluvou x xxxxxxx lidských xxxx a základních xxxxxx. Poskytuje xxxxxx xx xxxxxxxxxxx proces x xxxxx xxxxxxxxx xxxxxxxx, neboť xxxxxxxx xxxxxxxx se xxxxxxxxxxx xx xxxxxxx xxxxxxxxxxx xxxxxxxx řádem a xxxxxxx x xxxxxxxxxxx, xxxxxxxx xxxxxxxx správních xxxxxxx xxxx xxxxx xxxxxxxxx, xxxxxxxxx xxxx x kritéria xxxxxxxxxx x xxxxxxxx rozpětí xxxx pokut.
Navrhovaná právní xxxxxx je rovněž x xxxxxxx x Xxxxxxx x lidských xxxxxxx x xxxxxxxxxxx, xxxxxxxxx xxx č. 96/2001 Sb. m. s. Xxxxx v xxxxxxx xxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx mimo xxxx xxxxxxxxxx xxxxxxxxxx čl. 3 Xxxxxx, xxxxx xxxxxxx xxxxxxx xxxxxx, xxxxxx xx zřeteli xxxxxxxxx xxxxxxx a dostupné xxxxxx, učiní xxxxxxxxxxxx xxxxxxxx, aby x xxxxx xxx xxxxxxxxxx xxxxxxxxx xxxxxx xxxxxxxxxx xxxxxxxxx péče patřičné xxxxxxx. Xxxxxxxxx xxxxxxxxx xxxx patřičné kvality xxxxxx xxxxxxxx zajištění xxxxxx xxxxxxxx v Xxxxx republice v xxxxxxx xxxxxxxx xxxxxxxxx, xxx xxxx xxxxxx xxxxxxxxxxxxx mimo Českou xxxxxxxxx xx úkor xxxxxxxxxx náležitých potřeb xxxxxxxx x Xxxxx xxxxxxxxx.
Xxxxx xxx x xxxxx xxxxxxxxx situace, xxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxx xxxxx xxx dočasně x x xxxxxxxx xxxxxxx xxxxxxxx zásobování trhu xxxxxxxx xxxxxxxxx x Xxxxx republice xxxx xxxxxx distribucí xx xxxxxxxxx, nelze xxxxxxx x tom, xx xx tím xxxx xxxxxxx xxxx právo xxxxxxxx x xxxxxxxxxx xxxxx hospodářskou xxxxxxx xx smyslu čl. 26 xxxx. 1 Xxxxxxx xxxxxxxxxx práv a xxxxxx, xxxx xxxx x čl. 26 xxxx. 2 Xxxxxxx xx xxxxxxxxxx xxxxxxx, xx xxxxx může xxxxxxxx xxxxxxxx x xxxxxxx xxx xxxxx xxxxxxxx xxxxxxxx. Naopak podnikatel xxx získá informaci, xx xxx v Xxxxx xxxxxxxxx, xxxxx xxx x xxxxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx, xxxx naplněn, x xxxxx xxxxx xxxxxx xxx xxxx xxxxxxx xxxx xxxxxxxxxxxxxx aktivitu. Xxxxx xxxxx xxxxxxxx xx třeba xxxxxxxxx x xxxxxx práva xxxxxx xx xxxxxxx xxxxxx a xx xxxxxxxxx xxxxxxxxx xxxx xxxxxxxxxxx x článku 31 Xxxxxxx xxxxxxxxx taktéž xx xxxx xxxxxxxxxxxxx, xxxxxxxxxx x kulturních. Xxxxx podnikat xxx xxxxxx být vykonáváno xxx, že xx xxxx xxxxx xxxxxxx xxxxxxxx xxxxxxxx xxxxxx xx xxxxxx xxxxxx xxxxxxxxxxx ústavního práva.
Navrhovaný xxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx xxxx v xxxxxxx x xxxxxxxxxxxxx xxxxxxxxx, kterými xx Xxxxx republika xxxxxx.
Xxxxxxxxxx xxxxxx xxxxxx vychází x xxxxxxxx Xxxxxxxxxx xxxxxxxxxx a Xxxx (XX) č. 536/2014, xxxxx xxxxxxxx xx xxxxxxxx x České republice, xxxxxxx xxxxxxxxxx xxxxxx xxxxxxxxxxxx xxxxxxxxxx xxxxxx xxxxxxxx x xxxxxxxx xxx xx xxxxxxxxxxx, xxxxx xxxx xxxxxxxx xxxxxxxxx státu xxxxxxx xxxx xx xx xxxxxxxxx xx xxxxxxx.
Xxxxxxxxxx xxxxxx xx x xxxxxxx xxxxxxx xxxxxxxxx xxxx xxxxxxx x xxxxx míře naplňování xxxxx xxxxxx na xxxxxxx zdraví x xx náležitou zdravotní xxxx xxxxxxxxxxx x článku 31 Listiny xxxxxxxxxx xxxx x svobod xxx, xx by xxxx xxxxxxx xxxxxxx x xxxxxxx xxxxxx xxxx situací, xxx xx xxx xx xxxx České xxxxxxxxx xxxxxxxxxx xxxxxxxx přípravků xxxxxxxxx jejich xxxxxxxxx xxxxxxx.
Xxxxxxxx výše uvedených xxxxxxxx xxxxxxxxxxxx, xxxxxxxxxxxxxxxx, xxxxxxxxx, xxxxxxxxxxxxx, xxxxxxxxxxxx, xxxxxxxxxx únosnosti, xxxxxxxxx x xxxxxxxxxx xxxxxxxxx xxxxx xxxxxxxxxxxx navrhované xxxxxx xxxxxx x xxxxxx Xxxxxxxx xxxx, xxx xxxxxxx xx xxxxx xxxxxxxx xxxxxxxxxxxx xxxxxxxx xxxxxxx xxxxxxxxxxxxxx xxxxxxx x xxxxxx xxxxxxx xxxxxx a xxxxxx lidí. Xxxxxx xxxxxxxx xxxx xxx xxxxxxxxxxxxxx, zejména xxxx xxxxxxxx xxxxxxxx xxxxxxxxx x xxxxxxxx. X xxxxxx xxxxxxxx xxxx xxx opatření přijaté xxxxxxxx státem xxxxxxxxxx. Xx základě xxxxxxxxx xxxxxxxx navrhovaná xxxxxx xxxxxx xxxxx podmínkám xxxxxxxx.
Xxxxxxxxx obchod s xxxxxxxx přípravky napříč xxxxxxxxx státy Xxxxxxxx xxxx xx xxxxxxxxxx x xxxxxxx se xxxxxxx xxxxxxx pohybu xxxxx (xx. 34 x 35 Xxxxxxx x fungování Xxxxxxxx xxxx), xxxxx xxxxxxxxxxx xxxxx xx xxxxxxxxxx xxxxxx jednotného vnitřního xxxx Xxxxxxxx unie. Xxxxx xxxxxxxx xxxxxxxxx xxxx v xxxxxxxx xxxxxxxx xxxx být x xxxxxxxxx případech xxxxxxxx akutní xxxxxxxxxxxxx xxxxxxxxx léčivého xxxxxxxxx xx trhu x Xxxxx republice. Xx xxxxxxxxxxx xxxxxxxxx xxxx x za xxxxxx xxxxxx xxxx přitom xxx xxxxx Xxxxxxxx xxxx xxxxxxxxx členské xxxxx. Navrhovaná xxxxxx xxxxxx xx xxxxx x souladu x xxxxxx Evropské xxxx, xxx kterého lze xxxxxxxx xxxxxxxxx xxxxxxxx xx xxxxxx xxxxxxx xxxxxx x xxxxxx xxxx, x xxxxx xxxxxx xx xxxxx xxxxxxxxx xxxxxx xxxxxxxxxxxxx xxxxxxxx přípravků xxx xxxxxxx xxxxxxxx x Xxxxx xxxxxxxxx.
Xxxxxxxxxx členské xxxxx XX v xxxxxxxxxx xxxxxx přijímají xxxxxxx xxxxxxxx xx xxxxxx xxxxxxx xxxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx x xxxxxx jejich xxxxxxxxx, přičemž xx xxxxxx Xxxxxx xxxx xxxxxxx z nich xxxxxxxxxx na rozpor x xxxxxx Evropské xxxx. Xxxxxxxx xxxx xx strany Xxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxx x xxxxxx xxxxxx xx xxxxxxxx xxxxxxx xxxxxx zboží. Xx xxxxxxx xxxxxxx xxxxxxx z poslední xxxx (xxxxxxx Španělska) xxxx xxxxxxx k xxxxxx, že navrhovaný xxxxxx, xxxxx spočívá xx xxxxxxxxx xxxxxxx xxxxxxxx xxxxxxxxx, xxxxx xxxx xxxxxxxx nedostupností, x x xxxxxxxx xxxxxxxxxx xxxxxx distribuce xxxxxxxx přípravků uvedených xx xxxxx xxxxxxx xxxx xxxxxxx členský xxxx, xx x xxxxxxx s xxxxxx Xxxxxxxx xxxx. Xxxxxxxx xxxxxx xxxxxxxx přípravků xx xxxxxxxxx xxxx xxxxxxxxxxxx, vychází x xxxxxxxx xxxxx x xxxxxxxx dostupnosti xxxxxxxxxxx xxxxxxxx xxxxxxxxx xx xxxx, xxxxxxx systém xx naprosto xxxxxxxxxxxxx x možná xxxxxxxx xxxx xxxxxxxxxxxxx. Xxxx xxxxxxxxxx rozhodnutí Xxxxxxxxxx xxxxxxxx xxxxx, xxxxxx xx členským xxxxxx xxxxxxxx přijmout opatření xxxxxxx x zajištění xxxxxxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx xxx své xxxxxx a xxxxxxxx xxx xxxxxx xxxxxxxx xxxxxxx xxxxxx xxxxx. Xxxxxxxx xxxxxx úprava xxxxxxxx xxxx xxxxxxxx xxxxx s právní xxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx xx Xxxxxxxxx, xxxxx xxxx xx xxxxxx EK xxxxxxxx za xxxxxx xxxxxxxxx volný pohyb xxxxx, protože xxxxxxxxxxxxx xxxxxxxx xxxxxxx, xxxxxxxxxx xx xx xxxxxxx xxxxxxxx xxxxxx xxxxxxxxx, xxxxxxx, xxxxxxx nebyla xxxxxx omezena, xxx xxxx trvalého xxxxxxxxxx x nebyla dostatečně xxxxxxxxxx. X poslední xxxx xx jedná xxxxxxxxx x Polsko, xxx xxxxxxxxx x xxxxxxxx xxxxxxxxxxxx úprava xxxxxxxxx reexport x xxxxxx státu XX x xxxxxxxx x xxxx, xx v xxxxx opatření xxxxxxxxxxx xxxxxxxx jsou x Xxxxxx xxxxxx xxxxx xxxxxxxx k xxxx xxxxxxx, xxxxxx xxx xxxxx, xx se xxxx xx xxxxxxxx xxxxxxxx přípravků x Xxxxx xxxxxxxxx po xxxxxxxx xxxxxxxxxx xxxxxxxx x xxxxxxxxx státě xxxxx xxxxx.
Xxxxxxx členské xxxxx, xxxxx xxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxx, xxxxxxxxx ustanovení článku 81 xxxxxxxx 2001/83/XX x xxxxxxxxx xxxxxxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx xxx xxxxxxxx xxx xxxx.
Xxxxxxxx xxxxxxxx Komise x xxxxxxxxx pravomoci (EU) č. 1252/2014 ze xxx 28. xxxxxx 2014 xxxxxxxxxx směrnici Evropského xxxxxxxxxx x Rady 2001/83/XX, pokud xxx x xxxxxx a xxxxxx xxxxxxx výrobní xxxxx xxx xxxxxx xxxxx xxx xxxxxxx xxxxxx xxxxxxxxx, se xxxxxxxxx xxxxxxxx xxxxxx xxx xxxxxx látky xxx xxxxxxx léčivé xxxxxxxxx. Xxxxx xxxxxx xx xxx přispět x důsledné adaptaci xxxxxx xxxxxxxx x xxxxxxxxxx Xxxxx xxxxxxxxx.
Xxxxxxxxxxx xxxxx zákona xxxx x rozporu s xxxxxxxxxxx xxxxxxxx xxxxxx Xxxxxxxx xxxx x xx x souladu x obecnými xxxxxxxx xxxxx Evropské xxxx (xxxx. xxxxxx xxxxxx xxxxxxx, proporcionality x xxxxxx xxxxxxxxxxxx).
X. Xxxxxxxxxx xxxxxx navrhovaného řešení xx xxxxxx k xxxxxx xxxxxxxxxxxx
Xxxxxxxxxx xxxxxx xxxxxx xxxxxxxxxx žádné xxxxxxxxxx, xxxxx xx xxxx v rozporu xx xxxxxxx xxxxxxxxxxxx.
Xxxxxxxxxx xxxxxx xxxxxx xxxx xxxxxxxxxxxxx ani xxxxxxxxxx xxxxxx na xxxxxxx xxxx x xxx x xxxxxx k xxxxxxxxxxxx jednoho x xxxxxxx, neboť nijak xxxxxxxxxxx xxx xxxxxxxxxxxx xxxxx x xxxxxxx x xxxxxxxxx pro xxx xxxxxxx podmínky.
D. Xxxxxxxxxx dopadů navrhovaného xxxxxx xx vztahu x xxxxxxx xxxxxxxx x osobních xxxxx
Xxxxxxxxxx xxxxxx xxxxxx nezakládá xxxx zpracování xxxxxxxx xxxxx. Xxxxxxxxxxx právní xxxxxxx xxxx měněno xxx xxxxxxxxxx zpracování xxxxxxxx xxxxx. Xxxxxxxxxx xxxxxx xxxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxx žádné xxxxxxxxxx xxx oprávnění xxxxxxxx xxxxxxxx údajů.
Navrhovaná xxxxxx úprava xxxxxxxxx xxxx zpracování osobních xxxxx x xxxx xx měněno xxx xxxxxxxxxx xxxxxxxxxx osobních xxxxx x těchto xxxxxx. Xxxxx xxx x xxxxxxxxxx xxxxx x xxxxxxxxxx §33 xxxx. 2, §77 xxxx. 1 xxxx. x) x §82 xxxx. 3 písm. x), xxxxx xxxxxxx x podstatě pouze x tom, xx xxxxxxxxx xxxxxx poskytovaných xxxxx, včetně xxxxx xxxxxxxx, xxxxx xxxx, xx xxxxxxxx xxxxxx xx xxxx nacházet xxxxx x xxxxxx, xxxx xxxxxxx xxxxx x xxxxxxxxxxx xxxxxxxxxx Xxxxxx x xxxxxxx xxxxxxxx, xx. xx xxxxxxxx, avšak xxxxxx xxxxxx xxxxx, nově xxxx zákonem x xxxxxxxxx, zůstane xxxxxx xxxx xxxxx. Xxxxx xxx x xxxxxxxxxx §53x xx §53x, §54 x §55, xxxxxxxx xx xxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx, xxxx xxxxxx xxxxxxxxxxxxx xxxxx, včetně xxxxx osobních, xxxxxxx xxxxxx, xxxx xxxxx xx x ustanovení §51 a xxxx. xxxxxxxxx právní úpravy. Xxxxx jde x xxxxx x xxxxxxxxxx §101 odst. 1, xxxxx xxxxxxx pouze x xxx, xx xxxxxxxx inspektora xx xxxx moci inspektor xxxxxxxxxx i xxxxx, xxxx xxxx xxxxxxxxx xxxxxxx vykonávat podle xxxxxx xxxxxxxx předpisů xxx podle xxxxxx x xxxxxxxx a xxxxxx již xxxxx xxxxxxxxxx kontrolované xxxxx xxxxxxx xxxxxxxx x xxxxxxxxxx kontrole xxxxxxxx xx xxx. Xxxxx xx vyvolána xxxxxxxx xxxxxxxxxx xxxxxxx a xxxxxxxxxxx xxxxxxxxxx, x xx xxx xxxxxx xx xxxx xxxxxxxx xxxxxxxxxx, konkrétně, xxxxx xxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxx činnost x určitém xxxxxxx xxxxx vykonává, x xx xxxxxx poskytovaných xxxxxxxx xxxxx xxxxx xxxx xxxx.
X. Zhodnocení xxxxxxxxxx xxxxx (XXX)
Xxxxxxxxxx xxxxxx xxxxxx xxxxxxxxx xxxxxx korupčních xxxxx. Xxxxxxxxx xxxxxxxxxxx xxxxxxxxxx xxxxx je xxxxxxx xxx x jednotlivých xxxxxxx, kde se xxxxxxxxx xxxxxxxx řešení, x xx xxx x oblasti klinického xxxxxxxxx léčivých xxxxxxxxx, xxx x x xxxxxxx regulace xxxxxx xxxxxxxx přípravků. Xxxxxxxxxx xxxxx je xxxx xxxxxxxx přiměřený xxxxx, x xxxxxxx xxxxxxxx xx xxxxxxxxxx. Xxxxx xx x legislativní xxxxxxxxx systému sledování x xxxxxxxxxxxxx xxxxxx xxxxxxxxxxxxx xxxxxxxx přípravků xxx xxxxxxx pacientů x Xxxxx republice x přijímání příslušných xxxxxxxx xxxxxxxxxxx xxxxx xxxxxxxx xxxxxxxxx xxxx xxxxx České xxxxxxxxx. Xxxxxxxxxx xxxxxx xxxx xxxxxxxxx xxxxxxxxx Xxxxxxxx xxxxxx xxx xxxxxxxx xxxxx x Ministerstva xxxxxxxxxxxxx a x xxxx xxx xxxxxxx xxxxxxxxx pravomoci, xxxxx x kontextu těmto xxxxxxx xxx xxxxxxxx x xxxxxxxxxxx xxxxxxxxxx xx xxxxxxx x xxxxxx xxxxxxxx rozšíření, xxxxx xx představovalo xxxxxxxxxx korupční xxxxxx.
ZVLÁŠTNÍ XXXX
X §1 xxxx. 1 (xxxxxxxx xxxxxxxx xxx čarou)
Do xxxxxxxx pod čarou x. 2 xx xxxxxxxx odkaz na Xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Rady (EU) č. 536/2014 xx xxx 16. xxxxx 2014 x klinických xxxxxxxxxxx xxxxxxxxx léčivých xxxxxxxxx x x xxxxxxx xxxxxxxx 2001/20/ES x Xxxxxxxx Xxxxxx v xxxxxxxxx xxxxxxxxx (XX) č. 1252/2014 xx xxx 28. xxxxxx 2014 xxxxxxxxxx směrnici Xxxxxxxxxx xxxxxxxxxx x Xxxx 2001/83/XX, pokud xxx x xxxxxx a xxxxxx správné výrobní xxxxx pro účinné xxxxx xxx xxxxxxx xxxxxx xxxxxxxxx.
X §5 xxxx. 16:
Xxxxxxxx xxxxxxxx 16 do §5 xxxxxx xxxxxxxxxxxx xxxxxxxx xxxxxx léčivé xxxxx xxxxxxx xxxx xxxxxxx xxxxxxxx je xxxxxxxxxx xxx, xx x xxxxxxxxx právní xxxxxx xxxxxx xxxxxxxx xxxxx, xxx vytváří xxxxxxxxx xxxx, xxx není xxxxxx, xx xx xxxxx xxxxxxx rozumí x xxxxxx xxxxxx xxxxxxx. Xxxxx xxxx xxxxxxxx xxxxxxxxx nedostatečnou xxxxxxxxxxx xxxxxxxx 2001/83/ES (xx. 46x). K xxxxxxxx xxxxxxxx xxxx xxxxxxx xxxxxxxx Komise x xxxxxxxxx xxxxxxxxx (XX) č. 1252/2014 ze xxx 28. xxxxxx 2014 xxxxxxxxxx xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Xxxx 2001/83/ES, xxxxx xxx o zásady x xxxxxx xxxxxxx xxxxxxx xxxxx xxx xxxxxx xxxxx xxx xxxxxxx xxxxxx přípravky. Xxxxxxxx x xxx xx nacházející platí xxxxx xxxxx xxxxx xxx xxxxxx xxxxx xxx humánní xxxxxx xxxxxxxxx, x xxxxx xxxxxxxx xxxxxxx x xxxxxxxxxxx odstavci 16 xxxx xxx z xxxxxx potřeby xxxxxxxxx xxxxxx xxxxx a xxxxxxxxx se x xx xxxxxxxxxxx xxxxxx xxxxxxxxx x xxxxxxxxx xxxxxx xxxxxxxxx.
X §11 xxxx. x):
Xxxxxxx se xxxxxxxxxx x xxxxxx xxxxxx komise k xxxxxxxx xxxxxxxxxx x xxxxxxxxxxxxxxx klinickým xxxxxxxxxx, xxxxx x xxxxxxx xxxxxxxxxx nařízení č. 536/2014 xxxxxxxxx. Xxxxxx etických xxxxxx xx xx xxxxxxxxxxxx xxxxxxxxx státech, xxxxxxxxxx pro jakýkoli xxxxxx xxxxxxxxxxx x xxxxxxxx jsou mimo xxxx xxxxxxxxx xxxxxxxxxxxx xx xxxxxxxxxx, xxxxxxxxxxx, xxxxx xxxxxxxxxx xxxxxxxxx, xxxxxxxxxx xxxxxxxxxxxx. Xxxxxxxx xxxxxx etických komisí x Xxxxx republice, xxx xxxxxx xxxxxxxxxxx xxxx xxxxxxxxxxxxx zdravotních xxxxxx, xxxxx xxxx xxx x xxxxx xxxxxxxxxx xxxxxxxxx, xxxxxxx xxxxxxxxxxx xxxx xxxxxxxxxx, xxxxx xxxx mnohdy x xxxxx xxxxxxxxx xxxxxx komise, xx xxxxx x rozporu x požadavky xxxxxxxx. Xxxxxxxxxx právní xxxxxx xxxxxxxxx xxxxxxx etickou xxxxxx xxxx orgán Xxxxxxxx xxxxxx pro xxxxxxxx xxxxx, x xx i z xxxxxx, xx x xxxxxxx x xxxxxxxxx č. 536/2014 xxxx xxxxxx xx xxxxxxxxx xxxxxxxxxx xxxxxxxxx, xxxxxxxxxx xxxx x další xxxxx xxxxxxx x xxxxxxxx xxx xxxxxxxxx hodnocením xxxxx xxxxx xxx Xxxxxx xxxxx xxx xxxxxxxx xxxxx xx xxxxx xxxxxxx xxxxxx, x x xxxx xxxxxx xxxx xxxxxxx xxxxxxx xxxxxx xxxxxx x xxxxxx xxxxx. Xxxx xxx zohledněn xxxxxxxx xxxxxxxxx xxxxxxx x čl. 86 xxxxxxxx x. 536/2014 a xxxxxxxxx xxx, xx xx xxxxxx činnost xxx xxxxxxxx lze xxxxxxxx pouze xxxxx xxxxxxxx xx xxxxxxx xxxx.
Xxxxxxx xx xxxxxx xxxxx nová xxxxxxxxxx xxxxxxxx Xxxxxxxxxxxx xxxxxxxxxxxxx x vydání xxxxxxxx xxxxxx xxxxxx xxxxxxxxxxx xxxx xxxxxxxxxxxx distribuci xxxxxxxx xxxxxxxxx xx xxxxxxxxx. Xxxxxxxx xxxx xxx xxxxxx xxxxx x xxxxxxxxxxxx xxxxxxxxx. Xxxxxxxx xxxxxx xxxxxxxx xxxxxx xxxxxx k xxxxxxxxx dostupnosti xxxxxxxxx xxxxxxxx xxxxxxxxx jsou xxxxxxxxx stanoveny x xxxxx xxxxxxxxxx §77d.
K §11 xxxx. x:
Xxxxxxxxx xxxxxxxxxx §11 písm. x) xx xxxxxxxx xxx, xxx se xxxxxxxxxxx xxxxxxxxx x xxxx xxxxxxxxxx ustanoveními xxxxxx x) xxxx x) a xxxxxx xxx xxxx xxxxxxxx xxx ty případy, xxx Ministerstvo xxxxxxxxxxxxx xxxxxx xxxxxxxxxx xxxxx xxxxxx xxxxxxxxxxxx ustanovení.
K §11 xxxx. x):
Xx xxxxxx zajištění předvídatelnosti x xxxxxxxxxxxxxxxx postupu xxx xxxxxxx reexportů xx do §11 xxxxxx x xxxxxxxx xxxxxxxx písmeno q), xx xxxxxx xx xxxxxxxx xxxxxxxx Ministerstvem xxxxxxxxxxxxx xxxxxxx xxxxxxxx xxxxxxxxx (xxxxxx opatření xxxxxx povahy), xxx xxxxxxx xxxxxxxxxx na xxxx x Xxxxx xxxxxxxxx by xxxxx xxxxxxxxx xxxxxxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx při xxxxxxxxxxx xxxxxxxxxxx xxxxxx x České xxxxxxxxx.
X §13 xxxx. 2 xxxx. x) bod 1:
Xxxxxxxxx Xxxxxxxx xxxxxx xxx kontrolu xxxxx xx rozšiřuje x xxxxxxxx rozhodnutí x xxxxxxxxxx xxxxxxxx přípravku.
K §13 xxxx. 2 xxxx. a) bod 3:
Xxxxxxxx xx, aby xxxxxxxxxxx, xxxxxxx xx xxxxxxxxx splnění podmínek xxxxxxxxx xxxxx, xxx xxxxxx xxxxxxxxxx hodnocení xxxxxxx xxxxxxx klinické xxxxx, xxxxx být xxxxx xxxxxxxxxxxxx vydávány x xxxxxx xxxxxx, x to xxxxxxxxx xxxxxxxxxxx. Xxx xxxxxxxxxx xxxxxxxx xxxxxxxx xx xxxxxxxx xxxxxxxxx x xxxxxxx znalostí xxxxxxxxxxxx x oblasti xxxxxxxxxxx x správné xxxxxxxx xxxxx, xxxxxx xxxx x xxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxx xxxxxxxxx. Xxxxxxxx xxxxxxxxx xxxxx xx rozumí xxxxxx xxxxxxxxxx xxxxxxxx x xxxxxxxxx xxxxxxxxx xx xxxxxxx při navrhování, xxxxxxxxx, xxxxxxxxxx, sledování, xxxxxx, xxxxxxxxxxxxx x xxxxxxx xxxxxxxxxx xxxxxxxxx x xxx xxxxxxxxxxx xxxxx x xxxx, xxx se xxxxxxxxx, xx jsou xxxxxxxx xxxxx, bezpečnost x xxxxxxx xxxxxx xxxxxxxx xxxxxxxxx x xx xxxxx xxxxxxx v xxxxxxxxx hodnocení jsou xxxxxxxxxx x xxxxxxxx. Xxxxxxxx xxxxxxx klinické xxxxx xxxx xxxxxxxxxxx xxxxxxxxxx xxxxxxxx (xxxxxxxx xx xxxxxxxx XXX X6 Xxxxxxxxxxx konference xxx harmonizaci xxxxxxxxxxx xxxxxxxxx xx xxxxxxxxxx xxxxxxxxx xxxxx - xxxxxxxxx International Conference xx HarmonisationofTechnicalRequirementsforRegistrationofPharmaceuticalsforHuman Xxx-xxx. XXX, kde xxxx xxxxxxxx regulačních xxxxxxx x xxxxxxxxxxxxxxx xxxxxxxx Xxxxxx, Xxxxxxxx x XXX). Tento dokument xxxxxxx Xxxxxxxxxxx xxxxxxxxxx xxx xxxxxxxxxxx xxxxxxxxxxx xxxxxxxxx xx xxxxxxxxxx xxxxxxxxx xxxxx 1.5.1996, xxxx xxxxxxx pravidla xxxxxxx xxxxxxxx praxe, x xxxxx xxxxxxx xxxx xxxx promítnuta x xxxxxxxxx x xxxxxxxxxx xxxxxxx předpise.
K §13 odst. 2 xxxx. b):
Upravuje se xxxxxxxxx kompetence Státního xxxxxx xxx xxxxxxxx xxxxx s xxxxxxx xx xxxxx xxxx xxxxxxxxx. Stávající systém xxxxxxxxx xxx xxxxxxxxxx, xxx ohlašovací režim xxx vyřízení xxxxxxx x klinické xxxxxxxxx. Xxx xxxxxxxx se xxxx jednat již xxx o xxxxxx xxxxxxxxxx.
X §13 xxxx. 2 xxxx. x):
Xx základě xxxx xxxxxxxx kompetence Xxxxxx bude xxxxx xxxxxx xx xxxxxxx x jakosti, xxxxx xxxxxxxxx nepředstavuje xxxxxxxx xxxxxx xxxx xxxxxx, xxxxxxxx xx trhu. Xxxxxxxx xxxxxxxx Ústavu xxxx významně xxxxxxxxxx xxxxxxxxx xxxxxxxxxxx xxxxxx xxxxxx xx trhu x Xxxxx republice. Xxxxxxxxxx xxxxxxxx xxxxxxx xxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxx, xxxxx xxx ně představuje xxxxxxxxxxxxxxx zátěž, xxxxxxxxxx xxxxxxx x xxxxxxx xx xxxxxxxxxxx, xxxxx xxxxxx x tímto xxxxx xxxxxx x xxxxxxx xxxx xxxxx xxxxxxxxxx či zbytečně xxxxxxxxxx. Rozhodování Xxxxxx xxx xxxxxx ustanovení xx systematicky navázáno xx xxxxxxxxxx §23 xxxx. 2, xxx xxxxxxxxxxxx nesmí xxxxxxxx x xxxxxx xx xxxxxxx v xxxxxxx, xxxxx xxxxxxxxxx Xxxxx xxx §13 xxxx. 2 xxxx. x) xxxxx.
X §13 xxxx. 3 písm. x) x x):
Xxxxxxxx se xxxxxxxxx Xxxxxxxx ústavu xxx xxxxxxxx xxxxx xx xxxxxxx xxxxxxx xxxxxxx xx trhu x léčivými přípravky xxxxxxxxxxx pro Xxxxxxxxxxxx xxxxxxxxxxxxx informaci xxxxx §77x.
X §16 odst. 2 xxxx. x) xxx 1:
Působnost Xxxxxx xxx xxxxxx xxxxxxxx xxxxxxxxxxxxx xxxxxxxxxxxx a xxxxx xx rozšiřuje x vydávání xxxxxxxxxx x propadnutí xxxxxxxx xxxxxxxxx.
X §19x:
X nově xxxxxxxxx §19x se xxxxxxxxx xxxxxx základ xxxxxxxxxx Xxxxxxxx ústavu xxx xxxxxxxx xxxxx x Generálním ředitelstvím xxx x výměny xxxxxxxxx mezi xxxxxx xxxxxx xxx, xxx xxxx xxx xxxxxxx xxxxxxx xxxxx směrnice Xxxxxxxxxx parlamentu x Xxxx 2011/62/EU. Xxxxxx xxxxxxxxxx xx xxxxxxxx xxx na xxxxxxx xxxxxx, tak x xx xxxxxxx xxxxxxxxxx xx xxxxxxxxx, x xx xxxxxx xx xxxxxx xxxxxxxxxxxx takových xxxxxxx xxxxxxxxxx xx xxxxxxx xxxx xxxx. xx xxxxxx sledování xxxxxxxxx. Xxxxxxx xx xx xxxx x xxxxxxxxxx xxxxxxxxx xx xxx, a xxxxxxx x plošné xxxxxxxxxxxx. Xxx vložení xxxxxx xxxxxxxxxx xxx xxxxxxxxx xxxxxx xxx platný xxxxxx xxx, x xxxxx spolupráce x Xxxxxxxxxx xxxxxxxxxxxx cel xxxx xxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxx, jako xx xxxx x xxxxxx č. 226/2013 Sb., x xxxxxxx xxxxx x xxxxxxxxxxx výrobků na xxx. Xxxxxxx xx xxxxxxxx stanoví xxxxxxx x xxxxxxxxxx xxxxxxxxxxxx xxxxxxxxx x xxxxxxx xxxx xxx, aby Xxxxxx xxxxx xxx xxxxxxxx léčiv xxxx xx Generálního ředitelství xxx xxxxxx xxxxxxxx xxxxxxxxx.
X §21(Xxxxxxxx XXXX, xx. 49 xxxxxxxx):
X §21 se xxxxxxxx xxxxxxxx 1 z xxxx důvodu, xx xxxxxxxxxxxx, kdo xx xxxx xxxx zkoušejícím, xx xxxxxxxxx xxxx x §54 xxxx. 1 x to x návaznosti na xxxxxxxxx stanovené nařízením.
X §33 xxxx. 2:
Xx xxxxxx xxxxxxxxx xxxxxxxxxxxxx xxxxxxxxxx xxx xxxxxxx xxxxxxxxxxx xxxxxxxx přípravků xx xxxx x ČR xx nutné xxxxxxxx, xxx Xxxxxx ústav xxx kontrolu xxxxx xxxx pracovat x xxxxxxxxxx x xxxxxxxxx xxxxx umožňujícími získat xxxxxxx xxxxxxx o xxxxxxxxx xxxxxxxx přípravcích x xxxxxx objemu xx trhu v Xxxxx xxxxxxxxx.
Xxxxxxx xxxxxxxxx xx držitelů rozhodnutí x xxxxxxxxxx budou xxxxxxx x xxxxxxxxxx xxxxxxxxxxx dostupnosti xxxxxxxxxxxx xxxxxxxx xxxxxxxxx x xxxxxxxx spolehlivých podkladů xxx xxxxxxxxxx xxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx Xxxxxxxxxxxxx xxxxxxxxxxxxx xxxxx §11 písm. x) x xxxxx xxxxxxxxx xxxxxxxx Xxxxxxxxxxxx xxxxxxxxxxxxx xxxxx §11 xxxx. x). Xxxxxxxxxx xxxxxxxxxx xxxx Státnímu ústavu xxx xxxxxxxx léčiv xxx mají xxxxxxx x xxxxxxxx xxxxxxxxx xxxxx xxxxxxxxx xxxxxxxxxxxxx xxxxxxx (xxxxxxxxxxxx xxxxxxxx xxxxxxxxx x xxxxxxxxxxxxx xxxxxxxxx x výdeji xxxxxxxx xxxxxxxxx). Xxxxxx xxx xxxxxx xxxxxxx xxxxx dostatečné x xxxx, xxx xxxx xxxxx xxxxxx x xxxx xxxxxxxxx xxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx x Xxxxx republiky. Xxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxxx x registraci xxxxxxxxxx Xxxxxxxx xxxxxx pro xxxxxxxx xxxxx xxxxx x správné xxxxx x xxxxxx léčivých xxxxxxxxx dodávaných xx xxx xxxxxxx xxxxxxx xxxxx x xxxxxx x xxxxx xxxxxxxxxx xxxxxxxxxx xxxxxxx přípravkem. Xxxxxxxx komplexnějších xxxxx xxxxxx současnému stavu xxxx xxxxx přesněji xxxxx rozsah možného xxxxxx nedostupnosti xxxxxxxx xxxxxxxxx x také xxxxxxxx xxxxxxxx xxxxxxxx, xxxxx zamezí nedostupnosti xxxxxx léčivých xxxxxxxxx xxx xxxxxxxx x Xxxxx republice. X xxxxxxxx xxxxxxxxx xxxxxx xxxxxxx x účinnější xxxxxxxxxxxxxx nápravy xxx xxxxxxxx této xxxxxxx xxxxxxxxxx je xxxxxxxxx, xxx xxx xxxxxx xxxxx, časový xxxxxxxx x způsob xxxxxx xxxxxxxxxxx xxxxxx xxxxxxx xxxxxxxx prováděcím xxxxxxx xxxxxxxxx. Xxxxxxxxx xxxxxx xxxxxxx xx xxxxxxx xxxxxxxx xxxxxxxxx xxx XXXXXX xxxxxxxx xx xxxxxxx xxxxxxxx xxxxxxxxx x dále xxxxx xxxxxxxx xx xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx xxx xxx regulační správní xxxxxx, xx. xxx xxx XXXXXX, xxx x xxx XXXX. Xxxx je nutné xxxxxxxx xxxxxxx xxxxx xxxxxxx xxxxxxx xx xxxx x xxx xxxxx těch pravidelně xxxxxxxxxxxxx.
Xxxxxxxxxxxx xxxxxxx xx xxxxx x xxxxxxx xx xxxxxx xxxxxx x xxxxxxx xxxxxxxxx xxx, xxxxxxxx xx xxxxxx xxxxxxxxx xxxxxxxxxx x xxx dává xxxxxxx efektivně a xxxx xxxxxxxx xx xxxxx xxxxxxxxxx daného xxxxxxxx xxxxxxxxx xx xxxx. Xxxxx xx xxxx xx Xxxxx xxxxxxxxxx x jiné, xxxx. x xxxxxxx xxxxxxxx, xxxxx by xx Ústav xxxxxx xxxxxxxxx do xxxxxxxx xxxxxx, aby xx xxx xxxx xxxxx xxxxxxxxx, xxxxxxxxxx x xxxxxx xxxxx. X xxxxxxx xx xxxxxxx xxxx, xxxxxx má Xxxxx xx xxxxxxxxxx xxxxxxx o vývozu xxxxxxxx přípravků a xxxxxxxx xxxxxxx xxxxxxx x xxxxxx xxxxxxxx xxxxxx xxxxxx xx XX, by jiná xxxxx, xxx elektronická xxxxxx xxxxxxxxxx. Xxxxxx xx xxxxx xxxx x xxxxx, xx xxxxxxx jsou xxxxxxx xxxxxxxx xxxxxxxx x xxxxxxxxxx k internetu, xxxxxxxxxxxx xxxxxx používají xxxxxxxx, XX x xxxxxxxxxxxxx xxxxx xxx, xxxxx jim xxxx xxxxxx při jejich xxxxxx xxxxxxxxx xxxxxxx xxxxxxxxxx x uchovávání xxxxxxx a dokumentace xxx xxxxxx x xxxxx xxxxxx povinností xxx xxxxxxxxx xxxxxx xxxxxxxxxxxx xxxxxx x xxxxxxxx.
X §33 xxxx. 3 xxxx. a):
Jedná xx xxxxx x xxxxxxxxxxxx technické upřesnění xxxxxx xxxxxx xxxx xxxxx jejího xxxxxx, xxx xx xxx xxx současného právního xxxxx držitel xxxxxxxxxx x xxxxxxxxxx xxxxxxx xxxx xxxxxxxx x xxxxxxxxx xxxxxxxx xxxxxxxxx xx distribuce nebo xx lékárny. Xxxxxxxx xxxx „xxxxxxxxxx xxxx xxxxxxx“ xxxxxxxxx xxxxxx „xx xxx v Xxxxx xxxxxxxxx“.
X §34 xxxx. 2:
Xxxxx x xxxxxxxx x xxxxxxxxx xxxxx xxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx xx xxxxxxxxxxx xxxxxxxxxx. X ohledem xx skutečnost, že x prodloužení xxxxxxxxxx xxxxxxx xxxxxx v xxxxxx neodhadnutelných xxxxxxx, xx xxxxxxxxx xxxxxxx xxxxxxxx xxxxxx léčivého xxxxxxxxx x xxxxx xxx dochází x xxxxxxxx x dodávkách xx xxxxx xxx x xxx xx xxxxxxxx xxxxxxxxxxx léčivých xxxxxxxxx pro xxxxx xxxxxxxx. Tato xxxxxx xxxxxxxx xxxxxxxxx xxxxxx xxxxxxxxx x případě xxxx registrací x xxxxxxxxxx §35 odst. 2 x xxxxxxx xxxxxxxxxx v §36 xxxx. 4.
Xxx o xxxxxxxx xxxxxxxxxxx xxxxxx, xx xxxxx xx xxxxxxxxxx x rámci novelizace xxxxxxxxx materie xxxxxx.
K §51 xx 59:
Xxxxx x xxxxxxxxxxxx §51 xx 59 xxxx xxxxxxx xxx xxxxxxxxx xxxxxxxx xxxxxxxx č. 536/2014 xx xxxxxx x xxxxxxxx, neboť představují xxxxx xxxxx xxxxxx xxxxxxxxxx hodnocení xxxxxxxxx xxxxxxxx xxxxxxxxx, xxxxx xxxxxxxx na xxxxxxxx xxxxxx xxxxxxxxxx x xxxxxxxx č. 536/2014. X xxxxxx xxxxxxxxxxxx se xxxxxxxxx vypouštějí xx xxxxxxxxxx, která xxxx x xxxxxx o xxxxxxxx xxxxxxxxxxxx xxxxxxxxxxxxxx xx vztahu ke xxxxxxxx 2001/20/ES x xxxxx xxxx uvedena xxxxx v xxxxxxxx č. 536/2014 nebo která xx nařízením č. 536/2014 xxxxxxx, a dále xx x xxxxxx xxxxxxxxxxxx xxxxxxxx xx xxxxxx otázek, xxxxx xxxxxxxx přikazuje xxxxxxxxx xxxxx, xxx xx xxxxxxx, xxxxx zmocňuje xxxxxxx xxxx x xxxxxx úpravě.
K §51:
X xxxxx xxxxxxxxxx xx x xxxxxxxxxx xxxxxxxxx xx čl. 4 xx 9, čl. 15 až 24 x čl. 83 xxxx. 1 nařízení x. 536/2014 xxxxxxxxxxx xxxxxx základních xxxxxx xxxxxxxxxx hodnocení humánních xxxxxxxx přípravků.
V xxxxxxxx 1 (Xxxxxxxxx (18), (19); Xxxxxxxx II, čl. 7 xx 9; Xxxxxxxx XXX čl. 15 xx 24 xxxxxxxx) xx xxxxxxxx xxxxxxxx xxxxxxxxx Xxxxxxxx xxxxxx xxx xxxxxxxx xxxxx x oblasti klinického xxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx. Xx xx xxxxxxxxxx xxxxxxx o xxxxxxxx xxxxxxxxxx hodnocení xxxxxxxxx xxxxxxxx xxxxxxxxx x xxxxxxx o xxxxxxxx významné xxxxx xxxxxxxxxx hodnocení x xxxxxxxxx dohledu xxx xxxxxxxx xxxxxxxxxx xxxxxxxxx (Xxxxxxxx XXXX, čl. 77, čl. 78). Veškeré xxxxx xxxxxxxxx v souvislosti x vyřízením xxxxxxx x povolení klinického xxxxxxxxx (Xxxxxxxx XX xxxxxxxx č. 536/2014), xxxxxxx x xxxxxxxx xxxxxxxx xxxxx xxxxxxxxxx xxxxxxxxx (Xxxxxxxx XXX xxxxxxxx č. 536/2014) x xxxxxxxxx xxxxxxx (Xxxxxxxx XXXX xxxxxxxx č. 536/2014) se xxxxxxxx xx odborné xxxxx, xx xxxxx Xxxxxx ústav xxx xxxxxxxx xxxxx xxxxxx xxxxxxx xxxxxxx. (Kapitola XXX, čl. 86 a 87)
X xxxxxxxx 2 (Xxxxxxxxx (69); Xxxxxxxx XX, čl. 83 = Xxxxxxx xxxxxxxxx xxxxx) xx xxx xxxxxxx xxxxxxx na čl. 83 xxxx. 1 xxxxxxxx x. 536/2014, xxxxx x xxxxxxxxx postupů xxxxxxxxxxx v xxxxx xxxxxxxx xxxxxx xxxxxxxxx xxxxx xxxxx jedno xxxxxxx xxxxxxxxx místo.
V xxxxxxxx 3 (Xxxxxxxx XX, čl. 5 xx 8 xxxxxxxx) xx xxxxxxxx, xxx xxxxxxxx xxxxxxxxx xxxxxxxx členskému xxxxx xx Xxxxxx xxxxxxxxx. Z xxxxxx xxxxxxxxxxxx se x xxxxxxxxxxxx xxxxxxxxx odstavce 3 upravuje xxxxxxxxx x xxxxxxx, xxxx xx Xxxxx xxxxxxxxx xxxxxxxx státem xxxxxxxxxxx, xxxxxxxxx x xxxxxxx, xxxx xx Xxxxx xxxxxxxxx xxxxxxxx xxxxxxxx xxxxxx x xxxxxxxxx xxx xxxxxxxxx xxxxx XX xxxxxxxxx xxxxxx, xxxxxxxxxx se xxxxx x xxxxxxxxx státu. X odstavci 4 xx xxxxxxxx xxxxxx xxxxxxxxx xxx vydávání xxxxxxxxxx xx xxxxxxx xxxx.
X §52 (Xxxxxxxx X, čl. 34 xxxxxxxx):
X tomto xxxxxxxxxx x odstavci 1 (Xxxxxxxx V, čl. 29 xxxx. 7 x 8 xxxxxxxx) xx xxxxxxx xx ustanovení čl. 29 odst. 7 xxxxxxxx x. 536/2014, xxxxx xxxxxxxx xxxxxxxxx xxxxx, xxx xx xxxx xxxxxxx xxxx xxxxxxxxx, xxx kromě xxxxxxxxxxxxx xxxxxxxx uděleného xxxxxxx xxxxxxxxxxx zástupcem xxxxxx x xxxxxx x xxxxxxxxx hodnocení xxxxxxx x nezletilý, xxxxx xx xxxxxxx xxxxxxx xx názor x xxxxxxxx xxxxxxx xxxxxxx xxxxxxxxx. X xxxxxxxx xx xxxxxxx, xx bude vyžadován xxx nezletilé xxxxx xxxxxxx xxxxxxxxxxxxx souhlasu xxxxxxx ustanoveným xxxxxxxxx x xxxxxx xxxxxxxxx xxxxx, vyjadřující, xx xxxxxxx xxxxxxxxx xxxxxxxxx xx xxxxxxxxxxxx x xxxxxxxxx x informacích xxx pacienta přizpůsobených xxxx nezletilého, xxxx xxxxxxxxxxx zúčastnit xx xxxxxxxxxxx xxxxxxxxxx hodnocení. X odstavcích 2 x 3 xx xxxxxxxxxx možnost xxxx čl. 34 nařízení x. 536/2014, xxxxx xxxxxxxx xxxxxxxx xxxxxx xxxxxxxx xxxxxxxxx ochranná opatření xxxx xxxxxxx xxxxxx, xxxxx xxxx x xxxxxxx xxxxxxxxxxxx xxxx xxxxxxxx xxxxxxxxxx. V xxxxxxxxxx xx toto xxxxxxxxxx xx xxxxxxx, xx klinické xxxxxxxxx xxx xxxxxxxx x xxxxxxxxx skupin subjektů xxxxxxxxx xxx xxxxx, xxxxx xxxxxxxx xxxxxxx xxxxxxxxx xxxxxx, xx xxxxxxx základě xxx xxxxxxxx, xx xxxxx x xxxxxxxxx hodnocení xxxx xxx xxx xxxx xxxxxxxx hodnocení xxxxx xxxxxxx xx xxxxxxxxxxx přínos, který xxxxxxx xxx xxxxxxxxxxxxx xxxxxx a zátěží. Xxx je xxxxxxxx xxxxxxx xxxxxxxx xxxxxx xxxx do čistě xxxxxxxxxx xxxxxxxxxx xxxxxxxxx (xxxx. klinických xxxxxxxxx xxxxxxxxxxxxxxxxx nebo xxxxxxxxxxxxxxx), xxxxx xxx xxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxx xxxxx přínos. Za xxxxxxx skupiny xxxxxxxx xxxxxxxxx xx xxxxxx xxxxxxxx xxxxx xxxxxxxxxxx xx xx xxxxx, xxxxxxxxxxxxx xxxxxxx xxxx xx výkonu xxxxxx xxxxxx xxxxxxx, xxxx xxxxx pobývající x xxxxxxxx ústavní xxxx (xxxx. x xxxxxxxxxx xxxxxxxxxx poskytujících xxxxxxxx xxxx, xxxxxxxx xxxxxxxxxxx xxxxxxx péči nahrazující xxxx xxxxxx, xx.) x xxxxxx osoby, xxxxxxx xxxxxxxxxxx byla xxxxxxx soudem (xxxx. xxxxx, xxxxx nesmí xxxxxxxx se svým xxxxxxxx). Vzhledem k xxxx, že Česká xxxxxxxxx xxxxxxxxxx xxxxx x xxxxxxxxxxxx xxxxxx xxxx xxxxxx xxxxxxxxxx x účasti xx xxxxxxxxx hodnocení, xxx xxxxxxxx xxxxx xxxxxx xxxxxxxxx, xxxxxxxxx xxxxxxxxxx xxxxxxxx xxx xxxxxx xxxxx x xxxxxxxxx xxxxxxxxx. Xxxxxxx xxxxxxxxxx xxxxxxxxxxxxx xxxxxxxx pak xxxxxxxx x xx xxxxxxx xxxxxxxxxx x xxxxxx x xxxxxxxxxxx xxxxxxxx.
X §53 (Xxxxxxxxx (18); Kapitola X, xx. 2 (11):
Xxxxxx xxxxxxxx x xxxxxxxx xxxxxx xxxxxx nařízení č. 536/2014 ponechává x xxxxxxxxxx xxxxxxxxx xxxxx. Xxxxx xxxx xxxxxxxxxx xxxxxxx x tomu, xxx to, xx xx x současné xxxxxx xxxxxx xxxxxxxxx, xxxx x xxxx xxxxxx xxxxxx při xxxxx xxxxxxxxxxx xxxxxxx.
X xxxxxxxx 1 xx xxxxxxxxx působnost Xxxxxxxx xxxxxx xxx kontrolu xxxxx xxxxxxx xxxxxxx xxxxxx xxxx svůj xxxxx. Xxxxxx navrhované xxxxxx xxxxxx vychází x xxxxxxxxxxxxx xxxxxxxxx xxxxxxxxxxx xxxxxxxxx č. 536/2014: 1) Xx xxxxxxxxx xxxxxxxxxx hodnocení, xxxxxxxxxx xxxx klinického xxxxxxxxx x xxxxx xxxxx xxxxxxx s xxxxxxxx xxx xxxxxxxxx xxxxxxxxxx xxxx xxxxx jedna xxxxxx xxx Státní xxxxx pro xxxxxxxx xxxxx xx xxxxx xxxxxxx xxxxxx, x xxxx právní xxxxxx xxxxxx, aby x xxxx xxxxxx byla xxxxxxx xxxx xxxx xxxxxxx xxxxxx xxxxxx x xxxxxx xxxxx x xxxx xxxxxxxxx xxxxxxxxxxx technické zázemí xxxxxx komise. 2) Xxxxxxxxxx právní xxxxxx xxxxxxxxxx požadavek xxxxxxx x čl. 9 xxxxxxxx x. 536/2014, xxxxx xxxxxxxx, aby osoby xxxxxxxxxx žádost xxxxxx xxxxxxx xx xxxxxxxxxx, xxxxx klinického hodnocení, xxxxxxxxx zkoušejících x xxxxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx x neměly xxxxx xxxxxxxx či xxxxxx xxxxx, xxxxx xx xxxxx xxxxxxxx xxxxxx xxxxxxxxxxx.
X xxxxxxxx 2 (Kapitola XX, čl. 4, 6 x 7, čl. 8 xxxx. 4 a Kapitola XXX nařízení) xx xxxxxxxxx xxxxxxxxx xxxxxx xxxxxx. Xxxxx článku 4 xxxxxxxx x. 536/2014 xxxxxx xxxxxxx xxxxxxx xxxxxx xxxxxx x xxxxxxx x xxxxxxxx xxxxxxxx dotčeného členského xxxxx, x xxxxx xxxxxx xxxxxx xxxxxxxx x xxxxxxxx 2 xx především xxxxxxxx xxxxx xxxxxx xxxxxx xxxxxxxx.
X xxxxxxxx 3 xx stanovuje Xxxxxxxx xxxxxx xxx kontrolu xxxxx xxxxxxxxx xxxxxxxx xxxxxxxx xxx činnost xxxxxx xxxxxx (xxxx xxx xxxx).
X odstavci 4 je xxxxxxxxx, xx xxxxxx komise xxxx xxxxxxxxxx na xxxxxxx Xxxxxxx xxxxxxx Xxxxxxx ústavem pro xxxxxxxx léčiv po xxxxxxxxxx xxxxxxxx Xxxxxxxxxxxx xxxxxxxxxxxxx. Xxxxxxx xxx, xxxxxxxxxx činnost etické xxxxxx, xxxxxx xxxx xxxxxx xxxxxx xxx xxxxxxxxxxx souhlasu Xxxxxxxxxxxx xxxxxxxxxxxxx.
X §53x
X odstavci 1 se xxxxxxx xxxxxxx xxxxxx xxxxxx x jednotlivých samostatně xxxxxxxxxxx xxxxxx etické xxxxxx. Xxxx xx xxxxxxx xxxxxxxxx xx xxxxxxx jednotlivých skupin, xxxxx xxxxxxx x xxxxxxxxx xxxxxxx xxxxxxxx xxxxx (XXX X6) x x Xxxxxxxxx xxxxxxxxx, xxx oba xxxxxxxxx xxxx xxxxxxx xxx xxxxxxxxx xxxxxxxxxx xxxxxxx, x tedy x xxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx xx xxxxxx xxxxxxxx xxxxxxxx. Zároveň je x odstavci 1 xxxx možnost flexibilně xxxxxxxx na xxxxxxxx xxxxxxx x xxxx xxxxxxx xxxxxxxxx úpravou Xxxxxxx xxxxxx xxxxxx. Xxxxxxxxx xxxxx xxxx xxxxxxxxxxx xx xxxxxxxx xxx adaptaci xxxxxxxx č. 536/2014, která xxxxxx x xxxxxxxxxx xxxxxxx x délce 3 xxx. X xxxxxx xxxx xxxxxxxxxxx xxxxxx xxxx zadavatel xxxxx, xxx xxxxxxxx xxxxxx x povolení klinického xxxxxxxxx dle nařízení č. 536/2014 nebo dle xxxxxxxx xxxxxx legislativy. X xxxxxxxxxxxxx dvou xxxxxx xxxx xxxxxxxxxxx xxxxxxx x xxxxxxxx xxxxxxxxxx xxxxxxxxx xxx xxx x xxxxxxx x xxxxxxxxx xxxxxxxx č. 536/2014, xxx xxxxxx xxxxxxxx xxxxxxxxx schválená xx xxxxxxxx před xxxxxxx účinnosti xxxxxxxx č. 536/2014 xxxxx plnit xxxxxxxxx xxxxx dle xxxxxxxx platné xxxxxx xxxxxx, xxxx. předkládání x xxxxxxxxxxx xxxxxxxxxx xxxx xxxxxxxxxx xxxxxxxxx Xxxxxxx xxxxxxx xxx xxxxxxxx léčiv x xxxxxxxx komisemi, xxxxx xxxx klinické hodnocení xxxxxxxxx. Xxxxx xxxx xxxxx xxxxxxxxx xxxxxxxxxx xxxxxxx xxxxxxxx xxxxxx, xxx xxxxxxx již xxxxxxxxx nového systému xxxxxxxxxx x této xxxxxx xxxxxx. X xxxxxxx 3 xxxxxx xxxxxxxxxxx xxxxxx bude xxxxxxx xxxxx počet xxxxxx etické xxxxxx xxx Xxxxxxx xxxxxx xxx xxxxxxxx xxxxx xxx xxxxxxxx potřeby, xxxx xx xxxxxx, xx xxxxx skupin xxxxxx xxxxxx xx xxxxxxx (xxxxxxx xxx 3 xxxxxxx) x xx xxxxx xxxxxxxxxxx xxxxxx (za 3 xxxx po nabytí xxxxxxxxx xxxxxxxx č. 536/2014) xxxxxx xxx xxxxxx. Xxxxxxxxx xxxxxxx xxxxxx xxxxx vývoje v xxxx xxxxxxx xxxxxxxxxxx xxxxxx z xxxxx xxxxxxxxxxxxx xxxxxxx o xxxxxxxx xxxxxxxxxx hodnocení x Xxxxx xxxxxxxxx (xxxx-xx stejný xxxxx xxxxxxxxxx hodnocení xx xxxxx xxxx xxxxxx xxxxx xxx x xxxxxxxx době). Xxxxxx xxxxxx xxxxxx bude xxxxxxxxx x xxxxx xxxxx xxxxxx xxxxxx, xxxxx xxxx na xxxxxxx xxxxxxxx xxx xx 12-15 xxxxx x jedné xxxxxxx, xxx praxe xxxx xxxxxx, xx xx xxxx xxxxxx xxxxx xxxxxxx či opačně.
V xxxxxxxx 2se xxxxxxx, xx xxxxx xxxxxx xxxxxx jmenuje x xxxxxxxx xxxxxxx xxxxxxxxxxxxx. Xxxxxxxxxx tohoto odstavce xx zaručuje nezávislost xxxxxxxxxxx xxxxxx komise xx Xxxxxxx xxxxxx xxx xxxxxxxx xxxxx, xxxxx xxxx prostřednictvím xxxxx xxxxxxxxx zaměstnanců xxxxxxxxxx pouze xxxx xxxxxxxxx-xxxxxxxxxxx zázemí x xxxxxxxxxxxxxxx podporu xxxxxxxx xxxxxx xxxxxx. Zaměstnanci Xxxxxxxx xxxxxx pro xxxxxxxx léčiv xxxxxxxxxxx xxxxxxx etické xxxxxx xxxxxxx xxxxx xxxxxx xxxxxx, xxxxxxx zasahovat xx procesu xxxxxx xxxxxxxxxx xxxxxxx xxxxxx xxxxxx x nebudou xx xxxxxxx na xxxxxxxxxxx xxxxxx xxxxxx. Xxxxxx xxxxxx xxxx xxxxxxxxx schůzek, tvorba xxxxxx x jednání, xxxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxx xxxxxx Xxxxxx, x hlavně hlídání xxxxxxxxxx xxxxxxxxxxx xxxx. Xxxxxxxxx xxxxxxxxxxxx členů xxxxxx xxxxxx xxxxxxx xx xxxxxxxx xxxxx xxxxxxxxx xxxxxx Evropské xxxxxx agentury (XXX), xxxxxxx xxxx xxxx. Xxxxx pro xxxxxxx xxxxxxx (XXX), Xxxxx xxx xxxxxxx xxxxxx xxxxxxxxx (XXXX) aj., xxx xxxxxxx xxxxx xx xxxxxxxxxxx, technicky x xxxxxxxxxx xxxxxxx xx Xxxxxxxx xxxxxx xxxxxxxx, xxx xxxxxxx xxxxxxx x rozhodování xx nezávislé.
Dále xx x xxxxx xxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx xx složení skupiny xxxxxx komise x xxxxxx xxxxxx xxxxxxxx x xxxxxxxxxxxxx, jakožto xxxxxx nezávislé xxxxxxxxxx xxxxxxxxxxxx xxxxxx xxxxxx xxxxxx.
X xxxxxxxx 3 xx upraven požadavek xx členy xxxxxx xxxxxx x souladu x požadavky čl. 9 xxxxxxxx x. 536/2014, xxx xxxx xxxxxxxxx xxxxxx nezávislost xx xxxxxxxxxx, xxxxxxxxxxxx x xxxxxxx klinického xxxxxxxxx, xxxxxxx je xxxxxxxx xxxxxxxxx xx xxxxxxxxxx x oblasti xxxxxxxxxx xxxxxxxxx.
Xxxxxxxx 4 vychází x xxxxxxxxx právní xxxxxx, xxxxx xxxxxxxxx xxxxxxxx xxxxxxxxxxx xxxx, xxxxx odstranění xxxxxxxxxx xxxxxxxxx xx xxxxxxx xxxxxxx člena xxxxxx xxxxxx x xxxx xxxxxxxxx x etické xxxxxx, x současně xxxx reflektuje xxxxxxxxx xxxxxxxx správné klinické xxxxx, xxxxxxx dodržování xxxxxxxx č. 536/2014 xxxxxxxx.
Xxxxxxxx 5 pak xxxxxx xxxxxx xxxxxx xxxxxx xxxxxxxxxx xxxxxxxxxxx x xxxxxxxxxxx x xxxxxxxxxxxxx, xxxxx xx xxxxx x xxxxxxxxxxx xx xxxx xxxxxxxxx x xxxxxx xxxxxx.
Xxxxxxxx 6 xxx xxxxxxxxx xxxx, xxx členem xxxxxx xxxxxx xxxx taková xxxxx, xxxxx xx xxxxxxxxx xxxxxxxxx spočívajícího x tom, že xxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxxxx, stanovenou x xxxxxxxx 5. Xxxxx xx člen xxxxxx xxxxxx takového xxxxxxxxx xxxxxxx, xxxx xxxxxxxx x xxxxxx komisi xxxxxxx přímo ze xxxxxx.
X §53b x §53x
Xxxx xxxxxxxxxx xxxxxxx xxxxxxxxx xx xxxxxxx xxxxxx xxxxxx, xxxxx xxxxxxxxx x xxxxxxxx č. 536/2014 x xxxxxxx xxxxxxxx praxe XXX X6. Obě xxxxxxxxxx xxxxxxx ze skutečnosti, xx xx každé xxxxxxx o klinické xxxxxxxxx bude xxxxxxxxx xxxxxxxxxxx, která xxxx xxx xxx samostatné xxxxx –xxxxxxxxxxx, xxxxxxxx xx xxxxxxx, xx xxx se xxxxxxxx xxxx I hodnotící xxxxxx, která xx xxxxxxxx pro xxxxxxx xxxxxxx XX (Protokol, Xxxxxxxxxxxx´xXxxxxxxx, xxxxxxxxxxxxx dokumentace xx.), x dokumentace, xxxxxxxx se aspektů, xx něž xx xxxxxxxx xxxx II xxxxxxxxx xxxxxx, která xx konkrétní x xxxxxxxx xx xxxx xx konkrétnímu XX (Xxxxxxxxx xxx xxxxxxxx, xxxxxxxxxxx souhlas, seznam xxxxxxxxxxxx, xxxxx xxxxxxxxxx xxxxxxxxx, xxxxxxxxx xxxxxxxxx xx.). Dokumentaci, xxxxxxxx xx xxxxxxx, na xxx xx xxxxxxxx xxxx I xxxx xxxx XX xxxxxxxxx xxxxxx bude xxxxx xxxxxxxxx xxxxxxxxxx a xx x x xxxxxxx xxxxxx, xxx. 2 xxx. Xxx xxxxxx xxxx xxxx xxxxxxxxx vypracovat xxxxxxxxx xxxxxx (xxxxxxxxxxx xxxxx xxxxxxxxx dle xxxxxxxxxx Xxxxxxxx xxxxxx x Xxxxxxxx xxxxxx agentury (XXX), xxxx xx xx xxxx xxxxxxx x rámci xxxxxxxxxxxx xxx XXX). X xxxxx xxxxxxxxx xxxxxx xxxx xxxxxx xxxxx xxxxxxxxx xxxx žádosti, xxxxx xxxx xxxxxxxxx xxxxxxxxxx, x to xxxxxxxxxxxxxxx xxxxxxx. Xxxxxxxxx xxxxxxxxxx xx xxxxxxx xxxx bude xxxxxx xx po xxxxxx xxxx závěrů xxxxxxxx xx xxxxxxx, na xxx xx xxxxxxxx xxxx X x xxxx II hodnotící xxxxxx. Xxx bude xxxxxx xxxxxx xxxxxxxxxxxxx, xxx. xxxxxxxxx zpráva x xxxxxxxxxx x xxxxxxxxxx, na xxxxxx xxxxxx se xxxx x xxxxx xxxxxxxxxxxx xxx Xxxxxxxx xxxxxx xxxxxxxx xxxxxxx.
Xxxxxxxxxx §53b x xxxxxxxx 1 xxxxxxx xxxxxxxxxx etické xxxxxx x xxxxxxxxx xxxxxxx xxxxxxxx praxe XXX X 6 x Helsinské xxxxxxxxx xx xxxxxxxxx xxxxxxx xxxx, bezpečnosti x xxxxxx lidských xxxxxxxx xxxxxxxxxx xx výzkumu x xxxxxxxxx xxxxxxxx xxxxxxxxx. Xxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxxx a xxxxxxxxxxxx xxxxxxxxxxx xxxxxxxxxx xxxxxx xxxxxx, jak xx xxxxxxx v Xxxxxxxx XX, článku 8 xxxx. 4 xxxxxxxx x. 536/2014.
Ustanovení §53b x odstavci 2 xxxxxxx x xxxxxxxxx Xxxxxxxx XIII nařízení č. 536/2014, xxxxxxx klinické xxxxx XXX E 6 x Helsinské xxxxxxxxx, které xxxxxxxx xxxxxx xxxxxx xxxxxx xxx xxxxx klinického xxxxxxxxx, xx kterým xxxx xxxxxxx. Xxxxxx xx prováděn xx xxxxxxx písemných xxxxx x xxxxxxx xxxxxxxxxx xxxxxxxxx x xxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxxxxxxx xxxxxxxxxxx nebo hlavním xxxxxxxxxxx, je-li xxxxx (XXX X 6, xxxx 4.10.1: „Theinvestigatorshouldsubmitwrittensummariesofthe xxxxx status to xxx XXX/XXX annually, xx xxxx frequentlyifrequested xx xxx IBR/IEC.“, xxx XXX/XXX xx xxxxxx InstitutionalReviewBoard/Independent EthicsCommittee). Xxxxx xxxx x xxxxxxxxxx dohled xx Xxxxxxx xxxxxxx xxx xxxxxxxx léčiv, xxxxx Xxxxx xxxx xxxxxxxxx xxxxxx nad xxxxxxxxxx xxxxxxxxxx xxxxxxxxx prostřednictvím xxxxxxxx xxxxxxx xxxxxxxx xxxxx, případně xx xxxxxxx xxxxxxxxx xxxxxxxxx xx zpráv x xxxxxxxxxxx přípravku, hlášení xxxxxxxxxx xxxx xxxxxxxxxx xxxxxxxxx a s xxx souvisejícího přehodnocení xxxxxx xxxxxxx a xxxxxx xxxxxxxxx s xxxxxx subjektu xxxxxxxxx x xxxxx klinickém xxxxxxxxx, xxxxxxxx x xxxx úřední xxxxxxxx Xxxxxx (spolupráce x xxxxx skupiny ClinicalTrialsFacilitation Xxxxx (CTFG), XxxxxxxxxxxxXxxxxxxxXxxxxxxxx (XXX), Committeeformedicinalproductsforhuman xxx (XXXX) x jiných).
Ustanovení §53x v odstavci 3 xxxxxxx z xxxxxxxxx Xxxxxxxx XX článek 10, x xxxx článku 5 xxxx. 7 xxxxxxxx č. 536/2014 x xx správné xxxxxxxx xxxxx XXX X6, článku 3.2.6 (Xx XXX/XXX mayinvitenonmemberswithexpertise xx xxxxxxxxxxxxxxxxxxxxxxxxx.)
Xxxxxxxxxx §53x x xxxxxxxx 4 xxxxxxxxx etické komisi xxxxxxxxx xxxxxxxxx svou xxxxxxx x souladu x xxxxxxxxx nařízení č. 536/2014 x Xxxxxxxx xxxxx. (více viz xxxx).
Xxxxxxxxxx §53b x xxxxxxxx 5 xxxxx, xx jednotlivé činnosti xxxxxx xxxxxx xxxxx xxxxxxxxx xxxxx xxxxxxxxxx xxxxxxx (XXX X6, xx. 3.2.2 Xxx XXX/XXX shouldperformitsfunctionsaccording xx xxxxxxxxxxxxxxxxxxxxxxxxxx), xxx xx xxxx xxxxxxxx xxxxxxxx x xxxxxxxxxxxxx postup xxxxxxxxxxxx xxxxxx xxxxxxxx xxxxxx. Xxxxxxxx xxxxxx xxxxxxx xxxx xxxx, xxx budou xxxxxxx xxxxxx xxxxxx nakládat x xxxxxxxx zadavatelů, xxxxxxx jsou xxxxxxx xxxxxxxxxxx xxxxxx - Xxxxxxxx VII, Xxxxxxxx XXXX čl. 53 nařízení, xxx je xxxxxxx, xx xx zadavatel xxxx xxxxxxxxx „xxxxxxxx xxxxxxxx xxxxxx“, xxx. xxxxxxx xxxxxxxxxxxx se xxxxxxxxx xxxxxxxxx v Xxxxx republice (Xxxxx x xxxxxx xxxxxx), xxxxx xx xxxxxxx xxx x xxxxxx xxxxxxxxxxxxx; xxxx xxx xxxxx xxxxxxxxxxx Xxxxxxxxxxxx´xXxxxxxxx, x v neposlední xxxx dle Xxxxxxxx XXXX, čl. 52 z xxxxxxx xxxxxxxx xx xxxxxxxxx; další hlášení xxxx získávat xxxxxx xxxxxx xx xxxxxxxxxxxx, xxxxx x zprávy x průběhu xxxxxxxxxx xxxxxxxxx x xxxx xxxxxxx xxxxxxxxx xxxxxxxx xx xxxxxxxxx (Xxxxxxxx XXX, čl. 53 xxxxxxxx). Xxxx pracovní xxxxxx xxxx x xxxxxxxxx xxxxxxxxxx xxxx etickou xxxxxx x Xxxxxxx x zajištění xxxxxxxxx xxxxxxxxxx xxxxxx xxxxxx. Xxxxxxxx xxxxxxx budou xxxxxxxxxx xxxxxxxx xxx xxxxxxxxxx činnosti xxxxxx xxxxxx xxxxxxxxxxx x xxxxxxxxx xxxxxxxx č. 536/2014, x xxxxxxxxx harmonizace xxxxxxxx.
Xxxxxxxxxx §53c x xxxxxxxx 1 x 2 vychází x xxxxxxxxx nařízení č. 536/2014 kapitoly XX xxxxxx 4 x xxxxxxxxx xxxxxxxx xxxxxxxx. Xxxx xxxxxxxx xxxxxxxxxxx xxxxxxxx etické komise xx posouzení xxxxxxxxxxx, xxxxxxxx xx xxxxxxx, xx xxx xx xxxxxxxx xxxx X xxxxxxxxx xxxxxx, xxx xxx povolení žádosti x xxxxxxxx hodnocení, xxx pro povolení xxxxxxx x xxxxxxxxx xxxxx klinického xxxxxxxxx. Xxxxxx xxxxxxxxx xxxxxxx xx xxxxxxxx praxe; xxxxxx komise bude xxxxxxxxx (Xxxxxxxx II, čl. 6 xxxx. x) xxx x + Příloha č. I, xxxx. X) xxxxxxxxxxxxxx xxxxxxxxx klinického xxxxxxxxx, xxxx xx xxxxxx xxxxxxxxxx, xxxx xxxxxxxxx chce xxxx xxxxxxxx xxxxxxxxx xxxxxxxx (xxxx. nemají xxx xxxxxxxxx xxxxxxxx xxxxxxxxx, xxxxx xxxxxx xxxxxxx xxxxxx, xxxx. xxxxxxx xxx dávno prokázané, xxxx xxxx xxxxxxxxxx, xxx. xxxxxxxxx xxxxx xx xxx xxxxxxxxx x xxxx xxxxx xx x ní xxxxxx) x xxxxxxxxxx xxxxxxxxxx xxxxxxxxx, jímž xx xxxxxx xxxxxxxx xxxxxx (bude-li klinické xxxxxxxxx xxxxxxxxxxxxxx či xxxxxxxxxxxxx, s xxxxxxxxxxx xxxxxxxxx x xxxxxxx xxxx, jedná-li xx x xxxx I xx XX klinického xxxxxxxxx xxx xxxxx xxxxxx léčivého xxxxxxxxx, xxxx-xx xxxxxxx xxxxxxx xxxx aktivní xxxxxxxxxx, xxxxx-xx xx x xxxxxxxx hodnocení xxxxxxx xx xxxxxxxxxxx, xxxxxxxxx, xxxxxxxxx, xxxxx-xxxxx xx.). Xx xxxxxxx xxxxx xxxxxxxxx xxxxxxxxx xxx xxxxxxx poměr xxxxxxx x xxxxx xxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxx x xxxxxx xxxxxx x klinickém xxxxxxxxx.
Xxxxxxxxxx §53x x xxxxxxxx 3 xx 5 xxxxxxxx xxxxxxxxx xxxxxxxxx dokumentace, týkající xx xxxxxxx, xx xxx xx xxxxxxxx xxxx II xxxxxxxxx xxxxxx xxx území Xxxxx xxxxxxxxx. V xxxxxx xxxxxxxxxx xx xxxxxxx xx xxxxxxxx xxxxx x xxxxxxxxx xx x xxxxxx xxxxxxxxxx xxxxxxx žádostí xxxxxxxx xx xxxxx xxxxxxxxx xxxxx (informace xxx pacienty, xxxxxxxxx xxxxxxxxxx a xxxxxxxxxxxx, xxxxxxxxxxx xxxxxxxxxxxx, xxxxxxxxxxx xxxx klinického xxxxxxxxx, xxxxxxxxx xxxxxxxxx xxxxxxxxxx x xxxxx a xxxx…) x xxxxxxxxxx xxxxxx xxxxxx.
Xxxxxxxxxx §53x x odstavci 6 xxxxxx xxxxxxxxxxx za xxxxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxxxx etické xxxxxx.
Xxxxxxxxxx§53x x odstavci 7 x 8 blíže xxxxx možnosti, x xxxxxx xxxxxxxxx xxxx xxxxxxx etická xxxxxx xxx xxxxxxxxx xxxxxxxxxx x xxxxxxx xxxxx xxxx náležitosti. A xxxx xxxxxxx x xxxxxxxxx Xxxxxxxx XX článku 4 xxxxxxxx x. 536/2014, kde je xxxxxxxxx xxx členský xxxx xxxxxxxxx xxxxxxxx xxxxxxxxxx xxxx xxx xxxxxx xxxxxxx. Xxxx xxxxxxxxxx xx skládá x následujících xxxxx: 1. xxxxxxxx = xxxxxxxx xxxxx xxxxxxxxxxx xx formální stránce, 2. xxxxxxxxx - xxx xxxx X xxxxxxxxxxx (xxx xxxxxx xxxxxx - Protokol, Xxxxxxxxxxxx´xXxxxxxxx - posouzení x vypracování draftu xxxxxxxxx zprávy = xxxxxxxx xxxxxxxx a xxxxxxx event. xxxxxxxxxx, 3. vypořádání xxxxxxxxxx xx. odpovědi xxxxxxxxxx, 4. kompilace finální xxxxxxxxx zpráva x xxxxxxxxxx (povolení/povolení x xxxxxxxxx/xxxxxxxxx). To jsou xxxxxxxxxx xxxxx, xx xxxxx xx xxx xxxxxxxxx č. 536/2014 xxxxxxxx, xxx. xxx. čas xxx xxxxxx xxxxxxxxxx/xxxxxxxx. Xxxxx xxxxxx xxxx xxxxxx xxx xxxxxxxxx xxxxxxxxxxx, xxxxxxxx xx xxxxxxx, xx něž xx xxxxxxxx část X hodnotící xxxxxx, xxx x xxxxxxxxxxx, xxxxxxxx xx xxxxxxx, xx xxx xx xxxxxxxx xxxx XX xxxxxxxxx zprávy klinického xxxxxxxxx. Dle Xxxxxxxx XX čl. 4 xxxxxxxx x. 536/2014 xx xxxxxx xxxxxxx xxxxxxxxx xxx xxx posouzení xxxxxxx x xxxxxxxx xxxxxxxxxx xxxxxxxxx, xxx x xxx xxxxxxxxx xxxxxxx x xxxxxxxx xxxxxxxx změny.
Ustanovení §53x x xxxxxxxx 9 xxxxxx Xxxxxxxx xxxxxx xxx xxxxxxxx xxxxx, xxxxx xxxx etická xxxxxx orgánem Xxxxxx, xxxxxxxxx xxxxxxxxxx xxxxxxx x činnosti xxxxxx xxxxxx xx dobu 5 let.
K xxxxxxxxxx xxxxxxxxxx xxxxxx xxxxxx xx uvádí, xx xxx xxxxx nařízení, xxxxx xxxx stanovisko XX xxxxxxxxx, xxx Xxxxx žádost x xxxxxxxx xxxxxxxxx xxxxxxx. Xxxxxxxxx závaznost xxxxxxxx xxxxxxxx, lze ji xxxx dovodit. Xxxxxx xxxxxx xxxx o xxxx xxxxxx xxxxxxx xxxxx xxxxxxxxxx. Xxxxxxxxxx x žádosti x xxxxxxxx xxxxxxxxxx xxxxxxxxx xxxx xxxxxxxx xxxxxxxx xxxxx bude xxxxxxx Xxxxx, a xx x xxxxxx xxxxxxxxx xxxxxx. Vždy xxxx xxxxx se xxxxxxx xxxxx rozhodnutí, xxxxx xx xxxx xxxxxxxx xx xxxxxxxxxx xxxxxxx xxxxxxxx etické komise, x tomto smyslu xx stanovisko etické xxxxxx povahu xxxxxxxxx xxxxxxxx pro rozhodnutí. Xxxxxxxx xxxxxx bude xxx xxxxxxx xxxxxx xxxxx závěrům xxxxxx xxxxxx prostřednictvím odvolání xxxxx xxxxxxxxxx Xxxxxx.
Xx xx xxxx xxxxxxxx xxxxxxxxxx xxxxxxx komisí xx xxxxxxx přezkumu, x xxxxx xxxxxx xxxxxxxx. Xxxxxx xxxxxxxx xxxxxxxxxx xx xxxxxx xxxxxxxxxxxxxx v xxxxxxxxxx §53x.
X §54 (Xxxxxxxx XXXX, xx. 49 x 50, Kapitola XX, čl. 73 xxxxxxxx):
Xxxxxxxxxx xx xxxxxx xxxxxxxxxxxx a xxxxx xxxxxxxxxx xxxxxxxxx. Čl. 49 xxxxxxxx x. 536/2014 xxxxxxxxx xxxxxxx xxxx x tomu, aby xxxxx, kdo může xxx xxxxx xxxx xxxxxxxxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxxxx xx xxxxxxx xxxxxxxxxxx. Podle xxxxxxxxxx xxxxxx úpravy xxxxxxxxxxx x xxxxxxx zkoušejícím xxxx být pouze xxxxx xxxx xxxxx xxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx zákonem č. 95/2004 Sb., xx xxxxx xxxxxxxxxx xxxxxxxx, pro xxxxx xxxxxx xxxxxxxxxxxxxx xxxxxxxx, xxxxx xx xxxxxxxx xxxxxxx xxxxxxxx a xxxxxxxxxx x xxxx x xxxxxxxx x xxxxxxxxxxx xx stavy, xx xxxxxxx léčbu xx zaměřuje xxxx xxxxxxxx xxxxxxxxx x xx znalosti správné xxxxxxxx xxxxx.
Xxxxxxxx 2 xxxxxxx z xxxxxxxxx čl. 50 nařízení x. 536/2014 xx místa xxxxxxxxxx xxxxxxxxx. Xxxxx xxxxxxxxxx xxxxxxxxx mohou xxx jen x xxxxxxxxxxxxx zdravotních xxxxxx xx zdravotnických zařízeních, xx. xxxxxxxx xxxx, xxxxx jsou podle xxxxxx oprávněny x xxxxxxxxxxx xxxxxxxxxxx xxxxxx xxxxx xxxxxx č. 372/2011 Sb., xx xxxxx xxxxxxxxxx xxxxxxxx, a xxxxxx xxxxxxxx bude posuzována xxxxxxxxxx xxx každé xxxxxxxx hodnocení xx xxxxxxxxxxx xxxxxxxxx xx xxxxxxxxx xxxxxxxx x xxxxxxxxxx zajištění xxxxxxxx x xxxxxxxxx daného xxxxxxxxxx hodnocení.
Odstavec 3 x 4 stanovuje xxxxxxxxxxx xx xxxxxxxxxxxx xxxxxxxxx pro xxxxx xxxxxxxxxx xxxxxxxxx získat xxxxxxxxxx xxxxxxx xxxxxxxx xxxxx, vydaný Ústavem. Xxxxxxx xxxxxxx xx xxxxxxxxxx znění xxxxxx x léčivech a xxxxxxxx xxxxx, x xxxxxxxx pro xxxxxxxx xxxxxxx v xxxxxxxx 3 povinnost xxxxxx xxxxx certifikát, a xx x xxxxxx, xx xx jedná x xxxxx x xxxxxxxx xxxxxxxxx, která xxxxxxx xxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx (první xxxxxx člověku) xxxx xxxxxxxx xxxxxxxxx xxx xxxxxxxxx xxxx preventivního xxxxxxx xxx zúčastněné xxxxxxxx hodnocení (xxxxxxxxxxxxxxx xx farmakokinetická xxxxxxxx xxxxxxxxx).
X §55 (Xxxxxxxxx (26); Xxxxxxxx IV, xx. 26 xxxxxxxx x. 536/2014):
X tomto xxxxxxxxxx xxx o xxxxxxxx čl. 26 x 69 nařízení x. 536/2014, podle xxxxx xx měl členský xxxx určit xxxxxxxx xxxxxxxxx na dokumentaci xxxxxxxxxx xxxxxxxxx x xxxx xx xxx xxxxx xxxxx informací xxxxxxxxx v označení xx xxxxx. X §55 se vychází x xx zásady, xx xx xxxxxxxxx x xxxxxxxxxxx xxxxxxxxxx xxxxxxxxx, xx xxxxxxx xxxxxxxx xx xxxxx xxxxxxx xxxxxxxxx, xxxx xxx xxxxxxxxxx v xxxxxxx. Mimo jiné xxx xxxxxxxxx o xxxxxxxxx xxx pacienta, xxxxx pacienta, xxxxx xxx xxxxxxx studijní xxxxxxxx a návod x používání zdravotnického xxxxxxxxxx. Požadavek xx xxxxx znění xxxxxxxxx xx xxxxxx i xxx xxxxxxxxx, u xxxxx xx x xxxxxxx na vysokou xxxxxxxxx daného textu xxxxx dojít xxx xxxxxxx xxxxxxxx xx xxxxxxx jazyka k xxxxx interpretaci, například xxxxxxxx smlouvy. Xxxxxxx xxxxxxxxx x xxxxxxxxxxx xxxxxxxxxx xxxxxxxxx xx xxxxxxxxxxx x xxxxxxx, xxxxxxxxxxx xxxx xxxxxxxxxx. Xxxxx xxx x xxxxx informací xxxxxxxxx x xxxxxxxx xx xxxxx xxxxxxxx xxxxxxxxx xxx xxxxxxxx xxxxxxxxx, xxxxx xx určuje xxx, xx xxxxx xxxxxxx je čeština, xxxx-xx x xxxxxxxxxx Xxxxxxxx xxxxxx xxx xxxxxxxx xxxxx x xxxxxxxx klinického xxxxxxxxx xxxxxxx jinak. Xxxxxxx xxxxxxxx cizojazyčného xxxxx xxxxxxx ze xxxxxxxxxxx, xx x xxxxxxxxx xxxxxxxxxxxxx klinických hodnocení, xxxxx mají zařazen xxxxx nízký xxxxx xxxxxxxx (xxxxxx oblasti xxxxxxxx xxxxxxxxxx) by xxxx xxxxxxxxxxxx nárokem x zátěží xxx xxxxxxxxxx, xxx x xxxxxxxxx, které xxxxxx xxxxx, xxxxxxxxxx celé xxxxxxxx na obalu x xxxxxx xxxxxx. Xxxxxxxxxxxx xxxxxxxx xx xxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxx do xxxxxxxxx xxxxx xxxxxxxx xxxxxxxxx x xxxxxx xx xxxxxxx xxxxxxx xx v tomto xxxxxxx mohlo xxxx x xxxxxxxxx Xxxxx xxxxxxxxx x xxxxxxxxxx xxxxxxxxx, x xxxx xx xxxxxxxxxxxxxx xxxxx xxxxxxxx v xxxxxxxx x xxxxx xxxxxxx xxxxxxx xxxxxxxxxx. Xxxxxxxxxx xxxxxxxx xxxxxxxxx bude xxx xxxxxxxxx požadavkem xx xxxxx xxxx xxxxxxxxx x xxxxx, xxxxx bude xxxxx x přípravkem x xxxxxxxxxxxx xxxxx xxxxxxxxxxxx xxxxxxxxxxx a ti xxxxx povinni xx x xxx seznámit, xxx byli xxxxxxx xxxxxxxx xxxxxxx používání x zacházení s xxxxxxxxxx léčivým přípravkem.
K §56 (Xxxxxxxx XXXX, xx. 59 xxxx. 3; Xxxxxxxx XX, xx. 61 odst. 5 xxxx. x), xx. 68; Kapitola XXXXX, xx. 90 x 92 xxxxxxxx x. 536/2014):
X xxxxx xxxxxxxxxx xx především xxxxxxxx xx xxxxxxxxxx čl. 59 xxxx. 3 xxxxxxxx č. 536/2014, xxxxx vyžaduje, xxx xxxxxxx xxxx xxxxxxxx, xx za xxxxxx xxxxxxx x klinickém xxxxxxxxx budou xxxx xx jeho xxxxx xxxxxxxx neregistrované pomocné xxxxxx přípravky. X xxxxxxxx 2 se xxxxxxx xxxxxxxxx xxxxxx xxxxxx, xxxxx xx xxxxxxxxx xxx, xx xx xxxxxxxx uvádí xxxxxxx za xxxxxxxxxxx xxxxxxxx použít x xxxxx xxxxxxxxxx xxxxxxxxx x takové xxxxxxxxxxxx xxxxxxxxxx, které jinak xxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxx x xxxxxxxxxxxxxx xxxxxxxxxxxx. Tento xxxxxxxxx xxxxxxx x xxxxxxxxxx xxxxx zajistit xxxxxxxx x xxxxxxxxxx dat, xxxxxxxxx x klinického xxxxxxxxx. Toto xx xxxxxxxxx např. právě xxxxxxxxxxxxx xxxxxx použitím xxxxxxx typu xxxxxxxxxxxxxx xxxxxxxxxx xx xxxxx xxxxxxxxxxxx xxxxxxx (xxxxxxx xxxxx XX i 3. xxxx) x xxx x xx xxxxx xxxxxxx xxxxxxxxxx xxxxxxxxx. X xxxxxxxxxx xxxxxxxxx, xxxxx xxxx xxxxxxxx xx xxxxxxxxx xxxxxx xxxxxxxx, xxxxx xxxxxx xx provádí xxxxxxxxxxxxx prostředkem, x xxxxxxxxx takového klinického xxxxxxxxx xx usazen xx xxxxx zemi (xxxx. USA) xx xxxxxxxx xxxxxxxxxx xxxxxxxxxx, xxx xxxxxxx xxxxxxxxxx xxxxx používaly xxxxxxx, xxx xxxxxx xxxxxxxxxxxx xxxxxxxxxx xxx, xxx xxxxxxxx xxxxxx xxxxxx xxxxxxxxx xxxxxxxxxxx xxxxxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxxx. Používání xxxxxxxx xxxxxxxxxxxxxx prostředku xx xxxxxxxxx xxxxxxxxxx xxxxxxxxx xxxx zadavatele x xxxxxxxxx xxxx xxxxx tento xxxxxxxxxxxx xxxxxxxxxx na xxxxx Xxxxxxxx unie použít xxxxx xxx x xxxxx xxxxxxxxx hodnocení, x xx xxxxxxx x xxxxxxx na xxxxxxxxxx, že mnohdy xxx není xxxxxxxx xxxxxx xxxxxxxxxxxxxx xxxxxxxxxx. Xxxxxx pro xxxxx xxx xxx xxxxxxx, xxxxx xxxxxxxxxxxxx pro xxxxxxxx xxxxxxxx xxxxxxxxxx xxxxxxxxx xxxx tento xxxxxxxxxxxx xxxxxxxxxx xxxxxx xxxxxxxxxx, x xxxx xx nebude xxxxxxxxxx x Xxxxx republice. X xxxxxxx, že xx tato xxxxxx xxxxxx akceptována, xxxxx xxxxxxxxx Xxxxx xxxxxxxxx x xxxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxxxxxx, xxxxxxxx xxxx xxxxxxxx benefity xxx xxxxxxxxxxx populaci x Xxxxx xxxxxxxxx. (Xxxxxxxxx může být xxxx. xxxxxxx xxxxxxxxxx xxxxxxxxxxx x xxxxxxxxxxx xx 3. xxxx (XXX), xxxxx xxxxxx xxxx klinické hodnocení x České xxxxxxxxx xxxxxxxx. Jeho povolení xxxxxxx v xxxxxxxxx xxxxxxxxx xxxxxxx možnost xxxxx novým vyvíjeným xxxxxxxxxx, který xx xxxxxxxx xxxxxxxxxx může xxx dostupný x xxx české xxxxxxxx, x to i xxxxxx, že xxxxxxxxx xxxxxxxxx x xxxxx xxxxxxxxxx xxxxxxxxx xxxx xx jeho xxxxxxxx xxxxxx xxxxxxxxxxx x xxxxxxx x Xxxxx xxxxxxxxx, registrace xxxxxxxxxxx xxxxxxxx přípravku x xxxx xxxxxxxxxx na xxxx v České xxxxxxxxx xxxx xxxxxxxxx xxxxxxxxxxx xxxxxx zdravotnického xxxxxxxxxx, xxx xxxx xxxxxxx x xxxxxxxxx xxxxxxxxx xxxxxxxxx validitu x xxxxxxxxxx xxx. Xxxxx xxxxxxxxx může xxx zdravotnický xxxxxxxxxx xxxxxxxx xxx xxxxxxxxxx xxxxxx, xxxx. xxxxxx xxxx odebíraný xx xxxxxxxxx xxxxxxx, která xxxxxxx jeho xxxxxxxx x xxxxxxxx kvalitě xx xxxxxx xxxxxx, xx jeho dodání xx xxxxxxxxxxxxxx laboratoře x xxxxxxxxx. Použití xxxxxxxx xxxxxxxxxxxxxx xxxxxxxxxx xxxxxx neovlivní případnou xxxxxxxxxx xxxx xx xxxxxx xxxxxxxxxx, ale xxxxxx xxxxxx xxxxx xxxxxx xxxxxxxx v xxxxx xxxxxxxxx xxxxxxxxx x xxx x xxxxxxx léčby zatím xxxxxxxxxxxxxxx xxxxxxx xxxxxxxxxx).
X xxxxxxxx 2 se xxxxxxxx xxxxxxxxxx xxxxxxxxxx, xxxxxxx jsou xxxxxxxxxxxx xxxxxxxxxxx xxxxxx xxxxxxx xxxx xxxxxxxx státem xxxx územním xxxxxxxxxxxx xxxxxx, xxxxxxx xxxxxx xxxxx xxxx veřejná xxxxxxxx xxxxxxxxx, čímž xx xxxxxxx prostor xxx to, xxx xxxxxxx xxxx xxxx x některých xxxxxxx xxxxxxxxx xxxx přísné xxxxxxxxx, xxx x xxxx xxxxxxx xxxxx xxxxxx xxxxxxxxx xxxxxxxx.
X xxxxxxxxxx 3 až 5 xx xxx x xxxxxxx s xxxxxxxx xxxxxxxx xxxxxxxx xxxxxxx, xxx xxxxxxxxx xxxxxxxxx spolu s xxxxxxxxxxx xxxxxxx x xxxxxxxx xxxxxxxxxx hodnocení xxxxxxxx xxxxxxxx xx xxxxxxxx xxxxxxxxxxx státních xxxxxx. Jde x xxxxxxxxxxxx ustanovení čl. 92 xxxxxxxx x. 536/2014, xxxxx xxxxx xxxxx xxxxxxxxx xxxx xxxxxxx xxxxxxxx členských xxxxx xxxxxxxxxx xxxx zdravotní xxxxxxxx x organizovat xxxxxxxxxxxxx x xxxxxxxxxxx xxxxxxxxx péče. X xxxxxxx xx xxxxxxxx xxxxx xxxx xxxxxxxxx, xxx xxxxxx xxxxxxxxxx xx strany xxxxxxxxx xxxxx vede x xxxxxxxxxx tichému xxxxxxxx x klinickým hodnocením (xxxxxxxxx xxx xxxxxxxx xxxxxxxxx podmínek klinického xxxxxxxxx) xxxx x xxxxxx časových xxxxxxx xxxxx xxxxxxxxx xxxxxxxxx xxxxxxxxxxx orgánů xx xxxxxx Xxxxxxxx xxxxxx xxx xxxxxxxx xxxxx, xxx xx x xxxxxxxx důsledku vedlo x xxxxxxxxxx xxxxxxxxx xxxxxxxx klinických xxxxxxxxx xx území České xxxxxxxxx.
X xxxxxxxx 6 xx v xxxxxxx x xxxxxxxxx xxxxxxxx č. 536/2014, xxxxxxxxx (11) xxxxxxx možnost předložit xxxxxxxxxxxxx xxxxxxxxxxx xxxxxxxxxx xxxxxxxxx u xxxxxxxxxxxxxxxxxx x klastrových xxxxxxxxxx xxxxxxxxx xxxxxxxxxxx xxxxxxxxxxxx xxxxxxxxxx, xxxx by xxxx ohrožena xxxxxxxxxx xxxxxxxxxxxx xxxxxxxx xxxxxxxxx x xxxxxxxx xxxxxxxxx xxx.
X §57 (Xxxxxxxx XXX, xx. 42 xxxxxxxx x. 536/2014):
Toto xxxxxxxxxx x xxxxxxx x čl. 42 xxxx. 3 xxxxxxxx x. 536/2014 xxxxxxxx, aby Xxxxxx ústav xxx xxxxxxxx léčiv xxx xxxxxxx xxxxxxxx xxxxxxxxxxx x tomto nařízení xxxxxxx se zadavatelem xxxxxx, podle xxx xxxx xxxxxxxxx xxxxxxxxx xx xxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxx hlásit xxxxx xxxxxxxx přímo Xxxxxx. X případě xxxxxxxx takové xxxxxx xxx xxxxxx podezření xx závažné neočekávané xxxxxxxxx účinky agentuře xxxxx xxxxxxxxxx Xxxxx. Xxxxxxxx č. 536/2014 přímo xxxxxxxxx xxxx xxxxxxxxx xxxxxxxxx xxxxx.
X §58 (Xxxxxxxx XXX, xx. 76 xxxxxxxx x. 536/2014):
Xxxx xxxxxxxxxx je xxxxxxxxxxxx článku 76 xxxx. 1 xxxxxxxx č. 536/2014, xxxxxxxxxxx členským xxxxxx xxxxxxxxx zajistit, xxx xxxx zavedeny xxxxxxx xxxxxxx xxxxxxxx xxxxx (újmy xxxxxxxxx x xxxxxxxxxxx), xxxxxx xxxxxxx xxxxxxxxx xxxxx x xxxxxxxxxxx s xxxxxx v xxxxxxxxx xxxxxxxxx xxxxxxxxxx xx xxxxxx xxxxx, a xx x podobě xxxxxxxxx, ručení nebo xxxxxxx xxxxxx, xxxxx xx rovnocenná, xxxxx xxx x xxxx, x xxxxxxxxx xxxxxx x míře rizika.
V xxxxx ustanovení xx xxxxxxxx xxxxxxx, že xxxxxxx-xx xxxxxxxx xxxxxxxxxx xxxxxxxxx x důsledku xxxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxxxxx xx majetková xxxx, x xx xxxxxxx xx xxxxxx xxxx na xxxxxx, xx xxxxxxxxx xxxxxxx xx xxxxxxxx x xxxxxxx s xxxxxx xxxxxxxx předpisy, xxxxxxx xx xxxxxxxx xxxxxxxxx xx příslušná xxxxxxxxxx xxxxxxxxxx xxxxxxxx.
Xxxxxxxx xxxx xxxx xxxxxxxx státům xxxxxxx xxxxxxxx nižší xxxxxxxx xxx nekomerční xxxxxxxxxx. X preambuli č. 81 xxxxxxxx x. 536/2014 xx hovoří x xxxxxxxx xxxxxxx xxxxxxxxxxxx zadavatelů tím, xx xxxxxxx státy x xxxxxx xxxxx xxxxxxx příslušná xxxxxxxx. Xxxxxxx opatřením xxx xxxxxxx xxxxxxx nekomerčních xxxxxxxxxx je xxxx xxxxxxxxxx xxxxxxxxxx xxxxxxx x xxxxxxxx 3, xxxxx využívá při xxxxxxx stanovených podmínek xxxxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxx xxxxxxxx. Xxx xx xxxxxxx vytvářejí xxxxxxxxxxx xxx to, xxx komerční subjekty xxxxxxxxxxx xxxxxxxx xxxxxx xxxxxx xxxxxxxxxxxxxx a xxxx xxxxx xxxxxxxxx xxxx subjekty xxxxxxxxxx.
X §59 (Xxxxxxxx X, xx. 2 xxxxxxxx (20); Kapitola XI, xx. 74 xxxxxxxx x. 536/2014):
Xxxxxxxxxx xx xxxxxxx xxxx xx xxxx v xxxxxx č. 268/2014 Sb., x xxxxxxxxxxxxxx xxxxxxxxxxxx x x xxxxx zákona č. 634/2004 Xx., x xxxxxxxxx poplatcích, ve xxxxx xxxxxxxxxx předpisů, xxxxxxx plné moci xxxxxxxxx, xxxxx xxxxxx xxxxxxxxx ve xxxxxxxxx xxxxxxxx xxxxxxx xxxx xxxxx xxxxxxxxx xxxxxxxx xxxxxxxxxx, xx xxxxxxxxx xxxxx. Xxxxx xx x xxxxxxxxxx xxxxxxxxx x xxxxxxxxxx §30 xxxx. 5 xxxxxxxxx xxxx, xxxxx xxxxxxxx xxxxxxxxx oprávnění subjektu xxxxxxxxxxx xx xxxx xxxx. Xxxxxxxxxx xxxxxx xx xxxx xxxxxxxxxx xxxxxxxxxx xxxxxx xxxxxxxx, xxx xx xxxxxxxxx xxxxxxxxx xxxxxxxxx.
Xxxx xxxxxxxx, xxxxx mezi sebou xxxxxxx xxxxxxx xxxxx, xx jehož xxxxxxx xxxx xxxxxxxxx xxxxx xxxxx xxxx Xxxxxxxx xxxxxx xxx kontrolu xxxxx, xxxx xxxxxxxxx x xxxxxxxxx evropském xxxxxxxxx, kterým jedině xxxx xxxxx xxxxx x xxxxxxxx xxxxxxxxxx xxxxxxxxx, x to xxxxx prostřednictvím xxxxxxxxxx xxxxxxxxxx xxxxxxx. Žádost xxxx xxxxxxxx xxxxxxxxx xxxxxxxxxxx, xxxx subjektem xxxxxxxx xxxxxxxxxx. Xxxxxxxxxx, xx přístupy xx xxxxxx xxxxxxxxxx xxxxxxx xxxxx přidělovat některé xxxxxx Xxxxxxxx unie, x xx xx xx řádné xxxxxxxxxxxx xxxxxxxx činí xxxxx xxxxxx xxxxxx xxxxxxxxxxxx x xxxxxxxxx, že xxxxxxx zneužití neoprávněným xxxxxxxxx xxxx minimální.
Lhůty, x xxxxx xxxx xxxxxxxxxx xxxxxxxxx xxxxxxx, xxxx nastaveny nařízením x xxxx velice xxxxxx a xxxxxxx xxxxxxxxx řízení xxx xxxxxxxx je xxxx xxxxx 1x xxx xxxxxxxx xxxxxxxxxxx a xx xx 5 xxxxxxxxxxxx xxx (x 1x xxx doplnění xx xxxxxxx odborných xxxxxxxxxx, a xx xxxxx xx xxxx 12 xxxxxxxxxxxx xxx). Xxxxxxxxxx xxxxxx úprava xx zcela x xxxxxxx se xxxxxxxxx xxxxxx úpravou xxxxxxxxx xxxxxxxx, kdy plná xxx xxxx xxxxxxx xx xxxxxxx o xxxxxxxxx xxxxxxxxx zastoupení. Xxxxxxxx x tomu, xx xxxxxxxxxx xxxx xxxxxxxxxxxx xxxxxxxx x xxxxxxxxxx xx xxxx xxxxxxxxxx pouze xxxxxxxxxxxxxxx xxxxxxxxxxxxx xxxxxxx, xxxx xx xxxxxxxx xxxxxx xxxxxxxxx xxxxxxxx xxxx xxxxxxxxxx x xxx xxxxxxxxxx formalismu.
K §60 xxxx. 3 písm. x), xxxxx se xxxxxxxx.
Xxxx 1. xxxxx 2013 xxxxx xxxxxxxxx xxxxx č. 359/2012 Sb., xxxxxx xx xxxx xxxxx xx xxxxxxx xxxxxx xxxxx xxxxxx. Xxxxx xxxxxxxxxxx xxxxx §15 xxxx. 3 xxxx. x) zákona na xxxxxxx zvířat xxxxx xxxxxx se ustanovení xxxxxx zákona, která xxxxxxxx xxxxxxx xxxxxxxxx xxxxxx, nevztahují xx xxxxxxx, xxx xxxx xxxxxxx xxxxxxx použita xxx xxxxxxxxxxx klinická xxxxxxxxx xxxxxxxxxx xxx xxxxxxxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx. Xx 1. xxxxx 2013 tedy xxxxx xxxxxxxxx ke xxxxxxxxxxx projektů pokusů xxxxxx xxxxxxxxxx x xxxxxxxxx (souhlasu) xxxx xxxxxxxxxxx xxxxxxxx xxxxxx xx xxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxx xxx xxxxxxxxxx xxxxxxxxxxxxx léčivého xxxxxxxxx.
X §62 xxxx. 1, §64 xxxx. b) x x) x §66 xxxx. 4:
Obsah xxxxxxxxxxx xxxxxxxxxx xxxxxxxxxxxx xxxxxx xxxxxxxx přípravků, který xxxxxxxxx x xxxxxx xxxxxx výroby xxxxxxxxxxx xxxxxxxx xxxxxxxxx, je xxxxx xx souladu x xxxxxxxxx. Xxxxxxxx xxxxxxxx právní xxxxxx xxxx xxxxxxx x xx. 61.
X §70 xxxx. 1:
X textu xxxxxxxx 1 xx xxxxxxxx „xxxxx xxxxxxxxxx xxxxxxxx Xxxxxxxx xxxx“, x to xxxxx, xx xxxx xxxxxx xxx xxxxxxxx xxxxxxxx Xxxxxx x xxxxxxxxx xxxxxxxxx (XX) č. 1252/2014 xx xxx 28. xxxxxx 2014 xxxxxxxxxx xxxxxxxx Evropského xxxxxxxxxx x Xxxx 2001/83/XX, xxxxx xxx x xxxxxx x pokyny xxxxxxx xxxxxxx xxxxx xxx účinné látky xxx xxxxxxx xxxxxx xxxxxxxxx, které xxxxxxxx xxxxxxxx xxxxxxx praxi xxx léčivé xxxxx. Xxxx xxxxxxxx xx xxxx přímo xxxxxxxxxx, xxxxxxx xx xxxxxx, xxx bylo navázáno xx vnitrostátní xxxxxx xxx, xxxxxxx x xxxxxxx na xxxxxxxxxx xxxxxxxxx xxxxxx xx xxxx xxxxxxxx.
X §70 xxxx. 7:
Xxxxx nové xxxxxx x xxxxxxxxxxx xxxxxxxx 7 xx, xxx x xxxxxxxx xxxxx xxxxxxxxxxxxx xx xxxxxxx xxxx, xxxxx xx používají xxx xxxxxxxx xxxxxxxx xxxxxxxxx, xxx zřejmý jejich xxxxx, x xxx xxxx xxxxxxxx x xxxxxxx xx správnou xxxxxxx xxxxx pro xxxxxx xxxxx xxxxxxxxxxxx xxxxxxx xxxxxxxxxx stanoveným Xxxxxx.
X §77 xxxx. 1 xxxx. x):
Xxxxx xxxxxxxxx právní xxxxxx xx xxxxxx x xxxxxx poskytování údajů x xxxxxxxxxxxxxxx léčivých xxxxxxxxxxx xxxxxxxxxxx xxxxxx xxxxxx Státního xxxxxx xxx kontrolu xxxxx. X xxxxxxxx xxxxxxxxx xxxxxx xxxxxxx x xxxxxxxxx vymahatelnosti nápravy xxx xxxxxxxx této xxxxxxx xxxxxxxxxx je xxxxxxxxx, xxx byl xxxxxx údajů, xxxxxx xxxxxxxx x xxxxxx xxxxxx poskytování xxxxxx xxxxxxx xxxxxxxx xxxxxxxxxx xxxxxxx předpisem.
K §77 xxxx. 1 xxxx. x):
Xxxx je xxxxxxxx xxxxxxxxx povinnost xxxxxxxxxxxx xxxxxxxxxx x xxxxxxx x xxxxxxxxx xxxxxx xxxxxx vydaným podle §77x. Xxxx xx x xxxxx xxxxxxxxxx xxxxxxxx stanovena xxxxxxxxx xxxxxxxxxxxx při xxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxxxxxx požadovanou xxxxxxx xxxxxxxxxxxxxx xxxxxxxx xxxxxxxxx xx 48 hodin xx xxxxxxxx jeho xxxxxxxxx.
X §77 odst. 1 písm. x):
Xxxxxxx xx nová xxxxxxxxxx xxxxxxxxx xxxxxxxxxxxx v xxxxxxxxx, xxx hodlá xxxxxxxxxxxx xxxx xxxxx Xxxxx xxxxxxxxx xxxxxx xxxxxxxxx, xxxxx xx xxxxxx xx xxxxxxx xxx §77c. Po xxxxxxxx xxxxxxxxx xxxxxxxxxx xxxx být Xxxxxxxxxxxxx xxxxxxxxxxxxx vydáno xxxxxxxx xxxxxx xxxxxx, xxxxxx xxxx xxxx omezen xxxxxxxx xxx, xx xxxxxxx x akutní xxxxxxxxxxxxx léčivého xxxxxxxxx.
Xxx xxxxxxxxxxx xxxxxxxxxxxx povinnosti xx x xxxxxx xxxxxxxx uvedeno, že xxxxxxxx o distribuci xxxxxxxx přípravku xxxxxxxx xxxxxxxxxxxx xxxxxxxxxxxx, identifikaci xxxxxxxx přípravku, xxxxxxxx xxxxxxxx přípravku x xxxxxxx xxxxxxxxxx, xxxxx xxxxx distribuce a xxxxx plánované xxxxxxxxxx xxxxxxxx xxxxxxxxx. Rozsah xxxxx uváděných v xxxxxxxx a xxxxxx xxxxxx xxxxxxxxxxx xxxxxx xxxxxxxx xxxxxx stanoví xxxxxxxxx xxxxxx předpis.
Elektronické xxxxxxx je xxxxx x xxxxxxx na xxxxxx xxxxxx z xxxxxxx xxxxxxxxx dat, xxxxxxxx to xxxxxx xxxxxxxxx xxxxxxxxxx x xxx xxxx možnost xxxxxxxxx a xxxx xxxxxxxx xx xxxxx xxxxxxxxxx xxxxxx xxxxxxxx xxxxxxxxx xx trhu. Xxxxx xx xxxx xx Xxxxx xxxxxxxxxx x xxxx, resp. x xxxxxxx podobách, xxxxx xx je Xxxxx xxxxxx xxxxxxxxx xx xxxxxxxx podoby, xxx xx pak xxxx možné xxxxxxxxx, xxxxxxxxxx x xxxxxx xxxxx. X ohledem xx xxxxxxx dobu, xxxxxx má Xxxxx xx xxxxxxxxxx xxxxxxx x xxxxxx léčivých xxxxxxxxx x případné xxxxxxx xxxxxxx x xxxxxx xxxxxxxx xxxxxx xxxxxx xx XX, xx xxxx xxxxx, xxx xxxxxxxxxxxx nebyla xxxxxxxxxx. Rovněž je xxxxx vzít x xxxxx, že xxxxxxx xxxx xxxxxxx xxxxxxxx xxxxxxxx x xxxxxxxxxx x internetu, xxxxxxxxxxxx xxxxxx xxxxxxxxx xxxxxxxx, XX x xxxxxxxxxxxxx xxxxx xxx, která xxx jako xxxxxx xxx xxxxxx xxxxxx xxxxxxxxx xxxxxxx xxxxxxxxxx x uchovávání xxxxxxx x dokumentace xxx xxxxxx x řádné xxxxxx xxxxxxxxxx jim xxxxxxxxx xxxxxx ustanoveními xxxxxx o xxxxxxxx.
X §77x:
Xxxxx tohoto xxxxxxxxxx Xxxxx xxxxxxxx xxxxxxxxx xxxxxxx xx trhu x léčivými xxxxxxxxx, x xx xxxxxxx xx xxxxxx mezi xxxxxxx xxxxxx xxxxxxx xxxxxxxx přípravků xx xxx v České xxxxxxxxx podle §33 xxxx. 2 x xxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxxxx xx použitých xxx xxxxxxxxxxx xxxxxxxxxxx xxxxxx. Xx základě xxxx analýzy pak Xxxxx xxxxxxx Xxxxxxxxxxxx xxxxxxxxxxxxx xxxxxxxxx x xxxxxxx xx xxxx xxxxxxxxxxx x druhy xxxxxxxx xxxxxxxxx, xxx xxxxxxx xxxxxxxxxx xx xxxx x Xxxxx xxxxxxxxx by xxxxx xxxxxxxxx xxxxxxxxx xxxxxx xxxxxxxxxxxxx xxx poskytování xxxxxxxxxxx xxxxxx xxxxxxxxx x Xxxxx republice.
Po xxxxxxxxxxx xxxxxxx poskytnutých Xxxxxxxxxxxx zdravotnictví Xxxxxxx Xxxxxxxxxxxx zdravotnictví xxxx xxxxxx xxxxxxxx přípravků (xxxxxx přípravky xxxx xx seznam zařazovány xxxxxx xxxxxxxx xxxxxx xxxxxx), při xxxxxxx xxxxxxxxxx xx trhu x České republice xx mohlo xxxxxxxxx xxxxxxxxx jejich xxxxxxxxxxxxx xxx poskytování xxxxxxxxxxx xxxxxx xxxxxxxxx x Xxxxx republice. Xxxxx xxxxxx Xxxxxxxxxxxx zdravotnictví xxxxxxxx na xxxxx xxxxxxxxxxxxx xxxxxxxxx. Seznam xx průběžně xxxxxxxxxxxx x xxxxxxxxxxx. Xx xxxxxx xxxxxxx je xxxxxxxxx xxxxxx přípravek, xxxxx xxxx xxxxxxxxxxxx xxxxxxx xxxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxx xxxxxxxxxx, xxxxxxx xx xxx potřeby xxxxxxxx x České xxxxxxxxx xxxxxxxx, x xxxxxxx xxxxxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx xx xxxx xxxxxxx xxxxxxxxxx x xxxxxxxx xxxxx xxxxxxxx x České xxxxxxxxx x přímým xxxxxxx xx xxxxxxx xxxxxx xxxxxxxxxxxx x xxxxxxxxx xxxxxxxxxx xxxxxxxxxxx xxxxxxxxxxx služeb.
Na xxxxxx xx s xxxxxxx xx xxxxxxxx, xx xxxxxxxxxx předmětného léčivého xxxxxxxxx xx xxxx xxxxxxx dostupnost x xxxxxxxx léčby xxxxxxxx x Xxxxx xxxxxxxxx x xxxxxx dopadem xx xxxxxxx xxxxxx xxxxxxxxxxxx, mohly xxx xxxxxxxxxx všechny xxxxxx xxxxxxxxx, xxx xxxxxx xx xxxxxx xxxxxxxxxxxx xxxxxxxx. Xxxxx dopad xx xxxxxxx zdraví xxxxxxxxxxxx xxxx xxx x xxxxxxxxxx léčivého xxxxxxxxx xxxxxxxx k xxxxx jiné xxx xxxxx xxxxxxxxxx terapeutické xxxxxxxx. Xxxxxxxxx xx, xxx xxxxxx xxxxxxxxx xxxxx v xxxx xxxx nahraditelný xxxxxxx xxxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxx xxxxxxxxxx, xxxxxxx xx xxx xxxxxxx pacientů x Xxxxx republice xxxxxxxx.
Xxxxxxxx xxx stanovení xxxxxxxxxx xxx nalézt x xxxxxxx „xxxxxxxx xxxxxx“ x „zhoršení xxxxxxx aktuálních xxxxxx xxxxxxxx“ užitých x xxxxxxxxxx §77d odst. 2. Xxxxxxxx x xxxxxxx xxxxxx xxxxxxx x určitému xxxx, xxxxxxx x xxxxxxx xx xxxxxxxxx účelu x legitimity x xxxxxxxx evropského xxxxx xx xxxxxx, xx xxx je x xxxxxxx xxxxxx xxxxxxx x xxxx, xx xxxxxxx xx xxxxxx xxxxxxxxxxxxx analyzována. Xxxxxxxx xxxxxxx xxxxxxxxxx xxxxxx xxxxxxxx přitom xxxxxxxxxxx xxxxxxx, xx dostupnost xxxx xxxxxxxxx. Pro xxxxxxxxx účelu a xxxxxx xxxxxxxxxxx regulace xx xxxxxx logické, xx omezení xxxxxxxxx xxxx muset xxx xxxxxxx xx xxxxxx, xxx xxxxx jsou xxxxxx xxxxxx přípravky xx xxxx tak, xxx xx xxxx xxxxx xxxxxx x xxxxxxxxx XX.
Xxxxxx xxxxxxxxx xxxxx na xxxxxxx, xxxxx xx xxxx xxxxxxxx xxxxxxxxxxxx. Xxxxx xxxxxxx xxxxxx xxx xxxx xxxxxxxx na xxxxxx, bude xxxxxx xxxxxxxxxxxx x daný xxxxxxxxx z xxx xxxx vyřazen. Ale xxxxxxxx xxxxx xxxx xxxxxx xxxxxxxxx kritéria xxxxxxxx, může být xx xxxxxxx dlouhodobě, x to xxxxx, xx xxxxxxx xxxxxxxx x ČR je xxxxxx dlouhodobá xx xxxxx trvalá, a xxxxx xx nutné xxxx xxxxxxxxxx tímto xxxxxxxx xxxxxxxx. Při xxxxxxxxxxx xxxxxxx bude xxxx xxxxx xxxxxxxx, xx xxxxxxxx xxx xx, xxx xxxxxx xxxxxxxxx xxxx xx xxxxxxx xxxxxx, jsou xxxxx xxxxxxxx. Neznamená xx xxxx, že xxxxxxxx xxxxxxx xxxxxxxx xxxxxxxxx na xxxxxxx xxxx automaticky xxxxxxxx xx, že xxxx xxxxxx na xxxxxxx xxxxx.
Xxxxxxxxxx xxxx možné xxxxxx xxxxxxxxxxxxx xxx xxxxxxx léčivé xxxxxxxxx, xx xxxxxxxx xxx xxxxxxxx xxxx xx xxx ve vztahu xx xxxxxxxxxxx xxxxxxxx xxxxxxxxx x xxxxxxxxx xxxxxxx.
X §77d:
Státní xxxxx xxx xxxxxxxx xxxxx xx základě zákona x xxxxxxxx xxxxxxxxxxx xx xxxxxxxx rozhodnutí x registraci, xxxxxxxxxxxx x xxxxxxx xxxxx x xxxxxxxxx, xxxx. xxxxxxxx vydaných xxxxxxxx xxxxxxxxx, x nichž xxx xxxxxx xxxxxxxxx x dostupnosti léčivých xxxxxxxxx xx xxxx x České republice. Xxxx xxxxx, xxxxx xx xxxxx x xxxxxx xxxxxxxxx na xxxxxxx, xxxxxxxxxx xxxxxxxxxxx xxx, aby xxxx x xxxxxxx xxxxxxxx xxxxxxxxxxxx x xxxxxx xxxxxxxxxxxx xxxxxx xxxxxxxxx xx xxxxxxxxx xxxxx xxxxx xxxxxx xxxxxxxxxx Xxxxxxxxxxxx xxxxxxxxxxxxx xxxxxxxxxx xxxxxx x xxxxxx xxxxxxxx podle ustanovení §77x. Xxxxxx xxxx x návaznosti xx xxxxxxxx pro xxxxxx xxxxxxxx obecné xxxxxx Xxxxxxxxxxxxx zdravotnictví xxx §77x xxxxxxxxx xxxxx xxxxxxxxxxx xxxxxxxxxxxxx údajů x odůvodnění xxxxxxxxx xxxxx.
Xxxxxxxxxxxx xxxxxxxxxxxxx xx xxxxxxx §11 písm. x) vydá xxxxxxxx x zajištění xxxxxxxxxxx xxxxxxxxx xxxxxxxx přípravků x xxxxxxx, xx x) se xxxxx x léčivý xxxxxxxxx xxxxxxxx na xxxxxx xxxxxx xxxxx §77x, xxxxxxxxxx by xxxxx x tomu, xx xxxxxxxx zásoba xxxxxxxxxxx xxxxxxxx xxxxxxxxx xxx xxxxxxxxx potřebu pacientů x České republice, xxx xx zřejmé xxxxxxx x xxxxx xxxxxxxxxxxxx xxxxxxx xx xxxxxxxx xxxxxxxxxx x xxxxxxxxxx, xxxxxxxxxxxx x xxxxxxx x xxxxxxx x tímto zákonem x xxxxxx vyhodnocení, x c) veřejný xxxxx na xxxxxxx&xxxx; xxxxxx obyvatelstva x xx xxxxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx xxx xxxxxxx pacientů v Xxxxx xxxxxxxxx xxxxxxxxx xxx individuálním zájmem xx xxxxxxxxxxx jejich xxxxxxxxxx do xxxxxxxxx.&xxxx; Xxxx podmínky musí xxx xxxxxxx kumulativně, xx. xxxxxxx xxxxxxx.
Xxxxxxxx xxxxxxxxx xxx xxxxxx xxxxxxxx xxxxxx xxxxxx xxx xxxxxx xxxxxxxxxx xx xxxxxxx léčivého xxxxxxxxx na seznamu xxx §77c xxxxxx x xxxxxxxx.
Xxxxx se xxxxx o xxxxxxxx xxxxxxxxxxxxx, tato xx xxxxxxxxx xx xxxxxxxxxxxxxxx. Xxxxxxxx xx xx xxxxxxx xxx, že xxxxxxxx zásoba předmětného xxxxxxxx xxxxxxxxx xxx xxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxx xxxxxxxx x Xxxxx xxxxxxxxx. Xxxxxxxx xxxxxxx xxxxxxxx v Xxxxx xxxxxxxxx xx xxxxx transparentně vymezit, xxx je xxxxxxx xxx xx, xxx xxxx potřeby xxxx x xxxxxx konkrétním xxxxxxx xxxxx odůvodněny. X každého xxxxxxxx xxxxxxxxx xxxx xxx xxxxxxxxx x xxxxxxx xx frekvenci xxxxxxx xx výrobce, xxxxxxxxx xxxxxxx xxxxxxxx x xxxx zásob x xxxxxxxxxxxx, množství léčivého xxxxxxxxx xxxxxxxx xxxxxxxxxxxx xx xxxxxxx x xxxxx xxxxxx xxxxxxxx xxxxxxx oprávněnými x xxxxxx, včetně xxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxxxxxxx xxxx xxxxx Xxxxx xxxxxxxxx x předchozím xxxxxx.
Xxxxx písm. x) xxxx xxx xxxxxxx xxx podmínka xxxxxxxxx xxxxx xx xxxxxxx xxxxxx xxxxxxxxxxxx x xx xxxxxxxxx xxxxxxxxxxx xxxxxxxx přípravků pro xxxxxxxx xxxxxxx xxxxxxxx x České xxxxxxxxx. X konkrétním případě xxxx xxx xxxxx xxxxxxxxxx, že takto xxxxxxxxxx veřejný xxxxx xxxxxxxxx xxx xxxxxxxxxxxxx xxxxxx xx xxxxxxxxxxx xxxxxxxxxx xx zahraničí.
Co xx týče formy xxxxxxxx obecné xxxxxx, xxxxxx xxxxxx xxxxxxxx xxxxxx xxxxxx xx xxxxxxxx v xxxxxxxxxxxx §171 a xxxx. xxxxxx x. 500/2004 Xx., xxxxxxx xxx (xxxx xxx „xxxxxxx xxx“). Xxxxx opatření x samotné opatření xx navrhuje oznamovat xxxxx xxxxxxxx xxxxxxxxxxx xxxxxxx xxxxxxx. Xxxxx xxxxxx xxxxxx xxxxxxxx x xxxxxxxxxx §25 xxxxxxxxx xxxx xxxxx, xx xxxxxxxxx xxxx xx xxxxxxxx xx xxxxxxxxx xxxxxxxx xx xxxxxxxxx. Xxxx xxxxx xxx xxxxxx xxxxxxxx xx xxxxxxxx xxxxxxx xxxxxxxxx v xxxxx 5 xxx xxx, xxx xxxxx být xxxxxxxxxx xxxxxxxx x xxx xxxxxxxxxx xxxxxx.
Xxxxx xxxxxx xxxxxx, xx xxxxxxx orgán xxxxx xxxxxxx xxxxx, xxx x xxxxxx xxxxxxxx xxxxxxxx xxxxxxxxxx. Speciálně xx xxxxxx xxxx xxxxxxx lhůta 5 xxx xxx uplatnění xxxxxxxxxx x xxxxxx xxxxxxxx obecné povahy xxx dne xxxx xxxxxxxxxx tak, xxx xxxxxxxxxxx x xxxxxxx xxxxxxxxxx xxxxx xxxxx xx xxxxxx xxxx xxxxxx k xxxxxx xxxxxxxx xx xxxxxxxxxxx xxxxxxxx xxx.
Xxxxx xxxxxxxx xx xxxxxxx xxxxxxxxxxxx x lze x xxxx xxxxxxxx pouze xxxxxxx xxxxxxxxxx. Opět xxxxx xxxxxx xxxxxx, xx xxxxxxx, xxxxx xxxxx, povinnosti xxxx xxxxx xxxxx být xxxxxxxxx xxxxxx xxxxxx xxxxx xxxxxxx, může x xxxxxx xxxxxxxx x správního orgánu (x Xxxxxxxxxxxx xxxxxxxxxxxxx) xxx písemné xxxxxxxxxx. Xxxxxxxxxxxx xxxx xxxx xxxxxxx se připomínkami xxxxxxx xxxx xxxxxxxxx xxx xxxxxxxx xxxxxx xxxxxx x xxxxxxxxx xx s nimi x xxxx xxxxxxxxxx. Xxxxxxxxxx §175 xxxx. 2 správního xxxx xxxxxxxxxx xxxxxxx xxxxxx xxxxxxxxx xxxx, které xx xxxxx xxxxxxx xxxxxxxxxx xxxxxxx, se xxxxxxxxx. Xxxxxxxx xxxxxx xxxxxxxxx dnem v xxx stanoveným.
Co se xxxx xxxxxxxx xxxxxxxx xxxxxx xxxxxx, xxxxx xxxxxx xxxxxx xxx xxxxxxxxxx §173 xxxx. 2 xxxxxxxxx xxxx, xxxxx xxxxxxx v xxx, xx xxxxx xxxx xxxx xxxxx xxxxx xxxxxxx xxxxxxxxxx. Xxx ustanovení §174 xxxx. 2 správního xxxx xxxxxx opatření xxxxxx povahy x xxxxxxxx předpisy lze xxxxxxxx v přezkumném xxxxxx. Proti xxxxxxxx xxxxxx xxxxxx xxxxxxxx xxxxxxxx postup xxxxxxxx xxxxxx xxxxx xx xxxxxxxx soudnictví, x xx v xxxxxx x zrušení opatření xxxxxx xxxxxx xxx xxxxxxxxxx §101a x xxxx. zákona x. 150/2002 Sb., soudního xxxx xxxxxxxxx. Xxxxx xx xxxxxxx opatření xxxxxx povahy xxx xxxxx do 3 xxx od nabytí xxxx xxxxxxxxx x xxxx xxx xxxxx xxxxx, xxx tvrdí, xx jím byl xxxxxxx xx xxxxx xxxxxxx.
Xxxxx se xxxxx x xxxxxxx xxxxxxxx xxxxxxxx, xxx xxx xxxxxxx xxxxxxx xxxxxxxx, xxxxx xxxx opatření xxxxxxxxxx. Xx xxxxx xxxxxx a z xxxxxx xxxxxxxxx xxxxxxxxxxxxxxxx xxxxxx procesu xx xxxxx xxxxxxxxxx xxxxxxxxxxxx xxxxxx přetrvávání xxxxxxxx xxxxxx xxxxxx.
Xx účelem xxxxxxxxx možnosti xxxxxxxxxxx xxxxxxxxx x případě, xx se Ministerstvo xxxxxxxxxxxxx x xxxxx xxx činnosti dozví x riziku xxxxxxxxxx xxxxxxxx xxxxxxxxx, xxxxxx Xxxxxx ústav xxx xxxxxxxx xxxxx x xxxxxxxxxx xxxxx v xxxxxxx xxxxx §77c.
K §80 xxxx. 1:
Xxxxxxxx xx xxxxxx xxxxxxx xxxxxxxxxxxxxxx identifikačních xxxxx x elektronických xxxxxxx.
X §82 xxxx. 3 xxxx. x):
Xxxxx xxxxxxxxx xxxxxx xxxxxx je xxxxxx a xxxxxx xxxxxxxxxxx údajů x xxxxxxxx léčivých xxxxxxxxxxx xxxxxxxxxxx xxxxxx xxxxxx Xxxxxxxx ústavu xxx xxxxxxxx léčiv. X xxxxxxxx zachování právní xxxxxxx x xxxxxxxxx xxxxxxxxxxxxxx xxxxxxx xxx xxxxxxxx této zákonné xxxxxxxxxx xx xxxxxxxxx, xxx byl xxxxxx xxxxx, xxxxxx xxxxxxxx x způsob xxxxxx xxxxxxxxxxx formou xxxxxxx xxxxxxxx prováděcím právním xxxxxxxxx.
Xxxxxxxxxxxx xxxxxxx je xxxxx s ohledem xx veliké xxxxxx x xxxxxxx xxxxxxxxx xxx, umožňuje to xxxxxx efektivní xxxxxxxxxx x xxx xxxx xxxxxxx xxxxxxxxx x xxxx reagovat xx xxxxx xxxxxxxxxx xxxxxx xxxxxxxx xxxxxxxxx xx xxxx. Pokud xx xxxx xx Xxxxx xxxxxxxxxx v jiné, xxxx. x různých xxxxxxxx, musel by xx Ústav napřed xxxxxxxxx xx xxxxxxxx xxxxxx, aby xx xxx xxxx xxxxx xxxxxxxxx, vyhodnotit a xxxxxx xxxxx. X xxxxxxx na xxxxxxx xxxx, kterou xx Xxxxx xx zpracování xxxxxxx x vývozu xxxxxxxx xxxxxxxxx x xxxxxxxx předání xxxxxxx x vydání xxxxxxxx xxxxxx xxxxxx na XX, xx jiná xxxxx, xxx xxxxxxxxxxxx xxxxxx xxxxxxxxxx. Xxxxxx xx xxxxx vzít x xxxxx, xx xxxxxxx xxxx xxxxxxx xxxxxxxx xxxxxxxx x xxxxxxxxxx x xxxxxxxxx, xxxxxxxxxxxx xxxxxx xxxxxxxxx xxxxxxxx, XX x xxxxxxxxxxxxx formu xxx, xxxxx xxx xxxx xxxxxx při xxxxxx xxxxxx poskytuje xxxxxxx xxxxxxxxxx a xxxxxxxxxx xxxxxxx x xxxxxxxxxxx xxx xxxxxx x xxxxx xxxxxx xxxxxxxxxx xxx uložených jinými xxxxxxxxxxxx xxxxxx x xxxxxxxx.
K bodům 37 x 38
K §82 odst. 4:
Xxxxxxxxxx xxxxxxx xx xxxxxxxxx xxxxx.
X §101 xxxx. 1:
Xxxxxx ústav xxx xxxxxxxx xxxxx xx xxxxxxxx xxxx xxxxxxxxx xxxxx xxxxx řadou xxxxxxxx předpisů, xxxxx xxxxxxx xxx různé xxxxxxx. Kontrolu Xxxxxx xxxxx xxx xxxxxxxx xxxxx xxxxxxxx xxxxx xxxxxx xxxxxxxx xxxxxxxx:
xxxxx č. 378/2007 Sb., x xxxxxxxx - rezort MZ,
zákon č. 296/2008 Sb., x lidských xxxxxxx x xxxxxxx - rezort XX,
xxxxx č. 167/1998 Sb., x xxxxxxxxxx xxxxxxx&xxxx; - rezort XX,
xxxxx č. 123/2000 Sb., x xxxxxxxxxxxxxx prostředcích - xxxxxx MZ (od 1. xxxxx 2015 xxxxx č. 268/2014 Sb.),
zákon č. 372/2011 Sb., x xxxxxxxxxxx službách - rezort XX,
xxxxx č. 40/1995 Sb., x regulaci xxxxxxx - rezort XXX,
xxxxx č. 102/2001 Sb., o xxxxxx xxxxxxxxxxx xxxxxxx - xxxxxx XXX,
xxxxx č. 634/1992 Sb., o xxxxxxx xxxxxxxxxxxx - xxxxxx XXX,
xxxxx č. 265/1991 Sb., o xxxxxxxxxx xxxxxx Xxxxx xxxxxxxxx v xxxxxxx xxx x zákon č. 526/1990 Sb., x cenách - xxxxxx MF,
zákon č. 477/2001 Sb., x xxxxxxx - rezort XXX,
xxxxx č. 78/2004 Sb., o xxxxxxxxx x xxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxx a xxxxxxxxxxx xxxxxxxx - xxxxxx XXX,
xxxxx č. 272/2013 Sb., x xxxxxxxxxxxx xxxx - xxxxxx XX.
Xxxxx x xxxxxxxxx x xxxxxx xxxxxx xx xxxxxxxx, xx xx xxxxxxxxxx xxxxxxxxx xxx xxxxxx xxxxxxxx průkazem. U xxxxxxx xxxxx xxxxxxxx xxxxxxxx, x xxxxx xxxxxxxxxx o průkazu xxxxxxxxxx xxxxx, xx xxxx xx 1.1.2014 xxxxxxxxxx prokazovat písemným xxxxxxxxx vystaveným xx xxx. Xxx xxxxxxxxx xxxxxxxxxx se xxxxxxxxxx xxxxxxxx na kontrolu xxxxxxxxxx povinností uložených xxxxx xxxxxxx xxxxxx xxxx. xx xxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxx x xxxxxxxx x xxxxxxx x xxxxxxxx xxxxxxx. V xxxxxxx xxxxxxx se xxxx xxxxxxxxxx xxxxxxxxxx jak xxxxxxxxxx xxxxxxxx (podle xxxxxx o léčivech), xxx x xxxxxxxxx (xxxxx zákona x xxxxxxxx xxxxxxx).
X ohledem xx xxxxxxxxxx prokazování xxxxxxxxxx Xxxxxxxx xxxxxx xxx kontrolu xxxxx x k zajištění xxxxxx xxxxxxx xxxxxxxxxxxxxx xxxx se xxxxxxxx xxxxx xxxxxxxxxx xxx, xxx xxxxxxxx xx xxxxxxxx xxxx xxxxxxxx xxxxx průkazu inspektora x xxx xx xxxxxxxxxx Státního ústavu xxx xxxxxxxx léčiv xxx xxxxx xxxxxxxxxx xxxxxxxxxxxx podle právních xxxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxx xxxxx xxxxxxxx, x xxx xx xxxxxx xxxxxxxxxx, x xx xxxxx x xxxxxxx x kontrolním xxxxx. Xxxxxxx x §22 odst. 1 xxxxxx o xxxxxxxx xx xxxxxxxx xxxxxxxxxxxx xxxxxxx „xxxxxxxxxx“ xxx xxxxxxxxxxx Xxxxxxxx ústavu xxx xxxxxxxx xxxxx x Xxxxxx xxx xxxxxx xxxxxxxx xxxxxxxxxxxxx xxxxxxxxxxxx x léčiv, xxxxx xxxxxxxxxx kontrolní xxxxxxx, navrhovaná úprava xx se xxxx xxxxxxxxx i xx xxxxxxxxxx Xxxxxx xxx xxxxxx xxxxxxxx xxxxxxxxxxxxx xxxxxxxxxxxx x léčiv.
K §101 xxxx. 5 xxxx. x):
Xxxxxxxx xxxxxx xxxxxxxxx xxxxxxxxx x xxxxxxx xxxxxxxx přípravků xxxx x xxxxxxxxx xxxxx xxxxxx o xxxxxxxx xxxxxxxx neprovázaně, xxxxxxx x v omezené xxxx xxxxx xxx xxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx, x xxxxxxxx xxxxx x xxxxxxxxxx situacích zůstávají xxxxxxxxx. X praxi xx přitom xxxxx xxxxxxx vyskytují xxxxxxx, xxx Státní ústav xxx xxxxxxxx xxxxx xxxxxx, že s xxxxxxxx xxxxxxxxx xxxxxxxxx xxxxx, xxxxx x xxxx nejsou podle xxxxxx oprávněny. Xxxxxxx xx xxxxx o xxxxxxx, xxx xxxx xxxxxx přípravky xxxxxxxx xx xxxxxxxxx. Xxxxxx xxxxxxxxx xxxx xxxxxx xxxxxx xxxxxxxxxx zbožím x x xxxxxx xxxxxxx xxxxxxxxx xxxxxx xx xxxxxxxx, xxx x xxxx xxxx xxxxxxxxx xxx takovým xxxxxxxx, xxxxx xxxxx xxxxxxxx, a xxx xxxxxx zacházení xxxxxxxxxxxxx xxxxx xx osoby, xxxxx xxxx k xxxx xxxxxxxxx. X xxxxxx důvodu xx x návrhu novely xxxxxx zpřesňován xxxxxx Xxxxxx při zajišťování, xxxxxxxxxx x odstraňování xxxxxxxx xxxxxxxxx u xxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxx x xxxxxx. Dále xx dosavadní xxxxxx xxxxxx xxxxxxxxx o xxxxxx xxxxxxxx propadnutí xxxxxxxx xxxxxxxxx.
X§103 odst. 6 xxxx. x):
Xxxxxxxxx x doplnění xxxxxxxxxxx xxxxx xxxxxxxxxx tak, xxx xxxxxxxxxxx všechny xxxxxxx xxxxxxxx, xxxxx xxxxxxxxx x léčivými xxxxxxxxx.
K §105 odst. 2:
Xxxxxxxx xx xxxxxxx x), x) x x), xxxxx xxxxxxxx xxxxxxx xxxxxxx xxxxxxxxxxxx pro xxxxxx xxxxxxxxxxx xxxxxxx xxxxxxxx přípravku xxxxxxxxxxxxx xxx ustanovení §77 xxxx. 1 xxxx. x) (xxxxxxx xxxx xx xxx xxxxxxxxx x držitelů xxxxxxxxxx x xxxxxxxxxx), xxxxxxxxxx xxxxxxxxx xxxxxxxxxx xxx xxxx xxxxxxxxxx ustanovení §77 xxxx. 1 xxxx. q) x xxxxxxxx opatření obecné xxxxxx xxxxxxxx dle xxxxxxxxxx §77x.
X §105 xxxx. 5:
X xxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxxxx xxxxxxx xxxxxxxxx x xxxxxxxxxxxxx hrozby nedostupnosti xxxxxxxx xxxxxxxxx xx xxxx xxx potřeby xxxxxxxx v České xxxxxxxxx xx xxxxxx xxxxxxx xxxxxx xxxxxxxx xxxxxxxxxx x xxxxxxxxxx xxxxxxxxxxx x xxxxxxxxxxxx xxxxx x xxxxxx xxxxxxx léčivého xxxxxxxxx xxxxxxxxx na xxx x Xxxxx republice xxxxx §33 xxxx. 2.
K bodům 46 xx 65
X §105 xxxx. 6 x 7, §106 xxxx. 3, §107 xxxx. 1 x 2, §108 odst. 5, 8 x 11:
X xx. 94 xxxxxxxx xx ukládá xxxxxxxx xxxxxx xxxxxxxx xxxxxx za xxxxxxxx xxxxxx xxxxxxxx a xxxxxxxx xxxxxxx xxxxxxxx xxxxxxxx x xxxxxx xxxxxxxxxxx, přičemž xxxxxxxxx xxxxxx xxxx xxx xxxxxx, xxxxxxxxx x xxxxxxxxxx. Nově xx xxxxx doplňuje zákon x léčivech x xxxxxxxx xxxxxxxx xxxxxxxxxxx x xxxxxxxx xxxxxxxxxx xxxxxxxxxxx xxx xxxxxxxxx, xxx xxxxx xxxxxxx xxxxxxx x xxxx xxxxxxx stávající právní xxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxxx x zákoně x léčivech.
K §107 xxxx. 1:
Xxx xxxxxx xxxxxxxxxxx xxxxxxx léčivého xxxxxxxxx xxxxxxxxxxxxx xxx xxxxxxxxxx §77 xxxx. 1 písm. x) xx stanoví (xxxxxxx, xxxx xx již xxxxxxxxx x xxxxxxx xxxxxxxxxxxx deliktu xxxxxxxx xxxxxxxxxx x xxxxxxxxxx) xxxxxx do 20 xxx. Xx, xxx xxxxxx xxxxxxxxxx plánované xxxxxxxxxx xxx xxxx xxxxxxxxxx xxxxxxxxxx §77 xxxx. 1 písm. x) se stanoví xxxxxx xx 5 xxx. Xx x xxx xxxxxx porušení xxxxxxxx xxxxxx povahy xxxxxxxx dle xxxxxxxxxx §77x se xxxxxxx xxxxxx xx 20 xxx. Xx.
Xxxxx jde x xxxx xxxxxx, xx xxxxx xxxxxxxxxxx, xx xxxxxxxx xxxxxxx xxxxxx x xxxxxxxx č. 70/2013 Sb., xxxx xxxxxxxxxxx x xxxx, že xxxxx xxxxxxx xxxxx x tomto xxxxxx xxxx v průměru xxxxxxx, x čemuž xxxxx xxxxxxxxxxx xxxxxxxxxxx xxxxxxxx zmiňované v xxxxxxxx xxxxxx x xxxxxx zákonu: „ …xx xxxxxx xxxx xxxxxxxx xxxxxx i xxxxx xxxxxxx xxxxx xx xxxxxxxx xxxxxxxxx xxxxxxx x ostatních xxxxxxxxx xxxxxxxxxx xxxxxxx x xxxxxxxx. X xxxxxxxxx xxxxxxxxxx xxxxxxxx x aplikační xxxxx, xxxxx xxxxxxxx x xxx, xx xxxxxxxxx xxxx sankcí xx xxxxxxxxxxx xxxxxxx se x mnoha xxxxxxxxx xxx míjí xxxxxxx. X praxi xx xxxxxxx, že pro xxxxxxx farmaceutické xxxxx xxxxxxxxxxxxx hrozba xxxxxxx x maximální xxxx xxxxx xxxxxx výraznou xxxxxxxx xxxx, xxx xx svém xxxxxxxx xxxxxxxxx xxxxxxxxxxx x xxxxxxxxxx xxxx xxxx xxxxxxx xxxxxx. Xxxxxxxxx xxxxxxx pokut v xxxx oblasti rovněž xxxxxxxxxx za xxxxxxxxxx xxxxxx x xxxxxxxx xxxxxxxx x ostatních xxxxxxxxx xxxxxxx Evropské xxxx. Xxxxxxxxx xxxxxx xx xxxxx xxxxxxx xxxxxxxxx xxxxxx xxxxxxxxxx xxxxx na xxxxxxxxxxxx xxxxxxxx, což xx xxxx xxxxxxxx xxxx xxxx xx xxxxxxx xxxxxxxx xxxxxxxxxx xxxxxxxxxxx xxxxxx x této xxxxxxx. X xx xxxxxxxxxxx xxxxxxx xxxxx xxxxxxx xxxxx xxxx xxxxx nedosahují výše, xxxxx je stanovena x jiných xxxxxxxx xxxxxxxxxx, xxxx například x xxxxxx č. 634/1992 Sb., x xxxxxxx xxxxxxxxxxxx, xx xxxxx xxxxxxxxxx xxxxxxxx, x xxxx xx xx xxxxxxx xxxxxxx xxxxxxx xxxxxxxxx xxxxx xxxxxxx xxxxx xx xx xxxx 50 000 000 Xx.“.
Xxxx xxxxxxxxxxxx xxxxxxx xxxxxx xx xxxxx xxxxx xxxxx schválený Xxxxxxxxxxx Xxxxx xxxxxxxxx xxxxxxxxxxx, a x xxxxxx xxxxxxxx x xxxxxxxx. Xxxx xxxxxxxxxx x xxxxxxxxxx xxxxx xxxxxxx xxxxx za xxxxxxxx nově xxxxxxxxxxx xxxxxxxxx deliktů.
Správní xxxxxxx xxxxxxxxxxx v nezajištění xxxxxxx léčivého xxxxxxxxx xxxxx §77 xxxx. 1 xxxx. x), xxxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx xxxx území Xxxxx xxxxxxxxx podle §77 odst. 1 xxxx. x) xxxx x distribuci xxxxxxxx xxxxxxxxx xxxx xxxxx&xxxx; Xxxxx xxxxxxxxx x xxxxxxx x xxxxxxxxx xxxxxx povahy Xxxxxxxxxxxx xxxxxxxxxxxxx xxxxxxx xxxxx §77x by natolik xxxxxxxx xxxx xxxxxx x xxxxxx pravidel xxxxxxxxxxx xxxxxxx xxxxxx xxxxxxxx xxxxxxxx xxxxxxxx xxxxxxx xxxxxxxx v Xxxxx xxxxxxxxx, že xx xx xxxxx xxxxxxxxx možnosti, xxx xxxxx za takové xxxxxxx xxxxxxx xxxx xxxxx xxxxxx xxxxxx x xxxxxxxx možné xxxx xxxxx zákona x léčivech, xxxxxx xx již xxxxx xxxxxxxxx xxxxxx úpravy xxxxxx 20 000 000 Xx.
Xxxxx jde x nově stanovený xxxxxxx xxxxxx xxxxxxxxxxx x xxx, xx xxxxxxx rozhodnutí x xxxxxxxxxx xxxxxxxxxx údaje x objemu xxxxxxx xxxxxxxx přípravku xxxxxxxxx xx trh x Xxxxx republice xxxxx §33 xxxx. 2, xxx svou xxxxxxxxx x obdobný xxxxxxx xxxxxx, xxxxxx xx xxxxx xxxxxxxxx právní xxxxxx xxxx dopustit xxxxxxxxxxx xxxxx §77 xxxx. 1 xxxx. x) nebo xxxxxxxxxxxx xxxxxxxxx x xxxxxx xxxxxxxx přípravků xxxxx §82 xxxx. 3 xxxx. d). Xx xxxxx zcela odůvodněné, xxx xxxx horní xxxxx správního xxxxxxx xxxxxxxx xxxxxxxxxx x xxxxxxxxxx xxxxxxxxxx xxxx xxxxx sazby xxxxxxxxx xxxxxxxxx xxxxxxx xxxxxxxxx xxxxxx xxxxxxx.
Xxxxx xxx x xxxxxxx xxxxxxx x oblasti xxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx, xx xxxxx x xxxx řadě xxxxxxxxx, xx xxxx xxxxxx xxxx, xxx xxxxx xxxx, xx xxxxx xxxxxxxxxxx protiprávní xxxxxxx xxxxxxxxx x xxxxxx o léčivech, xxxx xx xxxx xxxxxxxxxx xxxxxxxxxxx xxxxxxx xxxxxxxxx již x xxxxxxxx č. 536/2014, xx. x xxxxx xxxxxxxxxxx xxxxxxxx Xxxxxxxx xxxx. Xxx stanovení xxxxx xxxxxxx xxxxxxx pokut xx xxxxxx xxxxxxxxxxx xxxxxxx xx tudíž xxxxxxxxx dosavadní xxxxxx xxxx.
X §107 odst. 2:
Xxx xxxxxx xxxxxxxx xxxxxxxx obecné xxxxxx xxxxxxxx xxx ustanovení §11 xxxx. g) xx stanoví též xxxxxxx xxxxxxx sankce xxxxxxxxxxx x xxxxxx xxxxxxxx.
X §108a x §108x:
X xxxxxx xxxxxx xxxxxxx se x xxxxxx upravují podmínky xxx xxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx x xxxxxxx léčivého xxxxxxxxx x xxxxxxxx xx xxxxxxx xxxxxxx, že xxxxxxxxxx takového xxxxxxxx xxxxxxxxx se xxxxx xxxx.
X §112 xxxx. 6:
Xxxx xxxxxxxx xxxxxxxx 6 xxxxxxxxx xxxxxxxx xxxxx rozhodnout x xxxxxxx xxxxxxxxxx xx xxxxxxxxxx účtu Státního xxxxxx xxx xxxxxxxx xxxxx na xxxxxxxx xxxx xxxxxxxx rozpočtu Xxxxx xxxxxxxxx xxx Xxxxxxxxxxxx xxxxxxxxxxxxx.
K bodům 68 xx 72
X §114 odst. 1, 2 x 4:
Xxx xx xxxxx xxxxx x xxxxxxxxxxxx xxxxxxxxxx úpravu xxxxxxxxxxxx xxxxxxxxxxxx ustanovení k xxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxx xxx, kde xx zákon výslovně xxxxxxxxxxx. Přitom xx xxxxxxxxxx ta skutečnost, xx xxx x xxxxxxxxxx §114 xxxx. 1 zákona o xxxxxxxxxxx xxxxxxxxx Ministerstva xxxxxxxxxxxxx x xxxxxx xxxxxxxx x x xxxxxxxxxx §114 xxxx. 2 zákona x xxxxxxxxx působnost Ministerstva xxxxxxxxxxxxx a Xxxxxxxxxxxx xxxxxxxxxxx k vydání xxxxxxxx.&xxxx; Po xxxxxx xxx xxxxx x xxxxxxxxx xxxxxxxx vyhlášky x správné klinické xxxxx xxx, xx xxx oblast veterinárních xxxxxxxx xxxxxxxxx xx xxxx xxxxxxxx xxxxxxx xx gesce Ministerstva xxxxxxxxxxx.
X §114 xxxx. 2:
X tomto xxxx xxx jen o xxxxxxxxxxxx technické xxxxx x xxxxxx xxxxxxxxxxxx xxxxxxxxxx, xxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxxx xxx xxxxxx klinického xxxxxxxxx xxxxxxxxx xxxxxxxx přípravků xxxx xxxxxxxxxxx xxxxxxxxxxxx xxxxxxxxxxxx xxxxxx.
Xxxxxxxxx xxxxxxxxxx xxxx xxxxxxxx xxx, xxx respektovala ustanovení článku 98 nařízení x. 536/2014.
X důvodu odstranění xxxxxxxxxx xxxxxxxxxxx xx xxxxxxxx xxxxxxx, xx xxxxx x státní xxxxxx xx xxxxxx xxxxxxxxx xx xxxxx xxxxxx komise.
Jedná se x ustanovení reflektující xxxxxxx xxxxxxxxx xxxxxxx xxxxxxxxxx v xxxxxxx xx směrnicí Xxxxxxxxxx xxxxxxxxxx x Rady (XX) 2015/1535 xx xxx 9. xxxx 2015 x xxxxxxx xxx poskytování xxxxxxxxx x xxxxxxx xxxxxxxxxxx xxxxxxxx a předpisů xxx xxxxxx xxxxxxxxxx xxxxxxxxxxx, v xxxxxxx xxxxx.
K čl. V (Účinnost):
Nabytí xxxxxxxxx xxxxxx se xxxxxxxxx xxxxxxxx ve xxxxxx xx xxxxxx skupinám xxxxxxxxxx xxxxxx xxxxxx.
Xx xxxx, xxxxxxxxxx xxxxxxx xxxxxxxx nového režimu xxxxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxx přípravků xx xxxx nabýt xxxxxxxxx xxxxxxxxx 6 xxxxxx xx xxx xxxxxxxxxx xxxxxxxx Xxxxxx x Xxxxxxx xxxxxxxx Xxxxxxxx unie xxxxx čl. 82 xxxx. 3 xxxxxxxx x. 536/2014, xxxxxxx xxx, kdy xxxx toto xxxxxxxx xxxxxxxxxx, xxxxxx Xxxxxxxxxxxx xxxxxxxxxxxxx formou sdělení xx Xxxxxx xxxxxx.
Xx xxxxx, ustanovení xxxxxxxx xx xxxxxxxxx xxxxx xxxxxx xxxxxx, Xxxxxxx, xxxxxxxxx řádu etické xxxxxx x xxxxxxxxxx xxxxxxx etické xxxxxx, xx měla xxxxx xxxxxxxxx již xxxxxx xxxx xxxxxxxxxxxx xxxxxx xx dni zveřejnění xxxxxxxx Xxxxxx v Xxxxxxx xxxxxxxx Xxxxxxxx xxxx xxxxx čl. 82 xxxx. 3 xxxxxxxx x. 536/2014, xxxxx xxxxxx xxxxxx xxxx xxx nabytím xxxxxxxxx xxxxxxxx xxxxxxx xxxxx xxxxxxxx x není xxxxx, xxx s xxxxxxx a xxxxxxxxxx xxxxxx xxxxxx bylo xxxxxxxx xx x xxx xxxxxx xxxxxxxxx xxxxxxxx č. 536/2014.
Za xxxxx, xxxxxxxxxx xxxxxxx omezení xxxxxxxxx xxxxxxxx xxxxxxxxx xx xxxx xxxxx xxxxxxxxx xxxxxx xxxx xxxxxxxx xxxxxxxxxxxx xxxxxx xxxxxxxxxxxxx po dni xxxxxxxxx zákona, xxxxx xxxxxxxxxx xxxxxxx xxxxxxxxx x vyhodnocování hrozby xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx xxx xxxxxxxx potřeby xxxxxxxx v Xxxxx xxxxxxxxx a xxxxxxxxx xxxxxxxxxxx opatření xxxxxxxxxxx xxxxxxxxxx léčivých přípravků xx xxxxxxxxx x xxxx xxxxxxxxx, xxx xxxxxxxxxxx takové xxxxxx xxxxxxx takových opatření xxxxxxxxxx, xx xxxxxxxx xxxxxx čas xxxxxxxx, x xx xxxxxxx xx xxxxxx xxxxxxxx xxxxxxxxxx x xxxxxxxxxx xxxxxxxx xxxxxxxxx, distributorů x xxxxxxxxxxx xxxxxxxxx xxxxx.
Xx xxxxxx, xxxxxxx xxxxxxxxxx obsažená x xxxxxx xxxxxx by xxxx xxxxx xxxxxxxxx xx xxxxxxxx, a xxxx je xx xxxxx, xxx xxxxxx xxxxxxxxx xxxxxx dnem xxxxxxxxxxxx měsíce xxxxxxxxxxxxx xx dni xxxxxxxxx xxxxxx.
X Praze xxx 13. xxxxx 2016
xxxxxxxx xxxxx
Xxx. Bohuslav Xxxxxxx x. x.
xxxxxxx xxxxxxxxxxxxx
XXXx. Xxxxxxxxx Xxxxxxx, XXX, x. x.
ROZDÍLOVÁ XXXXXXX XXXXXX XXXXXXXX XXXXXXXX S XXXXXXXX EU
Rozdílová tabulka x návrhu xxxxxx xxxxxx č. 378/2007 Xx., x léčivech x o xxxxxxx xxxxxxxxx xxxxxxxxxxxxx xxxxxx (xxxxx x xxxxxxxx)
|
Xxxxxxxxxx xxxxxx předpis (xxxx. xxxx xxxxxx předpis) |
Odpovídající xxxxxxx XX |
|
|
Xxxxxxxxxx (xxxx, §, odst., xxxx. xxxx.) |
Xxxxx č. |
Ustanovení (čl., xxxx., písm., bod., xxxx.) |
|
Xx. 2 xxxx. 1 |
||
|
Xx. 83 |
||
|
Xx. 4 |
||
|
Xx. 8 odst. 1 |
||
|
Čl. 1 xxx 22 |
||
| §51 | ||
|
Kapitola XX, xx. 4 |
||
|
Xxxxxxxx XX, xx. 9 |
||
|
Xxxxxxxx XX čl. 83 |
||
|
Xxxxxxxx XX, xx. 2, xxxx. 2, xxx 12 |
||
|
Xxxxxxxx XX, xx. 5 |
||
|
Xxxxxxxx II, xx. 2, xxxx. 2, xxx 12 |
||
|
Kapitola II, xx. 6, xxxx. 5 x 7 |
||
|
Xxxxxxxx XX, xx. 7 |
||
|
Xxxxxxxx XX, xx. 8 |
||
|
Xxxxxxxx X, čl. 34 |
||
|
Kapitola X, xx. 2, xxx 11 |
||
|
Kapitola XX, xx. 4 |
||
|
Kapitola II, xx. 9 |
||
|
Xxxxxxxx XX, xx. 8 xxxx. 4 |
||
|
XXX X6 |
||
|
Xxxxxxxx II, xx. 9 |
||
|
XXX E6 |
||
|
Kapitola XX, xx. 4 |
||
|
Xxxxxxxx XX, xx. 8 xxxx. 4 |
||
|
Xxxxxxxx II, xx. 6 |
||
|
Xxxxxxxx XX, xx. 4 |
||
|
Xxxxxxxx XX, xx. 7 |
||
|
Xxxxxxxx XX, xx. 28, xxxx. x) |
||
|
Xxxxxxxx II, xx. 7, xxxx. 1 xxxx. x) |
||
|
Xxxxxxxx XXX, xx. 20 |
||
|
Xxxxxxxx XX, xx. 4 |
||
|
Xxxxxxxx I, xx. 4 |
||
|
Xxxxxxxx X, xx. 2, xxx 15 x 16 |
||
|
Xxxxxxxx XXXX, čl. 49 |
||
|
Kapitola XX, xx. 73 |
||
|
Kapitola XXXX, čl. 50 |
||
|
Kapitola XX, xx. 26 |
||
|
Kapitola XXXX, xx. 59 xxxx. 3 |
||
| 32014R0536 |
Xxxxxxxx XVIII, xx. 92 |
|
|
Xxxxxxxx IX, xx. 61, xxx 5x |
||
|
Xxxxxxxx X, xx. 68 |
||
|
Xxxxxxxx XVIII, xx. 90 |
||
|
Xxxxxxxxx 81 |
||
|
Xxxxxxxx VII, xx. 42 xxxx. 3 |
||
|
Xxxxxxxx XII, čl. 76 |
||
|
Xxxxxxxx X, xx. 2, xxx 20 |
||
| §64 písm. b) |
Čl. 8 xxxx. 1 |
|
|
Čl.1 |
||
|
Čl.1 |
||
|
Čl. 94 |
||
|
Xx. 8 xxxx. 1 |
||
|
Xx. 15 |
||
|
Xx. 35 |
||
|
Xx. 36 |
||
|
Xx. 37 odst. 1 |
||
|
Xx. 37 xxxx. 5 |
||
|
Xx. 37 odst. 6 |
||
|
Xx. 38 xxxx. 1 |
||
|
Xx. 37 xxxx. 4 |
||
|
Xx. 41. xxxx. 3 |
||
|
Xx. 42 odst. 1 |
||
|
Xx. 47 |
||
|
Xx. 49 |
||
|
Xx. 52 |
||
|
Xx. 54 xxxx. 1, 2 |
||
|
Xx. 55 |
||
|
Xx. 56 |
||
|
Xx. 57 |
||
|
Čl. 58 |
||
|
Kapitola XXX, čl. 76 xxxx. 1, 2 |
||
|
Xx. 94 |
||
|
Xx. 94 |
||
|
Čl. 28 xxxx. 1 |
||
|
Xx. 41 xxxx. 1 |
||
|
Xx. 47 |
||
|
Xx. 49 |
||
|
Xx. 54 xxxx. 1 |
||
|
Xx. 58 |
||
|
Xx. 73 |
||
|
Xx.94 |
||
|
Xx. 28 xxxx. 1 |
||
|
Xx. 41 odst. 1 |
||
|
Xx. 47 |
||
|
Xx. 49 |
||
|
Čl. 54 xxxx. 1 |
||
|
Xx. 58 |
||
|
Xx. 73 |
||
|
Xxxxx předpisu EU (xxx Celex) |
Název předpisu XX |
|
XXXXXXXX XXXXXXXXXX PARLAMENTU X XXXX (XX) x. 536/2014 xx xxx 16. dubna 2014 x xxxxxxxxxx xxxxxxxxxxx humánních léčivých xxxxxxxxx a o xxxxxxx xxxxxxxx 2001/20/XX |
|
|
XXXXXXXX XXXXXX v xxxxxxxxx xxxxxxxxx (EU) x. 1252/2014 ze xxx 28. května 2014 xxxxxxxxxx xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Xxxx 2001/83/XX, xxxxx xxx x xxxxxx x xxxxxx xxxxxxx xxxxxxx xxxxx xxx xxxxxx xxxxx xxx xxxxxxx xxxxxx xxxxxxxxx |
|
| 32004L0027 |
XXXXXXXX XXXXXXXXXX XXXXXXXXXX X XXXX x. 2004/27/ES xx xxx 31. xxxxxx 2004, kterou xx xxxx xxxxxxxx 2001/83/XX x xxxxxx Společenství xxxxxxxxx xx xxxxxxxxx xxxxxxxx xxxxxxxxx |
Zdroj xxxxx www.psp.cz


