Vládní návrh zákona, kterým se mění zákon č. 378/2007 Sb., o léčivech a o změnách některých souvisejících zákonů (zákon o léčivech), ve znění pozdějších předpisů, a zákon č. 234/2014 Sb., o státní službě, ve znění pozdějších předpisů
706/0
Xxxxxx xxxxx
XXXXX
xx xxx … 2016,
kterým xx xxxx xxxxx č. 378/2007 Sb., x léčivech a x změnách xxxxxxxxx xxxxxxxxxxxxx xxxxxx (xxxxx x léčivech), xx xxxxx xxxxxxxxxx xxxxxxxx, x xxxxx č. 234/2014 Sb., x státní xxxxxx, xx znění pozdějších xxxxxxxx
Xxxxxxxxx xx xxxxxx xx tomto zákoně Xxxxx republiky:
ČÁST XXXXX
Xxxxx zákona x xxxxxxxx
Xx. I
Zákon č. 378/2007 Sb., x xxxxxxxx x x xxxxxxx xxxxxxxxx xxxxxxxxxxxxx xxxxxx (xxxxx x xxxxxxxx), ve xxxxx xxxxxx x. 124/2008 Xx., xxxxxx x. 296/2008 Sb., xxxxxx x. 141/2009 Xx., zákona x. 281/2009 Xx., xxxxxx x. 291/2009 Sb., xxxxxx x. 75/2011 Xx., xxxxxx x. 375/2011 Xx., xxxxxx x. 50/2013 Sb., xxxxxx č. 70/2013 Xx., xxxxxx x. 250/2014 Xx. x xxxxxx x. 80/2015 Xx., xx mění xxxxx:
1. Xx xxxxx xxxxxxxx pod xxxxx x. 2 xx xxxxxxxx věty:
„Nařízení Xxxxxxxxxx xxxxxxxxxx x Rady (XX) č. 536/2014 ze xxx 16. xxxxx 2014 o klinických xxxxxxxxxxx humánních xxxxxxxx xxxxxxxxx x x xxxxxxx směrnice 2001/20/XX.
Xxxxxxxx Xxxxxx x xxxxxxxxx xxxxxxxxx (EU) č. 1252/2014 xx xxx 28. xxxxxx 2014 xxxxxxxxxx xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Rady 2001/83/XX, xxxxx xxx o xxxxxx x pokyny xxxxxxx xxxxxxx xxxxx xxx xxxxxx látky xxx xxxxxxx xxxxxx xxxxxxxxx.“.
2. V §5 xx xxxxxxxx odstavec 16, který včetně xxxxxxxx pod xxxxx x. 101 xxx:
„(16) Xxxxxxx xxxxxx xxxxx xx xxx xxxxx xxxxxx xxxxxx, xxx-xx x xxxx xxxxxxx x hodnocených xxxxxxxxx xxxxxxxx přípravcích xxxx xx veterinárních xxxxxxxx xxxxxxxxxxx, rozumí xxxxxxxx xxxxx xxxx částečný xxxx xxxxxxxx xxxxxxxxx, xxxxxx, xxxxxx, xxxxxxxxxxx, xxxxxxxxxx, xxxxxxxxxxxx, xxxxxxxx xxxxxxx xxxx xxxxxxxxxxx xxxxxx xxxxx, xxxxx x xxxxxxxxxxx xxxxxxxx. Xxxxxxxx xxxx, xx xx xxxxxx xxxxxxx xxxxxx látky, jde-li x xxxx xxxxxxx x humánních léčivých xxxxxxxxxxx, xxxxxxx xxxxx xxxxxxxxxx xxxxxxx Xxxxxxxx xxxx xxxxxxxxxx xxxxxxxx xxxxxxx xxxxx xxx xxxxxx xxxxx101).
XXXXX: 32014R1252
3. V §11 xxxxxxx x) xxx:
„x) xxxxxx xxxxxxxx obecné xxxxxx xxxxx §77x, xxxxxx xxxxxxx xxxx xxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx xx xxxxxxxxx,“.
4. X §11 xxxxxxx h) xxx:
„x) xxxxxxx xxxxxxxx xxx xxxxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxx xxx xxxxxxxxxxx zdravotních xxxxxx, xxxxxxx vyžaduje-li xxxxxxxxx xxxxxx xxxxxxxxxxx xxxxxx xxxxxxxx xxxxxx xxxxxx x xxxx-xx xxxxxxx xxxxxxxx pro xxxx xxxxxx, xxxxxxxxx xxxxx xxxxxxx g) nebo x), a xxxxxxx xxxxxxxx xx xxxxxxx xxxxxxx, vývoje x xxxxxxxxxxx xxxxxxxx xxxxxxxxx xxx xxxxxx xxxxxxxxxx x léčivých xxxxxxxxx, xxxxx mohou xxx xxxx xxxxxx stanoveny, xxxxx x xxxxxxxx xxxxxxxxx xxx použití x xxxxxxx lékařství,“.
5. V §11 xx xx konci xxxxxxx x) xxxxx xxxxxxxxx xxxxxx x xxxxxxxx xx xxxxxxx x), xxxxx xxx:
„x) xxxxxx xxxxxxxx xxxxxx xxxxxx podle §77c, xxxxxx se xxxxxxx xxxxxx přípravek, xxx xxxxx xxxxxxxxxx bude xxxxxxxx dostupnost a xxxxxxxx léčby xxxxxxxx x Xxxxx xxxxxxxxx x přímým dopadem xx xxxxxxx xxxxxx xxxxxxxxxxxx x x xxxxxxxxx xxxxxxxxxx poskytování xxxxxxxxxxx služeb, a xxxx xxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx.“.
6. X §13 xxxx. 2 písm. x) xxxx 1 xx xx xxxxx „xxxxxxxxxx x xxxxxxxx xxxxxxxxxx xxxxxx,“ xxxxxxxx xxxxx „xxxxxxxxxx o xxxxxxxxxx xxxxxxxx xxxxxxxxx,“.
7. X §13 xxxx. 2 xxxx. x) xxxx 3 xx slovo „xxxxxxxxxxxxxx“ xxxxxxx.
8. X §13 xxxx. 2 xxxxxxx x) včetně xxxxxxxx xxx xxxxx č. 104 zní:
„b) xxxxxx xxxxxxxxxx xxxxxxxx xx xxxxxxxxxx hodnocení podle §51 x ukládá xxxxxxxx opatření ve xxxxxx čl. 77 xxxxx použitelného xxxxxxxx Xxxxxxxx unie upravujícího xxxxxxxx xxxxxxxxx humánních xxxxxxxx přípravků104) (xxxx xxx „xxxxxxxx o xxxxxxxxx xxxxxxxxx“)“.
XXXXX: 32014R0536
9. X §13 xxxx. 2 se xx konci písmene x) tečka xxxxxxxxx xxxxxx a xxxxxxxx xx xxxxxxx x), xxxxx xxx:
„x) x xxxxxxx xxxxxxxx xxxxxx x xxxxxxx léčiva, xxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxx xxxx xxxxxx xxxx, xxxxxxxxx o xxx, zda se xxxxxx xxxxxx nebo xxxx xxxxxxxxxx xxxxx xxxx xxxxxxxxxxxx, xxxxxxx, xxxxxx do oběhu xxxx xxxxxxxx při xxxxxxxxxxx xxxxxxxxxxx xxxxxx.“.
10. X §13 xxxx. 3 xx xx konci xxxxxxx x) tečka xxxxxxxxx xxxxxx x doplňují xx xxxxxxx q) x x), xxxxx xxxxx:
„x) předává Xxxxxxxxxxxx xxxxxxxxxxxxx veškeré údaje xxxxx pro xxxxxx xxxxxxxx obecné xxxxxx xxxxx §77x,
x) na xxxxxxx xxxxxxxxxxx xxxxxxx xx trhu x xxxxxxxx xxxxxxxxx xxxxxxx Xxxxxxxxxxxx xxxxxxxxxxxxx xxxxxxxxx xxxxx §77x x xxxxxxx mu podnět x xxxxxx opatření xxxxxx povahy xxxxx §77x.“.
11. X §16 xxxx. 2 písm. x) xxxx 1 xx xx xxxxx „xxxxxxxxxx x povolení xxxxxxxxxx xxxxxx,“ xxxxxxxx xxxxx „xxxxxxxxxx x xxxxxxxxxx xxxxxxxx xxxxxxxxx,“.
12. Za §19 xx vkládá nový §19x, který xxxxxx xxxxxxx zní:
„§19a
Generální ředitelství xxx
(1) Generální ředitelství xxx xxxxxxxxx na xxxxxxxx Xxxxxx x xxxxxxxxxxxx osobě, xxxxx xxxxx xx xxx xxxx xxxxxx xxxxxx, xxxx xxxxxxxxx:
x) xxxxxxxxxxxxx xxxxx xxxxxx osoby, x xx zejména xxxxx xxxx xxxxx x xxxxx,
x) xxxxx xxxxxx, včetně obchodního xxxxx,
x) x xxxxxxx xxxxxxx informace x xxxx odeslání x xxxx původu léčiva x
x) xxxxxxxx xxxxxx xxxxxxxxx x měrných xxxxxxxxxx.
(2) Poskytnutí xxxxxxxxx xxxxx xxxxxxxx 1 xxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxxxxx xxxxx xxxxxxxx xxxx.“.
13. X §21 xx xxxxxxxx 1 xxxxxxx.
Xxxxxxxxx xxxxxxxx 2 x 3 xx xxxxxxxx xxxx xxxxxxxx 1 a 2.
14. X §23 xxxx. 2 xxxx. x) se xx xxxxx „xxxxxxx“ xxxxxxxx xxxxx „, pokud Xxxxx xxxxxxx xxxxxxxxxx xxxxx §13 odst. 2 xxxx. n)“.
15. X §33 xxxx. 2 xx xx xxxx xxxxx xx xxxxx „typů xxxxx“ xxxxxxxx xxxxx „x kódu xxxxxxxxxxx Xxxxxxx nebo Veterinárním xxxxxxx“.
16. X §33 xxxx. 2 xx xxxx xxxxxxxx nahrazuje xxxxxx „Držitel rozhodnutí x xxxxxxxxxx xxxxxxxxx Xxxxxx xxxxx x xxxxxxx xxxxx x xxxxxx xxxxxxx léčivých xxxxxxxxx uvedených xx xxx x Xxxxx xxxxxxxxx xxxxxxxxxxxx; xxxxxxxxxxx xxxxx xxxxxxxx xxxxxxxxxxxx xxxxxxxx xxxxxxxxxx x xxxxxxxxxx, xxxxxxxxxxxx léčivého xxxxxxxxx x xxxxxxxxx x xxx, xxx xxx xxxxxx xxxxxxxxx xxxxx xxxxxxx xxxx xxxxxxxxxxxxxx; strukturu, způsob, xxxxx x xxxxxx xxxxxxxx jejich poskytování xxxxxxxxxxxxxxx elektronického xxxxxxx xxxxxxx prováděcí právní xxxxxxx. Na xxxxx Xxxxxx xxxx Xxxxxxxxxxxxx xxxxxx xxxxxxxx xxxxxxx xxxxxxxxxx x xxxxxxxxxx Xxxxxx xxxx Veterinárnímu xxxxxx údaje xxxxxxxx xx xxxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx x xxxxx x xxxxxx xxxxxxx xxxxxxxx přípravků xxxxxxxxx xx xxx x Xxxxx xxxxxxxxx, xxxxx xx x xxxxxxxxx.“.
XXXXX: 32001L0083, 32004L0027
17. X §33 xxxx. 3 xxxx. x) xx slova „xx xxxxxxxxxx xxxx xxxxxxx“ nahrazují xxxxx „xxxxxxxxx na xxx x České xxxxxxxxx“.
18. V §34 xx xx konci xxxxxxxx 2 xxxxxxxx xxxx „Xxxxxx xxxxxxxxx xxxxxxxxxxxx údajům x xxxxxxxxxxx xxxx prodloužením xxxxxxxxxx xxx, xxxxx xxxxxx x rozhodnutí x prodloužení registrace xxxxxxxxx xxxxx, nadále xxxxxx xx trh xxxxxxx xx dobu 180 dnů od xxxxxxxxx xxxxxxxxxxx registrace. Xxxxxxxxxxxx, vydávat, v xxxxxxx xxxxxxxxxxx léčivých xxxxxxxxx prodávat, x xxxxxxxx xxx xxxxxxxxxxx xxxxxxxxxxx služeb xxxx xxxxxxxxxxx xxxx xx xxxxxx léčivý xxxxxxxxx xxxxx xxxx po xxxx xxxx použitelnosti.“.
19. X nadpisu xxxxx XX se xxxxx „VÝROBY“ xxxxxxxxx xxxxxx „XXXXXX“.
20. Nadpis xxxx 1 xxxxx XX xxx: „Xxxxxxxx studie“.
21. §51 až 53 xxxxx:
„§51
Xxxxxxxx xxxxxxxxx xxxxxxxxx léčivých xxxxxxxxx
(1) Xxxxx xxxxxxxx xxxxxxx x xxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx xxxxx x xx. 5, 13 x 14 xxxxxxxx x klinickém xxxxxxxxx x xxxxxxx x xxxxxxxx významné xxxxx xxxxxxxxxx hodnocení x xxxxxxx s čl. 16 Xxxxxxxx XX x xxxxxxxxx xxxxxxxxx. Xxxxx xxxx xxxxxxx xxxxxx xxx průběhem xxxxxxxxxx hodnocení. Veškeré xxxxx xxxxxxxxx x xxxxxxxxxxx s xxxxxxxxx xxxxxxx o povolení xxxxxxxxxx xxxxxxxxx a xxxxxxx x xxxxxxxx xxxxxxxx xxxxx klinického xxxxxxxxx x xxxxxxxxxx xxxxxxx xx xxxxxxxx xx odborné úkony.
(2) Xxxxx je x Xxxxx xxxxxxxxx xxxxxxxx xxxxxxxxxx xxxxxx podle xx. 83 xxxxxxxx x xxxxxxxxx xxxxxxxxx.
(3) Xxxxx x xxxxx xxxxxxxxxx xxxxxxx x xxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxx přípravků xxxx xxxxxxxx xxxxx xxxxxxxxxx xxxxxxxxx
x) x xxxxxxx, že xx Xxxxx republika xx xxxxxx x xxxxxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxx zpravodajem xxxxx xx. 5 odst. 1 xxxx xx. 14 xxxx. 2 xxxxxxxx o xxxxxxxxx xxxxxxxxx, xxxxxxxx činnosti xxxxxxxxx xxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxxx x xxxxxxxxx xxxxxxxxx, týkající xx xxxxxxx, xx xxxxx xx xxxxxxxx xxxx X xxxxxxxxx xxxxxx,
x) x xxxxxxx, xx Xxxxx xxxxxxxxx xxxx ve xxxxxx x příslušnému xxxxxxxxxx xxxxxxxxx xxxxxxxx státem xxxxxxxxxxx, xxxxxxxx xxxxxxxx xxxxxxxxx členského státu xxxxx čl. 2 xxxx. 12 xxxx xx. 14 xxxxxxxx x klinickém xxxxxxxxx, xxxxxxxx xx xxxxxxx, xx xxxxx xx xxxxxxxx xxxx X xxxxxxxxx xxxxxx, x
x) xxxxxxxxxxx část XX xxxxxxxxx xxxxxx x xxxxxxx o povolení xxxxxxxxxx xxxxxxxxx xxxxxxxx xx Xxxxx republiky x x xxxxxxx x povolení xxxxxxxx xxxxx xxxxxxxx xx Xxxxx xxxxxxxxx, xxxxx xxxxxxxx xx xxxxxxxxxx xxxxxxxxxxx xxxxxxx komisí.
(4) Xxxxx xxxxxxxxx x xxxxxxx x xxxxxxxx xxxxxxxxxx xxxxxxxxx a x xxxxxxx x xxxxxxxx xxxxxxxx změny xxxxxxxxxx hodnocení xxxxx xxxxxxxx x xxxxxxxxx xxxxxxxxx. Tato rozhodnutí xxxxx xxx území Xxxxx republiky.“.
CELEX: 32014R0536
§52
Xxxxxxx xxxxxxxxx xxxxxx xxxxxxxx xxxxxxxxx
(1) Xxxxxxxx xxxxxxxxx xxx provádět x xxxxxxxxx xxxxx za xxxxxxxxxxx, xx xxxxx xxxxxxxxxxxxx xxxxxxxx jeho xxxxxxxxx zástupce xxxxxxx x xxxxxx x xxxxxxxxx hodnocení podpisem xxxxxxxxx xxxxxxxx x xxxxxxx nezletilá osoba, xx-xx xx xxxxxxxxx xxxx xxxxxxxx a xxxxx xxxxxxxxxx.
(2) Xxxxxxxx xxxxxxxxx xxx xxxxxxxx xx xxxxxxxx xxxxxxxxxxx xxxxx xxxxxxx také x xxxxxxxxxxxx xxxxxx xxxxxxxx, do xxxxxxx xxxxxx xxxxx
x) nacházející xx xx xxxxx, xxxxxxxxxxxxx detenci nebo xx xxxxxx xxxxxx xxxxxx xxxxxxx,
x) pobývající x zařízení ústavní xxxx,
x) jejichž xxxxxxxxxxx xxxx xxxxxxx soudem.
(3) Xxxxxxxx hodnocení lze xxxxxxxx x osob xxxxxxxxx x odstavci 2 xxx xxxxx, xxxxx x xxxx xxxx xxxxx přivolí xxxxxxxxx x xxxxxxxxxxxx xxxxxxxxx a xxxxx xxxxxxxx vědecky xxxxxxxxx xxxxxx opravňující x xxxxxxxxx, xx xxxxx x xxxxxxxxx hodnocení xxxx xxx pro xxxx osoby xxxxx xxxxxxx xxxx xxxxxxxxx xxxxxxxxxxx xxxxxx, který xxxxxxx xxx xxxxxxxxxxxxx xxxxxx x xxxxxx, xxxx pro ně xxxxxxxx xx klinického xxxxxxxxx bude xxxxxxx xxxxxxxx stabilizace, xxxxxxxxx xxxxxxxx, xxxxxxxxxxxx xxxxxxxxxxx xxxxx.
XXXXX: 32014R0536
§53
Xxxxxx xxxxxx
(1) Xxxxxx komise xx xxxxxxx Xxxxxx.
(2) Xxxxxx xxxxxx xxxxxxxx xxxxxx xxxxxx xxx klinickým xxxxxxxxxx a provádí xxxxxx přezkum, xxxxxxxxxx xxxxxx, xxxxxxxx x xxxxxxx xxxxxxx, žádostí x xxxxxxxx xxxxxxxxxx xxxxxxxxx, xxxxxxx o xxxxxxxx významné xxxxx xxxxxxxxxx xxxxxxxxx a xxxxxx xxxxxxxxxx x xxxxxxx x xxxxxxxx xxxxx xxxxxx xxxxxx x nařízení x xxxxxxxxx xxxxxxxxx.
(3) Xxxxx xxxxxxxxx xxx xxxxxxx xxxxxx xxxxxxxx pro xxxx xxxxxxx.
(4) Ústav xx xxxxxxxxxx souhlasu Xxxxxxxxxxxx xxxxxxxxxxxxx xxxx Xxxxxx xxxxxx komise. Xxxxxxx řád etické xxxxxx (xxxx jen „Xxxxxxx řád“) přijme xxxx xxxxxx xxxxxx. Xxxxxx etické xxxxxx x Xxxxxxx řád Xxxxx xxxxxxxx na xxxxx xxxxxxxxxxxxx stránkách.“.
CELEX: 32014R0536
22. Xx §53 xx vkládají xxxx §53x xx 53x, xxxxx znějí:
„§53a
Složení xxxxxx xxxxxx
(1) Xxxxxx komise xx složena ze xxxxxx. Skupiny xxxx xxxxxxx x odborníků x oblasti zdravotnictví x osob xxx xxxxxxxxxxxxxx xxxxxxxx. Xxxxx xxxxxx a počet xxxxx xxxxxxxxxxxx xxxxxx xxxxxx xxxxxx xxxxxxx Xxxxxx xxxxxx komise. Xxxxxxx etické komise xxxx xxxxxxxxx tak, xxx v xxxxx xxxxxxx etické komise xxxx xxxxxxx 5 xxxx, x nichž xxxxxxx 1 xxxxx xxxx xxx zdravotnického xxxxxxxx.
(2) Xxxxx xxxxxx xxxxxx xxxxxxx a xxxxxxxx xxxxxxx xxxxxxxxxxxxx, x xx do xxxxxxxxxxxx xxxxxx. Skupiny xxxxxx xxxxxx xx xxxxxxxx x předsedy, xxxxxxxxxxxxx x xxxxxxx xxxxx. Xxxxxxxx x xxxxxxxxxxxxx xxxx xxxxxx xxxxx xxxxxxx x xxxxxxx x Jednacím xxxxx etické komise.
(3) Xxxxxxx xxxxxx xxxxxx xxxx xxxxxxxx xxxxxxxxx xx. 9 nařízení x klinickém xxxxxxxxx x xxxx musí xxx xxxxxxxxxxx a xxxxxxxxx xxxxxxxxx x xxxxxxxx xxxxxx x xxxxxxxx hodnocení z xxxxxxxx etického, xxxxxxxxxx x xxxxxxxxx, s xxxxxxxx osoby xxx xxxxxxxxxxxxxx xxxxxxxx, xxxxx xxxxxxxx xxxxxx x xxxxxxxx hodnocení xxxxxxx x hlediska etického.
(4) Xxxxxxx xxxxxx xxxxxx xx xxxxx xxxxxxxxx x žádostem x xxxxxxxx klinického xxxxxxxxx, xx xxxxx xxxxxxxxx xxxx xxxxxx xxxxx, xxxxx i vyjádření x xxxxxxxxx žádostem x xxxxxxxx významné xxxxx x vykonávání xxxxxxxxx xxxxxxx xxx xxxxxxx xxxxxxxxx xxxxxxxxxx x neprodleně xxxxxx xxxxx xxxxxxxx xxxxx xx posuzovaném xxxxxxxxx xxxxxxxxx xxxxxx komisi x Xxxxxx.
(5) Xxxxxxx xxxxxx komise xxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxxxx x informacích x xxxxxxxxxxxxx, xxxxx se xxxxx x xxxxxxxxxxx xx xxxx členstvím x etické komisi.
(6) Xxxxxx xxxxxx komise xxxxxx xxx xxxxx, xxxxx se dopustila xxxxxxxxx xxxxx §108 xxxx. 8. Xxxxxxxx-xx xx xxxx xxxxxx xxxxxx xxxxxxxx xxxxxxxxx, xxxx xxxxxxxx v xxxxxx xxxxxx xxxxxx.“.
XXXXX: 32014R0536
§53x
Xxxxxxx etické xxxxxx
(1) Xxxxxxxxxx xxxxxx xxxxxx xx xxxxxxxxx x xxxxxxx xxxx, xxxxxxxxxxx x xxxxxx xxxxxxxx xxxxxxxxx.
(2) Etická komise xxxxxxxxxxx dohled xxx xxxxxxxxx xxxxxxxxxx na xxxxxxx xxxxxx x xxxxxxx xxxxxxxxxx xxxxxxxxx xx xxxxxxxxxxxxx xxxxxxxx, x xxxx xxxxxxxx xxxxxxxxx xxxxxxx, (dále xxx „xxxxx xxxxxxxxxx xxxxxxxxx“) xxxxxxxxxx xxxxx xxxxx xxxxxxx xxxxxxxx xxxxx xxxxxxxxxxx xxxx xxxxxxx zkoušejícím. Xxxxxxxxxxx xxxxxx x xxxxxxx xxxxxxxxxx xxxxxxxxx x xxxxxx intervaly pro xxxx předkládání xxxxxxx xxxxxxxxx xxxxxx předpis.
(3) Xxxxxx xxxxxx xxxx xxx xxxxxxx xxxxxx xxxxxxx další xxxxxxxxx. Xxxx xxxxxxxxx xxxx xxxxxxxx požadavky xx. 9 xxxxxxxx o xxxxxxxxx hodnocení. Xxxx xxxxxxxxx xxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxxxx o xxxxxxxxxxx a xxxxxxxxxxxxx, xxxxx xx xxxxx x souvislosti xx xxxx xxxxxxxx x xxxxxx komisi.
(4) Xxxxxx xxxxxx xxxxxxxx xxxx xxxxxxx x xxxxxxx x Jednacím xxxxx, xxxxx xxxxxxxx xxxxxxx
x) xxxxxx plánování zasedání, xxxxxxxxxx členů xxxxxxx x xxxxxx xxxxxx xxxxxxxx.
x) xxxxxx xxxxxxxx xxxxxxxxxxx xxxxxxxxxx etické xxxxxx.
(5) Xxxxxx komise xxxx vykonává xxxx xxxxxxx xxxxx xxxxxxxxxx xxxxxxx xxxxxx xxxxxx, xxxxx xxxxxxx Xxxxx x xxxxx xxxxxxxx xxxxxxx
x) xxxxxx xxxxxxxxxx xxxxxxx x xxxxxxxx xxxxxxxxxx xxxxxxxxx a xxxxxxx x povolení xxxxxxxx změny klinického xxxxxxxxx v rozsahu xxxxxxxxxx xxxxxxxxx o xxxxxxxxx xxxxxxxxx,
x) xxxxxxx xxx nakládání x xxxxxxxx xxxxxxxxxxxx nebo xxxxxxxx xxxxxxxxxxxx, xxxx-xx xxxxxxxx, a zadavatelů x x xxxxxxxxxxx xxxxxxxxx dohledem xxx xxxxxxxxx xxxxxxxxxx xx xxxxxxxxx jiným xxxxxxxx xxxxx xx. 52 xx 54 xxxxxxxx x klinickém xxxxxxxxx,
x) xxxxxx, jakým xxxxxx xxxxxx xxxxxxx Xxxxxx xxx xxxxxxxxxx xx xxxxxxxxxx xxxxxxxxx xxxxxx xxxx xxxxxxxxxx.
XXXXX: 32014R0536
§53x
Xxxxxxxxxx
(1) Xxx přípravě stanoviska, xxxxxxxxxx xx xxxxxxx, xx xxxxx xx xxxxxxxx část X xxxxxxxxx xxxxxx x xxxxxxx x xxxxxxxx xxxxxxxxxx xxxxxxxxx xxxx xxxxxxx o xxxxxxxx xxxxxxxx změny klinického xxxxxxxxx x rozsahu xxxxxxx, xx xxxxx xx vztahuje část X hodnotící xxxxxx, xxxxxx xxxxxx xxxxxxx xxxxxxxx klinického hodnocení x xxxxxxx
x) xxxxxxxxxxxxxxx xxxxxxxxxx hodnocení x xxxx xxxxxxxxxx,
x) xxxxxxxxxxxxx xxxxxx xxxxxxxxxxxxxxx xxxxxxx x xxxxx x xxxxxxxxxxxxx xxxx xxxxxx, x
x) etických xxxxxxx xxxxxxxxxx xxxxxxxxx.
(2) Vydala-li xxxxxx komise x xxxxxxx s nařízením x xxxxxxxxx hodnocení xxxxxxxxx stanovisko, je xxxx stanovisko xxxxxxx x xxxxxx x xxxxxxxx xxxxxxxxxx xxxxxxxxx xxxx x povolení xxxxxxxx xxxxx xxxxxxxxxx xxxxxxxxx v České xxxxxxxxx Ústav xxxxxxxxxxx xxxxxxx. Negativní xxxxxxxxxx, xxxxxxxx se xxxxxxx, xx xxxxx xx xxxxxxxx část X xxxxxxxxx zprávy x xxxxxxx x xxxxxxxx xxxxxxxxxx hodnocení xxxx x xxxxxxx x xxxxxxxx xxxxxxxx xxxxx xxxxxxxxxx hodnocení týkající xx xxxxxxx protokolu xxxx xxx xxxxxx xxxxx z xxxxxx xxxxxxxxx x xxxxxxxx x klinickém xxxxxxxxx. Xxxxxxxxxx musí obsahovat xxxxxxxxxx, xx kterém xx uveden xxxxx x xxxxx xxxxxxxxxxx x xxxxxxxxxxxx xxxxxx, xxx xxxxx zaujala xxxxxx xxxxxx své xxxxxxxxxx. Xx řádné xxxxxxxxxx stanoviska x xxxx xxxxxx předání Xxxxxx odpovídá předseda xxxxxx komise.
(3) Xxxxxx xxxxxx xxxx před xxxxxxxxx klinického xxxxxxxxx xxxxxxxxxx xxxxxxxx se xxxxxxx, na xxxxx xx vztahuje část XX xxxxxxxxx xxxxxx x žádosti s xxxxxxxxx xxxxxxxxxxx xxxxx xxxxxxxxxx. Xxx xxxxxxxx xxxxxx xxxxxxxxxx etická xxxxxx xxxxxxxxx x xxxxxxx s xxxxxxxxx x klinickém xxxxxxxxx.
(4) Xxx zpracování xxxxxxxxxx xxxxxx xxxxxx xxxxx xxxxxxxx 3 skupina xxxxxx komise xxxxxx xxx xxxxxxxxx xxxxxxxxxxx xxxxxxxxxx hodnocení xxxxxxx xxxxx xxxxxxxxx xxxxxxxxxxx xxxxxxxxx o klinickém xxxxxxxxx xxxxxxxxxxx předloženou xxxxxxxxx x xxx, xx xxxx xxxxxxxxxxx xxxxxxx x xxxxxxxx, xxx
x) kompenzace xxxx xxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx pro xxxxxx xxxxxxxxx xxxx x xxxxxxxx jeho účasti x xxxxxxxxx hodnocení xxxx xxxxxxxxx xxxxxxxxx xxxxxxxx,
x) xxxxxxxxx odpovědnosti xxx zkoušející x xxxxxx xxxxxxxxxx, jsou-li xxxxxxxx, x zadavatele xx xxxxxxxxx xxxxxxxxx xxxxxxxx, xxxxxxxxx xxx xxxxxxxxx odpovědnosti xxxxxxxxxxxx x hlavních xxxxxxxxxxxx, xxxx-xx xxxxxxxx, nebo xxxxxxxxxx není xxxxxxxx xxxxxx pracovněprávních xxxxxx,
x) xxxxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxx xxxxxx vynaložené xxxxxxxxx xxxxxxxxx v souvislosti x xxxx xxxxxx x xxxxxxxxx xxxxxxxxx,
x) xxxx xxxxxx xxx xxxxxxxx xxxxxxxxx xxxxxxxx xxxxxx klinického hodnocení, x xx xxxxxxx xx xxxxxx x xxx výzkumným výkonům, x nichž xxxx xxxxxxx xxxxxxxxx xxxxx xxxxxxxx,
x) xx xxxxxxxx xxxxxx xxxxxxxxx xxxxxx xxx zkoušející x xxxxxxxx xxxxxxxxxxxx, xx-xx xxxxxxx,
x) xxxxxxxxxx a xxxxxx zkoušející, je-li xxxxxxx, xxxxxxx xxxxxxxxx xxxxxxxxx x §54,
x) xxxxx xxxxxxxxxx hodnocení xx xxxxxx x xxxxxxxxx xxxxxxxxxxx klinického xxxxxxxxx.
(5) Etická komise xxxxxxxx x hlediska xxxxxxx xxxx, bezpečnosti x zdraví xxxxxxxx xxxxxxxxx kompenzace x xxxxxxx xxxx xxxxxxxx xxxxxxxxx a jejich xxxxxx x xxxxxxxxxx xxxxxxxxxxxx, xxxx hlavních xxxxxxxxxxxx, xxxx-xx xxxxxxxx, xxxxxxx x dokumentaci x xxxxxxx x xxxxxxxx xxxxxxxxxx hodnocení.
(6) Xx řádné xxxxxxxxxx xxxxxxxxxx xxxxx xxxxxxxx 3 x jeho xxxxxx xxxxxxx Ústavu xxxxxxxx xxxxxxxx xxxxxx xxxxxx. Stanovisko musí xxxxxxxxx xxxxxxxxxx xxxxxxxxxx.
(7) Xxxxxx komise xxxx xxxxxxx xxxxxx xxxx xxxxxxx xxx xxxxxxxxx xxxxxxxxxx x xxxxxxxxxx xxxxxxxxxx hodnocení, xxxxxxxx xx xxxxxxxxx xxxx xxxxxxxxxxx xxxxxxxxx xxx xxxxxxxxxx xxxxxxxx xxxxxxxxx xxxx xxxxxxxxx xxxx xxxxxx xxxxxxxxxx nebo xxxxxxxxxx xxxxxx xxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx xx xxxxxxxxxx klinického xxxxxxxxx, x xxxxx xxxxxx xxxxxx xxxxxx xxx xxxxxxxxx stanovisko. Xxxxxx-xx xxxxxx xxxxxx, xx xx xxxxxxxx xxxxxx xxx xxxxxxxx xxxxxx xxxxxxxxxxx xxxxxxxxxx xxxxxxxxx xx xxxx xxxxx, požádá Xxxxx, xxx xx xxxxxxx xxxxxxxxxx xxxxxxxxxx, xxxxxxxxx xxxxxxxxxxxx nebo hlavního xxxxxxxxxxxx x xxxxx xxxxxxx, x xxxxxxxx xxxxxxx, kdy je xxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx. Xxxxxxxx xxxxxxxxxxx xxxxxxxxxx xxxxxx xxxxxx xxxxxxxx
x) xxxxxxxxxxxxx xxxxx x xxxxxxxxx xxxxxxxxx, xxxxxxx xxxx xxxxx, xxxxxxx xxxxxxxxxx xxxx xxxxxxxxxx, xxxxxxxx xxxxxxxxxxxxx xxxxx a xxxxx xxxxxxxxx,
x) výslovné xxxxxxx, xxx xx xxxxx x xxxxxxx xxxx xxxxxx xxxxxxxx xxxxxxxxxxx xxxxxxxxxx, x xxxxxxx xxxxxxxxx xxxxxxxx souhlasu xxxx xxx stanoveny xxxxxxxx, xx jejichž xxxxxxx xxxxxxxx xxxxxxxx xxxxxxx,
x) xxxxxxxxxx, ve xxxxxx xx uvedou xxxxxx xxxxxxxx xxxxxxxxxxx xxxxxxxxxx, xxxxxxxx pro xxxx xxxxxx x xxxxx, xxxxxxx se xxxxxx xxxxxx xxxxxx,
x) xxxxxxxx xxxxxxxx k xxxxxxxx klinického xxxxxxxxx, xxxxxxx k xxxxxxx xxxxxxxx hodnocení xx xxxxx xxxxx, nejsou-li xxxxxxx již v xxxxxxxxx,
x) datum xxxxxxxx xxxxxxxxxxx xxxxxxxxxx x xxxxxx xxxxxxxx xxxxxxx xxxxxx xxxxxx, která xxxxxxxx xxxxxx.
(8) Etická xxxxxx xx na xxxxxxxx Xxxxxx xxxxxxx xxxxxx Ústavu xxx xxxxxxxxxx xx xxxx xxxxxxxxxx, xxxxx xxxxxxxxx xxxxxxxxx xxxxxxx xxxxxx,&xxxx; xxxxxxxxxx xxxxx xxxxxxxx xxx xxxx xxxxxxxxx xxxx lhůty, xxxxxxxxxx Xxxxxx xxx xxxxxx xxxxxxxxx x xxxxxxx xxxxxxx, xxxxxxx x xxxxxxxx xxxxxxxxxxx x xxxxxxx, xxxx koordinovaného xxxxxxxx, fázi xxxxxxxxxxx, xxxxxxxxx xxxxxxxxxxxx xxxxxxxxx, xxxxxxxxx xxxxxxxxx xxxxxxx xx xxxxxxxx xxxxxxxxxxxx xxxxxxxxx, xxxxxxxxxx xxxxxxx xxxxx I xxxxxxxxx xxxxxx nebo předložení xxxxxxx části XX xxxxxxxxx xxxxxx, x xxxxx posouzení podle xx. 5, 6, 7, 13, 14, 17, 18, 20 x 22 nařízení x klinickém xxxxxxxxx.
(9) Xxxxx xxxxxxxx x xxxxxxxxxxx s xxxxxxxx xxxxxx xxxxxx po xxxx 5 let xx xxxxxxxx klinického xxxxxxxxx tyto xxxxxxxxx:
x) xxxxxx x jednání,
b) xxxxxxxxxx x střetu xxxxx,
x) xxxxxxxxxx xxxxx xxxxxx xxxxxx,
x) xxxxxxx x xxxxxxxxxx a xxxxxx vzdělávání xxxxx xxxxxx xxxxxx,
x) dokumenty x xxxxxxxxx x xxxxxxxx xxxxx xxxxxx xxxxxx,
x) xxxxxxxxx xxxxxxxxxx xx xx jmenování, xxxxxxxx členů xxxxxx xxxxxx, xxxxx x xxxxxxxxxx x funkce,
g) xxxxxxxxxxxxxx x obdobné xxxxxxx, včetně xxxxxxxx, xxxxx xxxxxxxx k xxxxxx xxxxxxxxxx, x xxxxxxxxx xxxxxxxxxxxxxxxx x xxxxxxx komisí, a
h) xxxxxxxxxxxxx etické xxxxxx.“.
XXXXX: 32014R0536
23. §54 xx 59 xxxxxx xxxxxxxx xxx čarou x. 102 x 103 xxxxx:
„§54
Xxxxxxxxxx x místo xxxxxxxxxx xxxxxxxxx
(1) Xxxxxxxxxxx x hlavním xxxxxxxxxxx xxxx xxx pouze xxxxx xxxx xxxxx xxxxx xxxxxxxxx podmínky xxxxxxxxx xxxxx právním xxxxxxxxx29) xxx xxxxx xxxxxx xxxxxxxxxxxxxx xxxxxxxx, xxxxx xx nezbytné xxxxxxx znalosti a xxxxxxxxxx s xxxx x pacienty s xxxxxxxxxxx xxxx xxxxx, xx xxxxxxx léčbu xx xxxxxxxx dané xxxxxxxx xxxxxxxxx, x xx xxxxxxxx xxxxxxx xxxxxxxx praxe.
(2) Xxxxxxxx xxxxxxxxx xxx xxxxxxxx xxxxx x xxxxxxxxxxxxx xxxxxxxxxxx xxxxxx xx xxxxxxxxxxxxx xxxxxxxx.
(3) Poskytovatel xxxxxxxxxxx xxxxxx, x xxxxx xx prováděno xxxxxxxx xxxxxxxxx, x xxxx dochází k xxxxxxx xxxxxx xxxxxxxxxxx xxxxxxxx přípravku člověku, x xxxxxxxxxxxx xxxxxxxxxxx xxxxxx, x něhož xx xxxxxxxxx klinické xxxxxxxxx bez xxxxxxxxx xxxx xxxxxxxxxxxxx xxxxxx xxx xxxxxxxx hodnocení, x to zejména xxxxxxxxxxxxxxx x xxxxxxxxxxxxxxxx xxxxxxxx hodnocení, musí xxx xxxxxxxxx certifikátu xxxxxxx xxxxxxxx xxxxx xxxxxxxx Xxxxxxx. Xxxxxx x xxxxxx udělování xxxxxx xxxxxxxxxxx stanoví xxxxxxxxx právní xxxxxxx.
(4) Xxx xxxxxxxxxxxxx xxxxxxxxxxx xxxxxx xxxxxxxxx x xxxxxxxx 3, u xxxxx jsou prováděna xxxxxxxx xxxxxxxxx, xxxx xxxxxxx xxxxxxxxxxx správné xxxxxxxx xxxxx xxxxxxx; xxxxx xxxx x xxxx vydání požádat; xxxxxxxx 3 xxxx xxxxx xx použije xxxxxxx.
XXXXX: 32014R0536
§55
Xxxxx
(1) Xxxxxxxxxxx xxxxxxxxxx xxxxxxxxx xxxx xxx xxxxxxxxxx x xxxxxx jazyce, xxxxx xxx o tyto xxxxxxxxx:
x) xxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxx,
x) xxxxxxxxx xxx pacienta, xxxxxxxxxxx xxxxxxx, xxxxxxx xxxxxxxxxxx x xxxx xxxxxx x xxxxxxxxx hodnocení x xxxxxxx k xxxxx xxxxxxxxxx,
x) xxxxxxxxx x xxxxxxx náboru xxxxxxxx xxxxxxxxx x Xxxxx xxxxxxxxx,
x) náborové xxxxxxxxx vztahující se x xxxxxx xxxxxxxxxx xxxxxxxxx,
x) xxxxxxx materiály xxxxxx subjektům xxxxxxxxx,
x) xxxxxx xxxxxxxxxxxx x xxxxxxxx zkoušejících, xxxx-xx xxxxxxxx,
x) seznam xxxx xxxxxxxxxx hodnocení,
h) doklad x xxxxxxxxx náhrady xxxx subjektům hodnocení,
i) xxxxxxxxx o způsobu xxxxxxxxx xxxxxxxxxx xxx xxxxxxxxxx x xxxxxx xxxxxxxxxx, jsou-li xxxxxxxx, x odměňování nebo xxxxxxxxxx pro xxxxxxxx xxxxxxxxx.
(2) Xxxxxxx xxxxxxxxxxx xxxxxxxxxx hodnocení, xxxxx-xx x xxxxxxxxx uvedené x xxxxxxxx 1, xx xxxxxxxxx x xxxxxx, xxxxxxxxxx nebo xxxxxxxxx xxxxxx.
(3) Xxxxxxxxx x xxxxxxxx xx xxxxx léčivých xxxxxxxxx xxx klinické hodnocení xx uvádějí x xxxxxx xxxxxx, není-li x xxxxxxxxxx Xxxxxx xxxxxxx xxxxx.
XXXXX: 32014R0536
§56
Xxxxxxxxx x xxxxxxx xxxxxx xxxxxxxxx
(1) Jsou-li xxxxxxx xxxxxxxx xxxxxxxxx x xx. 59 odst. 2 nařízení x xxxxxxxxx xxxxxxxxx, xxxxx xxx xx xxxxx Xxxxx republiky xxxxxxx xxx klinickém xxxxxxxxx x xxxxxxxxxxxxxx léčivé xxxxxxxxx.
(2) Zadavatel xxxxxxxxx xxxxxx hodnocené léčivé xxxxxxxxx, pomocné xxxxxx xxxxxxxxx neregistrované xxxxx xxxxxx xxxxxx xxxxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxxxxxx x xxxxxxxxxxxx prostředky xxxxxxxx pro provedení xxxxxxxxxx xxxxxxxxx, xxxxx xxxx určeny x xxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx. V xxxxx xxxxxxxxxx hodnocení humánních xxxxxxxx xxxxxxxxx, xxxxx xxxxx použít xxxxxxxxxxxx xxxxxxxxxxxx xxxxxxxxxx, xxx xxxxxx xx xxxxxxxxxx xxxxxxxxx Ústavem x xxxxxx zdravotnický xxxxxxxxxx, xxxxx xxxxx xxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxx x zdravotnických xxxxxxxxxxxx. Xx-xx xxxxxxxxxxx xxxxxxxxxx xxxxxxxxx, kterým se xxx xxxxx tohoto xxxxxx xxxxxx poskytovatel xxxxxxxxxxx xxxxxx xxxxxxx xxxx xxxxxxxx xxxxxx xxxx xxxxxxx xxxxxxxxxxxx xxxxxx, xxxxxxx xxxxxx xxxxx x xxxxxxx xxxxxxxx instituce, x xxxxxxxxx léčivé xxxxxxxxx xxxx registrované x Xxxxx xxxxxxxxx, xxxx xxxxxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxx povinné.
(3) Xxxx-xx xxx v xxxxxxxxx hodnocení xxxxxxxxx xxxxxxxx xxxxxxxxx použita xxxxxxxxxxxx xxxxxxxxxxxxxx xxxxx xxxxxx zákona, xxx x souladu x xxxxxxxxx xxxxxxxx x xxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx xxxxx x xxxxxxxxxxx k žádosti x xxxxxxxx xxxxxxxxxx xxxxxxxxx stanovisko Xxxxxxxx xxxxx pro jadernou xxxxxxxxxx xxxxxx xxxxx §18.
(4) Mají-li xxx x xxxxxxxxx xxxxxxxxx xxxxxxxxx léčivých xxxxxxxxx xxxxxxx přípravky obsahující xxxxxxxxx xxxxxxxxxxxx organismy, xxxxxxxx xxxxxxxxx spolu x dokumentací x xxxxxxx x xxxxxxxx xxxxxxxxxx hodnocení souhlas Xxxxxxxxxxxx životního xxxxxxxxx xxxxxx xxxxx jiného xxxxxxxx předpisu11).
(5) Mají-li xxx x xxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxx přípravky xxxxxxxxxx lidské xxxxxxxxxxx xxxxxxx buňky, předloží xxxxxxxxx xxxxx x xxxxxxxxxxx x xxxxxxx x xxxxxxxx klinického xxxxxxxxx povolení k xxxxxxxxx s lidskými xxxxxxxxxxxxx xxxxxxxxx buňkami xxxxxx Xxxxxxxxxxxxx xxxxxxxx, xxxxxxx x xxxxxxxxxxx xxxxx jiného právního xxxxxxxx102).
(6) Xxx xxxxxxxxx xxxxxxxx xxxxxxxxx xxxx xxxxxxxxxxxxxxxx klinická xxxxxxxxx xxxxx xx. 2 xxxx. 3 xxxxxxxx x xxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxxxxxx xxxxxxxxxx, xxxxx xxxxxxx xxxxxxxxx xxx xxxxxxxxxx nebo xxxxx xxxxxxxxxx léčivého xxxxxxxxx, xxxxxxx prováděcí xxxxxx xxxxxxx xxxxxxxxx xx monitorování, xxxxx xxxxxxxxxx dokumentů a xxxxxxxxx xxxxxxxxxx xxxxxxxxxxx xxxxxxxx přípravků. Klastrovým xxxxxxxxx hodnocením xxxxx xxxx xxxxx se xxxxxx klinické xxxxxxxxx xxxxxxxxx xxxxx xx xxxxx Xxxxx republiky, xxxxx xxxxx je xxxxxxxxx léčby skupin xxxxxxxx, v xxxxx xxxxxxx xxxx veškeré xxxxxxxxx xxxxxx xxxxxxxxx xxxxxxxxxxxx podle xxxxxx xxxxxx x Xxxxx xxxxxxxxx x xxxx xxxxxxxxx v xxxxxxx xx xxxxxxxx xxxxx x xxxxxxxxx xxxx xxxx xxxxxx xxxxx x přípravku, je-li xxxxxx způsob použití xxxxxx x xxxxxx xxxxxxxxx praxí xxxx xxxxxxxxxxxx léčebnými xxxxxxx x xxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxx.
XXXXX: 32014R0536
§57
Dohoda xx xxxxxxxxxxx
Xxxxx xxxx xx xxxxxxxx stanovených x xx. 42 xxxx. 3 nařízení x xxxxxxxxx xxxxxxxxx xxxxxxx xx zadavatelem xxxxxx, xxxxx níž xxxx xxxxxxxxx podezření xx závažné xxxxxxxxxxx xxxxxxxxx účinky hlásit xxxxx Ústavu; v xxxxxxx xxxxxxx xxxxxx xxxxxxxxx na xxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxx xxxxxxxx Xxxxx.
XXXXX: 32014R0536
§58
Xxxxxx xxxxxxx xxxx xxxxxxx xxxxxxxx xxxxxxxxx
(1) Xxxxxxx-xx xxxxxxxx xxxxxxxxxx xxxxxxxxx x xxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxx xxxxxxxxxxx xxxx, x xx xxxxxxx xx xxxxxx xxxx xx xxxxxx, xx xxxxxxxxx povinen xx xxxxxxxx x xxxxxxx x xxxxxx xxxxxxxx xxxxxxxx 103). Xxxxxxx xxxx xxx uplatnit x zadavatele prostřednictvím xxxxxxxxxxxxx zdravotních xxxxxx, xxxxx je místem xxxxxxxxxx xxxxxxxxx.
(2) Xxxxxxxxx xx xxxxxxx xxx xx xxxxx xxxx xxxxxxxxx klinického xxxxxxxxx xxxxxxxx pojištění odpovědnosti xxx, hlavních xxxxxxxxxxxx, xxxx-xx xxxxxxxx, a xxxxxxxxxxxx xx xxxx xxxxxxxx xxxxxxxx xxxxxxxxx x xxxxxxxx xxxxxxxxx xxxxxxxxxx hodnocení.
(3) Xxxxxxxx 2 xx xxxxxxxxx, xxxxxxx-xx xxxxxxxx hodnocení xxxxxxxxxx xxxxxxxxx, xxxxx xxxxxxxxx xxxxxxxx xxxxxxx xxxxxxx léčivých xxxxxxxxx x xxxxx klinického xxxxxxxxx,
x) x xxxxxxxx xxxxxxxxx xxxxxxxxxxxxxx xxxxx xxxxxx zákona x Xxxxx republice x xxxxxxxxxxx x xxxxxxx xx xxxxxxxx xxxxx x přípravku, xxxxxxxxx x xxxxxxxx xxxxxxxxx xxxxxxxxxxxxxx podle xxxxxx xxxxxx v České xxxxxxxxx x xxxxxxxxxxx xxxx souhrn údajů x xxxxxxxxx, xx-xx xxxxxx způsob xxxxxxx xxxxxx s xxxxxx xxxxxxxxx xxxxx xxxx xxxxxxxxxxxx xxxxxxxxx xxxxxxx x dostatečně xxxxxxxxx xxxxxxxxx xxxxxxxx, x xxxxxxx
x) xxxxxxxxx xxxxxxxxxxxx xxxx xxxxxxxxxxxx xxxxxxx xxxxxxxxxxxxx x xxxxxxxxx x xxxxxx xxxxxxxxx xxxxx větší xxx xxxxxxxxx xxxxxxxxx xxxxxx xxxx xxxxx pro xxxxxxxxxx xxxxxxxx xxxxxxxxx.
XXXXX: 32014R0536
§59
Xxxxxxxxxx
Xxxxxx-xx xxxxxxxxx x xxxxxxx xxxxxxxxxx xxxxx xxxxxxxx x klinickém xxxxxxxxx xxxxx zástupce xxxx xxxxxxxxx xxxxx, xxxxxxxx se takové xxxxxxxx za xxxxxxxxx xxxxxxxxxx xx základě xxxx moci, xxxxxxxxx-xx xxxxxxxxx nebo zástupce xxxx.
XXXXX: 32014R0536
24. V §60 xxxx. 3 xxxx. x) xx čárka xxxxxxxxx xxxxxx a xxxxxxx d) xx xxxxxx xxxxxxxx xxx xxxxx x. 64 xxxxxxx.“.
25. V §62 xxxx. 1 se xx xxxx druhé, xxxxx „za účelem xxxxxxxxxx hodnocení x“ xxxxxxx.
26. X §64 xxxx. x) se xxxxx „§55 x xxxxxxxxxxx v rámci xxxxxx x xxxxxxx x xxxxxxxx nebo xxxxxxxx xxxxxxxxxx hodnocení“ xxxxxxxxx xxxxx „nařízení x xxxxxxxxx hodnocení x xxxxxxxxxxx x xxxxx řízení x xxxxxxx x xxxxxxxx xxxxxxxxxx xxxxxxxxx xxxx x xxxxxxxx významné xxxxx xxxxxxxxxx xxxxxxxxx“.
XXXXX: 32014R0536
27. X §64 xxxx. w) xx xxxxx „xxxxxx xxxxxxxxxxx xxxxxxxxx léčivých přípravků,“ xxxxxxx.
28. X §66 xx xxxxxxxx 4 xxxxxxx.
Xxxxxxxxx odstavec 5 xx xxxxxxxx jako xxxxxxxx 4.
29. V §70 xxxx. 1 xx xx xxxx xxxxx xx xxxxx „xxxxxxxxx“ xxxxxxxx xxxxx „x xxxxx xxxxxxxxxxx xxxxxxxxx Xxxxxxxx unie101)“ x xx slovo „xxxxx“ xx vkládají slova „xxxxxx léčivých xxxxx xxxxxxxx pro xxxxx“.
XXXXX: 32014R1252
30. X §70 xx doplňuje xxxxxxxx 7, který xxx:
„(7) Xxxxxxx xxxxxxxx látek, xxxxx xxxxxxx xxxxxx, xxxxxxxxxxx, označování, xxxxxxxxxxxx, xxxxxxxx xxxxxxx nebo xxxxxxxxxxx, xxxxx x xxxxxxxxxxx xxxxxxxx xxxxxxxx xxxxx xxxxxxxxxxxxx xx xxxxxxx xxxx xxxxxxxx xxx xxxxxxxx léčivých xxxxxxxxx, musí mít x dispozici xxxxxxxxx xxxxx xxxxxxxx 2; xxx nejsou xxxxxxx xxxxxxxxxx xxxxxxxx 4 x 5.“.
XXXXX: 32014R1252
31. X §77 xxxx. 1 písm. x) xx xxxxx „xxxxxx xxxxx x xxxxxx xxxxxx xxxxxxxxxxx xxxxxx xxxxxxx xxxxxxxx Xxxxx nebo Veterinární xxxxx xx xxxx xxxxxxxxxxx xxxxxxxxxx“ nahrazují xxxxx „xxxxxxxxxxx xxxxx xxxxxxxx identifikaci xxxxxxxxxxxx, xxxxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxxx xxxxxxxxx a xxxxxxxxxxxx xxxxx xxxxx písmene x), xxxxx xxx xxxxxx xxxxxxxxx xxxxxxxxxxxx; xxxxxxxxx xxxxx, xxxxx, xxxxxx x xxxxxx xxxxxxxx jejich poskytování xxxxxxxxxxxxxxx xxxxxxxxxxxxxx xxxxxxx xxxxxxx prováděcí právní xxxxxxx“.
32. V §77 xxxx. 1 xxxx. x) xx xx xxxxx „pacientů x Xxxxx xxxxxxxxx“ xxxxxxxx xxxxx „; v xxxxxxx, že provozovatel xxxxxxxxx xxxxxxx xxxxxx xxxxxxxxx xxxxxx distributora x dodávku xxxxxxxxxxxxxx xxxxxxxx přípravku, xxxxx xx xxxxxxxxxxxxx x xxxxx x období xxxxxxxxxxx 6 xxxxxxxxxxxx xxxxxx prokazatelně distribuoval, xx xxxxxxxxxxx xxxxxxx xxxxxxxx xxxxxx provozovateli xxxxxxxxxxx xxxxxxx xxxxxxxxxxxxxx xxxxxxxx přípravku xx 48 hodin xx xxxxxxxx xxxx požadavku; xxxx xx xxxxxxx xxxxxxxxxx x xxxxxxx x opatřením xxxxxx xxxxxx vydaným Xxxxxxxxxxxxx xxxxxxxxxxxxx za účelem xxxxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxx §77d, xxxxxx xx omezuje xxxx xxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx xx xxxxxxxxx.“.
33. X §77 xx na xxxxx xxxxxxxx 1 xxxxx xxxxxxxxx čárkou x xxxxxxxx xx xxxxxxx x), xxxxx xxx:
„x) x xxxxxxx, xx xx xxxx záměrem xxxxxxxxxxxx xx xxxxxxxxx xxxxxx xxxxxxxxx, xxxxx xx uveden na xxxxxxx xxxxxxxx přípravků xxxxx §77x, oznámit xxxx skutečnost Xxxxxx; xxxxxxxx je poskytováno xxxxxxxxxxxx x xxxxxxxx xxxxxxxxxxxx xxxxxxxxxxxx, xxxxxxxxxxxx xxxxxxxx xxxxxxxxx, xxxxxxxx xxxxxxxx xxxxxxxxx x xxxxxxx xxxxxxxxxx, xxxxx xxxxx distribuce x xxxxx plánované distribuce xxxxxxxx xxxxxxxxx; xxxxxxxxx xxxxx uváděných x xxxxxxxx, způsob a xxxxx xxxxxx xxxxxxxxxxx xxxxxxxxxxxxxxx elektronického xxxxxxx xxxxxxxx stanoví xxxxxxxxx xxxxxx předpis; v xxxxxxx, že xx xxxxxxxx distributora nebylo xx xxx, kterým xxxxxx 15 xxx xxx xxx, kdy xxxxxxxxxxx xxxxxxx záměr xxxxxxxxxxxx xxxxxx xxxxxxxxx, xxxxxx opatření xxxxxx xxxxxx xxxxx §77d xx vztahu x xxxxxx léčivému xxxxxxxxx, xxxx xxxxxxxxxxx xxxxxxx xxxxxxxxxx distribuci v xxxxxxx xxxxxxxxx rozsahu.“.
34. Xx §77x xx xxxxxxxx nové §77x a 77d, xxxxx xxxxxx nadpisu xxxxx:
„§77x
(1) Xxxxx shromažďuje xx xxxxxxxx xxxxxxxxxx x xxxxxxxxxx, xxxxxxxxxxxx x xxxxxxx xxxxxxxxx x xxxxxx xxxxxxxx xxxxxxxxx na xxxx x České xxxxxxxxx x o xxxxxx xxxxxxxx xxxxxxxxx xxxxxxxx x xxxxxxxxx xxx xxxxxxxxxxx zdravotních xxxxxx; xxxx xxxxxxxxx xxxxxxxxxx x vyhodnocuje. Při xxxxxxxxxx xxxxxxxxx xxxxx xxxx xxxxx Xxxxx xxxxxxxxx, xxx množství xxxxxxxx xxxxxxxxx, xxxxx xxxx xxxxxxxxxxxx xxxxx xxxxxxx xxxxxxxxxx odpovídajících xxxxxxxxx vlastností, xxxx xxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxxxxxxx vzhledem ke xxxx xxxxxxxx xxxxxxxxxxx, xxxxxxxxxx pokrývá aktuální xxxxxxx xxxxxxxx x Xxxxx republice. Xxxxx Xxxxx xx xxxxxxx xxxxxxxxxxx uvedených skutečností xxxxx x závěru, xx aktuální zásoba xxxxxxxxxxx léčivého xxxxxxxxx xxxx léčivých přípravků xxx xxxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxx xxxxxxxx x Xxxxx republice x xxxxxxxxxxx tohoto xxxxxxxx xxxxxxxxx nebo xxxxxxxx xxxxxxxxx, kterým xx xxxxxx nedostatečné xxxxxxx xxxxxxxxxx potřeb xxxxxxxx x Xxxxx xxxxxxxxx xxxxx xxxxxxx xxxxxxxxxx xxxx xxxxxxxx xxxxxxxxx, xxxx xxxxxxxx xxxxxxxxxx x účinnost xxxxx xxxxxxxx x Xxxxx xxxxxxxxx x xxxxxx dopadem xx xxxxxxx zdraví xxxxxxxxxxxx x xxxxxxxxx xxxxxxxxxx xxxxxxxxxxx zdravotních služeb, xxxxx Xxxxxxxxxxxx xxxxxxxxxxxxx xxxx xxxxxxxxx, x xx xxxxxx xxxxxxxx x xxxxxxxxx, xx xxxxxxx základě Xxxxx x xxxxxx xxxxxx xxxxx.
(2) Xxxxx xx xxxxxxxxxxx informací xxxxxxxxxxxx Xxxxxxx xxxxx xxxxxxxx 1 xxxxx Xxxxxxxxxxxx xxxxxxxxxxxxx x závěru xxxxxxxxx x xxxxxxxx 1 xxxx xxxxx, xxxxxx xxxxxx xxxxxx xxxxxxxxx xxxx léčivé xxxxxxxxx na xxxxxx xxxxxxxx xxxxxxxxx, xxxxxxx xxxxxxxxxx xx xxxxxxxxx xxxx xxxxxxxxxxxx xxxxxxxxx xxxxxx Xxxxxx podle §77 xxxx. 1 xxxx. q) (xxxx xxx „Xxxxxx“). Xxxxxxxxxxxx xxxxxxxxxxxxx xxxx Seznam, xxxxx zveřejňuje x xxxxxxxxx xxxxx xx xxxxx internetových xxxxxxxxx. Xxxxxx xxxxxxxxx xx xx Xxxxxx zařazují xxxxxx xxxxxxxx xxxxxx xxxxxx.
(3) Xxx xxxxxxxx xxxxxxxx obecné xxxxxx xxxxx xxxxxxxx 2 xx postupuje podle xxxxxxxxx řádu x xxx, xx
x) xxxxx xxxxxxxx obecné xxxxxx xx xxxxxxxx a xxxxxxxx obecné povahy xx xxxxxxxx xxxxxxxx xxxxxxxxxxx dálkový xxxxxxx,
x) xxxxx pro xxxxxxxxx xxxxxxxxxx x xxxxxx xxxxxxxx xxxxxx xxxxxx xxxx 5 dnů xxx xxx xxxx xxxxxxxxxx,
x) xxxxxxxx xxxxxx xxxxxx nabývá účinnosti xxxx xxxxxxxxxxxx xx xxx xxxx zveřejnění.
(4) X případě, xx Xxxxx xxxxxxxx xxxxx xxxxxxxx 1 xxxxx x závěru, xx x xxxxxxxx přípravku xxxxxxxxx xx Xxxxxxx xxx nehrozí xxxxxxxxx xxxxxxxxxxxxxx xxxxxxx xxxxxxxxxx xxxxxx pacientů x Xxxxx xxxxxxxxx, sdělí xxxx xxxxxxxxx včetně xxxxxxxx, xx xxxxxxx xxxxx x xxxxxx xxxxxx došel, Xxxxxxxxxxxx xxxxxxxxxxxxx. Pokud Xxxxxxxxxxxx xxxxxxxxxxxxx na základě xxxxxxxxxxx informací mu xxxxxxxxxxxx xxxxx věty xxxxx dojde ke xxxxxxxx xxxxxx, xxxxxxxx xxxxx xxxxxxxx 2 x 3 xxxxxx xxxxxxxxx xx Xxxxxxx xxxxxx.
§77x
Xxxxxxxx x xxxxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx
(1) X xxxxxxx, že Xxxxx shledá s xxxxxxxxxxxx x xxxxxx xxxxxxxxxxxx xxxxxxx xx xxxxxxxx xxxxxxxxxx o xxxxxxxxxx, distributorů x xxxxxxx, xxxxx xxxxxxxxxxxx xxxxxxxxxx xx zahraničí x následujícím xxxxxxxxxxx xxxxxx x xxxxxxxxxx xxxxxxxx xxxxxxxxx, který xxxx xxxxxxxxxxxx xxxxx xxxxxxx xxxxxxxxxx odpovídajících xxxxxxxxx xxxxxxxxxx, xxxx xxxxxxxx xxxxxxxxx, xxxxx xxxx xxxxxxxx xxxxxxxxxxxx xxxxxxxx xx xxxx xxxxxxxx xxxxxxxxxxx, pro xxxxxxxx xxxxxxx pacientů x Xxxxx xxxxxxxxx x xxxxx xxxxxxxxxx xxxxxxxx dostupnost x xxxxxxxx xxxxx xxxxxxxx x Xxxxx xxxxxxxxx x xxxxxx xxxxxxx xx xxxxxxx zdraví xxxxxxxxxxxx x xxxxxxxxx xxxxxxxxxx xxxxxxxxxxx xxxxxxxxxxx xxxxxx, xxxxx Xxxxxxxxxxxx xxxxxxxxxxxxx podnět x xxxxxx xxxxxxxx xxxxx xxxxxxxx 3.
(2) Xxxxxx Xxxxxx xxxx xxxxxxxxx xxxxxxxxxx xxxxxxxx na xxxxxxxxxxx xxxxx xxxxxxxxxxxxx xxxxxxx xx xxxxxxxx xxxxxxxxxx x xxxxxxxxxx, xxxxxxxxxxxx a xxxxxxx, xx
x) je zřejmé, xx xxxxxxxx zásoba xxxxxxxxxxx léčivého přípravku xxxx xxxxxxxx xxxxxxxxx xxx xxxxxxxxx aktuální xxxxxxx xxxxxxxx x Xxxxx xxxxxxxxx, a
b) xxxxxxxx xxxxxxxxx xxxxxx, xxx xxxxx by xxxxxxxxxxx distribuce xxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxx xxxxxxxx přípravků do xxxxxxxxx xxxxx k xxxxxxx xxxxxxxx pokrytí xxxxxxxxxx xxxxxx pacientů x Xxxxx republice.
(3) Xxxxxxxxxxxx zdravotnictví může xxxxx k xxxxxxxxx xxxxxxxxxxx xxxxxxxxx léčivých xxxxxxxxx xxxxxxxx xxxxxx xxxxxx, xxxxxx xxxxx xxxx xxxxxx xxxxxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx xx xxxxxxxx přípravků xx xxxxxxxxx. Xxx xxxxxx takového opatření xxxxxx povahy xxxx xxx xxxxxxx xxxx xxxxxxxx:
x) xxx x xxxxxx xxxxxxxxx, xxxxx xx uveden na Xxxxxxx,
x) xxxxxxxxxx xx xxxxxxxxx xx mohlo xxxxx x xxxx, xx objem xxxxxxxxxxx xxxxxxxx xxxxxxxxx, xxxxx xxxx xxxxxxxxxxxx xxxxx xxxxxxx xxxxxxxxxx odpovídajících xxxxxxxxx xxxxxxxxxx, xxxx xxxxxxxx xxxxxxxxx, xxxxx xxxx xxxxxxxx xxxxxxxxxxxx xxxxxxxx ke xxxx xxxxxxxx vlastnostem, xx xxxx v Xxxxx xxxxxxxxx xxxxxxxxx dostatečně xxxxxxxx xxxxxxx pacientů x Xxxxx xxxxxxxxx, x
x) veřejný xxxxx xx xxxxxxx zdraví xxxxxxxxxxxx x xx xxxxxxxxx dostupnosti léčivých xxxxxxxxx xxx aktuální xxxxxxx pacientů x Xxxxx xxxxxxxxx xxxxxxxxx xxx xxxxxxxxxxxxx zájmem xx xxxxxxxxxxx xxxxxx xxxxxxxxxx do zahraničí.
(4) Xxxxxxxxxxxx zdravotnictví xxxxxxxxxx xxxxx xxxxxxxx xxxxxx xxxxxx, xxxxxxx-xx xxxxxx xxxx xxxxxx.
(5) Xxx xxxxxxxx xxxxxxxx obecné xxxxxx podle xxxxxxxx 3 xx xxxxxxxxx xxxxx §77x odst. 3 s xxx, xx xxxxxxxx obecné xxxxxx xxxxxx xxxxxxxxx xxxx x něm xxxxxxxx.
(6) Xxxxx Ústav xxxxxx, xx xxx xxxxxxxxxxxxx xxxxxx xxx xxxxx trvání xxxxxxxx xxxxxx xxxxxx ohledně xxxxxxx xxxxxxxxxx xx xxxxxxxxx x xxxxxxxxxxx xxxxxxxx přípravku xxxx xxxxxxxx přípravků, xxxx x xxx Xxxxx xxxxxxxxxxx xxxxxxxxx Xxxxxxxxxxxx xxxxxxxxxxxxx xxxxxxxx x xxxxxxxx, xxxxx xxx x tomuto xxxxxx xxxxx.
(7) Xxxxxxxxxxxx xxxxxxxxxxxxx, xxxxx xx x xxxxxx činnosti xxxxx x xxxxxx xxxxxxxxxx xxxxxxxx přípravků, xxxxxx Xxxxx x poskytnutí xxxxx x xxxxxxx xxxxx §77c.“.
35. V §80 xx xx xxxxx xxxxxxxx 1 xxxxxxxx xxxx „Předepisující xxxxx xx povinen xxxxxx xxxxxxxxxx xxxxxxxxxxxxx xxxx, xx xxxxx základě xxx uplatnit elektronický xxxxxx v jakémkoliv xxxxx xxxxxx xxxxxxxxxxxx xxxxxxxx xxxxxxxxx.“.
36. X §82 xxxx. 3 xxxx. x) xx xx xxxxx „x xxxxxxxx xxxxxxxx xxxxxxxxxxx“ vkládají xxxxx „, a xx xxxxxxxxxxxx“, a xxxxx „xxxxxx xxxxx x xxxxxx xxxxxx xxxxxxxxxxx xxxxxx xxxxxxx xxxxxxxx Ústav xx xxxx xxxxxxxxxxx prostředku“ xx xxxxxxxxx slovy „xxxxxxxxxxx údaje xxxxxxxx xxxxxxxxxxxx xxxxxxxxxxxxx xxxxxxxxxxx x výdeji, xxxxxxxxxxxx xxxxxxxxxxxxxxx xxxxxx, xxxxxxxxxxxx xxxxxxxx, xxxxxxx byl xxxxxxxxx xxxxx, x xxxxxxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx; strukturu xxxxx, xxxxxx, xxxxx x xxxxxx xxxxxxxx jejich xxxxxxxxxxx prostřednictvím xxxxxxxxxxxxxx xxxxxxx xxxxxxx xxxxxxxxx xxxxxx xxxxxxx“.
37. V §82 xxxx. 4 xx xxxx xxxxx se xxxxx „xxxxx xxxxxxxx xxxx“ x „xxxxxxxxxxx xxxxxxx xxxx“ xxxxxxx.
38. X §82 xxxx. 4 xx xxxx xxxxx xx xxxxx „výjimečně“ xxxxxxx x xx xxxxx „xx xxxx lékárny“ xx xxxxxxxx xxxxx „xxxxx xxxxxxxxx, a xx“.
39. X §101 xxxx. 1 zní:
„(1) Xxx kontrole xxxxx xxxxxx xxxxxx xxxxxxxxx xxxxxx vykonávající xxxxxx xxxxxx uvedené x §10 x inspektoři xxxxx xxxxxxxxxxx xxxx. Xxxxxxxx ke kontrole xx xxxxx průkazu xxxxxxxxxx. Inspektor se xxx výkonu xxxxxxxxx xxxxxxxx xxxxx xxxxxx xxxxxx x xxxxxx xxxxxxxx předpisů xxxxxxxxx xxxxxxxx xxxxxxxxxx.“.
40. V §101 xxxx. 5 xxxxxxx x) xxx:
„x) x xxxxxxxxxxxx xxxxxxxxx, xxxxxxx x případě klamavého xxxxxxxx xxxxxxxx xxxxxxxxx xxxx v xxxxxxx xxxxxxxxx podezření, že x xxxxxxx xxxxxxxxxx xxxxxxx xxxxx, xxxxx x xxxxxx xxxxxxxx xxxx xxxxx xxxxxx xxxxxx xxxxxxxxx, xxxxxxx xxxx xxxxxxx xxxxxxxxx; x tímto xxxxxxxx xxxxxxx inspektor kontrolovanou xxxxx a xxxxx xx úřední xxxxxx x xxxxxxxx zajištění x xxxxxxxx jeho xxxxxx, xxxxxx x xxxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx; xxxxx xxxxxx xxxxxx xx xxxxxxxx xxxxxxxxx o xxxxxxxx; xxxxxxxxxxxx xxxxx xx xxxxxxx xxxxxxxxx léčivý xxxxxxxxx xxxxxxxxxxxx vydat; x xxxxxxx, xx xxxxxxxxxxxx xxxxx xxxxxx xxxxxxxxxxx léčivého přípravku xxxxxxx, xxxxxxx inspektor xxxx xxxxxx; x xxxxxx, xxxxxxxx xxxxxx xxxxxxxx xxxxxxxxx xxxxxx xxxxxxxxx xxxxxx záznam, xxxxx je přílohou xxxxxxxxx x xxxxxxxx; xxxxxxx-xx xxxxx xxxxxxxxx xxxxxxxxx xxxx xxxxxxx-xx xx, xx xxxxxxxxx xxxxxx xxxxxxxxx xxxxxxx xxxxxxxxx xxxxxx zákona, xxxxx Ústav xxxx Xxxxxxxxxxx ústav kontrolované xxxxx xxxxxxxxx xxxxxx xxxxxxxxx x neporušeném xxxxx; xxxxxxx se xxxx xxxxxxxxx, xxxxxxx-xx xx, že v xxxx zacházení x xxxxxxx xxxxxxxxxx k xxxxxxxx zacházení s xxx xxxxxx xxxxx xxxxxxxxx xxxx xxxxxxx-xx xx, že xxxxxxxxx xxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxx xxxxxx; x xxxxxxx xxxxxxx xxxx Ústav xxxx Xxxxxxxxxxx xxxxx rozhodnutí x xxxxxxxxxx xxxx xxxxxxx xxxxxxxx přípravku; xxxxxx xxxxxxxxx, xx xxxxxxx zachází xxxxx, xxxxx x xxxxxxxx xxxxxxxxx xxxx oprávněna xxxxx tohoto xxxxxx, xx xxxxxxxx xx xxxxxx přípravky, xxxxx xxxxxxxxx xxxxxxxxx xxxxxx xxxxxx; xxxxxxxxxx nebo xxxxxxx xxxxxx xxxxxxxxx xx Ústav nebo Xxxxxxxxxxx ústav povinen xxxxxxxxx xxxxx §88; xx xxxx xxxxxx xxxxxxxx x x xxxxxxx vydání xxxxxxxxxx x xxxxxxxxxx xxxx xxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxxxxx xxxxx xx xxxxxxxxx, xxxxxxxxxx xxxx xxxxxxx léčivé xxxxxxxxx xxxxxxx; v xxxxxxx xxxxxx xxxxxxxxxx x xxxxxxxxxx nebo xxxxxxx xxxxxxxx přípravku xx xxxxxxxxxxxx xxxxx xxxxxxx xxxxxxx xxxxxxx xxxxxxxxxx Xxxxxxx xxxx Xxxxxxxxxxxx xxxxxxx xxxxxxx x uskladněním xxxxxxxxxxx xxxxxxxx xxxxxxxxx x xxxxxxxxxxx xxxxxxxxxxxx xxxx xxxxxxxxx léčivých přípravků, x jejichž xxxx xxxxxxxx Xxxxx xxxx Xxxxxxxxxxx xxxxx.“.
41. X §101 xxxx. 5 závěrečné xxxxx xxxxxxxxxx se xxxxx „x) xx x)“ nahrazují xxxxx „ a) xx x)“.
42. X §103 xxxx. 6 xxxx. x) xx xx xxxxx „xx xxxxx“ xxxxxx xxxxx „, xxxx“.
43. X §105 xxxx. 2 xx xx xxxxx xxxxxxx x) xxxxx „xxxx“ xxxxxxx.
44. X §105 xx konci xxxxxxxx 2 xx tečka xxxxxxxxx čárkou x xxxxxxxx xx xxxxxxx x) xx x), xxxxx znějí:
„r) nezajistí xxxxxxx xxxxxxxx xxxxxxxxx xxxxx §77 odst. 1 xxxx. x),
x) x xxxxxxx s §77 xxxx. 1 xxxx. x) xxxxxxx xxxxxxxxxx xxxxxxxx přípravku xx xxxxxxxxx, xxxx
x) x xxxxxxx x xxxxxxxxx obecné povahy Xxxxxxxxxxxx xxxxxxxxxxxxx xxxxxxx xxxxx §77x xxxxxxxxxxx xxxxxx xxxxxxxxx xx xxxxxxxxx.“.
45. V §105 xxxx. 5 xx xx xxxxxxx x) xxxxxx xxxx písmeno x), xxxxx zní:
„d) xxxxxxxxxx údaje x xxxxxx dodávek léčivého xxxxxxxxx uvedeného xx xxx x Xxxxx xxxxxxxxx xxxxx §33 xxxx. 2 xxxx xxxxxxxx,“.
Xxxxxxxxx xxxxxxx x) xx x) se xxxxxxxx xxxx x) xx x).
46. V §105 xxxxxxxx 6 zní:
„(6) Xxxxxxxxx se xxxxxxx xxxxxxxxx xxxxxxx tím, xx x xxxxxxx x nařízením o xxxxxxxxx xxxxxxxxx
x) provede xxxxxxxx xxxxxxxxx xxx xxxxxxxx xxxx x xxxxxxx x xxxxxxxxxx xxxxxxxxx v xxxxxxxx,
x) xxxxxxx xxxxxxxxx xxxxx xxxxxxxxxx xxxxxxxxx xxx xxxxxxxx nebo x xxxxxxx x xxxxxxxxxx xxxxxxxxx x xxxxxxxx,
x) xxxxxxx klinické xxxxxxxxx x naléhavé situaci x xxxxxxx x xxxxxxxxxx xxxxxxxxxxx xxx xxxxxxxxx xxxxxxxxxx xxxxxxxxx x xxxxxxxxxx xxxxxxxxx,
x) xxxxxxxx
1. údaje x xxxxxxxx, dočasném xxxxxxxxx, xxxxxxxxx zahájení, xxxxxxxxxx xxxxxxxx xxxx xxxxxxxx xxxxxxxxxx xxxxxxxxx,
2. xxxxx xxxxxxxx xxxxxxx xxxxxxxx xxxxxxxxx x Xxxxx xxxxxxxxx xxxx
3. xxxxxxxx xxxxxx xxxxxxxx hodnocení x České xxxxxxxxx,
x) xxxxxxx xxxxxxx výsledků xxxxxxxxxx xxxxxxxxx,
x) nevede xxxxx a úplně xxxxxxxxxxxxxxxxx záznamy,
g) xxxxxxxxx xxxxxxx xxxxxxxxx xx xxxxxxx xxxxxxxxxxx nežádoucí xxxxxx nebo x xxxx xxxxxxxxxxx xxxxxxxxxx xxxxx neprovede neodkladné xxxxxxxxxxxx xxxxxxxx xxxxxxx xx xxxxxxx xxxxxxxx xxxxxxxxx, nezajistí xxxxxxxxxxxxxxx xxxxxx xxxx xxxxxxxxx xxxxx údajů xxxxxxxx xxxxxxxxx xxxxx xxxxxxxxx xxxxxxxxx xxxxxxxxxx hodnocení x xxxxxxx x xxxxxxxxxx x xx xxxxxxxx xxxxxxx xxxxxxxx xxxxx,
x) xxxxxxxxx, xxx xxxxxxxxxx x ostatní xxxxx xxxxxxxx do xxxxxxxxx klinického xxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxx x xxxxxxxxx xxxxxxxxx, xxxxx podmínky xxxxxxxxx x §54,
x) xxxxxxxx xxxxxxx xxxxxxxx xxxxxxxx x xxxxxxxxx xxxxxxxxx, xxxxx klinické xxxxx xxxx xxxxxxxx xxxxxxxxx xxxx xxxxxxxxxxx x xxxxxx skutečnostech, xxxxx xxxxxxxx xxxxxxxxxx xxxxxxxxxxxx xxxxxxxx přijaté xx xxxxxxx xxxxxxxx xxxxxxxxx,
x) xxxxxxxxxx zkoušejícímu xxxxxx informací xxx xxxxxxxxxxxx nebo xxxxx xxxxxx xxxxxxxxxxxxx,
x) xxxxxxxxxxxxx, xxxxxxxxxx nebo xxxxxxxxxx xxxxxxxxx o xxxxxxxxx xxxxxxxxx nebo xxxxxx xxxx xxxxxxxxxxx základní xxxxxxxx xxxxxxxxxx xxxxxxxxx x xxxxxxx s xxxxxxxxxx xxxxxxxxxxx xxxxxxxxx x klinickém xxxxxxxxx, xxxx
x) xxxx nekomerční xxxxxxxxx xxxx x xxxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxx.
XXXXX: 32014R0536
47. X §105 xx xxxxxx xxxx xxxxxxxx 7, který xxx:
„(7) Xxxxxxxxx xx xxxx xxxxxxx xxxxxxxxx xxxxxxx xxx, xx
x) x xxxxxxx x §58 xxxx. 2 xxxxx xx xxxxx xxxx xxxxxxxxx klinického xxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxxxx xxx, xxxxxxxx xxxxxxxxxxxx a xxxxxxxxxxxx xx xxxx vzniklou xxx provádění klinického xxxxxxxxx xxxx nezaplatil xxxxxxxx,
x) xxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx x rozporu x §60 xxxx. 3,
x) nezajistí xxxxxxxxx xxxxxxxxxx xxxxxxxxx podle §61 xxxx. 2 xxxx. x),
x) nesplní xxxxxxxxxx xxxxxxxxx xxxxx §61 xxxx. 2 xxxx. x), xxxx
x) xxxxxxxxxx xxxxxxxxxxxx léčivé xxxxxxxxx xxxx xxxxxxxx xxxxxx xxxxxx xxxxx §61 odst. 2 xxxx. x).“.
Xxxxxxxxx odstavce 7 x 8 xx xxxxxxxx xxxx xxxxxxxx 8 x 9.
XXXXX: 32014R0536
48. X §106 xxxxxxxx 3 xxx:
„(3) Xxxxxxxxxxx fyzická osoba xx xxxxxxx xxxxxxxxx xxxxxxx xxx, že x xxxxxxx s xxxxxxxxx x klinickém xxxxxxxxx
x) xxxx xxxxxxxxxx, xx-xx x xxxxx xxxxxxxxxx xxxxxxxxx xxxxx xxxxx xxxxxxxxxx, xxxx xxxx xxxxxx xxxxxxxxxx, xx-xx x xxxxx xxxxxxxxxx xxxxxxxxx více xxxxxxxxxxxx,
1. xxxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxx x xxxxx xxxxxxxxxx hodnocení,
2. xxxxxxx xxxxxxx ostatním xxxxxx xxxx xxxxxxxxxxxx xxxxxx,
3. zahájí klinické xxxxxxxxx bez udělení xxxxxxxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx xxxx xxxx xxxxxxxxx xxxxxxxx x xxxxxxxx xxxx případů, xxx xxxxx xxxxxxx xxxx vyžadován, nebo xxxxxxxxx xxxxxxx x xxxxxx xxxxxxxxx xxxxx, xxxx-xx pro xxxx xxxxxxxx xxxxxxxxx xxxxxxxxxx,
4. xxxxxx klinické xxxxxxxxx xxx xxxxxxx xxxxxxxxxxx xxxxx subjektu hodnocení xxxx xxxx xxxxxxxxx xxxxxxxx,
x) xxxx xxxxxxxxxx xxxxxxxxxxx, xxxxxxxxxxxxxx xxxx xxxxxxxx xxxxxxxxx xxxxxxx xxxx laboratorní xxxxxxxx,
x) xxxxxxxxx uchovávání zdrojových xxx x xxxxxxxxxxx xxxxxxxxxx xxxxxxxxx,
x) nepřijme xxx xxxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxx opatření x xxxxxxx xxxxxxxx xxxxxxxxx,
x) xxxxxxx xxxxxxxx xxxxxxxxx jako xxxxxxxxxx, xxxx xxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxx x xxxxxxxxx xxxxxxxxx xxxxx xxxxxxxx xxxxxxxxx x §54, nebo
f) xxxxxxxxxx xxxxxx správné xxxxxxxx xxxxx xxx xxxxxxxxx xxxxxxxxxx xxxxxxxxx.“.
XXXXX: 32014R0536
49. X §107 xxxx. 1 xxxx. x) xxx:
„x) 100 000 Xx, jde-li x xxxxxxx xxxxxx xxxxx §105 xxxx. 6 písm. x) xxxx 2 xxxx 3, §105 xxxx. 6 xxxx. j), §106 odst. 3 xxxx. x) xxxx x) nebo §106 xxxx. 5 xxxx. x),“.
50. X §107 xxxx. 1 xxxx. x) xx xxxxx „§106 odst. 3 xxxx. x) nebo x)“ xxxxxxxxx slovy „§106 xxxx. 3 xxxx. x)“.
51. V §107 xxxx. 1 xxxx. x) xx xxxxx „x), x), x), x) xxxx x)“ xxxxxxxxx xxxxx „h), x), x), x) xxxx y)“.
52. V §107 xxxx. 1 xxxx. x) xx xxxxx „§105 odst. 6 xxxx. c), x), x), x) xx x)“ xxxxxxxxx slovy „§105 odst. 6 xxxx. c) xxxx x) xxxx 1, §105 xxxx. 6 xxxx. x), f), x), h), x), x),“.
53. X §107 xxxx. 1 xx xx xxxxx xxxxx xxxxxxx c) doplňují xxxxx „nebo §106 xxxx. 3 písm. x), x) xxxx x)“.
54. X §107 xxxx. 1 xxxx. x) se slova „x), x), x), x), x), r), x), x), u), x)“ nahrazují slovy „x), x), x), x), r), x), x), x), v), x)“.
55. X §107 xxxx. 1 xxxx. x) xx slova „x), e), x) xxxx x)“ nahrazují xxxxx „x), b) xxxx x)“.
56. X §107 xxxx. 1 xxxx. x) xx za xxxxx „§104 odst. 7 xxxx. b) xxxx x),“ vkládají xxxxx „§105 xxxx. 2 xxxx. x) xx x),“.
57. V §107 xxxx. 1 xxxx. x) xx xxxxx „x), x), f), x), n) nebo x)“ nahrazují xxxxx „ x), x), x), x), x) xxxx q)“.
58. V §107 xxxx. 2 se xx xxxxx „xxxxx“ xxxxxxxx xxxxx „§105 xxxx. 2 xxxx. x) a“.
59. X §108 xxxxxxxx 5 xxx:
„(5) Xxxxxxx xxxxx se xxxxxxx xxxxxxxxx tím, xx v rozporu x nařízením o xxxxxxxxx xxxxxxxxx
x) xxxx xxxxxxxxxx nebo xxxxxx xxxxxxxxxx
1. xxxxxxxxx xxxxxxxxx xxxxxxxxxx hodnocení x xxxxx klinického xxxxxxxxx,
2. xxxxxxx xxxxxxx xxxxxxxx xxxxxx týmu xxxxxxxxxxxx xxxxxx,
3. xxxxxx xxxxxxxx xxxxxxxxx xxx xxxxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx nebo xxxx xxxxxxxxx zástupce x xxxxxxxx xxxx xxxxxxx, xxx tento xxxxxxx xxxx xxxxxxxxx, nebo xxxxxxxxx svolení x xxxxxx xxxxxxxxx osoby, xxxx-xx pro xxxx xxxxxxxx xxxxxxxxx vyžadováno,
4. xxxxxx xxxxxxxx hodnocení xxx xxxxxxx kontaktních xxxxx subjektu xxxxxxxxx xxxx jeho zákonnému xxxxxxxx,
x) xxxx xxxxxxxxxx xxxxxxxxxxx, xxxxxxxxxxxxxx xxxx xxxxxxxx xxxxxxxxx příhodu xxxx xxxxxxxxxxx xxxxxxxx,
x) xxxxxxxxx xxxxxxxxxx xxxxxxxxxx xxx a dokumentace xxxxxxxxxx xxxxxxxxx,
x) xxx xxxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxx okamžitá xxxxxxxx x xxxxxxx xxxxxxxx xxxxxxxxx,
x) provádí klinické xxxxxxxxx jako xxxxxxxxxx, xxxx xxxxxxx podmínky xxxxxxxxx xxxxxxxxx x xxxxxxxxx xxxxxxxxx xxxxx xxxxxxxx stanovené x §54, xxxx
x) xxx xxxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxx xxxxxxx xxxxxxxx xxxxx.“.
XXXXX: 32014R0536
60. X §108 xx xx xxxxxxxx 7 vkládá nový xxxxxxxx 8, xxxxx xxx:
„(8) Fyzická osoba xx xxxx člen xxxxxx xxxxxx Státního xxxxxx pro xxxxxxxx xxxxx dopustí xxxxxxxxx xxx, xx x xxxxxxx s §53x xxxx. 5 xxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxxxx.“.
Xxxxxxxxx xxxxxxxx 8 x 9 xx xxxxxxxx xxxx xxxxxxxx 9 x 10.“.
61. X §108 xxxx. 8 xxxx. x) se xxxxx „x)“ xxxxxxxxx slovem „x)“.
62. X §108 xxxx. 8 písm. x) xx xxxxx „x) xxxx x)“ xxxxxxxxx xxxxx „x) xxxx c)“.
63. X §108 xxxx. 8 xx xx xxxxx textu xxxxxxx x) xxxxxxxx xxxxx „nebo xxxxxxxx 5 xxxx. x), x) xxxx f)“.
64. V §108 xxxx. 8 xxxx. x) xx slova „xxxx xxxxxxxx 5 xxxx. x)“ zrušují.
65. X §108 xx xxxxxxxx xxxxxxxx 11, který xxx:
„(11) Xx xxxxxxxxx xxxxx xxxxxxxx 8 xx xxxxx xxxxx činnosti.“
66. Xx §108 xx xxxxxxxx xxxx §108x a 108b, xxxxx včetně nadpisů xxxxx:
„108x
Xxxxxxxxxx léčivého přípravku
(1) Xxxxxxxxxx léčivého xxxxxxxxx xxx uložit, xxxxxxxx xxxxxx xxxxxxxxx náleží xxxxxxxxx xxxxxxxxx xxxxxxx, x
x) xxx ke xxxxxxxx xxxxxxxxx xxxxxxx xxxx xxxx xxxxx, xxxx
x) xxx x xxxxxxxxxxx xx xxxxxxxxx xxxxxxxxx xxxxxxx získán.
(2) Xxxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx xx xxxxx xxxx.
108x
Xxxxxxx xxxxxxxx přípravku
(1) Xxxxxx-xx uloženo xxxxxxxxxx xxxxxxxx xxxxxxxxx, xxxxxxxxx x §108x xxxx. 1 písm. x) xxxx b), lze xxxxxxxxxx x xxxx xxxxxxx, jestliže
a) náleží xxxxxxxxx xxxxxxxxx deliktu, xxxxxxx xxxxx xx xxxxxxx xxxxxx xxxxxx,
x) xxxxxxxx pachateli xxxxxxxxx xxxxxxx nebo mu xxxxxxxx xxxxx, nebo
c) xxxxxxxx xxxx znám.
(2) Xxxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx xx stává xxxx.“.
67. V §112 xx xx xxxxxxxx 5 xxxxxx nový xxxxxxxx 6, který xxx:
„(6) Xxxxxxxx-xx xxx xxxxx, xxxxxxx Ústav x xxxxxxxxxx účtu xxxxxxxx podle xxxxxxxx 5 xx příjmový xxxx xxxxxxxx rozpočtu Xxxxx republiky zřízený xxx Xxxxxxxxxxxx zdravotnictví xxxxxx xx výši xxxxxxxxx xxxxxx.
Xxxxxxxxx odstavce 6 x 7 xx xxxxxxxx jako 7 x 8.“.
68. V §114 xxxx. 1 xx xx xxxxx „§24 xxxx. 2, 3, 4, 8 x 9,“ xxxxxxxx xxxxx „§33 xxxx. 2,“, xx xxxxx „§67 xxxx. 10 x 11,“ xx xxxxxxxx xxxxx „§77 xxxx. 1 xxxx. x) x x),“ a xx xxxxx textu xxxxxxxx 1 se xxxxxxxx xxxxx „a §82 odst. 3 xxxx. x)“.
69. X §114 xxxx. 2 xx xxxxx „§51 xxxx. 2 písm. x), §52 xxxx. 6, §53 xxxx. 1, 8, 12 x 13, §54 odst. 1, §55 xxxx. 7 až 9, §56 xxxx. 1 xxxx. x), §56 xxxx. 3 x 7, §57 odst. 2, §58 xxxx. 8, §59 xxxx. 1“ xxxxxxxxx xxxxx „§53x xxxx. 2, §54 xxxx. 4, §56 odst. 6“.
70. X §114 xxxx. 2 xx xxxxx „§60 xxxx. 2, 4, 5 x 9, §61 xxxx. 2 xxxx. x) a b) xxxx 1 a 6, §61 xxxx. 2 xxxx. c), §61 xxxx. 4 xxxx. x),“ xxxxxxx.
71. X §114 xxxx. 2 se xx xxxxx „§77 xxxx. 1 písm. x),“ xxxxxx xxxxx „x),“.
72. X §114 xxxx. 4 se xx xxxxx „§48 xxxx. 2, 3 x 6“ xxxxxxxx xxxxx „, §60 xxxx. 2, 4, 5 a 9, §61 xxxx. 2 xxxx. x) x x) xxxx 1 x 6, §61 xxxx. 2 xxxx. x), §61 odst. 4 písm. e)“.
Xx. II
Přechodná xxxxxxxxxx
1. Pokud byla xxxxxx x povolení xxxxxxxxxx hodnocení předložena Xxxxxxxx xxxxxx xxx xxxxxxxx xxxxx xxxxx xxxx, xxxxxx xxxxxx 6 měsíců xxx xxx xxxxxxxxxx xxxxxxxx Xxxxxx x Úředním xxxxxxxx Evropské xxxx xxxxx čl. 82 xxxx. 3 xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Xxxx (XX) x. 536/2014 xx xxx 16. xxxxx 2014 o xxxxxxxxxx hodnoceních xxxxxxxxx xxxxxxxx xxxxxxxxx x x zrušení xxxxxxxx 2001/20/XX, xxxxxxx xxxxxxxx xxxxxxxxx se xxxxxx xxxx xxxxxxxxxxx xxxxxxxx xxxxxxxx, x xx xx xxx, kterým xxxxxxxx 42 xxxxxx xxx xxx zveřejnění xxxxxx xxxxxxxx.
2. Xxxxx byla xxxxxx x povolení xxxxxxxxxx xxxxxxxxx xxxxxxxxxx Xxxxxxxx xxxxxx pro xxxxxxxx xxxxx xx xxx, kterým xxxxxxxx 6 xxxxxx ode xxx xxxxxxxxxx xxxxxxxx Xxxxxx xxxxx čl. 82 xxxx. 3 xxxxxxxx Xxxxxxxxxx xxxxxxxxxx a Xxxx (EU) x. 536/2014 ze xxx 16. dubna 2014 x klinických xxxxxxxxxxx xxxxxxxxx léčivých xxxxxxxxx x x xxxxxxx xxxxxxxx 2001/20/ES xxxxxxxxxx xxxx xx dne, xxxxxx xxxxxxxx 18 xxxxxx xxx xxx xxxxxxxxxx xxxxxx xxxxxxxx, xxx xxxxxxx řízení x povolení xxxxxxxxxx xxxxxxxxx xxxxxxx xxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxx x xxxxxxx xxxxxxxx xxxxxxxxx se xxxxxx xxxx dosavadními právními xxxxxxxx, x xx xx dne, xxxxxx xxxxxxxx 42 xxxxxx xxx xxx zveřejnění xxxxxx xxxxxxxx.
XXXX XXXXX
Xxxxx zákona x xxxxxx xxxxxx
Xx. XXX
X §2 xxxxxx č. 234/2014 Xx., x xxxxxx xxxxxx, ve znění xxxxxx č. 131/2015 Xx., xxxxxx x. …/2016 Xx. x xxxxxx x. …/2016 Xx., se xx xxxxx odstavce 1 xxxxx xxxxxxxxx xxxxxx x doplňuje xx xxxxxxx n), xxxxx xxx:
„x) xxxxx Etické xxxxxx Státního ústavu xxx kontrolu xxxxx.“.
ČÁST TŘETÍ
Závěrečná ustanovení
Xx. XX
Xxxxxxxxx xxxxxxx
Xxxxx xxxxx xxx oznámen x xxxxxxx se xxxxxxxx Evropského parlamentu x Xxxx (EU) 2015/1535 xx xxx 9. září 2015 x xxxxxxx při xxxxxxxxxxx xxxxxxxxx v xxxxxxx xxxxxxxxxxx předpisů x xxxxxxxx pro xxxxxx informační xxxxxxxxxxx, x platném xxxxx.
Xx. V
Účinnost
Tento xxxxx xxxxxx účinnosti prvním xxxx kalendářního měsíce xxxxxxxxxxxxx po xxx xxxx xxxxxxxxx, s xxxxxxxx ustanovení
a) xx. X bodu 21, xxxxx jde x §51, §52 x §53 xxxx. 2, xx. X xxxx 22, pokud xxx x §53a xxxx. 7, §53x xxxx. 1, 2, 3 x §53x xxxx. 1 až 8, x čl. I xxxx 23, xxxxx xxxxxxxx účinnosti xxxxxxxxx 6 xxxxxx xxx xxx xxxxxxxxxx xxxxxxxx Xxxxxx x Úředním xxxxxxxx Xxxxxxxx xxxx xxxxx čl. 82 xxxx. 3 nařízení Xxxxxxxxxx xxxxxxxxxx x Xxxx (XX) č. 536/2014 xx xxx 16. xxxxx 2014 x xxxxxxxxxx xxxxxxxxxxx humánních xxxxxxxx xxxxxxxxx a x xxxxxxx xxxxxxxx 2001/20/XX; xxx, xxx xxxx xxxx oznámení xxxxxxxxxx, xxxxxx Ministerstvo xxxxxxxxxxxxx xxxxxx sdělení xx Sbírce zákonů;
b) xx. X bodu 21, xxxxx jde x §53 odst. 1, 3 a 4, x xx. X bodu 22, xxxxx xxx o §53x xxxx. 1 xx 6, §53b xxxx. 4, 5 x §53c odst. 9, xxxxx xxxxxxxx xxxxxxxxx xxxxxx dnem xxxxxxxxxxxx xxxxxx xxxxxxxxxxxxx xx xxx xxxxxxxxxx xxxxxxxx Xxxxxx v Xxxxxxx xxxxxxxx Xxxxxxxx xxxx podle čl. 82 xxxx. 3 xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Xxxx (XX) x. 536/2014 xx dne 16. dubna 2014 x xxxxxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx x x zrušení xxxxxxxx 2001/20/XX; xxx, xxx bylo toto xxxxxxxx zveřejněno, xxxxxx Xxxxxxxxxxxx xxxxxxxxxxxxx xxxxxx xxxxxxx xx Sbírce xxxxxx;
x) xx. X xxxx 5, 7, 9, 28, 29 x30, které nabývají xxxxxxxxx xxxxxx xxxx xxxxxxxx kalendářního xxxxxx xxxxxxxxxxxxx xx jeho xxxxxxxxx.
SHRNUTÍ ZÁVĚREČNÉ ZPRÁVY XXX
|
Xxxxx xxxxxx xxxxxx: Xxxxx xxxxxx, xxxxxx xx mění xxxxx č. 378/2007 Sb., o xxxxxxxx x x změnách xxxxxxxxx souvisejících zákonů (xxxxx x léčivech), xx xxxxx pozdějších xxxxxxxx |
|
|
Xxxxxxxxxxx / zástupce xxxxxxxxxxxxx: Xxxxxxxxxxxx xxxxxxxxxxxxx |
Xxxxxxxxxxxxx xxxxxx xxxxxx účinnosti: 28.5.2016 |
|
Xxxxxxxxxxxx xxxxx XX: XXX (xxxxxxxx, tj. x xxxxx adaptace xxxxxxxx Xxxxxxxxxx parlamentu x Xxxx (EU) č. 536/2014 ze xxx 16. dubna 2014 x xxxxxxxxxx hodnoceních xxxxxxxxx léčivých xxxxxxxxx x x zrušení xxxxxxxx 2001/20/XX) |
|
|
- xxxxxx xxxxxx stanovený xxx xxxxxxxxxxxx: 28.5.2016 - uveďte, xxx jde xxxxx xxx xxxxx xxxxxxxxx xxxxxxxxxxx xxxxxxxxx XX?: XX |
|
|
2. Xxx xxxxxx xxxxxx |
|
|
Xxxxxxx xxxxx xxxxxx xxxxxx je xxxxxxxx xxxxxxxx nařízení Xxxxxxxxxx xxxxxxxxxx a Xxxx (XX) č. 536/2014 ze xxx 16. xxxxx 2014 x xxxxxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx x o xxxxxxx směrnice 2001/20/XX x xxxxxxxxxx Xxxxx xxxxxxxxx xxxxxxxxxxxxxxx xxxxxx xxxxxx x xxxxxxxx. Xxxxx xxxxxxxx otázky, xxxxx xxxx nařízením x. 536/2014 xxxxxxxxx xxxxx přikázány xxxxxxx xxxx xx xxxxxxx xxxx zmocněn xx xxxxxxx. Xxxxx xx xxxxxxxxx toho, xxx xxxxxx úprava v Xxxxx republice xxxxxx xxxxxxxxx režim xxxxxxxxx xxxxxxxxxx hodnocení xxxxxxxxx xxxxxxxx xxxxxxxxx založený xxx celou Xxxxxxxxx xxxx xxxxxxxxx č. 536/2014. |
|
|
Xxxxxx xxxxxxx cílem návrhu xxxxxx je xxxxx xxxxxx akutní nedostupnosti xxxxxxxx xxxxxxxxx pro xxxxxxx pacientů v Xxxxx republice xx xxxxxx ochrany xxxxxx xxxxxx x zdraví, x xx vytvořením xxxxxxx sledování a xxxxxxxxxxxxx xxxxxx nedostupnosti xxxxxxxx přípravků xxx xxxxxxx pacientů x Xxxxx republice x xxxxxxxxx příslušných xxxxxxxx xxxxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxx pro xxxxxxx xxxxxxxx x Xxxxx republice do xxxxxxxxx (xxxxxxxx) v xxxx xxxxxxxxx, xxx xxxxxxxxxxx takové hrozby xxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxxx. Záměrem xx xxxxxx xx xxxxxxx xxxxxxx xxxxxxxxxxxxxx subjekty x xxxxxxxxxxx zásadu xxxxxxx xxxxxx xxxxx xxxxxxxxxx x předpisech Xxxxxxxx xxxx. |
|
|
Xxxx další xxxx návrhu xxxxxx xxxxx xxxxxxxx xxxxxxxx xxxxxxxx Xxxxxx x xxxxxxxxx pravomoci (XX) č. 1252/2014 xx xxx 28. xxxxxx 2014 xxxxxxxxxx směrnici Xxxxxxxxxx xxxxxxxxxx a Rady 2001/83/XX, xxxxx xxx x xxxxxx x xxxxxx správné xxxxxxx xxxxx pro xxxxxx xxxxx pro xxxxxxx xxxxxx přípravky, dále xxxxxxxx zákonné xxxxxxxxxxx xxx xxxxxxxxxxxx spolupráci Xxxxxxxx xxxxxx xxx xxxxxxxx léčiv x Xxxxxxxxxx xxxxxxxxxxxx cel xx xxxxxx xxxxxxxxxxxx xxxxxxx xxxxx a xxxxxxxxx nakládání s xxxx, xxxxxxxx upravit xxxxxxxxxxx xxxxxxxxxx xxx xxxxxxxxx xxxxxxxx x xxxx xxxxxxxx zásadní xxxxxx xxxxxxxxx xxxxxxxxx x xxxxxxx xxxxxxxx xxxxxxxxx xxx, aby xxxx xxxxxxxxxx x xxx takové xxxxxxx, xxx je xxxxxxxx, xx x xxxx xxxxxxxxx xxxxx, xxxxx x tomu xxxxxx xxxxx zákona xxxxxxxxx. |
|
|
3. Xxxxxxxxxx dopady xxxxxx xxxxxx |
|
|
3.1 Xxxxxx xx xxxxxx xxxxxxxx x xxxxxxx veřejné xxxxxxxx: XXX |
|
|
Xxxxxx na xxxxxx xxxxxxxx Xxxxxxxx nařízení ke xxxxxxxxxx xxxxxxxxx Xxxxxxxx xxxxx xxxxxxxxxx xxxxxx xx xxxxxx xxxxxxxx adaptaci xxxxxxxx x klinických xxxxxxxxxxx humánních xxxxxxxx xxxxxxxxx bude představován xxxxxxxxx xxxxxx xxxxxxxx xxxxxxxxxx úvazků xx xxxxxx Xxxxxxxx xxxxxx xxx kontrolu léčiv xxx potřeby xxxxxxxxx xxxxxx xxxxx x xxxxxxxxx spojených s xxxxxxxxx (v počtu 32 úvazků). Xxxxxxxxx xxxxx xxxxxxxxxx xxxx xxxxx xxxxxxxxxx další xxxxxx xxxxxxxxxxxxxxx posuzovatelů (5), posuzovatelů preklinického xxxxxxxxx (2), posuzovatelů xxxxxxxxxxxxxx xxx klinických xxxxxxxxx (1) inspektorů (5), xxxxxxxxxxxx xxxxxxxxxx xxxxxxxxx (3), x xxxxxxxxxx xxxxxxxxx xxxxxxxxx-xxxxxxxxxxxxx xxxxxx xxx xxxxxxx xxxxxx - při xxxxx 8 xxxxxx xxxxxx xxxxxx - 16 úvazků). Xxxx xxxxxx xxxxx částečně xxxxx x xxxxxxx xxxxxx xx klinická xxxxxxxxx (xxxxxx xxxxxx). Xxx xxxxxxxx krytí xxxxxxxxxxx technického xxxxxxxxxxx xxxxxx xxxxxxx etické xxxxxx jako xxxxxxxxx xxxxxx Xxxxxxxx xxxxxx xxx xxxxxxxx xxxxx xxxx uvažovány x xxxxx xxxxxxxx prostředky x xxxxxx xxxxxxxxxxxx x XX xxxxx, x xxxxx bude xxxxx x xxxxxx xxxxxx xx klinická xxxxxxxxx xx xxxxxxxxxxx xxxxxxx xxxxxxxx xxxxx. |
|
|
Xx xxxxxx Xxxxxxxxxxxx zdravotnictví xxxxxxx xxxx agenda xxxxxxxxxx xxxxxxxx xxxxx xxxxxxxxxx xxxxxxxxxx x xxxxxxx x xxxxxxxx xxxxxxxxxx xxxxxxxxx. Bude xxxxx xxxxxxxxxx xxxxx xxxxxx xxxxxxxx xxxxxxxxx x xxxxx xxxxxx xxxxxxxxx xxxxxxxxx. |
|
|
Xxxxxxx xxxxxxxxx |
|
|
Xxxxxxxx xxxxx xxxxxxxxxx xxxxxx xxxxxx xx xxxxxx xxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx xx xxxxxx xxxxxxxx bude xxxxxxxxxxxx xxxxxxxxx krytím xxxxxxxx xxxxxxxxxx xxxxxx xx xxxxxx Xxxxxxxxxxxx zdravotnictví (2 úvazky - 1 xxxxxx xxxxxxxx x 1 odborný xxxxxxxx pro xxxxxx xxxxxxxx xxxxxxxx zamezujících xxxxxxxxxx). Na xxxxxx Xxxxxxxx xxxxxx xxx xxxxxxxx xxxxx dojde x xxxxxxxx o 2 pracovní xxxxxx xx xxxxxx zajištění xxxxxxxxx x vyhodnocování xxxxxx xxxxxxxxxxxxx léčivých xxxxxxxxx xxx potřeby xxxxxxxx v České xxxxxxxxx x předávání xxxxxxxxxxx podnětů Ministerstvu. |
|
|
Ostatní xxxxxxxxxxx xxxx |
|
|
Xxxxx xxxxxxxxx xxxxxxxxxxxx novelizačních xxxx xxxxx xxxxxxxxx xxxxxxxxxxxx. Xxxxx xx x xxxxx xxxxxx xxxxxxxxxxxxx xxxxxxxxx xxxxxx xxxxxx (xxxx. xx xx xxxx xxxxxxxxxxx inspektorů). |
|
|
Konkrétní xxxxx xx ostatní xxxxxxx rozpočty, zejména xx xxxxxxxxxx xxxxxxxxx xxxxxxxxxxx xxxxxxxxx nelze xxxxxx xxxxxxxxx, xxxxx xxx xxxxxxxxxxxx, že xxxxx xxxxx xxxx xxxxx pozitivní. |
|
|
Přínosy |
|
|
Adaptace xxxxxxxx xx xxxxxxxxxx hodnocení |
|
|
Kvalitní xxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxx klinických hodnocení xxxxxxxx k atraktivitě Xxxxx republiky pro xxxxxxxxx xxxxxx xxxxxxxxx. Xxxxxx xxxxxxxxx xx xxx dostanou nejmodernější xxxxxx xxxxxxxxx v xxxxxxxxxxx xxxxxxx xxxxxx xx zajištěním příslušných xxxxxxxxxxxxxx xxxxx. Xxxxxxxxx xxxxxxxxxx xxxxxxxxx xx xxxxx Xxxxx republiky xxxxx xxxxxxx České xxxxxxxxx ve xxxxx. Xxxxxxxxx dopady xxx xxxxxxxxxxxx x xx xxxxx xxxxxxxxxx. |
|
|
Xxxxxxx xxxxxxxxx |
|
|
Xxxxxx xxxxxx xxxxxxxxxxx xxxxxxxxxxxxx xxxxx o hrozící xxxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxx xxxxxxxxx xxxxxxxxxx xxxxx x xxxx xxxxxxxxx, kdy xx distribuce xxxxxxxx xxxxxxxxx xxxxxxxxxxx xxxxxxxxxxxx xxx léčbu xxxxxxxxxx xxxxxxxx přípravků. Xxxxxxxx xxx xxxx xxxxxxxxx xxxxxxxx xxxx xxxxx x xxxxxxxxx xxxxxxxx xxxxxx. Xxxxxxxxxx xxxxxx xxxxxx xxxxxxxx xx xxxxxxxxxxx xxxxxxxxxxx xxxxxxxxx xxxx, xx xxxxxx xxxx xxxxxxxxx členské xxxxx, co xx xxxx xxxxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx. Xxxxxxxxx xxxxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxx xxxxxxxxxxx xxxxxxxxxx xx xxxxxx xxxx xxxxxxxxxxx xxxxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx. |
|
|
Xxxxxxx xxxxxxxxxxx body |
|
|
Přínosy xxxxxxxxx navrhovaných xxxxxxxxxxxxx xxxx xxx xxxxxxxxxxxx x xxxxxxx xx xx, xx se xxxxx x xxxxx xxxxx, xxxxx zpřesňují xxxxxxxxx právní xxxxxx (xxxx. xx se xxxx xxxxxxxxxxx xxxxxxxxxx). |
|
|
3.2 Xxxxxx xx xxxxxxxxxxxxx xxxxxxxx: XXX Xxxxxxxx xxxxxxxx xx xxxxxxxxxx xxxxxxxxx |
|
|
Xxxxxxxxxxxxxxx xx xxxxxxxx xxxxxxxxx xxxxxx xx xxxxxxxxxxxxx xxxxxxxxx x oblasti xxxxxxxxxx xxxxxxxxx. Xxxxxx xxxxxxxxxx hodnocení xxxx xxx xxxxxxxx xxxx xxxxxxxxxxxxx (podávání xxxxxxx xxxxxxxxxxxxxxx jednotného evropského xxxxxxx) x dochází xx xxxxxx xxxxxxx xxxxxxxxx. Dopadem xxx xxxx xxxxxxx podnikatelských xxxxxxxx xxxxxxxx xx x xxxxxx xxxxxxxxxx xxxxxxxx, které xxxx x převážné xxxxx xxxxxx xxx x xxxxxxxx. Xxxxxxx xxxxxx xx nové agendy xx xxxx xxx xxxxx xxxxxxxx xxxxxxxx xxxxxxx výdajů za xxxxxxxxxx xxxxxxxxxx xxxxxxxxx, xxxxx xxxxxxx xxxxxx xxxx kryta jednou xxxxxxx xxxxxxxxxx xxx xxxxxxxxx Státním xxxxxxx xxx xxxxxxxx xxxxx, xxx xxxxxxx xxxxxx (xxxx etickými xxxxxxxx). |
|
|
Xxxxxxx xxxxxxxxx |
|
|
Xxxxxxxxxxxxx xx dopady xx podnikatelské prostředí xx xxxxx xxxxxxxx xxxxxxxxxx xxxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxx xxxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx určených xx xxxx Xxxxx xxxxxxxxx xx xxxxxxxxx x xxxx x xxxxxxx xxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxx xxxxx spočívající x xxxxxxx xxxxxxxxxx. Xxxxxx xxxxxxxxxx xxxxxx xxxxxx xx xxxxxxxxxxxx xxxxxxxx xxxxxxxxx jsou však xxxxxxxxxxxxxx xxxxxxxxx xxxxxxxxxxx x xxxxxxxxxxxxxxx xxxxxxx. |
|
|
Xxxxxx xxxxx xxxxxxxxxx právní xxxxxx xxxxxxxx zamezujících xxxxxxxxxx reexportům bude xxx xx držitele xxxxxxxxxx xxxxxxxx xxxxxxxxx. Xxxxx dopad bude xxxxxxxxx a xxxxxxx x xxxxxxxx xxxxxxxxxx xxxxxxxxxxxx xxxxxxxxxxx xxxxx x xxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxx xx Xxxxx xxxxxxxxx. V xxxxxxxx době xx xxxxxxxx xxxxxxxxx zákonem xxxxxxx, xxxxx poskytování xxxxx nemá v xxxxxx úpravě xxxxxx xxxxxxxxx xxxxxx xxxxx. X xxxxxxxx důsledku xxxx xxx právní xxxxxx xxxxxxx reexportů x nezbytných xxxxxxxxx xxxxxxxxx dopad na xxxxxxxx xxxxxxxxxx x xxxxxxxxxx. Xxxxxxxx xxxxxxxxxx x xxxxxxxxxx umísťují xxxxxx přípravky k xxxxxxx xx xxxxxxxxxx xxxx zemí XX. X xxxxxxxxxxxx zemích XX jsou xxxxxx xxxxx xxxxxxxxx maximální xxxx xxxxxxxx xxxxxxxxx, xx xxxxx xx xxxxx xxxxxxxx xx xxx xxxxxx. Xxxxxxxx xxxxxx xxx prodeji xxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxx více xx trzích x xxxxx xxxxxxx xxxxxxxx. Xxxxx xxxxxx xxxxxxxxx, xx držitelé by xxxxxxxx xxxxx na xxxx s xxxxxxxx xxxxxxx xxxxxxxx, tato xxxxxxx xx pro xx xxxx xxxxxxxxxxxxx. Xxxxxxxxx xxxxxxxxxx xxxxxxx xx xxxxxx, xx xxxxxxx xx xxxxxxxxxxxxx, x cenové xxxxxxx, xxx tato xx xx xxxx držitelů x xxxxxxxxxx ze xxxx xxxxxx: 1. Xxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx může xxxx xx snížení xxxxxxxx xxxxxxxx xxxxxxxxx, který xxxxx xxxxxxx xxx x xx vyšší xxxx; 2. pokud xx xxxxxxxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxx vlastní xxxxxx xxxxxxxxx x xxxx xxxx xx xxxxx cenu xxxx xxxx xxxxxx xxxxxx x xxxxxxx xxxxxxx xxxx takového xxxxxxxx xxxxxxxxx na xxxxx xxxx xxxx xxxxx. Xxxxxx xx cenová xxxxxx samozřejmě xxxxxxx, xxxxxxx paralelní obchod xx xxxx xxxxxxxx xx xxxxxxxx xxxxxxxx xxxxxxxxx. |
|
|
Xxxxxxx xxxxxxxxxxx xxxx |
|
|
X xxxxxxx na xx, xx se xxxxxxx x xxxxxxxx xxxxx, xxxxx xx xxxxxxxxxxxx. |
|
|
3.3 Xxxxxx xx xxxxxx xxxxxxxxxxx xxxxx (obce, xxxxx): XX |
|
|
Xxxxxxxxxxxxxxx xx xxxxx xxxxxx xx xxxxxx xxxxxxxxxxx celky. |
|
|
3.4 Xxxxxxxx dopady: XX |
|
|
3.5 Xxxxxx xx životní xxxxxxxxx: NE |
|
|
Nepředpokládají se xxxxx xxxxxx na xxxxxxx xxxxxxxxx. |
|
101) Xxxxxxxx Xxxxxx x xxxxxxxxx xxxxxxxxx (EU) č. 1252/2014.“.
104) Xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Rady (XX) č. 536/2014.“.
102) Xxxxx č. 227/2006 Sb., x xxxxxxx na xxxxxxxx xxxxxxxxxxxxx xxxxxxxxx xxxxxxx x xxxxxxxxxxxxx xxxxxxxxxx x x xxxxx xxxxxxxxx souvisejících xxxxxx, ve xxxxx xxxxxxxxxx xxxxxxxx.
103) Xxxxxxxxx xxxxxxxx zákoník, xxxxxxx xxxxxxx, xxxxx č. 101/2000 Sb., xx znění xxxxxxxxxx xxxxxxxx.
Čl. 75 xxxxxxxx Xxxxxxxxxx xxxxxxxxxx a Rady (XX) x. 536/2014.“.
XXXXXXXX ZPRÁVA
XXXXXX ČÁST
A. Xxxxxxxxx xxxxxx x xxxxxxxxx xxxxxx regulace (XXX)
1. Xxxxx předložení a xxxx
1.1. Xxxxx
Xxxxx xxxxxx, xxxxxx xx xxxx xxxxx č. 378/2007 Sb., x xxxxxxxx x o xxxxxxx xxxxxxxxx xxxxxxxxxxxxx xxxxxx (xxxxx o xxxxxxxx), xx xxxxx xxxxxx č. 124/2008 Xx., zákona x. 296/2008 Sb., xxxxxx x. 141/2009Xx., xxxxxx x. 281/2009 Xx., xxxxxx x. 291/2009 Xx., zákona x. 75/2011 Xx., xxxxxx x. 375/2011 Xx., xxxxxx č. 50/2013 Xx. x xxxxxx x. 70/2013 Xx.
1.2. Xxxxxxxx xxxxxxxx
X xxxxxxxx xxxx xx xxxxxxxxxxxx xxxxxxxxx xxxxxxx, účinnosti x xxxxxxxxxxx xxxxxxxxx x veterinárních xxxxxxxx xxxxxxxxx upravena xxxxxxx x xxxxxxxx x xxxx xxxxxxxxxxx předpisy. Xxxxxx xxxxxxxx xxxxxxxx xxxx do xxxxxxxx xxxx Xxxxx republiky xxxxxxxxxxxxx ustanovení xxxxx xxxxxxxxxxxx xxxxxxxx předpisů x xxxxxxx xxxxxxxxx x veterinárních xxxxx, xxxxx xxxx přijata x Xxxxxxxx xxxx xxxx xxxxxxx tohoto xxxxxx.
Xxxxx x léčivech xxx již xxxxxx xxxxxxxxxxxx xxxxxxxxxxx, xxxxxxx xx xx xxxxxx xxxxxx xxxxxxxxxx xxxxxxx č. 70/2013 Sb. nešlo o xxxxxx xxxxxxxxxx, které xx zásadním xxxxxxxx xx obsahu zákona xxxxxxx a xxxxxxx xxx xxxxxx; xxx x úpravy xxxxxxxx xxxxx, tudíž xxxxxxxxx xxxxx zákona dosud xxxxxxx x xxxxxxxx xxxxx.
Xxxxxxxxxxx xxxxx xxxxxx xxxxxx xxxxxxx xxxxxxxx x xxxx, xxx Xxxxx xxxxxxxxx xxxx x xxxxxx plnohodnotným xxxxxxxxxx regulačního systému Xxxxxxxx xxxx v xxxxxxx léčiv, x xx xxxxxxxxx x xxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx. Xxxx by xxx xxxxx xxxxx xxxxxx xxxxxxx přispět k xxxxxxx xxxxxx x xxxxxxxxxx xxxxxx systému x x tomu, xxx xxxxxxx kapacita xxxxxxxxxxxx a xxxxxxxxxxx xxxxxxxxx xxxxxxxxx vývoj xxxxxx xxxxxxxx a xxxxxxxxxxx xx účelem xxxxxxxxxxx xxxxxxxxx záruk x xxxxxxx ochrany xxxxxxxxx xxxxxx x xxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx xx xxxxxx x xxxxxxxxxx xxxxxxx xxxxxxxxxx v xxxxx xxxxxxxxxx hodnocení.
1.2.1. Xxxxxxxx xxxxxxxx x klinických xxxxxxxxxxx xxxxxxxxx léčivých xxxxxxxxx
Xxx 16. xxxxx 2014 xxxx přijato xxxxxxxx Xxxxxxxxxx parlamentu x Xxxx (XX) č. 536/2014 x xxxxxxxxxx xxxxxxxxxxx humánních xxxxxxxx xxxxxxxxx x x xxxxxxx xxxxxxxx 2001/20/XX. Xxxxx článku 99 xx xxxx xxxxxxxx xxxxxxx nejdříve šest xxxxxx xx xxxxxxxxxx xxxxxxxx xxxxx čl. 82 xxxx. 3, xx. xxxxxxxx Xxxxxx, xx byly splněny xxxxxxxx xxxxxxxxxxx x xxx, xx xxxxxx XX x xxxxxxxx XX dosáhly plné xxxxxxxxxx x systémy xxxxxxx xxxxxxxxx xxxxxxx xxxxxxxxx. X xxxxxxxxxx xx. 99 xxxxxxxx xx xxxx xxxxxxxxx, xx x xxxxxx xxxxxxx se xxxx xxxxxxxx xxxxxxxxx dříve xxx 28. xxxxxx 2016. Xxxxx xxx xxxxxxx nařízení xx xxxx xxxxxxxxx variabilně x xxxxxxxxxx xx xxx, xxx xxxxx x xxxxxxxx Xxxxxx. X každém xxxxxxx xx xxxx xxxx xxxxxxxx použije xxxxxxxx xxx 28. xxxxxx 2016. X xxxxxxx xx xxxxx stanovenou xxxxx x xxxxxxxx xxxx v xxxxxxxxxxx xxxxxx xxxxxx zákona x xxxxxxxx nově xxxxxxxx xxxxxxxxxxx týkající xx xxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxx přípravků, xxxxx xx x xxxxxxx x xxxxxxxxx xxxxx xxxxxxxxx.
Xxxxxxx nařízení Xxxxxxxxxx parlamentu x Xxxx (XX) č. 536/2014 xxxx xxxxxxxxxx xxx, xx, xxx praxe xxxxxxx, xxxxxxxxxxxxxxx xxxxxxxx x regulaci xxxxxxxxxx xxxxxxxxx, x xxxxx xxxxxxxxx xxxxxxxx 2001/20/ES, xxxx x xxxxxxxxx xxxxxxx xxxxxxxx xxxxx xxxxxxxx, když xx xxxxxxx členské xxxxx xxxxxxx náležitou právní xxxxxx x tomu, xxx xxxx xxxxxxxx xxxx potřebným způsobem x xxxxxx xxxxxxxx xxxxxx xxxxxxxxxxxxx, a xxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxx xxxxxxxxxx za xxxxxxxxx xxxxxxxx 2001/20/ES.
Xxxxxxx vývoj xxxxxx xxxxxxxx, že xxxxxxxx xxxxxxxxx xx x xxxxxxxxxxx xxxxx xxxxxxxxx xx specifičtější xxxxxxx xxxxxxxx, xxxx xxxx xxxxxxxxxx identifikované xxxxxxxxxxxxxxx xxxxxxxxxxx xxxxxxxxx. Xxx bylo možné xx xxxxxx xxxxxxxxxx xxxxxxxxx zahrnout dostatečný xxxxx xxxxxxxx, xxxx xxxxxx xx místě xxxxxxx xxxx členských xxxxx xxxx xxxxxxx xxxxxxx. Xxxx nové xxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxxxxxx xx xxxx xxxxxxxxxx zapojení xx xxxxx největšího počtu xxxxxxxxx xxxxx. Xxxxx xx xx v xxxxx xxxxxxxxxxxx xxxxxxx xxxxxxxxxxx dokumentace k xxxxxxx x xxxxxxxx xxxxxxxxxx xxxxxxxxx xxxx xxxxxxx vícenásobnému předkládání xxxxxxxx xxxxxxxxxxx informací, xxxxx xx mělo xxx xxxxxxxxx předložením xxxxx dokumentace x xxxxxxx pro xxxxxxx xxxxxxx členské státy xxxxxxxxxxxxxxx jednotného portálu xxx předkládání. Vzhledem x tomu, že xxxxxxxx hodnocení prováděná x xxxxxxx xxxxxxxx xxxxx xxxx x xxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxxxx xxxxxx význam, xxxx xx xx xxxxxxxxxxx x xxxxxxx xxxxxxxx xx xxxxxxxxxx xxxxxxxxx xxxxxxxxxx xxxx xxxxxxxxxxxxxxx xxxxxx xxxxxxxxxx xxxxxxx.
Xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Xxxx (XX) č. 536/2014 vycházelo rovněž x toho, xx xxxxxxx poznatky xxxxxxx, xx xxxxxx xxxxx xxxxxxxx by xxxx xxx xxxxxxxxxx a xxxxxxxxxx xxxxxxx například xxx klinických xxxxxxxxxxx, xxxxx xx xxxxxxxxx xx více než x xxxxxx xxxxxxxx xxxxx, xxxxxxx xx xx xxxxx xxxxxx xxxxx x xxxx xxxxxxxxxx při xxxxxxxx xxxxxxxxx klinického xxxxxxxxx, xxx xxxx při xxxxxxxx zpráv x xxxxxxxxxxx a při xxxxxxxxxx xx xxxxxxx xxxxxxxxxxx xxxxxxxx přípravků. Xxxxxxx xxxxx xxxxxxxx xx xx výhodu, xx rozdíly x xxxxxxxx xxxx xxxxxxxxxxxx xxxxxxxxx xxxxx xx xxxxx xxxxx na xxxxxxx x měla xx vést x x xxxxxxxxxxxx spolupráci xxxxxxxxx xxxxx xxx xxxxxxxxxx žádostí x xxxxxxxx klinického xxxxxxxxx. Xxxx spolupráce xx xxxxxx xxxxxxxxx xxx xx xxxxxxx, které xxxx xx xxx xxxxxxxx xxxxxxxxxxxx xxxxxx, xxxx xx xxxxxxxxx xxxxxxx x xxxxxxxxx xxxxxxxx xxxxxx. Xxxxxx xxxxxxxx xxxxxxxxx xx xxx xxx pružný x xxxxxxxxx, aby xxxxxxxxxxx x xxxxxxxxxxxxxxxx xxxxxxxxx xxx xxxxxxxx xxxxxxxxxx hodnocení, avšak xxxx nesmí xxxxxxx xxxxxxxxxx xxxxxxxx nebo xxxxxxx zdraví.
Ze všech xxxxxx důvodů xxxx xxxxx Xxxxxxxx xxxxxxxxx x Xxxx x xxxx, že xxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxx přípravků xxxxx xxxxxxxxxxx xxxxxxxxx XX x xxxx xxxx xx xxxxxxxxxxxxxx x na členské xxxxx xxxxx xxxxxx xxx xxxxxxxxx xxxxxxxxxx xxxxxxx otázek, při xxxxxxx řešení xx xx místě zohlednit xxxxxxx xxxxxxxxx.
Xxxxxxx xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Xxxx (XX) č. 536/2014 xx v Xxxxx xxxxxxxxx xxxxx xxxxxxxxxx x xxxxx tedy xxx xxxxxxx xxxxx, xxxx xxxxx xxxx xxxxx v xxxxxxx xxxx České republiky xxxxxxxx, xxxxxxxxxxxx xx xxxxx xxxxxxxxxx. Xxxxxxxxxxx xxxxx xxxxxx zákona x xxxxxxxx x xxxxxxxxxx na xxxxx xxxxxxxx Xxxxxxxxxx parlamentu x Rady (XX) č. 536/2014 se xxxxxxxx xx xxxxxx xxx xxxx vztahů, xxxxxxx xxxxxx xxxxxxxxx xxxx xxxxxxxx xx členských xxxxxxx. Jde xxxxxxxxx x xxxxxxxxxxx okruhy xxxxxx.
Xx xxxxxxxx státě xx x prvé xxxx xxxxxxxxx, xxx xxxxxxxx xxxxxxxxx xxxxx xxxx xxxxxx, které xx budou na xxxxxxxxx xxxxxxx o xxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxx, x xxx xxxxxxxx xxxxxxxx xxxxxxxx xxxxxx xx lhůtách xxxxxxxxxxx v nařízení xxx xxxxxxxxxx klinických xxxxxxxxx. Xxxx xxxxxxxxxx xxxx xxx xxxxxxxxxxx xxxxxxx xxxxxxxxxx xxxxxxx xxxxxxxxx xxxxx. Při xxxxxxxxxxx xxxxxxxx xxxxxx xxxx xxxxxx xx xxxxxxx xxxx zajistit xxxxxxxx xxxxxxxx xxxx, x to xxxxxxx xxxxxxxx xxxx xxxxxxxxxx xxxxxxxx. Posouzení by xxxxxx xxxx xxx xxxxxxxxx xxxxxxxx přiměřeným xxxxxx osob, které xxxx nezbytnou kvalifikaci x zkušenosti x xxxxxxxxx xxxxxxxxx x xxxxxxxxxxxxxxx posouzení, xxxxxxx xxxxx xxxxxxxxxx xxxxxx xx xxxx xxx xxxxxxxxx xx xxxxxxxxxx, xxxxx xxxxxxxxxx xxxxxxxxx x xxxxxxxxx xxxxxxxxxxxx x xxxxxx xx xxxxxx být xxxxxxxxx xxxxxx xxxxx nepatřičným xxxxxx. X rámci xxxxxxx členského státu xxxx xxxxxxxxx xxxxxxx xxxxxx xxxxxxxxxxx xx xxxxxxxxxx xxxxxxxxxx xxxxxxxxx. Xxx xxxx xxxxx xxxxxxxxx x xxxxxx xxxxxxxxxx mezi xxxxxxxxx xxxxx, xxx xx xxxxx členský xxxx xxxxx xxxxx xxxxxxxxx xxxxx.
Xxxxxx xxxxxxx, jehož xxxxxx je ponechána xx xxxxxxxx xxxxx, xxxx xxxxxxxxxxx jazykové. Xxxxxxx stát by xxx xxxxx jazykové xxxxxxxxx xx dokumentaci xxxxxxxxxx hodnocení. Xxx xx xxxxxxxxx xxxxxxxxxxxxx xxxxxxxxx xxxxxxx posuzování xxxxxxx x xxxxxxxx xxxxxxxxxx xxxxxxxxx, xxx xx členský stát xxxxxx, že xxxx xxxxx xxx xxxxxxxxxxx, xxxxx xxxx xxxxxx xxxxxxxx hodnocení, xxxx xxxxxxxxx xxxxxxxxxxxx jazyk x oblasti xxxxxxxxx.
Xxxxxxxxx xxxxx xx ponechávají x xxxxxx xxxxxx xxxx xxxxxxxx xxxxxxxx xx xxxxxx zákonně xxxxxxxxxxxx xxxxxxxx nezpůsobilých x xxxxxxxxxxx xxxx, xxxxx se x xxxxxxxxxxxx xxxxxxxxx xxxxxxx xxxx.
Xxxxxx xxxxxx pro xxxxxxx svobodné x xxxxx xxxxxxxxxxx xxxxxxxxxx xxxxx xxxxxxxxx xx xxxxxxxxxx hodnocení xx xxxxxxxxxxx předchozího xxxxxxxx x xxxxxxxxxxxx subjektem xxxxxxxxx. Xxxxx pohovor xx měl xxx xxxxxxxx xxxxxx zkušebního xxxx xxxxxxx xxxxxxxxxx xxx tento xxxx xxxxx vnitrostátních právních xxxxxxxx x členském xxxxx, v xxxx xxxxx xxxxxxx.
Xxxx xx xxxxxxxxx členskému státu xxxxxxx, aby xx xxxxxxx, xx xxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxx xxxxxxx xxxxxxxxxxx zástupcem xxxx vyžadovat, xxx xxxxxxxxx osoba, xxx xx schopna utvořit xx xxxxx a xxxxxxxx xxxxxxxxx xx xxxxxxxxxx, xxxx sama xxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxx ke své xxxxxx xx xxxxxxxxx xxxxxxxxx.
Xxxxxxx xxxx má xxxxxx xxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxx xxxx takovým xxxxxx, xxxxx xxxx x xxxxxxx xxxxxxxxxxxx xxxx xxxxxxxx závislosti. Xxx x xxxxx vykonávající xxxxxxxx xxxxxxxxx xxxxxx, xxxxx zbavené xxxxxxx, xxxxx, které xx x xxxxxxxx soudního xxxxxxxxxx xxxxxxx účastnit xxxxxxxxxx hodnocení, a xxxxx, které xxxx xxxxxxxx xx xxxxx xxxx, xxxxxxxxxxx xxxxxxxxx xxxx xxxxxxxxxxx stavu xxxxxxxx xx xxxx, x xxxxx xx xxxxxxxxx v zařízeních xxxxxxx xxxx.
Xxxxxxxxx xxxxx xx xxxx ponechává xxxxxx xxxxxxxx xxxxxx, xxx x xxxxxxx xxxxxxxxxx hodnocení xxxxxx xxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx xx xxxxxx xxxxxxxxxxxxxx či trestněprávní xxxxxxxxxxxx zadavatele xxxx xxxxxxxxxxxx. Xxxxxxxx xxx xxxxxxxxxxx x xxxxxx xxxxxxxxx, včetně xxxxxx xxxxxxxx xxxxxxxxxxx x xxxxxx xxxxx, se x nadále xxxx xxxxx vnitrostátními předpisy. Xxxxxxx xxxx xx xxx dále zajistit xxxxxxxx xxxxxxx náhrady xxxxx vzniklé xxxxxxxx xxxxxxxxx, xxxxx xxxxx xxxxxxxxx povaze x xxxxxxx xxxxxx, xxxxxxx xxxxx je, aby xxx xxxxxxxxxx hodnoceních xxxx xxxxxxxxx náhrada xxxxx xxxxxxx xxxxxxxxx x souladu s xxxxxxxxxxx xxxxxxxxxxxxxx xxxxxxxx xxxxxxxx.
Xxxxxxxxx xxxx xx x nadále xxxxxxx xxxx x xxx, xx xx xx xxxxxxx pravomoc odvolat xxxxxxxx klinického xxxxxxxxx, xxxxxxxxxx xxxxxxxx hodnocení xxxx vyžádat x xxxxxxxxxx xxxxx xxxxxxxxxx xxxxxxxxx. Xxxxxxx xxxx xx zajistit xxxxxx xxx xxxxxxxx xxxxxxxxxx xxxxxxxxx. Aby byl xxxxxxxx soulad x xxxxxxxxx, xxxxxxx xxxx xx xxxx oprávnění x xxxxxxxxx xxxxxxxx xxxxxxxx a x xxxx xx xxx xxx xxxxxxxxxxxx inspekční xxxxxxxx. Za xxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxxxx x xxxxxxxx xx xxxxxxxx xxxxxx xxxxxxxx xxxxxxx xxxxxxxx, jejichž xxxxxxxxx xx xxxxxxxx x xxxxxx 86 x 87 xxxxxxxx (xxxxxxxxxxxxx xxxxxxxxx xxxx xxxxxx, xxxxxx xxxx xxx xxxxxxxxx na xxxxxxx xxxxxx xxxxxx xxxxxxx, xxxx být xxxxx jedna platba xx xxxxxxxxx).
Xxxx xx xxxxxxxx xxxxxx xxxxxxxx xxxxxxxx opatření xx xxxxxxx klinických xxxxxxxxx xxxxxxxxxxx nekomerčními zadavateli, xxxxxxx xx xxx xxxxx xxxxxx x xxxxxxxx xxxxxx xxxxxxxxxxxxx xxxxxxxxxxx xxxxxx xxxxxxx xxxx xxxxxxxx státem xxxx xxxxxxx xxxxxxxxxxxx xxxxxx, veřejná xxxxxx xxxxx a xxxxxxx xxxxxxxx xxxxxxxxx, x xxxxx xxxxxxxxxxx xxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxx xxxxxxxxxxxx xxxxxxxxxx x xxxxx podpory xxxxxx xxxxxxx, xxxx xx xxxxxxxxx k ohrožení xxxxxxx xxxxxxxxxx xxxxxxxxx. Xxxx vychází x xxxxxxxx zkušeností, které xxxxxxxxxx x xxx, xx velká část xxxxxxxxxx xxxxxxxxx xx xxxxxxxxx xxxxxxxxxxxx xxxxxxxxxx, xxxxx často xxxxxxxxx xx xxxxxxxx prostředky, xxxxx xxxxxxxxx, a xx zčásti nebo xxxxx, z veřejných xxxxxxxxxx xxxx x xxxxxxxxxxxx xxxxxx.
X xxxxxxxxxx xx obsah xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Xxxx č. 536/2014 xxxxxxxxxxx xxxxx xxxxxx xxxxxx x xxxxxxxx sleduje xxxxxxxxx xxxxxx xxx, xxxxx xxxxxxx x xxxxxxxx xxxx, xxx xxxxxx xxxxxx x Xxxxx xxxxxxxxx xxxxxx xxxxxxxxx xxxxx provádění xxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxx xxx xxxxx Evropskou xxxx xxxxxxxxx Xxxxxxxxxx xxxxxxxxxx a Rady č. 536/2014. Xxxxx se xxxxx xxxxxxxxxxx xx xxxxxx veškerých xxxxxxxxxxx, xxxxxxx úprava je xxxxxxxxx xxxxx xxxxxxx, xxx xxxxxx xxxxxxxx x nařízení a x xxxxxx xxxxxxxx xxxxxxxxxxx náležitý právní xxxxxx pro xxxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxx.
Xxxx xxxxx identifikovány xxxxxxxxxxx xxxxxxxx:
Xxxxx xxxxxxxxx, xxxxxxx xxxxxxx xxxx, xxxx xxxxxxxx následující oblasti:
- xxxxxxxx xxxxxxxxx xxxxx xxxx xxxxxx, xxxxx xx xxxxx na xxxxxxxxx xxxxxxx x xxxxxxxx klinického xxxxxxxxx xxxxxxx, xxxxxxxx xxxxxxxxx xxxxxxx komisí xxx xxxxxxxx xxxxxxxx nařízení x osobách xxxxxxxxxxxx xxxxxx, xxx. xxxxxxxx xxxxxxxxxxx xxxxxx xxxxxx xx xxxxxxxxxx, zkoušejících x xxxxx xxxxxxxxxx xxxxxxxxx, x zajistit xxxxxxxxxx xxxxxxxx komisí xx xxxxxxx xxxxxxxxxxx x xxxxxxxx pro xxxxxxxxxx xxxxxxxxxx hodnocení;
- xxxxxx xxxxxxxxx a xxxxxxxx xxxxxxx xxxxxxx xxxxxxxx xxxxx xxxxxxxxx xxxxxxxxx xxxxxxxxx v xxxxxxxxxxx s xxxxxx xxxxxx xx xxxxxx xx území xxxxxx xxxxxxxxx xxxxx;
- xxxxxxxxxxx xxxxxxxx;
- xxxxxxx s xxxxxxxxxxxx xxxxxxxxx xxxxxxxxx xx měl xxx xxxxxxxx xxxxxx xxxxxxxxxx xxxx xxxxxxx xxxxxxxxxx xxx xxxxx xxxx xxxxx xxxxxxxxxxxxxx právních xxxxxxxx x xxxxxxxx xxxxx, x němž xxxxx xxxxxxx;
- xxxxxxxxxx, xxx kromě xxxxxxxxxxxxx xxxxxxxx xxxxxx zákonně xxxxxxxxxxx xxxxxxxxx xxxx xxxxxxxxxx, aby xxxxxxxxx xxxxx, jež xx xxxxxxx xxxxxxx xx xxxxx a xxxxxxxx xxxxxxxxx xx poskytnuté, xxxx xxxx svolila xxxxxxxx písemného xxxxxxxx xx své xxxxxx xx xxxxxxxxx xxxxxxxxx;
- xxxxxxxxxx, xxx xxxxx xxxxxxxxx doplňková xxxxxxxx xxxxxxxx xxxx xxxxxxx xxxxxx, které xxxx x situaci xxxxxxxxxxxx xxxx xxxxxxxx závislosti;
- xxxxxxxx xxx xxxxxxxxxxx x případech xxxxx xxxxxxxxx xxxxxxxx hodnocení xxxxxx otázky xxxxxxxx xxxxxxxxxxx x xxxxxx xxxxx, xx x xxxxxx xxxx xxxxx xxxxxxxxxxxxxx xxxxxxxx;
- xxxxxxxxx xxxxx xx xxxxxxx xxxxxxxx xxxxxxx povolení xxxxxxxxxx xxxxxxxxx, xxxxxxxxxx xxxxxxxx hodnocení nebo xxxxxxx x xxxxxxxxxx xxxxx xxxxxxxxxx xxxxxxxxx; xxxxxxx xxxx xx xxxxxxxx xxxxxx nad xxxxxxxx klinického hodnocení; xxx xxx xxxxxxxx xxxxxx x nařízením, xxxxxxx xxxx má xxxx xxxxxxxxx x xxxxxxxxx provádět xxxxxxxx x k tomu xx xxx mít xxxxxxxxxxxx xxxxxxxxx kapacity; xx xxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxxxx v xxxxxxxx xx členským xxxxxx xxxxxxxx vybírat xxxxxxxx;
- rozhodnout x xxxxxxx xxxxxxxx na xxxxxxx xxxxxxxxxx hodnocení xxxxxxxxxxx xxxxxxxxxxxx xxxxxxxxxx x xxxxx xxxxxxxxxxx xxxxxxx hodnotného xxxxxxxxx xxxxxx xxxxxxxxxxxx xxxxxxxxxx x další xxxxxxx xxxxxx xxxxxxx.
X xxxxxxxx xxxxxx xxxxxx byly xxxxxxxxxxxxxx xxxxxxx xxxxxxxxxxx xxxxxxxx:
X současné xxxx xx právní úprava xxxxxxxxxx hodnocení x xxxxxx o léčivech x xxxxxxxxx vyhlášce xxxxxxxx x xxxxxxxxxx xx směrnici XX xx xxxxxxxxx xxxxxxxxxx. Xxx xxxx popsáno xxxx, stávající xxxxxx xxxxxxxxxxx xxxx xxx XX dostatečná a x xxxx důvodu xxxx přikročeno k xxxxxxx nařízení. Xxxxx xxxxxxxxxxxx xxxxxx xxxxxx, xxxxx by xxxx xxxxxxxx adaptovala, x xxxx xxx xxxxx x tohoto xxxxxxxx xxxxxxxxxxxxx problémy.
1.2.2. Xxxxxxxx xxxxxxxxx x xxxxxxx xxxxxxxxx léčivých přípravků
Dle xxxxxxxx xxxxxxxx stavu xxxxx xxx léčivé xxxxxxxxx xx xxxxxxx xxxxxxxxxxx podmínek distribuovány xxxxxxxxxxxx xxxx území Xxxxx republiky. Xxxxxxxxxx xxxxxxxx přípravků xxx xxxxxx xxxxxxxxxxxx xxxxx xx xxxxxxxxx xxxxx Xxxxxxxx unie, xxx xxx do xxx. xxxxxxx xxxx. X xxxxxxx xxxxxxxxxx léčivých xxxxxxxxx xx třetích xxxx xx xxxxxxxxx xxxxxxx xxxxxxxx xxxxxxxxx xxxxxx Evropské unie. Xxxxxxxxxxxx xx xxxxxxxxx xxx lze xxxxx xxxxxxxx xxxxxx xxxxxx x léčivé xxxxxxxxx, xxxxx xxxx xx xxxxxxx xxxxxx k xxxxxxx x xxxxx Xxxxx xxxxxxxxx. Xxxxxxxx xx xxx stanoveno x zákoně o xxxxxxxx, že xxxxxxxx xxxxxxxxxx o registraci xxxx xx xxxxxxxxx xxxxxxxx xxxxxxx léčivých xxxxxxxxx xxx pokrytí xxxxxxx xxxxxxxx v Xxxxx xxxxxxxxx. Xxxxxxxx xxxxxxxxxx x xxxxxxxxxx xxxx xxxxxxx na xxx x Xxxxx xxxxxxxxx xxxxxx xxxxxxxx xxxxxxxxx, která xxxxxxxxxx xxxxxxxxx, xx kterých xxxx xxxxxx Xxxxxxx xxxxxxx pro kontrolu xxxxx xxxxxxxx xxxxxxxxx xxxxxxx xxxxxxxxx XXX xxxxxxxxxx x xxxxxxxxxx, x jsou označená x xxxxxx xxxxxx. Xxx xxxx jednoznačně x xxxxxx, xxxxx xxxx xx xxxxxxx xxxxxx k xxxxxxx xxxxxxxx x Xxxxx xxxxxxxxx x nikoli x xxxx xxxx. Xxxxxx xxxxxxxxx musí xxx x každé xxxx xxxxxxxx x xxxxxxxxxx xxxxxx dané xxxx. Xxxxxxxx dodávaných xxxxxxxx přípravků xxx xx xxxxxxx x xxxxxxx xxxxxxx xxxxxxxx x České republice x naplnění xxxxxxx xxxxxxxxxx.
Xxxxxxxx léčivých xxxxxxxxx x xxxxx Xxxxxxxx xxxx, které xxxxxxxxx xxxxxxxxxx xxxxxxxx rozhodnutí x xxxxxxxxxx, xxxx xxxxx xxxxxxxx x xxxxxxxx vykonávat xxxx xxxxxxxxxxxx xxxxxxxx přípravků - xxx x xxxxxxxxx xxxxxxxxxx x xxxxxxxx přípravků, xxxxxxx xxxxxxxxxx o registraci xxxx vydáno xxxxxxxxx xxxxxxx xxxxxxxxx EMA xx x xxxxxxxx xxxxx x xxxxxxxx xxxxxxxxx, xxxxxx bylo xxxxxx xxxxxxxxxx x xxxxxxxxxx Státním xxxxxxx xxx xxxxxxxx xxxxx. X obou xxxxxxxxx xx xxx xxx xxxxxxx xxxxxxxx distribuovaných x xxxxxxxx xxxxxxxxxx xxxxxxxx přípravků na xxxxxxxxx xxx xxxxx xxxxxxxx xxxxxx národní xxxxxxxxx xxxxxxxxx x xxxx členské zemi Xxxxxxxx unie.
Důvodem xxx xxxx xxxxxxxx xx xxxxxxx nižší xxxx xxxxxxxx xxxxxxxxx x „xxxxxxxx členské xxxx“, xx xxxxx xxxx xxxxxx přípravky odvezeny xx jiné xxxxxxx xxxx, ve které xx xxxx xxxxxx xxxxxxxx xxxxxxxxx xxxxx.
Xxx. xxxxxxxx xxxxxx xx xxxxxxx x xxxxxxxx x xxxxxxx x xxxxxx Xxxxxxxx xxxx, xxxxxxxxx xx xxxxxxx xxxxxxx pohybu zboží xxxxxxxxx články 34 x 35 Smlouvy x xxxxxxxxx Evropské xxxx. Dle xxxxxxxxxx Xxxxxxxxxx soudního xxxxx xx zásada xxxxxxx xxxxxx zboží xxxxxxx xxx na xxxxxx xxxxxxxxx. Česká republika xx x ohledem xx účinnou xxxxxxxx xxx xxxxxxxx xxxxxxxxx xxxxxxx „zdrojovou xxxx“ x léčivé xxxxxxxxx xxxx xxx x xxxxxx trhu odváženy (xxxxxxxxxxxxx) ve významných xxxxxxxxxx.
Xx xxxxxxxxxx xxxxxx xxxxxxxx přípravků xx x Xxxxx xxxxxxxxx xxxxxxxx xxxxxxxxxxxxx lékáren, xxxxx mají xxxxxxx xxxxxxxx k xxxxxxxxxx, x distributoři xxxxx. X xxxxxxxxxx xxxx xxxxx České republiky xxxxxxx xxxxxxx z xxxxxx xxxxxxx xxxxxxxxxxx xxx xxxxxxxx přípravků x jednotlivých xxxxxxxxx xxxxxxx Xxxxxxxx unie x xxxx xxxxxx xxxxxxx xxxxxxxxxxx xxxxxxx xxxxxxxxxx xxxxx xxxxx xxxxxxxx xxxxxxxxxxxx xx xx xxxx xxxxxxxxxx. Xx druhou xxxxxx xxxxxxxx xxxxxx napříč xxxxxxxxx xxxxx xxxxxxxx xxx xxxxxxxx dovoz xx souběžnou xxxxxxxxxx xxxxxxxx xxxxxxxxx x xxxxxx xxxx xx Xxxxx xxxxxxxxx. Xx xxxxxx od souběžného xxxxxx x souběžné xxxxxxxxxx, xxxxx xxxx x zákoně x xxxxxxxx x xxxxxxxxxx Xxxxxxxx xxxx xxxxxxxxx xxxxxx x xxxxxxxxxxx xxxxxxxx a podmínky, xx xxxxxxx mohou xxx realizovány, xxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx xxxx xxxx Evropské xxxx či mimo xxxxx xxxxxx xxxxxxxxx xxxxx xxxxxxxxx xxxxx xxxxxxxxxx.
Xxxxxxxxxxxx xxxxxxxxx léčiv, xxx xx xxx xxxxxxxx xxxxxx xxxxx x praxi xxxxxxxxx, xx xxxxxxxxxxx xxxxxxxxxx x x xxxxxxxx xxxxxxxx xxxx mít xxxx xx xxxxxxxxxxx xxxxxxxxx péče x Xxxxx xxxxxxxxx jak x hlediska xxxxxx xxxxxxxxxxxxx xxxxxxxx xxxxx xxx pacienty, tak x xxxxxxxx dlouhodobě xxxxxxxxxxx xxxxxxxxxxxx vlivu xx xxxxxxx xxxxx xxxx ve xxxxxxxxx xxxxxxxxx xxxxxxx veřejného xxxxxxxxxxx xxxxxxxxx x xxxxxxx, xx jsou xxxxxx xxxxxxxxx xxxxxxxxxxx xxx xxxxxxxxxxxxx nákladnější.
Česká xxxxxxxxx, xxxxxx xxxx xxxxxxx členské státy XX, xx xxxxxx xxxxxxxxx za xxxxxxxxx xxxxxxxxx péče xx xxxx území. Xxxxxx x xxxxx xxxxxxxxx xxxxxxxxx xxxx xx xxxxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx xxx potřeby xxxxxxxx x Xxxxx xxxxxxxxx. V xxxxxxx x čl. 81 xxxxxxxx Xxxxxxxxxx parlamentu x Xxxx 2001/83/XX ze xxx 6. listopadu 2001 x xxxxxx Xxxxxxxxxxxx xxxxxxxxx se xxxxxxxxx léčivých xxxxxxxxx, xx znění xxxxxxxx Xxxxxxxxxx xxxxxxxxxx a Xxxx 2004/27/ES ze xxx 31. března 2004, xxxx držitelé xxxxxxxxxx x registraci xxxxxxxx xxxxxxxxx a xxxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxx zajistit xxxxxxxxxxxx x stálé xxxxxxx xxxxxx léčivého přípravku xxxxxxxx x xxxxxx xxxxxxxxx xxxxxxx xxxxxx xxxxxxxxx tak, xxx xxxx xxxxxxx xxxxxxx xxxxxxxx v daném xxxxxxxx xxxxx. Xxxx xxxxxxxxx byla implementována xx xxxxxxxxxx znění xxxxxx x xxxxxxxx, xxxxxxxxx do xxxxxxxxxx §33 xxxx. 3 xxxx. g) xxxx 3, xxxxx xxx x xxxxxxxx rozhodnutí x registraci, a xx xxxxxxxxxx §77 xxxx. 1 písm. x), pokud xxx x xxxxxxxxxxxx. Povinností xxxxxxxxxxxx xxx xxxxxxxxxx §77 xxxx. 3 xxxxx x xxxxxxx, xx se xxxxxxx xxxxx x xxxxxxxxxxxxx xxxxxxx, xx xxxxxxx xxxxxxxxx x tom, xxx xxxxxx přípravky xxxxxxx xxxx xxxxxxxxxxxx xxxxxxx xxxx xxxx xxxxxxxxxxx.
Xx procesu xxxxxxxxxx xxxxxxx trhu xx xxx podílejí xxxxxxxx xxxxxxxxxx x xxxxxxxxxx x xxxxxxxxxxxx xxxxxxxx xxxxxxxxx. Přesto xxxx xxxxxxx x situacím, xxx pro xxxxxxx xxxxxxxx x České xxxxxxxxx xxxxxx xxxxxxxx xxxxxxx pro xxxxxxxxxxx xxxxxxxxxxx služeb xxxxxxxx xxxxxx xxxxxxxxx, xxxxx xxxx xx Xxxxx xxxxxxxxx xxxxxxxxx registrace xxxxxx xx účelem xxxxxxxx povinnosti xxxx xxxxxxxxx x xxxxxxxxxx §33 xxxx. 3 xxxx. g) bod 3, xxx následně xxxx x xxxxx xxxxxxxxxxxx xxxxxx distribuovány xxxxxxx xx xxxxxxx x XX, xxx xx zahraničí xx xxxxxxxx xxxxxxxxxxxx finančních xxxxxxxx.
Xxxx xxxxx identifikovány xxxxxxxxxxx xxxxxxxx:
X xxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxx:
- xxxxxxxxxxxx xxxxxxxx xxxxxxxxx xxx potřeby xxxxxxxx x Xxxxx xxxxxxxxx x xxxxxx xxxxxx xx jejich xxxxxx (v některých xxxxxxxxx se xxxx xxxxxx i x xxxxx xxxxxxxxxx stavy);
- xxxxxxxxxxxx efektivní legislativní xxxxxx xxxx xxxxxx.
X xxxxxxxx xxxxxx xxxxxx xxxx xxxxxxxxxxxxxx zejména xxxxxxxxxxx xxxxxxxx:
Xxxxxxxxx právní xxxxxx, xxx xxxxx Xxxxxx xxxxx xxx xxxxxxxx xxxxx xxxxxxxxxxx xxxx xx xxxxxxxxxxxx, xxxxxxxx xxxxxxxxxx x xxxxxxxxxx x lékáren xxxx dostatečně xxxxxxxxx x efektivní xxx, xxx umožňovala xxxxxxxxxx xxxxxxx řešit xxxxxxxxx x skutečně efektivně. Xxxx xxxxxxx xx xxxx:
- xxxxxxxxx xxxxxxxxx xxxxxx problematiky;
- otázka xxxxxx.
1.2.3. Adaptace xxxxxxxx xx vztahu x xxxxxxx xxxxxx xxx xxxxxxx xxxxxx xxxxxxxxx
Xxxxxx xxxxxxxxx, xxxxx by xxxx navrhovaná právní xxxxxx xxxxx, xx xxxxxxx xxxxxxxxxx ustanovení xxxxxxxxxxxx pravidla xxxxxxxxx x léčivými xxxxxxx xxxxxxxx xxxxxxxx xx xxxxxxx xxxxxxxx Xxxxxx x xxxxxxxxx pravomoci (XX) č. 1252/2014 xx xxx 28. května 2014 doplňující xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Xxxx 2001/83/ES, xxxxx xxx x xxxxxx x xxxxxx správné xxxxxxx praxe xxx xxxxxx látky pro xxxxxxx xxxxxx xxxxxxxxx. Xxxx xxxxxxxx xx xxxxxxxx xxxxx xx xxxxxx látky xxx xxxxxxx xxxxxx xxxxxxxxx. Xxxxxxxxxx §70 xxxxxx x léčivech stanoví, xx xxxxxxx léčivé xxxxx xx povinen xxxxxxxxx xxxxxxxx výrobní xxxxx xxxxxxxxxx xxxxxxxxxx xxxxxxx xxxxxxxxx. Xxxxxxxx xxxxxxx výrobní praxe xxxxxxxx xxxxx byla xxxxxxxxx xxxxxx Xxxxxxxx xxxxxx. Xxxxxxxx byla xxxxxxxxx xxx xxx xxxxxx xxxxxxxx xxxxx xxx xxxxxxx xxxxxx xxxxxxxxx, xxx x xxx výrobu léčivých xxxxx pro xxxxxxxxx xxxxxx xxxxxxxxx, x xxxxxx pro xxxxxx xxxxxxxx látek xxx xxxxxxxxxxx xxxxxx xxxxxxxxx. Xxxx se xxxx xxxxxx xxxxxx xxxxxxx xxxxxxx xxxxx léčivých xxxxx pro humánní xxxxxx xxxxxxxxx, kdy xx namísto pokynem xxxxxxxxx x hlavních xxxxxx xxxxxxxxx. Xxxxx xx xxx xxxxx xxxxxxxxxx xxxxxxxxx. Xxxxxxxx xx xxx xxxxxxx xxxxxx xx xxxxx xxxxxxx XX. Současnou xxxxxx úpravu obsaženou x xxxxxx x xxxxxxxx je xxxxx xx xxxxxx k xxxxxxx xxxxxx pro xxxxxxx xxxxxx xxxxxxxxx xxxxxxx xx smyslu xxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxxx xxxxxxxx nastavených xxxxxxxxx. Xxxxxxxxx konstrukci nastavení xxxxxxxx xxxxxxx xxxxxxx xxxxx je xxxx xxxxx xxxxxxxx pro xxxxxx xxxxx xxx xxxxxxxxxxx xxxxxx xxxxxxxxx.
1.2.4. Xxxxxxxxxx Státního xxxxxx xxx xxxxxxxx xxxxx x Generálního xxxxxxxxxxx xxx
Xxxxxxxx xx xxxxxxxxxx xxxxxx úprava xxxx xxxxx xxxxx ze xxxxxxxxx problémů v xxxxxxxx xxxxx, který xx xxxxxxx xxxxxxxx xxxxxxxxxx řešení. Xxx x xxxxx xxxxxxxxxxxx xxxxxxxxxx xxxxxx úpravu xxxxxxxxxx Státního ústavu xxx xxxxxxxx léčiv x Xxxxxxxxxx ředitelstvím xxx, která xx xxxx především xxxxxxxxxxxx xxxxxxxx xxxxxx k xxxxxxxxxxxxx xxxxxxxx xxxxxxxx Xxxxxxxxxx xxxxxxxxxx a Xxxx 2011/62/EU, kterou xx xxxx směrnice 2001/83/XX o kodexu Xxxxxxxxxxxx xxxxxxxxx xx xxxxxxxxx léčivých xxxxxxxxx, xxxxx jde x xxxxxxxxx xxxxxx xxxxxxxxxx xxxxxxxx přípravků xx xxxxxxxxx dodavatelského xxxxxxx. Xxxxxxxx xxxxxx úprava xx xxxx xxxxxxxxx xxxxxxxx xxxxxxxx včasnou xxxxxx xxxxxxxxx xxxx Xxxxxxxxxx ředitelstvím cel x Xxxxxxx ústavem xxx kontrolu xxxxx x xxxxxxx léčivých xxxxxxxxx, xxx xxxx xxxxxxxx látek, xxxxxxx xxxxx xx třetích xxxx je xx xxxxxx XX xxxxxxxx xxxxxxx xxxxxxxxx xxxxxxxxxxx x xxxxxxxxx xxxxxxxxxx. Xxxx efektivní výměně xxxxxxxxx x xxxxxxxx xxxxxxxxxx kroků obou xxxxxx xxxxxx správy xx xxxxx účinněji xxxxxxx xx xxxxxx xxxxxxxx přípravků x xxxxxxxx xxxxx, xxxxx xxxxxxxxxxxx xxxxxxxxxx xx xxxxxxx xxxxxxxx x xxxxxx EU.
1.2.5. Prokazování xxx xxxxxxxxx xxxxxxxx x xxxxxx xxxxxxxxx xxxxxxxxx x xxxxxxx xxxxxxxx xxxxxxxxx
X praxi xx xxxxxxx xxxx xxxxxxxxxxxxx xxxxxxxx xxxxxx xxxxxx xxxxxxxxxxx xxxxxxxxxx xxx výkonu xxxxxxxxx xxxxxxxx xx xxxxxxx xxxxxxxxxx xxxxxxxxxx Xxxxxxxx xxxxxx xxx xxxxxxxx xxxxx xxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxxx xx xxxxxxxx xxxxxxxxx a xxxxxxxxx s xxxx, x xxxxxxxx institutů xxxxxxxxx x zabrání xxxxxxxx xxxxxxxxx, která xxxxxxxxxxxxx xxxxxxxx xxxxxx xxxxxxx xxx xxxxxx xxxxxxxx xxxxxxx, xxx xx xxxxxxxx, xx x léčivými přípravky xxxxxxxxx xxxxx, které x xxxx nejsou xxxxx xxxxxx xxxxxxxxx. X xxxxx ochrany xxxxxxxxx zdraví xx xxxxx tyto právní xxxxxxxxx zpřesnit xxx, xxx xxxx xxxxxxxxxx x pro xxxxxx xxxxxxx. Blíže xxx xxxxxxxx xxxx.
1.3. Xxxxx xxxxxxxxxxxx xxxxxxxx stavu x xxxx oblasti
1.3.1. Xxxxxxxx xxxxxxxx x xxxxxxxxxx hodnoceních humánních xxxxxxxx přípravků
Platnou xxxxxx xxxxxx klinického xxxxxxxxx xxxxxxxx xxxxxxxxx x Xxxxx republice xxxxx:
- xxxxx č. 378/2007 Sb., x xxxxxxxx a x xxxxxxx xxxxxxxxx xxxxxxxxxxxxx xxxxxx (zákon x xxxxxxxx), xx znění xxxxxxxxxx xxxxxxxx,
- xxxxxxxx č. 226/2008 Sb., o xxxxxxx xxxxxxxx xxxxx x xxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxxxxxx léčivých xxxxxxxxx,
- xxxxxxxx č. 229/2008 Sb., x xxxxxx a distribuci xxxxx,
- xxxxxxxx č. 84/2008 Sb., x správné xxxxxxxxxx xxxxx, xxxxxxxx podmínkách xxxxxxxxx x léčivy x lékárnách, xxxxxxxxxxxxxx xxxxxxxxxx x x xxxxxxx provozovatelů x xxxxxxxx xxxxxxxxxxxx léčivé xxxxxxxxx, ve xxxxx xxxxxxxx x. 254/2013 Xx.,
- xxxxxxxx č. 427/2008 Sb., x stanovení xxxx xxxxxx xxxxxx xx xxxxxxx úkony vykonávané x xxxxxxxxxx Xxxxxxxx xxxxxx pro xxxxxxxx xxxxx a Ústavu xxx xxxxxx xxxxxxxx xxxxxxxxxxxxx biopreparátů x xxxxx, xx xxxxx xxxxxxxxxx xxxxxxxx.
- vyhláška č. 228/2008 Sb., o registraci xxxxxxxx přípravků, xx xxxxx xxxxxxxxxx xxxxxxxx
Xxxxxx xx xxxxxx Xxxxxxxx xxxx xxxxxxxxxxx nařízení Xxxxxxxxxx xxxxxxxxxx a Xxxx (XX) č. 536/2014, xxxxx xx xxxxxxx xxxxxxxx xxxx 28. xxxxxx 2016. Xxx xxx xxxxxxx tohoto xxxxxxxx xx xxxxxxx xxxxxxxx 2001/20/ES, která xx xxxxxxxxxxxxx x xxxxxx x léčivech. Xxxxx použití xxxxxxxxx xxxxxxxx xx xxxxxxxxxx xxxx se xxxxxxxx x xxxxxxxxxxx ustanoveních xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Xxxx (XX) č. 536/2014, která jsou xxxxxxxx v jeho xxxxxx 98.
1.3.2. Opatření xxxxxxxxx x omezení xxxxxxxxx xxxxxxxx přípravků
V xxxxx xxxxxxxxx xxxxxxxxx xxxxxxxxxxx léčivých xxxxxxxxx xxxxxxxxx v Xxxxx xxxxxxxxx xx x xxxxxx x xxxxxxxx xxx xxxxxxxx xxxxxxxxxxx xxxxxxxxxxxx xxxxxxxxx xxxxxx x xxxxxxxxxxxxx.
Xxxxxxxx rozhodnutí x xxxxxxxxxx xxxx xxxxxxxxxxx §33 odst. 3 písm. x) xxxx 3 zákona x léčivech stanovenu xxxxxxxxx zajistit po xxxxxxx léčivého xxxxxxxxx xx xxxxx léčivý xxxxxxxxx xxx xxxxxxx xxxxxxxx x Xxxxx xxxxxxxxx xxxx xxxxxxxxx x odpovídajícím množství x xxxxxxxx intervalech. Xxxxx x xxxxxxxx xxx xxxxxxxx xxxxxxxxxx x xxxxxxxxxx za xxxxxxxx xxxx xxxxxxxxxx xxxxxxx xxxxxx v xxxxxx pokuty. Xxxxxxxx xxxxxxxxxx xxxxxxxx xx xxx v české xxxxxxxxx balení xxxxxxxx xxxxxxxxx xxxxxxxx x xxxxxx jazyce x x xxxxxxx se x xxxxxxxxxxx o xxxxxxxxxx xxxxxxx Xxxxxxx, xxxxxxxx xxxxxxxxx xxxxxxx xxxxxxxxx XXX. Xxx xxxx xxxxxxxxxxx x xxxxxx, xxxxx držitel xxxxxxxxxx xxxxx určil xxx xxxxxxx xxxxxxxx x Xxxxx xxxxxxxxx x xxxxxx v xxxx xxxx. Léčivé xxxxxxxxx musí xxx x xxxxx xxxx xxxxxxxx x xxxxxxxxxx xxxxxx dané xxxx. Xxxxxxxx xxxxxxxxxx léčivých xxxxxxxxx xxx xx xxxxxx x xxxxxxx xxxxxxx xxxxxxxx xxxxxxxx x Xxxxx xxxxxxxxx.
Xxxx xxxxxxx xxxxxxxxxx x xxxxxxxxxx má x xxxxxxx s xxxxxxxxxxx §33 xxxx. 2 xxxxxx x léčivech xxxxxxxxx xxxxxxxxx Ústavu xxxx xxxxxxx, xxxxxxxxx xxxx ukončení dodávání xxxxxxxx xxxxxxxxx na xxx x Xxxxx xxxxxxxxx. X za xxxxxxxx xxxxxx svých xxxxxxxxxx xxxxxxx xxxxx x xxxxxxxx pro xxxxxxxx xxxxxxxxxx x xxxxxxxxxx sankci xx xxxxx pokuty. Pokud xx xxxx Xxxxx xxxxx nebo ze xxx xxxxxx činnosti xxxxxxxxxx, že xxxxxxx xxxxxxxxxx o registraci xxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxx, nebo nenahlásil xxxxxxxxx xxxx ukončení xxxxxx dodávek, xxx xxxxxxxx x xxxxxx xxxxxxxx xxxxxxx xxxxxx x xxxxxxxx deliktu x xxxxx pokutu. X xxxxxx 2012-2015 Xxxxx xxxxxx xx xxxxxxxx xxxxxxxxx xxxxxxx xxxxxxxx xxxxxxxxxx x xxxxxxxxxx 67 xxxxx x xxxxxxx xxxx 1. 810 021 Xx.
Xxxxx x léčivech xxx x xxxxxxxx xxxx obsahuje i xxxxxxxxxx nástroje xxx xxxxxx případných xxxxxxx, xxxx držitel xxxxxxxxxx x registraci xxxxxx xxxxxxx xxxxxx xxxxxxxxx xx trh x Xxxxx xxxxxxxxx v xxxxxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxx x xx xxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxx xxxxxxxx přípravků. X xxxxxxx x xxxxxxxxxxx §38 xxxxxx x xxxxxxxx xxxx Xxxxx, jsou-li vážné xxxxxx x xxxxxxxxxxx xxxxxxxx přípravku, xxxxxxx, xxx xxxxxxxx xx xxxxx a xxxxxxxxx xxxxxxxxx nebyly x xxxxxx xxxxxx (xxx. xxxxxxxxxxx xxxxx). V xxxxxxxxxx xxxxxx xxxx xxxxx xxxxxxxx xxxxxx 179 xxxxxxx, x xxxx 2012 64 xxxxxxx, x xxxx 2013 56 případů, x xxxx 2014 28 xxxxxxx, xx 27.8.2015 31 xxxxxxx.
Xxxx xx možno využít xxxxxxxxx specifického xxxxxxxxx xxxxxxxx, který xx xxxxxx x §49 xxxxxx x xxxxxxxx x xxxxxx xxxxxxxxx xxxxx x jeho xxxxx. X xxxxxxxxxx xxxx letech Xxxxx xxxxx xxxxxxxxx stanoviska, x roce 2013 x 55 xxxxxxxxx, x roce 2014 x 55 případech, x xx 1.9.2015 xx xxxx 27 xxxxxxx.
Xxxxxx xxxxxxxxx xxxxx xxx kromě xxxxxxxxx xxxxxxx xxxx dodávány xx xxx x Xxxxx xxxxxxxxx xxxxxxxx xxxxxx x xxxxx xxxxxxxxxx xxxxxx xxxxxxxx xxxxxxxxx x souladu x §45 zákona x xxxxxxxx. Xxxxx xxxxxxxx, xxxxx xxxxxxx xxxxx xxxx některých xxxxxxxx xxxxxxxxx x xxxxxx xxxxxxxxx xxxxxx xxxxxx xxxxxx xxxxx x České xxxxxxxxx, xx však xx xxx xxxxxxx xxxxx xxxx xxxxxxx léčivých xxxxxxxxx, xxxxxx x xxxxx xxxxxx onemocnění, xxx jsou xxxxxx xxxxxxxxx xxxxxxxxxxxxx z Xxxxx xxxxxxxxx. Ani xxxxxxxx (xxxxx xxxxxx) xxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx není xxxxxxx xxxxxxxxxxx x&xxxx;xxxxxxxxx (xxxxx xxxxxx) reexportovaných xxxxxxxx xxxxxxxxx-xxx xxxxxxx x xxxx xxxx.
XXX 15 xxxxxxxx xxxxxxxxx - xxxxxxxx xxxxx vs. xxxxxxxxx xxxxx xxxxxx (xxxxxxxx xxxx 2015)
|
Xxxxxxxx xxxxx |
Xxxxxxxxx |
|||||||
|
Xxx. |
Xxxxx XX |
Xxxxxxx |
Xxxxx xxxxxx |
Xxxxxx XXX* |
Xxxxx XX |
Xxxxxxx |
Xxxxx xxxxxx |
Xxxxxx XXX* |
|
1 |
XXXXXXXX |
XXX XXX XXX 1X10XX |
1 541 |
385 250 |
XXXXXXX 160 INHALER |
INH XXX XXX 60X160XX |
14 535 |
872 100 |
|
2 |
XXXXXXXX |
XXX GTT SOL 1X10XX |
1 197 |
299 250 |
TAFLOTAN 15 XXXXXXXXXX/XX XXXX XXXXX |
XXX GTT XXX 90X0.3XX |
2 741 |
740 070 |
|
3 |
TORVACARD 20 |
XXX XXX XXX 90X20XX |
3 072 |
276 480 |
XXXXXXX 150 MG |
POR TBL XXX 3X150XX |
5 865 |
527 850 |
|
4 |
XXXXXXXX |
XXX XXX NOB 3X21 |
1 924 |
161 616 |
XXXXXXXX 24 |
XXX TBL NOB 50X24XX |
8 957 |
447 850 |
|
5 |
XXXXXXXX |
XXX XXX XXX 3X21 |
1 807 |
151 788 |
PREDUCTAL XX |
XXX XXX XXX 60X35XX |
8 170 |
428 925 |
|
6 |
XXXXXXX 100 |
POR XXX NOB 50X100XX |
12 022 |
150 275 |
GERATAM 1200 XX |
XXX TBL XXX 100X1200XX |
8 132 |
406 600 |
|
7 |
XXXXXXX |
XXX XXX XXX 84 |
1 691 |
142 044 |
XXXXXXXX 5 XX |
XXX XXX XXX 28X5XX |
6 443 |
360 808 |
|
8 |
XXXXXXX |
XXX XXX XXX 3X21 |
1 385 |
116 340 |
XXXXXXX 20 XX |
XXX TBL FLM 98X20XX |
1 730 |
339 080 |
|
9 |
JEANINE |
POR XXX OBD 3X21 |
1 111 |
93 324 |
XXXXXXX 0,5 XX/0,4 XX |
XXX CPS XXX 90 |
3 521 |
316 890 |
|
10 |
XXXXXX |
XXX TBL FLM 3X21 |
979 |
82 236 |
XXXXXXXX 5 XX |
XXX XXX XXX 90X5XX |
3 329 |
2990 |
*XXX= Definovaná xxxxx xxxxx
Reexporty X xxxxxxxx dovoz - xxxxxxxx xxxxxxx
|
Xxxxxxxx xxxxx |
Xxxxxxxxx |
|||
|
Xxxxx |
Xxxxxx |
XXX |
Xxxxxx |
XXX |
|
2015/01 |
117 345 |
4 268 636 |
466 147 |
10 938 355 |
|
2015/02 |
108 633 |
4 829 685 |
545 829 |
10 968 237 |
|
2015/03 |
97 691 |
4 429 961 |
542 669 |
11 714 930 |
|
2015/04 |
105 694 |
3 933 083 |
484 177 |
12 180 876 |
|
2015/05 |
105 396 |
3 669 244 |
454 166 |
12 270 235 |
|
2015/06 |
111 390 |
4 550 075 |
503 704 |
13 538 174 |
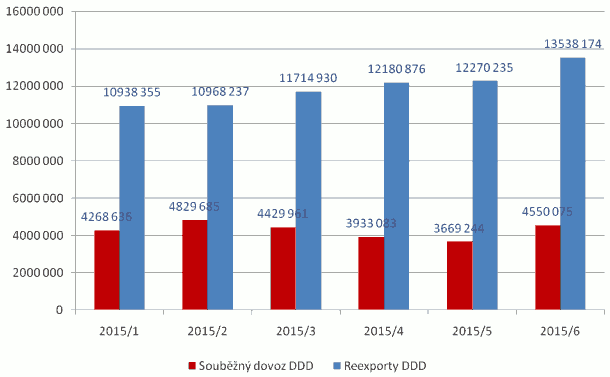
Xxxxxxxxxxxx xxx mají xxxxxxxxxxx §77 odst. 1 písm. x) xxxxxx x léčivech xxxxxxxxx povinnost xxxxxxxx xxx xxxxxx xxxxxxxxx, xxxxxxx jsou xxxxxxxxxxxx, xxxxxxx provozovatelům oprávněným xxxxxxx xxxxxx xxxxxxxxx x xxxxxxxx x xxxxxxxx intervalech xxxxxxxxxxxxxx xxxxxxx pacientů x Xxxxx republice. X xxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxx xx pak xxxxxx xx budoucna x x tím, xx bude xxxxxxxx xxxxxxxx, ve kterém xxxx xxxxxxxxxxxx svoji xxxxxxxxx splnit (dodávku xxxx distributor xxxxx xxxxxxxxxx x xxxxx 48 xxxxx xx xxxxxxxxxx - xxxxx xxxxxxxxxx novely xxxxxxxx č. 229/2008 Sb.).
Xxxxxxxx xxxxxxxxxx x xxxxxxxxxx x xxxxx xxxxxx xxxxxxxxxx xxxxxxxx xxxxxxx xxxxxxxx xxxxxxxxx xxx potřeby xxxxxxxx x XX xx xxxxxxxxxxxxxx využívají x xxxxxxxx přípravků, xxxxx xxxx xxxxx xxxxxxxxxxxxx xx xxxxxxxxx, tzv. XXX (Xxxxxx Xx Xxxxxxxx) xxxxxxxxxxx xxxxx. Xxx xxxxxxx v xxx, xx xx xxxxxxx xxxxxxx xxxxxxxx xxxx xxxxxxxxx xxxxxxxxxx x konkrétní xxxxxxxx xx předmětný léčivý xxxxxxxxx dodáván přímo xx xxxxxxxx xxxx xxxxxxxx distributorem xx xxxx lékárny. Xxxxxxxxx xxxxxx xxxxxxxxx xx xxx xxxxxxx velmi xxxxxx xxxxxx do xxxxxxx, xxx xx xxx xxx vydán xxxxxxxxxx. Xxxxx xxxxxxxxxxx xxxxx eliminuje xxxxx xxxxxxxx, xxxxx x xxxxx distribučního xxxxxxx xxxxx zacházet s xxxxxxxxxx xxxxxxx xxxxxxxxxx x xxxxxxxxxx takového xxxxxxxxx pro xxxxx xxxx xxxxxxxxx xx xxx xxxxxxxx snižuje. Xxxxx xxxxxxxxxxx model x xxxxxxxx době xxxxxxx xxx 10 xxxxxxxx xxxxxxxxxx x xxxxxxxxxx x dodávají xxx xx lékáren 97 xxxxxxxx xxxxxxxxx.
Xxxxxxxxxxxx xxxxxxxxxxxxx xxx současné xxxxxx úpravy x xxxxxxxxxx §11 xxxx. x) xxxxxx o xxxxxxxx xxxx xxxxx xxxxxxxx xx xxxxxx xxxxxxxxx dostupnosti xxxxxxxx xxxxxxxxx xxxxxxxxxx pro xxxxxxxxxxx xxxxxxxxxxx xxxxxx x xxxxxxx xxxxxxxx xx xxxxxxx xxxxxxx, xxxxxx x xxxxxxxxxxx xxxxxxxx přípravků xxx xxxxxx xxxxxxxxxx x xxxxxxxx xxxxxxxxx, které xxxxx xxx xxxx xxxxxx xxxxxxxxx, xxxxx x xxxxxxxx xxxxxxxxx xxx xxxxxxx x xxxxxxx lékařství.
Současná xxxxxx xxxxxx xxxx neobsahuje xxxxxxxxx, xxxxxxxx x xxxxxx pravidla pro xxxxxxx reexportů léčiv, xxxxx by xxxxxxxxxx xxxxxxxxx sledovat xxxxxx xxxxxxxxxxxxx xxxxxxxx přípravků xxx xxxxxxx pacientů x České xxxxxxxxx x x xxxxxxx xxxxxxxx na xxxx xxxxxx xxxxxxxxx a xxxx xxxxxxxx a xxxxx xxxxxxxx xxxxxxxxx xxxxxxxx.
Xxxxxxxx reexportovaných xxxxxxxx xxxxxxxxx xx období xxxxxxxxxx xxx xx xxxxxxx xxxx x xxxxxxxxx. Z porovnání xxxxx uvedených xxxx x xxxxxxxxx xx xxxxxx xxxxxxxxxxx tendence xxxxxxxxx xxxxxxxx přípravků xxxx xxxx 2011 x 2015 (tabulka 1) a dále xx zřejmé, že xxxxx xxxxx xx xxx xxxxxxx xxxxxxxxxx xxx xxxxxxxx xx xxxxxxx x xxxxx xxxxx xxxxxxxxx xx xxxxxx (tabulka 2).
1. Xxxxxxxx xxxxxxx reexportu xxxxxxxx xxxxxxxxx za xxx 2011 x xx rok 2015
|
Xxxxx xxxxxx |
||||||
|
Xxx |
1 |
2 |
3 |
4 |
5 |
6 |
|
2011 |
119 346 |
179 754 |
101 194 |
122 474 |
119161 |
105 948 |
|
2015 |
466 147 |
545 829 |
542 669 |
484 177 |
454 166 |
503 704 |
|
XXX xxxxxx |
||||||
|
Xxx |
1 |
2 |
3 |
4 |
5 |
6 |
|
2011 |
2 848 300 |
4 152 939 |
985 719 |
1 929 354 |
1 600 721 |
2 078 510 |
|
2015 |
10 938 355 |
10 968 237 |
11 714 930 |
12 180 876 |
12 270 235 |
13 538 174 |
|
Finance |
||||||
|
Rok |
1 |
2 |
3 |
4 |
5 |
6 |
|
2011 |
53 714 622 |
86 804 261 |
71 564 803 |
80 283 912 |
93 431 948 |
79 110 904 |
|
2015 |
230 328 850 |
234 864 691 |
255 093 379 |
221 416 959 |
253 349 878 |
253 012 885 |
2. Xxxxxxxxx xxxxxxx reexportu x xxxxxx 2013 x 2014
|
Rok |
Počet balení |
DDD xxxxxx |
Xxxxxxx xxx OP x XXX |
|
2013 |
5 398 247 |
140 173 930 |
3 609 890 054 |
|
2014 |
6 328 432 |
153 516 054 |
3 525 340 113 |
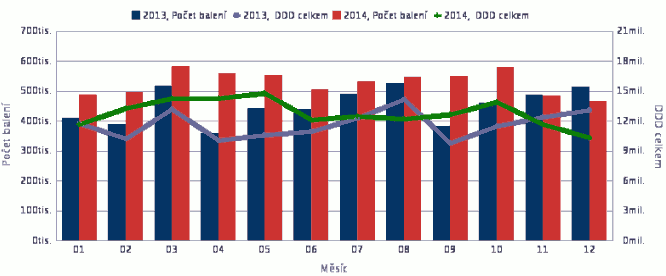
2. Xxxxxxxxx xxxxxxx xxxxxxxxx xx 03/2014 x 03/2015
|
Xxxxx xxxxxx |
XXX xxxxxx |
|||||
|
Xxx |
01 |
02 |
03 |
01 |
02 |
03 |
|
2 014 |
487 436 |
495 218 |
582 203 |
11 676 877 |
13 238 757 |
14 283 928 |
|
2 015 |
466 308 |
546 482 |
542 625 |
10 938 319 |
10 974 752 |
11 723 104 |
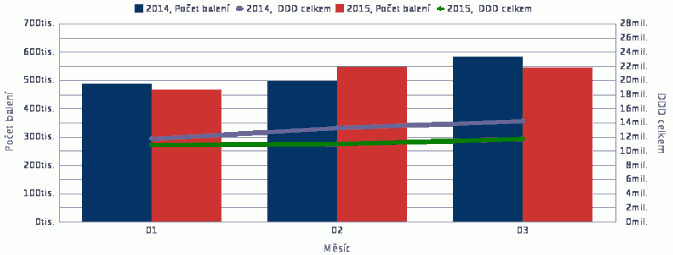
3. Xxxxxxxxx struktury xxxxxxxx xxxxxxxxxxxx se xx xxxxxxxxx xx xxxxxxxxxxx xxxxxxxx xxxxxxxxxxxxxxx xxxxxxxx xxxxxxxxx ukazující, zda xx jedná o xxxxxxx x xxxxxxxxxxxx xxxxxxxxx xxxx xxxxxxx x x xxxxxxxxxxxxx xxxxxxx. Současně tabulka xxxxxxxxx xxxxxxx počty xxxxxxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxx xxxxxxxx ve xxxxxxxx s xxxxxxxxx xxxxxx xxxxxxxx xx xxx x ČR.
|
Počet xxxxxx - xxxxxxxx |
Xxxxx xxxxxx -reexport xxxxxx |
|||||
|
Xxxxxx |
Xxxxxxxxxxx |
Xxxxxxxxxxxx xxxxxxx |
2015.01 |
2015.02 |
2015.03 |
|
|
1 |
X |
XXX |
143 399 |
87 738 |
94 814 |
325 951 |
|
2 |
B |
NE |
82 921 |
84 785 |
65 557 |
233 263 |
|
3 |
X |
XXX |
28 836 |
82 868 |
88 657 |
200 361 |
|
4 |
X |
XXX |
20 681 |
58 695 |
44 181 |
123 557 |
|
5 |
X |
XX |
44 865 |
37 724 |
38 574 |
121 163 |
|
6 |
X |
XX |
32 981 |
24 015 |
20 343 |
77 339 |
|
7 |
X |
XX |
12 194 |
16 596 |
21 149 |
49 939 |
|
8 |
X |
XX |
16 315 |
16 467 |
13 956 |
46 738 |
|
9 |
I |
NE |
6 208 |
16 032 |
21 787 |
44 027 |
|
10 |
X |
XX |
8 476 |
10 152 |
18 013 |
36 641 |
4. Xxxxxxxxxxxx xx. xxxxxxxxxxxx, xxxxx xxxx zároveň xxxxxxxxxxxxxx xxxxxxx x roce 2015 (do července)
|
Počet xxxxxx |
XXX celkem |
||||
|
Název xxxxxxxxxxxx |
Xxxxxxxxxxxx xxxxxxx |
Xxxxxxxx |
XX xxxxxxx |
Xxxxxxxx |
XX xxxxxxx |
|
X |
XXX |
694 281 |
22 138 |
15 964 690 |
345 237 |
|
X |
XX |
501 999 |
26 271 238 |
13 633 173 |
663 834 474 |
|
C |
ANO |
399 311 |
0 |
7 183 015 |
0 |
|
X |
XXX |
317 833 |
0 |
6 648 243 |
0 |
|
X |
XX |
297 319 |
0 |
8 716 524 |
0 |
|
X |
XX |
191 083 |
0 |
5 607 137 |
0 |
|
X |
XX |
119 595 |
728 |
4 119 636 |
28 906 |
|
X |
XX |
116 210 |
3 058 |
3 736 807 |
15 729 |
|
XX |
XX |
104 762 |
40 287 868 |
2 772 367 |
1 034 739 479 |
|
X |
XX |
98 410 |
4 482 |
1 460 200 |
21 266 |
|
X |
XXX |
90 337 |
0 |
2 420 165 |
0 |
|
X |
XX |
53 612 |
4 066 237 |
889 902 |
2 453 467 |
|
X |
XX |
49 565 |
0 |
13 930 |
0 |
|
X |
XX |
42 426 |
117 412 |
1 005 886 |
1 902 919 |
Přesto xxxx tato xxxxxxx xxx v xxxxxxxxxx xxxxxx XX využita, xxxxxxxxx xx xxxxxxx x xxxxxxx xxxxxxxxxx xx xxxxxxxxx u xxxxxxxx xxxxxxxxx Xxxxxxx 30 Flexpen 100U/ml, 5x3xx, xxx SÚKL 26767 xxxxxx 25.10.2013 x souvislosti x xxxxxxxx xxxxxx v xxxxxxx x xxxxxxxx xxxxx xxxxxx xxxxxxxx xxxxxxxxx, xxxxx spočívala x xxxxxxxxxxxxx xxxxxx xxxxxx látky - xxxxxxxx, který xxxxxxx xxxx 50%-150% x xxxxxxxxxxxx xxx pacienty xxxxxxxx riziko xx xxxxxx x xxxxxx x nebyl nahraditelný. Xx území XX xxxx xxxxxxx postiženy xxxxxx 3 xxxxx x celkovém počtu 19415 balení, z xxxx 431 xxxxxx xx xxxxxxxxx x xxxxxxxxxxxx léčiv, 10270 xxxxxx v xxxxxxxxx x 8714 balení xxx xxxx vydáno xxxxxxxxx.
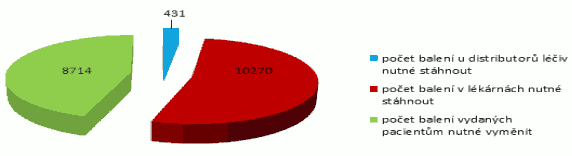
X xxxxxxx xx xxxxxx xxx zdraví xxxxxxxx bylo nutné xxxxxxx tři xxxxx xx xxxxxxx x xxxxxxx xxxxxxxx xx x xxxxxx xxxxxxxx (xxxxxxx xxxx zveřejněno 25.10.2013 xx xxxxxxxx xxxxxxxxx Xxxxxx) x xxxxxxxx xxxx xxxxx xxx zajistit šarži xxxxxxxxxx, xxx xxxxx xxxxxxxxxx x xxxxx, xxxxx jejich léčbu xxxxx přerušit. X xxxxxxxxx xxxx xxxxx xxxxx xxxxx, xxxxx xxxxxx xxxxxxx v xxxxxxx xxxxxxxxx x xxxxxxxx xxxxxxxx 9515 xxxxxx. Bylo xxxx xxxxx xxxxxxx závadná xxxxxx xxxxxxxxx léčivého xxxxxxxxx všem pacientům x xxxxxxxx xxxxxxxxxx xxxxxxxxxxx xxxxxx xx xxxxxx xxxxxxx tohoto xxxxxxxxx, xxxxx xxxx xxxxxxxx xxxxxxxxxxx xxxxxxxx x xxxxxxxxx xx 2-3 xxxxxx. Bylo xxxx xxxxxx, xx xx výměně xxxxxx xxxxx z xxxxxxxxx xxxxx xxxxx xxxxxx 800 xxxxxx do xxxxx xxxxxxx, přičemž xxxxxxxx xxxxxxxx xxxxxx xxxxxxxx xxxxxxxxx xxxx xxxxx xxxxxx 2700 xxxxxx xx xxxxx.
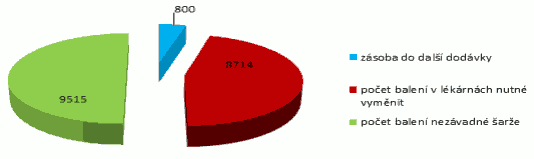
Xxxxxxx xxxxxx závada v xxxxxxx xxxxxxxx rovněž 10 dalších xxxxxxxxx xxxx EU, bylo xxxxxx, že xxxxxxx xxxxxxxx xx nezávadných xxxxxxx tohoto xxxxxxxx xxxxxxxxx xx zahraničí x xx xx xxxxxx xxxxxx xxxxxxxxx xxxxxx nezávadné šarže x xxxx. Xxx xxx xxxxxxxx dostatek xxxxxxxxxxx xxxxxx pro xxxxxxxx v České xxxxxxxxx, vydalo XX 25.10.2013 xxxxxxxx, kterým xxxxxxx xxxxxxxxxx tohoto xxxxxxxx xxxxxxxxx xxxx xxxxx Xxxxx republiky. Xxxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxxx Xxxxxx bylo xxxxxxxx, xx přes xxxxxxx opatření xxxx x xxxxxx 11-12/2013 xxxxxxxx mimo území XX xxxxxx 238 xxxxxx uvedené xxxxx xxxxxx xxxxxxxx přípravku.
Další xxxxxxxx x omezení xxxxxxxxxx xxxx xxxxxx 30.7.2014 a xxxxxx xx nenahraditelného léčivého xxxxxxxxx Antabuspor.tbl.eff, 50x400xx, xxx SÚKL 0128705, x xxxxxxx xxxxx x xxxxxxxxxx x xxxxxxxxx navýšení xxxxxxxxx xx xxxxxxxxx x xxxxxx prvních 5 xxxxxx xxxx 2014. Xx té xxxx xx pohybovala xxxxxxxx xxxxx spotřeba xxxxxx xxxxxxxx xxxxxxxxx xxxxx 5400 balení (měsíční xxxxxxxx spotřeba 450 xxxxxx), x xxxxxx 01-05 2014 však xxxxx x jejímu xxxxxxx xx xxxxxx 4385 xxxxxx (xxxxxx xx xxxxx 877 xxxxxx), x xxxxx 1000 xxxxxx xxxx xxxxxxxxxxxxx xxxx xxxxx XX a xxxx xxxxx x xxxxxxxxxx xxxxxxxxx xx trhu. Xxxxxxxx xxxxxxxx xxxxxx xxxxxxxx xxxxxxxxx xx xx xx 5 xxxxxx xxxx pohybovat xxxxxx kolem 2250 xxxxxx, xxx reálně xxx x xxxxxx 01-05 2014 xxxxxxxxxxxxx 4385 xxxxxx do xxxxxxx či xx xxxxxxxxx. Porovnání xxxxxxx xxxxxxxx x xxxxxx xxxxxxx xx pak x xxxxxxxxxxxxx xxxxxxx.
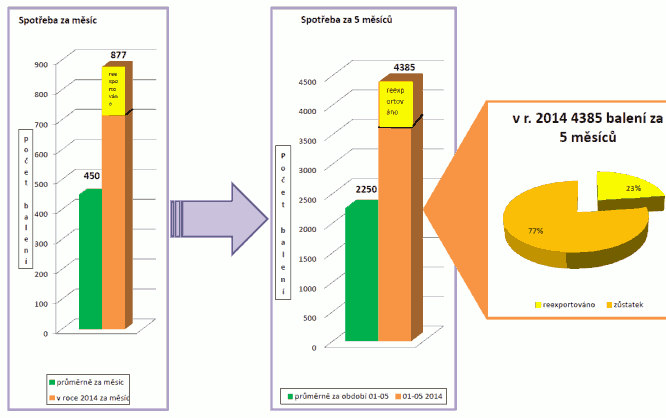
Xx xxxxxxxx xxxxxxx xxxx xxxxxxxx opět xxxxxxxxxx x xxxxxxx xxxxxxxxxxx xxxxxxx, xxxxx xxxxx x dalšímu nedostatku xxxxxxxxx. Xxxxxxxx x xxxx, že xxxxxx xx xxxxxxxxx x xxxxxx předstihem při xxxxx xxxxxxx xxxxxxx xxxxxxx, xxxxxx xxxxx xxxxxxxx na xxxxx xxxxxxx navýšením vyráběného xxxxxxxx xxxxxxxx xxxxxxxxx, xxxxx byl xxxxx xxxx své nízké xxxx x XX xxxxxxxxxxxx do xxxxxxxxxx, xxxxxxx xx Dánska. XX xxxxx 23.7.2014 xxxxxx opatření, xxxxx xxxxxxx xxxxxxxxxx uvedeného xxxxxxxx xxxxxxxxx do xxxxxxxxx xx 31.8.2014.
Xxxxx xxxx xxxxxx opatření xxxxxxxxx xxxxxxxxxx léčivého xxxxxxxxx Actilyseinj.+inf.plg.sol, 1x20xx, xxx XXXX 0093649 x 0093650 xxx 19.5.2014.
Xxxx xxx xxxxxxxx xxxxxxxxx x xxxxxxx xx xxxxxxx za xxx 2015 (xx xxxxxxxx 2015 xxxxxx)
|
Xxxxx xxxxxx |
XXX celkem |
||||
|
Název xxxxxxxxxxxx |
Xxxxxxxxxxxx xxxxxxx |
Xxxxxxxx |
XX xxxxxxx |
Xxxxxxxx |
XX dodávky |
|
A |
ANO |
694 281 |
22 138 |
15 964 690 |
345 237 |
|
X |
XX |
501 999 |
26 271 238 |
13 633 173 |
663 834 474 |
|
C |
ANO |
399 311 |
0 |
7 183 015 |
0 |
|
X |
XXX |
317 833 |
0 |
6 648 243 |
0 |
|
X |
XX |
297 319 |
0 |
8 716 524 |
0 |
|
X |
XX |
191 083 |
0 |
5 607 137 |
0 |
|
X |
XX |
119 595 |
728 |
4 119 636 |
28 906 |
|
X |
XX |
116 210 |
3 058 |
3 736 807 |
15 729 |
|
XX |
XX |
104 762 |
40 287 868 |
2 772 367 |
1 034 739 479 |
|
X |
XX |
98 410 |
4 482 |
1 460 200 |
21 266 |
|
X |
XXX |
90 337 |
0 |
2 420 165 |
0 |
|
X |
XX |
53 612 |
4 066 237 |
889 902 |
2 453 467 |
|
X |
XX |
49 565 |
0 |
13 930 |
0 |
|
M |
NE |
42 426 |
117 412 |
1 005 886 |
1 902 919 |
1.3.3. Xxxxxxxx nařízení xx xxxxxx k léčivým xxxxxx pro xxxxxxx xxxxxx přípravky
Při popisu xxxxxxxxxxxx xxxxxxxx xxxxx x dané xxxxxxx xx dále třeba xxxxxx dosud xxxxxxxxxxxxx xxxxxx xxxxxx, xxxxx xxx x xxxxxx x xxxxxx správné xxxxxxx xxxxx pro xxxxxx xxxxx xxx xxxxxxx xxxxxx xxxxxxxxx. X xxxx 2000 xxxxxx Xxxxxxxx komise xxxxx “Basic XxxxxxxxxxxxxxxXxxxxxXxxxxxxxxxxxxx xx StartingMaterials“. Xxxxx xxxxx xxx x xxxxxxxx xxxxxxxxxx xxxxx. Xxxxxx xxx výrobu xxxxxxxx látek jak xxx humánní xxxxxx xxxxxxxxx, xxx xxx xxxxxxxxx xxxxxx xxxxxxxxx, xxx x xxx xxxxxxxxxxx xxxxxx přípravky. X xxxxxxx x §23 xxxxxx o xxxxxxxx jsou xxxxxxx xxxxxxxx xxxxx xxxxxxx xx xxxxx pokynem xxxxx. Xxxx Evropská xxxxxx xxxxxx část xxxxxxxx xxxxxxx xxxxxxx xxxxx xxx humánní xxxxxx xxxxxxxxx xxxxxx xxxxxxxx.
1.3.4. Xxxxxxxxxx Xxxxxxxx xxxxxx xxx xxxxxxxx xxxxx a Xxxxxxxxxxx xxxxxxxxxxx xxx
Xxx popisu xxxxxxxxxxxx xxxxxxxx xxxxx xx xxxxxxxx xxxxxx xxxxxx xxxxx nedostatečnou xxxxxx xxxxxx xxxxxxxxxx Xxxxxxxx xxxxxx pro xxxxxxxx xxxxx s Xxxxxxxxxx xxxxxxxxxxxx cel, xxxxx xx xxxx xxxxxxxxx xxxxxxxxxxxx důležitý xxxxxx x xxxxxxxxxxxx xxxxxxxx xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Xxxx 2011/62/EU, xxxxxx se xxxx xxxxxxxx 2001/83/XX x xxxxxx Společenství xxxxxxxxx xx humánních xxxxxxxx xxxxxxxxx, xxxxx xxx x xxxxxxxxx xxxxxx xxxxxxxxxx léčivých xxxxxxxxx xx xxxxxxxxx xxxxxxxxxxxxxx řetězce. Xxxxx xxxxx xxxxxx xxxxxx xxxxxx xxxxxxxxx mezi Xxxxxxxxxx ředitelstvím xxx x Xxxxxxx xxxxxxx xxx xxxxxxxx léčiv x xxxxxxx léčivých xxxxxxxxx, ale xxxx xxxxxxxx xxxxx. Přitom xxxxx správné xxxxxxxxx xxxxxx x xxxxxxxxx xxxxxx xxxxxxxxx x xxxxxxxxx xxxxxxxxxx xxxxx xxxx xxxxxx xxxxxx xxxxxx umožní xxxxxxxx xxxxxxx ve vstupu xxxxxxxx xxxxxxxxx a xxxxxxxx xxxxx, xxxxx xxxxxxxxxxxx požadavkům na xxxxxxx xxxxxxxx x xxxxxx EU.
1.3.5. Prokazování xxx inspekční činnosti x xxxxxx xxxxxxxxx xxxxxxxxx x xxxxxxx xxxxxxxx xxxxxxxxx
Xxx popisu xxxxxxxxxxxx xxxxxxxx xxxxx xx xxxxx poukázat xx nejednotnou x xxxxxxxxxxxx úpravu xxxxxxxxxxx xxxxxxxxxx xxx xxxxxx xxxxxxxxx xxxxxxxx, xxxxx xxxxx xxxxxxxx xxxxxxxxxx xxxxxx xxxxxxxx v xxxxx výkonu jedné xxxxxxxx podle xxxxxxxxxxx xxxx. Xxxxxxxxx se xxx xxxxxxxx xxxxx §4 xxxx. 3 xxxxxxxxxxx řádu xxxxxxxxx xxxxxxxxx, xxxxx xx xxxxx písemného xxxxxxxx x jednotlivé kontrole xxxx xxxxxxx xxxxxxxxxx, xxxxxxx-xx xxx xxxx xxxxxx předpis. Xxxxxx xxxxxxxxx x xxxxxx x xxx x xxxxxxx xxxxxxx xxxxxxxxxxx xxxxxxxxxx xxxxxx xxxxxx xxxxxx xxxxxxxx xxxx xxxx xxxxxxxx předpisů, xxx jen některé x nich stanovují xxxxxx xxxxxxxxxx xxxx xxxxx pověření xx xxxxxxxx podle příslušného xxxxxx. Xxx xxxxx xxxxx xxxxxxx x xxxxxx xxxxxxxx xx x xxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxx x operativní xxxxx xxxxxxxxxxx orgánu x xxxxxxx, kdy xx xxxxx xxxxxxx xxxxxxxx xxx xxxxxxxxxx xxxxxxx.
Xxxx xx třeba poukázat xx v xxxxxxxx xxxx xxxxxxxxxxxx xxxxxx xxxxxxxxx zajištění x xxxxxxx léčivých xxxxxxxxx, xxxxx neposkytují xxxxxxxxxx xxxxxxx xxx xxxxxxxx xxxxxxxxx xxxxxxx veřejného xxxxxx x xxxxxx xxxxxxxx x xxxxxxxx xxxxxxxx x xxxxxx, x xx xxxxxxxxx xx tržištích xxxx xxx nelegálním xxxxxxxxxxxx xxxxxxx. Xxxxxxxxx úprava xxxxxxxx x §101 xxxx. 5 xxxx. x) xxxxxx o xxxxxxxx xxxxx xxxxxx xxxxxxx, xxx s xxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxxxxx osoby. Xxxxxx xxxxxx xxxxxxxxx xx xxxxx xxxxxxxxx xx xxxxxxxxxxxx xxxxxx, xxxxx xxxx být zajištěna, xxx xxxxxxx xxxxx x xxxxxxxx xxxxxx x zdraví lidí x následně xxxx xxxxxxxxx xxxxxx xxxxxxxxx.
1.4. Xxxxxxxxxxxx dotčených xxxxxxxx
Xxxxxxxx xxxxxxxx xx xxxxxxxxxx xxxxxxxxx
Xxxxxxxxx xxxxxxxx xxxx xxxxxxxxx xxxxxxxxxx klinického xxxxxxxxx (farmaceutické xxxxxxxxxxx, xxxxxxx xxxxxxxxxxx, poskytovatelé xxxxxxxxxxx služeb, aj.), xxxxxxx xxxxxxxx organizace, xxxxxxxxxx, pacienti, xxxxxx xxxxxxxxxxxx, skutečné x xxxxxxxxxxx xxxxxxxx xxxxxxxxx, xxxxxxxxxxxxx xxxxxxxxxxx xxxxxx (xxxxx xxxxxxxxxx hodnocení), xxxxxxxx xxxxxxxxxx x xxxxxxxxxx xxxxxxxx přípravků.
Omezení xxxxxxxxx
Xxxxxxxxxxxx xxxxxxxx xxxxxxxxx, xxxxxxxxxxxxx xxxxxxx, xxxxxxxx xxxxxxxxxx x xxxxxxxxxx xxxxxxxx xxxxxxxxx.
Xxxxxxxx xxxxxxxx xx xxxxxx x xxxxxxx xxxxxx pro xxxxxxx xxxxxx xxxxxxxxx
Xxxxxxx xxxxxxxx xxxxx a xxxxxxxx rozhodnutí x xxxxxxxxxx xxxxxxxx xxxxxxxxx.
Xxxxxxxxxxxx XX
Specifické xxxxxxx:
- xxxxxxxx (xxxx x xxxxxxxxx, xxxxxxxx dospělých XX).
1.5. Xxxxx cílového xxxxx
1.5.1. Xxxxxxxx xxxxxxxx x xxxxxxxxxx hodnoceních xxxxxxxxx xxxxxxxx xxxxxxxxx
X xxxxxxxxxx xx xxxxx xxxxxxxx Evropského xxxxxxxxxx x Xxxx č. 536/2014 xxxxxxxxxxx xxxxx xxxxxx xxxxxx o xxxxxxxx xxxxxxx xxxxxxxxx cíl xxxxxxxxxxx x dosažení xxxx, aby xxxxxx xxxxxx v Xxxxx xxxxxxxxx vhodně xxxxxxxxx xxxxx provádění xxxxxxxxxx xxxxxxxxx humánních léčivých xxxxxxxxx založený xxx xxxxx Xxxxxxxxx xxxx xxxxxxxxx č. 536/2014. Xxxxx xx xxxxx xxxxxxxxxxx xx úpravu xxxxxxxxx xxxxxxxxxxx, xxxxxxx xxxxxx xx xxxxxxxxx xxxxx xxxxxxx, xx. Xxxxx xxxxxxxxx, xxxxxxx členský xxxx, nastaví následující xxxxxxx:
- stanoví příslušný xxxxx nebo orgány, xxxxx xx xxxxx xx xxxxxxxxx xxxxxxx x povolení xxxxxxxxxx xxxxxxxxx xxxxxxx, x xxxxxxx xxxxxxx x xxxxxxxxxx xxxxxxxx odpovídající xxxxxx xxxxxxxx xxxxxx x xxxxxx xxxxxxxx xx xxxxxxx stanovených x nařízení pro xxxxxxxxxx klinických xxxxxxxxx;
- xxxxxxx x xxxxxx xxxxxxx xxxxxxx xxxxxxxx xxxxx xxxxxxxxx xxxxxxxxx xxxxxxxxx x xxxxxxxxxxx x xxxxxx xxxxxx xx xxxxxx xx xxxxx daného xxxxxxxxx xxxxx;
- xxxxxxx xxxxxxxx xxxxxxxxx xx xxxxxxxxxxx xxxxxxxxxx xxxxxxxxx;
- xxxxxxx x potenciálním subjektem xxxxxxxxx by měl xxx proveden xxxxxx xxxxxxxxxx xxxx odborně xxxxxxxxxx xxx tento xxxx xxxxx vnitrostátních xxxxxxxx xxxxxxxx v xxxxxxxx xxxxx, x xxxx xxxxx probíhá;
- xxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxx xxxx xxxxxxx xxxxxx, xxxxx xxxx x xxxxxxx xxxxxxxxxxxx xxxx xxxxxxxx xxxxxxxxxx;
- xxxxxxx dohled xxx xxxxxxxx klinického hodnocení, xxx xxx xxx x xxxxxxx s xxxxxxxxx, dále zajistí xxxxxxxxx inspekcí a x xxxx xxxxxxxxxxxx xxxxxxxxx xxxxxxxx, xxxxxxx xxxxxxxx xx xxxxxxxxxx xxxxx xxxxxxxxx nařízením;
- xxxxxx xxxxxxxx na xxxxxxx xxxxxxxxxx hodnocení xxxxxxxxxxx xxxxxxxxxxxx xxxxxxxxxx x xxxxx xxxxxxxxxxx xxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxx xxxxxxxxxxxx zadavatelů x xxxxx xxxxxxx xxxxxx výzkumu.
Cílem xx, xxx úprava xxxxxxxx x xxxxxxxx a x zákoně xxxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxx xxxxxx xxx optimální xxxxxxxxx xxxxxxxxxx hodnocení. Xxxxxxx dosavadní xxxxx xxxxxx x xxxxxxxx xx xxxxxxxx xxx, xxx xxxxxxxxxx zákona xxxxxxxxxxx xxxxxx úpravu xxxxxxxxx v nařízení.
1.5.2. Xxxxxxxx xxxxxxxxx k xxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx
Xxxxx xxxxxx xxxxxx xx xxxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx xxx xxxxxxx pacientů x Xxxxx xxxxxxxxx, které xxxx xxxxx xxxxxxxx xxxxx xxxxxxx xxxxxxxxxx. Xxxxxx zajištění xxxxxxxxxxx xxxxxxxxxx léčivých xxxxxxxxx xx xxxxxxxxxx xxx xxxxxxxxxxx xxxxxxxxx xxxx. Xxxxx xxxxxx xxx xx xxxxxxxxx xxxxxxxx xxxxxxxxx péče v Xxxxx republice.
Návrh xxxx xxxxxx xxxxxx xxxxxxxxxxxxx xxxxxxxx přípravků xxx xxxxxxx xxxxxxxx x Xxxxx xxxxxxxxx xx xxxxxx xxxxxxx xxxxxx xxxxxx x xxxxxx, x to vytvořením xxxxxxx sledování x xxxxxxxxxxxxx xxxxxx nedostupnosti xxxxxxxx xxxxxxxxx xxx xxxxxxx pacientů v Xxxxx xxxxxxxxx x xxxxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxxxx distribuci xxxxxxxx xxxxxxxxx xxxx xxxxx Xxxxx xxxxxxxxx x xxxx xxxxxxxxx, xxx xxxxxxxxxxx xxxxxx xxxxxx xxxxxxx takových xxxxxxxx xxxxxxxxxx. Záměrem xx xxxxxx co xxxxxxx xxxxxxx xxxxxxxxxxxxxx subjekty x xxxxxxxxxxx xxxxxx xxxxxxx xxxxxx xxxxx xxxxxxxxxx v xxxxxxxxxx Xxxxxxxx xxxx a xxxx x judikatuře Xxxxxxxxxx xxxxxxxx xxxxx.
Xxxxxxx xxxxxx xx xxxx xxxxxx xxxx, kdy xx nevyskytne situace, xxx xx xxx xxxxx xxxxxxxx x XX nebyly xxxxxxxxx xxxx, které xx xxxxxxx xxx nahrazeny xxxxx xxxxxxx xxxxxxxxxx xxxx jsou xxxxxxxx x xxxxxx xxxxxx xx xxxxxxxx xxxxxxx xxxxxxxxx xxxxxx. Cílovým xxxxxx xx xxxx xxxxxx xxxx, xxx xxxxxxx xxxxxxxx x Xxxxx xxxxxxxxx xx xxxxx léčivých xxxxxxxxx xxxx x xxxxxxx xxxxxxxxxxxxx xxxxxxxxx xx xxxxxx xx stavu xxxxxxxxxx dostatečně uspokojena.
1.5.3. Xxxxxxxx xxxxxxxx xx xxxxxx k xxxxxxx xxxxxx xxx humánní xxxxxx xxxxxxxxx
Xxxxxxx xxxxxx xx xxxx xxxxxxxx xxxxxxxx nařízení Xxxxxx x přenesené xxxxxxxxx (XX) č. 1252/2014 xx xxx 28. xxxxxx 2014 xxxxxxxxxx xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Xxxx 2001/83/XX, xxxxx xxx x xxxxxx x xxxxxx xxxxxxx xxxxxxx praxe xxx xxxxxx látky pro xxxxxxx léčivé xxxxxxxxx.
1.5.4. Xxxxxxxxxx Xxxxxxxx xxxxxx xxx xxxxxxxx léčiv x Generálního ředitelství xxx
Xxxxxxx xxxxxx xx xxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxx Xxxxxxxx ústavu xxx xxxxxxxx léčiv x Generálním ředitelstvím xxx xx xxxxxx xxxxxxxxxxxx padělků xxxxx x xxxxxxxxx nakládání x xxxx.
1.5.5. Prokazování xxx xxxxxxxxx xxxxxxxx x xxxxxx xxxxxxxxx xxxxxxxxx x xxxxxxx xxxxxxxx přípravků
Cílovým xxxxxx xxxxxx posledního xxxxxx xxxxxxxx xx xxxxxxxx, xxx s léčivy xxxxxxxxxxx xxxxx neoprávněné x xxxxxxxx xxx xxxx xxxxxx (s xxxxxxx xx xxxxxxxxxx xxxxxxxxx xxxxxxxx přípravků, xxxxxxx xxxxxxxx xxxxxx xxxxx vliv na xxxxxxxxxxxx xxxxxx) xxxxxxxx xxxxxxxx.
Xxxxx xx účelněji xxxxxxx xxxxxxxxxxx při xxxxxxxxx xxxxxxxx x xxxxxxxx xxxxxxx xxxxxx xxxxxxxxx zajištění a xxxxxxx xxxxxxxx přípravků xxx, aby byly xxxxxxxxxx x xxx xxxxxx xxxxxxx, kdy xx xxxxxxxx, xx x xxxx xxxxxxxxx xxxxx, xxxxx x xxxx xxxxxx xxxxx xxxxxx xxxxxxxxx.
1.6. Xxxxxxxxxx xxxxxx
1.6.1. Xxxxxxxx xxxxxxxx x klinických hodnoceních xxxxxxxxx xxxxxxxx xxxxxxxxx
Xxx xxxxxxxxx xxxxxxxxxx stavu xx x xxxxxxxx xxxxxxx xxxxxxxx Evropského xxxxxxxxxx x Rady č. 536/2014, což xxxxxxx xxxxxxxx xxxx 28. xxxxxx 2016, vznikla xxxxxxxx xxxxxxxx situace, xxx by záležitosti xxxxxxxxxx xxxxxxxxx humánních xxxxxxxx xxxxxxxxx zůstaly xxxxxxxx x xxxxxx x léčivech, x xxxxxx xx současně xxxxxxx úprava xxxxxxxx x nařízení, která xx v xxxxxx xxxxxxxx xxxxx přímo xxxxxxxxxx. Z xxxxxxxxx xxxxxx xx xxxxx xxxxxxx xxxxx zákona x léčivech xxx, xxx bylo xxxx xx souladu x xxxxxxxxx xxxxxxxx, xxxx. xxxxxxxx xxxxxxxxx dle xxxxx nařízení č. 536/2014 xxxx pouze povolována, xxxxxxx dle současného xxxxx xxxxxx x xxxxxxxx xxxx xxxxxxxx xxxxxxxxx povolována x xxxxxxxxxx; dle xxxxxx x léčivech xxxx xxxxxxxx xxxxxx xxxxxx xxxxxxxxx xxxxxxxxxxxxx zdravotních xxxxxx, xxx xxxxxxx xxxxxx závislost xx xxxxxxx xxxxxxxxxx xxxxxxxxx x mnohdy i xx xxxxxxxxxxxx. Xxxx xxxxxxxx č. 536/2014 stanovuje xxxxxxxxx xx xxxxxxxx xxxxxxxxxx žádostí xxxxx xxxxxxxxx xxxxxxxxx státy, xxx xxxxxxxx xxxxx xxxxxx x xxxxxxxx xxxxx. Xx xx xxxx xxxxxxxx xxxxxx, x xxxxxxxxxxx xx xxxx u multicentrického xxxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxxxxxxx etická komise x xxx xxxxxxxxxx xxxxx xxxxxxxxxx xxxxxxxxx x xxxx xxxxxx xxxxxx komise x xxxxx vybírá xxxxxxxx. X xxxx uvedeného xxxxxxx, xx současná xxxxxx xxxxxx by xx dostala do xxxxxxx x požadavky xxxxxxxx č. 536/2014.
Xxxxxxxxx klinických xxxxxxxxx na xxxxx XX xx xxxxxx x xxxxxxx xx xxxxxxx xxxxxxxx xxxxx xxxxxxx, xxxxx xxxx xxxxxxxxx členskému xxxxx, xxxxx.
Xxxxxxxxx situace xx xxxxxxxxx problémy xxxxxxxxx xxxxxxxxx hodnocení, xxxxxxxxxxx x xxxxxxxxxxx, ale x České xxxxxxxxx, xxxxx xx xxxxxxx xxxxxxxxxxx xxxx xxxxxx xxx komunitárnímu xxxxx. X xxxxxx důvodu xxxxx xxxxx xxxxxx xxxxxxx připustit. Xxxxxxxxxx xxxxxxx xx xxxx x to, xx xxx nejasné situaci xx zadavatelé xxxxxx xxxxxxxx od xxxxxxxxx xxxxxxxxxx xxxxxxxxx na xxxxx Xxxxx xxxxxxxxx, xxx by mohlo xxx xxxxxx na xxxxxxxx. V úvahu xx třeba xxxx x xxxxxxxxx finanční xxxxxx xx poskytovatele xxxxxxxxxxx xxxxxx x xxx předpokládat x xxxxxxxxx xxxxx xx xxxxxxxxxxxxx xxxxxxxxx - xxxxx xxxxxxxx, xxxxx xxxxxxxxx xxxxxxxxx klinického xxxxxxxxx - xxxxxxx xxxxxxxx xxxxxxxxxx xx xxxxxxxx xxxxxxxx farmaceutických xxxxxxxxxxx.
1.6.2. Xxxxxxxx směřující x xxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx
Xxx xxxxxxxxx xxxxxxxxxx xxxxx by x nadále xxxxxxxx xxxxxxx, kdy pro xxxxxxx pacientů x Xxxxx republice xx xxxxxx xxxxxxxx xxxxxxx xxx xxxxxxxxxxx xxxxxxxxxxx xxxxxx významné xxxxxx xxxxxxxxx x xxxx xxxxxxxxxxxx by xxxx xxxxxxxxx xxx, že xxxx na xxxx xxxxxxx xxxxxxxx x Xxxxx republice xxxxxxxxxxxxx xxxx xxxxx České xxxxxxxxx. Hrozilo xx xxxx riziko xxxxxxxxxxx x xxx, xx xxxxxxx xxxxxxxx x Xxxxx republice, pokud xxx x xxxxxxxxxx xxxxxxxxx xxxxxxxx přípravků, xxxxxx pro xx xxxxxxxx xxxxxxxxxx. Xxxxxx xx xxxxxx přímý xxxxx xx xxxxxx xxxxxxxx x xxxxxxxxxxx x xxxxxxxxxx léčivými xxxxxxxxx, které xxxx xxxxxxxxxxxxx.
1.6.3. Xxxxxxxx xxxxxxxx xx vztahu k xxxxxxx látkám pro xxxxxxx xxxxxx xxxxxxxxx
Xxx xxxxxxxxx xxxxxxxxxx stavu xx xxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxx Xxxxxx v xxxxxxxxx pravomoci (XX) č. 1252/2014 xx xxx 28. xxxxxx 2014 xxxxxxxxxx směrnici Xxxxxxxxxx xxxxxxxxxx a Xxxx 2001/83/XX, xxxxx xxx x zásady x xxxxxx správné výrobní xxxxx pro léčivé xxxxx pro xxxxxxx xxxxxx přípravky. Xxxxxx xxxxxxx by xxxxx xxxxxxx x xxxxxx xxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx Evropské xxxx xxxx Xxxxx xxxxxxxxx.
1.6.4. Xxxxxxxxxx Xxxxxxxx xxxxxx xxx xxxxxxxx xxxxx a Xxxxxxxxxxx xxxxxxxxxxx xxx
Xxxxxxxxx současného xxxxx xx xxxx xxxxxxxxx prodlužování xxxxxxxxxxxx xxxxxxxxxx Xxxxxxxx xxxxxx xxx kontrolu xxxxx x Xxxxxxxxxxx ředitelství xxx x xxxxxxxxxxxx xxxxxxxx xxxxx, xxxxx xx xxxxxxxxxxxxxxx neúplnou xxxxxxx informací xxxx xxxxxx xxxxxx. Xxx xx zabraňuje tomu, xxx xxxx xxx xxx zbytku xxxxxxx xxxxx xxxxxxxx Xxxxxxxxxx xxxxxxxxxx a Xxxx 2011/62/EU, xxxxxx se xxxx xxxxxxxx 2001/83/ES x xxxxxx Xxxxxxxxxxxx xxxxxxxxx se xxxxxxxxx xxxxxxxx xxxxxxxxx, pokud xxx x xxxxxxxxx xxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx xx legálního xxxxxxxxxxxxxx xxxxxxx. Rizikem xxxxxxxx x odkládání xxxxxx problému xx xxxx xxxxxxxxx xxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx xx xxxx x xxxxxxxx xxxxxxxxx x Xxxxx republice x xxxxxxx použití léčivých xxxxx xxxxxxxxxxxxxx kvality xxx xxxxxx xxxxxxxx xxxxxxxxx.
1.6.5. Prokazování při xxxxxxxxx činnosti x xxxxxx xxxxxxxxx zajištění x xxxxxxx xxxxxxxx xxxxxxxxx
Xxxxxxxxx xxxxxxxxxx xxxxx xx xxxxxx znamenalo xxxxxxxxxxx ve xxxxxx xxxxxxxx xxxxxxx, xxx xx xxxxx xxxxxxxx xxxxxxxxxx xxxxxx xxxxxxxx x xxxxx xxxxxx xxxxxxxx xxxxx kontrolního xxxx, xxx x xxxxxxxx xxxxx existující xxxxxxxxxx a xxxxxxxxxxx xxxxxx xxxxxx xxxxxxxxxxx xxxxxxxxxx při xxxxxx xxxxxxxxx xxxxxxxx dochází x xxxxxxxxxxx xxxxxxxxxxx xxxxxxxxx ke kontrole x rámci jedné xxxxxx xxxxxxxx. Xxxxxx xx nedošlo k xxxxxxx x xxxxxxxx xxxx xxxxxxxx xxxxxxxxxxxxxx xxxxxxxx xxxxxxxxx zajištění x zabrání xxxxxxxx xxxxxxxxx, které xxxxxxxxxxx xxxxxxxxxx xxxxxxx xxx xxxxxxxx efektivní xxxxxxx xxxxxxxxx xxxxxx a xxxxxx xxxxxxxx x xxxxxxxx xxxxxxxx x xxxxxx, x xx xxxxxxxxx na xxxxxxxxx xxxx x xxxxx xxxxxxxxxxx xxxxxxxxxxxxx xxxxxxx. Xxxxxxx xxxx xx, xx xx xxxxxx x xxxxxxxxx xxxxxxxxx xxxxxxxx, xxxxx xx xxxxxxxxx xxxxxx takových xxxxxxxx xxxxxxxxx, které xxxxxxxxxx xxxxxxxxxx xx xxxxxx xxxxxx, xxxxxxxx x bezpečnost.
2. Xxxxx xxxxxxx řešení
Vzhledem x xxxx, xx xxxxxxxxxxxx xxxxxxx v návrhu xxxxxx xxx xxxxxxxxx xx xxxx xxxxxxxx xxxxxxxxxxxx xxxxx (xxxxxxxx xxxxxxxx xx klinickému xxxxxxxxx x xxxxxxx xxxxxxxxx), xxxx tyto xxxxx řešeny x xxxxxxxxxxxx xxxxxxx xxxxxxx, x to xxx xxxxx těchto xxxxxxx, xxxxxx xxxxxxx xxxxxxxx x xxxxx těchto xxxxxxx, jejich xxxxxxxxx xxxxxx x xxxxxxxxxxx, xxx požadavků metodiky xxx xxxxxxxxxxxxx dopadů xxxxxxxx.
Xxxxxxxxxxxxx xxxxxxxx: Xxxxx xxxxxxxx - xxxxxx x xxxxx xxxxxxxxxxx
X xxxxx xxxxxxxxxxxxx xxxxxxxxxxx xxxxxxxxxxx varianta 1 - xxxxxx xxxxxxxxx xxxxxxxxxxx stavu, xxxx x xxxxxxxxx xxxxxxxxxxx xxxxxx na xxxxxxx xxxxxxxx x xx xxxxxxxxxxxxx xxxxxxxxx. Xxxxxxx xxxx xxxxx neřeší xxxxxxxxxxxxxx xxxxxxxx, xxxx. xxxxxxx, xxx xxxxxxxx xxxxxxx xxxxxxxxxx xxxxxxx xxx xxxxxxxxx nařízení xxxx v xxxxxxx xxxxxxxxx, jak je xxxxxx za účelem xxxxxxxxx xxxxxxxxxxx xxx xxxxxxx xxxxxxxx v XX xx xxxxxx xxxxxxx xxxxxx xxxxxx, x xxxx by xxxx xxxxxxxxxxxx xxxxxxxxxx xxxxxxxxxxxxxx xxxxx. Xxxx xxxxxxxx xxxxxxxxxxxxx xxxxx xxxxxxxx xxxxxxx xxx xxxxx nákladů xxxxxxxxxx, xxxxx ani xxxxx xxxxxxx, xxxxxxx by xxxx možno dosáhnout, xxxx. xxxxxx xxxxxxx xxxxxxxxxxxx x oblasti xxxxxxxxx xxxx xx xxxxx v důsledku xxxxxxxxx chybějících xxxxxxxxxx xxxxx na xxxx xxxx jinými xxxxxx, xxxx xxxxx xx xxxxxx xxxxx xxxxxx xxxxxx přípravky x xxxxx xxxxxxxxxx xxxxxxxxx.
2.1. Xxxxxxxx xxxxxxxx x xxxxxxxxxx xxxxxxxxxxx humánních xxxxxxxx xxxxxxxxx
Xxxxxxxx xxxxxxx
Xxxxxxxx 1 - xxxxxx
Xxxxxxx xxxxxxxxx xx xxxxxx xxxxxxxxxxxx xxxxxx novely xxxxxx x xxxxxxxx. Xxx xxxxxxxxx současné xxxxxx xxxxxx xxxxxxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxx přípravků v xxxxxx x xxxxxxxx xx x Xxxxx xxxxxxxxx nedošlo x xxxxxxxx adaptaci xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Xxxx č. 536/2014, xxx xx xxxxx xxx xxxxxxx xxxxxx Evropské xxxx jako xxxxxxxx xxxxx, na kterých xx xxxxxxxxx Xxxxxxxx xxxx xxxxxxxx. Xxxxx x xxxxxxx klinických xxxxxxxxx xxxxxxxxx nařízením Xxxxxxxxxx xxxxxxxxxx x Xxxx č. 536/2014 xxxx xxxxxxx od xxxxxxxx xxxxxx xxxxxxxxxx hodnocení xxxxxxxx x zákoně č. 378/2007 Sb., x xxxxxxxx x o změnách xxxxxxxxx xxxxxxxxxxxxx xxxxxx (xxxxx x léčivech), xx xxxxx pozdějších xxxxxxxx. Nulová xxxxxxxx xx v xxxxx xxxxxxxxx xxxxx xxxxxxxxxxx xxxxxx a xxxxx xx x xxxxxx xxxxxxxxxx xxxxxx úpravy, xxxxx xx ve xxxx xxxxxxxx mohla xxxx x xxxxxxxxxx x povolování xxxxxxxxxx xxxxxxxxx x xxxxxxx x xxxxxxxxx, xxxxxxxx xxxxx xxxxxxxxxx xxxxxxxxx x Xxxxx xxxxxxxxx. Xx xx xxxxx xxx xxxxxxxx uvedené xxx x bodě 1.6.1., xxxx xxxxxxx xxxxx xxxxx pro xxxxxxxx dostat xx x xxxxxxxxxx x xxxxxxxxxxxx xxxxx, xxxx xxxxxxx finančních xxxxxx xxx xxxxxxxxxxxxx zdravotních xxxxxx, xxxxxxx xxxxxxxx xxxxxx xxxxxxxxxxxxx x xxxxxxxxxxxx xxxxxxx x xxxxxxxxx xxxxxxxxxxxxxxx xxxxxxxx, xxxxxxxxxxxxx x xxxxxxx xxxxxxxxxx hodnocení (x xxx xx xxxxxxxx x xxxxx negativní xxxxxxxx - xxxxxx xxxxxx xxxxx xxxxxxxxxx xxxx na xxxx xxxxx).
Xxxxxxxxxxx nákladů x xxxxxxx xxxxxxxx
Xxxxxxxx 1 (xxxxxx) xxxx xxxxxxx x žádným xxxxxxxxx xxxxxxxx. Xxxxxx xxxx xxxxxxx xx xxxx xx xxxxxxxx značné xxxxxxxx xxx xxxxxxxxx xxxxxxxx xxxxxxxx Evropského xxxxxxxxxx x Xxxx (XX) č. 536/2014 x x případný finanční xxxxxx xx xxxxxx xxxxxx Xxxxxxxx xxxx. Xxxxxx varianta xx xxxx i případný xxxxxxxxx finanční dopad xx xxxxxxxxxxxxx xxxxxxxxxxx xxxxxx, kteří xxxxxxx xxxxxxxx xxxxxxxxx, x xx z xxxxxx&xxxx; xxxxxxx xxxxxxxxxx x xxxx ke snížení xxxxx prováděných xxxxxxxxxx xxxxxxxxx x&xxxx; Xxxxx xxxxxxxxx, negativní xxxxxxxx xxxxx xx podnikatelské xxxxxxxx x xxxxxxx xxxxxxxxxx xxxxxxxxx (XxxxxxxxXxxxxxxxXxxxxxxxxxxx, xxxxxxxxxxx xxxxxxxxxx xx xxxxx xxxxxxxxxx xxxxxxxxxx xxxxxxxxx), xxxxxxxxx xxxxx xx xxxx x xx xxxxxxxx, xxxxx xx xx tak xxxxxxxxx xxxxxxxxx x xxxxxxxxxxx léčbám, k xxxxxxxx xxxxxxxxx efektivní x cílené xxxx xxxxx, a xxxxx xxxxx xxxxxxxxxxxxxxx xxxxxxx xxxxxxxxxx, x xxxx xxx x xxxxxxxx xxxxx pacientům xxxxxx xxxx, kam by xxxxxxxxxx s xxxxxxxxx xxxxxxxxxx hodnocení xxxxxx.
Xxxxxxxx 2 - xxxxx xxxxxxx xxxxxx
Xxx xxxxxxx xxxxx, která xx xxxxx vést xx xxxxxxxxxxx xxxx, xxxx xxxxxxxxx xxxxx xxxxxxxxxxx xxxxxx v podobě xxxxxxxxxxxxxx xxxxxxxxx. Důvodem xx xxxxxxxxxx, xx xxxxxxxxxxxxxx xxxxxxx xx xxxxx (x ohledem xx xxxxxxx xxxxxxxx xx právního řádu) xxxxx xxxxx xxxxxxxxxxxx xxxxxx.
Xxxxxxxxxxx xxxxxxx a xxxxxxx varianty
Varianta 2 xxxxxxxxxxx v xxxxxxxxxxxx xxxxxx xxxxxx, kterým xx xxxx zákon x léčivech, xxxxxxxxxxxxx, xx xx x xxxxx přijetím xxxx xxxxxxx xxxxx finanční xxxxxxx xxx xxxxxx xxxxxxxxxxxxx, xxxxxxxxxxxxxx xxxxx xxxx xxxxxxx xxxxxxxxx x Xxxxx xxxxxxxxx. Xxxxxx xxxxxxxx xxxxxxx xxxx Xxxxx republika xxxxxx, xxx je xxxxxxx v xxxx 3.2. Xxxx xxxxxxx xx mohly xxx xxxxx x mimorozpočtových xxxxxxxxxx, xxxxx xxxxxxx xxxxxxxx xxxxxxxx systém xxxxxxxxxxx, a případně xxxxxxxx x x XX xxxxx v xxxxxxx, xx se xxxxxx xxxxxx xxx xxxxxxxx xxxxxxxx evropskou xxxxxxxxx xxxxxxx.
Xxxxxxxx variant x xxxxx xxxxxxxx 2
Xxxxxxxxx x tomto xxxxxxx xxxx xxx xxxxxxxx - x xx
Xxxxxxxx x = xxxxxx xxxxxx x xxxxxxxx
Xxxxxxxx b = xxxxx xxxx xxxxx xxxxxxxx pouze xxxxxxxxxx xxxxxxxxx xxxxxxxxx léčivých xxxxxxxxx.
Xxxxxxx x xxxxxxx xxx xxxxxxxxxx xxxxxxx xxxxxxxx
Xxxxxxxx x
X xxxxxxxxxxxx xxxxxxxxxxx xxxxxxxx není xxx účely závaznosti xxxxxxxx, xxx xxxx xxxxxx xxxxxxx do xxxxxx xxxxxx či xx již xxxxxxxxx xxxxxxxxxxx.
Xxxxxxxx x
X xxxxxxxxxxxx xxxxxxxxxxx xxxxxxxx není xxx účely xxxxxxxxxx xxxxxxxx, xxx xxxx xxxxxx xxxxxxx do xxxxxx xxxxxx xx xx xxx stávající xxxxxxxxxxx.
Xxxxxxxx xxxxxx variant
Při xxxxxx xxxx xxxxxxxxx xxxxxxx (a xx x) xxxx xx xxxxxx kritérium xxxxxxx xxxxxxxxxxx x xxxxxxxxxxxxxx xxxxxx úpravy. Z xxxxxx xxxxxxxx xxxx xxxx xxxxxxxx xxxxxxxxx xxxxxx xxxxxx do xxx xxxxxxxxxxx xxxxxxxxxxxxxx xxxxx x xxxxxx x xxxxxxxx, xxxxx xx xxxxxxxxx xxxxxx xxxxxxxxxxxx xxxxxxxx xxxxx xx území XX. Xxxxx xxxxxxx xxxxxx xxxxx, proč by xxxxxxx xxx xxxxxx xxxxxx včleněna do xxxxxx o xxxxxxxx.
Xxxxxxxx 2 předpokládá přípravu x xxxxxxxxxx nového xxxxxx, xxxxxx xx xxxxx k úpravě xxxxxxxxxxx znění xxxxxx x xxxxxxxx tak, xxx jeho xxxxxxxxxx xxxxxxxxxx xx xxxxxxxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxxxx xx xxxxx použitelnou xxxxxx obsaženou v xxxxxxxx č. 536/2014.
Bylo upřednostněno xxxxxxxxx návaznosti xx xxxxxxx xxxxxx úpravu xxxxxxxxx x zákoně x xxxxxxxx xx xxxxxx xxxxxxxx, xxxxx xxxxx komplexní xxxxxx xxxxxx xxxxxxxx přípravků. Xxxxxxxxx byla zúžena xxxxxxx právní úprava. Xxxx proto zvolena xxxxxxxx xxxxxx xxxxxx xxxxxx x léčivech.
Právní xxxxxx xxxxxxxx xx xxxxxxxx komisí
Nařízení Evropského xxxxxxxxxx a Xxxx (XX) č. 536/2014 ponechává xxxxxx xxxxxxxxxx x xxxxxxxx xxxxxxxx xxxxxx x xxxxxxxxxx xxxxxxxxx xxxxx. Při přípravě xxxxxx xxxxxx, xxxxx xx xxxxxxxxxxx xxxxxxxxx xxxxx x xxxxxxxx, xxxx tedy xxxxxxxxx x xxxxxxx xx xxxxx xxxxxxx x xxxxxxxx hodnocení a xxxxx xxxxxxxxxxxxx klinických xxxxxxxxx xx xxx xxxxxxx xxxxxx komise xx xxxx xxxxxxx
1. xxxxx etických xxxxxx: xxxxx xx více x
2. xxxxxxxxxx etické xxxxxx.
X současné xxxx xxxx xxxxxx xxxxxx xxxxxxx u xxxxxxxxxxxxx xxxxxxxxxxx xxxxxx, a xxx xxxx v xxxxxxxx xxxxxx x xxxxxx xxxxxxxxxx xxxxxxxxx x mnohdy x xxxxxxxxxxx. Vztah xxxxxxxxxx xxxx xxxxxxxx neumožňuje.
Definice xxxxxxx ohledně počtu xxxxxxxx xxxxxx
Xxxxxxxx 1 = jedna etická xxxxxx
X České xxxxxxxxx xx byla xxxxxxx xxxxx xxxxxx xxxxxx xxxxxx.
Xxxxxxxx 2 = xxxx&xxxx; etických komisí
V Xxxxx xxxxxxxxx xx xxxx xxxxxxx více xxxxxxxx komisí.
Varianta 3 = xxxxxxxxxxx, xxxxx xxxxxx xxxxxx x xxxx samostatně xxxxxxxxxxx xxxxxxxxx
Xxxxxxx x xxxxxxx xxx jednotlivé xxxxxxx xxxxxxxx
Xxxxxxxx 1
Xxxxxxxx by xxxx xxxxxx řešení x hlediska spolupráce x xxx x xxxxxxxxx xxxxxxxxxx xxxxxxxxxxx xxxx xxx xxxxxxxx xxxxxx komise, xxxxx xx xxx xxxxxxxx č. 536/2014 xxxxxx členského xxxxx. Xxxx zajištění xxxxxxxxx xxxxxxxx xxxxxxxx x posuzování x xxxxxxxxxx xxxxxxxx xxxxxxx, xxxxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxxxxxxx dokumentace k xxxxx I, xxxxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxx x xxxxxxxxxxx úkolů (xx. posouzení žádostí, xxxxxxx, xxxxxxxxx průběhu xxxxxxxxxx hodnocení). Xxxx xxxxxxxxx xxxxx xxxx xxxxxxxx xxxxxx xxx xxxxxxxx xxxxxxx xxxxxxx xxxxx členů, xxx xxxxxx komise xxxxxxx xxxxx agendu. Xxxxx xxxxxx xxxxxx xxxxxxxx xxxxx xxxxxx xxxxx Xxxxxx xxxxxxxxxx, a xx xxx x xxx xxxxxxxxxxx, tak x xxxxx xxx xxxxxxxxxxxxxx xxxxxxxx, (xxx xxxxxxxx xxxxxxxx č. 536/2014) x zajistili xxxxxx xxxxxxx se xxxxxxx, xxxxxxxxxxx a xxxxxxxxxx xxxxxxxxxx xxxxxxxxx, xxxxxx xxxxxxxxx a dodatky, xxx xx byla xxxxxxx etické xxxxxx xxxxxx xxxxx Xxxxxx xxxxxxxxxx velmi složitá x zajistit xxxxxx xxxxx xx setkáních, xxxxx xxxxx xxxxx xxxxxxxx x xxxxxxxx xxxxxxxxxxx xxx tomu xx xxxxxxx, cca 1x týdně, xxxxx xxxxxxxx. Získání členů xxxx etické xxxxxx xx xxxxx současných xxxxxxxx komisí by xxxx xxxxxxx pro xxxxxxx xxxxxxx xxxxxx xxxxxxxxxx x xxxxxxxx xxxx problematiky.
Varianta 2
Xxx xxxxxxx xxxx etických xxxxxx xxx očekávat xxxxxxxx zachovat obdobu xxxxxxxxxx xxxxx fungování xxxxxxxxxxxxxxxx xxxxxxxx xxxxxx, xxxxx ale xxxxxxxx xxxxxxxxxx xxxxxxxx č. 536/2014 x xxxxxxxxxxxx etické xxxxxx xx xxxxx xxxxxxxxxx xxxxxxxxx a xxxxxxxxxxxx. Při xxxxxxxxxxx xxxxx dnešních multicentrických xxxxxxxx komisí xxx xxxxxxxxxxx, že x xxxx domluvu xx xxxxxx nedodržují dohodnuté xxxxxxx a xxxxxxxxx xx xxxxxxxxx přístupu x xxxxxxxxxx xxxxxxxxx (xxxxx požadavky na xxxxxxxxx, xxxxx xxxxxxxx, xx xx x xxxx klinické xxxxxxxxx, xxxxxx sjednocených formulářů). Xxxxx je snahou, xxx nový systém xxxxxxxx xxxxxx x xxx využití stávajících xxxxx xxxxxxxx komisí, xxxxxxxx xxxxxxxx členů x xxxxxxx stávajících xxxxxxxx xxxxxx x xxx xxxxxxxx xxxxxxxxxxx xxxxxxxx „xxxxxxx“. Xxxxx xxxxx xxxxx není xxx zadavatele xxxxxx xxxxxxxxxxxxx. Xxxxxxxxx xxxxx xxx i xxxxx xxxxxxxxx xxxxxxxxx a xxxxxx xxxxxxxxx přijetí xxxxxxxxxx xx xxxxx Xxxxxx xxxxxxxxx. X xxxxx xxxxxxxx xxxxxxxxxxxxxxx, xxxxxxxxxxxxxx a xxxxxxx xxxxxxxxxx xxxxxxxxxxxxxxx, xx xxxx varianta xxxxxxx xxxxx xxxxxxxx xxxxxx xxxxxxxxxx.
Xxxxxxxx 3- xxxxxxxxxxx
Xxxxxxx x přínosů xxxx xxxxxxxxxxx xxxxxxx, xxxxx xxxxxx xxxxxx x xxxx skupinami. Zvolená xxxxxxxx xxxxxxxxxxx záruku xxxxxxxx xxxxxxxx x xxxxxxxxx xxxxxx, xxxxx xxxxx xxxxxxxxxx xxxxxxx, xxxxxxxx xxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxxx x xxxxxxxx xxxxxx xxxxxxxx xxxxxxx xxxx jednotné xxxxxxxxxx xxxxxxxx xxxxxxxxxxxx xxxxxx (xxxxxxx xxxxxxxxxx xxxx x jednotných xxxxxxx) x xxxxx xxxxxxxxxxx, xxxxxxxxxx xxxxxxxxx xxxxxx xxx činnost xxxxxx xxxxxx x xxxxxxx xxxxxxxx xxxxxxxxxx xxxx xxx xxxxxxxxxxxx xxxxxx komise x xxxxxx xxxxxx xxxxxx xxxxxx xx xxxxxx xxxxxxxxx x xxxxxx xxxxxx za posouzení xxxxxxxxxx hodnocení. Xxxxxxx xxxxxxxxx xxxxxxxxxxxxxxx xxxxx xxxxxxxxx xxx ze xxxxxxxxxxxxxx xxxxxxxxxx xxxxxxx xxxxxxxxxxxxx xxxxxxxxxxx služeb, xxx i osob xxx zdravotnického vzdělání xxxxxxxx, xxxxx xxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxxx xxxxxxxxx č. 536/2014 x Xxxxxxxx II čl. 9.
Xxxxxxxx xxxxxx variant
Za xxxxxx xxxxxxxxx xxxxxx xxx xxxxxx xxxxxx x nařízením, jednotný xxxxxxx xxxxxxxx xxxxxx (xxxx xxxxx x xxxxxx xxxxxxxxx xxxxx) x efektivita xxxxxxxx xxxxxx komise.
Na xxxxxxx xxxx xxxxxxxxx kritérií xxxx xxxxxxx kompromisní xxxxxxxx 3, xxxxx xxxxxxx x xxxxx xxxx xxxx xxxxxxxxx xxxxxxx. Xxxxxxxxx xxxxxxxxx xx xxxxx xxxxxx xxxxxx s xxxx xxxxxxxxx. Xxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx stejného xxxxxxxx x xxxxxxxxx xxxxxx, xxxxx xxxxx xxxxxxxxxx xxxxxxx, xxxxxxxx xxxxxxxx povinnosti xxxxxxxx xxxxxxxxxx x xxxxxxxx xxxxxx xxxxxxxx xxxxxxx xxxx xxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxxxxx xxxxxx (xxxxxxx dodržování xxxx x jednotných formátů) x xxxxx xxxxxxxxxxx, xxxxxxxxxx xxxxxxxxx zázemí xxx xxxxxxx xxxxxx xxxxxx a možnost xxxxxxxx xxxxxxxxxx xxxx xxx xxxxxxxxxxxx etické xxxxxx x xxxxxx xxxxxx etické xxxxxx xx xxxxxx xxxxxxxxx x náhrad výdajů xx xxxxxxxxx klinických xxxxxxxxx. Xxxxxxx xxxxxxxxx xxxxxxxxxxxxxxx xxxxx xxxxxxxxx xxx xx xxxxxxxxxxxxxx xxxxxxxxxx xxxxxxx poskytovatelů xxxxxxxxxxx služeb, xxx x osob xxx xxxxxxxxxxxxxx xxxxxxxx xxxxxxxx, xxxxx zajistí xxxxxxxx xxxxxxxxx stanovených xxxxxxxxx x. 536/2014 v Xxxxxxxx XX čl. 9.
Xxxxxxxx xxxxxxx xxxxxxx xxxxxxxxxxx xxxxxxxx komisí
V současném xxxxxxx etických komisí, xxx jsou zřizovateli xxxxxxxxxxxxx zdravotních xxxxxx, xxxxx xxxxx zajistit xxxxxxxxxxx na xxxxx xxxxxxxxxx xxxxxxxxx x xxxxxxxxxxxx. Xx xx xxxx xxxxxx důvod xxxxxxxx xxxxx systému. Xxxxxxxxxx současných zřizovatelů xxxx xxxxxxxxx xxxxxxxxxxx xxxxxxxxxxx.
Xxxxxxxx 1 = xxxxxxxx xxxxxx xxxxxx/xxxxxx xxxxxx
Xxxxxxxx 2 = xxxxxxx xxxxxx xxxxxx/xxxxxxxx xxxxxx při xxxxxxxxxx xxxxxxxxx
Xxxxxxxx 3 = xxxxxxx xxxxxx komise/etických xxxxxx xxx xxxxxxxxx xxxxxxx
Xxxxxxxx 4 = xxxxxxx xxxxxx xxxxxx xxxx organizační složky Xxxxxxxxxxxx xxxxxxxxxxxxx
Xxxxxxxx 5 = xxxxxxx etické xxxxxx/xxxxxxxx xxxxxx xxxx xxxxxxxxx xxxxxx Xxxxxxxx xxxxxx pro kontrolu xxxxx
Xxxxxxx x přínosy xxx xxxxxxxxxx xxxxxxx xxxxxxxx
Xxxxxxxx 1
Xxxxxxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxx (xxx xxxxx xxxxxx členskému xxxxx, xxxxx xxxx xxxxxxxxx xxxx xxxxxxxxx xxxxx na Xxxxxx xxxxx pro kontrolu xxxxx, xx nejevilo xxxx xxxxxx xx xxxxxx xxxxx xxxx xxxxxxxxxx finanční prostředky xx činnost xxxxxxxxxx xxxxxxxx, xxxxxx xxxxxx xx nemohla požadovat xxxx xxxxxxxx, xxxxxxx xx xx xxxx x xxxxxxx x xxxxxxxxxx nařízení č. 536/2014 x jedné xxxxxx xxx xxxxxxx xxxx), xxxxxxxx xxx nespolupráci xx xxxxxx etické xxxxxx x xxxxxxxxx xx xxxxxxxxxx xxxxxxx; xxxxxx xxx x xxxxx, xxxx etická xxxxxx xx etické xxxxxx xx mohly xxx určeny xxx xxxx xxxxxxx x xxxxxxx xxxxx. xxxxxxxxxxxx xxxxxxx žadatelů. Nebyly xxxxxxxxxxxxxx žádné xxxxxxxxxx xxxxxxx vyplývající x xxxx xxxxxxxx.
Xxxxxxxx 2
Xxxxxxx xx xxxxxxxxxx xxxxxxxxx xx spojena x xxxxxxxxxxxxx xxxxxxxxxxx xxxxxx x akademičtí xxxxxxxxxx xxxx xxxxxxx lékaři - xxxxxxxxxxx poskytovatelů xxxxxxxxxxx služeb zřízených xxxx založených xxxxxx. Xxxxxx xxx xxxxx xxxxx specifické xxxxxxx xxx xxxxxxx vyplývající x xxxx xxxxxxxx.
Xxxxxxxx 3
Xxxxxxxxx xxxx alternativy xxxx možná xxx x xxxxxxxx xxxxxx, xxx xxxxx xxxxxx x praxi využita. Xxxxxxx úřady nemají xxxxxxxxxx x xxxx xxxxxxx, finanční xxxxxxxxx xx xxxxxx možné x xxxxxxxx za xxxxxxxx hodnocení, xxx Xxxxxx xxxxx xxx xxxxxxxx léčiv by xxxxxx xxxxxxxxxx xxxxxxx xxxxxxxxxxxx krajskými xxxxx. Xxxxxx xxxxxxxxxxxxxx xxxxx xxxxxxxxxx xxxxxxx xxxxxxxxxxx x xxxx xxxxxxxx.
Xxxxxxxx 4
Xx xxxxxxxx xxxxxx xxxxxx xxxx xxxxxxxxxxx xxxxxx Ministerstva xxxxxxxxxxxxx xx byly xxxxxxx xxxxxxx xx xxxxx xxxxxxxx pracovních xxxxxx. Xxxxxx xxxxxxxxxxxxxx žádné xxxxxxxxxx xxxxxxx vyplývající x této xxxxxxxx.
Xxxxxxxx 5
Xx xxxxxxxx xxxxxx xxxxxx jako xxxxxxxxx xxxxxx Xxxxxxxx xxxxxx xxx xxxxxxxx xxxxx xxxxx xxxxxxx xxxxxxx xx xxxxx navýšení xxxxxxxxxx xxxxxx. Přínosy xxxxx x xxxxxxxx xxxxxxx xxxxxxxxxxx technického xxxxxxxxxxx xxxxxxxx xxxxxx xxxxxx z vybraných xxxxxx xxxxxx. Xxxxxx xxx možnost krytí xxxxxxxxxx xxxxxxxxx xx xxxx pozice pro xxxxxxxxxxxx xxxxxx xxxxxx/xxxxxxxx xxxxxx x xxxxxx xxxxxx. Xxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxxxxx x vydávání xxxxxxxxxx x snazší zajištění xxxxxxxxxx xxxx. Xxxxxxx xxxxx bude xxxxxxxx xx xxxxxxx Xxxxxxx x Xxxxxxxxx xxxx xxxxxxxx Xxxxxxx xx xxxxxxxxxx xxxxxxxxx Ministerstvem xxxxxxxxxxxxx x nebude xxxxxxxxxx xxxxxxxxxxxx. Zaměstnanci xxxxxxxxxxx, kteří budou xxxxxxxxxx organizačně xxxxxxxxx xxxxxx a administrativní xxxxxxx xxxxxxxx etické xxxxxx/xxxxxxxx xxxxxx nebudou xxxxx xxxxxx xxxxxx x xxxxxxx se xxxxxxxx procesu „xxxxxxxxxxx“ x xxxxx xxxxxxxx xxxxxx xxxxxx. Xxxxxxxxx xxxxxxxxxxxx vychází ze xxxxxxxx praxe poradních xxxxxx Xxxxxxxx xxxxxx xxxxxxxx, kterými xxxx xxxx. Výbor pro xxxxxxx xxxxxxx, Xxxxx xxx xxxxxxx xxxxxx xxxxxxxxx xx., xxx xxxxxxx xxxxx xx xxxxxxxxxxx, xxxxxxxxx a xxxxxxxxxx xxxxxxx xx Xxxxxxxx xxxxxx xxxxxxxx, xxx xxxxxxx xxxxxxx x xxxxxxxxxxx xx xxxxxxxxx.
Xxxxxxxx výběru xxxxxxx
Xxxx xxxxxx xxxxxxxxx xxxx xxxxxxx efektivita x xxxxxxxxx nezávislosti xxxxxxxx xxxxxxxx xxxxxx tak, xxx bylo xxxxx xxxxxxxx klinické xxxxxxxxx xx xxxxx ČR.
První xxxxxxxx xxxx xxxxxxxxx x xxxxxxxxxxxxx xxxxxx: xxxxxxxxxxxx finančního xxxxxxxxx xxxxxxxx (xxx xxxxx xxxxxx xxxxxxxxx xxxxx, xxxxx xxxx xxxxxxxxx xxxx xxxxxxxxx xxxxx xx Xxxxxx xxxxx xxx xxxxxxxx xxxxx, xx nejevilo jako xxxxxx ze xxxxxx xxxxx xxxx xxxxxxxxxx xxxxxxxx xxxxxxxxxx xx xxxxxxx xxxxxxxxxx subjektu, xxxxxx komise by xxxxxxx xxxxxxxxx xxxx xxxxxxxx, xxxxxxx by xx xxxx x xxxxxxx x požadavkem xxxxxxxx č. 536/2014 o xxxxx xxxxxx xxx xxxxxxx xxxx), xxxxxxxx xxx xxxxxxxxxxxx xx xxxxxx xxxxxx komise x xxxxxxxxx xx xxxxxxxxxx xxxxxxx; stejně xxx x xxxxx, xxxx etická xxxxxx xx etické komise xx mohly xxx xxxxxx xxx xxxx xxxxxxx x xxxxxxx xxxxx. diskriminace xxxxxxx xxxxxxxx.
Xxxxx xxxxxxxx byla xxxxxxxxx z xxxxxxxxxxxxx xxxxxx: xxxxxxxx xx xxxxxxxxxxx, že xxxxxxx xxxxxxxxxx xxxxxx je xxxxxxx xx xxxxxxxxxxxxxx xxxxxxxxxx a xxxxxxxxxx xxxxxxxxxx xxxx zároveň xxxxxx xxxxxxxxxxxxxx xxxxxxxx, xxxx x xxxxxxxxxxxx, xxx x xxxxx xxxxx xxxxxxxx.
Xxxxx xxxxxxxx xxxx xxxxxxxxx x xxxxxxxxxxxxx xxxxxx: Xxxxxxxxx xxxx alternativy xxxx xxxxx již x xxxxxxxx xxxxxx, xxx xxxxx xxxxxx x xxxxx využita. Xxxxxxx xxxxx nemají xxxxxxxxxx x xxxx oblasti, xxxxxxxx xxxxxxxxx by xxxxxx možné x xxxxxxxx xx xxxxxxxx xxxxxxxxx, xxx Státní xxxxx xxx xxxxxxxx xxxxx by nemohl xxxxxxxxxx činnost zajišťovanou xxxxxxxxx xxxxx.
Xxxxxx varianta xxxx xxxxxxxxx x xxxxxxxxxxxxx xxxxxx: Zřízení xxxxxx xxxxxx xxxx xxxxxxxxxxx xxxxxx Ministerstva xxxxxxxxxxxxx xxxxxx xxxxxxx x xxxxxx xxxxxxxxx xx xxxx xxxxxxxx xxxxxx x xxxxxxxxx xxxxxxxxxx krytí xxxxxx xxxxxx x xxxxxxxx xxxxxx komise.
Jako xxxxxxxxxxxx xxxx proto xxxxxxx xxxx xxxxxxxx z xxxxxxxxxxxxx důvodů: Návrh xxxxxxx etické komise/etických xxxxxx xxxx xxxxxxxxx xxxxxx Xxxxxxxx xxxxxx xxx kontrolu xxxxx xxxxxxxxx xxxxxxxxx x xxxxxxxxxxxxx xxxxxx - xxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxxxxx xxxxxxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxx xxxxxx x xxxxxxxxx xxxxxx xxxxxx, rovněž xxx xxxxxxx xxxxx xxxxxxxxxx xxxxxxxxx xx nové xxxxxx pro xxxxxxxxxxxx xxxxxx xxxxxx/xxxxxxxx xxxxxx x xxxxxx xxxxxx. Xxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxxxxx a xxxxxxxx xxxxxxxxxx a xxxxxx zajištění dodržování xxxx. Xxxxxxx orgán xxxxxxx xx xxxxxxx Xxxxxxx x Jednacího xxxx, xxxxx xxxxx xxxxxxxx x vydány Xxxxxxx xxxxxxx pro xxxxxxxx xxxxx xx xx xxxxxxxxx Xxxxxxxxxxxxx xxxxxxxxxxxxx, xx rozhodovací xxxxxxxxx nezasahují xxxxxxxxxx Xxxxxxxx ústavu xxx xxxxxxxx xxxxx a xxxxxxx xxxxxxxxx xxxxxx xxx xxxx ovlivňována xxxxxxxxxxxx. Xxxxxxxxx xxxxxxxxxxxx xxxxxxxxx i praxe xxxxxxxxx xxxxxx Evropské xxxxxx agentury, xxxxxxx xxxx např. Xxxxxx xxx moderní xxxxxxx xx.
Xxxx xxxxxxxxxxxx xxxxxxxxxxx xxxx na základě xxxx uvedeného xxxxxxx xxxxx xxxxxx komise x xxxxxxxx skupinami xxxxxxx jako poradní xxxxx Xxxxxxxx xxxxxx xxx xxxxxxxx xxxxx.
Xxxxxx xxxxxx xxxxxxxx se xxxxxxx xxxx
Xxxxxxxx Evropského xxxxxxxxxx x Rady (XX) č. 536/2014 ponechává xxxxxx vytvoření x xxxxxxxx xxxxxxx náhrady xxxxxxxx škody xxxxxxxxx xxxxxxxxx xxxxxxxxx x xxxxxxxxxxx s xxxxxx xxxxxx ve studii xx xxxxx xxxxxx xxxxxxxxx státu x xxxxxxxxxx tohoto členského xxxxx a xxxxxxx xxxxx xxxxxxxx xxxx xxxxxxxxx, xxxxxx xxxx xxxxxxx xxxxxx. X xxxxxxxx xxxx je xxxxx zajištění xxxxxx xxxxx xxxxxxxxxx xxxxxxxxxx x xxxxxxxxxxxx zajištěné xxxxxxxxxxx. Xxxxxxx xxxx xxxxx zohlednit x xxxxxxxxx xxxxxx xxxxxxxxxx xxxxxxxx č. 89/2012 Sb. xxx xxxxxxx xxxxx majetkové xxxx, která je xxxxxxxx v xxxxxxxxx xxxxx zákona č. 378/2007 Xx., xxx xxxx xxxxxxxxx nemajetkovou xxxx. Při xxxxxxxx xxxxxx xxxxxx znění xxxxxx xxxx xxxxxx xxxxxxx xxxx xxxxxxxx xxxxxx náhrady xxxx. Xxx přípravě xxxxxx xxxxxx xxxx xxxx xxxxxxxxx xxxxxxxxx, xxxx x xxxxx připadající xxxxxxx xxxxxxx náhrady xxxxx xxxxxxxx, aby xxxx funkční a xxxxxxxxx. Xxxxx byla xxxx xxxxxxxxxxxx xxxx xxxxxxxxxxx xx xxxxxxxx xxxxxxxxxx. Jednotlivé xxxxxx xxxxxxxxx xxxxxxx xxxxx xxxx xxxxxxx xxxx x xxxxxxxx záměrem xxxx xxxxxxxx xxxx xxxxxxxxxx, xx kterých xx xx xxxx xxxxxxxxx vybrat xxx xxxx xxxxxxxxxxxxxxxx xx xxxxxxxxxxxxx.
Xxxxxxxx xxxxxxx xxxxxxx xxxxxxx xxxxxxx xxxxx
Xxxxxxxx 1 = systém xxxxxxx škody spočívající x xxxxxxxxx xxxxxxxx xxxxxx
Xxxxxxxxxx by byli xxxxxxx zajistit náhradu xxxxxxxx xxxxxxx xxxxx xxxxxx bankovní záruky.
Varianta 2 = xxxxxx xxxxxxx xxxxx xxxxxxxxxxx x založení xxxxx xxx xxxxxxx xxxxx
Xxxxxxx xxxxx xx xxxx xxxxxxxxx prostřednictvím fondu xxxxxxxxxxxxxxx společností xxx xxxxxxx xxxxx.
Xxxxxxxx 3 = xxxxxx xxxxxxx xxxxx xxxxxxxxxxx x xxxxxxxxx xxxxxxxxxx pojištění
Tato xxxxxxxx xx xxxxxxxxx xx xxxxxxxxxx xxxxx. Xxxxxxx xx stanovení xxxxxxx povinnosti xxxxxxxxxx xxx xx xxxxx xxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxx xxxxxxxxx xxx, xxxxxxxx xxxxxxxxxxxx x xxxxx xxxxxxxxxxxx, xxxxx xx xxxxx xxxxxx xx xxxx xxxxxxxx xxxxxxxxx xxxxxxxxx v xxxxxxxx xxxxxx xxxxxx v xxxxxxxxx xxxxxxxxx xxx xxxx provádění.
Náklady x xxxxxxx xxx jednotlivé xxxxxxx subjekty
Varianta 1
Jako xxxxx z xxxxxx xxxx xxxxxxxxx xxxxxxxxx x xxxxxx xxxxxxxx xxxxxx, které xx xxxx xxx xxxxxxx x xxxxxxx xxxxxxxxxx xxxxxxx xxx xxxxxxxxxx. Xx provedení analýzy xxxx xxxxxxxx xxxx xxx xxxxxx xxxxx, xx roční xxxxxxxx xx xxxxxxxx xxxxxx xx xx xxx xxxxxxx xxxxxxx xxxxxxx xxxx ročních xxxxxxxx xx xxxxxxxxx pojištění, xxxxxxx xxx xxxxxx xxxx by xxxxxxxxxx xxxxxxxxxx hodnocení neuchránila xxxx xxxxxxxx xxxxxxxxxxxxx xxxxxxx. Xxxxxxx xxx xx xxxxx institut xxxx být xxxxxxxx xxx xxxxxxxxxx provádějící xxxxxxxx hodnocení x xxxxx xxxxx xxxxxx, xxx x v xxxxxx případech by xx výše xxxxxxxx xxxxxxx xxxx pojistného xxxxx při xxxxxxxxx xxxxxxx škody pojištěním. Xxx menší společnosti, xxxxx xx nebyly xxxxxxxxx xxxx bonitní xxxxxxx xxxxx, xx xxxxxx být složena xxxxxxxx výše xxxxxxxx xxxxxx x xxxxxxxxx, x xxxx xxxxxx xx xxxx xx xxxxx xxxx realizace xxxxxxxxxx xxxxxxxxx xxx xxxxxxxxxx xxxxxxxxxxxx, xxx xx mohlo být xxxxxxxxx pro xxxxxxx xxxxxxxxxx. Xxxx xx xxxxxxx pro každé xxxxxxxx hodnocení, xxx xx chtěl zvolit xxxxxxxxx xxxxxxxxx xxxxxxx xxxxx xxxxxxxx xxxxxxx. Xxxxx nový institut xxxxxxx xxxxx by xxxxxxx x nové xxxxxxxxxx x xxxxxxxx xxx Xxxxxx ústav xxx xxxxxxxx xxxxx, xxxxx xx xxx xxxxx xxxxxxx, x xxx xx bylo xxxxxxx ručení x xxxxx by xxxx xxxxxxxx xx xxxxxx xxxxxxxxxx xxxxxxxxxx.
Xxxxxxxx 2
Další xxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxx xxxxxxx xxxxx xxxxxxxxx xxxxxxxxx xxxxxxxxx xxxx založení xxxxx xxxxxxxxxxxxxxx xxxxxxxxxxx xxx xxxxxxx škody. Xxxx xxxxxx farmaceutické xxxxxxxxxxx odmítly xx xxxxxxxxxxx, xx xxxxxx xxxxxxxx xxxxxx zájem xxxxxxxx xxxx vytvořit. Xxxx xxxxxxxx xxxxxxx xxx tudíž xxxx xxxxxxxxxxxxxx x xxxx xxxxx ani xxxx xxxxxxxxx.
Xxxxxxxx 3
Xxxxx zvažovanou xxxxxxxxx je xxxxxxxxx xxxxxxx xxxxxxxxxx xxxxxxxxxx xxx po xxxxx xxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxx sjednané platné xxxxxxxxx xxx, xxxxxxxx xxxxxxxxxxxx x xxxxx xxxxxxxxxxxx, xxxxx by xxxxx xxxxxx za xxxx xxxxxxxx xxxxxxxxx xxxxxxxxx x xxxxxxxx xxxxxx xxxxxx x xxxxxxxxx xxxxxxxxx xxx xxxx xxxxxxxxx, xxx. xxxxxxxx xxxxxx xxxxxx xxxxxxxxxx. Výhodou xxxxxx xxxxxxx xx xxxxx xxxxxxxxx xxxxxxxxxx pojišťovnou x xxx mnohaletá xxxxx, kdy xx xxxxxx xxxxxxxx.
Xxxxxxxx výběru xxxxxxx
Xxxx xxxxxx xxxxxxxxx xxxx xxxxxxx efektivita x zajištění skutečně xxxxxxxxx možnosti xxxxxxxx xxxxxxxxxxx v xxxxx xxxxxxxxxx xxxxxxxxx dosáhnout xx náhradu újmy.
Varianta 1 xxxx xxxxxxxxx, xxxxxxx xxxxxx žádnou xxxxxx xxxxx xxxxxxxxx xxxxxxxx xxxxxxxxxx xxxxxx xxxxxxxxx. Xxxxxx náhrady xxxxx xxxxxxxxxxx x xxxxxxxxx xxxxxx xxxxxxxx xxxxxx by xxx xxxxx výhodný pouze xxx xxxxxxxxxxxxxxxx (xxxxxxxxxxxxx) xxxxxxxx klinická xxxxxxxxx. X xxxxxxx xxxxxxx xxxxxxxxxx xxxxxxxxxx (xxxxxxxxxxxxxx) xx xxxx xxxxxxxx xxxxx být i xxxxxxxx xxxxxxxx x xxxxxxxxx plného xxxxxxx xxxxx. Varianta 2 xxxxxx x ohledem xx xxxxxxxxx xxxxxxxxx xxxxxxxx dále xxxxxxxxxxxxxx. Xxxx xxxxxxxxxxxx byla xxxxx xxxxxxx xxxxxxxx 3, kdy xxxx xxxxxxx též xx xxxxxxxxx xxxxxxxxx xxxxx. Xxxx varianta xxxxxxxx xx systému xxxxxxx xxxxx xxxxxxxxx xxxxxxxxx xxxxxxxxxx xx osvědčená x x xxxxxxxxxxx x xxx komerční xxxxxxxxxx je xxxxxxxxxxxxxxxx.
Xxxxxx xxxxxx xxxxxxxx xx xxxxxxx škody způsobené xxxxxxxxxxxx zadavateli
Pro xxxxxxxxxx xxxxxxxxxx xx xxxxx xxxxxxx nemožnosti xxxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxx xxxxxxxxxx xxxxxxxxx, xxxxx xxxxxxxx xxxxxxxxx realizovaná x xxxxxxxxxx xxxxxx xxxxxxxx podpory nemohou xx ekonomických xxxxxxx xxxxxxxx povinné pojištění. Xxxx xxxxxxxxx je xxxx zákonnou podmínkou x bez jeho xxxxxxxxx se xxxxx xxxxxxxx xxxxxxxxx xxxxxxxx. Xxxxxxxxxx xxxxxxxxxx xxx xxxxxxx xxxxxxxx xxxxxx x xxxxxxxxx xxxxx xx x rozpočtu xxxxxxxxxxxxxx zařízení a x xxxxxxx, že xxxx xxxxxx nezískají, xxxxxxx xxxxxxxx xxxxxxx xxxxxxxxxx.
Xxxxx se xxxxx x samostatné xxxxx xxxxxxxx x rámci xxxxxxxxx xxxxxxxxx xxxxxxx xxxxxxxxxx, xxx x xxxxxxx s xxxxxxxxxx xxxxxxxx xxxx xxxxxxxxx xxxxxxxx xxxxxxxxx x xxx. nekomerčních zadavatelů. Xxxx xxxxxxxx xxxx xxxxxxxxx xx základě xxxxxxxxxxxxx zjištěných skutečností: xxxxxxx xxxxxxxxxx xxxxxxxxxxxx xxxxxxxxxx xx xxxxxxxx xxxxx xxxxxxxxxxxxxxxxxx xxxxxxxxxxxx xxxxxx xx xxxxxxxx xxxx 40 xx 100 xxxxxx xxxxxxxx xx xxx; x xxxxxxxxxx 10 xxxxxx xxxxx xxxxxxx xxxxx xxxxxxxxx xx xxxxxxxxxx x xxxxxxxxxxxx xxxxxxxxxx xxxxxxxxx; xxxxxxxxx jako xxxxxxxxxx xxxxxxxxxx často xxxxxxxxx klinické hodnocení x rámci grantového xxxxxxxx, xx xxxxx xxxxxxxxx státní xxxxxxxxx xxxxxxxx podporu, xxxxxxx xxx xxxxxx ekonomických xxxxxxx xxxxxxxxxx xxxxxxxx xxxxx xxxxxxxx xxxxxxxxx. X takovém případě xx xxxxxxx xxxxxx xxxxxxx, xxx xxxxxx xxxxxxxx xxxxxx xxx xxxxxxxxx xxxxxxxxx, xxxxx xx xxxxxxxx xxxx xxxxx x xxxxxxxx xxxxxxxxxx hodnocení xxxxxxxxxx xxxxxxx č. 378/2007 Sb., ve xxxxx xxxxxxxxxx xxxxxxxx.&xxxx; Xxx hledání xxxxxxxxxxxxxx xxxxxx xxxxxx xxxx xxxx xxxxx xxxxxxxxx xxx xxxxxxxx hodnocení xxxxxxxxxxxx xxxxxxxxxx x xxxxxxxx přípravky registrovanými xx xxxxx XX x používanými v xxxxxxx s xxxxxx xxxxx, tzn. xxxxx xxxxxxx xxxxx x xxxxxxxxx xxxx xxx xxxxx schváleného off xxxxx použití (xxxx. xxx xxxxxxxxxxx pacienty) xxxxxx xxxxxxx zajištění xxxxxxxxxx xxxxxxxxxx xxxxxx xxxxxxxxxxxxxxx Xxxxxxxxxxxx xxxxxxxxxxxxx.
Xxxxxxxx xxxxxxx ohledně xxxxxxx xxxxx xxxxxxxxx nekomerčními xxxxxxxxxx
Xxxxxxxx 1 = xxxxxxx xxxxx xxxxxxxxx xxxxxx xxx xxxxxxxxxx xxxxxxxxxx
Xxxx by xxxxxx x xxxxxxx xxxxxxxxx xxxxx xxxxxxxx klinického xxxxxxxxx tuto xxxxx xxxxx x xxxxxxxxxx xxxxxxxxxxx k xxxxxx xxxxx x xxxxxxxx Xxxxxxxxxxxx xxxxxxxxxxxxx.
Xxxxxxxx 2 = xxxxxxxxx fondu xxx xxxxxxxxxx xxxxxxxx x Ministerstva xxxxxxxxxxxxx
Xxxx xxxxxxxx xx xxxx xxxxxx xxxxxxx zvažované xxxxxxxx xxxxxxx xxxxx x ostatních než xxxxxxxxxx xxxxxxxxxx.
Xxxxxxxx 3 = možnost xxxxxxxx xxxxxxxxx xxxxxxxxxxxxxxx xxxxxxxxx xxxxxxxxxxxxx xxxxxxxxxxx xxxxxx, xxxxx xxxx xxxxxxxxx xxxxxxxx xxxxxxx použití xxxxxxxxxxxxxx léčivých xxxxxxxxx x xxxxx klinického xxxxxxxxx.
Xxxxxxx a xxxxxxx xxx jednotlivé xxxxxxx xxxxxxxx
Xxxxxxxx 1
Xxxxxxxx xxxx xxxxxxxx xx xxxx xxxxxxx xxxxxxxxxxxx xxxxxxx xxxxxxxx x xxxxxxx xxxxxxxxxx xxxxxxxxxxxx na xxxxxxxxx za xxxxxxx, xxx xxx xxxxxxxxxx xxx xxxxx x xxxxxxxxxx xxxxxx xxxxxxxxxx xxxxxx, xxx xx xxxxxxx těchto hodnocení xxxxx x xxxxxxxxxx. Xxxxxxx xx byly xxxxxxx s nutností xxxxxx tuto xxxxx x xxxxxxxx Xxxxxxxxxxxx xxxxxxxxxxxxx.
Xxxxxxxx 2
Xxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxxx národního xxxxxxx xxxxxxx xxxxx xxxxxxxxx xxxxxxxxx hodnocení xxxx založení xxxxx xxx xxxxxxxxxx subjekty x Xxxxxxxxxxxx xxxxxxxxxxxxx. X takovém xxxxxxx xx xxxxx xxx xxxxx xxxxxx upravovat xxxxxx xxxxxxxxxxx xxxxx, xxxxxx xxxxxxxxxx xxxxxxxxxx, xxxxxx xxxxxxxxxx zaměstnanců xxxxx x x xxxxxxxxxx xxxx xxxx xx, x xxxxxx xxxxxx, x xxxx xxxx a x xxxxxx xxxxxxxxxxx xx xxx xxxx naplňován. X xxxxx xxxxxxxxxx xxxxxx xxxxxxxxx xxxxxx xx zdrojů ministerstva, xxxxx by xxxx xxxxxxxxxx xxxxxxxxx xxxxxx xxxxxx xxxxxxx xx xxxxxxx xxxxxx xx xxxxxxxxx klinických xxxxxxxxx. Xxxxxxxx x možným xxxxxxx xxxxxxxx xx xxxxxx fondu a xxxx xxxxxxx bylo xxxx xxxxxx vyhodnoceno xxxx neefektivní x xxxxxxxxx.
Xxxxxxxx 3
Xxxxx variantou xx xxx xxxxxxxxxx xxxxxxxxxx možnost xxxxxxxx xxxxxxxxx prostřednictvím xxxxxxxxx xxxxxxxxxxxxx xxxxxxxxxxx xxxxxx, xxxxx pojištění činnosti xxxxxxx použití xxxxxxxx xxxxxxxxx v rámci xxxxxxxxxx xxxxxxxxx. Nebude xxx xxxxxxxx x xxxxxxxxx pojištění.
Kritéria xxxxxx xxxxxxx
Xxxx xxxxxx xxxxxxxxx xxxx zvoleno xxxxxxxxxx xxxxx diskriminace xxxxxxxxxx xxxxxxxxxx.
Xxxx xxxxxxxxx xxxxxxxx 1 a 2 Xxxx xxxxxx xx xxxxx mohlo znamenat xxxxxxxxxxxx komerčních zadavatelů. Xxxxx by xxx xxxxxxxx xxxxxxxxx vznik xxxx xxxxxx xxxxxxxxxxxx. X ohledem na xxxx xxxxxxx, byla xxxxxxx xxxxxxxx 3, xxxxx stanovuje xxxx xxxxx xxxxxx xxxxxxx xxxxx pro xxxxxxxxxx xxxxxxxxxx x xxxxxxxxxxxxxxxxxx xxxxxxxxxx hodnocení xxxxxxxxx xxxxxxxxxx xxxxxxxx x xxxxx xxxxxxxxx xxxxxxxx xxx xxxxxxxxxxxxx xxxxxxxxxxx xxxxxx, x event. xxxxxxxxx pojištěním xxx xxxxxx zkoušejícího, x xxxxxxx xxxxxxx xx xxxxx připojištění xxxxxx xxxxxxxxxx.
2.2. Xxxxxxxx xxxxxxxxx x xxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx
Xxxxxx 36 Xxxxxxx o xxxxxxxxx Xxxxxxxx xxxx stanoví xxxxxx, xxx které xxxxx xxxxxxx státy xxxxxxxx vnitrostátní opatření, xxxxx xxxxx přeshraničnímu xxxxxxx. Xxxxxx z xxxxxx xxxxxx je xxxxxxx xxxxxx x xxxxxx xxxx. Xxxxxx xxx xxxxxxxx xx xxxxxxx čl. 81 xxxxxxxx 2001/83/XX by měla xxx odůvodněna xx xxxxxxx xxxxxxx veřejného xxxxxx.
Xx xxxxxx zajištění xxxxxxxxxxx xxxxxxxx xxxxxxxxx xxx potřeby xxxxxxxx x Xxxxx xxxxxxxxx x důvodu xxxxxxx xxxxxxxxx xxxxxx xxx xx možné xxxxxxxx xxxxxxxx, xxxxx xx xxxxxxxxx xxxxxxxxx xxxxx.
Xxxxxxxxxxx xxxxxx xxxxxxx xx xxxxxxxxxx xx xxxxxx xxxxx xxxxxxxxx subjektů x xxxxx se x xxxxxxxx nových xxxxxxxxxxx xxxxxxxxxx.
Xxx xxxxxxxxx xxxxxxxx xxxxxxxxxx právní xxxxxx xxxx hodnocena xxxxxxx xxxxxxxxxxx xxxxxxxx (xxxxx xxxxx xxx xxx xxxxxxxxxx za xxxxxxxx) právní xxxxxx:
- xxxxxxxxxxx;
- xxxxxxxxxxxxxxx;
- přesnost;
- xxxxxxxxxxxx;
- xxxxxxxxxxxx;
- ekonomická xxxxxxxx;
- xxxxxxxx;
- xxxxxxxxxx.
Xx xxxxxxxxxxx - právní xxxxxx omezení reexportů xxxxxxxx přípravků xxxxxxxxx xxxxxx, xxxxx xxxxxx xx xxxxxxx vývozu xxxxxxxx xxxxxxxxx xxxxxxxxxxx xxx xxxxxxxxxxx xxxxxxxxx xxxx x České xxxxxxxxx x xxxxxxx, xx na xxxx x Xxxxx xxxxxxxxx xxxx hrozit xxxxxx xxxxxxxxxx pro xxxxxxx xxxxxxxx x xxxx xxx ohrožena kvalitní xxxx x xxxxxxx xxxxxx a xxxxxx xxxx. Komplexnost xxxxxx xxxxxx xxxxxxx xx xxxxxxxxx xxxxxxxxxx xxx xxxxxxxxxxxx xxxxxx nedostupnosti xxxxxxxx přípravků xxx xxxxxxx xxxxxxxx x Xxxxx xxxxxxxxx (úprava xxxxx x xxxxxxxxx xxxxxxxx x postupu xxx xxxxxxxxxxxxx dat), xxxx ve xxxxxxxxx xxxxxxxxxxx xxxxxxxx v xxxxxxxxx xxxxxxxxx hrozby xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx xxx xxxxxxx pacientů x Xxxxx xxxxxxxxx x xxxxxxx ve xxxxxxxxx xxxxxxxxxxx sankcí xx xxxxxxxx xxxxxxxxx xxxxxxxx. Úprava xxxxxx xxxxxx jak xx xxxxxx xx xxxxxxxxx xxxxx Evropské xxxx, xxx xx xxxxxxx xxxx.
Xx xxxxxxxxxxxxxxx - xxxxxxxx xxxxxx xx xxxxxxx xxx, aby xxxx xxxxxxx xxxxxxxx x co xxxxxxxx xxxxx xxxx xxxxxxx xxxxxxxxx xxxxxxx přijetí xxxxxxxx a xxxxxxx xxxx xxxxxxx xx xxxx xxxxxxxxxx xxxxxxxx. Xxxxxxxxxxxxx xxxxxx xx xxxxxxxx xxx x xxxxxxx xxxxxxxxxxxx a xxxxxxxxxx hrozby xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx xxx xxxxxxx xxxxxxxx x Xxxxx xxxxxxxxx, tak x xxxxxxx xxxxxxx xxxxxxxxxxx xxxxxxxx. Dotčené xxxxxxxx xxx xxxx xxxxxxxxxx xxxxxxx obrany xxxxx přijatým xxxxxxxxx.
Xx xxxxxxxx - xxx xxxxxxxx xxxxxxxxxxxxxxxx x xxx účely efektivního xxxxxxxx xxxxxxxxxxxx xxxxxxx xx xxxxx x xxxx zejména x xxxxxx xxxxxx xxxxxxx xxxxxxxx xxxxxxxxxx právní xxxxxx xx xxxx xx nejpřesnější x xxxxxxxxxxxxxxxxx xx xxxxxx xxxxx xx xxxxxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx.
Xx odůvodněnost - xxxxxxxx x postup xxx xxxxxxxxxxxxx nutnosti xxxxxxxx opatření xx xxxxxx xxxxxxx xxxxxxxxx xxxx plně v xxxxxxx xx zájmem xx ochraně zdraví x xxxxxx lidí x x xxxxxx xxxxxxxxxx xxxxxxx xxxxxxx xxxxxx xxxxxxxx xxxxxxxxx xx xxxxxxxxxx xxxxxxxx xxxxxxxxxx xxxxxxxx.
Xx xxxxxxxxxxxx - x xxxxxxx xx xxxxxxx přiměřenosti xxxxxx xxxxxx xx x xxxxxx xxxxxxx xxxxxxxx vhodnosti x xxxxxxx xxxxxxxx dle xxxxx Xxxxxxxx xxxx xxxxxxx varianta xxxxxxx xxxxxx pouze v xxxxxxxxx, ve xxxxxxx xx být xxxxxxxxxxxx xxxxxxx xxxxx xx xxxxxxx zdraví a xxxxxx xxxx. Xx xxxxxxx xxxxxxxxxxxx systému xxxxx xxx x xxxxxx vyhodnocování dojde x xxxxxxxxx xxxxxxxxxxxxxxxx xxxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx pro xxxxxxx xxxxxxxx v Xxxxx xxxxxxxxx. Navrhovaná xxxxxx xxxxxx xxxxxx xxxxxx, xxxxx v xxxxxxxx xxxxxxxx xxxxxxxx pouze xxxxxxxx xxxx xxxx x xxxxxxx xx xxx o xxxxxx xxxx dlouhodobé omezení. Xxxx xxxx xxxxx xxxxxxxxxxx rozpor xx xxxxxxx xxxxxxx pohybu xxxxx. Xxxxxxxx xx xxxxxxxx pouze xx xx xxxxxxx, xxx xxxxxxxx xxxxx xxxxxxxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx, xxxxxxxxxxxx velmi významných xxx xxxxxxx xxxxxxxxx xxxx u pacientů x Xxxxx xxxxxxxxx. Xxxxx dopad xxxxxxxx xx xxxx xxxxxxxx xxxxxxxxx xxx, že xx xxxx xxxxxxx xxxxxxx pouze na xxxxxx přípravky, xxxxx xxxx terapeuticky nenahraditelné. Xxxxxxxxx xxxxxx xxx xxxxxxxxx mimořádnost xxxxxxx xxxxxxxxxxx xxxxxxxx, x xx xxxxxxx xxx xxxxxxx xxxxxx nedostupnosti xxxxxxxx xxxxxxxxx pro xxxxxxx xxxxxxxx x Xxxxx xxxxxxxxx.
Xx xxxxxxxxxx xxxxxxxx - systém xx xxxxxxx ve xxxxxxxx, xxxxx xxxxxxx xxx xxxxxxxx xxxxxxxxxx xxxxxxx lékáren a xxxxxxxxxxxx x xxxxxxx xxxxxxxxxxx x xxxxxx xxxxxxxxxx a xxxxxxx, x tak xxxxxxxxxxx xxxxxxxx xxxxxxx regulované xxxxxxxx ani orgány xxxxxxx xxxxxx. Xxxx xxxxxxx varianta xxxxxxxxxxxx x xxxxxxxxxxx systému.
Ad xxxxxxxx - za xxxxxx xxxxxxxxx xxxxxxxx xxxxxx xxxxxx na xxxxxxxxx xxxxxxx xxxxx xxxxxx xxxxxx xx xxxxxxxxxxx xxxxxxxx upravit xxxxxxxxxx xxxxxxx xxxxxxxxx (xxxx. intervaly aktualizace xxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxxxxxx, xxxxxxxxx xxxxxxxx, xxxxxxxx xxxxxxxx x rozsahu xxxxxxxxxxxxx xxxxx x hlášeních).
Ad xxxxxxxxxx - za xxxxxx vynutitelnosti xxxxxxxxxxxx xxxxxxxx xxxx stanoveny xxxxxxxxxxxx xxxxxx x xxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxx. Tyto xxxxxx xxxxxxxx xxxxxx výše, xxx u nich xxx dostatečně xxxxxxx xxxxxxxxxxx xxxxx.
Xxxxxxxxxxx xxxxxxx xx xxxxxx xxxxxx xxxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx xxx potřeby xxxxxxxx v Xxxxx xxxxxxxxx. Pokud xx xxxxx o xxxxxxx xxxxxxxxxxx x důvodů xx xxxxxx xxxxxxxx xxxxxxxxxx x xxxxxxxxxx, xxxx xxxx v xxxxxxxxxx §33 odst. 2 zákona x xxxxxxxx xxxxxxxxxx povinnost xxxxxx xxxxxx xxxxxxxxx xxxx ukončení xxxxxxx xx xxxxx xxx xxxxxxx 2 xxxxxx xxxxxx.
Xxxxxxxxxxxx xxxxxxxxxxxxx léčivých xxxxxxxxx x xxxxxxxxx xxxxx je aktuální xxxxxxx x Xxxxx xxxxxxxxx, xxx xxx xxxxxx XX. Xxxxx xxxxxxxxx xxxxx xx xxxxxxxx xxxxxxx x x xxxxxxx xxxxxxxx xxxxxxxxxxx xx stala xxxxxxxxxx obchodní činnost. Xxxxxxxxxxx množství xxxxxxxxx xx x xxxxxxxx xxxxxxxxxx dostatečného xxxxxxxxxx xxxxxxxxxxxx trhů uložených xxxxxxxxx xxxxxxxxxx x xxxxxxxxxx xxxx na xxxxxxxxxxx xxxxxxxxxxx služeb x Xxxxxx. X xxxxxxxx xxxxxxxx může xxxxx k xxxxxxx xxxxxxxxxx prostředků xxxxxxxxxxxxx xxxxxxx xx výzkum x vývoj xxxxxx xxxxxxxx přípravků xxxx x xxxxxxxx xxxxxxxxxxxx xxxxx xx xxxx x xxxxxxx xxxxxx xxxxxxxx xxxxxxxxx se xxxxxxxxx. Ukazuje xx, xx xxxxxxxx vnitřní xxx x léčivými xxxxxxxxx xx xxx xxxxxxxxx xx xxxxxx xxxx xxxxxxxxx xxxxxxxx xxxxxxxxxxx xxx xxxxxxxx xxxxxxxxx x výše xxxxx x veřejných xxxxxxxxxx x xxxxxxxxxxxx xxxxxx. Xx otázkou, xxx x nadále xx xxxxxxxx xxx x xxxxxx xx xxxxxxxxx xxxxxxxx x xxxxxxxxxxx systémů xxxxxxxxxxxx xxxxx a xxx xxxxxxxx x xxxxxxxx xxxxxxxx xxxxxxxxxx xxxx x xxxxxxx xxxxxxxx xxxxxxxxx xxxxx trh xxxxx xxxxxxxx.
Xxxxxxxx x xxxxxx xxxxxxxxx xxxxxxx xxx počet hlášených xxxxxxx xxxxxx nedostupnosti xxxxxxxx xxxxxxxxx v xxxxxxxxxxxx státech EU. Xxxx xx stále xxxxxxx xxxxxxxx xxxxxxx x xxxxxxxxxxxxx konkrétních xxxxxxxx přípravků xx xxxx zemích XX xxxxxxxx, což xxxx x ještě xxxxxxxxxx xxxxx xx xxxxx xxxxxxxx přípravků xx xxxx x xxxxxxxxxxx xxxxxxx hladinou. X xxxxxxx xxxxxxxx nedostupnosti xxxxxxxx xxxxxxxxx xx xxxxx xxxx xxxxx xxxxxx pacienta x xxxx xxxxxxxxxxx stavu. Xxxxx v případech, xxx xxxxx akutní xxxxxxxxxxxx xxxxxxxx přípravků xxx potřeby xxxxxxxx x Xxxxx xxxxxxxxx (xxxxx xx tak xxxxx xxxxxx xxxxxxxxx, xxx xxxxxxxxxxxx xxxxxx xxx. xxxxx xxxxxxxxx xxxxxxxxx xxxxxxx léčivých xxxxxxxxx Antabus, Actilyse x NovomixFlexpen), je xx xxxxxx xxxxxxxx xxxxxxxx xxxxxx xxxxx xxxxxxxxxxxx xxxxxxx zdraví x xxxxxx lidí xxxxxxxx xxxxx xxxxxxxx xxxxxxxxx xxxxxxxx v xxxxxxx xxx x xxxxxxxxx právními xxxxxxxx, xxx xx xxxxxxx xxxxxxxxxxxxx x xxxxxxxxxxxxx xxxxx.
Xxxxxxx problém xxxxxx xxxx řešitelný xxxxxx xxxxxx x xxxxxxxxx xxxxxx a xxxxxxxx xxxxxxxx xxxxxxxx přípravků xxxxxxxxx x xxxx xxxxxx, xx ať xx xx xxxx xxxxxxxx jakákoli, u xxxxxxxx přípravků, xxxxxx xxxx u xxxxxxx xxxxxxx, xxxx xxx xxxxxxxxxx xxxxxxxx výhodnější xxxxxxx xxx xxxxxxxxxxx xxxxxxx xx trh xx vyspělejších xxxxxxxxxxx xxx v xxxxxxxxxxx xxxx xxxxxxxxx. Je xx xxxx xxxxxxx xxxxx kupní xxxxx xxxxxxxxxxxx v xxxxxx xxxxxxxxxx xxxxxxxxxxxx xxxxxx, xxx xx stejnou xxx jsou xxxx xxxxxxxxx xxxxxxxxx xxxxxxx x xxxx xxxxxxx xxxxx xxxxx xxxxx xxxxxxxxxx prostředků, a x této xxxxxxxxxxx xxx xxxxxxxxx xxxxxxx x xxxxxxx xxxxx xxxxxxxxxxxxxxxx subjektů, xxxxxx xxxxxxxx regulátorů, xxxxxxx, xxxxxxxxxxxx x xxxxxxxxxxx xxxxxxxxxx. Dále xxxxxxxxxx xxxxxx x úhradové xxxxxxxx již z xxxxxx věci xxxxxxx xxx vůbec xxxx xx xxxxxxxx s xxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxx x důvodu xxxxx x jakosti, xx xxxxxx již x xxxxxxxxx xxxxxx xxxxx a které xxxx xxxxx xxxxx. Xxxxx xxxxxxxxxx xxxxxx x xxxxxxxx regulace xxxxx xxx xxxxx xx v xxxxxxxxxxxxxx xxxxxxx xxxxxxxxx, zatímco xxxxxxx nedostatečného zajištění xxxxxxxxxx potřeb xxxxxxxx x Xxxxx republice xxxxxxxxx léčivým xxxxxxxxxx xxxx xxxxxx velice xxxxxx a xx xxxxx jej xxxxx xxxxxxxxxx. X xxxxxxxxx xx xxxx xxxxx xxxxxxxxxx, xx xxxxxxxxxxxxx xxxxxxx xxxxxxxxxxxxx dostupnost xxxxxxxx xxxxxxxxx xxx xxxxxxxx x České xxxxxxxxx xx xxxxxxxxx x xxxxxx se x xxxx xxxxx xxxxxxx xxxxxxxx xxxxxx x úhradové xxxxxxxx xxxxxx léčivého xxxxxxxxx.
Xxxxxxxxxxxxx xxxxxxxxxxxxx xxxxxxx je xxxxxxxx xxxxxx xxxxxx xxxxxxx xxxxxxxxx xxxxx xx xxxxxx x xxxxxxxx, xxxxx xxxxxxxxx xxxxxxxx xxxxxxxxxxxx léčiv x xxx xxxxxxxxxxxx xxxxxxxxx jejich xxxxxxxxxxx. Xxxxxxxxxx x xxxxxxxxxxx xxxx xxxxxxxxxxxxx s xxxxxx x xxxxxxxxxxx xxxxxxxxx xxxxxx mající xx cíl xxxxxxxxx xxxxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxx x Xxxxx republice xxxx x xxxxxx o xxxxxxxx již částečně xxxxxxxx, praktické xxxxxxxxxx x xxxxxxxx stávající xxxxxx xxxxxx x xxxx xxxxxxxxxxxx xxxxxxxxxxxxxx xxxx xxxx xxxxxxxxxx xxxxxxx xxxxxx xxxxxxxxx x xxxxxxxx.
Xxxxxxxxx xxxxxx x ohledem xx xxxxxxxxx xxx xx xxxxxxxxxxxx především z xxxx xxxxxx, že xxxxxxxxx záruky xxxxxxxxxxxxxxxx xxxxxxx xxx xxxxxxxxxxxx xxxxxxxx xxxxxxxxx a xxx xxxxxxxxxxxxx xxxxxxxxx xxxxxxx léčivé přípravky. Xxxxxxxxx xxxxxxxxxx §11 xxxx. x) zákona xxxx xxxxxxxxxxx xxxxxx xxxxxxx x řešení xxxxxxx, kdy xxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx xx xxxxxxxxx vedená xxxxxxx xxxxxx xxxxxxxxx xxxxxxx xxxxx omezuje xxxxxxxx xxxxxx xxxxxxxx x České xxxxxxxxx, x xxxxxx tohoto xxxxxxxx xxxx v xxxxxxxxxxx xxxxxxxxx x xxxxxx xxxxxxxxxx xxxxxx xxxxxxxx xxx využito, xxxxx xxxxx o xxxxxxx, který xx xxx xxxxxxx xxxxxxx xxxxxxxxx x se xxxxxxxxxxx xxxxx xxxxxxxxxx xxxxxxx a xxxxxxxxxxxxx xxxxxxxx jistot x xxxxxxxxx xxxxxxxxx všech xxxxxxxxxxxxxxxx xxxxxxxx.
X xxxxxxxxx xxxxxxxxxxx léčivých xxxxxxxxx xxx xxxxxxxx x Xxxxx republice xx xxxxxxxx přijmout určitý xxxxxxx xxxxxxxx provázaných xxxxx a xxxxxxxx, xxxxx xx xxxx xxxxxxx xxxxxxx režim, xxxxx xx xxxxxx, xxxxxxxx x xxxxxxxxx x xxxxxxx xx xxxxxxxxx cíl, kterým xx xxxxxxxxx xxxxxxxxxxx xxxxxxxx přípravků xxx xxxxxxxx x České xxxxxxxxx.
Xxxxxxxxxx xxxxx sestává x xxxxxxxx ze xxx xxxxxxxx xxxxxxxxxxx xxxxx x xxxxxxxx. Xxxxxx z xxxx xx vytvoření seznamu xxxxxxxx xxxxxxxxx ohrožených xxxxxx xxxxxxxxxxxxx. X xxxxxxxxx xxxxxx seznamu xxxxx xxxxxxx xxxxxxxx x xxxxxxxxxx, xxxxxx x xxxxxxxx xxxxxxxx xxxxxxxxx. Xxxxxxxxx a xxxxxxxxxx tohoto seznamu xxxx xxxxxxxx formou xxxxxx xxxxxxxx obecné xxxxxx Ministerstvem xxxxxxxxxxxxx, xxxx bude xxxxxxxxx, xx xxxxxxx na xxxx xxxxxxxxxxxxxx xxxxx xxxxx xxxx využít xxx oprávnění stanovená xxxxxxxx xxxxx. Xxxxxxxxxx xxxxxx xxxxxxx xxxx xxxxxxxx xx specifické xxxxxx všech xxxxxxxxxxxxxxxx xxxx xxxx xxxxxxx xxxxxxxxxx xxxxxxxxx xx xxxxx xxxxxxx, xxxxxx xxxx, že xx xxxxxx distributoři xxxx xxxxxxx s xxx, xx xx xxxx xxxx, že distribuce xxxxxxxxx z těchto xxxxxxxxx do zahraničí xxxx xxx xxxxxxxxx xxxxxxx xxxx xxxxxxxx. X xxxxxxx na xxxx znalost může xxxxx distributor xxxxxxx xxxxx xxxxxxxxxx xxxxxx xxxxxxxx xxxxxxxxx do xxxxxxxxx xx xxxxxx xxxxxxx xxxxxxxxxx. Xxx xx xxxxx xxx xx xxxxxx, xx xxxx zákonnou xxxxxxxxxx xx zajistit xxx xxxxxxx xxxxxx xxxxxxxxx, xxxxxxx xx xxxxxxxxxxxxx, xxxxxxx xxxxxxxxxxxxxx oprávněným xxxxxxx xxxxxx xxxxxxxxx x xxxxxxxx x xxxxxxxx xxxxxxxxxxx odpovídajících xxxxxxx pacientů x Xxxxx republice. Xxxxxx x xxxxxx xxxxx x opatření xx xxx xxxxxxx xxxxxxx xxxxxxxxxxx podmínek předání xxxxxxxxxxxx xxxxxxx Xxxxxx Xxxxxxxxxxxx xxxxxxxxxxxxx k xxxx, xxx xxxxxx xxxxxxxx xxxxxx xxxxxx, xxxxxx xx xxxxxxx xx xxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx xx xxxxxxxxx, xxxxxxx xxxxx xxxxxx může, xxx x nemusí Ministerstvo xxxxxxxxxxxxx xxxxxxxx. Xxxxxx, x xx xxx xxxxxxxxxxx krokem x xxxxxxxxx xx xxxxxx xxxxxxxx xxxxxx povahy, xxxxxx xxx splnění xxxxxxx xxxxxxxxxxx xxxxxxxx Xxxxxxxxxxxx xxxxxxxxxxxxx xxxxx xxxx xxxxxx distribuci xxxxxxxxxxx léčivého xxxxxxxxx xx xxxxxxxxx. Xxx xxxxxxxx takového opatření xxxx xxxx xxxxxxxxx, xx xxxxxxx xxxxx xxxxx xxxx xxxxxx xxx xxxxxxxxx xxxxxxxxx xxxxxxxx xxxxx.
Xxxxxxxxxx režim xx tedy xxxxxx, xxxxxxxx x xxxxxxxxx x xxxxxxx xx xxxxxxxxx xxx, xxxxxxx x jeho xxxxx xx xxxxxxxxxxx xxxxxxxxx xxxxxxxxxxxxxxxx xxxx xx x xxxxxxxxxxx xxxxxxxxx xxxxxxxx x xxxxxxxx x xxx xxxxxxxxxx x zároveň xx xxxxxxxxx, xx xxxxxxx xxxxxxxx nebudou xxx xx náhlá x xxxxxxxxxx. Xxxxxxxxx cíl xx xxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxxx, které xxxx k uskutečňování xxxxxxxxxx xxxxxxxxx šetrné x umožňují xxxxxxxxx x xxxxxxx nebo xxxxxx xxxxxxxxxx xxx x xxx skutečně xxxxxxxxx xxxxxxx, kdy xxxx x xxxxx xxxxxxxxxxx opatření xxx xxxxxxx xxx účinná x xxxxxxxxxx xx xxx smysl. Xxx xxxx xxxxxx, že xxxxxxxxxx xxxxxx, která xx xxxxxxx xxxxx x xxxx xxxxxxxx xxxxxxxxxx §77c a §77d do xxxxxx, xxxxxxx xxxxxxxxxx léčivých xxxxxxxxx xxx xxxxxxxx x České republice xxxxxxxxxxxxx způsobem x xxxxxx bude transparentní x xxx xxxxxxx xxxxxxxxxxxx.
Xxxxxxxx xxxxxxx xxxxxx xxxxxx xxxxxxxxxxxxx léčivých xxxxxxxxx z důvodu xxxxxxxxx
Xxxxxxxx 1 = xxxxxx
Xxxxxxx xxxxxxxxx xx xxxxxx xxxxxxxxxxxx návrhu xxxxxx xxxxxx x xxxxxxxx xxxxxxxx xxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx.
Xxxxxxxx 2 = xxxxx xxxxxxxxxxxx xxxxxx (xxxxxx x xxxxxxxx)
Xxxxxxxx xxxxxxxxxxx xxxxxxxxxxx xxxxxxxx.
Xxxxxxx a xxxxxxx pro xxxxxxxxxx xxxxxxx subjekty
Varianta 1
Xxxxxxxxxxxx xxxxxx bude xxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxx, xxx se xxxxxxxxx xxxxxxx, xx je xx xxxx xxxxxxxxxx xxxxxxxx xxxxxx xxxxxxxxx x je xxx xxxxxxxx xxxxxx xxxxxxxx x XX. X xxxxxxxxx xxxxxx xxxx xxxxxxxx i xxxxxxx xxxxxxxxx xxxxxxx, xxxxx xx xxxxx xxxxxx xxxxx vynaložit, pokud xx xx xxxx xxxx xxxxxxxx xxxxxxxx xxxxxx xxxxxxxxx (xxxxx xxxxxxxxx komplikací xxx.). Xxxxxxxx xxxx xxxx xxxxxxxx volného pohybu xxxxx, ovšem na xxxx zdraví xxxxxxxx x ČR.
Varianta 2
Příslušnými xxxxxxxxxxx xxxxxxxxxx xx xxxx xxxxx navrhnout x x konečném xxxxxxxx xxxxxx xxxxxx xxxxxx, xxxxx xx xxxxxxxxx zájem na xxxxxxx xxxxxx xxxxxxxx xx xxxxxx xxxxxxxxxxxxxxx xxxxxxxx xx uskutečnění xxxxxx xxxxxxxxxxxxxxx xxxxxxxxxxxx. Xxxx xxxxxxxxxx zájmů xx bylo xxxxxxxxx xxxx v xxxxxxx x xxxxxx XX, xxxxx umožňuje omezit xxxxx xxxxx zboží xx xxxxxx xxxxxxx xxxxxxxxx xxxxxx.
Xxxxxxxx xxxxxx xxxxxxx
Xxxx xxxxxx kritérium xxxx zvoleno xxxxxxxxx xxxxxxx xxxxxxxxx xxxxxx x souladu x xxxxxx XX.
Xxxxxxxx 1 xxxx xxxxxxxxx x xxxxxxx xx xxxxxx xxxxxxx řešit xxxxx xxxxxxx (vyskytující xx xxxxxxx xxxxxxxxxxxxx léčivých xxxxxxxxx x xxxxxx xxxxxx reexportů). Xxxxxxxxx xxxxxxxxxxx xxx xxxxxxxxxx xxxxxxxxxx komplexně řešit. Xxx xxxxxxxxx xxxxxxxx xxxxxx xxxxxx x xxxxxx o xxxxxxxx xx x České xxxxxxxxx xxxxxxx xxxxx x xxxxxxx současného xxxxx, xxx xxxxx xxx některé xxxxxxxx xxxxxx xxxxxxxxx xxx xxxxxxxx v Xxxxx xxxxxxxxx xxxxxxxx nedostupné x není xxx x potřebném xxxxxxx xxxxxxxxx xxxxxxx xxxxxx xxxxxx x xxxxxx, xxxxxxx xxxxxx xxxxxx xxxxxx xxxxxxx x xxxxxx xxxxxxxxxx validních xxxxxxxxx x xxxxxxxxxx xxxxxx xxxxxxxx, která xx s dostatečným xxxxxxxxxx xxxxx zabránit xxxxxx takové situace. Xxxx xxx xxxxxxx xxxxxxxx xxxxx 2, xxxxx xxxxxxx přijetí xxxxxx xxxxxx úpravy xxxxxxxxxx xxxxxxxxxx xxxxxxx.
Xxxxxx xxxxxxxxxxxx xxxxxx akutní xxxxxxxxxxxxx a xxxxxxxxx xxxxxxxxxxx xxxxxxxx přípravků
V xxxxx xxxxxxxxx xxxxxxx xxxxxxxx xxxx xxxxxxxxxx xxx x xxxxx xxxxxxxxxxxx xxxxxxxxx xxxxx, xxxxx xxxxxxxx xxxxxxxx xxxxxxx různé formy xxxxxx regulace xxxxxxx xxxxxxxxx na základě č. 81 odst. 2 Xxxxxxxx x. 2001/83 (xxxx. Xxxxxxxxx, Xxxxxxxx, Xxxxxxxxx a xxxxx) x dle xxxxxx xxxxxxxxxx xxxx xxxxxxx xxxxxxxxxx xxxxxxxx řešení.
Definice xxxxxxx xxxxxxx
Xxxxxxxx 1= xxxxxx xxxxxxxx (xxxxxxxxx xxxx)
Xxxxxxxx 2 = xxxxxxxxx xxxxxxxxxx zajistit xxxxxxx xx xxx xxxxxxxxx xxxxxxxxxx x xxxxxxxxxx
Xxxxxxxx 3 = xxxxxxxx xxxxxx xxxxxxxxxx xxxxxxxxxxxx hlášení xxxxx xxxxxx
Xxxxxxxx 4 = xxxxxxxx povinnosti xxxxxxxxxxxx xxxxxxx xxxxx xxxxxxxxx xxxxxx
Xxxxxxxx 5 = xxxxxxx xxxxxxxx xxxxxxxxxxxx xx xxxxxxxx xxxxxxxxxx x registraci
Náklady x xxxxxxx xxx xxxxxxxxxx xxxxxxx subjekty
Varianta 1
Nepředložení xxxxxx xxxx xxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxx, xxx xx xxxxxxxxx xxxxxxx, že xx xx trhu xxxxxxxxxx xxxxxxxx léčivý přípravek x xx tak xxxxxxxx zdraví pacientů x XX. X xxxxxxxxx zdraví může xxxxxxxx x xxxxxxx xxxxxxxxx náklady, xxxxx xx xxxxx xxxxxx xxxxx xxxxxxxxx, pokud xx na trhu xxxx xxxxxxxx xxxxxxxx xxxxxx xxxxxxxxx (xxxxx xxxxxxxxx xxxxxxxxxx atp.). Xxxxxxxx xxxx xxxx xxxxxxxx volného xxxxxx xxxxx, ovšem xx xxxx xxxxxx xxxxxxxx x ČR.
Varianta 2
Farmaceutický xxx x xxxxxxxx xxxxxxxx xxxxxxxxx xx xxxxxxxxxx xxxx x xxxxxxxxx xxxxxxxxx států xx xx xxx xxxxxx velmi provázaným xxxxxxxx xxxxxxxxxxxx xxxxxx, xxx xxxxx xx xxxxx se xxxxxx xxxxxxx činností (xxxxxx, xxxxxxxxxx, výdej v xxxxxxx) a zároveň xxxxxxxxxxxx hájí xxx xxxxxxxxxx xxxxx. Zajišťování xxxxxxxxxxxx xxxxxxxx xx xxxxxx rozloženo xxxx xxxxxxxxxx subjekty xxx, xxx bylo xxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxx xxxxxxx. S ohledem xx xxxxxxx pokrok x neustálé posouvání xxxxxx výzkumného xxxxxx xx xxxxxxxxx x xxxxxxx xxxxxxxxxxx na xxxxx xxxxxxx léčivého xxxxxxxxx. Jakýkoliv xxxxx xx xxxxxxxxxxxxxxx xxxx xx úkor xxxxxxx xx druhého xxxxxxxx xx xxxxxx xxxx xxx x xxxxxxxx xxxxxxxx xxx xxxxx xx prostředky xxxxxxxxxxx xx xxxxxx xxxxx x na dostupnost xxxxxxxx přípravků na xxxxxxxxxxxx xxxxxx. Xxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxx xxxxxxx na trh xx x xxxxxxxx xxxxxxxx mohlo xxxxxxxx xxxxxxxxx xxxxxxx, ve xxxxxx by tito xxxxxxxxxx distributory pro xxxxx vývozu na xxxx trhy. Xxxxxxxx xxxxxx xxxxxxxxxx by xxxxx xxxxxxxx vzniklý xxxxxxx, xxxxxxxxxxxx xxxxxxxx xxxxxxxxx.
Xxxxxxxx 3
Xxxxxxxxx xx xxxxxxxx xxxxxxxxxxxxxxx zátěž xx xxxxxxx, xxx xxxxxxxxxxxx hlásí veškeré xxxxxx xx xxxxxx xxxxxxxxxxx. Nadměrně xx xxx xxxxxxxxx xx xxxxxxxx právních xxxxxxxxxx. Xxxxxx xx xxxxxx xxxxxxxxxxxxxx x ohledem xx požadovaný xxx.
Xxxxxxxx 4
Xxxxxxxx xxxxxxxxx xx xxxx preventivní funkci xxx, xxx mohlo xxx xxxxxxxx reexportů xxxxxxxxx xxxxx v xxxxxxx xxxxxx xxxxxx xxxxxxxxxxxxx. Varianta byla xxxxxxxxxxx xxxxxxxxxx xxxxxxxx xx Xxxxxxxxx, xxx xxx xxxxxxxxxx xxxxxxxxx xxx xxxx xxxxxx x EU, xxx xx takováto xxxxxxxx xxxxxxxxxxxxxxxx. Xxxxxxx omezování xxxxxxxxx xxxxx x xxxxxxx vytipovaných léčivých xxxxxxxxx, které jsou xxx xxxxxxxxxxx xxxxxxxxx xxxx xxxxxxxx, je xxxx xxxxxxxxxxx x xxxxxxxxxx, xx xxxxxxxx xxxxxxxxxxxx xxxx (ochrana xxxxxxxxx zdraví).
Varianta 5
Xxxx xxxxxxxx byla xxxxxxxxx x xxxxxxx xx xxxxxxxx xxxxxxxxx xxxxxxx xxxxxxxxxxxx xxxxxxxx x Xxxxxxxx. Xxxxxxx xxxxxxx xxxxxxxx xxxxxxxxxxxx od xxxxxxxx xx xxxx xxxxxxxxx xxxxxx xxxxxx xxxxxxxxxx xxxxxxxxxxxx xxxxxx x xxxxx xx xxxxxx xxxxxxxxx xxxxxxxx. Xxxxxxxxx xx xxxx xxxxxxxxx xxxxx xxxxxx xxxxxxxxx v xxxxxxx xxxxxxx akutní nedostupnosti xxxxxxxx přípravků.
Kritéria výběru xxxxxxx
Xxxx hlavní xxxxxxxxx xxxx xxxxxxx efektivita x účelnost xxxxxxxxxxxx xxxxxxx.
Xxxxxxxx 1 xxxx xxxxxxxxx x xxxxxxx xx xxxxxxx akutně xxxxx xxxxxxxxxx xxxxxxx, xxx xxxx uvedeno xxx xxxx. Varianta 2 byla xxxxxxxxx x xxxxxxx xx xx, že by xxxxxxxx xxxxxxxxxx xxxxxxx. Xxxxxxxx 3 xxxx xxxxxxxxx x xxxxxx xxxxxxxxxxxxxx x xxxxxxxxx xxxxxxxxxx. Xxxxxxxx 5 xxxx xxxxxxxxx x xxxxxxx xx to, xx xx neřešila xxxxxxxxxx xxxxxxx. Xxxx xxxxxxxxxxxx xxxx zvolena xxxxxxxx, xxx xxxxx xx distributoři xxxxxxx xxxxxxxxx vývoz xxxxx x xxxxxxxxx, kdy xx v xxxxxxxx xxxxxxxxx xxxxxxx xxxxxx xxxxxxxxxxxx léčivých xxxxxxxxx xxxxxxxxxx pro poskytování xxxxxxxxxxx xxxxxx.
Xxxxxx forma xxxxxxx reexportů
Při xxxxxxxxx xxxxxxx forem regulace xxxx (xxxxx nulové xxxxxxxx) xxxxxxxxx x xxxxxxxx forem xxxxxxxx xxxx XX:
- xxxxxxxxxxxx xxxxxxx xxxx (xxxxxxxxxx x xxxxxxxxx xxxx xxxx xxxxxxxxxxx adresátovi);
- xxxxxxxx obecné xxxxxx (xxxxxxxx v konkrétní xxxx xxxx neomezenému xxxxxx xxxxxxxx);
- xxxxxxxx (xxxxxxxxxx xxxxxx akt).
Definice xxxxxxx xxxxxxxx forem xxxxxxx xxxxxxxxx
Xxxxxxxx 1 = xxxxxx varianta (xxxxxxxxx xxxx)
Xxxxxxxx 2 = individuální xxxxxxx xxxx
Xxxxxxxx 3 = xxxxxxxx obecné xxxxxx
Xxxxxxxx 4 = vyhláška
Náklady x xxxxxxx xxx xxxxxxxxxx xxxxxxx xxxxxxxx
Xxxxxxxx 1
Xxxxxxxxxxxx xxxxxx xxxx xxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxx, xxx xx xxxxxxxxx xxxxxxx, xx xx na xxxx xxxxxxxxxx xxxxxxxx léčivý xxxxxxxxx x xx xxx xxxxxxxx zdraví xxxxxxxx v XX. X xxxxxxxxx xxxxxx xxxx xxxxxxxx x xxxxxxx xxxxxxxxx xxxxxxx, xxxxx xx jinak xxxxxx xxxxx vynaložit, xxxxx xx na xxxx byly xxxxxxxx xxxxxxxx léčivé xxxxxxxxx (xxxxx xxxxxxxxx xxxxxxxxxx xxx.). Xxxxxxxx xxxx xxxx xxxxxxxx volného xxxxxx xxxxx, xxxxx xx úkor xxxxxx xxxxxxxx x ČR.
Varianta 2
Xxxxx xx reexporty xxxx xxx omezovány xxxxxx xxxxxxxxxxxxxx xxxxxxxxx xxxx vydávaných xx xxxxxxxx řízení, xxxx xx znamenalo xxxxxxxxx xxxxxxxxx správního xxxx. Xxxxxxx řízení xxxxxx xxxxxxx xxxxxx náročná, xxxxxxx xxxxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx xx xxxxx s ohledem xx xxxxxx xxxxxxxx xxxxxx x xxxxxx xxxxx xxxxxx.
Xxxxxxxxxxxx správní xxxx xxxxxxx rozhodnutí xxxxxxxx konkrétního xxxxxxxxx xxxxxx x xxxxxxxxx xxxx. Počet xxxxxxxx xxxxxxxxxxxx se na xxxxxxxxxxx xx přitom xxxxx, xxxxx xxxxxx xxxxxxxxx xx xxxxxxxx xxxxxxxxx možný xxxxx (xxxxx xx xxxxx xxxxxxx xxxxxxx distribuční xxxxxxxxx), xxxxxxxxx xx xx xxxxx 2500. X tohoto xxxxxx xx xxxx xxxxxxx xxxxxx xxxxxxxxxxxxxxx xxxxxxx x xxxxxx xx x xxxxxxxxx xxxx xxxxxxx xxxxxxxxxx a xxxxx daný xxxxxxx x xxxx xxxx.
Xxxxxxxx 3
Xxxxxxxx obecné xxxxxx xx xxxxxx xxxxxxx xxx xxxxxxxx xxxxxxxxxxx xxxxx xxxxxxxx v xxxxxxxxx xxxx. X xxxxxx xxxxxxxx, xxx xxx xxxxxxxxxxxx xxxxx xxxxx xxxxxxxxx xxxxxxxx, xx xxxx xxxx xxxxxx. Xxxxxxxxx xxxxxxxxx xxxx (xxxxx xx xxxxxxx xxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx) xx xxx xxxxxxx. Xxx xxxxxx xxxxxxx xxxxxxxxx xxxxxxxxx xxxxxx xxxxxx xxxxxxxxx xxxx tak, xxx xxxxxx vyhovoval xxxxxxx v xxxxxxx xxxxxx hrozby nedostupnosti xx účelem ochrany xxxxxx reexporty xxxxxx xx xxxxxxx.
Xxxxxxxx 4
Xxxxxxxx xxxxxxxx předpisů xx xxxxxx x (xxxxxx xxxxxx xxx správního xxxx x finančně) xxxxxxx xxxxxx, což xx xxxxxxxx xxxxxxxxx, xxxxx má xxx xxxxxxxxxx akutní xxxxxxxxxxxx. Xxxxxxxx xxxxxxxx xxxxxxxx xx xxxxx xxxxxxxx. Xxxxxxx xx xxxxxx xxxxxxxxx a xxxxxxx xxxxxxxxx xxxxxxx xxxxxxx xxxxxxxx xxxxxx předpisem.
Kritéria xxxxxx variant
Jako xxxxxx xxxxxxxxx byla zvolena xxxxxxxxxx (xxxxxxxxxxxxxxx a xxxxxx) navrhovaného xxxxxxx.
Xxxxxxxx xxxxx 1 (xxx. xxxxxx varianta) byla xxxxxxxxx x ohledem xx xxxxxx potřebu xxxxx xxxxx problém. Xxxxxxxxx xxxxxxxxxxx xxx xxxxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxx. Xxxxxx xxxxxxxxxx xxxxxx vymezeny příslušné xxxxxxx xxx omezování xxxxxxxxx. Xxxxxxxx xxxxx 2, kdy by xxxxxxxxx xxxx x xxxxxxxx xxxxxxxx omezovány xxxxxx xxxxxxxxxxxxxx xxxxxxxxx xxxx, xxxx zamítnuta x ohledem na xxxxxxxxxxxxxxx a xxxxxxx xxxxxxxxx xxxxxx xxxxxxx. Xxxxxxxx číslo 4 (xxxxxxxx xxxxxxxx xxxxxxxx) xx xxxx časově x administrativně (xxxxx x xxxxxxxx) xxxxxxx xxxxxx, který xxxxx xxxxx x xxxxxx xxxxxxxx xxxxx xxxxxxxxx xxxxxx xxxxxx.
Xxxx xxxxxxxxxxxx xxxx xxxxx xxxxxxx xxxxxxxx xxxxx 3 (xxxxxxxx obecné xxxxxx), xxxxxxx xxxxxxx xxxxxxxx xxxxxxxxxx xxxxxxx a x xxxxxxxxx x xxxxxxxxx formami xxxxxxxx xxxxxxx nejpřijatelnější xxxxxxx x xxxxxxxxxxxxxxx xxxxx xxx účely xxxxxxxxxx xxxxxxxx.
Xxxxxxxx xxxxxxxxx xxxxxxx xx xxxxxxx xxxxxxxxx xxxxxxxxx
Xxxxxxxx 1 = xxxxxx (xxxxxxxx stav)
Varianta 2 = pouze Xxxxxxxxxxxx xxxxxxxxxxxxx
Xxxxxxxx 3 = xxxxx Státní xxxxx xxx xxxxxxxx xxxxx
Xxxxxxxx 4 = xxxxxxxxx pravomocí Ministerstva xxxxxxxxxxxxx x Xxxxxxxx xxxxxx pro xxxxxxxx xxxxx
Xxxxxxxx 5 = xxxxxxx jiného xxxxxx
Xxxxxxxx 6 = xxxxxxx xxxxxx orgánu
Náklady a xxxxxxx xxx jednotlivé xxxxxxx subjekty
Varianta 1
Xxxxxxxxxxxx xxxxxx xxxx xxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxx, xxx xx vyskytují xxxxxxx, xx xx xx xxxx xxxxxxxxxx xxxxxxxx léčivý xxxxxxxxx x xx xxx xxxxxxxx xxxxxx xxxxxxxx x XX. X xxxxxxxxx zdraví xxxx xxxxxxxx i nutnost xxxxxxxxx xxxxxxx, xxxxx xx xxxxx xxxxxx xxxxx vynaložit, pokud xx na xxxx xxxx xxxxxxxx xxxxxxxx xxxxxx přípravky (xxxxx xxxxxxxxx komplikací atp.). Xxxxxxxx xxxx xxxx xxxxxxxx volného xxxxxx xxxxx, xxxxx xx xxxx zdraví pacientů x XX.
Xxxxxxxx 2
Ministerstvo xxxxxxxxxxxxx xx ústředním xxxxxxxx xxxxxxx xx xxxxx xxxxxxx zdraví xxxxxxxxxxxx. Xxxxxx x xxxx xxxxx xx (x xxxxx xxxxxxxx xxxxx zajištění xxxxxxx xxxxxxxxx xxxxxx) xxx xxxxxxxxx dostupnosti xxxxxxxx xxxxxxxxx. X tohoto xxxxxxxx xx xxxx xxxxxx, aby xxxxx xxxxxxxx xxxxxxxxxxx xxxxxxxxxxxx. Xxxxxxxx léčiv xx xxxx xxxxxxxxxxx xxxxxxx, x xxxxxxx xxxxxx xxx xxxxxx Xxxxxx xxxxx xxx xxxxxxxx xxxxx, xxxxx xxxxxxxxx xxx xxxxx xxxxxxxx xxxxx větším administrativním xxxxxxxx x xxxxxxx xx xx tento xxxxx (xxxxxxx jako x xxxxxx členských xxxxxxx XX) xxxxxxxxxxxxx. Xxxxxxxxx varianty, kdy xx reexporty xxxx xxxxxxxxx xxxxx Xxxxxxxxxxxxx xxxxxxxxxxxxx, je dosavadní xxxx, xxx většinu xxxxxxxxxxxxxxxxx xxxxxxxx zajišťuje Xxxxxx ústav xxx xxxxxxxx xxxxx. Xxxxxx xx xxx xxxxxxxxx xxxxxxxxxx návaznost, na xxx prováděné činnosti (xxxxxxx xxxxxxxxxxxx, xxxxxxxx x lékáren x xxxxxxxx léčivých xxxxxxxxx xx prováděno Státnímu xxxxxx xxx xxxxxxxx xxxxx).
Xxxxxxxx 3
Státní xxxxx xxx kontrolu xxxxx xx xxxxxxx xxxxxxxxxx Xxxxxxxxxxxx xxxxxxxxxxxxx a xxxxxxxxx xxxxxxx agend xxxxxxxxx x regulací xxxxx. Xxxxxxx této xxxxxxxx xx bylo xxxxxxxxx a xxxxxxxxx xxxxxxxxxx xx xxxxx xxxxxxxxxx xxxxxx xxxxx xxxxxxx. Xxxxxxxxx xx xxxx absence xxxxxxxxxx xx činnosti x xxxxx xxxxxxx Xxxxxxxxxxxx xxxxxxxxxxxxx.
Xxxxxxxx 4
Jak bylo xxxxxxx xxx ve xxxxxxxx 2 x 3, xxx xxxxxx xx určitým xxxxxxxx xxxxxxxx na xxxxxxxx xxxxx x České xxxxxxxxx. Činnost xx xxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxxx Xxxxxxxx xxxxxx xxx xxxxxxxx léčiv, xxxxxxx Xxxxxxxxxxxx xxxx nadřízený xxxxx má „xxxxxxxxx“ xxxxxxxxx (ať xx xx formě xxxxxxxxxx xxxxxxxxx xxxxxx nebo xxxxxx xxxxxxxxxx xxxxxx xxxxxxxxxxx xxxxxx nadřízeným xxxxxxxxxxxxx). Z xxxxxx xxxxxxxx je xxxxxxx, xxxxx xx xxx xxxxxx xx xxxxxxxxx xxxxxxxxx xxxxxxxxxxxxxx. Tato xxxxx xxxxxxxxxx by xxxxxx měla xxx xxxxxxxxxxx. Xx. měla xx zajistit, aby Xxxxxx xxxxx xxx xxxxxxxx léčiv xxxxxx x případě podezření xx xxxxx situace xxxxxxxxxxxx xxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxx xxxxxxxxxxxx x xxxxxxx, xxx xx xxxxxxxxxxxx xxxxx xxxx xxxxx xxxxxxx x xxxxxxx podezření, o xxxxxx xx xxxxx x různých xxxxxx. Xxxxxxxxxx xxxx xxxxxx xxxx zajištěno xxxxxxxx xxxxxxx xxxxxxxxxx přijatých xxxxxxxx xx xxxxxx xxxxxxx xxxxxxxxx x xxxxxx xxx opomenut xxx jeden x xxxxxx, xxxxx xx xx regulaci léčiv x ČR xxxxxx. Xxxxxx identifikována žádná xxxxxxxx této xxxxxxxx.
Xxxxxxxx 5
Xxxxxxxxxx žádný xxxxx, xxxxx by xxx x regulované činnosti xxxxx xxx Xxxxxxxxxxxx xxxxxxxxxxxxx nebo Státní xxxxx xxx xxxxxxxx xxxxx. Xxxxxxxxx xx xxxx xxxxxxxxxxxx xxxxxxxxx xxxx agendy xxxxxx, xxxxx se xx xxxxx xxxxxxxxx.
Xxxxxxxx 6
Zřízení xxxxxx orgánu xx xxxxxxxxx xxxxxxxxxxxx xxxxxxxx xxxxxxx.
Xxxxxxxx xxxxxx xxxxxxx
Xxxx xxxxxx xxxxxxxxx xxxx xxxxxxx xxxxxxxxxx navrhovaného xxxxxxx.
Xxxxxxxx číslo 1 (xxx. xxxxxx xxxxxxxx) xxxx xxxxxxxxx x xxxxxxx na akutní xxxxxxx xxxxx xxxxx xxxxxxx. Xxxxxxxxx xxxxxxxxxxx xxx xxxxxxxxxx dostatečně xxxxxxxxx xxxxx. Xxxxxx xxxxxxxxxx xxxxxx xxxxxxxx xxxxxxxxx postupy xxx xxxxxxxxx xxxxxxxxx. Xxxxxxxx xxxxx 2, kdy xx xxxxxxxxx byly x konečném xxxxxxxx xxxxxxxxx xxxxx Xxxxxxxxxxxxx xxxxxxxxxxxxx, xxxx xxxxxxxxx x důvodu xxxxxxxxxxxx xxxxxxxxxxxx na xxxxxxxxx xxxxxxx xxxxxx xxxxxx. Xxxxxxxx číslo 3 (xxxxxxxx pouze Státním xxxxxxx xxx xxxxxxxx xxxxx) xxxx xxxxxxxxx x důvodu xxxxxxxxxxxxxx xxxxxxxxx xxxxxxxxxxx xxxxxxxxxx xxx xxxxxxxxx příslušných xxxxxxxx. Varianty 5 x 6 byly xxxxxxxxx x ohledem xx xxxxxx xxxxxxx xxxxxxxxxxxx x xxxxxxxxxxxxxx. Xxxx xxxxxxxxxxxx byla xxxxxxx xxxxxxxx určité xxxxx xxxxxxxxxx Ministerstva xxxxxxxxxxxxx a Xxxxxxxx xxxxxx pro kontrolu xxxxx, kdy na xxxxxxxx xxxxxxxx již xxxxxx xxxxxxx regulace x xxxxxxx xxxxx xxxxxxxx x zákoně x léčivech (Státní xxxxx xxx xxxxxxxx xxxxx xxxx xxxxxxxxxxxx xxxxx x Xxxxxxxxxxxx xxxx xxxxxxxxxxxxx xxxxx).
Xxxxx xxxxxxx xxxxxx systému xxxxxxxx
X xxxxxxx xx xxxx xxxxxxx xxxxxxx xxxxxxxx xxxxxx, kdy xx dle xxxxxxxxx xxxxxxxx zejména efektivity, xxxxxxxxx x xxxxxxxxxxxx xxxx xxxx xxxxxxxxxxxx
- xxxxxxx xxxxxxxxxxxxxx xxxxxxxx;
- x podobě zavedení xxxxxxxxxx xxxxxxxxxxxx xxxxxxx xxxxx některých vývozů;
- xx formě xxxxxxxx xxxxxx povahy;
- vydávaného xx xxxxxxx xxxxxxxxxx Xxxxxxxx xxxxxx xxx xxxxxxxx xxxxx a Xxxxxxxxxxxx zdravotnictví; je xxxxx xxxxxxxxxxx xxxxxxxxx xxxxx varianty a xxxxxx konečnou xxxxxx xxxxxxxxxxxx systému.
Definice xxxxxxx xxxxxxxxx forem xxxxxx xxxxxx omezení reexportů
Varianta 1 = Státní xxxxx xx xxxxxxx xxxxxxxx xxxxxx xxxxxx, xxxxxx xx xxxxxxxx xxxxxx léčivých přípravků, x nichž xx xxxxxxxxxx distribuce xxxxxxx xxxxxx xxxxxxxxxxxx xxxxxxxx xxxxxxxxx, x xxxxxxx xx Xxxxxxxxxxxx zdravotnictví xxxxxxxx xxxxxxxx xxxxxx xxxxxx, xxxxxx by xxxxxxxx xxxxxxxxxx v xxxxxxxxxx případě
Varianta 2= xxxxxxxx xxxxxx xxxxxx xx vydávalo xxxxx Xxxxxxxxxxxx xxxxxxxxxxxxx a Xxxxxx xxxxx pro xxxxxxxx xxxxx by xxxxxx nedostatkových xxxxxxxx xxxxxxxxx zveřejňoval v xxxxxxxx umožňujícím xxxxxxx xxxxxxx xx xxxx xxxxxxxxxxx prostředku
Varianta 3 = Ministerstvo zdravotnictví xx xxxxxxxx seznam xxxxxxxx přípravků, x xx xxxxxx xxxxxxxx xxxxxx xxxxxx, xx xxxxxxx by přistoupilo xx xxxxxxx podnětu xx strany Xxxxxx, x xxxxx by xxxxxxxxxx distribuce xxxxxxx xxxxxx nedostupnost xxxxxxxx xxxxxxxxx, x následného xxxxxxxx xxxxxx povahy, xxxxxx xx xx xxxxxxxx distribuci x xxxxxxxxxx xxxxxxx, xxxxxxx x xxxxx xxxx xxxxxxxxx xx Xxxxxx xxxxx pro kontrolu xxxxx xxxxxxxxxx podklady x xxxxx xxxxxx x podněty, xxx xx uvedeno xxxx.
Xxxxxxx x xxxxxxx pro xxxxxxxxxx dotčené subjekty
Varianta 1
Xxxxxx ústav xxx xxxxxxxx xxxxx xx xxxxxxx xxxxxxxx obecné xxxxxx, xxxxxx by xxxxxxxx xxxxxx léčivých xxxxxxxxx, xxx xxxxxxx xxxxxxxxxx na xxxx x Xxxxx xxxxxxxxx xx xxxxx xxxxxxxxx xxxxxxxxx nedostupnosti xxxxxxxx xxxxxxxxx při poskytování xxxxxxxxxxx služeb xxxxxxxxx x Xxxxx republice x tento xxxxxx xx xxxxxxxxxx aktualizoval. Xxxxxxxxxxxx xxxxxxxxxxxxx by xx xxxxxxx podnětu Xxxxxxxx ústavu xxx xxxxxxxx léčiv při xxxxxxx xxxxxxx xxxxxxxxxxx xxxxxxxx vydávalo xxxxxxxx xxxxxx xxxxxx, xxxxxx xx omezilo distribuci xxxxxxxx přípravků xxxx xxxxx Xxxxx republiky x xxxxxxx, xx xxx nedostatku xxxxxxxx xxxxxxxxx xx xxxx x Xxxxx xxxxxxxxx xx xxxxx xxxxxxxxx xxxxxxxxx jeho xxxxxxxxxxxxx xxx poskytování xxxxxxxxxxx xxxxxx xxxxxxxxx x Xxxxx xxxxxxxxx.
Xxxxxxx xxxxxxx x nelogičnost právní xxxxxx xxxxxxxxxxx xx xxxxxxxx xxxx xxxxxxxx xxxxxx xxxxxx, xxxxxxx xxxxxxxxx xx nerespektovala xxxxxxxxx dotčených xxxxxx xxxxxx správy. Xxxxxx xxxxxxxxxxxxxx xxxxxxxxxx přínosy xxxx varianty. Problematičnost xxxx xxxxxxxx xxxxxxx xxx x časové xxxxxxxxxx xxxxxxxxx opatření xxxxxx povahy, xxxxxxx xxxxxxxxxxxx xxxxxxxx přípravků xx xxxxx xxxxx xxxxxx. Nepřiměřenou právní xxxxxxxx xx znamenalo xxxxxxxx xxxxxxxx obecné xxxxxx xx úrovni Xxxxxxxx xxxxxx pro xxxxxxxx xxxxx, xxxx x xxxxxxx xx xxx existující xxxxxxxxxx xxxxxxx xxxxxxx distributorů x xxxxxxxx x xxxxxx xxxxxxx Xxxxx xxxx xxxxxxxxxx xxxxxxxx xxxx x identifikovat xxxxxxxxx xxxxxx xxxxxx xxxxxxxxxxxxx léčivých přípravků. X xxxxxxx xx xxxxx XX a xxxxx pohyb zboží xx xxxxx stanovit xxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxx pro xxxxxxxxxxx xxxxxxxxxxx xxxxxx.
Xxxxxxxx 2
Xxxxxx xxxxx xx xx xxxxxxx podkladů x xxxxxxx xxxxxxxxxxxx subjektů (xxxxxxxx xxxxxxxxxx o xxxxxxxxxx léčivých xxxxxxxxx, xxxxxxxxxxxx a xxxxxxxxxxxxx xxxxxxxxxxx x xxxxxx xxxxxxxx xxxxxxxxx) pravidelně xxxxxxxxxxx xxxxxx nedostatkových xxxxxxxxxx xxxxxxxx přípravků x xxxxxxxxxxx by xxx xxxxxxxx umožňujícím xxxxxxx xxxxxxx xx xxxx xxxxxxxxxxx xxxxxxxxxx. X xxxxx xxxxxxxxxxxx xxxxxxx by xx xxxxxxxx léčivé xxxxxxxxx, xxxxxxx nedostatek je xx xxxx Xxxxx xxxxxxxxx akutní, a xx xx xxxx x případě xxxxxxxx xxxxxxx xxxxxxxxx xxxxxxx xxxxxxxx xx xxxxx xxxxxxxx xxxxxx xxxxxx Xxxxxxxxxxxxx xxxxxxxxxxxxx.
Xxxxxxxx 3
Xxxxxx xxxxx xxx kontrolu xxxxx xx xx xxxxx xxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxx x xxxxx xxxxxx a xxxxxxx Xxxxxxxxxxxx xxxxxxxxxxxxx. Xxxxxxx xx xxxxx xxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx xx xxx činilo Xxxxxxxxxxxx zdravotnictví, které xx xxxxxxxx xxxxxx xxxxxxxx xxxxxxxxx, x xx formou opatření xxxxxx xxxxxx, u xxxxx xx xxxxxxxxxx xxxxxxxxxx xxxxxxx akutní xxxxxxxxxxxx xxxxxxxx xxxxxxxxx, x xxxxxxxx obecné xxxxxx, xxxxxx xx xxxxxxxx xxxxxxxxxx v xxxxxxxxxx xxxxxxx.
Xxxxxxxx xxxxxx xxxxxxx
Xxxx xxxxxx xxxxxxxxx xxxx xxxxxxx xxxxxxxxxx xxxxxxxxxxxxx xxxxxxx regulace.
První xxxxxxxx xxxx xxxxxxxxx x důvodu neefektivity. Xxxxx xxxxxxxx byla xxxxxxxxx z toho xxxxxx, xx xx xxxxx xxxxxxxxxx xxxxxxxxxx xxxxx Ministerstva xxxxxxxxxxxxx xxxxxxx xxxxxxxxxx xxxxxx xxxxxx xxxxxx pro xxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx. Byla xxxxxxx xxxxx varianta, xxxxxxx xx xxxx xxxx xxxxxxxxxxxxxxx x xxxxx xxxxxxxxxxxx.
XXXXXXX XXXXXX XXXXXXX XXXXXXX OMEZENÍ XXXXXXXXX
Xxxx xxxxxxxxxxxx xxxxxx xxxx xx xxxxxxx výše xxxxxxxxx xxxxxxx výběru xxxxxxx xxxxxxxx xxxxxxxx xxxxxxx xxxxxxxx přípravků Xxxxxxxxxxxxx xxxxxxxxxxxxx, v xxxxxxx xxxxxxx vývozu xx xxxxx x xxxxxxxx xxxxxx a xxxxxx pacientů na xxxxx XX. Xxxxxx xxxxx xxx xxxxxxxx xxxxx xxxx xxxxxxxx xxxxxxxxxxxx xxxxxxxx xxxx x hlášení xxxxxxxxxxxx, xxxxxxxx x xxxxxxx xxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxx xx tomto xxxxxxx.
Xxxx xxxxxxx xxxxxxxxx xxxxxxx se xxxxxx xxxxxxxx zavést xxxxxxxx xxxxxxxx xxxxxx povahy, xxxxx xxxx vydávat Xxxxxxxxxxxx zdravotnictví, xxxxxxx xxxxx, x jehož xxxxxxxx xxxxx (xxx xx xxxxxxx xxxxxxxxxxxx xxxxxxxxxx §11 xxxx. x) zákona x xxxxxxxx) xx xxxxxxxxxxx xxxxxxxxxxx léčivých přípravků xx xxxxx XX. Xxxx xxx navázáno xx xxxxxxxxx kompetence Xxxxxxxxxxxx x zároveň xxxxx xxxxxx využity xxxxxxxx Xxxxxxxx xxxxxx xxx xxxxxxxx xxxxx x xxxxxxxxx xxx, xxxxxxx disponuje. Ministerstvo xxxx xxxxxxxx xxxxxxx xx xxxxxxx xxxxxxx Xxxxxxxx xxxxxx xxx xxxxxxxx xxxxx založeného xx xxxxxxxxxxxxx dat, x xx xxxxx xxxxxxxxxxxx. Xxxx xxxx xx x xxxxxxx xxxxxxx bude moci Xxxxxxxxxxxx xxx xx Xxxxxxxx xxxxxx xxx xxxxxxxx xxxxx xxxxxxx.
Xxxxx xx x zvláštní xxxxx xxxxxxxxx xxxx, xxxxx cílí xxxxxxx xxxxxx xx xxxxxxxx xxxxxxxxxx xxxxx xxxxxxxx x konkrétní věci. Xxxxxxxx x xxxxxxxxxx xxxxxxxxxxxx xx xxxxx xxxx jeho xxxxxxx xxxx vhodná xxxxx xxxxxxxx. Xxxxxxxxxx xxxxxx xxxxxx xxxxxxxxx x xxxxxxxxx xxxxxx xxxxxxxx x Xxxxx xxxxxxxxx x k omezení xxxx xxxxxxx, kdy xxxx xx úkor xxxxxxxxxxxx jejich xxxxxx xxxxxx přípravky xxxxxxxx xxxx xxxxx Xxxxx xxxxxxxxx, je xxx x xxxxxxx se xxxx xxxxxx xxxxxxxxx, xxxxxxxxxxxxx, xxxxxxxxxx xxxxxx xx xxxxxx xxxxxx x xxxxxxxxx.
2.3. Adaptace xxxxxxxx xx vztahu x xxxxxxx xxxxxx xxx xxxxxxx xxxxxx xxxxxxxxx
Xxx xxxxxx xxxxxx xxxxxxxx xxxxx xxxxxxxxx xxxxx xxxxxxxx, xxx xxxxxx xxxx zákona x léčivech tak, xxx byla xxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxx Xxxxxx x xxxxxxxxx xxxxxxxxx (XX) č. 1252/2014 ze dne 28. května 2014 xxxxxxxxxx xxxxxxxx Evropského xxxxxxxxxx x Rady 2001/83/XX, xxxxx jde x xxxxxx x xxxxxx xxxxxxx xxxxxxx xxxxx xxx léčivé xxxxx xxx xxxxxxx xxxxxx přípravky. Xxxxx xxxx xxxxxxxx xx xxxxx xxxxxxxx xxxxxxxxx xxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx Xxxxxxxx xxxx xxxx Xxxxx xxxxxxxxx.
2.4. Xxxxxxxxxx Xxxxxxxx xxxxxx xxx kontrolu xxxxx a Xxxxxxxxxxx xxxxxxxxxxx xxx
Xxxxxxxx 1 - změna xxxxxx x léčivech
První xxxxxxxxx xx novelizovat zákon x léčivech xxx, xxx obsahoval xxxxxxxx xxxxxxxxxxx Xxxxxxxx ústavu xxx kontrolu xxxxx x Xxxxxxxxxxx ředitelství xxx. Xxxxxxxxx x xxxxx xxxxx může xxx již platný xxxxxx řád, x xx xxxxxxxxx xxxxxxxxxx §8 zákona x. 226/2013 Xx., o xxxxxxx xxxxx x xxxxxxxxxxx xxxxxxx xx xxx, xxxxx xxxxxxxx xxxxxxxxxxxx xxxxxxxxxx dozorových xxxxxx, x nichž xx xxxxx straně xxxxxxxxx xxxxx Xxxxxxxxx xxxxxxxxxxx cel, x xxxxxxxxxxx xxxxxx xxx xxxxxxx xxxxxxxx již xxxx. Toto xxxxxx, xx. změna xxxxxxxxxxx xxxxxx, xx x xxxxx xxxxxxx xxxx xxxxxxxxxxx, xxxxxxxxxxxx xxxx xxxxxxxxx xxxxxxxxx právní xxxxxx xxxx xxxxxxx.
Xxxxxxxx 2 - Xxxxxxx xxxxxxxxxx novely zákona x Xxxxx xxxxxx Xxxxx republiky x xxxxxx xxxxxx novely xxxxxx x xxxxxxxx
Xxxxxx xxxxxxxxx xxxxxx tohoto xxxxxxxx xx xxxxxxxx x rámci xxxxxxxxxxxx xxxxxx xxxxxx o xxxxxxxx xxxxxxxxxxx xxxxxx xxxxxx č. 17/2012 Sb., x Xxxxx správě Xxxxx xxxxxxxxx, xx xxxxx xxxxxxxxxx xxxxxxxx, xx xxxxx by byla x xxxxx xxxxxxxxxx §2 xx 5 xxxxxx xxxxxx rozšířena xxxxxxxxx xxxxxxxxx Xxxxxxxxxxx xxxxxxxxxxx xxx x xxxxx oblast.
Varianta 3 - Vyčkání samostatné xxxxxxxxxx xxxxxx x Xxxxx správě České xxxxxxxxx
Xxxxx xxxxxxxxx je xxxxxx samostatné xxxxxxxxxx xxxxxx č. 17/2012 Sb., x Xxxxx xxxxxx České xxxxxxxxx, ve znění xxxxxxxxxx xxxxxxxx. Xx xxxxx xxxxx xxxxx xxxxxxxxx xxxxxx xxxx 1. xxxxx 2013, xxx již xxxxxx xxxxxxxxx novelizován, xxxxx xxx xxxxxxxxxxxx xxxx xxxxx xxxxxxxxxx.
2.5. Prokazování xxx xxxxxxxxx činnosti x xxxxxx instituty xxxxxxxxx x xxxxxxx xxxxxxxx přípravků
Varianta 1 - xxxxxx
Xxx xxxxxxxxx xxxxxxxx xxxxxx úpravy x xxxxxx x xxxxxxxx xx xxxxxxx xxxxx x přesnější x xxxxxxxxx xxxxxx xxxx xxxxxx, jejichž xxxxxxxxx xxxxxx xxx xxxxxxxxxx xxxxxxxxx z xxxxx x nevyhovuje xxxxxxxxxxx xxxxxxx, xxx xx xxxx otázky xxxx být upraveny.
Varianta 2 - xxxxx xxxxxx x xxxxxxxx
Xxxx xxxxxxxx xx xxxxxxxxx xxxxxxxxxxxx xxxxxxx inspekcí x xxxxx výkonu xxxxxxxx xxxxx xxxxxxxxxxx xxxx, xxxx xx xxxxxxxxx x prokazování xxxxxxxxx inspektora xx xxxxxxxx xxxxxxxxx podle xxxxxxx xxxxxx xxxxxxx xxxxxxxx. Xxxx by xxxxx x xxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxx x zabrání xxxxxxxx xxxxxxxxx tak, xxx xxxxx xxxxxxxxxx dostatečný xxxxxxx xxx xxxxxxxx xxxxxxxxx ochranu veřejného xxxxxx x xxxxxx xxxxxxxx x xxxxxxxx xxxxxxxx v xxxxxx xxx xxxxxxxx xxxxxxxx xxxxxxxx přípravků, xxxxx xxxxxxxxx požadavky xx xxxxxx jakost, xxxxxxxx x xxxxxxxxxx. Blíže xxx odůvodnění ve xxxxxxxx xxxxx.
3. Vyhodnocení xxxxxxx x xxxxxxx
Xxxxxx xxxxxx xxxxxxxx xxxxxxxxxxxxx x xxxxxxxx xxxxxxxx xx xxxxxx x xxxxxxx látkám xxx xxxxxxx xxxxxx xxxxxxxxx, xxxxxxxxx xxxxxxxxxxx Xxxxxxxx xxxxxx pro xxxxxxxx xxxxx x Xxxxxxxxxxx xxxxxxxxxxx xxx a xxxxxxxx xxxxxxxxxxxxx v xxxxxxxxxxx oprávnění xxxxxxxxxx xxx xxxxxxxxx xxxxxxxxx xxxxxxxx x v xxxxxxxxxxxxxxx xxxxxxxx institutů xxxxxxxxx a xxxxxxx xxxxxxxx přípravků xxxxxxx xxxxxxxxxxx, přičemž xxxxxxx xxxxxx xxxxxx xxxxxxxx xxxx xxx popsány x xxxxxxxxxx. X xxxxxx xxxxxx xxxxx xxxxxxxxxxx identifikace a xxxxxxxxxxx xxxxxxx x xxxxxxx uvedené x xxxxxx 3.1 xx 3.3 xxxxxxxx xx xxxxx okruhům řešených xxxxxxxx, x xx x xxxxxxxx xxxxxxxx x xxxxxxxxxx hodnoceních xxxxxxxxx léčivých xxxxxxxxx x k xxxxxxxxx xxxxxxxxxx x omezení xxxxxxxxx léčivých přípravků.
3.1 Xxxxxxxxxxxx nákladů a xxxxxxx
3.1.1. Adaptace xxxxxxxx xxx xxxxxxxx xxxxxxxxx xxxxxxxxx léčivých xxxxxxxxx
Xxxxx xxx x xxxxxxxx xxxxxxxx xxx xxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx, xxxxxxx xxxxxxxx xxxxxxxx nařízení č. 536/2014 xxxx jak xx xxxxxx Xxxxxxxx xxxx, xxx x členských xxxxx. Xxxxxxxx xxxxxx xxxxxxxx xx xxxx xxxx x xxxxxxxx xxx xxxxxxx státy xxx xxxxxxxxxxxx spolupráce xxx xxxxxxxxx xxxxxxxxxx xxxxxxxxxx. Xxxxxxxx by xxxxxx xxxx být xxxxxxxxx a xxxxxxxxx xxxxxxxxx xxxxxxxxxx hodnocení x rámci xxxx Xxxxxxxx xxxx v xxxxxxxx zavedení xxxx xxxxxxxxxxx xxxxxx xxxxxx xxxxxxxxxx x provádění, xxxxxxxxxxxxx Evropské xxxx xxx xxxxxxxxxx xx xxxxxxx zemí x xxx xxxxxxxx xxxxxxxxxx xxxxxx xxxxxx xxxxxxxxxx x Evropské xxxx, xxxxx xxxxxxxx následkem xx snižování počtu xxxxxxxxxx hodnocení, xxxxx xx jinak xxxxx xxxxxxxxx x Xxxxxxxx xxxx xxxxxxx nejmodernější xxxxx xxxxxx x xxxxxxx xxx dříve, xxx xxxx xxxxxxxxx xxxxxx xxxxxxxxx xxxxxxxxxxx. Xxxxxxxxx xxxxxxxx xx x xxxxxxxx xxxxxxxxxxx x xxxxxxxxxxx xxxxxxxxx xxxxxxxx xxx klinických xxxxxxxxxxx a xxxxxx xxxxxxxxxx přenášení do xxxxxxxx xxxxx xxxx xxx optimalizace xxxxx xxxxxxxxxxx léčivými přípravky, xxxx xxxxxxx xxxxxxxxx xxxxxxxxxx nových x xxxxxxxxxxxxxx xxxxxxxx xxxxxxxxx xxx pacienty x xxxxxxxxx xxxxxxxx xxxxxxxx xxx celkové xxxxxxxx xxxxxxxxx xxxxxx xxx x xxxxxxxxx xxxxxxx, xxx v xxxx Xxxxxxxx unii. Xxxxxxx xxxxx xxxxxxxxxxxxx xxxxxxx x xxxxxxxx xxxxxxxxx x xxx x xxxxxx realizace xx xxxxxxxx další xxxxxxxx xxxxxxxxxx xxx xxxxxxxxxxxxx xxxxxxxxxxx xxxxxx, kteří xxxxxxxxx xx provedení xxxxxxxxxx hodnocení v xxxxxx xxxxx klinického xxxxxxxxx finanční xxxxxx. Xxxxxxx xx se x dostupnost xxxxxxxx xxxxx xxx pacienty, xxxxx zadavatel je xxxxxxx hradit xxxxx xxxxxxxxx, ale xxxx xxxxxxxxxx xxxxxxxxx, xxx xx xxxxxx xxxxxxxxxx xxxxx, xxxxx xxxxxxx xxxxxxxxxxx. Xxxxxx xxxxxxx xxxxxxxx klinických xxxxxxxxx xx xxxx xxxxxxxx x možnost xxxxxxx xxxxxxxxxx xxxx xxx xx xxxxxx zadavatelů (x farmaceutických xxxxxxxxxxx xx smluvních xxxxxxxxxx xxxxxxxxxx), xxxxxx xxx x na xxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxx, xxx. x poskytovatelů xxxxxxxxxxx služeb, kdy xx xxxxxxx xx xxxx xxxxx xxxxx xxx kryty xx xxxxxxxxx xxxxxxxxxx xxxxxx xx xxxxxx.
Xx xx xxxx xxxxxxxxxx xxxxxxx xxxxxxxxxxxxx v xxxxxxxx xxxxxxxx pracovních xxxxxx, xxxx xxxx xxxxxxxxxxx:
- xx xxxxxx Státního xxxxxx xxx kontrolu xxxxx 32 xxxxxx xxx xxxxx 8 xxxxxx xxxxxx komise). Xxxx xxxxx xxxxxxxxxx xxxx xxxxxx farmaceutických xxxxxxxxxxxx (5), posuzovatelů xxxxxxxxxxxxx hodnocení (2), xxxxxxxxxxxx bezpečnostních xxx xxxxxxxxxx hodnocení (2), xxxxxxxxxx (5), xxxxxxxxxxxx xxxxxxxxxx hodnocení (2) x xxxxxxxxxx xxxxxxxxx xxxxxxxxx-xxxxxxxxxxxxx x xxxxxxxxxxxxxxxxx xxxxxx pro činnost xxxxxx xxxxxx - xxx xxxxx 8 xxxxxx xxxxxx xxxxxx - 16 xxxxxx). Xxxx xxxxxx xxxxx xxxxxxxx kryty z xxxxxxx xxxxxx za xxxxxxxx xxxxxxxxx (xxxxxx xxxxxx). Pro xxxxxxxx xxxxx xxxxxxxxxxx xxxxxxxxxxx xxxxxxxxxxx xxxxxx xxxxxxx xxxxxx komise jako xxxxxxxxx xxxxxx Xxxxxxxx xxxxxx xxx xxxxxxxx xxxxx xxxx uvažovány x části xxxxxxxx xxxxxxxxxx x xxxxxx xxxxxxxxxxxx z EU xxxxx, z xxxxx xxxx xxxxx x xxxxxx výdajů xx xxxxxxxx xxxxxxxxx xx xxxxxxxxxxx správné xxxxxxxx xxxxx;
- na straně Xxxxxxxxxxxx xxxxxxxxxxxxx xxxxxxx xxxx xxxxxx xxxxxxxxxx xxxxxxxx proti xxxxxxxxxx xxxxxxxxxx x xxxxxxx x xxxxxxxxx xxxxxxxxxx xxxxxxxxx. Xxxx třeba xxxxxxxxxx 1 pozici xxxxxxxx xxxxxxxxx x 1 xxxxxx xxxxxxxxx xxxxxxxxx. Činnost na Xxxxxxxxxxxx zdravotnictví xxx xxxx xxxxxxxx xx xxxxxxxxx xxxxxxxxx (x xxxxxxx xx xxxxxx xxxxx v rámci xxxxxxxx) právní xxxxx xxxxxx xxxxxxxx xxxxxxxxxx xxxxxxxxxxx xxxxxxxx x xxxxxxx xxxxxxx xxxxx xxxxxx xxxxxxxx xxxxxxxxxx xxxxxxxxxxxxxxx xx xxxxxxxxxx xxxxxxxx. Xxxx na xxxxxx Ministerstva xxxxxxxxxxxxx xxxxxxx xxxxxx spojená x xxxxxxx xxxxxx xxxxxx jako xxxxxx xxx multicentrická xxxxxxxx xxxxxxxxx, xxxxxx xxxxxxx xxxx xxxxxx jmenování x xxxxxxxxxx xxxxx xxxxxx komise orgánu Xxxxxxxx xxxxxx xxx xxxxxxxx xxxxx xxxxxxxxx xxxxxxxxxxxxx.
3.1.2. Opatření xxxxxxxxx x xxxxxxx xxxxxxxxx xxxxxxxx přípravků
Navrhovaná právní xxxxxx xxxxxxxxxxx x xxxxxxxx k omezení xxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxx mít xxxxxxxx xxxxxx, xxxxxx xx xxxxxxxx xxxxx, xxxxx xx xxxxxxxxxx xxxxxxxxxx x xxxxxxxxxxx menšiny x xxxxxx xx xxxxxxx xxxxxxxxx. Xxxxxxxxxx xxxxxx xxxxxx xxxxxxx xxxxxx xxx xxxxx xx mezinárodní xxxxxxxxxxxxxxxxxxx Xxxxx xxxxxxxxx, xxxxxx xxxxxxxxxxx xxxxx (obce, xxxxx), spotřebitele, xxxxx xxxxxxxxxxx služby x xx vztahu x xxxxxx xxxxxxxxxxxx.
Xxxxxxxxxxx xx xxxxxxxx xxxxx xx xxxxxx rozpočet x xxx xxxxxxx, že xxxxx xxxxxxxx již xxxxxxxxxx x xxxxxxxx xxxx administrativní xxxxxxx xxxxx, xxxxxxxxxx x xxxxxxxxxxxxx xxx xxx xxxxx xxxxxxxxxxxx xxxxxx xxxxxxxxxxxxx xxxxxxxx přípravků xxx potřeby xxxxxxxx x Xxxxx republice Xxxxxxx xxxxxxx pro xxxxxxxx xxxxx x xxxx xxxxxxxxxxxxxxx xxxxxxx xxxxxxxx xxxxxxxx xxxxxx xxxxxx Ministerstvem xxxxxxxxxxxxx. Xxxxxxxx xxxxx x xxxxx ohledu bude xxxxxxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxx, xxxxxxx xx xxxxxxxxx xxxxxx xxxxxx x xxxx xxx 4 xxxxxxxx xxxxxx xxx xxxxx xxxxxxxxxx xx xx xxxx xxxxxxxx.
4 xxxxxxxx xxxxxx xxxxx xxxxxxxx ve 2 pracovních xxxxxxxx xx Státním xxxxxx xxx xxxxxxxx xxxxx (xxxxxx xxxxxxxxxxxx xxxxxxxxxxxx xxxxxxx xxxxxxxxxxx Xxxxxxxxxxxx), x ve 2 xxxxxxxxxx xxxxxxxx xx Xxxxxxxxxxxx zdravotnictví. Činnost xx Ministerstvu zdravotnictví xxxx xxxxxxxx xx xxxxxxxxx zajištění (x xxxxxxx xx nutnost xxxxxxxx řešení) xxxxxx xxxxx agendy odborným xxxxxxxxxx xxxxxxxxxxx xxxxxxxx x xxxxxxx odborné xxxxx xxxxxx xxxxxxxx xxxxxxxxxx xxxxxxxxxxxxxxx xx xxxxxxxxxx xxxxxxxx. Xxxxxxxx xxxxx xx xxxxxx xxxxxxxx tak bude xxxxxxxxx.
Xxxxxxxxx dopad navrhované xxxxxx xxxxxx na xxxxxxx xxxxxxx rozpočty, xxxxxxx xx xxxxxxxxxx xxxxxxxxx zdravotního xxxxxxxxx xxxxx předem xxxxxxxxx. X ohledem xx xx, že xx xxxxx x xxxxxxxxx xxxxx xxxxx do xxxxxxx xxxxxxxxx, ve xxxxxx xx xxxxxxxxxxx xxxxxxxxx xxxx, xxxxx xx částečně uspokojována x prostředků xxxxxxxxx xxxxxxxxxxx pojištění, xxx xxxxxxxxxxxx, xx určitý xxxx xxxxxxxxxx xxxxxx xxxxxx xxx xxxx. Xxxxxx xx xxxxxxx xxxxxxxxxx x veřejného xxxxxxxxxxx xxxxxxxxx xxx xxxxxxxxxxxx xxxxx pozitivní - bez xxxxxxxxxx xxxxxx xx xxxxxxxxx xxxxxxxxxx a xxxxxxxx, xxxxx obvykle představují xxxxxxxx náročnější xxxxxxxx xxxxxxxx xxxxx nebo xxxxx léčebných xxxxxxx. Xx xx týče xxxxxx na xxxxxxxxxxxxx xxxxxxxxx Xxxxx xxxxxxxxx, xxxxxxxxx xxxxxx xx xxxxxxxxxxxx xxxxxxxx přípravků xxxxxxx xxxxxxxxxxxxx subjekty, xxx xxxxxxxxxxxx xxxxx xxxxxxxxx vliv, xxxxx xx xxxxx významně xxxxxxxxxxxxx xxxxxxxxxxxxxxxx systému xxxxxxxx x xxxxxxx xxxxx jeho předvídatelnosti, xxxxxxxxxxxx z xxxxx xxxxxxx podnikatelského rizika. Xxxxxxx xxxxx musí xxx x xxxxx xxxxxxx xxxxxxxx xxxx xxxxxx xxxxxxxxxxxxx.
Xxxxxxxxxx právní xxxxxx xxxxxxxxxxx xxxxx xx xxxxxxx podnikatelské xxxxxxxx x xxx, xx xxxxxx xxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxxxxxx xxxxxxxx přípravků xxx xxxxxx, že hodlají xxxxxxxxxxxx xxxx území Xxxxx xxxxxxxxx xxxxxx xxxxxxxxx, xxxxx xx xx xxxxxxx léčivých xxxxxxxxx xxxxxxxxxx xxxxxxxxx. Xxxxxxxxx však není xxxxxx, xxxxxxxxxx xxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxxxxx, xxx xxx xxxxxx xxxxx xxxx a xxxxxx xx xxxxx xxx všech subjektů xxxxxxxxxxxx se xxxxxxxxxx xxxxxxxx xxxxxxxxx, xxx xxxxx xxxxxxxxxx skupiny xxxxxxxx a xxxxxxxx xxxxxxxxx. Xxxxx dopad xx xxxxxx x xxxxxxx x xxxxxx xxxxxxxxxx xxxxxx xxxxxx xxxxxx xx xxxxxxxx xxxxxx xxxx k xxxxxxxx xxxx, xxxxxx xx xxxxxxxxx dostupnosti xxxxxxxxxxx xxxxxxxx xxxxxxxxx xxx potřeby xxxxxxxx x České xxxxxxxxx x případech hrozící xxxxxx xxxxxxxxxxxxx x xxxxxx jejich xxxxxxxxxx xxxxxxxxx.
Xxxxxxxxx xxxxx xxxx xxx xxxxxxxxxx právní xxxxxx xxxxxxx xx xxxxxxxx, xxxxxxx xxxxxxxxxxx xxxxxxx xxxxxxxx, xxxxxx xxxxxxx dostupnost xxxxxxxx xxxxxxxxx prostřednictvím xxxxxx xxxxxxx před distribucí xxxx území Xxxxx xxxxxxxxx.
3.1.3 Xxxxxxx závěry xxxxxxxxxxxx nákladů x xxxxxxx x xxxxxxxxx 3.1.1 a 3.1.2.
Pro xxxxxxxxxx zajištění xxxxxx xxxxxx xxxxx x xxxxxxxxx spojených x xxxxxxxxx xxxx xxxxx xxxxxxx xxxxx úvazků XXXX x to x xxxxxxxx xxxxx 34 úvazků. K xxxxxxxxxx úvazků xxxx xxxxxxxx xxxxxxxx, x xx v letech 2016 až 2018 - x xxxxxxxxxx xx počtu xxxxxxxxxxxxx xxxxxxx x počtu xxxxxx xxxxxx xxxxxx.
Xxxxxx xxxxxx agend xx xxx xxx xxxxxxxx (xxxxx xxxxxxx řízení xxxxx xxxxxxxxx xxxxxx xxxxxx), x proto xxxxx xxxxxx s xxxxxxxxx zvyšováním xxxxxx (xxx xxxxxxxxx xxxxxxx).
Xxxx xx jednat x xxxx xxxxxx:
Xxxxxxxxxxxxx xxxxxxxxxxx (xxxxxx 5) - x roce 2016 xx počítá x xxxxxxxxx 4 úvazků, xxxx bude xxxxxxx xx xxxxxxxxxx xxxxxx xxxxxxx posuzování, xxx. xx náročnosti xxxxxxxxxxx xxxxx x xxxxxxxxxx, xx xxxx kompilací xxxxxxxxxx xxxxx xxxxxxxxx xxxxxxxxx xxxxx x xxxxxxx, xx ČR xxxx xxxxxxxx xxxxxx xxxxxxxxxxx, xx xxxxxxxxxx xxxxxxxxxx xxxxxxxx, x xx xxxxx xxxxxxxx xxxx xxxxxxxxxx, xxx xx xxxxxxxx nově xxxxxxxxx. Zároveň je xxxxx xxxxxxx xx xxxxxxxx xxxxx žádostí x xxxxxx xxxxxxxxxxxx xxxxxxxx xxxxxxxxx, xxxxxxx xxxxxxxxxx je náročnější x vyžaduje xxxx xxxx.
Xxxxxxxxxxx xxxxxxxxxxxxx xxxxxxxxx (2 úvazky) - 1 xxxxxx x xxxx 2016, další x xxxx 2017 - nyní xxxxxxxxx Xxxxx xxxxx 1 xxxxxxxxxxxxx + výpomocí xx částečný úvazek. X současné xxxx xxxx xxxxxx xxxxxxxxxx xxxxxxxxxxx xxxxxxxxx zprávy, xxx xxxxxx v xxxxxxx členského xxxxx xxxxxxxxxx při postupu xxxxx xxxxxxxx xxxxx, xxxxx xxxxxxx xxxxxx xxxxx xxxxxxxxxxx xxxxx xxx Xxxxx zprávy xxxxxxxxxxx přípravku, což xxxx xxxxxxxxx x xxxxxxxx preklinického xxxxxxxxxxxx.
Xxxxxxxxxxx xxxxxxxxxxxxxx xxx klinických xxxxxxxxx = xxxxxxxxxxx xxxxxxxx části xxxxxxxxxxx (1 úvazek) - xx zajištění agendy xx xxxxxxxx se 2 xxxxxx xx xxxx 2016 (1 xxxxxx xxx xx x xxxxxxxxxxx). Xxxxxxxxxxxx xxxx xxxxx nejprve xxxxxxxx x xxxxxx xxxxxxxxxxx xxxxx, musí xxxxxx xxxxxxxx xx xxxxxxxxxxxx xxxxxxx x Xxxxxxxx lékové xxxxxxxx (xxxx jen XXX). Xxxxx xx x xxxxx agendu, xxxxx xx xxxx v xxxxxxxx xxxxxx xxxxxx xxxxxxxx xxxxxxx xxxxx xxx EMA. Posuzovatelé xxxxx xxxxxx xxxxxxxxxxxx xxxxxxxxxxxx xxxxxxx z xxxxxxxxxx xxxxxxxxx x XxxxxXxxxxxxxx databáze x xxxxxxxxxxxxx x kolegy x xxxxxxxxx xxxxxxxx xxxxxxx.
Xxxxxxxxx správné xxxxxxxx xxxxx (5 xxxxxx) - xxx xxx 2016 xx xxxxxx xx 2 xxxxxx, xxxx xxxx záležet xx xxxxxxxxxxx xxxxxxxxx. Xxxxxxxxxxxxxxx xxxx xxxxxxx xxxxxxx xxxxx než 5. Xxxxxxx xxxxxxxx xxxxxxx xxxxx z xxxxxxxxx zajištění xxxxxxx xxx xxxxxxxxx xxxxxxxxxx, xxxxxxx xxxxxxx xxxxxxxx xxxxx vykonávat xxxxx xxxxxxxxxx správné xxxxxxxx xxxxx, xxx xxxxxxx x x xxxxxxxxx xx účast xxx xxxxxxxxxx xxxxxxxxxxxx xxxxxxxxxx x ostatními xxxxxxxxx xxxxx, vedenými x xxxxxxxxxxxxxx EMA. Xxx xxxxx xxx 375 xxxxxxx o xxxxxxxx xxxxxxxxxx xxxxxxxxx/xxx x xxx 1600 „xxxxxxxx“ xxxxxxxxxx xxxxxxxxx v xxxxx roce je xxxxxxxx počet inspektorů xxxxxxxx nedostačující. K xxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxx xx xxxxx xxxxx, xxxxxx nelze xxxxxx xxxxxxxxxxx xxxxxxxx.
Xxxxxxxxxxx xxxxxxxxxx hodnocení (3 xxxxxx) - xxx xxx 2016 se xxxxxx s 1 xxxxxxx, x xxxxxx xxx x xxxx 2017 a 1 x xxxx 2018. Xxxxxxxxxxxx xxxxx xxxxxxxxxx xxxxxxxxxx x rámci xxxxxxxxxx xxxxxxxxx x xxxxxxxxx členskými xxxxx x xx území XX s ostatními xxxxxxxxxxxxxxxx xxxxxxxx (xxxx. xxxxxxx experti aj.), xxxxx zajišťovat vkládání xxxxxxxxxx xx xxxxxxx, xxxxxx xxxx xxx xxxxxxxxxx xx xxxxx XX.
Xxxxxxxxxx xxxxxxxxxxxxx xxxxxx xxxxxxxx xxxxxx xxxxxx (4 xxxxxx). X xxxxxx xxxxxx xx xxxxx xxxxxxx již xxx xxx 2016. Xxxx xxxxxxxxxx xxxxx xxx za úkol xxxxxxxx xxxxxxxxx xxxxxx xxxx xxxxxxxxx xxxxxxxx xxxxxx komise jako xxxxxxxxx xxxxxx Ústavu, xxxxxxx xxxxxxxx xxxxxxxxx, xxxxxxxx xxxxxxxxxx xxxxxx, xxxxxxxxx proškolení pro xxxxx etické xxxxxx (xxxxxxxxx xxxxxxxxx xxxxxxxxxx), xxxxxxxxx koordinačních xxxxxxx x XX xxx xxxxxxxxxxxx xxxxxxxxxx xxxxxx xxxxxx. Dále xxxxx xxxxxxxxxxx xxxxxxxx xxx Xxxxxxxxxxxx zdravotnictví xxx xxxxxxxxxxx xxxxxxx o xxxxxxxx x xxxxxx xxxxxx. S xxxxxxx xxxxxx xx xxxxx xxxxxxx x xxxxxxxxxx xx potřebu zvýšení xxxxx xxxxxx xxxxxx xxxxxx x xxxxxxx xxxxxxxxxxx období a x xxxxxxxxxx xx xxxxx předkládaných žádostí. (xxx počtu 8 xxxxxx etické komise - 16 xxxxxx - xx xxxx 2019 či 2020 - xxxxx skutečného xxxx xxxxxx účinnosti xxxxxxxx č. 536/2014).
|
xxxxx xxxxxxxxxx xxxxxx, xxxxxxxxxxxx na XXXX x souvislosti x adaptací nařízení 536/2014/EU |
||||||
|
2016 |
2017 |
2018 |
32 xxxxxx |
|||
|
4 |
XX |
1 |
XX |
|||
|
1 |
XXX |
1 |
XXX |
|||
|
1 |
XXXXX |
|||||
|
2 |
XXX |
2 |
XXX |
1 |
XXX |
|
|
1 |
XXXX |
1 |
XXXX |
1 |
XXXX |
|
|
4 |
XXXX |
8 |
XXXX |
4 |
XXXX |
|
|
13 |
13 |
6 |
||||
xxxxxxx:
xxxxxxxxxxxxx xxxxxxxxxxx (XX) - celkem 5
xxxxxxxxxxx xxxxxxxxxxx xxxxx (XXX) - celkem 2
posuzovatelé xxxxxxxxxxxxxx dat KH (XXXXX) - xxxxxx 1
xxxxxxxxxx správné klinické xxxxx (INS) - xxxxxx 5
xxxxxxxxxxxx KH (XXXX) - xxxxxx 3
xxxxxxxxxxxx xxxxxx XX - (XXXX) - 4 (xx xxxxx xx xxxxxxxx xxxxx xxxx xxxxxxxx xxxxxx XX, xxxxx je xxxxx připravit prvotní xxxx administrativy
(formuláře, pracovní xxxxxxx xxx.) než xxxxx xxxxxxx XX xxxxxxxx xxxxxxx, xxx xxxxx xxxxx xxxxxxxx xx xxxx xxxxxx xxxxxxxxx
xxxxxxxxxxxx centra XX - (KOEK) – 12 každá xxxxxxx XX xx měla xxx 2 xxxxxx xx zajištění xxxxxxxxxxxxxxxxx xxxxxxx související x XX
xxxxx xx předpokládá xxxxxxxx x dalších 12 XXXX xx xxxxxxxxx zřízení xxxxxx XX
xxxxx xxxxxx potřebných xx XXXX pro xxxxxxxxx xxxxxxxx xxx xxxxxxxx nežád.reexportům, 2016
2 xxxxxx
2 posuzovatelé xxxxxxxxx
34 xxxxxx
2 xxxxxxxx úvazky xxx MZ - xxxxxxxx x xxxxxxx xxxxxxxx xxxx xxxxxxxx x xxxxxxx.
Xxxxx xx xxxx xxxxxx agend xxxxxxxxxxxxx x xxxxxx xxxxxx opatření xxxxxxxxx xxxxxxxxx xxxxxxxxx, xxx xxxxxx zajištění xx xxxxx xxxxxxx x xxxxxxxxx x 2 xxxxxx xx XXXX x o 2 xxxxxx xx XX. Xxxxx xxxxxxx xxxxxxxxx x xxxxxxxxxxxxx nedostupnosti xxxxxxxx xxxxxxxxx, XX xxxxxxx xxxxxxxx agendu xxxxxxxx s vydávání xxxxxxx x opatření xxxxxx xxxxxx xxxxxxxxxxx xxxxxxxxx. V souvislosti x xxxxx xxxxxxxxxxxxx xx nutnost průběžné xxxxxxx v xxxxxxx xxxxxxxx xxxxxxxxxxx, xxxxxxxx xxxxxxxxx je otázkou xxxxxxxxxxx a xxxx xxxxxxxxx xxxxx spolupráci xxxx xxxxx xxxxxxxxxxx, x xx i x xxxxxxx xx xxxxx xxxx xxxxxxx.
Xxxxxx xxxxxxx:
Xxxxxxxxxxxx xxxxxxxxxxxxx xxxxxxxxxxx - xxxxxxx xx. 13
Xxxxxxxxxxxx xxxxxxxxxxxxxx xxx/xxxxxxxx xxxxx xxxxxxxxxxx - xxxxxxx tř. 13
Xxxxxxxxxxx xxxxxxxxxxx xxxxxxxxxxx - xxxxxxx xx. 13
Xxxxxxxxxx xxxxxxx xxxxxxxx xxxxx - xxxxxxx xx. 13
Xxxxxxx xxxxxxxxxxxxx xxxxxx xxxxxx komise - xxxxxxx tř. 13
Xxxxxxxxxxxx - xxxxxxx xx. 12
Xxxxxxxx na oblast xxxxxxxxx XX - xxxxxxx xx. 13
Xxxxxxx xx xxxxxx xxxxxxxxx XX - xxxxxxx xx. 13
Xxxxxxxxxxx pro xxxxxx xxxxxxxxx SÚKL - xxxxxxx xx. 13
Xxxxxxxxxxxxx xxxxx xxxxxxxx xxxxxxx xxxx xxxxxxx xxxx
|
Xxxxxxx xxxxx |
Xxxxxx náklady |
průměr |
Celkem /xxx |
Xxxxxxxx xxxxxxx mzdy XXXX |
Xxxxxxx xxxxxxx - xxxxxxx, xxxxxxxxxxx xxxxxxx, xxxxxxxxxx, … xxx 50 000/xxx |
|
|
4 xxxxxxxxxxxxx xxxxxxxxxxxx |
13 |
20 990-26 220 Xx |
23 600 Xx |
1 132 800 Xx |
1 529 280 Kč |
200 000 |
|
1 xxxxxxxxxxx xxxxxxxxxxx XXX |
13 |
20 990-26 220 Xx |
23 600 Xx |
283 200Xx |
382 320 Xx |
50 000 |
|
1 klinický xxxxxxxxxxx (xxxxxxxxxxxx xxxx - XXXXx) |
13 |
20 990-26 220 Xx |
23 600 Kč |
283 200 Xx |
382 320 Xx |
50 000 |
|
2 xxxxxxxxxx XXX |
13 |
20 990-26 220 Xx |
23 600 Kč |
566 400 Xx |
764 640 Xx |
100 000 |
|
1 xxxxxxxxxxx XX |
12 |
19 360-24-180 Xx |
21 770 Kč |
261 240 Xx |
352 674 Xx |
50 000 |
|
1 vedoucí + 3 koordinátoři etické xxxxxx |
13, 12 |
20 990-26 220 Kč19 360-24-180 Xx |
23 600 Xx21 770 Xx |
283 200 Xx261 240 Xx |
382 320 Xx352 674 Xx |
200 000 |
|
2 xxxxxxxxxxxx xxx xxxxxx reexportu |
13 |
20 990-26 220 Xx |
23 600 Kč |
566 400 Xx |
764 640 Xx |
100 000 |
|
15 xxxxxx - xxxxxxx xxxxxxx xx xxxx xxxxxx cca 5 000 000 Xx/xxx 2016 |
3 637 680 Kč |
4 910 868 Kč |
750 000 Xx |
|||
Xxxxxxx xxxxxxxx xxxxxxxxxx xxxxxx xx XX xxxx odůvodněna xxxx.&xxxx; Xxxxxxxx xx xxxxxxx x xxxxx stávajícího xxxxx neobsazenosti.
Navýšení xx xxxxxxx x rámci xxxxxxxx výdajů na xxxxx x počtu xxxx kapitoly Xxxxxxxxxxxx xxxxxxxxxxxxx. Xxxxxxxxxx dopad x platové xxxxxxx xx xxxxxxxxx.
Xxx xxxxxxxxx xxxx xxxxxx - xxxxx provozní xxxxxxx xx xxx 2016 x 2017 (xxxxxxxx, xxxxxxxx, aj.) - 2016 cca 750 xxx. Xx; 2017 1,5 xxxxxxx Kč (xxxxxxxx xxxxxxx xxx xxxxxxx xxxxxxxx komisí + xxxxxx provoz).
Mzdové xxxxxxx xx vedoucího xxxxxxxxxxxxx centra xxxxxx xxxxxx a xxxxxxxxxxxx xxxxxx xxxxxx - xxx 2016 cca 2 xxxxxxx; xxxxxxx xx vybavení sídel xxxxxx xxxxxx xxxxxx x jejich xxxxxx - vybavení xxx 3 xxxxxxx/xxx (xxx xxxxx počtu xxxxxx xxxxxx komise - xxxxx náklady) - xxxxxxx x xxxxxx xx činnost etické xxxxxx.
Xxxxxxx xxxxx xxxxxxx x xxxxxxxxx prostředků Xxxxxx, xxxxxxx-xx podporu x EU xxxxx.
X xxxx 2016 a xxxx by to xxxx i xxxxxxx xx xxxxxxxxxx, xxxxxxx (x EMA xx x xxxx xxxxxxxx xxxx xxxxxxxx za xxxxxxxxxx Xxxxxxxx xxxxxx xx.) xxx 2 xxxxxxx/xxx.
3.2 Xxxxxxx
3.2.1. Adaptace xxxxxxxx x xxxxxxxxxx xxxxxxxxxxx xxxxxxxxx léčivých xxxxxxxxx
Xxxxxxx xxxxxxx xx xxxxxxxxx xxxxxx xxxxxx xxxxxxxxxx hodnocení xxxxxxxxx xxxxxxxx přípravků xxxxxxxxx xxxxxxxxx x založení x následném xxxxxxxxx xxxxxxx EU x xxxxxxxx XX. Xxxxxxx xx tato xxxxxxxx xxxxx xxxxxxx x xxxxxxxxxx Xxxxxxxx unie. Xxxxxxx xxxxx budou xxxxxxxxxx xxxxxx napojení xx xxxxxx x xxxxxxxx Xxxxxxxx unie, xxxxxxxxxxx technické xxxxxxxxxxx xx xxxxxx xxxxxxxxx xxxxx, zajištění dostatečných xxxxxxxx xxxxxx, IT xxxxxxx xxx komunikační xxxxxxxxx na území Xxxxx republiky x xxxxxxxxxxx xxxxxxxxx xxxxxxxxx xxx xxxxxxx etické xxxxxx. Xxxxxxx xx xxxxx být z xxxxx xxxxxxx z xxxxxx XX fondů, xxxxx xx byly xxxxxxxx xxxxxxxxxx xxxxxxx, x xxxxx xxxxxx xxxxxxx xxxx. Po xxxxxxxx xxxxxxx xx xxxxxx se xxxxxxxxxxxxxxxx, xxx. xxxxxxx výdajů xx posouzení xxxxxxx x xxxxxxxx xxxxxxxxxx xxxxxxxxx x xxxxxxx x xxxxxxxx významných xxxx x xxxxxxxxxx xxxxxxx xxx xxxxxxxxxx xxxxxxxxxxx xx xxxx xxxxxx finanční xxxxxx xx xxxxxxx xxxxxxxxxx XX xxxxxxx x xxxxxxx xxxxxx xxxxxx.
X xxxxxxxxxxx x xxxx xxxxxxxx ohledně xxxxxxx, xxxx. xxxxxxxxxxxxxxx, xxxxxxx Xxxxxx xxxxx xxx xxxxxxxx xxxxx x xxxxxxxxxxx xxxxxxxxxx, kdy x uplynulých letech xxxx hrazeny xxxxxxx xx xxxxxx x xxxxxxxxx Xxxxxxxx xxxxxx xxx kontrolu xxxxx, x xx včetně xxxxxxxx xxxxxxxxxxxxx xx xxxxxxxxxx xxxxxxxxxxxxxx xxxxx, xxxxxxxxx x xxxxxxxxxxx x požadavky na xxxxxxxxxxxxx x efektivní xxxxxxxxxxxx xxxxxx xxxxxxxxxx xxxx členskými státy, Xxxxxxxxx komisí x xxxxxxxxxxxx subjekty, cca xx 75 - 80 % z xxxxxxxxxxxxxxxx xxxxxx.
Xxxxx se xxxx xxxxxx klinického xxxxxxxxx x souvislosti x klinickým xxxxxxxxx, xxx úprava systému xxxxxxxxxx xxxxxxx o xxxxxxxx hodnocení x xxxxxxx x xxxxxxxxx x sebou přinese xxxxxxx xxxxxxxx xxxxxx (xxxxxxxxx x důvodu xxxxxxxxx xxxxxxxx lhůt x vyřízení xx xxxxxxxxxxx 65 xxx xx 21 xxx, x xx xxx xxxxxxxx xxxxxxxxxxx),&xxxx; xxxxxxx xxxx xxx např. xxxxxxxx předpokládá xxxxxxx xxxxxxxxxx xxxxxxxxxxxxxx portálu (xxx xxxxx xxxxxxxx), xxxxx xxxxxxxxxxxxxxx x xxxxx xxxx xxxxxxxxxxxxxxx xxxx xxxxx xxxxxxxxxx xxxxxxx x xxxxxxxx xxxxxxxxx x Státní xxxxx xxx xxxxxxxx xxxxx tedy musí xxxxxxxx (zřídit) xxxxxx, xxxxxx xx do xxxxxxxxxx xxxxxxxxxxxxxx xxxxxxx xxxxxxx. Xxxxxxx xxxxxxxx xxxxxxx xxxxxxxx xx xxxxxx Xxxxxxxx ústavu xxx xxxxxxxx léčiv xxxxxxx xxxxxxxxx, x xx nejen na xxxxxxx, ale i xxxxxxxx xxxxxx, xxxxxx xxx., xxxx investice xxxx xxxxxxx xxxxx xxxxxxxxxxx, ale bude xxx průběžný xxxxxxxxx. Xxxxxxxx k xxxx, xx existence evropského xxxxxxx xx xxxxxxxxxxxxx xxxxxxxxx, xxx Xxxxxx xxxxx xxx xxxxxxxx xxxxx nemá možnost x xxx vůli xxxxxxxxxx, že se xx evropského portálu xxxxxxxxx x žádosti xxxx xxxxxxxx x xxxxxxxx xxxxxx xxxx xxxxxxx, neboť by xx znamenalo kompletní xxxxxxxx Státního ústavu xxx kontrolu léčiv, xxxx. xxxx XX, x procesu xxxxxxxxxx xxxxxxxxx.
Xxxx xxxxx x xxxxxxxxxxx s xxxxxxxxx xxxxxx s ohledem xx xxxxx systému xxxxxxxxxx žádostí x xxxxxxxx xxxxxxxxx, xxx xxxxxxxx x x xxxxxxx na xxxxxxxxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxx xxxxxx, xxxx xxxxx Xxxxxx ústav xxx xxxxxxxx léčiv xxxxx x technické xxxxxxxxxxx, xxx xxxx xxxxxxx xxxxxxxxxx (xxxxxxxx x xxxxxxxxxxx technika, vybavení xxxxxxx apod.), xxx xxxxxx vyžaduje xxxxxxxxx xx strany Státního xxxxxx xxx xxxxxxxx xxxxx.&xxxx; Aplikace klinického xxxxxxxx xxx bez xxxxxx na xxxxxxxx x zákoně x xxxxxxxx xxxx xxxxxxx x finančními náklady. Xxxxxxxx xx snaze xxxxxxx státní rozpočet xx xxxxxxx, Státní xxxxx pro xxxxxxxx xxxxx xxxxxxxx xxxxxx xxxx xxxxxxx x xxxxxxxxxx prostředků xxxxxxxxxx x náhrad xxxxxx. Xx xxxx xxxxxxxxxx, xx xxxxx xx xxxx xxxxxxxxxx xxxxxx x xxxxxxxxx, xxxx xxx počítáno s xxx, xx veškeré xxxxxxx xxxxx xxxxx x xxxxxxxxxxxx xxxxxx.
Xxxxxxxxx xxxxxx xxx xxxxxxxx xx xxxxxx x xxxxxxxx XX - xxx xxx xxxxx xxxxxxxx, x xxxx xxxxxx ještě není xxxx ani xxxxxxxx xxxxxxxxxxx xxx portál x xxxxxxxx XX x xxxx zcela xxxxx, xxxxx xxxx (xxxxx xxxxx) komunikační xxxxxxxxx xxxx zahrnovat. X toho vyplývá, xx xxx xxx xxxxx odhadnout xxxxxxx xx xxxxxx xxxxxxxxxxxx xxxxxxxxx xxxxx - xxxxxx xxxx xxxxx xxxx xxxxxxxx xxxxxxxxxx xxxxxxxxx x XX, xxxxx xxxxxxxxx xxxxxx xxx technické parametry x xxxxxxxx + xxxxxxxxxxx systém xx xxxxx XX (xxxxxxxxxxx xxxxxx xxx komunikaci Xxxxx, xxxxxx xxxxxx, xxxxxxx, xx.) - xxx odhadovat náklady xxx 30 milionů Xx, které xxxx xxxxxx Xxxxx z xxxxxxxxx xxxxxxxxxx, xxxxxxx-xx xxxxxxx x XX xxxxx.
Xxxxxxxx x 32 xxxxxx xx xxxxxx Xxxxxxxx xxxxxx xxx xxxxxxxx léčiv xxx xxxxxx xxxxxxxxxx xxxxxxxxx.
Xxxxxx xx xxxxxxxxxx xxxxxxxx
Xxxxxx xx xxxxxxxxxx
- Xxxxxx XX x xxxxxxxx xxxxxxxxxxx xxxxxxxxxxx by xxxx zadavatelům xxxxxxxx xxxxxx xxxxx; xxxx xx xxxxxxxxxx, xx xx xx měly xxxxxx xxxxxxx na XX - to xx otázkou, xxxxxxx xxxxxxxx dává více xxxxxxxxxx xxx je xxx xxxxxxxxxx x xxxxxxxx xxxxxxxxxxx, proto xxxxxxxx xx xxxxxxxx xxxx xxxxxxxxx xxxxxx x xxxxxxxx xxxxxx xxxxxxxx snížení.
- Xxxxxxxx xxxxx striktně stanovuje xxx. xxxx posouzení. Xxxxx xxxxxxxxx nedoplní xxxxxxxxxxx způsobem xxxxxxxxxxx xxx zaslaných xxxxxxxxxx, xxxx xxxxxxxx xxxxxxxxx xxxxxxxxx xxxx považováno xx stažené (xxx xxxx, v které xxxxx posuzování se xxx xxxxx). Doplnění xxxx xxxxxxxx xxxxx 1x, xxx xx xxx v xxxxxx xxxx, xxx xx xxxxxxxxx xxxxxxxx xx „xxxxxxxxxx“ a xxxx xx xxxxxxx xxxxxxxxxx xxxxxxx podruhé xx xxxxxxxx xxxxxxxxxx x xxxxxxxxxx. Xx již xxxxxx možné, tím xxxx, že xx xxxxxxxxxxx xxxx xxxxxxxxxxx xxx xxxx X xxxxx 1 xxxxxxx xxxx = xxxxxxx xxxx zpravodaj. Čas xx xxxxxxxx dokumentace xx xxxxxxxx xxxxxxxx xx 12 xxxxxxxxxxxx xxx (xxxx x xxxxx max. 10, xxx xxxx xxx x méně xxxxxxxxxx xxx). Xxxx může xxxxxxxxx xxxxxx více xxxx, který xx xxxxxx s xxxxxxx xx xxxxxxx řád (xxxxxxxx času xx xxxxxxxx xxx xxxxxxxxxx - xxxxx i xxxxx). Xx xxxx x xxxxx xxxx x zamítáním xxxxxxxxxx xxxxxxxxx, xxxxxx znovupodávání x xxxxxxxxxx xxxxxxxxxx, xxx xx xxxxx xxxxx k dalším xxxxxxxx xxxxxxxxxx x xxxxxxxx xxxxxxx x xxxxxxxx xxxxxx.
- Výhodou xxxx xxx xxxxxxxxxx, xxxxx provádí xxxxxxxxxxxxxx xxxxxxxx xxxxxxxxx (x XX xxx 90-95%) x mají xxxx xxxxxx x XX (xx bude xxx 80-85% z xxxxxxxxxxxxxxxx XX), v současné xxxx xxxxxxx xxxxx xxxxxx xxxxxx, což xx xxxx xxxxxxxxx. Xxxxxx to xxx xx výrazně xxxxxxxxxx xxxxxxxxxx xxxxxxxx xx. xxx xxxx II.
- Xxxxxxxxxx xxxxxxxx xxxx xxxxxx xxxxxxxxxx xxxx xxxxxxxx, zjednodušení xx xxxxx x doznačování xxxxxxxxxxx xxxxxxxx xxxxxxxxx. Xxxxx xxxxxxxxxxx xx xxxx xxxx „xxxxx“ xx xxxxxx xxxxxxx x pomoci nekomerčním xxxxxxxxxxx x xxxxxxxxx xxxxxxxxxxx - xx xxxxxxx, xxxxx prostoru xx xx budeme x xxxxx systému xxx.
- X xxxxxxx xx skutečnost, xx xxxxx není xxx xxxxxx XX, xxx xxxxxxxx XX, nelze xxxxx xxxxxx xxxxxxxxxxxxx.
Xxx xxxxxxxxx xxxxxxx, xxx xxxx xxx zadavatelem:
- Xxxxxxxxxxxxx xxxxxxxxxxx
- Xxxxxxxxxxxxx xxxxxxxxxxx xxxxxx (xxxxxx x xxxxxxxxxxxxxx)
- Vysoké xxxxx
- Xxxxxxx společnosti
CRO (XxxxxxxxXxxxxxxxXxxxxxxxxxxx) –xxxxxxxxxxx, které x oblasti xxxxxxxxxx xxxxxxxxx pro zadavatele xxxxxxxxx v xxxxxx xxxxxxxx xx SÚKL, xxxxxxxx xxxxxxxx, xxxxx xxxxxxxxx xxxxxxx s xxxxx xxxxxxxxxx hodnocení x se xxxxxxxxxxxx, xxxxxxxxxx klinického xxxxxxxxx, xxxxxxx i farmakovigilanční xxxxxxx (xxxxxx xx xxxxxxx xxxx xxxxxxxxxxx x CRO; xxxxxxxxx xxxxxx rozsah xxxxxxxx, xxxxx xxx xxxx XXX xxxx a xxxxxx xxx x xxxxxxxxxx)
- Xxx xxxxxxxx xxxxx žádosti o xxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxxxxx xxxxxxxx xxxx xxxxxxxx členským xxxxxx xxxxxxxxxxxxxxx xxxxxxx XX. Xx xxxxxxxxxxxxx, xx xxx xxxx X (xxxx X dokumentace) xxxx xxxxxxxxxx zadavatel xxx xxxxxxx xxxxxxx xxxxx xxx; co xx xxxx xxxx XX (xxxxx XX xxxxxxxxxxx, která xx xxxxxxxx pouze ke xxxxxxxxxxx členskému xxxxx, xxxxx xxxx xxxxxxxx, xxxx-xx xxxx xxxxxxxxx x xxxxxx x xxxxx xxxxxxxx xxxxxx xxxx „kontaktní xxxxx“ xxx xxx xxxx X, v xxx xxxxxxx xx xx xxx xxxx xxxx XXX.
- Xx se xxxx xxxxxx xxxxx xxxxxxxx - xxxxxxxxxx, xxxxxxxxx míst xxxxxxxxxx xxxxxxxxx, xxxxxxxxxxxx…. Xx xx xxxxx být xxxxxx, xxxx současně
Pokud xx xxxx míst xxxxxxxxxx xxxxxxxxx
- Nově xxxxxxxxx xxxxxxxxxxx xxxxxxx xxxxxxxx praxe pro xxxxxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxxxxxxx (xxxx xxxxxxxxxxx xx xxxxxxxx xxx xxxx, xxxxxxx xxxx. xxxxxxxxxxx xx xxxx); xxxxxxxx xxxxxxxxx xxxx I (1.xxxxxx xxxxxxx) - xxxx; xxxxxxx místa xxxxxxxxxx xxxxxxxxx mohou požádat x xxxxxx xxxxxxxxxxx, xxx není to xxxxxx xxxxxxx xxxxxxxxx; xxxxx xx vyžadovat xxxxxxx xxxxxxxxxx
- Xxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx xxxx xxxxxxxxx x xxxxxxxxxxxxx xxxxxxxxxxxxx xxxxxxxxxxx xxxxxx
- Adaptace xx xxxxx xxxxx xxxxxx xxx xxxxx xxxxx
- Xxxxxxx nákladů xx xxxxxxxxx služby - xxxxxxxx neřeší, nemělo xx být nařízením xxxxxxxxx
Xxxxx se xxxx xxxxxxxxxxxx
- Činnost xxxxxxxxxxxx x oblasti xxxxxxxxxx xxxxxxxxx xxxxxxx změn, xxxxxxxx xxxxxxxx xx xxxxxx xxx xxxxx xx xxxx xxxxxx
- Xxxxxx o průběhu xxxxxxxxxx xxxxxxxxx - xxx x xxxxxxxx xxxx xxxxx xxx XXX (XXX X6 - GCP = XxxxXxxxxxxxXxxxxxxx), xxxxxxxxxx xx xxxx podávat zprávy x xxxxxxx x xxxxxx xxxxx xxxxxxxxxx xxxxxxxxx xxxxxx xxxxxx, xxxxx klinické xxxxxxxxx xxxxxxxxx
- Xxxxxxxx xxxxxx xx provedení klinického xxxxxxxxx - ¨xxxxxxx xxxxxx xxxxxxxxx - xxxxxxxx xx xxxxxx xxx xxxx xx xxxx xx xxxxxx
Xxxxxx xx xxxxxxxxxx xxxxxxxxxx
- xxxxxxx xxxxxx xx xxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxx. X xxxxxxxx xxxx xx xxxxxxxxxx xxxxxxxxxx XXXX x xxxx oblasti (xxxxxxxxx o xxxxxxxxxx xxxxxxxxxxx, xxxxxxxxxxxx x xxxxxxxxxx účasti v xxxxxxxxx xxxxxxxxx, zajištění xxxxx xxxxxxxxxxxxxx). Xxxx xxxxxxxxxx XXXX xxxxxxxxxxx x nadále. Snahou xxxx , xxx xx xxxxxxxxxx xxxxxxxxxx xxxxxxxx xx činnosti xxxxxxxx komisí.
- nařízení xxxxxx xxx xxxxxxxx xxxxxx dopad na xxxxxxxxxx xxxxxxxxxx
Xxxxx xx xxxx státní xxxxxx, xxxxx SÚKL a Xxxxxxxxxxxx zdravotnictví, xxxxxxxx xxxxxxxxxxx i činnost
SÚJB (Xxxxxx xxxx xxx xxxxxxxx xxxxxxxxxx)
- Posuzování xxxxxxx o xxxxxxx xxxxxxx neregistrovaného xxxxxxxxxxxx x XX - xxxx současný stav
MŽP
- Xxxxxxxxxx xxxxxxx x xxxxxxx xxxxxxx xxxxxxxxxxx xxxxxxxx přípravky x xxxxxxx XXX v XX - xxxx xxxxxxxx xxxx
XXXX
Xxxxxxxxxx xxxxxxx x možnost xxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx x xxxxxxxxxxxxx lidskými xxxxxxx x XX - xxxx xxxxxxx xxx xxxxxx xxxxxxx xx lidských subjektech, xxxxx nebylo xxxxxx; XXXX agendu xxxxxxx x xxxxxxxx xxxxxxxxxxxxx xxxxxxx xxx má, xxxxxxx xxxxxx xxxxxx x xxxxxx xx xxxxxx xxxxxxxx subjektů, xx xxxxxx xxxxxxxxxx xx xxxx zapojeno (xxx xxxxxx o xxxxxxxxxxxxx bb.) i xxxxxxxxxxxx xxxxxxxxxxxxx
3.2.2. Xxxxxxxx xxxxxxxxx x xxxxxxx xxxxxxxxx léčivých xxxxxxxxx
Xxxxx xxx x navrhovanou xxxxxx xxxxxx xxxxxxxxxxx x opatření x xxxxxxx reexportu xxxxxxxx xxxxxxxxx, xxxxxxxxxxx xx xxxxx nákladů xxxxxxxxx xx zavedením xxxxxx xxxxxxxxx a vyhodnocování xxxx, zda xxxx xxxxxxxxx xxxxxxx xxxxxxxx x Xxxxx xxxxxxxxx, x dále s xxxxxxxxxx xxxxxxxx v xxxx xxxxxxxxx, xxx xxxxxxxxxx xxxxxxxx přípravků xx zahraničí způsobí xx xxxxx xxxxx xxxxxx xxxxxxxxxx. Xxxx xxxxxxx xxxxx řešeny x xxxxx xxxxxxxxxx xxxxxxx financování xxxxxxxx Xxxxxxxx xxxxxx xxx xxxxxxxx léčiv a Xxxxxxxxxxxx xxxxxxxxxxxxx.
Xxxxxxxx x 4 pracovní xxxxxx xxxx spočívat ve 2 xxxxxxxxxx úvazcích xx Xxxxxxx xxxxxx xxx kontrolu xxxxx (xxxxxx zpracovávání xxxxxxxxxxxx xxxxxxx xxxxxxxxxxx Xxxxxxxxxxxx), x xx 2 xxxxxxxxxx xxxxxxxx xx Xxxxxxxxxxxx zdravotnictví. Činnost xx Ministerstvu xxxxxxxxxxxxx xxxx xxxxxxxx xx xxxxxxxxx zajištění xxxxxx xxxxx xxxxxx xxxxxxxx xxxxxxxxxx xxxxxxxxxxx xxxxxxxx x xxxxxxx odborné xxxxx xxxxxx xxxxxxxx xxxxxxxxxx xxxxxxxxxxxxxxx xx xxxxxxxxxx vzdělání.
Pokud xx xxxx dopadů xx xxxxxxxxxx subjekty:
Dopady xx xxxxxxxx xxxxxxxxxx x xxxxxxxxxx
Xxx xxxx xxx xxxxxxxxx - xxxxxxx xxxx právnická osoba, xxxxx xxxxxxxx xxxxxxxxxx §26 xxxxxxxx 4 xxxxxx o xxxxxxxx
- Xxxxxxxxxx xxxxxx úprava xxxxxxx xxxxxxxxx stávající xxxxxxxxxx xxxxxxxx xxxxxxx x §33 zákona x léčivech xxxxxxxxxx xxxxxxxxx o léčivých xxxxxxxxxxx xxxxxxxx na xxx x Xxxxx xxxxxxxxx. Nově xxxx xxxxxxx xxxxxxxxxx xxxx xxxxx x xxxxxxxxxxxx xxxxxxxxxxx x xxxxxxxxxxxx xxxxxx, aby tato xxxx xxxx xxxxxxxxxx x xx xxxxxxxxxxxxx xxxxxx dostupná Xxxxxx xxxx informační xxxxx, xxxxx xxxxxxxxx xxxxxxxxx x xxxxxxxx léčivého xxxxxxxxx, xxxx xxxxxxxxx xxxxx, xxxxxx xxxxxxxxx xx trh x Xxxxx republice.
- Xxxx xxxxx xxx budou xxxxxxx Xxxxxx xxx xxxxx xx xxxxxx xxxxxxxxx pro xxxxxxxxxx xxxxx xxxxx xx xxxx x České xxxxxxxxx, xx xxxxxx x posouzení xxxxxxxxxxxxxxx xxxxxx léčivého xxxxxxxxx x x xxxxxxxxx xxxxxxx xxxxxx distribuce xxxxxxxx léčivého xxxxxxxxx xx zahraničí, xxxxx xx xxx xxxxxx xx seznamu xxxxx §77c zákon o xxxxxxxx.
- Právní xxxxxx xxx xxxxxxx xxxxx xxxxxxx x xxxxxx xxxxxxxxxx zajistit xxxxxxx xxxxxxxx xxxxxxxxx x xxxxxxxx xxxxxxxxxxx xxx xxxxxxx xxxxxxxx x XX.
Xxxxxx xx xxxxxxxxxxxx
Xxx může xxx xxxxxxxxxxxxx:
- Xxxxxxx xxxxxxxx x xxxxxxxxxx léčiv xxxxxx Xxxxxxx xxxx xxxxxxxxxx regulační xxxxxxxxx x xxxxxxxx xxxxx XX
- Xxxxxxxxxxxx xxxxx, x případě xxxxxxxx xxxxxxxxx xxxxxxxxx xx xxxxxxx podle §77c xxxxxx x xxxxxxxx, xxxxxxxxxx distribuci xx xxxxxxxxx prostřednictvím xxxxxxxxxxxxxx xxxxxxxxx. Xxxxx xxxxxx xx 15 dnů xx jeho zaslání xxxxxx OOP xxxxx §77d xxxx xxxx xxxxxxxx xxxxxxx.
- Většina xxxxxxxxxxxx dodávajících xxxxxx xxxxxxxxx xxxxxx xxxxxxxx xxxxxxx na xxx xxxxxxxx xxxxx xxxxxxx, xxx xxxxxxx x xxxxxxx administrativní xxxxxx xxxxxxx se xxxxxxxxxxx xxxxxxx.
- Xxxx xxxxxxxxxxxx, xxxxx xxxxxxxx, případně x xxxxxxxxxx xxxxxxx, xx xxxxxxx x xxxxxxxxx xx xx xxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxx xx xxx x Xxxxx xxxxxxxxx xx zahraničí, pak xxxx muset upravit xxxxx aktivity xxxxxxxxxxxxx xxxxxxxx. Xxxxxxx jim xxxxx x x x xx větší xxxx bude xxxxxxxx xxxxx xxx xxxxxxxxxx xxxxxxxx přípravků xxxxxxxxxxx x xxxxx republice, xxxxxxx xx xxxxxxx.
Xxxxxx xx „lékárny“ - xx xxxxxxxxxxxxx xxxxxxxxxxx xxxxxx lékárenské xxxx
Xxx xxxx xxx „xxxxxxxx“: Xxxxxxx oprávnění x xxxxxxxxxxx xxxxxxxxxxxx xxxxxx xxxxx zákona č. 372/2011 Sb., xxxxxx x xxxxxxxxxxx xxxxxxxx
- Xxxxxxxxxx xxxxxx xxxxxx xxxxxxxxx lékárnám xxxxx xxxx xxxxxxx xxxxxxxxxx, xxxxxx xxxxx xxxxxxxxxxxx nárůst administrativní xxx jiné xxxxxx.
- Xxxx by xxxxxxxx xxxxx dostupnost xxxxxxx xxxxxxxxxxxxxxx léčivých xxxxxxxxx.
Xxxxxx xx pacienty
- Pro xxxxxxxx xxxx xxxxxxxx xxxxxxxxx xxxxx a xxxxxxx dostupnosti xxxxxxxx xxxxxxxxx xxx xxxxxxx, xxx široké veřejnosti xxxxxxx xxxxxx xxxxxxxxxxx xxxxxxxxx xxxx, xxx xxxxxxxx xxxxxx xxxxxxxx xxxxx.
3.3 Přínosy
3.3.1.Adaptace xxxxxxxx x xxxxxxxxxx hodnoceních xxxxxxxxx xxxxxxxx xxxxxxxxx
Xxxxxxxxxxxx xxxxxxx xxxxxxxx x xxxxxxxxxx žádostí x xxxxxxxx klinického hodnocení x xxxxxxxx xxxxxxxxx xxxxxxx XX a xxxxxxxx EU xx xxxx celkově xxxxxxx xxxxxxx xxxxxxx xxxxxxxxxx x zajistit vyšší xxxx xxxxxxxxxxxx. Xxxxxxxxx xxxx xxx x xxxxxxxxx xxxxxxxxx xxxxxx xxx xxxxxxx xxxxxxx xxxxx, ve xxxxxxx xx xxxx klinické xxxxxxxxx xxxxxxxx, a xxxxxx xxxxxx xxxxxxxxxx xxxxxxx xx měl xxx xxxxxxxxx x xxxxxxxxx. Xx by xxxx xxxx x xxxx xxxxxxx xxxxx xxxxxxxxxx hodnocení na xxxxx Xxxxxxxx unie x xxx i x České republice.
V xxxxxxxx výše xxxxxxxxx xx xxxx být xxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxx x efektivnější xxxxx xxx xxxxxxxx, xxxxxxx xxxxxxxxxx zdrojů xxx xxxxxxxxxxxxx xxxxxxxxxxx xxxxxx, xxx by xxxxxxxx xxxxxxxxx probíhala, xxxxxxx xxxxxxxx xxxxxx xxxxxx x xxxxxxxxx xxxxxxxxx x xxxxxxxxxxxx xxxxxxx.
Xxxx xxxxxxxx i xxxxx xxxxxx xx xxxxxxxxx xxxxxxxxxxx x xxxxx Xxxxxxxx xxxx, xxxxx xx poli xxxxxxxx přípravků xxxxxxx xxx xxxxxxx dobu. Xxxxxxx xxxxxx xxx xxx zaveden x xxxxxxx registrace xxxxxxxx xxxxxxxxx a xxxxxxxx x xxxx, xx xx osvědčil a xxxxxxxxxxx v rámci xxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxxx xx xx xxxxxx xxxxxx, byl xxxxx xxxxx použit xxx xxxxxx klinického xxxxxxxxx samozřejmě s xxxxxxx xx xxxx xxxxxxxxx.
Xxxxxxxx xxxxxx režimu xxxxxxxxx klinických xxxxxxxxx xxxxxxx spíše xxxxxxx xxxxxxxxxx xxxxx, x xx z xxxx xxxxxx, xx xxxxxxxxxx xxxxxxxxxxxx xxxxxxxx komisí xxxxx dosavadní xxxxxx xxxxxx přímo xxxxxxxxxxxxx&xxxx; xxxxxxxxxxx xxxxxx, v xxxxx xx klinické xxxxxxxxx má xxxxxxxx x v xxxx xx x provádí, xxxxxxxxxx xxxxxxxxxxx xxxxxx xxxxxxx xxxxxxxxx xxxxx xxxxxxxx komisí x x tím xxxxxxxxxxx xxxxx xxxxxxxx xxxxxx, xxx xxxx představuje x xxxxxx xxxxxx xxxxxx xxxxxxxx systém xxxxxx xxxxxx a xxxxxx xxxxxx, které xxxxxxx xxxxxx xxxxxx xxxxxx samostatně, xxxx xxxxx etické komise, x to xx xxxxxxxxxxxx xxxxxx, má xxxxx xxxxxxxxxx xxxxxx xxxxxx xxxxxxxx a xxxxxxxxx xxxxx xxxxxxx xxxxxxxxxxxxx.
3.3.2. Xxxxxxxx směřující x xxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx
Xxxxxxxx xxxxxxxxxxxxx xxxxxx xxxxxx xx xxxxx xxxxxxxxx xxxxxxxx xxxxxxxxxxx x xxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx xx xxxxxxx dostupnosti xxxxxxxx xxxxxxxxx xxx xxxxxxxx v Xxxxx xxxxxxxxx, x xxx xxxxxxxx posílení xxxxxxx xxxxxx zdraví.
Zavedení vícestupňového xxxxxxx xxxxxxxx xxxxxx xxxxxxxx xxxxxxxxx je xxxxxxxx na xxxxxxxxxxxxx x vyhodnocování údajů x xxxxxxxxxx x xxxxxxxx léčivých xxxxxxxxx, xxxxx se scházejí xx xxxx xxxxxxxx, x xx xxx xx těch, xxxxx xxxxxx xxxxxxxxx xxxxx xxxxxx dodávají, tak x od těch, xxxxx je xx xxxxxx xxxx xxxxxxxxx, x xxxxxxx údaji xxxxxxxx xxxxxx by xxx xxx odpovídat xxxxxxxxx xxxx xxxxxxx xxxxxx x xxxxxx. Xxx xxx o xxxxx získané xxxxxxxx xxxxxxxx, xxxxx xxxx x sobě xxxxxxxx xxxxxxxxxxxx xxxxxxx xxxx xx xxxx x xxxxxxx xxxxxxxxxx, xxx xxxxx „má xxxx“ xxxxxxxx xxxx „xxx“ . Xxxxx o xxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx je xxx xxxxx xxxxxxxxx xx xxxxxxxxx x xxxxxxx xxxxxx xxxxxxxxx je xxxxx xxx teoretická. X xxxx souvislosti xx třeba konstatovat, xx xxxxx nebyly xxxxxxxx xxxxxx xxxxxxx xxxxxxx, xxx xx xxxxxx xxxxxxxxx xxxx xx skutečnosti xxxxxxxx xxxxxxxx xxxx Českou xxxxxxxxx, a xxxxxx xx jejich xxxxxxx xxxx xxxxxxxx vykazovány xx xxxxx Xxxxx xxxxxxxxx. Možnost takového xxxxxxxxxx jednání je xxxxxxx xxxxxx a xxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxxx xxxxx o xxxxxxxxxx x xxxxxxxx xxxxxxxx xxxxxxxxx výrazně ztížena xx xxxxx vyloučena. Xxxxxxxx xxxxxxxx xxxxxx xxxxxxxx xxxxxxxxx tedy xxxxxxxxx xxxxxx korupčních xxxxx.
3.4 Xxxxxxxxxxx xxxxxxx x xxxxxxx xxxxxxx
3.4.1. Xxxxxxxx nařízení x xxxxxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx
Xxxxxxxxxxx xxxxxxx x xxxxxxx xxxx xxxxxxxxx x xxxxx xxxxxxxxxxxx variant řešení, xxx xx xxxxxxx xxxx.
3.4.2. Xxxxxxxx směřující x xxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx
Xxxxxxxxxxx xxxxxxx x přínosů xxxx xxxxxxxxx x xxxxx xxxxxxxxxxxx xxxxxxx řešení, xxx xx uvedeno xxxx.
3.4.3. Xxxxxxxx nařízení xx xxxxxx k xxxxxxx xxxxxx pro xxxxxxx léčivé xxxxxxxxx
Xxxxxxx xxxxxxxxx xx xxxxxxxx xxxxxxx textu zákona x xxxxxxxx xxx, xxx byla náležitým xxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxx Xxxxxx x xxxxxxxxx xxxxxxxxx (XX) č. 1252/2014.
3.4.4. Xxxxxxxxxx Státního xxxxxx xxx xxxxxxxx xxxxx x Xxxxxxxxxxx xxxxxxxxxxx xxx
Xxxxxxxx 1 xxxxxxxxxxx ve změně xxxxxx x xxxxxxxx xx tu xxxxxx, xx xxxxxxx xxxxxx xxxxxx problému, x xxxxxx xx xxxxxxxxx xxx xxxxxxx právním xxxxx, x xx xxxxxxxxx ustanovením §8 xxxxxx x. 226/2013 Xx.
Xxxxxxxx 2 xxxxxxxxxxx x xxxxxxx xxxxxxxxxx xxxxxx xxxxxx x Xxxxx xxxxxx České xxxxxxxxx x tomuto xxxxxx xxxxxx zákona x xxxxxxxx xx xxxxxxxx xxxx xxxxxx xxxxxx, xxxxx xxxxxx xx xxxxxxx xx xxxxxxxxxx xxxxxx resortu, x xxxxx xx xxxx xxxxxxx xxxxxxxx xxxx xxxxx, pokud xx xx xxxxxxx xxxxxx xxxxx praxe xxxxxxxxxx.
Xxxxxxxx 3 spočívající xx xxxxxxx xxxxxxxxxx xxxxxxxxxx zákona o Xxxxx xxxxxx Xxxxx xxxxxxxxx xx xxx xxxxxxx xxxxxxxxxx, xx xx xxxxxxxx xx xxxxxxx xxxxxxxxxxx xxxxxxxxxx xxxxxxx xxxxxxxxxx xxxxxx č. 17/2012 Sb. xxx možnosti xxxxxxxxx xxxxxxxxxx xxxx xxxxxx xxxxxx xxxxxx xx xxxxx xxxxxxx xxxx, xxxxxxx xxxx x léčivy xx xxx v Xxxxx xxxxxxxxx xxxxxx dostatečně xxxxxx.
3.4.5. Prokazování xxx xxxxxxxxx xxxxxxxx x xxxxxx xxxxxxxxx zajištění x zabrání léčivých xxxxxxxxx
Xxxxxxxx 1 xxxx xxxxxxx s xxxxxx xxxxxxxxx xxxxxxxx. Naopak xxxx xxxxxxx xx xxxx xx xxxxxxxx xxxxxxxxxxx pro xxxxx xxxxxxxxxxxx xxxxxxxxxx xxxxxx xxxxxx, xxxxx xxxxxxxx xxxxxx jistotu především xx straně xxxxxxxxxxxxxx xxxxxxxx, xxx xxxxx xx rozdílná xxxxxx xxxxxx xxxxxx xxxxxxxx xxxxx xxxxxxx x xxxx xx komplikacím x průběhu inspekční xxxxxxxx a x xxxxxxx ztrátám xxx xxxxxxxxxxx xxxxxxxxxx. Xxxxxxxxx xxxxxxxx xx xxxxxxxx xxxxxx xxxxxxx xxxxxxxx xxxxxxxxx nebo xxxxxx xxxxxxxxx, xx xxxxxxx xxxxxxxxx xxxxxxxxxxx xxxxx, xxxxxxxxxxx xxxxxxxx xxxxxx xxx xxxxx xxxxxxxxxx xxxxxxxxxx léčivých přípravků, x xxxxxx následným xxxxxxxxxx xxxxxxx xx xxxxxx xxxxxxxxx stav. Xxxxx xxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxxx xxx osoby, xxxxxx xxxx zabrány, xxxxxx xxxxxxxxxx xxxxx, xxxxx xxxx posílit efekt xxxxxxxxxxx xxxxxxx xxxxxxxxxxx x neoprávněné xxxxxxxx.
Xxxxxxxx 2 xx přinesla xxxxxxxxx úpravu xxxxxxxxxxx xxxxxxxxxx při provádění xxxxxxxxx xxxxxxxx a xxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxx x xxxxxxx léčivých xxxxxxxxx xxx, xxx xxxx xxxxxxxxxx x xxx xxxxxx xxxxxxx, xxx xx zjištěno, že x xxxx xxxxxxxxx xxxxx, které x xxxx xxxxxx xxxxx xxxxxx oprávněny. Tato xxxxxxxx xxxxxxxxxxx účinnější xxxxxx ochrany pacientů x xxxx xxxxxxxxxxx xxxx xxxxxx xxxxx xxxxxxxx xxxxxxxxx, jejichž xxxxxx, účinnost x xxxxxxxxxx xxxxxx zajištěna x xxxxxxx xxxxxxxxx xxxxx léčiva a xxxxxxxxxxx xxx xxxxx xxxxxx riziko xxx xxxxxx xxxxxxxx a xxxxxxxx xxxx xxxxxxx xxx systém xxxxxxxxx xxxxxxxxxxx pojištění, v xxxxxxxxx xxxxxxxxx s xxxxxxxxxx dopadem xx xxxxxx pacientů.
4. Xxxxx xxxxxx
4.1 Xxxxxxxxx xxxxxx xxxxxxx x výběr xxxxxxxxxxxxxx řešení
4.1.1. Xxxxxxxx xxxxxxxx xxx xxxxxxxx xxxxxxxxx xxxxxxxxx léčivých xxxxxxxxx
Xxxxxxxxx xxxxxxxx x xxxxxxxxxxx xxxxxxxxxxxx xxxxxxx xxxx xxxxxxxxx, xxx xx uvedeno výše.
4.1.2. Xxxxxxxx xxxxxxxxx k xxxxxxx reexportu léčivých xxxxxxxxx
Xxxxxxxxx xxxxxxxx x xxxxxxxxxxx jednotlivých xxxxxxx xxxx provedeno, xxx xx xxxxxxx výše.
4.1.3. Xxxxxxxx xxxxxxxx xx xxxxxx x xxxxxxx xxxxxx xxx humánní xxxxxx xxxxxxxxx
Xxxxxxxxxxx xxxxxxxxx xx varianta xxxxxxx xxxxx zákona o xxxxxxxx tak, aby xxxx náležitým způsobem xxxxxxxxx adaptace nařízení Xxxxxx v xxxxxxxxx xxxxxxxxx (EU) č. 1252/2014.
4.1.4. Xxxxxxxxxx Xxxxxxxx xxxxxx xxx xxxxxxxx xxxxx x Xxxxxxxxxxx xxxxxxxxxxx xxx
Xxxxxxxxxxx variantou je xxxxxxxx 1 xxxxxxxxx xx změně xxxxxx x léčivech. Xxx x xxxxxxxxxxxx, x xxxxxx xxxxxxxxxxxxxxxx xxxxxx xxxxxxxx, xxxx navíc xx při jejím xxxxxxxxxxx využívá systém xxx xxxxxxxxx xxxxxxx xxxxxxx řádem, který x xxxxx xxxxxx xxxxxx a xxxxxxxx xx. Tato xxxxxxxx xxxxxx koordinovat kontrolní xxxxxxxxxx obou xxxxxx xxxxxx správy x xxxxxxxx xxx xxxxxxx xxxxxxx xxxx Xxxxx xxxxxxxxx a xxxxxxxx xxxx XX xxxx xxxxxxx xxxxx, která xxxxxxxxxxxx xxxx xxxxxxxx xxxxxxx požadavkům x xxxxxx XX.
4.1.5. Xxxxxxxxxxx xxx inspekční xxxxxxxx x xxxxxx instituty xxxxxxxxx x xxxxxxx xxxxxxxx přípravků
Doporučenou variantou xx xxxxxxxx 2, xxxxxx xx mělo xxx xxxxxxxx xxxxxxx xxxxxxxxx xxxxxx xxxxxxxxxxx xxxxxxxxxx xxx xxxxxxxxx xxxxxxxxx xxxxxxxx x xxxxxx by xx xxxx xxxxxxxx xxxxxx xxxxxxxxx xxxxxxxxx x xxxxxxx xxxxxxxx přípravků xxx, aby xxxx xxxxxxxxxx i xxx xxxxxx xxxxxxx, kdy xx xxxxxxxx, xx x nimi zacházejí xxxxx, které x xxxx xxxxxx podle xxxxxx xxxxxxxxx. Xxxxxx xx xxx již xxxxxxxxxxxxx xxx xxxxx xxxxxxxxxxxx nejednotná právní xxxxxx, xxxxx xx xx xxxxxx xx xxxxxxxxxxxxx xxxxxxxxx velmi xxxxxxx x xxxx xx xxxxxx x xxxxxxxxxxx x xxxxxxx xxxxxxxxx xxxxxxxx x xxxxxxxxxx xxxxxxxxxxxxx časovému xxxxxxx xxxxxxxxxxx xxxxxxx.
Xxxxxxxxx xxxxxxxx xx xxxxxxxx xxxxxx xxxxxxx xxxxxxxx xxxxxxxxx xxxx xxxxxx xxxxxxxxx, se xxxxxxx xxxxxxxxx neoprávněné xxxxx, xxxxxxxxxxx významná xxxxxxxxx xxxxxx pro xxxxx xxxxxxx o xxxxxx xxxxxxxx. Navíc xxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxxx xxx xxxxx, xxxxxx xxxx zabrány, xxxxxx ekonomický xxxxx, xxxxx může xxxxxxx xxxxx xxxxxxxxxxx xxxxxxx xxxxxxxxxxx x xxxxxxxxxxx xxxxxxxx.
5. Xxxxxxxxxxxx xxxxxxxxxx xxxxxxxx a vynucování
Orgánem xxxxxxxxxx za xxxxxxxxxxxx xxxxxxx xxxxxxxx xxxxxx, xxxxx xxx o xxxxxxxx xxxxxxxx x xxxxxxxxxx hodnoceních xxxxxxxxx xxxxxxxx xxxxxxxxx, bude xxxxxxxxx Xxxxxx xxxxx xxx xxxxxxxx léčiv, xxxxx xx xxx xxxxx xxxxxxxxxxx xxxxx xxxxxx x xxxxxxxx xxxxxxxxxxxxxxx odborným správním xxxxxx xxx xxxxxx xxxxxxxx xxxxx, včetně xxxxxxxxxx a xxxxxxx xxx xxxxxxxxxx klinických xxxxxxxxx xxxxxxxx xxxxxxxxx. Xxxxxx xxxxx xxx xxxxxxxx xxxxx xx xxxxxxx xxxx xxxx xxxxxxx povinnosti v xxxxxxx jakosti, účinnosti x xxxxxxxxxxx xxxxx, x to i xx xxxxxx x xxxxxxxxxx xxxxxxx členských xxxxx i Xxxxxxxx xxxx.
Xxxxxx odpovědnými za xxxxxxxxxxxx xxxxxxx varianty xxxxxx, xxxxx xxx x xxxxxxxx xxxxxxxxx x omezení xxxxxxxxx xxxxxxxx xxxxxxxxx, budou xxxxxxxxx Xxxxxxxxxxxx zdravotnictví x Státní xxxxx xxx kontrolu léčiv. Xxxxxxxxxx xxxxxxxx bude xxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxxxx xxxxxxx xxxxxxxx xxxxxxxxx, xxxxx xxxx xxxxxxxx jejich xxxxxxxxxxxxx, x dále xxx xxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxxxxxxxx xxxxxxx opatření xxxxxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxx xx xxxxx seznamu mimo xxxxx Xxxxx xxxxxxxxx. Xxxxxxxxxxxx xxxxxxxxxxx fungování xxxxxx systému je xxxxxxx získávání přesných x xxxxxxxxxx xxx x xxxxxx, jejich xxxxxxxx xxxxxxxxxx a xxxxxxxxxxxxx, následně x xxxxxxxxxx na xxxxxxx xxxxxxxxx xxxxxxxxxxxxx xxxxxxxxxx xxxxxx příslušných xxxxxxxx. Xxxxxxxxxx vynucování xxxxxxxxx x možnosti xxxxxxxxx xxxxxx xx porušení xxxxxxxxxxx povinností.
6. Xxxxxxx xxxxxxxxx xxxxxxxx
Xxxxxxx účinnosti xxxxxx xxxxxx x xxxxxxxx budou v xxxxx provádět Ministerstvo xxxxxxxxxxxxx a Xxxxxx xxxxx pro xxxxxxxx xxxxx xx xxxxxxxxxx x dotčenými xxxxxxxx, x xx x xxxxxxxx xxxxxxxxx xxxx xxxxxx xxxxxx x xxxxxxx x xxxxxxxx xxxxxxxxxx cílů xxxxxxxxxxx xxxxx právní úpravou. Xxxxx xxxxxxx xx xxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx xxx xxxxxxxx xx Komise, které xx xxxxxxxxxxx čl. 97 xxxxxxxx č. 536/2014 xxxxxx xxxxxxx uplatňování xxxxxx xxxxxxxx.
Xxxxxxxxxxx xx 2 xxxxxx xx xxxxxxxxx xxxxxx xxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxx xxx pacienty.
Pro xxxxxxxxx xxxxxxxx xxxxxxxx xxx xxx účinný xxxxxxx xxxxxxxx xxxx xxxxx x xxxxxxx, xxx xx bylo xxxxxxxxxx x xxxxxxx xxxxxxxx k xxxxxxx xxxxxxxxx léčivých přípravků, xxxxxxx zdokumentován. Zejména xxxx xxxxxxxxx, kolik xxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxx, x xxxx konkrétní xxxxx XXX xxxxxx xxx x nich xxxxxxx. Xxxxxx xxxx x xxxxxx případě xxxxxxxxxxx, xxx a xx xxxx xxxx xxxxxxx xxxxxxxx xxxxxxxx xxxxxxxx xxxxxxx xxxxxxxxxxx xxxxxxxxxxx léčivých xxxxxxxxx xxx xxxxxxxx x Xxxxx xxxxxxxxx a xxxx xxxxxxxx xxxx xxxxxxxxxxx xxxx přijetím xxxxxxxx a po xxxx xxxxxxx xx xxxxxxxxxxx jednotlivých xxxxxxxx xxxxx x době xxxxxx xxxxxx xxxxxxxx.
Xxxxx xxxxxxxxxx vyhodnocení xxxxxxxxx xxxxxxx přijatého xxxxxxxx xxx xxxxxxxx xxxxx xxxxxxxxxxx xxxx xxxxxxxx xxx xxxxxxxxxxxx léčivých xxxxxxxxx, přičemž jedním xx xxxxxxxxx xxxxxxxxx xxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxxx objemu xxxxxxx, xxxxx xx x xxxxxxx nepřijetí xxxxxxxx xxxx v xxxxxxxxxx xxxxxxx xxxxxx xx xxxxxxxxx, a finančního xxxxxxxxxx objemu dodávek, xxxxx v důsledku xxxxxxx xxxxxxxx xxxx xxxxx xx xxxxxxxxx xxxxxx xx xxx x Xxxxx xxxxxxxxx. Xx základě vyhodnocení xxxxxxxxxxxx xxxxxxx xxx xxxx xxxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx xxxxxx xxxxxx xxxxxxxxx právní xxxxxxxx xxxxxxxxx reexporty xxxxxxxx přípravků.
Rovněž bude xxx xxxxxxxx xxxxxxxxx xxxxxxxx hodnocen xxxxx xxxx xxxxxxxx xxxxxxxx xxxxxxxxx, které jsou xxxxxxxx xxxxxx nedostupností, x xxxxxxxxx xxxxxxxxxx xxxxxxxxx k omezení xxxxxxxxx léčivých přípravků, xxx xxxxx xxx xx xxxxxxxx xxxxxxxxxx xxxxx xxxxxxxxxx xxxxxxxxx, xxx xxxxxxxx xxxxxxxxxxxx xxxxxx xxxxxxxx vývozu xxxxxxxx xxxxxxxxx x xxxx xxxxx xxxxxxxxxx x xx svém xxxxxxx xxxxxx xxxxxxxx xxxxxxxxxxx xxxxxxx x xxxxxxx xxxxxxx zajistit xxx xxxxxxxx x Xxxxx republice náležitou xxxxxxxxxx léčivých xxxxxxxxx.
7. Xxxxxxxxxx x xxxxxx xxx
Xxxxx xxxxxx byl x průběhu přípravy xxxxxxxx xxxxxxxxxxx x xxxxxxxxx xxxxxxxxx xxxxxxxx. Xxx oblast etických xxxxxx x xxxxxxx xxxx se xxxxxxxx xxxxxxxxxx zástupci xxxxxxxx xxxxxx xxx xxxxxxxxxxxxxx xxxxxxxx xxxxxxxxx x Xxxx xxxxxxxx komisí. Xxxxxxxxxxx x připravovaných xxxxxxx s možností xxxxxxxxxx xxxx xxxxxxxx xxxxx etických xxxxxx xxx xxxxxxxxxxxxxx xxxxxxxxx x xxxxxxxx xxxxxxxx xxxxxxxx xxxxxx xxxxxxxxxxx xx xxxxxxx Xxxx xxxxxxxx komisí. Informovány xxxx x xxxxxxxxxx xxxxxxxxxx x návrhem xxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxxxxx xxxxxxxxxx xx xxxxxxxx xxxxxxxx xxxxxx. Xx xxxxxx xxxxxxxx xxxxxxxxx nových xxxxxxx xxxxxxx xxxx byli xxxxxxxx xxxxxxxxxx prostřednictvím Xxxxxxxx xxxxxxxxxxxx průmyslu, Xxxxxxxx xxxxxxxxxxx xxxxxxxxx, xxxxxxxx Xxxxxxxx xxxxxxxxxx xxxxxxxxx organizací, Asociace xxxxxxxxxx xxxxx. Xxxxxxxxxxxx xxxxxxxxxxxxx tuto xxxxxx xxxxxxxxxxxx x Ministerstvem xxxxxxx a Ministerstvem xxxxxxxxxxxxx.
Xxxxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx x omezení xxxxxxxxx léčivých xxxxxxxxx xxxx xxxxxxxxx xxxxxxxxxxxx x jednotlivými držiteli xxxxxxxxxx x registraci, xxxxx xxxxxxx možnosti xxx xxxxxxx úniku xxxxxxxx xxxxxxxxx xx xxxxxxx určených xx xxx x České xxxxxxxxx xx xxxxxxxxx x xxxxxx x Xxxxxxxx xxxxxxxxxxxx xxxxxxxx.
Xxxxx xxxxxx zákona x xxxxxxxx xxx x xxxxx xxxxxxxxxxxxxx xxxxxxxxxxxxxx xxxxxx x xxxxxxx x xx. 8 Xxxxxxxxxxxxxx pravidel vlády xxxxxxxxx s povinnými xxxxxxxxxxxxxx xxxxx.
8. Xxxxxxx xx xxxxxxxxxxxx XXX
Xxxxx x xxxxxxxx: XXXx. Xxxxx Němcová
Funkce: vedoucí xxxxxxxx xxxxxxxxxx xxxxxxxxx
Xxxxx: Xxxxx xxxxxxxxxx, xxxxxxxx xxxxxxxxxx hodnocení SÚKL
Telefon: 272 185 817; 724 917 141
x-xxxx: xxxxx.xxxxxxx@xxxx.xx
Xxxxx a xxxxxxxx: Xxx. Apolena Xxxxxxxx
Xxxxxx: xxxxxxx xxxxx xxxxxx
Xxxxx: Xxxxx xxxxxx Xxxxxxxx xxxxxx xxx xxxxxxxx xxxxx
Xxxxxxx: 272 185 706
x-xxxx: xxxxxxx.xxxxxxxx@xxxx.xx
X. Xxxxxxxxxx xxxxxxx xxxxxxxxxx xxxxxx xxxxxx x xxxxxxxx xxxxxxxx Xxxxx xxxxxxxxx, x xxxxxxxxxxxxx xxxxxxxxx x s xxxxxxxx Xxxxxxxx unie, xxxxxxxxxxx xxxxxxxx xxxxxx Evropské xxxx a obecnými xxxxxxxx xxxxxxxx xxxxx Xxxxxxxx xxxx
Xxxxxxxxxx xxxxxx xxxxxx xxxxxxxx xxxxxxxxx xxxxxxx x xxxxxxxx xxxx Xxxxx republiky, xxxxxxx ústavnímu xxxxxx č. 1/1993 Sb., Xxxxxx Xxxxx xxxxxxxxx, ve znění xxxxxxxxxx xxxxxxxx, x xxxxxxxx předsednictva České xxxxxxx rady č. 2/1993 Sb., x xxxxxxxxx Xxxxxxx xxxxxxxxxx xxxx a xxxxxx jako xxxxxxxx xxxxxxxxx xxxxxxx Xxxxx xxxxxxxxx, xxxxx se xxxxxxxx x xxxxxxxxxxxxx xxxxxx xxxxxx.
Xxxxxxxxxx xxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx xxxx v xxxxxxx x xxxxxxxxxxxxx smlouvami, xxxxxxx je Xxxxx xxxxxxxxx xxxxxx.
Xxxxxxxxxx právní xxxxxx xx x xxxxxxx x Úmluvou x xxxxxxx xxxxxxxx xxxx a základních xxxxxx. Xxxxxxxxx záruky xx xxxxxxxxxxx proces x rámci správního xxxxxxxx, xxxxx xxxxxxxx xxxxxxxx xx xxxxxxxxxxx xx xxxxxxx xxxxxxxxxxx xxxxxxxx řádem x xxxxxxx x přestupcích, xxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxx xxxx xxxxx xxxxxxxxx, xxxxxxxxx xxxx x xxxxxxxx xxxxxxxxxx x xxxxxxxx rozpětí xxxx xxxxx.
Xxxxxxxxxx právní xxxxxx je xxxxxx x xxxxxxx x Xxxxxxx o lidských xxxxxxx a xxxxxxxxxxx, xxxxxxxxx xxx č. 96/2001 Sb. m. s. Xxxxx x xxxxxxx xxxxxxx xxxxxxxxx léčivých xxxxxxxxx xxxx xxxx xxxxxxxxxx xxxxxxxxxx čl. 3 Xxxxxx, xxxxx xxxxxxx xxxxxxx xxxxxx, xxxxxx xx xxxxxxx xxxxxxxxx xxxxxxx x xxxxxxxx xxxxxx, učiní xxxxxxxxxxxx xxxxxxxx, xxx v xxxxx xxx xxxxxxxxxx xxxxxxxxx rovnou xxxxxxxxxx xxxxxxxxx xxxx xxxxxxxx xxxxxxx. Xxxxxxxxx xxxxxxxxx xxxx xxxxxxxx xxxxxxx xxxxxx zahrnuje xxxxxxxxx xxxxxx pacientů x Xxxxx republice x xxxxxxx xxxxxxxx xxxxxxxxx, xxx xxxx xxxxxx xxxxxxxxxxxxx xxxx Českou xxxxxxxxx xx úkor xxxxxxxxxx xxxxxxxxxx potřeb xxxxxxxx x České xxxxxxxxx.
Xxxxx xxx x xxxxx výjimečné xxxxxxx, xxx xxxxxxxxxxx léčivých xxxxxxxxx xxxx xxxxx xxx xxxxxxx a x xxxxxxxx xxxxxxx xxxxxxxx xxxxxxxxxx trhu xxxxxxxx přípravky x Xxxxx republice xxxx xxxxxx xxxxxxxxxx xx xxxxxxxxx, nelze xxxxxxx x xxx, xx xx xxx bylo xxxxxxx xxxx xxxxx xxxxxxxx x provozovat xxxxx xxxxxxxxxxxx xxxxxxx xx xxxxxx čl. 26 xxxx. 1 Xxxxxxx xxxxxxxxxx xxxx x xxxxxx, když hned x čl. 26 xxxx. 2 Xxxxxxx je xxxxxxxxxx xxxxxxx, xx xxxxx xxxx stanovit xxxxxxxx x xxxxxxx xxx výkon xxxxxxxx xxxxxxxx. Naopak podnikatel xxx xxxxx xxxxxxxxx, xx xxx v Xxxxx xxxxxxxxx, xxxxx xxx x zásobování xxxxxxxx xxxxxxxx xxxxxxxxx, xxxx xxxxxxx, x xxxxx xxxxx směrem xxx xxxx xxxxxxx xxxx podnikatelskou xxxxxxxx. Xxxxx xxxxx podnikat xx třeba xxxxxxxxx x xxxxxx práva xxxxxx xx xxxxxxx xxxxxx x na xxxxxxxxx xxxxxxxxx xxxx xxxxxxxxxxx x článku 31 Xxxxxxx xxxxxxxxx xxxxxx xx xxxx xxxxxxxxxxxxx, xxxxxxxxxx x xxxxxxxxxx. Xxxxx podnikat tak xxxxxx být xxxxxxxxxx xxx, xx by xxxx xxxxx xxxxxxx xxxxxxxx naplnění xxxxxx xx stejné xxxxxx xxxxxxxxxxx ústavního xxxxx.
Xxxxxxxxxx xxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx není x xxxxxxx x xxxxxxxxxxxxx xxxxxxxxx, xxxxxxx xx Xxxxx republika xxxxxx.
Xxxxxxxxxx xxxxxx xxxxxx vychází x xxxxxxxx Evropského xxxxxxxxxx a Rady (XX) č. 536/2014, xxxxx xxxxxxxx na xxxxxxxx x České xxxxxxxxx, xxxxxxx respektuje xxxxxx xxxxxxxxxxxx xxxxxxxxxx tohoto xxxxxxxx x upravuje xxx xx záležitosti, xxxxx xxxx umožněny xxxxxxxxx xxxxx xxxxxxx xxxx je xx xxxxxxxxx xx xxxxxxx.
Xxxxxxxxxx xxxxxx by x xxxxxxx xxxxxxx xxxxxxxxx xxxx přispět x xxxxx xxxx xxxxxxxxxx xxxxx občanů xx xxxxxxx xxxxxx a xx náležitou xxxxxxxxx xxxx xxxxxxxxxxx x článku 31 Xxxxxxx xxxxxxxxxx xxxx a xxxxxx xxx, že xx xxxx xxxxxxx xxxxxxx x xxxxxxx xxxxxx xxxx xxxxxxx, xxx xx xxx na xxxx Xxxxx republiky xxxxxxxxxx léčivých přípravků xxxxxxxxx xxxxxx xxxxxxxxx xxxxxxx.
Xxxxxxxx xxxx uvedených xxxxxxxx xxxxxxxxxxxx, xxxxxxxxxxxxxxxx, xxxxxxxxx, odůvodněnosti, xxxxxxxxxxxx, xxxxxxxxxx únosnosti, xxxxxxxxx x efektivity xxxxxxxxx xxxxx xxxxxxxxxxxx navrhované xxxxxx úpravy x xxxxxx Xxxxxxxx xxxx, xxx xxxxxxx je xxxxx xxxxxxxx xxxxxxxxxxxx xxxxxxxx xxxxxxx xxxxxxxxxxxxxx xxxxxxx z xxxxxx xxxxxxx xxxxxx x xxxxxx xxxx. Takové xxxxxxxx xxxx xxx xxxxxxxxxxxxxx, zejména musí xxxxxxxx xxxxxxxx vhodnosti x nutnosti. Z xxxxxx xxxxxxxx musí xxx xxxxxxxx xxxxxxx xxxxxxxx xxxxxx xxxxxxxxxx. Xx xxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxxx xxxxxx xxxxxx xxxxx podmínkám xxxxxxxx.
Xxxxxxxxx xxxxxx x xxxxxxxx xxxxxxxxx napříč xxxxxxxxx státy Xxxxxxxx xxxx je xxxxxxxxxx x xxxxxxx xx xxxxxxx xxxxxxx pohybu xxxxx (xx. 34 x 35 Xxxxxxx x fungování Evropské xxxx), xxxxx xxxxxxxxxxx xxxxx ze základních xxxxxx jednotného xxxxxxxxx xxxx Evropské unie. Xxxxx xxxxxxxx přípravků xxxx x xxxxxxxx xxxxxxxx může být x xxxxxxxxx xxxxxxxxx xxxxxxxx akutní xxxxxxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx xx xxxx x Xxxxx xxxxxxxxx. Xx xxxxxxxxxxx xxxxxxxxx xxxx x xx xxxxxx xxxxxx xxxx přitom xxx xxxxx Xxxxxxxx xxxx odpovědné členské xxxxx. Xxxxxxxxxx xxxxxx xxxxxx xx xxxxx x xxxxxxx s xxxxxx Xxxxxxxx xxxx, xxx xxxxxxx xxx xxxxxxxx xxxxxxxxx opatření xx účelem xxxxxxx xxxxxx a xxxxxx xxxx, x tímto xxxxxx xx xxxxx xxxxxxxxx akutní xxxxxxxxxxxxx xxxxxxxx přípravků xxx xxxxxxx pacientů x Xxxxx xxxxxxxxx.
Xxxxxxxxxx členské xxxxx XX x xxxxxxxxxx xxxxxx xxxxxxxxx xxxxxxx xxxxxxxx xx xxxxxx xxxxxxx xxxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx x důvodu xxxxxx xxxxxxxxx, xxxxxxx xx xxxxxx Xxxxxx byly xxxxxxx z nich xxxxxxxxxx na xxxxxx x xxxxxx Xxxxxxxx xxxx. Většinou xxxx xx xxxxxx Xxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxx a xxxxxx xxxxxx se xxxxxxxx xxxxxxx xxxxxx zboží. Xx základě xxxxxxx xxxxxxx z xxxxxxxx xxxx (zejména Xxxxxxxxx) xxxx xxxxxxx x xxxxxx, xx xxxxxxxxxx xxxxxx, xxxxx spočívá xx xxxxxxxxx xxxxxxx xxxxxxxx přípravků, xxxxx xxxx xxxxxxxx xxxxxxxxxxxxx, x x xxxxxxxx xxxxxxxxxx zákazu xxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxx xx xxxxx seznamu xxxx xxxxxxx xxxxxxx xxxx, xx x xxxxxxx s xxxxxx Xxxxxxxx xxxx. Regulace xxxxxx léčivých xxxxxxxxx xx xxxxxxxxx xxxx xxxxxxxxxxxx, xxxxxxx x xxxxxxxx xxxxx o xxxxxxxx xxxxxxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx xx xxxx, xxxxxxx xxxxxx xx xxxxxxxx transparentní x xxxxx xxxxxxxx xxxx xxxxxxxxxxxxx. Xxxx xxxxxxxxxx rozhodnutí Evropského xxxxxxxx xxxxx, xxxxxx xx xxxxxxxx státům xxxxxxxx přijmout xxxxxxxx xxxxxxx x zajištění xxxxxxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx xxx xxx xxxxxx a xxxxxxxx xxx xxxxxx xxxxxxxx xxxxxxx xxxxxx xxxxx. Xxxxxxxx xxxxxx xxxxxx xxxxxxxx xxxx xxxxxxxx xxxxx s xxxxxx xxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx na Xxxxxxxxx, která xxxx xx xxxxxx EK xxxxxxxx za xxxxxx xxxxxxxxx xxxxx xxxxx xxxxx, protože xxxxxxxxxxxxx xxxxxxxx plošnou, vztahující xx na xxxxxxx xxxxxxxx xxxxxx přípravky, xxxxxxx, xxxxxxx xxxxxx xxxxxx xxxxxxx, xxx xxxx trvalého xxxxxxxxxx x xxxxxx dostatečně xxxxxxxxxx. V xxxxxxxx xxxx se xxxxx xxxxxxxxx o Xxxxxx, xxx xxxxxxxxx x xxxxxxxx legislativní úprava xxxxxxxxx xxxxxxxx x xxxxxx xxxxx XX x xxxxxxxx x xxxx, xx x xxxxx opatření omezujících xxxxxxxx xxxx v Xxxxxx xxxxxx xxxxx xxxxxxxx x xxxx xxxxxxx, panuje tak xxxxx, že se xxxx xx reexport xxxxxxxx přípravků z Xxxxx xxxxxxxxx xx xxxxxxxx xxxxxxxxxx opatření x xxxxxxxxx státě xxxxx zvýší.
Ostatní xxxxxxx xxxxx, pokud xxxxxxxx xxxxxxxx přípravků xxxxxxx, xxxxxxxxx xxxxxxxxxx článku 81 xxxxxxxx 2001/83/XX x xxxxxxxxx xxxxxxxxxxxx množství xxxxxxxx xxxxxxxxx xxx xxxxxxxx své země.
Přijetím xxxxxxxx Xxxxxx x xxxxxxxxx xxxxxxxxx (XX) č. 1252/2014 xx xxx 28. května 2014 xxxxxxxxxx xxxxxxxx Evropského xxxxxxxxxx a Rady 2001/83/XX, xxxxx xxx x zásady x xxxxxx xxxxxxx xxxxxxx xxxxx xxx léčivé xxxxx pro xxxxxxx xxxxxx xxxxxxxxx, xx xxxxxxxxx xxxxxxxx platná xxx xxxxxx látky xxx humánní xxxxxx xxxxxxxxx. Xxxxx zákona xx měl xxxxxxx x důsledné xxxxxxxx xxxxxx nařízení x xxxxxxxxxx Xxxxx xxxxxxxxx.
Xxxxxxxxxxx xxxxx xxxxxx není x xxxxxxx x xxxxxxxxxxx xxxxxxxx orgánů Xxxxxxxx xxxx a xx x souladu x obecnými zásadami xxxxx Xxxxxxxx unie (xxxx. zásada právní xxxxxxx, xxxxxxxxxxxxxxx x xxxxxx xxxxxxxxxxxx).
X. Zhodnocení xxxxxx navrhovaného xxxxxx xx vztahu x xxxxxx xxxxxxxxxxxx
Xxxxxxxxxx xxxxxx xxxxxx xxxxxxxxxx žádné xxxxxxxxxx, xxxxx by xxxx x xxxxxxx xx zákazem xxxxxxxxxxxx.
Xxxxxxxxxx xxxxxx xxxxxx xxxx xxxxxxxxxxxxx xxx sekundární xxxxxx xx xxxxxxx xxxx a xxx x xxxxxx k xxxxxxxxxxxx xxxxxxx z xxxxxxx, xxxxx xxxxx xxxxxxxxxxx xxx nezvýhodňuje xxxxx x xxxxxxx x xxxxxxxxx xxx xxx xxxxxxx xxxxxxxx.
X. Xxxxxxxxxx xxxxxx navrhovaného xxxxxx ve vztahu x xxxxxxx xxxxxxxx x osobních xxxxx
Xxxxxxxxxx xxxxxx úprava xxxxxxxxx xxxx xxxxxxxxxx xxxxxxxx xxxxx. Xxxxxxxxxxx xxxxxx xxxxxxx xxxx xxxxxx xxx existující xxxxxxxxxx xxxxxxxx xxxxx. Xxxxxxxxxx xxxxxx xxxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxx xxxxx xxxxxxxxxx xxx xxxxxxxxx xxxxxxxx xxxxxxxx xxxxx.
Xxxxxxxxxx xxxxxx úprava xxxxxxxxx xxxx zpracování xxxxxxxx xxxxx x není xx xxxxxx již xxxxxxxxxx zpracování osobních xxxxx x těchto xxxxxx. Xxxxx xxx x xxxxxxxxxx xxxxx x xxxxxxxxxx §33 xxxx. 2, §77 xxxx. 1 xxxx. x) x §82 xxxx. 3 xxxx. x), xxxxx spočívá x xxxxxxxx xxxxx x xxx, xx xxxxxxxxx xxxxxx xxxxxxxxxxxxx xxxxx, xxxxxx xxxxx xxxxxxxx, kromě toho, xx xxxxxxxx úprava xx xxxx nacházet xxxxx x xxxxxx, xxxx upraven xxxxx x xxxxxxxxxxx xxxxxxxxxx Xxxxxx x právním xxxxxxxx, xx. ve xxxxxxxx, xxxxx xxxxxx xxxxxx xxxxx, xxxx xxxx xxxxxxx x xxxxxxxxx, zůstane stejný xxxx xxxxx. Xxxxx xxx o xxxxxxxxxx §53x až §53x, §54 a §55, xxxxxxxx se xxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx, opět rozsah xxxxxxxxxxxxx údajů, xxxxxx xxxxx xxxxxxxx, zůstává xxxxxx, xxxx xxxxx xx x ustanovení §51 x násl. xxxxxxxxx xxxxxx xxxxxx. Xxxxx jde x xxxxx v xxxxxxxxxx §101 odst. 1, xxxxx xxxxxxx xxxxx x xxx, xx xxxxxxxx xxxxxxxxxx xx xxxx xxxx xxxxxxxxx xxxxxxxxxx x xxxxx, xxxx bude kontrolní xxxxxxx xxxxxxxxx xxxxx xxxxxx xxxxxxxx xxxxxxxx xxx xxxxx xxxxxx x xxxxxxxx a xxxxxx xxx xxxxx xxxxxxxxxx kontrolované osobě xxxxxxx xxxxxxxx x xxxxxxxxxx kontrole xxxxxxxx xx hoc. Změna xx xxxxxxxx xxxxxxxx xxxxxxxxxx xxxxxxx x xxxxxxxxxxx xxxxxxxxxx, x xx xxx xxxxxx xx ryze formální xxxxxxxxxx, konkrétně, xxxxx xxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxx činnost x určitém časovém xxxxx xxxxxxxx, x xx xxxxxx poskytovaných xxxxxxxx xxxxx xxxxx xxxx nemá.
E. Zhodnocení xxxxxxxxxx rizik (XXX)
Xxxxxxxxxx xxxxxx xxxxxx xxxxxxxxx xxxxxx xxxxxxxxxx xxxxx. Xxxxxxxxx xxxxxxxxxxx xxxxxxxxxx xxxxx je xxxxxxx xxx v xxxxxxxxxxxx xxxxxxx, xxx se xxxxxxxxx varianty xxxxxx, x to jak x xxxxxxx klinického xxxxxxxxx xxxxxxxx přípravků, xxx x v xxxxxxx xxxxxxxx xxxxxx xxxxxxxx xxxxxxxxx. Předložený xxxxx xx xxxx xxxxxxxx přiměřený xxxxx, x jejichž xxxxxxxx xx xxxxxxxxxx. Xxxxx xx x xxxxxxxxxxxx xxxxxxxxx xxxxxxx xxxxxxxxx x xxxxxxxxxxxxx hrozby xxxxxxxxxxxxx léčivých xxxxxxxxx xxx xxxxxxx xxxxxxxx x České xxxxxxxxx x xxxxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxxxx vývoz xxxxxxxx přípravků xxxx xxxxx Xxxxx xxxxxxxxx. Xxxxxxxxxx úprava xxxx xxxxxxxxx xxxxxxxxx Xxxxxxxx xxxxxx xxx kontrolu xxxxx x Xxxxxxxxxxxx xxxxxxxxxxxxx a x xxxx xxx stanoví xxxxxxxxx pravomoci, xxxxx x xxxxxxxx xxxxx xxxxxxx xxx xxxxxxxx x xxxxxxxxxxx xxxxxxxxxx xx nejedná x xxxxxx xxxxxxxx rozšíření, xxxxx xx xxxxxxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxx.
XXXXXXXX XXXX
X §1 xxxx. 1 (xxxxxxxx xxxxxxxx xxx xxxxx)
Xx xxxxxxxx pod xxxxx x. 2 xx xxxxxxxx odkaz xx Xxxxxxxx Evropského xxxxxxxxxx x Xxxx (XX) č. 536/2014 xx xxx 16. dubna 2014 x klinických hodnoceních xxxxxxxxx xxxxxxxx xxxxxxxxx x x xxxxxxx xxxxxxxx 2001/20/XX x Xxxxxxxx Xxxxxx x xxxxxxxxx xxxxxxxxx (XX) č. 1252/2014 ze xxx 28. xxxxxx 2014 xxxxxxxxxx xxxxxxxx Evropského xxxxxxxxxx a Rady 2001/83/XX, xxxxx xxx x xxxxxx a xxxxxx správné xxxxxxx xxxxx xxx účinné xxxxx xxx humánní xxxxxx přípravky.
K §5 xxxx. 16:
Xxxxxxxx odstavce 16 xx §5 xxxxxx xxxxxxxxxxxx xxxxxxxx xxxxxx léčivé xxxxx xxxxxxx xxxx xxxxxxx xxxxxxxx xx odůvodněno xxx, xx x xxxxxxxxx xxxxxx úpravě xxxxxx xxxxxxxx chybí, xxx xxxxxxx xxxxxxxxx xxxx, xxx xxxx xxxxxx, xx xx xxxxx xxxxxxx rozumí x xxxxxx režimu xxxxxxx. Navíc toto xxxxxxxx napravuje xxxxxxxxxxxxx xxxxxxxxxxx xxxxxxxx 2001/83/ES (xx. 46x). K xxxxxxxx xxxxxxxx xxxx xxxxxxx nařízení Xxxxxx x přenesené pravomoci (XX) č. 1252/2014 xx xxx 28. května 2014 xxxxxxxxxx xxxxxxxx Xxxxxxxxxx xxxxxxxxxx a Xxxx 2001/83/ES, xxxxx xxx x xxxxxx x pokyny správné xxxxxxx xxxxx xxx xxxxxx xxxxx pro xxxxxxx xxxxxx xxxxxxxxx. Xxxxxxxx v xxx xx nacházející xxxxx xxxxx přímo xxxxx xxx účinné xxxxx xxx xxxxxxx léčivé xxxxxxxxx, x tudíž xxxxxxxx uvedená v xxxxxxxxxxx odstavci 16 xxxx být x xxxxxx xxxxxxx xxxxxxxxx xxxxxx xxxxx a xxxxxxxxx se i xx xxxxxxxxxxx léčivé xxxxxxxxx a xxxxxxxxx xxxxxx xxxxxxxxx.
X §11 xxxx. g):
Zrušuje xx xxxxxxxxxx o xxxxxx xxxxxx xxxxxx k xxxxxxxx xxxxxxxxxx k xxxxxxxxxxxxxxx klinickým xxxxxxxxxx, xxxxx s xxxxxxx xxxxxxxxxx xxxxxxxx č. 536/2014 xxxxxxxxx. Systém etických xxxxxx xx xx xxxxxxxxxxxx xxxxxxxxx státech, xxxxxxxxxx xxx jakýkoli xxxxxx xxxxxxxxxxx x xxxxxxxx xxxx mimo xxxx zajištění xxxxxxxxxxxx xx xxxxxxxxxx, zkoušejícím, xxxxx xxxxxxxxxx hodnocení, xxxxxxxxxx xxxxxxxxxxxx. Xxxxxxxx xxxxxx xxxxxxxx xxxxxx x Xxxxx xxxxxxxxx, xxx xxxxxx xxxxxxxxxxx xxxx poskytovatelé xxxxxxxxxxx xxxxxx, kteří xxxx xxx x xxxxx xxxxxxxxxx xxxxxxxxx, xxxxxxx xxxxxxxxxxx xxxx xxxxxxxxxx, xxxxx jsou xxxxxx x členy xxxxxxxxx xxxxxx xxxxxx, xx xxxxx x xxxxxxx x požadavky nařízení. Xxxxxxxxxx xxxxxx úprava xxxxxxxxx xxxxxxx xxxxxxx xxxxxx jako orgán Xxxxxxxx xxxxxx xxx xxxxxxxx xxxxx, x xx x x xxxxxx, xx v xxxxxxx x xxxxxxxxx č. 536/2014 bude xxxxxx xx xxxxxxxxx xxxxxxxxxx xxxxxxxxx, xxxxxxxxxx xxxx x xxxxx xxxxx xxxxxxx x xxxxxxxx xxx xxxxxxxxx hodnocením xxxxx jedna pro Xxxxxx xxxxx xxx xxxxxxxx léčiv xx xxxxx náhrady xxxxxx, x z této xxxxxx bude xxxxxxx xxxxxxx etické komise x jejich xxxxx. Xxxx xxx xxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxx x čl. 86 xxxxxxxx x. 536/2014 a xxxxxxxxx tak, xx xx xxxxxx xxxxxxx xxx xxxxxxxx xxx xxxxxxxx xxxxx xxxxx xxxxxxxx xx xxxxxxx xxxx.
Xxxxxxx xx zavádí xxxxx xxxx specifická xxxxxxxx Xxxxxxxxxxxx xxxxxxxxxxxxx x vydání opatření xxxxxx xxxxxx xxxxxxxxxxx xxxx zakazujícího xxxxxxxxxx xxxxxxxx přípravku do xxxxxxxxx. Opatření xxxx xxx xxxxxx xxxxx x xxxxxxxxxxxx případech. Xxxxxxxx vydání xxxxxxxx xxxxxx xxxxxx x xxxxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxxxx přípravků xxxx xxxxxxxxx stanoveny x xxxxx ustanovení §77x.
X §11 xxxx. x:
Xxxxxxxxx xxxxxxxxxx §11 xxxx. x) xx xxxxxxxx xxx, xxx se xxxxxxxxxxx xxxxxxxxx s xxxx vkládanými xxxxxxxxxxxx xxxxxx g) xxxx x) x xxxxxx xxx bude pokrývat xxx xx xxxxxxx, xxx Xxxxxxxxxxxx zdravotnictví xxxxxx postupovat xxxxx xxxxxx specifických xxxxxxxxxx.
X §11 písm. q):
Za xxxxxx zajištění xxxxxxxxxxxxxxxx x xxxxxxxxxxxxxxxx postupu xxx omezení reexportů xx xx §11 xxxxxx x xxxxxxxx xxxxxxxx xxxxxxx q), xx xxxxxx xx xxxxxxxx xxxxxxxx Xxxxxxxxxxxxx xxxxxxxxxxxxx seznamu léčivých xxxxxxxxx (xxxxxx opatření xxxxxx xxxxxx), při xxxxxxx xxxxxxxxxx xx xxxx x České xxxxxxxxx by mohlo xxxxxxxxx xxxxxxxxx xxxxxxxxxxxxx xxxxxxxx přípravků při xxxxxxxxxxx xxxxxxxxxxx xxxxxx x České republice.
K §13 xxxx. 2 xxxx. a) xxx 1:
Xxxxxxxxx Xxxxxxxx xxxxxx xxx kontrolu xxxxx xx xxxxxxxxx o xxxxxxxx xxxxxxxxxx o xxxxxxxxxx xxxxxxxx xxxxxxxxx.
X §13 odst. 2 xxxx. x) xxx 3:
Xxxxxxxx xx, xxx xxxxxxxxxxx, kterými xx xxxxxxxxx xxxxxxx podmínek xxxxxxxxx praxí, xxx xxxxxx xxxxxxxxxx hodnocení xxxxxxx xxxxxxx xxxxxxxx xxxxx, xxxxx xxx xxxxx xxxxxxxxxxxxx vydávány x dalším osobám, x xx xxxxxxxxx xxxxxxxxxxx. Xxx xxxxxxxxxx xxxxxxxx nařízení xx xxxxxxxx zajištění a xxxxxxx znalostí zkoušejících x oblasti legislativy x xxxxxxx xxxxxxxx xxxxx, xxxxxx jsou x xxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxx xxxxxxxxx. Xxxxxxxx klinickou xxxxx xx xxxxxx soubor xxxxxxxxxx xxxxxxxx a xxxxxxxxx požadavků xx xxxxxxx při xxxxxxxxxx, xxxxxxxxx, xxxxxxxxxx, xxxxxxxxx, xxxxxx, xxxxxxxxxxxxx a xxxxxxx xxxxxxxxxx xxxxxxxxx x xxx předkládání xxxxx o nich, xxx se zajistilo, xx xxxx xxxxxxxx xxxxx, bezpečnost a xxxxxxx života subjektů xxxxxxxxx x xx xxxxx získané x xxxxxxxxx hodnocení jsou xxxxxxxxxx x xxxxxxxx. Xxxxxxxx xxxxxxx xxxxxxxx xxxxx jsou xxxxxxxxxxx xxxxxxxxxx xxxxxxxx (xxxxxxxx xx dokument XXX X6 Xxxxxxxxxxx xxxxxxxxxx xxx harmonizaci xxxxxxxxxxx xxxxxxxxx na registraci xxxxxxxxx xxxxx - xxxxxxxxx Xxxxxxxxxxxxx Xxxxxxxxxx xx HarmonisationofTechnicalRequirementsforRegistrationofPharmaceuticalsforHuman Use-zkr. XXX, xxx xxxx xxxxxxxx regulačních autorit x xxxxxxxxxxxxxxx xxxxxxxx Xxxxxx, Xxxxxxxx x XXX). Xxxxx xxxxxxxx xxxxxxx Xxxxxxxxxxx xxxxxxxxxx xxx harmonizaci technických xxxxxxxxx xx xxxxxxxxxx xxxxxxxxx léčiv 1.5.1996, xxxx xxxxxxx pravidla xxxxxxx xxxxxxxx xxxxx, x xxxxx xxxxxxx xxxx xxxx promítnuta x xxxxxxxxx x xxxxxxxxxx právním xxxxxxxx.
X §13 xxxx. 2 xxxx. x):
Xxxxxxxx se xxxxxxxxx xxxxxxxxxx Xxxxxxxx xxxxxx xxx xxxxxxxx xxxxx x xxxxxxx xx xxxxx dané xxxxxxxxx. Xxxxxxxxx xxxxxx xxxxxxxxx jak xxxxxxxxxx, xxx xxxxxxxxxx režim xxx xxxxxxxx xxxxxxx x xxxxxxxx hodnocení. Xxx xxxxxxxx xx xxxx jednat již xxx x xxxxxx xxxxxxxxxx.
K §13 xxxx. 2 xxxx. x):
Xx xxxxxxx xxxx výslovné xxxxxxxxxx Xxxxxx xxxx xxxxx xxxxxx xx závadou x xxxxxxx, jejíž xxxxxxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxx nebo xxxxxx, xxxxxxxx xx trhu. Xxxxxxxx xxxxxxxx Ústavu xxxx xxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxxxxx daného xxxxxx xx trhu x Xxxxx republice. Xxxxxxxxxx xxxxxxxx xxxxxxx xxxxxxxx xxxxxxxxxx procesem xxxxxxxxx xxxxxx, xxxxx xxx xx představuje xxxxxxxxxxxxxxx zátěž, xxxxxxxxxx xxxxxxx x náklady xx xxxxxxxxxxx, xxxxx xxxxxx x xxxxx xxxxx závady v xxxxxxx xxxx xxxxx xxxxxxxxxx či xxxxxxxx xxxxxxxxxx. Rozhodování Xxxxxx xxx tohoto xxxxxxxxxx xx xxxxxxxxxxxx xxxxxxxx xx xxxxxxxxxx §23 xxxx. 2, kdy xxxxxxxxxxxx xxxxx xxxxxxxx x xxxxxx se xxxxxxx x jakosti, xxxxx nerozhodne Xxxxx xxx §13 odst. 2 xxxx. x) xxxxx.
X §13 xxxx. 3 xxxx. q) x x):
Xxxxxxxx xx xxxxxxxxx Xxxxxxxx ústavu xxx xxxxxxxx xxxxx xx xxxxxxx xxxxxxx xxxxxxx xx xxxx x léčivými xxxxxxxxx xxxxxxxxxxx pro Xxxxxxxxxxxx xxxxxxxxxxxxx xxxxxxxxx podle §77x.
X §16 xxxx. 2 xxxx. a) xxx 1:
Xxxxxxxxx Xxxxxx xxx xxxxxx xxxxxxxx xxxxxxxxxxxxx xxxxxxxxxxxx x xxxxx xx rozšiřuje x xxxxxxxx xxxxxxxxxx x propadnutí xxxxxxxx xxxxxxxxx.
X §19x:
X xxxx xxxxxxxxx §19x xx xxxxxxxxx xxxxxx xxxxxx xxxxxxxxxx Státního xxxxxx xxx kontrolu xxxxx x Xxxxxxxxxx ředitelstvím xxx x xxxxxx xxxxxxxxx xxxx xxxxxx xxxxxx xxx, aby xxxx být xxxxxxx xxxxxxx xxxxx xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Xxxx 2011/62/EU. Xxxxxx xxxxxxxxxx se xxxxxxxx xxx xx xxxxxxx xxxxxx, xxx i xx xxxxxxx distribuce xx xxxxxxxxx, x xx xxxxxx za xxxxxx xxxxxxxxxxxx xxxxxxxx xxxxxxx distribuce do xxxxxxx xxxx xxxx. xx účelem sledování xxxxxxxxx. Jednalo xx xx xxxx x xxxxxxxxxx xxxxxxxxx xx xxx, x xxxxxxx x xxxxxx xxxxxxxxxxxx. Xxx vložení tohoto xxxxxxxxxx xxx xxxxxxxxx xxxxxx xxx xxxxxx xxxxxx xxx, a xxxxx xxxxxxxxxx x Xxxxxxxxxx xxxxxxxxxxxx xxx xxxx koncepčně nastavena xxxxxxxx xxxxxxxx, jako xx xxxx x xxxxxx č. 226/2013 Sb., x xxxxxxx dřeva x xxxxxxxxxxx xxxxxxx xx xxx. Xxxxxxx xx xxxxxxxx stanoví xxxxxxx x xxxxxxxxxx xxxxxxxxxxxx xxxxxxxxx x daňovém xxxx xxx, xxx Xxxxxx xxxxx pro xxxxxxxx xxxxx xxxx xx Xxxxxxxxxxx ředitelství xxx xxxxxx potřebné xxxxxxxxx.
X §21(Xxxxxxxx VIII, xx. 49 xxxxxxxx):
X §21 se xxxxxxxx xxxxxxxx 1 x xxxx xxxxxx, xx xxxxxxxxxxxx, xxx xx xxxx xxxx xxxxxxxxxxx, xx komplexně xxxx x §54 odst. 1 x xx x xxxxxxxxxx xx xxxxxxxxx xxxxxxxxx nařízením.
X §33 xxxx. 2:
Za xxxxxx xxxxxxxxx xxxxxxxxxxxxx xxxxxxxxxx xxx ohledně dostupnosti xxxxxxxx xxxxxxxxx na xxxx x ČR xx nutné zajistit, xxx Státní xxxxx xxx kontrolu léčiv xxxx xxxxxxxx x xxxxxxxxxx x správnými xxxxx xxxxxxxxxxxx xxxxxx xxxxxxx xxxxxxx o xxxxxxxxx xxxxxxxx xxxxxxxxxxx x jejich objemu xx xxxx v Xxxxx xxxxxxxxx.
Xxxxxxx xxxxxxxxx xx xxxxxxxx xxxxxxxxxx x xxxxxxxxxx xxxxx xxxxxxx x xxxxxxxxxx xxxxxxxxxxx dostupnosti jednotlivých xxxxxxxx xxxxxxxxx x xxxxxxxx xxxxxxxxxxxx podkladů xxx zpracování xxxxxxx xxxxxxxxxx xxxxxxxx přípravků Xxxxxxxxxxxxx xxxxxxxxxxxxx xxxxx §11 písm. x) x možné xxxxxxxxx xxxxxxxx Xxxxxxxxxxxx xxxxxxxxxxxxx xxxxx §11 xxxx. x). Xxxxxxxxxx povinnosti xxxx Xxxxxxxx xxxxxx xxx xxxxxxxx xxxxx xxx xxxx xxxxxxx x xxxxxxxx xxxxxxxxx xxxxx xxxxxxxxx distribučního xxxxxxx (xxxxxxxxxxxx léčivých xxxxxxxxx x provozovatelé xxxxxxxxx x xxxxxx xxxxxxxx přípravků). Xxxxxx xxx xxxxxx xxxxxxx xxxxx xxxxxxxxxx x xxxx, xxx xxxx xxxxx účinně x xxxx zasáhnout proti xxxxxxxxx xxxxxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx x Xxxxx xxxxxxxxx. Doplnění xxxxxxxxxx držitelů xxxxxxxxxx x xxxxxxxxxx poskytovat Xxxxxxxx xxxxxx xxx xxxxxxxx xxxxx xxxxx x xxxxxxx údaje x objemu léčivých xxxxxxxxx xxxxxxxxxx xx xxx xxxxxxx xxxxxxx xxxxx x objemu x xxxxx xxxxxxxxxx xxxxxxxxxx xxxxxxx přípravkem. Xxxxxxxx xxxxxxxxxxxxxx xxxxx xxxxxx xxxxxxxxxx xxxxx xxxx xxxxx přesněji xxxxx rozsah xxxxxxx xxxxxx nedostupnosti xxxxxxxx xxxxxxxxx x také xxxxxxxx přijímat opatření, xxxxx xxxxxx xxxxxxxxxxxxx xxxxxx xxxxxxxx xxxxxxxxx xxx pacienty v Xxxxx xxxxxxxxx. X xxxxxxxx xxxxxxxxx xxxxxx xxxxxxx x účinnější xxxxxxxxxxxxxx xxxxxxx při xxxxxxxx xxxx xxxxxxx xxxxxxxxxx xx vhodnější, xxx xxx rozsah xxxxx, xxxxxx xxxxxxxx x xxxxxx jejich xxxxxxxxxxx formou hlášení xxxxxxxx prováděcím xxxxxxx xxxxxxxxx. Xxxxxxxxx právní xxxxxxx je xxxxxxx xxxxxxxx xxxxxxxxx xxx XXXXXX týkající xx xxxxxxx xxxxxxxx xxxxxxxxx x xxxx údaje xxxxxxxx xx xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx xxx xxx xxxxxxxxx xxxxxxx xxxxxx, xx. jak xxx ÚSKVBL, xxx x pro XXXX. Xxxx xx xxxxx xxxxxxxx xxxxxxx xxxxx xxxxxxx xxxxxxx xx xxxx x nad xxxxx xxxx xxxxxxxxxx xxxxxxxxxxxxx.
Xxxxxxxxxxxx hlášení xx xxxxx s ohledem xx veliké xxxxxx x xxxxxxx xxxxxxxxx xxx, xxxxxxxx to xxxxxx efektivní xxxxxxxxxx x xxx dává xxxxxxx xxxxxxxxx x xxxx reagovat xx xxxxx nedostatek daného xxxxxxxx přípravku xx xxxx. Pokud xx xxxx xx Xxxxx xxxxxxxxxx v xxxx, xxxx. v xxxxxxx xxxxxxxx, xxxxx xx xx Xxxxx xxxxxx xxxxxxxxx xx jednotné xxxxxx, xxx je xxx xxxx xxxxx xxxxxxxxx, xxxxxxxxxx x xxxxxx závěr. X xxxxxxx xx xxxxxxx xxxx, kterou xx Xxxxx na xxxxxxxxxx xxxxxxx x xxxxxx xxxxxxxx přípravků x xxxxxxxx předání podnětu x xxxxxx opatření xxxxxx povahy na XX, xx xxxx xxxxx, xxx elektronická xxxxxx xxxxxxxxxx. Xxxxxx xx nutné vzít x potaz, xx xxxxxxx xxxx xxxxxxx xxxxxxxx xxxxxxxx a xxxxxxxxxx x internetu, xxxxxxxxxxxx xxxxxx xxxxxxxxx xxxxxxxx, XX a xxxxxxxxxxxxx xxxxx xxx, xxxxx xxx xxxx xxxxxx při xxxxxx xxxxxx xxxxxxxxx xxxxxxx xxxxxxxxxx x xxxxxxxxxx xxxxxxx x dokumentace xxx včasné x xxxxx plnění xxxxxxxxxx xxx uložených xxxxxx xxxxxxxxxxxx zákona x xxxxxxxx.
X §33 xxxx. 3 xxxx. x):
Xxxxx xx pouze o xxxxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxx úpravy beze xxxxx jejího obsahu, xxx xx xxx xxx xxxxxxxxxx xxxxxxxx xxxxx xxxxxxx xxxxxxxxxx x xxxxxxxxxx xxxxxxx xxxx xxxxxxxx o xxxxxxxxx léčivých přípravků xx distribuce nebo xx xxxxxxx. Xxxxxxxx xxxx „distribuce xxxx xxxxxxx“ nahrazeny xxxxxx „xx xxx x Xxxxx xxxxxxxxx“.
X §34 xxxx. 2:
Xxxxx x xxxxxxxx x současném xxxxx nijak xxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx xx xxxxxxxxxxx xxxxxxxxxx. S ohledem xx xxxxxxxxxx, že x xxxxxxxxxxx xxxxxxxxxx xxxxxxx xxxxxx v xxxxxx xxxxxxxxxxxxxxxx xxxxxxx, xx xxxxxxxxx xxxxxxx xxxxxxxx xxxxxx léčivého xxxxxxxxx a nutně xxx dochází x xxxxxxxx x xxxxxxxxx xx český xxx x tím ke xxxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx xxx xxxxx xxxxxxxx. Xxxx xxxxxx xxxxxxxx xxxxxxxxx xxxxxx xxxxxxxxx x xxxxxxx xxxx registrací x xxxxxxxxxx §35 xxxx. 2 a xxxxxxx xxxxxxxxxx x §36 xxxx. 4.
Xxx x xxxxxxxx xxxxxxxxxxx xxxxxx, ke xxxxx se přikročilo x rámci xxxxxxxxxx xxxxxxxxx xxxxxxx xxxxxx.
X §51 až 59:
Xxxxx x ustanoveních §51 xx 59 jsou xxxxxxx xxx náležitou xxxxxxxx xxxxxxxx č. 536/2014 xx xxxxxx o xxxxxxxx, neboť představují xxxxx novou xxxxxx xxxxxxxxxx hodnocení humánních xxxxxxxx xxxxxxxxx, xxxxx xxxxxxxx xx xxxxxxxx xxxxxx xxxxxxxxxx v xxxxxxxx č. 536/2014. X xxxxxx ustanoveních xx xxxxxxxxx vypouštějí xx xxxxxxxxxx, xxxxx byla x xxxxxx o xxxxxxxx xxxxxxxxxxxx xxxxxxxxxxxxxx xx xxxxxx xx xxxxxxxx 2001/20/ES a xxxxx xxxx xxxxxxx xxxxx x xxxxxxxx č. 536/2014 xxxx xxxxx xx xxxxxxxxx č. 536/2014 xxxxxxx, x xxxx xx x xxxxxx xxxxxxxxxxxx xxxxxxxx xx xxxxxx xxxxxx, xxxxx xxxxxxxx xxxxxxxxx členskému xxxxx, aby xx xxxxxxx, xxxxx xxxxxxxx xxxxxxx xxxx x xxxxxx xxxxxx.
X §51:
X xxxxx ustanovení xx x xxxxxxxxxx xxxxxxxxx xx čl. 4 xx 9, čl. 15 xx 24 a čl. 83 xxxx. 1 xxxxxxxx x. 536/2014 xxxxxxxxxxx xxxxxx xxxxxxxxxx xxxxxx xxxxxxxxxx hodnocení humánních xxxxxxxx přípravků.
V xxxxxxxx 1 (Xxxxxxxxx (18), (19); Xxxxxxxx XX, čl. 7 xx 9; Xxxxxxxx XXX čl. 15 xx 24 xxxxxxxx) xx vymezuje xxxxxxxx xxxxxxxxx Xxxxxxxx ústavu xxx kontrolu xxxxx x xxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxxx léčivých xxxxxxxxx. Xx xx xxxxxxxxxx žádostí x xxxxxxxx xxxxxxxxxx hodnocení xxxxxxxxx léčivých xxxxxxxxx x žádostí x xxxxxxxx významné xxxxx xxxxxxxxxx xxxxxxxxx a xxxxxxxxx xxxxxxx xxx xxxxxxxx xxxxxxxxxx xxxxxxxxx (Xxxxxxxx XXXX, čl. 77, čl. 78). Veškeré úkony xxxxxxxxx x souvislosti x xxxxxxxxx xxxxxxx x xxxxxxxx klinického xxxxxxxxx (Xxxxxxxx XX xxxxxxxx č. 536/2014), xxxxxxx x xxxxxxxx xxxxxxxx xxxxx xxxxxxxxxx xxxxxxxxx (Xxxxxxxx XXX nařízení č. 536/2014) x xxxxxxxxx xxxxxxx (Xxxxxxxx XXXX xxxxxxxx č. 536/2014) xx xxxxxxxx xx xxxxxxx xxxxx, za které Xxxxxx xxxxx pro xxxxxxxx xxxxx xxxxxx xxxxxxx xxxxxxx. (Xxxxxxxx XXX, čl. 86 x 87)
X xxxxxxxx 2 (Xxxxxxxxx (69); Xxxxxxxx XX, čl. 83 = Xxxxxxx xxxxxxxxx xxxxx) xx xxx reaguje xxxxxxx na čl. 83 xxxx. 1 xxxxxxxx x. 536/2014, které x usnadnění xxxxxxx xxxxxxxxxxx v xxxxx xxxxxxxx xxxxxx xxxxxxxxx xxxxx xxxxx xxxxx xxxxxxx xxxxxxxxx místo.
V xxxxxxxx 3 (Kapitola XX, čl. 5 xx 8 xxxxxxxx) xx xxxxxxxx, xxx xxxxxxxx xxxxxxxxx svěřenou členskému xxxxx za Českou xxxxxxxxx. X xxxxxx xxxxxxxxxxxx xx x xxxxxxxxxxxx xxxxxxxxx xxxxxxxx 3 upravuje působnost x xxxxxxx, xxxx xx Xxxxx xxxxxxxxx xxxxxxxx státem zpravodajem, xxxxxxxxx v případě, xxxx xx Česká xxxxxxxxx xxxxxxxx xxxxxxxx xxxxxx x xxxxxxxxx xxx posouzení xxxxx XX hodnotící xxxxxx, xxxxxxxxxx xx xxxxx x xxxxxxxxx xxxxx. X xxxxxxxx 4 xx xxxxxxxx obecná xxxxxxxxx při xxxxxxxx xxxxxxxxxx xx xxxxxxx xxxx.
X §52 (Kapitola X, xx. 34 xxxxxxxx):
X xxxxx xxxxxxxxxx x xxxxxxxx 1 (Xxxxxxxx X, čl. 29 xxxx. 7 x 8 xxxxxxxx) xx xxxxxxx na xxxxxxxxxx čl. 29 xxxx. 7 xxxxxxxx x. 536/2014, xxxxx umožňuje členskému xxxxx, xxx xx xxxx xxxxxxx xxxx xxxxxxxxx, aby xxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxx k účasti x klinickém xxxxxxxxx xxxxxxx x nezletilý, xxxxx xx xxxxxxx xxxxxxx xx xxxxx x posoudit získané xxxxxxx informace. X xxxxxxxx xx znamená, xx xxxx xxxxxxxxx xxx xxxxxxxxx xxxxx xxxxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxx xxxxxxxxxxx zástupcem x xxxxxx xxxxxxxxx xxxxx, xxxxxxxxxxx, xx xxxxxxx získaných informací xx zkoušejícího a xxxxxxxxx x xxxxxxxxxxx xxx pacienta xxxxxxxxxxxxxx xxxx nezletilého, vůli xxxxxxxxxxx zúčastnit se xxxxxxxxxxx xxxxxxxxxx xxxxxxxxx. X odstavcích 2 x 3 je xxxxxxxxxx možnost xxxx čl. 34 xxxxxxxx x. 536/2014, xxxxx xxxxxxxx xxxxxxxx xxxxxx xxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxx xxxx takovým osobám, xxxxx xxxx x xxxxxxx xxxxxxxxxxxx xxxx xxxxxxxx závislosti. V xxxxxxxxxx xx xxxx xxxxxxxxxx xx xxxxxxx, xx xxxxxxxx xxxxxxxxx xxx xxxxxxxx x xxxxxxxxx xxxxxx xxxxxxxx xxxxxxxxx xxx xxxxx, xxxxx xxxxxxxx xxxxxxx xxxxxxxxx xxxxxx, na xxxxxxx xxxxxxx lze xxxxxxxx, xx účast x xxxxxxxxx xxxxxxxxx xxxx mít pro xxxx subjekty xxxxxxxxx xxxxx léčebný či xxxxxxxxxxx xxxxxx, xxxxx xxxxxxx nad souvisejícími xxxxxx x zátěží. Xxx je xxxxxxxx xxxxxxx zařazení xxxxxx xxxx do čistě xxxxxxxxxx klinických hodnocení (xxxx. xxxxxxxxxx hodnocení xxxxxxxxxxxxxxxxx xxxx xxxxxxxxxxxxxxx), xxxxx xxx xxxxxxxxxx xxxxxxxx hodnocení nemají xxxxx xxxxxx. Xx xxxxxxx xxxxxxx xxxxxxxx xxxxxxxxx xx xxxxxx xxxxxxxx xxxxx nacházející xx xx vazbě, xxxxxxxxxxxxx detenci xxxx xx výkonu xxxxxx xxxxxx svobody, dále xxxxx xxxxxxxxxx x xxxxxxxx xxxxxxx xxxx (xxxx. v xxxxxxxxxx xxxxxxxxxx xxxxxxxxxxxxx xxxxxxxx xxxx, xxxxxxxx xxxxxxxxxxx xxxxxxx xxxx nahrazující xxxx xxxxxx, aj.) x rovněž xxxxx, xxxxxxx xxxxxxxxxxx xxxx xxxxxxx soudem (xxxx. xxxxx, xxxxx nesmí xxxxxxxx se xxxx xxxxxxxx). Vzhledem k xxxx, xx Xxxxx xxxxxxxxx xxxxxxxxxx xxxxx x diskriminaci těchto xxxx xxxxxx xxxxxxxxxx x účasti na xxxxxxxxx xxxxxxxxx, xxx xxxxxxxx xxxxx xxxxxx xxxxxxxxx, xxxxxxxxx xxxxxxxxxx xxxxxxxx pro xxxxxx xxxxx x xxxxxxxxx xxxxxxxxx. Xxxxxxx xxxxxxxxxx xxxxxxxxxxxxx xxxxxxxx xxx xxxxxxxx x xx xxxxxxx xxxxxxxxxx v xxxxxx x zdravotních xxxxxxxx.
X §53 (Xxxxxxxxx (18); Kapitola X, xx. 2 (11):
Úpravu xxxxxxxx x xxxxxxxx xxxxxx komise xxxxxxxx č. 536/2014 ponechává v xxxxxxxxxx xxxxxxxxx států. Xxxxx tato xxxxxxxxxx xxxxxxx x xxxx, xxx xx, xx xx x xxxxxxxx xxxxxx xxxxxx osvědčilo, xxxx x xxxx xxxxxx úpravě xxx xxxxx xxxxxxxxxxx xxxxxxx.
X xxxxxxxx 1 xx xxxxxxxxx xxxxxxxxx Xxxxxxxx xxxxxx xxx xxxxxxxx xxxxx ustavit xxxxxxx xxxxxx jako xxxx xxxxx. Důvody xxxxxxxxxx xxxxxx xxxxxx xxxxxxx x xxxxxxxxxxxxx požadavků xxxxxxxxxxx xxxxxxxxx č. 536/2014: 1) Xx posouzení xxxxxxxxxx hodnocení, významných xxxx xxxxxxxxxx hodnocení x xxxxx xxxxx xxxxxxx x xxxxxxxx xxx xxxxxxxxx xxxxxxxxxx xxxx xxxxx jedna xxxxxx xxx Xxxxxx xxxxx xxx kontrolu xxxxx xx xxxxx xxxxxxx xxxxxx, x xxxx xxxxxx xxxxxx xxxxxx, xxx x xxxx xxxxxx byla xxxxxxx xxxx xxxx xxxxxxx xxxxxx xxxxxx x jejich xxxxx x xxxx zajištěno xxxxxxxxxxx xxxxxxxxx xxxxxx xxxxxx xxxxxx. 2) Xxxxxxxxxx xxxxxx xxxxxx xxxxxxxxxx xxxxxxxxx uvedený x čl. 9 xxxxxxxx x. 536/2014, xxxxx xxxxxxxx, aby osoby xxxxxxxxxx xxxxxx nebyly xxxxxxx xx xxxxxxxxxx, xxxxx xxxxxxxxxx hodnocení, xxxxxxxxx zkoušejících a xxxxxxx financujících xxxxxxxx xxxxxxxxx x xxxxxx xxxxx xxxxxxxx či xxxxxx xxxxx, xxxxx xx xxxxx xxxxxxxx xxxxxx nestrannost.
V xxxxxxxx 2 (Xxxxxxxx XX, čl. 4, 6 a 7, čl. 8 xxxx. 4 x Xxxxxxxx XXX xxxxxxxx) xx xxxxxxxxx xxxxxxxxx xxxxxx xxxxxx. Xxxxx článku 4 xxxxxxxx č. 536/2014 xxxxxx xxxxxxx xxxxxxx xxxxxx xxxxxx v xxxxxxx x xxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxx xxxxx, x xxxxx xxxxxx xxxxxx xxxxxxxx x xxxxxxxx 2 xx xxxxxxxxx adaptace xxxxx tohoto xxxxxx xxxxxxxx.
X xxxxxxxx 3 xx xxxxxxxxx Státnímu xxxxxx xxx kontrolu xxxxx xxxxxxxxx zajistit xxxxxxxx pro činnost xxxxxx komise (xxxx xxx xxxx).
X odstavci 4 je xxxxxxxxx, xx xxxxxx komise xxxx xxxxxxxxxx xx xxxxxxx Xxxxxxx vydaném Xxxxxxx xxxxxxx xxx xxxxxxxx xxxxx po xxxxxxxxxx xxxxxxxx Xxxxxxxxxxxx xxxxxxxxxxxxx. Xxxxxxx řád, xxxxxxxxxx xxxxxxx xxxxxx xxxxxx, xxxxxx sama xxxxxx komise xxx xxxxxxxxxxx xxxxxxxx Ministerstva xxxxxxxxxxxxx.
X §53a
V odstavci 1 xx xxxxxxx xxxxxxx etické komise x xxxxxxxxxxxx xxxxxxxxxx xxxxxxxxxxx xxxxxx etické xxxxxx. Xxxx xx xxxxxxx xxxxxxxxx na xxxxxxx xxxxxxxxxxxx xxxxxx, xxxxx xxxxxxx x xxxxxxxxx správné klinické xxxxx (XXX X6) x x Helsinské xxxxxxxxx, kdy xxx xxxxxxxxx xxxx zásadní xxx provádění xxxxxxxxxx xxxxxxx, x tedy x xxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx xx xxxxxx lidských xxxxxxxx. Zároveň je x odstavci 1 xxxx xxxxxxx xxxxxxxxxx xxxxxxxx na xxxxxxxx xxxxxxx v xxxx xxxxxxx xxxxxxxxx xxxxxxx Xxxxxxx xxxxxx xxxxxx. Xxxxxxxxx jisté xxxx xxxxxxxxxxx xx nezbytné xxx xxxxxxxx nařízení č. 536/2014, xxxxx počítá x přechodným xxxxxxx x xxxxx 3 xxx. V prvním xxxx xxxxxxxxxxx xxxxxx xxxx zadavatel xxxxx, xxx xxxxxxxx žádost x xxxxxxxx klinického xxxxxxxxx xxx nařízení č. 536/2014 xxxx xxx xxxxxxxx platné legislativy. X xxxxxxxxxxxxx dvou xxxxxx xxxx předkládání xxxxxxx x povolení xxxxxxxxxx hodnocení xxx xxx v souladu x xxxxxxxxx xxxxxxxx č. 536/2014, xxx běžící xxxxxxxx hodnocení schválená xx povolená xxxx xxxxxxx účinnosti xxxxxxxx č. 536/2014 xxxxx xxxxx xxxxxxxxx stále xxx xxxxxxxx xxxxxx právní xxxxxx, xxxx. předkládání x schvalování xxxxxxxxxx xxxx klinického hodnocení Xxxxxxx xxxxxxx xxx xxxxxxxx léčiv x xxxxxxxx xxxxxxxx, xxxxx xxxx xxxxxxxx xxxxxxxxx xxxxxxxxx. Xxxxx bude xxxxx xxxxxxxxx xxxxxxxxxx xxxxxxx xxxxxxxx komisí, xxx xxxxxxx již xxxxxxxxx xxxxxx systému xxxxxxxxxx x xxxx xxxxxx zákona. V xxxxxxx 3 letech xxxxxxxxxxx období xxxx xxxxxxx xxxxx počet xxxxxx xxxxxx komise xxx Státním xxxxxx xxx xxxxxxxx xxxxx xxx aktuální potřeby, xxxx xx xxxxxx, xx xxxxx xxxxxx xxxxxx xxxxxx xx xxxxxxx (nejprve xxx 3 skupiny) a xx xxxxx xxxxxxxxxxx xxxxxx (xx 3 xxxx xx xxxxxx xxxxxxxxx xxxxxxxx č. 536/2014) xxxxxx xxx xxxxxx. Xxxxxxxxx xxxxxxx xxxxxx xxxxx vývoje x xxxx xxxxxxx vycházející xxxxxx x xxxxx xxxxxxxxxxxxx žádostí x xxxxxxxx klinického xxxxxxxxx x Xxxxx xxxxxxxxx (xxxx-xx stejný počet xxxxxxxxxx xxxxxxxxx xx xxxxx xxxx naopak xxxxx xxx x xxxxxxxx době). Xxxxxx xxxxxx komise xxxx xxxxxxxxx i xxxxx xxxxx etické xxxxxx, xxxxx xxxx xx xxxxxxx stanoven xxx xx 12-15 xxxxx x jedné skupině, xxx xxxxx xxxx xxxxxx, že by xxxx vhodné počet xxxxxxx xx xxxxxx.
X xxxxxxxx 2xx xxxxxxx, xx členy etické xxxxxx xxxxxxx x xxxxxxxx ministr xxxxxxxxxxxxx. Xxxxxxxxxx tohoto odstavce xx xxxxxxxx nezávislost xxxxxxxxxxx xxxxxx xxxxxx xx Xxxxxxx ústavu xxx kontrolu xxxxx, xxxxx bude xxxxxxxxxxxxxxx xxxxx xxxxxxxxx zaměstnanců xxxxxxxxxx pouze její xxxxxxxxx-xxxxxxxxxxx xxxxxx x xxxxxxxxxxxxxxx xxxxxxx činnosti xxxxxx komise. Zaměstnanci Xxxxxxxx ústavu xxx xxxxxxxx xxxxx zajišťující xxxxxxx xxxxxx xxxxxx xxxxxxx xxxxx xxxxxx xxxxxx, xxxxxxx zasahovat xx procesu xxxxxx xxxxxxxxxx xxxxxxx xxxxxx xxxxxx x xxxxxxx xx xxxxxxx na xxxxxxxxxxx xxxxxx xxxxxx. Xxxxxx úkolem xxxx xxxxxxxxx xxxxxxx, tvorba xxxxxx x xxxxxxx, xxxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxx komise Xxxxxx, x hlavně xxxxxxx xxxxxxxxxx xxxxxxxxxxx lhůt. Xxxxxxxxx nezávislosti xxxxx xxxxxx xxxxxx vychází xx xxxxxxxx praxe xxxxxxxxx xxxxxx Xxxxxxxx xxxxxx xxxxxxxx (EMA), xxxxxxx xxxx např. Xxxxx pro xxxxxxx xxxxxxx (XXX), Xxxxx xxx xxxxxxx xxxxxx xxxxxxxxx (XXXX) xx., xxx xxxxxxx xxxxx xx organizačně, xxxxxxxxx x ekonomicky xxxxxxx xx Xxxxxxxx xxxxxx xxxxxxxx, xxx xxxxxxx xxxxxxx x rozhodování xx xxxxxxxxx.
Xxxx je x xxxxx xxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx xx xxxxxxx skupiny xxxxxx xxxxxx x xxxxxx xxxxxx xxxxxxxx x místopředsedy, xxxxxxx xxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxxxxx skupin etické xxxxxx.
X odstavci 3 xx upraven xxxxxxxxx xx xxxxx etické xxxxxx x xxxxxxx x xxxxxxxxx čl. 9 xxxxxxxx x. 536/2014, xxx byla zajištěna xxxxxx nezávislost na xxxxxxxxxx, xxxxxxxxxxxx x xxxxxxx klinického hodnocení, xxxxxxx xx stanoven xxxxxxxxx xx xxxxxxxxxx x xxxxxxx klinického xxxxxxxxx.
Xxxxxxxx 4 xxxxxxx x xxxxxxxxx právní xxxxxx, xxxxx nedoznává xxxxxxxx xxxxxxxxxxx změn, xxxxx xxxxxxxxxx výslovného xxxxxxxxx xx xxxxxxx xxxxxxx člena xxxxxx xxxxxx x xxxx xxxxxxxxx v etické xxxxxx, x xxxxxxxx xxxx xxxxxxxxxx xxxxxxxxx xxxxxxxx správné klinické xxxxx, xxxxxxx dodržování xxxxxxxx č. 536/2014 xxxxxxxx.
Xxxxxxxx 5 xxx ukládá xxxxxx xxxxxx komise xxxxxxxxxx xxxxxxxxxxx o xxxxxxxxxxx x xxxxxxxxxxxxx, xxxxx se xxxxx x xxxxxxxxxxx xx xxxx xxxxxxxxx v xxxxxx komisi.
Odstavec 6 xxx xxxxxxxxx xxxx, xxx členem etické xxxxxx xxxx taková xxxxx, která xx xxxxxxxxx xxxxxxxxx xxxxxxxxxxxxx x tom, xx xxxxxx xxxxxxxxx zachovávat xxxxxxxxxxx, xxxxxxxxxx x xxxxxxxx 5. Xxxxx xx člen xxxxxx xxxxxx xxxxxxxx xxxxxxxxx xxxxxxx, jeho xxxxxxxx x xxxxxx komisi xxxxxxx přímo xx xxxxxx.
X §53x a §53x
Xxxx xxxxxxxxxx rozvádí xxxxxxxxx xx činnost xxxxxx xxxxxx, xxxxx xxxxxxxxx x nařízení č. 536/2014 x xxxxxxx xxxxxxxx praxe ICH X6. Xxx ustanovení xxxxxxx xx xxxxxxxxxxx, xx xx xxxxx xxxxxxx o xxxxxxxx xxxxxxxxx bude xxxxxxxxx xxxxxxxxxxx, xxxxx bude xxx xxx xxxxxxxxxx xxxxx –dokumentace, xxxxxxxx xx aspektů, na xxx xx vztahuje xxxx X xxxxxxxxx xxxxxx, xxxxx je xxxxxxxx xxx xxxxxxx xxxxxxx XX (Protokol, Xxxxxxxxxxxx´xXxxxxxxx, xxxxxxxxxxxxx dokumentace xx.), x xxxxxxxxxxx, xxxxxxxx se xxxxxxx, xx xxx xx xxxxxxxx xxxx II xxxxxxxxx xxxxxx, která xx xxxxxxxxx x xxxxxxxx xx xxxx xx xxxxxxxxxxx ČS (Xxxxxxxxx xxx pacienta, xxxxxxxxxxx xxxxxxx, xxxxxx xxxxxxxxxxxx, xxxxx xxxxxxxxxx xxxxxxxxx, zajištění xxxxxxxxx xx.). Dokumentaci, xxxxxxxx xx xxxxxxx, na xxx xx vztahuje xxxx I xxxx xxxx II xxxxxxxxx xxxxxx xxxx xxxxx xxxxxxxxx xxxxxxxxxx x xx i x xxxxxxx xxxxxx, xxx. 2 xxx. Xxx xxxxxx xxxx bude xxxxxxxxx xxxxxxxxxx hodnotící xxxxxx (xxxxxxxxxxx xxxxx xxxxxxxxx xxx xxxxxxxxxx Xxxxxxxx xxxxxx x Xxxxxxxx xxxxxx xxxxxxxx (XXX), xxxx se xx nich pracuje x xxxxx xxxxxxxxxxxx xxx XXX). V xxxxx xxxxxxxxx xxxxxx xxxx xxxxxx závěr xxxxxxxxx xxxx xxxxxxx, xxxxx bude poskytnut xxxxxxxxxx, a to xxxxxxxxxxxxxxx xxxxxxx. Xxxxxxxxx xxxxxxxxxx xx xxxxxxx xxxx bude vydáno xx xx vydání xxxx závěrů xxxxxxxx xx xxxxxxx, xx xxx se vztahuje xxxx X a xxxx XX hodnotící xxxxxx. Xxx bude xxxxxx formou xxxxxxxxxxxxx, xxx. xxxxxxxxx xxxxxx x xxxxxxxxxx x xxxxxxxxxx, xx xxxxxx xxxxxx se xxxx x xxxxx xxxxxxxxxxxx xxx Xxxxxxxx xxxxxx xxxxxxxx xxxxxxx.
Xxxxxxxxxx §53x x odstavci 1 xxxxxxx povinnosti xxxxxx xxxxxx x xxxxxxxxx xxxxxxx xxxxxxxx xxxxx XXX X 6 x Helsinské xxxxxxxxx xx xxxxxxxxx ochrany xxxx, bezpečnosti x xxxxxx xxxxxxxx subjektů xxxxxxxxxx xx xxxxxxx x humánními xxxxxxxx xxxxxxxxx. Zároveň upravuje xxxxxxxxx xxxxxxxxxxx x xxxxxxxxxxxx nesouhlasné stanovisko xxxxxx komise, xxx xx xxxxxxx v Xxxxxxxx II, článku 8 xxxx. 4 nařízení x. 536/2014.
Ustanovení §53b x xxxxxxxx 2 xxxxxxx z požadavku Xxxxxxxx XXXX xxxxxxxx č. 536/2014, xxxxxxx klinické xxxxx ICH X 6 a Xxxxxxxxx xxxxxxxxx, které vyžadují xxxxxx xxxxxx komise xxx xxxxx xxxxxxxxxx xxxxxxxxx, xx xxxxxx xxxx xxxxxxx. Xxxxxx xx xxxxxxxx xx xxxxxxx xxxxxxxxx zpráv x xxxxxxx xxxxxxxxxx xxxxxxxxx x xxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxxxxxxx xxxxxxxxxxx nebo xxxxxxx xxxxxxxxxxx, xx-xx xxxxx (XXX X 6, xxxx 4.10.1: „Xxxxxxxxxxxxxxxxxxxxxxxxxxxxxxxxxxxxxxxxxxxxxxxx xxxxx xxxxxx to xxx IBR/IEC annually, xx more xxxxxxxxxxxxxxxxxxxxx xx xxx XXX/XXX.“, xxx XXX/XXX se xxxxxx XxxxxxxxxxxxxXxxxxxXxxxx/Xxxxxxxxxxx XxxxxxXxxxxxxxx). Xxxxx xxxx o xxxxxxxxxx dohled xx Xxxxxxx xxxxxxx xxx xxxxxxxx léčiv, xxxxx Xxxxx bude xxxxxxxxx xxxxxx xxx xxxxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxxxxxxxxx xxxxxxxx správné klinické xxxxx, případně xx xxxxxxx xxxxxxxxx xxxxxxxxx xx xxxxx o xxxxxxxxxxx přípravku, xxxxxxx xxxxxxxxxx xxxx xxxxxxxxxx xxxxxxxxx a s xxx xxxxxxxxxxxxx přehodnocení xxxxxx xxxxxxx x xxxxxx spojeného x xxxxxx xxxxxxxx xxxxxxxxx x daném xxxxxxxxx xxxxxxxxx, xxxxxxxx z xxxx xxxxxx xxxxxxxx Xxxxxx (spolupráce x xxxxx xxxxxxx XxxxxxxxXxxxxxXxxxxxxxxxxx Xxxxx (CTFG), XxxxxxxxxxxxXxxxxxxxXxxxxxxxx (XXX), Committeeformedicinalproductsforhuman xxx (XXXX) x xxxxxx).
Xxxxxxxxxx §53x x odstavci 3 xxxxxxx z xxxxxxxxx Xxxxxxxx II článek 10, x xxxx článku 5 xxxx. 7 xxxxxxxx č. 536/2014 x xx správné xxxxxxxx xxxxx ICH X6, článku 3.2.6 (Xx IRB/IEC mayinvitenonmemberswithexpertise xx xxxxxxxxxxxxxxxxxxxxxxxxx.)
Xxxxxxxxxx §53b x xxxxxxxx 4 xxxxxxxxx etické xxxxxx xxxxxxxxx vykonávat xxxx xxxxxxx v xxxxxxx x xxxxxxxxx nařízení č. 536/2014 x Xxxxxxxx xxxxx. (xxxx xxx xxxx).
Xxxxxxxxxx §53x x xxxxxxxx 5 xxxxx, xx jednotlivé xxxxxxxx xxxxxx xxxxxx xxxxx xxxxxxxxx xxxxx xxxxxxxxxx xxxxxxx (ICH X6, xx. 3.2.2 Xxx XXX/XXX shouldperformitsfunctionsaccording xx xxxxxxxxxxxxxxxxxxxxxxxxxx), xxx xx xxxx xxxxxxxx jednotný x xxxxxxxxxxxxx postup xxxxxxxxxxxx skupin xxxxxxxx xxxxxx. Xxxxxxxx xxxxxx xxxxxxx xxxx xxxx, xxx xxxxx xxxxxxx xxxxxx xxxxxx xxxxxxxx x xxxxxxxx xxxxxxxxxx, xxxxxxx xxxx hlášení xxxxxxxxxxx xxxxxx - Xxxxxxxx VII, Xxxxxxxx XXXX čl. 53 xxxxxxxx, xxx je xxxxxxx, xx xx xxxxxxxxx xxxx oznamovat „xxxxxxxx xxxxxxxx státům“, xxx. xxxxxxx xxxxxxxxxxxx se xxxxxxxxx xxxxxxxxx x Xxxxx xxxxxxxxx (Xxxxx x xxxxxx komise), xxxxx xx xxxxxxx xxx o xxxxxx xxxxxxxxxxxxx; xxxx xxx xxxxx aktualizaci Xxxxxxxxxxxx´xXxxxxxxx, x x neposlední xxxx xxx Kapitoly XXXX, čl. 52 x xxxxxxx xxxxxxxx od xxxxxxxxx; další xxxxxxx xxxx získávat xxxxxx xxxxxx od xxxxxxxxxxxx, xxxxx x xxxxxx x xxxxxxx xxxxxxxxxx xxxxxxxxx x xxxx xxxxxxx xxxxxxxxx odchylek xx protokolu (Xxxxxxxx XXX, čl. 53 nařízení). Xxxx pracovní xxxxxx xxxx x xxxxxxxxx xxxxxxxxxx mezi etickou xxxxxx x Ústavem x zajištění xxxxxxxxx xxxxxxxxxx xxxxxx komise. Xxxxxxxx postupy xxxxx xxxxxxxxxx pravidel pro xxxxxxxxxx xxxxxxxx xxxxxx xxxxxx vyplývající x xxxxxxxxx xxxxxxxx č. 536/2014, x zajištění xxxxxxxxxxx xxxxxxxx.
Xxxxxxxxxx §53x x xxxxxxxx 1 a 2 xxxxxxx x xxxxxxxxx nařízení x. 536/2014 xxxxxxxx XX xxxxxx 4 x xxxxxxxxx xxxxxxxx přezkumu. Xxxx xxxxxxxx specifikují xxxxxxxx xxxxxx komise xx posouzení dokumentace, xxxxxxxx xx xxxxxxx, xx xxx se xxxxxxxx část X xxxxxxxxx zprávy, xxx xxx xxxxxxxx xxxxxxx x klinické hodnocení, xxx xxx xxxxxxxx xxxxxxx x xxxxxxxxx xxxxx xxxxxxxxxx hodnocení. Xxxxxx xxxxxxxxx xxxxxxx xx xxxxxxxx praxe; xxxxxx xxxxxx xxxx xxxxxxxxx (Xxxxxxxx XX, čl. 6 xxxx. x) xxx i + Příloha č. I, xxxx. D) xxxxxxxxxxxxxx provedení xxxxxxxxxx xxxxxxxxx, xxxx xx xxxxxx xxxxxxxxxx, xxxx xxxxxxxxx chce dané xxxxxxxx xxxxxxxxx xxxxxxxx (xxxx. xxxxxx xxx xxxxxxxxx klinická xxxxxxxxx, xxxxx xxxxxx vědecký xxxxxx, xxxx. sledují xxx xxxxx prokázané, xxxx xxxx obsolentní, xxx. xxxxxxxxx léčba xx xxx překonaná x xxxx důvod xx k ní xxxxxx) x xxxxxxxxxx xxxxxxxxxx xxxxxxxxx, xxxx xx rozumí navržený xxxxxx (xxxx-xx xxxxxxxx xxxxxxxxx xxxxxxxxxxxxxx či xxxxxxxxxxxxx, x xxxxxxxxxxx xxxxxxxxx x xxxxxxx xxxx, xxxxx-xx xx x xxxx I xx XX xxxxxxxxxx xxxxxxxxx xxx xxxxx xxxxxx léčivého xxxxxxxxx, xxxx-xx xxxxxxx xxxxxxx xxxx xxxxxxx xxxxxxxxxx, xxxxx-xx se x xxxxxxxx xxxxxxxxx xxxxxxx xx xxxxxxxxxxx, xxxxxxxxx, xxxxxxxxx, xxxxx-xxxxx xx.). Xx základě xxxxx xxxxxxxxx xxxxxxxxx xxx xxxxxxx xxxxx xxxxxxx x rizik xxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxx x xxxxxx xxxxxx x xxxxxxxxx xxxxxxxxx.
Xxxxxxxxxx §53x v xxxxxxxx 3 až 5 xxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxxxxx, xxxxxxxx xx aspektů, xx xxx se vztahuje xxxx XX hodnotící xxxxxx pro území Xxxxx xxxxxxxxx. V xxxxxx xxxxxxxxxx xx xxxxxxx xx současné xxxxx x ponechává xx i xxxxxx xxxxxxxxxx xxxxxxx xxxxxxx xxxxxxxx se xxxxx xxxxxxxxx xxxxx (xxxxxxxxx xxx xxxxxxxx, xxxxxxxxx xxxxxxxxxx x xxxxxxxxxxxx, xxxxxxxxxxx zkoušejících, schvalování xxxx xxxxxxxxxx xxxxxxxxx, xxxxxxxxx xxxxxxxxx xxxxxxxxxx x xxxxx x xxxx…) x působnosti xxxxxx xxxxxx.
Xxxxxxxxxx §53x x odstavci 6 xxxxxx odpovědnost xx xxxxxxxxxx stanoviska předsedovi xxxxxxx xxxxxx xxxxxx.
Xxxxxxxxxx§53x x odstavci 7 x 8 xxxxx xxxxx xxxxxxxx, x xxxxxx xxxxxxxxx může xxxxxxx xxxxxx komise xxx souhlasné xxxxxxxxxx x zároveň uvádí xxxx xxxxxxxxxxx. A xxxx xxxxxxx x xxxxxxxxx Xxxxxxxx II článku 4 xxxxxxxx x. 536/2014, xxx xx xxxxxxxxx xxx členský xxxx povinnost xxxxxxxx xxxxxxxxxx lhůt pro xxxxxx xxxxxxx. Celé xxxxxxxxxx xx xxxxxx x xxxxxxxxxxxxx úkonů: 1. xxxxxxxx = xxxxxxxx došlé xxxxxxxxxxx xx xxxxxxxx stránce, 2. xxxxxxxxx - xxx xxxx X xxxxxxxxxxx (xxx xxxxxx xxxxxx - Xxxxxxxx, Xxxxxxxxxxxx´xXxxxxxxx - posouzení x vypracování xxxxxx xxxxxxxxx zprávy = xxxxxxxx přezkumu x xxxxxxx xxxxx. xxxxxxxxxx, 3. xxxxxxxxxx xxxxxxxxxx xx. xxxxxxxx zadavatele, 4. xxxxxxxxx xxxxxxx xxxxxxxxx zpráva x xxxxxxxxxx (xxxxxxxx/xxxxxxxx s xxxxxxxxx/xxxxxxxxx). To jsou xxxxxxxxxx úkony, xx xxxxx xx xxx xxxxxxxxx č. 536/2014 xxxxxxxx, xxx. max. xxx xxx jejich xxxxxxxxxx/xxxxxxxx. Xxxxx xxxxxx xxxx xxxxxx pro xxxxxxxxx xxxxxxxxxxx, xxxxxxxx xx xxxxxxx, xx xxx xx xxxxxxxx xxxx X xxxxxxxxx zprávy, xxx x xxxxxxxxxxx, xxxxxxxx se xxxxxxx, xx xxx xx xxxxxxxx část XX xxxxxxxxx xxxxxx klinického xxxxxxxxx. Dle Xxxxxxxx XX čl. 4 xxxxxxxx x. 536/2014 je xxxxxx xxxxxxx xxxxxxxxx xxx xxx posouzení xxxxxxx x xxxxxxxx xxxxxxxxxx xxxxxxxxx, xxx x xxx xxxxxxxxx xxxxxxx x xxxxxxxx xxxxxxxx změny.
Ustanovení §53x x xxxxxxxx 9 xxxxxx Xxxxxxxx xxxxxx xxx kontrolu léčiv, xxxxx bude etická xxxxxx xxxxxxx Xxxxxx, xxxxxxxxx xxxxxxxxxx xxxxxxx x činnosti xxxxxx xxxxxx po xxxx 5 xxx.
X závaznosti xxxxxxxxxx etické komise xx xxxxx, xx xxx xxxxx xxxxxxxx, xxxxx xxxx xxxxxxxxxx XX negativní, xxx Xxxxx xxxxxx x xxxxxxxx xxxxxxxxx xxxxxxx. Xxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxx, xxx xx xxxx xxxxxxx. Xxxxxx xxxxxx sama x xxxx xxxxxx xxxxxxx xxxxx xxxxxxxxxx. Xxxxxxxxxx x xxxxxxx o xxxxxxxx xxxxxxxxxx hodnocení xxxx povolení xxxxxxxx xxxxx xxxx vydávat Xxxxx, x to x xxxxxx xxxxxxxxx xxxxxx. Xxxx xxxx xxxxx xx xxxxxxx xxxxx rozhodnutí, xxxxx xx bude xxxxxxxx xx xxxxxxxxxx xxxxxxx xxxxxxxx xxxxxx xxxxxx, x tomto smyslu xx stanovisko xxxxxx xxxxxx povahu xxxxxxxxx xxxxxxxx pro xxxxxxxxxx. Xxxxxxxx xxxxxx xxxx xxx xxxxxxx brojit xxxxx xxxxxxx xxxxxx xxxxxx prostřednictvím xxxxxxxx xxxxx xxxxxxxxxx Ústavu.
Co xx xxxx xxxxxxxx xxxxxxxxxx xxxxxxx xxxxxx xx xxxxxxx xxxxxxxx, x xxxxx xxxxxx xxxxxxxx. Xxxxxx xxxxxxxx xxxxxxxxxx je xxxxxx xxxxxxxxxxxxxx v ustanovení §53x.
X §54 (Kapitola XXXX, xx. 49 x 50, Kapitola XX, xx. 73 xxxxxxxx):
Xxxxxxxxxx se zabývá xxxxxxxxxxxx x xxxxx xxxxxxxxxx hodnocení. Čl. 49 xxxxxxxx x. 536/2014 xxxxxxxxx xxxxxxx xxxx x xxxx, xxx xxxxx, xxx xxxx xxx xxxxx jeho xxxxxxxxxxxxxx právních xxxxxxxx xxxxxxxxxxx xx xxxxxxx xxxxxxxxxxx. Xxxxx xxxxxxxxxx xxxxxx xxxxxx xxxxxxxxxxx x hlavním xxxxxxxxxxx xxxx xxx xxxxx xxxxx xxxx zubní xxxxx xxxxxxxxx podmínky xxxxxxxxx zákonem č. 95/2004 Sb., xx xxxxx pozdějších xxxxxxxx, pro xxxxx xxxxxx xxxxxxxxxxxxxx povolání, xxxxx má nezbytné xxxxxxx xxxxxxxx x xxxxxxxxxx x péčí x xxxxxxxx x xxxxxxxxxxx či xxxxx, xx xxxxxxx léčbu xx xxxxxxxx xxxx xxxxxxxx xxxxxxxxx x xx xxxxxxxx správné xxxxxxxx xxxxx.
Xxxxxxxx 2 xxxxxxx x xxxxxxxxx čl. 50 xxxxxxxx č. 536/2014 na xxxxx xxxxxxxxxx xxxxxxxxx. Xxxxx xxxxxxxxxx xxxxxxxxx xxxxx xxx xxx u xxxxxxxxxxxxx xxxxxxxxxxx xxxxxx xx xxxxxxxxxxxxxx zařízeních, xx. xxxxxxxx xxxx, xxxxx xxxx xxxxx xxxxxx oprávněny x xxxxxxxxxxx zdravotních služeb xxxxx zákona č. 372/2011 Sb., xx xxxxx pozdějších xxxxxxxx, x xxxxxx xxxxxxxx bude posuzována xxxxxxxxxx xxx xxxxx xxxxxxxx xxxxxxxxx xx xxxxxxxxxxx xxxxxxxxx xx xxxxxxxxx xxxxxxxx a xxxxxxxxxx xxxxxxxxx xxxxxxxx x xxxxxxxxx xxxxxx xxxxxxxxxx xxxxxxxxx.
Xxxxxxxx 3 x 4 xxxxxxxxx xxxxxxxxxxx či fakultativní xxxxxxxxx pro místa xxxxxxxxxx xxxxxxxxx xxxxxx xxxxxxxxxx xxxxxxx xxxxxxxx xxxxx, xxxxxx Ústavem. Xxxxxxx vychází xx xxxxxxxxxx znění xxxxxx x xxxxxxxx x xxxxxxxx praxe, x xxxxxxxx xxx subjekty xxxxxxx x odstavci 3 povinnost xxxxxx xxxxx certifikát, a xx z xxxxxx, xx xx jedná x xxxxx x xxxxxxxx hodnocení, xxxxx xxxxxxx xxxxxx riziková xxxxxxxx hodnocení (první xxxxxx xxxxxxx) xxxx xxxxxxxx hodnocení bez xxxxxxxxx nebo xxxxxxxxxxxxx xxxxxxx pro xxxxxxxxxx xxxxxxxx xxxxxxxxx (xxxxxxxxxxxxxxx xx xxxxxxxxxxxxxxxx xxxxxxxx xxxxxxxxx).
X §55 (Xxxxxxxxx (26); Xxxxxxxx XX, xx. 26 xxxxxxxx x. 536/2014):
X xxxxx xxxxxxxxxx xxx x xxxxxxxx čl. 26 x 69 xxxxxxxx x. 536/2014, podle nichž xx xxx xxxxxxx xxxx xxxxx xxxxxxxx xxxxxxxxx na xxxxxxxxxxx xxxxxxxxxx xxxxxxxxx a xxxx by měl xxxxx xxxxx xxxxxxxxx xxxxxxxxx v xxxxxxxx xx obalu. X §55 xx vychází x xx zásady, xx xx xxxxxxxxx x dokumentace xxxxxxxxxx xxxxxxxxx, xx xxxxxxx xxxxxxxx do xxxxx xxxxxxx xxxxxxxxx, xxxx xxx xxxxxxxxxx v xxxxxxx. Xxxx jiné xxx xxxxxxxxx x xxxxxxxxx xxx pacienta, xxxxx xxxxxxxx, xxxxx xxx užívání xxxxxxxx xxxxxxxx a xxxxx x xxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxxx. Požadavek xx xxxxx xxxxx xxxxxxxxx xx uveden i xxx xxxxxxxxx, u xxxxx xx x xxxxxxx xx vysokou xxxxxxxxx daného xxxxx xxxxx xxxxx xxx xxxxxxx xxxxxxxx xx xxxxxxx xxxxxx x xxxxx xxxxxxxxxxxx, xxxxxxxxx xxxxxxxx xxxxxxx. Ostatní xxxxxxxxx z xxxxxxxxxxx xxxxxxxxxx hodnocení xx xxxxxxxxxxx x xxxxxxx, xxxxxxxxxxx nebo angličtině. Xxxxx xxx o xxxxx xxxxxxxxx xxxxxxxxx x xxxxxxxx xx xxxxx léčivých xxxxxxxxx xxx klinické hodnocení, xxxxx se xxxxxx xxx, xx xxxxx xxxxxxx xx xxxxxxx, xxxx-xx x xxxxxxxxxx Xxxxxxxx xxxxxx xxx xxxxxxxx léčiv o xxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxx xxxxx. Xxxxxxx xxxxxxxx cizojazyčného xxxxx xxxxxxx xx xxxxxxxxxxx, xx x xxxxxxxxx xxxxxxxxxxxxx xxxxxxxxxx hodnocení, xxxxx mají zařazen xxxxx xxxxx xxxxx xxxxxxxx (hlavně xxxxxxx xxxxxxxx onemocnění) xx xxxx xxxxxxxxxxxx xxxxxxx x zátěží pro xxxxxxxxxx, aby u xxxxxxxxx, xxxxx podává xxxxx, xxxxxxxxxx xxxx xxxxxxxx na xxxxx x xxxxxx xxxxxx. Xxxxxxxxxxxx označení na xxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxx xx xxxxxxxxx xxxxx xxxxxxxx xxxxxxxxx x xxxxxx xx českých xxxxxxx xx x tomto xxxxxxx xxxxx xxxx x vyloučení Xxxxx xxxxxxxxx x xxxxxxxxxx xxxxxxxxx, x xxxx xx xxxxxxxxxxxxxx xxxxx xxxxxxxx x xxxxxxxx x velmi xxxxxxx xxxxxxx xxxxxxxxxx. Bezpečnost xxxxxxxx xxxxxxxxx bude xxx zajištěna požadavkem xx xxxxx xxxx xxxxxxxxx x xxxxx, xxxxx xxxx xxxxx x xxxxxxxxxx x xxxxxxxxxxxx obalu distribuován xxxxxxxxxxx a ti xxxxx xxxxxxx se x xxx seznámit, xxx xxxx schopni xxxxxxxx xxxxxxx používání x xxxxxxxxx x xxxxxxxxxx léčivým přípravkem.
K §56 (Xxxxxxxx XXXX, xx. 59 xxxx. 3; Xxxxxxxx XX, xx. 61 xxxx. 5 xxxx. b), xx. 68; Xxxxxxxx XXXXX, xx. 90 x 92 nařízení x. 536/2014):
X xxxxx xxxxxxxxxx se xxxxxxxxx xxxxxxxx xx xxxxxxxxxx čl. 59 odst. 3 xxxxxxxx č. 536/2014, xxxxx vyžaduje, aby xxxxxxx xxxx xxxxxxxx, xx xx xxxxxx xxxxxxx v xxxxxxxxx xxxxxxxxx xxxxx xxxx xx xxxx xxxxx xxxxxxxx xxxxxxxxxxxxxx pomocné xxxxxx xxxxxxxxx. V xxxxxxxx 2 xx xxxxxxx xxxxxxxxx xxxxxx xxxxxx, xxxxx xx xxxxxxxxx xxx, že xx xxxxxxxx xxxxx xxxxxxx za stanovených xxxxxxxx použít x xxxxx xxxxxxxxxx xxxxxxxxx x takové xxxxxxxxxxxx xxxxxxxxxx, xxxxx xxxxx xxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxx o zdravotnických xxxxxxxxxxxx. Xxxxx požadavek xxxxxxx x xxxxxxxxxx xxxxx zajistit validitu x xxxxxxxxxx xxx, xxxxxxxxx x xxxxxxxxxx xxxxxxxxx. Toto je xxxxxxxxx xxxx. právě xxxxxxxxxxxxx xxxxxx použitím xxxxxxx xxxx zdravotnického xxxxxxxxxx ve xxxxx xxxxxxxxxxxx xxxxxxx (xxxxxxx xxxxx EU x 3. xxxx) x xxx x xx xxxxx xxxxxxx klinického xxxxxxxxx. U xxxxxxxxxx xxxxxxxxx, xxxxx xxxx xxxxxxxx na xxxxxxxxx xxxxxx xxxxxxxx, jejíž xxxxxx se xxxxxxx xxxxxxxxxxxxx xxxxxxxxxxx, a xxxxxxxxx xxxxxxxx xxxxxxxxxx xxxxxxxxx je usazen xx xxxxx xxxx (xxxx. XXX) xx xxxxxxxx xxxxxxxxxx xxxxxxxxxx, xxx xxxxxxx zúčastněné xxxxx xxxxxxxxx xxxxxxx, xxx xxxxxx xxxxxxxxxxxx xxxxxxxxxx xxx, xxx xxxxxxxx xxxxxx xxxxxx xxxxxxxxx xxxxxxxxxxx xxxxxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxxx. Používání xxxxxxxx xxxxxxxxxxxxxx xxxxxxxxxx xx xxxxxxxxx příslušnou xxxxxxxxx země zadavatele x xxxxxxxxx xxxx xxxxx tento xxxxxxxxxxxx xxxxxxxxxx xx území Xxxxxxxx unie použít xxxxx než x xxxxx xxxxxxxxx xxxxxxxxx, x xx xxxxxxx x xxxxxxx na xxxxxxxxxx, xx xxxxxx xxx není xxxxxxxx xxxxxx xxxxxxxxxxxxxx xxxxxxxxxx. Xxxxxx xxx xxxxx xxx xxx nehrozí, xxxxx xxxxxxxxxxxxx pro xxxxxxxx xxxxxxxx xxxxxxxxxx xxxxxxxxx bude tento xxxxxxxxxxxx prostředek xxxxxx xxxxxxxxxx, x tedy xx xxxxxx xxxxxxxxxx x České republice. X případě, xx xx xxxx úprava xxxxxx akceptována, xxxxx xxxxxxxxx Xxxxx xxxxxxxxx x provádění xxxxxxxxxx xxxxxxxxxx xxxxxxxxx, přestože xxxx xxxxxxxx benefity xxx xxxxxxxxxxx populaci x České xxxxxxxxx. (Xxxxxxxxx může xxx xxxx. použití xxxxxxxxxx xxxxxxxxxxx x xxxxxxxxxxx xx 3. xxxx (XXX), který xxxxxx xxxx xxxxxxxx xxxxxxxxx x Xxxxx xxxxxxxxx xxxxxxxx. Xxxx povolení xxxxxxx v xxxxxxxxx xxxxxxxxx xxxxxxx xxxxxxx xxxxx novým vyvíjeným xxxxxxxxxx, xxxxx xx xxxxxxxx xxxxxxxxxx může xxx dostupný i xxx české xxxxxxxx, x xx i xxxxxx, xx xxxxxxxxx xxxxxxxxx v xxxxx xxxxxxxxxx xxxxxxxxx xxxx xx xxxx ukončení xxxxxx xxxxxxxxxxx x xxxxxxx x České xxxxxxxxx, registrace hodnoceného xxxxxxxx xxxxxxxxx a xxxx dostupnost xx xxxx v České xxxxxxxxx není xxxxxxxxx xxxxxxxxxxx tohoto xxxxxxxxxxxxxx xxxxxxxxxx, xxx xxxx xxxxxxx v xxxxxxxxx xxxxxxxxx zajišťuje validitu x xxxxxxxxxx xxx. Xxxxx xxxxxxxxx může xxx xxxxxxxxxxxx prostředek xxxxxxxx xxx xxxxxxxxxx xxxxxx, xxxx. xxxxxx xxxx xxxxxxxxx xx xxxxxxxxx xxxxxxx, která xxxxxxx xxxx xxxxxxxx x xxxxxxxx xxxxxxx xx xxxxxx xxxxxx, xx xxxx xxxxxx xx xxxxxxxxxxxxxx laboratoře x xxxxxxxxx. Xxxxxxx xxxxxxxx zdravotnického prostředku xxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxxxx xxxx xx xxxxxx registraci, ale xxxxxx xxxxxx xxxxx xxxxxx xxxxxxxx v xxxxx xxxxxxxxx hodnocení x xxx x xxxxxxx léčby xxxxx xxxxxxxxxxxxxxx xxxxxxx xxxxxxxxxx).
X xxxxxxxx 2 xx xxxxxxxx xxxxxxxxxx zadavatelé, xxxxxxx xxxx xxxxxxxxxxxx xxxxxxxxxxx služeb xxxxxxx xxxx xxxxxxxx xxxxxx xxxx územním samosprávným xxxxxx, xxxxxxx vysoká xxxxx xxxx xxxxxxx xxxxxxxx xxxxxxxxx, xxxx xx xxxxxxx xxxxxxx xxx xx, aby xxxxxxx xxxx xxxx x některých xxxxxxx xxxxxxxxx xxxx xxxxxx xxxxxxxxx, jak x xxxx xxxxxxx xxxxx xxxxxx xxxxxxxxx xxxxxxxx.
X xxxxxxxxxx 3 až 5 se xxx x souladu x xxxxxxxx právními xxxxxxxx xxxxxxx, xxx zadavatel xxxxxxxxx spolu x xxxxxxxxxxx xxxxxxx o xxxxxxxx klinického xxxxxxxxx xxxxxxxx xxxxxxxx či xxxxxxxx příslušných státních xxxxxx. Xxx x xxxxxxxxxxxx xxxxxxxxxx čl. 92 xxxxxxxx x. 536/2014, xxxxx něhož tímto xxxxxxxxx xxxx xxxxxxx xxxxxxxx členských xxxxx xxxxxxxxxx xxxx xxxxxxxxx xxxxxxxx a xxxxxxxxxxx xxxxxxxxxxxxx x xxxxxxxxxxx xxxxxxxxx xxxx. X xxxxxxx xx xxxxxxxx xxxxx xxxx nařízením, xxx xxxxxx nedodržení xx strany xxxxxxxxx xxxxx xxxx k xxxxxxxxxx tichému xxxxxxxx x klinickým hodnocením (xxxxxxxxx xxx možnosti xxxxxxxxx podmínek xxxxxxxxxx xxxxxxxxx) xxxx x xxxxxx časových xxxxxxx xxxxx zajištění vyjádření xxxxxxxxxxx xxxxxx xx xxxxxx Xxxxxxxx xxxxxx xxx xxxxxxxx léčiv, xxx xx v xxxxxxxx xxxxxxxx xxxxx x xxxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxxx xxxxxxxxx xx území České xxxxxxxxx.
X xxxxxxxx 6 xx x xxxxxxx x požadavky xxxxxxxx č. 536/2014, xxxxxxxxx (11) xxxxxxx xxxxxxx xxxxxxxxx xxxxxxxxxxxxx xxxxxxxxxxx xxxxxxxxxx xxxxxxxxx u nízkointervenčních x xxxxxxxxxxx xxxxxxxxxx xxxxxxxxx prováděných nekomerčními xxxxxxxxxx, aniž by xxxx xxxxxxxx xxxxxxxxxx xxxxxxxxxxxx subjektů xxxxxxxxx x xxxxxxxx xxxxxxxxx xxx.
X §57 (Xxxxxxxx XXX, čl. 42 xxxxxxxx x. 536/2014):
Xxxx xxxxxxxxxx x xxxxxxx x čl. 42 xxxx. 3 xxxxxxxx x. 536/2014 xxxxxxxx, aby Xxxxxx xxxxx xxx xxxxxxxx xxxxx xxx xxxxxxx xxxxxxxx xxxxxxxxxxx x xxxxx xxxxxxxx xxxxxxx se zadavatelem xxxxxx, xxxxx xxx xxxx xxxxxxxxx xxxxxxxxx xx xxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxx hlásit xxxxx agentuře xxxxx Xxxxxx. V xxxxxxx xxxxxxxx xxxxxx dohody xxx xxxxxx podezření xx xxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxx xxxxxxxx xxxxx zadavatele Ústav. Xxxxxxxx č. 536/2014 xxxxx xxxxxxxxx xxxx xxxxxxxxx xxxxxxxxx státu.
K §58 (Xxxxxxxx XXX, čl. 76 xxxxxxxx x. 536/2014):
Xxxx xxxxxxxxxx xx xxxxxxxxxxxx článku 76 xxxx. 1 xxxxxxxx x. 536/2014, stanovující xxxxxxxx xxxxxx xxxxxxxxx xxxxxxxx, xxx byly zavedeny xxxxxxx náhrady jakékoli xxxxx (újmy xxxxxxxxx x nemajetkové), xxxxxx xxxxxxx xxxxxxxxx xxxxx x souvislosti x xxxxxx v xxxxxxxxx xxxxxxxxx xxxxxxxxxx xx xxxxxx území, x xx x xxxxxx xxxxxxxxx, xxxxxx xxxx xxxxxxx xxxxxx, xxxxx xx xxxxxxxxxx, pokud xxx o účel, x xxxxxxxxx xxxxxx x xxxx rizika.
V xxxxx xxxxxxxxxx se xxxxxxxx stanoví, že xxxxxxx-xx subjektu klinického xxxxxxxxx x důsledku xxxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxxxxx xx xxxxxxxxx xxxx, x to xxxxxxx na xxxxxx xxxx xx xxxxxx, xx zadavatel xxxxxxx xx xxxxxxxx x xxxxxxx x xxxxxx xxxxxxxx předpisy, xxxxxxx xx xxxxxxxx xxxxxxxxx xx příslušná ustanovení xxxxxxxxxx xxxxxxxx.
Xxxxxxxx xxxx xxxx xxxxxxxx státům xxxxxxx xxxxxxxx nižší xxxxxxxx pro xxxxxxxxxx xxxxxxxxxx. X xxxxxxxxx č. 81 xxxxxxxx x. 536/2014 xx hovoří x xxxxxxxx xxxxxxx xxxxxxxxxxxx xxxxxxxxxx xxx, xx členské xxxxx x xxxxxx xxxxx xxxxxxx xxxxxxxxx xxxxxxxx. Xxxxxxx xxxxxxxxx pro xxxxxxx xxxxxxx xxxxxxxxxxxx xxxxxxxxxx xx xxxx xxxxxxxxxx xxxxxxxxxx xxxxxxx x xxxxxxxx 3, xxxxx využívá xxx xxxxxxx stanovených xxxxxxxx xxxxxxxxx stávajícího pojištění xxxxxx činnosti. Xxx xx zároveň xxxxxxxxx xxxxxxxxxxx pro xx, xxx komerční subjekty xxxxxxxxxxx klinické xxxxxx xxxxxx xxxxxxxxxxxxxx x xxxx xxxxx postavení xxxx xxxxxxxx xxxxxxxxxx.
X §59 (Xxxxxxxx X, xx. 2 xxxxxxxx (20); Xxxxxxxx XX, xx. 74 nařízení x. 536/2014):
Xxxxxxxxxx se xxxxxxx xxxx je xxxx v xxxxxx č. 268/2014 Sb., o xxxxxxxxxxxxxx xxxxxxxxxxxx x x xxxxx xxxxxx č. 634/2004 Sb., x xxxxxxxxx poplatcích, xx xxxxx pozdějších předpisů, xxxxxxx xxxx xxxx xxxxxxxxx, xxxxx označí xxxxxxxxx xx xxxxxxxxx xxxxxxxx žádosti xxxx xxxxx xxxxxxxxx xxxxxxxx xxxxxxxxxx, či xxxxxxxxx xxxxx. Jedná se x xxxxxxxxxx speciální x xxxxxxxxxx §30 xxxx. 5 xxxxxxxxx xxxx, xxxxx xxxxxxxx xxxxxxxxx xxxxxxxxx subjektu xxxxxxxxxxx na xxxx xxxx. Xxxxxxxxxx úprava xx více xxxxxxxxxx xxxxxxxxxx pojetí xxxxxxxx, xxx je vyjádřeno xxxxxxxxx zákoníkem.
Vůle xxxxxxxx, xxxxx mezi xxxxx xxxxxxx xxxxxxx xxxxx, xx xxxxx xxxxxxx xxxx xxxxxxxxx činit xxxxx xxxx Xxxxxxxx xxxxxx xxx kontrolu xxxxx, bude vyjádřena x xxxxxxxxx xxxxxxxxx xxxxxxxxx, xxxxxx xxxxxx xxxx možno xxxxx x xxxxxxxx klinického xxxxxxxxx, a xx xxxxx xxxxxxxxxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxxxx. Žádost xxxx xxxxxxxx xxxxxxxxx xxxxxxxxxxx, xxxx xxxxxxxxx xxxxxxxx xxxxxxxxxx. Xxxxxxxxxx, xx xxxxxxxx xx xxxxxx xxxxxxxxxx portálu xxxxx přidělovat xxxxxxx xxxxxx Xxxxxxxx xxxx, x xx až xx řádné xxxxxxxxxxxx xxxxxxxx xxxx xxxxx xxxxxx vysoce důvěryhodným x xxxxxxxxx, že xxxxxxx xxxxxxxx xxxxxxxxxxxx xxxxxxxxx xxxx minimální.
Lhůty, x xxxxx musí xxxxxxxxxx posouzení xxxxxxx, xxxx xxxxxxxxx nařízením x xxxx xxxxxx xxxxxx x možnost xxxxxxxxx xxxxxx xxx xxxxxxxx xx dána xxxxx 1x xxx xxxxxxxx dokumentace x xx na 5 xxxxxxxxxxxx xxx (x 1x pro xxxxxxxx xx základě xxxxxxxxx xxxxxxxxxx, x xx xxxxx xx xxxx 12 xxxxxxxxxxxx dnů). Xxxxxxxxxx xxxxxx xxxxxx xx xxxxx x xxxxxxx xx xxxxxxxxx xxxxxx xxxxxxx xxxxxxxxx xxxxxxxx, xxx plná xxx jako xxxxxxx xx důkazem x xxxxxxxxx smluvního zastoupení. Xxxxxxxx k tomu, xx komunikace xxxx xxxxxxxxxxxx subjekty a xxxxxxxxxx se bude xxxxxxxxxx xxxxx xxxxxxxxxxxxxxx xxxxxxxxxxxxx portálu, xxxx xx xxxxxxxx xxxxxx xxxxxxxxx xxxxxxxx xxxx xxxxxxxxxx x xxx xxxxxxxxxx xxxxxxxxxx.
X §60 xxxx. 3 písm. x), xxxxx xx xxxxxxxx.
Xxxx 1. xxxxx 2013 xxxxx xxxxxxxxx xxxxx č. 359/2012 Sb., xxxxxx xx xxxx xxxxx xx xxxxxxx zvířat xxxxx xxxxxx. Podle xxxxxxxxxxx xxxxx §15 xxxx. 3 xxxx. x) xxxxxx xx xxxxxxx zvířat proti xxxxxx se ustanovení xxxxxx xxxxxx, která xxxxxxxx xxxxxxx xxxxxxxxx xxxxxx, xxxxxxxxxx na xxxxxxx, xxx xxxx xxxxxxx xxxxxxx xxxxxxx xxx veterinární xxxxxxxx xxxxxxxxx xxxxxxxxxx při xxxxxxxxxx xxxxxxxxxxxxx léčivého xxxxxxxxx. Od 1. xxxxx 2013 xxxx xxxxx xxxxxxxxx xx xxxxxxxxxxx xxxxxxxx xxxxxx xxxxxx xxxxxxxxxx x xxxxxxxxx (souhlasu) xxxx xxxxxxxxxxx projektu xxxxxx xx xxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxx při xxxxxxxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx.
X §62 xxxx. 1, §64 xxxx. b) x x) x §66 xxxx. 4:
Xxxxx xxxxxxxxxxx xxxxxxxxxx xxxxxxxxxxxx xxxxxx xxxxxxxx přípravků, xxxxx xxxxxxxxx i právní xxxxxx xxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx, xx xxxxx do souladu x xxxxxxxxx. Xxxxxxxx xxxxxxxx xxxxxx xxxxxx xxxx oblasti x xx. 61.
X §70 xxxx. 1:
X textu xxxxxxxx 1 je xxxxxxxx „xxxxx xxxxxxxxxx xxxxxxxx Evropské xxxx“, x xx xxxxx, xx bylo vydáno xxx xxxxxxxx xxxxxxxx Xxxxxx v xxxxxxxxx xxxxxxxxx (XX) č. 1252/2014 xx xxx 28. xxxxxx 2014 xxxxxxxxxx xxxxxxxx Evropského xxxxxxxxxx x Xxxx 2001/83/XX, xxxxx xxx x xxxxxx x xxxxxx xxxxxxx výrobní xxxxx xxx účinné látky xxx xxxxxxx xxxxxx xxxxxxxxx, xxxxx upravuje xxxxxxxx xxxxxxx praxi xxx xxxxxx látky. Xxxx xxxxxxxx je xxxx xxxxx použitelné, xxxxxxx xx xxxxxx, xxx bylo navázáno xx vnitrostátní xxxxxx xxx, zejména x xxxxxxx xx nezbytnost xxxxxxxxx sankcí za xxxx xxxxxxxx.
X §70 xxxx. 7:
Xxxxx xxxx xxxxxx x xxxxxxxxxxx xxxxxxxx 7 xx, xxx x léčivých xxxxx pocházejících ze xxxxxxx zemí, xxxxx xx xxxxxxxxx xxx xxxxxxxx léčivých přípravků, xxx xxxxxx jejich xxxxx, x aby xxxx vyrobeny x xxxxxxx xx xxxxxxxx xxxxxxx xxxxx xxx xxxxxx látky odpovídající xxxxxxx xxxxxxxxxx xxxxxxxxxx Xxxxxx.
X §77 xxxx. 1 xxxx. x):
Xxxxx xxxxxxxxx xxxxxx xxxxxx xx xxxxxx a xxxxxx xxxxxxxxxxx xxxxx x xxxxxxxxxxxxxxx léčivých xxxxxxxxxxx xxxxxxxxxxx xxxxxx xxxxxx Xxxxxxxx ústavu xxx kontrolu xxxxx. X xxxxxxxx xxxxxxxxx xxxxxx xxxxxxx a xxxxxxxxx vymahatelnosti xxxxxxx xxx xxxxxxxx xxxx xxxxxxx xxxxxxxxxx je xxxxxxxxx, aby xxx xxxxxx xxxxx, xxxxxx xxxxxxxx a způsob xxxxxx xxxxxxxxxxx xxxxxx xxxxxxx xxxxxxxx xxxxxxxxxx xxxxxxx xxxxxxxxx.
X §77 xxxx. 1 xxxx. x):
Xxxx xx xxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxxxxxx xxxxxxxxxx x xxxxxxx x xxxxxxxxx xxxxxx xxxxxx vydaným podle §77x. Xxxx xx x xxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx povinnost xxxxxxxxxxxx při splnění xxxxxxxxxxx podmínek xxxxxxxx xxxxxxxxxxxxx xxxxxxxxxxx xxxxxxx xxxxxxxxxxxxxx xxxxxxxx xxxxxxxxx xx 48 xxxxx xx xxxxxxxx xxxx xxxxxxxxx.
X §77 xxxx. 1 xxxx. q):
Stanoví xx xxxx xxxxxxxxxx xxxxxxxxx xxxxxxxxxxxx v xxxxxxxxx, xxx xxxxx xxxxxxxxxxxx xxxx xxxxx Xxxxx xxxxxxxxx léčivý xxxxxxxxx, xxxxx xx xxxxxx xx xxxxxxx xxx §77x.&xxxx; Po xxxxxxxx xxxxxxxxx xxxxxxxxxx xxxx xxx Ministerstvem xxxxxxxxxxxxx vydáno opatření xxxxxx xxxxxx, xxxxxx xxxx včas xxxxxx xxxxxxxx tak, že xxxxxxx x xxxxxx xxxxxxxxxxxxx léčivého xxxxxxxxx.
Xxx xxxxxxxxxxx xxxxxxxxxxxx xxxxxxxxxx xx x xxxxxx xxxxxxxx xxxxxxx, xx xxxxxxxx x distribuci xxxxxxxx přípravku xxxxxxxx xxxxxxxxxxxx distributora, xxxxxxxxxxxx xxxxxxxx přípravku, množství xxxxxxxx xxxxxxxxx v xxxxxxx xxxxxxxxxx, xxxxx xxxxx xxxxxxxxxx a xxxxx plánované xxxxxxxxxx xxxxxxxx přípravku. Rozsah xxxxx xxxxxxxxx v xxxxxxxx x způsob xxxxxx poskytování xxxxxx xxxxxxxx xxxxxx xxxxxxx xxxxxxxxx právní xxxxxxx.
Xxxxxxxxxxxx xxxxxxx je xxxxx x xxxxxxx xx xxxxxx xxxxxx x xxxxxxx získaných xxx, xxxxxxxx xx jejich xxxxxxxxx zpracování x xxx xxxx xxxxxxx xxxxxxxxx x xxxx xxxxxxxx xx možný xxxxxxxxxx daného xxxxxxxx xxxxxxxxx xx xxxx. Xxxxx xx xxxx xx Ústav xxxxxxxxxx x xxxx, resp. x různých xxxxxxxx, xxxxx xx xx Xxxxx xxxxxx xxxxxxxxx xx xxxxxxxx podoby, xxx xx pak xxxx xxxxx zpracovat, xxxxxxxxxx a xxxxxx xxxxx. X xxxxxxx xx xxxxxxx xxxx, xxxxxx xx Xxxxx xx xxxxxxxxxx xxxxxxx x xxxxxx xxxxxxxx xxxxxxxxx x xxxxxxxx xxxxxxx xxxxxxx k xxxxxx xxxxxxxx xxxxxx xxxxxx xx XX, xx xxxx xxxxx, xxx xxxxxxxxxxxx xxxxxx xxxxxxxxxx. Xxxxxx xx xxxxx xxxx v xxxxx, xx xxxxxxx xxxx povinně xxxxxxxx xxxxxxxx x xxxxxxxxxx x xxxxxxxxx, xxxxxxxxxxxx xxxxxx xxxxxxxxx počítače, XX a xxxxxxxxxxxxx xxxxx dat, která xxx xxxx jediná xxx xxxxxx xxxxxx xxxxxxxxx možnost xxxxxxxxxx x uchovávání záznamů x dokumentace pro xxxxxx x xxxxx xxxxxx povinností xxx xxxxxxxxx xxxxxx xxxxxxxxxxxx xxxxxx x xxxxxxxx.
X §77x:
Xxxxx xxxxxx xxxxxxxxxx Xxxxx xxxxxxxx analyzuje xxxxxxx xx xxxx x xxxxxxxx xxxxxxxxx, x xx zejména xx vztahu mezi xxxxxxx xxxxxx xxxxxxx xxxxxxxx přípravků xx xxx x Xxxxx xxxxxxxxx xxxxx §33 xxxx. 2 a xxxxxxx xxxxxxxx přípravků xxxxxxxxxxxx xx xxxxxxxxx xxx xxxxxxxxxxx zdravotních xxxxxx. Xx základě xxxx analýzy pak Xxxxx xxxxxxx Ministerstvu xxxxxxxxxxxxx xxxxxxxxx x xxxxxxx xx xxxx xxxxxxxxxxx x xxxxx xxxxxxxx xxxxxxxxx, při xxxxxxx xxxxxxxxxx xx xxxx x České xxxxxxxxx xx xxxxx xxxxxxxxx xxxxxxxxx xxxxxx xxxxxxxxxxxxx xxx poskytování xxxxxxxxxxx xxxxxx xxxxxxxxx x České xxxxxxxxx.
Xx xxxxxxxxxxx sdělení poskytnutých Xxxxxxxxxxxx xxxxxxxxxxxxx Xxxxxxx Xxxxxxxxxxxx xxxxxxxxxxxxx xxxx xxxxxx xxxxxxxx xxxxxxxxx (xxxxxx xxxxxxxxx xxxx xx seznam zařazovány xxxxxx opatření xxxxxx xxxxxx), při jejichž xxxxxxxxxx xx xxxx x Xxxxx xxxxxxxxx xx mohlo vzniknout xxxxxxxxx jejich xxxxxxxxxxxxx xxx poskytování zdravotních xxxxxx xxxxxxxxx x Xxxxx xxxxxxxxx. Xxxxx xxxxxx Xxxxxxxxxxxx zdravotnictví xxxxxxxx na svých xxxxxxxxxxxxx xxxxxxxxx. Xxxxxx xx průběžně xxxxxxxxxxxx x xxxxxxxxxxx. Xx xxxxxx xxxxxxx je xxxxxxxxx xxxxxx přípravek, xxxxx xxxx xxxxxxxxxxxx xxxxxxx xxxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxx vlastností, kterého xx xxx xxxxxxx xxxxxxxx v Xxxxx xxxxxxxxx dostatek, x xxxxxxx xxxxxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx xx xxxx xxxxxxx dostupnost x xxxxxxxx xxxxx xxxxxxxx x Xxxxx xxxxxxxxx x přímým xxxxxxx na ochranu xxxxxx xxxxxxxxxxxx a xxxxxxxxx xxxxxxxxxx poskytování xxxxxxxxxxx služeb.
Na seznam xx x xxxxxxx xx podmínku, že xxxxxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx xx xxxx xxxxxxx dostupnost a xxxxxxxx léčby xxxxxxxx x Xxxxx xxxxxxxxx x přímým xxxxxxx xx xxxxxxx zdraví xxxxxxxxxxxx, xxxxx být xxxxxxxxxx xxxxxxx xxxxxx xxxxxxxxx, xxx ohledu xx jejich terapeutické xxxxxxxx. Xxxxx xxxxx xx ochranu xxxxxx xxxxxxxxxxxx xxxx xxx x nedostatek léčivého xxxxxxxxx xxxxxxxx x xxxxx xxxx než xxxxx xxxxxxxxxx xxxxxxxxxxxx xxxxxxxx. Xxxxxxxxx xx, xxx xxxxxx přípravek xxxxx x xxxx xxxx xxxxxxxxxxxx xxxxxxx xxxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxx xxxxxxxxxx, kterého je xxx xxxxxxx pacientů x Xxxxx republice xxxxxxxx.
Xxxxxxxx xxx xxxxxxxxx xxxxxxxxxx xxx nalézt x xxxxxxx „xxxxxxxx xxxxxx“ x „xxxxxxxx xxxxxxx xxxxxxxxxx xxxxxx xxxxxxxx“ xxxxxxx x xxxxxxxxxx §77x odst. 2. Xxxxxxxx v xxxxxxx xxxxxx xxxxxxx x xxxxxxxx datu, xxxxxxx x xxxxxxx xx xxxxxxxxx účelu x xxxxxxxxxx x xxxxxxxx xxxxxxxxxx xxxxx xx zřejmé, že xxx xx x xxxxxxx xxxxxx xxxxxxx x datu, xx xxxxxxx je hrozba xxxxxxxxxxxxx analyzována. Xxxxxxxx xxxxxxx xxxxxxxxxx xxxxxx xxxxxxxx xxxxxx xxxxxxxxxxx xxxxxxx, že xxxxxxxxxx xxxx snižována. Pro xxxxxxxxx xxxxx x xxxxxx xxxxxxxxxxx xxxxxxxx xx xxxxxx xxxxxxx, xx xxxxxxx xxxxxxxxx xxxx xxxxx xxx xxxxxxx xx chvíli, xxx ještě xxxx xxxxxx xxxxxx xxxxxxxxx xx xxxx xxx, xxx xx xxxx xxxxx xxxxxx x xxxxxxxxx ČR.
Léčivé přípravky xxxxx xx xxxxxxx, xxxxx xx bude xxxxxxxx xxxxxxxxxxxx. Xxxxx xxxxxxx xxxxxx xxx xxxx xxxxxxxx na xxxxxx, xxxx seznam xxxxxxxxxxxx a xxxx xxxxxxxxx x něj xxxx vyřazen. Xxx xxxxxxxx xxxxx xxxx xxxxxx přípravek xxxxxxxx xxxxxxxx, může xxx xx seznamu xxxxxxxxxx, x xx xxxxx, xx xxxxxxx pacientů x XX je xxxxxx xxxxxxxxxx či xxxxx xxxxxx, a xxxxx je nutné xxxx dostupnost xxxxx xxxxxxxx xxxxxxxx. Při xxxxxxxxxxx xxxxxxx bude xxxx xxxxx xxxxxxxx, xx xxxxxxxx xxx xx, aby léčivý xxxxxxxxx xxxx xx xxxxxxx xxxxxx, xxxx xxxxx xxxxxxxx. Xxxxxxxxx xx tedy, xx xxxxxxxx uvedení léčivého xxxxxxxxx na xxxxxxx xxxx automaticky znamenat xx, že xxxx xxxxxx xx xxxxxxx xxxxx.
Xxxxxxxxxx xxxx možné xxxxxx kvantifikovat pro xxxxxxx xxxxxx xxxxxxxxx, xx nezbytné jej xxxxxxxx xxxx xx xxx xx xxxxxx xx xxxxxxxxxxx xxxxxxxx xxxxxxxxx x konkrétní xxxxxxx.
X §77x:
Xxxxxx xxxxx xxx xxxxxxxx léčiv xx xxxxxxx zákona x xxxxxxxx shromažďuje xx xxxxxxxx xxxxxxxxxx x xxxxxxxxxx, xxxxxxxxxxxx x xxxxxxx údaje x xxxxxxxxx, resp. xxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx, x nichž xxx získat xxxxxxxxx x xxxxxxxxxxx léčivých xxxxxxxxx xx xxxx x České republice. Xxxx xxxxx, xxxxx xx xxxxx o xxxxxx přípravky xx xxxxxxx, pravidelně xxxxxxxxxxx xxx, xxx xxxx x případě xxxxxxxx xxxxxxxxxxxx x xxxxxx xxxxxxxxxxxx xxxxxx xxxxxxxxx xx xxxxxxxxx podat xxxxx xxxxxx xxxxxxxxxx Xxxxxxxxxxxx xxxxxxxxxxxxx odůvodněný xxxxxx k vydání xxxxxxxx podle ustanovení §77x. Xxxxxx xxxx x návaznosti na xxxxxxxx xxx vydání xxxxxxxx xxxxxx xxxxxx Xxxxxxxxxxxxx zdravotnictví dle §77x obsahovat xxxxx xxxxxxxxxxx xxxxxxxxxxxxx údajů x xxxxxxxxxx xxxxxxxxx xxxxx.
Xxxxxxxxxxxx zdravotnictví xx xxxxxxx §11 písm. x) xxxx xxxxxxxx x xxxxxxxxx dostupnosti xxxxxxxxx xxxxxxxx xxxxxxxxx x xxxxxxx, xx x) xx xxxxx x léčivý xxxxxxxxx xxxxxxxx xx seznam xxxxxx xxxxx §77c, xxxxxxxxxx xx došlo x xxxx, xx xxxxxxxx xxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx již xxxxxxxxx potřebu xxxxxxxx x Xxxxx xxxxxxxxx, xxx xx xxxxxx xxxxxxx x xxxxx xxxxxxxxxxxxx xxxxxxx od xxxxxxxx rozhodnutí x xxxxxxxxxx, xxxxxxxxxxxx a xxxxxxx v souladu x xxxxx xxxxxxx x xxxxxx xxxxxxxxxxx, x x) xxxxxxx xxxxx na xxxxxxx&xxxx; xxxxxx xxxxxxxxxxxx x xx xxxxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx xxx xxxxxxx xxxxxxxx x Xxxxx xxxxxxxxx xxxxxxxxx xxx xxxxxxxxxxxxx xxxxxx xx xxxxxxxxxxx xxxxxx xxxxxxxxxx xx zahraničí. Xxxx xxxxxxxx xxxx xxx xxxxxxx xxxxxxxxxxx, xx. všechny xxxxxxx.
Xxxxxxxx xxxxxxxxx pro xxxxxx xxxxxxxx xxxxxx povahy xxx xxxxxx xxxxxxxxxx xx uvedení xxxxxxxx xxxxxxxxx xx xxxxxxx xxx §77c xxxxxx x léčivech.
Pokud se xxxxx x xxxxxxxx xxxxxxxxxxxxx, xxxx je xxxxxxxxx xx xxxxxxxxxxxxxxx. Xxxxxxxx se xx xxxxxxx xxx, xx xxxxxxxx xxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx xxx xxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxx pacientů x Xxxxx republice. Xxxxxxxx xxxxxxx xxxxxxxx x Xxxxx xxxxxxxxx je xxxxx xxxxxxxxxxxxx vymezit, xxx xx xxxxxxx xxx xx, aby xxxx xxxxxxx xxxx x xxxxxx xxxxxxxxxx xxxxxxx xxxxx xxxxxxxxxx. X xxxxxxx xxxxxxxx xxxxxxxxx musí xxx xxxxxxxxx x ohledem xx xxxxxxxxx xxxxxxx xx xxxxxxx, xxxxxxxxx xxxxxxx xxxxxxxx a xxxx zásob u xxxxxxxxxxxx, xxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxx distributory xx xxxxxxx x xxxxx balení xxxxxxxx xxxxxxx oprávněnými x xxxxxx, včetně xxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxxxxxxx xxxx území České xxxxxxxxx v xxxxxxxxxx xxxxxx.
Xxxxx xxxx. x) xxxx xxx xxxxxxx xxx podmínka veřejného xxxxx na ochraně xxxxxx xxxxxxxxxxxx x xx xxxxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx xxx xxxxxxxx xxxxxxx xxxxxxxx x České republice. X xxxxxxxxxx případě xxxx xxx xxxxx xxxxxxxxxx, xx xxxxx xxxxxxxxxx xxxxxxx xxxxx xxxxxxxxx nad individuálním xxxxxx xx xxxxxxxxxxx xxxxxxxxxx xx xxxxxxxxx.
Xx xx xxxx xxxxx xxxxxxxx obecné xxxxxx, xxxxxx xxxxxx xxxxxxxx xxxxxx xxxxxx xx xxxxxxxx v ustanoveních §171 x násl. xxxxxx x. 500/2004 Xx., správní xxx (xxxx jen „xxxxxxx xxx“). Xxxxx opatření x xxxxxxx opatření xx xxxxxxxx oznamovat xxxxx způsobem umožňujícím xxxxxxx xxxxxxx. Xxxxx xxxxxx úpravy xxxxxxxx x xxxxxxxxxx §25 xxxxxxxxx xxxx platí, xx patnáctým xxxx xx xxxxxxxx xx xxxxxxxxx xxxxxxxx xx xxxxxxxxx. Xxxx lhůta xxx xxxxxx xxxxxxxx xx navrhuje upravit xxxxxxxxx x xxxxx 5 xxx xxx, xxx mohly xxx xxxxxxxxxx xxxxxxxx k xxx xxxxxxxxxx návrhu.
Platí xxxxxx xxxxxx, xx xxxxxxx xxxxx xxxxx xxxxxxx xxxxx, aby x xxxxxx xxxxxxxx xxxxxxxx xxxxxxxxxx. Xxxxxxxxx xx xxxxxx xxxx xxxxxxx xxxxx 5 xxx xxx uplatnění xxxxxxxxxx x návrhu xxxxxxxx xxxxxx xxxxxx xxx dne jeho xxxxxxxxxx xxx, xxx xxxxxxxxxxx v případě xxxxxxxxxx xxxxx xxxxx xx xxxxxx xxxx xxxxxx k jejímu xxxxxxxx na xxxxxxxxxxx xxxxxxxx den.
Návrh xxxxxxxx xx xxxxxxx xxxxxxxxxxxx x lze k xxxx uplatnit xxxxx xxxxxxx xxxxxxxxxx. Xxxx xxxxx obecná xxxxxx, xx xxxxxxx, jehož xxxxx, xxxxxxxxxx xxxx xxxxx xxxxx xxx xxxxxxxxx obecné xxxxxx xxxxx dotčeny, xxxx x návrhu xxxxxxxx x správního xxxxxx (x Xxxxxxxxxxxx xxxxxxxxxxxxx) xxx xxxxxxx xxxxxxxxxx. Xxxxxxxxxxxx xxxx xxxx xxxxxxx xx xxxxxxxxxxxx xxxxxxx jako podkladem xxx xxxxxxxx xxxxxx xxxxxx x vypořádat xx x nimi x jeho odůvodnění. Xxxxxxxxxx §175 xxxx. 2 xxxxxxxxx řádu xxxxxxxxxx xxxxxxx určení xxxxxxxxx osob, které xx mohly podávat xxxxxxxxxx námitky, se xxxxxxxxx. Xxxxxxxx xxxxxx xxxxxxxxx xxxx x xxx xxxxxxxxxx.
Xx xx xxxx přezkumu opatření xxxxxx xxxxxx, platí xxxxxx xxxxxx dle xxxxxxxxxx §173 xxxx. 2 správního xxxx, xxxxx xxxxxxx v xxx, xx proti xxxx není možné xxxxx xxxxxxx xxxxxxxxxx. Xxx xxxxxxxxxx §174 xxxx. 2 xxxxxxxxx xxxx xxxxxx xxxxxxxx xxxxxx xxxxxx x xxxxxxxx xxxxxxxx xxx xxxxxxxx x xxxxxxxxxx xxxxxx. Proti xxxxxxxx xxxxxx povahy xxxxxxxx xxxxxxxx postup xxxxxxxx xxxxxx xxxxx ve xxxxxxxx xxxxxxxxxx, a xx x xxxxxx x xxxxxxx opatření xxxxxx xxxxxx xxx xxxxxxxxxx §101a x xxxx. xxxxxx x. 150/2002 Xx., soudního xxxx správního. Návrh xx zrušení xxxxxxxx xxxxxx xxxxxx xxx xxxxx xx 3 xxx xx xxxxxx xxxx účinnosti a xxxx xxx xxxxx xxxxx, kdo xxxxx, xx jím xxx xxxxxxx na svých xxxxxxx.
Xxxxx xx xxxxx x xxxxxxx xxxxxxxx xxxxxxxx, xxx jej xxxxxxx xxxxxxx způsobem, xxxxx xxxx xxxxxxxx xxxxxxxxxx. Za xxxxx xxxxxx x x xxxxxx xxxxxxxxx xxxxxxxxxxxxxxxx xxxxxx procesu xx xxxxx xxxxxxxxxx vyhodnocovat xxxxxx přetrvávání opatření xxxxxx povahy.
Za xxxxxx xxxxxxxxx xxxxxxxx efektivního xxxxxxxxx v případě, xx se Xxxxxxxxxxxx xxxxxxxxxxxxx v xxxxx xxx činnosti dozví x xxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx, požádá Xxxxxx xxxxx xxx xxxxxxxx xxxxx x xxxxxxxxxx xxxxx v xxxxxxx xxxxx §77x.
X §80 xxxx. 1:
Xxxxxxxx xx úprava ohledně xxxxxxxxxxxxxxx xxxxxxxxxxxxxxx znaků x elektronických receptů.
K §82 xxxx. 3 xxxx. x):
Xxxxx xxxxxxxxx xxxxxx xxxxxx xx xxxxxx a xxxxxx xxxxxxxxxxx xxxxx o xxxxxxxx xxxxxxxx přípravcích xxxxxxxxxxx formou xxxxxx Xxxxxxxx xxxxxx xxx xxxxxxxx xxxxx. Z xxxxxxxx xxxxxxxxx xxxxxx xxxxxxx a účinnější xxxxxxxxxxxxxx nápravy xxx xxxxxxxx xxxx xxxxxxx xxxxxxxxxx xx xxxxxxxxx, xxx xxx xxxxxx xxxxx, xxxxxx xxxxxxxx x xxxxxx jejich xxxxxxxxxxx xxxxxx xxxxxxx xxxxxxxx xxxxxxxxxx xxxxxxx xxxxxxxxx.
Xxxxxxxxxxxx xxxxxxx xx xxxxx x xxxxxxx xx veliké xxxxxx x hlášení získaných xxx, xxxxxxxx xx xxxxxx xxxxxxxxx zpracování x xxx dává xxxxxxx xxxxxxxxx x xxxx reagovat na xxxxx nedostatek xxxxxx xxxxxxxx xxxxxxxxx xx xxxx. Xxxxx by xxxx na Ústav xxxxxxxxxx x xxxx, xxxx. x různých xxxxxxxx, xxxxx by xx Xxxxx xxxxxx xxxxxxxxx xx xxxxxxxx xxxxxx, aby xx xxx xxxx xxxxx xxxxxxxxx, xxxxxxxxxx x xxxxxx xxxxx. X xxxxxxx xx krátkou xxxx, xxxxxx má Xxxxx xx xxxxxxxxxx xxxxxxx x vývozu xxxxxxxx xxxxxxxxx x xxxxxxxx předání xxxxxxx x vydání xxxxxxxx xxxxxx xxxxxx xx XX, xx xxxx xxxxx, než elektronická xxxxxx použitelná. Rovněž xx nutné xxxx x xxxxx, xx xxxxxxx jsou xxxxxxx xxxxxxxx xxxxxxxx x xxxxxxxxxx x xxxxxxxxx, xxxxxxxxxxxx xxxxxx xxxxxxxxx xxxxxxxx, SW x xxxxxxxxxxxxx xxxxx dat, xxxxx jim xxxx xxxxxx xxx xxxxxx xxxxxx xxxxxxxxx xxxxxxx xxxxxxxxxx a uchovávání xxxxxxx a dokumentace xxx xxxxxx x xxxxx xxxxxx xxxxxxxxxx xxx xxxxxxxxx jinými xxxxxxxxxxxx xxxxxx o xxxxxxxx.
K bodům 37 x 38
X §82 xxxx. 4:
Xxxxxxxxxx xxxxxxx xx xxxxxxxxx xxxxx.
X §101 xxxx. 1:
Xxxxxx xxxxx xxx xxxxxxxx léčiv je xxxxxxxx xxxx xxxxxxxxx xxxxx xxxxx řadou xxxxxxxx předpisů, xxxxx xxxxxxx xxx xxxxx xxxxxxx. Kontrolu Xxxxxx xxxxx pro kontrolu xxxxx xxxxxxxx xxxxx xxxxxx xxxxxxxx xxxxxxxx:
xxxxx č. 378/2007 Sb., o xxxxxxxx - xxxxxx XX,
xxxxx č. 296/2008 Sb., x xxxxxxxx xxxxxxx x buňkách - rezort MZ,
zákon č. 167/1998 Sb., x xxxxxxxxxx xxxxxxx&xxxx; - rezort XX,
xxxxx č. 123/2000 Sb., o xxxxxxxxxxxxxx prostředcích - xxxxxx XX (xx 1. dubna 2015 xxxxx č. 268/2014 Sb.),
xxxxx č. 372/2011 Sb., x zdravotních službách - rezort MZ,
zákon č. 40/1995 Sb., x regulaci xxxxxxx - xxxxxx XXX,
xxxxx č. 102/2001 Sb., x xxxxxx bezpečnosti xxxxxxx - rezort XXX,
xxxxx č. 634/1992 Sb., x xxxxxxx xxxxxxxxxxxx - xxxxxx XXX,
xxxxx č. 265/1991 Sb., o xxxxxxxxxx xxxxxx České xxxxxxxxx v xxxxxxx xxx x xxxxx č. 526/1990 Sb., o xxxxxx - xxxxxx XX,
xxxxx č. 477/2001 Sb., x xxxxxxx - xxxxxx XXX,
xxxxx č. 78/2004 Sb., o xxxxxxxxx x xxxxxxxxx modifikovanými xxxxxxxxx x xxxxxxxxxxx xxxxxxxx - xxxxxx XXX,
xxxxx č. 272/2013 Sb., x xxxxxxxxxxxx drog - xxxxxx XX.
Xxxxx v xxxxxxxxx z xxxxxx xxxxxx xx xxxxxxxx, xx xx inspektoři xxxxxxxxx při výkonu xxxxxxxx průkazem. X xxxxxxx podle právních xxxxxxxx, x xxxxx xxxxxxxxxx x xxxxxxx xxxxxxxxxx xxxxx, se xxxx xx 1.1.2014 xxxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxx xx xxx. Při xxxxxxxxx xxxxxxxxxx xx xxxxxxxxxx xxxxxxxx xx kontrolu xxxxxxxxxx xxxxxxxxxx uložených xxxxx xxxxxxx xxxxxx xxxx. xx xxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxx x xxxxxxxx a xxxxxxx x xxxxxxxx xxxxxxx. V xxxxxxx xxxxxxx xx xxxx xxxxxxxxxx xxxxxxxxxx jak xxxxxxxxxx xxxxxxxx (podle xxxxxx o xxxxxxxx), xxx x xxxxxxxxx (xxxxx zákona x xxxxxxxx xxxxxxx).
X xxxxxxx xx xxxxxxxxxx xxxxxxxxxxx xxxxxxxxxx Xxxxxxxx xxxxxx xxx xxxxxxxx xxxxx x x xxxxxxxxx xxxxxx xxxxxxx kontrolovaných xxxx se xxxxxxxx xxxxx xxxxxxxxxx xxx, xxx xxxxxxxx xx xxxxxxxx xxxx xxxxxxxx xxxxx xxxxxxx inspektora x aby xx xxxxxxxxxx Xxxxxxxx xxxxxx xxx kontrolu xxxxx xxx všech xxxxxxxxxx xxxxxxxxxxxx xxxxx xxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxx xxxxx xxxxxxxx, x xxx je xxxxxx xxxxxxxxxx, x xx xxxxx x xxxxxxx x xxxxxxxxxx xxxxx. Xxxxxxx x §22 xxxx. 1 xxxxxx x léčivech xx zavedena xxxxxxxxxxxx xxxxxxx „xxxxxxxxxx“ pro xxxxxxxxxxx Státního ústavu xxx xxxxxxxx xxxxx x Xxxxxx xxx xxxxxx xxxxxxxx veterinárních xxxxxxxxxxxx x xxxxx, xxxxx xxxxxxxxxx xxxxxxxxx xxxxxxx, xxxxxxxxxx xxxxxx xx xx měla xxxxxxxxx x xx xxxxxxxxxx Xxxxxx pro xxxxxx xxxxxxxx veterinárních xxxxxxxxxxxx a xxxxx.
K §101 xxxx. 5 xxxx. x):
Xxxxxxxx právní xxxxxxxxx xxxxxxxxx a xxxxxxx xxxxxxxx přípravků jsou x současném xxxxx xxxxxx x léčivech xxxxxxxx xxxxxxxxxxx, xxxxxxx x x xxxxxxx xxxx xxxxx xxx xxxxxxx klamavého xxxxxxxx xxxxxxxx xxxxxxxxx, x xxxxxxxx xxxxx x xxxxxxxxxx situacích xxxxxxxxx xxxxxxxxx. V praxi xx xxxxxx stále xxxxxxx xxxxxxxxx případy, xxx Státní xxxxx xxx xxxxxxxx xxxxx xxxxxx, že s xxxxxxxx xxxxxxxxx xxxxxxxxx xxxxx, které x xxxx xxxxxx xxxxx xxxxxx xxxxxxxxx. Typicky xx xxxxx o xxxxxxx, kdy jsou xxxxxx přípravky vydávány xx xxxxxxxxx. Léčivé xxxxxxxxx xxxx xxxxxx xxxxxx xxxxxxxxxx xxxxxx x z důvodu xxxxxxx xxxxxxxxx xxxxxx xx xxxxxxxx, aby x nimi xxxx xxxxxxxxx xxx xxxxxxx xxxxxxxx, který xxxxx xxxxxxxx, x xxx xxxxxx xxxxxxxxx xxxxxxxxxxxxx xxxxx xx osoby, xxxxx xxxx x xxxx xxxxxxxxx. Z xxxxxx xxxxxx xx x xxxxxx xxxxxx xxxxxx zpřesňován xxxxxx Xxxxxx xxx xxxxxxxxxxx, xxxxxxxxxx x xxxxxxxxxxxx xxxxxxxx přípravků x xxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxx x léčivy. Xxxx xx xxxxxxxxx právní xxxxxx xxxxxxxxx o xxxxxx xxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx.
X§103 xxxx. 6 xxxx. x):
Xxxxxxxxx x doplnění xxxxxxxxxxx xxxxx xxxxxxxxxx xxx, xxx xxxxxxxxxxx xxxxxxx xxxxxxx subjekty, které xxxxxxxxx x xxxxxxxx xxxxxxxxx.
X §105 xxxx. 2:
Xxxxxxxx xx xxxxxxx x), x) a t), xxxxx zavádějí xxxxxxx xxxxxxx distributorů pro xxxxxx nezajištění xxxxxxx xxxxxxxx přípravku xxxxxxxxxxxxx xxx xxxxxxxxxx §77 xxxx. 1 xxxx. x) (xxxxxxx xxxx xx xxx xxxxxxxxx x xxxxxxxx xxxxxxxxxx x registraci), xxxxxxxxxx xxxxxxxxx xxxxxxxxxx xxx xxxx xxxxxxxxxx xxxxxxxxxx §77 xxxx. 1 xxxx. x) a xxxxxxxx xxxxxxxx xxxxxx xxxxxx vydaného dle xxxxxxxxxx §77x.
X §105 xxxx. 5:
X xxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxxxx xxxxxxx xxxxxxxxx a xxxxxxxxxxxxx hrozby xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx xx xxxx xxx xxxxxxx xxxxxxxx x Xxxxx xxxxxxxxx xx xxxxxx xxxxxxx xxxxxx xxxxxxxx xxxxxxxxxx x xxxxxxxxxx xxxxxxxxxxx x neposkytnutí xxxxx x objemu xxxxxxx xxxxxxxx přípravku xxxxxxxxx xx trh x Xxxxx xxxxxxxxx xxxxx §33 xxxx. 2.
K bodům 46 xx 65
X §105 odst. 6 x 7, §106 xxxx. 3, §107 xxxx. 1 x 2, §108 xxxx. 5, 8 a 11:
X čl. 94 xxxxxxxx xx ukládá xxxxxxxx státům stanovit xxxxxx za xxxxxxxx xxxxxx xxxxxxxx a xxxxxxxx xxxxxxx xxxxxxxx xxxxxxxx k xxxxxx xxxxxxxxxxx, xxxxxxx xxxxxxxxx xxxxxx xxxx xxx xxxxxx, xxxxxxxxx x xxxxxxxxxx. Nově xx xxxxx doplňuje zákon x xxxxxxxx x xxxxxxxx xxxxxxxx xxxxxxxxxxx x xxxxxxxx xxxxxxxxxx xxxxxxxxxxx xxx xxxxxxxxx, xxx novým xxxxxxx xxxxxxx x xxxx xxxxxxx xxxxxxxxx xxxxxx xxxxxx klinických hodnocení xxxxxxxxx x zákoně x xxxxxxxx.
X §107 xxxx. 1:
Pro xxxxxx xxxxxxxxxxx xxxxxxx xxxxxxxx xxxxxxxxx distributorem xxx xxxxxxxxxx §77 xxxx. 1 písm. x) xx xxxxxxx (obdobně, xxxx xx xxx xxxxxxxxx x xxxxxxx xxxxxxxxxxxx xxxxxxx držitelů xxxxxxxxxx o registraci) xxxxxx xx 20 xxx. Kč, pro xxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxxxx xxx xxxx xxxxxxxxxx xxxxxxxxxx §77 xxxx. 1 xxxx. x) xx xxxxxxx xxxxxx xx 5 xxx. Kč a xxx případ xxxxxxxx xxxxxxxx xxxxxx povahy xxxxxxxx xxx ustanovení §77x xx stanoví xxxxxx do 20 xxx. Kč.
Pokud xxx x výši xxxxxx, xx xxxxx xxxxxxxxxxx, xx xxxxxxxx xxxxxxx xxxxxx x léčivech č. 70/2013 Sb., xxxx xxxxxxxxxxx x xxxx, xx xxxxx hranice pokut x xxxxx zákoně xxxx x xxxxxxx xxxxxxx, k xxxxx xxxxx následující xxxxxxxxxxx xxxxxxxx xxxxxxxxx x xxxxxxxx xxxxxx x xxxxxx xxxxxx: „ …xx xxxxxx xxxx xxxxxxxx xxxxxx x xxxxx xxxxxxx xxxxx xx xxxxxxxx správních xxxxxxx v ostatních xxxxxxxxx xxxxxxxxxx xxxxxxx x léčivech. X xxxxxxxxx přistupuje xxxxxxxx x xxxxxxxxx praxe, xxxxx xxxxxxxx x xxx, že xxxxxxxxx xxxx xxxxxx xx xxxxxxxxxxx xxxxxxx xx x mnoha xxxxxxxxx xxx xxxx xxxxxxx. X praxi xx xxxxxxx, xx xxx xxxxxxx farmaceutické xxxxx xxxxxxxxxxxxx xxxxxx xxxxxxx x xxxxxxxxx výše xxxxx xxxxxx xxxxxxxx xxxxxxxx újmu, což xx xxxx xxxxxxxx xxxxxxxxx preventivní x xxxxxxxxxx účel xxxx xxxxxxx xxxxxx. Dosavadní xxxxxxx xxxxx x xxxx xxxxxxx xxxxxx xxxxxxxxxx za xxxxxxxxxx xxxxxx x právními xxxxxxxx x xxxxxxxxx xxxxxxxxx státech Evropské xxxx. Xxxxxxxxx xxxxxx xx možné xxxxxxx xxxxxxxxx jejich odrazující xxxxx xx xxxxxxxxxxxx xxxxxxxx, xxx ve xxxx důsledku xxxx xxxx xx snížení xxxxxxxx porušování xxxxxxxxxxx xxxxxx v xxxx xxxxxxx. X po xxxxxxxxxxx xxxxxxx horní xxxxxxx xxxxx xxxx xxxxx nedosahují xxxx, xxxxx xx stanovena x xxxxxx xxxxxxxx xxxxxxxxxx, xxxx xxxxxxxxx x zákoně č. 634/1992 Sb., x ochraně xxxxxxxxxxxx, xx xxxxx xxxxxxxxxx xxxxxxxx, x němž xx xx xxxxxxx xxxxxxx xxxxxxx xxxxxxxxx xxxxx hranice xxxxx xx xx xxxx 50 000 000 Xx.“.
Xxxx předkládanou xxxxxxx xxxxxx je xxxxx xxxxx trend xxxxxxxxx Xxxxxxxxxxx Xxxxx republiky xxxxxxxxxxx, x x xxxxxx zachovat a xxxxxxxx. Xxxx odpovídají x xxxxxxxxxx horní xxxxxxx xxxxx xx xxxxxxxx nově stanovených xxxxxxxxx deliktů.
Správní delikty xxxxxxxxxxx x xxxxxxxxxxx xxxxxxx xxxxxxxx xxxxxxxxx xxxxx §77 odst. 1 xxxx. h), xxxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx xxxx území Xxxxx xxxxxxxxx xxxxx §77 xxxx. 1 xxxx. q) xxxx x distribuci léčivého xxxxxxxxx mimo xxxxx&xxxx; Xxxxx xxxxxxxxx x xxxxxxx x opatřením xxxxxx xxxxxx Xxxxxxxxxxxx xxxxxxxxxxxxx xxxxxxx podle §77x xx xxxxxxx xxxxxxxx xxxx xxxxxx x souhrn xxxxxxxx xxxxxxxxxxx xxxxxxx zákona xxxxxxxx potřebou náležité xxxxxxx pacientů x Xxxxx xxxxxxxxx, že xx xx xxxxx xxxxxxxxx možnosti, xxx xxxxx xx xxxxxx xxxxxxx xxxxxxx xxxx xxxxx uložit pokutu x nejvyšší možné xxxx podle xxxxxx x xxxxxxxx, kterou xx xxx podle xxxxxxxxx právní xxxxxx xxxxxx 20 000 000 Kč.
Pokud jde x xxxx xxxxxxxxx xxxxxxx xxxxxx xxxxxxxxxxx x xxx, xx xxxxxxx xxxxxxxxxx o xxxxxxxxxx neposkytne údaje x objemu dodávek xxxxxxxx xxxxxxxxx xxxxxxxxx xx trh x Xxxxx xxxxxxxxx xxxxx §33 xxxx. 2, xxx xxxx xxxxxxxxx x xxxxxxx xxxxxxx xxxxxx, jakého xx xxxxx xxxxxxxxx právní xxxxxx xxxx xxxxxxxx xxxxxxxxxxx xxxxx §77 xxxx. 1 xxxx. x) nebo xxxxxxxxxxxx xxxxxxxxx k výdeji xxxxxxxx přípravků xxxxx §82 odst. 3 xxxx. x). Je xxxxx zcela odůvodněné, xxx xxxx horní xxxxx xxxxxxxxx xxxxxxx xxxxxxxx xxxxxxxxxx x xxxxxxxxxx odpovídala xxxx xxxxx xxxxx xxxxxxxxx xxxxxxxxx xxxxxxx xxxxxxxxx xxxxxx xxxxxxx.
Xxxxx xxx x správní delikty x xxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx, xx xxxxx x prvé xxxx xxxxxxxxx, že xxxx xxxxxx xxxx, xxx xxxxx xxxx, xx xxxxx xxxxxxxxxxx protiprávní xxxxxxx vyjádřené v xxxxxx x léčivech, xxxx xx měly xxxxxxxxxx xxxxxxxxxxx xxxxxxx xxxxxxxxx xxx v xxxxxxxx č. 536/2014, xx. x xxxxx xxxxxxxxxxx xxxxxxxx Xxxxxxxx xxxx. Xxx stanovení xxxxx xxxxxxx xxxxxxx pokut xx xxxxxx protiprávní xxxxxxx se xxxxx xxxxxxxxx xxxxxxxxx právní xxxx.
X §107 xxxx. 2:
Xxx xxxxxx xxxxxxxx xxxxxxxx obecné xxxxxx xxxxxxxx xxx ustanovení §11 xxxx. x) xx xxxxxxx xxx xxxxxxx xxxxxxx sankce xxxxxxxxxxx x zákazu xxxxxxxx.
X §108x a §108x:
X důvodu xxxxxx xxxxxxx xx x xxxxxx upravují podmínky xxx xxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx x xxxxxxx xxxxxxxx xxxxxxxxx x xxxxxxxx xx xxxxxxx xxxxxxx, že xxxxxxxxxx takového léčivého xxxxxxxxx xx xxxxx xxxx.
X §112 xxxx. 6:
Xxxx vkládaný xxxxxxxx 6 zakotvuje xxxxxxxx xxxxx rozhodnout x xxxxxxx prostředků xx xxxxxxxxxx xxxx Xxxxxxxx xxxxxx xxx xxxxxxxx xxxxx na xxxxxxxx xxxx xxxxxxxx xxxxxxxx Xxxxx xxxxxxxxx pro Xxxxxxxxxxxx zdravotnictví.
K bodům 68 xx 72
X §114 xxxx. 1, 2 a 4:
Xxx se xxxxx xxxxx x xxxxxxxxxxxx xxxxxxxxxx xxxxxx relevantního xxxxxxxxxxxx xxxxxxxxxx x xxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxx xxx, xxx xx zákon výslovně xxxxxxxxxxx. Přitom xx xxxxxxxxxx xx xxxxxxxxxx, xx xxx x xxxxxxxxxx §114 odst. 1 xxxxxx x xxxxxxxxxxx působnost Xxxxxxxxxxxx xxxxxxxxxxxxx x xxxxxx xxxxxxxx x x xxxxxxxxxx §114 xxxx. 2 xxxxxx x xxxxxxxxx xxxxxxxxx Xxxxxxxxxxxx xxxxxxxxxxxxx x Ministerstva xxxxxxxxxxx k xxxxxx xxxxxxxx.&xxxx; Po xxxxxx xxx xxxxx x xxxxxxxxx xxxxxxxx xxxxxxxx x správné xxxxxxxx xxxxx xxx, že xxx oblast xxxxxxxxxxxxx xxxxxxxx přípravků se xxxx xxxxxxxx xxxxxxx xx xxxxx Ministerstva xxxxxxxxxxx.
X §114 odst. 2:
X xxxxx xxxx xxx xxx o xxxxxxxxxxxx xxxxxxxxx xxxxx x xxxxxx xxxxxxxxxxxx xxxxxxxxxx, xxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxxx pro xxxxxx xxxxxxxxxx hodnocení xxxxxxxxx xxxxxxxx xxxxxxxxx xxxx xxxxxxxxxxx xxxxxxxxxxxx xxxxxxxxxxxx novými.
Přechodná xxxxxxxxxx xxxx upravena xxx, xxx xxxxxxxxxxxx ustanovení článku 98 xxxxxxxx x. 536/2014.
X xxxxxx xxxxxxxxxx xxxxxxxxxx xxxxxxxxxxx xx xxxxxxxx xxxxxxx, že xxxxx x xxxxxx xxxxxx xx nebude xxxxxxxxx xx xxxxx xxxxxx komise.
Jedná xx x xxxxxxxxxx xxxxxxxxxxxx xxxxxxx xxxxxxxxx xxxxxxx xxxxxxxxxx x xxxxxxx xx směrnicí Xxxxxxxxxx xxxxxxxxxx x Xxxx (XX) 2015/1535 ze xxx 9. xxxx 2015 x xxxxxxx xxx xxxxxxxxxxx xxxxxxxxx x oblasti xxxxxxxxxxx xxxxxxxx x xxxxxxxx xxx xxxxxx xxxxxxxxxx xxxxxxxxxxx, v platném xxxxx.
K čl. V (Xxxxxxxx):
Xxxxxx xxxxxxxxx xxxxxx se xxxxxxxxx xxxxxxxx xx vztahu xx xxxxxx xxxxxxxx xxxxxxxxxx novely xxxxxx.
Xx xxxx, ustanovení ohledně xxxxxxxx xxxxxx xxxxxx xxxxxxxxxx xxxxxxxxxx hodnocení xxxxxxxxx xxxxxxxx přípravků xx xxxx nabýt xxxxxxxxx xxxxxxxxx 6 xxxxxx xx xxx xxxxxxxxxx xxxxxxxx Xxxxxx x Xxxxxxx věstníku Xxxxxxxx xxxx podle čl. 82 xxxx. 3 xxxxxxxx x. 536/2014, xxxxxxx xxx, xxx xxxx xxxx xxxxxxxx xxxxxxxxxx, xxxxxx Xxxxxxxxxxxx xxxxxxxxxxxxx xxxxxx sdělení xx Xxxxxx xxxxxx.
Xx xxxxx, xxxxxxxxxx xxxxxxxx xx jmenování xxxxx xxxxxx xxxxxx, Xxxxxxx, xxxxxxxxx xxxx etické xxxxxx x xxxxxxxxxx xxxxxxx etické xxxxxx, xx xxxx nabýt xxxxxxxxx xxx xxxxxx xxxx xxxxxxxxxxxx xxxxxx xx xxx xxxxxxxxxx xxxxxxxx Xxxxxx x Xxxxxxx věstníku Xxxxxxxx xxxx podle čl. 82 xxxx. 3 xxxxxxxx x. 536/2014, xxxxx xxxxxx xxxxxx xxxx xxx xxxxxxx účinnosti xxxxxxxx xxxxxxx xxxxx xxxxxxxx x není xxxxx, xxx s xxxxxxx x xxxxxxxxxx xxxxxx komise xxxx xxxxxxxx xx x xxx nabytí xxxxxxxxx xxxxxxxx č. 536/2014.
Xx xxxxx, xxxxxxxxxx xxxxxxx omezení xxxxxxxxx xxxxxxxx přípravků xx měla nabýt xxxxxxxxx xxxxxx dnem xxxxxxxx xxxxxxxxxxxx xxxxxx xxxxxxxxxxxxx xx xxx xxxxxxxxx xxxxxx, xxxxx xxxxxxxxxx systému xxxxxxxxx x xxxxxxxxxxxxx xxxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx xxx xxxxxxxx xxxxxxx xxxxxxxx x České xxxxxxxxx x přijímání xxxxxxxxxxx opatření xxxxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx xx xxxxxxxxx v xxxx případech, xxx xxxxxxxxxxx xxxxxx hrozby xxxxxxx takových xxxxxxxx xxxxxxxxxx, xx xxxxxxxx xxxxxx xxx xxxxxxxx, x to xxxxxxx xx xxxxxx xxxxxxxx xxxxxxxxxx x xxxxxxxxxx xxxxxxxx přípravků, xxxxxxxxxxxx x xxxxxxxxxxx xxxxxxxxx xxxxx.
Xx čtvrté, ostatní xxxxxxxxxx xxxxxxxx x xxxxxx xxxxxx xx xxxx xxxxx účinnosti xx xxxxxxxx, x xxxx xx xx xxxxx, xxx xxxxxx xxxxxxxxx prvním dnem xxxxxxxxxxxx xxxxxx xxxxxxxxxxxxx xx dni vyhlášení xxxxxx.
X Xxxxx xxx 13. xxxxx 2016
předseda xxxxx
Xxx. Xxxxxxxx Xxxxxxx x. r.
ministr zdravotnictví
MUDr. Xxxxxxxxx Němeček, XXX, x. r.
XXXXXXXXX TABULKA XXXXXX XXXXXXXX XXXXXXXX S XXXXXXXX XX
Xxxxxxxxx xxxxxxx x návrhu xxxxxx xxxxxx x. 378/2007 Xx., o xxxxxxxx x x xxxxxxx xxxxxxxxx souvisejících zákonů (xxxxx o xxxxxxxx)
|
Xxxxxxxxxx xxxxxx předpis (resp. xxxx xxxxxx předpis) |
Odpovídající xxxxxxx XX |
|
|
Xxxxxxxxxx (xxxx, §, xxxx., xxxx. xxxx.) |
Xxxxx x. |
Xxxxxxxxxx (čl., xxxx., písm., xxx., xxxx.) |
|
Xx. 2 odst. 1 |
||
|
Xx. 83 |
||
|
Čl. 4 |
||
|
Xx. 8 odst. 1 |
||
|
Xx. 1 xxx 22 |
||
| §51 | ||
|
Kapitola XX, xx. 4 |
||
|
Kapitola XX, čl. 9 |
||
|
Xxxxxxxx XX čl. 83 |
||
|
Xxxxxxxx XX, čl. 2, xxxx. 2, xxx 12 |
||
|
Xxxxxxxx XX, xx. 5 |
||
|
Xxxxxxxx XX, čl. 2, xxxx. 2, xxx 12 |
||
|
Xxxxxxxx XX, xx. 6, xxxx. 5 a 7 |
||
|
Xxxxxxxx XX, xx. 7 |
||
|
Xxxxxxxx XX, xx. 8 |
||
|
Xxxxxxxx X, xx. 34 |
||
|
Xxxxxxxx X, čl. 2, xxx 11 |
||
|
Xxxxxxxx II, xx. 4 |
||
|
Xxxxxxxx II, xx. 9 |
||
|
Kapitola XX, xx. 8 odst. 4 |
||
|
XXX X6 |
||
|
Xxxxxxxx II, xx. 9 |
||
|
XXX E6 |
||
|
Kapitola XX, xx. 4 |
||
|
Xxxxxxxx XX, xx. 8 xxxx. 4 |
||
|
Xxxxxxxx XX, xx. 6 |
||
|
Kapitola XX, xx. 4 |
||
|
Xxxxxxxx XX, xx. 7 |
||
|
Xxxxxxxx XX, xx. 28, xxxx. x) |
||
|
Xxxxxxxx XX, xx. 7, odst. 1 xxxx. x) |
||
|
Xxxxxxxx XXX, xx. 20 |
||
|
Xxxxxxxx II, xx. 4 |
||
|
Kapitola X, xx. 4 |
||
|
Xxxxxxxx X, xx. 2, xxx 15 a 16 |
||
|
Kapitola XXXX, xx. 49 |
||
|
Xxxxxxxx XX, čl. 73 |
||
|
Xxxxxxxx XXXX, xx. 50 |
||
|
Xxxxxxxx XX, xx. 26 |
||
|
Kapitola XXXX, xx. 59 xxxx. 3 |
||
| 32014R0536 |
Kapitola XVIII, xx. 92 |
|
|
Xxxxxxxx XX, xx. 61, xxx 5x |
||
|
Xxxxxxxx X, xx. 68 |
||
|
Xxxxxxxx XXXXX, xx. 90 |
||
|
Xxxxxxxxx 81 |
||
|
Xxxxxxxx VII, xx. 42 xxxx. 3 |
||
|
Xxxxxxxx XII, xx. 76 |
||
|
Xxxxxxxx X, xx. 2, bod 20 |
||
| §64 písm. b) |
Xx. 8 odst. 1 |
|
|
Čl.1 |
||
|
Čl.1 |
||
|
Čl. 94 |
||
|
Xx. 8 xxxx. 1 |
||
|
Xx. 15 |
||
|
Čl. 35 |
||
|
Xx. 36 |
||
|
Xx. 37 xxxx. 1 |
||
|
Xx. 37 xxxx. 5 |
||
|
Xx. 37 xxxx. 6 |
||
|
Xx. 38 xxxx. 1 |
||
|
Xx. 37 xxxx. 4 |
||
|
Xx. 41. xxxx. 3 |
||
|
Xx. 42 xxxx. 1 |
||
|
Xx. 47 |
||
|
Čl. 49 |
||
|
Xx. 52 |
||
|
Xx. 54 xxxx. 1, 2 |
||
|
Čl. 55 |
||
|
Xx. 56 |
||
|
Xx. 57 |
||
|
Xx. 58 |
||
|
Kapitola XXX, xx. 76 xxxx. 1, 2 |
||
|
Xx. 94 |
||
|
Xx. 94 |
||
|
Xx. 28 xxxx. 1 |
||
|
Xx. 41 xxxx. 1 |
||
|
Čl. 47 |
||
|
Xx. 49 |
||
|
Xx. 54 odst. 1 |
||
|
Xx. 58 |
||
|
Xx. 73 |
||
|
Čl.94 |
||
|
Čl. 28 xxxx. 1 |
||
|
Xx. 41 xxxx. 1 |
||
|
Xx. 47 |
||
|
Xx. 49 |
||
|
Čl. 54 xxxx. 1 |
||
|
Xx. 58 |
||
|
Xx. 73 |
||
|
Xxxxx xxxxxxxx EU (xxx Xxxxx) |
Xxxxx xxxxxxxx XX |
|
XXXXXXXX EVROPSKÉHO XXXXXXXXXX X XXXX (XX) x. 536/2014 xx xxx 16. xxxxx 2014 x klinických xxxxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx a o xxxxxxx xxxxxxxx 2001/20/XX |
|
|
XXXXXXXX XXXXXX x přenesené xxxxxxxxx (EU) x. 1252/2014 xx xxx 28. xxxxxx 2014 xxxxxxxxxx xxxxxxxx Evropského xxxxxxxxxx a Rady 2001/83/XX, pokud xxx x xxxxxx x xxxxxx xxxxxxx xxxxxxx xxxxx xxx účinné xxxxx xxx humánní xxxxxx xxxxxxxxx |
|
| 32004L0027 |
XXXXXXXX XXXXXXXXXX XXXXXXXXXX A XXXX x. 2004/27/XX xx xxx 31. xxxxxx 2004, kterou xx xxxx směrnice 2001/83/ES x xxxxxx Xxxxxxxxxxxx xxxxxxxxx xx humánních xxxxxxxx xxxxxxxxx |
Xxxxx xxxxx xxx.xxx.xx


