Právní předpis byl sestaven k datu 31.01.2020.
Zobrazené znění právního předpisu je účinné od 01.01.2020 do 31.01.2020.
Vyhláška o způsobu předepisování léčivých přípravků, údajích uváděných na lékařském předpisu a o pravidlech používání lékařských předpisů
54/2008 Sb.
ČÁST PRVNÍ - OBECNÁ USTANOVENÍ
Úvodní ustanovení §1
Zacházení s lékařskými předpisy §2
Zacházení s lékařskými předpisy označenými modrým pruhem §3 §4
ČÁST DRUHÁ §5 §6 §6a §7 §8 §9 §10 §11 §11a §12 §13 §14 §15 §16
ČÁST TŘETÍ - PŘEDEPISOVÁNÍ LÉČIVÝCH PŘÍPRAVKŮ ZA ÚČELEM POSKYTOVÁNÍ VETERINÁRNÍ PÉČE
Způsob předepisování §17
Údaje uváděné na receptu §18
Údaje uváděné na předpisu pro medikované krmivo §19
Uchovávání předpisů pro medikované krmivo §20
Údaje uváděné na předpisu pro veterinární autogenní vakcíny §21
Uchovávání předpisů pro veterinární autogenní vakcíny §22
Předepisování léčivých přípravků za účelem jejich distribuce chovatelům §23
ČÁST ČTVRTÁ - PŘECHODNÁ, ZRUŠOVACÍ A ZÁVĚREČNÁ USTANOVENÍ
Přechodná ustanovení §24
Zrušovací ustanovení §25
Závěrečné ustanovení §26
Příloha č. 1 - Vzor receptu
Příloha č. 2 - Vzor žádanky
č. 405/2008 Sb. - Čl. II
Ministerstvo xxxxxxxxxxxxx xx projednání s Xxxxxxxxxxxxx xxxxxxxxxxx, Xxxxxxxxxxxxx xxxxxx, Xxxxxxxxxxxxx vnitra, Xxxxxxxxxxxxx xxxxxxxxxxxxx a Xxxxxxxxxxxxx xxxxxxx xxxxxxx xxxxx §114 xxxx. 3 x x xxxxxxxxx §80 xxxxxx x. 378/2007 Xx., x xxxxxxxx x x změnách xxxxxxxxx xxxxxxxxxxxxx xxxxxx (xxxxx x xxxxxxxx):
ČÁST XXXXX
XXXXXX USTANOVENÍ
§1
Úvodní xxxxxxxxxx
(1). Xxxx xxxxxxxx xxxxxxx způsob předepisování xxxxxxxx xxxxxxxxx, xxxxx xxxxxxx na lékařském xxxxxxxx a pravidla xxxxxxxxx xxxxxxxxxx předpisů.
(2). Xxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxx používají xxxxxxxx xxxxxxxx1), x xx
x) xxxxxxx xxxxxx xxx xxxxxxxxxxxxx
1. xxxxxxxx xxxxxxxxx xxxxxxxxxxxx xxxxxx xxxxx zařazené do xxxxxxx I2) (xxxx xxx "xxxxxx xxxxx") xxxx xxxxxxxxxxxx xxxxx xxxxxxxx do xxxxxxx XX3) (dále jen "xxxxxxxxxxxx xxxxx"), xxxxx xxxx xxxxxxxx modrým xxxxxx; vzor xxxxxx xxxxxxx je xxxxxx x příloze č. 1 xxxx xxxxxxxx,
2. xxxxxxxxx xxxxxxxx xxxxxxxxx x xxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxx x xxxx 1, xx xxxxxx xxxxxxxxxxx xxxxxxxxxxx služeb, a xx i xxx xxxxxx opakovaný xxxxx xxxxx §6 odst. 4,
3. veterinárních xxxxxxxx xxxxxxxxx x humánních xxxxxxxx xxxxxxxxx, x xxxxxxxx léčivých xxxxxxxxx xxxxxxxxx x xxxx 1, xx xxxxxx xxxxxxxxxxx xxxxxxxxxxx xxxx, x to x xxx jejich xxxxxxxxx xxxxx xxxxx §6 xxxx. 4,
x) xxxxxxxxxx xxxxxxxxxxxxx zdravotních xxxxxx (xxxx xxx "xxxxxxxxxxxx") x xxxxxxxxx nebo xxxxxxxxxxx xxxx xxxxxxxxxxx xxxxxxxxx veterinární xxxxxxxx5), xx xxxxxx xxxxxxxxx, xxxxxx xxxxxxxxxxxx xxxxxxxxx, x výjimkou xxxxxxxx xxxxxxxxx xxxxxxxxx x xxxxxxx x) xxxx 1 (xxxx jen "xxxxxxx"),
x) xxxxxxx na xxxxxx xxxxxxxxx uvedené x xxxxxxx a) xxxx 1, které xxxx označeny xxxxxx xxxxxx; xxxx xxxx xxxxxxx je xxxxxx x příloze č. 2 této xxxxxxxx.
(3) Pro xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx xxx xxxx xxxxxx
x) recept x xxxxxxxxxxxx podobě (xxxx xxx "elektronický xxxxxx") zaslaný xxxxxxxxxxxxxx xxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxxxxxxx receptů6) xxxxxxxxx xxxxxxxxx xxxxxxxxxxxxx podpisem xxxxxxxxxxxxxxx xxxxxx xxxxx xxxxxx xxxxxxxx xxxxxxxx7) (xxxx xxx "xxxxxxxxxxxx xxxxxx"), xxxx
x) xxxxxxx x xxxxxxxxxxxx xxxxxx (xxxx jen "xxxxxxxxxxxx xxxxxxx") xxxxxxxx xxxxxxxxxxxxxx xxxxxxx x xxxxxxxxx xxxxxxxxxx kódem xxxxxxxxxx xxxxxxxxxxxxxx, je-li zasílána x rámci lokální xxxxxxxxxx xxxx xxxxxx xxxxxxxxxxxxxx xxxxxxxx lékárně, xxxxx xx jeho xxxxxxxx; nebo xxxxxxxxxx xxxxxxxxxxxxx xxxxxxxx, xx-xx xxxxxxxx lékárně mimo xxxx xxxxxxx počítačovou xxx,
xx xxxxxxxxxxx, xx xxxxxxx náležitosti xxxxx §6 xxxx 13.
(4) Xx lékařském xxxxxxxx x na xxxxxx x xxxxxxx nesmějí xxx umístěny xxxxx xxxx xxxxx, které xx omezovaly čitelnost xxxxx xxxxxxxxxxxx xxxxxxxxxxxxxx xxxx xxxxx xx xxxx reklamní charakter.
(5) Xxxxxxxx xxxxxxx, s xxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxxx xxxxxx xxxxxx, xxx opatřit proti xxxx xxxxxxxx ochrannými xxxxx.
§2
Xxxxxxxxx s lékařskými xxxxxxxx
Xxxxxxxx předpisy se xxxxxxxx tak, xxx xx xxxxxxxxx xxxxxx xxxxxx xxxx xxxxxxxx x možnosti jejich xxxxxxxx. Xxxxxxxxxx xxxxxxxx xxxxxxxx nelze xxxxxxx xxxxxxxx poskytovatele, fyzické xxxx xxxxxxxxx xxxxx xxxxxxxxx xxxxxxxxx xxxxxxx xxxxxxxxxxx xxxxxxxx5).
Xxxxxxxxx x lékařskými xxxxxxxx xxxxxxxxxx modrým xxxxxx
§3
(1) Výrobu a xxxxxxxxxx lékařských xxxxxxxx xxxxxxxxxx modrým xxxxxx xxxxxxxxxxx xxxxxx xxxxxxxxx xxxxxx xxxxx xxxx x xxxxxxxxxx xxxxxxxxxx x smluvně zajištěného xxxxxxx xxxxxx tiskopisů, x to xx xxxxxxx objednávek poskytovatelů xxxx xxxxxxxxx xxxx xxxx xxxxxxxxxxx xxxx xxxxxxxxxxx x xxxxxx xxxxxxxxx xxxxxxxxxxxxx činností5) (xxxx xxx "xxxxxxxxx xxxxx") x místem xxxxxx xxxxxx xxxxxxxx xx xxxxxxxxx obvodech xxxxxxxx xxxxx xxxx x xxxxxxxxxx xxxxxxxxxx8).
(2) Xxx xxxxxxxxxxx xxxxxxx xxxxxxxxxx lékařských xxxxxxxx xxxxxxxxxx xxxxxx pruhem xxxxxxxxx xxxxxx xxxxx xxxx s xxxxxxxxxx xxxxxxxxxx jejich xxxxxxxxxxxx xxxxxx v rozsahu xxxxxxx jedné xxxxxx xxxxxx xxxxxxx xxxxxxxxxx xx xxxxxxxxx xxxxxxxxxx xxx.
(3) Lékařské xxxxxxxx xxxxxxxx modrým pruhem xxxxxxxx xxxxxxxxxxx xxxxx xxxxx uvedených v přílohách č. 1 a 2 xxxx xxxxxxxx x xx xxxxxxx xx xxxxxxx pověřený zaměstnanec xxxxxxxx xxxxx xxxx x rozšířenou xxxxxxxxxx. Xxxxxxxx xxxxxxxxxxx xx xxxxxxx xxxxxxx xxx xxxxxxxx xxxxxxxxxxx lékařských xxxxxxxx xxxxxxx xxxxxxxxx x převzetí xxxxxxx xxxxxxxx a otiskem xxxxxxx xxxxxxxx úřadu xxxx x rozšířenou xxxxxxxxxx.
(4) Xxxxxx xxxx xxxx x xxxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxx modrým xxxxxx xx xxxxxxxx xxxxxxxxx x vyzve oprávněnou xxxxx k xxxxxx xxxxxxxxxx. Xxxxxxxx xxxxxxxx xxxxxxxx xxxxxx pruhem xxxxx xxx obecními xxxxx xxxx x xxxxxxxxxx xxxxxxxxxx vydány xxxxx oprávněným osobám xxxx xxxxxx pověřeným xxxxxxxxx8).
(5) X xxxxxx xxxxxxxxxx předpisů xxxxxxxxxx xxxxxx xxxxxx vede xxxxxx úřad xxxx x xxxxxxxxxx xxxxxxxxxx xxxxx xxxxxxxxx, která xxxxxxxx xxxxx x xxxxx xxxxxxxx xxxxxxxxxx xxxxxxxx, včetně xxxxxx xxxxxxxxxx xxxxx x xxxxxxxxxxxxx údaje o xxxxxxxxx osobě. Převzetí xxxxxxxxxx xxxxxxxx xxxxxxxxxx xxxxxx xxxxxx potvrdí xxxxxxxxx osoba nebo xxxx pověřený xxxxxxxx8) xx originálu objednávky x xxxxxxxx v xxxxx tiskopisů.
(6) Ztráta xxxx xxxxxxxx nevyplněného xxxxxxxxxx xxxxxxxx označeného xxxxxx pruhem xx xxx xxxxxxxxxx odkladu xxxxxx xxxxxxxx xxxxx xxxx x xxxxxxxxxx xxxxxxxxxx, xxxxx xxxx xxxxxxxxx xxxxxxxxx xxxxx xxxxx, a xxxxxxxx xx xxxx ztráta xxxx xxxxxxxx xxxxxx x Xxxxxxx Xxxxx xxxxxxxxx.
§4
(1) Xxxxxxxx-xx oprávněné xxxxx lékařské předpisy xxxxxxxx xxxxxx xxxxxx xxxx osobám, xxxxx xxxx x oprávněné xxxxx x pracovním xxxxxx xxxx v xxxxxxxx xxxxxx, vede xxxxxxxxx osoba x xxxxx výdeji evidenci xxxxx §3 xxxx. 5.
(2) Znehodnocené xxxx xxxxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxx modrým xxxxxx, xxxxxx xxxxxx průpisů, xxxxxxxxx xxxxx, xxxxxx xxxx tyto lékařské xxxxxxxx xxxxxx xxxxxxxxxx xxxxxx, xxxx osobě.
(3) Xxxxxxxxx xxxxx vede x odevzdaných znehodnocených xxxx xxxxxxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxxx xxxxxx, xxxxxx jejich xxxxxxx, evidenci. Xxxxxx xxxxxxxx xxxxxxxx xxxxx xxxxxxxxx xxxxx xxxxxx xxxxxxxxxxx xxxxxxxx xxxxx xxxx s xxxxxxxxxx xxxxxxxxxx x xxxxxxxxx. Xxxxx xxxxxx xxxx xxxxxxxxx xxxxxxxxxxxx xxxxxx x likvidaci xxxxxxxxxx xxxxxxxx xxxxxxxxxx xxxxxx xxxxxx, xxxxxx xxxxxx xxxxxxx, x němž xxxxxxx xxxxxx xxxxxxxx xx oprávněné xxxxx.
(4) X xxxxxxxxxx předpisech xxxxxxxxxx xxxxxx xxxxxx, xxxxxx jejich průpisů, xxxxxxxxx obecním xxxxxx xxxx s xxxxxxxxxx xxxxxxxxxx xxxxx tyto xxxxxx xxxxx evidenci.
(5) Xx zacházení x xxxxxxxxxx xxxxxxxx xxxxxxxxxx xxxxxx xxxxxx xx xxxxxxxx xxxxxxx xxxxxxxxxx §2.
(6) Xxxxxxxx xxxxxxxx xxxxxxxx modrým xxxxxx xxxxxx pro oprávněné xxxxx v působnosti Xxxxxxxxxxxx xxxxxx xxxx xxxxxxxxxxxx x xxxxxxxx xxxx xxxx. Xxx xxxxxxxxx s xxxxxx xxxxxxxxxx xxxxxxxx xxxxx xxxxxxxxxx §3 xxxx. 3 až 6 x xxxxxxxx 1 xx 5 xxxxxx xxxxxxxxxx x tím, xx xxxxxxxx svěřené xxxxxx xxxxxxxxxxx obecnímu xxxxx xxxx x xxxxxxxxxx xxxxxxxxxx xxxxxxxxx Xxxxxxxxxxxx obrany. Xxxxxx xxxx xxxxxxxx lékařských xxxxxxxx xxxxxxxxxx xxxxxx xxxxxx xx hlásí xxxxxxxxxxx xxxxxxxxxx xxxxxxxxxxxxxx xxxxxx a vojenské xxxxxxx.
§6
§6 xxxxxx xxxxxxx xxxxxxxxx č. 329/2019 Sb.
§6x
§6x zrušen xxxxxxx xxxxxxxxx č. 329/2019 Sb.
§7
§7 xxxxxx xxxxxxx xxxxxxxxx č. 413/2017 Sb.
§8
§8 xxxxxx xxxxxxx xxxxxxxxx č. 413/2017 Sb.
§9
§9 xxxxxx xxxxxxx xxxxxxxxx č. 413/2017 Sb.
§10
§10 xxxxxx xxxxxxx xxxxxxxxx č. 413/2017 Sb.
§11
§11 xxxxxx xxxxxxx xxxxxxxxx č. 413/2017 Sb.
§11x
§11x zrušen xxxxxxx xxxxxxxxx č. 413/2017 Sb.
§12
§12 zrušen xxxxxxx xxxxxxxxx č. 413/2017 Sb.
§13
§13 zrušen xxxxxxx xxxxxxxxx č. 329/2019 Sb.
§14
§14 zrušen xxxxxxx xxxxxxxxx č. 329/2019 Sb.
§15
§15 xxxxxx xxxxxxx xxxxxxxxx č. 329/2019 Sb.
§16
§16 xxxxxx xxxxxxx xxxxxxxxx č. 329/2019 Sb.
XXXX XXXXX
XXXXXXXXXXXXX LÉČIVÝCH XXXXXXXXX ZA XXXXXX XXXXXXXXXXX VETERINÁRNÍ XXXX
§17
Xxxxxx xxxxxxxxxxxxx
(1) Xx xxxxx xxxxxx xxx xxxxxxxxx
x) xxxxx druh xxxxxxxx xxxxxxxxx, xxxxx xxxxxxxx xxxxxx látky nebo xxxxxxxxxxxx látky, nebo
b) xxxxxxx xxx druhy xxxxxxxxx léčivých xxxxxxxxx.
(2) Xxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx xx vyznačí xxxxx balení nebo xxxxx xxxxxxx xxxxxxx x xxxxx v xxxxxxxxx xxxxxx.
(3) Xxxxxx xxxxxxxxx xxxxxxxxxx omamné xxxxx nebo psychotropní xxxxx xx xxxxxxxxxxx xx xxxxxxx označené xxxxxx pruhem.
(4) Při xxxxxxxxxxxxx léčivých xxxxxxxxx xxxxxxxxx x odstavci 3 xx
x) xxxxxxxx xxxxx xxxx x 2 xxxxxxx; xxxxx xxxx x první xxxxxx xx xxxxx xxx xxxxx xxxxxxxxxxxx xxxxxxxx xxxxxxxxx x xxxxxxx; druhý xxxxxx xx xxxxxxxxx x xxxxx použitých receptů,
b) xxxxxxx xxxxx uvedené x xxxxxxxx 2 x v §18 xxxx. 1.
(5) Jestliže xx xx výdej xxxxxxxx xxxxxxxxx xxxxxxxx, xxxxxxxxx xx podle §6 xxxx. 4 xxxxxxx, x xxxxxxxxx xxxxxxxxx z xxxxxxxx xxx xxxxxxxxxxx xxxxxxxxxxx xxxx xx postupuje xxxxx §12 obdobně, x jedná-li xx x vystavení xxxxxx x xxxxxxx, postupuje xx xxxxx §15 xxxxxxxxx.
§18
Xxxxx xxxxxxx na xxxxxxx
(1) Na xxxxxxx xx xxxxxxx xxxx xxxxx:
x) xxxxx, xxxxxxxx xxxxx, xxxxxxxx, xxxxxx xxxxx xxxxxxxx xxxxxx, xxxxxxxx xxxxx xxxxxx xx xxxxx Xxxxx xxxxxxxxx, xxx-xx o xxxxxxx, a telefonní xxxxx chovatele xxxxxxx, xx-xx xxx xxxxxxx xxxxx; x xxxxxxxxx xxxxx xxxxx xxxx xxxxxxxx firma, xxxxx x xxxxxxxxx číslo; xxxxxxxxx čísla xx xxxxxxx jen x xxxxxxx, xx x xxx xxxxxx uživatelé xxxxxxxx,
x) xxxx zvířete, xxx xxxxx xx xxxxxx xxxxxxxxx xxxxxxxxxxxx,
x) xxxxxxxxxx léčivý xxxxxxxxx, x to
1. xxxxxxxx xxxxx, xxx nímž xxx xxxxxx xxxxxxxxx xxxxxxxxxxx10), xxxxxx xxxxx, xxxx x xxxxxxxx xxxxxx, xxxx
2. xxxxxxxxx xxxxx nebo jeho xxxxxxxxx xxxxx xxxx xxxxxxx uvedená v Xxxxxx lékopisu11), x xx x xxx xxxx xxxxxxxxxx xxxxxx x případě, že xx xxxxx x xxxxxxxxxxxx xxxxxx xxxxxxxxx,
x) xxxxx k xxxxxxx,
x) xxxxx xxxxxxxxx,
x) otisk xxxxxxx xxxxxxxxxxxx xxxxx, xxxxxxxx jména, příjmení x xxxxx xxxxxxxxx, xxxxxxxx místo výkonu xxxxx xxxxxxxxxxxxxxx xxxxxxxxxxxxx xxxxxx; xxxxx xxxxxxxxxxx xxxxx xxxxxxxx xxxxxxx xxxxxxxxxxx xxxxxxxi5) xxxx xxxxxxxxxxx xxxxxxx xxxx xxxxxxxxx xxxxx xxxxxxxxx xxxxxxxxx xxxxxxx veterinární xxxxxxxx5), xxxxx se xxxx jméno, případně xxxxx, xxxxxxxx x xxxxx pravidelného xxxxxxxxxxx xxxxxxxxxxx péče této xxxxx, jde-li x xxxxxxxx xxxxx, xxxx xxxxx x sídlo, xxx-xx o xxxxxxxxxx xxxxx, xxxxxxxxx xxxxx x
x) xxxxxx xxxxxxxxxxxxx xxxxxx.
(2) Doba xxxxxxxxx xxxxxxx se xxxx xxxxx §14 xxxxxxx.
§19
Xxxxx xxxxxxx xx xxxxxxxx pro xxxxxxxxxx xxxxxx
(1) Předpis xxx xxxxxxxxxx xxxxxx15) xxxxxxxx
x) xxxxx, xxxxxxxx xxxxx, xxxxxxxx x místo xxxxxxxxx, případně xxxxx xxxxxx praxe xxxxxxxxxxxxxxx xxxxxxxxxxxxx xxxxxx,
x) xxxxx xxxxxxxxxxxx premixu16), který xx xxx xxxxxx xxx xxxxxx xxxxxxxxxxxx xxxxxx, včetně uvedení xxxx,
x) xxxxxxxxxxx xxxxxx xxxxx xxxxxxxx x xxxxxxxxxxx xxxxxx,
x) xxxxx, xxxxxxxx jména, xxxxxxxx x xxxxx xxxxxxxxx xxxxxxxxx xxxxxxx, x xxxxxxx má xxx xxxxxxxxxx xxxxxx xxxxxxx, xxx-xx o fyzickou xxxxx, xxxx xxxxx x xxxxx, xxx-xx x xxxxxxxxxx osobu,
e) xxxxx, případně xxxxx, xxxxxxxx a xxxxx xxxxxxxxx xxxxx, která xx příjemcem xxxxxxxxxxxx xxxxxx, xxx-xx x xxxxxxxx osobu, xxxxx x xxxxx, xxx-xx x xxxxxxxxxx osobu17),
f) xxxxxx a xxxxxxxxxxx xxxxx xxxxxxxxxxxx5), xxx xx xxx xxxxxxxxxx xxxxxx použito,
g) xxxx, xxxxxxxxx x počet xxxxxx, xxx která xx xxx xxxxxxxxxx xxxxxx vyrobeno,
h) xxxxxxxx xxxx xxxxxxxxxxx indikaci,
i) xxxxxxxx medikovaného krmiva,
j) xxxxxx a dobu xxxxxxxxx xxxxxxxxxxxx xxxxxx, xxxxxx xxxxxxxxx podávání x množství, ve xxxxxx xx xxxxxxxxxx xxxxxx xxxxxxxxxx do xxxxx xxxxx xxxxx, xxxxx medikované xxxxxx xxxx xxxxxxxxx jako xxxxxx xxxxxx,
x) jméno, xxxxxxxx jména, příjmení x místo xxxxxxxxx xxxxxxx xxxxxxxxxxxx xxxxxx, xxx-xx o xxxxxxxx xxxxx, xxxx xxxxx x xxxxx, jde-li x právnickou osobu,
l) xxxxxx xxx chovatele xxxxxx, včetně xxxxxxxxxx xxxxxxxxxx,
x) xxxxx xxxxxxxxx xxxxxxxx xxx medikované xxxxxx,
x) xxxx "Výrobu xxxx uvedení xxxxxxxxxxxx xxxxxx do xxxxx xxxxx na xxxxx xxxxxxx xxx medikované xxxxxx xxxxxxxx",
x) otisk xxxxxxx obsahujícího jméno, xxxxxxxx jména, příjmení x místo podnikání, xxxxxxxx xxxxx xxxxxx xxxxx xxxxxxxxxxxxxxx xxxxxxxxxxxxx xxxxxx; xxxxx xxxxxxxxxxx xxxxx xxxxxxxx xxxxxxx xxxxxxxxxxx činnosti5) xxxx xxxxxxxxxxx xxxxxxx xxxx xxxxxxxxx xxxxx oprávněné xxxxxxxxx odborné veterinární xxxxxxxx5), uvádí se xxxx jméno, případně xxxxx, xxxxxxxx x xxxxx xxxxxxxxxxxx xxxxxxxxxxx xxxxxxxxxxx xxxx této xxxxx, jde-li x xxxxxxxx osobu, xxxx xxxxx a xxxxx, xxx-xx x xxxxxxxxxx xxxxx, a
p) podpis xxxxxxxxxxxxx lékaře, který xxxxxxx xxx xxxxxxxxxx xxxxxx xxxxxxxx.
(2) Xxxxxxx xxx xxxxxxxxxx krmivo xx xxxxxxxxxx xxxxx xxxxx xxxxxxxx xxx xxxxxxxxxx xxxxxx, který xxxxxxxx Xxxxx pro xxxxxx xxxxxxxx veterinárních xxxxxxxxxxxx a léčiv xx svém xxxxxxxxxxx xxxxxxxxxx.
(3) Předpis pro xxxxxx xxxxxxxxxxxx xxxxxx xxxxxxxxx xxxxxxxxxxx lékař x pěti xxxxxxxxxxxx. Xxxxx vyhotovení uchovává xxxxxxxxxxx xxxxx, který xxxxxxx xxx xxxxxxxxxx xxxxxx vystavil, ostatní 4 xxxxxxxxxx xxxxxxxx xxx xxxxxxxxxx xxxxxx xxxxxxx xxxxxxxxxxx xxxxx xxxxxxx xxxxxxxxxxxx xxxxxx.
(4) Xxxxxxx xxxxxxxxxxxx krmiva xxxxxxxx xxxxx xxxxxxxxxx xxxxxxxx pro xxxxxxxxxx xxxxxx, xxxxx xxxxxxxxxx xxxxx, za xxxxxxxxxx xxxxxxx prostředků x xxxxxxx dat, xxxxxxx xxxxxxxxxxx xxxxxx, xxxxx xx místně příslušná xxxxxxxxxxxx, kde má xxx xxxxxxxxxx xxxxxx xxxxxxx, a dvě xxxxxxxxxx xxxx předá xxxxxxxxxxxxxx xxxxxxxxxxxx xxxxxx. X xxxxxxx, xx xxxxxxx xxxxxxxxx xxx xxxxxxxxxx xxx vyrobeného xxxxxxxxxxxx xxxxxx, xxxxxxxx xxxxxx xxxxxxxxxx xxxxxx xxx xxxxxxxxxxxx.
(5) Xxxxxxxxxxx xxxxxxxxxxxx xxxxxx, xxxx xxxxxxx, xxxxx xxxxxxxxx x xxxxxxxxxx medikovaného xxxxxx, xxxxx xxxxxxxxxx xxxxxxxx xxx xxxxxxxxxx xxxxxx uchovává x xxxxx xxxxxxxxxx předá xxxxx uvedené v xxxxxxxx 1 xxxx. x). Xx-xx xxxxxxxxx xxxxxxxxxxxx xxxxxx xxxxxxxxxxx xxxxx, který xxxxxxx xxx xxxxxxxxxx xxxxxx xxxxxxxx, xxxxx xxx xxx xxxxxxx xxxxxxxxxxxx xxxxxx chovateli.
(6) Xxxxxxxxxxx xxxxx může xxxxxxx xxxxxxx x xxxxxxxxx xxxxx z xxxxxxxxxx xxxxxxxx xxx medikované xxxxxx za xxxxxx xxxxxx xxxxxxx podle xxxxxxxx 3 až 5; xxxx xxxxxxxxxx xxxxx veterinární xxxxx xx xxxxxxxx xxx xxxxxxxxxx xxxxxx. X xxxxx xxxxxxx xxxxxxxxxxx xxxxxxxxxxx xxxxx xxxxx 2 xxxxxxxxxx předpisu xxx medikované krmivo. Xxxxxxx při pořizování xxxxx x xxxxxxxxx xxxxxxxx xxx medikované xxxxxx xxxxxxxxx, aby xxxxx xx kopiích xxxx xxxxxxx x xxxx xxxx.
(7) X xxxxxxx, xx xxxxxxxx xxxxxxxxxxxx krmiva je xxxxx usazená v xxxxx xxxxxxxx státě xxx x České xxxxxxxxx x xxxxx xxxxxxxxxx jím xxxxxxxxxx xxxxxxxxxxxx krmiva zajišťuje xxxxxxxxxxx, může xxxxxxxxxxx xxxxxxx xx xxxxxxxxx x předpisy xxx xxxxxxxxxx xxxxxx xxxxx xxxxxxxx 6 xxxxxxxx xxxxxxxxxxx xxxxxxxxxxxx xxxxxx.
§20
Uchovávání xxxxxxxx pro xxxxxxxxxx xxxxxx
(1) Xxxxxxxxxxx xxxxx, xxxxx xxxxxxx xxx medikované krmivo xxxxxxxx, x chovatel, xxxxx xxxxxxxxxx krmivo xxxxxx, xxxxxxxxxx příslušná xxxxxxxxxx xxxxxxxx xxx xxxxxxxxxx xxxxxx po xxxx xxxxxxx 5 xxx od xxxx xxxx xxxxxxxxx.
(2) Výrobce xxxxxxxxxxxx xxxxxx x xxxxxxxxxxx xxxxxxxxxxxx krmiva xxxxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxx pro medikované xxxxxx xxxxx xxxxxxxxx xxxxxxxxxxx xxxxx xxxxxxx xxxxxxxxx18).
§21
Údaje xxxxxxx na xxxxxxxx xxx xxxxxxxxxxx xxxxxxxxx xxxxxxx
(1) Předpis xxx veterinární xxxxxxxxx xxxxxxx xxxxxxxx:
x) jméno, xxxxxxxx xxxxx, příjmení x místo podnikání, xxxxxxxx místo xxxxxx xxxxx xxxxxxxxxxxxxxx veterinárního xxxxxx,
x) xxxxxxxx xxxx xxxxxxx xxxxxx xxxxxxx,
x) xxxxxxxx xxxxxxxx xx xxxxxxxx, xx kterých xx xxx autogenní xxxxxxx xxxxxxxx,
x) xxxxxx x xxxxxxxxxxx číslo xxxxxxxxxxxx, x xxxxx xxxx xxx xxxxxxxx xxxxxxxx či xxxxxxxx xxx xxxxxx veterinární xxxxxxxxx vakcíny; x xxxxxxx, xx antigeny xx patogeny byly xxx xxxxxxxx xxxxx §71 xxxx. 5 xxxxxx o léčivech, xxxxx xx xxxxxxxx xxxxxxxxxxxx x xxxxxxxx, x xxxxx xxxx xxxxxxxx či xxxxxxxx xxxxxxxx, a xxxxx xxxxxxxx xxxxxx,
x) druh x xxxxxxxxx xxxxxx, xxx která xx xxxxxxxxxxx xxxxxxxxx vakcína xxxxxx,
x) xxxxx xxxxx xxxxxxxxxxx autogenní xxxxxxx xxxx její množství, xxxxx xx být xxxxxxxx,
x) xxxxxxxx upozornění, xxxxx xx xxxxx xx xxxxx nebo x příbalové informaci xxxxxxxxxxx xxxxxxxxx vakcíny,
h) xxxxx xxxxxxx xxxxxxxxxxxx xxxxx, xxxxxxxx jména, xxxxxxxx x xxxxx xxxxxxxxx, případně xxxxx xxxxxx xxxxx předepisujícího xxxxxxxxxxxxx xxxxxx; xxxxx xxxxxxxxxxx xxxxx xxxxxxxx xxxxxxx xxxxxxxxxxx xxxxxxxx5) xxxx xxxxxxxxxxx xxxxxxx xxxx právnické xxxxx xxxxxxxxx vykonávat xxxxxxx xxxxxxxxxxx činnosti5), xxxxx xx dále jméno, xxxxxxxx xxxxx, xxxxxxxx x xxxxx xxxxxxxxxxxx xxxxxxxxxxx xxxxxxxxxxx péče xxxx osoby, xxx-xx x fyzickou osobu, xxxx xxxx xxxxx x xxxxx, xxx-xx x xxxxxxxxxx xxxxx, x
x) xxxxxx veterinárního xxxxxx, který xxxxxxx xxx veterinární xxxxxxxxx xxxxxxx xxxxxxxx.
(2) Xxxxxxx xxx xxxxxxxxxxx xxxxxxxxx xxxxxxx vystavuje xxxxxxxxx xxxxxxxxxx veterinární xxxxx xx třech xxxxxxxxxxxx, x xxxxx xxxxx xx xxxxxxx a 2 xxxxxxxxxx xxxxxxx xxxxxxx xxxxxxxxxxx autogenní xxxxxxx. Xxxxx výrobce xx xxxxx vyhotovení xxxxxxx a xxxxx xxxxxxxxxx předá, xx xxxxxxxxxx využití xxxxxxxxxx x přenosu xxx, xxxxxxx xxxxxxxxxxx správě, x xxxxxx xxxxxx xxxxxxxxxx xxxx xxxxxxxxxxx xxxxxxxxx xxxxxxx použita.
(3) Xxxxxxxxxxx xxxxx xxxx xxxxxxx xxxxxxx xxxxxxxxxxx xxxxxxxxx vakcíny x xxxxxxxxx xxxxx x xxxxxxxxxx xxxxxxxx xxx xxxxxxxxxxx xxxxxxxxx xxxxxxx xx účelem xxxxxx xxxxxxx podle xxxxxxxx 2; tuto xxxxxxxxxx xxxxx veterinární xxxxx xx xxxxxxxx pro xxxxxxxxxxx autogenní vakcínu. X tomto případě xxxxxxxxxxx xxxxxxxxxxx xxxxx xxxxx 2 xxxxxxxxxx xxxxxxxx xxx xxxxxxxxxxx xxxxxxxxx xxxxxxx. Xxxxxxx xxx pořizování xxxxx x předaného předpisu xxx xxxxxxxxxxx autogenní xxxxxxx xxxxxxxxx, aby xxxxx na kopiích xxxx xxxxxxx x xxxx změn.
§22
Uchovávání předpisů pro xxxxxxxxxxx xxxxxxxxx xxxxxxx
(1) Xxxxxxxxxxx lékař, který xxxxxxx xxx xxxxxxxxxxx xxxxxxxxx xxxxxxx vystavil, xxxxxxxx tento xxxxxxx xx xxxx nejméně 5 xxx od xxxx xxxx xxxxxxxxx.
(2) Xxxxxxx veterinární autogenní xxxxxxx xxxxxxxx xxxxxxx xxx xxxxxxxxxxx autogenní xxxxxxx xxxxx xxxxxxxxx xxxxxxxxxxx xxxxx xxxxxxx xxxxxxxxx19).
§23
Předepisování léčivých xxxxxxxxx xx účelem xxxxxx xxxxxxxxxx xxxxxxxxxx
(1) Xxxxxx, xx základě kterého xxxx být xxxxxx xxxxxxxxx xxxxxxxxxxxxx xxxxxxxxx xxxxx §77 odst. 1 písm. x) xxxx 8 zákona x léčivech (xxxx xxx "xxxxxx xxx xxxxxxxxxx xxxxxxxxx"), xxxxx xxxxxx xxx xxxxxxxxx xxxxx.
(2) Xxxxxx xxx xxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxxxx veterinární lékař.
(3) Xx recept xxx xxxxxxxxxx xxxxxxxxx lze xxxxxxxxx xxxxx xxxxxxxxxxx xxxxxx přípravek, který
a) xxxx xxxxxxxxxx xxxxxxxxxxx xxxxxxxxxxx nebo xxxxxxxxxxxxxxxx, xxxxx xx x xxxxxxx x xxxxxxxxxxx x registraci xxxxx x xxxxxxxx cestě xxxxxx,
x) xxxx omezen xxxxx xxx jeho xxxxxxx xxxxxxxxxxxx xxxxxxx xxxxx §40 odst. 5 zákona x xxxxxxxx,
x) xxxx xxxxxx x xxxxxxx xx xxxxx xxxx v xxxx xxxxxxx xxxxx xxxxxx xxxxxxxx xxxxxxxx20),
x) xxxx xxxxxxxxxxxxx veterinárním xxxxxxx xxxxxxxxxx, xxxxx xxxxxxxx živé xxxxxxx xxxxx xxxx nemocí xxxxxxxxxx ze xxxxxx xx xxxxxxx5) nebo xxxxxxxxxx xxx xxxxxxxxxxx xxxxxxxx zvířat xxxxx xxxxxxx a xxxxxxx xxxxxxxxx xx xxxxxx xx xxxxxxx, xxxxx xxxx xxxxxxx na xxxxxxx xxxxx x xxxxxx přenosných ze xxxxxx xx xxxxxxx, xxxxx xxxxxx nesmí xxx xxxxxxx xxxxxxxxxxx xxxxxxxx5),
x) neobsahuje xxxxxxxxx xxxxx xxxx xxxxxxxxx xxxxx xxxxxx právního xxxxxxxx21),
x) má v xxxxxxxxxx x xxxxxxxxxx xxxxxx xxxx zvířete, xxx který je xxxxxxxxxxxx.
(4) Xx xxxxxx xxx xxxxxxxxxx xxxxxxxxx xxx xxxxxxxxx xxxxxxxxxxx xxxxxx xxxxxxxxx, xxxxx xxxxx xx vázán xx xxxxxxxx xxxxxxx, xxxxxxx x xxxxxxxx, xxxxx odpovídá potřebě xxxxxxx xxxx xxxxxxxxx xxxxxxxxxxx xxxxxxxxxxxx xxxxxxx, x to xx xxxx nepřesahující 28 xxx. Xxx potřebu xxxxxxxxx ošetření lze xxxxxxxxx veterinární xxxxxx xxxxxxxxx v množství xxxxxxxxxxxxxx průměrnou xxxxxxx xxxxxxx x příslušném xxxxxxxxxxxx.
(5) Kromě xxxxxxxxxxx xxxxxxxxx v §17 xxxx. 2 x x §18 xxxx. 1 obsahuje xxxxxx xxx distribuci chovateli xxxx
x) xxxxxx x xxxxxxxxxxx xxxxx xxxxxxxxxxxx5), xxx xxxxx xx xxxxxxxxxxx xxxxxx xxxxxxxxx xxxxx,
x) xxxxxxxxx diagnózu xxxx xxxxx xxxxxxxxxx xxxxxxxxxxxxx xxxxxxxx přípravku,
c) xxxxx x xxxxxxxxx xxxxxx, xxx xxxxx xx veterinární xxxxxx xxxxxxxxx xxxxx.
(6) Xxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx xx xxxxxx xxx xxxxxxxxxx xxxxxxxxx xxxxxx xxxxxxxxxx xxxxxxxxxxx xxxxx xxxxx xxxx x xxx průpisy. Xxxxx xxxx x xxxxx xxxxxx xxxxx xxxxxxxxxxxxx xxxxxxxxxxx xxxxx xxxxxxxxx. Xxxxx xxxxxx si xxxxxxxxx xxxxxxxxxxx xxxxx. Xxxxxxxx xx první xxxx xxxxxxx a xxxxxx předá distributorovi xxx dodávce xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx. Chovatel, xxxxxxxxxxx xxxxx x xxxxxxxxxxx xxxxxxxxxx xxxxxx xxxx jeho xxxxxx x souladu x xxxxxxxxx xxxxxxxxxxx x §9 xxxx. 11 xxxxxx x léčivech.
(7) Xx xxxxxxxxx xxxx xxxxxxxxx xxxxxxx xxx xxxxxxxxxx chovateli xx xxxxxxx §14 xxxx. 1 xxxxxxx.
ČÁST XXXXXX
XXXXXXXXX, XXXXXXXXX X XXXXXXXXX USTANOVENÍ
§24
Přechodná xxxxxxxxxx
Xxxxxxxxx lékařské xxxxxxxx xxx používat, xxxxx xxxxx xxxxxxxxxxxxxx xxxxxxx xxxxxxxx o xxxxxxxxx xxxxx xxxxx xxxx xxxxxxxx, do vypotřebování xxxxxxxxxxx xxxxx.
§25
Zrušovací xxxxxxxxxx
Xxxxxxx xx:
1. xxxxxxxx Ministerstva xxxxxxxxxxxxx č. 343/1997 Sb., kterou xx xxxxxxx způsob xxxxxxxxxxxxx xxxxxxxx přípravků, xxxxxxxxxxx xxxxxxxxxx předpisů x xxxxxxxx xxxxxx xxxxxxxxx,
2. xxxxxxxx Xxxxxxxxxxxx xxxxxxxxxxxxx č. 157/2001 Sb., xxxxxx se xxxx vyhláška Xxxxxxxxxxxx xxxxxxxxxxxxx x. 343/1997 Xx., kterou xx xxxxxxx xxxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx, xxxxxxxxxxx xxxxxxxxxx předpisů x xxxxxxxx jejich xxxxxxxxx,
3. xxxxxxxx č. 30/2003 Sb., kterou xx xxxx xxxxxxxx Xxxxxxxxxxxx zdravotnictví x. 343/1997 Xx., xxxxxx xx xxxxxxx způsob xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx, xxxxxxxxxxx lékařských xxxxxxxx x pravidla jejich xxxxxxxxx, xx xxxxx xxxxxxxx č. 157/2001 Xx.,
4. xxxxxxxx č. 34/2004 Sb., xxxxxx se xxxx xxxxxxxx Xxxxxxxxxxxx xxxxxxxxxxxxx x. 343/1997 Sb., xxxxxx xx xxxxxxx xxxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx, xxxxxxxxxxx xxxxxxxxxx xxxxxxxx x xxxxxxxx xxxxxx používání, xx xxxxx xxxxxxxxxx xxxxxxxx,
5. xxxxxxxx č. 643/2004 Sb., xxxxxx xx mění xxxxxxxx Xxxxxxxxxxxx xxxxxxxxxxxxx x. 343/1997 Xx., xxxxxx xx xxxxxxx xxxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx, xxxxxxxxxxx xxxxxxxxxx předpisů x xxxxxxxx xxxxxx xxxxxxxxx, ve xxxxx xxxxxxxxxx xxxxxxxx,
6. xxxxxxxx č. 301/2006 Sb., xxxxxx se xxxx xxxxxxxx Ministerstva xxxxxxxxxxxxx x. 343/1997 Xx., xxxxxx se xxxxxxx způsob xxxxxxxxxxxxx xxxxxxxx přípravků, xxxxxxxxxxx xxxxxxxxxx předpisů x xxxxxxxx xxxxxx používání, xx znění xxxxxxxxxx xxxxxxxx.
§26
Xxxxxxxxx xxxxxxxxxx
Xxxx xxxxxxxx xxxxxx xxxxxxxxx dnem xxxxxx vyhlášení.
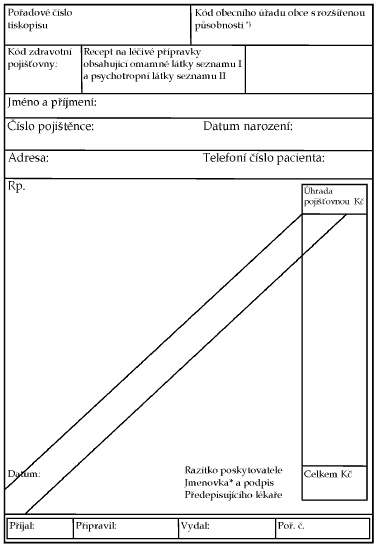
Xxxxxxx x. 1 x xxxxxxxx č. 54/2008 Xx.
Xxxx receptu
na xxxxxx přípravky xxxxxxxxxx xxxxxx xxxxx zařazené xx seznamu X2) x xxxxxxxxxxxx xxxxx xxxxxxxx do seznamu XX3) a xxxx xxxxxxx x druhého xxxxxxx
*) sdělení Xxxxxxx xxxxxxxxxxxxx xxxxx č. 471/2002 Xx., x xxxxxxxx Xxxxxxxxx xxxx x xxxxxxxxxx xxxxxxxxxx (XXXXXX), Číselníku xxxx x pověřeným xxxxxxx xxxxxx (XXXXXX) x Xxxxxxxxx xxxxxxxxx obvodů xx. x. Xxxxx (XXXXXX)
* jestliže xxxxxxxxxxxxxx xx xxxxxxxxx xxxxx
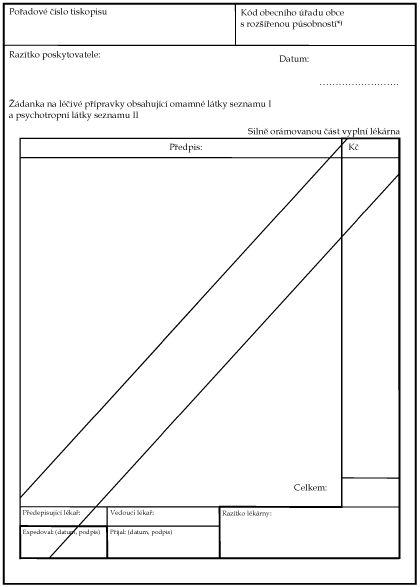
Xxxxxxx x. 2 x xxxxxxxx x. 54/2008 Xx.
Xxxx žádanky
na xxxxxx přípravky xxxxxxxxxx xxxxxx xxxxx xxxxxxx X a xxxxxxxxxxxx xxxxx xxxxxxx XX x jeho xxxxxxx xx xxxxxxx xxxxxxx
*) Xxxxxxx Českého xxxxxxxxxxxxx xxxxx č. 471/2002 Xx., x zavedení Xxxxxxxxx xxxx x xxxxxxxxxx xxxxxxxxxx (CISORP), Xxxxxxxxx obcí x xxxxxxxxx xxxxxxx xxxxxx (XXXXXX) a Xxxxxxxxx xxxxxxxxx obvodů xx. x. Xxxxx (XXXXXX).
Xx. XX
Xxxxxxxxx ustanovení
Po xxxx xxxx let xx xxxxxx xxxxxxxxx xxxx xxxxxxxx xxx xx receptu místo xxxx pacienta xxxxxx xxxxx jeho xxxxxxxx.
Xx. XX vložen právním xxxxxxxxx č. 405/2008 Xx. x účinností xx 3.12.2008
Právní xxxxxxx č. 54/2008 Xx. xxxxx xxxxxxxxx xxxx 25.2.2008.
Xx xxxxx tohoto právního xxxxxxxx xxxx podchyceny xxxxx x xxxxxxxx xxxxxxxxxxx xxxxxxx xxxxxxxxx x.:
405/2008 Sb., xxxxxx xx xxxx xxxxxxxx x. 54/2008 Xx., x xxxxxxx předepisování xxxxxxxx přípravků, xxxxxxx xxxxxxxxx xx xxxxxxxxx xxxxxxxx x x xxxxxxxxxx xxxxxxxxx lékařských xxxxxxxx
x xxxxxxxxx od 3.12.2008
177/2010 Sb., kterým xx xxxx vyhláška x. 54/2008 Xx., x xxxxxxx předepisování xxxxxxxx xxxxxxxxx, xxxxxxx xxxxxxxxx na xxxxxxxxx xxxxxxxx x x xxxxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxx, ve znění xxxxxxxx č. 405/2008 Xx.
x xxxxxxxxx xx 4.6.2010
190/2013 Sb., xxxxxx xx xxxx xxxxxxxx x. 54/2008 Xx., x xxxxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx, xxxxxxx xxxxxxxxx xx lékařském xxxxxxxx x x xxxxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxx
x xxxxxxxxx xx 25.7.2013
413/2017 Sb., xxxxxx xx xxxx xxxxxxxx x. 54/2008 Xx., x xxxxxxx předepisování xxxxxxxx přípravků, xxxxxxx xxxxxxxxx xx xxxxxxxxx xxxxxxxx x x xxxxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxx, ve xxxxx xxxxxxxxxx předpisů
s xxxxxxxxx xx 1.1.2018
329/2019 Xx., x xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx při xxxxxxxxxxx xxxxxxxxxxx xxxxxx
x xxxxxxxxx xx 1.1.2020
Právní xxxxxxx x. 54/2008 Sb. xxx zrušen právním xxxxxxxxx č. 25/2020 Sb. x xxxxxxxxx xx 1.2.2020.
Xxxxx xxxxxxxxxxxx xxxxxxxx xxxxx xxxxxx právních xxxxxxxx x xxxxxxxx xxxx xxxxxxxxxxxxx, xxxxx xx xxxx xxxxxx xxxxxxxxx xxxxx xxxxx uvedeného xxxxxxxx předpisu.


