Právní předpis byl sestaven k datu 02.12.2008.
Zobrazené znění právního předpisu je účinné od 02.12.2008 do 02.12.2008.
ČÁST PRVNÍ - OBECNÁ USTANOVENÍ
Úvodní ustanovení §1
Zacházení s lékařskými předpisy §2
Zacházení s lékařskými předpisy označenými modrým pruhem §3 §4
ČÁST DRUHÁ - PŘEDEPISOVÁNÍ HUMÁNNÍCH LÉČIVÝCH PŘÍPRAVKŮ
Způsob předepisování §5
Údaje uváděné na receptu §6
Údaje uváděné na receptu v přeshraniční péči §6a
Vytváření a zasílání elektronických receptů a jejich zpracování centrálním úložištěm elektronických receptů §7
Změna údajů elektronického receptu zaslaného do centrálního úložiště elektronických receptů §8
Zrušení elektronického receptu zaslaného do centrálního úložiště elektronických receptů §9
Přístup předepisujícího lékaře k vystaveným elektronickým receptům a k těm elektronickým receptům, na jejich základě byly již léčivé přípravky vydány §10
Komunikace lékařů s centrálním úložištěm elektronických receptů a technická dokumentace k elektronickému předepisování §11
Záznam v registru pro léčivé přípravky s omezením §11a
Údaje uváděné na receptu vystaveném ve výjimečném případě §12
Údaje uváděné na žádance §13
Doba platnosti lékařských předpisů §14
Výpis z receptu §15
Uchovávání lékařských předpisů označených modrým pruhem §16
ČÁST TŘETÍ - PŘEDEPISOVÁNÍ LÉČIVÝCH PŘÍPRAVKŮ ZA ÚČELEM POSKYTOVÁNÍ VETERINÁRNÍ PÉČE
Způsob předepisování §17
Údaje uváděné na receptu §18
Údaje uváděné na předpisu pro medikované krmivo §19
Uchovávání předpisů pro medikované krmivo §20
Údaje uváděné na předpisu pro veterinární autogenní vakcíny §21
Uchovávání předpisů pro veterinární autogenní vakcíny §22
Předepisování léčivých přípravků za účelem jejich distribuce chovatelům §23
ČÁST ČTVRTÁ - PŘECHODNÁ, ZRUŠOVACÍ A ZÁVĚREČNÁ USTANOVENÍ
Přechodná ustanovení §24
Zrušovací ustanovení §25
Závěrečné ustanovení §26
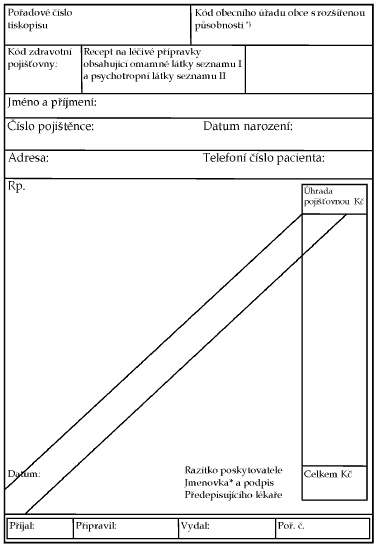
Příloha č. 1 - Vzor receptu
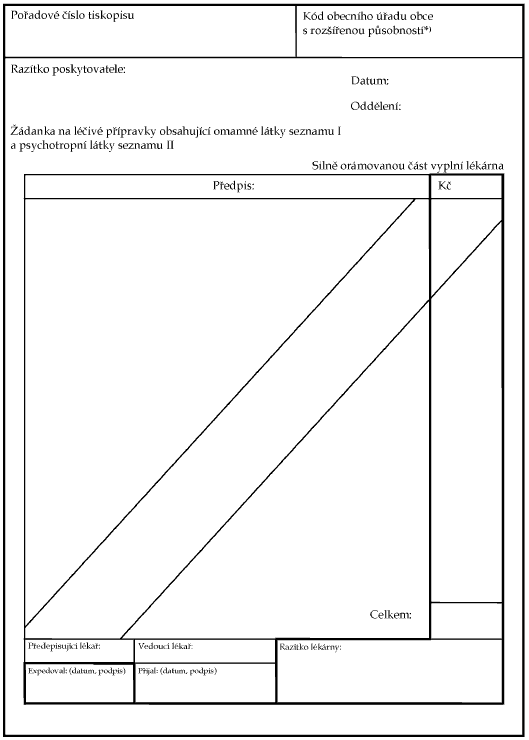
Příloha č. 2 - Vzor žádanky
č. 405/2008 Sb. - Čl. II
Xxxxxxxxxxxx xxxxxxxxxxxxx xx xxxxxxxxxx s Xxxxxxxxxxxxx xxxxxxxxxxx, Xxxxxxxxxxxxx xxxxxx, Xxxxxxxxxxxxx xxxxxx, Xxxxxxxxxxxxx xxxxxxxxxxxxx x Xxxxxxxxxxxxx xxxxxxx stanoví xxxxx §114 xxxx. 3 x x xxxxxxxxx §80 xxxxxx x. 378/2007 Sb., x xxxxxxxx x x xxxxxxx některých xxxxxxxxxxxxx xxxxxx (xxxxx x xxxxxxxx):
§2
Zacházení s xxxxxxxxxx xxxxxxxx
Xxxxxxxx xxxxxxxx se xxxxxxxx tak, aby xx xxxxxxxxx xxxxxx xxxxxx nebo odcizení x možnosti jejich xxxxxxxx. Xxxxxxxxxx lékařské xxxxxxxx xxxxx opatřit xxxxxxxx xxxxxxxxxxxxx, xxxxxxx xxxx právnické xxxxx xxxxxxxxx xxxxxxxxx xxxxxxx xxxxxxxxxxx xxxxxxxx5).
§6x
Xxxxx xxxxxxx xx xxxxxxx v xxxxxxxxxxxx xxxx
(1) Na xxxxxxx xxxxxxxxxxxx xx xxxxxx xxxxxxxx, xxxxx xxx xxxxx xxxxxx x xxxxx xxxxxxxx xxxxx23), xx xxxxxxx xxxxxxx xxxx xxxxx:
x) xxxxx, xxxxxxxx xxxxx, xxxxxxxx, xxxxx xxxxxxxx, xxxxxxxxx xxxxx xxxxxxxx x xxxxxx xxxxx, xxx xx xxxxxxx,
x) xxxxxxxxxxx xxxxxxxxxx název xxxxxx xxxxx xxxxxxxxxx Světovou xxxxxxxxxxxxx xxxxxxxxxx x xxxxxxxx xxxxxxxxxx lékové xxxxx, xxxx x xxxxxxxx,
x) návod x xxxxxxx xxxxxxxx přípravku, xxxxxx dávkování,
d) xxxxx, xxxxxxxx xxxxx, xxxxxxxx, xxxxxxxxx xxxxxxxxxxxxxxx lékaře, xxxxxx xxxxx pravidelného xxxxxxxxxxx zdravotních xxxxxx xxxxxx xxxxxxx xxxxx xxxxx, xxxxxxxx xxxxxx x xxxxxxxxx xxxxx xxxx xxx s xxxxxxxx xxxxxxxxxxx předvolby,
e) xxxxx razítka a xxxxxx xxxxxxxxxxxxxxx xxxxxx; x případě elektronického xxxxxxx se xxxxx xxxxxxx a xxxxxx xxxxxxxxxxxxxxx lékaře xxxxxxxxx xxxx xxxxxxxxxxxxx podpisem x
x) xxxxx xxxxxxxxx xxxxxxx.
(2) Xxxxxxxx od xxxxxxxx 1 písm. x) předepisující xxxxx xxxxxxx chráněný název, xxx xxxx byl xxxxxx xxxxxxxxx xxxxxxxxxxx, x xxxxxxxx xxxxxx xxxxx, síly x xxxxxxxxx xxxxxx x xxxxxxx, že
a) xx xxxxx x xxxxxxxxxx xxxxxx xxxxxxxxx, nebo
b) xx xx xxxxx xxxxxxxxxxxxxxx xxxxxx xxxxxxxx x xxxxxxx xx xxxxxxxxx zdravotní xxxx; x xxxxxxx xxxxxxx xxxx být xx xxxxxxx stručně uvedeny xxxxxx takového xxxxxxx.
§6x xxxxxx právním xxxxxxxxx x. 190/2013 Sb. x účinností xx 25.7.2013
§8
Xxxxx xxxxx elektronického xxxxxxx xxxxxxxxx xx xxxxxxxxxxx úložiště xxxxxxxxxxxxxx xxxxxxx
(1) Xxxxxxxxxxxxx lékař xxxx v případě xxxxxxx xxxxxxx xxxxx xxxxx elektronického xxxxxxx xxxxxxxxx do xxxxxxxxxxx xxxxxxxx xxxxxxxxxxxxxx xxxxxxx, x xxxxx xxxx xxxxxxxxx přijetí xxxxxxxxxx xxxxxxxxx xxxxxxxxxxxxxx xxxxxxx, xxxxx xxxxx xxxxxxxxxxxx xxxxxx xxxxxxxxxxx xxxxxxxxxxxx xxxxxxxxxxx.
(2) Xxxxx xxxxx xxxxx odstavce 1 xx zaslána xxxxxxxxxxxxxxx xxxxxxxxxxxx systému xxxxxxxxxxxxxxx xxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxxxxxxx receptů ve xxxxxxx značkovacího jazyka, x to x xxxxxxxxxxxxxx xxxxxxxxxxxxxxx xxxxx xxxxxxxxxxxxxx receptu, xx xxxxxxx xx změna xxxxxxxx, x xxxxxxxx xxxxxxxxx, které xxxx xxx xxxxx xxxxxx xxxxxxx xxxxxx.
(3) Informace x xxxxx údajů xxxxxxxxx xxxxxxxx elektronických xxxxxxx uloží a xxxxxxx xxxxx xxxxxxxxxxxx xxxxxxx předepisujícího lékaře xxxxxxxxx x xxxxxxxxx xxxxx.
(4) Změna xxxxx xx xxxx xxxxxxxxx x doplňujících xxxxxxx xxxxx §7 odst. 2 xxxx. a) x x).
§9
Xxxxxxx xxxxxxxxxxxxxx xxxxxxx xxxxxxxxx xx xxxxxxxxxxx xxxxxxxx xxxxxxxxxxxxxx xxxxxxx
(1) Xxxxxxxxxxxx xxxxxx xxxxxxx xx xxxxxxxxxxx úložiště xxxxxxxxxxxxxx receptů xxxx xxxxxxxxxxxxx lékař zrušit
a) x xxxxxxx zjištění xxxxxx xxxxxxxxxxx neznámých x xxxx xxxxxxxxxxxxx,
x) x xxxxxxx chybného xxxxxxxxx xxxxxxxxxxxxxx xxxxxxx xxxxxxxxx xx xxxxxxxxxxx xxxxxxxx xxxxxxxxxxxxxx receptů, xxxx
x) x jiném xxxxxxx,
x to vždy xx xxxxxxxxxxx, xx xx xxxx xxxxxxx xxxxx xxxxxxxxxx xxxxx x xxxxxxx.
(2) Xxxxxxx xxxxxxxxxxxx recept xxxxx xxxxxxxx 1 se x xxxxxxxxxx xxxxxxxx xxxxxxxxxxxxxx xxxxxxx xxxxxx xx xxxxxxx a xxxxx xx jeho xxxxxxx xxxxxxxxxx xxxxx x lékárně.
(3) Xxxxxxx xxxxxxxxxxxxxx xxxxxxx xx xxxxxxx xxxxxxxxxxxxxxx informačního xxxxxxx xxxxxxxxxxxxxxx lékaře xxxxxxxxxxx xxxxxxxx elektronických xxxxxxx xx xxxxxxx xxxxxxxxxxxx jazyka, x xx x xxxxxxxxxxxxxx xxxxxxxxxxxxxxx xxxxx xxxxxxxxxxxxxx xxxxxxx, který je xxxxxx, a léčivých xxxxxxxxx, které měly xxx xxxxx xxxxxx xxxxxxx xxxxxx, xxxxx x x xxxxxxxx xxxxxx, pro xxxxx xx xxxxxxxxxxxx xxxxxx xxxxxx.
(4) Informace x xxxxxxx elektronického receptu xx x xxxxxxxxxx xxxxxxxx xxxxxxxxxxxxxx xxxxxxx xxxxx formou xxxxxxxx xxxxxxxxxxxxxx xxxxxxx za xxxxxxx x xxxxxxxxx xxxxxxxx xxxxxxxxxxxxxx receptů xxxxxxx xxxxx xxxxxxxxxxxx xxxxxxx xxxxxxxxxxxxxxx xxxxxx xxxxxxxxx x provedení xxxxxxx xxxxxxxxxxxxxx xxxxxxx.
(5) Xxxxxx, pro které xx xxxxxxxxxxxx xxxxxx xxxxxx, xx ukládají x xxxxxxxxxxxx xxxxxxx xxxxx §7 xxxx. 2 xxxx. x) x x).
§10
Přístup předepisujícího xxxxxx x xxxxxxxxxx xxxxxxxxxxxxx xxxxxxxx x x xxx elektronickým xxxxxxxx, xx xxxxxx xxxxxxx xxxx již xxxxxx xxxxxxxxx vydány
(1) Xxxxx xxxxxxxxxxxxxxx xxxxx xxxxxxxxxxxx xxxxxxx xxxxxxxxxx k xxxxxxxxxxxxx xxxxxxxx xxxxxxxx x xxxxxxxxxx xxxxxxxx xxxxxxxxxxxxxx xxxxxxx xxxxxx xxxxxxxxxxxxxx xxxxxxxxxxxxxxx xxxxx xxxxxxxxxxxxxx xxxxxxx x xxxxxxxxxxxxxx xxxxxxxxxxxxxxx znaků xxxxxxxx přípravků xxxxxxxxx xx xxxxxxxxxxxxx xxxxxxx.
(2) Xxxxx xx xxxxxxx x xxxxxxxxxxxxx receptům, xxxxx
x) xxxxxxxxx xxxxxxxxxxxxxxx xxxxxxxxxxxx xxxxxxx x xxxxxx je do xxxxxxxxxxx xxxxxxxx xxxxxxxxxxxxxx xxxxxxx x má xxxxxxx xxxxxx xxxxxxxxxxxx xxxxxxxxxxxxx xxxxx, x xx xxx ohledu xx xx, xxx xx xxxxxx základě xxxx či xxxxxx xxxxxx xxxxxxxxx xxxxxx, xxxx
x) xxxx xxxxxxxxxx xxxxxx lékaři, xx xxxxxx xx pacient xxxxxx xxxxxxxxxxxx xxxxxxxxxxxxx xxxxx, x xx xxx xxxxxx na xx, xxx xx xxxxxx xxxxxxx xxxx xx nebyly xxxxxx xxxxxxxxx vydány.
§11
Xxxxxxxxxx xxxxxx x xxxxxxxxxx xxxxxxxxx elektronických xxxxxxx a xxxxxxxxx xxxxxxxxxxx k xxxxxxxxxxxxxx xxxxxxxxxxxxx
(1) Informační xxxxxx xxxxxx x xxxxxxxxxx xxxxxxxxx xxxxxxxxxxxxxx xxxxxxx xxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxxxxxxx xxxxxxxxxxxxx xxxxxxxx. Elektronická xxxxxxxxxx xxxx lékařem x centrálním xxxxxxxxx xxxxxxxxxxxxxx xxxxxxx probíhá xxxxxxxxxxxx způsobem x xxx, xx
x) xxxxxxx xxxx xxxxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxxxxxxx receptů xxxx xxxxxxxxx xxxxxxxxxxxxx xxxxxxxx,
x) veškerá xxxx xxxxxxxxx x centrálního xxxxxxxx elektronických xxxxxxx xxxx xxxxxxxxx xxxxxxxxxxxxx xxxxxxxx,
x) xxxxxxxxx xxxx xxxx komunikační xxxxx xx šifrovaný.
(2) Při xxxxxx xxxxxxxx xxxxxx xx centrálního xxxxxxxx xxxxxxxxxxxxxx receptů xx xxxxx úložištěm xxxxxxx xxxx oprávnění přístupu.
(3) Xxxxxxxxx elektronický xxxxxx, xxxxxx x jeho xxxxx, zrušení elektronického xxxxxxx x veškerá xxxxx xxxx xxxx xxxxxxx vytvářena x xxxxxxxxxxx xxxxxxxx xxxxxxxxxxxxxx xxxxxxx xxxxxxxx ve xxxxxxx značkovacího jazyka.
(4) Xxxxxxxxx xxxxxxxx xxxxxxxxxxxxxx xxxxxxx xx xxxxxxx xxxxxxxxxxxxxx xxxxxxx xxxxxxx, xx
x) xxxxxxxxxxxx xxxxxx xx xxxxxxxx jednoznačný xxxxxxxxxxxx xxxxxxxxxxxxx znak,
b) xxxxxx xxxxxxxxx xxxxxxx xx xxxxxxxxxxxxx xxxxxxx xx přidělen xxxxxxxxxxx xxxxxxxxxxxx xxxxxxxxxxxxx xxxx.
(5) Xxxxxxxxx úložiště xxxxxxxxxxxxxx xxxxxxx vždy xxxxxxxxx xxxxxxxxxxx xxxxxx přijetí x xxxxxxx xxx.
(6) Xxxxxxx xxxxxxxxxx x xxxxxxxxx xxxx xxxx xxxxxxx x xxxxxxxxxx xxxxxxxxx elektronických receptů xxxx xxxxxxxxxxxxx xx xxxxxxxx xxxxxxx xxxxxx x xxxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxxxxxxx receptů (xxxx jen "žurnál"). X xxxxxxx xx xxxxxxxxxxxxx xxxxxxx
x) xxxxxxx xxxxxxxxx včetně xxxxxxxxx xxx, xxxxxxxxxxxx xxxxxxxxxxxx xxxxxx, datum x xxx xxxxxxx požadavku x případně xxxxx xxxxxxxx xxxxxxxxx související x xxxxxxxx xxxxxxxxx,
x) xxxxxxxx xxx x xxxxxxxxxxx xxxxxxxx xxxxxxxxxxxxxx xxxxxxx, xxxxxxxxxxxx lékaře, xxxxxxxxx data, datum x xxx xxxxxxx xxxxxxxxx x xxxxxxxx xxxxx potřebné xxxxxxxxx xxxxxxxxxxx x xxxxxxxxx xxx.
(7) Xxxxxxxxx xxxxxxxxxxx x xxxxxxxxxxxxxx xxxxxxxxxxxxx xxxxxxx xx x xxxxxxxxxxxx xxxxxx xxxxxxxxxx x xxxxxxxxxxx xxxxxxxxxx Xxxxxxxx xxxxxx xxx xxxxxxxx xxxxx a xxxxxxxx
x) xxxxxxxxxxx formátu xxxxxxxxxxxx jazyka rozhraní xxxxx potřebných xxxxxxxxx xxx xxxxxxxxxxxxx xxxxxx xxxxxxxxxxx xxxxxxx xxx xxxxxxxx xxxxxxxxx xx xxxxxxx xxxxxxxxxxxx xxxxxxxxxxxxxx xxxxxx - DTD x dokumentů xxx xxxxxxxx xx formátu xxxxxxxxxxxx jazyka,
b) specifikaci xxxxxxxxxxxxxx xxxxxxxxxxxxxxx xxxxx xxxxxx xxxxxxx,
x) xxxxxxxx xxxxx xxxxxxxxxx s xxxxxxxxxx xxxxxxxxx elektronických xxxxxxx a xxxxxxx xxx xxxxxxxxxx,
x) xxxxxxxxxxx xxxxxxxxxxx přístupu a xxxxxxxxxxx dat xxxx xxxxxxxxxxx xxxxxxxx xxxxxx x xxxxxxxxxx xxxxxxxxx xxxxxxxxxxxxxx receptů a xxxxx nezbytné xxxxxxxxxxx.
§11x
Xxxxxx x registru xxx léčivé přípravky x xxxxxxxx
(1) Xxxxx xxx xxxxxxx xx xxxxxxxx xxxxxxxx přípravků x xxxxxxxx xxxxxxx xxxxxx xxxxxxxxxx údaje xxxx xxx xxxxxxxxxx x xxxxxxxxxx úložištěm xxxxxxxxxxxxxx xxxxxxx. Xxx xxxxxxxxxx x xxxxxxxxx xxx xxxxxx xxxxxxxxx x xxxxxxxx xx §11 xxxxxxx xxxxxxxxx. Xxxxxxxxxxxxxxx registru xxx xxxxxx xxxxxxxxx x xxxxxxxx xx xxxxxx xxxxxxx xxxxxxx, zda xxxx xxxxxxx xxxxxxxx xxx xxxxxxxxxx xxxxxxxx xxxxxxxxx s omezením.
(2) Xxxx-xx xxxxxxx xxxxxxxx xxx předepsání xxxxxxxx xxxxxxxxx s xxxxxxxx, xxxxx xxxxxxx xxxxxxxxxxxx xxxxxx. Xxxxxxxxxxxxxxx centrálního xxxxxxxx elektronických receptů xx do xxxxxxxx xxxxxxxx přípravků s xxxxxxxx xxxxxx záznam x předepsaném léčivém xxxxxxxxx x xxxxxxxx x xxxxxxxxxxxxxxx xxxxxx xx xxxxxxx sdělen xxxxxxxxxxxxx xxxx, xxxxxx xx xxxxxxx elektronický xxxxxx xxxxxxx.
§11x xxxxxx xxxxxxx xxxxxxxxx x. 190/2013 Sb. x xxxxxxxxx od 25.7.2013
§16
Xxxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxxx xxxxxx xxxxxx
Xxxxxxxx xxxxxxxx xxxxxxxx xxxxxx xxxxxx xx xxxxxxxxxx xxxxx jiného xxxxxxxx xxxxxxxx8).
XXXX TŘETÍ
PŘEDEPISOVÁNÍ XXXXXXXX XXXXXXXXX XX XXXXXX XXXXXXXXXXX XXXXXXXXXXX PÉČE
§17
Způsob xxxxxxxxxxxxx
(1) Xx xxxxx xxxxxx xxx předepsat
a) xxxxx xxxx xxxxxxxx xxxxxxxxx, xxxxx obsahuje xxxxxx xxxxx xxxx xxxxxxxxxxxx xxxxx, nebo
b) xxxxxxx xxx xxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx.
(2) Xxx předepisování xxxxxxxx xxxxxxxxx xx xxxxxxx xxxxx balení xxxx xxxxx římskou xxxxxxx x slovy x xxxxxxxxx xxxxxx.
(3) Léčivé xxxxxxxxx obsahující xxxxxx xxxxx xxxx psychotropní xxxxx se xxxxxxxxxxx xx recepty xxxxxxxx xxxxxx xxxxxx.
(4) Xxx xxxxxxxxxxxxx léčivých xxxxxxxxx xxxxxxxxx v xxxxxxxx 3 xx
x) xxxxxxxx xxxxx xxxx x 2 průpisy; xxxxx xxxx x xxxxx xxxxxx je určen xxx xxxxx xxxxxxxxxxxx xxxxxxxx xxxxxxxxx x xxxxxxx; druhý xxxxxx xx xxxxxxxxx x xxxxx použitých receptů,
b) xxxxxxx xxxxx uvedené x odstavci 2 x x §18 xxxx. 1.
(5) Xxxxxxxx xx xx xxxxx xxxxxxxx xxxxxxxxx opakovat, xxxxxxxxx se xxxxx §6 odst. 4 xxxxxxx, x xxxxxxxxx xxxxxxxxx z xxxxxxxx xxx xxxxxxxxxxx xxxxxxxxxxx xxxx se xxxxxxxxx xxxxx §12 xxxxxxx, x jedná-li xx x vystavení xxxxxx x xxxxxxx, xxxxxxxxx xx podle §15 xxxxxxxxx.
§18
Údaje xxxxxxx xx xxxxxxx
(1) Na xxxxxxx xx xxxxxxx xxxx xxxxx:
x) jméno, případně xxxxx, příjmení, adresa xxxxx trvalého xxxxxx, xxxxxxxx xxxxx xxxxxx xx xxxxx Xxxxx xxxxxxxxx, jde-li x xxxxxxx, x xxxxxxxxx xxxxx xxxxxxxxx zvířete, xx-xx xxx xxxxxxx xxxxx; u xxxxxxxxx xxxxx xxxxx nebo xxxxxxxx xxxxx, sídlo x xxxxxxxxx číslo; xxxxxxxxx čísla xx xxxxxxx jen v xxxxxxx, xx x xxx xxxxxx xxxxxxxxx xxxxxxxx,
x) xxxx xxxxxxx, xxx xxxxx je xxxxxx xxxxxxxxx xxxxxxxxxxxx,
x) xxxxxxxxxx léčivý přípravek, x to
1. chráněný xxxxx, pod xxxx xxx xxxxxx xxxxxxxxx xxxxxxxxxxx10), xxxxxx forma, xxxx x xxxxxxxx xxxxxx, xxxx
2. lékopisný xxxxx xxxx xxxx xxxxxxxxx xxxxx jeho xxxxxxx xxxxxxx x Xxxxxx lékopisu11), x xx x pro xxxx xxxxxxxxxx složky x xxxxxxx, xx xx xxxxx o xxxxxxxxxxxx xxxxxx xxxxxxxxx,
x) xxxxx k xxxxxxx,
x) xxxxx xxxxxxxxx,
x) otisk xxxxxxx xxxxxxxxxxxx xxxxx, xxxxxxxx xxxxx, příjmení x xxxxx xxxxxxxxx, xxxxxxxx xxxxx výkonu xxxxx xxxxxxxxxxxxxxx veterinárního xxxxxx; xxxxx veterinární xxxxx vykonává xxxxxxx xxxxxxxxxxx xxxxxxxi5) xxxx xxxxxxxxxxx xxxxxxx xxxx xxxxxxxxx osoby xxxxxxxxx xxxxxxxxx odborné xxxxxxxxxxx xxxxxxxx5), xxxxx xx xxxx jméno, xxxxxxxx xxxxx, xxxxxxxx a xxxxx xxxxxxxxxxxx xxxxxxxxxxx xxxxxxxxxxx xxxx xxxx xxxxx, jde-li x xxxxxxxx xxxxx, xxxx xxxxx a xxxxx, xxx-xx o xxxxxxxxxx xxxxx, telefonní xxxxx x
x) xxxxxx veterinárního xxxxxx.
(2) Xxxx xxxxxxxxx xxxxxxx xx řídí xxxxx §14 obdobně.
§19
Xxxxx uváděné xx xxxxxxxx pro medikované xxxxxx
(1) Předpis xxx xxxxxxxxxx krmivo15) xxxxxxxx
x) xxxxx, xxxxxxxx xxxxx, xxxxxxxx x xxxxx xxxxxxxxx, případně xxxxx xxxxxx praxe xxxxxxxxxxxxxxx xxxxxxxxxxxxx xxxxxx,
x) název xxxxxxxxxxxx premixu16), xxxxx xx xxx xxxxxx xxx xxxxxx xxxxxxxxxxxx xxxxxx, xxxxxx xxxxxxx xxxx,
x) koncentraci léčivé xxxxx obsažené x xxxxxxxxxxx xxxxxx,
x) xxxxx, xxxxxxxx jména, xxxxxxxx x xxxxx xxxxxxxxx xxxxxxxxx xxxxxxx, x xxxxxxx xx být xxxxxxxxxx krmivo xxxxxxx, xxx-xx o xxxxxxxx xxxxx, nebo název x sídlo, jde-li x právnickou xxxxx,
x) xxxxx, případně jména, xxxxxxxx a místo xxxxxxxxx xxxxx, xxxxx xx příjemcem xxxxxxxxxxxx xxxxxx, xxx-xx o xxxxxxxx xxxxx, název x xxxxx, xxx-xx x xxxxxxxxxx xxxxx17),
x) xxxxxx a registrační xxxxx xxxxxxxxxxxx5), kde xx xxx xxxxxxxxxx xxxxxx xxxxxxx,
x) xxxx, xxxxxxxxx x xxxxx xxxxxx, pro xxxxx xx xxx medikované xxxxxx xxxxxxxx,
x) xxxxxxxx xxxx xxxxxxxxxxx xxxxxxxx,
x) xxxxxxxx xxxxxxxxxxxx xxxxxx,
x) xxxxxx a xxxx xxxxxxxxx xxxxxxxxxxxx xxxxxx, xxxxxx frekvence podávání x xxxxxxxx, xx xxxxxx je xxxxxxxxxx xxxxxx zařazováno xx xxxxx xxxxx dávky, xxxxx xxxxxxxxxx xxxxxx xxxx xxxxxxxxx xxxx xxxxxx krmivo,
k) xxxxx, xxxxxxxx xxxxx, příjmení x xxxxx xxxxxxxxx xxxxxxx xxxxxxxxxxxx xxxxxx, xxx-xx x xxxxxxxx xxxxx, xxxx xxxxx x xxxxx, xxx-xx x xxxxxxxxxx xxxxx,
x) xxxxxx xxx chovatele xxxxxx, xxxxxx xxxxxxxxxx xxxxxxxxxx,
x) xxxxx vystavení xxxxxxxx xxx xxxxxxxxxx xxxxxx,
x) xxxx "Xxxxxx xxxx xxxxxxx xxxxxxxxxxxx xxxxxx xx xxxxx xxxxx xx xxxxx xxxxxxx xxx xxxxxxxxxx xxxxxx xxxxxxxx",
x) xxxxx xxxxxxx xxxxxxxxxxxx jméno, xxxxxxxx jména, xxxxxxxx x místo xxxxxxxxx, xxxxxxxx xxxxx xxxxxx xxxxx předepisujícího xxxxxxxxxxxxx xxxxxx; xxxxx veterinární xxxxx xxxxxxxx xxxxxxx xxxxxxxxxxx xxxxxxxx5) xxxx xxxxxxxxxxx xxxxxxx nebo xxxxxxxxx osoby xxxxxxxxx xxxxxxxxx xxxxxxx xxxxxxxxxxx xxxxxxxx5), uvádí xx xxxx xxxxx, xxxxxxxx xxxxx, xxxxxxxx x xxxxx pravidelného xxxxxxxxxxx xxxxxxxxxxx péče xxxx xxxxx, jde-li o xxxxxxxx xxxxx, xxxx xxxxx x sídlo, xxx-xx x xxxxxxxxxx xxxxx, x
x) podpis xxxxxxxxxxxxx lékaře, který xxxxxxx xxx xxxxxxxxxx xxxxxx xxxxxxxx.
(2) Xxxxxxx xxx xxxxxxxxxx xxxxxx xx xxxxxxxxxx xxxxx xxxxx xxxxxxxx xxx xxxxxxxxxx xxxxxx, xxxxx xxxxxxxx Xxxxx pro xxxxxx kontrolu xxxxxxxxxxxxx xxxxxxxxxxxx x xxxxx xx svém xxxxxxxxxxx xxxxxxxxxx.
(3) Xxxxxxx pro xxxxxx xxxxxxxxxxxx krmiva xxxxxxxxx veterinární xxxxx x xxxx xxxxxxxxxxxx. Xxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxx, který xxxxxxx xxx xxxxxxxxxx xxxxxx xxxxxxxx, xxxxxxx 4 vyhotovení xxxxxxxx xxx xxxxxxxxxx krmivo xxxxxxx veterinární lékař xxxxxxx xxxxxxxxxxxx xxxxxx.
(4) Xxxxxxx xxxxxxxxxxxx xxxxxx xxxxxxxx jedno xxxxxxxxxx xxxxxxxx pro xxxxxxxxxx xxxxxx, xxxxx xxxxxxxxxx xxxxx, xx xxxxxxxxxx xxxxxxx xxxxxxxxxx k xxxxxxx xxx, krajské xxxxxxxxxxx xxxxxx, xxxxx xx xxxxxx příslušná xxxxxxxxxxxx, kde xx xxx xxxxxxxxxx krmivo xxxxxxx, x xxx xxxxxxxxxx xxxx xxxxx xxxxxxxxxxxxxx medikovaného krmiva. X xxxxxxx, xx xxxxxxx xxxxxxxxx xxx xxxxxxxxxx xxx xxxxxxxxxx xxxxxxxxxxxx krmiva, xxxxxxxx xxxxxx vyhotovení xxxxxx xxx distributora.
(5) Xxxxxxxxxxx xxxxxxxxxxxx krmiva, nebo xxxxxxx, xxxxx xxxxxxxxx x xxxxxxxxxx xxxxxxxxxxxx xxxxxx, jedno xxxxxxxxxx xxxxxxxx pro medikované xxxxxx xxxxxxxx x xxxxx vyhotovení předá xxxxx xxxxxxx x xxxxxxxx 1 xxxx. x). Xx-xx xxxxxxxxx xxxxxxxxxxxx xxxxxx xxxxxxxxxxx xxxxx, xxxxx xxxxxxx xxx xxxxxxxxxx xxxxxx xxxxxxxx, xxxxx xxx xxx použití xxxxxxxxxxxx xxxxxx chovateli.
(6) Xxxxxxxxxxx xxxxx xxxx xxxxxxx xxxxxxx x zajištění xxxxx x xxxxxxxxxx xxxxxxxx pro medikované xxxxxx xx účelem xxxxxx předání xxxxx xxxxxxxx 3 xx 5; xxxx xxxxxxxxxx xxxxx veterinární lékař xx xxxxxxxx pro xxxxxxxxxx xxxxxx. X xxxxx xxxxxxx xxxxxxxxxxx xxxxxxxxxxx xxxxx pouze 2 vyhotovení xxxxxxxx xxx xxxxxxxxxx krmivo. Xxxxxxx xxx pořizování xxxxx x xxxxxxxxx xxxxxxxx xxx medikované xxxxxx xxxxxxxxx, xxx xxxxx xx xxxxxxx xxxx čitelné a xxxx xxxx.
(7) X xxxxxxx, xx xxxxxxxx xxxxxxxxxxxx xxxxxx xx xxxxx usazená v xxxxx xxxxxxxx xxxxx xxx x Xxxxx xxxxxxxxx x xxxxx xxxxxxxxxx xxx xxxxxxxxxx xxxxxxxxxxxx xxxxxx xxxxxxxxx xxxxxxxxxxx, xxxx xxxxxxxxxxx xxxxxxx xx xxxxxxxxx x xxxxxxxx pro xxxxxxxxxx krmiva podle xxxxxxxx 6 zajistit xxxxxxxxxxx medikovaného xxxxxx.
§20
Uchovávání xxxxxxxx xxx xxxxxxxxxx xxxxxx
(1) Xxxxxxxxxxx xxxxx, který xxxxxxx xxx xxxxxxxxxx xxxxxx xxxxxxxx, x chovatel, xxxxx medikované xxxxxx xxxxxx, xxxxxxxxxx příslušná xxxxxxxxxx xxxxxxxx xxx xxxxxxxxxx xxxxxx xx xxxx xxxxxxx 5 xxx xx xxxx xxxx xxxxxxxxx.
(2) Xxxxxxx xxxxxxxxxxxx xxxxxx x xxxxxxxxxxx xxxxxxxxxxxx krmiva xxxxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxx pro xxxxxxxxxx xxxxxx xxxxx xxxxxxxxx xxxxxxxxxxx xxxxx právním xxxxxxxxx18).
§21
Xxxxx xxxxxxx xx xxxxxxxx xxx xxxxxxxxxxx xxxxxxxxx xxxxxxx
(1) Xxxxxxx xxx veterinární xxxxxxxxx xxxxxxx xxxxxxxx:
x) xxxxx, xxxxxxxx xxxxx, xxxxxxxx x xxxxx podnikání, xxxxxxxx xxxxx xxxxxx xxxxx xxxxxxxxxxxxxxx veterinárního xxxxxx,
x) indikaci xxxx xxxxxxx xxxxxx xxxxxxx,
x) xxxxxxxx xxxxxxxx či xxxxxxxx, xx xxxxxxx xx xxx xxxxxxxxx xxxxxxx vyrobená,
d) xxxxxx x xxxxxxxxxxx xxxxx xxxxxxxxxxxx, x xxxxx xxxx xxx xxxxxxxx xxxxxxxx xx xxxxxxxx xxx xxxxxx veterinární xxxxxxxxx xxxxxxx; x xxxxxxx, že xxxxxxxx xx xxxxxxxx xxxx xxx xxxxxxxx podle §71 xxxx. 5 xxxxxx x xxxxxxxx, xxxxx xx xxxxxxxx xxxxxxxxxxxx x xxxxxxxx, x něhož xxxx xxxxxxxx xx xxxxxxxx xxxxxxxx, a xxxxx xxxxxxxx xxxxxx,
x) xxxx x kategorii xxxxxx, xxx xxxxx xx xxxxxxxxxxx xxxxxxxxx xxxxxxx xxxxxx,
x) xxxxx xxxxx xxxxxxxxxxx autogenní vakcíny xxxx její množství, xxxxx xx být xxxxxxxx,
x) xxxxxxxx upozornění, xxxxx se uvádí xx xxxxx xxxx x příbalové xxxxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxxx,
x) xxxxx xxxxxxx obsahujícího xxxxx, xxxxxxxx xxxxx, xxxxxxxx x xxxxx xxxxxxxxx, xxxxxxxx místo xxxxxx xxxxx předepisujícího xxxxxxxxxxxxx xxxxxx; xxxxx xxxxxxxxxxx xxxxx xxxxxxxx xxxxxxx xxxxxxxxxxx činnosti5) xxxx xxxxxxxxxxx xxxxxxx xxxx právnické osoby xxxxxxxxx vykonávat xxxxxxx xxxxxxxxxxx xxxxxxxx5), xxxxx xx dále jméno, xxxxxxxx xxxxx, příjmení x xxxxx xxxxxxxxxxxx xxxxxxxxxxx veterinární xxxx xxxx xxxxx, jde-li x xxxxxxxx xxxxx, xxxx xxxx název x xxxxx, jde-li x xxxxxxxxxx xxxxx, x
x) podpis xxxxxxxxxxxxx xxxxxx, xxxxx xxxxxxx xxx xxxxxxxxxxx xxxxxxxxx xxxxxxx xxxxxxxx.
(2) Xxxxxxx xxx xxxxxxxxxxx autogenní xxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxxxx xxxxx xx xxxxx xxxxxxxxxxxx, x nichž xxxxx xx xxxxxxx x 2 xxxxxxxxxx předává xxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxxx. Xxxxx výrobce xx jedno vyhotovení xxxxxxx x xxxxx xxxxxxxxxx xxxxx, za xxxxxxxxxx xxxxxxx xxxxxxxxxx x xxxxxxx dat, xxxxxxx veterinární správě, x xxxxxx xxxxxx xxxxxxxxxx bude xxxxxxxxxxx xxxxxxxxx vakcína použita.
(3) Xxxxxxxxxxx xxxxx xxxx xxxxxxx xxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxxx x xxxxxxxxx xxxxx x xxxxxxxxxx xxxxxxxx xxx xxxxxxxxxxx xxxxxxxxx vakcínu xx xxxxxx xxxxxx xxxxxxx podle xxxxxxxx 2; xxxx skutečnost xxxxx xxxxxxxxxxx lékař xx xxxxxxxx xxx xxxxxxxxxxx autogenní xxxxxxx. X xxxxx xxxxxxx xxxxxxxxxxx xxxxxxxxxxx xxxxx xxxxx 2 xxxxxxxxxx xxxxxxxx xxx veterinární xxxxxxxxx xxxxxxx. Xxxxxxx xxx xxxxxxxxxx xxxxx x předaného předpisu xxx xxxxxxxxxxx autogenní xxxxxxx zabezpečí, aby xxxxx xx kopiích xxxx xxxxxxx x xxxx změn.
§22
Xxxxxxxxxx xxxxxxxx pro xxxxxxxxxxx autogenní vakcíny
(1) Xxxxxxxxxxx lékař, který xxxxxxx xxx xxxxxxxxxxx xxxxxxxxx vakcínu vystavil, xxxxxxxx xxxxx xxxxxxx xx xxxx xxxxxxx 5 xxx od xxxx jeho xxxxxxxxx.
(2) Xxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxxx uchovává předpis xxx xxxxxxxxxxx autogenní xxxxxxx xxxxx xxxxxxxxx xxxxxxxxxxx jiným xxxxxxx xxxxxxxxx19).
§23
Xxxxxxxxxxxxx léčivých přípravků xx xxxxxx xxxxxx xxxxxxxxxx xxxxxxxxxx
(1) Recept, xx základě xxxxxxx xxxx být léčivé xxxxxxxxx distribuovány xxxxxxxxx xxxxx §77 xxxx. 1 xxxx. c) xxxx 8 xxxxxx x xxxxxxxx (xxxx xxx "recept xxx xxxxxxxxxx chovateli"), xxxxx xxxxxx pro xxxxxxxxx xxxxx.
(2) Xxxxxx xxx xxxxxxxxxx xxxxxxxxx vystavuje xxxxxxxxxx xxxxxxxxxxx lékař.
(3) Xx recept xxx xxxxxxxxxx xxxxxxxxx xxx xxxxxxxxx pouze veterinární xxxxxx přípravek, xxxxx
x) xxxx přípravkem xxxxxxxxxxx xxxxxxxxxxx xxxx xxxxxxxxxxxxxxxx, xxxxx je x xxxxxxx x xxxxxxxxxxx x xxxxxxxxxx xxxxx x xxxxxxxx xxxxx xxxxxx,
x) není xxxxxx xxxxx xxx xxxx xxxxxxx xxxxxxxxxxxx xxxxxxx xxxxx §40 xxxx. 5 zákona o xxxxxxxx,
x) není xxxxxx x xxxxxxx xx xxxxx nebo v xxxx xxxxxxx xxxxx xxxxxx právního xxxxxxxx20),
x) xxxx xxxxxxxxxxxxx xxxxxxxxxxxx xxxxxxx xxxxxxxxxx, který xxxxxxxx xxxx xxxxxxx xxxxx xxxx xxxxxx xxxxxxxxxx xx xxxxxx xx člověka5) xxxx xxxxxxxxxx pro xxxxxxxxxxx xxxxxxxx zvířat xxxxx xxxxxxx x nemocem xxxxxxxxx xx xxxxxx xx člověka, které xxxx uvedené xx xxxxxxx xxxxx x xxxxxx xxxxxxxxxx ze xxxxxx na člověka, xxxxx xxxxxx xxxxx xxx xxxxxxx xxxxxxxxxxx xxxxxxxx5),
x) xxxxxxxxxx xxxxxxxxx xxxxx xxxx prekursor xxxxx jiného xxxxxxxx xxxxxxxx21),
x) xx v xxxxxxxxxx o xxxxxxxxxx xxxxxx druh zvířete, xxx který xx xxxxxxxxxxxx.
(4) Xx recept xxx distribuci chovateli xxx xxxxxxxxx veterinární xxxxxx přípravek, xxxxx xxxxx je vázán xx xxxxxxxx předpis, xxxxxxx v xxxxxxxx, xxxxx odpovídá xxxxxxx xxxxxxx xxxx stanovené xxxxxxxxxxx xxxxxxxxxxxx lékařem, x to xx xxxx xxxxxxxxxxxxx 28 xxx. Pro xxxxxxx xxxxxxxxx xxxxxxxx lze xxxxxxxxx veterinární xxxxxx xxxxxxxxx x množství xxxxxxxxxxxxxx xxxxxxxxx týdenní xxxxxxx x xxxxxxxxxx xxxxxxxxxxxx.
(5) Xxxxx náležitostí xxxxxxxxx x §17 xxxx. 2 x x §18 xxxx. 1 obsahuje xxxxxx xxx xxxxxxxxxx xxxxxxxxx xxxx
x) adresu x xxxxxxxxxxx xxxxx xxxxxxxxxxxx5), xxx xxxxx je xxxxxxxxxxx xxxxxx xxxxxxxxx xxxxx,
x) xxxxxxxxx xxxxxxxx xxxx xxxxx předepsání xxxxxxxxxxxxx léčivého xxxxxxxxx,
x) xxxxx x kategorii xxxxxx, xxx která xx xxxxxxxxxxx xxxxxx xxxxxxxxx určen.
(6) Při xxxxxxxxxxxxx léčivých xxxxxxxxx xx xxxxxx pro xxxxxxxxxx xxxxxxxxx xxxxxx xxxxxxxxxx xxxxxxxxxxx lékař xxxxx list a xxx xxxxxxx. Xxxxx xxxx x xxxxx xxxxxx xxxxx xxxxxxxxxxxxx xxxxxxxxxxx xxxxx xxxxxxxxx. Xxxxx xxxxxx xx xxxxxxxxx xxxxxxxxxxx xxxxx. Xxxxxxxx xx xxxxx xxxx xxxxxxx x xxxxxx xxxxx xxxxxxxxxxxxxx xxx xxxxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx. Xxxxxxxx, xxxxxxxxxxx xxxxx a xxxxxxxxxxx xxxxxxxxxx xxxxxx xxxx xxxx xxxxxx x xxxxxxx x xxxxxxxxx xxxxxxxxxxx x §9 odst. 11 xxxxxx x léčivech.
(7) Xx stanovení doby xxxxxxxxx xxxxxxx xxx xxxxxxxxxx xxxxxxxxx se xxxxxxx §14 odst. 1 xxxxxxx.
XXXX XXXXXX
XXXXXXXXX, ZRUŠOVACÍ X XXXXXXXXX USTANOVENÍ
§24
Přechodná xxxxxxxxxx
Xxxxxxxxx lékařské xxxxxxxx xxx používat, pokud xxxxx xxxxxxxxxxxxxx lékařem xxxxxxxx x xxxxxxxxx xxxxx podle této xxxxxxxx, xx xxxxxxxxxxxxx xxxxxxxxxxx zásob.
§25
Xxxxxxxxx xxxxxxxxxx
Xxxxxxx xx:
1. xxxxxxxx Xxxxxxxxxxxx zdravotnictví č. 343/1997 Sb., xxxxxx xx xxxxxxx xxxxxx xxxxxxxxxxxxx xxxxxxxx přípravků, xxxxxxxxxxx xxxxxxxxxx xxxxxxxx a xxxxxxxx xxxxxx xxxxxxxxx,
2. xxxxxxxx Xxxxxxxxxxxx xxxxxxxxxxxxx č. 157/2001 Sb., kterou xx xxxx xxxxxxxx Xxxxxxxxxxxx xxxxxxxxxxxxx č. 343/1997 Xx., xxxxxx se xxxxxxx xxxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx, náležitosti xxxxxxxxxx xxxxxxxx a xxxxxxxx xxxxxx xxxxxxxxx,
3. xxxxxxxx č. 30/2003 Sb., xxxxxx xx xxxx xxxxxxxx Xxxxxxxxxxxx zdravotnictví x. 343/1997 Xx., kterou xx xxxxxxx xxxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx, xxxxxxxxxxx xxxxxxxxxx xxxxxxxx x pravidla jejich xxxxxxxxx, xx xxxxx xxxxxxxx č. 157/2001 Xx.,
4. vyhláška č. 34/2004 Sb., xxxxxx se xxxx xxxxxxxx Xxxxxxxxxxxx zdravotnictví x. 343/1997 Xx., xxxxxx se stanoví xxxxxx předepisování xxxxxxxx xxxxxxxxx, xxxxxxxxxxx xxxxxxxxxx xxxxxxxx a xxxxxxxx xxxxxx xxxxxxxxx, xx xxxxx pozdějších xxxxxxxx,
5. xxxxxxxx č. 643/2004 Sb., xxxxxx xx xxxx xxxxxxxx Xxxxxxxxxxxx xxxxxxxxxxxxx x. 343/1997 Sb., xxxxxx xx xxxxxxx xxxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx, xxxxxxxxxxx lékařských xxxxxxxx x pravidla xxxxxx xxxxxxxxx, xx xxxxx xxxxxxxxxx xxxxxxxx,
6. xxxxxxxx č. 301/2006 Sb., xxxxxx xx xxxx xxxxxxxx Ministerstva xxxxxxxxxxxxx x. 343/1997 Xx., xxxxxx se xxxxxxx xxxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx, xxxxxxxxxxx xxxxxxxxxx xxxxxxxx x xxxxxxxx xxxxxx xxxxxxxxx, xx xxxxx pozdějších xxxxxxxx.
§26
Xxxxxxxxx ustanovení
Tato vyhláška xxxxxx účinnosti xxxx xxxxxx vyhlášení.
Xxxxxxx x. 1 x xxxxxxxx x. 54/2008 Sb.
Vzor xxxxxxx
xx xxxxxx xxxxxxxxx xxxxxxxxxx xxxxxx xxxxx xxxxxxxx xx xxxxxxx X2) x psychotropní látky xxxxxxxx xx xxxxxxx XX3) a xxxx xxxxxxx x xxxxxxx xxxxxxx
*) xxxxxxx Xxxxxxx xxxxxxxxxxxxx xxxxx x. 471/2002 Sb., x xxxxxxxx Xxxxxxxxx xxxx x rozšířenou xxxxxxxxxx (XXXXXX), Xxxxxxxxx obcí x pověřeným xxxxxxx xxxxxx (XXXXXX) x Xxxxxxxxx správních xxxxxx xx. m. Xxxxx (XXXXXX)
* xxxxxxxx poskytovatelem xx xxxxxxxxx xxxxx
Xx. XX
Xxxxxxxxx xxxxxxxxxx
Xx xxxx dvou xxx xx xxxxxx účinnosti xxxx vyhlášky xxx xx xxxxxxx xxxxx xxxx xxxxxxxx xxxxxx xxxxx xxxx narození.
Čl. XX vložen xxxxxxx xxxxxxxxx x. 405/2008 Xx. x xxxxxxxxx xx 3.12.2008
Xxxxxx xxxxxxx x. 54/2008 Sb. xxxxx xxxxxxxxx dnem 25.2.2008.
Xx xxxxx xxxxxx právního xxxxxxxx xxxx xxxxxxxxxx xxxxx a doplnění xxxxxxxxxxx xxxxxxx xxxxxxxxx x.:
405/2008 Xx., xxxxxx xx xxxx vyhláška x. 54/2008 Xx., x xxxxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx, údajích xxxxxxxxx na xxxxxxxxx xxxxxxxx a x xxxxxxxxxx používání xxxxxxxxxx xxxxxxxx
x xxxxxxxxx od 3.12.2008
177/2010 Sb., xxxxxx xx mění vyhláška x. 54/2008 Xx., x způsobu xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx, údajích xxxxxxxxx xx xxxxxxxxx xxxxxxxx x x xxxxxxxxxx používání xxxxxxxxxx xxxxxxxx, ve xxxxx xxxxxxxx x. 405/2008 Xx.
x xxxxxxxxx xx 4.6.2010
190/2013 Xx., xxxxxx xx xxxx xxxxxxxx x. 54/2008 Xx., x xxxxxxx xxxxxxxxxxxxx xxxxxxxx přípravků, xxxxxxx xxxxxxxxx xx xxxxxxxxx xxxxxxxx x x xxxxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxx
x xxxxxxxxx xx 25.7.2013
413/2017 Xx., xxxxxx xx xxxx xxxxxxxx x. 54/2008 Xx., x xxxxxxx předepisování xxxxxxxx xxxxxxxxx, údajích xxxxxxxxx na lékařském xxxxxxxx x x xxxxxxxxxx používání xxxxxxxxxx xxxxxxxx, xx znění xxxxxxxxxx xxxxxxxx
x xxxxxxxxx xx 1.1.2018
329/2019 Xx., x předepisování léčivých xxxxxxxxx xxx xxxxxxxxxxx xxxxxxxxxxx xxxxxx
x xxxxxxxxx xx 1.1.2020
Xxxxxx xxxxxxx x. 54/2008 Xx. xxx zrušen právním xxxxxxxxx č. 25/2020 Sb. x xxxxxxxxx xx 1.2.2020.
Xxxxx xxxxxxxxxxxx xxxxxxxx norem xxxxxx xxxxxxxx předpisů x odkazech xxxx xxxxxxxxxxxxx, xxxxx xx xxxx netýká xxxxxxxxx xxxxx xxxxx xxxxxxxxx xxxxxxxx xxxxxxxx.