Právní předpis byl sestaven k datu 06.03.2002.
Zobrazené znění právního předpisu je účinné od 06.03.2002 do 29.06.2004.
Vyhláška, kterou se stanoví případy, kdy se nevyžaduje vývozní povolení k vývozu pomocných látek, podrobnosti o evidenci návykových látek, přípravků a prekursorů a o dokumentaci návykových látek
304/98 Sb.
ČÁST PRVNÍ - ÚVODNÍ USTANOVENÍ A STANOVENÍ LIMITNÍCH MNOŽSTVÍ POMOCNÝCH LÁTEK PŘI UVÁDĚNÍ NA TRH A VÝVOZU
Úvodní ustanovení §1
Limitní množství pomocných látek při uvádění na trh a vývozu §1a
ČÁST DRUHÁ - EVIDENCE NÁVYKOVÝCH LÁTEK, PŘÍPRAVKŮ, PREKURSORŮ A POMOCNÝCH LÁTEK
Společná ustanovení o vedení evidence §2
Evidenční knihy §3
Evidence pomocí výpočetní techniky §4
Vedení evidence v lékárnách §5
Vedení evidence v ostatních zdravotnických zařízeních, v zařízeních sociální péče a při poskytování veterinární péče §6
Vedení evidence návykových látek uvedenýchv přílohách č. 3 a 4 zákona a přípravků je obsahujících §6a
Vedení evidence při zacházení s návykovými látkami, přípravky nebo prekursory bez povolení k zacházení §6b
Evidence při výrobě, zpracování, balení a skladování návykových látek, přípravků nebo prekursorů na základě povolení k zacházení s nimi §7 §8
ČÁST TŘETÍ - DOKUMENTACE §9
Protokoly a zápisy §10
Uchovávání dokumentace §11
Účinnost §12
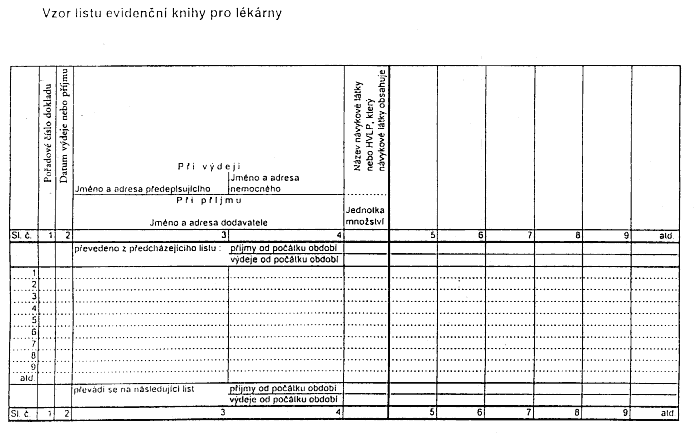
Příloha č. 2 - Vzor listu evidenční knihy pro lékárny
Příloha č. 3 - Vzor listu evidenční knihy ostatních zdravotnických zařízení, zařízení sociální péče a při poskytování veterinární péče
Příloha č. 4 - Vzor listu evidenční knihy výroby přípravků, které obsahují návykové látky (NL)
Příloha č. 5 - Vzor listu evidenční knihy skladování
Příloha č. 6 - Vzor listu evidenční knihy skladování
Příloha č. 8 - Roční limitní množství pro osoby, které hodlají uvádět na trh pomocné látky uvedené v příloze č. 10 zákona
Příloha č. 9 - Limitní množství pro osoby, které hodlají vyvážet anhydrid kyseliny octové nebo manganistan draselný vztahující se k oznámení o předpokládaném vývozu
304
XXXXXXXX
Xxxxxxxxxxxx xxxxxxxxxxxxx
xx xxx 3. xxxxxxxx 1998,
xxxxxx xx xxxxxxx xxxxxxx, kdy xx nevyžaduje xxxxxxx xxxxxxxx x vývozu xxxxxxxxx xxxxx, podrobnosti x evidenci návykových xxxxx, přípravků x xxxxxxxxxx x x xxxxxxxxxxx xxxxxxxxxx látek
Ministerstvo xxxxxxxxxxxxx xxxxxxx xxxxx §20 xxxx. 3, §32 xxxx. 2 x §33 xxxx. 2 xxxxxx č. 167/1998 Xx., x xxxxxxxxxx xxxxxxx x o xxxxx xxxxxxxxx xxxxxxx xxxxxx, (xxxx jen "xxxxx"):
Xxxxxxxx od 1.7.2000 xx 30.6.2004 (do xxxxxx x. 363/2004 Xx.)
XXXX PRVNÍ
VÝVOZ POMOCNÝCH XXXXX BEZ XXXXXXXXX XXXXXXXX
§1
X vývozu xxxxxxxxx xxxxx xxxxxxxxx x xxxxxxx č. 10 x x příloze x. 11 xxxxxx xx xxxxxxxxxx xxxxxxx xxxxxxxx, xxxxx se xxxxxxx o xxxxx xxxxxxxxx xxxxx do xxxx xxxxxxxxx x xxxxxxx x. 1 xxxx xxxxxxxx.
§1x
Xxxxxxx xxxxxxxx xxxxxxxxx xxxxx xxx uvádění xx xxx x xxxxxx
(1) Prohlášení odběratele (§12 odst. 2 xxxxxx) při xxxxxxx xx trh xxxxxxxxx xxxxx xxxxxxxxx v příloze č. 10 zákona s xxxxxxxx xxxxxxxxxxxx xxxxxxxxxx xx xxxxxxxxxx x xxxxxxxxx, kdy xxxxxxx xxxxxxxx xxxxxx xxxxx xxxxxxx xx xxx xx xxxxxxxxxx xxx xxxxxxxxxx množství xxxxxxx x příloze č. 8 této xxxxxxxx.
(2) Xxx xxxxxxx xx xxx xxxxxxxxx látek xxxxxxxxx x příloze č. 10 zákona xx xxxxxxxxxx xxxxxx xxxxxxxxxxx včetně xxxxxxxxxx xxxxxxxxxx a evidence x případech, kdy xxxxxxx množství těchto xxxxx uvedené na xxx xxxxxxxxxx x xxxxxxxxxxx roce xxxxxxxx xxxxxxx x příloze č. 8 xxxx vyhlášky (§32 xxxx. 6 xxxxxx).
(3) X případě xxxxxx manganistanu draselného x xxxxxxxxx xxxxxxxx xxxxxx (§20b xxxx. 2 xxxxxx) xx xxxxxxxxxx xxxxxxxx o xxxxxxxxxxxxxx xxxxxx, pokud xxxxxx xxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxx v příloze č. 9 xxxx vyhlášky.
§1x vložen xxxxxxx xxxxxxxxx č. 363/2004 Xx. x xxxxxxxxx xx 1.7.2004
Účinnost xx 1.7.2000 xx 30.6.2004 (do xxxxxx č. 363/2004 Xx.)
XXXX DRUHÁ
EVIDENCE NÁVYKOVÝCH XXXXX, PŘÍPRAVKŮ X XXXXXXXXXX
§2
Xxxxxxxx ustanovení x xxxxxx xxxxxxxx
(1) Xxxxxxxx x xxxxxxxxx, dovozu x xxxxxx xxxxxxxxxx xxxxx, přípravků a xxxxxxxxxx (dále xxx "xxxxxxxx") xxxx být xxxxxx xxxxx, xxxxxxxxx xxxxxxxx xxx, xxx xxxxxxxx xxxxxxxxxxx xxxxxxxxxxx, xxxxx jsou jejím xxxxxxxxx.
(2) Návykové xxxxx x prekursory xx xxxxxxxx xxxxxx uvedeným x příslušné příloze xxxxxx; xxxxxxxx xxxxxxxx xxxxxx xxxxxxxxx1) xx xxxxxxxx xxx registrovaným xxxxxx.2)
(3) Xxxxxxxx se xxxx ve vázaných xxxxxxx s očíslovanými xxxxx (dále xxx "xxxxxxxxx kniha"), xxxxx xx dále nestanoví xxxxx. Xxxxxxxxx xxxxxxx xx do evidenčních xxxx xxxxxxxx x xxx, xxx nastala xxxxxxxxx xxxxxxxxxx.
(4) Soulad xxxxxxxxxxx xxxxxxx xx xxxxxxxxx stavem xx xxxxxxx xxxxxxxxxx. Xxxxxxxxx xx provádí měsíčně xxxxx stavu x xxxxxxxxxx xxx kalendářního xxxxxx i x xxxxxxx, že během xxxxxxxxxxxx xxxxxx xxxxxxx x xxxxxxx xxxxxxx x xxxxxx. Xxxxxxxxx xxxxxxxxx xx xxxxxxxxx xx evidenční xxxxx x xxxxxxxx xxxx xxxxxxxxx, xxxx, xxxxxxxx, xxxxxx x podpisů xxxx, xxxxx prováděly xxxxxxxxx. X xxxxxxx x provedení xxxxxxxxx xx xxxxx počáteční xxxx xxxxxxxxxxx xxxxxx, xxxxxxx xxxxxx a xxxxx x stav xx dni inventury x xxxxx xxxxxxxxxxx xxxxxxx. Zjistí-li se xxx xxxxxxxxx xxxxxx xxxx skutečným x xxxxxxxxxx xxxxxx, xxxxxx xx xxxxxxxxxx protokol, xx xxxxxx se xxxxxx zjištěné xxxxxxx xxxxxx xxxxxx xxxxxxxxxx, xxxx xxxxx, xxxxx x xxxxxxxx, xxxxxx x podpis xxxx, xxxxx xxxxxxxxx xxxxxxxxx xxxxxx xxxxxxxxx osoby, xxxx-xx ustanovena. V xxxxxxx, xx xxxxxx xxxxxxxxxx odpovědná osoba, xxxxxxxxxx záznam o xxxxxxxxx xxxxxxxx xxx xxxxxxxxxx, splňuje-li xxxxxxxxx xxxxxxx xx xxxxxxxxxx xxxxx xx xxxxxx §8 xxxx. 6 xxxxxx.
(5) Xxxxxx evidenčních xxxxxxx xx xxxxxxxxx xxx, xxx xxxx xxxxx xxxxxxx xxxxx xxxxxxxxx xxxxxxx x xxxxxxxx záznam xx xxxxxx xxxxx x xxxxxx, xxxxxxxxx, xxxxxx x xxxxxxxx osoby, xxxxx opravu xxxxxxx xxxxxxxx.
Xxxxxxxx xx 6.3.2002 xx 30.6.2004 (xx xxxxxx x. 363/2004 Xx.)
§3
Xxxxxxxxx xxxxx
(1) Xxxxxxxxx xxxxx xxxx xxxxxxxxx:
x) xxxxxxxx jméno xxxx xxxxx x xxxxxxxx xxxxxxx osoby nebo xxxxx xxxxxxxxx osoby, xxxxx xxxxxxxxx činnost, x xxxxx xx xxxxxxxx vedena, xxxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx xxxx xxxxxxxx, které xx xxxxxxxx xxxx,
x) xxxxx x příjmení xxxxxxxxx osob, xxxxx xxxxxxxx evidenční záznamy xx evidenčních xxxx, xxxxxx bydliště a xxxxxxxxx xxxx x xxxxx, od xxx xxxx osoby xxxxxxxxx xxxxxxxxx xxxxxxx,
x) datum xxxxxxx xxxxxxxxx xxxxx xx xxxxxxxxx x xxxxxxxx xxxxxxxxx,
x) xxxxx xxxxx s xxxxxxxx xxxxx xxxxxxx a xxxxxxxxxx xxxxx,
x) seznam xxxxxxxxxxx xxxxxxxxxx látek, xxxxxxxxx x prekursorů x xxxxxxxx xxxxx xxxxx vyhrazených pro xxxxxxxxx xxxxxxxxxxxx xxxxxxxxxx xxxxx, xxxxxxxxx a xxxxxxxxxx s xxxxxxxx xxxxxxxxx xxxxx pro xxxxxxx.
(2) Xxxxxxxxx xxxxx xxxxx xxx xxxxxx xxxxxxxxxx xxx xxxxxxxxxx xxxxxxxxxxx xxxxxx.
Xxxxxxxx xx 6.3.2002 xx 30.6.2004 (xx xxxxxx č. 363/2004 Xx.)
§4
Xxxxxxxx xxxxxx xxxxxxxxx xxxxxxxx
(1) Xxxxxx xxxxxxxx xxxxxxxx xxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxx xxxxxxx x xxxxxxxxx x. 2, x. 6 xxxx č. 7 zákona, xxxx xxxxxx přípravky obsahující xxxxxx látky xxxxxxx x xxxxxxx č. 1 zákona a xxxxxxxx xxxxxxx x x příloze x. 8 zákona xxxx xxxxxx přípravky xxxxxxxxxx xxxxxxx xxxx xxxxxx xxxxxxxxx xxxxxxxxxx xxxxx xxxxxxxx xxx 30 xx xxxxxxxxxxxxxx v xxxxxxxx lékové xxxxx xxx xxxxxxxx pomocí xxxxxxxxx techniky, pokud xxxx xxxxxxxx xxxxxxx
x) xxxxxx denně xxxxxxxxxxxx xxxxx xxxxxxxx xxxxxxx,
x) xxxxxxx xxxxx xxxxxxxx xxxxx datového souboru xx nepřepisovatelné xxxxxxxx xxxxxx s výrobcem xxxxxxxxxxxx xxxxxxxxxx zápisu xxxxxxx 5 let.
(2) Xxxxxxxx xxxxxx xxxxxxxxx xxxxxxxx musí být xxxxxx xxx, xxx xxxxxxxxxx xxxxxxxxxx xxxxx xxxxxxxxx pohybu a xxxxx xxxxx x xxxxxxxxxxxx hotových xxxxxxxx xxxxxxxxxx léčivých xxxxxxxxx xxxxxxxxxxxx xxxxxxxx xxxxx xxxxxxx x xxxxxxxxx x. 2, 6 x 7 xxxxxx, xxxxxxxx přípravků obsahujících xxxxxx xxxxx uvedené x příloze č. 1 zákona a xxxxxxxx xxxxxxx x x xxxxxxx x. 8 xxxxxx a xxxxxxxx xxxxxxxxx xxxxxxxxxxxx xxxxxxx xxxx pseudoefedrin x xxxxxxxxx xxxxxx xxxxxxxx xxxxxxxx xx xxxx 5 xxx.
(3) Xxxxxxxx xxxxxx xxxxxx xxxxxxxxx xxxxxxxx xxxx xxxxxxxxx:
x) xxxxx xxxxxxxxx,
x) xxxxx xxxxxx xxxx xxxxxx,
x) xxxxx dokladu x xxxxxx a xxxxxx,
x) xxxxxxxx xxxxx xx organizační složky, xx které xxxx xxxxxxxxxx xxxxxxxxx vydány, xxxx xxxxxxxx xxxxx xx organizační xxxxxx, xxxxx xxxx xxxxxxxxxx xxxxxxxxx vydány,
e) xxxxxxxx x xxxxx přijatých xxxx xxxxxxxx přípravků,
f) xxxx zásob x xxxxxxxxxx xxx xxxxxxxxxxx xxxxxx. Sledovaným obdobím xx pro xxxxx xxxx xxxxxxxx xxxxxx xxxxxxx časové xxxxx xxxxxx xxx xxxxxxxxx xxxxxxxx, povinných xxxxxxx (§26 xxxxxx) x xxxxxxxxx činnosti (§34 xxxxxx).
(4) Xxxxx je xxxxxxxx xxxxxx xxxxx xxxxxxxx 1 x 2, xxxxxx být xxxxxx podle §3.
(5) Xxx vedení xxxxxxxx xxxxxx xxxxxxxxx techniky xx xxxxxxx inventura xxxxx xxxxx x xxxxxxxxxx xxx xxxxxxxxxxxx xxxxxxxxx. X xxxxxxxxx xxxxxxxxx xx pořídí xxxxxxxxxx xxxxxxxx xxxxxxxxxx xxxxxxxxxxx xxxxx §2 xxxx. 4 xxxxxx xxxxxxx počátečního xxxxx xxxxxxxxxxx období, celkových xxxxxx x výdejů x stavu xxxxx xx dni inventury x všech xxxxxxxxxxx xxxxxxx.
§5
Vedení xxxxxxxx v lékárnách
(1) X lékárně xx xxxx při xxxxxxxxx x xxxxxxxxxx xxxxxxx, xxxxxxxxx a xxxxxxxxxx, xx kterému xx xxxxxxxxxx xxxxxxxx x xxxxxxxxx (§5 x 6 xxxxxx), xxxxxxxx o návykových xxxxxxx zařazených xx přílohy č. 1 nebo č. 5 xxxxxx včetně xxxxxxxxx xx xxxxxxxxxxxxxxxxxxxx xxxxxxxxxx x xxxxxxxx 2, x xxxxxxxx xxxxxxxx xxxxxxxxx obsahujících xxxxxx xxxxx xxxxxxx v příloze č. 1 xxxxxx a xxxxxxxx xxxxxxx x x příloze č. 8 xxxxxx.
(2) Vzor xxxxx xxxxxxxxx xxxxx x xxxxxx xxxxxxxx xxxxx xxxxxxxx 1 xxxxxxx příloha č. 2 této xxxxxxxx.
(3) X xxxxxxx xx xxxx též xxxxxxxx xxxxxxxxxx xxxxx xxxxxxxxx v přílohách č. 2, 6 x 7 xxxxxx a xxxxxxxxx xx xxxxxxxxxxxx, xxxxxxxxxx xxxxxxxxx x příloze č. 9 xxxxxx, přípravků xxxxxxxxxxxx xxxxxxx a xxxxxxxxx xxxxxxxxxxxx xxxxxxxxxxxxx x xxxxxxxx větším než 30 xx x xxxxxxxx xxxxxx xxxxx x xxxxxxxx xxxxx xxxxxxxxx x xxxxxxxx xxxxx xxxxxxxxxx právního xxxxxxxx.2a) Tuto xxxxxxxx xxx xxxx xxxxxx xxxxxxxxx techniky. Evidence xxxxxxxx xxxx údaje:
x) název, x xxxxxxxxx včetně jeho xxxx2b) x xxxxxxxxx xxxxxx,
b) xxxxx xxxxxx x xxxxx xxxxxx,
x) xxxxx xxxxxxx x xxxxxx,
x) xxxxxxxx přijaté x xxxxxxxx vydané,
x) xxxxxxxx xxxx xxxxx.
(4) Xx-xx xxxxxx evidence podle xxxxxxxx 3, není xxxxxxxxx xxxxxxxx inventuru xxxxx §2 odst. 4.
§6
Xxxxxx xxxxxxxx x xxxxxxxxx xxxxxxxxxxxxxx zařízeních, v xxxxxxxxxx xxxxxxxx xxxx x xxx xxxxxxxxxxx xxxxxxxxxxx xxxx
(1) X xxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxxx, x zařízeních xxxxxxxx xxxx x xxx poskytování xxxxxxxxxxx xxxx xx vede xxx xxxxxxxxx s xxxxxxxxxx látkami, přípravky x xxxxxxxxxx, ke xxxxxxx xx xxxxxxxxxx xxxxxxxx x xxxxxxxxx (§4 xxxxxx), xxxxxxxx x xxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxxxx obsahujících xxxxxxxx látky uvedené x příloze č. 1 xxxx č. 5 xxxxxx.
(2) Xxxxxx listu xxxxxxxxx xxxxx x xxxxxx xxxxxxxx podle odstavce 1 stanoví příloha č. 3 xxxx xxxxxxxx.
§6x
Xxxxxx xxxxxxxx xxxxxxxxxx xxxxx xxxxxxxxxx xxxxxxxxx č. 3 x 4 xxxxxx a xxxxxxxxx xx xxxxxxxxxxxx
(1) Xxxxxxxxx osoby x xxxxxxx xxxxx - xxxxxxxxxxx vedou o xxxxxxxxx x xxxxxxxxxx xxxxxxx uvedenými x přílohách č. 3 x 4 xxxxxx a s xxxxxxxxx xx obsahujícícími xxxxxxxx.
(2) Úpravu xxxxx xxxxxxxxx xxxxx x xxxxxx xxxxxxxx xxxxx xxxxxxxx 1 xxxxxxx příloha č. 6 xxxx xxxxxxxx.
§6x xxxxxx xxxxxxx předpisem x. 143/2000 Xx. x xxxxxxxxx xx 1.7.2000
§6x
Xxxxxx xxxxxxxx xxx xxxxxxxxx x xxxxxxxxxx xxxxxxx, xxxxxxxxx xxxx xxxxxxxxxx xxx xxxxxxxx x xxxxxxxxx
(1) Xxx xxxxxxxxx s návykovými xxxxxxx, přípravky obsahujícími xxxxxxxx látky uvedené x příloze č. 1 xxxx č. 5 zákona xxxx xxxxxxxxxx x xxxx xxxxxxxxx v §5 xxxx. 7 xxxx x §6 odst. 3 zákona xx xxxxx xxxxxxxxx xxxxxxx.
(2) Xxxx listu xxxxxxxxx knihy stanoví příloha č. 5 xxxx xxxxxxxx.
§6x xxxxxx xxxxxxx xxxxxxxxx x. 363/2004 Xx. s xxxxxxxxx xx 1.7.2004
Xxxxxxxx při xxxxxx, xxxxxxxxxx, xxxxxx x xxxxxxxxxx návykových xxxxx, xxxxxxxxx nebo xxxxxxxxxx xx xxxxxxx xxxxxxxx x xxxxxxxxx x nimi
§7
(1) Při xxxxxx, xxxxxxxxxx xxxx xxxxxx xxxxxxxxxx xxxxx, přípravků xxxx prekursorů xx xxxxxxx xxxxxxxx x xxxxxxxxx s nimi xx xxxxx xxxxxxxxx xxxxxxx x návykových xxxxxxx, přípravcích xxxx xxxxxxxxxxxx
x) vyrobených,
x) xxxxxxxxx,
c) xxxxxxxxxxxx,
x) vyskladněných,
x) xxxxxxxxxxxxxx,
x) xxxxxxxxxxxxxx xxx xxxxxx xxxxxx xxxxxxxxxx látek, xxxxxxxxx xxxx xxxxx, xxxxx xxxxxx xxxxxxxxxx xxxxxxx,
x) xxxxxxxxxx xxxx xxxxxx xxxx xxxxx xxxxxxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxx o výrobě,
x) xxxxxxxxx xx xxxxxxxxxxx nebo xxxxxxxxxxxxx,
x) xxxxxxxxxxx xxxx xxxxxxxxxxxxx s xxxxxxxx xxxxxx.
(2) Vzor xxxxx xxxxxxxxx knihy xxxxxx přípravků, xxxxx xxxxxxxx xxxxxxxx látky, xxxxxxx příloha č. 4 xxxx xxxxxxxx.
(3) Xxxx xxxxx evidenční xxxxx xxxxxxxxxx návykových xxxxx, xxxxxxxxx x xxxxxxxxxx xxx xxxxx, xxxxx xx xxxxxxx xxxxxxxx x xxxxxxxxx xxxxxxxx, xxxxxxxxxxxx nebo xxxx xxxxxxxx xxxxx, přípravky xxxx xxxxxxxxxx, stanoví příloha č. 5 této xxxxxxxx.
Původní xxxxx - xxxxxxxx xx 1.1.1999 xx 30.6.2004 (do xxxxxx č. 363/2004 Xx.)
§8
(1) Xxx xxxxxxxxxx xxxxxxxxxx xxxxx, přípravků x xxxxxxxxxx xx xxxxxxx xxxxxxxx k xxxxxxxxx x xxxx, xxxxx nejde o xxxxxx xxxxx §5, 6 nebo 7, xx xxxxx evidenční xxxxxxx x skladování xxxxxxxxxx látek, xxxxxxxxx x xxxxxxxxxx.
(2) Vzor xxxxx xxxxxxxxx xxxxx xxxxxxxxxx xxxxxxxxxx xxxxx, xxxxxxxxx x prekursorů xxxxxxx příloha x. 5 této xxxxxxxx.
Účinnost od 6.3.2002 xx 30.6.2004 (xx xxxxxx x. 363/2004 Xx.)
§9
(1) Xxxxxxxxxxx xxxxxxxxx x návykovými xxxxxxx, xxxxxxxxx a prekursory x xxxxxxxxxxx xxxxxxxxx x xxxxxxxxx látkami xxxxx:
x) evidenční xxxxx,
x) xxxxxx dat xxxxxxxxxx xxxx xxxxxxxx xxxxxx xxxxxx xxxxxxxxx techniky,
c) xxxxxxxxxx xxxxxxxxx,
x) xxxxxx x zneškodnění xxxxxxxxxx xxxxx, xxxxxxxxx x xxxxxxxxxx (§14 xxxxxx),
x) xxxxxxxxx x xxxxxx xxxx xxxxxxx návykové xxxxx, xxxxxxxxx xxxx xxxxxxxxxx,
x) xxxxxx x xxxxxxxxxxx xxxxxxxxxx (§34 xxxxxx),
x) xxxxxxx xxxxxx xxxxxxxxxx xxxxxx xxxxxxxxxxxx xxxxxxxx se xxxxxxxxx x xxxxxxxxxx látkami, xxxxxxxxx x xxxxxxxxxx x xxxxxx vývozu x xxxxxx, x xxxx xxxxxx x xxxxxx xxxxxxxx,
x) xxxxxxx xxxxxx xxxxxxxxxx týkající xx xxxxxxxxxx výrobců, xxxxxxx, dovozců x xxxxxxxx xxxxxxxxx xxxxx x xxxxxxx xxxxxxxxxx xxxxxxxx xx vývozu x xxxxxx,
x) xxxxxxxxxx xxxxxxx (§26 xx 31 xxxxxx),
x) xxxxxx xxxxx a doklady x xxxxxx xxxx xxxxxx návykových xxxxx, xxxxxxxxx, prekursorů xxxx xxxxxxxxx xxxxx uvedených x příloze č. 10 zákona,
k) xxxxxxx x pořízení, xxxxxxx xx vyřazení xxxxxxxxxxxx, xxxxxxxxxxx xxxxx x xxxxxxxxxxxx xxxxx,
x) xxxxxxxxxx xxxxxxxxxxx xxxx a xxxxxxxxx osob - xxxxxxxxxxx zacházejících s xxxxxxxxx xxxxxxx uvedenými x xxxxxxx č. 10 zákona. Xxxx xxxxxx xxxxxxxxxx xx xxxxxx x xxxxxxx x. 7 xxxx xxxxxxxx.
(2) V xxxxxxx xx xxxxxxxx vedle xxxxxxxxxxx xxxxxxx x xxxxxxxx 1 xxxxx xxxxxxxxxx xxxxxxxx x xxxxxx xxxxxx a xxxxx žádanky x xxxxxx xxxxxx (§13 xxxx. 2 xxxxxx).
(3) X ostatních xxxxxxxxxxxxxx xxxxxxxxxx xxxx xxxxxxxxxx xxxxxxx xxxxxxxx péče xx xxxxxxxxxx xxxxx xxxxxxxxxxx xxxxxxx x xxxxxxxx 1 xxxxx xxxxxxxxx xxxxxxx3) xxxxxxxxxx xxxxxx pruhem a xxxxx použitých xxxxxxx4) xxxxxxxxxx xxxxxx pruhem.
Účinnost xx 1.7.2000 xx 30.6.2004 (xx xxxxxx x. 363/2004 Xx.)
§10
Xxxxxxxxx x zápisy
Při xxxxxxxxxx xxxxxxxxx x xxxxxx podle §9 xxxx. 1 xxxx. x), x) a x) se xxxxxxxxx xxxxx xxxxxxxxxx xxxxxxxxxx xxx xxxxxx xxxxxxxxxxx xxxxxxx (§2). Xxxxxx xxxxx §9 xxxx. 1 xxxx. x), x), x) xxxx x) xxxx vždy xxxxxxxx xxxxxxxxx xxxxx (§9 xxxxxx). X xxxxxxx, že xxxxxx xxxxxxxxxx xxxxxxxxx osoba, xxxxxxxxxx xxxxx xxx xxxxxxxxxx, xxxxxxx-xx požadavky xxxxxxx na xxxxxxxxxx xxxxx ve smyslu §8 xxxx. 6 xxxxxx.
Xxxxxxxx xx 6.3.2002 xx 30.6.2004 (do xxxxxx x. 363/2004 Xx.)
§11
Xxxxxxxxxx dokumentace
Dokumentace zacházení x xxxxxxxxxx látkami, xxxxxxxxx, prekursory x xxxxxxxxxxx xxxxxxxxx s xxxxxxxxx xxxxxxx xxxxxxxxx x xxxxxxxxx x. 10 x 11 xxxxxx se xxxxxxxx xx dobu 5 xxx xx xxxxxxxx xxxxxxxxx, popřípadě xx xxxxxxxxxx xxxxxxx x xxx xxxxx xxxx, xxxxx x těchto xxxxxxxxxxx xxxxxxx xxxxxxx.
§12
Xxxxxxxx
Xxxx xxxxxxxx nabývá xxxxxxxxx xxxx 1. xxxxx 1999.
Xxxxxxx:
XXXx. David, XXx. v. x.
Xxxxxxxx xx 6.3.2002 xx 30.6.2004 (do xxxxxx x. 363/2004 Xx.)
Xxxxxxx x. 1 x xxxxxxxx x. 304/1998 Xx.
Xxxxxxx, xx xxxxxxx xx xxxxxxxx xxxxxxxx x vývozu xxxxxxxxx xxxxx
(xxxx xxxxxx xxxx označeny xxxxxxxxxx (*) x xxxxxxx xxxxxxxxx pomocné látky)
-
Včetně xxxx uvedených látek xx xxxxx xxxxxxxxx, xxx existence xxxxxxxx xxxx xx xxxxx, x xxxxxxxx xxxxxxxx xxxxxxxxxxxxxx a xxxxxxxx xxxxxx.
Příloha x. 2 x xxxxxxxx č. 304/1998 Sb.
Xxxxxxx x. 3 x xxxxxxxx x. 304/1998 Sb.
Vzor listu xxxxxxxxx knihy ostatních xxxxxxxxxxxxxx zařízení, xxxxxxxx xxxxxxxx xxxx a xxx xxxxxxxxxxx xxxxxxxxxxx xxxx
|
Xxxxx XX X*, XX XX* (xxxx, xxxx x xxxxxxxx):
|
||||||
|
Xxxxx
|
Xxx xxxxxx
|
Xxxxxxx: xxxxx
|
Xxxxxx
|
Xxxxx
|
Xxxx kusů
|
|
|
příjmu xxxx
|
xxxxx bloku x x. xxxxxxx
|
xxxxxxxxx
|
xxxx xxxxxx
|
&xxxx; | &xxxx; |
xxxxxxx, xxxxxx apod.
|
|
výdej
|
Při výdeji
|
|||||
|
č. xxxxxxxxx
|
xxxxxxx
|
&xxxx; | &xxxx; | &xxxx; | &xxxx; | |
|
1
|
2
|
3
|
4
|
5
|
6
|
7
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
* OL X - xxxxxx xxxxx xxxxxxx v příloze č. 1 xxxxxx č. 167/1998 Xx.
* XX II - xxxxxxxxxxxx látky xxxxxxx v xxxxxxx x. 5 zákona x. 197/1998 Xx.
Xxxxxxx x. 4 x vyhlášce x. 304/1998 Xx.
Xxxx xxxxx xxxxxxxxx knihy xxxxxx xxxxxxxxx, které xxxxxxxx xxxxxxxx xxxxx (XX)
|
Xxxxxxxx xxxxx xxxxxx
|
Xxxxxx xxxxx xxxxxxxx xx xxxxxx
|
Xxxxx xxxxxxxx šarže
|
Datum předání xx xxxxxx xxxxxxxx xxxxxxx
|
Xxxxxxxx xxxxxxx xxxxxx, x xxxxx xxxxxx XX, prekursorů
|
Skutečné xxxxxxx xxxxxx v x
|
Xxxxx x x XX, xxxxxxxxxx, xxxxxxxxxx x xxxxx výrobě xxxx xxxxxxxxxxxx
|
Xxxxxxxx
|
Xxxxxxx podpis xxxxxxxxxx xxxxxxxxxxxxx xxxxx
|
| &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; |
| &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; |
| &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; |
| &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; |
| &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; |
| &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; |
| &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; |
| &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; |
| &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; |
| &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; |
Původní xxxxx - xxxxxxxx xx 1.1.1999 xx 30.6.2004 (do xxxxxx x. 363/2004 Xx.)
Xxxxxxx x. 5 x xxxxxxxx x. 304/1998 Sb.
Vzor xxxxx xxxxxxxxx xxxxx xxxxxxxxxx
Xxxxx xxxxxxxx látky (XX), xxxxxxxxx a xxxxxxxxxx
______________________________________________________________________________________
Xxxxx Xxxxx xxxxxxx Xxxxx x adresa Množství Množství Stav xxxxx
xxxxxx (xxxxxxxxxx x Xxxxx xxxxx xxxxxxxxxx xxxx xxxxxxxxx xxxxxxxx x
x xxxxxxxxx xxxxx) xxxxxxxx XX, xxxx- XX, xxxxxxxxxxx
xxxxxx xxxxx a přípravků datu
prekursorů a xxxxxxxxxx
______________________________________________________________________________________
______________________________________________________________________________________
______________________________________________________________________________________
______________________________________________________________________________________
______________________________________________________________________________________
______________________________________________________________________________________
______________________________________________________________________________________
______________________________________________________________________________________
______________________________________________________________________________________
______________________________________________________________________________________
______________________________________________________________________________________
______________________________________________________________________________________
______________________________________________________________________________________
______________________________________________________________________________________
______________________________________________________________________________________
______________________________________________________________________________________
______________________________________________________________________________________
______________________________________________________________________________________
______________________________________________________________________________________
Xxxxxxxxx xxxxxxxx je x XX x xxxxxxxxxx 1 g x x xxxxxxxxx 1 xxxxxx.
Xxxxxxx x. 6 x xxxxxxxx č. 304/1998 Xx.
Xxxx xxxxx xxxxxxxxx xxxxx xxxxxxxxxx
Xxxxx xxxxxxxx xxxxx (XX) xxxxxxx x xxxxxxxxx x. 3 x 4 xxxxxx
Xxxxx xxxxxxxxx xxxxxxxxxxxx xxxxxxxx látky xxxxxxx x xxxxxxxxx x. 3 a 4 xxxxxx
|
Xxxxx
|
Xxxxx xxxxxxx
|
Xxxxx x adresa
|
Jednotka
|
Množství
|
Množství
|
Stav xxxxx
|
Xxxxx xxxxx
|
|
xxxxxx
|
(xxxxxxxxxxx a
|
dodavatele
|
množství
|
přijatých XX
|
xxxxxxxx XX
|
x xxxxxxxxxxx
|
xxxxx SÚKL
|
|
a xxxxxx
|
xxxxxxxxxx xxxxx)
|
xxxx xxxxxxxx
|
&xxxx;
|
x xxxxxxxxx
|
x přípravků
|
datu
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Příloha č. 6 xxxxxxx xxxxxxx xxxxxxxxx x. 143/2000 Xx. x xxxxxxxxx xx 1.7.2000
Účinnost od 6.3.2002 xx 30.6.2004 (xx xxxxxx x. 363/2004 Xx.)
Xxxxxxx x. 7 x xxxxxxxx x. 304/1998 Xx.
Xxxx xxxxxxxxxx
Xxxxxxx x. 8 x xxxxxxxx č. 304/1998 Sb.
Roční xxxxxxx xxxxxxxx xxx xxxxx, xxxxx xxxxxxx xxxxxx xx xxx xxxxxxx xxxxx uvedené x příloze č. 10 zákona (§12 xxxx. 3 x §32 xxxx. 6 xxxxxx)
|
Xxxxxxxxxxx nechráněný xxxxx (XXX) x českém xxxxxx
|
Xxxxxxxx
|
|
Xxxxxxxx xxxxxxxx xxxxxx
|
20 xxxxx
|
|
Xxxxxxxx antranilová
|
1 kg
|
|
Kyselina xxxxxxxxxxx
|
1 xx
|
|
Xxxxxxxxx
|
0,5 kg
|
Včetně xxxx xxxxxxxxx xxxxx xx xxxxx xxxxxxxxx, xxx xxxxxxxxx xxxxxxxx xxxx je xxxxx.
Xxxxx x pro xxxxx xxxxxx xxxxx xxx xxxxxxxx na xxxxx xxxxx xxxxx, xxxxx xx x dané xxxxx xxxxxxxx.
Xxxxxxx x. 8 xxxxxxx xxxxxxx xxxxxxxxx č. 363/2004 Xx. s xxxxxxxxx xx 1.7.2004
Xxxxxxx x. 9 x xxxxxxxx č. 304/1998 Xx.
Xxxxxxx množství xxx osoby, které xxxxxxx vyvážet xxxxxxxx xxxxxxxx octové xxxx xxxxxxxxxxx draselný xxxxxxxxxx xx x xxxxxxxx x xxxxxxxxxxxxxx vývozu (§20b xxxx. 2 xxxxxx)
|
Xxxxxxxxxxx xxxxxxxxxx xxxxx (XXX) x xxxxxx xxxxxx
|
Xxxxxxx množství v xx (xxxxxx)
|
|
Xxxxxxxx kyseliny xxxxxx
|
100
|
|
Xxxxxxxxxxx xxxxxxxx
|
100
|
Xxxxxxx č. 9 xxxxxxx xxxxxxx xxxxxxxxx x. 363/2004 Xx. s xxxxxxxxx xx 1.7.2004
Xxxxxxxxx
Xxxxxx předpis č. 304/98 Xx. xxxxx xxxxxxxxx dnem 1.1.1999.
Ve xxxxx xxxxxx xxxxxxxx xxxxxxxx xxxx xxxxxxxxxx změny x doplnění xxxxxxxxxxx xxxxxxx xxxxxxxxx č.:
143/2000 Sb., xxxxxx se xxxx xxxxxxxx x. 304/98 Xx., xxxxxx xx xxxxxxx případy, xxx xx nevyžaduje vývozní xxxxxxxx x xxxxxx xxxxxxxxx látek, podrobnosti x xxxxxxxx xxxxxxxxxx xxxxx, xxxxxxxxx a xxxxxxxxxx x x xxxxxxxxxxx návykových xxxxx
x xxxxxxxxx xx 1.9.2000
82/2002 Xx., xxxxxx se xxxx xxxxxxxx č. 304/98 Xx., kterou xx xxxxxxx xxxxxxx, xxx se xxxxxxxxxx xxxxxxx povolení k xxxxxx pomocných xxxxx, xxxxxxxxxxx x xxxxxxxx xxxxxxxxxx xxxxx, xxxxxxxxx x xxxxxxxxxx a x xxxxxxxxxxx xxxxxxxxxx xxxxx, xx xxxxx xxxxxxxx x. 143/2000 Xx.
s xxxxxxxxx xx 6.3.2002
363/2004 Xx., xxxxxx xx xxxx xxxxxxxx x. 304/98 Xx., xxxxxx xx xxxxxxx xxxxxxx, kdy xx xxxxxxxxxx xxxxxxx povolení x xxxxxx xxxxxxxxx xxxxx, podrobnosti x xxxxxxxx xxxxxxxxxx látek, xxxxxxxxx x prekursorů x x xxxxxxxxxxx xxxxxxxxxx xxxxx, ve xxxxx xxxxxxxxxx xxxxxxxx
x xxxxxxxxx od 1.7.2004
Právní xxxxxxx x. 304/98 Xx. xxx xxxxxx xxxxxxx xxxxxxxxx č. 123/2006 Sb. x účinností od 1.5.2006.
Xxxxx xxxxxxxxxxxx xxxxxxxx xxxxx xxxxxx právních xxxxxxxx x odkazech xxxx xxxxxxxxxxxxx, xxxxx xx xxxx netýká derogační xxxxx xxxxx xxxxxxxxx xxxxxxxx předpisu.
1) Xxxxxxxx Rady 92/109/EHS xx xxx 14. xxxxxxxx 1992 x xxxxxx xxxxxxxx xxxxx používaných x xxxxxxxxxx xxxxxx xxxxxxxx x psychotropních látek x o xxxxxx xxxxxxx na xxx.
Xxxxxxxx Xxxxxx 93/46/EHS ze xxx 22. xxxxxx 1993, xxxxxx xx xxxxxxxxx x xxxx xxxxxxx směrnice Rady 92/109/XXX x výrobě xxxxxxxx xxxxx xxxxxxxxxxx x nedovolené xxxxxx xxxxxxxx x xxxxxxxxxxxxxx xxxxx a o xxxxxx xxxxxxx na xxx.
Xxxxxxxx Xxxx (XXX) č. 3677/90 xx xxx 13. xxxxxxxx 1990 x opatřeních, xxxxx xxxx xxx xxxxxxx xx xxxxxx xxxxxxxx xxxxxxxxxx xxxxxxxx xxxxx x nedovolené xxxxxx xxxxxxxx x xxxxxxxxxxxxxx xxxxx, xx znění xxxxxxxx Xxxx (XXX) x. 900/92 x xxxxxxxx Xxxx (XX) x. 988/2002.
Xxxxxxxx Komise (XX) č. 1485/96 ze xxx 26. xxxxxxxx 1996, xxxxxx xx xxxxxxx prováděcí xxxxxxxx xx směrnici Xxxx 92/109/XXX, xxxxx xxx x prohlášení odběratele x xxxxxxxxx xxxxxxx xxxxxxxx xxxxx xxxxxxxxxxx x nedovolené xxxxxx xxxxxxxx x psychotropních xxxxx, ve xxxxx xxxxxxxx Xxxxxx (ES) x. 1533/2000.
1a) Xx. 2 xxxx. 3 nařízení Xxxx (XXX) č. 3677/90.
1x) Xxxxx č. 101/2000 Sb., o xxxxxxx xxxxxxxx xxxxx x x xxxxx xxxxxxxxx xxxxxx, xx xxxxx xxxxxxxxxx předpisů.
1c) Xx. 2 xxxx. 2 xxxxxxxx Xxxx (EHS) č. 3677/90.
1x) §2 xxxx. 3 a 11 xxxxxx x. 79/1997 Xx. o xxxxxxxx x x xxxxxxx x xxxxxxxx xxxxxxxxx xxxxxxxxxxxxx xxxxxx.
2x) §21 xxxx. 1 xxxx. x) x g) xxxxxx č. 79/1997 Xx., ve znění xxxxxx č. 149/2000 Xx.
2b) §3 xxxx. 5 xxxx. x) bod 2 xxxxxxxx x. 343/1997 Xx., xxxxxx xx xxxxxxx xxxxxx x xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx, xxxxxxxxxxx xxxxxxxxxx xxxxxxxx x xxxxxxxx xxxxxx xxxxxxxxx.
2x) Xx. 2 xxxx. 1 xxxxxxxx Xxxx (XXX) č. 3677/90, xx xxxxx xxxxxxxx Xxxx (XXX) x. 900/92 a xxxxxxxx Xxxx (XX) x. 988/2002.
2d) Nařízení Xxxxxx (XX) č. 1485/96, xx xxxxx xxxxxxxx Komise 93/46/XXX a nařízení Xxxxxx (ES) x. 1533/2000.
3) §3 xxxx. 5 písm. x) vyhlášky x. 343/1997 Xx., xxxxxx xx stanoví xxxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx, xxxxxxxxxxx xxxxxxxxxx předpisů x xxxxxxxx xxxxxx xxxxxxxxx.
4) §3 xxxx. 6 xxxxxxxx x. 343/1997 Sb.
5) Xx. 2 xxxx. 4 nařízení Xxxx (EHS) č. 3677/90, xx xxxxx xxxxxxxx Xxxx (XXX) x. 900/92.


