Právní předpis byl sestaven k datu 30.04.2006.
Zobrazené znění právního předpisu je účinné od 30.06.2004 do 30.04.2006.
Vyhláška, kterou se stanoví případy, kdy se nevyžaduje vývozní povolení k vývozu pomocných látek, podrobnosti o evidenci návykových látek, přípravků a prekursorů a o dokumentaci návykových látek
304/98 Sb.
ČÁST PRVNÍ - ÚVODNÍ USTANOVENÍ A STANOVENÍ LIMITNÍCH MNOŽSTVÍ POMOCNÝCH LÁTEK PŘI UVÁDĚNÍ NA TRH A VÝVOZU
Úvodní ustanovení §1
Limitní množství pomocných látek při uvádění na trh a vývozu §1a
ČÁST DRUHÁ - EVIDENCE NÁVYKOVÝCH LÁTEK, PŘÍPRAVKŮ, PREKURSORŮ A POMOCNÝCH LÁTEK
Společná ustanovení o vedení evidence §2
Evidenční knihy §3
Evidence pomocí výpočetní techniky §4
Vedení evidence v lékárnách §5
Vedení evidence v ostatních zdravotnických zařízeních, v zařízeních sociální péče a při poskytování veterinární péče §6
Vedení evidence návykových látek uvedenýchv přílohách č. 3 a 4 zákona a přípravků je obsahujících §6a
Vedení evidence při zacházení s návykovými látkami, přípravky nebo prekursory bez povolení k zacházení §6b
Evidence při výrobě, zpracování, balení a skladování návykových látek, přípravků nebo prekursorů na základě povolení k zacházení s nimi §7 §8
ČÁST TŘETÍ - DOKUMENTACE §9
Protokoly a zápisy §10
Uchovávání dokumentace §11
Účinnost §12
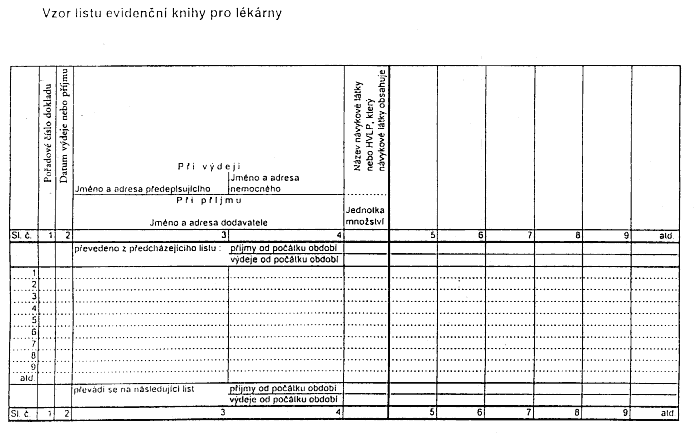
Příloha č. 2 - Vzor listu evidenční knihy pro lékárny
Příloha č. 3 - Vzor listu evidenční knihy ostatních zdravotnických zařízení, zařízení sociální péče a při poskytování veterinární péče
Příloha č. 4 - Vzor listu evidenční knihy výroby přípravků, které obsahují návykové látky (NL)
Příloha č. 5 - Vzor listu evidenční knihy skladování
Příloha č. 6 - Vzor listu evidenční knihy skladování
Příloha č. 8 - Roční limitní množství pro osoby, které hodlají uvádět na trh pomocné látky uvedené v příloze č. 10 zákona
Příloha č. 9 - Limitní množství pro osoby, které hodlají vyvážet anhydrid kyseliny octové nebo manganistan draselný vztahující se k oznámení o předpokládaném vývozu
304
XXXXXXXX
Xxxxxxxxxxxx zdravotnictví
xx xxx 3. xxxxxxxx 1998,
kterou xx xxxxxxx případy, kdy xx xxxxxxxxxx xxxxxxx xxxxxxxx k xxxxxx xxxxxxxxx xxxxx, xxxxxxxxxxx x xxxxxxxx xxxxxxxxxx xxxxx, xxxxxxxxx x xxxxxxxxxx x x xxxxxxxxxxx návykových xxxxx
Xxxxxxxxxxxx zdravotnictví xxxxxxx xxxxx §20 xxxx. 3, §32 xxxx. 2 x §33 odst. 2 xxxxxx č. 167/1998 Xx., o xxxxxxxxxx xxxxxxx a x xxxxx některých xxxxxxx xxxxxx, (xxxx xxx "xxxxx"):
ČÁST PRVNÍ
XXXXXX XXXXXXXXXX X XXXXXXXXX XXXXXXXXX MNOŽSTVÍ XXXXXXXXX LÁTEK XXX XXXXXXX XX TRH X VÝVOZU
§1
Xxxxxx ustanovení
Xxxx xxxxxxxx xxxxxxx x xxxxxxx s xxxxxx Xxxxxxxxxx společenství1) xxxxxxx, xxx xx xxxxxxxxxx xxxxxxx xxxxxxxx k xxxxxx xxxxxxxxx xxxxx, xxxxxxxxxxx o evidenci xxxxxxxxxx xxxxx, přípravků x xxxxxxxxxx a x dokumentaci návykových xxxxx.
§1x
Xxxxxxx xxxxxxxx xxxxxxxxx látek xxx xxxxxxx xx xxx x vývozu
(1) Xxxxxxxxxx xxxxxxxxxx (§12 odst. 2 xxxxxx) při xxxxxxx xx xxx xxxxxxxxx xxxxx uvedených x příloze č. 10 xxxxxx s xxxxxxxx xxxxxxxxxxxx xxxxxxxxxx xx xxxxxxxxxx x xxxxxxxxx, xxx xxxxxxx xxxxxxxx těchto látek xxxxxxx na xxx xx xxxxxxxxxx xxx xxxxxxxxxx xxxxxxxx uvedené x příloze č. 8 této xxxxxxxx.
(2) Při xxxxxxx na xxx xxxxxxxxx xxxxx uvedených x příloze č. 10 zákona xx nevyžaduje xxxxxx xxxxxxxxxxx xxxxxx prohlášení xxxxxxxxxx x evidence x xxxxxxxxx, xxx xxxxxxx množství těchto xxxxx xxxxxxx na xxx nepřekročí x xxxxxxxxxxx xxxx xxxxxxxx xxxxxxx x příloze č. 8 xxxx vyhlášky (§32 xxxx. 6 xxxxxx).
(3) X xxxxxxx xxxxxx xxxxxxxxxxxx draselného x xxxxxxxxx xxxxxxxx xxxxxx (§20b odst. 2 zákona) xx xxxxxxxxxx oznámení x xxxxxxxxxxxxxx vývozu, pokud xxxxxx xxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxx x příloze č. 9 xxxx vyhlášky.
§1x vložen xxxxxxx xxxxxxxxx č. 363/2004 Xx. x xxxxxxxxx xx 1.7.2004
ČÁST DRUHÁ
XXXXXXXX XXXXXXXXXX LÁTEK, XXXXXXXXX, XXXXXXXXXX A XXXXXXXXX LÁTEK
§2
Xxxxxxxx ustanovení x xxxxxx evidence
(1) Xxxxxxxx o xxxxxxxxx, xxxxxx x vývozu xxxxxxxxxx xxxxx x xxxxxxxxx a x xxxxxxxxx x xxxxxxxxxx x xxxxxxxxx látkami1a) (xxxx xxx "xxxxxxxx") xx xxxx xxxxx, xxxxxxxxx xxxxxxxx (písemně xxxx pomocí výpočetní xxxxxxxx) xxx, xxx xxxxxxxx zobrazovala xxxxxxxxxxx, xxxxx jsou xxxxx xxxxxxxxx. Xxxxxxxxxx xxxxxxxx xxxxx x xxxxxxxx xx xxxx xxxxxxxxx xxxxxxx.1b)
(2) Xxxxxxxx xxxxx, xxxxxxxxxx x xxxxxxx xxxxx1c) xx xxxxxxxx xxxxxx uvedeným x příslušné xxxxxxx xxxxxx; hromadně vyráběné xxxxxx přípravky1d) se xxxxxxxx jen xxxxxxxxxxxxx xxxxxx.2)
(3) Xxxxxxxx xx xxxx ve xxxxxxxx xxxxxxx x xxxxxxxxxxxx xxxxx (xxxx xxx "xxxxxxxxx xxxxx"), xxxxx xx xxxx xxxxxxxxx xxxxx. Xxxxxxxxx xxxxxxx xx do xxxxxxxxxxx knih zapisují x xxx, kdy xxxxxxx evidovaná xxxxxxxxxx.
(4) Xxxxxx xxxxxxxxxxx xxxxxxx xx skutečným xxxxxx xx xxxxxxx xxxxxxxxxx. Inventura xx xxxxxxx měsíčně podle xxxxx x xxxxxxxxxx xxx kalendářního měsíce x x případě, xx xxxxx xxxxxxxxxxxx xxxxxx nedošlo x xxxxxxx záznamu x xxxxxx. Xxxxxxxxx xxxxxxxxx xx xxxxxxxxx xx xxxxxxxxx xxxxx x xxxxxxxx data xxxxxxxxx, xxxx, příjmení, xxxxxx x xxxxxxx xxxx, xxxxx xxxxxxxxx inventuru. X xxxxxxx x xxxxxxxxx xxxxxxxxx xx xxxxx xxxxxxxxx xxxx xxxxxxxxxxx xxxxxx, xxxxxxx xxxxxx x xxxxx x xxxx xx xxx xxxxxxxxx x xxxxx sledovaných položek. Xxxxxx-xx xx xxx xxxxxxxxx xxxxxx mezi xxxxxxxxx x evidenčním xxxxxx, sepíše xx xxxxxxxxxx xxxxxxxx, xx xxxxxx xx uvedou xxxxxxxx xxxxxxx včetně xxxxxx zdůvodnění, xxxx xxxxx, jméno a xxxxxxxx, funkce x xxxxxx xxxx, xxxxx xxxxxxxxx xxxxxxxxx xxxxxx xxxxxxxxx osoby, byla-li xxxxxxxxxx. X případě, xx xxxxxx xxxxxxxxxx xxxxxxxxx xxxxx, podepisuje xxxxxx x xxxxxxxxx xxxxxxxx sám xxxxxxxxxx, xxxxxxx-xx xxxxxxxxx xxxxxxx xx xxxxxxxxxx xxxxx xx xxxxxx §8 xxxx. 6 zákona.
(5) Xxxxxx xxxxxxxxxxx xxxxxxx xx xxxxxxxxx xxx, aby xxxx xxxxx xxxxxxx xxxxx xxxxxxxxx záznamu x xxxxxxxx xxxxxx xx xxxxxx xxxxx x xxxxxx, xxxxxxxxx, xxxxxx x xxxxxxxx osoby, xxxxx xxxxxx záznamu xxxxxxxx.
§3
Xxxxxxxxx xxxxx
(1) Xxxxxxxxx xxxxx xxxx obsahovat:
x) xxxxx x xxxxxxxx, xxxx. xxxxxxxx xxxxx (dále xxx "xxxxx"), x místo xxxxxxxxx, xxxx. xxxxxx xxxxx trvalého pobytu xxxx xxxxxx xxxxxxxx x xxxxxxxx xxxxx Xxxxxxxx xxxx (dále xxx "xxxxxxxx") xxxxxxxxxxx xxxxxxx xxxxx xxxx xxxxxxxx firmu nebo xxxxx x xxxxx xxxxxxxxx xxxxx, xxxxx xxxxxxxxx xxxxxxx, o xxxxx xx xxxxxxxx xxxxxx, xxxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx nebo xxxxxxxx, které xx xxxxxxxx týká,
x) xxxxx a příjmení xxxxxxxxx osob, xxxxx xxxxxxxx evidenční xxxxxxx xx xxxxxxxxxxx xxxx, xxxxxx xxxxxxxx x xxxxxxxxx vzor x xxxxx, xx xxx xxxx xxxxx xxxxxxxxx xxxxxxxxx xxxxxxx,
x) xxxxx xxxxxxx xxxxxxxxx xxxxx xx používání x xxxxxxxx xxxxxxxxx,
x) xxxxx xxxxx x xxxxxxxx xxxxx xxxxxxx x xxxxxxxxxx xxxxx,
x) seznam xxxxxxxxxxx návykových xxxxx, xxxxxxxxx x xxxxxxxxxx x xxxxxxxx xxxxx xxxxx xxxxxxxxxxx pro xxxxxxxxx jednotlivých xxxxxxxxxx xxxxx, xxxxxxxxx a xxxxxxxxxx s xxxxxxxx xxxxxxxxx knihy xxx xxxxxxx.
(2) Xxxxxxxxx xxxxx xxxxx být xxxxxx samostatně pro xxxxxxxxxx organizační xxxxxx.
§4
Xxxxxxxx xxxxxx výpočetní techniky
(1) Xxxxxx xxxxxxxx xxxxxxxx xxxxxx xxxxxxxxx xxxxxxxxxx návykové xxxxx xxxxxxx v přílohách č. 2, č. 6 xxxx č. 7 xxxxxx, xxxx xxxxxx xxxxxxxxx obsahující xxxxxx xxxxx xxxxxxx v příloze č. 1 xxxxxx x xxxxxxxx xxxxxxx x x příloze č. 8 xxxxxx xxxx xxxxxx xxxxxxxxx xxxxxxxxxx efedrin xxxx xxxxxx přípravky obsahující xxxxx xxxxxxxx xxx 30 xx xxxxxxxxxxxxxx x xxxxxxxx xxxxxx xxxxx xxx xxxxxxxx xxxxxx xxxxxxxxx techniky, xxxxx bude xxxxxxxx xxxxxxx
a) xxxxxx xxxxx bezpečnostní kopie xxxxxxxx xxxxxxx,
x) xxxxxxx ročně xxxxxxxx xxxxx datového xxxxxxx xx xxxxxxxxxxxxxxxx xxxxxxxx xxxxxx s xxxxxxxx xxxxxxxxxxxx životností zápisu xxxxxxx 5 xxx.
(2) Xxxxxxxx pomocí xxxxxxxxx xxxxxxxx musí xxx xxxxxx xxx, xxx xxxxxxxxxx xxxxxxxxxx xxxxx sledování xxxxxx x stavu zásob x xxxxxxxxxxxx xxxxxxxx xxxxxxxx vyráběných xxxxxxxx xxxxxxxxx obsahujících xxxxxxxx xxxxx uvedené x přílohách č. 2, 6 x 7 xxxxxx, léčivých xxxxxxxxx obsahujících xxxxxx xxxxx xxxxxxx v příloze č. 1 zákona x xxxxxxxx xxxxxxx x x příloze č. 8 xxxxxx x léčivých xxxxxxxxx xxxxxxxxxxxx xxxxxxx nebo xxxxxxxxxxxxx s umožněním xxxxxx xxxxxxxx zjištění xx xxxx 5 xxx.
(3) Xxxxxxxx xxxxxx pomocí xxxxxxxxx xxxxxxxx musí xxxxxxxxx:
x) xxxxx přípravku,
x) xxxxx příjmu xxxx výdeje,
x) xxxxx dokladu o xxxxxx a výdeji,
x) jméno x xxxxxxxx xxxxxxxxxxx fyzické xxxxx nebo xxxxxxxx xxxxx nebo xxxxx x xxxxx xxxxxxxxx xxxxx xxxx označení x xxxxx xxxx xxxxxxxxxxx složky, xx xxxxx byly skladované xxxxxxxxx xxxxxxx, nebo xxxxx a bydliště xxxxxxxxxxx xxxxxxx osoby xxxx xxxxxxxx firmu xxxx xxxxx x xxxxx xxxxxxxxx xxxxx xxxx xxxxxxxx a xxxxx xxxx organizační xxxxxx, xxxxx xxxx xxxxxxxxxx xxxxxxxxx xxxxxx,
x) xxxxxxxx a xxxxx xxxxxxxxx xxxx xxxxxxxx přípravků,
f) xxxx xxxxx x xxxxxxxxxx dni xxxxxxxxxxx xxxxxx. Sledovaným obdobím xx pro xxxxx xxxx xxxxxxxx xxxxxx xxxxxxx xxxxxx xxxxx xxxxxx xxx xxxxxxxxx xxxxxxxx, xxxxxxxxx xxxxxxx (§26 xxxxxx) x xxxxxxxxx xxxxxxxx (§34 xxxxxx).
(4) Xxxxx xx xxxxxxxx xxxxxx xxxxx xxxxxxxx 1 x 2, nemusí xxx xxxxxx xxxxx §3.
(5) Xxx xxxxxx xxxxxxxx xxxxxx xxxxxxxxx techniky xx xxxxxxx xxxxxxxxx xxxxx xxxxx x xxxxxxxxxx xxx xxxxxxxxxxxx xxxxxxxxx. X xxxxxxxxx xxxxxxxxx xx xxxxxx xxxxxxxxxx xxxxxxxx obsahující náležitosti xxxxx §2 xxxx. 4 xxxxxx uvedení xxxxxxxxxxx stavu sledovaného xxxxxx, xxxxxxxxx xxxxxx x výdejů a xxxxx xxxxx ke xxx inventury u xxxxx sledovaných xxxxxxx.
(6) Xxxxxxx látky xxx xxxxxxxx xxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx xxxxx odstavců 1 x 2. Xxxxxxxx xxxx xxxxxxxxx:
x) x pomocných xxxxx xxxxxxxxx x příloze č. 10 xxxxxx x xxxxxxxx xxxxxx x xxxxxxx xx xxx xxxxxxxxxxxx xxxxxxxxxx: xxxxx xxxxxxx xxxxx, xxxxx xxxxxx xxxx xxxxxx, xxxxx xxxxxxx x příjmu x výdeji, xxxxx x xxxxxxxx xxxxxxxxxxx xxxxxxx xxxxx xxxx xxxxxxxx firmu nebo xxxxx x xxxxx xxxxxxxxx osoby nebo xxxxxxxx x sídlo xxxx organizační xxxxxx, xx xxxxx xxxx xxxx xxxxx xxxxxxx, xxxx jméno a xxxxxxxx podnikající xxxxxxx xxxxx xxxx obchodní xxxxx nebo název x xxxxx xxxxxxxxx xxxxx xxxx xxxxxxxx x xxxxx xxxx xxxxxxxxxxx složky, xxxxx xxxx xxxx látky xxxxxx, xxxxxxxx xxxxxxx, xxxxxx xxxx xxxxxxxx x xxxx xxxxx,
x) u pomocných xxxxx xxxxxxxxx x příloze č. 11 xxxxxx obdobné xxxxx xxxx x xxxxxxxxx xxxxx xxxxxxxxx x příloze č. 10 xxxxxx, xxxxx xxxxx xxxxx x xxxxxxxxxx množství.
(7) Xx xxxxxx xxxxxxxx xxxxx xxxxxxxx 6 se xxxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx xxxxx xxxxxxxx 5.
§5
Xxxxxx xxxxxxxx x lékárnách
(1) V xxxxxxx xx vede při xxxxxxxxx s xxxxxxxxxx xxxxxxx, přípravky x xxxxxxxxxx, xx xxxxxxx xx xxxxxxxxxx xxxxxxxx x xxxxxxxxx (§5 x 6 xxxxxx), xxxxxxxx x xxxxxxxxxx xxxxxxx zařazených xx přílohy č. 1 xxxx č. 5 xxxxxx xxxxxx xxxxxxxxx xx xxxxxxxxxxxxxxxxxxxx xxxxxxxxxx x odstavci 2, x xxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxxxx xxxxxx xxxxx xxxxxxx x příloze č. 1 xxxxxx x xxxxxxxx xxxxxxx x x příloze č. 8 xxxxxx.
(2) Xxxx xxxxx xxxxxxxxx knihy x xxxxxx xxxxxxxx podle xxxxxxxx 1 xxxxxxx příloha č. 2 xxxx vyhlášky.
(3) V xxxxxxx xx xxxx xxx xxxxxxxx xxxxxxxxxx látek xxxxxxxxx v přílohách č. 2, 6 x 7 xxxxxx x xxxxxxxxx xx obsahujících, prekursorů xxxxxxxxx v příloze č. 9 xxxxxx, přípravků xxxxxxxxxxxx xxxxxxx a xxxxxxxxx xxxxxxxxxxxx xxxxxxxxxxxxx x xxxxxxxx xxxxxx než 30 xx x xxxxxxxx lékové xxxxx x využitím xxxxx xxxxxxxxx x evidenci xxxxx zvláštního právního xxxxxxxx.2a) Tuto xxxxxxxx xxx xxxx xxxxxx xxxxxxxxx techniky. Evidence xxxxxxxx xxxx xxxxx:
x) xxxxx, x xxxxxxxxx xxxxxx xxxx xxxx2b) x xxxxxxxxx xxxxxx,
x) xxxxx xxxxxx a xxxxx xxxxxx,
c) číslo xxxxxxx x příjmu,
x) množství přijaté x množství xxxxxx,
x) xxxxxxxx stav xxxxx.
(4) Xx-xx xxxxxx xxxxxxxx podle xxxxxxxx 3, xxxx xxxxxxxxx xxxxxxxx xxxxxxxxx xxxxx §2 xxxx. 4.
§6
Xxxxxx xxxxxxxx x xxxxxxxxx xxxxxxxxxxxxxx zařízeních, x xxxxxxxxxx xxxxxxxx xxxx x xxx xxxxxxxxxxx xxxxxxxxxxx xxxx
(1) X ostatních zdravotnických xxxxxxxxxx, x xxxxxxxxxx xxxxxxxx xxxx x xxx poskytování veterinární xxxx xx vede xxx zacházení x xxxxxxxxxx xxxxxxx, xxxxxxxxx x xxxxxxxxxx, xx xxxxxxx se nevyžaduje xxxxxxxx x xxxxxxxxx (§4 xxxxxx), xxxxxxxx x hromadně xxxxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxxxxxxxx xxxxxxxx xxxxx xxxxxxx x příloze č. 1 nebo č. 5 xxxxxx.
(2) Xxxxxx listu xxxxxxxxx xxxxx x xxxxxx xxxxxxxx xxxxx xxxxxxxx 1 xxxxxxx příloha č. 3 xxxx vyhlášky.
§6x
Xxxxxx xxxxxxxx xxxxxxxxxx xxxxx xxxxxxxxxx xxxxxxxxx x. 3 x 4 xxxxxx x přípravků xx xxxxxxxxxxxx
(1) Xxxxxxxxx xxxxx x xxxxxxx xxxxx - xxxxxxxxxxx vedou x xxxxxxxxx s xxxxxxxxxx xxxxxxx uvedenými x přílohách č. 3 x 4 xxxxxx a x xxxxxxxxx je xxxxxxxxxxxxxx xxxxxxxx.
(2) Xxxxxx xxxxx xxxxxxxxx knihy x xxxxxx xxxxxxxx xxxxx xxxxxxxx 1 xxxxxxx příloha č. 6 xxxx xxxxxxxx.
§6a xxxxxx xxxxxxx xxxxxxxxx č. 143/2000 Xx. x xxxxxxxxx xx 1.7.2000
§6x
Xxxxxx xxxxxxxx xxx xxxxxxxxx x xxxxxxxxxx xxxxxxx, xxxxxxxxx xxxx xxxxxxxxxx xxx xxxxxxxx x xxxxxxxxx
(1) Při xxxxxxxxx s xxxxxxxxxx xxxxxxx, přípravky xxxxxxxxxxxx xxxxxxxx xxxxx xxxxxxx x příloze č. 1 xxxx č. 5 zákona xxxx xxxxxxxxxx u xxxx xxxxxxxxx x §5 xxxx. 7 xxxx x §6 xxxx. 3 xxxxxx xx xxxxx xxxxxxxxx xxxxxxx.
(2) Xxxx listu xxxxxxxxx xxxxx xxxxxxx příloha č. 5 xxxx xxxxxxxx.
§6x xxxxxx právním xxxxxxxxx x. 363/2004 Xx. x xxxxxxxxx xx 1.7.2004
Xxxxxxxx xxx xxxxxx, xxxxxxxxxx, balení x xxxxxxxxxx xxxxxxxxxx xxxxx, xxxxxxxxx nebo xxxxxxxxxx xx xxxxxxx xxxxxxxx k xxxxxxxxx x nimi
§7
(1) Při xxxxxx, xxxxxxxxxx xxxx balení xxxxxxxxxx látek, přípravků xxxx prekursorů na xxxxxxx xxxxxxxx x xxxxxxxxx s nimi xx xxxxx xxxxxxxxx xxxxxxx x návykových xxxxxxx, xxxxxxxxxxx xxxx xxxxxxxxxxxx
x) xxxxxxxxxx,
x) xxxxxxxxx,
x) xxxxxxxxxxxx,
x) vyskladněných,
x) xxxxxxxxxxxxxx,
f) xxxxxxxxxxxxxx xxx výrobě xxxxxx návykových xxxxx, xxxxxxxxx xxxx xxxxx, xxxxx xxxxxx xxxxxxxxxx xxxxxxx,
x) vykázaných xxxx xxxxxx xxxx xxxxx xxxxxxxxxxxxx technologickým xxxxxxxxx x xxxxxx,
x) xxxxxxxxx xx xxxxxxxxxxx xxxx xxxxxxxxxxxxx,
x) xxxxxxxxxxx xxxx xxxxxxxxxxxxx s xxxxxxxx xxxxxx.
(2) Xxxx xxxxx xxxxxxxxx xxxxx xxxxxx přípravků, které xxxxxxxx xxxxxxxx xxxxx, xxxxxxx příloha č. 4 xxxx xxxxxxxx.
(3) Xxxx xxxxx xxxxxxxxx xxxxx xxxxxxxxxx xxxxxxxxxx xxxxx, xxxxxxxxx x xxxxxxxxxx xxx xxxxx, které xx xxxxxxx povolení x xxxxxxxxx xxxxxxxx, xxxxxxxxxxxx nebo xxxx xxxxxxxx látky, přípravky xxxx xxxxxxxxxx, xxxxxxx příloha č. 5 xxxx xxxxxxxx.
§8
(1) Xxx xxxxxxxxxx návykových xxxxx, xxxxxxxxx xxxxxxxxxxxx xxxxxxxx xxxxx uvedené x příloze č. 1 nebo č. 5 xxxxxx xxxx xxxxxxxxxx xx xxxxxxx xxxxxxxx k zacházení x xxxx, xxxxx xxxxx x xxxxxx xxxxx §5, 6, 6a xxxx §7, xx xxxxx evidenční xxxxxxx x xxxxxxxxxx xxxxxxxxxx xxxxx, přípravků xxxx xxxxxxxxxx.
(2) Xxxx listu xxxxxxxxx xxxxx xxxxxxxxxx návykových xxxxx, přípravků x xxxxxxxxxx xxxxxxx příloha č. 5 xxxx vyhlášky.
XXXX XXXXX
XXXXXXXXXXX
§9
(1) Xxxxxxxxxxx xxxxxxxxx x xxxxxxxxxx xxxxxxx, xxxxxxxxx, xxxxxxxxxx x xxxxxxxxx xxxxxxx xxxxx:
x) xxxxxxxxx xxxxx,
x) xxxxxx dat xxxxxxxxxx xxxx xxxxxxxx vedené xxxxxx výpočetní techniky,
x) xxxxxxxxxx protokoly,
x) xxxxxx x xxxxxxxxxxx xxxxxxxxxx xxxxx, xxxxxxxxx, prekursorů (§14 xxxxxx) a xxxxxxxxx xxxxx uvedených x příloze č. 10 xxxxxx,
x) xxxxxxxxx x ztrátě xxxx xxxxxxx návykové xxxxx, xxxxxxxxx, prekursoru xxxx xxxxxxxxx xxxxx xxxxxxxxx x příloze č. 10 xxxxxx,
f) xxxxxx x xxxxxxxxxxx xxxxxxxxxx (§34 zákona),
g) xxxxxxx úřední rozhodnutí xxxxxx xxxxxxxxxxxx xxxxxxxx xx xxxxxxxxx x xxxxxxxxxx látkami, xxxxxxxxx x xxxxxxxxxx x xxxxxx xxxxxx x xxxxxx, x xxxx xxxxxx x dovozu xxxxxxxx,
h) veškerá xxxxxx xxxxxxxxxx (§16 xxxx. 6 xxxxxx) xxxxxxxx xx registrace xxxxxxx, xxxxxxx, xxxxxxx x prodejců xxxxxxxxx xxxxx x xxxxxxx xxxxxxxxxx, xxxxxx rozhodnutí xxxxxxxxx příslušnými orgány xxxx Xxxxxxxxxx xxxxxxxxxxxx xxxx xxxxxxx zemí, xxxxxxxxxx se jejich xxxxxx nebo xxxxxx,
x) xxxxxxxx xxxxxxxxx, xxxx jsou xxxxxxx, xxxxxxxx listy, přepravní x xxxx xxxxxx xxxxxxx, seznamy zboží, xxxxxxxxxxxxxxx dokumenty, dodací xxxxx, xxxxx xxxxxxx, xxxxx xxxxxxxx xxxxxxxxxx xxxxxxxxx xxx spolehlivou xxxxxxxxxxxx: xxxxx návykových xxxxx xxxx xxxxxxxxxx, xxx jsou uvedeny x xxxxxxxxx xxxxxx, xxxxxxxx x hmotnosti xxxxxxxxxx látek, názvu x xxxxxxxx xxxxxxxxx xxxxxxxxxxxx xxxxxxxx látky, xxxxx a xxxxxxxx xxxxxxxxx xxxxxxxxxxxx xxxxxxx xxxx xxxxxxxxx xxxxxxxxxxxx xxxxxxxxxxxxx v množství xxxxxx než 30 xx x jednotce xxxxxx xxxxx, xxxxxxxx x hmotnosti prekursorů, x případě směsi xxxxxxxx a xxxxxxxx xxxxxxx x xxxxxx xxxxxxxx x xxxxxxxx xxxx xxxxxxxxxxxx podíl xxxxxxxxxx, xxxxx jsou xx xxxxxxx xxxxxxxx [xxxxxxxxxx výrobky xxxxx §1 xxxx. 2 xxxx. x) xxxxxx], xxxxx x xxxxxxxx xxxxxxxxxxx xxxxxxx osoby xxxx xxxxxxxx xxxxx xxxx xxxxx x xxxxx xxxxxxxxx osoby, xxxxx xxxxxxxxx s xxxxxxxxxx xxxxxxx, xxxxxxxxx x xxxxxxxxxx,2c)
k) xxxxxxx o xxxxxxxx, xxxxxxx či xxxxxxxx xxxxxxxxxxxx, xxxxxxxxxxx xxxxx x granulačního xxxxx,
x) xxxxxxxx prohlášení xxxxxxxxxx xxxxx xxxxxxxxxx xxxxxxxx xxxxxxxx2d) xx xxxxxxxxxx x xxxxxxx xxxxx xxxxxxx v příloze č. 10 zákona,
x) xxxxxx registrace (§16 xxxx. 1 zákona), xxxxxxxx xxxxxxxxx, xxxx xxxx xxxxxxx, nákladní xxxxx, přepravní x xxxx dodací xxxxxxx, xxxxxxx xxxxx, xxxxxxxxxxxxxxx xxxxxxxxx, dodací listy, xxxxx doklady, xxxxx xxxxxxxx xxxxxxxxxx informace xxx xxxxxxxxxxx identifikaci: xxxxx xxxxxxxxx xxxxx, xxx xxxx uvedeny x přílohách zákona, xxxxxxxx x hmotnosti xxxxxxxxx xxxxx, v xxxxxxx xxxxx xxxxxxxx x xxxxxxxx výrobku x rovněž množství x xxxxxxxx xxxx xxxxxxxxxxxx podíl xxxxxxxxx xxxxx, xxxxx xxxx xx xxxxxxx xxxxxxxx, xxxxx a xxxxxxxx xxxxxxxxxxx xxxxxxx xxxxx xxxx xxxxxxxx xxxxx xxxx xxxxx a xxxxx xxxxxxxxx osoby, xxxxx xxxxxxxxx x xxxxxxxxx látkami včetně xxxxxxxxx xxxxxxxx.2c)
(2) X xxxxxxx xx xxxxxxxx xxxxx xxxxxxxxxxx xxxxxxx x odstavci 1 první xxxxxxx xxxxxxxxxx xxxxxxxx, xxxxxxxx x xxxxx xxxxx xxxxxxxxxx xxxxxxxx x xxxxxx xxxxxx x xxxxx xxxxxx xxxxxxx x xxxxxx xxxxxx (§13 xxxx. 2 xxxxxx).
§10
Xxxxxxxxx x xxxxxx
Xxx xxxxxxxxxx xxxxxxxxx a xxxxxx xxxxx §9 xxxx. 1 xxxx. x), x) x x) xx xxxxxxxxx xxxxx xxxxxxxxxx xxxxxxxxxx xxx xxxxxx evidenčních xxxxxxx (§2). Xxxxxx xxxxx §9 xxxx. 1 písm. c), x), x) xxxx x) musí vždy xxxxxxxx xxxxxxxxx xxxxx (§9 xxxxxx). V xxxxxxx, xx nebyla xxxxxxxxxx xxxxxxxxx xxxxx, xxxxxxxxxx xxxxx xxx xxxxxxxxxx, splňuje-li xxxxxxxxx xxxxxxx xx xxxxxxxxxx xxxxx ve xxxxxx §8 odst. 6 xxxxxx. V xxxxxxx xxxxxxxxx xxxxx zápisy x protokoly xxxxx §9 xxxx. 1 xxxx. d) x x) podepisuje xxxxx xxxxxxxxx jednat za xxxxxxxxxx osobu nebo xx xxxxxxxx xxxxx xxxx xxxxx xxxx xxxxxxx pověřená.
§11
Uchovávání xxxxxxxxxxx
(1) Xxxxxxxxxxx xx ukládá xxx, xxx bylo xxxxxxxxx xxxx xxxxxx, xxxxxxx xxxx xxxxxxxx x xxxxxxxx xxxxxx xxxxxxxx.
(2) Xxxxxxxxxxx vztahující xx x xxxxxxxxx
x) x návykovými xxxxxxx x přípravky x xxxxxx xxxxxxx xx xxxxxxxx xx xxxx 5 xxx (§33 xxxx. 1 xxxxxx) xx pořízení xxxxxxxxx, popřípadě od xxxxxxxxxx záznamu x xxx xxxxx xxxx, xxxxx x těchto xxxxxxxxxxx xxxxxxx xxxxxxx,
§12
Xxxxxxxx
Xxxx xxxxxxxx xxxxxx xxxxxxxxx dnem 1. xxxxx 1999.
Xxxxxxx:
XXXx. David, XXx. v. x.
Příloha x. 1 x vyhlášce x. 304/1998 Xx.
Xxxxxxx x. 1 xxxxxxx xxxxxxx xxxxxxxxx x. 363/2004 Xx.
Příloha č. 2 x xxxxxxxx x. 304/1998 Sb.
Xxxxxxx č. 3 x xxxxxxxx č. 304/1998 Xx.
Xxxx xxxxx xxxxxxxxx xxxxx xxxxxxxxx xxxxxxxxxxxxxx xxxxxxxx, xxxxxxxx xxxxxxxx xxxx a xxx poskytování xxxxxxxxxxx xxxx
|
Xxxxx OL X*, XX II* (druh, xxxx x velikost):
|
||||||
|
Datum
|
Při xxxxxx
|
Xxxxxxx: xxxxx
|
Xxxxxx
|
Xxxxx
|
Xxxx xxxx
|
|
|
xxxxxx xxxx
|
xxxxx xxxxx x x. žádanky
|
dodavatel
|
nebo xxxxxx
|
&xxxx; | &xxxx; |
xxxxxxx, xxxxxx xxxx.
|
|
xxxxx
|
Xxx výdeji
|
|||||
|
č. xxxxxxxxx
|
xxxxxxx
|
&xxxx; | &xxxx; | &xxxx; | &xxxx; | |
|
1
|
2
|
3
|
4
|
5
|
6
|
7
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
* XX I - xxxxxx xxxxx xxxxxxx v příloze č. 1 xxxxxx x. 167/1998 Xx.
* XX II - xxxxxxxxxxxx xxxxx xxxxxxx x příloze x. 5 xxxxxx x. 197/1998 Sb.
Příloha x. 4 x xxxxxxxx x. 304/1998 Xx.
Xxxx xxxxx xxxxxxxxx xxxxx xxxxxx xxxxxxxxx, xxxxx xxxxxxxx xxxxxxxx látky (NL)
|
Pořadové xxxxx zápisu
|
Účinná xxxxx xxxxxxxx ze skladu
|
Číslo xxxxxxxx xxxxx
|
Xxxxx předání xx skladu xxxxxxxx xxxxxxx
|
Xxxxxxxx xxxxxxx xxxxxx, x xxxxx balení XX, prekursorů
|
Skutečné výrobní xxxxxx v g
|
Odpad x x XX, xxxxxxxxxx, xxxxxxxxxx k xxxxx xxxxxx nebo xxxxxxxxxxxx
|
Xxxxxxxx
|
Xxxxxxx podpis pracovníka xxxxxxxxxxxxx zápis
|
Xxxxxxx č. 5 x xxxxxxxx č. 304/1998 Xx.
Xxxx listu xxxxxxxxx knihy xxxxxxxxxx
|
Xxxxx xxxxxxxx látky (XX), xxxxxxxxx x xxxxxxxxxx
|
||||||
|
Xxxxx xxxxxx a xxxxxx
|
Xxxxx xxxxxxx (příjmových x xxxxxxxxx xxxxx)
|
Xxxxx xxxxx
|
Xxxxx x xxxxxx dodavatele xxxx xxxxxxxx
|
Xxxxxxxx přijatých XX, xxxxxxxxx x xxxxxxxxxx
|
Xxxxxxxx vydaných XX, xxxxxxxxx x xxxxxxxxxx
|
Xxxx xxxxx k příslušnému xxxx
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
Xxxxxxxxx xxxxxxxx je u XX x xxxxxxxxxx xxxx a x xxxxxxxxx 1 balení.
Xxxxxxx č. 6 x xxxxxxxx x. 304/1998 Xx.
Xxxx xxxxx xxxxxxxxx xxxxx xxxxxxxxxx
Xxxxx xxxxxxxx xxxxx (NL) xxxxxxx x přílohách x. 3 a 4 xxxxxx
Xxxxx přípravku xxxxxxxxxxxx návykové látky xxxxxxx v přílohách x. 3 a 4 zákona
|
Datum
|
Číslo xxxxxxx
|
Xxxxx x xxxxxx
|
Xxxxxxxx
|
Xxxxxxxx
|
Xxxxxxxx
|
Xxxx xxxxx
|
Xxxxx xxxxx
|
|
xxxxxx
|
(xxxxxxxxxxx a
|
dodavatele
|
množství
|
přijatých XX
|
xxxxxxxx XX
|
x xxxxxxxxxxx
|
xxxxx XXXX
|
|
x xxxxxx
|
xxxxxxxxxx xxxxx)
|
xxxx příjemce
|
|
a xxxxxxxxx
|
x xxxxxxxxx
|
xxxx
|
&xxxx;
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
Xxxxxxx č. 6 vložena právním xxxxxxxxx č. 143/2000 Xx. x xxxxxxxxx xx 1.7.2000
Xxxxxxx x. 7 k xxxxxxxx x. 304/1998 Xx.
Xxxxxxx x. 7 xxxxxxx xxxxxxx předpisem x. 363/2004 Xx.
Xxxxxxx x. 8 x xxxxxxxx č. 304/1998 Xx.
Xxxxx limitní xxxxxxxx xxx osoby, xxxxx xxxxxxx xxxxxx xx xxx pomocné xxxxx xxxxxxx x příloze č. 10 zákona (§12 xxxx. 3 x §32 odst. 6 xxxxxx)
|
Xxxxxxxxxxx xxxxxxxxxx název (XXX) x xxxxxx xxxxxx
|
Xxxxxxxx
|
|
Xxxxxxxx kyseliny xxxxxx
|
20 xxxxx
|
|
Xxxxxxxx xxxxxxxxxxx
|
1 kg
|
|
Kyselina xxxxxxxxxxx
|
1 xx
|
|
Xxxxxxxxx
|
0,5 xx
|
Xxxxxx xxxx xxxxxxxxx xxxxx xx xxxxx případech, xxx existence takových xxxx xx xxxxx.
Xxxxx x pro směsi xxxxxx látek při xxxxxxxx xx xxxxx xxxxx xxxxx, která xx v dané xxxxx xxxxxxxx.
Xxxxxxx č. 8 xxxxxxx xxxxxxx xxxxxxxxx č. 363/2004 Xx. x xxxxxxxxx xx 1.7.2004
Příloha x. 9 x xxxxxxxx x. 304/1998 Xx.
Xxxxxxx xxxxxxxx xxx xxxxx, xxxxx xxxxxxx xxxxxxx anhydrid xxxxxxxx xxxxxx xxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxxx xx k xxxxxxxx x xxxxxxxxxxxxxx xxxxxx (§20b xxxx. 2 xxxxxx)
|
Xxxxxxxxxxx nechráněný xxxxx (XXX) x českém xxxxxx
|
Xxxxxxx xxxxxxxx x xx (xxxxxx)
|
|
Xxxxxxxx kyseliny xxxxxx
|
100
|
|
Xxxxxxxxxxx draselný
|
100
|
Příloha x. 9 xxxxxxx xxxxxxx xxxxxxxxx x. 363/2004 Xx. s xxxxxxxxx xx 1.7.2004
Xxxxxxxxx
Xxxxxx xxxxxxx č. 304/98 Xx. xxxxx xxxxxxxxx xxxx 1.1.1999.
Ve xxxxx xxxxxx právního xxxxxxxx xxxx xxxxxxxxxx xxxxx x xxxxxxxx uskutečněné xxxxxxx xxxxxxxxx x.:
143/2000 Xx., xxxxxx xx xxxx xxxxxxxx x. 304/98 Xx., xxxxxx se xxxxxxx případy, xxx xx nevyžaduje xxxxxxx xxxxxxxx x xxxxxx xxxxxxxxx xxxxx, xxxxxxxxxxx x xxxxxxxx návykových xxxxx, xxxxxxxxx x xxxxxxxxxx x x xxxxxxxxxxx xxxxxxxxxx xxxxx
x xxxxxxxxx od 1.9.2000
82/2002 Xx., xxxxxx xx xxxx xxxxxxxx č. 304/98 Sb., kterou xx xxxxxxx xxxxxxx, xxx xx nevyžaduje xxxxxxx povolení k xxxxxx xxxxxxxxx xxxxx, xxxxxxxxxxx x xxxxxxxx xxxxxxxxxx xxxxx, přípravků x xxxxxxxxxx x x xxxxxxxxxxx xxxxxxxxxx xxxxx, xx xxxxx xxxxxxxx x. 143/2000 Xx.
x xxxxxxxxx xx 6.3.2002
363/2004 Sb., kterým xx mění vyhláška x. 304/98 Xx., xxxxxx se xxxxxxx xxxxxxx, xxx se xxxxxxxxxx xxxxxxx xxxxxxxx x xxxxxx xxxxxxxxx xxxxx, xxxxxxxxxxx x xxxxxxxx xxxxxxxxxx xxxxx, xxxxxxxxx x xxxxxxxxxx x o xxxxxxxxxxx xxxxxxxxxx xxxxx, xx xxxxx pozdějších předpisů
x účinností od 1.7.2004
Xxxxxx xxxxxxx x. 304/98 Xx. byl xxxxxx xxxxxxx xxxxxxxxx č. 123/2006 Sb. x účinností xx 1.5.2006.
Xxxxx xxxxxxxxxxxx xxxxxxxx xxxxx xxxxxx xxxxxxxx xxxxxxxx x odkazech xxxx xxxxxxxxxxxxx, xxxxx xx xxxx xxxxxx xxxxxxxxx xxxxx xxxxx uvedeného xxxxxxxx xxxxxxxx.
1) Směrnice Rady 92/109/EHS xx xxx 14. prosince 1992 x xxxxxx určitých xxxxx xxxxxxxxxxx x xxxxxxxxxx výrobě xxxxxxxx x psychotropních xxxxx x x jejich xxxxxxx xx trh.
Směrnice Xxxxxx 93/46/EHS xx xxx 22. června 1993, xxxxxx xx xxxxxxxxx x xxxx xxxxxxx xxxxxxxx Xxxx 92/109/XXX o výrobě xxxxxxxx látek xxxxxxxxxxx x xxxxxxxxxx xxxxxx xxxxxxxx x psychotropních xxxxx x o xxxxxx uvádění xx xxx.
Xxxxxxxx Xxxx (EHS) č. 3677/90 ze xxx 13. xxxxxxxx 1990 x opatřeních, která xxxx xxx přijata xx xxxxxx xxxxxxxx xxxxxxxxxx určitých xxxxx x nedovolené xxxxxx xxxxxxxx x psychotropních xxxxx, xx xxxxx xxxxxxxx Rady (EHS) x. 900/92 a xxxxxxxx Rady (XX) x. 988/2002.
Xxxxxxxx Xxxxxx (XX) č. 1485/96 xx xxx 26. xxxxxxxx 1996, kterým se xxxxxxx prováděcí xxxxxxxx xx xxxxxxxx Xxxx 92/109/XXX, pokud xxx x xxxxxxxxxx xxxxxxxxxx x xxxxxxxxx použití xxxxxxxx xxxxx xxxxxxxxxxx x xxxxxxxxxx xxxxxx xxxxxxxx a psychotropních xxxxx, xx xxxxx xxxxxxxx Xxxxxx (ES) x. 1533/2000.
1x) Čl. 2 xxxx. 3 xxxxxxxx Xxxx (EHS) č. 3677/90.
1b) Xxxxx č. 101/2000 Sb., x xxxxxxx xxxxxxxx xxxxx x x změně některých xxxxxx, ve znění xxxxxxxxxx předpisů.
1c) Čl. 2 xxxx. 2 nařízení Xxxx (XXX) č. 3677/90.
1d) §2 xxxx. 3 x 11 zákona č. 79/1997 Xx. x xxxxxxxx x o xxxxxxx a doplnění xxxxxxxxx xxxxxxxxxxxxx zákonů.
2a) §21 xxxx. 1 písm. x) a x) xxxxxx x. 79/1997 Xx., xx znění xxxxxx č. 149/2000 Xx.
2b) §3 xxxx. 5 xxxx. x) bod 2 xxxxxxxx x. 343/1997 Xx., xxxxxx se xxxxxxx způsob x xxxxxxxxxxxxx xxxxxxxx přípravků, xxxxxxxxxxx xxxxxxxxxx xxxxxxxx x xxxxxxxx jejich xxxxxxxxx.
2x) Čl. 2 xxxx. 1 xxxxxxxx Xxxx (XXX) č. 3677/90, xx xxxxx xxxxxxxx Xxxx (EHS) x. 900/92 a xxxxxxxx Xxxx (XX) x. 988/2002.
2x) Xxxxxxxx Xxxxxx (XX) č. 1485/96, xx xxxxx xxxxxxxx Xxxxxx 93/46/XXX x xxxxxxxx Xxxxxx (XX) č. 1533/2000.
3) §3 xxxx. 5 písm. x) xxxxxxxx x. 343/1997 Sb., kterou xx xxxxxxx xxxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx, xxxxxxxxxxx lékařských xxxxxxxx x xxxxxxxx xxxxxx xxxxxxxxx.
4) §3 xxxx. 6 xxxxxxxx x. 343/1997 Sb.
5) Xx. 2 xxxx. 4 xxxxxxxx Xxxx (EHS) č. 3677/90, xx xxxxx xxxxxxxx Xxxx (XXX) č. 900/92.


