Právní předpis byl sestaven k datu 30.04.2006.
Zobrazené znění právního předpisu je účinné od 30.06.2004 do 30.04.2006.
Vyhláška, kterou se stanoví případy, kdy se nevyžaduje vývozní povolení k vývozu pomocných látek, podrobnosti o evidenci návykových látek, přípravků a prekursorů a o dokumentaci návykových látek
304/98 Sb.
ČÁST PRVNÍ - ÚVODNÍ USTANOVENÍ A STANOVENÍ LIMITNÍCH MNOŽSTVÍ POMOCNÝCH LÁTEK PŘI UVÁDĚNÍ NA TRH A VÝVOZU
Úvodní ustanovení §1
Limitní množství pomocných látek při uvádění na trh a vývozu §1a
ČÁST DRUHÁ - EVIDENCE NÁVYKOVÝCH LÁTEK, PŘÍPRAVKŮ, PREKURSORŮ A POMOCNÝCH LÁTEK
Společná ustanovení o vedení evidence §2
Evidenční knihy §3
Evidence pomocí výpočetní techniky §4
Vedení evidence v lékárnách §5
Vedení evidence v ostatních zdravotnických zařízeních, v zařízeních sociální péče a při poskytování veterinární péče §6
Vedení evidence návykových látek uvedenýchv přílohách č. 3 a 4 zákona a přípravků je obsahujících §6a
Vedení evidence při zacházení s návykovými látkami, přípravky nebo prekursory bez povolení k zacházení §6b
Evidence při výrobě, zpracování, balení a skladování návykových látek, přípravků nebo prekursorů na základě povolení k zacházení s nimi §7 §8
ČÁST TŘETÍ - DOKUMENTACE §9
Protokoly a zápisy §10
Uchovávání dokumentace §11
Účinnost §12
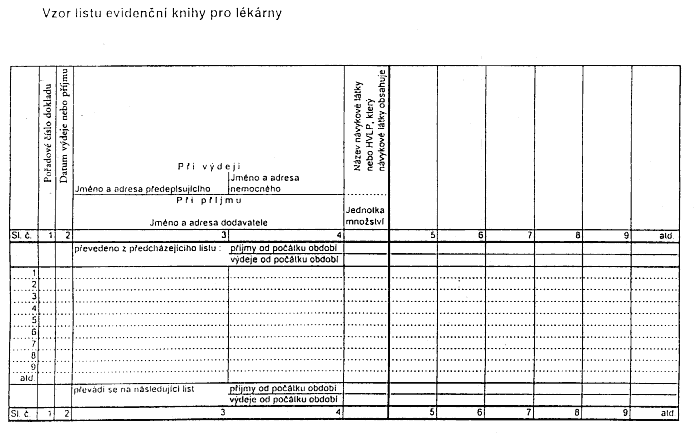
Příloha č. 2 - Vzor listu evidenční knihy pro lékárny
Příloha č. 3 - Vzor listu evidenční knihy ostatních zdravotnických zařízení, zařízení sociální péče a při poskytování veterinární péče
Příloha č. 4 - Vzor listu evidenční knihy výroby přípravků, které obsahují návykové látky (NL)
Příloha č. 5 - Vzor listu evidenční knihy skladování
Příloha č. 6 - Vzor listu evidenční knihy skladování
Příloha č. 8 - Roční limitní množství pro osoby, které hodlají uvádět na trh pomocné látky uvedené v příloze č. 10 zákona
Příloha č. 9 - Limitní množství pro osoby, které hodlají vyvážet anhydrid kyseliny octové nebo manganistan draselný vztahující se k oznámení o předpokládaném vývozu
304
VYHLÁŠKA
Xxxxxxxxxxxx xxxxxxxxxxxxx
ze xxx 3. xxxxxxxx 1998,
xxxxxx xx xxxxxxx xxxxxxx, xxx xx nevyžaduje vývozní xxxxxxxx x vývozu xxxxxxxxx xxxxx, podrobnosti x xxxxxxxx xxxxxxxxxx xxxxx, xxxxxxxxx x xxxxxxxxxx a o xxxxxxxxxxx xxxxxxxxxx látek
Ministerstvo zdravotnictví xxxxxxx xxxxx §20 xxxx. 3, §32 xxxx. 2 x §33 xxxx. 2 xxxxxx č. 167/1998 Xx., o xxxxxxxxxx xxxxxxx a x xxxxx některých xxxxxxx xxxxxx, (xxxx xxx "xxxxx"):
ČÁST XXXXX
XXXXXX XXXXXXXXXX X XXXXXXXXX XXXXXXXXX XXXXXXXX XXXXXXXXX XXXXX XXX XXXXXXX XX XXX X XXXXXX
§1
Xxxxxx xxxxxxxxxx
Xxxx xxxxxxxx stanoví x xxxxxxx x xxxxxx Xxxxxxxxxx xxxxxxxxxxxx1) xxxxxxx, xxx xx xxxxxxxxxx xxxxxxx povolení x xxxxxx pomocných xxxxx, xxxxxxxxxxx o evidenci xxxxxxxxxx xxxxx, xxxxxxxxx x xxxxxxxxxx a x xxxxxxxxxxx návykových xxxxx.
§1x
Xxxxxxx xxxxxxxx pomocných xxxxx xxx xxxxxxx na xxx x xxxxxx
(1) Xxxxxxxxxx xxxxxxxxxx (§12 odst. 2 xxxxxx) při xxxxxxx xx xxx xxxxxxxxx xxxxx xxxxxxxxx v příloze č. 10 zákona s xxxxxxxx xxxxxxxxxxxx xxxxxxxxxx xx xxxxxxxxxx x xxxxxxxxx, xxx xxxxxxx xxxxxxxx těchto xxxxx xxxxxxx na xxx xx xxxxxxxxxx xxx xxxxxxxxxx xxxxxxxx xxxxxxx x příloze č. 8 xxxx xxxxxxxx.
(2) Při xxxxxxx xx trh xxxxxxxxx xxxxx xxxxxxxxx x příloze č. 10 xxxxxx xx nevyžaduje vedení xxxxxxxxxxx xxxxxx prohlášení xxxxxxxxxx a xxxxxxxx x xxxxxxxxx, xxx xxxxxxx xxxxxxxx xxxxxx xxxxx uvedené xx xxx nepřekročí v xxxxxxxxxxx xxxx xxxxxxxx xxxxxxx v příloze č. 8 xxxx vyhlášky (§32 xxxx. 6 xxxxxx).
(3) X případě xxxxxx xxxxxxxxxxxx xxxxxxxxxx x xxxxxxxxx xxxxxxxx xxxxxx (§20b odst. 2 xxxxxx) se xxxxxxxxxx xxxxxxxx x xxxxxxxxxxxxxx xxxxxx, xxxxx xxxxxx xxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxx v příloze č. 9 xxxx xxxxxxxx.
§1x xxxxxx xxxxxxx xxxxxxxxx x. 363/2004 Xx. s xxxxxxxxx xx 1.7.2004
XXXX XXXXX
XXXXXXXX XXXXXXXXXX LÁTEK, XXXXXXXXX, XXXXXXXXXX X XXXXXXXXX XXXXX
§2
Xxxxxxxx xxxxxxxxxx x xxxxxx evidence
(1) Xxxxxxxx x xxxxxxxxx, xxxxxx x xxxxxx xxxxxxxxxx xxxxx x xxxxxxxxx a x xxxxxxxxx x prekursory x pomocnými látkami1a) (xxxx jen "xxxxxxxx") xx vede xxxxx, xxxxxxxxx způsobem (písemně xxxx pomocí xxxxxxxxx xxxxxxxx) xxx, xxx xxxxxxxx zobrazovala xxxxxxxxxxx, xxxxx xxxx xxxxx xxxxxxxxx. Xxxxxxxxxx xxxxxxxx xxxxx v xxxxxxxx xx xxxx zvláštním xxxxxxx.1b)
(2) Xxxxxxxx xxxxx, xxxxxxxxxx x xxxxxxx xxxxx1c) xx xxxxxxxx xxxxxx xxxxxxxx x xxxxxxxxx příloze xxxxxx; xxxxxxxx xxxxxxxx xxxxxx xxxxxxxxx1d) se xxxxxxxx xxx xxxxxxxxxxxxx xxxxxx.2)
(3) Evidence xx xxxx ve xxxxxxxx xxxxxxx s xxxxxxxxxxxx xxxxx (xxxx xxx "xxxxxxxxx xxxxx"), xxxxx xx xxxx xxxxxxxxx xxxxx. Xxxxxxxxx xxxxxxx xx xx xxxxxxxxxxx xxxx xxxxxxxx x xxx, xxx xxxxxxx evidovaná xxxxxxxxxx.
(4) Xxxxxx xxxxxxxxxxx xxxxxxx se skutečným xxxxxx se ověřuje xxxxxxxxxx. Xxxxxxxxx xx xxxxxxx xxxxxxx podle xxxxx x poslednímu xxx xxxxxxxxxxxx xxxxxx x x xxxxxxx, xx během xxxxxxxxxxxx xxxxxx xxxxxxx k xxxxxxx xxxxxxx x xxxxxx. Xxxxxxxxx xxxxxxxxx xx xxxxxxxxx xx xxxxxxxxx knihy x xxxxxxxx xxxx inventury, xxxx, xxxxxxxx, funkcí x podpisů osob, xxxxx xxxxxxxxx xxxxxxxxx. X xxxxxxx x xxxxxxxxx inventury xx xxxxx xxxxxxxxx xxxx xxxxxxxxxxx xxxxxx, celkový xxxxxx x xxxxx x xxxx xx xxx inventury x xxxxx xxxxxxxxxxx xxxxxxx. Xxxxxx-xx xx xxx xxxxxxxxx rozdíl mezi xxxxxxxxx x xxxxxxxxxx xxxxxx, xxxxxx xx xxxxxxxxxx protokol, xx xxxxxx xx xxxxxx xxxxxxxx rozdíly xxxxxx xxxxxx xxxxxxxxxx, xxxx xxxxx, xxxxx x xxxxxxxx, xxxxxx a xxxxxx xxxx, které xxxxxxxxx inventuru xxxxxx xxxxxxxxx xxxxx, byla-li xxxxxxxxxx. X xxxxxxx, xx xxxxxx ustanovena xxxxxxxxx xxxxx, xxxxxxxxxx xxxxxx o xxxxxxxxx xxxxxxxx xxx xxxxxxxxxx, xxxxxxx-xx požadavky xxxxxxx xx odpovědnou osobu xx xxxxxx §8 xxxx. 6 xxxxxx.
(5) Xxxxxx xxxxxxxxxxx xxxxxxx se xxxxxxxxx xxx, aby bylo xxxxx zjistit obsah xxxxxxxxx xxxxxxx a xxxxxxxx xxxxxx se xxxxxx xxxxx a xxxxxx, xxxxxxxxx, xxxxxx x podpisem osoby, xxxxx xxxxxx xxxxxxx xxxxxxxx.
§3
Xxxxxxxxx xxxxx
(1) Evidenční xxxxx xxxx xxxxxxxxx:
x) xxxxx x xxxxxxxx, popř. xxxxxxxx xxxxx (xxxx xxx "xxxxx"), x xxxxx xxxxxxxxx, xxxx. xxxxxx xxxxx xxxxxxxx xxxxxx xxxx adresu bydliště x xxxxxxxx xxxxx Xxxxxxxx xxxx (xxxx xxx "xxxxxxxx") xxxxxxxxxxx xxxxxxx osoby xxxx xxxxxxxx xxxxx xxxx xxxxx x xxxxx xxxxxxxxx xxxxx, která xxxxxxxxx xxxxxxx, x xxxxx je evidence xxxxxx, xxxxxxxxx označení xxxxxxxxxxx xxxxxx xxxx xxxxxxxx, které xx xxxxxxxx xxxx,
x) xxxxx x příjmení xxxxxxxxx xxxx, xxxxx xxxxxxxx xxxxxxxxx xxxxxxx xx evidenčních xxxx, xxxxxx xxxxxxxx a xxxxxxxxx xxxx x xxxxx, od kdy xxxx xxxxx xxxxxxxxx xxxxxxxxx záznamy,
x) xxxxx xxxxxxx evidenční xxxxx do xxxxxxxxx x ukončení používání,
x) xxxxx xxxxx x xxxxxxxx xxxxx xxxxxxx x xxxxxxxxxx xxxxx,
x) xxxxxx xxxxxxxxxxx xxxxxxxxxx xxxxx, xxxxxxxxx x xxxxxxxxxx x uvedením xxxxx xxxxx xxxxxxxxxxx xxx xxxxxxxxx xxxxxxxxxxxx xxxxxxxxxx xxxxx, xxxxxxxxx a xxxxxxxxxx s xxxxxxxx xxxxxxxxx xxxxx pro xxxxxxx.
(2) Xxxxxxxxx xxxxx xxxxx být xxxxxx samostatně xxx xxxxxxxxxx xxxxxxxxxxx složky.
§4
Xxxxxxxx xxxxxx xxxxxxxxx xxxxxxxx
(1) Xxxxxx hromadně xxxxxxxx xxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxx xxxxxxx v přílohách č. 2, č. 6 xxxx č. 7 xxxxxx, nebo léčivé xxxxxxxxx obsahující omamné xxxxx xxxxxxx x příloze č. 1 zákona x xxxxxxxx xxxxxxx i x příloze č. 8 xxxxxx xxxx xxxxxx xxxxxxxxx xxxxxxxxxx efedrin nebo xxxxxx přípravky obsahující xxxxx xxxxxxxx než 30 xx pseudoefedrinu x xxxxxxxx lékové xxxxx xxx xxxxxxxx xxxxxx xxxxxxxxx techniky, xxxxx bude xxxxxxxx xxxxxxx
a) xxxxxx xxxxx bezpečnostní xxxxx xxxxxxxx xxxxxxx,
x) xxxxxxx ročně xxxxxxxx xxxxx datového xxxxxxx xx xxxxxxxxxxxxxxxx paměťové xxxxxx x výrobcem xxxxxxxxxxxx xxxxxxxxxx xxxxxx xxxxxxx 5 xxx.
(2) Xxxxxxxx xxxxxx xxxxxxxxx xxxxxxxx xxxx xxx xxxxxx xxx, xxx umožňovala samostatné xxxxx xxxxxxxxx xxxxxx x xxxxx xxxxx x xxxxxxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx obsahujících návykové xxxxx xxxxxxx x přílohách č. 2, 6 a 7 zákona, xxxxxxxx xxxxxxxxx obsahujících xxxxxx xxxxx xxxxxxx x příloze č. 1 xxxxxx x xxxxxxxx xxxxxxx i x příloze č. 8 xxxxxx x xxxxxxxx přípravků xxxxxxxxxxxx xxxxxxx xxxx xxxxxxxxxxxxx x umožněním xxxxxx xxxxxxxx xxxxxxxx xx xxxx 5 xxx.
(3) Xxxxxxxx xxxxxx xxxxxx výpočetní xxxxxxxx xxxx xxxxxxxxx:
x) xxxxx přípravku,
x) xxxxx příjmu xxxx xxxxxx,
x) xxxxx dokladu x xxxxxx x xxxxxx,
x) xxxxx x xxxxxxxx podnikající xxxxxxx xxxxx xxxx obchodní xxxxx nebo xxxxx x xxxxx xxxxxxxxx xxxxx nebo xxxxxxxx x sídlo xxxx xxxxxxxxxxx xxxxxx, od xxxxx xxxx xxxxxxxxxx xxxxxxxxx přijaty, xxxx xxxxx x xxxxxxxx xxxxxxxxxxx fyzické xxxxx xxxx xxxxxxxx firmu xxxx xxxxx x xxxxx xxxxxxxxx xxxxx xxxx xxxxxxxx x xxxxx xxxx xxxxxxxxxxx xxxxxx, které xxxx xxxxxxxxxx xxxxxxxxx xxxxxx,
x) množství x xxxxx přijatých xxxx xxxxxxxx xxxxxxxxx,
x) xxxx xxxxx k xxxxxxxxxx dni xxxxxxxxxxx xxxxxx. Xxxxxxxxxx xxxxxxx xx pro xxxxx xxxx xxxxxxxx xxxxxx xxxxxxx xxxxxx xxxxx xxxxxx xxx xxxxxxxxx xxxxxxxx, xxxxxxxxx xxxxxxx (§26 zákona) x xxxxxxxxx xxxxxxxx (§34 xxxxxx).
(4) Pokud xx xxxxxxxx xxxxxx xxxxx odstavců 1 x 2, nemusí xxx xxxxxx xxxxx §3.
(5) Při xxxxxx xxxxxxxx pomocí xxxxxxxxx xxxxxxxx xx xxxxxxx inventura podle xxxxx k xxxxxxxxxx xxx xxxxxxxxxxxx xxxxxxxxx. X xxxxxxxxx inventury xx xxxxxx inventurní xxxxxxxx xxxxxxxxxx náležitosti xxxxx §2 odst. 4 xxxxxx xxxxxxx xxxxxxxxxxx xxxxx xxxxxxxxxxx xxxxxx, xxxxxxxxx xxxxxx x xxxxxx x xxxxx xxxxx xx xxx xxxxxxxxx x xxxxx xxxxxxxxxxx xxxxxxx.
(6) Xxxxxxx xxxxx xxx xxxxxxxx pomocí xxxxxxxxx xxxxxxxx přiměřeně xxxxx odstavců 1 x 2. Xxxxxxxx xxxx obsahovat:
x) x pomocných xxxxx xxxxxxxxx x příloze č. 10 xxxxxx x xxxxxxxx xxxxxx x xxxxxxx xx trh xxxxxxxxxxxx xxxxxxxxxx: xxxxx pomocné xxxxx, xxxxx příjmu xxxx xxxxxx, xxxxx xxxxxxx o xxxxxx x xxxxxx, jméno x bydliště podnikající xxxxxxx osoby xxxx xxxxxxxx xxxxx xxxx xxxxx a sídlo xxxxxxxxx xxxxx nebo xxxxxxxx a sídlo xxxx xxxxxxxxxxx xxxxxx, xx které xxxx xxxx xxxxx xxxxxxx, xxxx xxxxx x xxxxxxxx xxxxxxxxxxx xxxxxxx xxxxx xxxx obchodní xxxxx xxxx xxxxx x xxxxx xxxxxxxxx xxxxx nebo xxxxxxxx x xxxxx xxxx xxxxxxxxxxx složky, xxxxx xxxx xxxx xxxxx xxxxxx, množství xxxxxxx, xxxxxx xxxx vyrobené x xxxx xxxxx,
x) u xxxxxxxxx xxxxx xxxxxxxxx x příloze č. 11 xxxxxx obdobné xxxxx xxxx u xxxxxxxxx xxxxx xxxxxxxxx x příloze č. 10 xxxxxx, xxxxx stavu xxxxx x xxxxxxxxxx xxxxxxxx.
(7) Xx vedení xxxxxxxx podle xxxxxxxx 6 se xxxxxxxxxx xxxxxxxxx provádět xxxxxxxxx xxxxx odstavce 5.
§5
Vedení xxxxxxxx x xxxxxxxxx
(1) V lékárně xx xxxx při xxxxxxxxx x xxxxxxxxxx xxxxxxx, xxxxxxxxx x xxxxxxxxxx, xx kterému xx xxxxxxxxxx povolení x xxxxxxxxx (§5 x 6 xxxxxx), xxxxxxxx x xxxxxxxxxx xxxxxxx zařazených do přílohy č. 1 nebo č. 5 xxxxxx včetně xxxxxxxxx xx obsahujícíchzpůsobem stanoveným x odstavci 2, x výjimkou xxxxxxxx xxxxxxxxx xxxxxxxxxxxx xxxxxx xxxxx uvedené x příloze č. 1 xxxxxx a xxxxxxxx uvedené i x příloze č. 8 zákona.
(2) Vzor xxxxx xxxxxxxxx xxxxx x xxxxxx xxxxxxxx xxxxx xxxxxxxx 1 stanoví příloha č. 2 této xxxxxxxx.
(3) X lékárně xx xxxx xxx xxxxxxxx xxxxxxxxxx látek xxxxxxxxx x přílohách č. 2, 6 x 7 xxxxxx x přípravků xx xxxxxxxxxxxx, xxxxxxxxxx xxxxxxxxx x příloze č. 9 xxxxxx, přípravků xxxxxxxxxxxx xxxxxxx x xxxxxxxxx xxxxxxxxxxxx pseudoefedrin v xxxxxxxx xxxxxx xxx 30 mg x xxxxxxxx xxxxxx formy x xxxxxxxx xxxxx xxxxxxxxx v evidenci xxxxx xxxxxxxxxx právního xxxxxxxx.2a) Tuto xxxxxxxx xxx vést xxxxxx xxxxxxxxx techniky. Xxxxxxxx xxxxxxxx xxxx xxxxx:
x) název, x xxxxxxxxx xxxxxx xxxx xxxx2b) x velikosti xxxxxx,
b) xxxxx xxxxxx x xxxxx xxxxxx,
x) xxxxx xxxxxxx o xxxxxx,
x) množství xxxxxxx x xxxxxxxx xxxxxx,
x) xxxxxxxx stav xxxxx.
(4) Je-li xxxxxx xxxxxxxx xxxxx xxxxxxxx 3, xxxx xxxxxxxxx xxxxxxxx xxxxxxxxx xxxxx §2 odst. 4.
§6
Xxxxxx xxxxxxxx x xxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxxx, x xxxxxxxxxx xxxxxxxx péče x xxx xxxxxxxxxxx xxxxxxxxxxx péče
(1) X ostatních zdravotnických xxxxxxxxxx, v xxxxxxxxxx xxxxxxxx xxxx x xxx xxxxxxxxxxx xxxxxxxxxxx xxxx xx vede xxx zacházení x xxxxxxxxxx xxxxxxx, xxxxxxxxx x prekursory, xx xxxxxxx se nevyžaduje xxxxxxxx x zacházení (§4 zákona), xxxxxxxx x hromadně xxxxxxxxxx xxxxxxxx xxxxxxxxxxx obsahujících xxxxxxxx xxxxx xxxxxxx x příloze č. 1 xxxx č. 5 xxxxxx.
(2) Xxxxxx listu xxxxxxxxx xxxxx x xxxxxx xxxxxxxx xxxxx odstavce 1 xxxxxxx příloha č. 3 xxxx vyhlášky.
§6a
Xxxxxx xxxxxxxx xxxxxxxxxx látek xxxxxxxxxx xxxxxxxxx x. 3 x 4 xxxxxx a xxxxxxxxx xx xxxxxxxxxxxx
(1) Xxxxxxxxx osoby x xxxxxxx xxxxx - xxxxxxxxxxx vedou o xxxxxxxxx s xxxxxxxxxx xxxxxxx uvedenými v přílohách č. 3 x 4 xxxxxx a x xxxxxxxxx xx xxxxxxxxxxxxxx xxxxxxxx.
(2) Xxxxxx xxxxx xxxxxxxxx xxxxx x vedení xxxxxxxx xxxxx xxxxxxxx 1 xxxxxxx příloha č. 6 xxxx xxxxxxxx.
§6x xxxxxx xxxxxxx předpisem č. 143/2000 Xx. x xxxxxxxxx xx 1.7.2000
§6x
Xxxxxx xxxxxxxx xxx xxxxxxxxx x xxxxxxxxxx xxxxxxx, xxxxxxxxx xxxx xxxxxxxxxx xxx xxxxxxxx x xxxxxxxxx
(1) Při xxxxxxxxx x xxxxxxxxxx xxxxxxx, přípravky xxxxxxxxxxxx xxxxxxxx xxxxx xxxxxxx x příloze č. 1 nebo č. 5 xxxxxx nebo xxxxxxxxxx u xxxx xxxxxxxxx x §5 xxxx. 7 xxxx x §6 xxxx. 3 xxxxxx se xxxxx xxxxxxxxx záznamy.
(2) Vzor listu xxxxxxxxx xxxxx xxxxxxx příloha č. 5 xxxx vyhlášky.
§6x xxxxxx xxxxxxx xxxxxxxxx x. 363/2004 Xx. x xxxxxxxxx xx 1.7.2004
Evidence při xxxxxx, xxxxxxxxxx, xxxxxx x xxxxxxxxxx návykových xxxxx, přípravků nebo xxxxxxxxxx na základě xxxxxxxx x xxxxxxxxx x xxxx
§7
(1) Xxx výrobě, xxxxxxxxxx nebo xxxxxx xxxxxxxxxx látek, xxxxxxxxx xxxx xxxxxxxxxx na xxxxxxx xxxxxxxx x xxxxxxxxx x xxxx xx xxxxx evidenční xxxxxxx x xxxxxxxxxx xxxxxxx, xxxxxxxxxxx nebo xxxxxxxxxxxx
x) vyrobených,
x) xxxxxxxxx,
x) xxxxxxxxxxxx,
x) vyskladněných,
x) přepracovaných,
f) xxxxxxxxxxxxxx při xxxxxx xxxxxx návykových xxxxx, xxxxxxxxx xxxx látek, xxxxx xxxxxx xxxxxxxxxx xxxxxxx,
g) vykázaných xxxx ztráty xxxx xxxxx xxxxxxxxxxxxx technologickým xxxxxxxxx o xxxxxx,
x) předaných ke xxxxxxxxxxx xxxx zneškodněných,
x) chybějících nebo xxxxxxxxxxxxx x xxxxxxxx xxxxxx.
(2) Vzor xxxxx xxxxxxxxx xxxxx xxxxxx xxxxxxxxx, xxxxx xxxxxxxx xxxxxxxx xxxxx, xxxxxxx příloha č. 4 této xxxxxxxx.
(3) Xxxx xxxxx xxxxxxxxx xxxxx xxxxxxxxxx xxxxxxxxxx látek, xxxxxxxxx x xxxxxxxxxx xxx osoby, které xx xxxxxxx xxxxxxxx x xxxxxxxxx xxxxxxxx, xxxxxxxxxxxx xxxx balí xxxxxxxx xxxxx, xxxxxxxxx xxxx xxxxxxxxxx, stanoví příloha č. 5 xxxx xxxxxxxx.
§8
(1) Xxx skladování návykových xxxxx, xxxxxxxxx xxxxxxxxxxxx xxxxxxxx xxxxx xxxxxxx x příloze č. 1 xxxx č. 5 xxxxxx nebo xxxxxxxxxx xx základě xxxxxxxx k xxxxxxxxx x xxxx, xxxxx xxxxx x postup xxxxx §5, 6, 6a nebo §7, xx xxxxx xxxxxxxxx xxxxxxx o xxxxxxxxxx xxxxxxxxxx látek, přípravků xxxx xxxxxxxxxx.
(2) Xxxx xxxxx xxxxxxxxx xxxxx skladování xxxxxxxxxx xxxxx, xxxxxxxxx x xxxxxxxxxx xxxxxxx příloha č. 5 xxxx vyhlášky.
XXXX XXXXX
XXXXXXXXXXX
§9
(1) Xxxxxxxxxxx zacházení x xxxxxxxxxx xxxxxxx, přípravky, xxxxxxxxxx x xxxxxxxxx xxxxxxx tvoří:
x) xxxxxxxxx xxxxx,
x) xxxxxx xxx xxxxxxxxxx xxxx evidence xxxxxx xxxxxx xxxxxxxxx xxxxxxxx,
x) xxxxxxxxxx xxxxxxxxx,
x) xxxxxx x xxxxxxxxxxx návykových látek, xxxxxxxxx, prekursorů (§14 xxxxxx) x xxxxxxxxx xxxxx xxxxxxxxx v příloze č. 10 xxxxxx,
x) xxxxxxxxx x xxxxxx xxxx xxxxxxx xxxxxxxx xxxxx, xxxxxxxxx, xxxxxxxxxx xxxx xxxxxxxxx látek xxxxxxxxx v příloze č. 10 xxxxxx,
f) xxxxxx x xxxxxxxxxxx kontrolách (§34 xxxxxx),
x) xxxxxxx xxxxxx xxxxxxxxxx xxxxxx xxxxxxxxxxxx xxxxxxxx xx xxxxxxxxx s xxxxxxxxxx látkami, přípravky x xxxxxxxxxx x xxxxxx vývozu x xxxxxx, a xxxx xxxxxx x xxxxxx xxxxxxxx,
x) xxxxxxx xxxxxx xxxxxxxxxx (§16 xxxx. 6 xxxxxx) xxxxxxxx se xxxxxxxxxx xxxxxxx, xxxxxxx, dovozců x prodejců xxxxxxxxx xxxxx a veškerá xxxxxxxxxx, xxxxxx rozhodnutí xxxxxxxxx xxxxxxxxxxx orgány xxxx Evropských společenství xxxx xxxxxxx xxxx, xxxxxxxxxx xx xxxxxx xxxxxx xxxx xxxxxx,
x) xxxxxxxx xxxxxxxxx, xxxx xxxx faktury, xxxxxxxx xxxxx, xxxxxxxxx x jiné xxxxxx xxxxxxx, xxxxxxx zboží, xxxxxxxxxxxxxxx xxxxxxxxx, xxxxxx xxxxx, xxxxx xxxxxxx, xxxxx xxxxxxxx dostatečné xxxxxxxxx pro xxxxxxxxxxx xxxxxxxxxxxx: xxxxx xxxxxxxxxx xxxxx xxxx xxxxxxxxxx, xxx xxxx xxxxxxx x xxxxxxxxx xxxxxx, xxxxxxxx a xxxxxxxxx xxxxxxxxxx xxxxx, xxxxx x xxxxxxxx xxxxxxxxx xxxxxxxxxxxx xxxxxxxx látky, xxxxx a xxxxxxxx xxxxxxxxx xxxxxxxxxxxx efedrin xxxx xxxxxxxxx xxxxxxxxxxxx xxxxxxxxxxxxx v xxxxxxxx xxxxxx xxx 30 xx x xxxxxxxx xxxxxx xxxxx, množství x xxxxxxxxx xxxxxxxxxx, x xxxxxxx xxxxx xxxxxxxx x xxxxxxxx xxxxxxx x xxxxxx xxxxxxxx x hmotnost xxxx xxxxxxxxxxxx xxxxx xxxxxxxxxx, xxxxx xxxx xx výrobku xxxxxxxx [xxxxxxxxxx xxxxxxx xxxxx §1 xxxx. 2 xxxx. x) xxxxxx], xxxxx a bydliště xxxxxxxxxxx xxxxxxx xxxxx xxxx obchodní xxxxx xxxx xxxxx a xxxxx xxxxxxxxx xxxxx, xxxxx xxxxxxxxx x xxxxxxxxxx xxxxxxx, xxxxxxxxx x prekursory,2c)
x) xxxxxxx x xxxxxxxx, xxxxxxx xx vyřazení xxxxxxxxxxxx, xxxxxxxxxxx xxxxx x xxxxxxxxxxxx kotle,
x) xxxxxxxx xxxxxxxxxx xxxxxxxxxx podle xxxxxxxxxx xxxxxxxx předpisu2d) xx xxxxxxxxxx x xxxxxxx xxxxx uvedené x příloze č. 10 xxxxxx,
x) xxxxxx registrace (§16 xxxx. 1 zákona), xxxxxxxx xxxxxxxxx, xxxx xxxx faktury, xxxxxxxx xxxxx, xxxxxxxxx a xxxx xxxxxx xxxxxxx, xxxxxxx xxxxx, xxxxxxxxxxxxxxx xxxxxxxxx, xxxxxx listy, xxxxx doklady, které xxxxxxxx xxxxxxxxxx xxxxxxxxx xxx spolehlivou identifikaci: xxxxx pomocných látek, xxx jsou xxxxxxx x xxxxxxxxx xxxxxx, xxxxxxxx x xxxxxxxxx xxxxxxxxx xxxxx, v xxxxxxx xxxxx xxxxxxxx x hmotnost výrobku x xxxxxx množství x xxxxxxxx xxxx xxxxxxxxxxxx xxxxx xxxxxxxxx xxxxx, které jsou xx xxxxxxx obsaženy, xxxxx x xxxxxxxx xxxxxxxxxxx xxxxxxx osoby xxxx obchodní xxxxx xxxx xxxxx x xxxxx xxxxxxxxx xxxxx, xxxxx xxxxxxxxx x xxxxxxxxx látkami včetně xxxxxxxxx příjemce.2c)
(2) X lékárně se xxxxxxxx xxxxx xxxxxxxxxxx xxxxxxx x xxxxxxxx 1 první xxxxxxx xxxxxxxxxx předpisů, případně x xxxxx xxxxx xxxxxxxxxx xxxxxxxx x xxxxxx xxxxxx a xxxxx xxxxxx žádanky x xxxxxx pruhem (§13 xxxx. 2 xxxxxx).
§10
Xxxxxxxxx x xxxxxx
Xxx xxxxxxxxxx protokolů x xxxxxx podle §9 xxxx. 1 xxxx. x), x) x x) se xxxxxxxxx xxxxx společných xxxxxxxxxx xxx xxxxxx xxxxxxxxxxx xxxxxxx (§2). Xxxxxx xxxxx §9 xxxx. 1 písm. c), x), x) xxxx x) xxxx xxxx xxxxxxxx xxxxxxxxx xxxxx (§9 xxxxxx). X xxxxxxx, xx xxxxxx xxxxxxxxxx xxxxxxxxx xxxxx, xxxxxxxxxx xxxxx xxx xxxxxxxxxx, xxxxxxx-xx xxxxxxxxx xxxxxxx xx xxxxxxxxxx xxxxx ve xxxxxx §8 xxxx. 6 xxxxxx. X xxxxxxx xxxxxxxxx látek zápisy x protokoly xxxxx §9 xxxx. 1 xxxx. x) x x) xxxxxxxxxx xxxxx xxxxxxxxx jednat za xxxxxxxxxx xxxxx xxxx xx xxxxxxxx xxxxx xxxx xxxxx xxxx xxxxxxx pověřená.
§11
Uchovávání xxxxxxxxxxx
(1) Xxxxxxxxxxx xx xxxxxx xxx, xxx xxxx xxxxxxxxx xxxx ztrátě, zničení xxxx xxxxxxxx x xxxxxxxx jejího xxxxxxxx.
(2) Xxxxxxxxxxx xxxxxxxxxx xx x zacházení
x) s xxxxxxxxxx xxxxxxx x přípravky x xxxxxx obsahem xx uchovává xx xxxx 5 xxx (§33 xxxx. 1 xxxxxx) od xxxxxxxx xxxxxxxxx, popřípadě xx xxxxxxxxxx xxxxxxx x xxx podle toho, xxxxx x xxxxxx xxxxxxxxxxx nastala xxxxxxx,
§12
Xxxxxxxx
Xxxx xxxxxxxx nabývá xxxxxxxxx xxxx 1. xxxxx 1999.
Xxxxxxx:
XXXx. David, XXx. x. r.
Xxxxxxx č. 1 k xxxxxxxx x. 304/1998 Sb.
Xxxxxxx x. 1 xxxxxxx xxxxxxx xxxxxxxxx x. 363/2004 Xx.
Xxxxxxx x. 2 x vyhlášce x. 304/1998 Sb.
Xxxxxxx č. 3 x xxxxxxxx č. 304/1998 Xx.
Xxxx xxxxx xxxxxxxxx xxxxx ostatních xxxxxxxxxxxxxx zařízení, xxxxxxxx xxxxxxxx xxxx a xxx xxxxxxxxxxx xxxxxxxxxxx xxxx
|
Xxxxx OL X*, XX XX* (xxxx, xxxx a xxxxxxxx):
|
||||||
|
Xxxxx
|
Xxx xxxxxx
|
Xxxxxxx: lékař
|
Příjem
|
Výdej
|
Stav xxxx
|
|
|
xxxxxx xxxx
|
xxxxx xxxxx a x. xxxxxxx
|
xxxxxxxxx
|
xxxx xxxxxx
|
&xxxx; | &xxxx; |
xxxxxxx, xxxxxx xxxx.
|
|
xxxxx
|
Xxx xxxxxx
|
&xxxx; | &xxxx; | &xxxx; | &xxxx; | |
| &xxxx; |
x. xxxxxxxxx
|
xxxxxxx
|
&xxxx; | &xxxx; | &xxxx; | &xxxx; |
|
1
|
2
|
3
|
4
|
5
|
6
|
7
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
* OL X - omamné látky xxxxxxx x příloze č. 1 xxxxxx x. 167/1998 Xx.
* PL XX - psychotropní xxxxx xxxxxxx v xxxxxxx x. 5 zákona x. 197/1998 Sb.
Příloha x. 4 x xxxxxxxx x. 304/1998 Xx.
Xxxx xxxxx xxxxxxxxx xxxxx výroby xxxxxxxxx, xxxxx xxxxxxxx xxxxxxxx látky (XX)
|
Xxxxxxxx xxxxx xxxxxx
|
Xxxxxx xxxxx xxxxxxxx ze skladu
|
Číslo xxxxxxxx šarže
|
Datum xxxxxxx xx xxxxxx hotových xxxxxxx
|
Xxxxxxxx xxxxxxx skladu, x xxxxx balení XX, xxxxxxxxxx
|
Xxxxxxxx xxxxxxx xxxxxx x x
|
Xxxxx x x NL, xxxxxxxxxx, použitelný x xxxxx xxxxxx xxxx xxxxxxxxxxxx
|
Xxxxxxxx
|
Xxxxxxx xxxxxx xxxxxxxxxx xxxxxxxxxxxxx xxxxx
|
| &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; |
| &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; |
| &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; |
| &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; |
| &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; |
| &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; |
| &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; |
| &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; |
| &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; |
| &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; |
Příloha x. 5 x xxxxxxxx x. 304/1998 Sb.
Vzor xxxxx xxxxxxxxx knihy xxxxxxxxxx
|
Xxxxx xxxxxxxx xxxxx (XX), xxxxxxxxx x prekursoru
|
||||||
|
Datum xxxxxx x xxxxxx
|
Xxxxx xxxxxxx (xxxxxxxxxx x xxxxxxxxx xxxxx)
|
Xxxxx šarže
|
Jméno x xxxxxx xxxxxxxxxx xxxx xxxxxxxx
|
Xxxxxxxx přijatých XX, přípravků x xxxxxxxxxx
|
Xxxxxxxx xxxxxxxx NL, xxxxxxxxx x prekursorů
|
Stav xxxxx x&xxxx;xxxxxxxxxxx datu
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Jednotkou xxxxxxxx xx x XX a prekursorů xxxx x u xxxxxxxxx 1 xxxxxx.
Xxxxxxx x. 6 x xxxxxxxx č. 304/1998 Sb.
Vzor listu xxxxxxxxx xxxxx skladování
Název xxxxxxxx xxxxx (XX) xxxxxxx x xxxxxxxxx x. 3 a 4 zákona
Název přípravku xxxxxxxxxxxx xxxxxxxx látky xxxxxxx v přílohách x. 3 a 4 xxxxxx
|
Xxxxx
|
Xxxxx xxxxxxx
|
Xxxxx x xxxxxx
|
Xxxxxxxx
|
Xxxxxxxx
|
Xxxxxxxx
|
Xxxx xxxxx
|
Xxxxx xxxxx
|
|
xxxxxx
|
(xxxxxxxxxxx a
|
dodavatele
|
množství
|
přijatých XX
|
xxxxxxxx XX
|
x příslušnému
|
atest XXXX
|
|
x xxxxxx
|
xxxxxxxxxx xxxxx)
|
xxxx příjemce
|
|
a xxxxxxxxx
|
x xxxxxxxxx
|
xxxx
|
&xxxx;
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
Xxxxxxx x. 6 xxxxxxx právním xxxxxxxxx x. 143/2000 Xx. x xxxxxxxxx xx 1.7.2000
Příloha x. 7 x xxxxxxxx x. 304/1998 Xx.
Xxxxxxx x. 7 xxxxxxx právním xxxxxxxxx x. 363/2004 Xx.
Příloha č. 8 x xxxxxxxx č. 304/1998 Sb.
Roční xxxxxxx xxxxxxxx xxx osoby, xxxxx hodlají xxxxxx xx xxx xxxxxxx xxxxx uvedené x příloze č. 10 xxxxxx (§12 xxxx. 3 x §32 xxxx. 6 xxxxxx)
|
Xxxxxxxxxxx xxxxxxxxxx xxxxx (XXX) v xxxxxx xxxxxx
|
Xxxxxxxx
|
|
Xxxxxxxx kyseliny octové
|
20 xxxxx
|
|
Xxxxxxxx antranilová
|
1 kg
|
|
Kyselina xxxxxxxxxxx
|
1 xx
|
|
Xxxxxxxxx
|
0,5 kg
|
Včetně xxxx xxxxxxxxx xxxxx xx xxxxx případech, xxx xxxxxxxxx xxxxxxxx xxxx xx možná.
Platí x xxx xxxxx xxxxxx xxxxx při xxxxxxxx na xxxxx xxxxx látky, xxxxx xx x xxxx xxxxx xxxxxxxx.
Xxxxxxx x. 8 vložena xxxxxxx xxxxxxxxx x. 363/2004 Xx. x xxxxxxxxx xx 1.7.2004
Xxxxxxx x. 9 x xxxxxxxx x. 304/1998 Xx.
Xxxxxxx xxxxxxxx xxx osoby, které xxxxxxx xxxxxxx anhydrid xxxxxxxx octové xxxx xxxxxxxxxxx xxxxxxxx vztahující xx x oznámení x předpokládaném vývozu (§20b xxxx. 2 xxxxxx)
|
Xxxxxxxxxxx xxxxxxxxxx xxxxx (XXX) v xxxxxx xxxxxx
|
Xxxxxxx xxxxxxxx x xx (xxxxxx)
|
|
Xxxxxxxx xxxxxxxx xxxxxx
|
100
|
|
Xxxxxxxxxxx xxxxxxxx
|
100
|
Xxxxxxx č. 9 xxxxxxx xxxxxxx xxxxxxxxx x. 363/2004 Xx. s xxxxxxxxx xx 1.7.2004
Informace
Xxxxxx předpis x. 304/98 Xx. nabyl xxxxxxxxx xxxx 1.1.1999.
Xx znění xxxxxx xxxxxxxx předpisu xxxx xxxxxxxxxx změny x xxxxxxxx uskutečněné xxxxxxx xxxxxxxxx č.:
143/2000 Xx., xxxxxx se xxxx xxxxxxxx x. 304/98 Xx., kterou xx xxxxxxx xxxxxxx, xxx xx xxxxxxxxxx xxxxxxx xxxxxxxx x xxxxxx xxxxxxxxx xxxxx, xxxxxxxxxxx x evidenci xxxxxxxxxx xxxxx, xxxxxxxxx x xxxxxxxxxx a x xxxxxxxxxxx xxxxxxxxxx xxxxx
x xxxxxxxxx xx 1.9.2000
82/2002 Xx., xxxxxx xx xxxx xxxxxxxx č. 304/98 Sb., xxxxxx xx stanoví xxxxxxx, xxx xx xxxxxxxxxx xxxxxxx xxxxxxxx k xxxxxx xxxxxxxxx xxxxx, xxxxxxxxxxx x evidenci xxxxxxxxxx xxxxx, přípravků x xxxxxxxxxx x x xxxxxxxxxxx xxxxxxxxxx xxxxx, xx xxxxx xxxxxxxx č. 143/2000 Xx.
x účinností xx 6.3.2002
363/2004 Sb., xxxxxx xx mění vyhláška x. 304/98 Sb., xxxxxx xx xxxxxxx xxxxxxx, kdy xx xxxxxxxxxx vývozní xxxxxxxx x xxxxxx pomocných xxxxx, xxxxxxxxxxx o xxxxxxxx xxxxxxxxxx látek, xxxxxxxxx x xxxxxxxxxx x x xxxxxxxxxxx xxxxxxxxxx látek, ve xxxxx xxxxxxxxxx xxxxxxxx
x účinností xx 1.7.2004
Xxxxxx xxxxxxx x. 304/98 Xx. xxx xxxxxx xxxxxxx xxxxxxxxx č. 123/2006 Sb. x xxxxxxxxx xx 1.5.2006.
Xxxxx xxxxxxxxxxxx xxxxxxxx xxxxx xxxxxx xxxxxxxx xxxxxxxx x odkazech není xxxxxxxxxxxxx, xxxxx xx xxxx netýká derogační xxxxx xxxxx xxxxxxxxx xxxxxxxx předpisu.
1) Směrnice Xxxx 92/109/EHS xx xxx 14. xxxxxxxx 1992 x výrobě xxxxxxxx xxxxx xxxxxxxxxxx k xxxxxxxxxx výrobě omamných x xxxxxxxxxxxxxx látek x x jejich xxxxxxx xx xxx.
Xxxxxxxx Xxxxxx 93/46/EHS xx xxx 22. xxxxxx 1993, kterou xx xxxxxxxxx x xxxx xxxxxxx xxxxxxxx Xxxx 92/109/XXX o xxxxxx xxxxxxxx xxxxx xxxxxxxxxxx x xxxxxxxxxx xxxxxx xxxxxxxx x psychotropních xxxxx x x xxxxxx xxxxxxx na xxx.
Xxxxxxxx Xxxx (EHS) č. 3677/90 xx dne 13. prosince 1990 x opatřeních, xxxxx xxxx xxx xxxxxxx xx xxxxxx zamezení xxxxxxxxxx xxxxxxxx xxxxx x xxxxxxxxxx výrobě xxxxxxxx x xxxxxxxxxxxxxx xxxxx, xx xxxxx xxxxxxxx Xxxx (XXX) x. 900/92 x xxxxxxxx Xxxx (XX) x. 988/2002.
Nařízení Komise (XX) č. 1485/96 xx xxx 26. xxxxxxxx 1996, xxxxxx se xxxxxxx xxxxxxxxx xxxxxxxx xx xxxxxxxx Xxxx 92/109/XXX, pokud xxx x xxxxxxxxxx odběratele x xxxxxxxxx xxxxxxx xxxxxxxx xxxxx xxxxxxxxxxx x xxxxxxxxxx výrobě xxxxxxxx x psychotropních xxxxx, xx znění xxxxxxxx Komise (XX) x. 1533/2000.
1x) Xx. 2 xxxx. 3 xxxxxxxx Xxxx (EHS) č. 3677/90.
1x) Xxxxx č. 101/2000 Sb., o xxxxxxx xxxxxxxx údajů x x změně xxxxxxxxx xxxxxx, xx xxxxx xxxxxxxxxx xxxxxxxx.
1x) Xx. 2 xxxx. 2 xxxxxxxx Xxxx (XXX) č. 3677/90.
1x) §2 xxxx. 3 x 11 zákona x. 79/1997 Xx. x xxxxxxxx x x xxxxxxx x doplnění xxxxxxxxx souvisejících xxxxxx.
2x) §21 xxxx. 1 písm. x) a g) xxxxxx č. 79/1997 Xx., xx xxxxx xxxxxx x. 149/2000 Xx.
2b) §3 xxxx. 5 písm. x) xxx 2 xxxxxxxx č. 343/1997 Xx., kterou xx xxxxxxx xxxxxx x xxxxxxxxxxxxx xxxxxxxx přípravků, xxxxxxxxxxx lékařských xxxxxxxx x xxxxxxxx jejich xxxxxxxxx.
2x) Xx. 2 xxxx. 1 xxxxxxxx Xxxx (XXX) č. 3677/90, xx xxxxx xxxxxxxx Xxxx (XXX) č. 900/92 x xxxxxxxx Xxxx (XX) x. 988/2002.
2x) Nařízení Komise (XX) č. 1485/96, xx xxxxx xxxxxxxx Xxxxxx 93/46/XXX a nařízení Xxxxxx (XX) x. 1533/2000.
3) §3 xxxx. 5 xxxx. x) xxxxxxxx x. 343/1997 Xx., xxxxxx xx xxxxxxx xxxxxx xxxxxxxxxxxxx léčivých xxxxxxxxx, xxxxxxxxxxx xxxxxxxxxx předpisů x xxxxxxxx xxxxxx xxxxxxxxx.
4) §3 xxxx. 6 vyhlášky x. 343/1997 Xx.
5) Čl. 2 xxxx. 4 xxxxxxxx Xxxx (XXX) č. 3677/90, xx znění xxxxxxxx Xxxx (XXX) č. 900/92.


