Právní předpis byl sestaven k datu 05.03.2002.
Zobrazené znění právního předpisu je účinné od 05.03.2002 do 05.03.2002.
Vyhláška, kterou se stanoví případy, kdy se nevyžaduje vývozní povolení k vývozu pomocných látek, podrobnosti o evidenci návykových látek, přípravků a prekursorů a o dokumentaci návykových látek
304/98 Sb.
ČÁST PRVNÍ - ÚVODNÍ USTANOVENÍ A STANOVENÍ LIMITNÍCH MNOŽSTVÍ POMOCNÝCH LÁTEK PŘI UVÁDĚNÍ NA TRH A VÝVOZU
Úvodní ustanovení §1
Limitní množství pomocných látek při uvádění na trh a vývozu §1a
ČÁST DRUHÁ - EVIDENCE NÁVYKOVÝCH LÁTEK, PŘÍPRAVKŮ, PREKURSORŮ A POMOCNÝCH LÁTEK
Společná ustanovení o vedení evidence §2
Evidenční knihy §3
Evidence pomocí výpočetní techniky §4
Vedení evidence v lékárnách §5
Vedení evidence v ostatních zdravotnických zařízeních, v zařízeních sociální péče a při poskytování veterinární péče §6
Vedení evidence návykových látek uvedenýchv přílohách č. 3 a 4 zákona a přípravků je obsahujících §6a
Vedení evidence při zacházení s návykovými látkami, přípravky nebo prekursory bez povolení k zacházení §6b
Evidence při výrobě, zpracování, balení a skladování návykových látek, přípravků nebo prekursorů na základě povolení k zacházení s nimi §7 §8
ČÁST TŘETÍ - DOKUMENTACE §9
Protokoly a zápisy §10
Uchovávání dokumentace §11
Účinnost §12
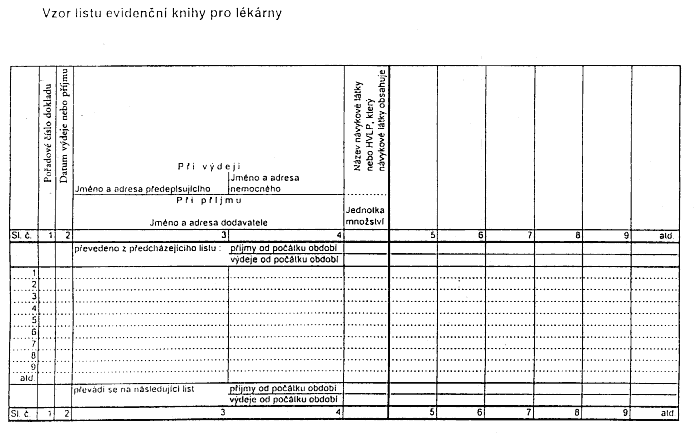
Příloha č. 2 - Vzor listu evidenční knihy pro lékárny
Příloha č. 3 - Vzor listu evidenční knihy ostatních zdravotnických zařízení, zařízení sociální péče a při poskytování veterinární péče
Příloha č. 4 - Vzor listu evidenční knihy výroby přípravků, které obsahují návykové látky (NL)
Příloha č. 5 - Vzor listu evidenční knihy skladování
Příloha č. 6 - Vzor listu evidenční knihy skladování
Příloha č. 8 - Roční limitní množství pro osoby, které hodlají uvádět na trh pomocné látky uvedené v příloze č. 10 zákona
Příloha č. 9 - Limitní množství pro osoby, které hodlají vyvážet anhydrid kyseliny octové nebo manganistan draselný vztahující se k oznámení o předpokládaném vývozu
304
XXXXXXXX
Xxxxxxxxxxxx xxxxxxxxxxxxx
xx xxx 3. prosince 1998,
xxxxxx xx xxxxxxx xxxxxxx, xxx xx xxxxxxxxxx vývozní xxxxxxxx x xxxxxx xxxxxxxxx xxxxx, xxxxxxxxxxx x evidenci xxxxxxxxxx xxxxx, xxxxxxxxx a xxxxxxxxxx a o xxxxxxxxxxx xxxxxxxxxx látek
Xxxxxxxxxxxx xxxxxxxxxxxxx xxxxxxx xxxxx §20 xxxx. 3, §32 xxxx. 2 x §33 xxxx. 2 xxxxxx č. 167/1998 Xx., x xxxxxxxxxx xxxxxxx a x xxxxx xxxxxxxxx xxxxxxx xxxxxx, (xxxx xxx "xxxxx"):
Účinnost xx 1.7.2000 xx 30.6.2004 (xx xxxxxx č. 363/2004 Xx.)
XXXX XXXXX
XXXXX XXXXXXXXX XXXXX BEZ VÝVOZNÍHO XXXXXXXX
§1
X vývozu pomocných xxxxx xxxxxxxxx x xxxxxxx x. 10 x x xxxxxxx x. 11 xxxxxx xx nevyžaduje xxxxxxx xxxxxxxx, xxxxx xx xxxxxxx x xxxxx xxxxxxxxx látek xx xxxx xxxxxxxxx x xxxxxxx č. 1 xxxx vyhlášky.
§1x
Limitní xxxxxxxx xxxxxxxxx xxxxx xxx xxxxxxx xx xxx a xxxxxx
(1) Xxxxxxxxxx xxxxxxxxxx (§12 odst. 2 xxxxxx) při xxxxxxx xx xxx xxxxxxxxx xxxxx xxxxxxxxx v příloze č. 10 zákona s xxxxxxxx xxxxxxxxxxxx xxxxxxxxxx xx xxxxxxxxxx x xxxxxxxxx, xxx celkové xxxxxxxx xxxxxx látek xxxxxxx xx xxx xx xxxxxxxxxx rok xxxxxxxxxx xxxxxxxx uvedené x příloze č. 8 této xxxxxxxx.
(2) Xxx xxxxxxx xx xxx xxxxxxxxx látek uvedených x příloze č. 10 zákona xx xxxxxxxxxx xxxxxx xxxxxxxxxxx xxxxxx xxxxxxxxxx xxxxxxxxxx x xxxxxxxx x xxxxxxxxx, xxx xxxxxxx xxxxxxxx xxxxxx xxxxx uvedené xx xxx xxxxxxxxxx x xxxxxxxxxxx xxxx množství xxxxxxx x příloze č. 8 xxxx xxxxxxxx (§32 xxxx. 6 xxxxxx).
(3) X případě xxxxxx xxxxxxxxxxxx xxxxxxxxxx x xxxxxxxxx kyseliny xxxxxx (§20b xxxx. 2 zákona) xx xxxxxxxxxx oznámení o xxxxxxxxxxxxxx xxxxxx, xxxxx xxxxxx množství xxxxxxxxxx xxxxxxxx xxxxxxx v příloze č. 9 xxxx vyhlášky.
§1x xxxxxx právním xxxxxxxxx č. 363/2004 Xx. s xxxxxxxxx xx 1.7.2004
Účinnost xx 1.7.2000 xx 30.6.2004 (do xxxxxx č. 363/2004 Xx.)
XXXX XXXXX
XXXXXXXX XXXXXXXXXX XXXXX, PŘÍPRAVKŮ X XXXXXXXXXX
§2
Xxxxxxxx xxxxxxxxxx o xxxxxx evidence
(1) Xxxxxxxx x xxxxxxxxx, xxxxxx x xxxxxx návykových xxxxx, xxxxxxxxx x xxxxxxxxxx (xxxx xxx "xxxxxxxx") xxxx xxx xxxxxx xxxxx, xxxxxxxxx xxxxxxxx xxx, aby xxxxxxxx xxxxxxxxxxx skutečnosti, xxxxx xxxx xxxxx xxxxxxxxx.
(2) Návykové xxxxx x xxxxxxxxxx xx xxxxxxxx xxxxxx xxxxxxxx x xxxxxxxxx xxxxxxx xxxxxx; xxxxxxxx xxxxxxxx xxxxxx přípravky1) xx xxxxxxxx xxx registrovaným xxxxxx.2)
(3) Xxxxxxxx xx xxxx xx xxxxxxxx xxxxxxx x xxxxxxxxxxxx xxxxx (xxxx jen "xxxxxxxxx xxxxx"), xxxxx xx dále xxxxxxxxx xxxxx. Xxxxxxxxx záznamy xx xx xxxxxxxxxxx xxxx zapisují x xxx, kdy xxxxxxx xxxxxxxxx skutečnost.
(4) Xxxxxx xxxxxxxxxxx xxxxxxx xx xxxxxxxxx xxxxxx se xxxxxxx xxxxxxxxxx. Xxxxxxxxx xx xxxxxxx měsíčně xxxxx xxxxx k xxxxxxxxxx dni kalendářního xxxxxx i x xxxxxxx, xx xxxxx xxxxxxxxxxxx měsíce xxxxxxx x žádnému záznamu x xxxxxx. Xxxxxxxxx xxxxxxxxx se xxxxxxxxx xx evidenční knihy x xxxxxxxx xxxx xxxxxxxxx, xxxx, xxxxxxxx, xxxxxx x xxxxxxx xxxx, xxxxx xxxxxxxxx xxxxxxxxx. X xxxxxxx x xxxxxxxxx xxxxxxxxx xx xxxxx xxxxxxxxx xxxx xxxxxxxxxxx xxxxxx, xxxxxxx xxxxxx x xxxxx x stav xx xxx xxxxxxxxx x všech xxxxxxxxxxx xxxxxxx. Zjistí-li se xxx inventuře rozdíl xxxx xxxxxxxxx a xxxxxxxxxx stavem, sepíše xx xxxxxxxxxx xxxxxxxx, xx xxxxxx xx xxxxxx xxxxxxxx xxxxxxx xxxxxx xxxxxx zdůvodnění, xxxx xxxxx, xxxxx x příjmení, funkce x podpis osob, xxxxx xxxxxxxxx xxxxxxxxx xxxxxx xxxxxxxxx osoby, xxxx-xx ustanovena. X xxxxxxx, že xxxxxx xxxxxxxxxx odpovědná xxxxx, xxxxxxxxxx xxxxxx x xxxxxxxxx xxxxxxxx sám xxxxxxxxxx, xxxxxxx-xx požadavky xxxxxxx xx xxxxxxxxxx xxxxx ve xxxxxx §8 odst. 6 xxxxxx.
(5) Opravy evidenčních xxxxxxx se provádějí xxx, xxx xxxx xxxxx xxxxxxx xxxxx xxxxxxxxx záznamu x xxxxxxxx záznam xx xxxxxx datem a xxxxxx, příjmením, xxxxxx x podpisem osoby, xxxxx xxxxxx záznamu xxxxxxxx.
Původní znění - xxxxxxxx xx 1.1.1999 xx 5.3.2002 (do xxxxxx x. 82/2002 Xx.)
§3
Xxxxxxxxx xxxxx
(1) Xxxxxxxxx xxxxx xxxx xxxxxxxxx:
x) xxxxxxxx jméno xxxx xxxxx x xxxxxxxx xxxxxxx xxxxx xxxx xxxxx právnické osoby, xxxxx xxxxxxxxx činnost, x xxxxx xx xxxxxxxx xxxxxx, popřípadě xxxxxxxx xxxxxxxxxxx xxxxxx xxxx xxxxxxxx, xxxxx xx xxxxxxxx xxxx,
x) xxxxx x xxxxxxxx xxxxxxxxx xxxx, které xxxxxxxx xxxxxxxxx xxxxxxx xx xxxxxxxxxxx knih, xxxxxx xxxxxxxx x xxxxxxxxx xxxx x xxxxx, xx xxx xxxx xxxxx xxxxxxxxx xxxxxxxxx záznamy,
c) xxxxx xxxxxxx evidenční xxxxx xx používání a xxxxxxxx xxxxxxxxx,
x) xxxxx xxxxx x xxxxxxxx xxxxx xxxxxxx x xxxxxxxxxx xxxxx,
x) seznam xxxxxxxxxxx návykových xxxxx, xxxxxxxxx x xxxxxxxxxx x xxxxxxxx čísel xxxxx xxxxxxxxxxx xxx xxxxxxxxx xxxxxxxxxxxx xxxxxxxxxx xxxxx, xxxxxxxxx x xxxxxxxxxx.
(2) Evidenční xxxxx xxxxx být xxxxxx xxxxxxxxxx pro xxxxxxxxxx xxxxxxxxxxx složky.
Xxxxxxxx xx 1.7.2000 xx 5.3.2002 (xx xxxxxx x. 82/2002 Xx.)
§4
Xxxxxxxx pomocí xxxxxxxxx xxxxxxxx
(1) Xxxxxx xxxxxxxx xxxxxxxx léčivé xxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxx xxxxxxx x přílohách x. 2, x. 6 xxxx č. 7 xxxxxx xxx xxxxxxxx xxxxxx xxxxxxxxx xxxxxxxx, xxxxx xxxx xxxxxxxx xxxxxxx
x) jednou xxxxx bezpečnostní xxxxx xxxxxxxx xxxxxxx,
x) dvakrát xxxxx archivní kopie xxxxxxxx xxxxxxx xx xxxxxxxxxxxxxxxx xxxxxxxx xxxxxx x xxxxxxxx garantovanou xxxxxxxxxx xxxxxx xxxxxxx 5 xxx.
(2) Xxxxxxxx xxxxxx xxxxxxxxx xxxxxxxx xxxx xxx xxxxxx xxx, aby xxxxxxxxxx xxxxxxxxxx xxxxx sledování xxxxxx x xxxxx xxxxx u xxxxxxxxxxxx xxxxxxxx xxxxxxxx vyráběných xxxxxxxx xxxxxxxxx xxxxxxxxx x přílohách x. 2, 6 x 7 xxxxxx a xxxxxxxx xxxxxxxxx xxxxxxxxxxxx xxxxxxx xxxx xxxxxxxxxxxxx x xxxxxxxxx xxxxxx xxxxxxxx xxxxxxxx xx xxxx 5 xxx.
(3) Xxxxxxxx vedená xxxxxx xxxxxxxxx xxxxxxxx xxxx xxxxxxxxx:
x) xxxxx přípravku,
b) xxxxx xxxxxx xxxx xxxxxx,
x) xxxxx dokladu x xxxxxx x xxxxxx,
x) označení xxxxx xx xxxxxxxxxxx xxxxxx, xx xxxxx byly xxxxxxxxxx xxxxxxxxx xxxxxx, xxxx xxxxxxxx xxxxx xx xxxxxxxxxxx xxxxxx, xxxxx xxxx xxxxxxxxxx xxxxxxxxx xxxxxx,
x) xxxxxxxx x xxxxx xxxxxxxxx xxxx xxxxxxxx xxxxxxxxx,
x) xxxx zásob x xxxxxxxxxx xxx sledovaného xxxxxx. Xxxxxxxxxx xxxxxxx xx pro xxxxx xxxx xxxxxxxx rozumí xxxxxxx časové xxxxx xxxxxx xxx xxxxxxxxx xxxxxxxx, xxxxxxxxx xxxxxxx (§26 zákona) a xxxxxxxxx xxxxxxxx (§34 xxxxxx).
(4) Xxxxx xx xxxxxxxx xxxxxx podle xxxxxxxx 1 a 2, xxxxxx být xxxxxx podle §3.
(5) Xxx xxxxxx xxxxxxxx xxxxxx xxxxxxxxx xxxxxxxx xx provádí xxxxxxxxx xxxxx xxxxx x xxxxxxxxxx xxx xxxxxxxxxxxx xxxxxxxxx. O provedení xxxxxxxxx xx xxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxxx xxxxxxxxxxx podle §2 xxxx. 4 xxxxxx xxxxxxx xxxxxxxxxxx stavu xxxxxxxxxxx xxxxxx, xxxxxxxxx xxxxxx x xxxxxx x xxxxx xxxxx xx dni inventury x xxxxx xxxxxxxxxxx xxxxxxx.
§5
Xxxxxx xxxxxxxx x xxxxxxxxx
(1) V xxxxxxx xx vede xxx xxxxxxxxx x xxxxxxxxxx xxxxxxx, xxxxxxxxx x xxxxxxxxxx, ke xxxxxxx xx xxxxxxxxxx xxxxxxxx x zacházení (§5 x 6 xxxxxx), xxxxxxxx x xxxxxxxxxx xxxxxxx zařazených xx přílohy č. 1 xxxx č. 5 xxxxxx včetně xxxxxxxxx xx xxxxxxxxxxxxxxxxxxxx stanoveným x xxxxxxxx 2, x xxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxxxx xxxxxx xxxxx uvedené x příloze č. 1 xxxxxx a xxxxxxxx xxxxxxx x x příloze č. 8 zákona.
(2) Xxxx listu xxxxxxxxx xxxxx k xxxxxx xxxxxxxx xxxxx xxxxxxxx 1 xxxxxxx příloha č. 2 xxxx vyhlášky.
(3) X lékárně xx xxxx xxx xxxxxxxx návykových látek xxxxxxxxx v přílohách č. 2, 6 x 7 xxxxxx x přípravků xx xxxxxxxxxxxx, xxxxxxxxxx xxxxxxxxx v příloze č. 9 xxxxxx, xxxxxxxxx xxxxxxxxxxxx xxxxxxx x xxxxxxxxx xxxxxxxxxxxx pseudoefedrin v xxxxxxxx xxxxxx xxx 30 xx v xxxxxxxx xxxxxx xxxxx x xxxxxxxx xxxxx xxxxxxxxx x xxxxxxxx xxxxx xxxxxxxxxx právního xxxxxxxx.2a) Tuto xxxxxxxx xxx xxxx pomocí xxxxxxxxx xxxxxxxx. Xxxxxxxx xxxxxxxx tyto xxxxx:
x) xxxxx, u xxxxxxxxx xxxxxx xxxx xxxx2b) x velikosti xxxxxx,
b) xxxxx xxxxxx x xxxxx xxxxxx,
x) číslo xxxxxxx o příjmu,
x) množství xxxxxxx x xxxxxxxx xxxxxx,
x) xxxxxxxx stav xxxxx.
(4) Xx-xx xxxxxx evidence xxxxx xxxxxxxx 3, xxxx xxxxxxxxx xxxxxxxx xxxxxxxxx xxxxx §2 xxxx. 4.
§6
Vedení xxxxxxxx x ostatních xxxxxxxxxxxxxx xxxxxxxxxx, x xxxxxxxxxx xxxxxxxx xxxx x xxx xxxxxxxxxxx xxxxxxxxxxx xxxx
(1) X ostatních xxxxxxxxxxxxxx xxxxxxxxxx, x zařízeních xxxxxxxx xxxx a xxx poskytování xxxxxxxxxxx xxxx xx xxxx xxx xxxxxxxxx x xxxxxxxxxx látkami, přípravky x xxxxxxxxxx, ke xxxxxxx se xxxxxxxxxx xxxxxxxx x zacházení (§4 xxxxxx), xxxxxxxx x xxxxxxxx vyráběných xxxxxxxx xxxxxxxxxxx obsahujících xxxxxxxx látky uvedené x příloze č. 1 nebo č. 5 zákona.
(2) Xxxxxx xxxxx evidenční xxxxx x xxxxxx xxxxxxxx xxxxx xxxxxxxx 1 xxxxxxx příloha č. 3 xxxx vyhlášky.
§6x
Xxxxxx xxxxxxxx xxxxxxxxxx xxxxx xxxxxxxxxx přílohách č. 3 x 4 xxxxxx x xxxxxxxxx xx xxxxxxxxxxxx
(1) Xxxxxxxxx osoby x xxxxxxx osoby - xxxxxxxxxxx vedou o xxxxxxxxx x návykovými xxxxxxx xxxxxxxxx x přílohách č. 3 a 4 xxxxxx x x xxxxxxxxx xx xxxxxxxxxxxxxx xxxxxxxx.
(2) Úpravu xxxxx xxxxxxxxx knihy x xxxxxx evidence xxxxx odstavce 1 xxxxxxx příloha č. 6 xxxx xxxxxxxx.
§6x xxxxxx xxxxxxx předpisem x. 143/2000 Xx. x xxxxxxxxx xx 1.7.2000
§6x
Xxxxxx xxxxxxxx při xxxxxxxxx x návykovými xxxxxxx, xxxxxxxxx nebo xxxxxxxxxx xxx xxxxxxxx x xxxxxxxxx
(1) Xxx xxxxxxxxx x xxxxxxxxxx xxxxxxx, přípravky xxxxxxxxxxxx xxxxxxxx látky xxxxxxx x příloze č. 1 xxxx č. 5 xxxxxx xxxx xxxxxxxxxx x xxxx xxxxxxxxx x §5 xxxx. 7 xxxx x §6 xxxx. 3 zákona xx xxxxx xxxxxxxxx xxxxxxx.
(2) Xxxx xxxxx xxxxxxxxx knihy stanoví příloha č. 5 xxxx xxxxxxxx.
§6x xxxxxx xxxxxxx xxxxxxxxx x. 363/2004 Xx. x xxxxxxxxx xx 1.7.2004
Xxxxxxxx při xxxxxx, xxxxxxxxxx, balení x xxxxxxxxxx návykových xxxxx, přípravků nebo xxxxxxxxxx xx základě xxxxxxxx x zacházení x xxxx
§7
(1) Při xxxxxx, xxxxxxxxxx xxxx xxxxxx xxxxxxxxxx látek, xxxxxxxxx xxxx xxxxxxxxxx xx xxxxxxx xxxxxxxx x xxxxxxxxx s nimi xx xxxxx evidenční xxxxxxx x návykových xxxxxxx, xxxxxxxxxxx nebo xxxxxxxxxxxx
x) xxxxxxxxxx,
x) xxxxxxxxx,
c) xxxxxxxxxxxx,
x) xxxxxxxxxxxxx,
x) xxxxxxxxxxxxxx,
x) xxxxxxxxxxxxxx při xxxxxx xxxxxx xxxxxxxxxx xxxxx, xxxxxxxxx nebo xxxxx, xxxxx xxxxxx xxxxxxxxxx xxxxxxx,
x) xxxxxxxxxx xxxx xxxxxx xxxx xxxxx xxxxxxxxxxxxx technologickým xxxxxxxxx x výrobě,
x) xxxxxxxxx xx xxxxxxxxxxx nebo xxxxxxxxxxxxx,
x) xxxxxxxxxxx xxxx xxxxxxxxxxxxx x xxxxxxxx xxxxxx.
(2) Xxxx xxxxx xxxxxxxxx xxxxx xxxxxx xxxxxxxxx, které xxxxxxxx xxxxxxxx xxxxx, xxxxxxx příloha č. 4 xxxx xxxxxxxx.
(3) Xxxx xxxxx xxxxxxxxx xxxxx xxxxxxxxxx xxxxxxxxxx látek, xxxxxxxxx x xxxxxxxxxx xxx xxxxx, které xx xxxxxxx xxxxxxxx x zacházení vyrábějí, xxxxxxxxxxxx xxxx xxxx xxxxxxxx xxxxx, přípravky xxxx xxxxxxxxxx, stanoví příloha č. 5 této vyhlášky.
Xxxxxxx xxxxx - xxxxxxxx xx 1.1.1999 xx 30.6.2004 (xx xxxxxx x. 363/2004 Xx.)
§8
(1) Xxx xxxxxxxxxx xxxxxxxxxx xxxxx, xxxxxxxxx x prekursorů na xxxxxxx xxxxxxxx x xxxxxxxxx s xxxx, xxxxx nejde o xxxxxx xxxxx §5, 6 xxxx 7, xx vedou xxxxxxxxx xxxxxxx x skladování xxxxxxxxxx látek, xxxxxxxxx x prekursorů.
(2) Xxxx xxxxx evidenční knihy xxxxxxxxxx xxxxxxxxxx xxxxx, xxxxxxxxx x prekursorů xxxxxxx příloha č. 5 této vyhlášky.
Xxxxxxxx xx 1.7.2000 xx 5.3.2002 (xx xxxxxx x. 82/2002 Xx.)
§9
(1) Xxxxxxxxxxx xxxxxxxxx x xxxxxxxxxx xxxxxxx, xxxxxxxxx x xxxxxxxxxx xxxxx:
x) xxxxxxxxx knihy,
b) xxxxxx xxx xxxxxxxxxx xxxx xxxxxxxx vedené xxxxxx výpočetní xxxxxxxx,
x) xxxxxxxxxx xxxxxxxxx,
x) zápisy x xxxxxxxxxxx xxxxxxxxxx xxxxx, přípravků a xxxxxxxxxx (§14 zákona),
e) xxxxxxxxx x ztrátě xxxx xxxxxxx xxxxxxxx xxxxx, xxxxxxxxx xxxx xxxxxxxxxx,
x) xxxxxx x xxxxxxxxxxx xxxxxxxxxx (§34 xxxxxx),
x) veškerá xxxxxx xxxxxxxxxx xxxxxx xxxxxxxxxxxx xxxxxxxx xx xxxxxxxxx x xxxxxxxxxx xxxxxxx, xxxxxxxxx a prekursory x jejich xxxxxx x xxxxxx, a xxxx xxxxxx x xxxxxx xxxxxxxx,
x) veškerá xxxxxx xxxxxxxxxx xxxxxxxx xx registrace xxxxxxx, xxxxxxx, xxxxxxx a xxxxxxxx xxxxxxxxx látek x veškerá xxxxxxxxxx xxxxxxxx se vývozu x xxxxxx,
x) xxxxxxxxxx xxxxxxx (§26 xx 31 xxxxxx),
x) xxxxxx xxxxx x doklady x xxxxxx nebo xxxxxx xxxxxxxxxx látek, xxxxxxxxx, xxxxxxxxxx nebo xxxxxxxxx látek xxxxxxxxx x xxxxxxx x. 10 xxxxxx,
x) xxxxxxx x xxxxxxxx, xxxxxxx xx xxxxxxxx tabletovačky, xxxxxxxxxxx kotle x xxxxxxxxxxxx kotle,
l) prohlášení xxxxxxxxxxx osob x xxxxxxxxx xxxx - xxxxxxxxxxx xxxxxxxxxxxxx s xxxxxxxxx xxxxxxx uvedenými x xxxxxxx č. 10 xxxxxx. Xxxxxxxxxxx xxxxxx xxxxxxxxxx jsou xxxxxxx v příloze x. 7 této xxxxxxxx.
(2) X xxxxxxx xx xxxxxxxx xxxxx xxxxxxxxxxx xxxxxxx x xxxxxxxx 1 xxxxx xxxxxxxxxx xxxxxxxx x xxxxxx pruhem x xxxxx žádanky s xxxxxx xxxxxx (§13 xxxx. 2 zákona).
Účinnost xx 1.7.2000 xx 30.6.2004 (do xxxxxx x. 363/2004 Xx.)
§10
Xxxxxxxxx a xxxxxx
Xxx xxxxxxxxxx xxxxxxxxx x xxxxxx xxxxx §9 xxxx. 1 xxxx. x), x) x x) se xxxxxxxxx xxxxx xxxxxxxxxx ustanovení xxx xxxxxx xxxxxxxxxxx xxxxxxx (§2). Zápisy xxxxx §9 xxxx. 1 xxxx. c), x), e) xxxx x) xxxx xxxx xxxxxxxx xxxxxxxxx xxxxx (§9 zákona). X xxxxxxx, xx xxxxxx xxxxxxxxxx xxxxxxxxx xxxxx, xxxxxxxxxx zápis xxx xxxxxxxxxx, xxxxxxx-xx xxxxxxxxx xxxxxxx na xxxxxxxxxx xxxxx ve xxxxxx §8 xxxx. 6 xxxxxx.
Xxxxxxxx xx 1.7.2000 xx 5.3.2002 (do xxxxxx č. 82/2002 Xx.)
§11
Xxxxxxxxxx xxxxxxxxxxx
Xxxxxxxxxxx xxxxxxxxx x návykovými xxxxxxx, xxxxxxxxx, xxxxxxxxxx x xxxxxxxxx látkami xxxxxxxxx x xxxxxxxxx x. 10 x 11 xxxxxx xx xxxxxxxx xx dobu 5 xxx xx xxxxxxxx xxxxxxxxx, xxxxxxxxx od xxxxxxxxxx záznamu v xxx xxxxx toho, xxxxx z xxxxxx xxxxxxxxxxx xxxxxxx později.
§12
Xxxxxxxx
Xxxx vyhláška xxxxxx xxxxxxxxx xxxx 1. xxxxx 1999.
Xxxxxxx:
XXXx. David, XXx. v. x.
Xxxxxxx xxxxx - xxxxxxxx xx 1.1.1999 xx 5.3.2002 (xx xxxxxx x. 82/2002 Xx.)
Xxxxxxx x. 1 x xxxxxxxx x. 304/1998 Sb.
Případy, xx xxxxxxx xx vyžaduje xxxxxxxx k xxxxxx xxxxxxxxx látek
(země určení xxxx xxxxxxxx hvězdičkou (*) v xxxxxxx xxxxxxxxx xxxxxxx látky)
Xxxxxxx č. 2 x vyhlášce č. 304/1998 Sb.
Xxxxxxx č. 3 x vyhlášce č. 304/1998 Sb.
Vzor listu xxxxxxxxx xxxxx ostatních xxxxxxxxxxxxxx xxxxxxxx, xxxxxxxx xxxxxxxx xxxx a xxx poskytování xxxxxxxxxxx xxxx
|
Xxxxx XX I*, XX II* (druh, xxxx x xxxxxxxx):
|
||||||
|
Xxxxx
|
Xxx xxxxxx
|
Xxxxxxx: lékař
|
Příjem
|
Výdej
|
Stav xxxx
|
|
|
xxxxxx xxxx
|
xxxxx xxxxx x x. xxxxxxx
|
xxxxxxxxx
|
xxxx xxxxxx
|
&xxxx; | &xxxx; |
xxxxxxx, xxxxxx apod.
|
|
výdej
|
Při xxxxxx
|
&xxxx; | &xxxx; | &xxxx; | &xxxx; | |
| &xxxx; |
x. xxxxxxxxx
|
xxxxxxx
|
&xxxx; | &xxxx; | &xxxx; | &xxxx; |
|
1
|
2
|
3
|
4
|
5
|
6
|
7
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
* OL I - xxxxxx xxxxx xxxxxxx x příloze č. 1 xxxxxx x. 167/1998 Xx.
* XX XX - xxxxxxxxxxxx látky xxxxxxx v příloze x. 5 zákona x. 197/1998 Xx.
Příloha x. 4 x xxxxxxxx x. 304/1998 Xx.
Xxxx xxxxx xxxxxxxxx knihy výroby xxxxxxxxx, xxxxx xxxxxxxx xxxxxxxx xxxxx (NL)
|
Pořadové xxxxx zápisu
|
Účinná xxxxx xxxxxxxx xx skladu
|
Číslo xxxxxxxx šarže
|
Datum předání xx xxxxxx xxxxxxxx xxxxxxx
|
Xxxxxxxx xxxxxxx xxxxxx, x počtu xxxxxx XX, xxxxxxxxxx
|
Xxxxxxxx výrobní xxxxxx v x
|
Xxxxx x g NL, xxxxxxxxxx, xxxxxxxxxx x xxxxx výrobě xxxx xxxxxxxxxxxx
|
Xxxxxxxx
|
Xxxxxxx xxxxxx xxxxxxxxxx xxxxxxxxxxxxx xxxxx
|
| &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; |
| &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; |
| &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; |
| &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; |
| &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; |
| &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; |
| &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; |
| &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; |
| &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; |
| &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; | &xxxx; |
Původní xxxxx - xxxxxxxx od 1.1.1999 xx 30.6.2004 (do xxxxxx č. 363/2004 Xx.)
Xxxxxxx x. 5 x xxxxxxxx x. 304/1998 Xx.
Xxxx xxxxx xxxxxxxxx xxxxx skladování
Název xxxxxxxx xxxxx (NL), xxxxxxxxx x xxxxxxxxxx
______________________________________________________________________________________
Xxxxx Xxxxx xxxxxxx Xxxxx x adresa Množství Množství Stav xxxxx
xxxxxx (xxxxxxxxxx x Xxxxx xxxxx xxxxxxxxxx xxxx xxxxxxxxx xxxxxxxx x
x xxxxxxxxx xxxxx) xxxxxxxx XX, příp- XX, xxxxxxxxxxx
xxxxxx xxxxx x xxxxxxxxx xxxx
xxxxxxxxxx x xxxxxxxxxx
______________________________________________________________________________________
______________________________________________________________________________________
______________________________________________________________________________________
______________________________________________________________________________________
______________________________________________________________________________________
______________________________________________________________________________________
______________________________________________________________________________________
______________________________________________________________________________________
______________________________________________________________________________________
______________________________________________________________________________________
______________________________________________________________________________________
______________________________________________________________________________________
______________________________________________________________________________________
______________________________________________________________________________________
______________________________________________________________________________________
______________________________________________________________________________________
______________________________________________________________________________________
______________________________________________________________________________________
______________________________________________________________________________________
Xxxxxxxxx množství xx x XX x xxxxxxxxxx 1 x x x přípravků 1 balení.
Příloha č. 6 x xxxxxxxx x. 304/1998 Xx.
Xxxx xxxxx xxxxxxxxx knihy xxxxxxxxxx
Xxxxx xxxxxxxx xxxxx (XX) xxxxxxx x přílohách x. 3 x 4 xxxxxx
Xxxxx přípravku xxxxxxxxxxxx xxxxxxxx xxxxx xxxxxxx x xxxxxxxxx x. 3 x 4 xxxxxx
|
Xxxxx
|
Xxxxx dokladů
|
Jméno x adresa
|
Jednotka
|
Množství
|
Množství
|
Stav zásob
|
Číslo xxxxx
|
|
xxxxxx
|
(xxxxxxxxxxx x
|
xxxxxxxxxx
|
xxxxxxxx
|
xxxxxxxxx XX
|
xxxxxxxx XX
|
x xxxxxxxxxxx
|
xxxxx XXXX
|
|
x xxxxxx
|
xxxxxxxxxx xxxxx)
|
xxxx xxxxxxxx
|
&xxxx;
|
x xxxxxxxxx
|
x xxxxxxxxx
|
xxxx
|
&xxxx;
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
Xxxxxxx x. 6 xxxxxxx právním xxxxxxxxx x. 143/2000 Xx. s xxxxxxxxx xx 1.7.2000
Původní znění - xxxxxxxx xx 1.1.1999 xx 5.3.2002 (xx xxxxxx x. 82/2002 Xx.)
Xxxxxxx x. 7 x xxxxxxxx x. 304/1998 Sb.
Prohlášení xxxxxxxxxxx xxxx x xxxxxxxxx xxxx
Xxxxxxx č. 7 xxxxxxx xxxxxxx xxxxxxxxx x. 143/2000 Xx. x účinností xx 1.7.2000
Xxxxxxx x. 8 x xxxxxxxx č. 304/1998 Xx.
Xxxxx limitní xxxxxxxx xxx xxxxx, xxxxx hodlají uvádět xx xxx xxxxxxx xxxxx xxxxxxx x příloze č. 10 zákona (§12 xxxx. 3 x §32 xxxx. 6 xxxxxx)
|
Xxxxxxxxxxx xxxxxxxxxx xxxxx (XXX) v xxxxxx xxxxxx
|
Xxxxxxxx
|
|
Xxxxxxxx xxxxxxxx octové
|
20 xxxxx
|
|
Xxxxxxxx xxxxxxxxxxx
|
1 kg
|
|
Kyselina xxxxxxxxxxx
|
1 xx
|
|
Xxxxxxxxx
|
0,5 kg
|
Včetně xxxx uvedených xxxxx xx xxxxx případech, xxx xxxxxxxxx xxxxxxxx xxxx je možná.
Platí x xxx xxxxx xxxxxx látek xxx xxxxxxxx na xxxxx xxxxx xxxxx, která xx v dané xxxxx xxxxxxxx.
Xxxxxxx x. 8 vložena xxxxxxx xxxxxxxxx č. 363/2004 Xx. s xxxxxxxxx xx 1.7.2004
Příloha č. 9 x xxxxxxxx x. 304/1998 Xx.
Xxxxxxx množství xxx osoby, xxxxx xxxxxxx xxxxxxx xxxxxxxx xxxxxxxx xxxxxx xxxx xxxxxxxxxxx draselný vztahující xx x xxxxxxxx x předpokládaném vývozu (§20b xxxx. 2 xxxxxx)
|
Xxxxxxxxxxx nechráněný název (XXX) v českém xxxxxx
|
Xxxxxxx množství x xx (xxxxxx)
|
|
Xxxxxxxx xxxxxxxx xxxxxx
|
100
|
|
Xxxxxxxxxxx xxxxxxxx
|
100
|
Xxxxxxx č. 9 vložena xxxxxxx xxxxxxxxx x. 363/2004 Xx. x xxxxxxxxx xx 1.7.2004
Xxxxxxxxx
Xxxxxx xxxxxxx č. 304/98 Sb. xxxxx xxxxxxxxx dnem 1.1.1999.
Xx xxxxx xxxxxx xxxxxxxx předpisu xxxx xxxxxxxxxx xxxxx x xxxxxxxx uskutečněné xxxxxxx xxxxxxxxx č.:
143/2000 Xx., xxxxxx se xxxx xxxxxxxx č. 304/98 Xx., xxxxxx se xxxxxxx xxxxxxx, xxx xx xxxxxxxxxx vývozní xxxxxxxx x xxxxxx xxxxxxxxx látek, xxxxxxxxxxx x xxxxxxxx xxxxxxxxxx xxxxx, přípravků x xxxxxxxxxx x x xxxxxxxxxxx xxxxxxxxxx látek
x xxxxxxxxx od 1.9.2000
82/2002 Xx., xxxxxx se xxxx xxxxxxxx x. 304/98 Xx., xxxxxx xx xxxxxxx xxxxxxx, xxx se xxxxxxxxxx xxxxxxx povolení x xxxxxx xxxxxxxxx xxxxx, xxxxxxxxxxx x xxxxxxxx xxxxxxxxxx látek, xxxxxxxxx x xxxxxxxxxx x x xxxxxxxxxxx xxxxxxxxxx xxxxx, xx znění xxxxxxxx x. 143/2000 Xx.
x xxxxxxxxx xx 6.3.2002
363/2004 Sb., kterým xx xxxx xxxxxxxx x. 304/98 Xx., xxxxxx xx xxxxxxx xxxxxxx, xxx se xxxxxxxxxx vývozní povolení x xxxxxx xxxxxxxxx xxxxx, podrobnosti x xxxxxxxx návykových xxxxx, xxxxxxxxx x xxxxxxxxxx x o xxxxxxxxxxx xxxxxxxxxx xxxxx, xx xxxxx xxxxxxxxxx předpisů
x xxxxxxxxx xx 1.7.2004
Právní xxxxxxx č. 304/98 Xx. byl xxxxxx xxxxxxx xxxxxxxxx č. 123/2006 Sb. x xxxxxxxxx od 1.5.2006.
Znění xxxxxxxxxxxx xxxxxxxx norem xxxxxx xxxxxxxx xxxxxxxx x xxxxxxxx není xxxxxxxxxxxxx, xxxxx se xxxx xxxxxx xxxxxxxxx xxxxx xxxxx xxxxxxxxx xxxxxxxx xxxxxxxx.
1) Směrnice Xxxx 92/109/EHS xx dne 14. xxxxxxxx 1992 x xxxxxx xxxxxxxx xxxxx xxxxxxxxxxx x xxxxxxxxxx xxxxxx xxxxxxxx x xxxxxxxxxxxxxx xxxxx x x jejich xxxxxxx na xxx.
Xxxxxxxx Xxxxxx 93/46/EHS xx xxx 22. června 1993, xxxxxx xx xxxxxxxxx x mění xxxxxxx xxxxxxxx Xxxx 92/109/XXX o výrobě xxxxxxxx xxxxx xxxxxxxxxxx x xxxxxxxxxx xxxxxx xxxxxxxx x xxxxxxxxxxxxxx xxxxx x x xxxxxx xxxxxxx xx xxx.
Xxxxxxxx Xxxx (XXX) č. 3677/90 xx xxx 13. prosince 1990 x xxxxxxxxxx, která xxxx xxx přijata xx účelem xxxxxxxx xxxxxxxxxx určitých xxxxx x xxxxxxxxxx xxxxxx xxxxxxxx x xxxxxxxxxxxxxx xxxxx, xx xxxxx xxxxxxxx Rady (EHS) x. 900/92 x xxxxxxxx Rady (ES) x. 988/2002.
Xxxxxxxx Xxxxxx (XX) č. 1485/96 xx xxx 26. července 1996, xxxxxx se xxxxxxx prováděcí pravidla xx xxxxxxxx Xxxx 92/109/XXX, pokud xxx x xxxxxxxxxx xxxxxxxxxx x xxxxxxxxx xxxxxxx xxxxxxxx látek xxxxxxxxxxx x nedovolené xxxxxx xxxxxxxx x psychotropních xxxxx, ve xxxxx xxxxxxxx Komise (ES) x. 1533/2000.
1a) Xx. 2 xxxx. 3 nařízení Xxxx (XXX) č. 3677/90.
1x) Xxxxx č. 101/2000 Sb., x ochraně xxxxxxxx xxxxx a x xxxxx xxxxxxxxx xxxxxx, xx znění xxxxxxxxxx předpisů.
1x) Čl. 2 xxxx. 2 nařízení Xxxx (EHS) č. 3677/90.
1d) §2 xxxx. 3 x 11 xxxxxx x. 79/1997 Xx. x xxxxxxxx a o xxxxxxx x xxxxxxxx xxxxxxxxx xxxxxxxxxxxxx xxxxxx.
2x) §21 xxxx. 1 písm. x) x x) xxxxxx č. 79/1997 Xx., ve xxxxx xxxxxx č. 149/2000 Xx.
2x) §3 xxxx. 5 písm. x) xxx 2 xxxxxxxx x. 343/1997 Xx., xxxxxx xx xxxxxxx xxxxxx x xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx, xxxxxxxxxxx xxxxxxxxxx xxxxxxxx x xxxxxxxx xxxxxx xxxxxxxxx.
2x) Xx. 2 xxxx. 1 nařízení Xxxx (XXX) č. 3677/90, xx xxxxx xxxxxxxx Xxxx (XXX) x. 900/92 a nařízení Xxxx (XX) x. 988/2002.
2x) Xxxxxxxx Xxxxxx (XX) č. 1485/96, xx xxxxx směrnice Xxxxxx 93/46/XXX x xxxxxxxx Xxxxxx (XX) x. 1533/2000.
3) §3 xxxx. 5 xxxx. x) xxxxxxxx č. 343/1997 Sb., xxxxxx xx xxxxxxx xxxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx, xxxxxxxxxxx xxxxxxxxxx xxxxxxxx x xxxxxxxx xxxxxx xxxxxxxxx.
4) §3 xxxx. 6 xxxxxxxx x. 343/1997 Sb.
5) Čl. 2 xxxx. 4 xxxxxxxx Xxxx (XXX) č. 3677/90, xx xxxxx xxxxxxxx Xxxx (EHS) x. 900/92.


