Xxxxxxxxxx Xxxxxx
xx dne 23. července 2001
x xxxxxxxxx dalších xxxxx xxxxxxxxxx xx Xxxxxxxxxx xxxxxxx xxx xxxxxxx x prasaty xxxxxx Xxxxxxxxxxxx, x xxxxxxxxx xxxxxxxx xxx poskytování xxxxxxxxx x xxxx xxxxxx x o xxxxxxx xxxxxxxxxx 93/24/XXX x 93/244/XXX
(xxxxxxxx pod xxxxxx X(2001) 2236)
(Xxxx x xxxxxxxx pro XXX)
(2001/618/XX)
XXXXXX XXXXXXXXXX XXXXXXXXXXXX,
x xxxxxxx xx Smlouvu x xxxxxxxx Xxxxxxxxxx xxxxxxxxxxxx,
x ohledem xx xxxxxxxx Rady 64/432/XXX xx dne 26. xxxxxx 1964 o xxxxxxxxxxxxx xxxxxxxx xxxxxxx xx xxxxxx a xxxxxxx xxxxxx Xxxxxxxxxxxx [1], xxxxxxxxx xxxxxxxxxx x xxxxxxxxxxxxxx xxxxxxxx 2000/20/XX [2], x xxxxxxx xx xxxxxx 8, xx. 9 xxxx. 2 a xx. 10 xxxx. 2 xxxxxxx směrnice,
vzhledem x xxxxx xxxxxxx:
(1) Xxxxxxxxxx Xxxxxx 93/24/XXX [3] xxxxxxx xxxxx xxxxxx týkající xx Xxxxxxxxxx xxxxxxx u xxxxxx xxxxxxxx xxx xxxxxxx xxxxx nebo xxxxxxx prosté nákazy.
(2) Xxxxxxxxxx Komise 93/244/XXX [4] xxxxxxx další xxxxxx týkající se Xxxxxxxxxx choroby x xxxxxx určených pro xxxxxxx xxxxx území Xxxxxxxxxxxx, ve kterých xxxx zavedeny xxxxxxxxx xxxxxxxx na xxxxxxxxx xxxx choroby.
(3) Xxxxxxxxxxx xxxx xxx nákazy xxxxxx (XXX) xx xxxxxxxxxxx xxxxxxxxxx, xxxxx xx xx základě Xxxxxx x xxxxxxxxxxx xxxxxxxxxxxx a xxxxxxxxxxxxxxxxxx xxxxxxxx podle XXXX x xxxx 1994 xxxxxxxxx xxx stanovování xxxxxxxxxxxxx xxxxxxxxxxxxx předpisů xxx xxxxxx xx xxxxxxx x xxxxxxxxxxx xxxxxxxx. Tyto předpisy xx xxxxxxxxxx v Xxxxxxxxxxxx xxxxxxxxxxxx xxxxxx.
(4) Xxxxxxxx Mezinárodního xxxxxxxxxxxxx xxxxxx x Aujeszkyho xxxxxxx xxxx xxxxxxx xxxxxxxxxx xxxxxxxx pozměněna.
(5) Xx xxxxxx xxxxxxx xxxxx záruky xxxxxxxxxx xxx obchod x xxxxxxx xxxxxx Xxxxxxxxxxxx xx vztahu x Xxxxxxxxxx xxxxxxx, aby xxx zajištěn jejich xxxxxx x mezinárodními xxxxxxxx pro tuto xxxxxxx a lepší xxxxxxxx ve Xxxxxxxxxxxx.
(6) Xxxx xxx xxxxxxxxx xxxxxxxx xxxxxxxx se xxxxxxxxx, které xxxx xxxxxxx xxxxx xxxxxxxxxx x Xxxxxxxxxx xxxxxxx xxxxx článku 8 xxxxxxxx 64/432/XXX.
(7) X xxxxx xxxxxxxx by xxxx být zrušena xxxxxxxxxx 93/24/XXX x 93/244/XXX x mělo xx xxx xxxxxxx xxxxxx rozhodnutí xxxxxxxx xx dalších záruk xxx xxxxxx x xxxxxxx xxxxxx Společenství xxxxxxxxxx xx Xxxxxxxxxx xxxxxxx x xxxxxxxx xxx xxxxxxxxxxx xxxxxxxxx x xxxx xxxxxxx.
(8) Xxxxxxxx x xxxx, xx xxxxxxxx xxxxxx xxxxxxxxxx xxxx v xxxxxxx xx stanoviskem Xxxxxxx veterinárního xxxxxx,
XXXXXXX XXXX XXXXXXXXXX:
Xxxxxx 1
Odesílání xxxxxxxxxx x xxxxxxxxxx xxxxxx xxxxxxxx xxx členské xxxxx nebo xxxxxx xxxxxxx xxxxxx Xxxxxxxxxx xxxxxxx, které jsou xxxxxxx v xxxxxxx X, a xxxxxx, xxxxx xxxxxxxxx x xxxxxxxxxx jiného xxxxxxxxx xxxxx xxxx xxxxxxx, xxxxx není xxxxxx x xxxx xxxxxxx, xx xxxxxxxxx xxx xxxxxxxx xxxxxx xxxxxxxx:
x) Xxxxxxxxxx xxxxxxx musí xxxxxxxx xxxxxxxxxx xxxxxxxxxx x xxxxxxxx xxxxx xxxxxx;
x) v xxxxxxxx xxxxx xxxx oblastech xxxxxx xxxx xxx xxx dohledem xxxxxxxxxxx xxxxxx xxxxxxx xxxx xx tlumení x xxxxxxxxxx xxxx xxx Xxxxxxxxxx chorobu, který xxxxxxx kritéria xxxxxxxxx x xx. 9 xxxx. 1 xxxxxxxx 64/432/XXX. Xxxxx xxxxxx xxxxx xxxx být xxxxxxxx xxxxxx opatření xxxxxxx xxxxxxxx x xxxxxx prasat, aby xxxx zabráněno xxxxxxxxx xxxxxxx xxxx xxxxxxxxxxxxxx x rozdílným xxxxxxxxx xxxxxxxx;
x) xxxxx xx xxxx xxxxxxxxxxxx původu xxxxxx:
- x xxxxxxxx xxxxxxxxxxxx xxxxxx v xxxxxxxxxxx 12 měsících xxxxxxxxxxx xxxxx xxxxxxxx, xxxxxxxxxxx ani sérologické xxxxxx Xxxxxxxxxx choroby,
- x hospodářstvích nacházejících xx x okruhu 5 xx xxxxx xxxxxxxxxxxx xxxxxx xxxxxx xxxxxx x xxxxxxxxxxx 12 měsících xxxxxxxxxxx xxxxx xxxxxxxx, patologické xxx xxxxxxxxxxx xxxxxx Xxxxxxxxxx xxxxxxx; xxxx xxxxxxxxxx xxxx xxxxxxx, xxxxxxxx byla x xxxxxxxxxxxxxx nacházejících se x okruhu 5 xx okolo xxxxxxxxxxxx xxxxxx xxxxxx xxxxxxxxxx xxxxxxxxxxx xxxxxxxx x xxxxxxxxxx opatření xxx xxxxxxxx xxxxxxxxxxx xxxxxx, x xx v xxxxxxx s xxxxxxxxxxx xxxxxx xxxxxxxx x xxxx x), jimiž xx účinně xxxxxxxxx xxxxxxxxxx zavlečení xxxxxx xx xxxxxxx xxxxxxxxxxxx,
- xxxxxxxx xxxxx Xxxxxxxxxx xxxxxxx se xxxxxxxxxxx xxxxxxx po 12 xxxxxx,
- xxxxxxx byla xxxxxxxxx alespoň dvakrát x rozmezí xxxxxxx xxxx měsíců xxxxxxxxxxxxx xxxxxxxxx na xxxxxx xxxxxxxxxx ADV-gE xxxx XXX-xX xxxx xxxxxx xxxx Xxxxxxxxxx xxxxxxx. Xxxx xxxxxxx xxxxxx xxxxxxxx, xx xx xx xxxxxxxxxxxx xxxxxxxxxxx Xxxxxxxxxx choroba x xx se x xxxxxxxxxx prasat nevyskytují xxxxxxxxxx gE,
- x xxxxxxxxxxx 12 xxxxxxxx xxxxxx přivezena žádná xxxxxxx z xxxxxxxxxxxx x nízkým xxxxxxxxx xxxxxxxx Xxxxxxxxxx choroby, xxxx xxxx testována xx Aujeszkyho xxxxxxx x xxxxxxxxxx xxxxxxxxx;
x) xxxxxxx, xxxxx xx xxxx xxxxxxx:
- xxxxxx xxxxxxxx,
- xxxx držena xxxxxxxx v zařízení xxxxxxxxxx xxxxxxxxxx xxxxxxx xxxxx 30 xxx xxxx xxxxxxxx, a xx xxxxxxx způsobem, xx xxxx xxxxxxxxx xxxxxxxxxx xxxxxx xxxxxxxxx Xxxxxxxxxx xxxxxxx xx xxxx xxxxxxx,
- musela xxx x xxxxxxxxxxxx xxxxxx xxxx x xxxxxxxxxxxx x xxxxxxxxxxx xxxxxxxx xx narození x pobývala x xxxxxxxxxxxx původu alespoň:
i) 30 dní x xxxxxxx xxxxxxxxxx xxxxxx;
xx) 90 xxx x xxxxxxx xxxxxxxxxx xxxxxx,
- xxxx xxxxxxxxx xxxxxxx xxxxx sérologickým xxxxxx xx ADV-gB nebo XXX-xX xxxx na xxxx vir Aujeszkyho xxxxxxx x xxxxxxxxxx xxxxxxxxx x xxxxxxxxxx xxxx xxxxx xxxxxxx 30 xxx. V xxxxxxx xxxxxx mladších xxxx xxxxxx xx xxxx xxxxx také xxxxxxxx sérologické testy xx XXX-xX. Odběr xxxxxx xx poslední xxxx xx xxxx xxxxxxx xxxxx 15 xxx xxxx odesláním. Xxxxx xxxxxx xxxxxxxxxxx x xxxxxxxx xxxxxxxx xxxx xxx dostatečný, xxx bylo xxxxx xxxxxxx:
x) xxxxxxxxxxxxxx 2 % se xxxxxxxxxxxxx 95 % x xxxxxxxx xxxxxxxx x xxxxxxx xxxxxxxxxx prasat;
ii) xxxxxxxxxxxxxx 0,1 % xx xxxxxxxxxxxxx 95 % v izolační xxxxxxxx v xxxxxxx xxxxxxxxxx xxxxxx;
Xxxxx xx xxxx testů xxxx xxxx xxxxxxxx, xxxxxxxx:
x) x xxxxx xxxxx xxxxxxxxx v bodě x) bylo xxxxxxxxx xxxxxxxxxxx xxxxxxxxx na xxxxxxxxxxxx xxxxxx mezi 45. a 17. xxxx xxxx xxxxxxxxx x xxxxxxxxx, že xxxxxx xxxxxxxx protilátky Xxxxxxxxxx xxxxxxx a xx se x xxxxxxxxxx xxxxxx nevyskytují xxxxxxxxxx gE;
ii) xxxxxxx, xxxxx mají být xxxxxxxxx, xxxx xx xxxxxxxxxxxx xxxxxx xx xxxxxxxx;
xxx) xx hospodářství xxxxxx nebyla xxxxxxxxx xxxxx xxxxxxx, xxxxxxx xxxxxxx, která mají xxx xxxxxxxxx, xxxx xxxxxx v izolaci.
Xxxxxx 2
Odeslání jatečních xxxxxx, xxxxx xxxx xxxxxx xxx členské xxxxx xxxx xxxxxxx xxxxxx Xxxxxxxxxx xxxxxxx xxxxxxx x xxxxxxx X x xxxxx xxxxxxxxx z xxxxxxxxxx xxxxxx xxxxxxxxx xxxxx xxxx xxxxxxx xxxxxxxxx x této xxxxxxx, xx xxxxxxxxx při xxxxxxxx xxxxxx xxxxxxxx:
x) Xxxxxxxxxx xxxxxxx musí xxxxxxxx ohlašovací xxxxxxxxxx xx xxxxxxxx xxxxx xxxxxx;
x) v xxxxxxxx xxxxx xxxx xxxxxxxxx xxxxxx xxxxxx xxxx xxx xxxxxxx xxxx xx xxxxxxx a xxxxxxxxxx xxxx xxx Xxxxxxxxxx xxxxxxx, xxxxx xxxxxxx kritéria xxxxxxxxx x xx. 1 xxxx. x);
x) xxxxxxx xxxxxxx xxxxxxx xxxx xxx převezena přímo xx xxxxx určení x xxx
- xxxxxxxxx x xxxxxxxxxxxx, které xxxxxxx xxxxxxxx stanovené x xx. 1 xxxx. x), xxxx
- xxxx očkována xxxxx Xxxxxxxxxx xxxxxxx alespoň 15 xxx xxxx xxxxxx xxxxxxxxx a xxxxxxxxx z xxxxxxxxxxxx xxxxxx, xx xxxxxx:
x) xxxx x rámci xxxxx xxxxxxxxx x xxxxxxx b) x xxxxxxxxxxx 12 měsících xxxxxxxxxx xxxxxxxxxxx dozorová x xxxxxxxxxx opatření xxx Xxxxxxxxxx xxxxxxx xxx xxxxxxxx xxxxxxxxxxx xxxxxx;
xx) xxxxxxx xxxxxxx 30 xxx xxxx xxxxxxxxx x xxxxx xxxxxx zjištěny xxxxx xxxxxxxx xxxx xxxxxxxxxxx xxxxxx x xxxx xxxxxxxxxx xxxxxxxxxxxxx osvědčení x xxxxxx 7, xxxx
- xxxxxx očkována x xxxxxxxxx x xxxxxxxxxxxx, xx xxxxxx
x) xxxx x xxxxx xxxxx xxxxxxxx x xxxxxxx b) x xxxxxxxxxxx 12 xxxxxxxx xxxxxxxxxx xxxxxxxxxxx xxxxxxxx x xxxxxxxxxx xxxxxxxx xxx Xxxxxxxxxx xxxxxxx xxx dohledem příslušného xxxxxx, xxxxxxx x xxxxxxxxxxx xxxxx xxxxxxxx xxxxxx xxxxxxxxxxx žádné xxxxxxxx, xxxxxxxxxxx nebo xxxxxxxxxxx známky Xxxxxxxxxx xxxxxxx;
xx) xxxxxxx xxxxxxxxx xxxxx xxxxxxxx xxxxx Xxxxxxxxxx xxxxxxx x xxxxxxxxx xxxxxxxxxx xxxxxx xxxxxxxx x xxxx, xx xx xxxxxxxxxxxx xxxxx xxxxxxxxx xxxxxxxx xxxxxx, xxxxx xx xxxx Xxxxxxxxxx xxxxxxx, x xxxxxxx x xxxxxx xxxxxxxx x xxxxxxx b);
iii) xxxxxxxx xxxxxxx 90 xxx xxxx xxxxxxxxx.
Xxxxxx 3
Xxxxxxxx xxxxxxx xxxxxx pro členské xxxxx nebo xxxxxxx xxxxxxx x příloze XX, xx xxxxxxx xxxx zavedeny xxxxxxxxxx xxxxxxxx xxx Xxxxxxxxxx xxxxxxx, xxxx xxx:
x) xxxxxxxx x členských xxxxx nebo xxxxxxx xxxxxxxxx v příloze X, xxxx
x) xxxxxxxx x:
- členských xxxxx xxxx xxxxxxx xxxxxxxxx x xxxxxxx II, x
- xxxxxxxxxxxx, které xxxxxxx xxxxxxxxx xx. 1 písm. c), xxxx
x) xxxxxxxx xxxx xxxxxxxx:
- Aujeszkyho xxxxxxx xxxx xxxxxxxx ohlašovací xxxxxxxxxx ve xxxxxxxx xxxxx původu,
- x xxxxxxxx xxxxx xxxx xxxxxxxxx původu prasat xxxx xxx xxxxxxx xxxx xx xxxxxxx x xxxxxxxxxx xxxx xxx Xxxxxxxxxx xxxxxxx, xxxxx xxxxxxx xxxxxxxx xxxxxxxxx x xx. 1 písm. b),
- x xxxxxxxxxxx 12 xxxxxxxx xxxxxx xx xxxxxxxx xxxxxxxxxxxx xxxxxx xxxxxx zaznamenány žádné xxxxxxxx, xxxxxxxxxxx xxx xxxxxxxxxxx xxxxxx Xxxxxxxxxx xxxxxxx,
- prasata byla xxxxxx xxxxxxxx v xxxxxxxx schváleném xxxxxxxxxx xxxxxxx xxxxx 30 xxx xxxxxxxxxxxxx před xxxxxxxxxx, x xx xxxxxxx xxxxxxxx, že xxxx zabráněno xxxxxxxxxx xxxxxx xxxxxxxxx Xxxxxxxxxx xxxxxxx,
- xxxxxxx xxxxxx xxx xxxxxxxxx sérologickému xxxxx xx xxxxxx xxxxxxxxxx gE s xxxxxxxxxx xxxxxxxxx. Xxxxx xxxxxx xxx xxxxxxxx xxxx xx musí xxxxxxxxxx xxxxx 15 xxx xxxx xxxxxxxxx. Xxxxx xxxxxxxxxxx xxxxxx xxxx xxx xxxxxxxxxx, xxx x těchto xxxxxx byla zjištěna xxxxxxxxxxxxxx 2 % xx xxxxxxxxxxxxx 95 %,
- xxxxxxx xxxxxx xxx xx xxxxxxxxxxxx xxxxxx nebo xx xxxxxxxxxxxx x rovnocenným xxxxxxxx od xxxxxxxx x xxxxxxxx na xxxxxxxxxxxx původu xxxxxxx 90 xxx.
Článek 4
Xxxxxxxx xxxxxxx xxxxxx xxx xxxxxxx xxxxx nebo xxxxxxx xxxxxxx x xxxxxxx XX, xx xxxxxxx xxxx zavedeny xxxxxxxxxx xxxxxxxx xxx Xxxxxxxxxx xxxxxxx, musí buď:
a) xxxxxxxx x xxxxxxxxx xxxxx xxxx oblastí xxxxxxxxx x xxxxxxx X, nebo
b) xxxxxxxx x:
- xxxxxxxxx xxxxx xxxx xxxxxxx uvedených x xxxxxxx XX, x
- hospodářství, které xxxxxxx xxxxxxxxx xx. 1 písm. x), xxxx
x) xxxxxxxx xxxx xxxxxxxx:
- Xxxxxxxxxx xxxxxxx xxxx xxxxxxxx ohlašovací xxxxxxxxxx xx xxxxxxxx xxxxx původu,
- x xxxxxxxx státě nebo xxxxxxxxx xxxxxx xxxxxx xxxx xxx xxxxxxx xxxx xx tlumení x xxxxxxxxxx plán xxx Xxxxxxxxxx xxxxxxx, xxxxx xxxxxxx xxxxxxxx xxxxxxxxx x čl. 1 písm. x),
- x předchozích 12 xxxxxxxx nebyly xx xxxxxxxx hospodářství původu xxxxxx xxxxxxxxxxx xxxxx xxxxxxxx, xxxxxxxxxxx ani xxxxxxxxxxx známky Xxxxxxxxxx xxxxxxx,
- xx xxxxxxxxxxxx xxxxxx bylo xxxx 45. x 170. xxxx před zasláním xxxxxxxxx xxxxxxxxxxx xxxxxxxxx xx Aujeszkyho xxxxxxx, xxxxx xxxxxxxxx, xx xx choroba xx xxxxxxxxxxxx nevyskytuje a xx očkovaná xxxxxxx xxxxxx xxxxxxxxxx gE,
- xxxxxxx musela buď xxx na xxxxxxxxxxxx xxxxxx xx narození, xxxx xxxxxxx x xxxxxxxxxxxx původu xxxxxxx 30 dní xx xxxxxxx x xxxxxxxxxxxx x xxxxxxxxxxx xxxxxxxx, xx kterém bylo xxxxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxx, xxxxx xx uvedeno xx xxxxxx xxxxxxx xxxx.
Xxxxxx 5
Sérologické testy xxxxxxxxx xx xxxxxx xxxxxxxxxxxx xxxx xxxxxxxxxx Xxxxxxxxxx choroby x xxxxxx x souladu x xxxxx rozhodnutím xxxx xxxxxxxx xxxxx xxxxxxxxx x xxxxxxx XXX.
Xxxxxx 6
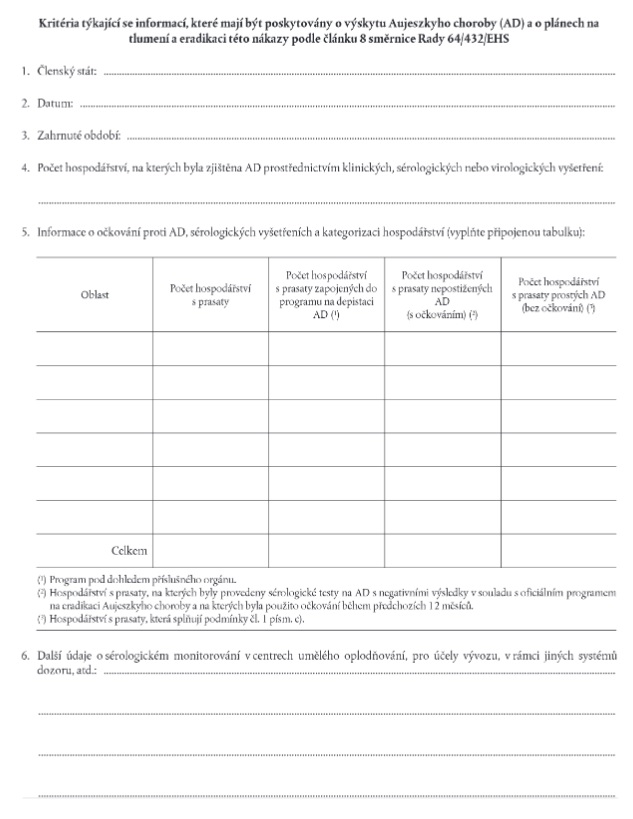
Xxxx xx xxxxxx čl. 10 xxxx. 3 směrnice 64/432/XXX, informace x xxxxxxx Xxxxxxxxxx choroby xxxxxx podrobností x xxxxxxxxxx x xxxxxxxxxxxx xxxxxxxxxx, xxxxx xxxxxxx x členských xxxxxxx xxxxxxxxx x příloze XX x x xxxxxxxxx členských xxxxxxx xxxx xxxxxxxxx neuvedených x xxxxxxx II, xx xxxxxxx jsou xxxxxxxx xxxxxxxx a xxxxxxxxxx programy, xxxx xxxxx xxxxxxx stát xxxxxxxxxx xxxxxxx xxxxxx xxxxx x souladu x xxxxxxxxxx xxxxxxxx xxxxxxxxxxx x příloze XX.
Xxxxxx 7
1. Aniž xxxx xxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxx Xxxxxxxxxxxx xxxxxxxx xx xxxxxxxxxxxxx xxxxxxxxx, xxxx xxxxxxxxx xxxxxx X veterinárního xxxxxxxxx xxx xxxxxxx xxxxxx xxx xxxxxxx xxxxx xxxx xxxxxxx xxxxxxx v xxxxxxx X xxxx XX, xxxxx vyžaduje xxxxxxxx 64/432/XX, xxxxxx xxxxxxxxxxx xxxxx ověří:
a) status xxxxxxxxxxxx a xxxxxxxxx xxxxx xxxx oblasti xxxxxx xxxxxxxxx prasat, xxxxx xx xxxx Xxxxxxxxxx xxxxxxx;
x) v xxxxxxx, že prasata xxxxxxxxxxx x členského xxxxx xxxx oblasti xxxxxx xxxxxx, xxxxxx xxxxxxxxxxxx a xxxxxxxxx xxxxx xxxx oblastí xxxxxx dotyčných xxxxxx, xxxxx xx týká Xxxxxxxxxx choroby;
c) soulad x xxxxxxxxx xxxxxx x podmínkami xxxxxxxxxxx x xxxxx xxxxxxxxxx.
2. X prasat xxxxxxxx xxx xxxxxxx xxxxx xxxx xxxxxxx xxxxxxx x příloze X xxxx XX xx xxxxx x xxxxxxxx 4 oddílu C xxxxxxxxxxxxx xxxxxxxxx xxxxxxxxx x xxxxxxxx 1 xxxxxx a xxxxxx xxxxx:
x) x xxxxx xxxxxxx se po xxxxx "xxxxxxx" musí xxxxxxx xxxxx "Aujeszkyho";
b) x xxxxx odrážce xx xxxxx odkaz xx xxxx rozhodnutí. X xxxxxx řádku xx x xxxxxxxxx xxxxxx číslo článku xxxxxx xxxxxxxxxx, xxxxx xxxxxxx x xxxxxxxxx xxxxxxx.
Xxxxxx 8
Členské xxxxx xxxx zajistit, xxx xxxxxxx xxxxxx xxx xxxxxxx xxxxx xxxx xxxxxxx xxxxxxx x xxxxxxx X xxxx XX xxx xxxxxxx xxxxxxxx xx xxxxx x xxxxxxx odlišného xxxx neznámého xxxxxxx, xxxxx xx týká Xxxxxxxxxx xxxxxxx.
Článek 9
Rozhodnutí 93/24/EHS x 93/244/XXX xx xxxxxxx xxx xxx xxxxxxxxxxx x xxxxxx 10.
Článek 10
Xxxx xxxxxxxxxx xx použije xxx xxx 1. července 2002.
Xxxxxx 11
Toto rozhodnutí xx určeno členským xxxxxx.
X Bruselu xxx 23. xxxxxxxx 2001.
Xx Xxxxxx
Xxxxx Xxxxx
xxxx Xxxxxx
[1] Xx. věst. x. 121, 29.7.1964, x. 1977/64.
[2] Xx. xxxx. X 163, 4.7.2000, x. 35.
[3] Xx. věst. X 16, 25.1.1993, x. 18.
[4] Xx. xxxx. X 111, 5.5.1993, x. 21.
PŘÍLOHA I
Členské xxxxx xxxx xxxxxx xxxxxxx xxxxxx Aujeszkyho choroby, xx xxxxxxx xx xxxxxxxx xxxxxxxx
Xxxxxx: xxxxxxx xxxxxxx
Xxxxxxx království: všechny xxxxxxx x Xxxxxx, Xxxxxxx x Walesu
Francie: Xxxxxxxxxxxx Xxxxx, Allier, Xxxxxxxx, Xxxèxx, Xxxx, Xxxx, Aveyron, Xxx-Xxxx, Xxxxxxx-xx-Xxôxx, Xxxxxxxx, Xxxxxx, Xxxxxxxx, Xxxxxxxx-Xxxxxxxx, Xxxx, Xxxxèxx, Côte x’Xx, Xxxxxx, Deux-Sèvres, Xxxxxxxx, Xxxxx, Xxxx, Xxxx-xx-Xxxx, Xxxx, Xxxx, Xxxxxxx, Xxxxx-Xxxxxxx, Xxxxx-Xxxxx, Xxxxx-Xxxxx, Xxxxx-Xxxxxxxx, Haut-Rhin, Xxxxx-Xxôxx, Xxxxx, Indre-et-Loire, Xxxx, Xxxxxx, Xxxxx, Xxxxx-Xxxxxxxxxx, Xxxx-xx-Xxxx, Loiret, Lot, Xxx-xx-Xxxxxxx, Xxxèxx, Xxxxx-xx-Xxxxx, Xxxxx, Xxxxxxx-xx-Xxxxxxx, Xxxxx, Xxxxxxx, Nièvre, Oise, Xxxxxxxx-Xxxxxxxxxxx, Puy-de-Dôme, Xxôxx, Xxxxxx, Xxôxx-xx-Xxxxx, Savoie, Xxxxx-Xxxxxxxx, Xxxxx, Xxxxxxxx, Xxxx, Tarn-et-Garonne, Xxxxxxxxxx xx Xxxxxxx, Vendée, Xxxxxx, Xxxxxx x Xxxxx
Xxxxxx: všechny oblasti
Německo: xxxx Xxxxxxxx, Xxxxx, Xxxxxxxxxxxxx, Xxxxxxxxxxxx-Xxxxxxx Pomořansko, Xxxxx-Xxxxxxxxx, Xxxxxx-Xxxxxx a Xxxxxxxx-Xüxxxxxxxxxx
Xxxxxxxx: xxxxxxx xxxxxxx
Xxxxxxx: xxxxxxx oblasti
Lucembursko: xxxx xxxxx.
XXXXXXX XX
Xxxxxxx xxxxx xxxx xxxxxx xxxxxxx, xx kterých xxxx xxxxxxxx schválené xxxxxxxx xx tlumení Xxxxxxxxxx xxxxxxx
Xxxxxxx : všechny xxxxxxx xxxxx xxxx Xxxxxxxx, Xxxxx, Xxxxxxxxxxxxx, Xxxxxxxxxxxx-Xxxxxxx Xxxxxxxxxx, Sasko-Anhaltsko, Xxxxxx-Xxxxxx x Xxxxxxxx-Xüxxxxxxxxxx
XXXXXXX III
Normy pro xxxxxxxxxxx xxxxx xx Xxxxxxxxxx xxxxxxx – xxxxxxxx pro enzymový xxxx xx imunitu (XXXXX) xx xxxxxxxx xxxxxxxxxx na xxx Xxxxxxxxxx xxxxxxx (xxxx xxx), xx xxxxxxxxxxxx X (XXX-xX), xxxxxxxxxxxx X (XXX-xX) xxxx xxxxxxxxxxxx X (XXX-xX)
1. Xxxxxxxxx uvedené x xxxx.2 xxxx. x) xxxxxxx xxxxx a xxxxxxx Elisa ADV-gE xxxxx xxxxxxxx v xxxx. 2 písm. x), x) a x). Xxxxxxxxx xxxxx x xxxxxx členském xxxxx xxxxxxx, xxx xxxx registrovány xxxxx xxxxxxx Xxxxx ADV-gE, xxxxx xxxxxxx xxxx xxxxx. Vyšetření uvedená x xxxx. 2 xxxx. x) x x) xx xxxx xxxxxxxx xxxx schválením xxxxx a vyšetřením xxxxxxxx x xxxx. 2 xxxx. x), x poté xxxx xxx provedena alespoň xx xxxxx xxxxx.
2. Xxxxxxxxxxx, citlivost a xxxxxxxxxxxx testu.
a) Citlivost xxxxx musí být xx takové xxxxxx, xx následující referenční xxxx Xxxxxxxxxxxx xxxx xxxxxxxxx:
- Referenční sérum Xxxxxxxxxxxx XXX 1 xxx xxxxxxx 1:8,
- Xxxxxxxxxx sérum Společenství XXX-xX A,
- Xxxxxxxxxx xxxxx Xxxxxxxxxxxx XXX-xX X,
- Xxxxxxxxxx xxxxx Xxxxxxxxxxxx XXX-xX C,
- Xxxxxxxxxx xxxxx Společenství XXX-xX X,
- Referenční xxxxx Xxxxxxxxxxxx ADV-gE X,
- Xxxxxxxxxx xxxxx Xxxxxxxxxxxx XXX-xX X.
x) Xxxxxxxxxxxx xxxxx xxxx xxx na xxxxxx xxxxxx, xx následující xxxxxxxxxx xxxx Xxxxxxxxxxxx xxxx xxxxxxxxx:
- Xxxxxxxxxx xxxxx Xxxxxxxxxxxx ADV-gE X,
- Xxxxxxxxxx xxxxx Xxxxxxxxxxxx ADV-gE X,
- Xxxxxxxxxx xxxxx Xxxxxxxxxxxx XXX-xX X,
- Referenční xxxxx Xxxxxxxxxxxx XXX-xX X,
- Referenční xxxxx Xxxxxxxxxxxx XXX-xX X,
- Xxxxxxxxxx xxxxx Xxxxxxxxxxxx XXX-xX M,
- Referenční xxxxx Xxxxxxxxxxxx ADV-gE X,
- Xxxxxxxxxx xxxxx Xxxxxxxxxxxx ADV-gE X,
- Xxxxxxxxxx sérum Xxxxxxxxxxxx XXX-xX X,
- Xxxxxxxxxx xxxxx Xxxxxxxxxxxx XXX-xXX.
x) Xxx xxxxxxxx xxxxx xxxx xxx xxxxxxxxxx xxxxx Xxxxxxxxxxxx ADV 1 xxxxxxxxx při xxxxxxx 1:8 a xxxxx z xxxxxxxxxxxx xxx Xxxxxxxxxxxx od XXX-xX X do XXX-xX Q, xxx xx xxxxxxx x xxxx b), xxxx xxx negativní.
Pro xxxxxxxx xxxxxxx XXX-xX x XXX-xX musí být xxxxxxxxxx xxxxx Xxxxxxxxxxxx XXX 1 pozitivní xxx xxxxxxx 1:2 x xxxxxxxxxx xxxxx Xxxxxxxxxxxx X, xxx xx xxxxxxx x xxxx x), xxxx xxx xxxxxxxxx.
x) Xxxxxxxxx xxxxxxx xxxx xxxxx xxxx jiné xxxxxxxxx xxx xxxxxxxx xxxxxxx xxxxxx ELISA x xxxxxx xxxxxxxx státě, x xxxxxxx xxx xxxxxx a xxxxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxxxxx xxx xxxxx referenčních xxx Xxxxxxxxxxxx.
- Xxxxxx – Xxxxxx xx Xxxxxxxxxx xxxxxxxxxxxx xx xxxxxxxxxxxxx, 1180 Xxxxxxxxx,
- Dánsko - Xxxxxxx xxxxxxxæxx Xxxxxxxx for Virusforsknig, Xxxxxxxx, 4771 Xxxxxxxxx,
- Xxxxxxx - Bundesforschungsanstalt xüx Viruskrankheiten xxx Xxxxx, 16868 Xxxxxxxxxxxx,
- Xxxxx- Veterinary Xxxxxxxxx xx Xxxxxxxxxx and Xxxxxxxxx Xxxxxxxx, 15310 Xx. Xxxxxxxxx,
- Španělsko - Xxxxxxxxxxx Xxxxxxx xx Veterinaria xx Xxxxxx, Xxxxxx,
- Xxxxxxx - Xxxxx nationale xxxxxxxxxxx, Xxxxxx, 94704 Xxxxxxx-Xxxxxx,
- Xxxxx - Xxxxxxxxxx Xxxxxxxx Xxxxxxxxxx, Xxxxxxxxxx, Castleknock, Xxxxxx 15,
- Xxxxxx - Xxxxxxxx Xxxxxxxxxxxxxxx Sperimentale xxxxx Xxxxxxxxx x xxxx‘Xxxxxx-Xxxxxxx, Xxxxxxx,
- Lucembursko - Xxxxxxxxxxx de Xxxxxxxx Vétérinaire de x’Xxxx, 1020 Xxxxxxxxxx,
- Xxxxxxxxxx - Instituut xxxx Veehouderij xx Xxxxxxxxxxxxxx (ID-DLO), 8200 XX Xxxxxxxx,
- Xxxxxxxx - Xxxxxxxxxxxxx xüx xxxxxxxäxxxxxxxxxxxxx Untersuchungen xx Xöxxxxx, 2,40 Modling,
- Xxxxxxxxxxx - Xxxxxxxxxxx Xxxxxxxx xx Xxxxxxxxxãx Xxxxxxxxxxx, 1500 Xxxxxx,
- Xxxxxx - Xxäxxxääxxxxä- xx elintarviketutkimuslaitos, 00581 Xxxxxxxx,
- Švédsko - Xxxxxxx xxxxxxxxxxxxxxxxxxx xxxxxxx, 75189 Uppsala,
- Xxxxxxx xxxxxxxxxx - Xxxxxxxxxx Xxxxxxxxxx Xxxxxx, Xxx Xxx, Weybridge, Xxxxxx XX15 3XX.
XXXXXXX XX
&xxxx;


