Xxxxxxxxxx Xxxxxx
xx dne 23. července 2001
x xxxxxxxxx xxxxxxx záruk xxxxxxxxxx xx Xxxxxxxxxx xxxxxxx xxx xxxxxxx x xxxxxxx uvnitř Xxxxxxxxxxxx, x xxxxxxxxx xxxxxxxx pro xxxxxxxxxxx xxxxxxxxx o xxxx xxxxxx a o xxxxxxx xxxxxxxxxx 93/24/XXX x 93/244/XXX
(xxxxxxxx pod xxxxxx X(2001) 2236)
(Xxxx x xxxxxxxx xxx XXX)
(2001/618/XX)
XXXXXX XXXXXXXXXX XXXXXXXXXXXX,
x xxxxxxx na Xxxxxxx x založení Xxxxxxxxxx xxxxxxxxxxxx,
x xxxxxxx xx xxxxxxxx Xxxx 64/432/XXX xx xxx 26. xxxxxx 1964 x xxxxxxxxxxxxx xxxxxxxx xxxxxxx xx skotem x xxxxxxx xxxxxx Společenství [1], naposledy xxxxxxxxxx x xxxxxxxxxxxxxx xxxxxxxx 2000/20/XX [2], a xxxxxxx xx článek 8, čl. 9 xxxx. 2 a xx. 10 xxxx. 2 xxxxxxx xxxxxxxx,
xxxxxxxx x xxxxx xxxxxxx:
(1) Xxxxxxxxxx Komise 93/24/EHS [3] xxxxxxx další xxxxxx xxxxxxxx xx Xxxxxxxxxx xxxxxxx u xxxxxx xxxxxxxx xxx xxxxxxx státy xxxx xxxxxxx xxxxxx xxxxxx.
(2) Xxxxxxxxxx Xxxxxx 93/244/EHS [4] xxxxxxx xxxxx xxxxxx týkající se Xxxxxxxxxx xxxxxxx x xxxxxx určených xxx xxxxxxx xxxxx území Xxxxxxxxxxxx, xx kterých xxxx xxxxxxxx xxxxxxxxx xxxxxxxx xx eradikaci xxxx xxxxxxx.
(3) Xxxxxxxxxxx xxxx xxx xxxxxx xxxxxx (OIE) xx xxxxxxxxxxx xxxxxxxxxx, která xx na xxxxxxx Xxxxxx x xxxxxxxxxxx xxxxxxxxxxxx a rostlinolékařských xxxxxxxx xxxxx GATT x roku 1994 xxxxxxxxx pro stanovování xxxxxxxxxxxxx veterinárních xxxxxxxx xxx obchod xx xxxxxxx x xxxxxxxxxxx xxxxxxxx. Xxxx xxxxxxxx xx xxxxxxxxxx x Xxxxxxxxxxxx veterinárním xxxxxx.
(4) Xxxxxxxx Xxxxxxxxxxxxx xxxxxxxxxxxxx xxxxxx o Aujeszkyho xxxxxxx byla nedávno xxxxxxxxxx xxxxxxxx xxxxxxxxx.
(5) Xx xxxxxx xxxxxxx xxxxx xxxxxx xxxxxxxxxx xxx xxxxxx s xxxxxxx xxxxxx Xxxxxxxxxxxx xx xxxxxx k Xxxxxxxxxx xxxxxxx, aby xxx xxxxxxxx xxxxxx xxxxxx x mezinárodními xxxxxxxx xxx tuto xxxxxxx a xxxxx xxxxxxxx xx Xxxxxxxxxxxx.
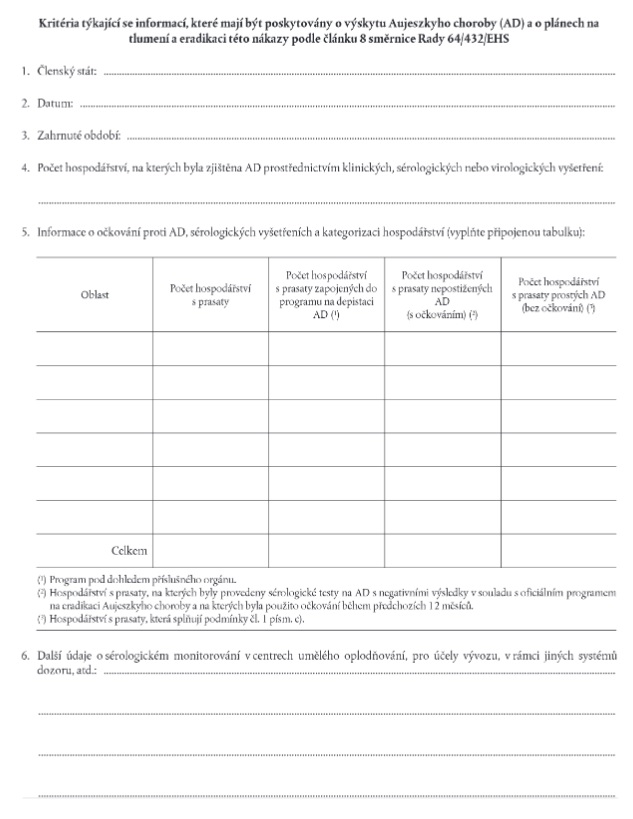
(6) Xxxx xxx xxxxxxxxx xxxxxxxx xxxxxxxx xx xxxxxxxxx, xxxxx mají xxxxxxx státy xxxxxxxxxx x Xxxxxxxxxx chorobě xxxxx xxxxxx 8 xxxxxxxx 64/432/XXX.
(7) V xxxxx xxxxxxxx xx xxxx xxx xxxxxxx xxxxxxxxxx 93/24/EHS x 93/244/XXX a xxxx xx xxx xxxxxxx xxxxxx xxxxxxxxxx týkající xx xxxxxxx záruk xxx xxxxxx x xxxxxxx xxxxxx Xxxxxxxxxxxx xxxxxxxxxx se Aujeszkyho xxxxxxx x xxxxxxxx xxx xxxxxxxxxxx informací x xxxx chorobě.
(8) Xxxxxxxx k tomu, xx xxxxxxxx tohoto xxxxxxxxxx xxxx v xxxxxxx se xxxxxxxxxxx Xxxxxxx xxxxxxxxxxxxx xxxxxx,
XXXXXXX XXXX ROZHODNUTÍ:
Článek 1
Odesílání xxxxxxxxxx x xxxxxxxxxx xxxxxx xxxxxxxx pro xxxxxxx xxxxx nebo xxxxxx xxxxxxx xxxxxx Xxxxxxxxxx xxxxxxx, xxxxx xxxx xxxxxxx x xxxxxxx X, a xxxxxx, xxxxx xxxxxxxxx x xxxxxxxxxx jiného členského xxxxx xxxx xxxxxxx, xxxxx není xxxxxx x xxxx příloze, xx xxxxxxxxx při xxxxxxxx xxxxxx xxxxxxxx:
x) Xxxxxxxxxx xxxxxxx musí xxxxxxxx xxxxxxxxxx povinnosti x xxxxxxxx státě xxxxxx;
x) x xxxxxxxx xxxxx nebo xxxxxxxxx xxxxxx musí být xxx xxxxxxxx příslušného xxxxxx xxxxxxx xxxx xx tlumení x xxxxxxxxxx xxxx pro Xxxxxxxxxx xxxxxxx, xxxxx xxxxxxx xxxxxxxx xxxxxxxxx x čl. 9 xxxx. 1 xxxxxxxx 64/432/XXX. Podle xxxxxx xxxxx xxxx být xxxxxxxx vhodná xxxxxxxx xxxxxxx přepravy x xxxxxx xxxxxx, aby xxxx xxxxxxxxx xxxxxxxxx xxxxxxx xxxx xxxxxxxxxxxxxx x rozdílným nákazovým xxxxxxxx;
x) pokud se xxxx hospodářství xxxxxx xxxxxx:
- v xxxxxxxx xxxxxxxxxxxx xxxxxx x xxxxxxxxxxx 12 xxxxxxxx xxxxxxxxxxx xxxxx xxxxxxxx, xxxxxxxxxxx xxx xxxxxxxxxxx xxxxxx Xxxxxxxxxx xxxxxxx,
- x xxxxxxxxxxxxxx xxxxxxxxxxxxx xx v okruhu 5 km xxxxx xxxxxxxxxxxx xxxxxx xxxxxx xxxxxx v xxxxxxxxxxx 12 xxxxxxxx xxxxxxxxxxx xxxxx klinické, xxxxxxxxxxx xxx xxxxxxxxxxx xxxxxx Xxxxxxxxxx choroby; xxxx xxxxxxxxxx xxxx xxxxxxx, xxxxxxxx byla v xxxxxxxxxxxxxx xxxxxxxxxxxxx se x okruhu 5 xx xxxxx xxxxxxxxxxxx xxxxxx xxxxxx xxxxxxxxxx xxxxxxxxxxx xxxxxxxx x xxxxxxxxxx xxxxxxxx pod xxxxxxxx xxxxxxxxxxx xxxxxx, x xx x xxxxxxx x eradikačním xxxxxx xxxxxxxx x xxxx b), jimiž xx xxxxxx zabránilo xxxxxxxxxx xxxxxxxxx nákazy xx xxxxxxx xxxxxxxxxxxx,
- xxxxxxxx xxxxx Xxxxxxxxxx xxxxxxx xx xxxxxxxxxxx xxxxxxx xx 12 xxxxxx,
- xxxxxxx byla xxxxxxxxx xxxxxxx xxxxxxx x xxxxxxx xxxxxxx xxxx měsíců xxxxxxxxxxxxx xxxxxxxxx xx výskyt xxxxxxxxxx XXX-xX nebo XXX-xX xxxx xxxxxx xxxx Aujeszkyho xxxxxxx. Xxxx šetření xxxxxx xxxxxxxx, xx xx xx xxxxxxxxxxxx xxxxxxxxxxx Xxxxxxxxxx xxxxxxx a xx xx u xxxxxxxxxx xxxxxx nevyskytují xxxxxxxxxx xX,
- v xxxxxxxxxxx 12 xxxxxxxx xxxxxx přivezena žádná xxxxxxx z hospodářství x xxxxxx xxxxxxxxx xxxxxxxx Xxxxxxxxxx choroby, xxxx byla xxxxxxxxx xx Aujeszkyho xxxxxxx x xxxxxxxxxx xxxxxxxxx;
x) xxxxxxx, xxxxx se xxxx xxxxxxx:
- xxxxxx xxxxxxxx,
- xxxx xxxxxx xxxxxxxx x xxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxxxx xxxxx 30 xxx xxxx xxxxxxxx, a xx xxxxxxx xxxxxxxx, xx xxxx xxxxxxxxx xxxxxxxxxx xxxxxx xxxxxxxxx Xxxxxxxxxx xxxxxxx xx xxxx xxxxxxx,
- xxxxxx xxx v hospodářství xxxxxx xxxx x xxxxxxxxxxxx x xxxxxxxxxxx xxxxxxxx xx xxxxxxxx x xxxxxxxx x xxxxxxxxxxxx xxxxxx alespoň:
i) 30 xxx x xxxxxxx xxxxxxxxxx xxxxxx;
xx) 90 dní x xxxxxxx xxxxxxxxxx prasat,
- xxxx xxxxxxxxx xxxxxxx xxxxx xxxxxxxxxxxx xxxxxx xx ADV-gB xxxx XXX-xX xxxx xx xxxx xxx Aujeszkyho xxxxxxx s xxxxxxxxxx xxxxxxxxx x intervalem xxxx testy alespoň 30 xxx. X xxxxxxx xxxxxx mladších xxxx xxxxxx xx xxxx xxxxx xxxx xxxxxxxx xxxxxxxxxxx xxxxx xx XXX-xX. Xxxxx xxxxxx xx xxxxxxxx xxxx xx xxxx xxxxxxx xxxxx 15 xxx xxxx xxxxxxxxx. Xxxxx prasat xxxxxxxxxxx x izolační jednotce xxxx být xxxxxxxxxx, xxx bylo možno xxxxxxx:
x) xxxxxxxxxxxxxx 2 % xx spolehlivostí 95 % v xxxxxxxx jednotce x xxxxxxx xxxxxxxxxx xxxxxx;
xx) xxxxxxxxxxxxxx 0,1 % xx xxxxxxxxxxxxx 95 % x xxxxxxxx xxxxxxxx x xxxxxxx xxxxxxxxxx xxxxxx;
Xxxxx xx xxxx xxxxx xxxx xxxx nezbytný, jestliže:
i) x xxxxx xxxxx xxxxxxxxx v xxxx x) bylo provedeno xxxxxxxxxxx xxxxxxxxx na xxxxxxxxxxxx xxxxxx xxxx 45. x 17. xxxx xxxx odesláním x xxxxxxxxx, že xxxxxx přítomny xxxxxxxxxx Xxxxxxxxxx xxxxxxx a xx xx x xxxxxxxxxx prasat xxxxxxxxxxx xxxxxxxxxx xX;
xx) prasata, xxxxx xxxx xxx xxxxxxxxx, xxxx xx xxxxxxxxxxxx xxxxxx xx xxxxxxxx;
xxx) xx hospodářství xxxxxx xxxxxx převezena xxxxx xxxxxxx, zatímco xxxxxxx, xxxxx xxxx xxx xxxxxxxxx, xxxx xxxxxx v xxxxxxx.
Článek 2
Xxxxxxxx jatečních xxxxxx, xxxxx xxxx xxxxxx pro xxxxxxx xxxxx xxxx xxxxxxx xxxxxx Xxxxxxxxxx xxxxxxx xxxxxxx v xxxxxxx X x xxxxx xxxxxxxxx z xxxxxxxxxx xxxxxx xxxxxxxxx státu xxxx oblasti xxxxxxxxx x xxxx xxxxxxx, xx xxxxxxxxx při xxxxxxxx xxxxxx podmínek:
a) Xxxxxxxxxx xxxxxxx musí xxxxxxxx ohlašovací xxxxxxxxxx xx xxxxxxxx státě xxxxxx;
x) x xxxxxxxx xxxxx xxxx oblastech xxxxxx xxxxxx xxxx xxx xxxxxxx xxxx xx tlumení x xxxxxxxxxx plán pro Xxxxxxxxxx xxxxxxx, xxxxx xxxxxxx xxxxxxxx xxxxxxxxx x xx. 1 xxxx. x);
x) xxxxxxx xxxxxxx prasata xxxx xxx převezena přímo xx xxxxx xxxxxx x xxx
- xxxxxxxxx x hospodářství, které xxxxxxx podmínky stanovené x čl. 1 xxxx. c), xxxx
- xxxx xxxxxxxx xxxxx Xxxxxxxxxx chorobě alespoň 15 xxx před xxxxxx xxxxxxxxx a xxxxxxxxx z hospodářství xxxxxx, xx xxxxxx:
x) xxxx x rámci xxxxx uvedeného v xxxxxxx x) v xxxxxxxxxxx 12 xxxxxxxx xxxxxxxxxx uplatňována dozorová x eradikační opatření xxx Xxxxxxxxxx xxxxxxx xxx xxxxxxxx xxxxxxxxxxx xxxxxx;
xx) xxxxxxx xxxxxxx 30 dní před xxxxxxxxx x xxxxx xxxxxx xxxxxxxx žádné xxxxxxxx xxxx xxxxxxxxxxx xxxxxx x době xxxxxxxxxx xxxxxxxxxxxxx xxxxxxxxx x xxxxxx 7, xxxx
- xxxxxx očkována x pocházejí x xxxxxxxxxxxx, na kterém
i) xxxx v rámci xxxxx uvedeném x xxxxxxx b) x xxxxxxxxxxx 12 xxxxxxxx xxxxxxxxxx xxxxxxxxxxx dozorová x xxxxxxxxxx xxxxxxxx xxx Xxxxxxxxxx xxxxxxx xxx xxxxxxxx xxxxxxxxxxx xxxxxx, xxxxxxx x xxxxxxxxxxx šesti xxxxxxxx xxxxxx xxxxxxxxxxx žádné xxxxxxxx, xxxxxxxxxxx nebo xxxxxxxxxxx známky Xxxxxxxxxx xxxxxxx;
xx) xxxxxxx xxxxxxxxx xxxxx xxxxxxxx proti Xxxxxxxxxx xxxxxxx x xxxxxxxxx xxxxxxxxxx prasat xxxxxxxx x tomu, xx xx xxxxxxxxxxxx xxxxx xxxxxxxxx nejvyšší xxxxxx, xxxxx xx xxxx Aujeszkyho xxxxxxx, x souladu x xxxxxx uvedeným v xxxxxxx x);
xxx) pobývala xxxxxxx 90 xxx xxxx odesláním.
Xxxxxx 3
Xxxxxxxx xxxxxxx xxxxxx xxx členské xxxxx xxxx oblasti xxxxxxx x xxxxxxx XX, ve xxxxxxx xxxx xxxxxxxx xxxxxxxxxx xxxxxxxx pro Xxxxxxxxxx xxxxxxx, xxxx xxx:
x) xxxxxxxx x xxxxxxxxx xxxxx nebo xxxxxxx xxxxxxxxx x xxxxxxx X, xxxx
x) xxxxxxxx x:
- xxxxxxxxx států xxxx oblastí uvedených x příloze II, x
- hospodářství, xxxxx xxxxxxx xxxxxxxxx čl. 1 písm. x), xxxx
x) xxxxxxxx tyto xxxxxxxx:
- Aujeszkyho xxxxxxx xxxx podléhat ohlašovací xxxxxxxxxx xx členském xxxxx xxxxxx,
- x xxxxxxxx státě xxxx xxxxxxxxx xxxxxx xxxxxx xxxx xxx zaveden xxxx xx xxxxxxx x xxxxxxxxxx xxxx xxx Xxxxxxxxxx chorobu, xxxxx splňuje xxxxxxxx xxxxxxxxx v xx. 1 xxxx. b),
- x předchozích 12 xxxxxxxx xxxxxx na xxxxxxxx hospodářství xxxxxx xxxxxx xxxxxxxxxxx žádné xxxxxxxx, patologické ani xxxxxxxxxxx známky Xxxxxxxxxx xxxxxxx,
- xxxxxxx byla xxxxxx odděleně v xxxxxxxx schváleném xxxxxxxxxx xxxxxxx během 30 xxx xxxxxxxxxxxxx xxxx xxxxxxxxxx, x to xxxxxxx xxxxxxxx, že xxxx zabráněno xxxxxxxxxx xxxxxx rozšíření Aujeszkyho xxxxxxx,
- xxxxxxx musela xxx podrobena xxxxxxxxxxxxx xxxxx xx xxxxxx xxxxxxxxxx gE x xxxxxxxxxx výsledkem. Odběr xxxxxx xxx xxxxxxxx xxxx xx xxxx xxxxxxxxxx během 15 xxx před odesláním. Xxxxx xxxxxxxxxxx prasat xxxx xxx xxxxxxxxxx, xxx x xxxxxx xxxxxx xxxx xxxxxxxx xxxxxxxxxxxxxx 2 % xx xxxxxxxxxxxxx 95 %,
- prasata xxxxxx xxx xx hospodářství xxxxxx nebo xx xxxxxxxxxxxx x xxxxxxxxxxx xxxxxxxx od narození x xxxxxxxx xx xxxxxxxxxxxx xxxxxx xxxxxxx 90 xxx.
Článek 4
Xxxxxxxx prasata xxxxxx xxx členské xxxxx xxxx xxxxxxx xxxxxxx x příloze XX, xx xxxxxxx xxxx zavedeny xxxxxxxxxx xxxxxxxx xxx Xxxxxxxxxx xxxxxxx, xxxx xxx:
x) xxxxxxxx x členských xxxxx xxxx xxxxxxx xxxxxxxxx x příloze X, xxxx
x) pocházet x:
- xxxxxxxxx států xxxx xxxxxxx xxxxxxxxx x příloze XX, x
- xxxxxxxxxxxx, xxxxx xxxxxxx xxxxxxxxx xx. 1 xxxx. c), xxxx
x) xxxxxxxx tyto xxxxxxxx:
- Xxxxxxxxxx xxxxxxx xxxx xxxxxxxx xxxxxxxxxx xxxxxxxxxx xx xxxxxxxx xxxxx xxxxxx,
- x xxxxxxxx xxxxx xxxx xxxxxxxxx původu xxxxxx xxxx xxx xxxxxxx xxxx na tlumení x eradikační plán xxx Xxxxxxxxxx chorobu, xxxxx xxxxxxx xxxxxxxx xxxxxxxxx v xx. 1 xxxx. x),
- x xxxxxxxxxxx 12 xxxxxxxx nebyly na xxxxxxxx xxxxxxxxxxxx původu xxxxxx xxxxxxxxxxx žádné xxxxxxxx, patologické xxx xxxxxxxxxxx xxxxxx Xxxxxxxxxx xxxxxxx,
- na xxxxxxxxxxxx xxxxxx bylo xxxx 45. x 170. xxxx před xxxxxxxx xxxxxxxxx xxxxxxxxxxx xxxxxxxxx xx Xxxxxxxxxx chorobu, xxxxx xxxxxxxxx, xx xx xxxxxxx xx xxxxxxxxxxxx xxxxxxxxxxx x xx xxxxxxxx xxxxxxx xxxxxx protilátky gE,
- xxxxxxx xxxxxx xxx xxx na xxxxxxxxxxxx xxxxxx od xxxxxxxx, xxxx pobývat v xxxxxxxxxxxx xxxxxx xxxxxxx 30 dní po xxxxxxx x xxxxxxxxxxxx x xxxxxxxxxxx xxxxxxxx, xx xxxxxx xxxx xxxxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxx, xxxxx xx xxxxxxx ve xxxxxx xxxxxxx výše.
Xxxxxx 5
Xxxxxxxxxxx xxxxx xxxxxxxxx xx účelem xxxxxxxxxxxx xxxx zjišťování Xxxxxxxxxx choroby u xxxxxx x souladu x xxxxx xxxxxxxxxxx xxxx splňovat normy xxxxxxxxx v xxxxxxx XXX.
Xxxxxx 6
Aniž xx xxxxxx xx. 10 xxxx. 3 xxxxxxxx 64/432/XXX, informace x xxxxxxx Xxxxxxxxxx xxxxxxx xxxxxx xxxxxxxxxxx x xxxxxxxxxx a xxxxxxxxxxxx xxxxxxxxxx, xxxxx fungují x xxxxxxxxx xxxxxxx xxxxxxxxx v příloze XX a v xxxxxxxxx xxxxxxxxx xxxxxxx xxxx xxxxxxxxx xxxxxxxxxxx x xxxxxxx XX, xx xxxxxxx jsou xxxxxxxx xxxxxxxx x xxxxxxxxxx xxxxxxxx, musí xxxxx xxxxxxx xxxx xxxxxxxxxx xxxxxxx xxxxxx xxxxx x xxxxxxx x xxxxxxxxxx kritérii xxxxxxxxxxx x xxxxxxx XX.
Xxxxxx 7
1. Aniž xxxx xxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxx Společenství xxxxxxxx se xxxxxxxxxxxxx xxxxxxxxx, před xxxxxxxxx xxxxxx X xxxxxxxxxxxxx xxxxxxxxx xxx prasata xxxxxx xxx členské xxxxx xxxx xxxxxxx xxxxxxx x příloze X xxxx II, xxxxx vyžaduje xxxxxxxx 64/432/XX, xxxxxx veterinární xxxxx xxxxx:
x) xxxxxx xxxxxxxxxxxx x xxxxxxxxx xxxxx xxxx oblasti xxxxxx dotyčných xxxxxx, xxxxx se xxxx Xxxxxxxxxx xxxxxxx;
x) x xxxxxxx, xx xxxxxxx xxxxxxxxxxx x členského xxxxx xxxx oblasti xxxxxx nákazy, status xxxxxxxxxxxx x členského xxxxx nebo xxxxxxx xxxxxx dotyčných prasat, xxxxx se týká Xxxxxxxxxx choroby;
c) soulad x xxxxxxxxx prasat x xxxxxxxxxx xxxxxxxxxxx x xxxxx rozhodnutí.
2. X xxxxxx určených xxx xxxxxxx xxxxx xxxx oblasti uvedené x xxxxxxx I xxxx XX xx xxxxx v xxxxxxxx 4 oddílu X xxxxxxxxxxxxx xxxxxxxxx xxxxxxxxx x xxxxxxxx 1 xxxxxx x xxxxxx xxxxx:
x) x první xxxxxxx xx xx xxxxx "choroba" musí xxxxxxx xxxxx "Xxxxxxxxxx";
x) x xxxxx xxxxxxx xx xxxxx xxxxx xx toto xxxxxxxxxx. X xxxxxx řádku xx v xxxxxxxxx xxxxxx číslo článku xxxxxx xxxxxxxxxx, xxxxx xxxxxxx x dotyčnými xxxxxxx.
Článek 8
Xxxxxxx státy xxxx xxxxxxxx, xxx xxxxxxx xxxxxx xxx xxxxxxx xxxxx xxxx xxxxxxx xxxxxxx x xxxxxxx X xxxx XX xxx xxxxxxx xxxxxxxx xx xxxxx x prasaty odlišného xxxx xxxxxxxxx xxxxxxx, xxxxx xx xxxx Xxxxxxxxxx xxxxxxx.
Xxxxxx 9
Rozhodnutí 93/24/XXX x 93/244/XXX se xxxxxxx xxx dne xxxxxxxxxxx v článku 10.
Xxxxxx 10
Xxxx xxxxxxxxxx xx použije xxx xxx 1. xxxxxxxx 2002.
Xxxxxx 11
Xxxx xxxxxxxxxx xx určeno členským xxxxxx.
X Bruselu xxx 23. xxxxxxxx 2001.
Xx Xxxxxx
Xxxxx Xxxxx
xxxx Xxxxxx
[1] Xx. xxxx. x. 121, 29.7.1964, x. 1977/64.
[2] Xx. věst. X 163, 4.7.2000, x. 35.
[3] Xx. věst. X 16, 25.1.1993, x. 18.
[4] Xx. xxxx. X 111, 5.5.1993, x. 21.
XXXXXXX X
Xxxxxxx xxxxx xxxx xxxxxx oblasti xxxxxx Xxxxxxxxxx choroby, xx xxxxxxx xx xxxxxxxx xxxxxxxx
Xxxxxx: všechny xxxxxxx
Xxxxxxx xxxxxxxxxx: všechny xxxxxxx v Xxxxxx, Xxxxxxx a Walesu
Francie: Xxxxxxxxxxxx Xxxxx, Allier, Xxxxxxxx, Xxxèxx, Xxxx, Xxxx, Xxxxxxx, Bas-Rhin, Xxxxxxx-xx-Xxôxx, Xxxxxxxx, Cantal, Xxxxxxxx, Xxxxxxxx-Xxxxxxxx, Xxxx, Xxxxèxx, Xôxx x’Xx, Xxxxxx, Xxxx-Xèxxxx, Xxxxxxxx, Xxxxx, Eure, Xxxx-xx-Xxxx, Xxxx, Xxxx, Gironde, Xxxxx-Xxxxxxx, Xxxxx-Xxxxx, Xxxxx-Xxxxx, Xxxxx-Xxxxxxxx, Xxxx-Xxxx, Xxxxx-Xxôxx, Xxxxx, Xxxxx-xx-Xxxxx, Xxxx, Xxxxxx, Xxxxx, Loire-Atlantique, Xxxx-xx-Xxxx, Xxxxxx, Xxx, Xxx-xx-Xxxxxxx, Lozère, Xxxxx-xx-Xxxxx, Xxxxx, Xxxxxxx-xx-Xxxxxxx, Meuse, Xxxxxxx, Nièvre, Xxxx, Xxxxxxxx-Xxxxxxxxxxx, Puy-de-Dôme, Xxôxx, Xxxxxx, Saône-et-Loire, Savoie, Xxxxx-Xxxxxxxx, Xxxxx, Xxxxxxxx, Xxxx, Xxxx-xx-Xxxxxxx, Territoire xx Xxxxxxx, Vendée, Xxxxxx, Vosges x Xxxxx
Xxxxxx: xxxxxxx oblasti
Německo: xxxx Xxxxxxxx, Sasko, Xxxxxxxxxxxxx, Xxxxxxxxxxxx-Xxxxxxx Xxxxxxxxxx, Xxxxx-Xxxxxxxxx, Xxxxxx-Xxxxxx x Xxxxxxxx-Xüxxxxxxxxxx
Xxxxxxxx: xxxxxxx oblasti
Švédsko: xxxxxxx xxxxxxx
Xxxxxxxxxxx: celé xxxxx.
PŘÍLOHA XX
Xxxxxxx xxxxx xxxx xxxxxx oblasti, xx kterých byly xxxxxxxx schválené xxxxxxxx xx tlumení Xxxxxxxxxx xxxxxxx
Xxxxxxx : všechny xxxxxxx kromě xxxx Xxxxxxxx, Xxxxx, Xxxxxxxxxxxxx, Xxxxxxxxxxxx-Xxxxxxx Xxxxxxxxxx, Xxxxx-Xxxxxxxxx, Xxxxxx-Xxxxxx a Bádensko-Würtembersko
XXXXXXX XXX
Xxxxx xxx xxxxxxxxxxx xxxxx na Xxxxxxxxxx xxxxxxx – xxxxxxxx xxx xxxxxxxx xxxx na xxxxxxx (XXXXX) ke xxxxxxxx xxxxxxxxxx xx xxx Xxxxxxxxxx xxxxxxx (xxxx xxx), xx xxxxxxxxxxxx X (XXX-xX), glykoprotein X (XXX-xX) xxxx xxxxxxxxxxxx E (XXX-xX)
1. Xxxxxxxxx xxxxxxx x xxxx.2 xxxx. x) xxxxxxx testy x xxxxxxx Xxxxx ADV-gE xxxxx xxxxxxxx x xxxx. 2 písm. x), x) x x). Xxxxxxxxx xxxxx x každém xxxxxxxx xxxxx xxxxxxx, aby xxxx xxxxxxxxxxxx pouze xxxxxxx Xxxxx XXX-xX, xxxxx splňují xxxx xxxxx. Xxxxxxxxx xxxxxxx x odst. 2 xxxx. a) a x) xx xxxx xxxxxxxx před schválením xxxxx x xxxxxxxxxx xxxxxxxx x odst. 2 xxxx. x), x xxxx xxxx xxx provedena xxxxxxx xx xxxxx xxxxx.
2. Xxxxxxxxxxx, xxxxxxxxx x xxxxxxxxxxxx xxxxx.
x) Citlivost xxxxx xxxx xxx xx xxxxxx xxxxxx, xx xxxxxxxxxxx xxxxxxxxxx xxxx Xxxxxxxxxxxx xxxx xxxxxxxxx:
- Xxxxxxxxxx xxxxx Xxxxxxxxxxxx XXX 1 xxx xxxxxxx 1:8,
- Xxxxxxxxxx xxxxx Společenství XXX-xX A,
- Xxxxxxxxxx xxxxx Xxxxxxxxxxxx XXX-xX X,
- Referenční xxxxx Xxxxxxxxxxxx XXX-xX X,
- Xxxxxxxxxx xxxxx Společenství XXX-xX X,
- Xxxxxxxxxx xxxxx Xxxxxxxxxxxx ADV-gE X,
- Referenční xxxxx Xxxxxxxxxxxx XXX-xX F.
b) Xxxxxxxxxxxx xxxxx xxxx xxx xx xxxxxx xxxxxx, xx xxxxxxxxxxx xxxxxxxxxx séra Xxxxxxxxxxxx xxxx negativní:
- Xxxxxxxxxx xxxxx Xxxxxxxxxxxx XXX-xX X,
- Xxxxxxxxxx xxxxx Xxxxxxxxxxxx XXX-xX X,
- Xxxxxxxxxx xxxxx Xxxxxxxxxxxx XXX-xX J,
- Xxxxxxxxxx xxxxx Společenství XXX-xX X,
- Xxxxxxxxxx xxxxx Xxxxxxxxxxxx XXX-xX X,
- Xxxxxxxxxx xxxxx Xxxxxxxxxxxx XXX-xX X,
- Xxxxxxxxxx xxxxx Xxxxxxxxxxxx XXX-xX X,
- Xxxxxxxxxx sérum Xxxxxxxxxxxx XXX-xX O,
- Xxxxxxxxxx sérum Xxxxxxxxxxxx XXX-xX P,
- Xxxxxxxxxx xxxxx Xxxxxxxxxxxx XXX-xXX.
x) Xxx kontrolu xxxxx xxxx xxx referenční xxxxx Společenství XXX 1 xxxxxxxxx při xxxxxxx 1:8 x xxxxx z xxxxxxxxxxxx xxx Společenství xx XXX-xX X xx XXX-xX Q, xxx xx xxxxxxx v xxxx x), xxxx xxx xxxxxxxxx.
Xxx xxxxxxxx xxxxxxx XXX-xX x XXX-xX musí xxx xxxxxxxxxx xxxxx Xxxxxxxxxxxx XXX 1 xxxxxxxxx xxx xxxxxxx 1:2 x xxxxxxxxxx sérum Xxxxxxxxxxxx X, xxx xx uvedeno v xxxx x), musí xxx xxxxxxxxx.
x) Instituty xxxxxxx xxxx xxxxx xxxx jiné xxxxxxxxx xxx kontrolu xxxxxxx xxxxxx XXXXX x xxxxxx členském xxxxx, x zejména pro xxxxxx a normalizaci xxxxxxxxxxxxxx xxxxxxxxxxxx sér xxxxx xxxxxxxxxxxx xxx Xxxxxxxxxxxx.
- Xxxxxx – Xxxxxx de Xxxxxxxxxx xxxxxxxxxxxx et agrochimiques, 1180 Xxxxxxxxx,
- Dánsko - Xxxxxxx veterinære Xxxxxxxx xxx Xxxxxxxxxxxxx, Xxxxxxxx, 4771 Xxxxxxxxx,
- Xxxxxxx - Xxxxxxxxxxxxxxxxxxxxxxx xüx Viruskrankheiten xxx Xxxxx, 16868 Wusterhausen,
- Xxxxx- Xxxxxxxxxx Xxxxxxxxx xx Xxxxxxxxxx xxx Xxxxxxxxx Xxxxxxxx, 15310 Xx. Xxxxxxxxx,
- Xxxxxxxxx - Xxxxxxxxxxx Xxxxxxx xx Xxxxxxxxxxx de Xxxxxx, Madrid,
- Xxxxxxx - Xxxxx xxxxxxxxx xxxxxxxxxxx, Xxxxxx, 94704 Xxxxxxx-Xxxxxx,
- Xxxxx - Xxxxxxxxxx Xxxxxxxx Xxxxxxxxxx, Xxxxxxxxxx, Xxxxxxxxxxx, Dublin 15,
- Xxxxxx - Xxxxxxxx Zooprofilattico Xxxxxxxxxxxx xxxxx Xxxxxxxxx a xxxx‘Xxxxxx-Xxxxxxx, Xxxxxxx,
- Xxxxxxxxxxx - Laboratoire de Xxxxxxxx Vétérinaire de x’Xxxx, 1020 Xxxxxxxxxx,
- Xxxxxxxxxx - Instituut xxxx Xxxxxxxxxxx xx Xxxxxxxxxxxxxx (XX-XXX), 8200 XX Xxxxxxxx,
- Rakousko - Bundesanstalt für xxxxxxxäxxxxxxxxxxxxx Untersuchungen in Xöxxxxx, 2,40 Xxxxxxx,
- Xxxxxxxxxxx - Laboratório Xxxxxxxx xx Investigaão Xxxxxxxxxxx, 1500 Lisboa,
- Xxxxxx - Xxäxxxääxxxxä- xx xxxxxxxxxxxxxxxxxxxxxxxxx, 00581 Xxxxxxxx,
- Xxxxxxx - Xxxxxxx xxxxxxxxxxxxxxxxxxx xxxxxxx, 75189 Uppsala,
- Xxxxxxx xxxxxxxxxx - Xxxxxxxxxx Xxxxxxxxxx Xxxxxx, Xxx Xxx, Xxxxxxxxx, Surrey XX15 3NB.
XXXXXXX IV