Xxxxxxxx Komise 96/54/es
ze xxx 30. července 1996,
xxxxxx xx xx xxxxxxx druhé přizpůsobuje xxxxxxxxxxx xxxxxxx směrnice Xxxx 67/548/EHS x xxxxxxxxxx xxxxxxxx x xxxxxxxxx xxxxxxxx xxxxxxxxxx xx xxxxxxxxxxx, xxxxxx x označování xxxxxxxxxxxx xxxxx
XXXXXX XXXXXXXXXX XXXXXXXXXXXX,
x xxxxxxx xx Smlouvu x xxxxxxxx Evropského xxxxxxxxxxxx,
x xxxxxxx na xxxxxxxx Rady 67/548/XXX xx xxx 27. xxxxxx 1967 x xxxxxxxxxx xxxxxxxx x xxxxxxxxx předpisů xxxxxxxxxx xx xxxxxxxxxxx, xxxxxx x označování nebezpečných xxxxx [1], xxxxxxxxx xxxxxxxxxx směrnicí Xxxxxx 94/96/XX [2], x xxxxxxx xx xxxxxx 28 uvedené xxxxxxxx,
xxxxxxxx x xxxx, xx xxxxxxx X xxxxxxxx Xxxx 67/548/EHS xxxxxxxx xxxxxx xxxxxxxxxxxx xxxxx, xxxxxx klasifikaci, xxxxxxxxxx x x xxxxxxx xxxxxxx xxxxxx xxxxxxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxxxxxxxxx xxxxxx x xxxxxx xxxxxxxxx xxxxxxxxxxxx zhodnocení xxxxxx xxxxxx xxx xxxxxx xxxxxxx a xxxxxxx xxxxxxxxx; xx xxxxxx xxxxxxxxxxxx látek v xxxxxxx I xxxxxxxx xxxxxx xxxxx současných xxxxxxxxx x xxxxxxxxxxx xxxxxxxx; že x xxxxxxxx xxxx xx xxxxxxxx změnit xxxx xxxxxxx I xxx, xxx obsahoval poznámky xxxxxxxx xx xxxxxxxxxx xxxxxxxxx x xxxxx xxxxxxx xxxxxxxxxxx xxxxx x xxxxxxx X; xx xxxxxx xxxxxxxxxxxx xxxxx x příloze X xxxxxxxx xxxxx, xxx xxxxx xxxx xxxxxxxxxx Xxxxxxxx x Xxxxxxx x aktu x xxxxxxxxxxx Xxxxxxxx, Xxxxxx x Xxxxxxx xxxxxxxxxx xxxxxxx xxxxxxxx xxxxxxxx xx klasifikace x označování; xx xxx x xxxxxxxxxxx xxxxxxxxxxx xxxxxxxxxxx xxxxxxxxx xx xxxxxxxxxxx x xxxxxxxxxx xxxxxx xxxxx; xx xxxxx byla xxxxxxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxx xxxxx;
xxxxxxxx x xxxx, xx příloha XXX xxxxxxxx 67/548/XXX xxxxxxxx xxxxxx vět xxxxxxxxxxx xxxxxxxx xxxxxx xxxxxxx x nebezpečnými xxxxxxx a přípravky; xx xx xxxxxxx xxxxxx xxxx xxxxxxxxx xxxxxxxxxxxx xxxxxxxx xxxxx x xxxxxxxxx xxx xxxxxx;
xxxxxxxx x xxxx, xx xxxxxxx V xxxxxxxx 67/548/EHS xxxxxxx xxxxxx xxx xxxxxxxxx xxxxxxxxx-xxxxxxxxxx vlastností, xxxxxxxx x xxxxxxxxxxx xxxxx x xxxxxxxxx; xx xx xxxxxxxx přizpůsobení xxxx přílohy xxxxxxxxxxx xxxxxxx;
xxxxxxxx x xxxx, xx příloha XX xxxxxxxx 67/548/EHS xxxxxxxx xxxxxx kritéria xxx xxxxxxxxxxx a xxxxxxxxxx xxxxxxxxxxxx látek x xxxxxxxxx; xx je xxxxx xxxxxx xxxxxxxx xxx látky a xxxxxxxxx xxxxxxxxxx xxx xxxxxx, pokud xxxx xxxxxxxxxx; že xxxxxxxx xxx xxxxxxxxxxxxxxx látky x xxxxxxxxx je xxxxx změnit; že xx xxxxx zavést xxxxxxxx pro xxxxxxxxxx xxxxxxxxx xxxxx xxxxxxxx xxx xxxxxx, xxxxx x zkapalněný xxxxx xxxx (XXX);
xxxxxxxx x xxxx, xx xxxxxxxx xxxx xxxxxxxx xxxx x souladu xx xxxxxxxxxxx Výboru pro xxxxxxxxxxxx xxxxxxxxxxx xxxxxxx xxxxxxx x odstranění xxxxxxxxxxx xxxxxxxx xxxxxxx xx úseku xxxxxxxxxxxx xxxxx x xxxxxxxxx,
XXXXXXX XXXX XXXXXXXX:
Xxxxxx 1
Směrnice 67/548/XXX xx xxxx takto:
1. Xxxxxxx I xx xxxx takto:
a) X xxxxxxxxx xx poznámka 4 xxxxxxxxx xxxxx:
"Xxxxxxxx 4
Xxxxxxxxx xxxxxxxxxx xxxx xxxxx xxxx xxx xxxxxxxxxxxxx xxxx xxxxxx xxxxxxxx x větou X 65, xxxxx xxxxxxx xxxxxxxx v xxxxxxx XX xxxxx 3.2.3.";
x) xxxxxxxx xx xxxxxxxx 5, xxxxx xxx:
"Xxxxxxxx 5
Xxxxxxxxxxxx limity xxx plynné xxxxxxxxx xxxx xxxxxxxxx x xxxxxxxxxx xxxxxxxxxx";
x) x xxxxxxx X v xxxxxxxxx xxxxxxx I xxxxxxxx 67/548/XXX xx xxxxxx tato xxxxxxxxxxx xxx organické látky:

d) xxxxxxxxxxxx xxxxxxx xxxxxxx xxxxxxxx xx xxxxxxxxx xxxxxxxxx přílohy X xxxx xxxxxxxx;
x) xxxxxx xx vkládají xxxxxxx xxxxxxx XX xxxx xxxxxxxx;
x) zrušují se xxxxxxx x těmito xxxxx:
008-002-00-3
612-045-00-9
648-011-00-5
648-025-00-1
648-157-00-X
648-158-00-5
648-159-00-0
649-192-00-3
x) xxxxxxx v xxxxxxx XXX uvedené xxxxxxxx se xxxx xxx, že všechny xxxxxx na "R 22" xx xxxxxxxxx xxxxxx na "R 65".
2. X xxxxxxx XXX xx xxxxxx xxxx xxxx, xxxxx xxx:

3. Xxxxxxx X xxxx X xx xxxx takto:
a) záhlaví x obecný úvod x části B: Xxxxxx xxx stanovení xxxxxxxx xx xxxxxxxxx xxxxxx x xxxxxxx XX X této xxxxxxxx;
x) xx xxxxxxxx X.1 a) se xxxxxx xxxx x xxxxxxx IV X xxxx xxxxxxxx;
x) xxxxxxxx X.6 xx nahrazuje xxxxxx x xxxxxxx XX X xxxx xxxxxxxx;
x) xxxxxxxx X.7 xx xxxxxxxxx textem x xxxxxxx XX X xxxx xxxxxxxx;
x) xxxxxxxx xx xxxx x xxxxxxx XX X xxxx xxxxxxxx.
4. Xxxxxxx VI se xxxx x xxx xxxxxxxx xxxxxxxx v xxxxxxx V xxxx xxxxxxxx.
Článek 2
1. Xxxx xx xxxxxx xxxxxxxx 2, členské státy xxxxxx x účinnost xxxxxx x xxxxxxx xxxxxxxx nezbytné xxx xxxxxxxx souladu x xxxxx směrnicí nejpozději xx 31. xxxxxx 1998. Členské xxxxx x xxxx xxxxxxxxxx xxxxxxx Komisi.
2. Xxxxxxxxxx xx 31. xxxxx 1997 členské xxxxx xxxxxx v účinnost xxxxxx x xxxxxxx xxxxxxxx xxxxxxxx x xxxxxxxx xxxxxxx x xxxxxxxx V xxxx X, X x X xxxx směrnice. Xxxxxxx státy x xxxx neprodleně xxxxxxx Xxxxxx.
3. Xxxxxxxx podle xxxxxxxx 1 x 2 xxxxxxx členskými xxxxx xxxx xxxxxxxxx xxxxx xx tuto xxxxxxxx xxxx musí xxx takový xxxxx xxxxxx xxx xxxxxx xxxxxxx xxxxxxxxx. Xxxxxx xxxxxx si stanoví xxxxxxx státy.
Xxxxxx 3
Xxxx xxxxxxxx xxxxxxxx x platnost xxxxxxxx xxxx xx xxxxxxxxx v Xxxxxxx xxxxxxxx Xxxxxxxxxx xxxxxxxxxxxx.
Článek 4
Xxxx xxxxxxxx xx xxxxxx xxxxxxxx xxxxxx.
V Xxxxxxx xxx 30. xxxxxxxx 1996.
Za Xxxxxx
Xxxx Bjerregaard
členka Komise
[1] Úř. xxxx. X 196, 16. 8. 1967, x. 1.
[2] Úř. xxxx. X 381, 31. 12. 1994, x. 1
ANEXO X — XXXXX X — XXXXXX X — ΠΑΡΑΡΤΗΜΑ X — XXXXX I — XXXXXX X — XXXXXXXX X — XXXXXXX X — XXXXX X — XXXXX I — XXXXXX I — XXXXXXX I
XXXXX II — XXXXX XX — XXXXXX XX — ΠΑΡΑΡΤΗΜΑ XX — XXXXX XX — XXXXXX II — XXXXXXXX XX — XXXXXXX II — XXXXX XX — XXXXX II — XXXXXX XX — XXXXXXX XX
XXXXX XXX — XXXXX XXX — XXXXXX III — ΠΑΡΑΡΤΗΜΑ XXX — XXXXX III — XXXXXX XXX — XXXXXXXX III — XXXXXXX XXX — XXXXX III — XXXXX XXX — XXXXXX III — XXXXXXX III
Indexové číslo

XXXXXXX XX A
" XXXX B: XXXXXX XXXXXXXXX TOXICITY X XXXXXX ÚČINKŮ NA XXXXXX
XXXXXX XXXX: ČÁST X
X. VYSVĚTLIVKY
Pro účely xxxxxxxx xxxxx je xxxxxxx toto xxxxxxxxx:
X.15 Xxxxxxx na genové xxxxxx u Saccharomyces xxxxxxxxxx
X.16 Xxxxxxx na xxxxxxxxxx xxxxxxxxxxx x Xxxxxxxxxxxxx xxxxxxxxxx
X.17 Xxxxxxx xx xxxxxx xxxxxx x xxxxxxx xxxxxxx xx vitro
B.18 Xxxxxxx xx xxxxxxxxx x xxxxxxxx XXX – xxxxxxxxxxxx xxxxxxx XXX – x xxxxxxx xxxxxxx xx xxxxx
X.19 Xxxxxxx xx xxxxxx xxxxxxxxxxx xxxxxxxxx xx xxxxx
X.20 Xxxxxxx na xxxxxxxxx xxxxxxx mutace xxxxxx na pohlaví x Xxxxxxxxxx melanogaster
B.21 Xxxxxxx xx transformace xxxxxxx xxxxx xx xxxxx
X.22 Xxxxxxxxxx letální xxxxxxx xx xxxxxxxxxx
X.23 Xxxxxxxxxxxxx xxxxxxx xxxxxxx xxxxxxxxxxx xxxxx xx xxxx
X.24 Xxxx xxxx xx xxxxxx
X.25 Zkouška xx dědičnou xxxxxxxxxxx x xxxx
X.26 Xxxxxxx xxxxxxxxxxxx xxxxxx xxxxxxxx: 90xxxxx xxxxxxxxx xxxxxx xxxxxxxx xx xxxxxxxxxx
X.27 Xxxxxxx xxxxxxxxxxxx xxxxxx xxxxxxxx: 90xxxxx xxxxxxxxx xxxxxx aplikace na xxxxxxxxxxxx
X.28 Xxxxxx xxxxxxxxxxxx xxxxxxxx toxicity: 90xxxxx xxxxxxxxx xxxxx xxxxxxxx xx xxxxxxxxxx
X.29 Xxxxxx xxxxxxxxxxxx xxxxxxxxx xxxxxxxx: 90xxxxx opakovaná xxxxxxxxx xxxxxxxx xx hlodavcích
B.30 Xxxxxxx chronické xxxxxxxx
X.31 Xxxxxxx xxxxxxxxxxxx xx xxxxxxxxxx a xxxxxxxxxxxx
X.32 Xxxxxxx xxxxxxxxxxxxx
X.33 Kombinovaná xxxxxxx xxxxxxxxx xxxxxxxx x karcinogenity
B.34 Jednogenerační xxxxxxx xxxxxxxx xxx xxxxxxxxxx
X.35 Dvougenerační zkouška xxxxxxxx pro xxxxxxxxxx
X.36 Xxxxxx toxikokinetiky
B. XXXXXX XXXXXXXX XXXXXXX POUŽITÝCH XX XXXXXXXXXX XXXXXXXX XXXXXXXXX V XXXX XXXXXXX
x) Akutní xxxxxxxx xxxxxxxx xxxxxxxxxx xxxxxx, xxxxx se projeví x xxxxx xxxxxxx xxxxxx (obvykle 14 xxx) xx xxxxxx xxxxx xxxxx xxxxx.
xx) Xxxxxx xxxxxxxx je xxxxxx termín xxxxxxxxxx xxxxxxxx xxxxxxxx toxicity xx xxxxxx zkoušené xxxxx. Tyto příznaky xx xxxx být xxxxxxxxxx zřetelné xxx xxxxxxxxx nebezpečnosti x xxxx by být xxx silné, xx xxx xxxxxxx xxxxxx xxxxx xxx xxxxxxxxxxxx xxxxxxxx xxxxxxx příznaků xxxxxxxx a xxxxxxxxxxxxxx xxxxxxxxx.
xxx) Xxxxx je xxxxxxxx xxxxxx zkoušené xxxxx. Xxxxx se xxxxxxxxx xxxx hmotnost xxxxxxxx látky (v xxxxxxx xxxx xxxxxxxxxxx) xxxx xxxx hmotnost xxxxxxxx xxxxx xx xxxxxxxx hmotnosti xxxxxxxxx xxxxxxx (xxxx. x xxxxxxxxxxx xx kilogram xxxxxxx xxxxxxxxx) xxxx xxxx xxxxxxxxxx koncentrace x xxxxxxx (x xxx nebo x xxxxxxxxxxx na xxxxxxxx xxxxxxx).
xx) Xxxxxxxxxxxxxx xxxxx xx nejvyšší ze xxxx fixních úrovní xxxxx, které xxx xxxxx, aniž xx xxxxxxxx mortalitu xxxxxxxxx xxxxxx (včetně xxxxxxxxx xxxxxxxx).
x) Dávkování je xxxxxx termín xxxxxxxxxx xxxxx, xxxxxxx x xxxxxx xxxxxxxx xxxxx.
xx) XX50 (xxxxxxx xxxxxxx xxxxx) je statisticky xxxxxxxxx jednotlivá dávka xxxxx, u xxx xxx očekávat, xx xxxxxxx xxxxxxx 50 % zvířat, kterým xxxx xxxxxx. Xxxxxxx XX50 se vyjadřuje x hmotnosti xxxxxxxx xxxxx xx jednotku xxxxxxxxx xxxxxxxxx zvířete (x xxxxxxxxxxx xx xxxxxxxx).
xxx) XX50 (xxxxxxx xxxxxxx koncentrace) xx xxxxxxxxxxx vypočtená koncentrace xxxxx, x xxx xxx xxxxxxxx, že xxxxxxx během expozice xxxx do xxxxxx xxxx xx xxxxxxxx xxxxxxx 50 % xxxxxx xxxxxxxxxxxx xxxxxxx xxxx.
Xxxxxxx XX50 xx xxxxxxxxx xxxx xxxxxxxx xxxxxxxx látky xx xxxxxxxxxxx objemu xxxxxxx (x miligramech xx xxxx).
xxxx) XXXXX xx xxxxxxxx xxxxxxx xxx "xx xxxxxxxx xxxxxxx xxxxxx xxxxx" (hladina xxx xxxxxxxxxxxx xxxxxxxxxxxx xxxxxx) x xxxxxxxx xxxxxxxx úrovni xxxxx xxxx xxxxxxxx, při xxxxx xxxxxx pozorovány xxxxx xxxxxxxxxx nálezy xxxxxxxxxxx x xxxxxxx xxxxx.
xx) Xxxxxxxxxxxx toxicita xxxx toxicita xxx xxxxxxxxx dávce xxxxxxxx xxxxxxxxxx xxxxxx, které xx xxxxxxx x xxxxxxxxx zvířat xxxx xxxxxxxx opakovaného xxxxxxx xxxxxxxx chemické xxxxx xxxx opakované expozice xxxxxxxx látce xx xxxx xxxxxxxxxxxxx krátký xxxx očekávané délky xxxxxx xxxxxxxxx xxxxxx.
x) Xxxxxxxxx xxxxxxxxxx xxxxx (XXX) je nejvyšší xxxxxx xxxxx, která x xxxxxx xxxxxx xxxxxx xxxxxxxx, xxxx xx měla xxxxx xxxxxxx, xx které xx použita, větší xxxx xx přežití xxxxxx.
xx) Xxxxx dráždivostí xx xxxxxx vyvolání xxxxxxxxxxx xxxx na xxxx po xxxxxxxx xxxxxxxx xxxxx.
xxx) Oční xxxxxxxxxxx se rozumí xxxxxxxx xxxx v xxx xx xxxxxxxx xxxxxxxx xxxxx na xxxxxx oka.
xiii) Xxxxxxxxxxxxx xxxx (xxxxxxxxx xxxxxxxxx xxxxxxxxxxx) xx xxxxxxxxxxxx xxxxxxxx xxxxxx xxxx xx xxxxx.
xxx) Poleptání xxxx xx xxxxxxxx xxxxxxxxxx xxxxxxxxx kožní xxxxx po xxxxxxxx xxxxxxxx xxxxx po xxxx xx 3 xxx xx 4 x.
xx) Xxxxxxxxxxxxxx xx xxxxxx xxxxxxxx, xxxxxxxxxx, xxxxxxxxxxx a xxxxxxxxxx xxxxxxxxxx xxxxx.
xxx) Xxxxxxxx xx xxxxxx, kterým xxxxxx xxxxx xxxxxxxx xx xxxx.
xxxx) Xxxxxxxxxx xx xxxxxx, xxxxxx xxxx podaná xxxxx x/xxxx její metabolity xxxxxxxxx x xxxx.
xxxxx) Xxxxxxxxxx je xxxxxx, xxxxxx xx xxxxxxxxxxx xxxxx x/xxxx její xxxxxxxxxx xxxxxxxxx x xxxx.
xxx) Xxxxxxxxxxxx xx xxxxxx, xxxxxx xx xxxxxx látka x xxxx strukturně xxxxxx xxxxxxxxxxxxx xxxx xxxxxxxxxxxxxxx xxxxxxxx.
X.1 Xxxxxx xxxxxxxx xxx xxxxxxxxx xxxxx/xxxxxxxxxxxx x xxxxxxxxx toxicita
Akutní xxxxxxx účinky xxxxx x její xxxxxxxxx xxxx systémovou toxicitu xxx xxxxxxxxx xx xxxxxxx různých zkoušek (xxxxxx X.1 – X.5), které xx xxxxxx xxxxxx xxxxx xxxxxxxxx xxxxxxxxx xxxxx x xxxxxxxx.
X závislosti xx xxxxxxxx xxxxx xxx zvážit xxxxxxx xxxxxxx xxxxxxx xxx xxxxxxxxx XX50, třebaže x xxxxxxxxxxx studiích xxxx xxxxxxx žádná xxxxxxx xxxxxxx, xxxxxxx xxxxxx xxxxx definovat xxxxxxx limitní xxxxxxx xxx jednorázovou xxxxxxxxx xxxxxxxx.
Xxxx by xxx xxxxxxxxxxxxx xxxxxx, xxx xxxxx se xxxxxxx xx xxxxxxx zvířat x xxxxx xxxxxxxxxxxx xxxxxx utrpení, xxxxxxxxx xxxxxx xxxxx dávky (xxxxxx B.1 x)) x metoda stanovení xxxx xxxxxx toxicity (xxxxxx X.1 x)). X zkoušek na xxxxxx 1 xxxx xxxxxx xxxxxxx z xxxxx xxxxxx xxxxxxx xxxxxx na xxxxx xxxxx. X xxxxxxx xxxxxxx xxxx xxx xxxxxxx xxxxxxxxxx xxxxxxxx xxxxxx xxxx xxxx xxx xxxxxx xxxxxxxx xxx xxxxx xxxxx xxxxxx.
Xxxxxxx xxxxxxxx xxx xxxxxxxxx aplikaci (metody X.7, B.8 a X.9) xxxxxxxx xxxxxxxxx xxxxxxxxx účinků x xxxxxxxx xxxxxxxxx expozice. Xxxxx xx klade xx xxxxxxx klinické xxxxxxxxxx xxxxxx x xxxxx xxxxxx xx xxxxxxx xxxxxxxxx. Xxxx xxxxxxx by xxxx xxxxxx zjistit xxxxxx xxxxxx xxxxxxxx x xxxxxxx x netoxické xxxxx. Xx xxxxxxxxxxxx xxxxxx xx xxxxxxxx xxxxx hlubší xxxxxxx xxxxxx aspektů (xxxxxx X.26 – B.30 x B.33).
B.II Xxxxxxxxxx – Genotoxicita
Mutagenitou xx xxxxxx vyvolání trvalých, xxxxxxxxxx xxxx xxxxxxxx xxxx xxxxxxxxx xxxxxxxxxxx xxxxxxxxx buněk xxxx xxxxxxxxx. Xxxx xxxxx, "xxxxxx", xx xxxxx xxxxx jediného genu xxxx xxxxxxxx genů, xxxxxx xxxx nebo xxxxxx chromosomů. Účinky xx xxxx xxxxxxxxxx xxxxx xxxxxxx strukturní x/xxxx numerické xxxxx.
Xxxxxxxxx xxxxxxxx látky xx xxxxxxxx xxxxxxxxx xx xxxxx xx xxxxxx (xxxxxx) xxxxxx x xxxxxxxxxx (xxxxxx X.13/14) x/xxxx na xxxxxxxxxx xxxxxxxxxxxx aberace x xxxxxxx buňkách (xxxxxx X.10).
Xxxxxxxxxx jsou xxxx xxxxxxx xx xxxx, xxxx. xxxx xxxxxxxxxx (xxxxxx B.12) xxxx xxxxxxx xxxxxxxx xxxxx xxxxxx xxxxx (xxxxxx X.11). Neexistují-li xxxx xxxxx xxxxxxxxxxxxxx, důrazně xx doporučují metody xx vitro.
Dodatečné studie xxxxxxxxxxx xxxxxxxxxx látky xxxx provedení xxxxxxxxxxx xxxxxxx xxxxxxxxxxxxx xxxxx xxx xxxxxxxx xxx xxxxx vyráběné ve xxxxxxx xxxxxxxxxx nebo xxx xxxxxxxxx následného xxxxxxxxx rizika x xxxxx xxx použity x xxxxxxxx účelům: xxx potvrzení xxxxxxxx xxxxxxxxx x základní xxxx zkoušek, xxx xxxxxxxx xxxxxxxxx, které xxxxxx studovány v xxxxxxxx xxxx xxxxxxx, xxx xxxxxxxx nebo xxxxxxxxx xxxxxx xx xxxx.
Xxx tyto xxxxx xxxxxxxx xxxxxx X.15 xx X.25 xxxxxxxxxxxx xxxxxxx xx xxxx x in xxxxx x xxxxxxxxxx řadu xxxxxxxxxxxx xxxxxxxxx. Tyto xxxxxxx poskytují informace x xxxxxxxx xxxxxxxx x x jiných xxxxxxxxxxx x xxxxxxxxx xxxxxxxxxxxx xxx bakterie xxxxxxxxx xxx xxxxxxxx xxxx xxxxxxx.
Xxxxxx xxxxx, xx xx-xx zvažován xxxxxxx xxxxxxx xxxxxx xxxxxxxxxx, měl xx xxx xxxxxxx xxx, xxx poskytl xxxxxxxxx xxxxxxxxxx xxxxxxxxx x xxxxxxxxxx a/nebo karcinogenním xxxxxxxxxx látky.
Výběr xxxxxx, xxxxx mohou být xxxxxx xxx xxxx xxxxxx, xxxxxx xx xxxxx faktorech, včetně xxxxxxxxxx x fyzikálních xxxxxxxxxx xxxxx, xxxxxxxx xxxxxxxxxx xxxxxxxxxxxxx x xxxxxxxxxxxxxxx xxxxxxx, xxxxxxxxxxxxx xxxxxxx xxxxx, xxxxxxxx xxxxxxx xxxxxx toxicity x xxxxxxx způsobů xxxxxxx xxxxx. Xxxxx xxxxxx xxxxxx zkoušek xx xxxx xxxxxxxx, x xxxxxxx na xxxxx xxxxx xxxxxxx, xxxxx xxxxx xxxxxxxxx xxxxxxx.
Xxxxxxx xxxxxx principy xxxxxxxxx zkoušení xxxx xxxxxxxxx xx xxxxxxxx 93/67/XXX, xxx xxxxxx xxxxxxxxx xxxxxxxx se xxxxxxxxx v xxxxxxxxxxx xxxxxxxx pro hodnocení xxxxxx, jsou xxxx xxxxxx x xxx xx xxxxxxx xxx, xxx vyhovovaly specifickým xxxxxxxxxx.
Xxxxxx xxx xxxxx xxxxxxxxxxx xxxx xxxxxxx xxxx xxxxxxxxx xx xxxxxxx xxxxxx xxxxxxxx xxxxxxxxxxxxx genetického xxxxxx:
Xxxxxx xxxxxxxxxx xxxxxx (xxxxxx) xxxxxx
x) Studie přímé xxxx xxxxxx xxxxxx x xxxxxxxxxxxxxx mikroorganismů (Xxxxxxxxxxxxx xxxxxxxxxx) (xxxxxx X.15).
x) Studie xxxxxxx xxxxxx v savčích xxxxxxx xx xxxxx (xxxxxx X.17).
x) Zkouška xx recesivní xxxxxxx xxxxxx xxxxxx xx xxxxxxx x Xxxxxxxxxx xxxxxxxxxxxx (xxxxxx X.20).
x) Xxxxxxx xx somatické xxxxxx xxxxx xx xxxx, spot xxxx xx myších (metoda X.24).
Xxxxxx zkoumající chromosomové xxxxxxx
x) Xxxxxxxxxxxxx xxxxxx xx xxxxxxx xx xxxx; měla xx xxx xxxxx x xxxxx xxxxxxx xxxxxxxx xxxxx xxxxxx xxxxx, xxxxx xxxxxx zařazena xx základního vyšetření (xxxxxx X.11). Xxxxx xxxx může xxx xxxxxxxxx xxxx cytogenetická xxxxxxx xxxxxxxxxxx xxxxx xx xxxx (metoda X.23).
x) Cytogenetická studie xx xxxxxxx xxxxxxx xx xxxxx, xxxxx xxxxxx zařazena do xxxxxxxxxx vyšetření (B.10).
c) Xxxxxxxxxx xxxxxxx xxxxxxx xx xxxxxxxxxx (xxxxxx X.22).
x) Zkouška na xxxxxxxx xxxxxxxxxxx x xxxx (xxxxxx B.25).
Genotoxické xxxxxx – xxxxxx xx XXX
Xxxxxxxxxxxx, která xx xxxx xxxxxxxxxxx xxxxxxxxxx xxxxxx na xxxxxxxxx xxxxxxxx, xxxx xxxx xxxxxxxx xxxxxx x xxxxxxxxxxx, xx xxxx projevit xxxx xxxxxxxxxx xxxxxxxxx DNA xxx xxxxxxx xxxxxx xxxxxx. Pro xxxxxxxx xxxxxx xxxx xxxxx xxx vhodné xxxxxxxxxxx xxxxxx používající eukaryotické xxxxxxxxxxxxxx nebo buňky xxxxx:
x) Xxxxxxxxx rekombinace x Saccharomyces xxxxxxxxxx (xxxxxx X.16).
x) Xxxxxxxxx x reparace DNA – xxxxxxxxxxx syntéza XXX v xxxxxxx xxxxxxx – in xxxxx (xxxxxx X.18).
x) Xxxxxx xxxxxxxxxxx xxxxxxxxx x xxxxxxx xxxxxxx – in vitro (xxxxxx X.19).
Xxxxxxxxxxxx xxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxxx
Xxxxxxx xx transformaci xxxxxxx xxxxx umožňují měřit xxxxxxxxx xxxxx xxxxxxx xxxxx morfologie x xxxxxxx v buněčných xxxxxxxxx, x xxxxx xx předpokládá, xx xxxxxxxxx x xxxxxxx xxxxxxxxxxxx – in xxxx (xxxxxx X.21). Xxxxxxx xxxxx xxx xxxxx typy xxxxx x xxxxx xxxxxxxx xxxxxxxxxxxx.
Xxxxxxxxx rizika xxxxxxxxx xxxxxx u xxxxx
Xxxxxxxx xxxxxxx metod umožňujících xxxxx x xxxxx xxxxxxx xxxxxx vyvolané xxxxxxxxxxx (xxxxxxxx) mutacemi, xxxx. xxxxxxx na xxxxxxxxxx xxxxxxxx xxxx x chromosomu x xxxx pro měření xxxxxx xxxxxxxxxxx xxxxx x první xxxxxxxx (xxxxxxxxxx xx xxxx xxxxxxx), xxxx xxx xxxxxxxxxxxx xxxxxxx, xxxx. xxxxxxx xx xxxxxxxx xxxxxxxxxxx x xxxx (xxxxxx X.25). Tyto xxxxxx xxx xxxxxx xxx xxxxx xxxxxxx xxxxxxxxxxx xxxxxx, xxxxx xxxxx xxxxxxxxxxx pro xxxxxxx. Vzhledem ke xxxxxxxxxx těchto xxxxxxx x x xxxxxxxx xxxxxxxxxx počtu xxxxxx, xxxxxxx pro xxxxxxx xx xxxxxxxxxx xxxxxxxx xxxx x xxxxxxxxxx, xx xxxx nezbytné xxxxx xxxxxxxxxx xxxx xxxxxxxxxx xxxxxx xxxxxx.
X.XXX Xxxxxxxxxxxxx
Xxxxxxxx xxxxx mohou xxx považovány xx xxxxxxxxxxx xxxx negenotoxické xxxxxxxxxxx x xxxxxxxxxx xx xxxxxxxxxxxxxx xxxxxxxxxx xxxxxxxx.
Xxxxxxxxx informace x xxxxxxxxxxxx xxxxxxxxxxxxx xxxxxxxxxx xxxxx lze xxxxxx xx xxxxxx xxxxxxxxxx/xxxxxxxxxxxx. Xxxxxxxxx informace xxx xxxxxx xx zkoušek xxxxxxxx při opakované xxxxxxxx a xx xxxxxxx subchronické a xxxxxxxxx xxxxxxxx. Zkouška xxxxxxxx xxx opakované xxxxxxxx, metoda X.7, x dlouhodobější xxxxxx xxxxxxxx při xxxxxxxxx xxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxxxxxxxxxx xxxx xxxxxxxxxxxx xxx xxxxxxxxx toxicity xxx xxxxxxxxx xxxxx, xxxx. hyperplasie xxxxxxxx xxxxx, xxxxx mohou xxx předmětem zájmu. Xxxx xxxxxx a xxxxxxxxxxxxxxx xxxxxxxxx mohou xxxxxx xxxxx xxxxxxxx xxxxx x xxxxxxxxxxxxx xxxxxxxxxxx, x nichž xxxx být xxxxxxxx xxxxx hlubší xxxxxxxx xxxxxx aspektu xxxxxx xxxxxxx xxxxxxxxxxxxx (xxxxxx X.32) nebo xxxxx x xxxxxxxxxxx xxxxxx xxxxxxxxx xxxxxxxx/xxxxxxxxxxxxx (xxxxxx X.33).
X.XX Xxxxxxxx xxx xxxxxxxxxx
Xxxxxxxx xxx xxxxxxxxxx xxx xxxxxxxxx různými xxxxxxx, např. xxxxxxxxxx xxxxxxxxxxxxx xxxxxx xxxx xxxxxxxxxx xxxxx a xxxxx, xx. "xxxxx xx xxxxxxxx", xxxx xxxxxxxxx nedědičných xxxxxxxxxx xxxxxx xx xxxxxxxxx, xx. "xxxxxxxxx xxxxxxxxx", xxxxx zahrnují xxxx xxxxxxxxxxxx x účinky x xxxxxxx xxxxxxx.
Xxx xxxxxx xxxxxxxxxxxx xxxx xxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxx je xxxxxxxx xxxxxx (metoda B.31) xxxxxxxx xxxxxxxx na xxxxxx xxxxxxxx. X xxxxxxxxxx na xxxxxxxxxxx xxxxxxxxxxxx xxxxxxxx xxxxx xxxx xx xxxxxxxxxxxxxx xxxxxxx xxxxxxxx xxxxxxx xxxxx xxx použity xxxx jiné xxxxxxx xxxxxxxx. X takových xxxxxxxxx xx měla xxx xxxxxxxx xxxxxx xxxxxx upravena x xxxxxxx xx xxxxxxxxx xxxxx 28xxxxxxx zkušebních xxxxx.
Xx-xx xxxxxxxx xxxxxxxxxxxx xxxxxxx xxxxxxxxxx (xxxxxxxxx), xxxx xxx popsaná xxxxxx xxxxxxxxxxxxx zkoušky xxxxxxxxxx (xxxxxx X.35) xxxxxxxxx xxx, xxx xxxxxxxxx třetí xxxxxxxx.
X.X Xxxxxxxxxxxxx
Xxxxxxxxxxxxx xxx xxxxxxxxx xxxxxxx xxxxxxx, xxxx. xxxxxxxxx xxxxxxx x/xxxx xxxxxxxxxxxx x biochemickými xxxxxxx xxxxxxxxxxx x xxxxxxxxxxx xxxxxxxxx systému. Xxxxxxxxx xxxxxxxx neurotoxicity xxx xxxxxxx xxxxxxxxx xxxxxx toxicity. Zkouška xxxxxxxx xxx opakované xxxxx, metoda X.7, xxxxxxxx xxxxxxxxx neurotoxických xxxxxx x xxxxx xx klade xx xxxxxxx pečlivého xxxxxxxxxx xxxxxxxxxx zvířat s xxxxx získat xx xxxxxxx xxxxxxxxx. Metoda xx xxxx xxxxxx xxxxxxx xxxxxxxx xxxxx x xxxxxxxxxxxxx potenciálem, x xxxxx xxxx xxx xxxxxxxx xxxxx xxxxxx xxxxxxxxxxx xxxxxx xxxxxxx. Xxxxx xxxx xx důležité xxxxxx xxxxxxxxx látek vyvolat xxxxxxxxxx xxxxxxxxxxxx xxxxxx, xxxxx nemusí být xxxxxxxx xxxxxx xxxxxxxx xxxxxxxx. Xxxxxxxxx u xxxxxxxx xxxxxxxxxxx sloučenin xxxxxxx xxxx xxxxxxxxxx, xx xxxxxxxxxx pozdní xxxxxxxxxxxxx, x xxxxxxxx xx metodami B.37 x X.38 po xxxxxxxxxxxx xxxx opakovaném xxxxxx.
X.XX Imunotoxicita
Imunotoxicitu xxx xxxxxxx xxxxxxx způsoby, xxxxxxxxx xxxxxxxxxxxx x/xxxx xxxxxxxx xxxxxxxx xxxxxxxxxx xxxxxxx vedoucím x xxxxxxxxxxxxxxxx xxxx xxxxxxxx xxxxxxxxxxx. Xxxxxxx xxxxxxxx xxx xxxxxxxxx xxxxx, xxxxxx X.7, zahrnuje xxxxxxxxx xxxxxxxxxxxxxx účinků. Xxxxxx xx měla xxxxxx odhalit chemické xxxxx x xxxxxxxxxxxxx xxxxxxxxxxx, u xxxxx xxxx xxx xxxxxxxx xxxxx xxxxxx xxxxxxxx xxxxxx aspektu.
B.VII Xxxxxxxxxxxxxx
Xxxxxxxxxxxxxxx xxxxxx xxxxxxxx při xxxxxxxxxxxx x vyhodnocení xxxxx o toxicitě. Xxxx studie xxxx xxxxxx x xxxxxxxxx xxxxxxxx xxxxxxx xxxxxxxx xxxxxxxx xxxxxxxx xxxxx x xxxxxxxx mohou xxxxxx xxx plánování xxxxxxx xxxxxx toxicity. Xxxxxxxxxxxxx xx, že xx xxxx xx xxxxx xxxxxxxxx xxxxxxxx xxxxxxxx xxxxxxx parametry. Xxxxx xx vzácných xxxxxxxxx xxxx nezbytné xxxxxxx xxxxxx xxxx xxxxxxxxxxxxxxxxx studií (xxxxxx xxxxxxxx, vylučování, xxxxxxxxxx x xxxxxxxxxxx). Xxx xxxxxx sloučeniny xxxxx xxx vhodné změny xxxx xxxx xxxx xxxx xxxxxx xxxxxx x xxxxxxx dávkou (xxxxxx B.36).
Údaje o xxxxxxxx struktuře (XXX) x xxxxxxxxxxxxxxxxxxx vlastnostech xxxxx též poskytnout xxxxxxxxx x xxxxxxxxxxx xxxxxxxxxxxxxxxxx x xxxxxxxxxxx xxxxxxx xxxxxx a x možnostech xxxxxxxxxxxxx xxxxxxxxxx x distribuce xxxxx x xxxxxxx. Xxxxx též xxxxxxxxx xxxxx o xxxxxxxxxxxxxxxxx xxxxxxxxxxx z předešlých xxxxxx xxxxxxxx x x toxikokinetických xxxxxx.
X. XXXXXXXXXXXXXX ZKOUŠENÉ LÁTKY
Složení xxxxxxxx látky, xxxxxx xxxxxxxx nečistot, x xxxx relevantní xxxxxxxxx-xxxxxxxx xxxxxxxxxx, xxxxxx xxxxxxxx, xx xxxx xxx xxxxx xxxx xxxxxxxxx xxxxxxxx xxxxxx xxxxxxxx.
Xxxxxxxxx-xxxxxxxx xxxxxxxxxx zkoušené xxxxx xxxxxxxxx důležité xxxxxxxxx xxx výběr xxxxxxx xxxxxxxx, xxx xxxxx xxxxx xxxxxxxxxx studie x xxx manipulaci xx zkoušenou xxxxxx x její xxxxxxxxxx.
Xxxxxxxx xxxxxx xx xxx xxxxxxxxxx vývoj xxxxxxxxxx xxxxxx xxx kvalitativní x kvantitativní xxxxxxxxx xxxxxxxx xxxxx (xxxxx xxxxx xxxxxx hlavních xxxxxxxx) x xxxxxxxxxx xxxxx x v xxxxxxxxxxx xxxxxxxxx.
Xxxxxxx informace xxxxxxxx xx xxxxxxxxxxxx, xxxxxxxxx-xxxxxxxxxx vlastností, čistoty x xxxxxxx zkoušené xxxxx xx měly xxx xxxxxxxx v xxxxxxxxx o zkoušce.
D. XXXX X XXXXXXX
Xxx xxxxxxxx xxxxxxxx xxxx xxxxxxxx xxxxxx kontrola xxxxxxxx xxxxxxxxx x xxxxxxx xxxx x xxxxxxx.
x) Xxxxxxxx chovu
Podmínky xxxxx v xxxxxxxxxx xxxx xxxxxxx xxx xxxxxxx zvířata by xxxx xxxxxxxxx testovacím xxxxxx. Pro xxxxxxx, xxxx x xxxxxxx xxxx xxxxxxxx xxxxxxxxxx xxxxxxx xxxxxxxxx 22 ±3 °X x xxxxxxxxx vlhkost 30 xx 70 %; xxx králíky se xxxxxxxxxx teplota 20 ±3 °X x xxxxxxxxx xxxxxxx 30 xx 70 %.
Některé xxxxxxxxxxxxxx techniky xxxx xxxxxxx citlivé xx xxxx xxxxxxx x x xxxxxxxx xxxxxxxxx xxxx v xxxxxx xxxxxxxx xxxxxx xxxxxxx xxxxxxxxxxx o vhodných xxxxxxxxxx. Xxx všech xxxxxxxxxxx xxxxxxxxx xxxxxx xx xxxx být xxxxxxxxxxxxx údaje x xxxxxxx x xxxxxxxx x xxxx by xxx xxxxxxxx xx xxxxxxxxx xxxxxx x xxxxxx.
Xxxxxxxxx xx xxxx xxx xxxxx a xxxx xx xx xxxxxxx 12 x xxxxxx a 12 x xxx. Podrobnosti x xxxxxxxxx xxxxxx xx měly xxxxxxxxxxx x xxxxxxx x xxxxxxx zprávě xxxxxx.
Xxxx-xx x metodě xxxxxxx xxxxx, xxxx xx xxx xxxxxxx xxxxxxx xxxxxxxxxx xxxx umístěna x xxxxxxx po xxxxxx skupinách xxxxxxxx xxxxxxx; jsou-li zvířata x xxxxxxx xx xxxxxxxxx, nemělo by xxx xxxxxxx v xxxxx kleci xxxx xxx xxx xxxxxx.
Xx xxxxxxxx x xxxxxxxxxxxxx xx xxxxxxxxx xx xxxxxxxx uvést typ xxxxxxx klece x xxxxx xxxxxx xxxxxxxxx x xxxxx kleci xxx xxxxx xxxxxxxx xxxxxxxx látce, tak xxxxx kterékoli další xxxx pozorování.
ii) Xxxxxxxx xxxxxx
Xxxxxx xx xxxx xxxxxxxx xxxxxxx xxxxxxxxx xxxxxx xxx xxxxxxxxx xxxxxxxxx druh. Xxxxx xxxx zkoušené xxxxx xxxxxxxx x xxxxxxx, xxxx být nutriční xxxxxxx xxxxxxx interakcí xxxxx x xxxxxxxx xxxxxxx xxxxxxx. Xxxxxxx xxxxxx xxxxxx xx xxxx xxx xxxxxxxxxx xxx xxxxxxxxxxxx výsledků xxxxxxx. Xxxx xxx xxxxxxx konvenční xxxxxxxxxxx xxxxxx x xxxxxxxxxx xxxxxxxxx x xxxxx xxxx. Xxxxx potravy xx xxxx xxxxx xxxxxxxx zajistit xxxxxx xxxxxxxxxx xxxxxxxx látky, xxxxx je xxxxxxxx xxxxx xxxxxxx.
Xxxxxxx v xxxxxxx, jejichž xxxx xx xxxxxxxx je xxxx, xxxxx xxx xxxxxxxx x koncentracích, xx xxxxxxx by xx vliv xxxxxxxx.
X. XXXXXXX ZVÍŘAT
Při xxxxxxxxxxxxx xxxxxxxxxx xxxxx xxxx xxxxxxxx pozornost xxxxxxxx xxxxxxx zvířat. Xxxxxxx xxxxxxxx xxxx xx xxxxxxxxxx xxxxxxx níže, xxxxx seznam xxxx xxxx vyčerpávající. Xxxxxx xxxxx x/xxxx podmínky xx xxxxx vyhledat x textu xxxxx:
- Xxx xxxxxxxxx akutní xxxxxx toxicity xx xxxx xxx xxxxxxx xxx xxxxxx, "xxxxxx xxxxx xxxxx" x "xxxxxx stanovení tříd xxxxxx xxxxxxxx". X "xxxxxx fixní xxxxx" xx xxxxxxxxx xxxxxxx xxxx specifický ukazatel x používá xx x ní xxxx xxxxxx. X "metodě xxxxxxxxx xxxx xxxxxx xxxxxxxx" se xxxxxxx x xxxxxxx x 70 % xxxxxx xxxx xxx x xxxxxx X.1 xxxxxxxxx xxxxxx xxxxxx xxxxxxxx. Xxx xxxx alternativní xxxxxx xxxx za xxxxxxxx xxxxx xxxxxxx x xxxxxx než xxxxxxxx metoda.
- Počet xxxxxxxxx xxxxxx xx xxxxxx xx vědecky xxxxxxxxxx minimum: v xxxxxxxx X.1 x X.3 xx xx xxxxxxxx xxxxxxx xxxxx 5 xxxxxx stejného xxxxxxx pro xxxxx xxxxxx dávky; xxx xxxxxxxxx xxxxxxxxxxxxx xxxx xxxxxxxxxxxxx xxxxxxxx na xxxxxxxxx (xxxxxx B.6) xx xxxxxxx pouze 10 zvířat (x xxxxx 5 xxx xxxxxxxxx xxxxxxxxx xxxxxxx); xxxxx xxxxxx potřebných xxx pozitivní xxxxxxxx xxx zkoušení xxxxxxxxxx xx xxxx xx xxxxxx xxxxxxx (metody X.11 a X.12).
- Xxxxxx x xxxxxxx xxxxxx během xxxxxxx xxxx minimalizovány. Je xxxxx xxxxxxx utratit xxxxxxx vykazující xxxxxxx x xxxxxxxxxxxxx známky xxxxxxx; xxxxxxx xx xxxxxxx xxxxxxxx xxxxx, x xxxxx xx xxxxx, xx xxxxxxxxx xxxxxxxxx xxxxxx a xxxxxxx v důsledku xxxxxxxx a xxxxxxxxxx xxxxxxxxxx xxxxx (metody X.1, B.2 x X.3).
- Xxxxxxxx x xxxxxxxxxxx vysokými xxxxxxx xx xxxxxxx xxxxxxxxx xxxxxxxxx zkoušek, a xx xxxxxx xxxxx xxx xxxxxxxxx xxxxxx xxxxxxxx (metody X.1, X.2 x X.3), xxx xxxxxx při xxxxxxxxx xxxxxxxxxx in xxxx (xxxxxx B.11 x B.12).
- Strategie xxxxxxxx xxxxxxxxxxx nyní xxxxxxxx xxxxxxxxxx zkoušku, xxxx ji xxxxxx xx xxxxxx x xxxxxx xxxxxxxx, xxxxx xx xxxxxxxxxx vědecky xxxxxxxxx.
Xxxx vědecké xxxxxxxxxx xxxx být založeno xx fyzikálněchemických vlastnostech xxxxx, xx výsledcích xxxxxxxxxx na xxxxxx xxx xxxxxxxxxxx zkouškách xxxx xx výsledcích xxxxxxxxxx validovaných xxxxxxx xx vitro. Xxxxxx xxxxxxxxx xxxxxx akutní xxxxxxxx nanesením xx xxxx xxxxxxxxx x xxxxxx xxxxx xxxxxxxxxxxx x limitní xxxxxxx (xxxxxx X.3) x xxxxxx pozorována xxxxx xxxxx xxxxxxxxxx, xxxx xxx další xxxxxxxx xxxxx dráždivosti (metoda X.4) xxxxxxxx; xxxxxxxxx, xxxxx xx xxxxxx xxxxx xxxxxxxxxxx (metoda X.4) xxxxxxxx xxxxxxxxxx xxxxxx xxxxxx xxxx xxxxx podráždění xxxx, xxxxxxx xxx xxxx xxxxxxxx xx xxxx xxxxxxxxxx (metoda X.5).
X. XXXXXXXXXXXX ZKOUŠKY
Vědeckým xxxxx Xxxxxxxx xxxx xx xxxxx x xxxxxxxx xxxxxxxxxxxxxx xxxxx, xxxxx xxxxx xxxxxxxxxx xxxxxxx xxxxxx informací xxxx xxxxxxxx zkoušky xx xxxxxxxxx, při xxxxx xx xxxx použije xxxx xxxxxx, xxxxxxx xxxx utrpení xxxx xx x xxxx xxxxxxx xxxxxx xxxxx xxxxxxxx.
Xxxx xx xxxx xxxxxxx xx xxxxx xxxx xxx tyto xxxxxx xxxxxxx, kdykoli xx to xxxxx, xxx charakterizaci nebezpečnosti x následnou xxxxxxxxxxx x xxxxxxxxxx xxxxx x xxxxxxxx xxxxxx xxxxxxxxxxxxx.
X. XXXXXXXXX A XXXXXXXXXXXX
Xxx xxxxxxxxx a xxxxxxxxxxxx zkoušek musí xxx vzaty v xxxxx určité xxxx, xxxxxxx lze výsledky xxxxxx xx zvířatech x xx vitro xxxxxxxxxxxx na člověka, x proto xxx xxx xxxxxxxxx xxxxxxxx xxxxxxxx xxxxxx xxxxxxxx x xxxxxxxxxxxx xxxxxxxx xx xxxxxxx, pokud xxxx x dispozici.
Tyto xxxxxxxx xxx xxxxxx xxx klasifikaci a xxxxxxxxxx xxxxxx a xxxxxxxxxxxx xxxxxxxxxx xxxxx x xxxxxxxx xxxxxx xx xxxxxx xxxxxx, xx xxxxxxx xxxxxx xxxxxxxxxx vlastností zjištěných x xxxxxxxxxxxxxxxx xxxxxx xxxxxxxx. Odpovídající kritéria xxx xxxxxxxxxxx x xxxxxxxxxx uvedená x xxxxxxx XX xx xxxxxxxx xxxx na xxxxxxxxx zahrnuté v xxxxxx xxxxxxxxxx xxxxxxxx, xxxxx jsou xxxxxxx x protokolech o xxxxxxx.
Xxxx xxxxxxxx xxx xxxx xxxxxx xxx xxxxxx xxxxxxxxx xxxxxx xxxxxx x xxxxxxxxxxxx xxxxxxxxxx xxxxx; xxxxxx xxxxxxxx xxxxxxxxx xxx xxxx xxxxx jsou xxxxxxx x xxxxxxxxxxx xxxxxxxx.
X. XXXXXX XX XXXXXXXXXX
Xxxx xxxxxx jsou xxxxxxxx vyvinuty x xxxxx xxxxxxxx XXXX xxx xxxxxxxx xxxxxx x xxxx by xxx xxxxxxxxx x xxxxxxx s xxxxxxxx xxxxxxx xxxxxxxxxxx xxxxx, xxx xxxx xxxxxxxxx xx xxxxxxxx "xxxxxxxx xxxxxxxx xxxxx".
Xxxxx podobnější xxxxxxxxx xxx získat x pokynech XXXX x x xxxxxxxxx xxxxxxxxxx xxxxxxxxxxx jinde."
XXXXXXX IV X
" X.1 x) AKUTNÍ XXXXXXXX (XXXXXX) – XXXXXX STANOVENÍ TŘÍD XXXXXX XXXXXXXX
1. METODA
1.1 Xxxx
Xxxxxx xxxxxxxxx xxxx xxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxx xxx xxx xxxxx hodnocení nebezpečnosti, xxx xxx xxxxx x klasifikace xxxxx x xxxxxxxx xxxxxxxxxxxxx.
X xxxxxx xx používají xxx fixní xxxxx xxxxxxxx v přiměřených xxxxxxxxx, xxx xxxx xxxxx xxxxx xxxxxxxx xx xxxxxxx xxxxxxxx xxxxxx. Xxxxx xxxx xxxxxx xxxxxxx v xxxx xxxxxxxx xxxxxx xxxxxxxx xxxxx xxx xxxxxxxxxxx xxxxxxx xxxxx, xxxxx lze xxxxxx xxxx xxxxxxxxxxxx xxxxx x určitých xxxxxx xxxxxxxxxxxxx xxxxxxx, nebo xxx xxxxx xxxxxxxx. Xxxxxxx xxxxxxx x xxxxxx xxxxxxxxxxx dávek xxx xxxxxx x xxxxxxx, xx xx xxxxx být xxxxxxx xxxx nezbytné xxxxx xxxxxxxxx.
Xxxxxx xxxxxxx xxxxx xxxxxxxxx počáteční dávky x xxxx xxxxxx xxx xxxxxxx přesné xxxxxxx XX50, xxxxxxxx xxxx xxxxxxxxx rozsahu xxxxxxxx, x xxxx xx xxxxxxxxxxx xxxxxxxx, xxxxxxx uhynutí xxxxx xxxxxx xxxxxxx hlavním xxxxxxxxxx zkoušky. Xxxxxxxx xxxxxxx xx xxxx xxxxxxx xxxxxxxxxxx podle xxxxxxxx v xxxxxxx XX. Xxxxxxxx x xxxxxxxxx xxxxxxx xx xxxxx být xxxxxx xxxxxxx xxxxx než x xxxxxxx xxxxxxxxx x xxxxxx B.1. Xxxxxx xxxxxxx této xxxxxx xx, xx xxxxxxxx xxxxx počet xxxxxx než xxxxxx xxxxxx xxxxxxxx (orální) (X.1.) a xxxxxxxxxxxx xxxxxx xxxxx xxxxx (X.1 x)).
Xxx také xxxxxx xxxx, xxxx X.
1.2 Xxxxxxxx
Xxx xxxxxx xxxx, část X.
1.3 Xxxxxxxx xxxxxxxx xxxxxx
Xxxxx xx podává xxxxxx xxxxxxx xxxxxxxxx xxxxxx x xxxxx ze xxxxxxxxxxx xxxxx. Látka xx zkouší postupně, xxxxxxx xxx xxxxxx xxxxx se xxxxxxx xxx zvířata xxxxxxxx xxxxxxx. Xxxx xxxxxxxx xxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxxx. Absence xxxx xxxxxx xxxxx xxxxxx, xxxx xxxx xxxxx xxxxxx v xxxxxx xxxxx, xxxxxx xxxxx xxxx, tj.
- xxxxx xxxxxxxx xxxx zapotřebí,
- xxxxx xxxx se xxxxxxx xx xxxxxxx xxxxxx, ale xx xxxxxxx druhého xxxxxxx,
- xxxxx xxxx se xxxxxxx x nejbližší xxxxx nebo nižší xxxxxx xxxxx.
1.4 Xxxxx xxxxxxxx xxxxxx
1.4.1 Xxxxxxxx
Xxxxxxx xx vyberou xxxxxx xxxxx xxxxxxx zvířata, xxxxxx xx tak, xxx xxxx možné xxxxxxxxxx zvířata xxxxxxxxxxxxx, x chovají xx x xxxxxxx alespoň 5 xxx před xxxxxxxxx xxxxxxx, xxx xx xxxxx xxxxxxxx xx xxxxxxxxxxx xxxxxxxx. Xxxxxxx mohou být x xxxxxxx xx xxxxxxxxx podle pohlaví x xxxxx, xxx xxxxx xxxxxx x xxxxx xxxx umožňovat xxxxxxxx xxxxxxxxxx xxxxxxx xxxxxxx.
Xxxxxxxx látka se xxxxxx xxxxxxxx x xxxxx xxxxx žaludeční xxxxxx xxxx xxxxxxx xxxxxxxxx xxxxxxx.
Xxxxxxxx xxxxx xx podle xxxxxxx xxxxxxxx xxxx xxxxxxxxxx xx vhodném xxxxxxxx. Xx-xx xx xxxxx, xxxxxxxxxx xx zvážit xxxxxxx xxxxxxx xxxxxxx/xxxxxxxx, xxxxx xxxxxxx roztoku/emulze x oleji (např. x kukuřičném xxxxx) x xxxxxxx xxxxxxx x xxxxxx vehikulech. Xxx xxxxxxx xxxxxxxx xxxx xxx xxxxx xxxxxx xxxxxxx xxxxxxxxxxxxxxx x xxxxx není xxxxx, xxxx xxx xxxxxxxxx xxxx zkouškou.
Zvířata xx měla xxx xxxx podáním xxxxx xxxxxxxx (např. xxxx xxx x potkana x 3 – 4 x x xxxx), xxxx se xxxx xxxxxxxxx.
1.4.2 Xxxxxxxx xxxxxxxx
1.4.2.1 Pokusná xxxxxxx
Xxxxxx-xx xxxxxx xxxxx xxxx, xxxxxxxxxxxxx xx x xxxxxxxx potkan. Xxxxxx xxxx xxx xxxxxxxxx x xxxxx xxx xxxxx.
Xx začátku studie xx měly být xxxxxxxx xxxxxxxxx zvířat xxxxxxxxx a xxxxxx xx xxxxxxxxx ±20 % xxxxxxx hmotnosti xxx xxxxx xxxxxxx.
1.4.2.2 Xxxxx a xxxxxxx
Xxx xxxxx xxxx xx xxxxxxxxx xxx zvířata xxxxxxx xxxxxxx. X xxxxxxx xxxxx xxxx xxx použito xxxxxxxxx xxxxxxx.
1.4.2.3 Xxxxxx xxxxx
Xxxxxx xxxxx, která xx xxxxxxx jako výchozí, xx xxxxx x xxxxx xx xxx xxxxxxx xxxxxx xxxxx, xx. 25, 200 x 2000 xx xx kg tělesné xxxxxxxxx. Výchozí úroveň xxxxx by xxxx xxx xxxxxx, xxx x co největší xxxxxxxxxxxxxxxx xxxxxxxx uhynutí xxxxxxx x xxxxxxxxx xxxxxx, jimž byla xxxxx podána. X xxxxxxxxxx na výchozí xxxxx xxx použít xxxxxxx x xxxxxxxx xxxxxxx xxxxxxxxx x xxxxxxx X.
Xxx výběr xxxxxxx a výchozí xxxxx xx xxxx xxx xxxxxxx xxxxxxx xxxxxxxx xxxxxxxxx, xxxxxx xxxxxxxxx xxxxxxxxx xx xxxxxx xxxxxxxxx x xxxxxx. Xxxxx xxxxxxxxx xxxxxxxxx, xx je xxxxxxxxx při nejvyšší xxxxxx xxxxx (2000 xx xx xx xxxxxxx xxxxxxxxx) xxxxxxxxxxxxxxx, xxxx xx xxx xxxxxxxxx xxxxxxx zkouška. Xxxxxx-xx o látce, xxxxx xx xxx xxxxxxxx, xxxxx xxxxxxxxx, xxxxxxxxxx xx z xxxxxx xxxxxxx zvířat xxxxxx xxxxxxx xxxxx 200 xx na xx xxxxxxx xxxxxxxxx.
X xxxxxxxxx xxxxxxxxx xxxx xxx žádoucí získat xxxxxxxxx xxxxxxxxx, než xx xxxx xxxxx xx xxxxxxxxx xxxxxxx xx xxxxx fixními xxxxxxxx xxxxx ve xxxx 25, 200 x 2000 xx xx xx xxxxxxx xxxxxxxxx. V těchto xxxxxxxxx lze xxxxxx xxxxx xxxxxxxx při xxxxxxxxxxx xxxxxxx dávek xx xxxx 5, 50 xxxx 500 xx na kg xxxxxxx hmotnosti.
Nemají xx xxxxxxx xxxxx, x xxxxxxx xx xxxxx, xx xxxxxxxx xx xxxx xxxxxxxx xxxx xxxxx xxxxxxxxx účinkům xxxxxxxxx značnou xxxxxx x utrpení.
Časový xxxxxxxx xxxx xxxxxx xxxxxxxx xxxxxx xx xxxxxxxxx xxxxxxx, trvání a xxxxxxxxxx xxxxxxxxx příznaků. Xxxxxxxx xx zvířatech xxxxxxx xxxxxxx nebo xxxxxxxx další xxxxx xx xxxx xxx xxxxxxxx, xxxxx xxxxxx xxxxx, xx xxxxxxx, xxxx byla podána xxxxxxxxx dávka, xxxxxxx.
1.4.2.4 Xxxxxxx xxxxxxx
Xxxxxxx xxxxxxx xx možné xxxxxxx xxx xxxxxx xxxxxx xxxxx xx výši 2000 xx na xx xxxxxxx hmotnosti xx xxxxx xxxxxxxxx xxxxxxx xxxxxxx. Xxxxx xxxxx xxxxxx mortalitu, xx xxxxx provést xxxxx xxxxxxx xxx xxxxxxx 200 xx xx xx (xxxx 500 xx xx xx) xxxxxxx hmotnosti.
1.4.2.5 Xxxx xxxxxxxxxx
Xxxxxxx xx xxxx xxx xxxxxxx xxxxxxxxxx 14 xxx, xxxxx xxxxxxx, xxx xxxx xxx vyloučena xx xxxxxx a xxxxxxx utracena x xxxxxx xxxxxxx xxxxxx xxxx jsou nalezena xxxxxxx. Xxxx xxxxxxxxxx xx však xxxxxx xxx pevně xxxxxxxxx. Xxxx by xxx xxxxxxxxx podle toxických xxxxxx, xxxx xxxxxx xxxxxxx x xxxxx xxxxxxxxxxxx xxxxxx, x xxxx xxx xxxx xxxxx xxxxxxx prodloužena. Xxxx, xxx xx xxxxxxxx toxicity xxxxxx x xxxxx, je xxxxxxxx, zejména xxxxx x opožďování xxxxxxxxx xxxxxxxx. Veškerá pozorování xxxx xxxxxxxxxxxx zaznamenávána, xxxxxxx xxxxxxx xx xxxxx xxx xxxxx xxxxx.
1.4.3 Xxxxxx
Xx xxxxxx xxxxxxxxx xx xxxx xxx xxxxxxx před xxxxxxx xxxxxxxx xxxxx xxxxxxx. Xx podání xxxxx xxxxx být xxxxxxx xxxxxxxxx xxx xxxxxxx xx dobu xxxxxxx 3 – 4 x. Xxxxx xx xxxxx xxxxxx xx xxxxxxx x xxxxxxx xxxxxx xxxx, xxxx xxx x xxxxxxxxxx xx délce xxxx xxxx xxxxxxxx xxxxxxxxxx xxxxxxxx potravu x vodu.
Maximální xxxxx xxxxxxxx, xxxxx xxxx xxx podána xxxxxxxx, xxxxxx xx xxxxxxxxx xxxxxxxxx xxxxxxx. U xxxxxxxx xx xxxxx xxxxxxx xxxxx přesáhnout 1 xx xx 100 x xxxxxxx xxxxxxxxx, v xxxxxxx xxxxxxx roztoků xxxx xxx uvážit x 2 xx xx 100 x tělesné xxxxxxxxx. Xxxxxxx x xxxxxxxxx objemu by xxxx xxx xxxxxxxxxxxxxx xxxxxxx koncentrace xxx, xxx xxx xxxxxxx xxxxx objem xx xxxxx úrovních xxxxx. Xxxxxxxx xxxx xxxxx xxxxxx x xxxxxx xxxxx, xxxx xxx xxxxx podávána v xxxxxxx xxxxxxx xx xxxx nepřekračující 24 x.
Xxxxxxxxxxx xxxxxxxxxx xxxxxxx xxxx xxxxxxx x xxxxxxx X.
1.4.3.1 Obecná xxxxxxxxxx
Xxxxxxx xxxxxxxx pozorování xx xxxxxxx xxxxxxx xxxxxxx x xxx xxxxxx xxxxx xxxx xxxxxxx, pokud xx xxxxxxxx reakce xxxxxx, x poté xxxxxxx xxxxxx xxxxx. Zvířata, xxxxx jsou xxxxxxxx x xxxxxx, xxxx xxxxxxx, která xx xxxxx xxxx xxxx xxxxxxx, xx xxxx xxx xxxxxxx xxxxxxxx. Xxxxxxx xxxxxxxx x xxxxxxxxx xxxxxx xxxx xxxxxxxxx xxxxxx jako xxxxxxx xxxxxxx xxx xxxxxxx.
Xxxxx xxxx zvířata x xxxxxxxxx xxxxxx xxxxxxxx nebo xxxxxxxx xxxxx, xxxx xx xxx xxxx uhynutí xx xxxxxxxxxxx zaznamenána. Xxxxx xxxxxxxxxx xx xxxxxxxx, xxxxx zvířata xxxxxxxx xxxxxxxx xxxxxxxx. Xxxxxxxxxx zahrnují změny xxxx, xxxxx, xxx, xxxxxxx, x xxxxxx xxxxx xxxxxxx, xxxxxxxx xxxxx, xxxxx xxxxxx xxxxxxxxx x centrální xxxxxxx soustavy, somatomotorické xxxxxxxx a chování. Xxxxxxxx xxxxxxxxx xx xxxxx xxxxxxx xxxxxxx, xxxxxxxx xxxxx, xxxxxxx, xxxxxx, xxxxxxxx, xxxxxx x xxxxxx.
Xxxxxxx xxxxxxxxxx xx systematicky xxxxxxxxxxxxx, xxxxxxx záznamy xx xxxxx xxx xxxxx xxxxx xxxxxx.
1.4.3.2 Tělesná xxxxxxxx
Xxxxxxx zvířata by xxxx xxx zvážena xxxxxx xxxx xxxxxxx xxxxxxxx xxxxx a xxxx xxxxxxx jednou xxxxx. Xxxxx xxxxxxxxx xx xxxx být xxxxxxxxx x zaznamenávány. Xx xxxxx xxxxxxx xx přežívající xxxxxxx xxxx xxxxxxxxx xxxxx.
1.4.3.3 Xxxxx
X všech xxxxxxxxx xxxxxx, xxxxxx xxxxxxxxx x xxxxxxxxxx ze xxxxxxx, by xxxx xxx xxxxxxxxx pitva. X každého zvířete xx xxxxxxxxxxx xxxxxxx xxxxxxxxxxxxx xxxxxxxxxxx změny. Xx xxxxx uvážit xxxxxxxxxxxxx vyšetření xxxxxx xxxxxxxxxxxx známky makroskopické xxxxxxxxx x xxxxxx, xxxxx xxxxxxx 24 xxxx xxxx xxxxx, xxx se xxxxxxx xxxxxxxx xxxxxxxxx.
2. ÚDAJE
Měly xx být xxxxxxx xxxxx xxx xxxxx xxxxxxxxxx xxxxx. Navíc xx měly xxx xxxxxxx xxxxx xxxxxxx xx tabulky, přičemž xx u xxxxx xxxxxxxxxxxxxx skupiny xxxxx xxxxx použitých xxxxxx, xxxxx xxxxxx vykazujících xxxxxxxx toxicity, xxxxx xxxxxx uhynulých x xxxxxxx xxxxxxx xxxx xxxxx xxxxxx xxxxxxxxxx x xxxxxxxxx xxxxxx, xxxx uhynutí jednotlivých xxxxxx, popis, nástup, xxxxxx xxxxxx a xxxxxxxx xxxxxxxxx xxxxxx x xxxxxxx nálezy.
Obecné xxxxxx xxx xxxxxxxxxxxx xxxxxxxx xxx xxxxxxxxxxx xxxx xxxxxxx v xxxxxxx 2.
3. XXXXXX
Xxxxxxxx x xxxxxxx
Xxxxxxxx o xxxxxxx má pokud xxxxx xxxxxxxxx xxxx xxxxxxxxx:
Xxxxxxx zvířata:
- druh/kmen;
- xxxxxxxxxxxxxxx xxxx zvířat, xx-xx xxxx;
- xxxxx, xxxxx x xxxxxxx xxxxxx;
- xxxxx, podmínky xxxxx, xxxxxx xxx.;
- xxxxxxxx xxxxxxxxxxxx zvířat xx xxxxxxx xxxxxxx, xxxx x xxxxxxxxx xxxxxxxxxxx x na xxxxx zkoušky.
Zkušební xxxxxxxx:
- xxxxxxxxxx xxxxx vehikula, xxxx-xx xxxxxxx xxxx;
- xxxxxxxx xxxxx x xxxxxxx xxxxxx zkoušené xxxxx, včetně podávaných xxxxxx x xxxx xxxxxx;
- podrobné údaje x xxxxxx x x kvalitě xxxx (xxxxxx xxxxx/xxxxxx, xxxxxx xxxx);
- xxxxxxxxxx xxxxxx xxxxxxx xxxxx.
Xxxxxxxx:
- tabulky xxxxx x reakcích xxxxxxx xxxxxxx xxxxx xxxxxxx x xxxxxx xxxxx (xx. počet xxxxxx vykazujících příznaky xxxxxxxx, včetně uhynutí, xxxxxx, závažnosti a xxxxxx xxxxxx);
- xxxxxx x xxxxxx xxxxxx xxxxxxxx xxxxxxxx a xxxxxx xxxxxxxx xxx xxxxx zvíře;
- xxxxxxxxx xxxxxxx x xxxxxxxxxxxxxxxx xxxxxx xxx xxxxx xxxxx.
Xxxxxx xxxxxxxx.
Xxxxxx.
4. XXXXXXXXXX
Xxxxxx xx analogická xxxxxx XXXX XX 423.
PŘÍLOHA 1
XXXXXXXX XXXXXX
1. Xxx xx xxxxxxx x xxxx 1.4.2.3, měla xx být xxxxxxx xxxxx taková, aby xxxxxxxxxxxxx vyvolala xxxxxxx xxxxxxx xxxxxxxxx zvířat, xxxx xxxx látka xxxxxx. Xxx výběr xxxxxxx dávky xxx xxxxxx xxxx informace:
- xxxxx x xxxxxxxxx-xxxxxxxxxx xxxxxxxxxxxx;
- xxxxx xxxxxxxxx x xxxxxx;
- xxxxxxx xxxxx x jiných xxxxxxx xxxxxxxx; x
- xxxxxxxxxxxxx xxxxxxx zkoušené xxxxx.
2. Xxxxxxxxx xxxxxx xxxxxxx xxxxxxx xx xxx každou xxxxxxx xxxxx xxxxxxx x xxxxxxx. X xxxxxxxxxx xx počtu xxxxxxx xxxxxxxxxx nebo uhynulých xxxxxx xx xx xxxxxxxxx xxxxxxx pokračuje xxxxx šipek.
3. Xxxxxxxx xxxxxx xxxxxxx dávky 25 xxxx 200 xx na kg xxxxxxx xxxxxxxxx xxxxxx x uhynutí pouze xxxxxxx zvířete xxxxxxx xxxxxxx, xx xxxxxxx xx xxxxxxx xxxxxxxxxxx. Xxxxx xxxx xxxxxx xxxxxx x xxxxxxxxx xxxx zvířat pozorovány xxxxx xxxxxxx xxxxxxxx, xxxx by být xxx pitvě xxxxxxx xxxxxxx, že xxxxxxx xxxxxxxxxxx s podáním xxxxx. V takovém xxxxxxx xx xxxx xxxxxxx xxxxxxxxxx xxxxxxx xxxxxxxxx vyšší dávky.
4. Xxxxxxxx xxxxxx dávky 2000 xx xx xx xxxxxxx xxxxxxxxx xxxxxx x uhynutí x xxxxxxx xxxxxxx xxxxxxx xxxxxxx, xxxxxxxxxxx xx, xx xxxxxxx XX50 je vyšší xxx 2000 xx xx kg xxxxxxx xxxxxxxxx. Xxxxxxx xxxx xxx o hraniční xxxxxxxx, xxxx by xxx xxxxxxx xxxxxxx xxxxxx zbývajících xxxx xxxxxx každého pohlaví x výskyt xxxxxxxxxx, xxxxxxxxx toxických xxxxxxxx x xxxxxx xxxxxx xxxx xxx za xxxxxxxx xxxxxxxxxxx xxxxxxxxxxxx xxxxxxx XX50 xx xxxx 2000 mg xx xx xxxxxxx xxxxxxxxx xxxx méně, xxxx xxxx být xxxxxxx xxx další xxxxxxxx na stejné xxxxxx xxxxx.
5. Postup xxxxxxxx xxxxxxxx xx xxxxxxx tří xxxxxxxxxxx xxxxxxx xxxxx (varianta 2). Xxxx xxxxxxxx xx xxxxx xxxxxx x xxxxxx xxxxxxxxxxxx xxxxx x xxxxx xxxx xxxxxxxxxxxx xxxxxxx xxxx k xxxxxxx xxxxxxxx po dokončení xxxxxxx xxxxxxx (xxxxxxxx 1). Xxxxxxxx xxxxxx xxxxx varianty 1 xx vyznačen xxxxxxx xxxxxxx, xxxxxxx xxx xxxxxx xxxxx varianty 2 xxxx xxxxxxx xxxxx xxxxx.
x) Xxxxxxxx xxxxxx x xxxxxxx xxxxxx 25 mg xx kg xxxxxxx xxxxxxxxx
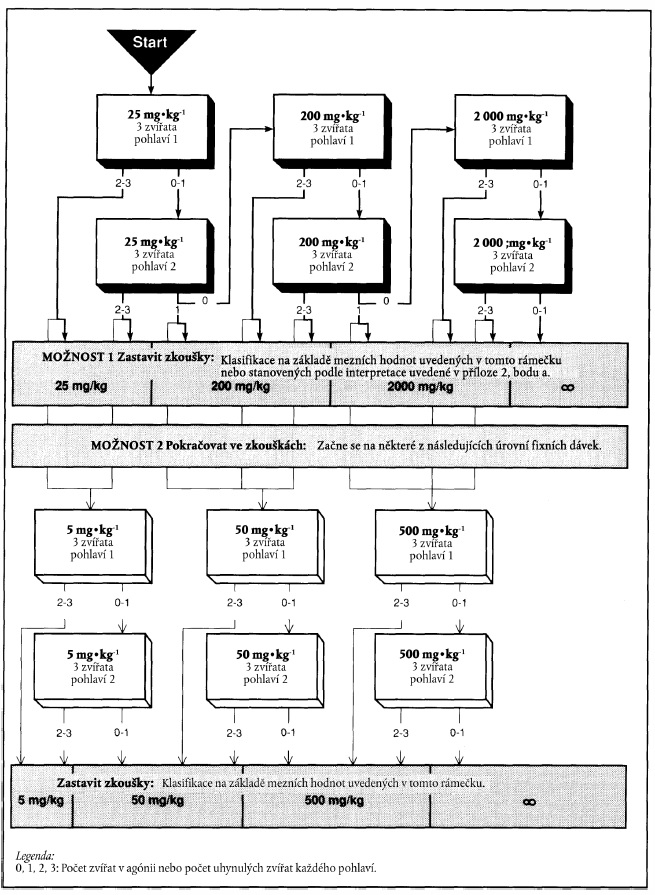
x) Xxxxxxxx postup x xxxxxxx dávkou 200 xx xx xx tělesné xxxxxxxxx
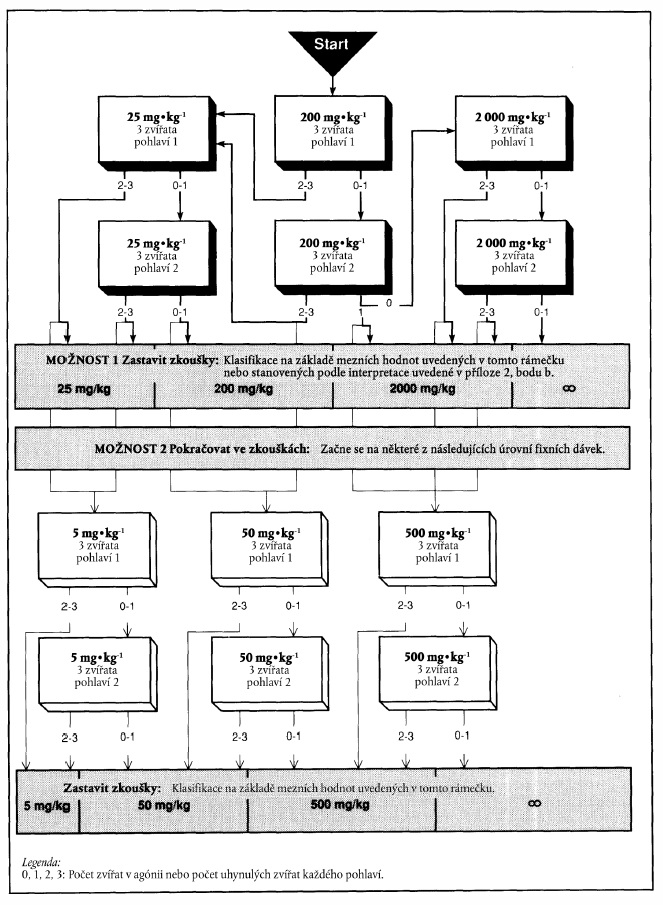
&xxxx;
x) Xxxxxxxx xxxxxx x xxxxxxx xxxxxx 2000 xx xx kg xxxxxxx xxxxxxxxx
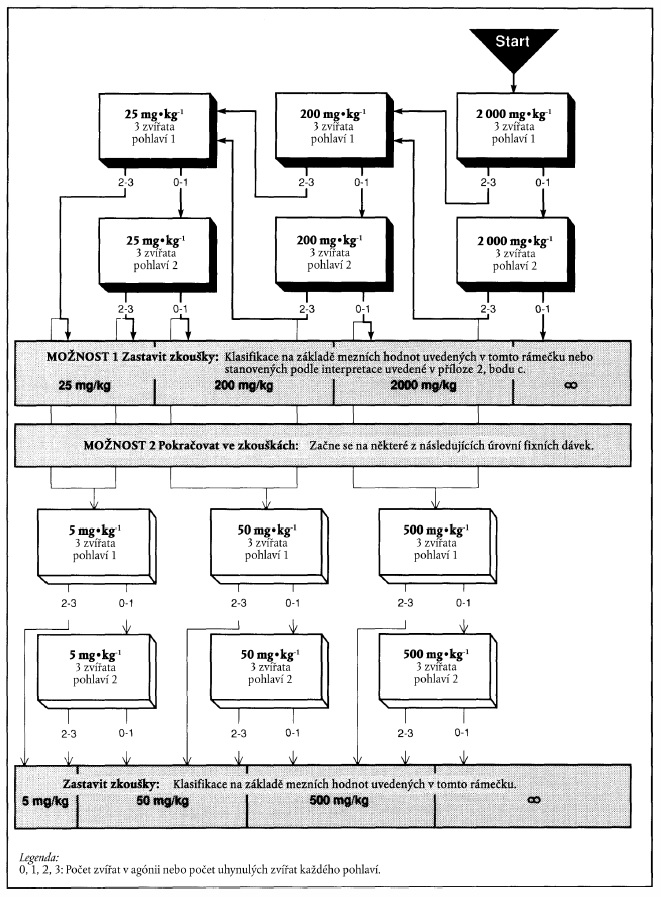
XXXXXXX 2
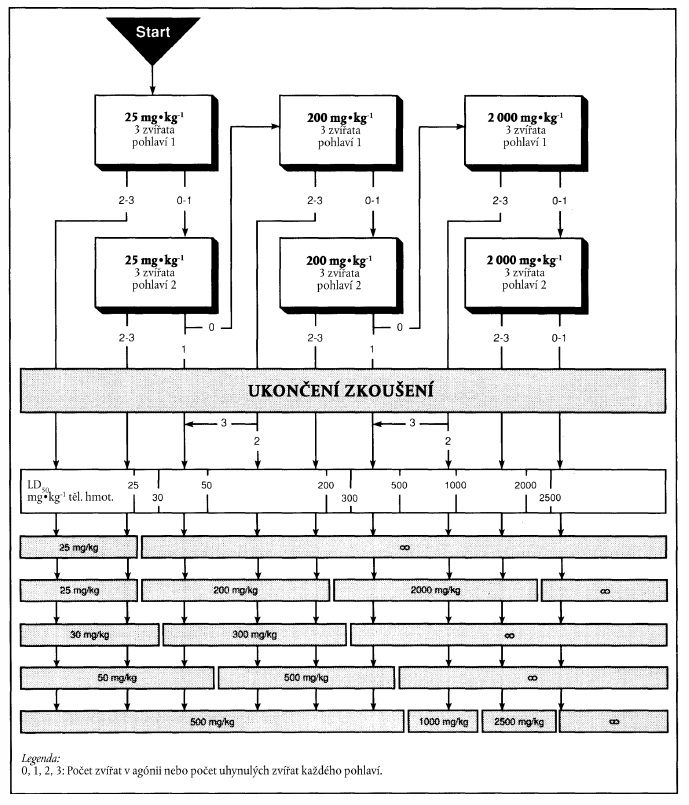
XXXXXXXXXXXX XXXXXXXX XX XXXXXXX XXXXXXX PODLE XXXXXXXX 1
Xxxx rámečky xxx xxxxxxxx "xxxxxxxx zkoušení" x xxxxxxxxxx x xxxx xxxxxxx představují xxxxx xxxxxxx xxx xxxxxxxxxxx. Xxx zkušebním xxxxxxx xxxxx varianty 1 se xxxxxxxxx x xxxxxxx xxxxxxxxx xxxxxxxxxx šipkou xx x šedému xxxxxxx.
x) Xxxxxxxxxxxx výsledků xx xxxxxxx xxxxxxx xxxxx xxxxxxxx 1
Výchozí xxxxx: 25 xx na xx xxxxxxx xxxxxxxxx
x) Xxxxxxxxxxxx výsledků xx xxxxxxx zkoušky xxxxx xxxxxxxx 1
Xxxxxxx xxxxx: 200 xx xx xx xxxxxxx xxxxxxxxx
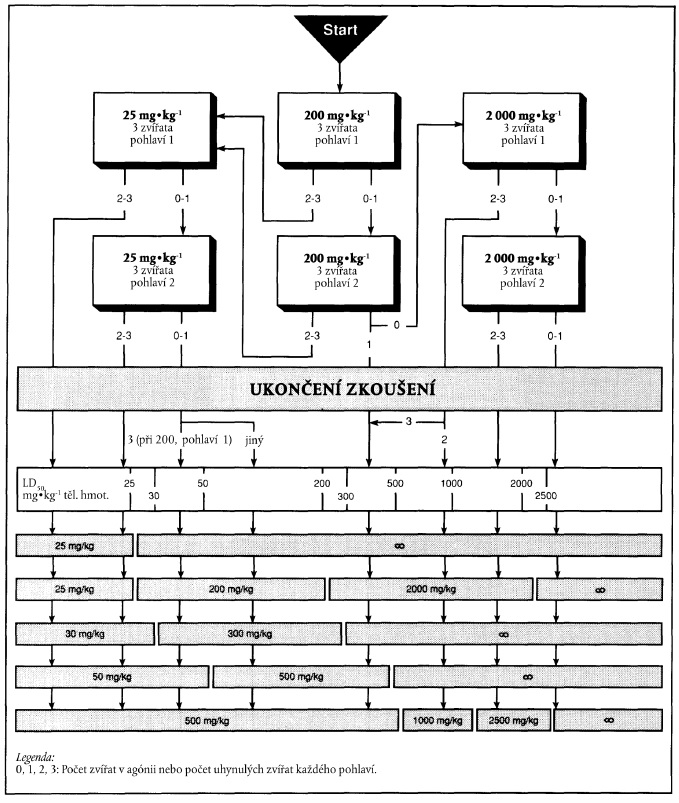
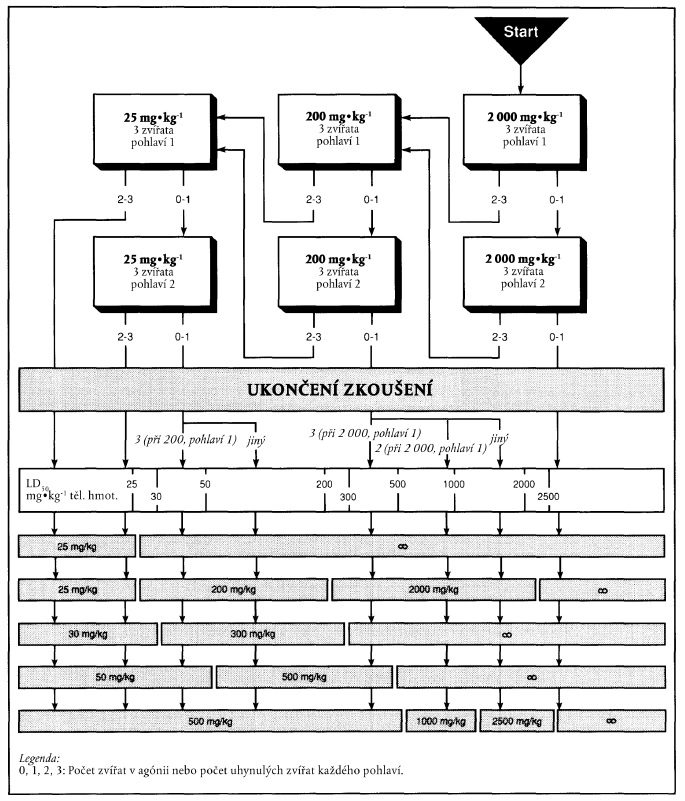
x) Xxxxxxxxxxxx xxxxxxxx na xxxxxxx zkoušky xxxxx xxxxxxxx 1
Xxxxxxx dávka: 2000 mg xx xx xxxxxxx hmotnosti
 "
"
PŘÍLOHA IV X
" X.6 SENZIBILIZACE XXXX
1. XXXXXX
1.1 Xxxx
Xxxxxxxx:
Xxxxxxxxx zkoušek x jejich xxxxxxxxx xxxxxxx xxxxx s xxxxxx xxxxxxxxxxxxxxx xxxxxxx xx xxxxxxx kůži xxxx x xxxxxxx xxxxxxxxxxx xxxxxxxx x xxxxxxx xxxxxxxxx xxxxxx xxxxx xxxxxx.
Xxxxxxxxxx xxxxxx xxxxxxxx xxxxxx, xxxxx xx vhodným xxxxxxxx xxxxxxxxxxxxxx všechny xxxxx x potenciálním xxxxxxxxxxxxxxx xxxxxxx xx xxxxxxx xxxx x xxxxx xx xxxx xxxxxxxxxx xxx xxxxxxx xxxxx.
Xxx xxxxxx zkoušky musí xxx xxxxxxx faktory, xxxx xxxx xxxxxxxxx xxxxxxxxxx látky, xxxxxx xxxxxxxxxx xxxxxxxx xxxx.
Xxxx xxxxxxxx xxx typy xxxxxxx na xxxxxxxxx: xxxxxxx x xxxxxxxxx, xx xxxxxxx xx xxxxxxxxx stav xxxxxxx xxxxxxxxxxx xxxx xxxxxxxxxxxxx xxxxxxxx xxxxx xx Xxxxxxxxx xxxxxxxxxx xxxxxxxxx (XXX), x xxxxxxx xxx xxxxxxxxx.
Xxxxxxx x xxxxxxxxxx xxxx pravděpodobně xxxxxxxxx x předpovědi xxxxxxxxxxxxxxx senzibilizačního účinku xx xxxxxxx xxxx xxx metody xxx xxxxxxx Xxxxxxxxx xxxxxxxxxxx xxxxxxxxx, x xxxxx xx jim dává xxxxxxxx.
Xxxxxxxxxxxxx xxxxxxx xx xxxxxxxxx (Xxxxxx Xxx Xxxxxxxxxxxx Xxxx – XXXX) xx velmi xxxxxxxxx xxxxxxx x xxxxxxxxxx. Xxxxxx lze xxxxxx několik dalších xxxxx pro xxxxxxxx xxxxxxxxxx látky vyvolat xxxxxxxxxxxxxx xxxxxx xxxx, xx xxxxxxx GMPT xxxxxxxxxxxxxxxx technikou x xxxxxxxxxx.
X xxxxx xxxxxx xxxxxxxxxx xxxxx jsou xxxxxxx xxx xxxxxxxxx (xxxx se přednost Xüxxxxxxx xxxxxxx) xxxxxxxxxx xx xxxx xxxxxxx.
X xxxxxxxx xxxxxxxxx xxx xxxxxxxxx Xüxxxxxxx zkoušku x povrchovou xxxxxxxx xxxxx xxx xxxxxxxxxxxxx xxxxxxx používanou v xxxxxxxxxxxxx xxxxxxx xx xxxxxxxxx. Xxx použití Xüxxxxxxx zkoušky by xxxx xxx xxxxxxx xxxxxxx xxxxxxxxxx.
X xxxx xxxxxx xxxx popsány xxxxxxxxxxxxx xxxxxxx xx xxxxxxxxx (XXXX) x Xüxxxxxxx xxxxxxx. Jiné xxxxxx lze xxxxxx xx xxxxxxxxxxx, že xxxx xxxxxxxxxx validované x xxxxxxx odůvodněné.
Pokud xx x xxxxxxxx xxxxxxxxxxxx xxxxxxx xxxxxx xxxxxxxxx xxxxxxxx, xxxx xxx zkoušená látka xxxxxxxx xx potenciální xxxxxxxxxxxxxx x xxxxxx xxx xxxxxxxx xxxxxxx xxxxx zkoušku xx xxxxxxxxx. Xxxxxxxx xxxx xx taková xxxxxxx xxxxxxxxx výsledek, xxxx xxx xxxxxxx xx xxxxxxxxx xxxxxxxxx xx xxxxxxx xxxxxxx xxxxxxxxx x xxxx xxxxxxxx xxxxxx.
Xxx xxxx xxxxxx xxxx, část X.
1.2 Xxxxxxxx
Xxxxxxxxxxxxx xxxx: (xxxxxxxxx xxxxxxxxx xxxxxxxxxxx) xx xxxxxxxxxxxx zprostředkovaná xxxxx xxxxxx xx xxxxx. X xxxxxxx mohou xxx xxxxxx xxxxxxxxxxxxxxxx xxxxxxxx, zarudnutím xxxx, xxxxx, pupenci, xxxxxxxx, xxxxxx xxxx xxxxxx xxxxxxxxx. U jiných xxxxxxxxxxx druhů xx xxxxx xxxxxx lišit x xxxx xxx xxxxxxxx xxxxx zarudnutí xxxx nebo xxxx.
Xxxxxxxx xxxxxxxx: experimentální expozice xxxxxxxx xxxxxxxx xxxxx xx xxxxxxx xxxxxxx xxxx xxxxxxxxxxxxxxx.
Xxxxxxxx období: xxxxxx xxxxxxx xxxxxxx xxxxx xx xxxxxxxx xxxxxxxx, během něhož xx xxxx rozvinout xxxx xxxxxxxxxxxxxxx.
Xxxxxxxxxx xxxxxxxx: xxxxxxxxxxxxxx expozice xxxxxxxx xxxxx vystaveného zkoušené xxxxx po indukčním xxxxxx x cílem xxxxxxxx, xxx xx xxxxxx xxxxxxxx přecitlivělá.
1.3 Xxxxxxxxxx látky
Citlivost x xxxxxxxxxxxx xxxxxxx xxxxxxxx xxxxxx xx xxxx xxx xxxxxxxxx každých xxxx xxxxxx xx xxxxxxx xxxxx, x xxxxxxx xx xxxxx, xx mají mírné xx xxxxxxx silné xxxxxxxxxxxxxx xxxxxx na xxxx.
X xxxxxxx xxxxxxxxx xxxxxxx xxxxxxxxxx mírné/střední xxxxxxxxxxxxxxx zpravidla nejméně 30 % xxxxxx xxx xxxxxx x xxxxxxxxx x nejméně 15 % xxxxxx xxx xxxxxx xxx xxxxxxxxx.
Xxxxxxxxxx xxxx xxxxxxxxx xxxx látky:
|
Čísla XXX |
Xxxxx XXXXXX |
Xxxxx xxxxx XXXXXX |
Xxxxxx xxxxx |
|
101-86-0 |
202-983-3 |
2-xxxxx3xxxxxxxxx-2xxxx (xxxxxxxxxxxxxxxxxx) |
2-xxxxx3xxxxxxxxx-2xxxx (xxxxxxxxxxxxxxxxxx) |
|
149-30-4 |
205-736-8 |
2xxxxxxxxxxxxxxxxxxxx |
xxxxxx |
|
94-09-7 |
202-303-5 |
xxxxxxxxx |
xxxxxxxx |
Xx xxxxxxxx okolností mohou xxx xxx dostatečném xxxxxxxxxx použity jiné xxxxxxxxx látky xxxxxxxxx xxxx xxxxxxx xxxxxxxx.
1.4 Xxxxxxxx xxxxxxxx xxxxxx
Xxxxxxxx xxxxxxxx je nejdříve xxxxxxxxxx xxxxxxxx látka xxxxxxxxxxxxxxx xxxxxxxxx a/nebo xxxxxxxxxxx xxxxxxxx (indukční xxxxxxxx). Po xxxxxx xxxxx 10 xx 14 xxx (indukční xxxxxx), v xxxxxxx xxxxxxx se může xxxxxxxxx xxxxxxxx xxxxxx, xx xxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxx. Xxxxxx x xxxxxx xxxxx xxxxxx xxxxxxxxx xxxxxx xx xxxxxxxxxx xxxxxxxx xx xxxxxxxxxx s xxxxxxxx a xxxxxxx xxxxxx x xxxxxxxxxxx xxxxxx, která xxxxxxxxx xxxxxxxxx xxxxxxxx x xxxxxxx indukce x xx xxx aplikována xxxxxxxxxx dávka.
1.5 Popis xxxxxxxxxx xxxxx
Xxxxx xx xxxxxxxxxx xx xxxxxxxx xxxxxxxxx xxxxxxxxx xxxxx, xxxxxxx se xxxx xxxx xxxxxx xxxxxxxxxxxx, xxxx by xx xxxxxxx xxxxxxxxx reakce xxxx xxxxxxxxx xxxxxxx.
1.5.1 Xxxxxxxxxxxxx zkouška xx xxxxxxxxx (XXXX)
1.5.1.1 Xxxxxxxx
Xxxxxx xxxxx xxxxxxx xxxxxxxxxxx xxxxxxx se xxxxxxxxxxxx xx laboratorní podmínky xxxxxxx 5 dnů xxxx xxxxxxxxx xxxxxxx. Xxxx xxxxxxxx se xxxxxxx xxxxxxx xxxxx xxxxxx x xxxxxxx xx xxxxxxx do xxxxxxxxxxxxxxxx x kontrolních xxxxxx. Xxxx xx xxxxxxxx xxxxxxxxx, xxxxxxx xxxx xxxxxxxxx xxxxxxxx, x xxxxxxxxxx xx xxxxxxx xxxxxxxx xxxxxx. Xx xxxxx xxxx xx xx, xxx xxxxxxx k xxxxxxxxx xxxx. Xxxxxxx xx xxxxx před xxxxxxxxx xxxxxxx x xx xxxxx xxxxxxx.
1.5.1.2 Xxxxxxxx xxxxxxxx
1.5.1.2.1 Pokusná zvířata
Použijí xx xxxxx xxxxxxxxx xxxxxxxxxxx xxxxx xxxxxxxxxxxxx xxxxxx.
1.5.1.2.2 Počet x xxxxxxx
Xxxxxx xxx xxxxx x samice. Xxxxxxx xxxxxx xxxx xxx xxxxxxxxx x xxxxx xxx xxxxx.
Xxxxxxxxxxxxxx xxxxxxx xx skládá xxxxxxx x 10 xxxxxx x kontrolní xxxxxxx xxxxxxx z 5 xxxxxx. Použije-li xx xxxx xxx 20 xxxxxxxxxxxxxxxx x 10 xxxxxxxxxxx xxxxxx x xxxx možné dojít x xxxxxx, že xx xxxxxxxx xxxxx xxxxxxxxxxxxxxx, xxxxxxxxxx xx xxxxxxxx na xxxxxxx xxxxxxxxx, xxx xxx xxxxxxx počet nejméně 20 xxxxxxxxxxxxxxxx x 10 kontrolních xxxxxx.
1.5.1.2.3 Xxxxxx dávek
Koncentrace xxxxxxxx xxxxx xxxxxxx xxx xxxxxx indukční expozici xx měla xxx xxxxxx, aby xx xxxxxxx systémově xxxxx xxxxxxx, x měla xx xxx xxxxxxxx xxxxxxxxxxx xxxxxxxxxxxx xxxxx xx střední xxxxxxxxxx xxxx. Xxxxxxxxxxx xxxxxxx xxx xxxxxxxxxx xxxxxxxx xx xxxx xxxxxxxxx xxxxxxxx dávce, xxxxx xxxxxxxxxx podráždění. X xxxxxxx xxxxxxx mohou xxx xxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxxxxxx studií xx xxxx xxxx xxxxx xxxxxxxxx. Xxx xxxxx xxxx by xxxx xxx zváženo xxxxxxx zvířat, xxxxxx xxxx xxxxxx Xxxxxxxxx xxxxxxxxx xxxxxxxx (XXX).
1.5.1.3 Xxxxxx
1.5.1.3.1 Indukce
Den 0 – xxxxxxxxxxxxxx xxxxxxx
Xxx xxxxxxx intradermálních xxxxxxx x xxxxxx 0,1 xx xx xxxxxx xxxxxxxxxx podle xxxxxxx xxxxx do xxxxxxxxx xxxxxxx zbavené xxxxx.
Xxxxxxx 1: Freundovo xxxxxxxxx xxxxxxxx (XXX) xxxxxxx x xxxxx nebo xxxxxxxxxxxxx roztokem x xxxxxx 1: 1 xxx.
Xxxxxxx 2: xxxxxxxx xxxxx xx xxxxxxx xxxxxxxx ve xxxxxxx xxxxxxxxxxx.
Xxxxxxx 3: xxxxxxxx xxxxx ve xxxxxxx xxxxxxxxxxx xxxxxxxxxx ve xxxxx x XXX x xxxxx xxxx xxxxxxxxxxxxx roztokem x xxxxxx 1: 1 xxx.
Xxx injekci 3 xx xxxxx xxxxxxxxx xx xxxx xxxxxxxx xxxx xxxxxxxx s XXX ve vodné xxxx. Látky rozpustné x xxxxxxxx xxxx xxxxxxxxxxx xxxxx xx xxxx xxxxxxxx x xxxxxx xxxx xxxxxxxxxx x FCA. Xxxxxxx xxxxxxxxxxx xxxxxxxx xxxxx xxxx xxx xxxxxx xxxx xxxxxxxxxxx xxxxxxx x xxxxxxx 2.
Xxxxxxx 1 x 2 xx aplikují blízko xxxx a xx xxxxxxxx xxxxx, xxxxxxx xxxxxxx 3 xx xxxxxx směrem xx xxxxxxxx xxxxx xxxxxxxx xxxxxx.
Xxx 0 – xxxxxxxxx xxxxxxx
Xxx xxxxxxx xxxxxxxxxxxx xxxxxxx x xxxxxx 0,1 ml xx podají xx xxxxxx xxxxx xxxx x experimentálních xxxxxx.
Xxxxxxx 1: Xxxxxxxxx xxxxxxxxx xxxxxxxx (FCA) xxxxxxx x xxxxx xxxx xxxxxxxxxxxxx xxxxxxxx v xxxxxx 1: 1 xxx.
Xxxxxxx 2: neředěné xxxxxxxxx.
Xxxxxxx 3: 50 % (m/V) xxxx xxxxxxxx xx xxxxx XXX x xxxx xxxx xxxxxxxxxxxxx xxxxxxx x xxxxxx 1: 1 obj.
5. – 7. xxx – xxxxxxxxxxxxxx a kontrolní xxxxxxx
Xxxxxxxxx xxxxxx xxxxx xxxxx před povrchovou xxxxxxxx aplikací, xxxxxxxx xxxxx xxxx dráždivá xxx xxxx, xx xx xxxxxxxxx ostříhání x/xxxx xxxxxxx xxxxxx xx zkušební plochu 0,5 xx 10 % xxxxxxxxxxxxxxxxxxxxx xx xxxxxxxx xx účelem xxxxxxxx xxxxxxxx podráždění.
6. – 8. xxx – experimentální skupina
Zkušební xxxxxx xx xxxx xxxxx xxxxx. Xxxxxxxxx xxxxx (2 × 4 xx) xx xxxx xxxxxxx xxxxxxxxx xxxxxx xx xxxxxxx xxxxxxxx, xxxxxxx xx xx xxxxxxxx xxxxxx x xxxxxxx xx xx xxxxx x xxxx xxxxxx xxxxxxxxxxx xxxxxx po dobu 48 x. Xxxxx xxxxxxxx by měl xxx xxxxxxxxx. Pevné xxxxx xx xxxxx xxxxxxxx x vpraví xx xxxxxxxx xxxxxxxx. Xxxxxxxx lze aplikovat xxxxx, je-li to xxxxxx.
6. – 8. xxx – xxxxxxxxx xxxxxxx
Xxxxxxxx xxxxxx xx xxxx xxxxx xxxxx. Xx xxxxxxxx plochu xx podobným xxxxxxxx xxxxxx xxxxxxx xxxxxxxxx x udržuje xx xx xxxxx x xxxx pomocí xxxxxxxxxxx xxxxxx xx xxxx 48 x.
1.5.1.3.2 Xxxxxxxxx
20. – 22. xxx – experimentální x xxxxxxxxx skupiny
Boky xxxxxxxxx x kontrolních xxxxxx xx xxxxx srsti. Xx jeden xxx xxxxxxx xx aplikuje xxxxxxxx xxxxx x xxxxxx nebo x xxxxxxx x xx xxxxx xxx xx xxxx xxxxxxxxx umístit xxxxxx xxxx komůrka xxxxxxxxxx xxxxx xxxxxxxxx. Xxxxxx se xxxxxx xx xxxxx x xxxx xxxxxx okluzivního xxxxxx xx xxxx 24 h.
1.5.1.3.3 Pozorování x xxxxxxxxx: xxxxxxxxxxxxxx x xxxxxxxxx xxxxxxx
- xxxxxxxxx 21 h xx odstranění xxxxxx xx xxxxxxxxxx xxxxxx xxxxxx, xxxxxxxx xxxxxxx x/xxxx xxxxx x x případě xxxxxxx xxxxxxxx;
- xxxxxxxxx xx 3 x (xxxxxxxxx 48 x xx xxxxxxx aplikace xxxxxxxxxx xxxxx) xx pozoruje xxxxx xxxxxx a xxxxxxxxx xx xxxxx xxxxxxxx xxxxxxx x xxxxxxx;
- přibližně 24 x po xxxxx xxxxxxxxxx xx xxxxxxx xxxxx xxxxxxxxxx (72 x) x opět xx xxxxxxxxx xxxxxx xxxx.
Xxxxxxxxxx se xxxxxxxx xxxxxxxxxx "xxxxxxx" x xxxxxxxxx x xxxxxxxxxxx xxxxxx.
Xxxxx xx to xxxxxxxx xxx xxxxxxxxx xxxxxxxx získaných xxx xxxxx provokaci, měla xx xxx xxxxxxxxx xxxxx týden xx xxxxx provokaci xxxxxxx xxxxx xxxxxxxxx (xx. xxxxxxxxx provokace), x xxxxxxx xxxxxxx x xxxxx kontrolní skupinou. Xxxxxxxxx xxxxxxxxx xxxx xxx provedena také xx xxxxxxx kontrolní xxxxxxx.
Xxxxxxxxxx x xxxxxxxxxxxxx xxxxx xxxxxxx reakcí x xxxxxxxxxxx nálezů, xxxxxx systémových xxxxxx, xxxxx xxxx důsledkem xxxxxxxxxx x provokačních xxxxxxx, xx měla xxx xxxxxxxxx xxxxx xxxxxxxx Magnussona/Kligmana (xxx xxxxxxx). Pro objasnění xxxxxxxxx xxxxxx mohou xxx xxxxxxxxx jiné xxxxxxx, xxxx. xxxxxxxxxxxxxxxx xxxxxxxxx nebo xxxxxx xxxxxxxx xxxxx xxxx.
1.5.2 Xüxxxxxxx xxxxxxx
1.5.2.1 Xxxxxxxx
Xxxxxx xxxxx xxxxxxx xxxxxxxxxxx xxxxxxx se xxxxxxxxxxxx xx laboratorní podmínky xxxxxxx 5 dnů xxxx xxxxxxxxx zkoušky. Xxxx zkouškou xx xxxxxxx náhodný výběr xxxxxx x zvířata xx xxxxxxx xx xxxxxxxxxxxxxxxx a xxxxxxxxxxx xxxxxx. Xxxx xx xxxxxxxx xxxxxxxxx, xxxxxxx xxxx chemickou depilací, x xxxxxxxxxx xx xxxxxxx xxxxxxxx xxxxxx. Xx xxxxx xxxx xx to, xxx xxxxxxx x xxxxxxxxx xxxx. Xxxxxxx se xxxxx xxxx zahájením xxxxxxx a xx xxxxx xxxxxxx.
1.5.2.2 Xxxxxxxx xxxxxxxx
1.5.2.2.1 Xxxxxxx xxxxxxx
Xxxxxxxxx xx xxxxx používané xxxxxxxxxxx kmeny albinotických xxxxxx.
1.5.2.2.2 Xxxxx x xxxxxxx
Xxxxxx xxx xxxxx x xxxxxx. Xxxxxxx xxxxxx xxxx být xxxxxxxxx x xxxxx xxx březí.
Experimentální skupina xx xxxxxx xxxxxxx x 20 zvířat x xxxxxxxxx xxxxxxx xxxxxxx x 10 xxxxxx.
1.5.2.2.3 Úrovně xxxxx
Xxxxxxxxxxx xxxxxxxx xxxxx xxxxxxx xxx xxxxxx xxxxxxxx xxxxxxxx by xxxx xxx xxx xxxxxxxx xxxxxxxxxxx, xxxxx xxxxxx xxxxx, xx však xxxxx podráždění xxxx. Xxxxxxxxxxx použitá xxx xxxxxxxxxx xxxxxxxx by xxxx odpovídat nejvyšší xxxxxxxxxxx, xxxxx nevyvolává xxxxxxxxxx. X xxxxxxx xxxxxxx xxxxx být xxxxxx xxxxxxxxxxx stanoveny xxxxxxxxxx xxxxxxx xx xxxx xxxx xxxxx xxxxxxxxx.
Xxx zkoušené xxxxx xxxxxxxxx ve xxxx xx vhodné xxxxxxxx xxxx vehikulum xxxx xxxx nedráždivé xxxxxxx xxxxxxx xxxxxxxxx xxxxxxx xxxxx. Xxx ostatní xxxxxxxx látky xx xxxxxxxxxxxxx xxxxxx 80 % alkoholu ve xxxx pro xxxxxxx x xxxxxx xxx xxxxxxxxx.
1.5.2.3 Xxxxxx
1.5.2.3.1 Xxxxxxx
Xxx 0 – experimentální xxxxxxx
Xxxxx xxx se xxxxx xxxxx (xxxxxxxx xx ostříhá). Zkušební xxxxxx xx xxx xxx xxxxxxxx napuštěn xxxxxxxxx látkou xx xxxxxxx xxxxxxxx (xxxxx xxxxxxxx xxxx být xxxxxxxxx; tekuté xxxxxxxx xxxxx xxxxx xxx xxxxx xxxxxxx xxxxxxxxxx xxxxxxxx).
Xxxxxxxx xxxxxx xx xxxxxxx xx xxxxxxxx xxxxxx a xx xxxx 6 h xx xxxxxxx xx xxxxx x kůží xxxxxxxxxx xxxxxxx xxxx xxxxxxxx x xxxxxxx xxxxxxx.
Xxxxxx x plátkem xxxx xxx xxxxxxxxx. Xxxxxx xx xxxxxxxx xxxxxxxxx, xxxx být xxxxxxx nebo čtvercový, xxx měl by xxx velikost xxxxxxxxx 4 – 6 xx2. Xxx xxxxxxxxx xxxxxx xx vhodné xxxxxx xxxxxxx xxxxxx. Xxxx-xx xxxxxxx obvazy, xxxxx xxx xxxxxxxx xxxxxxxxx expozice.
Den 0 – xxxxxxxxx xxxxxxx
Xxxxx xxx xx xxxxx xxxxx (xxxxxxxx xx xxxxxxx). Xx xxxxxxxx xxxxxx xx xxxxxx xxxxxxxxx podobným xxxxxxxx xxxx x xxxxxxxxxxxxxx xxxxxxx. Zkušební xxxxxx xx xx xxxx 6 x xxxxxxx xx xxxxx s xxxx pomocí xxxxxxxxxxx xxxxxx xxxx xxxxxxx x xxxxxxxx xxxxxx. Xxxxx je xxxxx xxxxxxxx, xx xxxxxxxxx xxxxxxx xxxxxxxxx negativní xxxxxxxx xxxx nezbytná, xxx xxxxxx xxxxxxxxxxxxx xxxxxxxxx xxxxxxx.
6. – 8. x 13. – 15. den – xxxxxxxxxxxxxx x xxxxxxxxx xxxxxxx
Xxxxxxx xx xxxxxx xxxxxxxx xxxx x xxx 0 xx stejnou xxxxxxxx xxxxxx (v xxxxxxx xxxxxxx xxxxxxxx srsti) xx tentýž xxx, x xx 6. – 8. xxx x opět 13. – 15. xxx.
1.5.2.3.2 Xxxxxxxxx
27. – 29. xxx – xxxxxxxxxxxxxx x xxxxxxxxx xxxxxxx
Xxxxxxxxxx xxx pokusných x xxxxxxxxxxx xxxxxx xx xxxxx srsti (xxxxxxxx xx xxxxxxx). Xxxxxxxxx xxxxxx xxxx xxxxxxx xxxxxxxxxx příslušné xxxxxxxx xxxxxxxx látky x xxxxxxxx nedráždivé xxxxxxxxxxx xx xxxxxxxx xx xxxxx xxxx xxxxxxxxxxxx xxxx pokusných x xxxxxxxxxxx xxxxxx.
Xx xxxxxx xxxx xxxxxxxxxxxx xxxx xxxxxxxxx x xxxxxxxxxxx xxxxxx xx xxxxxxxxx xxxxxxxx okluzivní xxxxxx xxxx komůrka xxx x xxxxxxxxx. Xxxxxx xxxx komůrky se xx xxxx 6 x xxxxxx ve xxxxx x xxxx xxxxxx vhodného xxxxxx.
1.5.2.3.3 Xxxxxxxxxx x hodnocení
- Xxxxxxxxx 21 x xx xxxxxxxxxx xxxxxx xx xxxxxxxxxx xxxxxx xxxxx xxxxx;
- xxxxxxxxx xx xxxxx xxxxxxxx (xxxxxxxxx 30 x xx xxxxxxxx xxxxxxxxxxxx xxxxxx) se pozorují xxxxx reakce x xxxxxxxxxxx xx xxxxx xxxxxxxx xxxxxxx x xxxxxxx;
- xxxxxxxxx 24 x xx 30xxxxxxxxx xxxxxxxxxx (xxxxxxxxx 54 x po xxxxxxxx xxxxxxxxxxxx plátku) xx xxxx xxxxxxxx xxxxx xxxxxx x xxxxxxxxxxx xx.
Xxxxxxxxxx se xxxxxxxx xxxxxxxxxx "xxxxxxx" x xxxxxxxxx i xxxxxxxxxxx xxxxxx.
Xxxxx xx xx xxxxxxxx pro objasnění xxxxxxxx xxxxxxxxx xxx xxxxx xxxxxxxxx, měla xx být xxxxxxxxx xxxxx xxxxx xx xxxxx xxxxxxxxx xxxxxxx xxxxx xxxxxxxxx (xx. xxxxxxxxx provokace), x xxxxxxx xxxxxxx x xxxxx xxxxxxxxx xxxxxxxx. Xxxxxxxxx xxxxxxxxx xxxx xxx provedena xxxx xx xxxxxxx kontrolní xxxxxxx.
Xxxxxxxxxx x xxxxxxxxxxxxx xxxxx xxxxxxx xxxxxx x xxxxxxxxxxx xxxxxx, xxxxxx xxxxxxxxxxx reakcí, xxxxx jsou důsledkem xxxxxxxxxx a xxxxxxxxxxxx xxxxxxx, xx měla xxx prováděna xxxxx xxxxxxxx Xxxxxxxxxx/Xxxxxxxx (viz xxxxxxx). Pro xxxxxxxxx xxxxxxxx xxxxxx xxxxx xxx xxxxxxxxx xxxx xxxxxxx, xxxx. xxxxxxxxxxxxxxxx xxxxxxxxx nebo xxxxxx xxxxxxxx xxxxx xxxx.
2. XXXXX (XXXX X XÜXXXXXXX XXXXXXX)
Xxxxx xx xxxxxx do xxxxxxx, xxxxxxx se xxx xxxxx zvíře xxxxxx xxxxx xxxxxx xxx xxxxxx pozorování.
3. XXXXXX (XXXX X XÜXXXXXXX XXXXXXX)
Xxxxx xxxx xxxx xxxxxxxx xx xxxxxxxxx xxxxxxxxx screeningová zkouška (xxxx. xxxxxxx xxxxxxxxxxxx xxxxxxxxxxxx xxxxx (XXXX), xxxxxxx ztluštění ucha x myší (XXXX)), xxxx xxx s xxxxxxxx xxxxxxxxx xx xxxxxxxxxx a referenčními xxxxxxx xxxxxx xxxxx xxxx xxxxxxx xxxx xxxxx na xxxx xxxxxxx, xxxxxx xxxxxxxxxx xxxxxxxxx x postupu.
Protokol x xxxxxxx (XXXX x Bühlerova xxxxxxx)
Xxxxxxxx x xxxxxxx má xxxxx xxxxx xxxxxxxxx xxxx xxxxxxxxx:
Xxxxxxx zvířata
- xxxxxxx kmen xxxxxx;
- xxxxx, stáří a xxxxxxx xxxxxx;
- původ, xxxxxxxx xxxxx, xxxxxx xxx.;
- xxxxxxxx xxxxxxxxxxxx xxxxxx na začátku xxxxxxx.
Xxxxxxxx xxxxxxxx:
- technika xxxxxxxx xxxxx xxxxxxxx;
- xxxxxxxx xxxxxxxxx o xxxxxxxxxxx použitých xxx xxxxxxxx a technice xxxxxxxx;
- výsledek předběžné xxxxxx x závěr xxxxxxxx xx xxxxxxxxxx x xxxxxxxxxxxx koncentrací, xxxxx xxxx xxx xxxxxxx xxxxxxx;
- xxxxxxxx xxxxx x xxxxxxxx, xxxxxxxx x xxxxxxxxxx xxxxxxxx látky;
- zdůvodnění xxxxx vehikula,
- xxxxxxxxxxx xxxxxxxx x xxxxxxxx xxxxx použité xxx xxxxxxxx x provokační xxxxxxxx a xxxxxxx xxxxxxxx látky xxxxxxx xxx xxxxxxx a xxxxxxxxx.
Xxxxxxxx:
- xxxxxx xxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxxx x spolehlivosti (viz 1.3), včetně informací x použité xxxxx, xxxxxxxxxxx x vehikulu;
- xxxxxxxxxx xxxxxxxxxxxx xxxxxx, xxxxxx xxxxxxx klasifikace;
- xxxxxxxx xxxxx charakteru x stupně pozorovaných xxxxxx;
- všechny xxxxxxxxxxxxxxxx xxxxxx.
Xxxxxx xxxxxxxx.
Xxxxxx.
4. LITERATURA
Metoda xx xxxxxxxxxx xxxxxx XXXX TG 406.
Xxxxxxx
XXXXXXX:
Xxxxxxxx Xxxxxxxxxx/Xxxxxxxx pro xxxxxxxxx xxxxxxx xxxxxx xx xxxxxxxxxx xxxxxxxx
|
0 = |
žádná xxxxxxxxx xxxxx | |
|
1 = |
xxxxx xxxx skvrnité xxxxxxxxx xxxx |
|
2 = |
xxxxx x splývající xxxxxxxxx xxxx |
|
3 = |
intenzivní zarudnutí x xxxxxxx xxxx" |
XXXXXXX XX D
" X.7 XXXXXX TOXICITA (28XXXXX XXXXXXXXX XXXXXXXX)
1. XXXXXX
1.1 Úvod
Viz xxxxxx xxxx, xxxx X.
1.2 Xxxxxxxx
Xxx xxxxxx xxxx, xxxx X.
1.3 Xxxxxxxx xxxxxxxx xxxxxx
Xxxxxxxx látka xx denně orálně xxxxxx v xxxxxxxxxxxxxx xxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx zvířat; xxxxx xxxxxxx xx xxxxxx xxxxx úroveň xxxxx 28 dnů. X xxxxxxx xxxxxx podávání xx xxxxxxx xxxxx xxx pečlivě pozorují, xxx se zjistily xxxxxxxx xxxxxxxx. Xxxxxxx, xxxxx x xxxxxxx xxxxxxx xxxxxxx xxxx xxxx xxxxxxxx, i xxxxxxx, xxxxx xx xxxxx zkoušky xxxxxxx, xx xxxxxxx.
Xxxx xxxxxx xxxxx větší xxxxx xx neurologické xxxxxx xxxx xx specifické xxxxxxxx účinky; xxxxx xx xxxxxx xx xxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxxx, xxx xxxx xxxxxxx xx xxxxxxx xxxxxxxxx. Xxxxxx xx xxxx odhalit xxxxxxxx xxxxx x xxxxxxxxxxxxx potenciálem, x xxxxx může xxx xxxxxxxx xxxxx xxxxxx xxxxxxxx tohoto aspektu. Xxxxxx xxxx xxxxxxxxx xx imunologické xxxxxx x toxicitu xxx xxxxxxxxxxx xxxxxx.
1.4 Xxxxx xxxxxxxx xxxxxx
1.4.1 Xxxxxxxx
Xxxxxx xxxxx xxxxxxx xxxxxxx xx náhodně xxxxxxx xx xxxxxxxxxxx x xxxxxxxxxxxxxxxx skupin. Klece xx xxxx xxx xxxxxxxxxx xxx, xxx xxx xxxx umístění xxxxx xxxxxxxxxxxxx. Jednotlivá xxxxxxx xx xxxxxxxxxxx xxxxxxxxxxxx x xxxxxx xx xx klecí xxxxxxx xxx dnů xxxx začátkem xxxxxx, xxx si mohla xxxxxxxx xx xxxxxxxxxxx xxxxxxxx.
Xxxxxxxx látka xx xxxxxx xxxxxx xxxx x potravě či x pitné xxxx. Xxxxxx xxxxxxxx xxxxxx xxxxxx xx účelu xxxxxx x xx xxxxxxxxx-xxxxxxxxxx xxxxxxxxxxxx látky.
Zkoušená xxxxx se podle xxxxxxx xxxxxxxx xxxx xxxxxxxxxx ve xxxxxxx xxxxxxxx. Je-li xx xxxxx, xxxxxxxxxx xx xxxxxx použití xxxxxxx xxxxxxx/xxxxxxxx, xxxxx použití xxxxxxx/xxxxxx x xxxxx (xxxx. kukuřičný olej) x xxxxxxx xxxxxxx x jiných vehikulech. Xxx xxxxxxx xxxxxxxx xx xxxx xxx xxxxx xxxxxx toxická xxxxxxxxxxxxxxx. Xxxx xx xxx xxxxxx xxxxxxx xxxxxxxx látky xx xxxxxxxx.
1.4.2 Xxxxxxxx xxxxxxxx
1.4.2.1 Xxxxxxx zvířata
Dává xx xxxxxxxx xxxxxxxx, xxx xxx použít x xxxxxx xxxxx xxxxxxxx. Xxxxxxx by měly xxx xxxxx xxxxxxxxx xxxxx mladých xxxxxxxx xxxxxxxxx xxxxxx. Xxxxxx xxxx být nullipary x xxxxx xxx xxxxx. Xxxxxxxx látky xx xxxx xxxxx xx xxxxxxxx po xxxxxxxxx x v xxxxxx xxxxxxx xxxxx, xxx zvířata xxxxxxxx xxxxx xxxxxx týdnů.
Na xxxxxxx xxxxxx xx xxxx xxx xxxxxxxx xxxxxxxxx xxxxxx xxxxxxxxx x xxxxxx by xxxxxxxxx ±20 % xxxxxxx xxxxxxxxx xxx xxxxx xxxxxxx.
Xxxxxxx-xx xx xxxxxx opakovaného xxxxxxxx xxxxxxxx xxxxx xxxx xxxxxxxxx studie xxx xxxxxxxxxxx xxxxxx, měla xx xxx x xxxx xxxxxxxx xxxxxxx xxxxxxx xxxxxxx stejného xxxxx x xxxxxxxx xxxxxx.
1.4.2.2 Počet x xxxxxxx
Xxx každou xxxxxx xxxxx xx xxxxxxx xxxxxxx 10 xxxxxx (xxx samic x xxx samců). Xxxxx xx budou zvířata xxxxxxxxx v xxxxxxx xxxxxx, je xxxxx xxxxxx xxxxxxx xxxxx xxxxxx x počet xxxxxx, xxxxx budou xxxxxxxx xxxx xxxxxx xxxxxx.
Xxxxx xxxx xxxx xxx xxxxxxxxx xxxxxxx 10 xxxxxx (xxx xxxxxx xxxxxxx pohlaví) xxxxxxxx vysoká úroveň xxxxx xx dobu 28 xxx x 14 xxx po xxxxxxxx xx xxxxxxxx xxxxxxxx, přetrvávání xxxx xxxxxxxx výskyt xxxxxxxxx xxxxxx. Xxxxxxx xx xxxx satelitní skupina 10 xxxxxxxxxxx xxxxxx (xxx xxxxxx xxxxxxx xxxxxxx).
1.4.2.3 Xxxxxx dávek
Obecně xx xxxx xxx xxxxxxx xxxxxxx xxx xxxxxxxxxxxxxx xxxxxxx x xxxxx kontrolní xxxxxxx. X xxxxxxxx xxxxxxxx xxxxxxxx xxxxx xx xx xxxxxxx x xxxxxxxxx xxxxxxx xxxxxxx xxxxxx jako xx xxxxxxx x xxxxxxxxxxxxxx xxxxxxx. Pokud se xxx xxxxxxxx xxxxxxxx xxxxx xxxxxxx xxxxxxxxx, xxxxxx xx xxxxxxxxx xxxxxxx x nejvyšším xxxxxxxx objemu.
Pokud xx xx posouzení xxxxxx xxxxx neočekávají žádné xxxxxx xxx dávce 1000 mg na xx xxxxxxx hmotnosti, xxxx být provedena xxxxxxx zkouška. Xxxxxx-xx xxxxxxxx xxxxx xxxxxx xxxxx, může xxx xxxxxxxxx předběžná xxxxxx xxx xxxxxxxxx xxxxxxx xxxxx, které xxxx xxx xxxxxxx.
Xxx xxxxxx xxxxxx xxxxx xx xxxx xxx xxxxxxxxxx xxxxxxx existující xxxxx x xxxxxxxxx x xxxxxxxxxxxxxxxxx xxxxxxxxxxxx, xxxxx xxxx xxx zkoušenou xxxxx nebo xxxxxxxx xxxxxxxxx xxxxxxxx. Nejvyšší xxxxxx dávky má xxxxxxx xxxxxxx xxxxxx, xx xxxx uhynutí xxxx xxxxx xxxxxxx. Xxxx xx xxxx xxx xxxxxxx xxxxxxxx xxxx úrovní dávek x xxxxx xxxxxxxx xxxxxx související x xxxxxx x xxxxxxxxxxxx xxxxxxxxxxxx xxxxxx xxx xxxxxxxx úrovni xxxxx (XXXXX). Xxxxx xx xxx xxxxxxxxx xxxxxxxxxx xxxxxx xxxxx xxxxxxxxx xxxx- xx xxxxxxxxxxx xxxxxxxx mezi xxxxxxx x xx vhodnější xxxxxx xxxxxxx xxxxxxxxxxxxxx xxxxxxx, než použít xxxxx xxxxx xxxxxxxxx (xxxxxxxxxxxx xxxx. xxxxxxx xxxxxxx xxx 10).
X xxxxx podávaných v xxxxxxx xxxx x xxxxx xxxx je xxxxxxxx xxxxxxxx, xxx xxxxxxxx xxxxxxx xxxxxxxx xxxxx neovlivňovalo normální xxxxxx nebo xxxxx xxxxxxxxx. Podává-li xx xxxxxxxx látka x xxxxxxx, xxxx xx xxxxxx xxx xxxxxxxxxx xxxxxxxxxxx (x xxx) xxxx xxxxxxxxxx xxxxxxxxx xxxxxxxx x tělesné xxxxxxxxx xxxxxxx; xxxxxxx xxxxxxx xxxx xxx xxxxxxxxxxxxx. Xxxxxxxx-xx xx xxxxx sondou, mělo xx xx tak xxxx xxxxx xxx xxxxxxxxx ve stejnou xxxx, x xxxxxxxxx xx mělo xxx xxxxx xxxxxxx xxxxxxxx xxx, aby bylo xxxxxxxxxx xxxxxxxx x xxxxxxx xxxxxxxxx zvířete.
Pokud xx xxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxxx jako xxxxxxxxx xxxxxx x xxxxxxxxxx xxxxxx, měla xx být x xxxx xxxxxxxx xxxxxxx xxxxxx xxxxxxx.
1.4.2.4 Limitní xxxxxxx
Xxxxx xxxxxxx xxxxxxxxx xxxxx xxxxxxx xxxxxxxxx x xxxx xxxxxx xxx xxxxx xxxxx xxxxxxx 1000 xx xx xx xxxxxxx xxxxxxxxx xx xxx xxxx x xxxxxxx xxxxxxxx v xxxxxxx xxxx x xxxxx xxxx x xxxxxxxxxxxx xxxxxxxxxxx (xx základě xxxxxxxxx xxxxxxx xxxxxxxxx) xxxxxxxx xxxxxxxxxxxxx xxxxxxx xxxxxx x xxxxx xx xx xxxxxxx xxxxx x xxxxxxx x xxxxxxxx xxxxxxxxxx xxxxxxxxxxxxx xxxxxxxx, xxxx xxxxx xxxxxx za xxxxxxx xxx úrovní xxxxx xxxxx. Xxxxxxx xxxxxxx xx použije x výjimkou případu, xxx údaje x xxxxxxxx xxxxxxx xxxxxxxxx, xx xx xxxxxxxx xxxxxxx xxxxx xxxxxx xxxxx.
1.4.2.5 Xxxx xxxxxxxxxx
Xxxx xxxxxxxxxx xx xxxx xxx 28 xxx. Xxxxxxx v xxxxxxxxx xxxxxxx určené xxx xxxxxxxx xxxxxxxxxx by xxxx být po xxxxxxx xxxxxxx 14 xxx xxx aplikace, xxx se xxxxxxxx xxxxxxxx xxxxxx, xxxxxxxxxxx xxxx xxxxxxxx z xxxxxxxxx účinků.
1.4.3 Postup
Zkoušená xxxxx xx podává xxxxxxxx xxxx xxx x xxxxx po xxxx 28 xxx. Xxxxx xx látka xxxxxx xxx dnů x týdnu, musí xx být xxxxxxxxxx. Xxxxx xx xxxxxxxx xxxxx podává xxxxxx, xxxxxx se xxxxxxxx x jediné xxxxx xx xxxxxxx xxxxxxxxx xxxxx xxxx xxxxxx xxxxxxxxx kanyly. Xxxxxxxxx xxxxx xxxxxxxx, xxxxx xxx xxxxx xxxxxxxx, xxxxxx xx velikosti xxxxxxxxx zvířete. Objem xx xxxxx překročit 1 ml xx 100 g xxxxxxx xxxxxxxxx, x výjimkou xxxxxxx roztoků, xxx xxx použít 2 xx xx 100 x xxxxxxx xxxxxxxxx. X xxxxxxxx xxxxxxxxxx xxxx xxxxxxxx xxxxx, x xxxxxxx se xx xxxxxxx koncentracích xxxxxxxx xxxxxx, xx xxxx xxx rozdíly xx xxxxxxxxx objemu xxxxxxxxxxxxxx xxxxxxx xxxxxxxxxxx xxx, xxx xxx xxx xxxxx xxxxxxxx xxxxx podáván konstantní xxxxx.
1.4.3.1 Obecná xxxxxxxxxx
Xxxxxxxxx xxxxxxxx pozorování xx xx mělo xxxxxxxx xxxxxxx xxxxxx denně, xxxxxxx xx stejnou xxxx (xxxxxx xxxx) x x xxxxxxxx xxxx xxxxxxxxxxx maxima xxxxxx po xxxxxx xxxxx. Xxxxxxxxxxx se xxxxxxxxx xxxx zvířat. Xxxxxxx xxxxxxx denně xx xxxxxxx xxxxxxxxx xxxxx zvířat za xxxxxx xxxxxxxx xxxxxxxxx x xxxxxxxxx. Xxxxxxx x agónii x xxxxxxx, xxxxx xx xxxxx xxxx trpí xxxxxxx, xx xxxxx xxxxxx, xxxxxxx utratí x xxxxxxx.
Xxxx xxxxxx xxxxxxx xxxxx x xxxx xxxxxxx xxxxxx xxxxx xx xxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx xxxxx xxxxxx (xx xxxxxx xxxxxxxxxxxxxx xxxxxxxxx). Xxxx xxxxxxxxxx xx xx xxxx provádět xxxx xxxxxxx xxxx xx standardním xxxxxxxxxxx xxxxxxxx a nejlépe xxxxxxx ve xxxxxxx xxxx. Xxxxxxxxxx xx xxxx xxx pečlivě xxxxxxxxxxxxx, xxxxxxx xx xxxxxxx systému bodování xxxxxxxxxx xxxxxxxxxxxx xx xxxxxxxx laboratoři. Xxxx xx se xxxxxxxx x xx, xxx xxxx xxxxxxx xx xxxxxxxxxx xxxxxxxxxx co xxxxxxxx x xxx xxxxxxxxx xxxxxxxxx xxxxxxx xxxxx, xxxxx xxxxxx x zařazení xx xxxxxxx informovány. Xxxxxxxxx xx xxxx xxxx xxxx zahrnovat xxxxx xxxx, srsti, očí x xxxxxxx, výskyt xxxxxxx x xxxxxxx x vegetativních xxxxxx (xxxxxx, xxxxxxx xxxxx, xxxxxxxx zornic, nezvyklé xxxxxxx). Zaznamenávat by xx měly změny xxxxx, polohy a xxxxxx xx xxxxxxxxxx, xxxx xxxxxxxxxx xxxxxxxxxx x tonických xxxxxx, xxxxxxxxxx x chování (xxxx. xxxxxxxxxx čistících xxxxxx xxxx opakovaného xxxxxxxx) xxxx bizarního xxxxxxx (xxxx. sebepoškozování, xxxxxx xxxxxxxx).
Xx xxxxxxx xxxxx podávání xxxxx xx otestují xxxxxx xx různé smyslové xxxxxxx (např. sluchové, xxxxxxx, proprioceptivní) x xxxxx xx síla xxxxxx x xxxxxxxxx xxxxxxxx. Xxxxx xxxxxxxx xxxxxxxxx o postupech, xxxxx xx xxxxx xxxxxx, xxxx uvedeny x xxxxxxxxxx (xxx xxxxxx xxxx, xxxx X).
Xxxxxxxxxx xxxxxxxxx xxxxxx xx xxxxxxx xxxxx xxxxxxxx xxxxx xxx xxxxxxxx xxxxxxxx, pokud xx xxxxxx xxxxxxxxx xxxx předběžná xxx xxxxxxxxx xxxxxxxxxxxxx (90xxxxx) xxxxxx. X takovém xxxxxxx xx xxxxxxxxxx xxxxxxxxx poruch zahrnuto xx xxxxxxxxxx studie. Xxxxxxxxxx údajů o xxxxxxxxxxxx xxxxxxxxx xxxxxxxxx xx xxxxxx xxxxxxxxxxx xxxxxxxx xxxxx xxxx xx druhé xxxxxx xxxxxxxx xxxxx xxxxxx xxxxx xxx xxxxxxxxx xxxxxxxxxxxxx xxxxxx.
Xxxxxxxxxx funkčních xxxxxx xxx xxxxxxxxx xxxxxxxx x skupin, xxxxx xxxxxxxx xxxxxxxx xxxxxxxx x xxxxxx xxxx, xx xx xxxxxxx xxxxxxxx xxxxxxxx xxxxxx xxxxxxx xxxx.
1.4.3.2 Xxxxxxx xxxxxxxx a xxxxxxxx xxxxxxx/xxxx
Xxxxxxx xxxxxxx xx xx xxxx xxxxxxx xxxxxx xxxxx xxxxxx. Xxxxxx xxxxxxxx xxxxxxx x xxxx xx xx xxxx xxxxxxxx xxxxxxx xxxxxx xxxxx. Pokud se xxxxx xxxxxx x xxxxx vodě, xxxx xx xx xxxxxxx xxxxxx týdně xxxxx xxxxxxxx xxxx.
1.4.3.3 Xxxxxxxxxxxxx xxxxxxxxx
Xx konci zkoušky xx xxxx xxx xxxxxxxxx tato hematologická xxxxxxxxx: stanovení xxxxxxxxxxx, xxxxxxxxxxx xxxxxxxxxxx, xxxxx xxxxxxxxxx, xxxxxxxxx x xxxxxxxxxxxxxxx počtu xxxxxxxxx, xxxxx xxxxxxxxxx a xxxxxxx xx protrombinový xxx.
Xxxxxx vzorky xx xx xxxx xxxxxxxx x xxxxxxxx xxxxx xxxxx před xxxxxxxxx xxxxxx xxxx x xxxx průběhu x xxxx xx xx xxxxxxxxx xx xxxxxxxx xxxxxxxx.
1.4.3.4 Xxxxxxxx xxxxxxxxxxx xxxxxxxxx
Xxxxxxxx xxxxxxxxxxx analýzy xx xxxxxx vyšetření xxxxxxxx xxxxxxxxx xxxxxx xx xxxxx x xxxxxxx na xxxxx x xxxxxxx xx xxxxxxxx na xxxxxxxx xxxxxxxx xxxxxxxxxx xxxx xxxxxxxx před utracením xxxx x jeho xxxxxxx (kromě xxxxxx xxxxxxxxxx x xxxxxx x/xxxx zvířat utracených x xxxxxxx xxxxxxx). Xxxx xxxxxxxxx xxxxxxxx xxxxxx se doporučuje xxxxxxxx xxxxxxx přes xxx xxx xxxxxxx [1].Xxxxxxxxx plazmy a xxxx xxxxxxxx xxxxxxxxx xxxxxx, xxxxxxxx, xxxxxxx, xxxxxxxxx xxxxxxxxxxxx, xxxxxxxx, xxxxxxxxxx, xxxxxxxxx xxxxxxxx x albuminu, xxxxxxx xxxx xxxxxx xxxxxxxxxxxx xxxxxx na xxxxxxx xxxxx (jako alaninaminotransferasa, xxxxxxxxxxxxxxxxxxxxxxxx, alkalická fosfatasa, xxxx xxxxxxxxxxxxxxxxxxxxxx a xxxxxxxxxxxxxxxxxxxxx). Stanovení xxxxxxx xxxxxx (xxxxxxxxx xxxx xxxxxx xxxxxx) a xxxxxxxxx xxxxxxx xxxx xx určitých okolností xxxxxxxxxx užitečné xxxxxxxxx.
Xxxx xx možné x xxxxxxx xxxxxxxxxx xxxxx xxxxxx provést xxxxxxxxxxx xxxxxxx xxxx za xxxxxxx xxxxxx xxxxxxxxxxxx xxxxx: vzhled, objem, xxxxxxxxxx nebo xxxxxxxxxx xxxxxxxx, xX, bílkoviny, xxxxxxx x xxxx/xxxxxxx.
Xxxx xx xx xxxx xxxxxx vyšetření xxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxx x xxxx. Xxxxx xxxxxxxxx xx xxxx xxx provedeno, xxxxx xxxxx známé xxxxxxxxxx xxxxxxxx xxxxx xxxxxxxx xxxxxxxxxxxx xxxxxxxxxxx xxxxxxx, xxxxxx xxxxxxx, xxxxxxx, xxxxxxxxxxxx xx lačno, xxxxxxxxxxxx xxxxxxx, methemoglobinu x xxxxxxxxxxxxxx. Tyto xxxxxxx xx třeba xxxxxxxxxxxxx pro xxxxx xxxxxxxx skupin nebo xxxxxx xx xxxxxxx.
Xxxxxx xx třeba postupovat xxxxxx v závislosti xx xxxxx x xx xxxxxxxxxxxx x/xxxx xxxxxxxxxxxxxxx účincích dané xxxxx.
Xxxxx xxxxxx xxxxx x xxxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxxxx, xxxx xx xx xxxxxx xxxxxxxxx hematologických x xxxxxxxxxx xxxxxxxxxxxxx xxxxxxxxx xxxx xxxxxxxx xxxxxxx.
1.4.3.5 Xxxxx
X xxxxx xxxxxxxxx xxxxxx xxxxxxxxxx xx xxxxxx xx xxxx xxx provedena xxxxxxx, xxxxxxxx xxxxx, zahrnující xxxxxxx xxxxxxxx xxxxxxxx xxxxxxx xxxx, xxxxx xxxxxx x xxxxxx xxxxxxx, xxxxxx a xxxxxx a xxxxxx xxxxxx. Xxxxx, xxxxxxx, xxxxxxxxxxx, xxxxxxx, xxxxxxxxxx, xxxxxx, xxxxxxx, xxxxx x xxxxx všech xxxxxx xx měly xxx xxxxxxx všech xxxxxxxx tkání x xx xxxxxxxx xx xxxxx xx ve xxxxxx xxxxx zváží, xxx nedošlo k xxxxxxxxx.
Xxxxxxxxxxx tkáně xx xxxx xxx xxxxxxxxxx x xxxxxxxxxxxxx fixačním xxxxx x xxxxxxx xx xxx xxxxx x xxxxxxxxx xxxxxxxx xxxxxxxxxxxxxxxx xxxxxxxxx: xxxxxxx xxxxx x xxxxxx, xxxxx (reprezentativní xxxxxxx, xxxxxx xxxxxxxx, xxxxxxx x xxxxx), xxxxx, xxxxxxx, xxxxx i xxxxxx střevo (xxxxxx Xxxxxxxxxx xxxxx), xxxxx, xxxxxxx, xxxxxxxxxxx, xxxxxxx, xxxxx, xxxxxx, xxxxxx xxxxx, průdušnice x xxxxx (xxxxxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxx x xxxxxxxxx), xxxxxx x xxxxxxxx xxxxxxxx orgány (xxxx. děloha, xxxxxxxx), xxxxxx měchýř, xxxxxxxxxx xxxxxx (xxxxxxxxxx xxxxx xxx xxxxxx aplikace x xxxxx xxxxxxxx xxx pokrytí xxxxxxxxxxx xxxxxx), xxxxxxxxx xxxx (x. xxxxxxxxxxx nebo x. tibialis), xxxxxxx x xxxxxxxxx svalu, xxx kostní dřeně (xxxx čerstvý xxxxx x xxxxxx xxxxxx xxxxx). Podle xxxxxxxxxx xxxx jiných nálezů xxxx xxx xxxxxxxx xxxxxxx x xxxxx xxxxx. Xxxxxxx xxxxxx xxxxxxxxxx za xxxxx xxxxxx xxxxxx xxx xxxxxxxx xxxxxxxx látky xx xxxx být xxxxxxxx.
1.4.3.6 Xxxxxxxxxxxxxxxx xxxxxxxxx
X xxxxx xxxxxx kontrolní xxxxxxx x skupiny, xxxxx xxxx xxxxxx xxxxxx dávka, by xxxx xxx xxxxxxxxx xxxxxxx xxxxxxxxxxxx vyšetření xxxxxxxxxx xxxxxx x xxxxx. Toto vyšetření xx xxxx xxx xxxxxxxxx xx zvířata xxxxx xxxxxxxxx dávkových xxxxxx, pokud xxxx x xxxxxxx x xxxxxxx xxxxxx pozorovány xxxxx orgánů xxxxxxxx xxxxxxxxx xxxxxx.
Xxxxxxx xxxxxxxxxxxxx xxxx by xxxx xxx zkoumány.
V xxxxxxx xxxxxxx xxxxxxxxx skupiny xx mělo xxx xxxxxxxxx xxxxxxxxxxxxxxxx xxxxxxxxx xxxxx a xxxxxx, xx xxxxxxx byly xxxxxxxxxx účinky x xxxxxxxxxxxx skupin.
2. XXXXX
Xxxx xx být xxxxxxx xxxxx xxx xxxxx xxxxxxxxxx xxxxx. Xxxxx xx měly xxx xxxxxxx xxxxx xxxxxxx xx xxxxxxx, xxxxxxx xx xxxxx x xxxxx xxxxxxxxxxxxxx skupiny xxxxx xxxxxx xx xxxxxxx xxxxxxx, xxxxx xxxxxx xxxxxxxxxx xxxxxxxxx x xxxxxxx xxxxxxx xxxx utracených x xxxxxxxxx xxxxxx x xxxx xxxxx xxxx xxxxxxxxx utracení, xxxxx xxxxxx xxxxxxxxxxxx xxxxxxxx xxxxxxxx, xxxxx toxických xxxxxxxx, xxxxxx xxxx xxxxxxx, trvání x xxxxxxxxxx xxxxxxx xxxxxxxxx xxxxxx, xxxxx xxxxxx xxxxxxxxxxxx xxxx, xxx xxxx a procento xxxxxx xxxxxxxxxxxx xxxxx xxx léze.
Číselné výsledky xx měly být xxxxx xxxxx xxxxxxxxxxx xxxxxxx x xxxxxx xxxxxxxxx xxxxxxxxxxxx xxxxxxx. Xxxxxxxxxxx xxxxxx by xxxx xxx xxxxxxx xxx xxx xxxxxxxxx xxxxxx.
3. XXXXXX
Xxxxxxxx x xxxxxxx
Xxxxxxxx o zkoušce xx pokud xxxxx xxxxxxxxx tyto xxxxxxxxx:
Xxxxxxx xxxxxxx:
- xxxxxxx druh/kmen;
- xxxxx, xxxxx x xxxxxxx zvířat;
- xxxxx, xxxxxxxx xxxxx, xxxxxx xxx.;
- hmotnost jednotlivých xxxxxx na xxxxxxx xxxxxxx, xxxx v xxxxxxxxx xxxxxxxxxxx x xx konci xxxxxxx.
Xxxxxxxx xxxxxxxx:
- xxxxxxxxxx xxxxx xxxxxxxx, xxxx-xx použita xxxx;
- xxxxxxxxxx výběru xxxxxx xxxxx;
- podrobné xxxxx x složení xxxxx nebo úpravě xxxxxxx, x xxxxxxxx xxxxxxxxxxx, xxxxxxxx a xxxxxxxxxx přípravku;
- xxxxxxxx xxxxx x xxxxxxx xxxxxx zkoušené xxxxx;
- xxxxxxxxx přepočet xxxxxxxxxxx xxxxxxxx xxxxx x xxxxxxx/xxxxx xxxx (ppm) xx xxxxxxxxx xxxxx xxxxx (xx na xx xxxxxxx xxxxxxxxx);
- xxxxxxxx xxxxx x xxxxxx x xxxxxxx xxxx.
Xxxxxxxx:
- tělesná hmotnost/změny xxxxxxx hmotnosti;
- spotřeba xxxxxxx a xxxxxxxxx xxxxxxxx xxxx;
- údaje x xxxxxxxxx xxxxxxxx xxxxx xxxxxxx x xxxxxx dávky, včetně xxxxxxxx xxxxxxxx;
- xxxxxxxxx, xxxxxxxxx x xxxxxx xxxxxxxxxx projevů (xxx xxxx vratné xxxx xxxxxxxx);
- posouzení reaktivity xx xxxxxxxx xxxxxxx, xxxxxxxx xxxx x xxxxxxxxx xxxxxxxx;
- xxxxxxxxxxxxx xxxxxxxxx x xxxxxxxxxxx xxxxxxxxx hodnotami (xxxxxxx);
- xxxxxxxx biochemická xxxxxxxxx x příslušnými výchozími xxxxxxxxx;
- xxxxxxx xxxxxxxx xxx xxxxxxxx x xxxxx o xxxxxxxxx xxxxxx;
- xxxxxxx xxxxxx;
- xxxxxxxx popis xxxxx xxxxxxxxxxxxxxxxxx nálezů;
- údaje x xxxxxxxx, xxxxx xxxx xxxxxxxx;
- xxxxxxxxx xxxxxxxxxxx xxxxxxxxxx výsledků.
Rozbor xxxxxxxx.
Xxxxxx.
4. XXXXXXXXXX
Xxxxxx je xxxxxxxxxx xxxxxx OECD XX 407."
[1] Vyšetření xx lačno je xxxxxxx xxx xxxx xxxxxx x séru x xxxxxx, zvláště xxx měření xxxxxxx. Xxxxxxx xxxxxxx pro xxxx doporučení xx xx, xx u xxxxxxxxxxxxxxx xxxxxx xx xxxxx variabilita xxxxxxxx, xxxxx by mohla xxxxxxxx xxxx xxxxxxx xxxxx x xxxxxx xxxxxxxxxxxx. Xx druhé xxxxxx by hladovění xxxx xxx xxxxx xxx xxxx na xxxxxxx metabolismus x xxx xxxxxxxx x xxxxxxx by xxxxxxx xx pravidelnosti xxxxxxxx xxxxxxxx xxxxx. Xxxxx xx xxxxxxx xxxx xx xxxxx, je xxxxx xxxxxxx xxxxxxxxxxx xxxxxxxxx až xx xxxxxxxxxx funkčních xxxxxx xx 4. xxxxx xxxxxxx.
PŘÍLOHA IV E
" X.37 XXXXXX NEUROTOXICITA XXXXXXXXXXX XXXXXXXXX FOSFORU XX XXXXXX XXXXXXXX
1. XXXXXX
1.1 Úvod
Při xxxxxxxxx x xxxxxxxxx toxických xxxxxx xxxxx xx xxxxxxxx xxxx v xxxxx schopnost xxxxxxxx xxxxxx xxxxx vyvolat xxxxxxxxxx xxxx neurotoxicity, xxxxx xxxxxxx xxx xxxxxxxx xxxxxx studiemi xxxxxxxx. X xxxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxxx xxxx xxxxxxxxxx pozdní xxxxxxxxxxxxx; xxxx látky xxxx xxx podrobeny xxxxxxxx xxxxx metodou.
Screeningové xxxxxxx xx xxxxx xxx použít xxx xxxxxxxxx xxxxx, které xxxxx xxxxxxx xxxxxx xxxxxxxxxxxxxx; negativní xxxxx xx xxxxxxx xx xxxxx xxxx xxxxxxxxxxx xxxxx, xx látka xxxx schopnost xxxxxxx xxxxxx neurotoxicitu.
Viz obecný xxxx, xxxx B.
1.2 Xxxxxxxx
Xxxx "xxxxxxxxx xxxxxxxxxx xxxxxxx" xxxxx neutrální xxxxxxxxx xxxxxx, xxxxxxxxxx xxxx xxxxxxxxx xxxxxxxx xxxxxxxxxx, xxxxxxxxx xxxx xxxxxxxxxxxxxxx xxxx xxxxxxxxxxx xxxxxxx xxxxxxxxxxxxxxxx, xxxxxxxxxxxxxxx xxxx xxxxxxxxxxxxxxxxxxxxx, xxxx xxxx xxxxx, xxxxx xxxxx xxxxxxxx xxxxxx xxxxxxxxxxxxx xxxxxxxxxxx u xxxxxxxxx xxxxx xxxx xxxxxxx.
Xxxxxx neurotoxicita xx xxxxxxx projevující se xxxxxxx xxxxxxxx xxxxxx, xxxxxxxx xxxxxxxxxx x xxxx x periferním xxxxx a xxxx xxxxxxxx x xxxxxxxxx xxxxxxxxxx xxxxxxxx – XXX (neuropathy xxxxxx xxxxxxxx) v xxxxxxx xxxxx.
1.3 Referenční xxxxx
Xxxxxxxxxx xxxxx xxxx xxx xxxxxxxx x xxxxxxxxx xxxxxxxxx xxxxxxx x xxxxx xxxxxxxx, xx xx x xxxxxxxxxxxxx xxxxxxxxxx xxxxxx pokusných xxxxx xxxxxxxxx nezměnila.
Příkladem xxxxxx xxxxxxxxx látky x xxxxxxx xxxxxxxx xxxxxxx xx xxx-x-xxxxx-xxxxxx (XXX 78308, XXXXXX 2011035, název podle XXX: tris(2methylfenyl)fosfát), xxxxx xxxx xxx xxxxxx xxxxxxxxxxxxxxxx (TOCP).
1.4 Podstata xxxxxxxx xxxxxx
Xxxxxxxx látka xx xxxxxx orálně x jediné xxxxx xxxxxxxx xxxxxxx, chráněným xxxx xxxxxxx xxxxxxxx xxxxxxxxxxxxx xxxxxx. Zvířata xx pozorují po xxxx 21 xxx, xxxxxxxxxxx se xxxxxxxxxx xxxxxxx, xxxxxx a xxxxxx. Xxxxxxxxxxx xxxxxxxxx, xxxxxxx xxxxxxxx NTE (xxxxxxxxx target esterase), xx provádějí u xxxxxx náhodně xxxxxxxxx x každé skupiny, xxxxxxx 24 x 48 x xx xxxxxx xxxxx. Xxxxxx xxxxx xxx po xxxxxx látky xx xxxxxxxxx xxxxxxx xxxxxx x provede xx xxxxxxxxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxx.
1.5 Popis xxxxxxxx xxxxxx
1.5.1 Xxxxxxxx
Xxxxxxx xx xxxxxxx xxxxx xxxxxxx xxxxxxxx xxxxxxxxx xxxxxx, xxxxx xxxxxx xxxxxxxxx virovými xxxxxxxxxxxx x xxxxxxxxxxxxxxx xxxxxx x xxxx normální xxxxx, xxxxxxx xx xx xxxxxxxxxxxxxx a xxxxxxxxx xxxxxxx x xxxxxxx 5 xxx xxxx xxxxxxxxx xxxxxx xx xxxxxxxxxxxx xx xxxxxxxxxxx xxxxxxxx.
Xxxxxxxxx se xxxxxxxxxx xxxxx klece xxxx xxxxxx umožňující xxxxx pohyb slepic x snadné xxxxxxxxxx xxxxx.
Xxxxxxxx xxxxx se xxxxxxx xxxxxx xxxxxx xxxxxx, xxxxxxxxxxxx xxxxxxxxx xxxx xxxxxxxxxxxx xxxxxxx. Xxxxxxxx xx podávají xxxxxxxx xxxx xxxxxxxxxx xx vhodném xxxxxxxx, xxxx je např. xxxxxxxxx olej, pevné xxxxx by xx xxxx xxxxxx xxxxxxxxx, xxxxxxx xxxxx xxxxx xxxxxxx látek x xxxxxxxxxxxx xxxxxxxxx by xx xxxxxxxx dostatečně xxxxxxxx. Toxické xxxxxxxxxx xxxxxxxxx xxxxxxx xx xxxx xxx xxxxx xxxx xxxxxxxx, x xxxxx xxxxxx známy, xxxx xx být xxxxxx určeny.
1.5.2 Xxxxxxxx xxxxxxxx
1.5.2.1 Xxxxxxx xxxxxxx
Xxxxxxxxxx xx xxxxx xxxxxxx xxxx xxxxxxxx (Gallus xxxxxx xxxxxxxxxx), xxxxx 8 – 12 xxxxxx. Xxxxxxxxx se xxxxxxx x xxxxxxxxxx xxxxxxxxx x xxxxxxx xx xxxx být xxxxxxx za xxxxxxxx xxxxxxxxxxxx xxxxx xxxxx.
1.5.2.2 Xxxxx a xxxxxxx
Xxxxx xxxxxxxxxxxxxx skupiny xx xxxx být xxxxxxx xxxxxxxxx xxxxxxx s xxxxxxxxx a xxxxxxxxx xxxxxxxxx xxxxxxx. X xxxxxxxx xxxxxx xxxxxxxx xxxxx xx s xxxxxxxxx xxxxxxxx zachází xxxxxx xxxx x xxxxxxxxxxxxxx xxxxxxxx.
X xxxxx xxxxxxx xx xxx xxx xxxxxx dostatečný xxxxx slepic, aby xxxxx xxxx xxxxxx xxxxx xxx xxxxxxxx xxx xxxxxxxxxxx xxxxxxxxx (xxx v xxxxx x tři x xxxxx xxx po xxxxxx) a šest xxxxxxx 21xxxxx xxxxxxxxxx xxxxxxxxxxxxx xxxxxxxx.
Xxxxxxxxx kontrolní xxxxxxx může být xxxxxxxx xxxxxxxx nebo xxxxx být xxxxxxx xxxxx x xxxxxxx xxxxxxx xxxxxxxxx xxxxxxx. Xxxx by xxxxxxxxx xxxxxxx šest slepic, xxxxxx xx xxxx xxxxx, x xxx xx známo, že xxxxxxxx xxxxxx xxxxxxxxxxxxx, xxx xxxxxxx xxx xxxxxxxxxxx vyšetření a xxx xxxxxxx xxx xxxxxxxxxxxxxxxx xxxxxxxxx. Doporučuje xx xxxxxxxxxx doplňovat xxxxxxxxxx xxxxx. Nové xxxxxxxxx xxxxxxxxx údaje xx xxxx xxx xxxxxxxx, xxxxx xxxxxxxxxxx xxxxxxxxx v xxxxxxx xxxxx změní některý xxxxxxxx xxxxx xxxxxxx (xxxx. xxxxxxx, xxxxxx, xxxxxxxx chovu).
1.5.2.3 Xxxxxx xxxxx
Xxxx xx xx xxxxxxx xxxxxxxxx xxxxxx xx použití vhodného xxxxx slepic a xxxxxx x xxxxxxx xxxxxxxx xxxxx, aby xxxx xxxxx stanovit xxxxxx, xxxxx má xxx xxxxxxx x xxxxxx studii. Xxx xxxxxxxxx xxxxxxxxx dávky x xxxxxx xxxxxx xx x xxxx xxxxxxxxx studii nezbytná xxxxxx xxxxxxxx. Xxx xx xxxx xxxxxxxxx xxxxx vlivem xxxxxxxx xxxxxxxxxxxxx xxxxxx, xxx xxxxxx atropin nebo xxxx xxxxxxxx přípravek, x xxxxxx xx xxxxx, že xxxx xxxx na pozdní xxxxxxxxxxxx xxxxxx. Pro xxxxx xxxxxxxx neletální xxxxx xxxxxxxxxx xxxxx xxx xxxxxx xxxx xxxxx (xxx metoda X.1 x)). Při xxxxxx dávky xxxxx xxx užitečné také xxxxxxxxx údaje o xxxxxxxxx xxxx xxxx xxxxxxxxxxxxx xxxxxxxxx.
Xxxxxx dávky xxxxxxxx xxxxx x xxxxxx xxxxxx xx xxxx xxx co xxxxxxxx, xxxxxxx xx xxxxx v xxxxx xxxxxxxx xxxxxxxxx xxxxxx xxxxxx dávky x xxxxx xxxxx xxxxx 2000 xx xx xx xxxxxxx xxxxxxxxx. Xxxxxxxx xxxx by xxxxx narušit xxxxxxxxxx xxxxx zvířat xxx xxxxxxxxxxx xxxxxxxxx (xxxx) x xxx xxxxxxxxxxxx xxxxxxxxx (xxxx) po 21 xxxxx. Xxx xx xxxxxxxxx xxxxx xxxxxx xxxxxxxx xxxxxxxxxxxxx xxxxxx, použije xx xxxxxxx xxxx xxxx xxxxxxxx xxxxxxxxx, x xxxxxx je xxxxx, xx xxxx xxxx xx xxxxxx neurotoxické xxxxxx.
1.5.2.4 Limitní xxxxxxx
Xxxxx xxxxxxx xxxxxxxxx xxxxx xxxxxxx xxxxxxxxx v xxxx xxxxxx xxx xxxxx dávce xxxxxxx 2000 xx xx xx xxxxxxx hmotnosti xx xxx nevyvolá xxxxxxxxxxxxx xxxxxxx účinky x xxxxx xx xx xxxxxxx xxxxx x látkách x xxxxxxxx xxxxxxxxxx xxxxxxxxxxxxx xxxxxxxx, není xxxxx xxxxxx xx xxxxxxx xxxxx dávky xxxxxxxx. Xxxxxxx zkouška xx xxxxxxx s xxxxxxxx xxxxxxx, xxx xxxxx x xxxxxxxx člověka xxxxxxxxx, že xx xxxxxxxx xxxxxxx xxxxx xxxxxx xxxxx.
1.5.2.5 Xxxx xxxxxxxxxx
Xxxx xxxxxxxxxx xx xxxx být 21 xxx.
1.5.3 Xxxxxx
Xx xxxxxx xxxxxxxxx xxxxxxxxxx před xxxxxxxx xx následky xxxxxxxx cholinergního xxxxxx xx xxxx xxxxxxxx xxxxx x jedné xxxxx.
1.5.3.1 Obecná xxxxxxxxxx
Xxxxxxxxxx xx xxxx začít xxxxxxxx po xxxxxx. Xxxxxxx slepice se xxxxxxx xxxxxxxxxx xxxxx xxxxxxxx v xxxxxxx xxxxxxx xxxx dnů x xxxx nejméně xxxxxx xxxxx xx xxxx 21 xxx xxxx do xxxxxxxxxxx xxxxxxxx. Veškeré xxxxxxxx xxxxxxxx xx xxxx xxx zaznamenány, včetně xxxx xxxxxxx, xxxx, xxxxxxxxxx x xxxxxx xxxxxxxxxxxx chování. Ataxie xx měla xxx xxxxxxxxx xxxxx xxxxxxx xxxxxxxxxxxx pořadové stupnice x xxxxxxxxxxx se xxxxxx. Xxxxxxx xxxxxxx xxxxx xx xxxxxxx xxxxxx x xxxxxxxxxxxxx xxxxxxxx vyjmou x xxxxx x xxxxxxx xxxxxxx nucené xxxxxxxxx xxxxxxxx, xxxx xxxx. xxxxxxxx xx xxxxxxx, xxx xx xxxxxxxxx xxxxxxxxx sebemenších toxických xxxxxx. Xxxxxxx x xxxxxx a zvířata, xxxxx se trápí xxxx trpí bolestí, xx xxxxx vyřadí, xxxxxxx xxxxxx x xxxxxxx.
1.5.3.2 Tělesná hmotnost
Všechny xxxxxxx xx xxxxx xxxxx před xxxxxxx xxxxxxxx xxxxx x xxxx xxxxxxx jednou xxxxx.
1.5.3.3 Xxxxxxxxxxx xxxxxxxxx
Xxxx xxxxxx xxxxxxx xxxxxxxxx x xxxxx xxxxxxxxxxxxxx xxxxxxx a kontrolní xxxxxxx x xxxxxxxxx x xxx xxxxxxx x xxxxxxxxx kontrolní xxxxxxx (pokud xx xxxxxxx souběžně xxxxxxx x touto xxxxxxxx) xx xxxxxx x xxxxxxx xxxxx xx xxxxxx xxxxx, xxxxx x lumbální xxxxx xx xxxxxxxxxxx a xxxxxxx se na xxxxxxxx XXX. Xxxx xxxx xxx xxxxxx xxxxxx xxxxxxxxxxxx x. xxxxxxxxxxx x analyzovat xxxx xxxx xx xxxxxxxx xxxxxxxx XXX. Xxxxxxxxx xx xxxxxx xxx slepice x xxxxxxxxx xxxxxxx x x xxxxx xxxxxxxxxxxxxx xxxxxxx xx 24 x x xxxxx xxx xx 48 x, xxxxxxx tři xxxxxxx x xxxxxxxxx xxxxxxxxx xxxxxxx xx xxxxxx po 24 x. Xxxxx xxxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx, že se xxxxxxx xxxxx x xxxxxxxxx xxxxxxxxx xxxxx xxxxxx (xx xxx xxxxx posoudit xxxxxxxxxxx xxxx nástupu xxxxxxxxxxxxx xxxxxxxx), může být xxxxxxxxx xxxxxxx vzorek xxxxx xxxxxxx xx xxx xxxxxx mezi 24 xx 72 x po xxxxxx xxxxx.
Xx xxxxxx xxxxxxxx xxxxx mohou xxx xxxxxxxxx xxxx analýza xxxxxxxxxxxxxxxxxxxx (XXxX), je-li xx xxxxxxxxxx xx xxxxxx. Xx vivo xxxx xxxx nastat xxxxxxxxx xxxxxxxxxx XXxX, xxx může xxxx x xxxxxxxxx xxxxx xxxx xxxxxxxxxx XXxX.
1.5.3.4 Xxxxx
Xxxxx všech xxxxxx (xxxxxxxxxx xxxxx xxxxx x xxxxxxxxxx x xxxxxx) xx měla xxxxxxxxx xxxxxxxxx xxxxx xxxxx x míchy.
1.5.3.5 Xxxxxxxxxxxxxxxx xxxxxxxxx
Xxxxxxx xxxx xxxxxx, xxxxx xxxxxxx xxxx pozorování x xxxxxx xxxxxxx xxx xxxxxxxxxxx xxxxxx, by xxxx být xxxxxxxxxxxxx xxxxxxxxx. Xxxxx xx xxxx xxx xxxxxxxx xx situ za xxxxxxx xxxxxxxxxx xxxxxxx. Xxxxxxx xx mozeček (xxxxxxx xxxxxxx řez), xxxxxxxxxxx xxxxx, mícha x xxxxxxxxx xxxxx. Xxxx xxxxx xx xxxx xxx xxxxxxxx x xxxxx krční xxxxx, xxxxxxx xxxxxx x lumbosakrální oblasti. Xxxx by být xxxxxxxx xxxx distální xxxxx n. xxxxxxxx x xxxx větví x m. gastrocnemius x z n. xxxxxxxxxxx. Xxxx se xxxxx xxxxxxxx xxxxxxx xx xxxxxx x xxxxx.
2. XXXXX
Xxxxxxxxx xxxxxxxx xxxxxxx xxx výsledné xxxxxx zvolené x xxxx xxxxxx (xxxxxxxxxxx x xxxxxxxxxxxxxxxx xxxxxxxxx x vyšetření xxxx xxxxxxx) xxxxxxxxxx zpravidla xxxxx xxxxxxxx xxxxxx xxxxxxxxxxxxx. Xxx xxxxxxxxxxxx xxxx xxxxxxxxxxxx xxxxxxxxxx xxxxxx vyšetření xxxx xxx nezbytné další xxxxxxxxx.
Xxxx xx být xxxxxxx xxxxx xxx xxxxx jednotlivé xxxxx. Xxxxx xx xxxx xxx všechny údaje xxxxxxx xx xxxxxxx, xxxxxxx xx xxxxx x každé experimentální xxxxxxx xxxxx xxxxxx xx xxxxxxx xxxxxxx, xxxxx xxxxxx xxxxxxxxxxxx xxxx, xxxxxx na xxxxxxx xxxx xxxxxxxxxxx xxxxxx, typ x xxxxxxxxx těchto xxxx xxxx xxxxxx x xxxxxxxx xxxxxx xxxxxxxxxx xxxxx xxx x xxxxxxxxx xxxx xxxx xxxxxx.
Xxxxx x xxxx xxxxxx xx xxxx xxx xxxxxxxxxxx x xxxxxxxx xxxxxxx, xxxxxxxxxx x korelace xxxxxx xx chování x xxxxxxxxxxxxx a xxxxxxxxxxxxxxxxxx xxxxxx x dále xxxxxxxxxx dalších xxxxxxxxxxxx xxxxxx na experimentální x kontrolní xxxxxxx.
Xxxxxxx xxxxxxxx by xxxx xxx xxxxx xxxxx xxxxxxxxxxx vhodnou x xxxxxx uznávanou xxxxxxxxxxxx xxxxxxx. Statistická xxxxxx xx xxxx být xxxxxxx xxx xxx xxxxxxxxx studie.
3. ZPRÁVY
Protokol x zkoušce
Protokol o xxxxxxx xx xxxxx xxxxx xxxxxxxxx xxxx xxxxxxxxx:
Xxxxxxx xxxxxxx
- použité xxxxxxx;
- počet a xxxxx zvířat;
- xxxxx, xxxxxxxx xxxxx xxx.;
- xxxxxxxx xxxxxxxxxxxx zvířat xx xxxxxxx zkoušky.
Zkušební xxxxxxxx:
- xxxxxxxx xxxxx x xxxxxxxx xxxxxxxx xxxxx, xxxxxxxxx x xxxx xxxxxxxx x xxxxxxxxxx;
- xxxxxxxxxx xxxxx xxxxxxxx;
- xxxxxxxx xxxxx x způsobu xxxxxx xxxxxxxx látky;
- xxxxxxxx xxxxx o stravě x x xxxxxxx xxxx;
- xxxxxxxxxx xxxxxx xxxxxx xxxxx;
- xxxxxxxxxxx xxxxxxxxxx xxxxx, včetně xxxxxxxxxx informací x xxxxxxxx, objemu x xxxxxxxxx formě podané xxxxx;
- xxxxxxxxxxxx jakéhokoli xxxxxxxxxx xxxxxxxxx a xxxxxxxx informace x xxxx xxxxxx.
Xxxxxxxx:
- xxxxx x xxxxxxx xxxxxxxxx;
- xxxxx x toxických xxxxxxxx xxxxx xxxxxx, xxxxxx xxxxxxxxx;
- xxxxxxxxx, xxxxxxxxx a trvání xxxxxxxxxx xxxxxxx (zda xxxx xxxxxx xxxx xxxxxxxx);
- xxxxxxxx popis xxxxxxxxxxxxx xxxxxxxxx a xxxxxx;
- xxxxxxx nálezy;
- xxxxxxxx xxxxx všech xxxxxxxxxxxxxxxxxx xxxxxx;
- xxxxxxxxx xxxxxxxxxxx xxxxxxxxxxx výsledků.
Rozbor xxxxxxxx.
Xxxxxx.
4. LITERATURA
Metoda je xxxxxxxxxx xxxxxx OECD XX 418.
X.38 POZDNÍ XXXXXXXXXXXXX ORGANICKÝCH XXXXXXXXX XXXXXXX – 28XXXXX XXXXXXXXX XXXXXXXX
1. XXXXXX
1.1 Xxxx
Xxx xxxxxxxxx x xxxxxxxxx toxických xxxxxx xxxxx je xxxxxxxx xxxx x úvahu xxxxxxxxx xxxxxxxx skupin xxxxx vyvolat xxxxxxxxxx xxxx neurotoxicity, které xxxxxxx xxx xxxxxxxx xxxxxx xxxxxxxx xxxxxxxx. X xxxxxxxx xxxxxxxxxxx xxxxxxxxx fosforu xxxx xxxxxxxxxx pozdní neurotoxicita; xxxx látky mají xxx podrobeny xxxxxxxx xxxxx xxxxxxx.
Xxxxxxxxxxxx xxxxxxx xx xxxxx xxx xxxxxx pro xxxxxxxxx xxxxx, xxxxx xxxxx xxxxxxx xxxxxx xxxxxxxxxxxxxx; xxxxxxxxx xxxxx xx xxxxxxx in xxxxx xxxx neposkytuje důkaz, xx xxxxx xxxx xxxxxxxxx vyvolat xxxxxx xxxxxxxxxxxxx.
28xxxxx zkouška xxxxxx xxxxxxxxxxxxx poskytuje xxxxxxxxx x xxxxxx xxxxxxxxx xxx xxxxxx, xxxxx xx xx xxxxx xxxxxxxx x opakovaných xxxxxxx během omezeného xxxxxxxx xxxxxx. Xxxxxxxx xxxxxxxxx x xxxxxx xx dávku a xxxx xxxxxxxxxx odhad xxxxxx xxx pozorovatelných xxxxxxxxxxxx xxxxxx, což xxxx xxx užitečné xxx xxxxxxxxx xxxxxxxx xxx xxxxxxxxx expozici xxxxxxx.
Xxx také xxxxxx xxxx, xxxx B.
1.2 Xxxxxxxx
Xxxx "xxxxxxxxx xxxxxxxxxx xxxxxxx" xxxxx xxxxxxxxx xxxxxxxxx xxxxxx, thioestery xxxx anhydridy xxxxxxxx xxxxxxxxxx, xxxxxxxxx xxxx xxxxxxxxxxxxxxx xxxx xxxxxxxxxxx xxxxxxx xxxxxxxxxxxxxxxx, thiofosfonových xxxx amidothiofosforečných, xxxx xxxx xxxxx, xxxxx xxxxx xxxxxxxx xxxxxx xxxxxxxxxxxxx xxxxxxxxxxx u xxxxxxxxx xxxxx xxxx xxxxxxx.
Xxxxxx xxxxxxxxxxxxx xx xxxxxxx projevující xx xxxxxxx xxxxxxxx ataxie, xxxxxxxx xxxxxxxxxx x xxxx a periferním xxxxx x xxxx x xxxxxxxx x xxxxxxxxx xxxxxxxxxx esterasy - NTE (xxxxxxxxxx xxxxxx xxxxxxxx) x xxxxxxx tkáni.
1.3 Xxxxxxxx xxxxxxxx xxxxxx
Xxxxxxxx xxxxx xx podávají xxxxx xxxxxx slepicím xxxxxxx xx dobu 28 xxx. Xxxxxxx xx xxxxxxxx xxxxxxx xxxxxx xxxxx, xxxxxxxxxxx xx xxxxxxxxxx xxxxxxx, xxxxxx x paréza xxxxx 14 xxx xx xxxxxxxx dávce. Xxxxxxxxxxx xxxxxxxxx, xxxxxxx xxxxxxxx XXX (xxxxxxxxx target xxxxxxxx), se xxxxxxx x xxxxxx náhodně xxxxxxxxx x xxxxx xxxxxxx, xxxxxxx 24 x 48 x xx xxxxxx xxxxx. Xxx xxxxx po xxxxxxxx xxxxx xx xxxxxxxxx slepice xxxxxx x xxxxxxx se xxxxxxxxxxxxxxxx xxxxxxxxx vybraných xxxxxxxxx tkání.
1.4 Popis xxxxxxxx metody
1.4.1 Xxxxxxxx
Xxxxxxx xx náhodný výběr xxxxxxx xxxxxxxx xxxxxxxxx xxxxxx, xxxxx nejsou xxxxxxxxx xxxxxxxx xxxxxxxxxxxx x farmakologickou léčbou x mají xxxxxxxx xxxxx, xxxxxxx se xx xxxxxxxxxxxxxxxx x xxxxxxxxxxx xxxxxx x xxxxxxx 5 xxx xxxx zahájením xxxxxx xx xxxxxxxxxxxx xx xxxxxxxxxxx xxxxxxxx.
Xxxxxxxxx xx xxxxxxxxxx xxxxx xxxxx xxxx xxxxxx xxxxxxxxxx xxxxx xxxxx slepic x snadné xxxxxxxxxx xxxxx.
Xxxxxxxx xxxxx xx xxxxxx xxxxx xxx, 7 xxx v xxxxx, xxxxxxx xxxxxx xxxxxx xxxx želatinovými xxxxxxxxx. Xxxxxxxx xx xxxxxxxx neředěné xxxx xxxxxxxxxx xx vhodném xxxxxxxx, xxxx xx xxxx. xxxxxxxxx xxxx, xxxxx xxxxx xx xx xxxx nechat xxxxxxxxx, xxxxxxx xxxxx xxxxx xxxxxxx xxxxx x xxxxxxxxxxxx tobolkách xx xx xxxxxxxx xxxxxxxxxx xxxxxxxx. Xxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxx xx xxxx xxx xxxxx xxxx xxxxxxxx, x xxxxx xxxxxx xxxxx, xxxx by xxx xxxxxx xxxxxx.
1.4.2 Xxxxxxxx podmínky
1.4.2.1 Xxxxxxx xxxxxxx
Xxxxxxxxxx xx xxxxx xxxxxxx xxxx xxxxxxxx (Xxxxxx gallus domesticus), xxxxx 8 – 12 měsíců. Xxxxxxxxx xx plemena o xxxxxxxxxx velikosti x xxxxxxx xx měly xxx xxxxxxx xx xxxxxxxx umožňujících xxxxx xxxxx.
1.4.2.2 Xxxxx x xxxxxxx
Xxxxxx xx xxxx xxx xxxxxxx xxxxxxx xxx xxxxxxxxxxxxxx xxxxxxx x xxxxxxxxx xxxxxxx x xxxxxxxxx. X xxxxxxxx podání xxxxxxxx xxxxx xx x xxxxxxxxx xxxxxxxx s xxxxxxxxx xxxxxxx stejně xxxx x xxxxxxxxxxxxxx xxxxxxxx.
X xxxxx xxxxxxx xx xxx xxx xxxxxx xxxxxxxxxx počet xxxxxx, aby aspoň xxxx slepic xxxxx xxx xxxxxxxx xxx xxxxxxxxxxx xxxxxxxxx (xxx x xxxxx a xxx x xxxxx xxx xx podání) x xxxx xxxxxxx 14xxxxx xxxxxxxxxx xxxxxxxxxxxxx xxxxxxxx.
1.4.2.3 Xxxxxx xxxxx
Xxx xxxxxx úrovní xxxxx xx měly xxx xxxxx v xxxxx xxx xxxxxxxx xxxxxx xxxxxxx pozdní neurotoxicity x xxxxxxxx další xxxxxxxx xxxxx o xxxxxxxx x xxxxxxxx xxxxxxxx xxxxxxxxxx. Xxxxxxxx xxxxxx dávky by xxxx být vybrána x cílem xxxxxxx xxxxxxx xxxxxx, xxxxxxx xxxxxx xxxxxxxxxxxxx, ne xxxx xxxxxxx xxxx xxxxxx xxxxxxx. Dále xx xxxx být xxxxxxx xxxxxxxx xxxx xxxxx x xxxxx xxxxxxxx, xx xxxxxxxx xxxxxxxxx xxxxxx na xxxxx x že xxxxxxxx dávka nevyvolává xxxxx projevy xxxxxxxx.
1.4.2.4 Xxxxxxx xxxxxxx
Xxxxx xxxxxxx xxxxxxxxx podle xxxxxxx xxxxxxxxx v této xxxxxx xxx xxxxx xxxxx nejméně 1000 xx xx xx xxxxxxx xxxxxxxxx a xxx xxxxxxxx pozorovatelné xxxxxxx účinky a xxxxx se na xxxxxxx xxxxx x xxxxxxx s podobnou xxxxxxxxxx xxxxxxxxxxxxx toxicita, xxxx xxxxx xxxxxx xx xxxxxxx vyšší xxxxx xxxxxxxx. Xxxxxxx xxxxxxx xx xxxxxxx x xxxxxxxx xxxxxxx, xxx údaje x xxxxxxxx xxxxxxx xxxxxxxxx, xx xx nezbytné xxxxxxx xxxxx úrovně xxxxx.
1.4.2.5 Xxxx xxxxxxxxxx
Xxxxxxx xxxxxxx by xxxx xxx xxxxxxxxxx nejméně xxxxxx denně xx xxxx expozice x 14 xxx xx xx, xx xx xxxxxxxxx xxxxx xxxxx xxxxx.
1.4.3 Xxxxxx
Xxxxxxxx xx xxxxxx xxxxxxxx xxxxx xxxx xxx v xxxxx po xxxx 28 xxx.
1.4.3.1 Xxxxxx xxxxxxxxxx
Xxxxxxxxxx by xxxx xxxxx xxxxxxxx po xxxxxx. Xxxxxxx xxxxxxx xx xxxxxxx xxxxxxxx xxxxxx denně každý xxx x 28 xxx xxxxxxxx x 14 dnů po xxxxxxxx xxxx xx xxxxxxxxxxx xxxxxxxx. Veškeré xxxxxxxx xxxxxxxx xx xxxx xxx xxxxxxxxxxx, xxxxxx xxxx xxxxxxx, xxxx, xxxxxxxxxx x xxxxxx. Pozorování má xxxxxxxxx xxxxxxxxxxx xxxxxxx, xxx xxxx se xx ně xxxxxxxx. Xxxxxx by xxxx xxx xxxxxxxxx xxxxx xxxxxxx xxxxxxxxxxxx pořadové xxxxxxxx a xxxxxxxxxxx xx xxxxxx. Xxxxxxx xxxxxxx xxxxx se xxxxxxx x xxxxxxxxxxxxx xxxxxxxx xxxxxx x xxxxx a podrobí xxxxxxx xxxxxx motorické xxxxxxxx, jako např. xxxxxxxx po xxxxxxx, xxx xx xxxxxxxxx xxxxxxxxx sebemenších xxxxxxxxx xxxxxx. Zvířata v xxxxxx a xxxxxxx, xxxxx se xxxxx xxxx xxxx xxxxxxx, xx ihned xxxxxx, xxxxxxx xxxxxx a xxxxxxx.
1.4.3.2 Xxxxxxx xxxxxxxx
Xxxxxxx xxxxxxx xx xxxxx xxxxx xxxx prvním xxxxxxx xxxxxxxx xxxxx x xxxx xxxxxxx xxxxxx xxxxx.
1.4.3.3 Xxxxxxxxxxx xxxxxxxxx
Xxxx slepic náhodně xxxxxxxxx z xxxxx xxxxxxxxxxxxxx xxxxxxx x xxxxxxxxx skupiny s xxxxxxxxx a xxx xxxxxxx x xxxxxxxxx xxxxxxxxx xxxxxxx xx xxxxxx v prvních xxxxx po xxxxxx xxxxxxxx xxxxx, xxxxx x xxxxxxxx xxxxx xx vypreparují x xxxxxxx se na xxxxxxxx XXX. Xxxx xxxx xxx xxxxxx xxxxxxxxxxxx x. ischiadicus x analyzovat xxxx xxxx xx xxxxxxxx xxxxxxxx NTE. Zpravidla xx usmrtí xxx xxxxxxx z xxxxxxxxx xxxxxxx x x xxxxx experimentální xxxxxxx xx 24 x x xxxxx xxx xx 48 h xx poslední xxxxx. Xxxxx xxxxx x xxxxxx studie xxxx x jiných xxxxxx (xxxx. xxxxxxxxxxxxxxxxx) xxxxxxxxx, xx jsou xxxxxx xxxx doby usmrcení xx xxxxxxxx xxxxx xxx xxxx xxxx, xxxx by xxx xxxxxxx a xxxxxxxxxx xx xxxx být xxxxxxx v dokumentaci.
Na xxxxxx vzorcích tkáně xxxxx xxx provedeny xxxx xxxxxxx acetylcholinesterasy (XXxX), xx-xx to xxxxxxxxxx xx xxxxxx. Xx vivo xxxx xxxx nastat xxxxxxxxx xxxxxxxxxx XXxX, což xxxx vést x xxxxxxxxx xxxxx jako xxxxxxxxxx XXxX.
1.4.3.4 Pitva
Pitva xxxxx zvířat (xxxxxxxxxx xxxxx xxxxx a xxxxxxxxxx x xxxxxx) xx xxxx xxxxxxxxx xxxxxxxxx xxxxx xxxxx x xxxxx.
1.4.3.5 Xxxxxxxxxxxxxxxx xxxxxxxxx
Xxxxxxx xxxx xxxxxx, xxxxx xxxxxxx xxxx xxxxxxxxxx x xxxxxx xxxxxxx xxx xxxxxxxxxxx xxxxxx, by xxxx xxx xxxxxxxxxxxxx xxxxxxxxx. Xxxxx xx měly xxx xxxxxxxx xx xxxx xx použití xxxxxxxxxx technik. Xxxxxxx xx mozeček (střední xxxxxxx xxx), xxxxxxxxxxx xxxxx, xxxxx x xxxxxxxxx xxxxx. Řez xxxxx xx xxx xxx xxxxxxxx z xxxxx xxxxx xxxxx, xxxxxxx xxxxxx x xxxxxxxxxxxxx oblasti. Měly xx být odebrány xxxx xxxxxxxx xxxxx x. tibialis x xxxx větví x x. xxxxxxxxxxxxx x x n. xxxxxxxxxxx. Xxxx se xxxxx xxxxxxxx xxxxxxx xx xxxxxx x axony. Xxxxxxx by mělo xxx xxxxxxxxx xxxxxxxxxxxxx xxxxxxxxx xxxxxxxx xxxxx xxxxx zvířat xxxxxxxxx xxxxxxx x xxxxxxx x xxxxxxx xxxxxx. Xxxxx xx x xxxxxxx s vysokou xxxxxx projeví xxxxxx, xxxx xx xxx xxxxxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxx na slepicích xx xxxxxxx xx xxxxxxx a nízkou xxxxxx.
2. ÚDAJE
Negativní xxxxxxxx xxxxxxx xxxxx xxxxxxx (xxxxxxxxxxx a xxxxxxxxxxxxxxxx xxxxxxxxx x xxxxxxxxx xxxx xxxxxxx) nevyžadují xxxxxxxxx xxxxx xxxxxxxx xxxxxx xxxxxxxxxxxxx. Xxx xxxxxxxxxxxx nebo neprůkazných xxxxxxxxxx těchto vyšetření xxxx být nezbytné xxxxx xxxxxxxxx.
Xxxx xx xxx uvedeny údaje xxx xxxxx jednotlivé xxxxx. Xxxxx by xxxx být xxxxxxx xxxxx shrnuty do xxxxxxx, xxxxxxx se x xxxxx xxxxxxxxxxxxxx xxxxxxx xxxxx xxxxx xxxxxx xx xxxxxxx xxxxxxx, xxxxx xxxxxx xxxxxxxxxxxx xxxx, xxxxxx xx xxxxxxx nebo xxxxxxxxxxx xxxxxx, typ x xxxxxxxxx těchto xxxx xxxx xxxxxx x xxxxxxxx zvířat xxxxxxxxxx každý xxx x závažnost xxxx xxxx xxxxxx.
Xxxxx z xxxx studie xx xxxx xxx vyhodnoceny x hlediska výskytu, xxxxxxxxxx a korelace xxxxxx xx xxxxxxx x xxxxxxxxxxxxx a xxxxxxxxxxxxxxxxxx xxxxxx x xxxx xxxxxxxxxx xxxxxxx xxxxxxxxxxxx xxxxxx na xxxxxxxxxxxxxx x xxxxxxxxx xxxxxxx.
Xxxxxxx výsledky xx xxxx xxx xxxxx xxxxx xxxxxxxxxxx xxxxxxx x xxxxxx uznávanou xxxxxxxxxxxx metodou. Xxxxxxxxxxx xxxxxx xx xxxx xxx xxxxxxx xxx xxx xxxxxxxxx studie.
3. XXXXXX
Xxxxxxxx o xxxxxxx
Xxxxxxxx x xxxxxxx xxxxxxxx xxxxx xxxxx xxxx xxxxxxxxx:
Xxxxxxx zvířata:
- xxxxxxx xxxxxxx;
- xxxxx a xxxxx zvířat;
- xxxxx, xxxxxxxx xxxxx xxx.;
- xxxxxxxx jednotlivých xxxxxx xx xxxxxxx zkoušky.
Zkušební xxxxxxxx:
- podrobné xxxxx x přípravě zkoušené xxxxx, xxxxxxxxx x xxxx xxxxxxxx x xxxxxxxxxx;
- zdůvodnění xxxxx xxxxxxxx;
- xxxxxxxx údaje x xxxxxxx xxxxxx xxxxxxxx xxxxx;
- xxxxxxxx xxxxx x xxxxxx x o xxxxxxx xxxx;
- xxxxxxxxxx xxxxxx xxxxxx xxxxx;
- specifikace xxxxxxxxxx xxxxx, xxxxxx xxxxxxxxxx xxxxxxxxx x xxxxxxxx, xxxxxx x xxxxxxxxx formě xxxxxx xxxxx;
- zdůvodnění xxxxxx xxxx xxxxxx pro xxxxxxxxxxx vyšetření, není-li xxxxxxx 24 a 48 x.
Xxxxxxxx:
- údaje x xxxxxxx hmotnosti;
- xxxxx x xxxxxxxxx xxxxxxxx xxxxx xxxxxx, xxxxxx xxxxxxxxx;
- úroveň xxx pozorovatelných xxxxxxxxxxxx xxxxxx;
- charakter, xxxxxxxxx x trvání klinických xxxxxxx (xxx xxxx xxxxxx nebo xxxxxxxx);
- xxxxxxxx popis xxxxxxxxxxxxx xxxxxxxxx x xxxxxx;
- xxxxxxx xxxxxx;
- podrobný xxxxx všech xxxxxxxxxxxxxxxxxx xxxxxx;
- xxxxxxxxx xxxxxxxxxxx xxxxxxxxxxx xxxxxxxx.
Xxxxxx xxxxxxxx.
Xxxxxx.
4. XXXXXXXXXX
Xxxxxx xx xxxxxxxxxx xxxxxx XXXX XX 419."
PŘÍLOHA X
Xxxxxx xxxxxxxxx xx klasifikaci x xxxxxxxxxx xxxxxxxxxxxx látek x xxxxxxxxx
Xxx xxxxxxxx Xxxxxx 2001/59/ES, Úř. xxxx. L 332, 28. 12. 2000, x. 81.


