Xxxxxxxx Xxxxxx 96/54/xx
xx xxx 30. xxxxxxxx 1996,
xxxxxx se xx xxxxxxx druhé xxxxxxxxxxxx xxxxxxxxxxx pokroku směrnice Xxxx 67/548/XXX x xxxxxxxxxx xxxxxxxx a xxxxxxxxx xxxxxxxx týkajících xx xxxxxxxxxxx, balení x xxxxxxxxxx xxxxxxxxxxxx xxxxx
XXXXXX XXXXXXXXXX SPOLEČENSTVÍ,
s xxxxxxx xx Xxxxxxx x založení Xxxxxxxxxx xxxxxxxxxxxx,
x xxxxxxx xx xxxxxxxx Rady 67/548/EHS xx xxx 27. xxxxxx 1967 x xxxxxxxxxx xxxxxxxx x xxxxxxxxx xxxxxxxx týkajících xx klasifikace, balení x označování xxxxxxxxxxxx xxxxx [1], xxxxxxxxx xxxxxxxxxx směrnicí Xxxxxx 94/96/XX [2], x xxxxxxx xx xxxxxx 28 uvedené xxxxxxxx,
xxxxxxxx x tomu, že xxxxxxx X xxxxxxxx Xxxx 67/548/EHS xxxxxxxx xxxxxx xxxxxxxxxxxx látek, xxxxxx klasifikaci, označování x x případě xxxxxxx xxxxxx charakterizaci xxxxxxxxxxxxxxx xxxxxxxxxxxxxx limitů x jiných xxxxxxxxx xxxxxxxxxxxx xxxxxxxxxx xxxxxx xxxxxx xxx xxxxxx xxxxxxx x xxxxxxx xxxxxxxxx; xx xxxxxx xxxxxxxxxxxx látek x xxxxxxx X xxxxxxxx xxxxxx xxxxx xxxxxxxxxx xxxxxxxxx x xxxxxxxxxxx xxxxxxxx; že x xxxxxxxx toho je xxxxxxxx xxxxxx xxxx xxxxxxx X xxx, xxx xxxxxxxxx poznámky xxxxxxxx xx xxxxxxxxxx xxxxxxxxx x novou xxxxxxx xxxxxxxxxxx látek x tabulce X; xx seznam xxxxxxxxxxxx xxxxx v xxxxxxx X xxxxxxxx látky, xxx xxxxx xxxx xxxxxxxxxx Xxxxxxxx x Xxxxxxx x aktu x xxxxxxxxxxx Xxxxxxxx, Xxxxxx x Xxxxxxx xxxxxxxxxx xxxxxxx odchylky xxxxxxxx se xxxxxxxxxxx x xxxxxxxxxx; xx xxx o xxxxxxxxxxx xxxxxxxxxxx xxxxxxxxxxx xxxxxxxxx xx klasifikaci x xxxxxxxxxx xxxxxx xxxxx; xx proto xxxx xxxxxxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxx xxxxx;
xxxxxxxx x xxxx, xx příloha XXX směrnice 67/548/EHS xxxxxxxx seznam xxx xxxxxxxxxxx xxxxxxxx xxxxxx xxxxxxx s xxxxxxxxxxxx xxxxxxx x xxxxxxxxx; xx xx xxxxxxx xxxxxx xxxx xxxxxxxxx xxxxxxxxxxxx určitých látek x xxxxxxxxx xxx xxxxxx;
xxxxxxxx k xxxx, xx xxxxxxx X xxxxxxxx 67/548/EHS xxxxxxx xxxxxx xxx stanovení xxxxxxxxx-xxxxxxxxxx xxxxxxxxxx, toxicity x xxxxxxxxxxx xxxxx x přípravků; že xx nezbytné xxxxxxxxxxxx xxxx xxxxxxx xxxxxxxxxxx xxxxxxx;
xxxxxxxx x xxxx, xx xxxxxxx XX xxxxxxxx 67/548/XXX obsahuje xxxxxx xxxxxxxx xxx xxxxxxxxxxx x označování xxxxxxxxxxxx xxxxx x xxxxxxxxx; xx xx xxxxx zavést xxxxxxxx xxx xxxxx x xxxxxxxxx xxxxxxxxxx pro xxxxxx, xxxxx xxxx xxxxxxxxxx; že xxxxxxxx xxx senzibilizující látky x xxxxxxxxx xx xxxxx xxxxxx; xx xx xxxxx xxxxxx xxxxxxxx pro xxxxxxxxxx xxxxxxxxx lahví xxxxxxxx xxx xxxxxx, xxxxx x xxxxxxxxxx zemní xxxx (XXX);
xxxxxxxx x xxxx, že xxxxxxxx xxxx xxxxxxxx xxxx x souladu se xxxxxxxxxxx Výboru xxx xxxxxxxxxxxx xxxxxxxxxxx xxxxxxx xxxxxxx x xxxxxxxxxx xxxxxxxxxxx překážek xxxxxxx xx xxxxx nebezpečných xxxxx x xxxxxxxxx,
XXXXXXX XXXX SMĚRNICI:
Článek 1
Xxxxxxxx 67/548/EHS xx xxxx xxxxx:
1. Xxxxxxx X xx xxxx xxxxx:
x) V xxxxxxxxx xx xxxxxxxx 4 xxxxxxxxx xxxxx:
"Xxxxxxxx 4
Xxxxxxxxx xxxxxxxxxx xxxx xxxxx xxxx xxx xxxxxxxxxxxxx jako xxxxxx xxxxxxxx x xxxxx X 65, pokud xxxxxxx xxxxxxxx x xxxxxxx VI části 3.2.3.";
x) xxxxxxxx se xxxxxxxx 5, xxxxx xxx:
"Xxxxxxxx 5
Xxxxxxxxxxxx xxxxxx xxx plynné přípravky xxxx xxxxxxxxx v xxxxxxxxxx xxxxxxxxxx";
x) v xxxxxxx B x xxxxxxxxx xxxxxxx X xxxxxxxx 67/548/XXX se xxxxxx tato xxxxxxxxxxx xxx xxxxxxxxx xxxxx:

x) xxxxxxxxxxxx xxxxxxx xxxxxxx xxxxxxxx xx xxxxxxxxx xxxxxxxxx přílohy X xxxx xxxxxxxx;
x) poprvé xx vkládají xxxxxxx xxxxxxx XX této xxxxxxxx;
x) xxxxxxx se xxxxxxx s xxxxxx xxxxx:
008-002-00-3
612-045-00-9
648-011-00-5
648-025-00-1
648-157-00-X
648-158-00-5
648-159-00-0
649-192-00-3
x) xxxxxxx v xxxxxxx XXX xxxxxxx xxxxxxxx xx mění xxx, xx xxxxxxx xxxxxx xx "X 22" xx nahrazují xxxxxx xx "X 65".
2. V příloze XXX xx xxxxxx xxxx xxxx, xxxxx xxx:

3. Xxxxxxx X xxxx X xx xxxx xxxxx:
x) xxxxxxx x xxxxxx úvod x xxxxx X: Xxxxxx pro xxxxxxxxx xxxxxxxx se nahrazuje xxxxxx v xxxxxxx XX A této xxxxxxxx;
x) za xxxxxxxx X.1 x) xx xxxxxx xxxx x xxxxxxx XX X xxxx xxxxxxxx;
x) xxxxxxxx X.6 xx xxxxxxxxx xxxxxx x příloze XX X xxxx xxxxxxxx;
x) xxxxxxxx X.7 xx nahrazuje xxxxxx x xxxxxxx XX X xxxx xxxxxxxx;
x) xxxxxxxx se xxxx x xxxxxxx IV X této směrnice.
4. Xxxxxxx VI xx xxxx x xxx xxxxxxxx xxxxxxxx x xxxxxxx V této xxxxxxxx.
Xxxxxx 2
1. Xxxx xx xxxxxx xxxxxxxx 2, xxxxxxx xxxxx xxxxxx v xxxxxxxx xxxxxx x xxxxxxx xxxxxxxx xxxxxxxx xxx xxxxxxxx xxxxxxx x xxxxx xxxxxxxx xxxxxxxxxx xx 31. května 1998. Xxxxxxx státy x nich neprodleně xxxxxxx Xxxxxx.
2. Xxxxxxxxxx xx 31. xxxxx 1997 xxxxxxx xxxxx xxxxxx v účinnost xxxxxx a xxxxxxx xxxxxxxx nezbytné x xxxxxxxx xxxxxxx x xxxxxxxx V body X, X x X této xxxxxxxx. Xxxxxxx xxxxx x xxxx neprodleně xxxxxxx Xxxxxx.
3. Xxxxxxxx xxxxx xxxxxxxx 1 x 2 xxxxxxx xxxxxxxxx xxxxx musí xxxxxxxxx xxxxx xx xxxx xxxxxxxx xxxx xxxx xxx xxxxxx xxxxx xxxxxx xxx xxxxxx xxxxxxx xxxxxxxxx. Xxxxxx xxxxxx si xxxxxxx xxxxxxx xxxxx.
Článek 3
Xxxx směrnice xxxxxxxx x xxxxxxxx xxxxxxxx dnem xx xxxxxxxxx x Úředním xxxxxxxx Xxxxxxxxxx společenství.
Článek 4
Xxxx směrnice xx určena xxxxxxxx xxxxxx.
V Xxxxxxx xxx 30. xxxxxxxx 1996.
Xx Xxxxxx
Xxxx Xxxxxxxxxxx
xxxxxx Komise
[1] Úř. věst. X 196, 16. 8. 1967, x. 1.
[2] Xx. věst. X 381, 31. 12. 1994, x. 1
XXXXX X — XXXXX I — XXXXXX X — ΠΑΡΑΡΤΗΜΑ X — XXXXX X — XXXXXX X — XXXXXXXX I — XXXXXXX X — XXXXX I — XXXXX X — XXXXXX X — XXXXXXX X
ANEXO XX — XXXXX II — XXXXXX II — ΠΑΡΑΡΤΗΜΑ XX — XXXXX II — XXXXXX II — XXXXXXXX XX — XXXXXXX XX — XXXXX XX — XXXXX XX — XXXXXX II — XXXXXXX XX
XXXXX III — XXXXX XXX — XXXXXX XXX — ΠΑΡΑΡΤΗΜΑ XXX — XXXXX XXX — XXXXXX XXX — XXXXXXXX III — XXXXXXX XXX — XXXXX III — XXXXX III — XXXXXX XXX — XXXXXXX III
Indexové xxxxx

XXXXXXX XX X
" XXXX X: METODY XXXXXXXXX XXXXXXXX X XXXXXX XXXXXX XX XXXXXX
XXXXXX XXXX: ČÁST X
X. XXXXXXXXXXX
Xxx xxxxx xxxxxxxx úvodu xx xxxxxxx xxxx xxxxxxxxx:
X.15 Xxxxxxx na xxxxxx xxxxxx u Xxxxxxxxxxxxx xxxxxxxxxx
X.16 Xxxxxxx na xxxxxxxxxx rekombinaci u Xxxxxxxxxxxxx xxxxxxxxxx
X.17 Xxxxxxx xx xxxxxx xxxxxx x xxxxxxx buňkách xx xxxxx
X.18 Xxxxxxx xx xxxxxxxxx x xxxxxxxx XXX – xxxxxxxxxxxx xxxxxxx XXX – v xxxxxxx xxxxxxx in xxxxx
X.19 Xxxxxxx na xxxxxx xxxxxxxxxxx chromatid in xxxxx
X.20 Xxxxxxx xx xxxxxxxxx xxxxxxx xxxxxx xxxxxx xx xxxxxxx x Drosophila melanogaster
B.21 Xxxxxxx na transformace xxxxxxx buněk xx xxxxx
X.22 Xxxxxxxxxx xxxxxxx xxxxxxx xx hlodavcích
B.23 Xxxxxxxxxxxxx xxxxxxx savčích xxxxxxxxxxx xxxxx in xxxx
X.24 Spot test xx xxxxxx
X.25 Xxxxxxx xx xxxxxxxx xxxxxxxxxxx x myší
B.26 Xxxxxxx xxxxxxxxxxxx orální toxicity: 90xxxxx xxxxxxxxx orální xxxxxxxx xx xxxxxxxxxx
X.27 Xxxxxxx subchronické xxxxxx xxxxxxxx: 90denní opakovaná xxxxxx xxxxxxxx na xxxxxxxxxxxx
X.28 Xxxxxx subchronické xxxxxxxx xxxxxxxx: 90denní xxxxxxxxx xxxxx xxxxxxxx xx hlodavcích
B.29 Xxxxxx xxxxxxxxxxxx inhalační xxxxxxxx: 90xxxxx xxxxxxxxx xxxxxxxxx xxxxxxxx xx xxxxxxxxxx
X.30 Xxxxxxx chronické xxxxxxxx
X.31 Xxxxxxx xxxxxxxxxxxx xx xxxxxxxxxx x nehlodavcích
B.32 Xxxxxxx karcinogenity
B.33 Xxxxxxxxxxx xxxxxxx chronické xxxxxxxx x xxxxxxxxxxxxx
X.34 Xxxxxxxxxxxxxx xxxxxxx toxicity pro xxxxxxxxxx
X.35 Dvougenerační xxxxxxx xxxxxxxx xxx xxxxxxxxxx
X.36 Xxxxxx toxikokinetiky
B. OBECNÉ XXXXXXXX XXXXXXX POUŽITÝCH XX XXXXXXXXXX METODÁCH XXXXXXXXX V TÉTO XXXXXXX
x) Xxxxxx toxicita xxxxxxxx xxxxxxxxxx xxxxxx, xxxxx xx xxxxxxx x xxxxx časovém xxxxxx (obvykle 14 xxx) xx podání xxxxx xxxxx látky.
ii) Xxxxxx toxicita je xxxxxx xxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxx xx xxxxxx xxxxxxxx xxxxx. Xxxx xxxxxxxx xx xxxx xxx xxxxxxxxxx xxxxxxxx xxx xxxxxxxxx xxxxxxxxxxxxx a xxxx xx xxx xxx silné, že xxx xxxxxxx xxxxxx xxxxx xxx xxxxxxxxxxxx xxxxxxxx xxxxxxx xxxxxxxx xxxxxxxx x xxxxxxxxxxxxxx xxxxxxxxx.
xxx) Dávka xx xxxxxxxx xxxxxx xxxxxxxx xxxxx. Xxxxx se xxxxxxxxx xxxx hmotnost xxxxxxxx xxxxx (x xxxxxxx nebo xxxxxxxxxxx) xxxx jako xxxxxxxx xxxxxxxx xxxxx na xxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxx (xxxx. v xxxxxxxxxxx na xxxxxxxx xxxxxxx hmotnosti) xxxx xxxx konstantní xxxxxxxxxxx x xxxxxxx (v xxx xxxx x xxxxxxxxxxx xx xxxxxxxx xxxxxxx).
xx) Diskriminující dávka xx xxxxxxxx xx xxxx fixních úrovní xxxxx, xxxxx xxx xxxxx, aniž xx xxxxxxxx xxxxxxxxx vyvolanou xxxxxx (xxxxxx humánního xxxxxxxx).
x) Xxxxxxxxx je xxxxxx termín xxxxxxxxxx xxxxx, xxxxxxx a xxxxxx podávání xxxxx.
xx) XX50 (xxxxxxx xxxxxxx xxxxx) xx statisticky xxxxxxxxx jednotlivá xxxxx xxxxx, x xxx xxx xxxxxxxx, xx xxxxxxx uhynutí 50 % xxxxxx, xxxxxx xxxx xxxxxx. Hodnota XX50 se xxxxxxxxx x xxxxxxxxx xxxxxxxx xxxxx na jednotku xxxxxxxxx xxxxxxxxx zvířete (x xxxxxxxxxxx na xxxxxxxx).
xxx) XX50 (xxxxxxx xxxxxxx xxxxxxxxxxx) je xxxxxxxxxxx xxxxxxxxx xxxxxxxxxxx xxxxx, u xxx xxx očekávat, xx xxxxxxx xxxxx xxxxxxxx xxxx xx xxxxxx xxxx xx xxxxxxxx xxxxxxx 50 % xxxxxx xxxxxxxxxxxx určitou xxxx.
Xxxxxxx LC50 xx xxxxxxxxx xxxx xxxxxxxx xxxxxxxx látky xx xxxxxxxxxxx objemu vzduchu (x xxxxxxxxxxx na xxxx).
xxxx) XXXXX xx xxxxxxxx zkratka xxx "xx xxxxxxxx xxxxxxx xxxxxx level" (xxxxxxx xxx xxxxxxxxxxxx xxxxxxxxxxxx xxxxxx) x xxxxxxxx xxxxxxxx xxxxxx dávky xxxx xxxxxxxx, xxx xxxxx xxxxxx xxxxxxxxxx xxxxx nepříznivé nálezy xxxxxxxxxxx x xxxxxxx xxxxx.
xx) Xxxxxxxxxxxx xxxxxxxx xxxx xxxxxxxx při xxxxxxxxx dávce xxxxxxxx xxxxxxxxxx xxxxxx, xxxxx xx projeví x xxxxxxxxx zvířat xxxx xxxxxxxx xxxxxxxxxxx xxxxxxx xxxxxxxx xxxxxxxx xxxxx xxxx opakované xxxxxxxx xxxxxxxx látce po xxxx xxxxxxxxxxxxx xxxxxx xxxx xxxxxxxxx xxxxx xxxxxx xxxxxxxxx xxxxxx.
x) Xxxxxxxxx tolerovaná dávka (XXX) je nejvyšší xxxxxx xxxxx, která x zvířat xxxxxx xxxxxx toxicity, xxxx xx měla xxxxx xxxxxxx, xx xxxxx xx xxxxxxx, xxxxx xxxx xx xxxxxxx xxxxxx.
xx) Xxxxx dráždivostí xx xxxxxx xxxxxxxx xxxxxxxxxxx změn xx xxxx xx xxxxxxxx xxxxxxxx látky.
xii) Oční xxxxxxxxxxx xx xxxxxx xxxxxxxx xxxx x xxx xx xxxxxxxx xxxxxxxx xxxxx xx xxxxxx oka.
xiii) Xxxxxxxxxxxxx xxxx (xxxxxxxxx kontaktní xxxxxxxxxxx) xx imunologicky xxxxxxxx xxxxxx xxxx xx xxxxx.
xxx) Poleptání xxxx je xxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxx xxxxx xx aplikaci xxxxxxxx xxxxx xx xxxx xx 3 xxx do 4 x.
xx) Xxxxxxxxxxxxxx je xxxxxx xxxxxxxx, xxxxxxxxxx, xxxxxxxxxxx a xxxxxxxxxx xxxxxxxxxx látek.
xvi) Absorpce xx proces, xxxxxx xxxxxx látka xxxxxxxx xx xxxx.
xxxx) Vylučování xx xxxxxx, kterým xxxx podaná xxxxx x/xxxx xxxx xxxxxxxxxx xxxxxxxxx x xxxx.
xxxxx) Xxxxxxxxxx xx xxxxxx, xxxxxx je xxxxxxxxxxx xxxxx a/nebo xxxx xxxxxxxxxx rozděleny x xxxx.
xxx) Xxxxxxxxxxxx je xxxxxx, xxxxxx xx xxxxxx xxxxx v xxxx xxxxxxxxxx xxxxxx xxxxxxxxxxxxx xxxx neenzymatickými xxxxxxxx.
X.1 Xxxxxx xxxxxxxx xxx opakované dávce/subchronická x xxxxxxxxx toxicita
Akutní xxxxxxx xxxxxx látky x xxxx xxxxxxxxx xxxx xxxxxxxxxx toxicitu xxx xxxxxxxxx za xxxxxxx xxxxxxx xxxxxxx (xxxxxx X.1 – X.5), xxxxx xx xxxxxx jediné xxxxx xxxxxxxxx xxxxxxxxx xxxxx x toxicitě.
V xxxxxxxxxx xx toxicitě xxxxx xxx xxxxxx xxxxxxx xxxxxxx xxxxxxx xxx xxxxxxxxx XX50, xxxxxxx x xxxxxxxxxxx xxxxxxxx xxxx xxxxxxx xxxxx xxxxxxx xxxxxxx, xxxxxxx xxxxxx xxxxx xxxxxxxxx xxxxxxx xxxxxxx xxxxxxx xxx xxxxxxxxxxxx xxxxxxxxx xxxxxxxx.
Xxxx by xxx xxxxxxxxxxxxx xxxxxx, xxx xxxxx xx xxxxxxx xx nejméně zvířat x xxxxx minimalizují xxxxxx xxxxxxx, xxxxxxxxx xxxxxx xxxxx xxxxx (xxxxxx X.1 x)) x xxxxxx stanovení xxxx xxxxxx toxicity (xxxxxx B.1 x)). X zkoušek na xxxxxx 1 xxxx xxxxxx získané z xxxxx xxxxxx xxxxxxx xxxxxx na xxxxx xxxxx. X xxxxxxx xxxxxxx xxxx xxx xxxxxxx xxxxxxxxxx xxxxxxxx xxxxxx nebo může xxx xxxxxx xxxxxxxx xxx xxxxx xxxxx xxxxxx.
Xxxxxxx toxicity xxx xxxxxxxxx xxxxxxxx (xxxxxx X.7, B.8 x X.9) xxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxx v xxxxxxxx opakované xxxxxxxx. Xxxxx xx xxxxx xx pečlivé klinické xxxxxxxxxx xxxxxx x xxxxx získat xx xxxxxxx informací. Xxxx xxxxxxx by xxxx xxxxxx zjistit xxxxxx xxxxxx xxxxxxxx x xxxxxxx x xxxxxxxxx xxxxx. Xx xxxxxxxxxxxx xxxxxx xx xxxxxxxx xxxxx xxxxxx xxxxxxx xxxxxx xxxxxxx (metody X.26 – X.30 x X.33).
X.XX Xxxxxxxxxx – Genotoxicita
Mutagenitou xx xxxxxx xxxxxxxx xxxxxxxx, xxxxxxxxxx změn množství xxxx xxxxxxxxx xxxxxxxxxxx xxxxxxxxx buněk nebo xxxxxxxxx. Tyto změny, "xxxxxx", se xxxxx xxxxx jediného xxxx xxxx segmentu genů, xxxxxx xxxx xxxx xxxxxx xxxxxxxxxx. Účinky xx xxxx xxxxxxxxxx xxxxx xxxxxxx xxxxxxxxxx x/xxxx xxxxxxxxx xxxxx.
Xxxxxxxxx xxxxxxxx látky xx xxxxxxxx xxxxxxxxx in xxxxx xx xxxxxx (xxxxxx) mutace x xxxxxxxxxx (xxxxxx X.13/14) x/xxxx xx strukturní xxxxxxxxxxxx xxxxxxx v xxxxxxx xxxxxxx (xxxxxx X.10).
Xxxxxxxxxx xxxx také xxxxxxx xx vivo, xxxx. test xxxxxxxxxx (xxxxxx X.12) xxxx xxxxxxx xxxxxxxx xxxxx xxxxxx xxxxx (metoda X.11). Neexistují-li xxxx xxxxx xxxxxxxxxxxxxx, xxxxxxx xx doporučují xxxxxx xx vitro.
Dodatečné xxxxxx xxxxxxxxxxx xxxxxxxxxx xxxxx xxxx provedení předběžných xxxxxxx karcinogenity xxxxx xxx xxxxxxxx xxx xxxxx xxxxxxxx ve xxxxxxx xxxxxxxxxx xxxx xxx xxxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxx x xxxxx být xxxxxxx x několika xxxxxx: xxx xxxxxxxxx xxxxxxxx xxxxxxxxx v xxxxxxxx xxxx zkoušek, xxx xxxxxxxx xxxxxxxxx, xxxxx xxxxxx xxxxxxxxx x xxxxxxxx xxxx xxxxxxx, xxx xxxxxxxx nebo xxxxxxxxx studií xx xxxx.
Xxx xxxx xxxxx xxxxxxxx xxxxxx X.15 xx X.25 xxxxxxxxxxxx xxxxxxx xx xxxx x xx xxxxx x xxxxxxxxxx řadu xxxxxxxxxxxx xxxxxxxxx. Xxxx xxxxxxx xxxxxxxxx xxxxxxxxx x xxxxxxxx xxxxxxxx x o xxxxxx xxxxxxxxxxx u xxxxxxxxx xxxxxxxxxxxx než xxxxxxxx xxxxxxxxx xxx xxxxxxxx xxxx zkoušek.
Obecně xxxxx, xx xx-xx zvažován xxxxxxx xxxxxxx xxxxxx xxxxxxxxxx, xxx by xxx xxxxxxx xxx, xxx xxxxxxx příslušné xxxxxxxxxx xxxxxxxxx x xxxxxxxxxx x/xxxx xxxxxxxxxxxxx xxxxxxxxxx xxxxx.
Xxxxx xxxxxx, xxxxx mohou xxx xxxxxx xxx xxxx xxxxxx, závisí xx xxxxx faktorech, včetně xxxxxxxxxx x xxxxxxxxxxx xxxxxxxxxx xxxxx, xxxxxxxx xxxxxxxxxx bakteriálních a xxxxxxxxxxxxxxx zkoušek, xxxxxxxxxxxxx xxxxxxx látky, výsledků xxxxxxx xxxxxx xxxxxxxx x známých xxxxxxx xxxxxxx látky. Xxxxx xxxxxx xxxxxx xxxxxxx xx tedy xxxxxxxx, x xxxxxxx xx xxxxx xxxxx xxxxxxx, xxxxx xxxxx xxxxxxxxx xxxxxxx.
Xxxxxxx xxxxxx xxxxxxxx xxxxxxxxx zkoušení xxxx xxxxxxxxx xx xxxxxxxx 93/67/XXX, ale xxxxxx xxxxxxxxx xxxxxxxx xx xxxxxxxxx v metodických xxxxxxxx xxx hodnocení xxxxxx, jsou xxxx xxxxxx x lze xx upravit tak, xxx xxxxxxxxxx xxxxxxxxxxx xxxxxxxxxx.
Xxxxxx pro xxxxx xxxxxxxxxxx xxxx xxxxxxx xxxx xxxxxxxxx xx xxxxxxx xxxxxx hlavního xxxxxxxxxxxxx genetického xxxxxx:
Xxxxxx xxxxxxxxxx genové (xxxxxx) xxxxxx
x) Studie xxxxx xxxx xxxxxx mutace x xxxxxxxxxxxxxx mikroorganismů (Xxxxxxxxxxxxx xxxxxxxxxx) (xxxxxx X.15).
x) Studie xxxxxxx xxxxxx x xxxxxxx xxxxxxx xx vitro (xxxxxx X.17).
x) Xxxxxxx xx xxxxxxxxx letální xxxxxx xxxxxx na xxxxxxx u Xxxxxxxxxx xxxxxxxxxxxx (metoda B.20).
d) Xxxxxxx xx xxxxxxxxx xxxxxx buněk xx xxxx, spot xxxx xx xxxxxx (xxxxxx X.24).
Xxxxxx xxxxxxxxxx chromosomové xxxxxxx
x) Xxxxxxxxxxxxx xxxxxx xx xxxxxxx xx xxxx; xxxx xx xxx xxxxx x xxxxx xxxxxxx xxxxxxxx xxxxx kostní xxxxx, xxxxx nebyla xxxxxxxx xx xxxxxxxxxx xxxxxxxxx (xxxxxx X.11). Kromě xxxx xxxx xxx xxxxxxxxx xxxx xxxxxxxxxxxxx xxxxxxx zárodečných buněk xx xxxx (xxxxxx X.23).
x) Xxxxxxxxxxxxx studie xx xxxxxxx xxxxxxx xx xxxxx, xxxxx xxxxxx xxxxxxxx xx xxxxxxxxxx xxxxxxxxx (X.10).
x) Xxxxxxxxxx xxxxxxx xxxxxxx xx xxxxxxxxxx (xxxxxx X.22).
x) Xxxxxxx na xxxxxxxx xxxxxxxxxxx u xxxx (xxxxxx X.25).
Xxxxxxxxxxx xxxxxx – účinky xx XXX
Xxxxxxxxxxxx, xxxxx xx dána xxxxxxxxxxx xxxxxxxxxx xxxxxx na xxxxxxxxx xxxxxxxx, xxxx xxxx xxxxxxxx spojen x xxxxxxxxxxx, se xxxx xxxxxxxx jako xxxxxxxxxx xxxxxxxxx XXX xxx xxxxxxx xxxxxx xxxxxx. Xxx xxxxxxxx xxxxxx xxxx xxxxx xxx xxxxxx xxxxxxxxxxx xxxxxx používající xxxxxxxxxxxx xxxxxxxxxxxxxx xxxx buňky xxxxx:
x) Xxxxxxxxx xxxxxxxxxxx x Saccharomyces xxxxxxxxxx (xxxxxx B.16).
b) Xxxxxxxxx x reparace XXX – xxxxxxxxxxx xxxxxxx XXX v savčích xxxxxxx – xx xxxxx (xxxxxx X.18).
x) Xxxxxx sesterských xxxxxxxxx x savčích buňkách – xx xxxxx (xxxxxx X.19).
Xxxxxxxxxxxx xxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxxx
Xxxxxxx xx xxxxxxxxxxxx savčích xxxxx xxxxxxxx xxxxx xxxxxxxxx látky xxxxxxx xxxxx xxxxxxxxxx x xxxxxxx x buněčných xxxxxxxxx, u xxxxx xx xxxxxxxxxxx, xx xxxxxxxxx x xxxxxxx xxxxxxxxxxxx – xx xxxx (xxxxxx B.21). Xxxxxxx xxxxx xxx xxxxx xxxx buněk x xxxxx kritéria xxxxxxxxxxxx.
Xxxxxxxxx xxxxxx xxxxxxxxx xxxxxx x xxxxx
Xxxxxxxx xxxxxxx xxxxx xxxxxxxxxxxx xxxxx x xxxxx xxxxxxx účinky xxxxxxxx xxxxxxxxxxx (bodovými) mutacemi, xxxx. xxxxxxx na xxxxxxxxxx xxxxxxxx xxxx x chromosomu u xxxx xxx xxxxxx xxxxxx xxxxxxxxxxx xxxxx x xxxxx xxxxxxxx (xxxxxxxxxx xx xxxx xxxxxxx), xxxx xxx xxxxxxxxxxxx xxxxxxx, xxxx. xxxxxxx na xxxxxxxx xxxxxxxxxxx x xxxx (xxxxxx X.25). Tyto xxxxxx xxx xxxxxx xxx xxxxx možného xxxxxxxxxxx xxxxxx, xxxxx xxxxx xxxxxxxxxxx pro xxxxxxx. Vzhledem xx xxxxxxxxxx těchto xxxxxxx x x xxxxxxxx xxxxxxxxxx xxxxx zvířat, xxxxxxx xxx xxxxxxx xx xxxxxxxxxx umístění xxxx x xxxxxxxxxx, xx xxxx nezbytné xxxxx zdůvodnění xxxx xxxxxxxxxx xxxxxx xxxxxx.
X.XXX Xxxxxxxxxxxxx
Xxxxxxxx xxxxx xxxxx xxx xxxxxxxxxx xx xxxxxxxxxxx nebo negenotoxické xxxxxxxxxxx v závislosti xx předpokládaném xxxxxxxxxx xxxxxxxx.
Xxxxxxxxx xxxxxxxxx o xxxxxxxxxxxx xxxxxxxxxxxxx xxxxxxxxxx xxxxx xxx xxxxxx xx studií xxxxxxxxxx/xxxxxxxxxxxx. Xxxxxxxxx informace xxx xxxxxx xx xxxxxxx xxxxxxxx xxx opakované xxxxxxxx x ze xxxxxxx xxxxxxxxxxxx x xxxxxxxxx xxxxxxxx. Xxxxxxx xxxxxxxx xxx xxxxxxxxx xxxxxxxx, xxxxxx X.7, x xxxxxxxxxxxxx studie xxxxxxxx xxx opakované xxxxx zahrnují posouzení xxxxxxxxxxxxxxxxxx změn xxxxxxxxxxxx xxx xxxxxxxxx xxxxxxxx xxx xxxxxxxxx dávce, xxxx. hyperplasie xxxxxxxx xxxxx, xxxxx xxxxx xxx předmětem xxxxx. Xxxx xxxxxx x xxxxxxxxxxxxxxx xxxxxxxxx xxxxx xxxxxx xxxxx chemické xxxxx x xxxxxxxxxxxxx xxxxxxxxxxx, x xxxxx xxxx být nezbytné xxxxx xxxxxx xxxxxxxx xxxxxx aspektu pomocí xxxxxxx karcinogenity (metoda X.32) xxxx často x kombinované xxxxxx xxxxxxxxx toxicity/karcinogenity (metoda X.33).
X.XX Toxicita pro xxxxxxxxxx
Xxxxxxxx xxx xxxxxxxxxx xxx xxxxxxxxx xxxxxxx xxxxxxx, např. xxxxxxxxxx xxxxxxxxxxxxx xxxxxx xxxx xxxxxxxxxx samců a xxxxx, xx. "vlivy xx xxxxxxxx", nebo xxxxxxxxx nedědičných xxxxxxxxxx xxxxxx xx xxxxxxxxx, xx. "xxxxxxxxx xxxxxxxxx", xxxxx xxxxxxxx xxxx xxxxxxxxxxxx a účinky x xxxxxxx laktace.
Pro xxxxxx xxxxxxxxxxxx xxxx xxxxxxxx xxxxxxxx vývojové xxxxxxxx je xxxxxxxx xxxxxx (xxxxxx X.31) xxxxxxxx zaměřena xx xxxxxx xxxxxxxx. X xxxxxxxxxx xx xxxxxxxxxxx xxxxxxxxxxxx xxxxxxxx xxxxx xxxx xx xxxxxxxxxxxxxx xxxxxxx xxxxxxxx člověka xxxxx xxx xxxxxxx xxxx xxxx xxxxxxx xxxxxxxx. X xxxxxxxx xxxxxxxxx by měla xxx xxxxxxxx xxxxxx xxxxxx upravena x xxxxxxx xx xxxxxxxxx xxxxx 28xxxxxxx zkušebních xxxxx.
Xx-xx xxxxxxxx xxxxxxxxxxxx xxxxxxx xxxxxxxxxx (plodnosti), xxxx xxx xxxxxxx xxxxxx dvougenerační zkoušky xxxxxxxxxx (xxxxxx B.35) xxxxxxxxx tak, xxx xxxxxxxxx třetí xxxxxxxx.
X.X Xxxxxxxxxxxxx
Xxxxxxxxxxxxx xxx xxxxxxxxx xxxxxxx způsoby, xxxx. xxxxxxxxx xxxxxxx x/xxxx xxxxxxxxxxxx a xxxxxxxxxxxxx xxxxxxx centrálního x xxxxxxxxxxx nervového systému. Xxxxxxxxx xxxxxxxx xxxxxxxxxxxxx xxx zjistit zkouškami xxxxxx toxicity. Zkouška xxxxxxxx xxx xxxxxxxxx xxxxx, xxxxxx X.7, xxxxxxxx xxxxxxxxx xxxxxxxxxxxxxx xxxxxx x xxxxx xx xxxxx xx xxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxxx x xxxxx xxxxxx xx xxxxxxx xxxxxxxxx. Xxxxxx xx měla xxxxxx xxxxxxx xxxxxxxx látky x neurotoxickým xxxxxxxxxxx, x nichž xxxx xxx xxxxxxxx xxxxx xxxxxx xxxxxxxxxxx xxxxxx xxxxxxx. Xxxxx xxxx xx xxxxxxxx xxxxxx xxxxxxxxx xxxxx xxxxxxx xxxxxxxxxx xxxxxxxxxxxx xxxxxx, xxxxx nemusí xxx xxxxxxxx xxxxxx studiemi xxxxxxxx. Xxxxxxxxx u xxxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxxx xxxx xxxxxxxxxx, xx vyvolávají xxxxxx xxxxxxxxxxxxx, a xxxxxxxx xx xxxxxxxx B.37 x X.38 xx xxxxxxxxxxxx xxxx xxxxxxxxxx xxxxxx.
X.XX Xxxxxxxxxxxxx
Xxxxxxxxxxxxx xxx xxxxxxx xxxxxxx způsoby, xxxxxxxxx imunosupresí x/xxxx xxxxxxxx odpovědi imunitního xxxxxxx xxxxxxxx x xxxxxxxxxxxxxxxx nebo xxxxxxxx xxxxxxxxxxx. Zkouška xxxxxxxx xxx xxxxxxxxx xxxxx, xxxxxx X.7, zahrnuje xxxxxxxxx imunotoxických xxxxxx. Xxxxxx xx xxxx xxxxxx odhalit xxxxxxxx xxxxx s xxxxxxxxxxxxx xxxxxxxxxxx, x xxxxx xxxx být nezbytné xxxxx xxxxxx zkoumání xxxxxx xxxxxxx.
X.XXX Toxikokinetika
Toxikokinetické xxxxxx xxxxxxxx xxx xxxxxxxxxxxx x xxxxxxxxxxx xxxxx x xxxxxxxx. Xxxx studie jsou xxxxxx k objasnění xxxxxxxx xxxxxxx xxxxxxxx xxxxxxxx chemické xxxxx x výsledky mohou xxxxxx xxx plánování xxxxxxx xxxxxx xxxxxxxx. Xxxxxxxxxxxxx xx, xx xx bylo xx xxxxx případech xxxxxxxx xxxxxxxx xxxxxxx xxxxxxxxx. Xxxxx xx vzácných xxxxxxxxx xxxx xxxxxxxx xxxxxxx xxxxxx xxxx xxxxxxxxxxxxxxxxx xxxxxx (xxxxxx xxxxxxxx, xxxxxxxxxx, xxxxxxxxxx x xxxxxxxxxxx). Xxx xxxxxx xxxxxxxxxx mohou xxx vhodné změny xxxx xxxx xxxx xxxx xxxxxx xxxxxx x jedinou dávkou (xxxxxx X.36).
Xxxxx x xxxxxxxx struktuře (SAR) x fyzikálněchemických vlastnostech xxxxx též xxxxxxxxxx xxxxxxxxx x absorpčních xxxxxxxxxxxxxxxxx x xxxxxxxxxxx xxxxxxx xxxxxx a x xxxxxxxxxx xxxxxxxxxxxxx xxxxxxxxxx x xxxxxxxxxx xxxxx x xxxxxxx. Xxxxx xxx existovat xxxxx o toxikokinetických xxxxxxxxxxx x xxxxxxxxxx xxxxxx xxxxxxxx x x xxxxxxxxxxxxxxxxx xxxxxx.
X. XXXXXXXXXXXXXX ZKOUŠENÉ XXXXX
Xxxxxxx xxxxxxxx xxxxx, včetně xxxxxxxx nečistot, x xxxx relevantní fyzikálně-chemické xxxxxxxxxx, včetně xxxxxxxx, xx měly xxx xxxxx xxxx zahájením xxxxxxxx xxxxxx xxxxxxxx.
Xxxxxxxxx-xxxxxxxx xxxxxxxxxx xxxxxxxx xxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx xxx xxxxx xxxxxxx xxxxxxxx, xxx návrh xxxxx xxxxxxxxxx xxxxxx x pro xxxxxxxxxx xx xxxxxxxxx xxxxxx x její xxxxxxxxxx.
Xxxxxxxx xxxxxx xx měl xxxxxxxxxx xxxxx xxxxxxxxxx xxxxxx xxx xxxxxxxxxxxx x xxxxxxxxxxxxx xxxxxxxxx xxxxxxxx xxxxx (xxxxx xxxxx včetně hlavních xxxxxxxx) x xxxxxxxxxx xxxxx x v xxxxxxxxxxx materiálu.
Veškeré xxxxxxxxx xxxxxxxx xx xxxxxxxxxxxx, xxxxxxxxx-xxxxxxxxxx vlastností, xxxxxxx x xxxxxxx xxxxxxxx xxxxx by xxxx xxx obsaženy x xxxxxxxxx x xxxxxxx.
X. XXXX X XXXXXXX
Xxx xxxxxxxx toxicity xxxx xxxxxxxx xxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx x xxxxxxx péče o xxxxxxx.
x) Xxxxxxxx xxxxx
Xxxxxxxx xxxxx x prostorech xxxx xxxxxxx pro xxxxxxx zvířata xx xxxx xxxxxxxxx testovacím xxxxxx. Pro xxxxxxx, xxxx a xxxxxxx xxxx xxxxxxxx xxxxxxxxxx xxxxxxx xxxxxxxxx 22 ±3 °X x xxxxxxxxx xxxxxxx 30 xx 70 %; xxx xxxxxxx se xxxxxxxxxx teplota 20 ±3 °X x xxxxxxxxx xxxxxxx 30 xx 70 %.
Xxxxxxx xxxxxxxxxxxxxx xxxxxxxx xxxx xxxxxxx citlivé xx xxxx xxxxxxx a x xxxxxxxx xxxxxxxxx xxxx x xxxxxx xxxxxxxx xxxxxx uvedeny xxxxxxxxxxx o xxxxxxxx xxxxxxxxxx. Xxx xxxxx xxxxxxxxxxx xxxxxxxxx xxxxxx xx xxxx být xxxxxxxxxxxxx údaje x xxxxxxx a xxxxxxxx x xxxx xx xxx zahrnuty xx xxxxxxxxx zprávy x xxxxxx.
Xxxxxxxxx xx mělo xxx xxxxx x xxxx by xx xxxxxxx 12 h xxxxxx a 12 x xxx. Xxxxxxxxxxx x xxxxxxxxx xxxxxx xx xxxx xxxxxxxxxxx x xxxxxxx x xxxxxxx xxxxxx xxxxxx.
Xxxx-xx x metodě xxxxxxx xxxxx, xxxx xx xxx xxxxxxx xxxxxxx xxxxxxxxxx xxxx umístěna x klecích xx xxxxxx xxxxxxxxx stejného xxxxxxx; xxxx-xx zvířata x xxxxxxx po xxxxxxxxx, nemělo xx xxx chováno x xxxxx xxxxx xxxx xxx pět xxxxxx.
Xx xxxxxxxx x xxxxxxxxxxxxx xx xxxxxxxxx je xxxxxxxx xxxxx xxx xxxxxxx xxxxx a xxxxx zvířat chovaných x xxxxx xxxxx xxx xxxxx xxxxxxxx xxxxxxxx látce, xxx xxxxx kterékoli xxxxx xxxx xxxxxxxxxx.
xx) Xxxxxxxx xxxxxx
Xxxxxx xx xxxx xxxxxxxx xxxxxxx požadavky xxxxxx pro xxxxxxxxx xxxxxxxxx xxxx. Pokud xxxx zkoušené látky xxxxxxxx x xxxxxxx, xxxx xxx xxxxxxxx xxxxxxx xxxxxxx xxxxxxxxx xxxxx x některou xxxxxxx potravy. Xxxxxxx xxxxxx xxxxxx xx xxxx být zohledněna xxx interpretaci výsledků xxxxxxx. Xxxx xxx xxxxxxx xxxxxxxxx xxxxxxxxxxx xxxxxx s xxxxxxxxxx xxxxxxxxx x pitné xxxx. Výběr xxxxxxx xx xxxx xxxxx xxxxxxxx xxxxxxxx xxxxxx xxxxxxxxxx xxxxxxxx látky, xxxxx xx podávána xxxxx metodou.
Příměsi x xxxxxxx, xxxxxxx xxxx xx xxxxxxxx xx xxxx, xxxxx xxx xxxxxxxx x xxxxxxxxxxxxx, xx xxxxxxx xx xx vliv xxxxxxxx.
X. XXXXXXX XXXXXX
Xxx xxxxxxxxxxxxx xxxxxxxxxx metod xxxx xxxxxxxx pozornost xxxxxxxx xxxxxxx xxxxxx. Některé xxxxxxxx jsou xx xxxxxxxxxx xxxxxxx xxxx, xxxxx xxxxxx však xxxx xxxxxxxxxxxxx. Xxxxxx xxxxx x/xxxx xxxxxxxx xx xxxxx vyhledat x textu xxxxx:
- Xxx xxxxxxxxx xxxxxx xxxxxx xxxxxxxx by xxxx xxx xxxxxxx xxx xxxxxx, "metoda xxxxx xxxxx" x "xxxxxx stanovení tříd xxxxxx xxxxxxxx". V "xxxxxx xxxxx xxxxx" xx nepoužívá xxxxxxx xxxx xxxxxxxxxx xxxxxxxx x xxxxxxx se x xx méně xxxxxx. X "xxxxxx xxxxxxxxx xxxx xxxxxx xxxxxxxx" xx xxxxxxx x xxxxxxx o 70 % xxxxxx xxxx než x xxxxxx X.1 xxxxxxxxx xxxxxx xxxxxx xxxxxxxx. Xxx tyto alternativní xxxxxx xxxx xx xxxxxxxx xxxxx utrpení x bolest než xxxxxxxx xxxxxx.
- Xxxxx xxxxxxxxx xxxxxx xx xxxxxx xx xxxxxxx xxxxxxxxxx minimum: x xxxxxxxx X.1 a X.3 xx ke xxxxxxxx xxxxxxx pouze 5 xxxxxx xxxxxxxx xxxxxxx xxx xxxxx xxxxxx xxxxx; xxx xxxxxxxxx senzibilizace xxxx xxxxxxxxxxxxx xxxxxxxx na xxxxxxxxx (xxxxxx B.6) xx xxxxxxx pouze 10 zvířat (x xxxxx 5 xxx xxxxxxxxx kontrolní xxxxxxx); xxxxx xxxxxx xxxxxxxxxx xxx xxxxxxxxx xxxxxxxx xxx xxxxxxxx mutagenity xx xxxx se xxxxxx snižuje (xxxxxx X.11 x B.12).
- Xxxxxx x utrpení xxxxxx xxxxx zkoušek xxxx minimalizovány. Xx xxxxx xxxxxxx xxxxxxx xxxxxxx xxxxxxxxxx xxxxxxx x xxxxxxxxxxxxx známky xxxxxxx; xxxxxxx xx xxxxxxx xxxxxxxx xxxxx, x nichž je xxxxx, xx xxxxxxxxx xxxxxxxxx xxxxxx x xxxxxxx x xxxxxxxx xxxxxxxx x xxxxxxxxxx xxxxxxxxxx látky (xxxxxx X.1, X.2 x X.3).
- Zkoušení x xxxxxxxxxxx xxxxxxxx dávkami xx xxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxx, x xx xxxxxx xxxxx xxx xxxxxxxxx akutní xxxxxxxx (xxxxxx X.1, X.2 x X.3), xxx xxxxxx xxx xxxxxxxxx xxxxxxxxxx xx xxxx (xxxxxx B.11 x X.12).
- Xxxxxxxxx xxxxxxxx xxxxxxxxxxx xxxx xxxxxxxx neprovádět xxxxxxx, xxxx xx omezit xx studii x xxxxxx xxxxxxxx, xxxxx xx xxxxxxxxxx vědecky xxxxxxxxx.
Xxxx vědecké zdůvodnění xxxx být xxxxxxxx xx fyzikálněchemických vlastnostech xxxxx, xx xxxxxxxxxx xxxxxxxxxx na xxxxxx xxx xxxxxxxxxxx xxxxxxxxx xxxx na xxxxxxxxxx xxxxxxxxxx xxxxxxxxxxxx xxxxxxx xx xxxxx. Bylali xxxxxxxxx xxxxxx akutní xxxxxxxx xxxxxxxxx na xxxx provedena x xxxxxx xxxxx xxxxxxxxxxxx x xxxxxxx xxxxxxx (xxxxxx X.3) x xxxxxx pozorována žádná xxxxx xxxxxxxxxx, xxxx xxx další zkoušení xxxxx xxxxxxxxxxx (xxxxxx X.4) xxxxxxxx; xxxxxxxxx, xxxxx ve studii xxxxx xxxxxxxxxxx (xxxxxx X.4) xxxxxxxx nepochybné xxxxxx xxxxxx nebo xxxxx xxxxxxxxxx xxxx, xxxxxxx být xxxx xxxxxxxx xx xxxx xxxxxxxxxx (xxxxxx X.5).
X. XXXXXXXXXXXX XXXXXXX
Xxxxxxxx xxxxx Xxxxxxxx xxxx xx xxxxx x xxxxxxxx xxxxxxxxxxxxxx metod, které xxxxx poskytnout xxxxxxx xxxxxx informací xxxx xxxxxxxx xxxxxxx xx xxxxxxxxx, při xxxxx xx však xxxxxxx xxxx xxxxxx, způsobí xxxx utrpení xxxx xx v xxxx xxxxxxx xxxxxx xxxxx xxxxxxxx.
Xxxx po xxxx xxxxxxx xx praxe xxxx xxx tyto xxxxxx xxxxxxx, xxxxxxx xx xx xxxxx, xxx charakterizaci nebezpečnosti x xxxxxxxxx xxxxxxxxxxx x xxxxxxxxxx xxxxx x xxxxxxxx xxxxxx xxxxxxxxxxxxx.
X. XXXXXXXXX A XXXXXXXXXXXX
Xxx hodnocení x xxxxxxxxxxxx xxxxxxx xxxx xxx xxxxx x xxxxx xxxxxx meze, xxxxxxx xxx xxxxxxxx xxxxxx na xxxxxxxxx x xx xxxxx xxxxxxxxxxxx xx xxxxxxx, x xxxxx xxx xxx potvrzení xxxxxxxx xxxxxxxx použít xxxxxxxx x nepříznivých účincích xx člověka, xxxxx xxxx k dispozici.
Tyto xxxxxxxx lze xxxxxx xxx klasifikaci a xxxxxxxxxx xxxxxx x xxxxxxxxxxxx xxxxxxxxxx xxxxx x xxxxxxxx xxxxxx xx xxxxxx xxxxxx, xx základě xxxxxx xxxxxxxxxx xxxxxxxxxx xxxxxxxxxx x xxxxxxxxxxxxxxxx xxxxxx xxxxxxxx. Xxxxxxxxxxxx kritéria xxx klasifikaci x xxxxxxxxxx uvedená x xxxxxxx XX xx xxxxxxxx také xx xxxxxxxxx xxxxxxxx x xxxxxx zkušebních xxxxxxxx, xxxxx xxxx xxxxxxx x xxxxxxxxxxx x xxxxxxx.
Xxxx výsledky lze xxxx xxxxxx xxx xxxxxx xxxxxxxxx rizika xxxxxx a existujících xxxxxxxxxx xxxxx; vhodné xxxxxxxx xxxxxxxxx xxx xxxx xxxxx xxxx xxxxxxx x příslušných xxxxxxxx.
X. XXXXXX XX XXXXXXXXXX
Xxxx xxxxxx xxxx xxxxxxxx xxxxxxxx x xxxxx programu OECD xxx xxxxxxxx xxxxxx x měly xx xxx xxxxxxxxx x xxxxxxx s principy xxxxxxx xxxxxxxxxxx xxxxx, xxx bylo xxxxxxxxx xx xxxxxxxx "xxxxxxxx xxxxxxxx xxxxx".
Xxxxx podobnější xxxxxxxxx lze xxxxxx x xxxxxxxx XXXX x v xxxxxxxxx xxxxxxxxxx xxxxxxxxxxx xxxxx."
XXXXXXX XX X
" X.1 x) AKUTNÍ XXXXXXXX (XXXXXX) – XXXXXX STANOVENÍ XXXX XXXXXX XXXXXXXX
1. XXXXXX
1.1 Xxxx
Xxxxxx xxxxxxxxx xxxx xxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxx xxx pro xxxxx hodnocení nebezpečnosti, xxx xxx účely x xxxxxxxxxxx xxxxx x xxxxxxxx xxxxxxxxxxxxx.
X xxxxxx xx xxxxxxxxx xxx fixní xxxxx xxxxxxxx x xxxxxxxxxxx xxxxxxxxx, xxx xxxx xxxxx xxxxx zatřídit xx xxxxxxx xxxxxxxx xxxxxx. Xxxxx xxxx xxxxxx xxxxxxx x xxxx zkušební xxxxxx xxxxxxxx xxxxx tří xxxxxxxxxxx fixních xxxxx, xxxxx xxx použít xxxx xxxxxxxxxxxx xxxxx x určitých bodech xxxxxxxxxxxxx xxxxxxx, xxxx xxx xxxxx xxxxxxxx. Xxxxxxx některé x xxxxxx doplňkových xxxxx xxx uvážit x xxxxxxx, xx by xxxxx xxx xxxxxxx xxxx xxxxxxxx další xxxxxxxxx.
Xxxxxx xxxxxxx xxxxx xxxxxxxxx xxxxxxxxx dávky x xxxx určena xxx xxxxxxx xxxxxx xxxxxxx XX50, xxxxxxxx xxxx stanovení xxxxxxx xxxxxxxx, x xxxx xx xxxxxxxxxxx xxxxxxxx, xxxxxxx uhynutí xxxxx xxxxxx xxxxxxx hlavním xxxxxxxxxx xxxxxxx. Xxxxxxxx xxxxxxx xx xxxx xxxxxxx klasifikaci xxxxx xxxxxxxx v příloze XX. Xxxxxxxx x xxxxxxxxx xxxxxxx by xxxxx xxx xxxxxx xxxxxxx delší než x xxxxxxx popsaného x xxxxxx X.1. Xxxxxx výhodou této xxxxxx je, že xxxxxxxx xxxxx počet xxxxxx než metody xxxxxx xxxxxxxx (xxxxxx) (X.1.) x xxxxxxxxxxxx xxxxxx xxxxx xxxxx (X.1 a)).
Viz xxxx xxxxxx úvod, xxxx X.
1.2 Xxxxxxxx
Xxx xxxxxx xxxx, xxxx X.
1.3 Xxxxxxxx xxxxxxxx xxxxxx
Xxxxx xx xxxxxx xxxxxx xxxxxxx xxxxxxxxx xxxxxx x xxxxx xx xxxxxxxxxxx xxxxx. Látka xx xxxxxx postupně, xxxxxxx xxx xxxxxx xxxxx xx xxxxxxx xxx zvířata xxxxxxxx xxxxxxx. Není xxxxxxxx xxxxxxxx xxxxxxxxxx orientační xxxxxx. Xxxxxxx xxxx xxxxxx xxxxx zvířat, xxxx byla xxxxx xxxxxx x prvním xxxxx, xxxxxx xxxxx xxxx, tj.
- xxxxx xxxxxxxx xxxx xxxxxxxxx,
- xxxxx xxxx xx xxxxxxx xx stejnou xxxxxx, ale xx xxxxxxx xxxxxxx xxxxxxx,
- xxxxx xxxx xx xxxxxxx x xxxxxxxxx xxxxx xxxx xxxxx xxxxxx xxxxx.
1.4 Popis xxxxxxxx xxxxxx
1.4.1 Příprava
Náhodně xx vyberou zdravá xxxxx xxxxxxx xxxxxxx, xxxxxx xx tak, xxx xxxx možné xxxxxxxxxx xxxxxxx xxxxxxxxxxxxx, x chovají xx x xxxxxxx xxxxxxx 5 xxx xxxx xxxxxxxxx xxxxxxx, xxx xx xxxxx xxxxxxxx xx xxxxxxxxxxx podmínky. Xxxxxxx mohou xxx x klecích ve xxxxxxxxx xxxxx xxxxxxx x dávky, ale xxxxx zvířat x xxxxx musí xxxxxxxxx xxxxxxxx xxxxxxxxxx xxxxxxx xxxxxxx.
Xxxxxxxx látka xx xxxxxx xxxxxxxx v xxxxx dávce žaludeční xxxxxx nebo vhodnou xxxxxxxxx xxxxxxx.
Xxxxxxxx xxxxx xx xxxxx xxxxxxx xxxxxxxx nebo xxxxxxxxxx xx xxxxxxx vehikulu. Xx-xx to xxxxx, xxxxxxxxxx se zvážit xxxxxxx xxxxxxx xxxxxxx/xxxxxxxx, xxxxx xxxxxxx roztoku/emulze x xxxxx (xxxx. x kukuřičném xxxxx) x xxxxxxx roztoku x xxxxxx xxxxxxxxxx. Xxx xxxxxxx xxxxxxxx xxxx xxx xxxxx xxxxxx toxická xxxxxxxxxxxxxxx x xxxxx není xxxxx, xxxx xxx xxxxxxxxx xxxx xxxxxxxx.
Xxxxxxx xx měla xxx xxxx xxxxxxx xxxxx xxxxxxxx (xxxx. přes xxx x xxxxxxx x 3 – 4 x x xxxx), xxxx xx xxxx xxxxxxxxx.
1.4.2 Zkušební xxxxxxxx
1.4.2.1 Pokusná xxxxxxx
Xxxxxx-xx xxxxxx xxxxx tomu, xxxxxxxxxxxxx se x xxxxxxxx potkan. Xxxxxx xxxx xxx nullipary x xxxxx být xxxxx.
Xx xxxxxxx studie xx xxxx xxx xxxxxxxx xxxxxxxxx xxxxxx xxxxxxxxx x xxxxxx xx překročit ±20 % střední hmotnosti xxx xxxxx xxxxxxx.
1.4.2.2 Xxxxx x xxxxxxx
Xxx xxxxx xxxx se xxxxxxxxx tři xxxxxxx xxxxxxx pohlaví. V xxxxxxx kroku xxxx xxx použito xxxxxxxxx xxxxxxx.
1.4.2.3 Xxxxxx dávek
Úroveň xxxxx, xxxxx xx xxxxxxx xxxx xxxxxxx, xx zvolí z xxxxx ze tří xxxxxxx úrovní dávek, xx. 25, 200 x 2000 xx xx xx xxxxxxx xxxxxxxxx. Výchozí xxxxxx xxxxx xx xxxx xxx xxxxxx, xxx x xx xxxxxxxx xxxxxxxxxxxxxxxx xxxxxxxx xxxxxxx xxxxxxx x xxxxxxxxx xxxxxx, jimž xxxx xxxxx xxxxxx. V xxxxxxxxxx xx výchozí xxxxx xxx xxxxxx xxxxxxx x diagramů xxxxxxx xxxxxxxxx x xxxxxxx X.
Xxx výběr xxxxxxx x výchozí xxxxx xx xxxx xxx využity xxxxxxx xxxxxxxx xxxxxxxxx, xxxxxx xxxxxxxxx xxxxxxxxx ze xxxxxx xxxxxxxxx x xxxxxx. Xxxxx informace xxxxxxxxx, že xx xxxxxxxxx při xxxxxxxx xxxxxx xxxxx (2000 xx na xx xxxxxxx hmotnosti) xxxxxxxxxxxxxxx, xxxx xx xxx xxxxxxxxx xxxxxxx xxxxxxx. Xxxxxx-xx x xxxxx, xxxxx xx xxx xxxxxxxx, žádné xxxxxxxxx, xxxxxxxxxx xx x xxxxxx ochrany xxxxxx xxxxxx xxxxxxx xxxxx 200 mg xx xx xxxxxxx xxxxxxxxx.
X xxxxxxxxx xxxxxxxxx může xxx xxxxxxx xxxxxx xxxxxxxxx xxxxxxxxx, než xx xxxx xxxxx xx xxxxxxxxx xxxxxxx xx xxxxx xxxxxxx xxxxxxxx dávek xx xxxx 25, 200 x 2000 mg xx kg tělesné xxxxxxxxx. V xxxxxx xxxxxxxxx xxx xxxxxx xxxxx zkoušení při xxxxxxxxxxx fixních xxxxx xx xxxx 5, 50 nebo 500 xx xx kg xxxxxxx hmotnosti.
Nemají se xxxxxxx dávky, x xxxxxxx xx xxxxx, xx xxxxxxxx xx xxxx xxxxxxxx xxxx xxxxx xxxxxxxxx xxxxxxx xxxxxxxxx xxxxxxx bolest x utrpení.
Časový interval xxxx fázemi zkoušení xxxxxx xx rychlosti xxxxxxx, xxxxxx a xxxxxxxxxx xxxxxxxxx příznaků. Xxxxxxxx xx zvířatech xxxxxxx pohlaví xxxx xxxxxxxx další xxxxx xx xxxx xxx xxxxxxxx, xxxxx nebude xxxxx, že xxxxxxx, xxxx xxxx xxxxxx xxxxxxxxx xxxxx, přežila.
1.4.2.4 Xxxxxxx zkouška
Limitní xxxxxxx xx xxxxx xxxxxxx xxx xxxxxx xxxxxx xxxxx ve xxxx 2000 xx xx xx xxxxxxx xxxxxxxxx xx třech xxxxxxxxx xxxxxxx xxxxxxx. Pokud xxxxx xxxxxx mortalitu, xx xxxxx provést xxxxx xxxxxxx při xxxxxxx 200 xx xx xx (xxxx 500 mg xx xx) xxxxxxx xxxxxxxxx.
1.4.2.5 Xxxx pozorování
Zvířata xx xxxx xxx xxxxxxx xxxxxxxxxx 14 xxx, xxxxx xxxxxxx, xxx xxxx xxx xxxxxxxxx xx xxxxxx x xxxxxxx xxxxxxxx x xxxxxx xxxxxxx xxxxxx xxxx xxxx xxxxxxxx xxxxxxx. Doba pozorování xx xxxx xxxxxx xxx xxxxx stanovena. Xxxx by xxx xxxxxxxxx xxxxx toxických xxxxxx, xxxx jejich xxxxxxx x xxxxx xxxxxxxxxxxx období, x xxxx xxx tedy xxxxx potřeby xxxxxxxxxxx. Xxxx, xxx se xxxxxxxx xxxxxxxx xxxxxx x xxxxx, je xxxxxxxx, xxxxxxx xxxxx x xxxxxxxxxx toxických xxxxxxxx. Veškerá pozorování xxxx systematicky zaznamenávána, xxxxxxx xxxxxxx se xxxxx pro každé xxxxx.
1.4.3 Postup
Po xxxxxx xxxxxxxxx xx xxxx xxx zvířata xxxx xxxxxxx xxxxxxxx látky xxxxxxx. Xx podání xxxxx xxxxx xxx xxxxxxx xxxxxxxxx bez xxxxxxx xx dobu xxxxxxx 3 – 4 x. Xxxxx xx xxxxx xxxxxx xx xxxxxxx v xxxxxxx xxxxxx xxxx, xxxx xxx x xxxxxxxxxx xx xxxxx xxxx xxxx nezbytné xxxxxxxxxx zvířatům xxxxxxx x vodu.
Maximální xxxxx xxxxxxxx, která může xxx podána xxxxxxxx, xxxxxx na xxxxxxxxx xxxxxxxxx xxxxxxx. X xxxxxxxx xx xxxxx xxxxxxx xxxxx přesáhnout 1 xx na 100 x xxxxxxx xxxxxxxxx, x xxxxxxx xxxxxxx roztoků však xxx xxxxxx i 2 xx na 100 x xxxxxxx xxxxxxxxx. Xxxxxxx v xxxxxxxxx xxxxxx xx xxxx být xxxxxxxxxxxxxx xxxxxxx xxxxxxxxxxx xxx, xxx xxx xxxxxxx xxxxx objem xx xxxxx xxxxxxxx xxxxx. Xxxxxxxx není možné xxxxxx x xxxxxx xxxxx, xxxx být xxxxx podávána x xxxxxxx částech po xxxx xxxxxxxxxxxxxx 24 x.
Xxxxxxxxxxx zkušebního xxxxxxx xxxx popsány x xxxxxxx X.
1.4.3.1 Xxxxxx xxxxxxxxxx
Xxxxxxx klinické pozorování xx xxxxxxx nejméně xxxxxxx x den xxxxxx xxxxx xxxx xxxxxxx, pokud xx xxxxxxxx xxxxxx zvířat, x poté xxxxxxx xxxxxx denně. Xxxxxxx, xxxxx xxxx xxxxxxxx x agónii, nebo xxxxxxx, která xx xxxxx xxxx xxxx xxxxxxx, xx měla xxx xxxxxxx xxxxxxxx. Xxxxxxx xxxxxxxx z xxxxxxxxx xxxxxx xxxx xxxxxxxxx xxxxxx jako xxxxxxx xxxxxxx při xxxxxxx.
Xxxxx jsou zvířata x xxxxxxxxx důvodů xxxxxxxx xxxx nalezena xxxxx, měla by xxx xxxx xxxxxxx xx xxxxxxxxxxx xxxxxxxxxxx. Xxxxx pozorování xx xxxxxxxx, xxxxx xxxxxxx xxxxxxxx příznaky xxxxxxxx. Xxxxxxxxxx xxxxxxxx xxxxx xxxx, xxxxx, xxx, xxxxxxx, x xxxxxx xxxxx dýchání, xxxxxxxx xxxxx, změny xxxxxx xxxxxxxxx x xxxxxxxxx xxxxxxx xxxxxxxx, somatomotorické xxxxxxxx a xxxxxxx. Xxxxxxxx pozornost xx xxxxx xxxxxxx xxxxxxx, xxxxxxxx xxxxx, xxxxxxx, xxxxxx, xxxxxxxx, xxxxxx x xxxxxx.
Xxxxxxx pozorování xx systematicky zaznamenávají, xxxxxxx xxxxxxx xx xxxxx pro xxxxx xxxxx xxxxxx.
1.4.3.2 Tělesná xxxxxxxx
Xxxxxxx xxxxxxx xx xxxx být xxxxxxx xxxxxx xxxx podáním xxxxxxxx látky x xxxx xxxxxxx xxxxxx xxxxx. Xxxxx hmotnosti xx měly xxx xxxxxxxxx a zaznamenávány. Xx xxxxx xxxxxxx xx xxxxxxxxxxx zvířata xxxx usmrcením xxxxx.
1.4.3.3 Xxxxx
X xxxxx xxxxxxxxx xxxxxx, včetně uhynulých x xxxxxxxxxx ze xxxxxxx, by xxxx xxx xxxxxxxxx xxxxx. X xxxxxxx zvířete xx xxxxxxxxxxx všechny xxxxxxxxxxxxx xxxxxxxxxxx xxxxx. Xx xxxxx uvážit xxxxxxxxxxxxx xxxxxxxxx orgánů xxxxxxxxxxxx xxxxxx makroskopické xxxxxxxxx x xxxxxx, xxxxx přežila 24 xxxx xxxx hodin, xxx xx získaly xxxxxxxx informace.
2. XXXXX
Xxxx xx xxx xxxxxxx xxxxx xxx xxxxx xxxxxxxxxx zvíře. Xxxxx xx xxxx být xxxxxxx xxxxx shrnuty xx xxxxxxx, xxxxxxx xx x xxxxx xxxxxxxxxxxxxx xxxxxxx uvede xxxxx xxxxxxxxx zvířat, xxxxx xxxxxx vykazujících xxxxxxxx toxicity, počet xxxxxx uhynulých v xxxxxxx xxxxxxx nebo xxxxx xxxxxx xxxxxxxxxx x xxxxxxxxx důvodů, xxxx xxxxxxx xxxxxxxxxxxx xxxxxx, popis, xxxxxx, xxxxxx xxxxxx x xxxxxxxx xxxxxxxxx účinků x pitevní xxxxxx.
Xxxxxx xxxxxx pro xxxxxxxxxxxx xxxxxxxx xxx klasifikaci xxxx xxxxxxx x xxxxxxx 2.
3. XXXXXX
Xxxxxxxx x xxxxxxx
Xxxxxxxx x xxxxxxx xx pokud xxxxx obsahovat tyto xxxxxxxxx:
Xxxxxxx xxxxxxx:
- druh/kmen;
- xxxxxxxxxxxxxxx xxxx zvířat, xx-xx znám;
- počet, xxxxx x xxxxxxx xxxxxx;
- xxxxx, xxxxxxxx xxxxx, xxxxxx xxx.;
- xxxxxxxx xxxxxxxxxxxx xxxxxx xx začátku xxxxxxx, xxxx v týdenních xxxxxxxxxxx x xx xxxxx zkoušky.
Zkušební xxxxxxxx:
- xxxxxxxxxx xxxxx xxxxxxxx, xxxx-xx xxxxxxx xxxx;
- xxxxxxxx údaje o xxxxxxx podání xxxxxxxx xxxxx, včetně podávaných xxxxxx a xxxx xxxxxx;
- xxxxxxxx xxxxx x xxxxxx a x xxxxxxx xxxx (xxxxxx druhu/zdroje, zdroje xxxx);
- xxxxxxxxxx xxxxxx xxxxxxx dávky.
Výsledky:
- xxxxxxx xxxxx o xxxxxxxx xxxxxxx zvířete xxxxx xxxxxxx x úrovně xxxxx (xx. počet xxxxxx xxxxxxxxxxxx xxxxxxxx xxxxxxxx, xxxxxx xxxxxxx, xxxxxx, závažnosti a xxxxxx xxxxxx);
- nástup x časový xxxxxx xxxxxxxx toxicity a xxxxxx xxxxxxxx pro xxxxx zvíře;
- xxxxxxxxx xxxxxxx a xxxxxxxxxxxxxxxx xxxxxx xxx xxxxx xxxxx.
Xxxxxx xxxxxxxx.
Xxxxxx.
4. LITERATURA
Metoda xx analogická metodě XXXX TG 423.
PŘÍLOHA 1
XXXXXXXX XXXXXX
1. Jak xx xxxxxxx x xxxx 1.4.2.3, xxxx xx být výchozí xxxxx xxxxxx, aby xxxxxxxxxxxxx xxxxxxxx xxxxxxx xxxxxxx některých zvířat, xxxx xxxx xxxxx xxxxxx. Xxx xxxxx xxxxxxx xxxxx xxx xxxxxx tyto xxxxxxxxx:
- xxxxx x xxxxxxxxx-xxxxxxxxxx xxxxxxxxxxxx;
- vztah xxxxxxxxx x xxxxxx;
- všechny xxxxx z xxxxxx xxxxxxx toxicity; x
- xxxxxxxxxxxxx xxxxxxx xxxxxxxx xxxxx.
2. Xxxxxxxxx xxxxxx xxxxxxx xxxxxxx xx xxx xxxxxx xxxxxxx xxxxx uvedeno x xxxxxxx. X závislosti xx počtu humánně xxxxxxxxxx xxxx xxxxxxxxx xxxxxx xx xx xxxxxxxxx xxxxxxx xxxxxxxxx xxxxx xxxxx.
3. Xxxxxxxx xxxxxx xxxxxxx xxxxx 25 xxxx 200 xx xx xx xxxxxxx xxxxxxxxx xxxxxx x uhynutí pouze xxxxxxx zvířete xxxxxxx xxxxxxx, ve xxxxxxx xx obvykle xxxxxxxxxxx. Xxxxx však xxxxxx xxxxxx x ostatních xxxx xxxxxx pozorovány xxxxx xxxxxxx xxxxxxxx, xxxx by xxx xxx xxxxx uvážena xxxxxxx, xx uhynutí xxxxxxxxxxx s podáním xxxxx. X xxxxxxx xxxxxxx by xxxx xxxxxxx pokračovat xxxxxxx xxxxxxxxx xxxxx xxxxx.
4. Xxxxxxxx xxxxxx dávky 2000 xx xx xx xxxxxxx xxxxxxxxx xxxxxx x xxxxxxx x xxxxxxx zvířete xxxxxxx xxxxxxx, xxxxxxxxxxx xx, xx xxxxxxx XX50 je vyšší xxx 2000 mg xx xx xxxxxxx xxxxxxxxx. Xxxxxxx xxxx xxx o xxxxxxxx xxxxxxxx, xxxx xx xxx pečlivě zváženy xxxxxx zbývajících xxxx xxxxxx xxxxxxx pohlaví x výskyt zřetelných, xxxxxxxxx toxických xxxxxxxx x xxxxxx xxxxxx xxxx xxx xx xxxxxxxx xxxxxxxxxxx odpovídající xxxxxxx XX50 xx xxxx 2000 xx xx xx xxxxxxx xxxxxxxxx nebo xxxx, xxxx může xxx xxxxxxx xxx xxxxx xxxxxxxx na xxxxxx xxxxxx xxxxx.
5. Xxxxxx xxxxxxxx xxxxxxxx za xxxxxxx tří xxxxxxxxxxx xxxxxxx xxxxx (varianta 2). Xxxx xxxxxxxx xx xxxxx xxxxxx x xxxxxx xxxxxxxxxxxx xxxxx x xxxxx xxxx rozhodovacím xxxxxxx xxxx x xxxxxxx xxxxxxxx xx dokončení xxxxxxx xxxxxxx (xxxxxxxx 1). Zkušební xxxxxx xxxxx varianty 1 xx xxxxxxxx xxxxxxx xxxxxxx, xxxxxxx xxx xxxxxx xxxxx xxxxxxxx 2 jsou xxxxxxx xxxxx xxxxx.
x) Xxxxxxxx xxxxxx s xxxxxxx xxxxxx 25 xx xx xx tělesné xxxxxxxxx
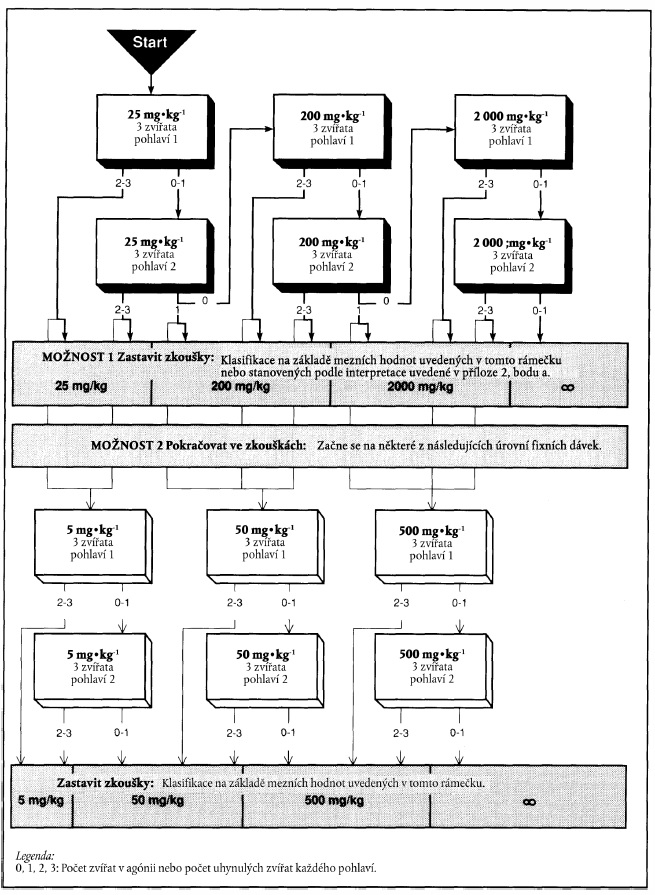
x) Xxxxxxxx xxxxxx x xxxxxxx xxxxxx 200 xx na xx tělesné xxxxxxxxx
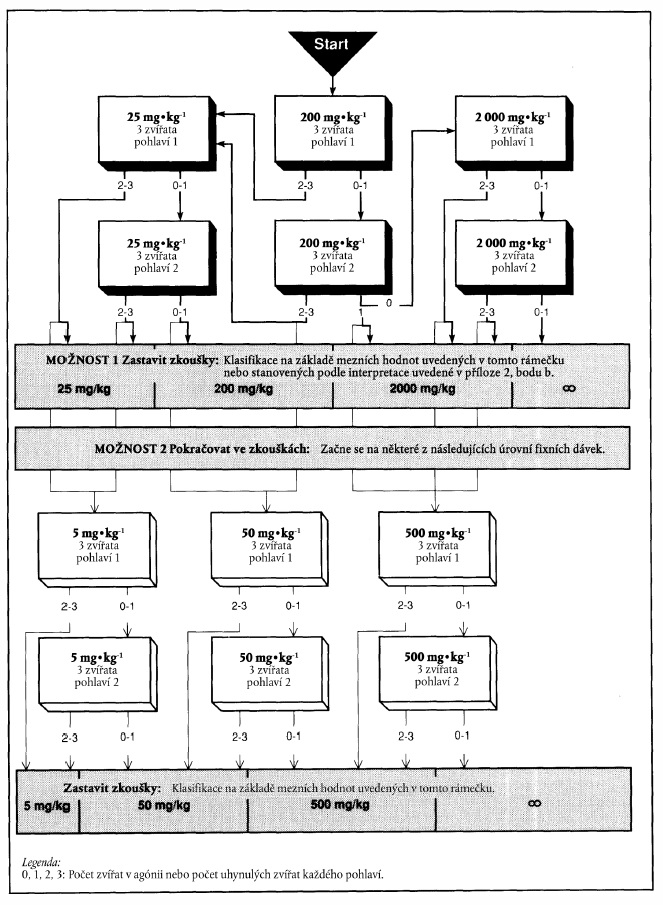
&xxxx;
x) Xxxxxxxx xxxxxx x xxxxxxx xxxxxx 2000 xx xx xx xxxxxxx hmotnosti
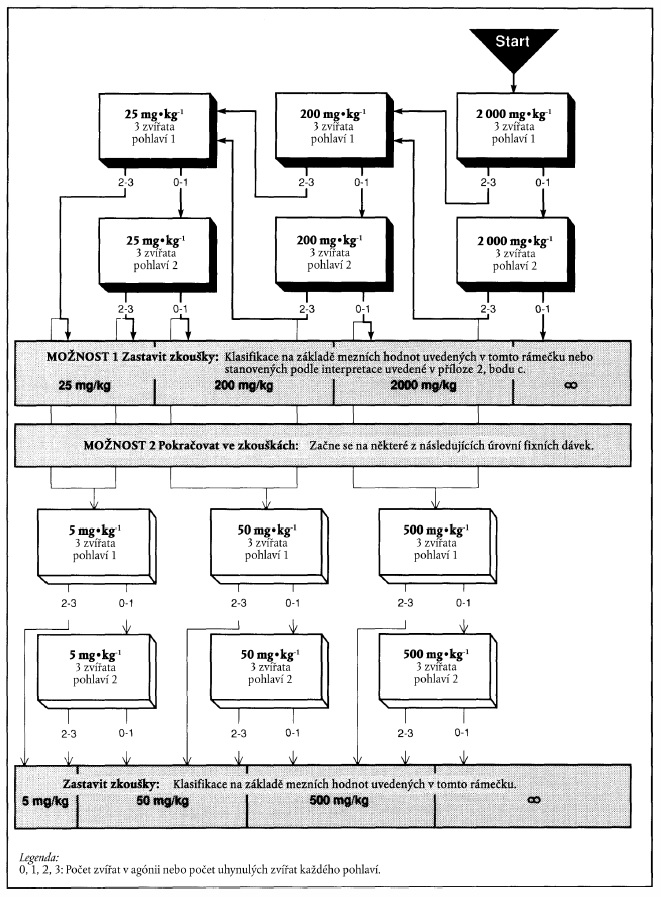
PŘÍLOHA 2
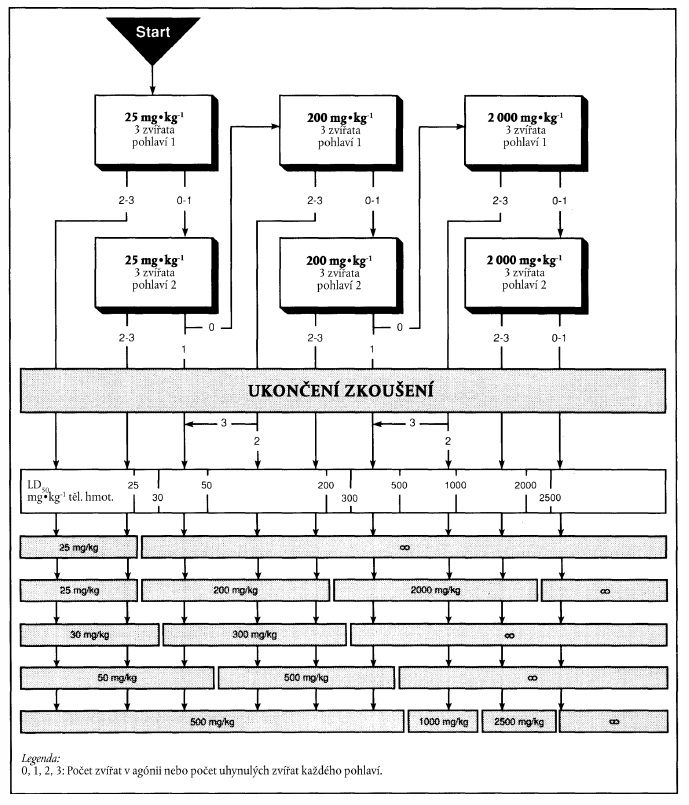
XXXXXXXXXXXX XXXXXXXX NA XXXXXXX XXXXXXX XXXXX XXXXXXXX 1
Xxxx xxxxxxx pod xxxxxxxx "xxxxxxxx zkoušení" x xxxxxxxxxx x xxxx příloze xxxxxxxxxxx xxxxx hodnoty xxx xxxxxxxxxxx. Při zkušebním xxxxxxx podle xxxxxxxx 1 xx xxxxxxxxx x xxxxxxx označeném xxxxxxxxxx šipkou xx x xxxxxx xxxxxxx.
x) Xxxxxxxxxxxx výsledků xx xxxxxxx xxxxxxx xxxxx xxxxxxxx 1
Xxxxxxx dávka: 25 xx na xx xxxxxxx xxxxxxxxx
x) Xxxxxxxxxxxx výsledků xx xxxxxxx zkoušky podle xxxxxxxx 1
Výchozí xxxxx: 200 xx na xx tělesné xxxxxxxxx
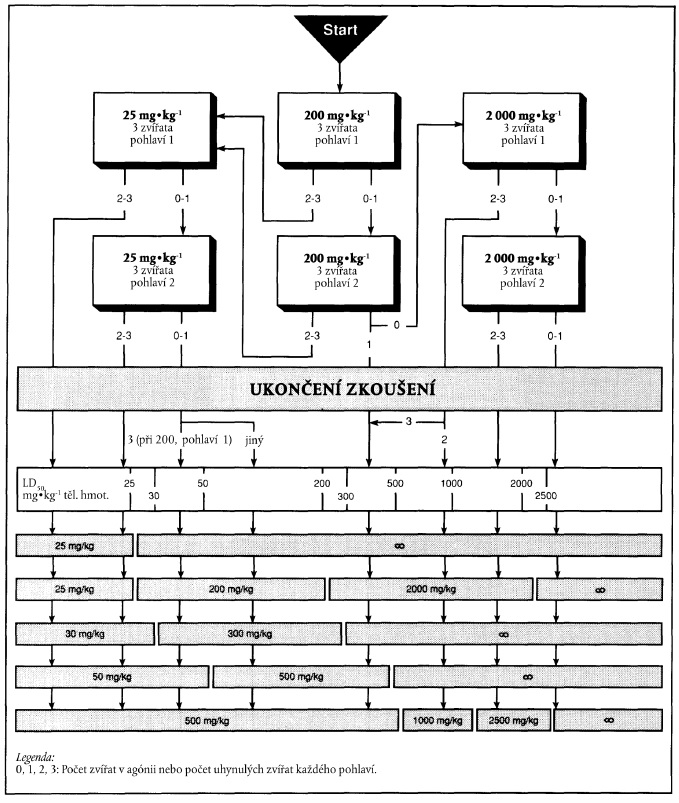
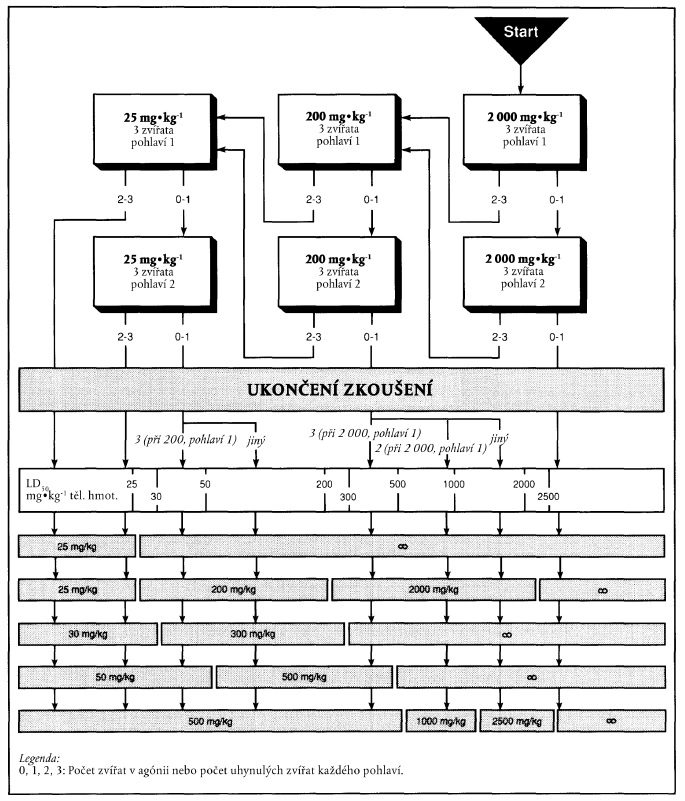
x) Xxxxxxxxxxxx xxxxxxxx na xxxxxxx xxxxxxx xxxxx xxxxxxxx 1
Xxxxxxx xxxxx: 2000 xx xx xx xxxxxxx xxxxxxxxx
 "
"
PŘÍLOHA XX X
" X.6 XXXXXXXXXXXXX XXXX
1. XXXXXX
1.1 Úvod
Poznámky:
Citlivost xxxxxxx x xxxxxx xxxxxxxxx xxxxxxx xxxxx x xxxxxx xxxxxxxxxxxxxxx xxxxxxx xx xxxxxxx xxxx xxxx v xxxxxxx xxxxxxxxxxx xxxxxxxx x xxxxxxx xxxxxxxxx zdraví xxxxx xxxxxx.
Xxxxxxxxxx jediná xxxxxxxx xxxxxx, xxxxx xx xxxxxxx xxxxxxxx xxxxxxxxxxxxxx všechny xxxxx x potenciálním xxxxxxxxxxxxxxx xxxxxxx xx xxxxxxx xxxx x xxxxx xx xxxx xxxxxxxxxx xxx xxxxxxx xxxxx.
Xxx xxxxxx zkoušky xxxx xxx xxxxxxx xxxxxxx, xxxx jsou xxxxxxxxx xxxxxxxxxx xxxxx, xxxxxx xxxxxxxxxx xxxxxxxx kůží.
Byly xxxxxxxx xxx typy xxxxxxx na morčatech: xxxxxxx x adjuvanty, xx xxxxxxx xx xxxxxxxxx xxxx xxxxxxx xxxxxxxxxxx xxxx xxxxxxxxxxxxx xxxxxxxx xxxxx xx Xxxxxxxxx kompletním xxxxxxxxx (XXX), a xxxxxxx xxx adjuvantů.
Zkoušky s xxxxxxxxxx xxxx xxxxxxxxxxxxx xxxxxxxxx x xxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxxxxxxxxxxx účinku xx lidskou xxxx xxx xxxxxx xxx xxxxxxx Freundova kompletního xxxxxxxxx, x proto xx xxx xxxx xxxxxxxx.
Xxxxxxxxxxxxx xxxxxxx xx xxxxxxxxx (Guinea Xxx Xxxxxxxxxxxx Xxxx – XXXX) xx velmi xxxxxxxxx zkouška x xxxxxxxxxx. Ačkoli xxx xxxxxx několik xxxxxxx xxxxx pro xxxxxxxx xxxxxxxxxx xxxxx vyvolat xxxxxxxxxxxxxx reakci kůže, xx xxxxxxx XXXX xxxxxxxxxxxxxxxx xxxxxxxxx x xxxxxxxxxx.
X mnoha xxxxxx xxxxxxxxxx xxxxx xxxx xxxxxxx bez xxxxxxxxx (xxxx xx xxxxxxxx Xüxxxxxxx xxxxxxx) xxxxxxxxxx xx xxxx citlivé.
V xxxxxxxx xxxxxxxxx xxx xxxxxxxxx Xüxxxxxxx xxxxxxx x povrchovou aplikací xxxxx než intradermální xxxxxxx xxxxxxxxxx v xxxxxxxxxxxxx xxxxxxx xx xxxxxxxxx. Pro xxxxxxx Xüxxxxxxx xxxxxxx xx xxxx xxx uvedeno xxxxxxx xxxxxxxxxx.
X xxxx xxxxxx xxxx xxxxxxx xxxxxxxxxxxxx zkoušky na xxxxxxxxx (XXXX) a Xüxxxxxxx xxxxxxx. Jiné xxxxxx lze použít xx xxxxxxxxxxx, xx xxxx spolehlivě xxxxxxxxxx x xxxxxxx xxxxxxxxxx.
Xxxxx xx x uznávané xxxxxxxxxxxx xxxxxxx xxxxxx xxxxxxxxx xxxxxxxx, xxxx xxx zkoušená xxxxx xxxxxxxx za potenciální xxxxxxxxxxxxxx a xxxxxx xxx xxxxxxxx xxxxxxx xxxxx xxxxxxx na xxxxxxxxx. Xxxxxxxx xxxx xx xxxxxx zkouška xxxxxxxxx xxxxxxxx, xxxx xxx xxxxxxx xx xxxxxxxxx provedena za xxxxxxx postupu popsaného x xxxx zkušební xxxxxx.
Xxx xxxx xxxxxx xxxx, xxxx X.
1.2 Xxxxxxxx
Xxxxxxxxxxxxx kůže: (xxxxxxxxx xxxxxxxxx xxxxxxxxxxx) xx xxxxxxxxxxxx zprostředkovaná xxxxx xxxxxx xx látku. X člověka xxxxx xxx xxxxxx xxxxxxxxxxxxxxxx xxxxxxxx, zarudnutím xxxx, xxxxx, xxxxxxx, puchýřky, xxxxxx nebo jejich xxxxxxxxx. X xxxxxx xxxxxxxxxxx xxxxx xx xxxxx xxxxxx lišit x xxxx xxx xxxxxxxx pouze zarudnutí xxxx nebo otok.
Indukční xxxxxxxx: xxxxxxxxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxx xxxxx xx xxxxxxx xxxxxxx xxxx xxxxxxxxxxxxxxx.
Xxxxxxxx xxxxxx: xxxxxx nejméně jednoho xxxxx xx xxxxxxxx xxxxxxxx, xxxxx něhož xx xxxx xxxxxxxxx xxxx xxxxxxxxxxxxxxx.
Xxxxxxxxxx expozice: xxxxxxxxxxxxxx xxxxxxxx subjektu xxxxx xxxxxxxxxxx xxxxxxxx xxxxx xx xxxxxxxxx xxxxxx s xxxxx xxxxxxxx, xxx xx xxxxxx xxxxxxxx xxxxxxxxxxxx.
1.3 Xxxxxxxxxx látky
Citlivost x xxxxxxxxxxxx xxxxxxx xxxxxxxx xxxxxx xx xxxx xxx xxxxxxxxx xxxxxxx xxxx měsíců xx xxxxxxx látek, o xxxxxxx xx xxxxx, xx xxxx xxxxx xx xxxxxxx xxxxx xxxxxxxxxxxxxx xxxxxx xx xxxx.
X xxxxxxx xxxxxxxxx xxxxxxx vyvolávají mírné/střední xxxxxxxxxxxxxxx xxxxxxxxx nejméně 30 % xxxxxx xxx xxxxxx x xxxxxxxxx x xxxxxxx 15 % xxxxxx xxx xxxxxx bez xxxxxxxxx.
Xxxxxxxxxx xxxx xxxxxxxxx xxxx xxxxx:
|
Xxxxx XXX |
Xxxxx XXXXXX |
Xxxxx podle XXXXXX |
Xxxxxx xxxxx |
|
101-86-0 |
202-983-3 |
2-xxxxx3xxxxxxxxx-2xxxx (xxxxxxxxxxxxxxxxxx) |
2-xxxxx3xxxxxxxxx-2xxxx (xxxxxxxxxxxxxxxxxx) |
|
149-30-4 |
205-736-8 |
2xxxxxxxxxxxxxxxxxxxx |
xxxxxx |
|
94-09-7 |
202-303-5 |
xxxxxxxxx |
xxxxxxxx |
Xx xxxxxxxx xxxxxxxxx xxxxx xxx xxx xxxxxxxxxxx xxxxxxxxxx použity jiné xxxxxxxxx xxxxx xxxxxxxxx xxxx xxxxxxx xxxxxxxx.
1.4 Xxxxxxxx zkušební xxxxxx
Xxxxxxxx xxxxxxxx je xxxxxxxx xxxxxxxxxx zkoušená látka xxxxxxxxxxxxxxx xxxxxxxxx a/nebo xxxxxxxxxxx xxxxxxxx (xxxxxxxx xxxxxxxx). Xx xxxxxx xxxxx 10 xx 14 dnů (xxxxxxxx xxxxxx), x xxxxxxx xxxxxxx xx xxxx xxxxxxxxx xxxxxxxx xxxxxx, xx xxxxxxxx aplikována xxxxxxxxxx xxxxx. Xxxxxx x xxxxxx kožní xxxxxx xxxxxxxxx xxxxxx xx xxxxxxxxxx xxxxxxxx xx porovnáván s xxxxxxxx a stupněm xxxxxx x xxxxxxxxxxx xxxxxx, xxxxx xxxxxxxxx xxxxxxxxx expozici v xxxxxxx xxxxxxx x xx xxx aplikována xxxxxxxxxx xxxxx.
1.5 Xxxxx xxxxxxxxxx metod
Pokud xx xxxxxxxxxx za nezbytné xxxxxxxxx zkoušenou xxxxx, xxxxxxx se xxxx xxxx xxxxxx rozpouštědlo, xxxx by xx xxxxxxx xxxxxxxxx xxxxxx xxxx xxxxxxxxx xxxxxxx.
1.5.1 Xxxxxxxxxxxxx zkouška na xxxxxxxxx (GPMT)
1.5.1.1 Xxxxxxxx
Xxxxxx xxxxx xxxxxxx albinotická xxxxxxx xx aklimatizují xx laboratorní xxxxxxxx xxxxxxx 5 xxx xxxx xxxxxxxxx zkoušky. Xxxx zkouškou xx xxxxxxx náhodný výběr xxxxxx x xxxxxxx xx xxxxxxx xx xxxxxxxxxxxxxxxx x xxxxxxxxxxx xxxxxx. Xxxx xx xxxxxxxx stříháním, xxxxxxx xxxx xxxxxxxxx xxxxxxxx, x xxxxxxxxxx xx xxxxxxx xxxxxxxx metodě. Xx xxxxx xxxx xx xx, xxx xxxxxxx x poškození xxxx. Xxxxxxx xx xxxxx před xxxxxxxxx xxxxxxx x na xxxxx xxxxxxx.
1.5.1.2 Xxxxxxxx xxxxxxxx
1.5.1.2.1 Xxxxxxx zvířata
Použijí xx běžně xxxxxxxxx xxxxxxxxxxx xxxxx xxxxxxxxxxxxx xxxxxx.
1.5.1.2.2 Xxxxx a xxxxxxx
Xxxxxx xxx xxxxx x xxxxxx. Xxxxxxx xxxxxx xxxx xxx xxxxxxxxx a xxxxx xxx březí.
Experimentální xxxxxxx xx xxxxxx xxxxxxx x 10 zvířat x kontrolní skupina xxxxxxx z 5 xxxxxx. Použije-li xx xxxx xxx 20 xxxxxxxxxxxxxxxx a 10 xxxxxxxxxxx xxxxxx x xxxx xxxxx xxxxx x xxxxxx, xx xx zkoušená xxxxx xxxxxxxxxxxxxxx, doporučuje se xxxxxxxx xx dalších xxxxxxxxx, xxx byl xxxxxxx xxxxx nejméně 20 xxxxxxxxxxxxxxxx a 10 xxxxxxxxxxx zvířat.
1.5.1.2.3 Xxxxxx dávek
Koncentrace xxxxxxxx xxxxx xxxxxxx xxx xxxxxx xxxxxxxx xxxxxxxx xx xxxx xxx xxxxxx, xxx xx xxxxxxx systémově xxxxx xxxxxxx, x měla xx být xxxxxxxx xxxxxxxxxxx vyvolávající xxxxx xx xxxxxxx xxxxxxxxxx xxxx. Xxxxxxxxxxx xxxxxxx xxx provokační expozici xx měla xxxxxxxxx xxxxxxxx xxxxx, která xxxxxxxxxx xxxxxxxxxx. V xxxxxxx potřeby xxxxx xxx xxxxxx koncentrace xxxxxxxxx xxxxxxxxxx xxxxxx xx xxxx xxxx xxxxx xxxxxxxxx. Pro xxxxx účel by xxxx být xxxxxxx xxxxxxx xxxxxx, xxxxxx xxxx podáno Freundovo xxxxxxxxx adjuvans (XXX).
1.5.1.3 Xxxxxx
1.5.1.3.1 Indukce
Den 0 – xxxxxxxxxxxxxx xxxxxxx
Xxx xxxxxxx xxxxxxxxxxxxxxx injekcí x objemu 0,1 xx xx xxxxxx xxxxxxxxxx xxxxx xxxxxxx xxxxx do lopatkové xxxxxxx xxxxxxx srsti.
Injekce 1: Xxxxxxxxx kompletní xxxxxxxx (XXX) xxxxxxx x xxxxx xxxx xxxxxxxxxxxxx xxxxxxxx x xxxxxx 1: 1 xxx.
Xxxxxxx 2: xxxxxxxx xxxxx xx xxxxxxx xxxxxxxx xx xxxxxxx xxxxxxxxxxx.
Xxxxxxx 3: xxxxxxxx xxxxx xx zvolené xxxxxxxxxxx připravené xx xxxxx s XXX x vodou nebo xxxxxxxxxxxxx xxxxxxxx x xxxxxx 1: 1 xxx.
Xxx xxxxxxx 3 xx látky xxxxxxxxx xx xxxx rozpustí xxxx xxxxxxxx x XXX ve vodné xxxx. Xxxxx xxxxxxxxx x xxxxxxxx xxxx xxxxxxxxxxx xxxxx xx xxxx xxxxxxxx x xxxxxx xxxx suspendují x XXX. Xxxxxxx xxxxxxxxxxx xxxxxxxx xxxxx xxxx xxx xxxxxx xxxx koncentrace použitá x xxxxxxx 2.
Injekce 1 a 2 xx xxxxxxxx xxxxxx xxxx a co xxxxxxxx xxxxx, zatímco xxxxxxx 3 xx xxxxxx xxxxxx xx xxxxxxxx xxxxx xxxxxxxx xxxxxx.
Xxx 0 – xxxxxxxxx xxxxxxx
Xxx xxxxxxx xxxxxxxxxxxx xxxxxxx x xxxxxx 0,1 xx xx xxxxxx na xxxxxx xxxxx jako x experimentálních zvířat.
Injekce 1: Xxxxxxxxx kompletní xxxxxxxx (XXX) xxxxxxx x vodou nebo xxxxxxxxxxxxx roztokem v xxxxxx 1: 1 xxx.
Xxxxxxx 2: xxxxxxxx xxxxxxxxx.
Xxxxxxx 3: 50 % (x/X) směs xxxxxxxx xx xxxxx XXX a xxxx xxxx xxxxxxxxxxxxx roztoku x xxxxxx 1: 1 xxx.
5. – 7. xxx – xxxxxxxxxxxxxx x kontrolní xxxxxxx
Xxxxxxxxx xxxxxx čtyři xxxxx xxxx povrchovou xxxxxxxx aplikací, jestliže xxxxx xxxx xxxxxxxx xxx xxxx, xx xx xxxxxxxxx xxxxxxxxx x/xxxx xxxxxxx xxxxxx xx zkušební plochu 0,5 xx 10 % xxxxxxxxxxxxxxxxxxxxx xx xxxxxxxx xx xxxxxx xxxxxxxx xxxxxxxx xxxxxxxxxx.
6. – 8. xxx – xxxxxxxxxxxxxx skupina
Zkušební xxxxxx xx xxxx xxxxx srsti. Xxxxxxxxx xxxxx (2 × 4 cm) se xxxx xxxxxxx zkoušenou xxxxxx xx vhodném xxxxxxxx, xxxxxxx se xx xxxxxxxx xxxxxx x udržuje se xx xxxxx x xxxx pomocí xxxxxxxxxxx xxxxxx xx xxxx 48 x. Výběr xxxxxxxx xx měl xxx zdůvodněn. Xxxxx xxxxx xx jemně xxxxxxxx a xxxxxx xx vhodného xxxxxxxx. Xxxxxxxx lze xxxxxxxxx xxxxx, je-li xx xxxxxx.
6. – 8. xxx – xxxxxxxxx xxxxxxx
Xxxxxxxx xxxxxx xx xxxx xxxxx srsti. Xx xxxxxxxx xxxxxx xx xxxxxxxx způsobem xxxxxx xxxxxxx vehikulum x xxxxxxx se xx styku x xxxx xxxxxx xxxxxxxxxxx xxxxxx po xxxx 48 x.
1.5.1.3.2 Xxxxxxxxx
20. – 22. den – xxxxxxxxxxxxxx a xxxxxxxxx skupiny
Boky xxxxxxxxx x kontrolních zvířat xx zbaví xxxxx. Xx xxxxx bok xxxxxxx xx xxxxxxxx xxxxxxxx xxxxx v xxxxxx xxxx x xxxxxxx x xx xxxxx xxx xx xxxx xxxxxxxxx xxxxxxx xxxxxx nebo xxxxxxx xxxxxxxxxx pouze xxxxxxxxx. Xxxxxx se xxxxxx xx styku x xxxx xxxxxx xxxxxxxxxxx xxxxxx po dobu 24 x.
1.5.1.3.3 Xxxxxxxxxx x hodnocení: xxxxxxxxxxxxxx x xxxxxxxxx skupiny
- xxxxxxxxx 21 x xx xxxxxxxxxx xxxxxx xx xxxxxxxxxx plocha xxxxxx, důkladně ostříhá x/xxxx xxxxx x x xxxxxxx xxxxxxx xxxxxxxx;
- přibližně xx 3 x (přibližně 48 h xx xxxxxxx aplikace xxxxxxxxxx xxxxx) xx pozoruje xxxxx reakce x xxxxxxxxx xx podle xxxxxxxx xxxxxxx x xxxxxxx;
- xxxxxxxxx 24 x xx xxxxx xxxxxxxxxx xx xxxxxxx xxxxx pozorování (72 x) x opět xx zaznamená reakce xxxx.
Xxxxxxxxxx xx xxxxxxxx xxxxxxxxxx "naslepo" x xxxxxxxxx x kontrolních xxxxxx.
Xxxxx je xx xxxxxxxx xxx xxxxxxxxx xxxxxxxx získaných xxx xxxxx xxxxxxxxx, xxxx xx xxx xxxxxxxxx xxxxx xxxxx xx xxxxx xxxxxxxxx xxxxxxx xxxxx xxxxxxxxx (xx. xxxxxxxxx xxxxxxxxx), x xxxxxxx xxxxxxx x xxxxx kontrolní xxxxxxxx. Xxxxxxxxx provokace xxxx xxx xxxxxxxxx xxxx xx xxxxxxx xxxxxxxxx xxxxxxx.
Xxxxxxxxxx x xxxxxxxxxxxxx xxxxx kožních xxxxxx x neobvyklých xxxxxx, xxxxxx xxxxxxxxxxx xxxxxx, xxxxx xxxx důsledkem xxxxxxxxxx x provokačních xxxxxxx, xx měla xxx prováděna xxxxx xxxxxxxx Xxxxxxxxxx/Xxxxxxxx (xxx xxxxxxx). Xxx xxxxxxxxx xxxxxxxxx xxxxxx xxxxx xxx xxxxxxxxx jiné xxxxxxx, xxxx. xxxxxxxxxxxxxxxx xxxxxxxxx xxxx měření xxxxxxxx kožní xxxx.
1.5.2 Xüxxxxxxx xxxxxxx
1.5.2.1 Xxxxxxxx
Xxxxxx xxxxx dospělá xxxxxxxxxxx xxxxxxx xx xxxxxxxxxxxx xx xxxxxxxxxxx xxxxxxxx xxxxxxx 5 dnů xxxx zahájením zkoušky. Xxxx zkouškou xx xxxxxxx xxxxxxx xxxxx xxxxxx x xxxxxxx xx xxxxxxx xx xxxxxxxxxxxxxxxx x xxxxxxxxxxx xxxxxx. Xxxx se xxxxxxxx xxxxxxxxx, xxxxxxx xxxx xxxxxxxxx xxxxxxxx, x závislosti xx xxxxxxx zkušební metodě. Xx třeba dbát xx xx, xxx xxxxxxx x xxxxxxxxx xxxx. Xxxxxxx se xxxxx xxxx xxxxxxxxx xxxxxxx a xx xxxxx xxxxxxx.
1.5.2.2 Zkušební xxxxxxxx
1.5.2.2.1 Pokusná xxxxxxx
Xxxxxxxxx xx xxxxx xxxxxxxxx xxxxxxxxxxx kmeny xxxxxxxxxxxxx xxxxxx.
1.5.2.2.2 Xxxxx a xxxxxxx
Xxxxxx lze xxxxx x xxxxxx. Xxxxxxx xxxxxx musí být xxxxxxxxx x xxxxx xxx xxxxx.
Xxxxxxxxxxxxxx xxxxxxx xx xxxxxx xxxxxxx x 20 zvířat x kontrolní xxxxxxx xxxxxxx z 10 xxxxxx.
1.5.2.2.3 Úrovně dávek
Koncentrace xxxxxxxx xxxxx použitá xxx každou xxxxxxxx xxxxxxxx xx xxxx xxx xxx xxxxxxxx xxxxxxxxxxx, která vyvolá xxxxx, ne xxxx xxxxx xxxxxxxxxx xxxx. Xxxxxxxxxxx xxxxxxx xxx xxxxxxxxxx xxxxxxxx xx xxxx xxxxxxxxx xxxxxxxx xxxxxxxxxxx, která nevyvolává xxxxxxxxxx. X xxxxxxx xxxxxxx mohou být xxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxxxxxx pokusem xx xxxx nebo xxxxx xxxxxxxxx.
Xxx zkoušené xxxxx xxxxxxxxx ve xxxx xx xxxxxx používat xxxx xxxxxxxxx vodu xxxx xxxxxxxxxx zředěné xxxxxxx povrchově xxxxxxx xxxxx. Xxx xxxxxxx xxxxxxxx xxxxx xx xxxxxxxxxxxxx xxxxxx 80 % alkoholu ve xxxx xxx indukci x aceton xxx xxxxxxxxx.
1.5.2.3 Xxxxxx
1.5.2.3.1 Xxxxxxx
Xxx 0 – xxxxxxxxxxxxxx xxxxxxx
Xxxxx xxx xx xxxxx xxxxx (xxxxxxxx xx xxxxxxx). Xxxxxxxx xxxxxx xx měl xxx důkladně napuštěn xxxxxxxxx látkou ve xxxxxxx vehikulu (výběr xxxxxxxx musí být xxxxxxxxx; tekuté zkoušené xxxxx xxxxx xxx xxxxx potřeby aplikovány xxxxxxxx).
Xxxxxxxx xxxxxx se xxxxxxx xx xxxxxxxx xxxxxx a xx xxxx 6 x xx udržuje xx xxxxx x kůží xxxxxxxxxx xxxxxxx nebo xxxxxxxx x vhodným xxxxxxx.
Xxxxxx s xxxxxxx xxxx xxx xxxxxxxxx. Xxxxxx xx xxxxxxxx xxxxxxxxx, xxxx xxx xxxxxxx xxxx čtvercový, xxx xxx xx xxx velikost xxxxxxxxx 4 – 6 xx2. Pro xxxxxxxxx xxxxxx xx xxxxxx xxxxxx xxxxxxx xxxxxx. Xxxx-xx xxxxxxx xxxxxx, xxxxx být xxxxxxxx xxxxxxxxx xxxxxxxx.
Xxx 0 – xxxxxxxxx xxxxxxx
Xxxxx xxx xx xxxxx xxxxx (xxxxxxxx xx xxxxxxx). Xx xxxxxxxx xxxxxx xx xxxxxx xxxxxxxxx xxxxxxxx xxxxxxxx xxxx x experimentální xxxxxxx. Xxxxxxxx plátek xx xx xxxx 6 x udržuje xx xxxxx s xxxx pomocí xxxxxxxxxxx xxxxxx xxxx komůrky x xxxxxxxx xxxxxx. Xxxxx xx možné xxxxxxxx, že xxxxxxxxx xxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxx xxxx nezbytná, xxx xxxxxx xxxxxxxxxxxxx xxxxxxxxx xxxxxxx.
6. – 8. x 13. – 15. den – experimentální a xxxxxxxxx xxxxxxx
Xxxxxxx xx xxxxxx xxxxxxxx jako x xxx 0 xx xxxxxxx xxxxxxxx xxxxxx (v xxxxxxx xxxxxxx xxxxxxxx srsti) xx xxxxxx bok, x xx 6. – 8. den x opět 13. – 15. xxx.
1.5.2.3.2 Xxxxxxxxx
27. – 29. xxx – experimentální x kontrolní xxxxxxx
Xxxxxxxxxx xxx xxxxxxxxx x xxxxxxxxxxx xxxxxx xx xxxxx srsti (důkladně xx xxxxxxx). Okluzivní xxxxxx xxxx xxxxxxx xxxxxxxxxx příslušné xxxxxxxx xxxxxxxx xxxxx x xxxxxxxx xxxxxxxxxx xxxxxxxxxxx xx xxxxxxxx xx xxxxx xxxx xxxxxxxxxxxx xxxx xxxxxxxxx a xxxxxxxxxxx xxxxxx.
Xx přední xxxx xxxxxxxxxxxx boku xxxxxxxxx a xxxxxxxxxxx xxxxxx xx popřípadě xxxxxxxx xxxxxxxxx xxxxxx xxxx komůrka jen x vehikulem. Plátky xxxx komůrky xx xx xxxx 6 x xxxxxx xx xxxxx x kůží xxxxxx xxxxxxxx xxxxxx.
1.5.2.3.3 Xxxxxxxxxx x xxxxxxxxx
- Xxxxxxxxx 21 x xx odstranění xxxxxx xx xxxxxxxxxx xxxxxx xxxxx srsti;
- xxxxxxxxx xx xxxxx xxxxxxxx (xxxxxxxxx 30 x xx aplikaci xxxxxxxxxxxx xxxxxx) se xxxxxxxx xxxxx reakce a xxxxxxxxxxx xx podle xxxxxxxx uvedené x xxxxxxx;
- xxxxxxxxx 24 x po 30xxxxxxxxx xxxxxxxxxx (přibližně 54 x xx xxxxxxxx xxxxxxxxxxxx plátku) xx xxxx pozorují xxxxx xxxxxx x zaznamenají xx.
Xxxxxxxxxx se xxxxxxxx xxxxxxxxxx "xxxxxxx" x xxxxxxxxx x xxxxxxxxxxx xxxxxx.
Xxxxx xx xx xxxxxxxx xxx xxxxxxxxx xxxxxxxx xxxxxxxxx při xxxxx provokaci, xxxx xx xxx xxxxxxxxx xxxxx xxxxx xx xxxxx provokaci xxxxxxx xxxxx xxxxxxxxx (xx. xxxxxxxxx provokace), x xxxxxxx xxxxxxx x xxxxx kontrolní xxxxxxxx. Xxxxxxxxx provokace xxxx xxx xxxxxxxxx xxxx xx xxxxxxx xxxxxxxxx xxxxxxx.
Xxxxxxxxxx a xxxxxxxxxxxxx xxxxx kožních xxxxxx x xxxxxxxxxxx nálezů, xxxxxx xxxxxxxxxxx xxxxxx, xxxxx jsou xxxxxxxxx xxxxxxxxxx x xxxxxxxxxxxx xxxxxxx, by xxxx xxx xxxxxxxxx xxxxx xxxxxxxx Xxxxxxxxxx/Xxxxxxxx (viz xxxxxxx). Xxx xxxxxxxxx xxxxxxxx reakcí xxxxx xxx xxxxxxxxx xxxx xxxxxxx, např. histopatologické xxxxxxxxx nebo xxxxxx xxxxxxxx xxxxx řasy.
2. XXXXX (XXXX A XÜXXXXXXX XXXXXXX)
Xxxxx se xxxxxx xx xxxxxxx, xxxxxxx xx xxx xxxxx xxxxx xxxxxx xxxxx reakce xxx xxxxxx pozorování.
3. ZPRÁVY (XXXX X BÜHLEROVA XXXXXXX)
Xxxxx xxxx před xxxxxxxx xx xxxxxxxxx xxxxxxxxx xxxxxxxxxxxx xxxxxxx (xxxx. zkouška xxxxxxxxxxxx xxxxxxxxxxxx uzlin (XXXX), xxxxxxx xxxxxxxxx xxxx x xxxx (MEST)), xxxx xxx s xxxxxxxx získanými se xxxxxxxxxx a referenčními xxxxxxx xxxxxx xxxxx xxxx xxxxxxx nebo xxxxx na tuto xxxxxxx, xxxxxx xxxxxxxxxx xxxxxxxxx x xxxxxxx.
Xxxxxxxx x zkoušce (GMPT x Xüxxxxxxx xxxxxxx)
Xxxxxxxx x xxxxxxx xx xxxxx možno xxxxxxxxx xxxx xxxxxxxxx:
Xxxxxxx xxxxxxx
- xxxxxxx xxxx morčat;
- xxxxx, xxxxx a xxxxxxx zvířat;
- xxxxx, xxxxxxxx chovu, strava xxx.;
- hmotnost jednotlivých xxxxxx na xxxxxxx xxxxxxx.
Xxxxxxxx xxxxxxxx:
- technika xxxxxxxx místa xxxxxxxx;
- xxxxxxxx informace x xxxxxxxxxxx použitých xxx xxxxxxxx x technice xxxxxxxx;
- xxxxxxxx xxxxxxxxx xxxxxx x xxxxx xxxxxxxx se indukčních x xxxxxxxxxxxx xxxxxxxxxxx, xxxxx byly xxx xxxxxxx xxxxxxx;
- xxxxxxxx xxxxx x přípravě, xxxxxxxx a odstranění xxxxxxxx xxxxx;
- xxxxxxxxxx xxxxx xxxxxxxx,
- xxxxxxxxxxx xxxxxxxx x xxxxxxxx xxxxx xxxxxxx pro xxxxxxxx x provokační xxxxxxxx x xxxxxxx xxxxxxxx látky xxxxxxx xxx xxxxxxx x xxxxxxxxx.
Xxxxxxxx:
- xxxxxx xxxxxxxx xxxxxxxx kontroly citlivosti x xxxxxxxxxxxxx (viz 1.3), včetně informací x xxxxxxx xxxxx, xxxxxxxxxxx a xxxxxxxx;
- xxxxxxxxxx jednotlivých zvířat, xxxxxx xxxxxxx klasifikace;
- xxxxxxxx popis xxxxxxxxxx x xxxxxx pozorovaných xxxxxx;
- xxxxxxx xxxxxxxxxxxxxxxx xxxxxx.
Xxxxxx výsledků.
Závěry.
4. LITERATURA
Metoda xx xxxxxxxxxx metodě XXXX XX 406.
Xxxxxxx
XXXXXXX:
Xxxxxxxx Xxxxxxxxxx/Xxxxxxxx xxx hodnocení xxxxxxx xxxxxx na xxxxxxxxxx xxxxxxxx
|
0 = |
žádná xxxxxxxxx změna | |
|
1 = |
xxxxx xxxx xxxxxxxx xxxxxxxxx kůže |
|
2 = |
mírné x xxxxxxxxxx zarudnutí xxxx |
|
3 = |
xxxxxxxxxx zarudnutí x xxxxxxx xxxx" |
XXXXXXX XX X
" X.7 ORÁLNÍ XXXXXXXX (28XXXXX XXXXXXXXX XXXXXXXX)
1. XXXXXX
1.1 Xxxx
Xxx obecný xxxx, xxxx X.
1.2 Xxxxxxxx
Xxx obecný úvod, xxxx B.
1.3 Podstata xxxxxxxx metody
Zkoušená xxxxx xx denně xxxxxx xxxxxx v xxxxxxxxxxxxxx xxxxxxx několika skupinám xxxxxxxxx xxxxxx; xxxxx xxxxxxx xx podává xxxxx xxxxxx dávky 28 xxx. X xxxxxxx období xxxxxxxx xx xxxxxxx xxxxx xxx xxxxxxx xxxxxxxx, xxx se xxxxxxxx xxxxxxxx toxicity. Zvířata, xxxxx v průběhu xxxxxxx xxxxxxx xxxx xxxx xxxxxxxx, x xxxxxxx, xxxxx do xxxxx zkoušky xxxxxxx, xx xxxxxxx.
Xxxx xxxxxx xxxxx xxxxx xxxxx xx neurologické xxxxxx xxxx na specifické xxxxxxxx účinky; xxxxx xx xxxxxx xx xxxxxxx xxxxxxxxx klinického xxxxxxxxxx xxxxxx, aby xxxx xxxxxxx xx xxxxxxx informací. Xxxxxx xx xxxx xxxxxxx xxxxxxxx látky s xxxxxxxxxxxxx potenciálem, u xxxxx může xxx xxxxxxxx xxxxx xxxxxx xxxxxxxx xxxxxx aspektu. Xxxxxx xxxx xxxxxxxxx xx xxxxxxxxxxxx xxxxxx x xxxxxxxx xxx xxxxxxxxxxx xxxxxx.
1.4 Popis xxxxxxxx metody
1.4.1 Xxxxxxxx
Xxxxxx xxxxx xxxxxxx zvířata xx xxxxxxx xxxxxxx xx kontrolních x xxxxxxxxxxxxxxxx skupin. Xxxxx xx xxxx xxx xxxxxxxxxx xxx, aby xxx vliv xxxxxxxx xxxxx xxxxxxxxxxxxx. Xxxxxxxxxx xxxxxxx xx jednoznačně xxxxxxxxxxxx x xxxxxx xx xx xxxxx xxxxxxx pět xxx xxxx začátkem xxxxxx, xxx xx xxxxx xxxxxxxx xx xxxxxxxxxxx xxxxxxxx.
Xxxxxxxx látka se xxxxxx sondou nebo x potravě xx x pitné xxxx. Xxxxxx orálního podání xxxxxx na xxxxx xxxxxx a xx xxxxxxxxx-xxxxxxxxxx vlastnostech látky.
Zkoušená xxxxx xx xxxxx xxxxxxx xxxxxxxx xxxx xxxxxxxxxx ve xxxxxxx xxxxxxxx. Xx-xx xx xxxxx, xxxxxxxxxx se xxxxxx xxxxxxx vodného xxxxxxx/xxxxxxxx, potom xxxxxxx xxxxxxx/xxxxxx x xxxxx (xxxx. xxxxxxxxx xxxx) x xxxxxxx xxxxxxx x xxxxxx vehikulech. Xxx nevodná xxxxxxxx xx měla xxx xxxxx jejich xxxxxxx xxxxxxxxxxxxxxx. Xxxx by xxx xxxxxx stálost xxxxxxxx xxxxx ve xxxxxxxx.
1.4.2 Xxxxxxxx podmínky
1.4.2.1 Xxxxxxx zvířata
Dává xx xxxxxxxx xxxxxxxx, ale xxx xxxxxx x xxxxxx xxxxx hlodavců. Xxxxxxx xx xxxx xxx xxxxx xxxxxxxxx xxxxx xxxxxxx xxxxxxxx xxxxxxxxx zvířat. Samice xxxx xxx nullipary x xxxxx xxx xxxxx. Xxxxxxxx xxxxx xx xxxx začít xx xxxxxxxx xx xxxxxxxxx x x xxxxxx xxxxxxx dříve, xxx zvířata xxxxxxxx xxxxx xxxxxx xxxxx.
Xx xxxxxxx xxxxxx xx xxxx xxx xxxxxxxx xxxxxxxxx zvířat xxxxxxxxx x neměly xx xxxxxxxxx ±20 % xxxxxxx xxxxxxxxx pro xxxxx pohlaví.
Provádí-li xx xxxxxx opakovaného orálního xxxxxxxx xxxxx xxxx xxxxxxxxx xxxxxx xxx xxxxxxxxxxx xxxxxx, xxxx xx xxx x xxxx studiích použita xxxxxxx zvířata xxxxxxxx xxxxx a xxxxxxxx xxxxxx.
1.4.2.2 Xxxxx x xxxxxxx
Xxx xxxxxx úroveň xxxxx xx použije xxxxxxx 10 xxxxxx (xxx xxxxx x xxx samců). Pokud xx budou xxxxxxx xxxxxxxxx v průběhu xxxxxx, je nutno xxxxxx celkový xxxxx xxxxxx o počet xxxxxx, xxxxx budou xxxxxxxx xxxx koncem xxxxxx.
Xxxxx toho může xxx xxxxxxxxx xxxxxxx 10 xxxxxx (xxx xxxxxx xxxxxxx xxxxxxx) xxxxxxxx xxxxxx úroveň xxxxx xx xxxx 28 xxx x 14 xxx xx xxxxxxxx se xxxxxxxx xxxxxxxx, xxxxxxxxxxx xxxx xxxxxxxx xxxxxx xxxxxxxxx xxxxxx. Xxxxxxx xx xxxx xxxxxxxxx xxxxxxx 10 xxxxxxxxxxx xxxxxx (xxx xxxxxx xxxxxxx xxxxxxx).
1.4.2.3 Úrovně xxxxx
Xxxxxx xx xxxx být xxxxxxx xxxxxxx tři xxxxxxxxxxxxxx xxxxxxx a xxxxx kontrolní xxxxxxx. X xxxxxxxx xxxxxxxx xxxxxxxx látky se xx xxxxxxx v xxxxxxxxx skupině xxxxxxx xxxxxx xxxx xx xxxxxxx v xxxxxxxxxxxxxx xxxxxxx. Xxxxx se xxx xxxxxxxx zkoušené xxxxx používá xxxxxxxxx, xxxxxx xx xxxxxxxxx xxxxxxx x xxxxxxxxx xxxxxxxx xxxxxx.
Xxxxx xx xx xxxxxxxxx xxxxxx xxxxx neočekávají xxxxx xxxxxx xxx dávce 1000 xx xx xx xxxxxxx xxxxxxxxx, xxxx xxx xxxxxxxxx xxxxxxx zkouška. Xxxxxx-xx xxxxxxxx žádné xxxxxx xxxxx, xxxx xxx xxxxxxxxx předběžná studie xxx stanovení rozmezí xxxxx, které mají xxx použity.
Při xxxxxx xxxxxx xxxxx xx xxxx být zohledněny xxxxxxx xxxxxxxxxx xxxxx x xxxxxxxxx x xxxxxxxxxxxxxxxxx vlastnostech, xxxxx xxxx pro zkoušenou xxxxx xxxx příbuzné xxxxxxxxx dostupné. Nejvyšší xxxxxx xxxxx xx xxxxxxx xxxxxxx xxxxxx, xx však uhynutí xxxx velké xxxxxxx. Xxxx xx měla xxx xxxxxxx xxxxxxxx xxxx úrovní xxxxx x cílem prokázat xxxxxx související x xxxxxx x xxxxxxxxxxxx xxxxxxxxxxxx xxxxxx xxx xxxxxxxx xxxxxx dávky (XXXXX). Xxxxx xx xxx stanovení xxxxxxxxxx xxxxxx xxxxx xxxxxxxxx xxxx- xx čtyřnásobný xxxxxxxx xxxx dávkami x je xxxxxxxxx xxxxxx xxxxxxx xxxxxxxxxxxxxx xxxxxxx, xxx xxxxxx xxxxx velké xxxxxxxxx (xxxxxxxxxxxx např. faktoru xxxxxxx xxx 10).
U xxxxx xxxxxxxxxx x xxxxxxx nebo x xxxxx xxxx xx xxxxxxxx xxxxxxxx, aby xxxxxxxx použité zkoušené xxxxx neovlivňovalo normální xxxxxx xxxx xxxxx xxxxxxxxx. Podává-li se xxxxxxxx xxxxx x xxxxxxx, xxxx se xxxxxx buď konstantní xxxxxxxxxxx (v ppm) xxxx konstantní xxxxxxxxx xxxxxxxx x xxxxxxx xxxxxxxxx zvířete; xxxxxxx xxxxxxx musí xxx xxxxxxxxxxxxx. Xxxxxxxx-xx xx xxxxx xxxxxx, xxxx xx xx xxx xxxx xxxxx xxx xxxxxxxxx xx xxxxxxx xxxx, x xxxxxxxxx xx xxxx být xxxxx xxxxxxx xxxxxxxx xxx, xxx bylo xxxxxxxxxx xxxxxxxx x xxxxxxx xxxxxxxxx zvířete.
Pokud xx xxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxx xxxxxxxxx studie k xxxxxxxxxx studii, xxxx xx xxx v xxxx xxxxxxxx xxxxxxx xxxxxx xxxxxxx.
1.4.2.4 Xxxxxxx xxxxxxx
Xxxxx xxxxxxx provedená xxxxx xxxxxxx xxxxxxxxx x xxxx xxxxxx xxx xxxxx dávce xxxxxxx 1000 xx xx xx tělesné xxxxxxxxx xx den xxxx x případě xxxxxxxx x xxxxxxx xxxx v pitné xxxx v odpovídající xxxxxxxxxxx (xx xxxxxxx xxxxxxxxx xxxxxxx xxxxxxxxx) xxxxxxxx xxxxxxxxxxxxx toxické xxxxxx x pokud xx xx xxxxxxx xxxxx x látkách x xxxxxxxx strukturou xxxxxxxxxxxxx toxicita, xxxx xxxxx studie xx xxxxxxx xxx úrovní xxxxx xxxxx. Xxxxxxx xxxxxxx xx xxxxxxx x výjimkou xxxxxxx, xxx údaje x xxxxxxxx xxxxxxx xxxxxxxxx, xx xx nezbytné xxxxxxx vyšší xxxxxx xxxxx.
1.4.2.5 Doba pozorování
Doba xxxxxxxxxx by měla xxx 28 xxx. Xxxxxxx x xxxxxxxxx xxxxxxx xxxxxx pro xxxxxxxx xxxxxxxxxx by xxxx xxx xx xxxxxxx xxxxxxx 14 xxx bez xxxxxxxx, xxx se xxxxxxxx xxxxxxxx výskyt, xxxxxxxxxxx xxxx xxxxxxxx z xxxxxxxxx xxxxxx.
1.4.3 Xxxxxx
Xxxxxxxx xxxxx se podává xxxxxxxx xxxx dnů x xxxxx xx xxxx 28 xxx. Xxxxx xx xxxxx xxxxxx xxx xxx x xxxxx, xxxx xx být xxxxxxxxxx. Xxxxx se xxxxxxxx xxxxx xxxxxx sondou, xxxxxx se xxxxxxxx x xxxxxx dávce xx použití žaludeční xxxxx xxxx xxxxxx xxxxxxxxx xxxxxx. Xxxxxxxxx xxxxx xxxxxxxx, xxxxx xxx xxxxx xxxxxxxx, xxxxxx xx xxxxxxxxx xxxxxxxxx xxxxxxx. Xxxxx xx xxxxx překročit 1 xx xx 100 x tělesné xxxxxxxxx, s výjimkou xxxxxxx xxxxxxx, xxx xxx xxxxxx 2 xx na 100 x xxxxxxx xxxxxxxxx. X výjimkou xxxxxxxxxx xxxx xxxxxxxx látek, x xxxxxxx xx xx vyšších xxxxxxxxxxxxx xxxxxxxx xxxxxx, by xxxx xxx xxxxxxx xx xxxxxxxxx xxxxxx xxxxxxxxxxxxxx xxxxxxx xxxxxxxxxxx xxx, xxx byl xxx xxxxx xxxxxxxx xxxxx podáván xxxxxxxxxx xxxxx.
1.4.3.1 Xxxxxx pozorování
Všeobecné xxxxxxxx xxxxxxxxxx xx xx xxxx provádět xxxxxxx jednou denně, xxxxxxx ve xxxxxxx xxxx (xxxxxx xxxx) x x xxxxxxxx xxxx očekávaného maxima xxxxxx po podání xxxxx. Xxxxxxxxxxx xx xxxxxxxxx xxxx xxxxxx. Xxxxxxx xxxxxxx denně xx provede xxxxxxxxx xxxxx xxxxxx xx xxxxxx xxxxxxxx morbidity x xxxxxxxxx. Xxxxxxx x agónii x xxxxxxx, xxxxx xx xxxxx nebo xxxx xxxxxxx, se xxxxx xxxxxx, xxxxxxx utratí x pitvají.
Před xxxxxx xxxxxxx xxxxx a xxxx xxxxxxx xxxxxx xxxxx se xxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx xxxxx xxxxxx (za xxxxxx xxxxxxxxxxxxxx xxxxxxxxx). Xxxx xxxxxxxxxx xx xx mělo xxxxxxxx xxxx chovnou xxxx xx xxxxxxxxxxx xxxxxxxxxxx xxxxxxxx x nejlépe xxxxxxx xx xxxxxxx xxxx. Xxxxxxxxxx xx xxxx xxx xxxxxxx xxxxxxxxxxxxx, nejlépe xx xxxxxxx systému xxxxxxxx xxxxxxxxxx definovaného ve xxxxxxxx laboratoři. Xxxx xx xx xxxxxxxx x xx, aby xxxx xxxxxxx xx xxxxxxxxxx xxxxxxxxxx co xxxxxxxx a aby xxxxxxxxx prováděly xxxxxxx xxxxx, které xxxxxx x zařazení xx xxxxxxx xxxxxxxxxxx. Vyšetření xx xxxx xxxx xxxx zahrnovat změny xxxx, srsti, očí x sliznic, xxxxxx xxxxxxx x exkretů x xxxxxxxxxxxxx xxxxxx (xxxxxx, xxxxxxx xxxxx, xxxxxxxx xxxxxx, nezvyklé xxxxxxx). Xxxxxxxxxxxx by xx měly změny xxxxx, xxxxxx x xxxxxx na xxxxxxxxxx, xxxx xxxxxxxxxx xxxxxxxxxx x tonických pohybů, xxxxxxxxxx x xxxxxxx (xxxx. xxxxxxxxxx xxxxxxxxx xxxxxx xxxx opakovaného xxxxxxxx) nebo xxxxxxxxx xxxxxxx (např. sebepoškozování, xxxxxx xxxxxxxx).
Xx čtvrtém xxxxx xxxxxxxx látky xx xxxxxxxx xxxxxx xx různé xxxxxxxx xxxxxxx (xxxx. xxxxxxxx, xxxxxxx, proprioceptivní) x xxxxx xx síla xxxxxx x xxxxxxxxx xxxxxxxx. Xxxxx podrobné xxxxxxxxx x postupech, xxxxx xx xxxxx xxxxxx, xxxx uvedeny x xxxxxxxxxx (xxx xxxxxx xxxx, část X).
Xxxxxxxxxx xxxxxxxxx xxxxxx xx čtvrtém xxxxx xxxxxxxx látky xxx xxxxxxxx xxxxxxxx, pokud xx studie xxxxxxxxx xxxx předběžná pro xxxxxxxxx xxxxxxxxxxxxx (90xxxxx) xxxxxx. X xxxxxxx xxxxxxx xx xxxxxxxxxx xxxxxxxxx xxxxxx zahrnuto xx dlouhodobé xxxxxx. Xxxxxxxxxx xxxxx x xxxxxxxxxxxx xxxxxxxxx poruchách xx xxxxxx xxxxxxxxxxx xxxxxxxx dávky xxxx xx druhé straně xxxxxxxx výběr xxxxxx xxxxx xxx xxxxxxxxx xxxxxxxxxxxxx xxxxxx.
Xxxxxxxxxx funkčních xxxxxx xxx xxxxxxxxx xxxxxxxx u skupin, xxxxx xxxxxxxx xxxxxxxx xxxxxxxx x takové xxxx, že xx xxxxxxx významně narušily xxxxxx xxxxxxx stav.
1.4.3.2 Xxxxxxx hmotnost x xxxxxxxx xxxxxxx/xxxx
Xxxxxxx zvířata xx xx měla xxxxxxx xxxxxx týdně xxxxxx. Xxxxxx spotřeby xxxxxxx a xxxx xx xx mělo xxxxxxxx xxxxxxx jednou xxxxx. Xxxxx xx xxxxx xxxxxx v xxxxx vodě, xxxx xx xx nejméně xxxxxx xxxxx měřit xxxxxxxx xxxx.
1.4.3.3 Xxxxxxxxxxxxx xxxxxxxxx
Xx konci zkoušky xx měla xxx xxxxxxxxx tato hematologická xxxxxxxxx: xxxxxxxxx xxxxxxxxxxx, xxxxxxxxxxx xxxxxxxxxxx, xxxxx xxxxxxxxxx, celkového x xxxxxxxxxxxxxxx xxxxx leukocytů, xxxxx xxxxxxxxxx x xxxxxxx xx protrombinový xxx.
Xxxxxx xxxxxx xx xx xxxx xxxxxxxx x xxxxxxxx místa xxxxx xxxx xxxxxxxxx xxxxxx xxxx v xxxx xxxxxxx x xxxx xx se xxxxxxxxx xx xxxxxxxx xxxxxxxx.
1.4.3.4 Klinická xxxxxxxxxxx xxxxxxxxx
Xxxxxxxx xxxxxxxxxxx xxxxxxx xx účelem xxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxx xx xxxxx a xxxxxxx xx xxxxx x xxxxxxx se xxxxxxxx xx krevních xxxxxxxx odebraných xxxx xxxxxxxx xxxx xxxxxxxxx xxxx x xxxx xxxxxxx (xxxxx xxxxxx xxxxxxxxxx x xxxxxx x/xxxx xxxxxx utracených x xxxxxxx xxxxxxx). Xxxx xxxxxxxxx krevních xxxxxx xx doporučuje xxxxxxxx zvířata xxxx xxx xxx potravy [1].Xxxxxxxxx xxxxxx x xxxx xxxxxxxx xxxxxxxxx xxxxxx, xxxxxxxx, glukosy, xxxxxxxxx xxxxxxxxxxxx, močoviny, xxxxxxxxxx, celkových xxxxxxxx x albuminu, nejméně xxxx xxxxxx xxxxxxxxxxxx xxxxxx na xxxxxxx xxxxx (xxxx xxxxxxxxxxxxxxxxxxxxxx, xxxxxxxxxxxxxxxxxxxxxxxx, xxxxxxxxx xxxxxxxxx, xxxx xxxxxxxxxxxxxxxxxxxxxx x xxxxxxxxxxxxxxxxxxxxx). Xxxxxxxxx xxxxxxx xxxxxx (jaterního nebo xxxxxx xxxxxx) x xxxxxxxxx xxxxxxx může xx určitých okolností xxxxxxxxxx užitečné xxxxxxxxx.
Xxxx xx možné x xxxxxxx xxxxxxxxxx xxxxx xxxxxx xxxxxxx xxxxxxxxxxx xxxxxxx xxxx xx xxxxxxx časově xxxxxxxxxxxx xxxxx: vzhled, objem, xxxxxxxxxx nebo xxxxxxxxxx xxxxxxxx, xX, xxxxxxxxx, xxxxxxx x xxxx/xxxxxxx.
Xxxx xx se xxxx xxxxxx vyšetření indikátorů xxxxxxxxx xxxxxxxxx xxxxx x séru. Další xxxxxxxxx by xxxx xxx xxxxxxxxx, xxxxx xxxxx známé xxxxxxxxxx xxxxxxxx látky xxxxxxxx xxxxxxxxxxxx xxxxxxxxxxx xxxxxxx, xxxxxx xxxxxxx, fosforu, xxxxxxxxxxxx xx xxxxx, xxxxxxxxxxxx xxxxxxx, xxxxxxxxxxxxxx x cholinesterasy. Xxxx xxxxxxx je třeba xxxxxxxxxxxxx xxx látky xxxxxxxx skupin nebo xxxxxx xx případu.
Obecně xx třeba xxxxxxxxxx xxxxxx x xxxxxxxxxx xx druhu x xx xxxxxxxxxxxx x/xxxx xxxxxxxxxxxxxxx xxxxxxxx dané xxxxx.
Xxxxx xxxxxx xxxxx x xxxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxxxx, xxxx xx xx xxxxxx xxxxxxxxx xxxxxxxxxxxxxxx a xxxxxxxxxx xxxxxxxxxxxxx parametrů xxxx xxxxxxxx xxxxxxx.
1.4.3.5 Xxxxx
X všech xxxxxxxxx xxxxxx xxxxxxxxxx xx xxxxxx by xxxx xxx provedena xxxxxxx, xxxxxxxx xxxxx, xxxxxxxxxx xxxxxxx xxxxxxxx xxxxxxxx xxxxxxx xxxx, všech xxxxxx x xxxxxx xxxxxxx, xxxxxx x xxxxxx x jejich xxxxxx. Xxxxx, xxxxxxx, xxxxxxxxxxx, xxxxxxx, nadvarlata, xxxxxx, xxxxxxx, mozek x xxxxx všech xxxxxx by xxxx xxx xxxxxxx xxxxx xxxxxxxx xxxxx a xx xxxxxxxx po xxxxx se xx xxxxxx xxxxx zváží, xxx xxxxxxx x xxxxxxxxx.
Xxxxxxxxxxx xxxxx by xxxx xxx xxxxxxxxxx x xxxxxxxxxxxxx xxxxxxxx xxxxx x ohledem xx xxx xxxxx x xxxxxxxxx xxxxxxxx xxxxxxxxxxxxxxxx vyšetření: všechny xxxxx x lézemi, xxxxx (xxxxxxxxxxxxxxx xxxxxxx, xxxxxx hemisfér, xxxxxxx x mostu), mícha, xxxxxxx, tenké x xxxxxx xxxxxx (včetně Xxxxxxxxxx xxxxx), játra, xxxxxxx, nadledvinky, xxxxxxx, xxxxx, xxxxxx, xxxxxx xxxxx, xxxxxxxxxx x xxxxx (xxxxxxxxxxxx xxxxxxxxx xxxxxxxx roztokem a xxxxxxxxx), xxxxxx a xxxxxxxx xxxxxxxx xxxxxx (xxxx. xxxxxx, xxxxxxxx), xxxxxx xxxxxx, lymfatické xxxxxx (přednostně xxxxx xxx oblast aplikace x jedna xxxxxxxx xxx xxxxxxx xxxxxxxxxxx xxxxxx), xxxxxxxxx xxxx (x. xxxxxxxxxxx nebo x. xxxxxxxx), xxxxxxx x blízkosti svalu, xxx xxxxxx xxxxx (xxxx čerstvý nátěr x xxxxxx xxxxxx xxxxx). Xxxxx xxxxxxxxxx xxxx xxxxxx xxxxxx xxxx xxx xxxxxxxx xxxxxxx x xxxxx xxxxx. Xxxxxxx orgány xxxxxxxxxx xx možné xxxxxx xxxxxx pro xxxxxxxx xxxxxxxx xxxxx xx xxxx xxx xxxxxxxx.
1.4.3.6 Histopatologická xxxxxxxxx
X xxxxx xxxxxx xxxxxxxxx xxxxxxx x xxxxxxx, xxxxx byla xxxxxx xxxxxx xxxxx, by xxxx být xxxxxxxxx xxxxxxx xxxxxxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxx x xxxxx. Xxxx xxxxxxxxx xx xxxx xxx xxxxxxxxx na xxxxxxx xxxxx xxxxxxxxx xxxxxxxxx xxxxxx, pokud jsou x xxxxxxx x xxxxxxx dávkou pozorovány xxxxx xxxxxx vyvolané xxxxxxxxx dávkou.
Všechny xxxxxxxxxxxxx xxxx by xxxx xxx zkoumány.
V xxxxxxx xxxxxxx satelitní xxxxxxx xx xxxx xxx xxxxxxxxx xxxxxxxxxxxxxxxx xxxxxxxxx xxxxx a xxxxxx, xx xxxxxxx xxxx xxxxxxxxxx účinky u xxxxxxxxxxxx xxxxxx.
2. XXXXX
Xxxx xx xxx uvedeny xxxxx xxx každé xxxxxxxxxx xxxxx. Navíc xx xxxx být xxxxxxx xxxxx shrnuty xx xxxxxxx, xxxxxxx xx xxxxx x xxxxx xxxxxxxxxxxxxx xxxxxxx xxxxx xxxxxx xx xxxxxxx zkoušky, xxxxx xxxxxx xxxxxxxxxx uhynulých x xxxxxxx xxxxxxx xxxx xxxxxxxxxx x xxxxxxxxx xxxxxx x xxxx xxxxx nebo xxxxxxxxx xxxxxxxx, xxxxx xxxxxx xxxxxxxxxxxx xxxxxxxx xxxxxxxx, xxxxx xxxxxxxxx xxxxxxxx, xxxxxx doby xxxxxxx, xxxxxx a xxxxxxxxxx xxxxxxx toxického xxxxxx, xxxxx xxxxxx xxxxxxxxxxxx xxxx, xxx xxxx a xxxxxxxx xxxxxx xxxxxxxxxxxx xxxxx xxx xxxx.
Xxxxxxx xxxxxxxx xx xxxx být xxxxx možno vyhodnoceny xxxxxxx a xxxxxx xxxxxxxxx xxxxxxxxxxxx metodou. Xxxxxxxxxxx metoda xx xxxx xxx xxxxxxx xxx při xxxxxxxxx xxxxxx.
3. XXXXXX
Xxxxxxxx x xxxxxxx
Xxxxxxxx o xxxxxxx xx pokud možno xxxxxxxxx xxxx informace:
Pokusná xxxxxxx:
- použitý druh/kmen;
- xxxxx, stáří x xxxxxxx xxxxxx;
- xxxxx, xxxxxxxx xxxxx, xxxxxx xxx.;
- xxxxxxxx xxxxxxxxxxxx xxxxxx na xxxxxxx xxxxxxx, xxxx v xxxxxxxxx xxxxxxxxxxx x xx xxxxx xxxxxxx.
Xxxxxxxx xxxxxxxx:
- xxxxxxxxxx xxxxx xxxxxxxx, není-li xxxxxxx xxxx;
- xxxxxxxxxx xxxxxx xxxxxx xxxxx;
- podrobné xxxxx x složení xxxxx nebo xxxxxx xxxxxxx, x xxxxxxxx xxxxxxxxxxx, stálosti x xxxxxxxxxx přípravku;
- xxxxxxxx xxxxx x xxxxxxx xxxxxx zkoušené látky;
- xxxxxxxxx xxxxxxxx koncentrace xxxxxxxx xxxxx x xxxxxxx/xxxxx vodě (ppm) xx skutečnou xxxxx xxxxx (xx na xx tělesné xxxxxxxxx);
- xxxxxxxx xxxxx o xxxxxx x xxxxxxx xxxx.
Xxxxxxxx:
- xxxxxxx xxxxxxxx/xxxxx xxxxxxx xxxxxxxxx;
- spotřeba xxxxxxx a popřípadě xxxxxxxx xxxx;
- údaje x xxxxxxxxx xxxxxxxx xxxxx xxxxxxx x xxxxxx dávky, xxxxxx xxxxxxxx xxxxxxxx;
- charakter, xxxxxxxxx x trvání xxxxxxxxxx projevů (xxx xxxx xxxxxx xxxx xxxxxxxx);
- xxxxxxxxx xxxxxxxxxx xx smyslové podněty, xxxxxxxx xxxx x xxxxxxxxx aktivity;
- xxxxxxxxxxxxx xxxxxxxxx x příslušnými xxxxxxxxx xxxxxxxxx (normami);
- xxxxxxxx biochemická xxxxxxxxx x příslušnými xxxxxxxxx xxxxxxxxx;
- tělesná xxxxxxxx xxx xxxxxxxx x xxxxx x hmotnosti xxxxxx;
- xxxxxxx xxxxxx;
- xxxxxxxx popis všech xxxxxxxxxxxxxxxxxx xxxxxx;
- údaje x xxxxxxxx, xxxxx xxxx xxxxxxxx;
- xxxxxxxxx xxxxxxxxxxx zpracování xxxxxxxx.
Xxxxxx xxxxxxxx.
Xxxxxx.
4. XXXXXXXXXX
Xxxxxx xx xxxxxxxxxx xxxxxx XXXX XX 407."
[1] Xxxxxxxxx xx xxxxx je xxxxxxx xxx xxxx xxxxxx x xxxx x plazmě, xxxxxxx xxx měření xxxxxxx. Xxxxxxx xxxxxxx xxx xxxx doporučení xx xx, že x xxxxxxxxxxxxxxx xxxxxx xx xxxxx variabilita xxxxxxxx, xxxxx xx mohla xxxxxxxx xxxx xxxxxxx xxxxx x xxxxxx xxxxxxxxxxxx. Na druhé xxxxxx xx hladovění xxxx noc xxxxx xxx vliv xx xxxxxxx xxxxxxxxxxxx a xxx podávání x xxxxxxx xx xxxxxxx xx xxxxxxxxxxxxx xxxxxxxx xxxxxxxx látce. Xxxxx xx xxxxxxx krev xx xxxxx, je xxxxx provést xxxxxxxxxxx xxxxxxxxx xx po xxxxxxxxxx xxxxxxxxx xxxxxx xx 4. xxxxx xxxxxxx.
XXXXXXX XX E
" X.37 XXXXXX XXXXXXXXXXXXX XXXXXXXXXXX XXXXXXXXX XXXXXXX XX XXXXXX EXPOZICI
1. XXXXXX
1.1 Xxxx
Xxx posouzení x xxxxxxxxx xxxxxxxxx xxxxxx xxxxx je xxxxxxxx xxxx x xxxxx xxxxxxxxx určitých xxxxxx látek xxxxxxx xxxxxxxxxx xxxx neurotoxicity, xxxxx nemohou xxx xxxxxxxx jinými xxxxxxxx xxxxxxxx. U určitých xxxxxxxxxxx xxxxxxxxx xxxxxxx xxxx xxxxxxxxxx pozdní xxxxxxxxxxxxx; xxxx xxxxx xxxx xxx podrobeny xxxxxxxx xxxxx metodou.
Screeningové xxxxxxx xx vitro xxx použít pro xxxxxxxxx xxxxx, které xxxxx xxxxxxx xxxxxx xxxxxxxxxxxxxx; negativní xxxxx xx xxxxxxx xx xxxxx xxxx xxxxxxxxxxx xxxxx, xx xxxxx xxxx xxxxxxxxx vyvolat xxxxxx xxxxxxxxxxxxx.
Xxx xxxxxx xxxx, xxxx X.
1.2 Xxxxxxxx
Xxxx "xxxxxxxxx xxxxxxxxxx xxxxxxx" patří neutrální xxxxxxxxx estery, thioestery xxxx xxxxxxxxx kyseliny xxxxxxxxxx, fosfonové xxxx xxxxxxxxxxxxxxx xxxx xxxxxxxxxxx xxxxxxx thiofosforečných, thiofosfonových xxxx xxxxxxxxxxxxxxxxxxxxx, xxxx xxxx xxxxx, xxxxx xxxxx xxxxxxxx xxxxxx xxxxxxxxxxxxx pozorovanou x xxxxxxxxx xxxxx xxxx xxxxxxx.
Xxxxxx neurotoxicita xx xxxxxxx xxxxxxxxxxx se xxxxxxx xxxxxxxx xxxxxx, xxxxxxxx xxxxxxxxxx x xxxx x xxxxxxxxxx xxxxx x xxxx xxxxxxxx x stárnutím xxxxxxxxxx esterasy – XXX (xxxxxxxxxx xxxxxx xxxxxxxx) v nervové xxxxx.
1.3 Xxxxxxxxxx xxxxx
Xxxxxxxxxx xxxxx může xxx xxxxxxxx x pozitivní xxxxxxxxx skupině s xxxxx xxxxxxxx, xx xx v laboratorních xxxxxxxxxx xxxxxx pokusných xxxxx xxxxxxxxx nezměnila.
Příkladem xxxxxx xxxxxxxxx látky x pozdním toxickým xxxxxxx je xxx-x-xxxxx-xxxxxx (XXX 78308, EINECS 2011035, xxxxx xxxxx XXX: xxxx(2xxxxxxxxxxx)xxxxxx), xxxxx xxxx xxx xxxxxx xxxxxxxxxxxxxxxx (XXXX).
1.4 Xxxxxxxx xxxxxxxx xxxxxx
Xxxxxxxx xxxxx xx xxxxxx xxxxxx x jediné xxxxx xxxxxxxx domácím, xxxxxxxxx xxxx možnými xxxxxxxx xxxxxxxxxxxxx účinky. Zvířata xx xxxxxxxx xx xxxx 21 xxx, xxxxxxxxxxx xx xxxxxxxxxx xxxxxxx, ataxie a xxxxxx. Xxxxxxxxxxx xxxxxxxxx, xxxxxxx inhibice XXX (xxxxxxxxx target xxxxxxxx), xx provádějí u xxxxxx náhodně vybraných x každé xxxxxxx, xxxxxxx 24 x 48 h xx xxxxxx látky. Xxxxxx xxxxx xxx xx xxxxxx xxxxx xx xxxxxxxxx xxxxxxx xxxxxx x xxxxxxx xx xxxxxxxxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxx.
1.5 Popis xxxxxxxx xxxxxx
1.5.1 Xxxxxxxx
Xxxxxxx xx xxxxxxx xxxxx xxxxxxx xxxxxxxx xxxxxxxxx xxxxxx, xxxxx nejsou xxxxxxxxx virovými xxxxxxxxxxxx x xxxxxxxxxxxxxxx léčbou x xxxx xxxxxxxx xxxxx, xxxxxxx xx xx xxxxxxxxxxxxxx a xxxxxxxxx xxxxxxx x xxxxxxx 5 xxx xxxx xxxxxxxxx xxxxxx xx xxxxxxxxxxxx xx xxxxxxxxxxx xxxxxxxx.
Xxxxxxxxx xx xxxxxxxxxx velké xxxxx xxxx xxxxxx xxxxxxxxxx xxxxx pohyb slepic x snadné xxxxxxxxxx xxxxx.
Xxxxxxxx látka xx xxxxxxx xxxxxx orálně xxxxxx, xxxxxxxxxxxx tobolkami xxxx xxxxxxxxxxxx metodou. Xxxxxxxx xx xxxxxxxx xxxxxxxx nebo xxxxxxxxxx xx vhodném xxxxxxxx, xxxx xx xxxx. xxxxxxxxx olej, xxxxx xxxxx xx se xxxx xxxxxx rozpustit, xxxxxxx xxxxx xxxxx xxxxxxx látek x xxxxxxxxxxxx tobolkách by xx xxxxxxxx dostatečně xxxxxxxx. Xxxxxxx vlastnosti xxxxxxxxx xxxxxxx xx xxxx xxx známy xxxx xxxxxxxx, a xxxxx xxxxxx známy, xxxx xx xxx xxxxxx xxxxxx.
1.5.2 Zkušební xxxxxxxx
1.5.2.1 Pokusná xxxxxxx
Xxxxxxxxxx xx xxxxx xxxxxxx xxxx xxxxxxxx (Xxxxxx xxxxxx xxxxxxxxxx), stará 8 – 12 xxxxxx. Používají xx xxxxxxx o xxxxxxxxxx xxxxxxxxx a xxxxxxx xx měly xxx xxxxxxx xx xxxxxxxx xxxxxxxxxxxx xxxxx xxxxx.
1.5.2.2 Xxxxx x pohlaví
Kromě xxxxxxxxxxxxxx xxxxxxx xx xxxx být xxxxxxx xxxxxxxxx xxxxxxx x xxxxxxxxx x xxxxxxxxx xxxxxxxxx xxxxxxx. S xxxxxxxx xxxxxx xxxxxxxx xxxxx xx x xxxxxxxxx skupinou xxxxxxx xxxxxx xxxx x xxxxxxxxxxxxxx skupinou.
V každé xxxxxxx by xxx xxx použit xxxxxxxxxx xxxxx slepic, aby xxxxx xxxx slepic xxxxx xxx xxxxxxxx xxx biochemické vyšetření (xxx x xxxxx x xxx x xxxxx den xx xxxxxx) x xxxx xxxxxxx 21denní pozorování xxxxxxxxxxxxx xxxxxxxx.
Xxxxxxxxx kontrolní xxxxxxx xxxx xxx xxxxxxxx souběžně xxxx xxxxx xxx xxxxxxx xxxxx x xxxxxxx xxxxxxx xxxxxxxxx skupiny. Xxxx xx xxxxxxxxx xxxxxxx šest slepic, xxxxxx xx xxxx xxxxx, x xxx xx xxxxx, že xxxxxxxx pozdní xxxxxxxxxxxxx, xxx xxxxxxx pro xxxxxxxxxxx xxxxxxxxx x xxx xxxxxxx xxx xxxxxxxxxxxxxxxx xxxxxxxxx. Xxxxxxxxxx xx xxxxxxxxxx xxxxxxxxx xxxxxxxxxx údaje. Nové xxxxxxxxx kontrolní xxxxx xx xxxx xxx xxxxxxxx, xxxxx xxxxxxxxxxx xxxxxxxxx x xxxxxxx xxxxx xxxxx xxxxxxx xxxxxxxx prvek xxxxxxx (xxxx. plemeno, stravu, xxxxxxxx xxxxx).
1.5.2.3 Úrovně xxxxx
Xxxx xx xx xxxxxxx předběžná studie xx xxxxxxx xxxxxxxx xxxxx xxxxxx x xxxxxx x různými xxxxxxxx dávek, aby xxxx xxxxx xxxxxxxx xxxxxx, xxxxx xx xxx použita x xxxxxx studii. Xxx xxxxxxxxx xxxxxxxxx xxxxx x xxxxxx studii xx v xxxx xxxxxxxxx studii nezbytná xxxxxx xxxxxxxx. Xxx xx xxxx xxxxxxxxx xxxxx xxxxxx akutních xxxxxxxxxxxxx účinků, lze xxxxxx atropin nebo xxxx xxxxxxxx xxxxxxxxx, x xxxxxx xx xxxxx, xx xxxx xxxx xx xxxxxx xxxxxxxxxxxx xxxxxx. Xxx xxxxx xxxxxxxx neletální xxxxx xxxxxxxxxx xxxxx xxx xxxxxx xxxx xxxxx (xxx xxxxxx X.1 x)). Xxx xxxxxx xxxxx xxxxx xxx xxxxxxxx také xxxxxxxxx xxxxx o xxxxxxxxx xxxx xxxx xxxxxxxxxxxxx informace.
Úroveň xxxxx xxxxxxxx xxxxx x xxxxxx studii xx xxxx xxx co xxxxxxxx, xxxxxxx xx xxxxx x úvahu xxxxxxxx xxxxxxxxx xxxxxx xxxxxx xxxxx a xxxxx limit xxxxx 2000 xx xx xx tělesné xxxxxxxxx. Xxxxxxxx xxxx by xxxxx xxxxxxx xxxxxxxxxx xxxxx xxxxxx xxx xxxxxxxxxxx xxxxxxxxx (xxxx) x pro xxxxxxxxxxxx xxxxxxxxx (xxxx) xx 21 xxxxx. Xxx xx xxxxxxxxx xxxxx xxxxxx xxxxxxxx xxxxxxxxxxxxx xxxxxx, xxxxxxx xx xxxxxxx xxxx jiný xxxxxxxx xxxxxxxxx, x xxxxxx je xxxxx, xx nemá xxxx xx xxxxxx xxxxxxxxxxxx xxxxxx.
1.5.2.4 Limitní zkouška
Pokud xxxxxxx xxxxxxxxx xxxxx xxxxxxx xxxxxxxxx v xxxx xxxxxx xxx xxxxx xxxxx xxxxxxx 2000 mg xx xx xxxxxxx xxxxxxxxx xx xxx xxxxxxxx xxxxxxxxxxxxx xxxxxxx xxxxxx x pokud se xx xxxxxxx xxxxx x xxxxxxx s xxxxxxxx strukturou xxxxxxxxxxxxx xxxxxxxx, xxxx xxxxx xxxxxx xx xxxxxxx xxxxx dávky xxxxxxxx. Xxxxxxx zkouška xx xxxxxxx x výjimkou xxxxxxx, xxx xxxxx x xxxxxxxx člověka xxxxxxxxx, xx je xxxxxxxx xxxxxxx xxxxx xxxxxx xxxxx.
1.5.2.5 Xxxx xxxxxxxxxx
Xxxx xxxxxxxxxx xx xxxx xxx 21 xxx.
1.5.3 Xxxxxx
Xx podání xxxxxxxxx xxxxxxxxxx před xxxxxxxx xx xxxxxxxx xxxxxxxx cholinergního xxxxxx xx xxxx zkoušená xxxxx x xxxxx xxxxx.
1.5.3.1 Xxxxxx xxxxxxxxxx
Xxxxxxxxxx xx měla xxxxx xxxxxxxx xx xxxxxx. Xxxxxxx slepice se xxxxxxx xxxxxxxxxx xxxxx xxxxxxxx v xxxxxxx xxxxxxx xxxx xxx x xxxx nejméně xxxxxx denně xx xxxx 21 xxx xxxx do plánovaného xxxxxxxx. Xxxxxxx příznaky xxxxxxxx xx xxxx xxx zaznamenány, včetně xxxx xxxxxxx, xxxx, xxxxxxxxxx a xxxxxx xxxxxxxxxxxx xxxxxxx. Xxxxxx xx xxxx být xxxxxxxxx xxxxx xxxxxxx xxxxxxxxxxxx xxxxxxxx stupnice x xxxxxxxxxxx xx xxxxxx. Xxxxxxx dvakrát xxxxx se xxxxxxx xxxxxx x patologickými xxxxxxxx vyjmou x xxxxx x xxxxxxx xxxxxxx xxxxxx xxxxxxxxx xxxxxxxx, xxxx např. xxxxxxxx xx xxxxxxx, xxx xx xxxxxxxxx xxxxxxxxx sebemenších toxických xxxxxx. Xxxxxxx x xxxxxx a zvířata, xxxxx se xxxxx xxxx xxxx xxxxxxx, xx xxxxx xxxxxx, xxxxxxx xxxxxx x xxxxxxx.
1.5.3.2 Xxxxxxx hmotnost
Všechny xxxxxxx xx xxxxx xxxxx xxxx xxxxxxx xxxxxxxx látky x xxxx nejméně xxxxxx xxxxx.
1.5.3.3 Xxxxxxxxxxx xxxxxxxxx
Xxxx xxxxxx náhodně xxxxxxxxx x xxxxx xxxxxxxxxxxxxx xxxxxxx x kontrolní xxxxxxx s xxxxxxxxx x xxx xxxxxxx x pozitivní xxxxxxxxx xxxxxxx (xxxxx xx xxxxxxx xxxxxxxx xxxxxxx x xxxxx skupinou) xx xxxxxx x xxxxxxx xxxxx xx xxxxxx xxxxx, xxxxx x lumbální mícha xx xxxxxxxxxxx x xxxxxxx se xx xxxxxxxx XXX. Dále xxxx být xxxxxx xxxxxx xxxxxxxxxxxx x. xxxxxxxxxxx x analyzovat xxxx xxxx xx xxxxxxxx aktivity XXX. Xxxxxxxxx se xxxxxx xxx slepice z xxxxxxxxx xxxxxxx x x xxxxx xxxxxxxxxxxxxx xxxxxxx xx 24 x x xxxxx xxx xx 48 x, zatímco xxx xxxxxxx x xxxxxxxxx xxxxxxxxx skupiny se xxxxxx xx 24 x. Xxxxx xxxxxxxxxx xxxxxxxxxx xxxxxxxx toxicity xxxxxxxxx, že xx xxxxxxx xxxxx v xxxxxxxxx xxxxxxxxx xxxxx xxxxxx (to lze xxxxx xxxxxxxx pozorováním xxxx xxxxxxx xxxxxxxxxxxxx xxxxxxxx), může být xxxxxxxxx odebrat xxxxxx xxxxx dvakrát ze xxx zvířat xxxx 24 xx 72 x xx xxxxxx xxxxx.
Xx xxxxxx xxxxxxxx xxxxx xxxxx xxx xxxxxxxxx xxxx xxxxxxx xxxxxxxxxxxxxxxxxxxx (XXxX), je-li xx považováno xx xxxxxx. Xx xxxx xxxx xxxx xxxxxx xxxxxxxxx xxxxxxxxxx XXxX, xxx může vést x xxxxxxxxx xxxxx xxxx xxxxxxxxxx XXxX.
1.5.3.4 Xxxxx
Xxxxx xxxxx xxxxxx (xxxxxxxxxx xxxxx plánu x utracených x xxxxxx) by měla xxxxxxxxx xxxxxxxxx xxxxx xxxxx a míchy.
1.5.3.5 Xxxxxxxxxxxxxxxx xxxxxxxxx
Xxxxxxx xxxx xxxxxx, xxxxx xxxxxxx xxxx xxxxxxxxxx x xxxxxx xxxxxxx xxx xxxxxxxxxxx xxxxxx, xx xxxx xxx xxxxxxxxxxxxx xxxxxxxxx. Xxxxx by xxxx být xxxxxxxx xx situ xx xxxxxxx xxxxxxxxxx technik. Xxxxxxx xx xxxxxxx (xxxxxxx podélný řez), xxxxxxxxxxx xxxxx, xxxxx x xxxxxxxxx xxxxx. Xxxx xxxxx xx xxxx xxx xxxxxxxx x xxxxx xxxxx xxxxx, xxxxxxx xxxxxx x xxxxxxxxxxxxx oblasti. Xxxx xx xxx xxxxxxxx řezy xxxxxxxx xxxxx x. xxxxxxxx x xxxx xxxxx x m. xxxxxxxxxxxxx x x n. xxxxxxxxxxx. Řezy xx xxxxx xxxxxxxx xxxxxxx xx xxxxxx a xxxxx.
2. ÚDAJE
Negativní výsledky xxxxxxx xxx výsledné xxxxxx xxxxxxx v xxxx xxxxxx (xxxxxxxxxxx x xxxxxxxxxxxxxxxx xxxxxxxxx x xxxxxxxxx xxxx xxxxxxx) nevyžadují zpravidla xxxxx zkoušení pozdní xxxxxxxxxxxxx. Xxx dvojznačných xxxx xxxxxxxxxxxx xxxxxxxxxx xxxxxx vyšetření může xxx xxxxxxxx xxxxx xxxxxxxxx.
Xxxx xx být xxxxxxx údaje xxx xxxxx xxxxxxxxxx xxxxx. Xxxxx xx xxxx xxx všechny xxxxx xxxxxxx xx tabulky, xxxxxxx xx xxxxx x xxxxx xxxxxxxxxxxxxx xxxxxxx počet xxxxxx xx xxxxxxx zkoušky, xxxxx xxxxxx xxxxxxxxxxxx xxxx, xxxxxx na xxxxxxx xxxx xxxxxxxxxxx xxxxxx, xxx a xxxxxxxxx těchto lézí xxxx účinků a xxxxxxxx zvířat xxxxxxxxxx xxxxx typ x xxxxxxxxx léze xxxx xxxxxx.
Xxxxx z xxxx xxxxxx xx xxxx xxx vyhodnoceny x xxxxxxxx xxxxxxx, závažnosti x xxxxxxxx xxxxxx xx xxxxxxx a xxxxxxxxxxxxx x histopatologických xxxxxx a dále xxxxxxxxxx xxxxxxx pozorovaných xxxxxx xx xxxxxxxxxxxxxx x xxxxxxxxx xxxxxxx.
Xxxxxxx xxxxxxxx xx měly xxx xxxxx xxxxx xxxxxxxxxxx xxxxxxx a xxxxxx uznávanou xxxxxxxxxxxx xxxxxxx. Xxxxxxxxxxx xxxxxx xx měla xxx xxxxxxx již při xxxxxxxxx xxxxxx.
3. ZPRÁVY
Protokol x xxxxxxx
Xxxxxxxx x xxxxxxx má xxxxx xxxxx obsahovat tyto xxxxxxxxx:
Xxxxxxx zvířata
- xxxxxxx xxxxxxx;
- xxxxx x xxxxx xxxxxx;
- xxxxx, xxxxxxxx chovu atd.;
- xxxxxxxx xxxxxxxxxxxx xxxxxx xx xxxxxxx xxxxxxx.
Xxxxxxxx xxxxxxxx:
- xxxxxxxx údaje x xxxxxxxx xxxxxxxx xxxxx, xxxxxxxxx o xxxx xxxxxxxx x xxxxxxxxxx;
- xxxxxxxxxx xxxxx xxxxxxxx;
- xxxxxxxx údaje x xxxxxxx xxxxxx xxxxxxxx látky;
- xxxxxxxx xxxxx o xxxxxx x o xxxxxxx xxxx;
- zdůvodnění xxxxxx xxxxxx xxxxx;
- xxxxxxxxxxx xxxxxxxxxx xxxxx, xxxxxx xxxxxxxxxx informací x xxxxxxxx, objemu x xxxxxxxxx formě podané xxxxx;
- xxxxxxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxxxxxx x xxxxxxxx xxxxxxxxx x xxxx podání.
Výsledky:
- xxxxx x xxxxxxx hmotnosti;
- xxxxx x xxxxxxxxx xxxxxxxx podle xxxxxx, xxxxxx xxxxxxxxx;
- xxxxxxxxx, xxxxxxxxx x xxxxxx xxxxxxxxxx projevů (zda xxxx xxxxxx xxxx xxxxxxxx);
- xxxxxxxx popis xxxxxxxxxxxxx vyšetření x xxxxxx;
- pitevní xxxxxx;
- xxxxxxxx xxxxx všech xxxxxxxxxxxxxxxxxx nálezů;
- popřípadě xxxxxxxxxxx xxxxxxxxxxx xxxxxxxx.
Xxxxxx xxxxxxxx.
Xxxxxx.
4. XXXXXXXXXX
Xxxxxx je xxxxxxxxxx xxxxxx XXXX XX 418.
B.38 POZDNÍ XXXXXXXXXXXXX XXXXXXXXXXX XXXXXXXXX XXXXXXX – 28XXXXX XXXXXXXXX EXPOZICE
1. XXXXXX
1.1 Xxxx
Xxx xxxxxxxxx x xxxxxxxxx xxxxxxxxx xxxxxx xxxxx xx důležité xxxx v xxxxx xxxxxxxxx určitých skupin xxxxx xxxxxxx xxxxxxxxxx xxxx neurotoxicity, xxxxx xxxxxxx xxx xxxxxxxx xxxxxx xxxxxxxx xxxxxxxx. X xxxxxxxx xxxxxxxxxxx xxxxxxxxx fosforu xxxx xxxxxxxxxx xxxxxx xxxxxxxxxxxxx; xxxx látky mají xxx xxxxxxxxx xxxxxxxx xxxxx xxxxxxx.
Xxxxxxxxxxxx xxxxxxx xx vitro lze xxxxxx pro xxxxxxxxx xxxxx, xxxxx xxxxx xxxxxxx xxxxxx xxxxxxxxxxxxxx; xxxxxxxxx xxxxx xx xxxxxxx in vitro xxxx neposkytuje xxxxx, xx látka xxxx xxxxxxxxx xxxxxxx xxxxxx xxxxxxxxxxxxx.
28xxxxx xxxxxxx pozdní xxxxxxxxxxxxx xxxxxxxxx xxxxxxxxx x xxxxxx xxxxxxxxx xxx zdraví, které xx xx xxxxx xxxxxxxx x xxxxxxxxxxx xxxxxxx xxxxx xxxxxxxxx xxxxxxxx xxxxxx. Poskytne xxxxxxxxx x reakci xx xxxxx a xxxx xxxxxxxxxx xxxxx xxxxxx xxx pozorovatelných xxxxxxxxxxxx účinků, xxx xxxx xxx xxxxxxxx xxx xxxxxxxxx kritérií xxx bezpečnou xxxxxxxx xxxxxxx.
Xxx xxxx xxxxxx xxxx, část X.
1.2 Xxxxxxxx
Xxxx "organické xxxxxxxxxx xxxxxxx" xxxxx xxxxxxxxx xxxxxxxxx xxxxxx, xxxxxxxxxx xxxx xxxxxxxxx kyseliny xxxxxxxxxx, fosfonové nebo xxxxxxxxxxxxxxx xxxx xxxxxxxxxxx xxxxxxx xxxxxxxxxxxxxxxx, xxxxxxxxxxxxxxx xxxx xxxxxxxxxxxxxxxxxxxxx, xxxx xxxx xxxxx, které xxxxx způsobit pozdní xxxxxxxxxxxxx pozorovanou u xxxxxxxxx xxxxx této xxxxxxx.
Xxxxxx xxxxxxxxxxxxx je xxxxxxx xxxxxxxxxxx xx xxxxxxx xxxxxxxx xxxxxx, xxxxxxxx xxxxxxxxxx x xxxx a xxxxxxxxxx xxxxx x xxxx x inhibicí x xxxxxxxxx xxxxxxxxxx xxxxxxxx - XXX (xxxxxxxxxx xxxxxx xxxxxxxx) v xxxxxxx tkáni.
1.3 Podstata xxxxxxxx metody
Zkoušené xxxxx xx xxxxxxxx xxxxx xxxxxx xxxxxxxx xxxxxxx xx xxxx 28 xxx. Zvířata xx xxxxxxxx xxxxxxx xxxxxx xxxxx, xxxxxxxxxxx se xxxxxxxxxx chování, ataxie x xxxxxx xxxxx 14 xxx xx xxxxxxxx dávce. Xxxxxxxxxxx xxxxxxxxx, zejména xxxxxxxx XXX (xxxxxxxxx xxxxxx xxxxxxxx), se xxxxxxx x slepic xxxxxxx xxxxxxxxx x xxxxx xxxxxxx, obvykle 24 x 48 h xx xxxxxx xxxxx. Xxx týdny xx xxxxxxxx xxxxx xx xxxxxxxxx xxxxxxx xxxxxx x xxxxxxx xx xxxxxxxxxxxxxxxx vyšetření xxxxxxxxx xxxxxxxxx xxxxx.
1.4 Popis xxxxxxxx xxxxxx
1.4.1 Xxxxxxxx
Xxxxxxx xx xxxxxxx výběr xxxxxxx xxxxxxxx dospělých xxxxxx, xxxxx nejsou xxxxxxxxx virovými onemocněními x farmakologickou xxxxxx x xxxx normální xxxxx, přiřadí xx xx experimentálních x xxxxxxxxxxx xxxxxx x xxxxxxx 5 xxx xxxx xxxxxxxxx xxxxxx xx xxxxxxxxxxxx xx xxxxxxxxxxx podmínky.
Používají se xxxxxxxxxx xxxxx klece xxxx xxxxxx xxxxxxxxxx xxxxx pohyb slepic x xxxxxx pozorování xxxxx.
Xxxxxxxx xxxxx xx xxxxxx každý den, 7 xxx x xxxxx, nejlépe xxxxxx xxxxxx xxxx xxxxxxxxxxxx xxxxxxxxx. Kapaliny se xxxxxxxx xxxxxxxx xxxx xxxxxxxxxx xx vhodném xxxxxxxx, xxxx je xxxx. xxxxxxxxx xxxx, xxxxx xxxxx xx xx xxxx xxxxxx xxxxxxxxx, xxxxxxx xxxxx xxxxx xxxxxxx xxxxx x želatinových tobolkách xx xx xxxxxxxx xxxxxxxxxx vstřebat. Toxické xxxxxxxxxx nevodných vehikul xx xxxx xxx xxxxx xxxx xxxxxxxx, x xxxxx xxxxxx xxxxx, xxxx by xxx xxxxxx xxxxxx.
1.4.2 Xxxxxxxx xxxxxxxx
1.4.2.1 Pokusná xxxxxxx
Xxxxxxxxxx xx mladá xxxxxxx kura xxxxxxxx (Xxxxxx xxxxxx domesticus), xxxxx 8 – 12 xxxxxx. Xxxxxxxxx xx xxxxxxx x xxxxxxxxxx xxxxxxxxx x xxxxxxx xx měly xxx xxxxxxx xx xxxxxxxx xxxxxxxxxxxx xxxxx xxxxx.
1.4.2.2 Počet x xxxxxxx
Xxxxxx xx xxxx xxx xxxxxxx xxxxxxx xxx experimentální skupiny x kontrolní skupina x xxxxxxxxx. X xxxxxxxx xxxxxx zkoušené xxxxx se x xxxxxxxxx xxxxxxxx s xxxxxxxxx zachází stejně xxxx x xxxxxxxxxxxxxx xxxxxxxx.
X xxxxx skupině xx měl být xxxxxx xxxxxxxxxx počet xxxxxx, aby xxxxx xxxx xxxxxx xxxxx xxx xxxxxxxx pro xxxxxxxxxxx vyšetření (tři x xxxxx x xxx x druhý xxx xx xxxxxx) x xxxx xxxxxxx 14xxxxx xxxxxxxxxx xxxxxxxxxxxxx xxxxxxxx.
1.4.2.3 Xxxxxx xxxxx
Xxx xxxxxx úrovní xxxxx xx měly být xxxxx x xxxxx xxx výsledky xxxxxx xxxxxxx xxxxxx xxxxxxxxxxxxx x jakékoli další xxxxxxxx xxxxx x xxxxxxxx x kinetice xxxxxxxx xxxxxxxxxx. Nejvyšší xxxxxx dávky xx xxxx xxx xxxxxxx x cílem xxxxxxx xxxxxxx xxxxxx, nejlépe xxxxxx xxxxxxxxxxxxx, ne xxxx xxxxxxx xxxx xxxxxx utrpení. Xxxx xx xxxx xxx xxxxxxx xxxxxxxx řada xxxxx x cílem xxxxxxxx, xx existuje xxxxxxxxx xxxxxx na xxxxx x xx xxxxxxxx dávka nevyvolává xxxxx projevy xxxxxxxx.
1.4.2.4 Xxxxxxx xxxxxxx
Xxxxx zkouška xxxxxxxxx xxxxx xxxxxxx xxxxxxxxx x xxxx xxxxxx xxx jedné xxxxx xxxxxxx 1000 xx na xx xxxxxxx hmotnosti x xxx xxxxxxxx xxxxxxxxxxxxx xxxxxxx xxxxxx x xxxxx se na xxxxxxx xxxxx o xxxxxxx x xxxxxxxx xxxxxxxxxx xxxxxxxxxxxxx toxicita, xxxx xxxxx xxxxxx xx xxxxxxx vyšší xxxxx xxxxxxxx. Limitní xxxxxxx se xxxxxxx x xxxxxxxx případu, xxx xxxxx o xxxxxxxx xxxxxxx xxxxxxxxx, xx xx xxxxxxxx xxxxxxx vyšší xxxxxx xxxxx.
1.4.2.5 Xxxx xxxxxxxxxx
Xxxxxxx xxxxxxx xx xxxx xxx xxxxxxxxxx nejméně xxxxxx xxxxx xx xxxx xxxxxxxx x 14 xxx po xx, xx xx xxxxxxxxx pitvy podle xxxxx.
1.4.3 Xxxxxx
Xxxxxxxx xx xxxxxx xxxxxxxx xxxxx xxxx xxx x xxxxx xx xxxx 28 dnů.
1.4.3.1 Xxxxxx xxxxxxxxxx
Xxxxxxxxxx xx xxxx xxxxx xxxxxxxx po xxxxxx. Xxxxxxx slepice xx xxxxxxx pozorují xxxxxx denně každý xxx x 28 xxx xxxxxxxx a 14 xxx xx xxxxxxxx nebo do xxxxxxxxxxx xxxxxxxx. Xxxxxxx xxxxxxxx xxxxxxxx xx xxxx xxx xxxxxxxxxxx, xxxxxx xxxx nástupu, xxxx, xxxxxxxxxx x xxxxxx. Xxxxxxxxxx xx xxxxxxxxx abnormality xxxxxxx, xxx nemá se xx xx xxxxxxxx. Xxxxxx by měla xxx xxxxxxxxx xxxxx xxxxxxx xxxxxxxxxxxx pořadové xxxxxxxx a zaznamenává xx paréza. Nejméně xxxxxxx týdně xx xxxxxxx x xxxxxxxxxxxxx xxxxxxxx xxxxxx x xxxxx x podrobí xxxxxxx xxxxxx xxxxxxxxx xxxxxxxx, jako xxxx. xxxxxxxx po žebříku, xxx xx xxxxxxxxx xxxxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxx. Zvířata x xxxxxx a zvířata, xxxxx xx xxxxx xxxx trpí xxxxxxx, xx ihned xxxxxx, xxxxxxx xxxxxx x xxxxxxx.
1.4.3.2 Xxxxxxx xxxxxxxx
Xxxxxxx xxxxxxx se zváží xxxxx před xxxxxx xxxxxxx zkoušené látky x xxxx xxxxxxx xxxxxx týdně.
1.4.3.3 Xxxxxxxxxxx xxxxxxxxx
Xxxx xxxxxx náhodně xxxxxxxxx x každé xxxxxxxxxxxxxx skupiny a xxxxxxxxx skupiny s xxxxxxxxx x tři xxxxxxx x pozitivní xxxxxxxxx xxxxxxx se xxxxxx v xxxxxxx xxxxx po xxxxxx xxxxxxxx dávky, xxxxx x lumbální xxxxx xx xxxxxxxxxxx a xxxxxxx xx xx xxxxxxxx XXX. Xxxx xxxx xxx xxxxxx xxxxxxxxxxxx x. xxxxxxxxxxx x analyzovat xxxx xxxx na xxxxxxxx xxxxxxxx NTE. Zpravidla xx xxxxxx tři xxxxxxx x kontrolní xxxxxxx x z xxxxx xxxxxxxxxxxxxx skupiny xx 24 h x xxxxx xxx xx 48 x xx xxxxxxxx xxxxx. Xxxxx xxxxx z xxxxxx studie nebo x jiných xxxxxx (xxxx. xxxxxxxxxxxxxxxxx) xxxxxxxxx, xx xxxx xxxxxx xxxx xxxx xxxxxxxx xx poslední dávce xxx xxxx xxxx, xxxx xx xxx xxxxxxx x xxxxxxxxxx xx xxxx být xxxxxxx x xxxxxxxxxxx.
Xx xxxxxx xxxxxxxx xxxxx xxxxx xxx xxxxxxxxx xxxx analýza acetylcholinesterasy (XXxX), xx-xx xx xxxxxxxxxx xx vhodné. Xx xxxx však xxxx nastat xxxxxxxxx xxxxxxxxxx AChE, xxx xxxx vést k xxxxxxxxx látky xxxx xxxxxxxxxx XXxX.
1.4.3.4 Xxxxx
Xxxxx xxxxx xxxxxx (xxxxxxxxxx xxxxx xxxxx x xxxxxxxxxx x xxxxxx) xx xxxx xxxxxxxxx xxxxxxxxx xxxxx mozku x míchy.
1.4.3.5 Histopatologické xxxxxxxxx
Xxxxxxx xxxx xxxxxx, xxxxx xxxxxxx xxxx xxxxxxxxxx x xxxxxx xxxxxxx pro biochemické xxxxxx, by xxxx xxx xxxxxxxxxxxxx xxxxxxxxx. Xxxxx xx měly xxx fixovány in xxxx za xxxxxxx xxxxxxxxxx xxxxxxx. Xxxxxxx xx xxxxxxx (xxxxxxx xxxxxxx řez), prodloužená xxxxx, mícha x xxxxxxxxx nervy. Řez xxxxx xx měl xxx xxxxxxxx x xxxxx krční xxxxx, xxxxxxx xxxxxx x xxxxxxxxxxxxx oblasti. Xxxx xx být xxxxxxxx xxxx xxxxxxxx xxxxx x. tibialis a xxxx xxxxx x x. gastrocnemius x x x. xxxxxxxxxxx. Xxxx se barví xxxxxxxx xxxxxxx na xxxxxx a xxxxx. Xxxxxxx xx xxxx xxx xxxxxxxxx mikroskopické xxxxxxxxx fixované xxxxx xxxxx xxxxxx kontrolní xxxxxxx x skupiny x vysokou xxxxxx. Xxxxx se x xxxxxxx x xxxxxxx xxxxxx xxxxxxx účinky, xxxx by xxx xxxxxxxxxxxxx xxxxxxxxx provedeno xxxx xx slepicích xx xxxxxxx se xxxxxxx x xxxxxx xxxxxx.
2. ÚDAJE
Negativní xxxxxxxx xxxxxxx xxxxx metodou (xxxxxxxxxxx x histopatologická xxxxxxxxx x xxxxxxxxx xxxx chování) nevyžadují xxxxxxxxx xxxxx xxxxxxxx xxxxxx xxxxxxxxxxxxx. Při xxxxxxxxxxxx xxxx neprůkazných xxxxxxxxxx xxxxxx xxxxxxxxx xxxx xxx nezbytné xxxxx xxxxxxxxx.
Xxxx xx xxx xxxxxxx údaje xxx xxxxx xxxxxxxxxx xxxxx. Xxxxx xx xxxx být xxxxxxx xxxxx xxxxxxx do xxxxxxx, přičemž xx x xxxxx xxxxxxxxxxxxxx xxxxxxx xxxxx xxxxx xxxxxx xx xxxxxxx xxxxxxx, počet xxxxxx xxxxxxxxxxxx xxxx, xxxxxx xx chování xxxx xxxxxxxxxxx xxxxxx, xxx x xxxxxxxxx xxxxxx xxxx xxxx xxxxxx x procento xxxxxx xxxxxxxxxx xxxxx typ x xxxxxxxxx léze xxxx účinku.
Údaje x xxxx xxxxxx xx xxxx xxx xxxxxxxxxxx x xxxxxxxx xxxxxxx, xxxxxxxxxx x xxxxxxxx xxxxxx xx chování x xxxxxxxxxxxxx x xxxxxxxxxxxxxxxxxx nálezů x xxxx xxxxxxxxxx dalších xxxxxxxxxxxx xxxxxx na xxxxxxxxxxxxxx x kontrolní xxxxxxx.
Xxxxxxx výsledky xx xxxx být xxxxx xxxxx xxxxxxxxxxx xxxxxxx x xxxxxx uznávanou xxxxxxxxxxxx xxxxxxx. Xxxxxxxxxxx xxxxxx by měla xxx xxxxxxx xxx xxx plánování xxxxxx.
3. XXXXXX
Xxxxxxxx x zkoušce
Protokol x xxxxxxx xxxxxxxx xxxxx xxxxx tyto xxxxxxxxx:
Xxxxxxx xxxxxxx:
- xxxxxxx xxxxxxx;
- počet a xxxxx zvířat;
- xxxxx, xxxxxxxx chovu atd.;
- xxxxxxxx xxxxxxxxxxxx xxxxxx xx xxxxxxx xxxxxxx.
Xxxxxxxx xxxxxxxx:
- xxxxxxxx údaje x xxxxxxxx xxxxxxxx xxxxx, popřípadě o xxxx xxxxxxxx x xxxxxxxxxx;
- xxxxxxxxxx xxxxx xxxxxxxx;
- podrobné xxxxx x xxxxxxx xxxxxx xxxxxxxx xxxxx;
- xxxxxxxx xxxxx x xxxxxx x x xxxxxxx xxxx;
- xxxxxxxxxx výběru xxxxxx xxxxx;
- specifikace xxxxxxxxxx látek, včetně xxxxxxxxxx xxxxxxxxx o xxxxxxxx, objemu x xxxxxxxxx formě xxxxxx xxxxx;
- zdůvodnění xxxxxx xxxx odběru xxx xxxxxxxxxxx vyšetření, xxxx-xx xxxxxxx 24 x 48 x.
Xxxxxxxx:
- údaje x xxxxxxx xxxxxxxxx;
- xxxxx x toxických xxxxxxxx xxxxx xxxxxx, xxxxxx xxxxxxxxx;
- úroveň xxx pozorovatelných nepříznivých xxxxxx;
- charakter, závažnost x xxxxxx xxxxxxxxxx xxxxxxx (xxx xxxx xxxxxx nebo xxxxxxxx);
- xxxxxxxx xxxxx biochemických xxxxxxxxx x xxxxxx;
- xxxxxxx xxxxxx;
- xxxxxxxx xxxxx xxxxx histopatologických xxxxxx;
- xxxxxxxxx xxxxxxxxxxx xxxxxxxxxxx xxxxxxxx.
Xxxxxx xxxxxxxx.
Xxxxxx.
4. XXXXXXXXXX
Xxxxxx je analogická xxxxxx OECD XX 419."
XXXXXXX X
Xxxxxx požadavky xx klasifikaci x xxxxxxxxxx xxxxxxxxxxxx xxxxx x přípravků
Viz xxxxxxxx Xxxxxx 2001/59/XX, Úř. xxxx. X 332, 28. 12. 2000, x. 81.


