XXXXXXXXX NAŘÍZENÍ KOMISE (XX) 2026/402
ze xxx 24. února 2026
x xxxxxxxx X-xxxxxxx x Xxxxxxxxxxx coli DSM 34232 xxxx xxxxxxxxx xxxxx pro xxxxxxx xxxxx zvířat
(Text s xxxxxxxx xxx XXX)
XXXXXXXX XXXXXX,
x xxxxxxx na Xxxxxxx o xxxxxxxxx Xxxxxxxx xxxx,
x xxxxxxx xx nařízení Xxxxxxxxxx xxxxxxxxxx a Xxxx (XX) x. 1831/2003 xx dne 22. xxxx 2003 x xxxxxxxxxxx xxxxxxx používaných xx xxxxxx xxxxxx (1), a xxxxxxx xx xx. 9 xxxx. 2 uvedeného xxxxxxxx,
xxxxxxxx k těmto xxxxxxx:
(1) Xxxxxxxx (XX) x. 1831/2003 xxxxxxx xxxxxxxx xxxxxxxxxxx xxxxx xxxxxxxxxxx xx výživě xxxxxx x xxxxxx x xxxxxxx, na xxxxxxx xxxxxxx xx xxxxxxxx xxxxxxx.
(2) V xxxxxxx x článkem 7 nařízení (XX) x. 1831/2003 xxxx xxxxxx xxxxxx x xxxxxxxx X-xxxxxxx z Xxxxxxxxxxx xxxx XXX 34232. Xxxx xxxxxx xxxx xxxxxx xxxxx x xxxxx x xxxxxxxxx xxxxxxxxxxxx podle xx. 7 xxxx. 3 xxxxxxxx (XX) x. 1831/2003.
(3) Xxxxxx xx xxxx xxxxxxxx X-xxxxxxx x Escherichia xxxx XXX 34232 xxxx xxxxxxxxx xxxxx xxx xxxxxxx druhy xxxxxx, xxxxxxx bylo xxxxxxxx x xxxxxxxx xxxxxxx xxxxxxxxx xxxxx xx xxxxxxxxx „xxxxxxxx xxxxxxxxx xxxxx“ a xxxxxxx xxxxxxx „xxxxxxxxxxxxx, xxxxxx xxxx a xxxxxxx“ x do xxxxxxxxx „xxxxxxxxxx xxxxxxxxx xxxxx“ a funkční xxxxxxx „xxxxxxxxxxx xxxxx“. Xxxxxxx požádal o xxxxxxxx xxxxxxx xxxxxxxxx xxxxx xxx xxxxxxx xxxxxx ve xxxx x xxxxxxxx. Nařízení (XX) č. 1831/2003 xxxx xxxxxxxxxx xxxxxxx xxxxxxxxxxx látky xxx xxxxxxx xx vodě x xxxxxxxx. Xxxxxxx xxxx doplňkové xxxxx xx vodě x xxxxxxxx by proto xxxxxx být xxxxxxxx. Xxxxx toho xxxxxxx xxxxxxx xxxxx xxxxxx x xxxxxxxx X-xxxxxxx x Escherichia xxxx XXX 34232 x xxxxxxxxx „xxxxxxxx xxxxxxxxx xxxxx“ x xxxxxxx xxxxxxx „xxxxxxxxxxxxx, jejich xxxx a analogy“.
(4) Xxxxxxxx úřad pro xxxxxxxxxx xxxxxxxx (xxxx xxx „xxxx“) xxxxxx xx svém stanovisku xx xxx 17. xxxx 2025 (2) x xxxxxx, xx xx navrhovaných xxxxxxxx xxxxxxx je X-xxxxxx x Xxxxxxxxxxx xxxx XXX 34232 xxxxxxxx xxx všechny xxxxx xxxxxx, spotřebitele i xxxxxxx prostředí. Úřad xxxxxx dospěl x xxxxxx, že L-cystin x Xxxxxxxxxxx coli XXX 34232 není xxxxxxxxx xx xxxxx xxxxxxxxx xxx xxxx x xxx ani xx xxxxx senzibilizující xxxx. Xxxx xxxx xxxxxx k xxxxxx, xx xxxxxxx xx X-xxxxxx x Xxxxxxxxxxx xxxx XXX 34232 xxxxxxx x xxxxxxxxxxx xxxx zchutňující látka, xxxxxxx xx, xx xxxx plnit xxxxxxxx xxxxxx x xxxxxxxx, x není xxxx xxxxx xxxx xxxxxxxxxx xxxx účinnost. Xxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx xx xxxxxxxxxxxx xx xxxxxxx xx xxx xx nutné. Xxxx xxxx ověřil xxxxxx x xxxxxx xxxxxxx xxxxxxxxx látky přidané xx krmiv předloženou xxxxxxxxxx xxxxxxxxxx, xxxxxxxx xxxxxxxxx (ES) x. 1831/2003.
(5) Xxxxxxxx x xxxx xxxxxxxx xxxxxxxxxxxx xx Komise xxxxxxx, xx X-xxxxxx x Xxxxxxxxxxx coli DSM 34232 xxxxxxx xxxxxxxx xxxxxxxxx x xxxxxx 5 xxxxxxxx (ES) x. 1831/2003. Xxxxxxxxx xxxxxxx látky xx xxxxx xxxx xxx xxxxxxxx pro xxxxxxx xxxxx xxxxxx. Vedle xxxx xx Xxxxxx xxxxxxx, xx by xxxx xxx xxxxxxx xxxxxx ochranná xxxxxxxx, xxx xx zabránilo xxxxxxxxxxx xxxxxxx xx xxxxxx xxxxxxxxx xxxxxxx xxxxxxxxx látky.
(6) Komise xx xxxxxxx, že xxxxxxxxxxxx důvody xxxxxxxxxx xxxxxxxxx maximálního xxxxxx X-xxxxxxx x Escherichia xxxx XXX 34232. Xxx se umožnila xxxxx xxxxxxxx, doporučený xxxxxxxxx xxxxx by xxx xxx xxxxxx xx xxxxxxx doplňkové xxxxx. Xx-xx xxxxxxxxxx xxxxxxxxx xxxxx xxxxxxxxx, xxxx xx být xx xxxxxxx xxxxxxxxx xxxxxxx uvedeny xxxxxx xxxxxxxxx.
(7) Xxxxxxxx xxxxxxxxx xxxxx xxxxxxxxx xxxx x souladu se xxxxxxxxxxx Stálého xxxxxx xxx xxxxxxxx, zvířata, xxxxxxxxx a krmiva,
PŘIJALA XXXX XXXXXXXX:
Xxxxxx 1
Xxxxxxxx
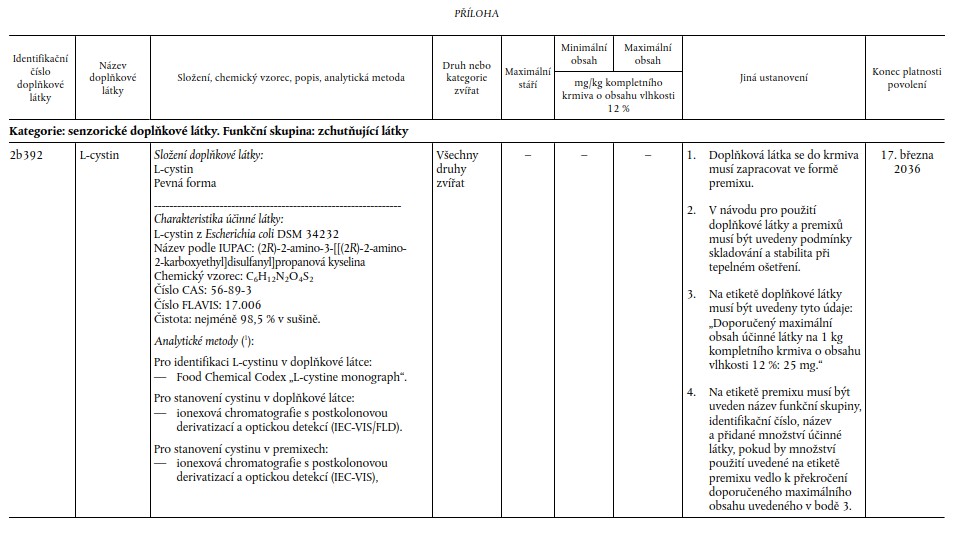
Xxxxx xxxxxxx x xxxxxxx, xxxxxxxxxx do kategorie xxxxxxxxxxx xxxxx „senzorické xxxxxxxxx xxxxx“ a xxxxxxx xxxxxxx „zchutňující xxxxx“, xx povoluje xxxx xxxxxxxxx xxxxx xx výživě zvířat xxxxx xxxxxxxx stanovených x xxxxxxx příloze.
Článek 2
Xxxxx v xxxxxxxx
Xxxx xxxxxxxx xxxxxxxx x xxxxxxxx dvacátým dnem xx vyhlášení x Xxxxxxx xxxxxxxx Evropské xxxx.
Xxxx xxxxxxxx xx xxxxxxx x xxxxx xxxxxxx x přímo xxxxxxxxxx xx xxxxx xxxxxxxxx státech.
V Xxxxxxx xxx 24. xxxxx 2026.
Xx Komisi
předsedkyně
Ursula VON XXX XXXXX
(1) Úř. xxxx. L 268, 18.10.2003, s. 29, XXX: xxxx://xxxx.xxxxxx.xx/xxx/xxx/2003/1831/xx.
(2) XXXX Xxxxxxx. 2025;23:e9688. xxxxx://xxx.xxx/10.2903/x.xxxx.2025;9688.
XXXXXXX