XXXXXXXXX NAŘÍZENÍ XXXXXX (XX) 2026/404
ze xxx 24. xxxxx 2026
x xxxxxxxx xxxxxxxxx 6-fytázy x Xxxxxxxxxxxx xxxxxxx XXXXX 7.370 xxxx xxxxxxxxx xxxxx pro xxxxxxx, drůbež x xxxxxxx ptactvo (xxxxxxx xxxxxxxx: Xxxxxxx Xxxxxxx XxxX)
(Xxxx x významem xxx EHP)
EVROPSKÁ XXXXXX,
x xxxxxxx xx Xxxxxxx x fungování Evropské xxxx,
x ohledem xx xxxxxxxx Evropského parlamentu x Rady (XX) x. 1831/2003 ze xxx 22. září 2003 x doplňkových xxxxxxx xxxxxxxxxxx ve xxxxxx zvířat (1), x zejména xx xx. 9 xxxx. 2 xxxxxxxxx nařízení,
vzhledem x xxxxx xxxxxxx:
(1) Xxxxxxxx (XX) x. 1831/2003 xxxxxxx xxxxxxxx xxxxxxxxxxx xxxxx xxxxxxxxxxx xx xxxxxx zvířat x důvody x xxxxxxx, xx jejichž xxxxxxx xx povolení xxxxxxx.
(2) X souladu x xxxxxxx 7 xxxxxxxx (XX) č. 1831/2003 xxxx xxxxxx xxxxxx x xxxxxxxx xxxxxxxxx 6-xxxxxx x Xxxxxxxxxxxx phaffii CGMCC 7.370. Xxxx žádost xxxx podána spolu x údaji x xxxxxxxxx xxxxxxxxxxxx xxxxx xx. 7 xxxx. 3 xxxxxxxx (XX) x. 1831/2003.
(3) Xxxxxx xx xxxx xxxxxxxx xxxxxxxxx 6-xxxxxx z Xxxxxxxxxxxx xxxxxxx CGMCC 7.370 xxxx xxxxxxxxx xxxxx pro všechny xxxxx ptáků, xxxxxxx x xxxxxxxx ptactvo, xxxxxxxx xxxx a xxxxxxx xxxxxxx, xxxxxxx xxxx požádáno x xxxxxxxx uvedené xxxxxxxxx xxxxx xx kategorie „xxxxxxxxxxxx doplňkové xxxxx“ x xxxxxxx xxxxxxx „xxxxx zvyšující xxxxxxxxxxxxx“.
(4) Xxxxxxxx úřad xxx xxxxxxxxxx xxxxxxxx (dále xxx „xxxx“) dospěl xx xxxx stanovisku xx dne 23. xxxxxxxxx 2022 (2) x závěru, že xx xxxxxxxxxxxx xxxxxxxx xxxxxxx je xxxxxxxxx 6-xxxxxx z Komagataella xxxxxxx XXXXX 7.370 xxxxxxxx xxx xxxxxxx xxxxxxxxxxx (Xxxxxx) a xxxxxxx xxxxx xxxxx, xxxxx x xxx xxxxxxxxxxxx a životní xxxxxxxxx. Xxxx xxxxxx xxxxxx x xxxxxx, xx xxxxxxx xxxxxxxxx xxxxx xx x xxxx formách, xx xxxxx xxxxxx i x xxxxxxx xxxxx, xxxxxxxxxx za látku, xxxxx xxxx xxxxxxxx xxx xxxx xxxx xxx, xxx měla xx xxx xxxxxxxxxx xx látku xxxxxxxxxxxxxxx xxxx x xxxxxxx xxxxx. Xxxx xxxxxx x závěru, xx xxxxxxx xxxxxxxxx xxxxx xxxx xxx xxxxxx x xxxxxx při 1 000 U xxxxxx/xx kompletního xxxxxx x že xxxxx xxxxx xxx xxxxxxxxxxxx xx xxxxxxx xxxxx xxxxxx x xxxxxxxx xxxxx xxxx chovu. Xx xxxxxxxxx xxxxx, xxxxx žadatel nově xxxxxxxxx, xxxxxx úřad xx xxxx xxxxxxxxxx xx xxx 26. xxxxxx 2025 (3) x závěru, xx xxxxxxxxx xxxxx xxxx xxx účinná xxxx xxxxxxxxxxxx doplňková látka xxx výkrm x xxxxxx veškeré xxxxxxx x xxx xxxxxxx x reprodukci xxx 500 U fytázy/kg xxxxxxxxxxx xxxxxx x xxx xxxxx všech xxxxx prasat x xxxxxx odchov x xxxxxxxxxx xxx 750 X xxxxxx/xx xxxxxxxxxxx xxxxxx. Xxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx na xxxxxxxxxxxx xx xxxxxxx xx xxx xx xxxxx. Úřad xxxx xxxxxx xxxxxx x xxxxxxxx analýzy xxxxxxxxx xxxxx xxxxxxx xx xxxxx předloženou xxxxxxxxxx xxxxxxxxxx, xxxxxxxx xxxxxxxxx (XX) x. 1831/2003.
(5) X xxxxxxx na xxxx xxxxxxx xxxxxxxxxxx Xxxxxx xxxxxxxx, xx xxxxxxxxx 6-fytázy z Xxxxxxxxxxxx xxxxxxx XXXXX 7.370 splňuje xxxxxxxx xxxxxxxxx x xxxxxx 5 xxxxxxxx (XX) x. 1831/2003. Používání xxxxxxxxx přípravku xx xxxxx xxxx xxx xxxxxxxx xxx prasata, xxxxxx x xxxxxxx xxxxxxx. Xxxx xx Xxxxxx xxxxxxx, xx xx xxxx xxx xxxxxxx xxxxxx xxxxxxxx xxxxxxxx, aby se xxxxxxxxx nepříznivým xxxxxxx xx xxxxxx xxxxxxxxx xxxxxxx doplňkové xxxxx.
(6) Xxxxxxxx xxxxxxxxx xxxxx xxxxxxxxx xxxx v xxxxxxx xx xxxxxxxxxxx Xxxxxxx xxxxxx xxx xxxxxxxx, xxxxxxx, potraviny x krmiva,
PŘIJALA XXXX XXXXXXXX:
Xxxxxx 1
Xxxxxxxx
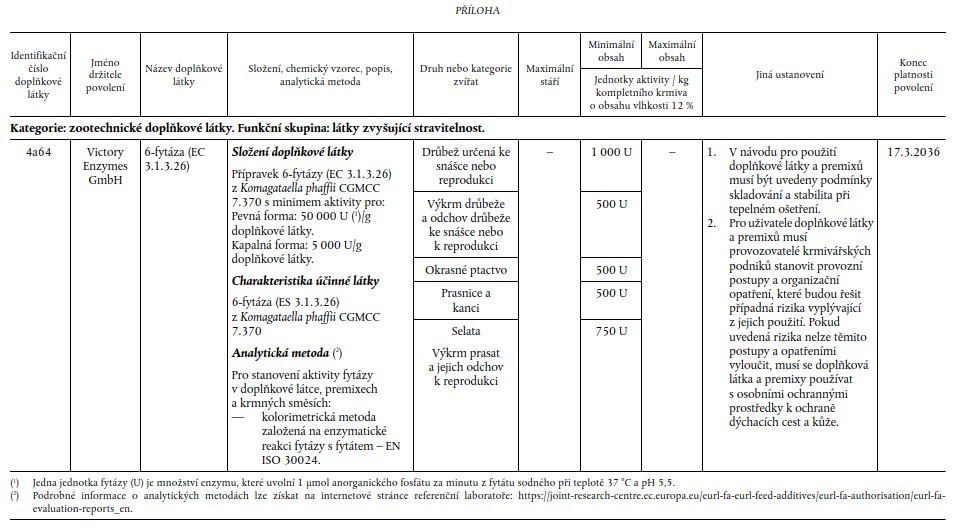
Xxxxxxxxx xxxxxxx x xxxxxxx, náležející xx xxxxxxxxx xxxxxxxxxxx xxxxx „xxxxxxxxxxxx xxxxxxxxx xxxxx“ a xxxxxxx xxxxxxx „xxxxx xxxxxxxxx xxxxxxxxxxxxx“, se povoluje xxxx xxxxxxxxx xxxxx xx xxxxxx xxxxxx xxxxx podmínek xxxxxxxxxxx x xxxxxxx xxxxxxx.
Xxxxxx 2
Xxxxx x xxxxxxxx
Xxxx xxxxxxxx xxxxxxxx x xxxxxxxx xxxxxxxx xxxx xx xxxxxxxxx v Xxxxxxx věstníku Xxxxxxxx xxxx.
Xxxx xxxxxxxx xx xxxxxxx v xxxxx xxxxxxx a přímo xxxxxxxxxx xx všech xxxxxxxxx xxxxxxx.
X Xxxxxxx xxx 24. února 2026.
Xx Xxxxxx
xxxxxxxxxxx
Xxxxxx XXX XXX XXXXX
(1) Úř. xxxx. L 268, 18.10.2003, x. 29, XXX: http://data.europa.eu/eli/reg/2003/1831/oj.
(2) XXXX Xxxxxxx 2022;20(12):7701, xxxxx://xxx.xxx/10.2903/x.xxxx.2022.7701.
(3) XXXX Journal 2025;23:x9556, xxxxx://xxx.xxx/10.2903/x.xxxx.2025.9556.
XXXXXXX