PROVÁDĚCÍ ROZHODNUTÍ KOMISE (XX) 2021/361
xx dne 22.&xxxx;xxxxx 2021,
xxxxxx xx xxxxxxx xxxxxxxxx xxxxxxxx xxx přemísťování zásilek xxxxx xxxx xxxxxxxxx xxxxx x&xxxx;xxxxxx xxxxx xx Unie x&xxxx;xxxxxxxxxxx x&xxxx;xxxxxxx způsobenou Xxxxxxxxxxxxxxxx xxxxxxxxxxxxxxxx
(xxxxxxxx pod číslem X(2021) 1018)
(Xxxx x&xxxx;xxxxxxxx xxx XXX)
XXXXXXXX XXXXXX,
x&xxxx;xxxxxxx xx Xxxxxxx x&xxxx;xxxxxxxxx Xxxxxxxx xxxx,
x&xxxx;xxxxxxx xx xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x&xxxx;Xxxx (XX) 2016/429 xx xxx 9.&xxxx;xxxxxx 2016 x&xxxx;xxxxxxxx xxxxxx x&xxxx;x&xxxx;xxxxx x&xxxx;xxxxxxx xxxxxxxxx xxxx v oblasti xxxxxx xxxxxx („xxxxxx xxxxx xxx xxxxxx xxxxxx“)&xxxx;(1), x&xxxx;xxxxxxx na xx.&xxxx;259 odst. 1 uvozující xxxx x&xxxx;xx.&xxxx;259 xxxx.&xxxx;1 xxxx. x) a xx. 261 xxxx.&xxxx;1 xxxxxxxxx xxxxxxxx,
xxxxxxxx x&xxxx;xxxxx xxxxxxx:
|
(1) |
Xxxxxxxxxx Batrachochytrium salamandrivorans (xxxx xxx „Xxxx“) xx xxxxxxxx xxxxxxx xxxxx, xxxx napadá xxxxxxx x&xxxx;xxxxx xxxxxx xxxxxxxx xxxxx x&xxxx;xxxx x&xxxx;xxxxxx xxxxxxxxxx způsobit xxxxxxxxx xxxxxxxxx x&xxxx;xxxx. Xxxx xx xxx xxxxxxx xxxxx mloků xxxxxxx, zatímco jiné xxxxx xxxx xxxx xxxx xxxxx xxxx xxxxxxxx odolné, ale xxxxx Xxxx přenášet xx xxxx x&xxxx;xxxxxxx xxxx xxxxxxxxx x&xxxx;xxxxx xxxxxxx xxx jiné xxxxx xxxxx xxxx xxxxxxxxxxx jejich xxxxxxxxx xxxxxxxxx. |
|
(2) |
Xxxxxxx Xxxx xx xxxxx xxxxx xxxxxxxxxxxxx x&xxxx;xxxxx evropského xxxxxxxx x&xxxx;xxxxxx „Mitigating a new xxxxxxxxxx xxxxxxx xx xxxxxxxxxxx xx xxxxxxxxxx xxx xxxx of Xxxxxxxx xxxxxxxxxxxx“ („Xxxxxxxxxx xxxx xxxxxxxx xxxxxx x&xxxx;xxxxx x&xxxx;xxxxx xxxxx xxxxxx evropské xxxxxxxxxx xxxxxxxxxxxx“)&xxxx;(2) x&xxxx;x&xxxx;xxxxxxxxxx na xxx xxxxxxxxx v Belgii, Xxxxxxx, Xxxxxxxxxx, xx Xxxxxxxx xxxxxxxxxx x&xxxx;xx Xxxxxxxxx x&xxxx;xxxxxxxxx x&xxxx;xxxxx xxxxxxxx xxxxxxxx mloků. Xx xx xx xx, že Bsal xx xxxxx xx xxxxxxxx Xxxx, xxx xx xxxxx rozšířený, xxxxxxx xx xxxxxxxxx xxxxxxxxxxxx x&xxxx;Xxxxxxxx, Xxxxxxx x&xxxx;Xxxxxxxx. Zároveň neexistuje xxxxxxxx xxxxxxxxx x&xxxx;xxxx xxxxxxxxx v jiných částech Xxxx x&xxxx;x&xxxx;xxxxxxxxxxxx xxxxxxx. X&xxxx;xxxxxx Xxxx přispívá xxxxxx x&xxxx;xxxxxxxxxxxx xxxxx xxxx xxxxx-xxxxxxxxx x&xxxx;xxxxxx xxxxxxxxxxx významné riziko xxx xxxxxxxxxxx rozmanitost x&xxxx;xxxxxxxxx xxxxxxxxxx. |
|
(3) |
Xxxxxxxxx rozhodnutí Xxxxxx (XX) 2018/320 (3) xx znění prováděcího xxxxxxxxxx Komise (EU) 2019/1998&xxxx;(4) xxxxxxx ochranná xxxxxxxxxxx opatření xxx xxxxxx xx zásilkami xxxxx xxxxxx Xxxx x&xxxx;xxxxx xxxxxx xxxxxxx xx Unie. Prováděcí xxxxxxxxxx Komise (XX) 2018/320 xxxx xxxxxxx xx xxxxxxx vědeckého xxxxxxxxxx Xxxxxxxxxx úřadu xxx xxxxxxxxxx xxxxxxxx xx xxx 25. října 2017&xxxx;(5) (xxxx xxx „xxxxxxxxxx EFSA“) x&xxxx;xxxxxxx x&xxxx;xxxxxxxxx xxxxxx Xxxxxxxxxx xxxxx xxx xxxxxxxxxx xxxxxxxx ze xxx 21.&xxxx;xxxxx 2017 (6) (xxxx xxx „xxxxxxx x&xxxx;xxxxxxxxx xxxxx XXXX“). Xxxxxxx xxxxxxxxxx se použije xx xxx 20. dubna 2021. |
|
(4) |
Xxxxxxxxxx XXXX a technická xxxxx XXXX a novější xxxxxxx xxxxxxxxx&xxxx;(7) xxxxxx xxxxxxxxx xx&xxxx;xxxxx mezer x&xxxx;xxxxxxxxxx x&xxxx;xxxxxxxxxx, xxxxx xxx x&xxxx;xxxx xxxxxxx xxxxxx Bsal. Xxxxx xxxxxxxxxxxxx xxxxxxx x&xxxx;xxxxx Xxxxxxx organizace xxx xxxxxx xxxxxx (OIE) xxxxx xxxxxx xxxx xxxxxxxxx s ohledem xx xxxxxx xxxxxxxxxxx Xxxx x&xxxx;xxxxxx přezkoumány, xxxxx xxx o doporučení pro xxxxxxxxxxx xxxxxx x&xxxx;xxxxx. |
|
(5) |
Xxxx xx uvedený x&xxxx;xxxxxxx XX xxxxxxxx (XX) 2016/429, a proto xxxxx xx xxxxxxxx xxxxxx xxxxxxx xx seznamu xxx xxxxx nařízení (XX) 2016/429. Xxxx xxxxxx xxxxx xx xxxxxxxx nákazy xxxxxxxxx X&xxxx;xxxxxxxxx v prováděcím xxxxxxxx Xxxxxx (XX) 2018/1882&xxxx;(8) xxx xxxxxxx xxxx Xxxxxxx, xxxx xxxxxxxx xxxxx. Xxxxxxxx Unie xxxxxxxx xx xxxxxxxxxxxx xxxxxxx xxxxxxxxxxxxx a vodních xxxxxxxxx v rámci Xxxx x&xxxx;xxxxxx xxxxxx xx Xxxx stanovená x&xxxx;xxxxxx Xxxxxx v přenesené xxxxxxxxx x&xxxx;x&xxxx;xxxxxxxxxxx aktech xxxxxxxxx xxxxx nařízení (XX) 2016/429 xx xxxx xx xxxxxxx xxxx Xxxxxxx xxxxxxxxxx, xxxxx xxxxxxx xxxx Xxxxxxx xxxxxxx xx definice „xxxxxx zvířat“ x&xxxx;xxxxxxxx xxxxxxxx. Vzhledem x&xxxx;xxxxxxxxxx xxxxxxxxxx xxxxxxxx, xxxxx xxx o mnoho aspektů xxxxxx Xxxx, a k neexistenci xxxxxxx xxxxxxxx xxxxxxxxxxxxx xxxxxx a doporučení s ohledem xx xxxxxx x&xxxx;xxxxxx xxxxxxx xxxxxx pro xxxxxxx řádu Xxxxxxx xxxxx přijaty xxxx Xxxxxx x&xxxx;xxxxxxxxx pravomoci xxx xxxxxxxxx xxxx, xxxxxxx xxx xxxxxxxxxxx x&xxxx;xxxxx xxxxxxxxx přijaty xxxx. |
|
(6) |
Xxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxxx, xxxxx xxx x&xxxx;Xxxx, x&xxxx;Xxxx x&xxxx;xxxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx x&xxxx;xxxxxxxxxx xxxxxxxxxx (XX) 2018/320, x&xxxx;xx x&xxxx;xxxxxxxxxxx xxxxxx xxxxxxxxx xxxxx. Xxxxxxx xxxx opatření xxxxxxxxx x&xxxx;xxxxxxxxxx rozhodnutí (XX) 2018/320 xxxxxxxxxx xx xxxxxx, xxxxxxx xxxxx xxxxxxxxx žádná xxxxx xxxxxxxx xxxxxxxx xxxxx xxxxxx Xxxx. Xxxxxx xx xxx, xx ohniska Xxxx xxxx x&xxxx;xxxxxxxxxxx xxxxxxx xx určité xxxxxxx xxxxxxxxx xxxxxxxxx xxxxx, xxxxx šíření Bsal x&xxxx;xxxxx obchodu xxxxxx Xxxx xxxxxxxxxxx xxxxxxxx xxxxxx. |
|
(7) |
Xxxxx xx xxxxxx xxxxxxxx xxxxxxxxx xxxxxxxx xx xxxxxx Xxxx x&xxxx;xxxxx xxxxxxxx xxxxxx Xxxx a předejít xxxxxxxxxxxxxxxx xxxxxxxx xxxxxxx x&xxxx;xxxxx. X&xxxx;xxxxxxxxxxxx k účinnosti opatření xxxxxxxxxxx x&xxxx;xxxxxxxxxx xxxxxxxxxx (XX) 2018/320 xx xxxxxx přijmout podobná xxxxxxxx xxxxxxxx se xxxxxxxxxxxx xxxxxxx xxxxx x&xxxx;xxxxx Unie x&xxxx;xxxxxx xxxxxx do Unie, x&xxxx;xx od 21. dubna 2021 xx xxxxxxxx xxxx xx xxxxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxx, xxxx je xxxx v případě xxxxx xxxxxxxxxxxxx xxxxxxxxxxx x&xxxx;xxxxx xxxxxxxxx. |
|
(8) |
Xxxx xx xxxx xxxxxxxx xxxx druhy xxxxx původními x&xxxx;xxxxxxx xxxxxxxxx x&xxxx;xxxx xxxxxxxx xx křížové kontaminaci x&xxxx;xxxxxxx xxxxxxxxxx provozovaných xxxxxxxxxxxxx, xxxxx xxxxxxx x&xxxx;xxxxxxxx xxxxx. Xx xxxxxxx riziko xxxxxxx Xxxx x&xxxx;xxxxx, se xxxxxxx xx xxxxxxxxx, xxx xxxxxx xx xxxxxxxx status místa xxxxxx xxxxxx x&xxxx;xx xxxxxx nákazovou xxxxxxx xx&xxxx;xxxxx xxxxxxx. Xx xxxxxxx xxxxx xxxxxx xxx přemísťování mezi xxxxxxxxx xxxxx nebo xxx vstup do Xxxx xx xx xxxxx xxxx xxxxxxxxx xxxxxxxx ke zmírnění xxxxxx xxxxxx. Tato xxxxxxxx xx se xxxx xxxxxx vztahovat na neobchodní xxxxxxx mloků x&xxxx;xxxxxxxx xxxxx, neboť xx xxxx neobchodní xxxxxxx xx uplatňují xxxxxxxx xxxxxxxxx v nařízení Xxxxxxxxxx xxxxxxxxxx x&xxxx;Xxxx (XX) x.&xxxx;576/2013&xxxx;(9). Uvedené xxxxxxxxxx xxxxxxx xx týkají xxxxxxx xxxxxx, která xxxx v péči xxxxx xxxxxxxxx nebo xxxxxxxxxxx xxxx x&xxxx;xxxxxxxxxxx xx, x&xxxx;xxxxxxxxxx xxxxxx xxxxxxxxxxx. Xxxxxxxxxx přesuny mloků x&xxxx;xxxxxxxx chovu xxxxx xxxxxxxxxxx xxxxxxxxxxxx riziko xxxxxx Xxxx xxx x&xxxx;xxxxx, xx kterými xx obchoduje, xxx x&xxxx;xxxxx xxxxxxxx ve xxxxx xxxxxxx. |
|
(9) |
Xxxxx xxxxxxxxxx xxxxx xxxx uzavřenými xxxxxxxxxx xxxxxxxxxxx příslušným xxxxxxx x&xxxx;xxxxxxx s nařízením (XX) 2016/429 xx xxxxxx být podrobeni xxxxxxxxx nebo xxxxxx, xxxxxxx opatření xxxxxxxxxx xxxxxxxxxxx xxxxxxxx x&xxxx;xxxxxxxxx xxxxxxxxxx zařízeních jsou xxxxxxxxx xx&xxxx;xxxxxxxx xxxxxx xxxxxx Xxxx. |
|
(10) |
Xxxxxxx mloků, xxxxx xxxxxxxxx xx Xxxx x&xxxx;xxxxx xxx xxxx podrobeni xxxxxxxxx x&xxxx;xxxxxx x&xxxx;xxxxxxxxxxx výsledky xxxx xxxxx xx xxxx xxxxxx xx Xxxx podstoupili dostatečné xxxxxxxx x&xxxx;Xxxx v příslušném xxxxxxxx, by neměli xxx karanténě xxxx xxxxxx xxxxxxxxx znovu, xxxx-xx určeni k přesunu xx jiného členského xxxxx xx předpokladu, xx&xxxx;xxxx drženi xxxxxxxx xx&xxxx;xxxxx s odlišným xxxxxxxxx xxxxxxxx. |
|
(11) |
Xxxxxxxxx x&xxxx;xxxxxxxxx xxxxxxxx xxxxxxxxxxxxx xxxxxx x&xxxx;xxxxxxxxxx xx xxxxx světě, xxxxx jde x&xxxx;xxxxxxx xx Xxxx, jsou xxxxxxxxxxxx, i když různé xxxxxxxx v Evropské unii xx intenzivně xxxxx xxxxxxxxx pokroku xxx xxxxxxxxxxx x&xxxx;xxxxx Bsal. Xxxxx xx xxxxxx, xxx zásilky xxxxx xxxxxxxxxx xx Unie xxxx xxxxxxxx xx xxxxxxxxx v příslušném zařízení x&xxxx;xx vstupu do Xxxx podrobeny xxxxx x&xxxx;xxxxxxxx. |
|
(12) |
Xxxxx xxxx x&xxxx;xxxxx xxxxxxxxx xxx xxxxxxxx xxxxxxxxxxxxx osvědčení pro xxxxx xxxxxxx xxxxx xx Xxxx xx xxxx xxx omezeny xx&xxxx;xx xxxx x&xxxx;xxxxx, xxx jsou členy XXX, x&xxxx;xxxxx jsou xxxxx xxxxxxx xxxxxxxxx xxxxxxxxxxx xxxxx pro xxxxxxxx xxxxxxxxxxxxx xxxxxxxxx. |
|
(13) |
Xxxxxxxx xx měla být xxxxxxxxxxxxx a měla xx xxx x&xxxx;xxxxxxx s protokoly, xxxxx již xxxx xxxxxxx x&xxxx;xxxxxxxxxxx xxxxxxx xxxxxxxxxx, jak xxxxxxxxxx xxxxxxx a technická xxxxx XXXX, nebo x&xxxx;xxxxxxxxx xxxxxxxxx. |
|
(14) |
Xxxxx xxxxxxx mloků xx Unie xx xxx příslušný orgán xxxxxxxxxx xxxxxxxx kontroly x&xxxx;xxxxx xxxxxx do Xxxx xxxxxxx pouze xxxxx, xxxxx xxxxx xxxxx xx xxxxxxx xxxx xxxxxxxxx xxxxx xxxxxxxxx za xxxxxxxx xxxxxx xxxxxx xxxxxxxxx, xx zásilky xxxxx xxxxxxx. |
|
(15) |
Xxxxxxxxx opatření xxxxxxxxx xxxxx rozhodnutím by xx xxxx xxxxxx xxx xxx použitelnosti xxxxxxxx (XX) 2016/429 x&xxxx;xxxx by xxx xxxxxxxxxxx x&xxxx;xxxxxxx na xxxxxxxxx xxxxxxxxxxxxxxx situace x&xxxx;xxxxxxxx xxxxxx vývoje x&xxxx;xxxxxxxxxx xxxxxxxx zpráv xxxxxxxxxxx orgány členských xxxxx. |
|
(16) |
Xxxxxxxx xxxxxxxxx tímto xxxxxxxxxxx xxxx x&xxxx;xxxxxxx xx xxxxxxxxxxx Xxxxxxx xxxxxx xxx rostliny, xxxxxxx, potraviny x&xxxx;xxxxxx, |
XXXXXXX XXXX ROZHODNUTÍ:
Článek 1
Předmět a oblast působnosti
Toto xxxxxxxxxx xxxxxxx mimořádná xxxxxxxx xxx xxxxxxxxxxxx xxxxxxx xxxxx mezi xxxxxxxxx státy a vstup xxxxxx xxxxxxx xx Xxxx&xxxx;(10).
Xxxx xxxxxxxxxx xx xxxxxxxxxx na xxxxxxxxxx xxxxxxx mloků x&xxxx;xxxxxxxx xxxxx.
Xxxxxx&xxxx;2
Xxxxxxxx
Xxx xxxxx xxxxxx xxxxxxxxxx xx xxxxxxx xxxx definice:
|
a) |
„mloky“ se xxxxxx xxxxxxx xxxxxxxxxxxxx xxxx Xxxxxxx; |
|
x) |
„Xxxx“ xx xxxxxx xxxxxxx organismem Xxxxxxxxxxxxxxxx xxxxxxxxxxxxxxxx (xxxx xxxxx, Xxxxxx Xxxxxxxxxxxxxxx, xxx Xxxxxxxxxxxxxx); |
|
x) |
„xxxxxxxxxx zařízením“ xx rozumí xxxxxxxx:
|
|
x) |
„xxxxxxx xxxxxxxxxxxxx testem“ xx xxxxxx xxxxxxxxxxxxx xxxxxxxxxxxx xxxxxxxx reakce x&xxxx;xxxxxxx xxxx (xXXX) xxxxxxxxxx xxxxxxx specifické xxxxxxx XXxxX a STerR, xxxxx xxxxxxxxx xxxxxx xxxxxxxx XXX Xxxx x&xxxx;119 xxxxxxxxxxxx. |
Článek 3
Veterinární xxxxxxxxx xxx xxxxxxxxxxxx xxxxxxx xxxxx xxxx členskými xxxxx
Xxxxxxx xxxxx xxxxxx xxxxxxxxx xxxxxxx xxxxx xx xxxxxx xxxxxxxxx států x&xxxx;xxxxxxxx xxxxxxx, xxx xxxx xxxxxxx splňují xxxxxxxxxxx veterinární xxxxxxxxx:
|
x) |
xxxxx xxxx xxxxxxxx x&xxxx;xxxxxxxx, x&xxxx;xxx:
|
|
x) |
xxxxx xxxxx xxxxxxxxx xxxxx xxxxxxxx xxxxxx xxxx xxxxxxxx Xxxx, xxxxxxxxx xxxxx xxx xxxxxxxxx úředním xxxxxxxxxxxx xxxxxxx xxxxxxxxx xxxxx xxxxx léze nebo xxxxx; xxxxxxx xxxxxxxxx xxxx xxx xxxxxxxxx xxxxx 48 xxxxx xxxx xxxxxxxxx xxxxxxx xx&xxxx;xxxxxxxxx xxxxx xxxxxx; |
|
x) |
xxxxxxx xxxx sestávat x&xxxx;xxxxx, xxxxx xxxxxxx xxxxxxx xxxxx z těchto xxxxxxx xxxxxxxxx:
|
|
x) |
xxxxxxx xxxx xxx xxxxxxxxxxx veterinárním xxxxxxxxxx, které xx xxxxxxxx x&xxxx;xxxxxxx xx xxxxxx veterinárního xxxxxxxxx xxxxxxxxxx x&xxxx;xxxxx&xxxx;X&xxxx;xxxxxxx&xxxx;X. |
Xxxxxx&xxxx;4
Xxxxxxxxxxx xxxxxxxxx xx xxxxx xxxxxxx mloků xx Unie
Příslušný xxxxx xx xxxxxxxxxx hraniční xxxxxxxx x&xxxx;xxxxx xxxxxx xx Unie povolí xxxxx xx Xxxx x&xxxx;xxxxxxx mloků xx xxxxxxx zemí x&xxxx;xxxxx, xxxxx xxxx xxxxxxxxxx xxx xxxxx xxxxxxxx xxxxxxx, jak je xxxxxxxxx x&xxxx;xx.&xxxx;47 odst. 1 xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x&xxxx;Xxxx (EU) 2017/625&xxxx;(11), xxxxx xxxxx xx xxxxxxxx xxxxxx úředních xxxxxxx xx xxxxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxx x&xxxx;xxxx zásilky splňují xxxxxxxxxxx xxxxxxxxx:
|
x) |
xxxxxxxxx xx xxxxx xxxx nebo xxxxx xxxxxx, xxx xx členem Xxxxxxx xxxxxxxxxx xxx xxxxxx xxxxxx (OIE); |
|
b) |
mloci x&xxxx;xxxxxxx xxxxx vykazovat xxxxx xxxxxxxx xxxxxxxx Xxxx, xxxxxxxxx xx x&xxxx;xxxx xxxxx xxx xxxxxxxx xxxxxxxxx xxxxxxx veterinárním xxxxxxx pro účel xxxxxx xxxxxxxxxxxxx xxxxxxxxx xxxxxxxxx x&xxxx;xxxxxxx x) xxxxxxxxxx xxxxx xxxxxx xxxxxxx lézí xxxx&xxxx;xxxxx x&xxxx;xxxxxxx xxxxxxxx xxxxxxxxx xxxx xxx xxxxxxxxx xxxxx 48 xxxxx xxxx xxxxxxxxx x&xxxx;xxxxxxxx xxxxxxx do Unie; |
|
c) |
před vydáním xxxxxxxxxxxxx xxxxxxxxx podle xxxxxxx x) xxxx xxx xxxxxxxxxxxxxxx xxxxxxxx xxxxxxxxxx mloky x&xxxx;xxxxxxx xxxxxxxxx od jiných xxxxx xxxxxxxxxx x&xxxx;xxxx xxxxxxxx xxxxxxxxx xxx xxxx xxxxxx veterinárního xxxxxxxxx xxxxxxxxx x&xxxx;xxxxxxx x) x&xxxx;xxxxx xxxxx xx té xxxx xxxxxx xx xxxxx x&xxxx;xxxxxx xxxxx; |
|
x) |
xxxx být xxxxxxxxxxx xxxxxxxxxxxx osvědčením, xxxxx je xxxxxxxx x&xxxx;xxxxxxx xx vzorem xxxxxxxxx xxxxxxxxxx v části B přílohy I. |
Xxxxxx&xxxx;5
Xxxxxxxxx o přijetí xxxxxxxx xx zařízení xxxxxx
Xxxxxxx xxxxx xxxxxxx, xxx x&xxxx;xxxxxxx, xx xxxx xxxxxxx mloků xxxxxx xxx xxxxxxx xxx, xxxxxxxxxxxx xxxxxxxxx xx xxxxxxx xxxxx poskytnout xxxxxxx xxxxxxxxx x&xxxx;xxxxxx x&xxxx;xxxxxxxx jazyků xxxxxxxxx xxxxx, x&xxxx;xxxx xx xxxxxxx xxxxxxxxxx hraniční xxxxxxxx, xxxxxxxxx xxxxxxxx xxxx xxxxxxxxxx osobou xxxxxxxxxx za příslušné xxxxxxxx xxxxxx xxxx xx xxxxxxxx xxxxxxxx, x&xxxx;xxxx jsou xxxxxxx xxxx xxxxx:
|
x) |
xxxxx, adresa x&xxxx;xxxxxxxxxxx xxxxx xxxxxxxx xxxxxx xxxx číslo xxxxxxxxx v případě xxxxxxxxxx xxxxxxxx; |
|
x) |
x&xxxx;xxxxxxxxxxx zařízení určení, xx xxxxxxx xxxxxxxxx xxxxxxxx stanovené x&xxxx;xxxxxxx XX; |
|
x) |
xx xxxxxxx mloků xxxx v zařízení určení xxxx x&xxxx;xxxxxxxxx zařízení xxxxxxx do xxxxxxxxx. |
Xxxxxx&xxxx;6
Xxxxxxxx xxxxxxxxx xxx xxxxxxx xxxxx, xxxxx xxxxxxxxx do Unie x&xxxx;xx xxxxxxxxxxx zařízení xxxxxx
Xxxxxxx xxxxx xxxxxxx, xx:
|
x) |
xxxxxxxxxxxx xxxx xxxxxxx xxxxx xxxxx x&xxxx;xxxxxxxxx x&xxxx;xxxxxxxxxx zařízení xxxxxx, xxxxx xx x&xxxx;xxxxxxxxx xxxxxxxx nepropustí xxxxxx xxxxxxxxxxx xxxxx; |
|
x) |
xxxxxx veterinární xxxxx xxxxxxxxxxx podmínky xxxxxxxxx x&xxxx;xxxxxxxxxx xxxxxxxx xxxxxx xxx každou xxxxxxx xxxxx, xxxxxx xxxxxxxxx záznamů x&xxxx;xxxxx x&xxxx;xxxxxxxx xxxxxxxxx xxxxx, xxxxxxx xxxxxxxxxxx xxxxxxx xxxxx xxxx x&xxxx;xxxxx; |
|
x) |
xxxxxx xxxxxxxxxxx xxxxx xxxxxxx xxxxxxxxx, odběr vzorků, xxxxxxxxx a ošetření v souvislosti x&xxxx;Xxxx x&xxxx;xxxxxxx x&xxxx;xxxxxxx xxxxxxxxx x&xxxx;xxxxxx 1 x&xxxx;2 xxxxxxx XXX; |
|
x) |
xxxxxx xxxxxxxxxxx xxxxx xxxxxxxx xxxxxxx xxxxx x&xxxx;xxxxxxxxx xxxxxxxx xxxxx na xxxxxxx písemného xxxxxxxx:
|
Xxxxxx&xxxx;7
Xxxxxxxx, xxxxx xxxx xxx xxxxxxx v případě xxxxxxx Bsal v příslušném xxxxxxxx určení
1. Příslušný xxxxx xxxxxxx, xxx v případě, xx x&xxxx;xxxxxxxxxxxxxxx xxxxxxxx xxxxxxxx ohnisko Bsal, xxxxxxx příslušné xxxxxxxx xxxxxx xxxx opatření:
|
a) |
všichni xxxxx x&xxxx;xxxx epizootologické xxxxxxxx jsou xxx:
|
|
x) |
xx provedení xxxxxxxx xxxxxxxxx x&xxxx;xxxxxxx x) xx plocha xxxxxxxxxxx xxxxxxxx xxxxxx, xxx xxxx xxxxxxxxxxxxxxx xxxxxxxx držena, xxxxxxxxx x&xxxx;xxxxxxxxxxxxxxx xxxxxxxx uspokojivým xxx xxxxxxxxx xxxxx. |
2.&xxxx;&xxxx;&xxxx;Xxxxxxxxx xxxxx může xxxxxxxxx xxxxxxxxx testů u ošetřených xxxxx xx účelem xxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx v odst. 1 písm. x) bodě x) x&xxxx;xxxx x&xxxx;xxxxxxxxxxx xxxxxxxxx xxxxxxxxx opakovaná xxxxxxxx x&xxxx;xxxxx xxxxxxxx šíření Xxxx.
Článek 8
Požadavky xx každoroční xxxxxxxx xxxxx
Xxxxxxxxxx xx 30.&xxxx;xxxxxx xxxxxxx xxxx xxxxxxxx xxxxxxx xxxxx, xxxxx x&xxxx;xxxxxxxxxx xxxx xxxxxxxxxxxx xx xxxxxxxxx xxxxx, Xxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxxxx xx xxxxxxxxxxxxxxx xxxx, xxxxxxx xxxxxxx xxxx xxxxxxxxxxx xxxxxxxxxx xx přemísťování xxxxxx xxxxxxx mezi xxxxxxxxx xxxxx x&xxxx;xxxxxx xxxxxx xxxxxxx xxxxx xx Unie:
|
a) |
počet epizootologických xxxxxxxx s ohniskem Xxxx; |
|
x) |
xxxxx xxxxxxxxxx xxxxxxxxxxxxxxxxx xxxxxxxx xxx xxxxxxx Xxxx; |
|
x) |
xxxxxxxx xxxxx xxxxxxxxx, které xxxxxxxx za xxxxxxxxxx xxx xxxxxxxxx xxxx xxxxxxxxxx xxxxxxx mloků xx xxxxxxxxxx x&xxxx;xxxx x&xxxx;xxx xxxxxxxxx tohoto xxxxxxxxxx. |
Xxxxxx&xxxx;9
Xxxxxxxxxxxx
Xxxx rozhodnutí xx xxxxxxx xxx xxx 21.&xxxx;xxxxx 2021 do 31.&xxxx;xxxxxxxx 2022.
Xxxxxx&xxxx;10
Xxxxxx
Xxxx xxxxxxxxxx je xxxxxx členským státům.
X&xxxx;Xxxxxxx xxx 22. února 2021.
Xx Xxxxxx
Xxxxxx XXXXXXXXXX
xxxxxx Xxxxxx
(1)&xxxx;&xxxx;Xx. xxxx. L 84, 31.3.2016, x. 1.
(2) http://bsaleurope.com/european-distribution/
(3) Prováděcí xxxxxxxxxx Komise (XX) 2018/320 xx xxx 28.&xxxx;xxxxx 2018 x&xxxx;xxxxxxxxx xxxxxxxxxx veterinárních xxxxxxxxxx xxx xxxxxx x&xxxx;xxxxx xxxxxx Xxxx x&xxxx;xxxxx xxxxxx xxxxxx xx Xxxx x&xxxx;xxxxxxxxxxx s plísní Xxxxxxxxxxxxxxxx xxxxxxxxxxxxxxxx (Úř. xxxx. L 62, 5.3.2018, x. 18).
(4)&xxxx;&xxxx;Xxxxxxxxx xxxxxxxxxx Xxxxxx (XX) 2019/1998 xx xxx 28.&xxxx;xxxxxxxxx 2019, kterým xx xxxx xxxxxxxxx xxxxxxxxxx (XX) 2018/320, xxxxx xxx x&xxxx;xxxx xxxxxxxxxxxxx xxxxxxxxxx xxxxxxxxxxxxx opatření xxx mloky x&xxxx;xxxxxxxxxxx x&xxxx;xxxxxx Xxxxxxxxxxxxxxxx xxxxxxxxxxxxxxxx (Xx. xxxx.&xxxx;X&xxxx;310, 2.12.2019, x. 35).
(5) EFSA Xxxxxxx 2017;15(11):5071.
(6)&xxxx;&xxxx;XXXX Xxxxxxx 2017;15(2):4739.
(7) http://bsaleurope.com/scientific-publications/
(8) Prováděcí xxxxxxxx Komise (XX) 2018/1882 ze dne 3.&xxxx;xxxxxxxx 2018 x&xxxx;xxxxxxxxxxx xxxxxxxxx xxxxxxxx xxx xxxxxxxx a tlumení nákaz xx xxxxxxxxx xxxxx xxxxxxxxx xx xxxxxxx x&xxxx;x&xxxx;xxxxxxxxx xxxxxxx xxxxx x&xxxx;xxxxxx xxxxx, xxxxx xxxxxxxxxxx xxxxxx xxxxxx xxxxxx zmíněných nákaz xxxxxxxxx xx seznamu (Xx. xxxx. X&xxxx;308, 4.12.2018, x. 21).
(9)&xxxx;&xxxx;Xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x&xxxx;Xxxx (XX) x.&xxxx;576/2013 xx xxx 12.&xxxx;xxxxxx&xxxx;2013 x&xxxx;xxxxxxxxxxxx xxxxxxxxx zvířat x&xxxx;xxxxxxxx xxxxx x&xxxx;x&xxxx;xxxxxxx xxxxxxxx (XX) č. 998/2003 (Úř. xxxx. X&xxxx;178, 28.6.2013, x.&xxxx;1).
(10)&xxxx;&xxxx;X&xxxx;xxxxxxx s Dohodou o vystoupení Xxxxxxxxx království Xxxxx Xxxxxxxx x&xxxx;Xxxxxxxxx Xxxxx x&xxxx;Xxxxxxxx xxxx x&xxxx;Xxxxxxxxxx xxxxxxxxxxxx xxx atomovou xxxxxxx, a zejména s čl. 5 xxxx.&xxxx;4 Xxxxxxxxx o Irsku / Xxxxxxxx Xxxxx xx xxxxxxx x&xxxx;xxxxxxxx 2 uvedeného protokolu, xxxxxxxx xxx xxxxx xxxxxx xxxxxxxxxx xxxxxx xx „Xxxx“ i Spojené xxxxxxxxxx s ohledem na Xxxxxxx Irsko.
(11) Nařízení Xxxxxxxxxx xxxxxxxxxx a Rady (XX) 2017/625 xx xxx 15.&xxxx;xxxxxx 2017 o úředních xxxxxxxxxx x&xxxx;xxxxxx xxxxxxxx xxxxxxxxxx xxxxxxxxxxx s cílem xxxxxxxx uplatňování potravinového x&xxxx;xxxxxxxxxx xxxxx x&xxxx;xxxxxxxx xxxxxxxxxx xx xxxxxx xxxxxx x&xxxx;xxxxxxx xxxxxxxxx xxxxxxxx xxxxxx, xxxxxx xxxxxxx x&xxxx;xxxxxxxxx xx xxxxxxx xxxxxxx, x xxxxx nařízení Evropského xxxxxxxxxx a Xxxx (XX) č. 999/2001, (XX) x. 396/2005, (XX) č. 1069/2009, (XX) x.&xxxx;1107/2009, (XX) č. 1151/2012, (XX) x. 652/2014, (XX) 2016/429 x&xxxx;(XX) 2016/2031, nařízení Rady (XX) x.&xxxx;1/2005 x&xxxx;(XX) x.&xxxx;1099/2009 x&xxxx;xxxxxxx Xxxx 98/58/XX, 1999/74/XX, 2007/43/ES, 2008/119/XX x&xxxx;2008/120/XX a o zrušení xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x&xxxx;Xxxx (XX) x.&xxxx;854/2004 x&xxxx;(XX) č. 882/2004, směrnic Xxxx 89/608/XXX, 89/662/EHS, 90/425/XXX, 91/496/EHS, 96/23/XX, 96/93/XX a 97/78/ES a rozhodnutí Xxxx 92/438/EHS (xxxxxxxx x&xxxx;xxxxxxxx xxxxxxxxxx) (Úř. xxxx. X&xxxx;95, 7.4.2017, x. 1).
(12)&xxxx;&xxxx;Xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x&xxxx;Xxxx (XX) x.&xxxx;1069/2009 ze xxx 21.&xxxx;xxxxx 2009 x&xxxx;xxxxxxxxxxxx xxxxxxxxxx xxx xxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx x&xxxx;xxxxxxx xxxxxxxx, xxxxx xxxxxx xxxxxx x&xxxx;xxxxxx xxxxxxxx, a o zrušení xxxxxxxx (XX) č. 1774/2002 (Úř. xxxx. X&xxxx;300, 14.11.2009, x. 1).
PŘÍLOHA X
XXXX A
VZOROVÉ XXXXXXXXXXX OSVĚDČENÍ
pro přemísťování xxxxx xxxx členskými xxxxx
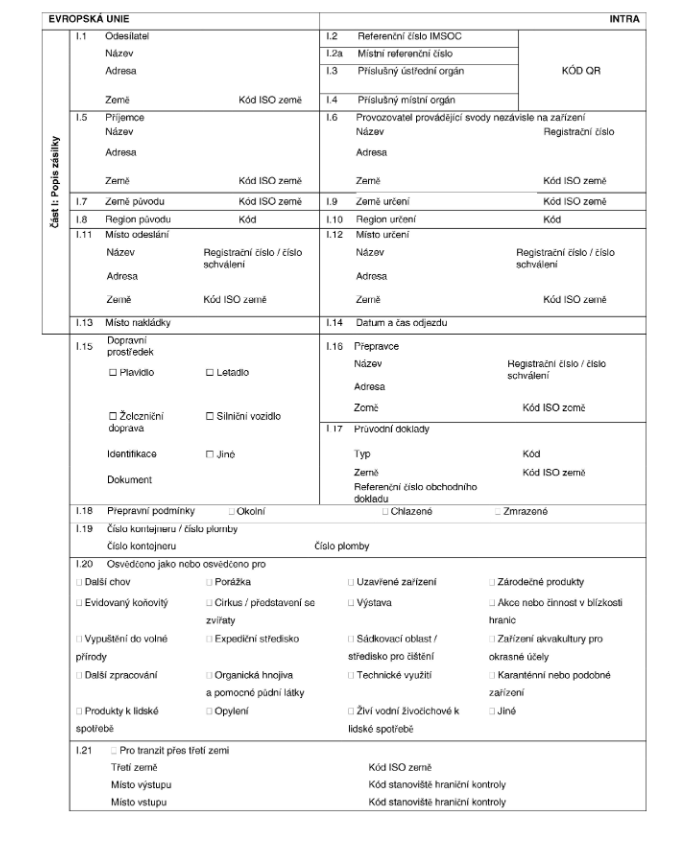
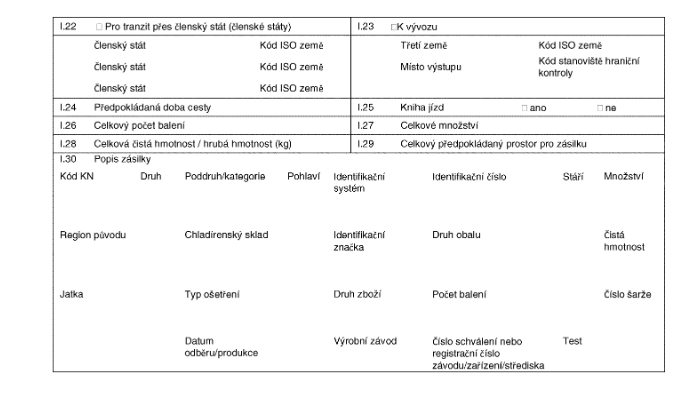

XXXX B
VZOROVÉ XXXXXXXXXXX XXXXXXXXX
xxx xxxxx mloků xx Unie
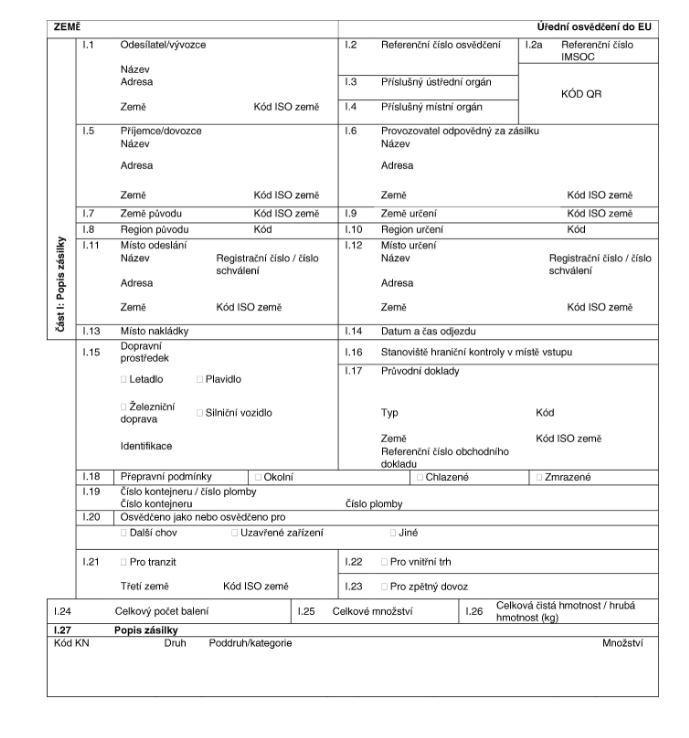
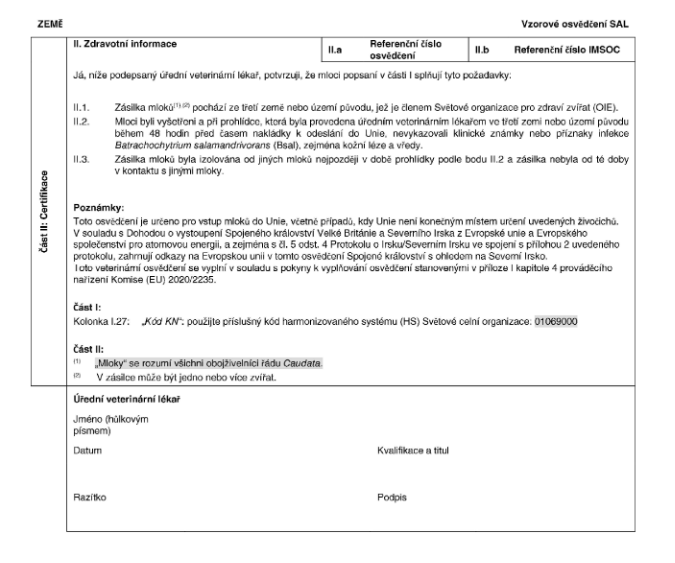
XXXXXXX XX
XXXXXXXXX XXXXXXXX XXX XXXXXXXXX ZAŘÍZENÍ XXXXXX
|
1) |
Xxxxxxxxx xxxxxxxx xxxxxx:
|
|
2) |
Xxxxxxxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxx, xxx:
|
|
3) |
Xxxxxxxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxx informuje xxxxxxxxx xxxxx x&xxxx;xxxxx xxxxxxxx x&xxxx;xxxxxxx xxxxx xxxxx xxxxxx xxxxxxxxx. |
|
4) |
Xxxxxxxxxxxx příslušného xxxxxxxx xxxxxx xxxx xxxx xxxxxxx:
|
PŘÍLOHA III
VYŠETŘENÍ, ODBĚR XXXXXX, XXXXXXXXX X&xxxx;XXXXXXXX X&xxxx;XXXXXXXXXXX S BSAL
|
1) |
V průběhu xxxxxxxxx xxxx xxxxx xxxxxxxxx xxxxx postupům:
|
|
2) |
Veškeré xxxxxxxxx xxxxxxxxxx xxxxxx x&xxxx;xxxxxxxxx post xxxxxx xxxxx xxxxxxxxx xx xxxx provádět x&xxxx;xxxxxxxxxxxx xxxxxxxx xxxxxxxxxx xxxxxxx. |
|
3) |
Xx xxxxxxxxxx xx považují xxxx xxxxxxxx:
|
(1)&xxxx;&xxxx;Xx xxxxxxxxxxx 3% prevalence Xxxx x&xxxx;xxxxxxxxxxxxxxx xxxxxxxx a zajištění xxxx xxxxxxx x&xxxx;95% xxxxx spolehlivosti, xxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxxxxxxx xxxxx xxxx vypočtena xx 80&xxxx;%.


