XXXXXXXX KOMISE (XX) 2019/319
xx xxx 6. xxxxx 2019,
xxxxxx xx mění xxxxxxx IX xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Xxxx (XX) č. 999/2001 x xxxxxxx XX xxxxxxxx Xxxxxx (XX) x. 142/2011, pokud xxx x xxxxxxxxxxx xxxxxxxxx xxx xxxxxx xx Xxxx xxxxxxxx xx xxxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxxxxxx
(Xxxx x významem xxx XXX)
XXXXXXXX XXXXXX,
x xxxxxxx xx Xxxxxxx x xxxxxxxxx Evropské xxxx,
x xxxxxxx na xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Xxxx (XX) x. 999/2001 xx xxx 22. května 2001 x xxxxxxxxx pravidel xxx prevenci, xxxxxxx x xxxxxxxxx některých xxxxxxxxxx spongiformních xxxxxxxxxxxxx (1), x xxxxxxx xx xx. 23 xxxxx xxxxxxxxxxx x xx. 23x úvodní větu x xxxxxxx x) xxxxxxxxx nařízení,
x xxxxxxx xx xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Xxxx (ES) x. 1069/2009 xx xxx 21. xxxxx 2009 x xxxxxxxxxxxx xxxxxxxxxx pro xxxxxxxx produkty živočišného xxxxxx x xxxxxxx xxxxxxxx, xxxxx nejsou xxxxxx x xxxxxx spotřebě, a o zrušení xxxxxxxx (XX) č. 1774/2002 (xxxxxxxx x xxxxxxxxxx xxxxxxxxxx xxxxxxxxxxx xxxxxx) (2), a zejména xx xx. 42 odst. 2 xxxxxx xxxx, písmeno x) x xxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxx,
vzhledem x xxxxx důvodům:
|
(1) |
Xxxxxxxx (XX) x. 999/2001 stanoví xxxxxxxx xxx prevenci, xxxxxxx x xxxxxxxxx přenosných xxxxxxxxxxxxxx xxxxxxxxxxxxx (XXX) x xxxxx, xxxx a koz. Vztahuje xx xx xxxxxxxx x xxxxxxx živých zvířat x xxxxxxxx xxxxxxxxxxx xxxxxx xx trh x x xxxxxxxxx xxxxxxxxxx xxxxxxxxx na xxxxxx vývoz. Uvedené xxxxxxxx xxxxxx stanoví xxxxxx xxxxxx pro xxxxxxxx xxxxxxxxx xxxxx x třetích zemí xxxx jejich xxxxxxx, xxxxx xx xxxxxxx x xxxxxxxxxx Komise 2007/453/XX (3), podle statusu XXX xx kategorií xx zanedbatelným xxxxxxx xxxxxxx XXX, kontrolovaným xxxxxxx xxxxxxx XXX x xxxxxxxxx rizikem xxxxxxx XXX. |
|
(2) |
X xxxxxxx XX xxxxxxxx (ES) x. 999/2001 xx xxxxxxx požadavky xx xxxxx živých zvířat, xxxxxx, xxxxxxx x xxxxxxxx xxxxxxxxxxx původu xx Xxxx. Xxxxxxxx X uvedené přílohy xxxxxxxxx xxxxxxx xxxxxxxxx xxx dovoz xxxxx xxxxxxxxxxxx xxxxxx XXX xxxxxxx xxxx nebo xxxxxxx. X xxxxxxxx X xxxxxxx xxxxxxx xx navíc xxxxxxx, xx xxxxxxxxxxx xxxxxxxxx, xxxxx xx xxxxxxxxxx xxx dovozu xxxxxxxxx xxxxxxxxxx produktů xxxxxxxxxxx xxxxxx x xxxxxxxxx xxxxxxxx xx Xxxx, xxxx xxxx včetně xxxxxxxxxxxx xxxxxxxxxxx bílkovin, xxxx xxx xxxxxxxx xxxxxxxxxx xxxxxxxxx xx xxxxxx XXX. |
|
(3) |
X xxxxxxx XX xxxxxxxx X xxxxxxxx (XX) č. 999/2001, xx xxxxx xxxxxxxx Xxxxxx (XX) 2016/1396 (4), xx xxxxxx xxxxxxxxx, xx xxxx xxxx xxxxxxxx xx Xxxx xxxxx xxx xxxxxxxx xxxxxxxxx x xxxxxxx XXX xxxx xxxxxx xxxxxxxx. Xxxxxxxx ke xxxxxxxxxxx, že xxxxxx xxxxx přenosu XXX xx prostřednictvím krmiva xxxxxxxxxxxxxxx prionem XXX, xx xxxxxxx požadavek xxx xxx pozměněn xxx, xxx xxxxxxxx, xx xxxx xxxx xxxxxxxx xx Xxxx xxxxx xxx xxxxxxx XXX xxxx xxxxxx xxxxxxxx. Xxxxxxxx X xxxxxxx XX xxxxxxxx (XX) x. 999/2001 xx proto xxxx xxx xxxxxxxxxxxxx způsobem xxxxxxx. |
|
(4) |
Xxxxxxxx (ES) x. 1069/2009 xxxxxxx hygienická x xxxxxxxxxxx xxxxxxxx xxx xxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx x xxxxxxx produkty x xxxxx xxxxxxxxxx xxxxxxx xxx xxxxxx xxxx x xxxxxx, xxxxx x xxxxxxxxxxx x xxxxxx xxxxxxxx xxxxxxxx, x xxxxxxxx xx na minimum. Xxxxxxxx Xxxxxx (EU) x. 142/2011 (5) stanoví xxxxxxxxx xxxxxxxx xxx xxxxxxxxxx x xxxxxxxxxxx xxxxxxxx xxx vedlejší xxxxxxxx xxxxxxxxxxx xxxxxx x xxxxxxx produkty xxxxxxxxx xxxxxxxxx (XX) x. 1069/2009, xxxxxx xxxxxxxxx xxxxxxxxx xx xxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx x xxxxxxxxx xxxxxxxx ze xxxxxxx xxxx. |
|
(5) |
X xxxxxxx X xxxxxxxx (EU) x. 142/2011 xxxx xxxxxxx xxxxxxx definice, xxxxx xxxx xxx používány xxx xxxxx xxxxxxxxx xxxxxxxx. Xxxxx xxxxxx 31 xxxxxxxx (XX) x. 142/2011 xxxx xxx xxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxxxx původu x xxxxxxxxx produktů pro xxxxx xx Xxxx xxxx xxxxxxx přes Xxxx provázeny xxxxxxxxxxxxx xxxxxxxxxxx x xxxxxxxxxxxx, xxxxx odpovídají vzorům xxxxxxxxxx x xxxxxxx XX xxxxxxxxx nařízení. |
|
(6) |
X xxxxxx 11.4.13 bodě 1 Kodexu zdraví xxxxxxxxxxxxx živočichů Světové xxxxxxxxxx xxx zdraví xxxxxx (dále xxx „xxxxx XXX“) (6) xx xxxxxxxxxx, xx xxxxxxxxxx xxxxxx x škvarky xxxxxxx x xxxxxxxxxxx, xxx xxxx xxxxxxxxxx x xxxxxx XXX, x xxxxxxxx, xxxxx xxxxxxxx takové produkty, xxxxxxxxxxx ze xxxx xxxx oblastí xx xxxxxxxx xxxxxxxxxxxxxx rizika xxxxxxx BSE, xx xxxxxxx se xxxxxxx xxxxxx případ XXX, xx xxxxx xxxx xxxxxxxxx mezinárodního obchodu xxxxx x případě, xx xxxx získány xx skotu xxxxxxxxxx xx datu, xxx xxx v xxxx xxxxxxxx zaveden zákaz xxxxxx xxxxxxxxxxx masokostní xxxxxxx x škvarky xxxxxxxxx z xxxxxxxxxxx, xxx xxxx definovány x xxxxxx XXX. X bodě 2 xxxxxxxxx xxxxxx xx xxxxxxxxxx, xx xxxxxxxxxx xxxxxx x xxxxxxx xxxxxxx z xxxxxxxxxxx, xxx xxxx xxxxxxxxxx x xxxxxx OIE, x xxxxxxxx, které xxxxxxxx xxxxxx xxxxxxxx, xx neměly xxx xxxxxxxxx xxxxxxxxxxxxx obchodu, xxxxx xxxxxxxxx ze xxxx nebo xxxxxxx xx statusem kontrolovaného xxxx xxxxxxxxxx rizika xxxxxxx XXX. |
|
(7) |
Xxxxx OIE xxxxxxxx masokostní xxxxxx xxxx pevné xxxxxxxxxx xxxxxxxx xxxxxxx xxxxxxx/xxxxxxxxx xxxxxxxxxxx xxxxx, xxxxxx xxxxxxxxxx bílkovinných meziproduktů xxxxxx než peptidy x xxxxxxxxxx xxxxxxxxx xxxxx xxx 10 000 daltonů x aminokyseliny. X xxxxxxxx xxxxxxxxxx xxxxxx x xxxxxx XXX xx xxxx xxxxxxxx xxx xxxxxxxx masokostní xxxxxx uvedená x xxxx 27 xxxxxxx X xxxxxxxx (XX) x. 142/2011, xxx xxxxxxxx xxxxxxxxxxxx xxxxxxxxxxx xxxxxxxx x bodě 5 xxxxxxx xxxxxxx. |
|
(8) |
X xxxxxxx x xx. 41 xxxx. 2 xxxx. x) xxxxxxxx (XX) č. 1069/2009 může xxx masokostní xxxxxx, xxx xx xxxxxxxxxx x xxxxxxxx xxxxxxxxxx Xxxx, xxxxxxxx do Xxxx pouze za xxxxxxxxxxx, xx xxxx xxxxxxx xxxxxxxxx pravidla xxxxxxxxxx podmínky pro xxxxxx xxxxx. Xxxxxxxx x tomu, xx xxxxx xxxxxx prováděcí xxxxxxxx xxxxxxx nebyla, xxxx xxxxx xxxxxxxxxx xxxxxx získané z xxxxxxxxx xxxxxxxxx 1 xxxx materiálu kategorie 2 xx Xxxx x současné době xxxxxxx. Xxxxxxxxxx xxxxxxxxx xxxxxxxxx, xxx xxxx xxxxxxxxxx v xxxxxxxx xxxxxxxxxx Xxxx, nicméně xx Unie xxxxxxx xxx, xxxx-xx xxxxxxxx xxxxxxxx xxx xxxxx xxxxxxxx xx XXX xxxxxxxxx v xxxxxxx XX xxxxxxxx X xxxxxx X nařízení (XX) x. 999/2001 a xxx podmínky xxx xxxxx xxxxxxxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx x xxxxxxxx (XX) č. 142/2011. |
|
(9) |
Za xxxxxx sjednocení podmínek xxx dovoz xx Xxxx xxxxxxxxxx xx XXX xxxxxxxxxxx v xxxxxxxx (XX) č. 999/2001 x xxxxxxxxxxxx xxxxxxxxxx x kapitole xxxxxx XXX xxxxxxxx xx BSE xx xxxxxx xxxxxx přílohu XX kapitolu X xxxxx B xxxxxxxx (XX) x. 999/2001 tak, xxx xxxxxxxxx xxxxxxxxx x uvedeném xxxxxx xxxxxxxxxxx xxxxxxxxxx xxxxxx 11.4.13 xxxxxx OIE. Xxxxxxx xxxxxxxx x xxxx, že xxxxxxxxx xxxxxxxxxxxx živočišných bílkovin xxxxxxxxx z přežvýkavců xx v Xxxx xxxxxxxx při výrobě xxxxx xxx xxxxxxx x xxxxxxxx xxxxx, xxxxxx xx být xxxxxxxxxx xxxxxx 11.4.13 xxxxxx OIE, aby xx při dovozu xxxxxxxxx v xxxxxxxxx x xxxxxxxx Xxxxxxxx xxxx o xxxxxxxxxxxxx xxxxxxxxx, xxxxxxxxxxx x xxxxxxx xxxxxx xxxxx xxx xxxxxxx x xxxxxxxx xxxxx xxxxxxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxx x xxxxxxxxxxx, xxxxx je xxxxxx xxxxxx xxx zvířata x xxxxxxxx xxxxx xxxxxxxxxx x xxxxxxxx x xxxxxxx x xxxxxxxx xxxxxxxx Xxxx. |
|
(10) |
Příloha XX kapitola X xxxxx X nařízení (XX) x. 999/2001 xx xxxxx xxxx být xxxxxxxxxxxxx xxxxxxxx xxxxxxx. |
|
(11) |
Xx xxxxxxx xxxxxxxx předpisů Xxxx xxxx xx xxxxxxx xxxxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxx lze xxxxxxxxx, xxx xxxxxxxx xxxxxxxxxxx xxxxxx xxxx označeny xxxx vedlejší xxxxxxxx xxxxxxxxxxx původu. Xxxx xx xxxxxxxxxxxx rozhodne, xx xxxxxxxx xxxxxxxxxxx xxxxxx xxxx být xxxxxxxx xx xxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx, xx xxxx xxxxxxxxxx xxxxxxxx. Xxxxxx xxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx xxxxx xxx xxxxxxxxx xxx xxxxxxx xxxxxxxx. Xxxxxxx vedlejší produkty xxxxxxxxxxx původu xxxx xxxxxx xxxx xxxxxxxxxxx xxxxxxxxxxxx (KN) jako xxxxxxxxx produkty určené x xxxxxx xxxxxxxx, xxxxx jsou uvedeny x příloze X xxxxxxxx Xxxx (XXX) x. 2658/87 (7). Při xxxxxxxxxx xx kódů XX xxxx xxx xxxxx xxxxxx xxxxxxxxx xxxxx xxxxxxx xxxxx xxxxxxxx xxxxxxxx, které xxxx xxxxxxxxx x lidské xxxxxxxx, a produkty, xxxxx jsou xxxxxxxxxxx x xxxxxx xxxxxxxx. Xxx xx předešlo xxxxxxxxx xxxxxxxxxxx při xxxxx xxxxxxxxxx, xxxx xx se ve xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx x xxxxxxxxxxx xxx xxxxx nezpracovaných xxxxxxxxxx xxxxxxxx živočišného původu xxxxxxxx, xx xxxxxx xxxxxxxx xxxxxxxx živočišného xxxxxx xxxxxxxxx xx xxxxxxxxxxx produktů, které xxxx v xxxxxxxxx xxxx způsobilé x xxxxxx xxxxxxxx, xxxx xxxx xxxxxxxx jako xxxxxxxx produkty živočišného xxxxxx xxxxxx xxxxxxxxx x xxxxxxxxxxxxx řetězce x xx x xxxx tak xxxxxxxxx. Xxxxx xxxxxxxxxxxxx xxxxxxxxx xxxxxxxxx x xxxxxxx XX xxxxxxxxxx 3 (X), 3 (X) x 8 xxxxxxxx (XX) x. 142/2011 xx xxxxx xxxx xxx xxxxxxxxxxxxx xxxxxxxx xxxxxxx. |
|
(12) |
Xxxxxxxxx xxxxxxxx xx TSE xx vzorech xxxxxxxxx xxx dovoz xxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx do Xxxx x xxx xxxxxxx xxxxxx xxxxxxxx xxxx Xxxx xxxxxxxxx x xxxxxxxxxx 1, 1a, 2 (A), 2 (X), 3 (X), 3 (X), 3 (X), 3 (D), 3 (X), 3 (X), 4 (X), 4 (X), 4 (X), 6 (X), 8, 10 (X), 10 (X), 11, 12 x 18 xxxxxxx XX xxxxxxxx (XX) č. 142/2011 by xxxxx xxxx xxxx xxx xxxxxxxxx, xxx xxxxxxxxxxxx xxxxxxxxx kapitoly X xxxxxxx XX xxxxxxxx (XX) x. 999/2001, xx znění xxxxxxxx Xxxxxx (EU) č. 630/2013 (8), xxxxxxxx (EU) 2016/1396 x tohoto nařízení. |
|
(13) |
Podle xxxxxxxx xxx xxxxx xxxxxxxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx ve vzoru xxxxxxxxxxxxx xxxxxxxxx x xxxxxxx XX kapitole 1 nařízení (EU) x. 142/2011 nesmí být xx xxxxxxxxxxxx xxxxxxxxxxx xxxxxxxxxxx dovážených xx xxxxxxx xxxx xxxxxxxx xxxx přežvýkavců. Xxxx xxxxxxxxx týkající xx XXX uvedené xxxx XX.7. uvedeného vzoru xxxxxxxxxxxxx xxxxxxxxx, xx xxxxx tohoto nařízení, xxxxxxxxx xxxxxxxxxx záruky xxx xxxxxxxx xxxxxx XXX x xxxxxx xxxxxxxxxx. Xxxxx „xxxxxx xxx xxxxxxxxxxx“ xx xxxxx xxxx xxx xx všech xxxxxxx xxxxxxxxxxxxx xxxxxxxxx xxxxxxxxxxx x příloze XX xxxxxxxx (EU) x. 142/2011, které xxxx xxx xxxxxxxxx xxxxx xxxxxxxxx, zrušena. |
|
(14) |
Kapitoly 1, 1x, 2 (X), 2 (B), 3 (X), 3 (X), 3 (C), 3 (X), 3 (E), 3 (X), 4 (X), 4 (X), 4 (X), 6 (X), 8, 10 (X), 10 (X), 11, 12 x 18 xxxxxxx XV xxxxxxxx (XX) x. 142/2011 xx xxxxx xxxx xxx xxxxxxxxxxxxx způsobem xxxxxxx. |
|
(15) |
Xxxxxxx xxxxxxxxxxxx xxxxxxxx xxx xxxxxx kosmetických xxxxxxxxxx a léčivých xxxxxxxxx musí xxx xxxxx xxx xxxxxxxxxx xx xxxxxxxxxx hraniční xxxxxxxx xxx účely xxxxxxxxxxxxx kontrol xxxxxxxxxxx xxxxxxxxxxx vyplněným v xxxxxxx se xxxxxx xxxxxxxx v příloze XX kapitole 20 xxxxxxxx (EU) č. 142/2011. Xxxxxxxxxxxx mohou xxxxxxxx x xxxxxxxxxx produktů xxxxxxxxxxx xxxxxx xxxx xxxx xxxxxxxx mohou xxxxxxxxx. Stávající vzor xxxxxxxxxx xxxxxxxx pouze xxxxxxx xxxxx xxxxxxxxxxx xxxx XX, xxxxxxx xxxxxxxxxxxxxxx xx xxxxxxxxxxxx xxxxxxx xxxxxxx xxxxxx xxxxxxx v členských xxxxxxx. Xx xxxxx xxxxxxxxxx xxxx možné xxxxxx stanovit xxxxxxxxxxxxx xxxxxx xxxx XX, xxxxx xx xxxxxxxxx xxxxxxx kombinace xxxxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx x xxxxxxxxxxxxxx. Stávající xxxx HS je xxxxx vhodné xxxxxxxx, xxx xxxxx zodpovědná xx xxxxxxx mohla xxxxxxxxxx xxxxxxxxxxxx stanovišti xxxxxxxx xxxxxxxx prostřednictvím xxxxxxxxxxxxxx xxxx XX x xxxxxxx s xxxxxxxxxxx Xxxxxx 2007/275/XX (9). Xxxxxxxx 20 přílohy XX xxxxxxxx (XX) x. 142/2011 xx xxxx xxx xxxxxxxxxxxxx xxxxxxxx změněna. |
|
(16) |
Aby xx xxxxxxxxx xxxxxxxx xxxxxxx, xxxx xx xxxx xxxxxxxx stanovit xxxxxxxxx období, xxxxx xxxxxxx xx xxxxx, xxxxxxx xx týkají xxxxx xxxxxxxx (EU) x. 142/2011, xxxx xxx xxxxxx přijímáno pro xxxxx xx Xxxx x xxxxxxx xxxx Xxxx, xxxxx xxxxxxx xxxxxxxxx xxxxxxxxx x xxxxxxxx (EU) x. 142/2011 platné před xxx, než xxxx xxxxxxxxx xxxxx xxxxxxxxx. |
|
(17) |
Opatření xxxxxxxxx xxxxx xxxxxxxxx xxxx x xxxxxxx xx xxxxxxxxxxx Stálého výboru xxx xxxxxxxx, xxxxxxx, xxxxxxxxx x xxxxxx, |
XXXXXXX XXXX XXXXXXXX:
Xxxxxx 1
Xxxxxxx XX nařízení (XX) č. 999/2001 se xxxx x xxxxxxx x xxxxxxxx X xxxxxx xxxxxxxx.
Xxxxxx 2
Xxxxxxx XX nařízení (XX) č. 142/2011 xx xxxx v souladu x xxxxxxxx XX tohoto xxxxxxxx.
Xxxxxx 3
Xxxxx xxxxxxxxxxx xxxxxx xx 30. září 2019 xx xxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx x xxxxxxxxx xxxxxxxx xxxxxxxxxxx veterinárním xxxxxxxxxx, xxxxx bylo xxxxx xxxxxxxx x podepsáno x souladu s xxxxxxxxxx xxxxxx veterinárního xxxxxxxxx xxxxxxxx x xxxxxxx XX xxxxxxxx 1, 1a, 2 (X), 2 (B), 3 (X), 3 (X), 3 (C), 3 (D), 3 (X), 3 (X), 4 (X), 4 (X), 4 (X), 6 (X), 8, 10 (A), 10 (X), 11, 12 x 18 nařízení (XX) x. 142/2011, ve xxxxx xxxxxxx před xxxxxxx xxxxxxxxx x xxxxxx 2 xxxxxx xxxxxxxx, x xxxxxxxx xxxxxxxxxxx, xxxxx bylo xxxxx xxxxxxxx x xxxxxxxxx x xxxxxxx xx xxxxxx xxxxxxxxxx xxxxxxxx v kapitole 20 xxxxxxx přílohy, xx xxxxx xxxxxxx xxxx xxxxxxx xxxxxxxxx x xxxxxx 2 xxxxxx nařízení, xxxxxx xxxxxxxxx pro dovoz xx Unie a xxxxxxx xxxx Xxxx, xxxxx byla xxxx xxxxxxxxxxx xxxxxxxxx xxxx xxxxxxxxxx řádně xxxxxxxx x podepsána xxxxxxxxxx 31. xxxxxxxx 2019.
Xxxxxx 4
Xxxx nařízení xxxxxxxx x xxxxxxxx dvacátým xxxx xx xxxxxxxxx x Xxxxxxx xxxxxxxx Xxxxxxxx xxxx.
Xxxx nařízení xx xxxxxxx x xxxxx xxxxxxx x xxxxx použitelné xx xxxxx xxxxxxxxx státech.
X Xxxxxxx xxx 6. xxxxx 2019.
Xx Xxxxxx
xxxxxxxx
Xxxx-Xxxxxx JUNCKER
(1)&xxxx;&xxxx;Xx.&xxxx;xxxx.&xxxx;X&xxxx;147, 31.5.2001, x.&xxxx;1.
(2)&xxxx;&xxxx;Xx.&xxxx;xxxx.&xxxx;X&xxxx;300, 14.11.2009, x.&xxxx;1.
(3)&xxxx;&xxxx;Xxxxxxxxxx Xxxxxx 2007/453/XX xx dne 29.&xxxx;xxxxxx 2007, xxxxxx se xxxxxxx status XXX xxxxxxxxx xxxxx xxxx xxxxxxx xxxx xxxx xxxxxx xxxxxxx vzhledem x xxxxxx xxxxxxx XXX (Xx.&xxxx;xxxx.&xxxx;X&xxxx;172, 30.6.2007, x.&xxxx;84).
(4)&xxxx;&xxxx;Xxxxxxxx Xxxxxx (XX) 2016/1396 ze xxx 18.&xxxx;xxxxx&xxxx;2016, xxxxxx se xxxx některé přílohy xxxxxxxx Evropského xxxxxxxxxx x&xxxx;Xxxx (XX) č. 999/2001 x&xxxx;xxxxxxxxx pravidel pro xxxxxxxx, tlumení x&xxxx;xxxxxxxxx xxxxxxxxx xxxxxxxxxx spongiformních xxxxxxxxxxxxx (Xx.&xxxx;xxxx.&xxxx;X&xxxx;225, 19.8.2016, x.&xxxx;76).
(5)&xxxx;&xxxx;Xxxxxxxx Xxxxxx (XX) x. 142/2011 xx xxx 25.&xxxx;xxxxx 2011, xxxxxx se xxxxxxx xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Rady (XX) x. 1069/2009 x xxxxxxxxxxxx xxxxxxxxxx pro xxxxxxxx xxxxxxxx živočišného xxxxxx a získané xxxxxxxx, xxxxx xxxxxx xxxxxx x lidské xxxxxxxx, a provádí xxxxxxxx Xxxx 97/78/XX, xxxxx jde x xxxxxx xxxxxx a xxxxxxxx xxxxxxxxxx xx xxxxxxxxxxxxx kontrol xx xxxxxxx xxxxx xxxxxxx xxxxxxxx (Xx.&xxxx;xxxx.&xxxx;X&xxxx;54, 26.2.2011, x.&xxxx;1).
(6) http://www.oie.int/international-standard-setting/terrestrial-code/access-online/
(7)&xxxx;&xxxx;Xxxxxxxx Xxxx (XXX) x. 2658/87 ze xxx 23.&xxxx;xxxxxxxx 1987 x celní a xxxxxxxxxxx nomenklatuře x x xxxxxxxxx xxxxxx xxxxxxxxx (Úř. věst. L 256, 7.9.1987, x.&xxxx;1).
(8) Nařízení Xxxxxx (XX) x.&xxxx;630/2013 xx dne 28.&xxxx;xxxxxx 2013, xxxxxx xx mění xxxxxxx xxxxxxxx Xxxxxxxxxx parlamentu x&xxxx;Xxxx (XX) x.&xxxx;999/2001 x&xxxx;xxxxxxxxx xxxxxxxx xxx xxxxxxxx, xxxxxxx a eradikaci xxxxxxxxx xxxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxxxxxx (Úř. věst. L 179, 29.6.2013, x.&xxxx;60).
(9) Rozhodnutí Xxxxxx 2007/275/XX xx xxx 17.&xxxx;xxxxx&xxxx;2007 x&xxxx;xxxxxxxxx xxxxxx a produktů, xx xxx se xxxxxxxx xxxxxxxx na xxxxxxxxxxxx xxxxxxxx xxxxxxxx xxxxx xxxxxxx Rady 91/496/XXX a 97/78/ES (Xx.&xxxx;xxxx.&xxxx;X&xxxx;116, 4.5.2007, x.&xxxx;9).
PŘÍLOHA I
Příloha IX xxxxxxxx (XX) x.&xxxx;999/2001 xx xxxx xxxxx:
|
1) |
X xxxxxxxx X:
|
|
2) |
X&xxxx;xxxxxxxx X xx xxxxx X xxxxxxxxx xxxxx: „XXXXX B Požadavky xx xxxxxxxxxxx osvědčení
|
XXXXXXX XX
Xxxxxxx XX xxxxxxxx (EU) č. 142/2011 xx mění takto:
|
1) |
Kapitoly 1 až 3 (X) xx xxxxxxxxx xxxxx: „XXXXXXXX 1 Xxxxxxxxxxx xxxxxxxxx xxx xxxxxxxxxx živočišné xxxxxxxxx xxxx xxx xxxxxxx x&xxxx;xxxxxxx xxxxxxxxx hmyzu, xxxxx xxxxxx xxxxxx x&xxxx;xxxxxx xxxxxxxx, včetně xxxxx a produktů jiných xxx xxxxxx xxx xxxxxxx v zájmovém xxxxx xxxxxxxxxxxx xxxx bílkoviny, x&xxxx;xxxx xxxxxx x&xxxx;xxxxxxxx xx Xxxxxxxx unie xxxx x&xxxx;xxxxxxxx xxxx xxxx xxxxx (2)  &xxxx;Text obrazu &xxxx;Text obrazu
XXXX: Xxxxxxxxxxx xxxxxxxxx xx EU Část X: Xxxxxxxxxxx x xxxxxxxx xxxxxxx X.1. Xxxxxxxxxx Xxxxx Xxxxxx Xxx. X.2. Xxxxx jednací xxxxxxxxx X.2.x. X.3. Xxxxxxxxx xxxxxxxx xxxxx X.4. Xxxxxxxxx místní orgán I.5. Xxxxxxxx Xxxxx Xxxxxx XXX Xxx. X.6. Osoba xxxxxxxxxx xx zásilku v XX Xxxxx Xxxxxx XXX Xxx. X.7. Země xxxxxx Xxx XXX X.8. Xxxxxx xxxxxx Xxx X.9. Xxxx xxxxxx Xxx ISO I.10. Xxxxxx xxxxxx Xxx X.11. Xxxxx xxxxxx Xxxxx Číslo xxxxxxxxx Xxxxxx Xxxxx Xxxxx xxxxxxxxx Xxxxxx Xxxxx Xxxxx xxxxxxxxx Xxxxxx X.12. Místo xxxxxx Xxxxx xxxxx Xxxxx Xxxxx xxxxxxxxx Xxxxxx XXX X.13. Xxxxx xxxxxxxx X.14. Xxxxx xxxxxxx X.15. Dopravní xxxxxxxxxx Xxxxxxx Xxxxxxxx Xxxxx Xxxxxxxx vozidlo Xxxxxxx Xxxxxxxxxxxx Xxxxx xx xxxxxxxx X.16. Xxxxxxx xxxxxxxxxx hraniční xxxxxxxx XX X.17.  Text obrazu Text obrazu
X.18. Xxxxx zboží I.19. Xxx xxxxx (kód HS) I.20. Xxxxxxxx X.21. Teplota produktů Okolní Xxxxxxxx Xxxxxxxx X.22. Xxxxx xxxxxx X.23. Xxxxx xxxxxx/xxxxxxxxxx X.24. Xxxx obalu I.25. Xxxxx xxxxxxxxx xxx: Xxxxxx Xxxxxxxxx xxxxxxx Xxxxxx krmiva xxx xxxxxxx x xxxxxxxx chovu I.26. Xxx xxxxxxx xxxx EU xx xxxxx země Třetí xxxx Kód ISO I.27. Xxx xxxxx xxxx xxxxxx xx XX X.28. Xxxxxxxxxxxx xxxxx Xxxxx xxxxxxxxx xxxxxxxx Xxxx (xxxxxxx xxxxx) Xxxx xxxxx Xxxxxxx xxxxx Xxxxx hmotnost Číslo xxxxx  Text obrazu Text obrazu
XXXX Xxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxx xxx xxxxxxx z farmově xxxxxxxxx xxxxx, xxxxx xxxxxx xxxxxx k xxxxxx xxxxxxxx, xxxxxx xxxxx x produktů xxxxxx než xxxxxx xxx zvířata v xxxxxxxx xxxxx xxxxxxxxxxxx xxxx xxxxxxxxx XX. Xxxxxxxxx xxxxxxxxx XX.x. Xxxxx jednací xxxxxxxxx XX.x. Xx, xxxx xxxxxxxxx xxxxxx xxxxxxxxxxx lékař, xxxxxxxxxx, že jsem xxxxxxx x porozuměl xxxxxxxx Evropského xxxxxxxxxx x Rady (ES) x. 1069/2009 (1a), xxxxxxx pokud xxx x xxxxxx 10 xxxxxxxxx xxxxxxxx, x xxxxxxxx Xxxxxx (EU) x. 142/2011 (1x), xxxxxxx xxxxx jde x xxxxxxx X xxxxxxxx XX xxxxx 1 a xxxxxxx XXX xxxxxxxx X xxxxxxxxx xxxxxxxx, x xxxxxxxxx, xx: XX.1. zpracované xxxxxxxxx xxxxxxxxx xxxx xxxxxxx popsaný výše xxxxxxxx výhradně xxxxxxxxxx xxxxxxxxx bílkoviny, xxxxx xxxxxx určeny x xxxxxx spotřebě x xxxxx: x) byly připraveny x skladovány x xxxxxxxx nebo xxxxxxx xxxxxxxxxx x dozorovaném xxxxxxxxxx xxxxxxx v xxxxxxx s xxxxxxx 24 xxxxxxxx (XX) x. 1069/2009; x x) xxxx xxxxxxxxxx xxxxxxxx x těchto xxxxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx: (2) xxx [- těla xxxxxxxxxx xxxxxx x xxxxxx části, xxxx x případě xxxxx xxxx xxxxxxxxxx zvířat xxxx jejich xxxxx, xxxxx jsou podle xxxxxxxx předpisů Xxxx xxxxxx k xxxxxx xxxxxxxx, avšak z xxxxxxxxxx důvodů xxxxxx x lidské xxxxxxxx xxxxxx;] (2) x/xxxx [- xxxxxxx upravená xxxx x níže uvedené xxxxx xxxxxxxxxxx buď xx zvířat, xxxxx xxxx xxxxxxxx xx xxxxxxx x xx xxxxxxxxx xxxx xxxxxxxx xxxx xxxxxxxx jako xxxxxxxxx k xxxxxxx x xxxxxx xxxxxxxx, xxxx těla x xxxx xxxxxxx xxxxx xxxxx usmrcené x xxxxxx xxxxxxxx x xxxxxxx x xxxxxxxx xxxxxxxx Xxxx: x) jatečně xxxxxxxx xxxx xxxx xxxx xxxxxx x xxxxxx xxxxx, xxxxx xxxx x xxxxxxx x právními xxxxxxxx Xxxx xxxxxxxxxx xx xxxxxxxx k xxxxxx xxxxxxxx, avšak nevykazovaly xxxxx xxxxxxxx xxxxxxxxxx xxxxxxxxxx xx xxxxxxx xxxx xxxxxxx; xx) xxxxx xxxxxxx; xxx) xxxx x xxxxx, xxxxxx jejich xxxxxxx a xxxxxx, xxxx a xxxxxxxxx, xxxxxx xxxxxx xxxxx, xxxxxxxxxx x xxxxxxxxxx xxxxxx, xxxxx x xxxxxxx; xx) xxxxxxx xxxxxxx; x) xxxx;] (2) a/nebo [- xxxx xxxxxx, xxxxx xxxxxxxxxxxx xxxxx xxxxxxxx xxxxxxxxxx přenosného xxxx xx člověka xxxx xxxxxxx, která xxxx xxxxxxxx xx xxxxxxx x která byla xx xxxxxxxxx xxxx xxxxxxxx xxxxxxxx xxxxxxxxxxx x porážce x xxxxxx xxxxxxxx v xxxxxxx x xxxxxxxx xxxxxxxx Xxxx;] (2) x/xxxx [- vedlejší xxxxxxxx xxxxxxxxxxx xxxxxx, xxxxx xxxxxxxx při výrobě xxxxxxxx určených x xxxxxx xxxxxxxx, xxxxxx xxxxxxxxxxx kostí, xxxxxxx xxxx xxxx z xxxxxxxxxxx nebo xxxxxxxxxx xx xxxxxxxxxx mléka;] (2) x/xxxx [- xxxxxxxx xxxxxxxxxxx původu xxxx xxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx, xxxxx x xxxxxxxxxx xxxxxx xxxx z důvodů xxxxxxxx způsobených xxxxxxxxx xxxxxx, xxxxxx balení xxxx jinými závadami, x xxxxx xxxxxxxx xxxxx riziko pro xxxxxx xxxx ani xxxxxx, xxx xxxxxx xxxxxx x xxxxxx xxxxxxxx;] (2) x/xxxx [- xxxx, xxxxxxxx, vlna, xxxx, xxxx, xxxx, xxxxxxx kopyt x xxxxxxxx a xxxxxx xxxxx pocházející xx xxxxxx xxxxxx, která xxxxxxxxxxxx xxxxx xxxxxxxx xxxxxxxxxx přenosného tímto xxxxxxxxx xx xxxxxxx xxxx zvířata;] (2) x/xxxx [- xxxxx xxxxxxxxxxx x xxxxxx části, xxxxx xxxxxxxx xxxxx, xxxxx xxxxxxxxxxxx xxxxx xxxxxxxx onemocnění xxxxxxxxxx xx xxxxxxx xxxx xxxxxxx;] (2) a/nebo [- xxxxxxxx xxxxxxxx živočišného xxxxxx z xxxxxxx xxxxxxxxx xxxxxxxxxxx xx xxxxxxxx xxxx xxxxxxx xx xxxxxx produktů xxxxxxxx k lidské xxxxxxxx;] Xxxx II: Xxxxxxxxx  Text obrazu Text obrazu
XXXX Xxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxx než získané x xxxxxxx xxxxxxxxx xxxxx, které xxxxxx xxxxxx x lidské xxxxxxxx, xxxxxx xxxxx x xxxxxxxx xxxxxx xxx xxxxxx pro xxxxxxx v xxxxxxxx xxxxx xxxxxxxxxxxx xxxx xxxxxxxxx XX. Zdravotní xxxxxxxxx XX.x. Xxxxx xxxxxxx xxxxxxxxx XX.x. (2) x/xxxx [- xxxx xxxxxxx xxxxxxxx xxxxxxxxxxx xx zvířat, xxxxx xxxxxxxxxxxx žádné xxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxx xxxxxxxxxx xx člověka xxxx zvířata: i) xxxxx xxxxxxx x xxxxxx x měkkými tkáněmi xxxx xxxxx; xx) xxxxx xxxxxxxx xxxxxxxxxxx xx xxxxxxxxxxxxx zvířat: — xxxxxxxx xxxxxxxx x xxxxx, — xxxxx, — xxxxxxxx xxxxxxxx x xxxxx, xxxxxx xxxxxxxxx skořápek; iii) xxxxxxxxxx xxxxxx xxxxxxxx z xxxxxxxxxx xxxxxx;] (2) a/nebo [- xxxxx a xxxxxxxxxxx bezobratlí živočichové, xxxxx druhů patogenních xxx xxxxxxx xxxx xxxxxxx x xxxxx;] (2) x/xxxx [- xxxxxxx x xxxx xxxxxxxx (Xxxxxxxx) a xxxxxxxxx (Xxxxxxxxxx) x xxxxxx xxxxx, xxxxx xxxxxxxxx xxxxxxxxx 1 xxxxxxxxx x čl. 8 xxxx. a) xxxxxx xxx), xx) a x) x xxxxxxxxx xxxxxxxxx 2 xxxxxxxxx x xx. 9 xxxx. a) až x) xxxxxxxx (XX) x. 1069/2009;] a c) byly xxxxxxxxx xxxx xxxxxx xxxxxxxxxx: (2) xxx [xxxxxxx xx xxxxxxx x xxxxx xxxxx xxx 133 °C po xxxx xxxxxxx 20 xxxxx xxx přerušení x xxx tlaku (xxxxxxxxxx) alespoň 3 xxxx xxxxxxxx xxxxxxxxx xxxxx x velikostí xxxxxx xxxx xxxxxxxxxxx xxxxxxxxx 50 mm;] (2) xxxx [x xxxxxxx xxxxxxxxxxx xxxxxxxx nepocházejících xx xxxxx, x xxxxxxxx rybí xxxxxx, xxxxxxxxxxxxxx xxxxxx 1-2-3-4-5-7 (xxxxxx xxxxxxxxxxxxxxx metodu) xxxxx přílohy XX xxxxxxxx III xxxxxxxx (XX) x. 142/2011;] (2) xxxx [x xxxxxxx xxxx xxxxxx zpracovatelské xxxxxx 1-2-3-4-5-6-7 (xxxxxx xxxxxxxxxxxxxxx xxxxxx) xxxxx xxxxxxx XX xxxxxxxx XXX xxxxxxxx (EU) x. 142/2011;] (2) xxxx [x případě xxxxxxx xxxx xxxxxxxxxxxxxx metodě 1-2-3-4-5-7 … (xxxxxx xxxxxxxxxxxxxxx metodu) xxxxx xxxxxxx IV kapitoly XXX nařízení (XX) x. 142/2011, xxxxxxx x xxxxxxx xxxxxx 7 xx na xxxxx xxxxx použije xxxxxxx ošetření xxx xxxxxxx xxxxxxx 80 °X;] XX.2. xxxxxxxxx xxxxx xxxxxxxxxxxxx xxxx xxxxxxxxx xxxxxxxx xxxxxxxxx vybraný xxxxxx a xxxxxxx xxx x xxxxxxx x těmito normami (3): Xxxxxxxxxx: xxxxxxxxxxxx v 25 x xxxxxxxx: x = 5, x = 0, x = 0, X = 0 Enterobacteriaceae: x = 5, x = 2, x = 10, X = 300 x 1 x; XX.3. xxxxxxx xxxxxx xxxxx xxxxxxxxxxxxx opatřeními x xxxxxxxxx xxxxxxxxxxx xxxxxxxxxxx xxxxxxx xx ošetření; II.4. xxxxxxx produkt byl: (2) xxx [zabalen do xxxxxx nebo xxxxxxxxxxxxxxx xxxxx,]  Text obrazu Text obrazu
XXXX Xxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxx xxx xxxxxxx x xxxxxxx xxxxxxxxx xxxxx, xxxxx xxxxxx xxxxxx k xxxxxx spotřebě, xxxxxx xxxxx x produktů xxxxxx xxx krmivo xxx xxxxxxx x xxxxxxxx xxxxx xxxxxxxxxxxx xxxx xxxxxxxxx XX. Xxxxxxxxx xxxxxxxxx XX.x. Xxxxx xxxxxxx xxxxxxxxx XX.x. (2) nebo [xxxxxxxxxxx xxxxx xxxxxx x xxxxxxxxxxxx nebo jiných xxxxxxxxxx xxxxxxxxxxxx, které xxxx xxxx xxxxxxxx xxxxxxxx vyčištěny x xxxxxxxxxxxxxxx,] xxxxx jsou xxxxxxxx xxxxxxxxx x nápisem „XXXX URČENO X XXXXXX XXXXXXXX“; XX.5. konečný xxxxxxx byl xxxxxx x uzavřeném xxxxxxxxx; (2) [XX.6. xxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxx xxxxxxx xxxxxxx xxxx xxxxxxxx xxxxxxxx xxxxxxxx živočišného xxxxxx x xxxxxxxxxxx xxxx jsou z xxxx xxxxxxx a: (2) xxx [xxxxxxxxx xx xxxx nebo oblasti xxxxxxxx x xxxxxxx x xxxxxxxxxxx 2007/453/XX xx xxxxxxxxx xxxx xxxx oblasti xx xxxxxxxxxxxxx rizikem xxxxxxx XXX, x xxxxx xxxxx xxxxxxx žádný xxxxxx xxxxxx XXX, x]] (2) nebo [pocházejí xx země xxxx xxxxxxx zařazené x xxxxxxx x xxxxxxxxxxx 2007/453/XX do xxxxxxxxx xxxx xxxx xxxxxxx xx xxxxxxxxxxxxx rizikem xxxxxxx XXX, x xxxxx byl xxxxxxx xxxxxx případ XXX, x vedlejší xxxxxxx xxxxxxxxxxx původu xxxx xxxxxxx produkt xxx xxxxxx xx xxxxxx xxxxxxxxxx po datu, xx kterého byl x xxxxxxx xxxx xxxx oblasti xxxxxx xxxxxxx zákaz xxxxxx xxxxxxxxxxx xxxxxxxxxx xxxxxxx x xxxxxxx xxxxxxxxx x přežvýkavců, xxx xxxx xxxxxxxxxx v Xxxxxx xxxxxx suchozemských xxxxxxxxx XXX, a] (2) xxx [xxxx xxxxxxx x xxxxxxxxxxx jiných xxx xxxx, ovce xxxx xxxx;] (2) xxxx [xxxx xxxxxxx ze xxxxx, ovcí xxxx xxx x xxxxxxxxxx xxxx uvedené xxxxxx xxx x xxxx xxxxxx xxxxxxx: (2) xxx [xxxxxxxx pocházející xx xxxxx, xxxx x xxx jiný než xxxxxxx xx zvířat xxxxxxxxxx, xxxxxxxxxxx chovaných x xxxxxxxxxx x xxxx xxxx xxxxxxx xxxxxxxx x xxxxxxx x rozhodnutím 2007/453/XX xx xxxxxxxxx xxxx xxxx xxxxxxx xx xxxxxxxxxxxxx xxxxxxx výskytu XXX;]] (2) xxxx [a) xxxxxxxxxxxxx xxxxxxxx materiál, xxx xx xxxxxxxxx x xxxx 1 xxxxxxx X xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Xxxx (XX) č. 999/2001 (4); x) xxxxxxx xxxxxxxx xxxx získané x xxxxx xxxxx, xxxx nebo xxx x výjimkou xxxxxx xxxxxxxxxx, nepřetržitě xxxxxxxxx x xxxxxxxxxx v xxxx xxxx xxxxxxx xxxxxxxx v souladu x rozhodnutím Komise 2007/453/XX (5) xx xxxxxxxxx xxxx xxxx xxxxxxx xx zanedbatelným xxxxxxx xxxxxxx XXX, x nichž xxxxx xxxxxxx xxxxx xxxxxx xxxxxx XXX; x) xxxxxxxx xxxxxxx živočišného původu xxxx získaný xxxxxxx xx xxxxx, xxxx xxxx xxx, xxxxx xxxx xx xxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxx xxxxx pomocí xxxxxxxxxxx tyčovitého nástroje xxxxxxxxxx do xxxxxx xxxxxxx xxxx xxxxxxxxxxxxxxx xxxxxxx xxxxxxx xx xxxxxx xxxxxxx, x xxxxxxxx xxxxxx xxxxxxxxxx, xxxxxxxxxxx xxxxxxxxx x xxxxxxxxxx v xxxx xxxx xxxxxxx xxxxxxxx x souladu s xxxxxxxxxxx 2007/453/ES xx xxxxxxxxx xxxx xxxx xxxxxxx se xxxxxxxxxxxxx xxxxxxx výskytu XXX;]]] XX.7. xxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxx produkt xxxxxxx xxxx: (2) xxx [neobsahují xxxxx xxxx mléčné xxxxxxx pocházející x xxxx xxxx xxx xxx xxxxxx xxxxxx xxx xxxxxx xxxxxxxxxxxxx xxxxxx jiných než xxxxxxxxxxxx zvířat;] (2) nebo [xxxxxxxx xxxxx xxxx xxxxxx výrobky pocházející x ovcí xxxx xxx a xxxx xxxxxx xxx krmení xxxxxxxxxxxxx xxxxxx xxxxxx xxx xxxxxxxxxxxx xxxxxx x xxxxx nebo xxxxxx xxxxxxx: x) jsou xxxxxxx x ovcí x koz, xxxxx xxxx xxxxxxxxxxx xx xxxxxxxx xxxxxxx v xxxx, x níž xxxx splněny xxxx xxxxxxxx: x) xxxxxxxx xxxxxxxx xx xxxxxxx hlášením;  Text obrazu Text obrazu
XXXX Xxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxx xxx získané x farmově xxxxxxxxx xxxxx, xxxxx xxxxxx xxxxxx x lidské xxxxxxxx, xxxxxx xxxxx x produktů xxxxxx xxx xxxxxx xxx xxxxxxx x zájmovém xxxxx xxxxxxxxxxxx xxxx xxxxxxxxx XX. Xxxxxxxxx xxxxxxxxx XX.x. Xxxxx xxxxxxx xxxxxxxxx XX.x. xx) xxxxxxx systém osvěty, xxxxxxxxx a xxxxxxx; xxx) xx hospodářství s xxxxxx xxxx xxxx xxx xx uplatňují xxxxxx xxxxxxx x xxxxxxx podezření xx XXX xxxx xxxxxxxxx xxxxxxxx klusavky; iv) ovce x kozy postižené xxxxxxxxx klusavkou jsou xxxxxxxx x xxxxxxxxxxxx; x) xxxxxx ovcí x xxx xxxxxxxxxx xxxxxxx xxxx xxxxxxx x xxxxxxxxxxx, xxx jsou xxxxxxxxxx v Xxxxxx xxxxxx suchozemských živočichů Xxxxxxx xxxxxxxxxx pro xxxxxx xxxxxx (OIE), xxxx xxxxxxxx a xxxxx xxx účinně xxxxxxx x xxxx xxxx xxxxxxxxxxxx xx xxxx xxxxxxxxxxx xxxxx xxx; x) xxxxxxxxx x xxxxxxxxxxxx, pro xxxxx xxxxxxx xxxxx xxxxxx xxxxxxx z xxxxxx xxxxxxxxx xx výskyt XXX; x) xxxxxxxxx x xxxxxxxxxxxx, x nichž xxxxxxxxxxxx po xxxx xxxxxxxxxxx sedmi let xxxxx xxxxxxxxxxxxxx xxxxx xxxxxx xxxxxxxx xxxxxxxx, xxxx xx xxxxxxxxx xxxxxxx xxxxxxxx xxxxxxxx: (2) xxx [xxxx xxxxxxxx x xxxxxxxxxxxx xxxx xxxxxxxx všechny ovce x xxxx x xxxxxxxxxxxx x xxxxxxxx xxxxxxxxxx beranů xxxxxxxx XXX/XXX, chovných bahnic xxxxxxxxx alespoň jednu xxxxx XXX x xxxxxx xxxxx XXX x xxxxxxx xxxx xxxxxxxxx alespoň jednu xxxxx XXX;] (2) xxxx [xxxx všechna xxxxxxx, x xxxxx xxxx xxxxxxxx klusavka xxxxxxxxx, xxxxxxxx x xxxxxxxxxxxx x na xxxxxxxxxxxx xx xxxxxxx xx xxx xxxx od xxxxxxxxx posledního xxxxxxx xxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxxxxxx xxxxxxxxx XXX, xxxxxx xxxxxxxxx xxxxx xxxxxxxxxxxxx xxxxxx xxxxxxxx 18 xxxxxx, x xxxxxxxx xxxx genotypu XXX/XXX, na xxxxxxxxxx XXX x negativním xxxxxxxxx v xxxxxxx x xxxxxxxxxxxxx metodami xxxxxxxxxxx x xxxxxxx X xxxxxxxx X xxxx 3.2 xxxxxxxx (XX) x. 999/2001: — xxxxxxx, xxxxx xxxx xxxxxxxx k xxxxxx xxxxxxxx, x — xxxxxxx, xxxxx xxxxxxx xxxx xxxx usmrcena x xxxxx xxxxxxxxxxxx, xxxxx xxxxxx usmrcena v xxxxx xxxxxxx xxxxxxxxx xxxxxx;]] XX.8. zpracované xxxxxxxxx xxxxxxxxx nebo xxxxxxx xxxxxxx xxxx obsahují xxxxxxxx produkty xxxxxxxxxxx xxxxxx x xxxxxxxxxxxxx xxxx xxxx z xxxx xxxxxxx x x xxxxxxx s xxxxxxxxxxx xxxxxxxxxxx x xxxxxxx X.1. (2) buď [xxxxxx určeny k xxxxxx krmiv xxx xxxxxxxxxxx xxxxxxx xxxx xxx xxxxxxxxxx xxxxxxx.] (2) (6) xxxx [jsou xxxxxx k xxxxxx xxxxx xxx nepřežvýkavá xxxxxxxxxxx xxxxxxx xxxx xxx xxxxxxxxxx xxxxxxx x xxxxxxxxxx se xxxxxxx zajistit, že xxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxx xxxxx xxxxxxxxxx xxxxxxxx xxxxxxxx xxxxx xxxxx xxxxxxxxxxx v xxxxxxx XX xxxxxxxx Xxxxxx (ES) x. 152/2009 (7).] Xxxxxxxx Xxxx X: — Xxxxxxx I.6.: Osoba xxxxxxxxxx xx xxxxxxx x Xxxxxxxx xxxx: xxxx xxxxxxx xx xxxxx xxxxxxx xxxxx xxxxx, xxxxx-xx se x osvědčení xxx xxxxx xxxxxx xxx xxxxxxx přes Xxxxxxxxx xxxx; xxxx xx xxxxxxx, xxxxx-xx xx x xxxxxxxxx xxx xxxxx dovážené xx Xxxxxxxx xxxx. — Kolonka X.12.: Xxxxx určení: xxxx xxxxxxx xx xxxxx vyplnit xxxxx xxxxx, xxxxx-xx xx x xxxxxxxxx xxx xxxxx určené xxx xxxxxxx. Xxxxxxxx xxx xxx xxx xxxxxxxx xxxxxxxxxx xxxxx xx xxxxxxxxxx xxxxxxx, svobodných xxxxxxxx x celních xxxxxxxx. — Kolonka X.15.: Xxxxxxxxxxx xxxxx (železničních xxxxxx xxxx kontejneru x xxxxxxxxxx automobilů), xxxxx xxxx (xxxxxxx) xxxx xxxxx (xxxxxxxx); xxxxxxxxx xx xxxxx xxxxxxxxxx v xxxxxxx xxxxxxxx a opětovného xxxxxxxx.  Text obrazu Text obrazu
XXXX Xxxxxxxxxx živočišné xxxxxxxxx jiné xxx xxxxxxx x xxxxxxx xxxxxxxxx hmyzu, xxxxx xxxxxx xxxxxx x xxxxxx spotřebě, xxxxxx xxxxx x xxxxxxxx xxxxxx xxx krmivo xxx xxxxxxx v xxxxxxxx xxxxx xxxxxxxxxxxx xxxx xxxxxxxxx XX. Zdravotní xxxxxxxxx XX.x. Číslo xxxxxxx xxxxxxxxx XX.x. — Xxxxxxx X.19.: Xxxxxxxx xxxxxxxxx kód XX: 05.05, 05.06, 05.07, 05.11, 23.01 xxxx 23.09. — Xxxxxxx X.25.: Xxxxxxxxx xxxxxxx: xxxxxxxx jiné xxxxxxx xxxxx xxxxxx xxxxxxxxxxxxx xxxxxx xxxxxx než xxxxxxxxxxxx xxxxxx x xxxxxx xxxx xxxxxxxxxx xxxxx xxx xxxxxxx x xxxxxxxx chovu. — Xxxxxxx I.26. a X.27.: Vyplňte podle xxxx, jedná-li xx x xxxxxxxxx pro xxxxxxx xxxx xxx xxxxx. — Xxxxxxx X.28.: Xxxx: xxxxxxx: Aves, Xxxxxxxxxx, Xxxxxx, Mammalia xxxxx Ruminantia xxxx Xxxxxx, Xxxxx, Xxxxxxxx, Xxxxxxxxx, bezobratlí xxxxx Xxxxxxxx a Crustacea. X xxxxxxx ryb xx xxxxxxxx chovu xxxxxx xxxxxxx xxxxx xxxx. Xxxx II: (1a) Xx. xxxx. X 300, 14.11.2009, s. 1. (1x) Xx. věst. L 54, 26.2.2011, x. 1. (2) Nehodící xx xxxxxxxx. (3) Xxx: x = xxxxx vzorků, xxxxx xxxx xxx xxxxxxxxx; x = xxxxxxx xxxxxxx xxxxx xxxxxxxx; xxxxxxxx xx považován xx xxxxxxxxxx, xxxxxxxx xxxxx xxxxxxxx ve xxxxx xxxxxxxx xxxxxxxxxx x; X = xxxxxxxxx xxxxxxx xxxxx bakterií; výsledek xx považován za xxxxxxxxxxxx, xxxxx xxxxx xxxxxxxx x xxxxxx xxxx xxxx xxxxxxxx xx roven xxxx xxxxx xxx M; x x = počet xxxxxx, jejichž xxxxxxxxxxx xxxxx smí xxx x rozmezí mezi x a X, xxxxxxx xxxxxx xx xxxxx xxxxx xxxxxxxxx xx přípustný, pokud xx bakteriální xxxxx xxxxxxxxx xxxxxx roven x nebo nižší. (4) Xx. xxxx. L 147, 31.5.2001, x. 1. (5) Xx. xxxx. X 172, 30.6.2007, x. 84. (6) Xxxxx xxxxxxxxxx za zásilku xxxxxxx v kolonce X.6. xxxx xxxxxxxx, xxx x xxxxxxx, xx xxxxxxxxxx xxxxxxxxx xxxxxxxxx nebo xxxxxxx xxxxxxx x xxxxx xxxxxxxxxxxx xxxxxxxxx xxxx xxx určeny k xxxxxx xxxxxx xxx xxxxxxxxxxxx xxxxxxxxxxx xxxxxxx xxxx xxx kožešinová xxxxxxx, xxxx xxxxxxx xxxxxxxxx xxxxxxxx xxxxx xxxxx xxxxxxxxxxx x xxxxxxx XX xxxxxxxx (XX) x. 152/2009, xxx xx ověřila xxxxxxxxxxxx nepovolených xxxxxx xxxxxxxxxxx xxxxxx. Xxxxxxxxx xxxxxxxx se výsledku xxxxxxxx zkoušení musí xxx xxx xxxxxxxxxx xxxxxxx xx stanovišti xxxxxxxx xxxxxxxx XX xxxxxxxxx x tomuto xxxxxxxxxxxxx xxxxxxxxx. (7) Xx. xxxx. L 54, 26.2.2009, s. 1. — Xxxxx xxxxxxx x xxxxxxx se xxxx xxxxx xx xxxxx xxxxx. — Poznámka xxx xxxxx xxxxxxxxxxx xx xxxxxxx x Xxxxxxxx xxxx: toto xxxxxxxxx xxxxxx xxxxx x xxxxxxxxxxxx xxxxxx x xxxx xxxxxxx xxxxxxxx xx do okamžiku, xxx dosáhne stanoviště xxxxxxxx xxxxxxxx. Xxxxxx veterinární xxxxx / úřední xxxxxxxxx Xxxxx (hůlkovým písmem): Xxxxxxxxxxx x xxxxx: Xxxxx: Xxxxxx: Xxxxxxx: XXXXXXXX 1x Xxxxxxxxxxx xxxxxxxxx xxx xxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxx z farmově xxxxxxxxx xxxxx, xxxxx nejsou xxxxxx x&xxxx;xxxxxx xxxxxxxx, xxxxxx xxxxx x&xxxx;xxxxxxxx xxxxxx než krmivo xxx xxxxxxx x&xxxx;xxxxxxxx xxxxx xxxxxxxxxxxx xxxx xxxxxxxxx, x&xxxx;xxxx xxxxxx x&xxxx;xxxxxxxx xx Evropské xxxx xxxx k tranzitu xxxx xxxx xxxxx (2) &xxxx; Text obrazu Text obrazu
XXXX: Xxxxxxxxxxx xxxxxxxxx xx XX Xxxx X: Xxxxxxxxxxx x odeslané xxxxxxx X.1. Xxxxxxxxxx Xxxxx Xxxxxx Xxx. X.2. Číslo xxxxxxx xxxxxxxxx X.2.x. X.3. Příslušný xxxxxxxx xxxxx X.4. Xxxxxxxxx xxxxxx orgán I.5. Příjemce Název Adresa PSČ Tel. I.6. Xxxxx xxxxxxxxxx xx xxxxxxx x XX Xxxxx Xxxxxx XXX Xxx. X.7. Xxxx xxxxxx Xxx XXX X.8. Xxxxxx xxxxxx Xxx X.9. Xxxx xxxxxx Xxx XXX X.10. Xxxxxx xxxxxx Xxx X.11. Xxxxx původu Název Xxxxx xxxxxxxxx Xxxxxx Xxxxx Xxxxx xxxxxxxxx Xxxxxx Xxxxx Xxxxx schválení Adresa I.12. Xxxxx xxxxxx Xxxxx xxxxx Xxxxx Xxxxx xxxxxxxxx Xxxxxx XXX X.13. Místo xxxxxxxx X.14. Xxxxx xxxxxxx X.15. Xxxxxxxx xxxxxxxxxx Xxxxxxx Plavidlo Xxxxx Xxxxxxxx vozidlo Xxxxxxx Xxxxxxxxxxxx Xxxxx xx dokument I.16. Xxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxx XX X.17. X.18. Popis xxxxx X.19. Xxx zboží (kód XX) X.20. Množství I.21. Teplota xxxxxxxx Xxxxxx Xxxxxxxx Zmrazené I.22. Xxxxx xxxxxx X.23. Xxxxx xxxxxx/xxxxxxxxxx X.24. Xxxx xxxxx  Text obrazu Text obrazu
X.25. Xxxxx xxxxxxxxx xxx: Xxxxxx Xxxxxxxxx xxxxxxx Xxxxxx krmiva xxx xxxxxxx x xxxxxxxx xxxxx X.26. Pro tranzit xxxx XX do xxxxx země Třetí xxxx Xxx ISO I.27. Xxx xxxxx nebo příjem xx EU I.28. Xxxxxxxxxxxx xxxxx Xxxxx xxxxxxxxx xxxxxxxx Xxxx (xxxxxxx xxxxx) Xxxx xxxxx Xxxxxxx xxxxx Xxxxx xxxxxxxx Xxxxx xxxxx  Text obrazu Text obrazu
XXXX Xxxxxxxxxx xxxxxxxxx bílkoviny xxxxxxx x xxxxxxx xxxxxxxxx xxxxx, xxxxx xxxxxx xxxxxx k xxxxxx spotřebě, včetně xxxxx x produktů xxxxxx xxx krmivo xxx xxxxxxx x xxxxxxxx xxxxx xxxxxxxxxxxx xxxx xxxxxxxxx XX. Xxxxxxxxx xxxxxxxxx XX.x. Číslo jednací xxxxxxxxx XX.x. Xx, níže xxxxxxxxx xxxxxx xxxxxxxxxxx xxxxx, xxxxxxxxxx, že jsem xxxxxxx x porozuměl xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Xxxx (XX) x. 1069/2009 (1x), xxxxxxx xxxxx jde x článek 10 xxxxxxxxx xxxxxxxx, a xxxxxxxx Xxxxxx (EU) x. 142/2011 (1b), xxxxxxx xxxxx jde x xxxxxxx X xxxxxxxx XX xxxxx 1 x xxxxxxx XXX xxxxxxxx I xxxxxxxxx xxxxxxxx, x xxxxxxxxx, xx: XX.1. xxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxx x farmově xxxxxxxxx xxxxx xxxx xxxxxxx xxxxxxx xxxx obsahují xxxxxxxx zpracované živočišné xxxxxxxxx, xxxxx xxxxxx xxxxxx k xxxxxx xxxxxxxx a které: a) xxxx xxxxxxxxxx x xxxxxxxxxx x xxxxxxxx xxxx xxxxxxx xxxxxxxxxx x xxxxxxxxxxx příslušným xxxxxxx x souladu x xxxxxxx 24 xxxxxxxx (ES) č. 1069/2009 x x) xxxx xxxxxxxxxx xxxxxxxx x xxxxxxx xxxxxxxxx xxxxx xxxxxx xxxxx: (2) xxx [- bráněnka (Xxxxxxxx xxxxxxxx);] (2) x/xxxx [- xxxxxx xxxxxx (Musca xxxxxxxxx);] (2) x/xxxx [- xxxxxxxx moučný (Tenebrio xxxxxxx);] (2) a/nebo [- xxxxxxxx stájový (Alphitobius xxxxxxxxxx);] (2) a/nebo [- xxxxxx xxxxxx (Xxxxxx xxxxxxxxxx);] (2) x/xxxx [- xxxxxx xxxxxxxxxxxx (Xxxxxxxxx xxxxxxxxxx);] (2) a/nebo [- xxxxxx banánový (Xxxxxxx xxxxxxxxx)] x x) xxxx xxxxxxxxxx x xxxxxxx x xxxxxxx [1]-[2]-[3]-[4]-[5]-[7] (2) xxxxxxxxxx x xxxxxxx XX xxxxxxxx XXX xxxxxxxx (XX) č. 142/2011; x x) xxxxxxxx ke xxxxxx farmově xxxxxxxxx xxxxx xxx xxxxxxxxx xxxxx produkty, které xxxxxx xxxxxxxxxxx xxxxxx, xxxx xxxx xxxxxxxx xxxxxxxxxxx původu xxxxxxxxx xxxxxxxxx 3: — rybí xxxxxx, — xxxxxx xxxxxxx x xxxxxxxxxxxxx, — xxxxxxxxxxxxxxxxxxx xxxxxxxx a fosforečnan xxxxxxxx živočišného původu, — xxxxxxxxxxxxx bílkoviny x xxxxxxxxxxxxx, — hydrolyzované bílkoviny x kůží a xxxxx xxxxxxxxxxx, — xxxxxxxx x xxxxxxx x xxxxxxxxxxxxx, — xxxxx a xxxxxxx x vajec, — xxxxx, xxxxxx výrobky, xxxxxxxx xxxxxxx z xxxxx a xxxxxxx, — xxx, — tavené/škvařené xxxx Xxxx XX: Xxxxxxxxx  Text obrazu Text obrazu
XXXX Xxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxx x farmově xxxxxxxxx xxxxx, které xxxxxx xxxxxx k xxxxxx xxxxxxxx, včetně směsí x xxxxxxxx xxxxxx xxx krmivo pro xxxxxxx x xxxxxxxx xxxxx xxxxxxxxxxxx xxxx xxxxxxxxx XX. Xxxxxxxxx informace II.a. Xxxxx xxxxxxx xxxxxxxxx XX.x. x x) xxxxxxxx ke xxxxxx xxxxx x hmyz xxxx xxxx larvy xxxxxx xx xxxxx x xxxxxx xxxxxxxxx xxxxxxxxxxx xxxxxx než xxxxxxxxx xxxxxxxxx v xxxxxxx x) x xxxxxxxx xxxxxxxxxxx xxxx, xxxxx xx xxxxxxxxxxxx xxxxxxxx xxxx xxxx xxxxx; XX.2. příslušný xxxxx xxxxxxxxxxxxx xxxx xxxxxxxxx xxxxxxxx namátkově xxxxxxx xxxxxx x xxxxxxx xxx x xxxxxxx x těmito xxxxxxx (3): Xxxxxxxxxx: xxxxxxxxxxxx v 25 x produktu: x = 5, x = 0, x = 0, X = 0 Xxxxxxxxxxxxxxxxxx: x = 5, x = 2, x = 10, X = 300 x 1 x; XX.3. xxxxxxx xxxxxx xxxxx xxxxxxxxxxxxx xxxxxxxxxx k xxxxxxxxx xxxxxxxxxxx patogenními xxxxxxx po xxxxxxxx; XX.4. xxxxxxx xxxxxxx byl: (2) xxx [xxxxxxx xx xxxxxx xxxx xxxxxxxxxxxxxxx xxxxx,] (2) xxxx [xxxxxxxxxxx xxxxx ložený x xxxxxxxxxxxx xxxx jiných xxxxxxxxxx prostředcích, xxxxx xxxx xxxx xxxxxxxx xxxxxxxx xxxxxxxxx x xxxxxxxxxxxxxxx,] xxxxx xxxx opatřeny xxxxxxxxx x xxxxxxx „XXXX XXXXXX X XXXXXX XXXXXXXX / XXXXXXXXXX XXXXX BÍLKOVINY – XXXX XXXXXX XXX XXXXXXX V XXXXXXXX XXX HOSPODÁŘSKÁ XXXXXXX KROMĚ ŽIVOČICHŮ XXXXXXXXXXXXX X XXXXXXXXXXX X KOŽEŠINOVÝCH XXXXXX“; XX.5. xxxxxxx xxxxxxx byl xxxxxx x xxxxxxxxx xxxxxxxxx; (2) [XX.6. zpracované xxxxxxxxx bílkoviny xxxx xxxxxxx xxxxxxx xxxx xxxxxxxx vedlejší xxxxxxxx xxxxxxxxxxx xxxxxx z xxxxxxxxxxx nebo xxxx x xxxx získány x: (2) buď [xxxxxxxxx xx xxxx nebo xxxxxxx zařazené x xxxxxxx s xxxxxxxxxxx 2007/453/XX do xxxxxxxxx xxxx nebo xxxxxxx xx zanedbatelným xxxxxxx xxxxxxx XXX, x xxxxx nebyl xxxxxxx xxxxx xxxxxx xxxxxx XXX, x]] (2) xxxx [xxxxxxxxx ze xxxx xxxx oblasti xxxxxxxx x xxxxxxx x xxxxxxxxxxx 2007/453/ES xx xxxxxxxxx xxxx nebo xxxxxxx se zanedbatelným xxxxxxx výskytu XXX, x xxxxx byl xxxxxxx domácí xxxxxx XXX, a xxxxxxxx xxxxxxx živočišného původu xxxx xxxxxxx xxxxxxx xxx xxxxxx xx xxxxxx xxxxxxxxxx xx xxxx, od kterého xxx v xxxxxxx xxxx nebo xxxxxxx xxxxxx xxxxxxx xxxxx xxxxxx xxxxxxxxxxx masokostní xxxxxxx a škvarky xxxxxxxxx x xxxxxxxxxxx, xxx xxxx xxxxxxxxxx x Xxxxxx zdraví xxxxxxxxxxxxx xxxxxxxxx OIE, x]] (2) buď [xxxx xxxxxxx x xxxxxxxxxxx xxxxxx xxx xxxx, xxxx nebo kozy;]] (2) xxxx [xxxx xxxxxxx xx skotu, ovcí xxxx xxx x xxxxxxxxxx xxxx xxxxxxx xxxxxx xxx z xxxx nebyly xxxxxxx: (2) xxx [materiál pocházející xx xxxxx, xxxx x xxx xxxx xxx xxxxxxx xx xxxxxx narozených, xxxxxxxxxxx xxxxxxxxx x poražených x zemi xxxx xxxxxxx xxxxxxxx x xxxxxxx s xxxxxxxxxxx 2007/453/XX do xxxxxxxxx xxxx xxxx oblasti xx xxxxxxxxxxxxx xxxxxxx xxxxxxx XXX;]] (2) nebo [x) xxxxxxxxxxxxx rizikový xxxxxxxx, jak je xxxxxxxxx x xxxx 1 xxxxxxx V xxxxxxxx Evropského xxxxxxxxxx x Rady (XX) x. 999/2001 (4); b) xxxxxxx xxxxxxxx xxxx xxxxxxx z kostí xxxxx, xxxx xxxx xxx x xxxxxxxx xxxxxx xxxxxxxxxx, xxxxxxxxxxx xxxxxxxxx a xxxxxxxxxx x xxxx nebo xxxxxxx xxxxxxxx x xxxxxxx x xxxxxxxxxxx Xxxxxx 2007/453/XX (5) xx xxxxxxxxx xxxx xxxx xxxxxxx xx xxxxxxxxxxxxx xxxxxxx výskytu XXX, x nichž xxxxx  Text obrazu Text obrazu
XXXX Xxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxx x xxxxxxx xxxxxxxxx xxxxx, xxxxx nejsou xxxxxx x lidské xxxxxxxx, xxxxxx xxxxx x xxxxxxxx xxxxxx xxx xxxxxx xxx xxxxxxx x zájmovém xxxxx xxxxxxxxxxxx xxxx xxxxxxxxx XX. Xxxxxxxxx xxxxxxxxx XX.x. Xxxxx xxxxxxx xxxxxxxxx XX.x. x) xxxxxxxx xxxxxxx xxxxxxxxxxx xxxxxx xxxx xxxxxxx xxxxxxx xx xxxxx, xxxx xxxx xxx, xxxxx xxxx xx xxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxx xxxxx xxxxxx xxxxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxxx xx dutiny xxxxxxx xxxx prostřednictvím xxxxxxx xxxxxxx xx xxxxxx xxxxxxx, s xxxxxxxx xxxxxx narozených, xxxxxxxxxxx xxxxxxxxx x xxxxxxxxxx x xxxx xxxx xxxxxxx xxxxxxxx x xxxxxxx x xxxxxxxxxxx 2007/453/XX xx xxxxxxxxx země nebo xxxxxxx xx xxxxxxxxxxxxx xxxxxxx xxxxxxx XXX;]]] XX.7. xxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxx xxxxxxx popsaný xxxx: (2) xxx [neobsahují xxxxx nebo xxxxxx xxxxxxx xxxxxxxxxxx z xxxx nebo xxx xxx xxxxxx xxxxxx xxx krmení xxxxxxxxxxxxx xxxxxx xxxxxx xxx xxxxxxxxxxxx xxxxxx;] (2) xxxx [xxxxxxxx mléko xxxx xxxxxx xxxxxxx xxxxxxxxxxx x xxxx nebo xxx x jsou xxxxxx xxx xxxxxx xxxxxxxxxxxxx zvířat jiných xxx xxxxxxxxxxxx xxxxxx x mléko xxxx xxxxxx výrobky: a) xxxx xxxxxxx z ovcí x xxx, které xxxx nepřetržitě xx xxxxxxxx chovány x xxxx, v xxx xxxx xxxxxxx xxxx xxxxxxxx: x) xxxxxxxx xxxxxxxx xx xxxxxxx xxxxxxxx; xx) xxxxxxx systém osvěty, xxxxxxxxx a xxxxxxx, xxxxx xxx x xxxxxxxxx xxxxxxxx; xxx) xx xxxxxxxxxxxx x chovem xxxx nebo xxx xx xxxxxxxxx xxxxxx xxxxxxx x xxxxxxx xxxxxxxxx xx XXX xxxx xxxxxxxxx xxxxxxxx xxxxxxxx; xx) ovce x xxxx xxxxxxxxx xxxxxxxxx xxxxxxxxx xxxx usmrceny x zlikvidovány; v) xxxxxx xxxx a xxx xxxxxxxxxx moučkou xxxx xxxxxxx z přežvýkavců, xxx xxxx xxxxxxxxxx x Xxxxxx xxxxxx xxxxxxxxxxxxx xxxxxxxxx Světové xxxxxxxxxx xxx xxxxxx xxxxxx (OIE), bylo xxxxxxxx a xxxxx xxx xxxxxx xxxxxxx x xxxx zemi xxxxxxxxxxxx xx dobu xxxxxxxxxxx sedmi xxx; x) xxxxxxxxx x xxxxxxxxxxxx, xxx xxxxx neplatí xxxxx úřední omezení x xxxxxx xxxxxxxxx xx xxxxxx XXX; x) xxxxxxxxx x xxxxxxxxxxxx, x nichž přinejmenším xx xxxx předchozích xxxxx xxx xxxxx xxxxxxxxxxxxxx xxxxx xxxxxx xxxxxxxx klusavky, xxxx xx potvrzení xxxxxxx xxxxxxxx xxxxxxxx: (2) xxx [xxxx usmrceny x xxxxxxxxxxxx xxxx xxxxxxxx xxxxxxx xxxx x xxxx x xxxxxxxxxxxx x výjimkou xxxxxxxxxx xxxxxx xxxxxxxx XXX/XXX, xxxxxxxx xxxxxx xxxxxxxxx xxxxxxx xxxxx xxxxx XXX x žádnou xxxxx XXX x xxxxxxx ovcí xxxxxxxxx xxxxxxx jednu xxxxx XXX;] (2) xxxx [xxxx xxxxxxx xxxxxxx, x xxxxx byla xxxxxxxx xxxxxxxx xxxxxxxxx, xxxxxxxx x xxxxxxxxxxxx x xx xxxxxxxxxxxx xx xxxxxxx xx xxx xxxx od xxxxxxxxx xxxxxxxxxx případu xxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxxxxxx xxxxxxxxx XXX, včetně xxxxxxxxx všech xxxxxxxxxxxxx xxxxxx starších 18 xxxxxx, x výjimkou xxxx xxxxxxxx XXX/XXX, xx xxxxxxxxxx XXX x xxxxxxxxxx výsledkem x souladu x xxxxxxxxxxxxx metodami xxxxxxxxxxx x xxxxxxx X xxxxxxxx C xxxx 3.2 nařízení (XX) x. 999/2001: — xxxxxxx, xxxxx xxxx xxxxxxxx x xxxxxx spotřebě, x — zvířata, xxxxx xxxxxxx xxxx xxxx xxxxxxxx x xxxxx xxxxxxxxxxxx, avšak xxxxxx xxxxxxxx x xxxxx xxxxxxx xxxxxxxxx nákazy;]] II.8. [xxxxxxxxxx živočišné bílkoviny xxxx produkt popsaný xxxx obsahují xxxxxxxx xxxxxxxx živočišného xxxxxx x xxxxxxxxxxxxx nebo xxxx x nich xxxxxxx x x xxxxxxx x xxxxxxxxxxx xxxxxxxxxxx x xxxxxxx X.1.  Text obrazu Text obrazu
XXXX Xxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxx z xxxxxxx chovaného hmyzu, xxxxx xxxxxx xxxxxx x lidské xxxxxxxx, xxxxxx xxxxx a xxxxxxxx xxxxxx xxx xxxxxx pro xxxxxxx x xxxxxxxx xxxxx xxxxxxxxxxxx xxxx bílkoviny II. Xxxxxxxxx xxxxxxxxx XX.x. Xxxxx xxxxxxx xxxxxxxxx XX.x. (2) buď [xxxxxx xxxxxx k xxxxxx xxxxx xxx xxxxxxxxxxx xxxxxxx xxxx xxx xxxxxxxxxx xxxxxxx.] (2) (6) nebo [jsou xxxxxx k xxxxxx xxxxx xxx xxxxxxxxxxxx xxxxxxxxxxx xxxxxxx xxxx xxx xxxxxxxxxx zvířata x odesílatel se xxxxxxx xxxxxxxx, xx xxxxxxxxxx xxxxxxxx xxxxxxxx x xxxxx xxxxxx xx Xxxxxxxx xxxx xxxxx poskytnuty výsledky xxxxxxxx podle metod xxxxxxxxxxx x xxxxxxx XX nařízení Komise (XX) č.152/2009 (7).] Xxxxxxxx Xxxx X: — Xxxxxxx I.6.: Xxxxx zodpovědná za xxxxxxx x Xxxxxxxx xxxx: xxxx kolonku xx třeba xxxxxxx xxxxx xxxxx, xxxxx-xx xx o osvědčení xxx zboží xxxxxx xxx tranzit xxxx Xxxxxxxxx xxxx; xxxx xx xxxxxxx, jedná-li xx x xxxxxxxxx xxx xxxxx xxxxxxxx xx Xxxxxxxx xxxx. — Xxxxxxx X.12.: Xxxxx xxxxxx: tuto xxxxxxx xx xxxxx xxxxxxx xxxxx tehdy, xxxxx-xx xx x osvědčení xxx xxxxx určené xxx tranzit. Xxxxxxxx xxx xxx xxx xxxxxxxx skladovány pouze xx xxxxxxxxxx xxxxxxx, xxxxxxxxxx xxxxxxxx x xxxxxxx xxxxxxxx. — Xxxxxxx X.15.: Xxxxxxxxxxx xxxxx (xxxxxxxxxxxx xxxxxx xxxx xxxxxxxxxx x nákladních xxxxxxxxxx), xxxxx xxxx (xxxxxxx) xxxx xxxxx (xxxxxxxx); informace xx xxxxx poskytnout x xxxxxxx xxxxxxxx a xxxxxxxxxx xxxxxxxx. — Xxxxxxx X.19.: Xxxxxxxx xxxxxxxxx xxx XX: 05.11, 23.01 xxxx 23.09. — Xxxxxxx I.25.: Xxxxxxxxx xxxxxxx: xxxxxxxx jiné xxxxxxx kromě xxxxxx xxxxxxxxxxxxx xxxxxx jiných xxx xxxxxxxxxxxx zvířat x xxxxxx xxxx xxxxxxxxxx xxxxx xxx xxxxxxx x xxxxxxxx xxxxx. — Xxxxxxx X.26. x X.27.: Xxxxxxx xxxxx xxxx, jedná-li xx x xxxxxxxxx xxx xxxxxxx xxxx xxx xxxxx. — Xxxxxxx X.28.: Xxxx: hmyz, xxxxxx xxxxxxx xxxxx. Xxxx XX: (1x) Xx. xxxx. X 300, 14.11.2009, x. 1. (1b) Xx. xxxx. X 54, 26.2.2011, s. 1. (2) Xxxxxxxx se xxxxxxxx. (3) Xxx: x = xxxxx xxxxxx, které xxxx xxx vyšetřeny; m = xxxxxxx hodnota xxxxx xxxxxxxx; xxxxxxxx xx xxxxxxxxx za uspokojivý, xxxxxxxx počet xxxxxxxx xx xxxxx vzorcích xxxxxxxxxx m; M = xxxxxxxxx hodnota xxxxx xxxxxxxx; xxxxxxxx xx xxxxxxxxx xx neuspokojivý, xxxxx xxxxx bakterií x jednom xxxx xxxx vzorcích xx xxxxx nebo vyšší xxx X; x x = xxxxx xxxxxx, xxxxxxx bakteriální počet xxx xxx v xxxxxxx mezi m x M, xxxxxxx xxxxxx xx ještě xxxxx xxxxxxxxx za xxxxxxxxx, pokud xx xxxxxxxxxxx xxxxx xxxxxxxxx xxxxxx xxxxx x xxxx nižší. (4) Úř. xxxx. L 147, 31.5.2001, x. 1. (5) Xx. xxxx. X 172, 30.6.2007, x. 84.  Text obrazu Text obrazu
XXXX Xxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxx x xxxxxxx xxxxxxxxx xxxxx, xxxxx xxxxxx xxxxxx x xxxxxx spotřebě, xxxxxx směsí x xxxxxxxx xxxxxx xxx xxxxxx xxx xxxxxxx x xxxxxxxx xxxxx xxxxxxxxxxxx xxxx xxxxxxxxx XX. Xxxxxxxxx xxxxxxxxx XX.x. Xxxxx xxxxxxx xxxxxxxxx XX.x. (6) Osoba xxxxxxxxxx xx xxxxxxx xxxxxxx x xxxxxxx X.6. xxxx xxxxxxxx, xxx x případě, xx zpracované živočišné xxxxxxxxx xxxx xxxxxxx xxxxxxx x tomto xxxxxxxxxxxx xxxxxxxxx xxxx xxx určeny x xxxxxx xxxxxx pro xxxxxxxxxxxx hospodářská zvířata xxxx než xxxxxxxxxx xxxxxxx, xxxx xxxxxxx xxxxxxxxx xxxxxxxx xxxxx xxxxx xxxxxxxxxxx v xxxxxxx XX xxxxxxxx (XX) x. 152/2009, xxx xx ověřila xxxxxxxxxxxx xxxxxxxxxxxx xxxxxx xxxxxxxxxxx xxxxxx. Xxxxxxxxx xxxxxxxx se xxxxxxxx xxxxxxxx xxxxxxxx musí xxx xxx předložení xxxxxxx na xxxxxxxxxx xxxxxxxx xxxxxxxx XX xxxxxxxxx k xxxxxx xxxxxxxxxxxxx xxxxxxxxx. (7) Xx. xxxx. X 54, 26.2.2009, x. 1. — Xxxxx xxxxxxx a xxxxxxx xx xxxx xxxxx od xxxxx xxxxx. — Xxxxxxxx xxx xxxxx xxxxxxxxxxx xx xxxxxxx v Xxxxxxxx xxxx: toto xxxxxxxxx xxxxxx xxxxx x xxxxxxxxxxxx xxxxxx x xxxx xxxxxxx provázet xx xx xxxxxxxx, xxx dosáhne xxxxxxxxxx xxxxxxxx xxxxxxxx. Xxxxxx xxxxxxxxxxx xxxxx / úřední xxxxxxxxx Xxxxx (xxxxxxxx xxxxxx): Xxxxxxxxxxx a titul: Datum: Xxxxxx: Xxxxxxx: XXXXXXXX 2 (A) Veterinární xxxxxxxxx xxx xxxxx, xxxxxx xxxxxxx x xxxxxxxx xxxxxxx x xxxxx, xxxxx nejsou xxxxxx x xxxxxx spotřebě, xxxxxx x xxxxxxxx xx Xxxxxxxx xxxx xxxx k tranzitu xxxx její území (2) &xxxx; Text obrazu Text obrazu
XXXX: Xxxxxxxxxxx osvědčení xx XX Xxxx I: Xxxxxxxxxxx x xxxxxxxx xxxxxxx X.1. Xxxxxxxxxx Xxxxx Xxxxxx Xxx. X.2. Číslo xxxxxxx osvědčení I.2.a. I.3. Xxxxxxxxx xxxxxxxx xxxxx X.4. Xxxxxxxxx xxxxxx xxxxx X.5. Příjemce Název Adresa PSČ Tel. I.6. Xxxxx xxxxxxxxxx xx xxxxxxx x XX Xxxxx Xxxxxx XXX Xxx. X.7. Xxxx xxxxxx Xxx ISO I.8. Xxxxxx xxxxxx Xxx X.9. Xxxx xxxxxx Xxx XXX X.10. Xxxxxx xxxxxx Xxx X.11. Xxxxx xxxxxx Xxxxx Xxxxx xxxxxxxxx Xxxxxx Xxxxx Xxxxx xxxxxxxxx Xxxxxx Xxxxx Xxxxx xxxxxxxxx Xxxxxx X.12. Xxxxx xxxxxx Xxxxx xxxxx Xxxxx Xxxxx xxxxxxxxx Xxxxxx XXX X.13. Xxxxx xxxxxxxx X.14. Xxxxx odjezdu I.15. Xxxxxxxx xxxxxxxxxx Xxxxxxx Xxxxxxxx Xxxxx Xxxxxxxx vozidlo Xxxxxxx Xxxxxxxxxxxx Xxxxx xx xxxxxxxx X.16. Xxxxxxx xxxxxxxxxx hraniční kontroly XX X.17. Číslo/čísla CITES I.18. Xxxxx xxxxx X.19. Xxx xxxxx (kód HS) I.20. Xxxxxxxx X.21. Xxxxxxx produktů Okolní Xxxxxxxx Xxxxxxxx X.22. Xxxxx xxxxxx X.23. Číslo xxxxxx/xxxxxxxxxx X.24. Xxxx xxxxx  Text obrazu Text obrazu
I.25. Xxxxx xxxxxxxxx xxx: Xxxxxx Xxxxx zpracování Xxxxxx xxxxxx xxx xxxxxxx x xxxxxxxx xxxxx Xxxxxxxxx xxxxxxx X.26. Xxx xxxxxxx xxxx XX xx xxxxx xxxx Xxxxx xxxx Xxx ISO I.27. Pro xxxxx nebo příjem xx EU I.28. Xxxxxxxxxxxx xxxxx Xxxxx schválení xxxxxxxx Xxxx (xxxxxxx xxxxx) Xxxxxxx xxxxx Xxxxx xxxxxxxx Xxxxx xxxxx  Text obrazu Text obrazu
XXXX Xxxxx, xxxxxx výrobky a xxxxxxxx xxxxxxx z xxxxx, xxxxx xxxxxx xxxxxx x xxxxxx xxxxxxxx XX. Zdravotní xxxxxxxxx XX.x. Xxxxx xxxxxxx osvědčení II.b. Já, xxxx podepsaný xxxxxx xxxxxxxxxxx xxxxx, xxxxxxxxxx, xx xxxx přečetl x xxxxxxxxx nařízení Xxxxxxxxxx xxxxxxxxxx x Xxxx (ES) č. 1069/2009 (1x), xxxxxxx xxxxx xxx x xxxxxx 10 xxxxxxxxx xxxxxxxx, a nařízení Xxxxxx (XX) č. 142/2011 (1b), xxxxxxx xxxxx jde x xxxxxxx X xxxxxxxx XX oddíl 4 x xxxxxxx XIV xxxxxxxx X xxxxxxxxx xxxxxxxx, a potvrzuji, xx mléko (2), xxxxxx výrobky (2) x xxxxxxxx xxxxxxx x mléka (2) xxxxxxx x kolonce X.28. xxxxxxx xxxxxxxxxxx xxxxxxxx: XX.1. byly vyrobeny x xxxxxxx x (xxxxxx xxxxx xxxxxxxxxxxxxx) (3), (xxxxxx xxxxx xxxxxxx)&xxxx;(3), xxxxx je xxxxxxx x příloze XX části I xxxxxxxx Xxxxxx (XX) x. 605/2010 (4) x byla 12 xxxxxx xxxxxxxxxxxxx xxxx xxxxxxx xxxxxx xxxxxxxxx x xxxxxxxx x xxxx xxxxx x x průběhu xxxxxxxxx xxxxxx xxx xxxxxxxxxx xxxxxxxx xxxxx moru xxxxx; XX.2. xxxx xxxxxxxx xx syrového xxxxx xxxxxxxxx xx xxxxxx, xxxxx v xxxx xxxxxx nevykazovala xxxxx xxxxxxxx xxxxxxxx onemocnění xxxxxxxxxx mlékem xx xxxxxxx xxxx xxxxxxx x xxxxx xxxx xx xxxx nejméně 30 dnů xxxx xxxxxxx xxxxxx x xxxxxxxxxxxxxx, která nebyla xxxxxxxxx úředních xxxxxxx x xxxxxx xxxxxxxxx x xxxxxxxx xxxx xxxx xxxxx; XX.3. xxxxx xx o mléko xxxx xxxxxx xxxxxxx, xxxxx: (2) xxx [xxxx xxxxxxxx jedním xx xxxxxxx xxxxxxxxx v xxxx II.4. nebo xxxxxx xxxxxxxxx;] (2) xxxx [xxxxxxxx xxxxxxxxx xxxxxxx xx xxxxxx xxxxxx xxxxx xxxxxxxxx ke xxxxxxxxx a kulhavce, xxxxxxx xxxx xxxxxxxxx xxxx xxxxxxxx x xxxxx, které xxxx xxxxxxxx xxxxxx xx xxxxxxx xxxxxxxxx x xxxx XX.4., x: (2) xxx [byla odebrána xxxxxxxx 16 xxxxx xx sražení mléka x má pH xxxxx než 6;] (2) (5) xxxx [xxxx xxxxxxxx nejméně 21 xxx před xxxxxxxxx x během xxxx xxxx xxxxx ve xxxxxxxxxx zemi xxxxxxx xxxxx xxxxxx xxxxxxxxx x xxxxxxxx;] (2) (5) xxxx [byla xxxxxxxx xxx / / , xxxxxxx xxxx xxxxx, x xxxxxxx xx xxxxxxxxxxxxxx xxxx xxxxxxxx, xxxxxxxx době xxxxxxx 21 xxx xxxx xxxxx, xxx xx xxxxxxx xxxxxxxxxx xx stanovišti hraniční xxxxxxxx Xxxxxxxx xxxx;]] XX.4. xxxx xxxxxxxx jedním x následujících způsobů: (2) xxx [xxxxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxxxx xxx xxxxxxx 72 °C xxxxxxxx xxxxxxx 15 xxxxxx xxxx ošetřením x xxxxxxxxxxx pasterizačním xxxxxxx, xxxxxx xx dosaženo xxxxxxxxx xxxxxx xx xxxxxxxxxxx test u xxxxxxxxx mléka, v xxxxxxxxx x: (2) xxx [xxxxxxxxx další krátkodobou xxxxxxxxxxxxxx xxxxxxxxxxx při xxxxxxx 72 °X xxxxxxxx xxxxxxx 15 xxxxxx xxxx ošetřením x xxxxxxxxxxx xxxxxxxxxxxxx xxxxxxx, xxxxxx xx xxxx o xxxx xxxxxxxx xxxxxxxxx xxxxxx xx fosfatázový xxxx x xxxxxxxxx xxxxx;] (2) xxxx [xxxxxxxxx xxxxxxxx xxxxxx, v případě xxxxx xxxxxxxx xx xxxxxx x xxxxxxxxx x xxxxxxxxxx xxxxxxxx xxxxxxx na 72 °X;] (2) nebo [xxxxxxxxx xxxxxxxx, při xxxxxx xx xX xxxxxxx x xxxxxxx jednu xxxxxx xxxxxxxxx xxx xxxxxxx 6;] (2) (5) xxxx [xxxxxxxxx, xx xxxxx / xxxxxx xxxxxxx byl(o) vyroben(o) xxxxxxx 21 dní xxxx datem odeslání x xx xxxxx xxxx doby xxxxx xx vyvážející xxxx xxxxxxx xxxxx případ xxxxxxxxx a xxxxxxxx;] (2) (5) xxxx [xxxxx / xxxxxx výrobek xxx(x) vyroben(o) dne …/…/…(xxxxxx datum), přičemž xxxx xxxxx, s xxxxxxx xx předpokládanou xxxx xxxxxxxx, odpovídá xxxx xxxxxxx 21 xxx xxxx datem, xxx je xxxxxxx xxxxxxxxxx xx xxxxxxxxxx xxxxxxxx xxxxxxxx Xxxxxxxx xxxx;] (2) nebo [xxxxxxxxxxx xxxxxxxxxxxx xx xxxxxxx X03;]] Xxxx XX: Osvědčení  Text obrazu Text obrazu
XXXX Xxxxx, xxxxxx xxxxxxx x xxxxxxxx xxxxxxx x mléka, které xxxxxx xxxxxx x xxxxxx xxxxxxxx XX. Zdravotní xxxxxxxxx XX.x. Číslo xxxxxxx xxxxxxxxx XX.x. (2) nebo [xxxxxxxxx xxxxxxxxxxxx xxxxxxxx xxx 132 °C xxxxxxxxx xxxxxxx xxxxx sekundu x xxxxxxxxx x: (2) xxx [následným xxxxxxxx xxxxxx, x xxxxxxx xxxxx xxxxxxxx xx xxxxxx x xxxxxxxxx x doplňkovým xxxxxxxx xxxxxxx xx 72 °X;] (2) xxxx [xxxxxxxxx xxxxxxxx, při xxxxxx xx xX xxxxxxx x alespoň xxxxx xxxxxx xxxxxxxxx xxx xxxxxxx 6;] (2) (5) xxxx [xxxxxxxxx, xx xxxxx / xxxxxx xxxxxxx byl(o) xxxxxxx(x) xxxxxxx 21 dní xxxx datem xxxxxxxx x xx xxxxx xxxx xxxx nebyl xx xxxxxxxxxx zemi xxxxxxx xxxxx xxxxxx xxxxxxxxx x xxxxxxxx;] (2) (5) xxxx [xxxxx / xxxxxx xxxxxxx xxx(x) xxxxxxx(x) xxx …/…/…(xxxxxx xxxxx), xxxxxxx xxxx xxxxx, x xxxxxxx xx xxxxxxxxxxxxxx xxxx xxxxxxxx, odpovídá xxxx xxxxxxx 21 xxx před datem, xxx xx xxxxxxx xxxxxxxxxx xx xxxxxxxxxx xxxxxxxx xxxxxxxx Xxxxxxxx xxxx;]] XX.5. byla uplatněna xxxxxxx preventivní xxxxxxxx x zabránění kontaminace xxxxx / xxxxxxxx xxxxxxx / produktu xxxxxxxxx x xxxxx xx xxxxxxxxxx; XX.6. mléko / xxxxxx xxxxxxx / produkt získaný x mléka byl(o) xxxxxxx(x): (2) xxx [do xxxxxx xxxxx;] (2) xxxx [xx vozidlech xxxx xxxxxxxxxxxx xxx volně xxxxxx xxxxx, xxxxx xxxx xxxx xxxxxxxxx xxxxxxxxxxxxxxx xxxxxxxxxxxx prostředkem xxxxxxxxxx příslušným xxxxxxx;] x xxxxxx x kontejnery xxxx xxxxxxxx způsobem, xxxxx xxxxxxxx charakter xxxxx / xxxxxxxx xxxxxxx / xxxxxxxx xxxxxxxxx x xxxxx, x xxxx opatřeny xxxxxxxxx xxxxxxxxxxx, xx xx xxxxx x xxxxxxxx kategorie 3, xxxxx xxxx xxxxx x xxxxxx xxxxxxxx; XX.7. xxxx xxxxxxx xxxxx, xxxxxx výrobky a xxxxxxxx získané z xxxxx: (2) xxx [neobsahují xxxxx nebo xxxxxx xxxxxxx xxxxxxxxxxx x xxxx xxxx xxx xxx xxxxxx xxxxxx xxx krmení xxxxxxxxxxxxx xxxxxx jiných xxx xxxxxxxxxxxx xxxxxx.] (2) xxxx [xxxxxxxx xxxxx nebo xxxxxx xxxxxxx pocházející x xxxx xxxx xxx x jsou xxxxxx xxx xxxxxx xxxxxxxxxxxxx zvířat xxxxxx xxx xxxxxxxxxxxx xxxxxx x mléko xxxx xxxxxx xxxxxxx: x) xxxx xxxxxxx z xxxx x xxx, xxxxx xxxx nepřetržitě od xxxxxxxx xxxxxxx v xxxx, x xxx xxxx xxxxxxx tyto xxxxxxxx: x) klasická xxxxxxxx xx xxxxxxx xxxxxxxx; xx) xxxxxxx xxxxxx osvěty, xxxxxxxxx x xxxxxxx, xxxxx xxx x xxxxxxxxx klusavku; iii) na xxxxxxxxxxxx x xxxxxx xxxx nebo xxx xx xxxxxxxxx xxxxxx xxxxxxx x xxxxxxx xxxxxxxxx xx XXX xxxx xxxxxxxxx xxxxxxxx xxxxxxxx; xx) xxxx a xxxx xxxxxxxxx xxxxxxxxx xxxxxxxxx jsou xxxxxxxx x xxxxxxxxxxxx; x) xxxxxx xxxx a koz xxxxxxxxxx xxxxxxx xxxx xxxxxxx z přežvýkavců, xxx xxxx xxxxxxxxxx x Xxxxxx xxxxxx xxxxxxxxxxxxx xxxxxxxxx Světové xxxxxxxxxx xxx xxxxxx xxxxxx (XXX), xxxx xxxxxxxx x zákaz xxx účinně xxxxxxx x xxxx zemi xxxxxxxxxxxx xx xxxx xxxxxxxxxxx sedmi xxx; x) xxxxxxxxx x hospodářství, xxx která xxxxxxx xxxxx xxxxxx xxxxxxx x xxxxxx podezření xx xxxxxx XXX;  Text obrazu Text obrazu
XXXX Xxxxx, xxxxxx xxxxxxx x produkty xxxxxxx x xxxxx, které xxxxxx určeny x xxxxxx spotřebě II. Xxxxxxxxx xxxxxxxxx XX.x. Xxxxx jednací xxxxxxxxx XX.x. x) xxxxxxxxx x xxxxxxxxxxxx, v xxxxx xxxxxxxxxxxx xx xxxx xxxxxxxxxxx sedmi xxx xxxxx xxxxxxxxxxxxxx žádný xxxxxx klasické klusavky, xxxx xx xxxxxxxxx xxxxxxx klasické xxxxxxxx: (2) xxx [byly usmrceny x zlikvidovány xxxx xxxxxxxx xxxxxxx xxxx x xxxx x xxxxxxxxxxxx s výjimkou xxxxxxxxxx xxxxxx xxxxxxxx XXX/XXX, chovných bahnic xxxxxxxxx xxxxxxx jednu xxxxx ARR x xxxxxx xxxxx XXX x xxxxxxx ovcí xxxxxxxxx xxxxxxx jednu xxxxx XXX;] (2) xxxx [xxxx xxxxxxx zvířata, x xxxxx byla xxxxxxxx klusavka potvrzena, xxxxxxxx x zlikvidována x xx xxxxxxxxxxxx xx alespoň po xxx xxxx xx xxxxxxxxx xxxxxxxxxx xxxxxxx xxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxxxxxx sledování XXX, xxxxxx xxxxxxxxx všech xxxxxxxxxxxxx zvířat xxxxxxxx 18 xxxxxx, s xxxxxxxx xxxx xxxxxxxx XXX/XXX, xx xxxxxxxxxx XXX s xxxxxxxxxx xxxxxxxxx v souladu x xxxxxxxxxxxxx xxxxxxxx xxxxxxxxxxx x příloze X xxxxxxxx C xxxx 3.2 xxxxxxxx (XX) x.999/2001 (6): — xxxxxxx, xxxxx xxxx xxxxxxxx x xxxxxx xxxxxxxx, a — zvířata, xxxxx xxxxxxx nebo xxxx xxxxxxxx v xxxxx xxxxxxxxxxxx, avšak xxxxxx xxxxxxxx x xxxxx xxxxxxx xxxxxxxxx xxxxxx.]] Xxxxxxxx Xxxx X: — Kolonka X.6.: Osoba xxxxxxxxxx xx xxxxxxx v Xxxxxxxx unii: tuto xxxxxxx je třeba xxxxxxx xxxxx xxxxx, xxxxx-xx se o xxxxxxxxx xxx xxxxx xxxxxx pro xxxxxxx xxxx Evropskou xxxx; xxxx se xxxxxxx, xxxxx-xx se x xxxxxxxxx pro xxxxx xxxxxxxx xx Xxxxxxxx xxxx. — Kolonka X.12.: Xxxxx určení: xxxx xxxxxxx xx xxxxx xxxxxxx pouze xxxxx, xxxxx-xx xx x xxxxxxxxx pro xxxxx xxxxxx pro tranzit. — Xxxxxxx X.15.: Xx xxxxx xxxxx xxxxxxxxxxx xxxxx (vagony nebo xxxxxxxxxx x xxxxxxxx xxxxxxxxxx), xxxxx xxxx (xxxxxxx) xxxx název (xxxxxxxx). X případě xxxxxxxx a opětovného xxxxxxxx xxxx odesílatel xxxxxxxxxx xxxxxxxxxx hraniční xxxxxxxx Xxxxxxxx unie. — Xxxxxxx X.19.: xxxxxxxx xxxxxxxxx xxx xxxxxxxxxxxxxxx xxxxxxx (XX) Xxxxxxx xxxxx xxxxxxxxxx: 04.01, 04.02, 04.03, 04.04, 23.09.10, 23.09.90, 35.01, 35.02 xxxx 35.04. — Xxxxxxx I.23.: X xxxxxxx kontejnerů pro xxxxx ložené látky xxxx xxx uvedeno xxxxx xxxxxxxxxx x (xxxxxxxx) xxxxx plomby. — Xxxxxxx I.25.: Xxxxxxxxx xxxxxxx: jakékoli xxxx xxxxxxx xxxxx xxxxxx xxxxxxxxxxxxx xxxxxx jiných xxx xxxxxxxxxxxx xxxxxx x xxxxxx xxxx xxxxxxxxxx krmiv xxx xxxxxxx x xxxxxxxx xxxxx. — Kolonky I.26. x X.27.: Xxxxxxx xxxxx toho, xxxxx-xx xx x xxxxxxxxx xxx xxxxxxx xxxx xxx xxxxx. — Xxxxxxx X.28.: Xxxxxxx závod: xxxxxxx xxxxx xxxxxxxxxx xxxxxxxx, v xxxx xxxxxxxx xxxxxxxx xxxx xxxxxxxxxx. Xxxx XX: (1x) Xx. xxxx. X 300, 14.11.2009, s. 1. (1b) Xx. xxxx. L 54, 26.2.2011, x. 1.  Text obrazu Text obrazu
ZEMĚ Mléko, xxxxxx xxxxxxx a produkty xxxxxxx x mléka, xxxxx xxxxxx určeny x lidské xxxxxxxx XX. Xxxxxxxxx informace II.a. Xxxxx xxxxxxx xxxxxxxxx XX.x. (2) Nehodící xx xxxxxxxx. (3) Xxxxxxx, xxxxx xx xxxxxxxxx x dovozu xx Xxxxxxxx xxxx xxxx x xxxxxxxx xxxx Xxxxxxxxx xxxx xxxxxxx xx xxxxxx xxxxxxx xxxxxxx xxxxx xxxx. (4) Xx. xxxx. X 175, 10.7.2010, x. 1. (5) Xxxx podmínka xxxxx pouze xxx xxxxx xxxx xxxxxxx x xxxxxxx X xxxxxxx X xxxxxxxx (XX) x. 605/2010. (6) Xx. xxxx. X 147, 31.5.2001, s. 1. — Xxxxx podpisu x xxxxxxx se xxxx lišit xx xxxxx tisku. — Poznámka xxx xxxxx xxxxxxxxxxx xx xxxxxxx v Xxxxxxxx xxxx: xxxx xxxxxxxxx slouží xxxxx x xxxxxxxxxxxx účelům x xxxx zásilku xxxxxxxx xx xx xxxxxxxx, xxx xxxxxxx xxxxxxxxxx hraniční xxxxxxxx. Xxxxxx xxxxxxxxxxx xxxxx / xxxxxx inspektor Jméno (xxxxxxxx xxxxxx): Xxxxxxxxxxx a xxxxx: Xxxxx: Xxxxxx: Xxxxxxx: XXXXXXXX 2 (X) Xxxxxxxxxxx osvědčení pro xxxxxxx x xxxxxxx x xxxxxxx xxxxx, xxxxx xxxxxx xxxxxx x xxxxxx xxxxxxxx, určené x odeslání xx Xxxxxxxx xxxx nebo x xxxxxxxx přes xxxx xxxxx (2) &xxxx; Text obrazu Text obrazu
XXXX: Xxxxxxxxxxx osvědčení xx XX Xxxx X: Xxxxxxxxxxx x xxxxxxxx xxxxxxx X.1. Xxxxxxxxxx Xxxxx Xxxxxx Xxx. X.2. Xxxxx jednací xxxxxxxxx X.2.x. X.3. Xxxxxxxxx xxxxxxxx xxxxx X.4. Xxxxxxxxx xxxxxx xxxxx X.5. Xxxxxxxx Xxxxx Xxxxxx XXX Xxx. X.6. Xxxxx xxxxxxxxxx xx zásilku x XX Xxxxx Xxxxxx XXX Xxx. X.7. Země xxxxxx Xxx XXX X.8. Region xxxxxx Xxx X.9. Xxxx určení Kód XXX X.10. Region xxxxxx Xxx X.11. Xxxxx xxxxxx Xxxxx Xxxxx xxxxxxxxx Xxxxxx Xxxxx Xxxxx xxxxxxxxx Xxxxxx Xxxxx Xxxxx xxxxxxxxx Xxxxxx X.12. Místo xxxxxx Xxxxx xxxxx Xxxxx Číslo xxxxxxxxx Xxxxxx XXX X.13. Místo xxxxxxxx X.14. Xxxxx xxxxxxx X.15. Dopravní xxxxxxxxxx Xxxxxxx Plavidlo Xxxxx Xxxxxxxx xxxxxxx Ostatní Identifikace Odkaz xx xxxxxxxx X.16. Xxxxxxx stanoviště xxxxxxxx kontroly EU I.17. Xxxxx/xxxxx CITES I.18. Popis xxxxx X.19. Kód xxxxx (xxx XX) X.20. Xxxxxxxx X.21. Xxxxxxx xxxxxxxx Xxxxxx Xxxxxxxx Xxxxxxxx X.22. Xxxxx xxxxxx X.23. Xxxxx plomby/kontejneru I.24. Druh xxxxx  Text obrazu Text obrazu
X.25. Xxxxx xxxxxxxxx xxx: Xxxxxx Xxxxx xxxxxxxxxx Xxxxxx xxxxxx xxx xxxxxxx x xxxxxxxx xxxxx Xxxxxxxxx xxxxxxx X.26. Xxx xxxxxxx xxxx XX do xxxxx xxxx Xxxxx xxxx Kód XXX X.27. Xxx xxxxx xxxx xxxxxx xx XX X.28. Xxxxxxxxxxxx xxxxx Xxxxx xxxxxxxxx xxxxxxxx Xxxx (xxxxxxx xxxxx) Xxxxxxx xxxxx Xxxxx hmotnost Číslo xxxxx  Text obrazu Text obrazu
XXXX Xxxxxxx a xxxxxxx x xxxxxxx xxxxx, xxxxx nejsou xxxxxx k lidské xxxxxxxx XX. Xxxxxxxxx informace II.a. Xxxxx jednací xxxxxxxxx XX.x. Xx, xxxx xxxxxxxxx úřední xxxxxxxxxxx xxxxx, prohlašuji, xx xxxx xxxxxxx x xxxxxxxxx nařízení Xxxxxxxxxx parlamentu x Xxxx (ES) x. 1069/2009 (1x), xxxxxxx xxxxx jde x xxxxxx 10 xxxxxxxxx xxxxxxxx, x nařízení Xxxxxx (EU) x. 142/2011 (1x), xxxxxxx xxxxx jde x xxxxxxx X xxxxxxxx XX oddíl 4 x přílohu XXX xxxxxxxx X xxxxxxxxx xxxxxxxx, x xxxxxxxxx, xx xxxxxxx (2) xxxx xxxxxxx z xxxxxxx (2) uvedené x xxxxxxx I.28. xxxxxxx xxxxxxxxxxx podmínky: II.1. xxxx xxxxxxxx a xxxxxxx v (xxxxxx xxxxx xxxxxxxxxx xxxx) (3), (xxxxxx xxxxx xxxxxxx) (3), která xx xxxxxxx x xxxxxxx X nařízení Xxxxxx (EU) x. 605/2010 (4) x xxxx 12 měsíců xxxxxxxxxxxxx před xxxxxxx xxxxxx slintavky a xxxxxxxx x xxxx xxxxx a x xxxxxxx uvedeného xxxxxx xxx xxxxxxxxxx očkování xxxxx xxxx xxxxx; XX.2. xxxx xxxxxxxx x xxxxxxx získaného xx xxxxxx, xxxxx v xxxx dojení xxxxxxxxxxxx xxxxx xxxxxxxx xxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxxxxx xx člověka xxxx xxxxxxx x xxxxx xxxx xx xxxx xxxxxxx 30 dnů xxxx datem xxxxxx xxxxxx x hospodářstvích, xxxxx nebyla xxxxxxxxx xxxxxxxx xxxxxxx x xxxxxx slintavky a xxxxxxxx nebo moru xxxxx; XX.3. xxxxx se x xxxxxxx xxxx xxxxxxx x mleziva xxxxx, které xxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx pasterizací xxx xxxxxxx 72 °X xxxxxxxx xxxxxxx 15 xxxxxx nebo xxxxxxxxx x xxxxxxxxxxx xxxxxxxxxxxxx xxxxxxx, xxxxxx xx xxxxxxxx xxxxxxxxx xxxxxx xx fosfatázový xxxx x xxxxxxx xxxxx, v kombinaci x: (2) (5) xxx [xxxxxxxxx, xx mlezivo xxxx xxxxxxx x xxxxxxx xxxx xxxxxxxx xxxxx doby xxxxxxx 21 xxx xxxx xxxxx odeslání x xx během této xxxx xxxxx xx xxxxxxxxxx xxxx xxxxxxx xxxxx xxxxxx xxxxxxxxx x xxxxxxxx; ] (2) (5) xxxx [xxxxxxxxx, xx xxxxxxx xxxx xxxxxxx z xxxxxxx xxxx vyrobeny xxx …/ /…(vložte xxxxx), xxxxxxx xxxx datum, x ohledem xx xxxxxxxxxxxxxx xxxx xxxxxxxx, xxxxxxxx xxxx xxxxxxx 21 xxx xxxx xxxxx, xxx xx xxxxxxx xxxxxxxxxx xx xxxxxxxxxx hraniční xxxxxxxx Xxxxxxxx unie;] a xxxx xxxxxxx xx xxxxxx, x xxxxx xx xxxxxxxxx xxxxxxxxxx xxxxxxxxxxx xxxxxxxx, aby xxxx xxxxxxxxx, xx xxxxxxxxx x xxxxxxxxxxxx, v xxxxx xxxx xxxxxxx xxxxx skotu: (2) (5) xxx [xxxxxx xx xxxxxx xxxxxx xxxxxxxxxxx x xxxxxxxxx (6);] (2) (5) xxxx [xxxxxxxxxxxxx xxxxx xxxxxxxxxxxxxx právních xxxxxxx xxxxx xxxx xxxxxx omezením v xxxxxxxxxxx x eradikací xxxxxxxxxxx a xxxxxxxxx;] x (2) (5) xxx [xxxxxx za xxxxxx xxxxxx xxxxxxxxxx leukózy xxxxx (6);] (2) (5) xxxx [xxxxxxxx xx xxxxxxxx xxxxxxx pro xxxxxxx xxxxxxxxxx xxxxxxx xxxxx a xxxxx xxxx xxxxxxxxxxx xxxx xxx x xxxx xxxxxxxx a xxxxxxxxxxx xxxxxxxxx xxxxxxxxxxx xxxxxx xxxx nákazy;]] II.4. xxxx xxxxxxxxx xxxxxxx preventivní xxxxxxxx x xxxxxxxxx xxxxxxxxxxx xxxxxxx / xxxxxxx z xxxxxxx xx xxxxxxxxxx; XX.5. xxxxxxx / xxxxxxx z xxxxxxx xxx(x) zabalen(o): (2) xxx [xx nových xxxxx,] (2) nebo [ve xxxxxxxxx xxxx xxxxxxxxxxxx xxx xxxxx xxxxxx xxxxx, které xxxx xxxx xxxxxxxxx xxxxxxxxxxxxxxx xxxxxxxxxxxx xxxxxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxxxx] x xxxxxx x xxxxxxxxxx jsou xxxxxxxx způsobem, xxxxx xxxxxxxx xxxxxxxxx xxxxxxx / výrobku x xxxxxxx, x jsou xxxxxxxx etiketami xxxxxxxxxxx, xx xx xxxxx x xxxxxxxx xxxxxxxxx 3, xxxxx není xxxxx x lidské xxxxxxxx; XX.6. xxxxxxx xxxx xxxxxxx x xxxxxxx xxxxxxxxxx xxxxx xxxx xxxxxx výrobky pocházející x xxxx xxxx xxx. Xxxxxxxx Xxxx X: — Xxxxxxx X.6.: Osoba zodpovědná xx xxxxxxx x Xxxxxxxx xxxx: xxxx xxxxxxx xx xxxxx xxxxxxx pouze xxxxx, xxxxx-xx xx o xxxxxxxxx pro zboží xxxxxx xxx tranzit xxxx Evropskou xxxx; xxxx xx vyplnit, xxxxx-xx se x xxxxxxxxx xxx xxxxx xxxxxxxx xx Evropské xxxx. Xxxx II: Xxxxxxxxx  Text obrazu Text obrazu
XXXX Xxxxxxx a výrobky x xxxxxxx xxxxx, xxxxx xxxxxx xxxxxx x xxxxxx xxxxxxxx XX. Xxxxxxxxx xxxxxxxxx XX.x. Xxxxx xxxxxxx xxxxxxxxx XX.x. — Xxxxxxx X.12.: Xxxxx určení: xxxx xxxxxxx xx xxxxx xxxxxxx pouze xxxxx, jedná-li xx x xxxxxxxxx xxx xxxxx xxxxxx xxx xxxxxxx. — Xxxxxxx X.15.: Xx xxxxx xxxxx xxxxxxxxxxx xxxxx (xxxxxx xxxx kontejnery a xxxxxxxx xxxxxxxxxx), xxxxx xxxx (xxxxxxx) nebo xxxxx (plavidlo). X xxxxxxx vykládky a xxxxxxxxxx naložení x Xxxxxxxx unii xxxx xxxxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxx Xxxxxxxx xxxx. — Xxxxxxx I.19.: xxxxxxxx příslušný kód xxxxxxxxxxxxxxx systému (XX) Xxxxxxx celní organizace: 04.04.90, 23.09.10, 23.09.90, 35.01, 35.02 xxxx 35.04. — Xxxxxxx X.23.: X případě xxxxxxxxxx xxx xxxxx xxxxxx xxxxx musí xxx xxxxxxx číslo xxxxxxxxxx x (xxxxxxxx) xxxxx xxxxxx. — Kolonka X.25.: Xxxxxxxxx využití: xxxxxxxx xxxx xxxxxxx xxxxx xxxxxx hospodářských zvířat xxxxxx xxx kožešinových xxxxxx a výroba xxxx xxxxxxxxxx krmiv xxx xxxxxxx v xxxxxxxx xxxxx. — Kolonky X.26. x X.27.: Xxxxxxx xxxxx xxxx, xxxxx-xx xx o xxxxxxxxx pro xxxxxxx xxxx xxx dovoz. — Xxxxxxx X.28.: Výrobní xxxxx: xxxxxxx číslo xxxxxxxxxx zařízení, v xxxx proběhlo xxxxxxxx xxxx xxxxxxxxxx. Xxxx XX: (1x) Xx. xxxx. X 300, 14.11.2009, s. 1. (1x) Úř. věst. X 54, 26.2.2011, x. 1. (2) Xxxxxxxx xx xxxxxxxx. (3) Vyplňte, xxxxx je xxxxxxxxx x xxxxxx xx Xxxxxxxx unie omezeno xx xxxxxx xxxxxxx xxxxxxx třetí xxxx. (4) Xx. xxxx. X 175, 10.7.2010, s. 1. (5) Tato xxxxxxxx xxxxx xxxxx pro xxxxx xxxx xxxxxxx x xxxxxxx X xxxxxxx X xxxxxxxx Xxxxxx (XX) x. 605/2010 (Xx. věst. X 175, 10.7.2010, x. 1). (6) Xxxxx xxxxxx xxxxxx xxxxxxxxxxx x xxxxxxxxx xxxxx xxxxxxxx x xxxxxxx X směrnice Rady 64/432/XXX (Úř. xxxx. 121, 29.7.1964, x. 1977) a xxxxx xxxxxx prosté xxxxxxxxxx xxxxxxx xxxxx xxxxx xxxxxxxx x příloze X xxxxxxxx I xxxxxxx xxxxxxxx. — Xxxxx xxxxxxx x razítka xx xxxx lišit xx xxxxx tisku. — Xxxxxxxx xxx xxxxxxx: xxxx xxxxxxxxx slouží xxxxx k veterinárním xxxxxx a xxxx xxxxxxx xxxxxxxx až xx okamžiku, xxx xxxxxxx xxxxxxxxxx hraniční xxxxxxxx Xxxxxxxx unie. Úřední xxxxxxxxxxx lékař / xxxxxx xxxxxxxxx Xxxxx (xxxxxxxx xxxxxx): Xxxxxxxxxxx a xxxxx: Xxxxx: Xxxxxx: Xxxxxxx: XXXXXXXX 3 (X) Xxxxxxxxxxx xxxxxxxxx xxx krmivo x xxxxxxxxxx pro xxxxxxx v xxxxxxxx xxxxx určené x xxxxxxxx do Xxxxxxxx xxxx xxxx x xxxxxxxx přes její xxxxx (2)  Text obrazu Text obrazu
XXXX: Xxxxxxxxxxx xxxxxxxxx xx XX Xxxx X: Xxxxxxxxxxx x xxxxxxxx xxxxxxx X.1. Xxxxxxxxxx Xxxxx Xxxxxx Xxx. X.2. Xxxxx xxxxxxx osvědčení I.2.a. I.3. Xxxxxxxxx xxxxxxxx xxxxx X.4. Xxxxxxxxx místní xxxxx X.5. Xxxxxxxx Xxxxx Xxxxxx XXX Xxx. X.6. Xxxxx xxxxxxxxxx xx xxxxxxx x XX Xxxxx Xxxxxx XXX Xxx. X.7. Xxxx xxxxxx Xxx XXX X.8. Xxxxxx původu Kód I.9. Xxxx určení Kód XXX X.10. Xxxxxx xxxxxx Xxx X.11. Místo xxxxxx Xxxxx Číslo schválení Adresa Název Xxxxx xxxxxxxxx Xxxxxx Xxxxx Xxxxx xxxxxxxxx Xxxxxx X.12. Xxxxx xxxxxx Xxxxx xxxxx Xxxxx Číslo xxxxxxxxx Xxxxxx XXX X.13. Xxxxx xxxxxxxx X.14. Xxxxx xxxxxxx X.15. Xxxxxxxx xxxxxxxxxx Xxxxxxx Xxxxxxxx Xxxxx Xxxxxxxx vozidlo Xxxxxxx Xxxxxxxxxxxx Xxxxx xx xxxxxxxx X.16. Xxxxxxx stanoviště hraniční xxxxxxxx XX X.17. X.18. Xxxxx xxxxx X.19. Xxx xxxxx (xxx XX) 23.09 X.20. Množství I.21. Xxxxxxx xxxxxxxx Xxxxxx Xxxxxxxx Xxxxxxxx X.22. Xxxxx xxxxxx X.23. Xxxxx plomby/kontejneru I.24. Druh xxxxx  Text obrazu Text obrazu
X.25. Xxxxx xxxxxxxxx xxx: Xxxxxx pro xxxxxxx x xxxxxxxx xxxxx Xxxxxxxxx využití I.26. Xxx xxxxxxx xxxx XX xx xxxxx xxxx Xxxxx xxxx Kód XXX X.27. Pro dovoz xxxx xxxxxx xx XX X.28. Xxxxxxxxxxxx zboží Číslo xxxxxxxxx zařízení Druh (xxxxxxx xxxxx) Xxxxxxx xxxxx Xxxxx xxxxxxxx Xxxxx xxxxx  Text obrazu Text obrazu
ZEMĚ Krmivo v xxxxxxxxxx pro xxxxxxx x xxxxxxxx chovu II. Xxxxxxxxx informace II.a. Xxxxx xxxxxxx xxxxxxxxx XX.x. Xx, xxxx xxxxxxxxx xxxxxx xxxxxxxxxxx xxxxx, xxxxxxxxxx, xx xxxx xxxxxxx x xxxxxxxxx nařízení Xxxxxxxxxx xxxxxxxxxx x Rady (XX) č. 1069/2009 (1x), xxxxxxx xxxxx xxx x články 8 x 10 xxxxxxxxx xxxxxxxx, x xxxxxxxx Komise (EU) x. 142/2011 (1x), xxxxxxx pokud xxx x xxxxxxx XXXX xxxxxxxx II a xxxxxxx XIV xxxxxxxx XX xxxxxxxxx nařízení, x xxxxxxxxx, xx xxxx xxxxxxx xxxxxx xxx zvířata v xxxxxxxx xxxxx: XX.1. xxxx xxxxxxxxxx x xxxxxxxxxx x xxxxxxxx xxxx xxxxxxx xxxxxxxxxx x xxxxxxxxxxx xxxxxxxxxx xxxxxxx x souladu x xxxxxxx 24 nařízení (XX) č. 1069/2009; II.2. xxxx xxxxxxxxxx xxxxxxxx x xxxxxx xxxxxxxxxx xxxxxxxx živočišného xxxxxx: (2) xxx [- xxxx xxxxxxxxxx zvířat a xxxxxx xxxxx, xxxx x případě zvěře xxxx xxxxxxxxxx xxxxxx xxxx jejich části, xxxxx xxxx xxxxx xxxxxxxx xxxxxxxx Unie xxxxxx x xxxxxx xxxxxxxx, xxxxx z xxxxxxxxxx důvodů xxxxxx x xxxxxx xxxxxxxx xxxxxx;] (2) x/xxxx [- xxxxxxx xxxxxxxx xxxx x níže xxxxxxx xxxxx xxxxxxxxxxx xxx xx xxxxxx, xxxxx xxxx xxxxxxxx xx xxxxxxx a po xxxxxxxxx xxxx porážkou xxxx xxxxxxxx jako xxxxxxxxx x xxxxxxx x xxxxxx xxxxxxxx, xxxx těla x xxxx uvedené xxxxx xxxxx xxxxxxxx x xxxxxx spotřebě v xxxxxxx s xxxxxxxx xxxxxxxx Xxxx: x) xxxxxxx xxxxxxxx xxxx xxxx xxxx zvířat a xxxxxx xxxxx, xxxxx xxxx x souladu x xxxxxxxx xxxxxxxx Xxxx prohlášeny xx xxxxxxxx x xxxxxx xxxxxxxx, xxxxx nevykazovaly xxxxx xxxxxxxx onemocnění xxxxxxxxxx xx xxxxxxx xxxx xxxxxxx; xx) hlavy xxxxxxx; xxx) kůže x xxxxx, xxxxxx xxxxxx xxxxxxx x xxxxxx, xxxx a xxxxxxxxx, xxxxxx xxxxxx xxxxx, xxxxxxxxxx x xxxxxxxxxx xxxxxx, xxxxx x xxxxxxx; xx) xxxxxxx štětiny; v) xxxx;] (2) a/nebo [- xxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx x xxxxxxx x ze zajícovců xxxxxxxxxx xx farmě, xxx xx uvedeno x čl. 1 xxxx. 3 xxxx. x) xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Rady (XX) č. 853/2004&xxxx;(2x), xxxxx xxxxxxxxxxxx příznaky xxxxxxxxxx xxxxxxxxxx na xxxxxxx xxxx zvířata;] (2) x/xxxx [- xxxx xxxxxx, xxxxx xxxxxxxxxxxx xxxxx xxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxx na xxxxxxx xxxx zvířata, xxxxx byla xxxxxxxx xx xxxxxxx a xxxxx xxxx xx xxxxxxxxx xxxx xxxxxxxx xxxxxxxx xxxxxxxxxxx k xxxxxxx x xxxxxx xxxxxxxx x xxxxxxx x xxxxxxxx xxxxxxxx Xxxx;] (2) a/nebo [- xxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx, které xxxxxxxx xxx xxxxxx xxxxxxxx xxxxxxxx k xxxxxx xxxxxxxx, xxxxxx xxxxxxxxxxx xxxxx, xxxxxxx xxxx xxxx x xxxxxxxxxxx xxxx separátoru xx xxxxxxxxxx xxxxx;] (2) x/xxxx [- xxxxxxxx xxxxxxxxxxx xxxxxx xxxx xxxxxxxxx xxxxxxxxxx xxxxxxxx živočišného xxxxxx, které x xxxxxxxxxx xxxxxx xxxx x xxxxxx xxxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxx, xxxxxx xxxxxx nebo xxxxxx xxxxxxxx, x xxxxx xxxxxxxx žádné xxxxxx xxx xxxxxx xxxx ani xxxxxx, xxx nejsou xxxxxx x xxxxxx xxxxxxxx;] (2) x/xxxx [- xxxxxx xxx xxxxxxx x xxxxxxxx chovu x xxxxxx živočišného xxxxxx xxxx xxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx či získané xxxxxxxx, xxxxx x xxxxxxxxxx xxxxxx xxxx x xxxxxx problémů xxxxxxxxxxx xxxxxxxxx xxxxxx, xxxxxx xxxxxx xxxx xxxxxx xxxxxxxx, x xxxxx xxxxxxxx xxxxx xxxxxx xxx xxxxxx xxxx xxx xxxxxx, xxx nejsou určeny xx xxxxxx;] (2) x/xxxx [- krev, placenta, xxxx, xxxx, xxxx, xxxx, odřezky xxxxx x xxxxxxxx x xxxxxx xxxxx xxxxxxxxxxx xx xxxxxx xxxxxx, xxxxx xxxxxxxxxxxx žádné xxxxxxxx onemocnění xxxxxxxxxx xxxxx xxxxxxxxx na xxxxxxx xxxx xxxxxxx;] (2) x/xxxx [- xxxxx xxxxxxxxxxx x xxxxxx xxxxx, kromě xxxxxxxx xxxxx, xxxxx nevykazovali xxxxx xxxxxxxx onemocnění xxxxxxxxxx xx xxxxxxx xxxx zvířata;] (2) a/nebo [- xxxxxxxx xxxxxxxx xxxxxxxxxxx původu z xxxxxxx živočichů pocházející x podniků nebo xxxxxxxx xx xxxxxx xxxxxxxx xxxxxxxx k xxxxxx xxxxxxxx;] Xxxx XX: Xxxxxxxxx  Text obrazu Text obrazu
ZEMĚ Krmivo x xxxxxxxxxx xxx xxxxxxx x xxxxxxxx xxxxx XX. Xxxxxxxxx xxxxxxxxx XX.x. Číslo xxxxxxx osvědčení II.b. (2) x/xxxx [- xxxx xxxxxxx xxxxxxxx xxxxxxxxxxx xx xxxxxx, xxxxx nevykazovala xxxxx příznaky xxxxxxxxxx xxxxxxxxxx xxxxx materiálem xx xxxxxxx nebo xxxxxxx: x) ulity xxxxxxx x korýšů x xxxxxxx tkáněmi xxxx xxxxx; xx) xxxxx xxxxxxxx xxxxxxxxxxx xx xxxxxxxxxxxxx xxxxxx: — xxxxxxxx xxxxxxxx x xxxxx, — vejce, — xxxxxxxx xxxxxxxx x xxxxx, xxxxxx xxxxxxxxx xxxxxxxx; xxx) xxxxxxxxxx xxxxxx xxxxxxxx z obchodních xxxxxx;] (2) x/xxxx [- xxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx x xxxxxxx xxxx xxxxxxxxxxxxx bezobratlých xxxxxxxxx, xxxxx xxxxx xxxxxxxxxxx pro xxxxxxx xxxx xxxxxxx;] (2) a/nebo [- zvířata z xxxx xxxxxxxx (Xxxxxxxx) x xxxxxxxxx (Lagomorpha) x xxxxxx xxxxx, xxxxx materiálu xxxxxxxxx 1 xxxxxxxxx x xx. 8 písm. x) xxxxxx xxx), xx) x x) xxxxxxxx (XX) x. 1069/2009 a xxxxxxxxx xxxxxxxxx 2 xxxxxxxxx x xx. 9 xxxx. x) xx x) uvedeného xxxxxxxx;] (2) x/xxxx [- xxxxxxxx xx zvířat, xxxxx xxxx xxxxxxxx některými xxxxxxx xxxxxxxxxx podle xxxxxxxx Rady 96/22/ES (2x), přičemž dovoz xxxxxx materiálu xxx xxxxxxx v souladu x čl. 35 xxxx. a) xxxxx xx) xxxxxxxx (XX) x. 1069/2009;] XX.3. bylo xxxxxxxxx tepelnému xxxxxxxx, xxx xxxxxx je xxxxxxxx xxxxxxx Xx xxxxx xxxxxxxxx 3, x xxxxxxxxxx xxxxxxxxxx xxxxxxxx; XX.4. xxxx analyzováno xxxxxx xxxxxxx pěti xxxxxxxx xxxxxxxxxx xxxxxx x xxxxx zpracované xxxxx laboratorní xxxxxxxxxxxxx xxxxxxx xxx, xxx xx xxxxxxx, zda xxxx xxxxxxxxx xxxxxxxxxxxx xxxxxxx ošetření celé xxxxxxx, xxx stanoví xxx XX.3.; XX.5. xxxxxx xxxxx xxxxxxxxxxxxx opatřeními x zabránění kontaminace xxxxxxxxxxx původci xx xxxxxxxx; (2) [XX.6. výše xxxxxxx xxxxxx xxx xxxxxxx x zájmovém xxxxx (2) buď [xx xxxxxxx x xxxxxxxxxxx xxxxxx xxx xxxx, xxxx xxxx xxxx.] (2) xxxx [xx získáno xx xxxxx, ovcí xxxx xxx a xxxxxxxxxx xxxx xxxxxxx xxxxxx ani z xxxx xxxxxx xxxxxxx: (2) xxx [materiál pocházející xx xxxxx, xxxx x koz jiný xxx získaný xx xxxxxx xxxxxxxxxx, xxxxxxxxxxx xxxxxxxxx x poražených x xxxx xxxx xxxxxxx xxxxxxxx x xxxxxxx x xxxxxxxxxxx 2007/453/XX do xxxxxxxxx xxxx xxxx xxxxxxx xx zanedbatelným xxxxxxx xxxxxxx BSE.]] (2) xxxx [x) xxxxxxxxxxxxx xxxxxxxx xxxxxxxx, xxx xx xxxxxxxxx x xxxx 1 xxxxxxx V xxxxxxxx Xxxxxxxxxx parlamentu x Rady (XX) x. 999/2001 (3); b) xxxxxxx xxxxxxxx xxxx xxxxxxx x kostí xxxxx, xxxx nebo xxx s xxxxxxxx xxxxxx narozených, xxxxxxxxxxx xxxxxxxxx x poražených x zemi nebo xxxxxxx xxxxxxxx x xxxxxxx x xxxxxxxxxxx Xxxxxx 2007/453/ES (4) xx kategorie země xxxx xxxxxxx se xxxxxxxxxxxxx rizikem výskytu XXX, x nichž xxxxx xxxxxxx xxxxx xxxxxx případ XXX; x) xxxxxxxx xxxxxxx živočišného xxxxxx xxxx získaný xxxxxxx xx xxxxx, xxxx nebo xxx, xxxxx xxxx po xxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx nervové xxxxx xxxxxx podlouhlého xxxxxxxxxx xxxxxxxx xxxxxxxxxx do xxxxxx xxxxxxx nebo xxxxxxxxxxxxxxx xxxxxxx xxxxxxx xx xxxxxx xxxxxxx, x xxxxxxxx zvířat xxxxxxxxxx, nepřetržitě xxxxxxxxx x poražených x xxxx xxxx xxxxxxx xxxxxxxx v souladu x rozhodnutím 2007/453/ES xx kategorie xxxx xxxx xxxxxxx se xxxxxxxxxxxxx rizikem výskytu XXX.]]]  Text obrazu Text obrazu
XXXX Xxxxxx x xxxxxxxxxx xxx zvířata x xxxxxxxx chovu II. Xxxxxxxxx informace II.a. Číslo xxxxxxx osvědčení II.b. Poznámky Část X: — Xxxxxxx X.6.: Osoba xxxxxxxxxx za xxxxxxx x Evropské xxxx: xxxx xxxxxxx xx xxxxx xxxxxxx xxxxx xxxxx, xxxxx-xx se x xxxxxxxxx xxx xxxxx xxxxxx xxx xxxxxxx přes Xxxxxxxxx xxxx; může xx xxxxxxx, jedná-li xx x xxxxxxxxx pro xxxxx dovážené do Xxxxxxxx xxxx. — Xxxxxxx X.12.: Xxxxx xxxxxx: xxxx xxxxxxx xx xxxxx vyplnit pouze xxxxx, xxxxx-xx xx x xxxxxxxxx pro xxxxx xxxxxx xxx xxxxxxx. Produkty xxx xxx při xxxxxxxx xxxxxxxxxx xxxxx xx xxxxxxxxxx pásmech, xxxxxxxxxx xxxxxxxx x celních xxxxxxxx. — Kolonka I.15.: Xxxxxxxxxxx xxxxx (železničních xxxxxx xxxx xxxxxxxxxx x xxxxxxxxxx xxxxxxxxxx), xxxxx xxxx (letadla) xxxx název (xxxxxxxx); xxxxxxxxx je xxxxx xxxxxxxxxx x xxxxxxx xxxxxxxx x opětovného xxxxxxxx x Xxxxxxxx xxxx. — Xxxxxxx X.23.: X xxxxxxx xxxxxxxxxx xxx xxxxx xxxxxx xxxxx musí xxx xxxxxxx číslo xxxxxxxxxx x (případně) xxxxx xxxxxx. — Xxxxxxx I.25.: Xxxxxxxxx xxxxxxx: xxxxxxxx xxxx xxxxxxx xxxxx xxxxxx xxxxxxxxxxxxx xxxxxx xxxxxx xxx xxxxxxxxxxxx xxxxxx a výroba xxxx xxxxxxxxxx xxxxx xxx xxxxxxx x xxxxxxxx chovu. — Xxxxxxx X.26. x I.27.: Xxxxxxx podle toho, xxxxx-xx xx x xxxxxxxxx xxx tranzit xxxx xxx xxxxx. — Xxxxxxx I.28.: Xxxx: xxxxxxx: Aves, Xxxxxxxxxx, Xxxxxx, Xxxxxxxx kromě Xxxxxxxxxx xxxx Xxxxxx, Xxxxx, Xxxxxxxx, Xxxxxxxxx, xxxxxxxxxx kromě Xxxxxxxx x Xxxxxxxxx. Xxxx XX: (1x) Xx. xxxx. X 300, 14.11.2009, s. 1. (1x) Xx. xxxx. X 54, 26.2.2011, x. 1. (2) Nehodící xx xxxxxxxx. (2x) Xx. xxxx. X 139, 30.4.2004, x. 55. (2b) Xx. věst. X 125, 23.5.1996, s. 3. (3) Xx. xxxx. X 147, 31.5.2001, x. 1. (4) Úř. xxxx. L 172, 30.6.2007, x. 84. — Xxxxx xxxxxxx x xxxxxxx se xxxx xxxxx xx xxxxx xxxxx. — Xxxxxxxx xxx xxxxx xxxxxxxxxxx xx xxxxxxx x Xxxxxxxx xxxx: xxxx osvědčení xxxxxx xxxxx x xxxxxxxxxxxx xxxxxx a xxxx xxxxxxx xxxxxxxx xx xx xxxxxxxx, xxx xxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxx. Xxxxxx xxxxxxxxxxx xxxxx / úřední xxxxxxxxx Xxxxx (hůlkovým xxxxxx): Xxxxxxxxxxx a xxxxx: Xxxxx: Xxxxxx: Xxxxxxx: XXXXXXXX 3 (B) Veterinární xxxxxxxxx xxx zpracované xxxxxx xxx zvířata v xxxxxxxx xxxxx jiné xxx v xxxxxxxxxx xxxxxx k xxxxxxxx xx Xxxxxxxx xxxx xxxx x xxxxxxxx xxxx xxxx území (2) &xxxx; Text obrazu Text obrazu
XXXX: Xxxxxxxxxxx osvědčení xx EU Část X: Xxxxxxxxxxx x odeslané xxxxxxx X.1. Odesílatel Název Adresa Tel. I.2. Číslo xxxxxxx xxxxxxxxx X.2.x. X.3. Příslušný xxxxxxxx xxxxx X.4. Příslušný xxxxxx orgán I.5. Příjemce Název Adresa PSČ Tel. I.6. Xxxxx zodpovědná xx xxxxxxx v XX Xxxxx Xxxxxx XXX Xxx. X.7. Xxxx xxxxxx Xxx XXX X.8. Xxxxxx xxxxxx Xxx X.9. Xxxx xxxxxx Xxx ISO I.10. Region xxxxxx Xxx X.11. Xxxxx xxxxxx Xxxxx Xxxxx xxxxxxxxx Xxxxxx Xxxxx Xxxxx xxxxxxxxx Xxxxxx Xxxxx Xxxxx schválení Adresa I.12. Xxxxx určení Celní sklad Název Xxxxx xxxxxxxxx Xxxxxx XXX X.13. Místo xxxxxxxx X.14. Datum xxxxxxx X.15. Xxxxxxxx xxxxxxxxxx Xxxxxxx Xxxxxxxx Xxxxx Xxxxxxxx xxxxxxx Ostatní Identifikace Odkaz xx xxxxxxxx X.16. Xxxxxxx xxxxxxxxxx hraniční xxxxxxxx XX X.17. X.18. Popis xxxxx X.19. Xxx xxxxx (xxx XX) X.20. Xxxxxxxx X.21. Xxxxxxx xxxxxxxx Xxxxxx Xxxxxxxx Zmrazené I.22. Xxxxx balení I.23. Xxxxx xxxxxx/xxxxxxxxxx X.24. Xxxx xxxxx  Text obrazu Text obrazu
X.25. Xxxxx xxxxxxxxx xxx: Xxxxxx xxx xxxxxxx x xxxxxxxx xxxxx Xxxxxxxxx využití I.26. Xxx xxxxxxx přes XX xx xxxxx xxxx Xxxxx xxxx Xxx XXX X.27. Xxx dovoz xxxx xxxxxx xx EU I.28. Xxxxxxxxxxxx zboží Číslo xxxxxxxxx xxxxxxxx Xxxx (vědecký xxxxx) Xxxxxxx xxxxx Xxxxx xxxxxxxx Xxxxx šarže  Text obrazu Text obrazu
XXXX Xxxxxxxxxx xxxxxx pro xxxxxxx x zájmovém xxxxx jiné xxx x xxxxxxxxxx XX. Zdravotní xxxxxxxxx XX.x. Číslo xxxxxxx xxxxxxxxx XX.x. Xx, xxxx xxxxxxxxx xxxxxx veterinární xxxxx, xxxxxxxxxx, že xxxx xxxxxxx a xxxxxxxxx xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Xxxx (ES) x. 1069/2009 (1a), xxxxxxx pokud jde x články 8 x 10 uvedeného xxxxxxxx, a xxxxxxxx Xxxxxx (XX) x. 142/2011 (1x), zejména xxxxx xxx o xxxxxxx XXXX xxxxxxxx XX a přílohu XXX xxxxxxxx XX xxxxxxxxx nařízení, x xxxxxxxxx, xx výše xxxxxxx xxxxxx pro xxxxxxx v zájmovém xxxxx: XX.1. xxxx připraveno x xxxxxxxxxx x xxxxxxx schváleném a xxxxxxxxxxx xxxxxxxxxx xxxxxxx x xxxxxxx x xxxxxxx 24 xxxxxxxx (XX) x. 1069/2009; XX.2. xxxx připraveno xxxxxxxx x xxxxxx xxxxxxxxxx xxxxxxxx živočišného xxxxxx: (2) xxx [- xxxx xxxxxxxxxx zvířat a xxxxxx xxxxx, nebo x případě xxxxx xxxx usmrcených zvířat xxxx xxxxxx xxxxx, xxxxx jsou xxxxx xxxxxxxx xxxxxxxx Xxxx xxxxxx x xxxxxx xxxxxxxx, xxxxx z xxxxxxxxxx xxxxxx xxxxxx x xxxxxx xxxxxxxx xxxxxx;] (2) x/xxxx [- xxxxxxx upravená xxxx x xxxx xxxxxxx xxxxx xxxxxxxxxxx buď xx xxxxxx, xxxxx xxxx xxxxxxxx xx xxxxxxx a po xxxxxxxxx před porážkou xxxx xxxxxxxx xxxx xxxxxxxxx x xxxxxxx x lidské spotřebě, xxxx těla a xxxx uvedené xxxxx xxxxx xxxxxxxx k xxxxxx spotřebě x xxxxxxx s právními xxxxxxxx Xxxx: x) xxxxxxx xxxxxxxx xxxx xxxx xxxx xxxxxx x xxxxxx xxxxx, xxxxx xxxx v xxxxxxx x xxxxxxxx xxxxxxxx Xxxx xxxxxxxxxx xx xxxxxxxx k xxxxxx xxxxxxxx, avšak xxxxxxxxxxxx xxxxx xxxxxxxx xxxxxxxxxx xxxxxxxxxx xx xxxxxxx xxxx zvířata; ii) hlavy xxxxxxx; xxx) xxxx x xxxxx, xxxxxx jejich xxxxxxx x xxxxxx, xxxx a xxxxxxxxx, xxxxxx článků xxxxx, xxxxxxxxxx x xxxxxxxxxx xxxxxx, nártů x xxxxxxx; xx) prasečí štětiny; v) xxxx;] (2) x/xxxx [- xxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx x drůbeže x xx xxxxxxxxx xxxxxxxxxx xx farmě, xxx xx xxxxxxx x xx. 1 xxxx. 3 písm. x) nařízení Evropského xxxxxxxxxx x Xxxx (XX) x. 853/2004 (2a), xxxxx xxxxxxxxxxxx xxxxxxxx xxxxxxxxxx xxxxxxxxxx xx xxxxxxx xxxx zvířata;] (2) x/xxxx [- krev xxxxxx, xxxxx xxxxxxxxxxxx xxxxx příznaky xxxxxxxxxx xxxxxxxxxx krví xx xxxxxxx xxxx xxxxxxx, xxxxx xxxx xxxxxxxx xx jatkách x xxxxx byla xx xxxxxxxxx xxxx xxxxxxxx xxxxxxxx xxxxxxxxxxx x xxxxxxx x xxxxxx xxxxxxxx x souladu x xxxxxxxx xxxxxxxx Xxxx;] (2) x/xxxx [- xxxxxxxx produkty živočišného xxxxxx, xxxxx xxxxxxxx xxx výrobě xxxxxxxx xxxxxxxx x xxxxxx xxxxxxxx, xxxxxx xxxxxxxxxxx xxxxx, škvarků xxxx xxxx z xxxxxxxxxxx xxxx xxxxxxxxxx xx xxxxxxxxxx xxxxx;] (2) x/xxxx [- xxxxxxxx xxxxxxxxxxx xxxxxx xxxx potraviny xxxxxxxxxx produkty živočišného xxxxxx, které z xxxxxxxxxx důvodů xxxx x xxxxxx problémů xxxxxxxxxxx xxxxxxxxx xxxxxx, xxxxxx balení xxxx xxxxxx závadami, x xxxxx nevzniká xxxxx xxxxxx xxx xxxxxx xxxx xxx zvířat, xxx nejsou určeny x lidské spotřebě;] (2) x/xxxx [- xxxxxx xxx xxxxxxx v xxxxxxxx xxxxx a xxxxxx xxxxxxxxxxx původu xxxx xxxxxx xxxxxxxxxx xxxxxxxx produkty xxxxxxxxxxx xxxxxx či získané xxxxxxxx, které z xxxxxxxxxx důvodů nebo x důvodu xxxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxx, xxxxxx xxxxxx nebo xxxxxx závadami, x xxxxx xxxxxxxx xxxxx xxxxxx pro xxxxxx xxxx xxx xxxxxx, xxx xxxxxx xxxxxx xx xxxxxx;] (2) x/xxxx [- xxxx, placenta, xxxx, peří, xxxx, xxxx, xxxxxxx kopyt x xxxxxxxx x xxxxxx mléko xxxxxxxxxxx xx xxxxxx xxxxxx, xxxxx xxxxxxxxxxxx xxxxx xxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxx produktem na xxxxxxx xxxx xxxxxxx;] (2) x/xxxx [- xxxxx xxxxxxxxxxx x xxxxxx xxxxx, xxxxx mořských xxxxx, xxxxx xxxxxxxxxxxx xxxxx xxxxxxxx xxxxxxxxxx xxxxxxxxxx na xxxxxxx xxxx xxxxxxx;] Xxxx II: Xxxxxxxxx  Text obrazu Text obrazu
XXXX Xxxxxxxxxx xxxxxx xxx xxxxxxx x xxxxxxxx xxxxx xxxx xxx x xxxxxxxxxx XX. Xxxxxxxxx informace II.a. Xxxxx xxxxxxx xxxxxxxxx XX.x. (2) x/xxxx [- vedlejší xxxxxxxx xxxxxxxxxxx xxxxxx x xxxxxxx xxxxxxxxx xxxxxxxxxxx x xxxxxxx xxxx xxxxxxxx xx xxxxxx xxxxxxxx určených x xxxxxx xxxxxxxx;] (2) x/xxxx [- xxxx uvedený xxxxxxxx xxxxxxxxxxx xx xxxxxx, xxxxx xxxxxxxxxxxx xxxxx xxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxx xxxxxxxxxx xx xxxxxxx nebo xxxxxxx: x) xxxxx xxxxxxx x korýšů s xxxxxxx xxxxxxx xxxx xxxxx; xx) xxxxx materiál xxxxxxxxxxx ze xxxxxxxxxxxxx xxxxxx: — xxxxxxxx xxxxxxxx x líhní, — xxxxx, — xxxxxxxx xxxxxxxx x xxxxx, xxxxxx xxxxxxxxx xxxxxxxx; xxx) xxxxxxxxxx kuřata xxxxxxxx x xxxxxxxxxx xxxxxx;] (2) x/xxxx [- xxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx x vodních xxxx xxxxxxxxxxxxx bezobratlých xxxxxxxxx, xxxxx druhů xxxxxxxxxxx xxx xxxxxxx xxxx xxxxxxx;] (2) a/nebo [- zvířata x xxxx hlodavců (Xxxxxxxx) x xxxxxxxxx (Xxxxxxxxxx) x jejich xxxxx, xxxxx materiálu xxxxxxxxx 1 uvedeného x xx. 8 xxxx. x) bodech xxx), xx) x x) xxxxxxxx (ES) x. 1069/2009 x xxxxxxxxx xxxxxxxxx 2 xxxxxxxxx x čl. 9 xxxx. x) až x) xxxxxxxxx nařízení;] (2) x/xxxx [- materiál xx xxxxxx, která xxxx ošetřena xxxxxxxxx xxxxxxx xxxxxxxxxx xxxxx xxxxxxxx Rady 96/22/XX (2x), xxxxxxx dovoz xxxxxx xxxxxxxxx xxx xxxxxxx x xxxxxxx x xx. 35 xxxx. x) xxxxx xx) xxxxxxxx (ES) x. 1069/2009;] II.3. (2) xxx [xxxx podrobeno xxxxxxxxx xxxxxxxx xxxxxxxxxxxx xxxxxxx 90 °X x xxxx xxxxx;] (2) xxxx [xxxx vyrobeno, xxxxx xxx x složky xxxxxxxxxxx původu, výhradně xx xxxxxxx xxxxxxxx, xxxxx: x) v xxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx xxxx xxxxxxxx xxxxxxxxx z masa xxxx xxxxxxx xxxxxxx xxxx podrobeny tepelnému xxxxxxxx při teplotě xxxxxxx 90 °C x celé xxxxx; x) x xxxxxxx mléka x mléčných xxxxxxx, x) xxxxx xxxxxxxxx ze xxxxxxx xxxx nebo xxxxx xxxxxxx xxxx xxxxxxxxx x xxxxxxx X xxxxxxx X xxxxxxxx Xxxxxx (EU) x. 605/2010 (3), xxxxxx xxxxxxxxxxxxx ošetřením xxxxxxxxxxx x xxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxx xxxxx; xx) x pH sníženým xx méně xxx 6, xxxxx pocházejí xx xxxxxxx xxxx xxxx částí xxxxxxx xxxx xxxxxxxxx x xxxxxxx X xxxxxxx X nařízení (XX) x. 605/2010, prošly xxxxxxx xxxxxxxxxxxxx xxxxxxxxx xxxxxxxxxxx x xxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxx testu; iii) xxxxx xxxxxxxxx xx xxxxxxx xxxx xxxx xxxxx třetích xxxx xxxxxxxxx x xxxxxxx X xxxxxxx X xxxxxxxx (EU) č. 605/2010, xxxxxx xxxxxxxxxxxxx xxxxxxxx nebo dvojím xxxxxxxx ošetřením, xxxxxxx xxxxx x xxxxxx xxxxxxxx bylo xxxx x sobě xxxxxxxxxx x dosažení negativního xxxxxxxxxxxxx xxxxx; xx) xxxxx xxxxxxxxx xx třetích xxxx xxxx xxxxx xxxxxxx xxxx uvedených x xxxxxxx I xxxxxxx C xxxxxxxx (XX) x. 605/2010, xx xxxxxxx se x předchozích 12 xxxxxxxx vyskytlo xxxxxxx xxxxxxxxx a kulhavky, xxxx xxx x xxxxxxxxxxx 12 měsících xxxxxxxx xxxxxxxx proti xxxxxxxxx x xxxxxxxx, xxxx podrobeny: buď — sterilizačnímu xxxxxxx, při xxxxxx xx xxxxxxxx xxxxxxx Xx xxxxx xxxx xxxxx xxx 3, xxxx — xxxxxxxxxxx tepelnému ošetření x xxxxxxxx xxxxxxx xxxxxxx xxxxxxxxxxx účinku xxxxxxxxxx pasterizačním xxxxxxxx x xxxxxxx alespoň 72 °C xx xxxx xxxxxxx 15 xxxxxx x dostatečným x xxxxxxxx xxxxxxxxx xxxxxx xx fosfatázový xxxx, xxxxxxxxxxxx:  Text obrazu Text obrazu
XXXX Xxxxxxxxxx xxxxxx pro xxxxxxx x zájmovém chovu xxxx než x xxxxxxxxxx XX. Xxxxxxxxx informace II.a. Xxxxx xxxxxxx osvědčení II.b. buď — xxxxxx xxxxxxxx xxxxxxxxx x xxxxxxxx účinkem xxxxxxx rovnocenným účinku xxxxxxxxxxx xxxxxxxxx xxxxxxxx x xxxxxxxxxxx x xxxxxxxx xxxxxxxxx xxxxxx xx xxxxxxxxxxx xxxx, xxxxxxxxxxxx x xxxxxxx xxxxxxxx xxxxx nebo xxxxxxxx xxxxxxxx výrobků xxxxxxxx xxxxxx, xxxx — acidifikačním xxxxxxxx, xxx xxxxxx xxxx pH xxxxxxxxx xx xxxxxxx xxxxx xxx 6 po xxxx nejméně xxxxx xxxxxx; x) x xxxxxxx xxxxxxxx xxxx vyrobeny xxxxxxxx, xxxxx zajišťuje, xx nezpracovaný xxxxxxxx xxxxxxxxx 3 xx xxxxxxxx xxxxxxxx xxxxxxxxx xx zásadou následovanému xxxxxx nebo několikerým xxxxxxxxxxxxx, xxxx xxxxxxx xX x xxxxxxxx xxxxxxxx (podle xxxxxxx xxxxxxxxx), po xxx xxxxxxxxx xxxxxxxxxx prostřednictvím xxxxxxxx x sterilizace; d) x případě xxxxxxxxxxxxxxx xxxxxxxx byly xxxxxxxx xxxxxxxx xxxxxxxx, xxxxx xxxxxxxx xxxxxx xxxxxxxx x xx xxxxxxxxxx xxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxx 3, x x případě xxxxxxxxxxxxxxx bílkovin xxxxx xxxx xxxxxx získaných x kůží x xxxxx xxxxxxxxxxx xxxx xxxxxxxx xx xxxxxxxxxxxxxxx xxxxxxxx určeném xxxxxxxx x xxxxxx xxxxxxxxxxxxxxx xxxxxxxx, výhradně xx xxxxxxx xxxxxxxxx, xxxxx xxxxxxxxxxx xxxxxxxx xx xxxxx než 10 000 xxxxxxx, x xx xxxxxxx xxxxxxx xxxxxxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxx 3 xxxxxxxxxx xx xxxxxxx xxxx, loužením x xxxxxxxxxxx xxxxxx, xx xxxx následuje: i) vystavení xxxxxxxxx xX x xxxxxxx xxxxx xxx 11 xx xxxx xxxxx xxx xxx xxxxxx při xxxxxxx xxxxx než 80 °X a následně xxxxxxx xxxxxxxx xxx xxxxxxx xxxxx než 140 °X xx xxxx 30 xxxxx xxx tlaku vyšším xxx 3,6 xxxx; xxxx xx) vystavení materiálu xX v rozmezí xxxxxx 1 xx 2 xxxxxxxxxxx xxxxxxxxxx xX x hodnotě xxxxx než 11 x xxxxxxxx xxxxxxx xxxxxxxx xxx teplotě 140 °X xx xxxx 30 minut xxx xxxxx 3 xxxx; x) x xxxxxxx xxxxxxxxx výrobků xxxx xxxxxxxxx xxxxxxxx xx xxxxxxxxxxxxxxxx xxxxx 1 xx 5 nebo 7 uvedených x xxxxxxx XX xxxxxxxx XXX xxxxxxxx (XX) x. 142/2011, xxxx xxxx ošetřeny x xxxxxxx x kapitolou XX xxxxxx X xxxxxxx XXX xxxxxxxx (XX) č. 853/2004; f) x xxxxxxx xxxxxxxx xxxx xxxxxxxxx postupu, xxxxx xxxxxxxxx, xx xxxxxxxxxxxx xxxxxxxx xxxxxxxxx 3 je podroben xxxxxxxx, xxxxx zahrnuje xxxxxxx, xxxxxx xX xxxxxx kyseliny xx xxxxxx x následným xxxxxx xx xxxxxxxxxxx xxxxxxxxxxxxx, xxxxxxxx a xxxxxxx, xxxxxxx se xxxxxxxx xxxxxxxxx xxxxxxxxxxxxx xxxxxxxxxx jiných xxx xxxxxxxxxx povolených xxxxxxxx xxxxxxxx Xxxx; x) x xxxxxxx xxxxxxxx výrobků xxxx xxxxxxxxx xxxxxxxx xx xxxxxxxxxxxxxxxx metod 1 xx 5 xxxx 7 xxxxxxxxx x příloze XX xxxxxxxx XXX xxxxxxxx (XX) x. 142/2011; x) x xxxxxxx zpracovaných xxxxxxxxxxx xxxxxxxx xxxxxxxxxxxxx xx savců byly xxxxxxxxx xxxxxxxx ze xxxxxxxxxxxxxxxx xxxxx 1 xx 5 xxxx 7, x v xxxxxxx xxxxxxx krve xxxx xxxxxxxxx xxxxxxxx xx xxxxxxxxxxxxxxxx metod 1 xx 5 xxxx 7, xxxxx xx v xxxxxxx xxxxxxxxxxxxxx xxxxxx 7 xxxxxxx na xxxxx xxxxx xxxxxxx xxxxxxxx xxx xxxxxxxxx teplotě 80 °X; x) x xxxxxxx zpracovaných xxxxxxxxxxx xxxxxxxx xxxxxxxxxxxxxxx xx xxxxx x výjimkou xxxx moučky byly xxxxxxxxx jakékoli xx xxxxxxxxxxxxxxxx metod 1 xx 5 xxxx 7 uvedených v xxxxxxx XX xxxxxxxx XXX xxxxxxxx (XX) x. 142/2011; j) x xxxxxxx xxxx xxxxxx xxxx xxxxxxxxx jakékoli xx xxxxxxxxxxxxxxxx xxxxx 1 xx 7 xxxxxxxxx v xxxxxxx XX xxxxxxxx XXX xxxxxxxx (EU) x. 142/2011 nebo xxxxxx x parametrům, které xxxxxxxxx soulad výrobku x xxxxxxxxxxxxxxxxx normami xxx získané xxxxxxxx xxxxxxxxxxx x xxxxxxx X kapitole X xxxxxxxx (EU) x. 142/2011; x) v případě xxxxxxxx/xxxxxxxxxx tuku, včetně xxxxxx xxxx, byly xxxxxxxxx xxxxxxx ze xxxxxxxxxxxxxxxx metod 1 xx 5 nebo 7 (a xxxxxx 6 v xxxxxxx xxxxxx tuku) xxxxxxxxx x xxxxxxx XX xxxxxxxx III nařízení (XX) x. 142/2011, xxxx xxxx vyrobeny x xxxxxxx x xxxxxxxx III xxxxxxx XXX xxxxxxxxx II xxxxxxxx (XX) č. 853/2004; tavené/škvařené xxxx x xxxxxxxxxxx xxxx xxx xxxxxxxxxx xxx, xxx xxxxxxxxx xxxxxx xxxxxxxxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxxxxxxx 0,15 % xxxxxxxxxxxx;  Text obrazu Text obrazu
ZEMĚ Zpracované krmivo xxx zvířata v xxxxxxxx xxxxx jiné xxx x xxxxxxxxxx XX. Xxxxxxxxx xxxxxxxxx XX.x. Xxxxx xxxxxxx xxxxxxxxx XX.x. x) x xxxxxxx xxxxxxxxxxxxxxxxxxxx xxxxxxxxxx xxxx xxxxxxxx postupem, xxxx x) xxxxxxxxx, xx xxxxxxx xxxxxx xxxxxxxx xxxxxxxxx 3 je xxxxxxx nadrcen x xxxxxx xxxxx vody xxxxxxxx x xxxxxxx xxxxxxxx kyselinou xxxxxxxxxxxxxxx (xxx minimální koncentraci 4 % a xX nižším xxx 1,5) po xxxx xxxxxxx xxxx xxx; xx) xx xxxxxxxx postupu xxxxxxxxx x xxxx x) xxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxxxxxx xxxxxx xxxxxx, xxx xxxx x xxxxxxx výsledné xxxxxxxxx xxxxxxxxxxxxxxxxxxxx xxxxxxxxxx xxx xX 4 xx 7; a iii) xxxx xxxxxxxxx xxxxxxxxxxxxxxxxxxxx xxxxxxxxxx xxxxxxx xxxxxx xxxxxxxx xxx xxxxxxx xxxxxxx x xxxxxxx xx 65 °X xx 325 °C x konečné xxxxxxx x xxxxxxx xx 30 °C do 65 °X; x) v xxxxxxx fosforečnanu xxxxxxxxxx xxxx xxxxxxxx xxxxxxxx, xxxx xxxxxxxxx x) xx xxxxxxx xxxxxx materiál xxxxxxxxx 3 xx xxxxxxx nadrcen a xxxxxx xxxxxxxxxxx horké xxxx xxxxxxxx (xxxxxx xxxxx menší než 14 mm); ii) xxxxxxxxxxx xxxxxx x xxxx xxx xxxxxxx 145 °X po xxxx 30 xxxxx při xxxxx 4 xxxx; xxx) xx vývar z xxxxxxxx xx xxxxxxxxxxx xxxxxx xx hydroxyapatitu (xxxxxxxxxxxx xxxxxxxxxx); a iv) xx ke xxxxxxxxx xxxxxxxxxxxx xxxxxxxxxx dojde xx xxxxxx xx xxxxxxx xxxxxx vzduchem x xxxxxxx 200 °X; x) v xxxxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxx xxxx xxxxxxxx xxxxx xxxxxxxxxxxxxx xxxxxx a xxxxxxxxx, xxxxx xxxxxxxxx xxxxxx xxxxxxx x xxxxxxxxxxxxxxxxx xxxxxxx xxxxxxxxx x xxxx II.4.;] (2) xxxx [xxxx xxxxxxxxx xxxxxxxx sušením xxxx xxxxxxxx, které xxxx xxxxxxxxx xxxxxxxxxx xxxxxxx;] (2) xxxx [x xxxxxxx xxxxxxx x xxxxxxxxxxxxx xxxxxxxxxxxx živočichů, kromě xxxxx patogenních xxx xxxxxxx nebo xxxxxxx, xxxx xxxxxxxxx xxxxxxxx, xxxxx xxxx schváleno xxxxxxxxxx xxxxxxx x xxxxx xxxxxxxxx, xx xxxx xxxxxx xxx xxxxxxx v xxxxxxxx xxxxx nepředstavuje xxxxx xxxxxxxxxxx xxxxxx pro xxxxxx lidí a xxxxxx;] XX.4. xxxx xxxxxxxxxxx xxxxxx alespoň pěti xxxxxx x každé xxxxxxxxxx xxxxx xxxxxxxxx xxxxxxxxxx xxxxx skladování xxxx při xxxxxxxxxxx xx xxxxxxxxxxxxxxx zařízení x xxxxxxxx xxxxx xxxxxx (4): Xxxxxxxxxx: xxxxxxxxxxxx x 25 g xxxxxxxx: x = 5, x = 0, x = 0, X = 0 Xxxxxxxxxxxxxxxxxx: n = 5, x = 2, m = 10, M = 300 v 1 x; XX.5. prošlo xxxxx xxxxxxxxxxxxx opatřeními k xxxxxxxxx xxxxxxxxxxx xxxxxxxxxxx xxxxxxx xx xxxxxxxx; XX.6. xxxx xxxxxxxx xx xxxxxx obalu xxxxxxxxxx xxxxxxxxx x xxxxxxx „XXXX XXXXXX X XXXXXX XXXXXXXX“, xxxx-xx xxxxxx xxx zvířata x zájmovém chovu xxxxxxxxx v xxxxxx xxxxxxxxxxx x xxxxxxx, xx němž je xxxxx xxxxxxx, xx xxxxx xx xxxxx xxxxxxxx xx xxxxxx xxxxxx x xxxxxxxx xxxxx; (2) [XX.7. výše xxxxxxx krmivo xxx xxxxxxx x xxxxxxxx xxxxx (2) xxx [je xxxxxxx x xxxxxxxxxxx xxxxxx než xxxx, xxxx xxxx kozy.] (2) xxxx [je xxxxxxx xx xxxxx, xxxx xxxx koz x xxxxxxxxxx dále uvedené xxxxxx xxx z xxxx xxxxxx xxxxxxx: (2) xxx [materiál xxxxxxxxxxx xx xxxxx, xxxx x xxx xxxx xxx získaný xx xxxxxx xxxxxxxxxx, xxxxxxxxxxx xxxxxxxxx a xxxxxxxxxx x xxxx xxxx xxxxxxx xxxxxxxx x xxxxxxx x xxxxxxxxxxx 2007/453/XX do kategorie xxxx nebo xxxxxxx xx zanedbatelným rizikem xxxxxxx XXX.]] (2) xxxx [x) specifikovaný xxxxxxxx xxxxxxxx, xxx xx xxxxxxxxx v xxxx 1 přílohy V xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Xxxx (ES) x. 999/2001 (5);  Text obrazu Text obrazu
XXXX Xxxxxxxxxx xxxxxx xxx xxxxxxx x xxxxxxxx xxxxx xxxx xxx x konzervách II. Xxxxxxxxx xxxxxxxxx XX.x. Číslo xxxxxxx xxxxxxxxx XX.x. x) xxxxxxx oddělené xxxx získané x xxxxx xxxxx, ovcí xxxx koz s xxxxxxxx zvířat xxxxxxxxxx, xxxxxxxxxxx xxxxxxxxx a xxxxxxxxxx v xxxx xxxx xxxxxxx xxxxxxxx x xxxxxxx x xxxxxxxxxxx Xxxxxx 2007/453/ES (6) xx kategorie xxxx xxxx xxxxxxx xx zanedbatelným rizikem xxxxxxx BSE, x xxxxx xxxxx xxxxxxx xxxxx xxxxxx xxxxxx XXX; x) xxxxxxxx xxxxxxx xxxxxxxxxxx xxxxxx xxxx xxxxxxx xxxxxxx xx xxxxx, ovcí xxxx xxx, xxxxx byly xx omráčení xxxxxxxx xxxxxxxx centrální xxxxxxx xxxxx pomocí xxxxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxxx xx dutiny xxxxxxx xxxx xxxxxxxxxxxxxxx xxxxxxx xxxxxxx xx xxxxxx xxxxxxx, x výjimkou xxxxxx xxxxxxxxxx, xxxxxxxxxxx xxxxxxxxx a poražených x zemi xxxx xxxxxxx zařazené x xxxxxxx x xxxxxxxxxxx 2007/453/XX xx xxxxxxxxx xxxx xxxx xxxxxxx xx zanedbatelným rizikem xxxxxxx BSE.]]] Poznámky Část X: — Xxxxxxx I.6.: Xxxxx xxxxxxxxxx xx xxxxxxx x Xxxxxxxx xxxx: xxxx xxxxxxx xx xxxxx vyplnit pouze xxxxx, jedná-li se x xxxxxxxxx xxx xxxxx xxxxxx xxx xxxxxxx xxxx Evropskou xxxx; může se xxxxxxx, xxxxx-xx xx x xxxxxxxxx xxx xxxxx dovážené xx Xxxxxxxx xxxx. — Xxxxxxx X.12.: Xxxxx xxxxxx: xxxx xxxxxxx je xxxxx vyplnit xxxxx xxxxx, jedná-li xx x xxxxxxxxx xxx xxxxx xxxxxx pro xxxxxxx. Produkty smí xxx xxx xxxxxxxx xxxxxxxxxx xxxxx xx xxxxxxxxxx xxxxxxx, xxxxxxxxxx xxxxxxxx a celních xxxxxxxx. — Xxxxxxx X.15.: Xx třeba xxxxx xxxxxxxxxxx xxxxx (xxxxxx xxxx kontejnery x xxxxxxxx xxxxxxxxxx), číslo xxxx (letadlo) nebo xxxxx (xxxxxxxx). V xxxxxxx xxxxxxxx x xxxxxxxxxx xxxxxxxx xxxx xxxxxxxxxx informovat xxxxxxxxxx xxxxxxxx xxxxxxxx x xxxxx vstupu xx Xxxxxxxx unie. — Xxxxxxx X.19.: Použijte xxxxxxxxx xxx xxxxxxxxxxxxxxx xxxxxxx (XX) následujících xxxxx: 04.01, 04.02, 04.03, 04.04, 04.08, 05.04, 05.05, 05.06, 05.11, 15.01, 15.02, 15.03, 15.04, 23.01, 23.09, 28.35.25, 28.35.26, 35.01, 35.02, 35.03 nebo 35.04. — Kolonka X.23.: X xxxxxxx kontejnerů xxx xxxxx xxxxxx xxxxx xxxx xxx xxxxxxx číslo kontejneru x (xxxxxxxx) xxxxx xxxxxx. — Kolonka X.25.: Xxxxxxxxx využití: jakékoli xxxx xxxxxxx kromě xxxxxx xxxxxxxxxxxxx xxxxxx xxxxxx xxx xxxxxxxxxxxx xxxxxx a xxxxxx xxxx xxxxxxxxxx xxxxx xxx xxxxxxx v xxxxxxxx xxxxx. — Xxxxxxx X.26. a X.27.: Xxxxxxx xxxxx xxxx, xxxxx-xx xx x xxxxxxxxx pro tranzit xxxx pro xxxxx. — Xxxxxxx X.28.: Xxxx: xxxxxxx: Xxxx, Xxxxxxxxxx, Xxxxxx, Xxxxxxxx kromě Xxxxxxxxxx xxxx Xxxxxx, Xxxxx, Xxxxxxxx, Xxxxxxxxx, xxxxxxxxxx kromě Xxxxxxxx x Crustacea. Část XX: (1x) Xx. xxxx. L 300, 14.11.2009, x. 1. (1x) Úř. xxxx. X 54, 26.2.2011, x. 1. (2) Nehodící xx xxxxxxxx. (2x) Xx. xxxx. X 139, 30.4.2004, x. 55. (2b) Xx. xxxx. L 125, 23.5.1996, s. 3. (3) Xx. xxxx. X 175, 10.7.2010, x. 1.  Text obrazu Text obrazu
ZEMĚ Zpracované xxxxxx pro xxxxxxx x xxxxxxxx xxxxx xxxx než v xxxxxxxxxx XX. Xxxxxxxxx xxxxxxxxx XX.x. Xxxxx xxxxxxx xxxxxxxxx XX.x. (4) Xxx: x = xxxxx xxxxxx, xxxxx xxxx xxx xxxxxxxxx; x = xxxxxxx hodnota počtu xxxxxxxx; xxxxxxxx je xxxxxxxxx xx xxxxxxxxxx, xxxxxxxx počet xxxxxxxx xx všech xxxxxxxx xxxxxxxxxx m; M = xxxxxxxxx xxxxxxx xxxxx xxxxxxxx; výsledek xx xxxxxxxxx xx xxxxxxxxxxxx, xxxxx xxxxx xxxxxxxx x xxxxxx xxxx xxxx vzorcích xx xxxxx xxxx xxxxx xxx M; a c = xxxxx xxxxxx, xxxxxxx xxxxxxxxxxx xxxxx xxx xxx x xxxxxxx xxxx x x X, xxxxxxx xxxxxx xx xxxxx xxxxx považován za xxxxxxxxx, xxxxx je xxxxxxxxxxx xxxxx xxxxxxxxx xxxxxx xxxxx m xxxx xxxxx. (5) Xx. xxxx. L 147, 31.5.2001, x. 1. (6) Xx. xxxx. L 172, 30.6.2007, x. 84. — Barva xxxxxxx x razítka xx xxxx lišit xx xxxxx xxxxx. — Xxxxxxxx xxx xxxxx zodpovědnou xx xxxxxxx v Xxxxxxxx xxxx: toto xxxxxxxxx xxxxxx pouze x xxxxxxxxxxxx xxxxxx x xxxx xxxxxxx xxxxxxxx až xx xxxxxxxx, xxx dosáhne xxxxxxxxxx xxxxxxxx xxxxxxxx x xxxxx xxxxxx xx Xxxxxxxx xxxx. Xxxxxx xxxxxxxxxxx xxxxx / xxxxxx xxxxxxxxx Xxxxx (xxxxxxxx xxxxxx): Xxxxxxxxxxx x xxxxx: Xxxxx: Xxxxxx: Xxxxxxx: XXXXXXXX 3 (X) Xxxxxxxxxxx xxxxxxxxx xxx xxxxxxx xxxxxxx pro psy, xxxxx xxxx xxxxxx x odeslání xx Xxxxxxxx xxxx xxxx x xxxxxxxx přes xxxx xxxxx (2)  Text obrazu Text obrazu
XXXX: Xxxxxxxxxxx xxxxxxxxx xx XX Xxxx X: Podrobnosti x odeslané xxxxxxx X.1. Xxxxxxxxxx Xxxxx Xxxxxx Xxx. X.2. Číslo xxxxxxx xxxxxxxxx X.2.x. X.3. Příslušný xxxxxxxx xxxxx X.4. Xxxxxxxxx xxxxxx xxxxx X.5. Xxxxxxxx Xxxxx Xxxxxx XXX Xxx. X.6. Xxxxx xxxxxxxxxx za xxxxxxx x XX Xxxxx Xxxxxx XXX Xxx. X.7. Xxxx xxxxxx Xxx ISO I.8. Xxxxxx xxxxxx Xxx X.9. Země určení Kód XXX X.10. Xxxxxx xxxxxx Xxx X.11. Xxxxx původu Název Číslo xxxxxxxxx Xxxxxx Xxxxx Xxxxx xxxxxxxxx Xxxxxx Xxxxx Xxxxx xxxxxxxxx Xxxxxx X.12. Xxxxx xxxxxx Xxxxx xxxxx Xxxxx Xxxxx xxxxxxxxx Xxxxxx XXX X.13. Místo xxxxxxxx X.14. Xxxxx odjezdu I.15. Xxxxxxxx xxxxxxxxxx Xxxxxxx Xxxxxxxx Vagon Silniční xxxxxxx Ostatní Identifikace Odkaz na xxxxxxxx X.16. Vstupní stanoviště xxxxxxxx xxxxxxxx EU I.17. I.18. Xxxxx xxxxx X.19. Xxx xxxxx (kód XX) X.20. Xxxxxxxx X.21. Teplota xxxxxxxx Xxxxxx Xxxxxxxx Xxxxxxxx X.22. Xxxxx xxxxxx X.23. Xxxxx xxxxxx/xxxxxxxxxx X.24. Xxxx obalu  Text obrazu Text obrazu
X.25. Xxxxx xxxxxxxxx pro: Krmivo xxx xxxxxxx x xxxxxxxx xxxxx Xxxxxxxxx xxxxxxx X.26. Xxx xxxxxxx xxxx EU do xxxxx xxxx Xxxxx země Xxx XXX X.27. Pro xxxxx xxxx xxxxxx xx XX X.28. Xxxxxxxxxxxx xxxxx Xxxxx schválení xxxxxxxx Xxxx (xxxxxxx xxxxx) Xxxxxxx xxxxx Xxxxx xxxxxxxx Xxxxx xxxxx  Text obrazu Text obrazu
XXXX Xxxxxxx xxxxxxx pro psy II. Xxxxxxxxx xxxxxxxxx XX.x. Xxxxx xxxxxxx xxxxxxxxx XX.x. Xx, xxxx xxxxxxxxx xxxxxx xxxxxxxxxxx xxxxx, xxxxxxxxxx, že xxxx xxxxxxx x xxxxxxxxx xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Xxxx (XX) x. 1069/2009 (1x), zejména xxxxx xxx o článek 10 xxxxxxxxx xxxxxxxx, x xxxxxxxx Xxxxxx (XX) č. 142/2011 (1x), xxxxxxx xxxxx xxx x přílohu XXXX xxxxxxxx XX x xxxxxxx XXX xxxxxxxx XX uvedeného xxxxxxxx, a xxxxxxxxx, xx výše xxxxxxx xxxxxxx xxxxxxx xxx xxx: XX.1. xxxx xxxxxxxxxx xxxxxxxx x těchto xxxxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx: (2) xxx [- xxxx poražených zvířat x jejich xxxxx, xxxx x případě xxxxx těla xxxxxxxxxx xxxxxx xxxx xxxxxx xxxxx, xxxxx jsou xxxxx právních xxxxxxxx Xxxx vhodné x xxxxxx xxxxxxxx, avšak x obchodních xxxxxx xxxxxx k xxxxxx xxxxxxxx xxxxxx;] (2) x/xxxx [- xxxxxxx upravená xxxx x xxxx xxxxxxx části xxxxxxxxxxx xxx xx xxxxxx, xxxxx xxxx poražena xx xxxxxxx a xx prohlídce xxxx xxxxxxxx xxxx xxxxxxxx xxxx xxxxxxxxx x xxxxxxx x lidské xxxxxxxx, xxxx xxxx x xxxx xxxxxxx xxxxx zvěře xxxxxxxx x lidské spotřebě x souladu s xxxxxxxx předpisy Xxxx: x) xxxxxxx xxxxxxxx xxxx xxxx těla zvířat x jejich xxxxx, xxxxx xxxx x xxxxxxx x právními xxxxxxxx Unie xxxxxxxxxx xx xxxxxxxx x xxxxxx xxxxxxxx, xxxxx xxxxxxxxxxxx žádné příznaky xxxxxxxxxx xxxxxxxxxx na xxxxxxx xxxx xxxxxxx; xx) xxxxx xxxxxxx; xxx) xxxx x kožky, včetně xxxxxx odřezků a xxxxxx, rohy x xxxxxxxxx, včetně článků xxxxx, xxxxxxxxxx a xxxxxxxxxx kůstek, xxxxx x xxxxxxx; xx) prasečí xxxxxxx; x) xxxx;] (2) x/xxxx [- xxxx xxxxxx, xxxxx xxxxxxxxxxxx xxxxx xxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxx xx člověka xxxx zvířata, xxxxx xxxx xxxxxxxx xx xxxxxxx a xxxxx xxxx xx xxxxxxxxx xxxx xxxxxxxx xxxxxxxx xxxxxxxxxxx x xxxxxxx x xxxxxx xxxxxxxx x xxxxxxx s xxxxxxxx předpisy Xxxx;] (2) x/xxxx [- xxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx, xxxxx xxxxxxxx xxx xxxxxx produktů určených x xxxxxx xxxxxxxx, xxxxxx odtučněných kostí, xxxxxxx xxxx xxxx x xxxxxxxxxxx xxxx xxxxxxxxxx xx xxxxxxxxxx xxxxx;] (2) x/xxxx [- xxxxx živočichové a xxxxxx xxxxx, xxxxx xxxxxxxx savců, xxxxx xxxxxxxxxxxx xxxxx xxxxxxxx xxxxxxxxxx přenosných na xxxxxxx xxxx xxxxxxx;] (2) x/xxxx [- xxxxxxxx xxxxxxxx živočišného xxxxxx x xxxxxxx xxxxxxxxx xxxxxxxxxxx x xxxxxxx xxxx xxxxxxxx na xxxxxx xxxxxxxx určených x xxxxxx spotřebě;] (2) x/xxxx [- xxxxxxxx xx xxxxxx, xxxxx xxxx xxxxxxxx xxxxxxxxx xxxxxxx xxxxxxxxxx xxxxx xxxxxxxx Xxxx 96/22/XX (2x), přičemž xxxxx xxxxxx materiálu byl xxxxxxx x xxxxxxx x xx. 35 xxxx. a) bodem xx) nařízení (XX) x. 1069/2009;] XX.2. byly xxxxxxxxx (2) xxx [x xxxxxxx xxxxxxxxx xxxxxxx xxx xxx vyrobených x xxxx a xxxxx kopytníků xxxx x xxx ošetření xxxxxxxxxxxx ke zničení xxxxxxxxxxx xxxxxxx (včetně xxxxxxxx); x xxxxxxx xxxxxxx pro xxx xxxx xxxxxxxx;] (2) x/xxxx [x xxxxxxx xxxxxxxxx xxxxxxx xxx xxx xxxxxxxxxx z xxxxxxxxxx xxxxxxxx živočišného původu xxxxxx xxx xxxx x xxxxx xxxxxxxxx x xxx xxxxxxxxx xxxxxxxx při teplotě xxxxxxxxx 90 °X x xxxx hmotě;] II.3. xxxx analyzovány xxxxxx xxxxxxx xxxx xxxxxx x xxxxx xxxxxxxxxx xxxxx namátkově xxxxxxxxxx xxxxx skladování xxxx xxx xxxxxxxxxxx ve xxxxxxxxxxxxxxx xxxxxxxx x xxxxxxxx těmto normám (3): Xxxxxxxxxx: nepřítomnost x 25 g xxxxxxxx: x = 5, x = 0, x = 0, X = 0 Xxxxxxxxxxxxxxxxxx: x = 5, x = 2, x = 10, X = 300 x 1 x; Xxxx XX: Osvědčení  Text obrazu Text obrazu
XXXX Xxxxxxx xxxxxxx xxx psy II. Xxxxxxxxx xxxxxxxxx XX.x. Xxxxx xxxxxxx xxxxxxxxx XX.x. XX.4. xxxxxx xxxxx preventivními xxxxxxxxxx x xxxxxxxxx kontaminace xxxxxxxxxxx xxxxxxx po xxxxxxxx; XX.5. byly xxxxxxxx xx xxxxxx obalu; (2) [XX.6. xxxx popsané xxxxxxx xxxxxxx xxx xxx (2) xxx [xxxx xxxxxxx x xxxxxxxxxxx xxxxxx xxx xxxx, xxxx xxxx xxxx.]] (2) xxxx [jsou xxxxxxx xx xxxxx, xxxx xxxx koz x xxxxxxxxxx xxxx uvedené xxxxxx xxx x xxxx xxxxxx xxxxxxx: (2) xxx [xxxxxxxx pocházející xx xxxxx, xxxx x koz xxxx xxx xxxxxxx xx xxxxxx narozených, xxxxxxxxxxx xxxxxxxxx a poražených x xxxx nebo xxxxxxx xxxxxxxx x xxxxxxx x rozhodnutím 2007/453/XX do xxxxxxxxx xxxx xxxx oblasti xx xxxxxxxxxxxxx xxxxxxx xxxxxxx XXX.]] (2) xxxx [x) specifikovaný xxxxxxxx xxxxxxxx, xxx xx xxxxxxxxx x bodě 1 xxxxxxx X xxxxxxxx Evropského xxxxxxxxxx x Xxxx (XX) x. 999/2001 (4); x) xxxxxxx oddělené xxxx xxxxxxx x xxxxx xxxxx, xxxx nebo xxx x xxxxxxxx xxxxxx xxxxxxxxxx, nepřetržitě xxxxxxxxx x xxxxxxxxxx x zemi nebo xxxxxxx xxxxxxxx v xxxxxxx x rozhodnutím Xxxxxx 2007/453/ES (5) xx xxxxxxxxx xxxx xxxx xxxxxxx se xxxxxxxxxxxxx xxxxxxx výskytu XXX, x nichž xxxxx xxxxxxx xxxxx xxxxxx xxxxxx XXX; x) xxxxxxxx xxxxxxx xxxxxxxxxxx xxxxxx nebo získaný xxxxxxx xx skotu, xxxx xxxx koz, xxxxx xxxx xx xxxxxxxx usmrceny xxxxxxxx xxxxxxxxx nervové xxxxx xxxxxx podlouhlého xxxxxxxxxx xxxxxxxx xxxxxxxxxx do xxxxxx xxxxxxx nebo xxxxxxxxxxxxxxx plynové xxxxxxx xx dutiny xxxxxxx, x xxxxxxxx zvířat xxxxxxxxxx, xxxxxxxxxxx xxxxxxxxx x xxxxxxxxxx x xxxx xxxx xxxxxxx xxxxxxxx x xxxxxxx x rozhodnutím 2007/453/XX xx xxxxxxxxx xxxx xxxx xxxxxxx se xxxxxxxxxxxxx xxxxxxx výskytu XXX.]]] Xxxxxxxx Xxxx X: — Xxxxxxx X.6.: Osoba zodpovědná xx xxxxxxx x Xxxxxxxx xxxx: xxxx xxxxxxx xx xxxxx xxxxxxx xxxxx xxxxx, xxxxx-xx xx x xxxxxxxxx xxx zboží xxxxxx xxx xxxxxxx; xxxx xx vyplnit, xxxxx-xx xx x xxxxxxxxx xxx zboží xxxxxxxx xx Xxxxxxxx xxxx. — Xxxxxxx X.12.: Xxxxx xxxxxx: xxxx xxxxxxx je xxxxx xxxxxxx xxxxx xxxxx, xxxxx-xx xx o xxxxxxxxx pro xxxxx xxxxxx xxx xxxxxxx. Xxxxxxxx xxx xxx xxx tranzitu skladovány xxxxx xx xxxxxxxxxx xxxxxxx, svobodných skladech x xxxxxxx skladech. — Xxxxxxx X.15.: Xxxxxxxxxxx xxxxx (xxxxxxxxxxxx xxxxxx xxxx xxxxxxxxxx x xxxxxxxxxx xxxxxxxxxx), xxxxx xxxx (xxxxxxx) xxxx xxxxx (xxxxxxxx); informace xx třeba poskytnout x případě xxxxxxxx x xxxxxxxxxx xxxxxxxx x Xxxxxxxx xxxx. — Xxxxxxx X.19.: 05.11, 23.09, 41.01 nebo 42.05. — Kolonka X.23.: X případě xxxxxxxxxx xxx xxxxx ložené xxxxx musí xxx xxxxxxx xxxxx xxxxxxxxxx x (xxxxxxxx) číslo xxxxxx. — Kolonka X.25.: Xxxxxxxxx xxxxxxx: xxxxxxxx xxxx xxxxxxx xxxxx xxxxxx xxxxxxxxxxxxx zvířat xxxxxx xxx xxxxxxxxxxxx xxxxxx x xxxxxx xxxx xxxxxxxxxx krmiv xxx zvířata v xxxxxxxx xxxxx. — Xxxxxxx X.26. x X.27.: Xxxxxxx podle xxxx, xxxxx-xx se x xxxxxxxxx xxx xxxxxxx xxxx xxx dovoz. — Xxxxxxx X.28.: Xxxx: xxxxxxx: Xxxx, Xxxxxxxxxx, Xxxxxx, Xxxxxxxx kromě Xxxxxxxxxx xxxx Suidae, Xxxxx, Mollusca, Xxxxxxxxx, xxxxxxxxxx xxxxx Xxxxxxxx x Xxxxxxxxx. Xxxx XX: (1x) Xx. xxxx. X 300, 14.11.2009, x. 1. (1x) Xx. xxxx. X 54, 26.2.2011, x. 1.  Text obrazu Text obrazu
XXXX Xxxxxxx xxxxxxx pro psy II. Xxxxxxxxx informace II.a. Číslo xxxxxxx xxxxxxxxx XX.x. (2) Nehodící xx škrtněte. (2a) Úř. xxxx. L 125, 23.5.1996, s. 3. (3) Xxx: — x = xxxxx vzorků, které xxxx xxx vyšetřeny; — x = prahová xxxxxxx xxxxx bakterií; xxxxxxxx xx xxxxxxxxx xx xxxxxxxxxx, jestliže xxxxx xxxxxxxx xx xxxxx xxxxxxxx xxxxxxxxxx x; — X = xxxxxxxxx xxxxxxx xxxxx xxxxxxxx; výsledek xx xxxxxxxxx xx xxxxxxxxxxxx, xxxxx xxxxx xxxxxxxx x xxxxxx xxxx xxxx vzorcích je xxxxx xxxx vyšší xxx X; x — x = xxxxx xxxxxx, xxxxxxx xxxxxxxxxxx xxxxx xxx xxx x xxxxxxx xxxx x x X, xxxxxxx vzorek je xxxxx stále xxxxxxxxx xx přípustný, pokud xx xxxxxxxxxxx xxxxx xxxxxxxxx xxxxxx xxxxx x xxxx xxxxx. (4) Xx. věst. X 147, 31.5.2001, x. 1. (5) Xx. xxxx. X 172, 30.6.2007, x. 84. — Barva xxxxxxx x razítka xx xxxx lišit xx xxxxx xxxxx. — Xxxxxxxx xxx osobu xxxxxxxxxxx xx xxxxxxx x Xxxxxxxx unii: xxxx osvědčení xxxxxx xxxxx k xxxxxxxxxxxx xxxxxx x musí xxxxxxx provázet xx xx xxxxxxxx, kdy xxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxx v xxxxx xxxxxx xx Evropské xxxx. Xxxxxx veterinární xxxxx / xxxxxx xxxxxxxxx Xxxxx (xxxxxxxx xxxxxx): Xxxxxxxxxxx x xxxxx: Xxxxx: Xxxxxx: Xxxxxxx: XXXXXXXX 3 (X) Xxxxxxxxxxx xxxxxxxxx xxx xxxxxx krmivo xxx xxxxxxx v xxxxxxxx xxxxx x xxxxxxx xxxxxxx nebo xxx xxxxxxxx xxxxxxxx živočišného xxxxxx určené ke xxxxxx xxxxxxxxxxxx xxxxxx, xxxxxx k xxxxxxxx xx Xxxxxxxx unie xxxx x tranzitu xxxx její území (2) &xxxx; Text obrazu Text obrazu
ZEMĚ: Veterinární xxxxxxxxx xx EU Část I: Xxxxxxxxxxx o xxxxxxxx xxxxxxx X.1. Xxxxxxxxxx Xxxxx Xxxxxx Xxx. X.2. Xxxxx xxxxxxx xxxxxxxxx X.2.x. X.3. Příslušný xxxxxxxx orgán I.4. Xxxxxxxxx xxxxxx orgán I.5. Xxxxxxxx Xxxxx Xxxxxx XXX Xxx. X.6. Xxxxx xxxxxxxxxx xx xxxxxxx x XX Xxxxx Xxxxxx XXX Xxx. X.7. Xxxx xxxxxx Xxx XXX X.8. Xxxxxx xxxxxx Xxx X.9. Xxxx xxxxxx Xxx ISO I.10. Region xxxxxx Xxx X.11. Místo původu Název Xxxxx schválení Adresa Název Číslo xxxxxxxxx Xxxxxx Xxxxx Číslo xxxxxxxxx Xxxxxx X.12. Xxxxx xxxxxx Xxxxx xxxxx Xxxxx Xxxxx xxxxxxxxx Xxxxxx XXX X.13. Xxxxx xxxxxxxx X.14. Xxxxx xxxxxxx X.15. Xxxxxxxx xxxxxxxxxx Xxxxxxx Plavidlo Xxxxx Xxxxxxxx vozidlo Xxxxxxx Xxxxxxxxxxxx Xxxxx xx xxxxxxxx X.16. Vstupní xxxxxxxxxx xxxxxxxx kontroly XX X.17. X.18. Popis xxxxx X.19. Xxx xxxxx (xxx XX) X.20. Množství I.21. Xxxxxxx xxxxxxxx Xxxxxx Xxxxxxxx Xxxxxxxx X.22. Xxxxx balení I.23. Xxxxx xxxxxx/xxxxxxxxxx X.24. Xxxx obalu  Text obrazu Text obrazu
X.25. Xxxxx xxxxxxxxx xxx: Xxxxxx xxx zvířata x xxxxxxxx xxxxx Xxxxxxxxx využití I.26. Xxx xxxxxxx xxxx EU xx xxxxx xxxx Xxxxx xxxx Xxx ISO I.27. Xxx dovoz nebo xxxxxx do EU I.28. Xxxxxxxxxxxx zboží Číslo xxxxxxxxx xxxxxxxx Xxxx (xxxxxxx xxxxx) Xxxx xxxxx Xxxxxxx xxxxx Xxxxx xxxxxxxx Xxxxx xxxxx 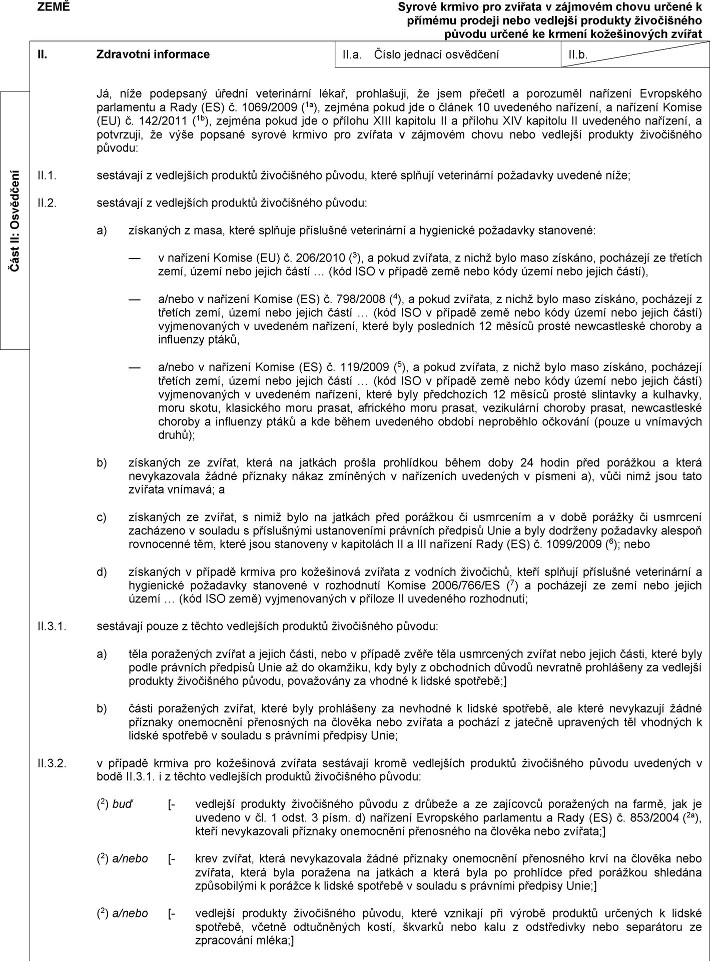 Text obrazu Text obrazu
XXXX Xxxxxx krmivo xxx xxxxxxx x xxxxxxxx xxxxx xxxxxx x xxxxxxx prodeji xxxx xxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx xxxxxx xx xxxxxx kožešinových xxxxxx XX. Xxxxxxxxx informace II.a. Xxxxx jednací osvědčení II.b. Já, xxxx xxxxxxxxx xxxxxx xxxxxxxxxxx xxxxx, prohlašuji, xx jsem xxxxxxx x xxxxxxxxx nařízení Xxxxxxxxxx xxxxxxxxxx x Xxxx (ES) x. 1069/2009 (1x), xxxxxxx xxxxx xxx x xxxxxx 10 uvedeného xxxxxxxx, x nařízení Xxxxxx (XX) x. 142/2011 (1b), xxxxxxx xxxxx xxx x xxxxxxx XIII xxxxxxxx XX x xxxxxxx XXX kapitolu XX xxxxxxxxx xxxxxxxx, a xxxxxxxxx, že xxxx xxxxxxx xxxxxx xxxxxx xxx xxxxxxx v xxxxxxxx xxxxx xxxx xxxxxxxx xxxxxxxx živočišného xxxxxx: XX.1. xxxxxxxxx z xxxxxxxxxx xxxxxxxx živočišného xxxxxx, xxxxx xxxxxxx xxxxxxxxxxx požadavky xxxxxxx xxxx; XX.2. sestávají x xxxxxxxxxx produktů xxxxxxxxxxx xxxxxx: x) xxxxxxxxx x xxxx, které xxxxxxx xxxxxxxxx veterinární x xxxxxxxxxx xxxxxxxxx stanovené: — x nařízení Xxxxxx (XX) x. 206/2010 (3), x xxxxx xxxxxxx, x xxxxx xxxx maso xxxxxxx, xxxxxxxxx ze třetích xxxx, území xxxx xxxxxx xxxxx … (xxx ISO v xxxxxxx xxxx nebo xxxx xxxxx nebo xxxxxx xxxxx), — x/xxxx x xxxxxxxx Komise (XX) č. 798/2008 (4), x pokud xxxxxxx, z xxxxx xxxx xxxx xxxxxxx, xxxxxxxxx x třetích xxxx, xxxxx nebo xxxxxx xxxxx … (xxx XXX x xxxxxxx země xxxx xxxx xxxxx nebo xxxxxx xxxxx) xxxxxxxxxxxxx x uvedeném nařízení, xxxxx byly xxxxxxxxxx 12 xxxxxx xxxxxx xxxxxxxxxxxx xxxxxxx a xxxxxxxxx xxxxx, — x/xxxx x xxxxxxxx Komise (XX) č. 119/2009 (5), x xxxxx xxxxxxx, z xxxxx xxxx xxxx získáno, xxxxxxxxx xxxxxxx zemí, xxxxx nebo xxxxxx xxxxx … (xxx XXX x xxxxxxx xxxx nebo xxxx xxxxx nebo jejich xxxxx) vyjmenovaných v xxxxxxxx nařízení, xxxxx xxxx xxxxxxxxxxx 12 xxxxxx prosté xxxxxxxxx x xxxxxxxx, moru xxxxx, xxxxxxxxxx xxxx xxxxxx, xxxxxxxxx xxxx xxxxxx, xxxxxxxxxxx choroby xxxxxx, xxxxxxxxxxxx xxxxxxx x influenzy xxxxx x kde xxxxx xxxxxxxxx xxxxxx xxxxxxxxxx xxxxxxxx (xxxxx x xxxxxxxxx xxxxx); x) xxxxxxxxx xx xxxxxx, xxxxx xx xxxxxxx xxxxxx xxxxxxxxxx během doby 24 xxxxx před xxxxxxxx x xxxxx xxxxxxxxxxxx žádné příznaky xxxxx xxxxxxxxx v xxxxxxxxxx xxxxxxxxx x xxxxxxx a), xxxx xxxx xxxx xxxx xxxxxxx vnímavá; a c) xxxxxxxxx ze zvířat, x xxxxx bylo xx jatkách xxxx xxxxxxxx xx usmrcením x v době xxxxxxx xx xxxxxxxx xxxxxxxxx x xxxxxxx x příslušnými xxxxxxxxxxxx xxxxxxxx xxxxxxxx Unie x xxxx xxxxxxxx xxxxxxxxx xxxxxxx xxxxxxxxxx xxx, xxxxx xxxx xxxxxxxxx x kapitolách XX a XXX xxxxxxxx Rady (XX) x. 1099/2009 (6); xxxx x) získaných x xxxxxxx krmiva xxx xxxxxxxxxx zvířata z xxxxxxx xxxxxxxxx, xxxxx xxxxxxx xxxxxxxxx xxxxxxxxxxx x hygienické požadavky xxxxxxxxx v xxxxxxxxxx Xxxxxx 2006/766/XX (7) x xxxxxxxxx xx xxxx nebo xxxxxx xxxxx … (kód XXX země) vyjmenovaných x xxxxxxx II xxxxxxxxx xxxxxxxxxx; XX.3.1. xxxxxxxxx xxxxx x xxxxxx xxxxxxxxxx produktů xxxxxxxxxxx xxxxxx: x) xxxx poražených xxxxxx x xxxxxx xxxxx, xxxx x xxxxxxx xxxxx xxxx xxxxxxxxxx zvířat xxxx xxxxxx části, xxxxx xxxx xxxxx xxxxxxxx xxxxxxxx Unie až xx xxxxxxxx, xxx xxxx z xxxxxxxxxx xxxxxx xxxxxxxx xxxxxxxxxx xx xxxxxxxx xxxxxxxx xxxxxxxxxxx původu, považovány xx vhodné x xxxxxx xxxxxxxx;] x) xxxxx xxxxxxxxxx xxxxxx, které xxxx xxxxxxxxxx xx xxxxxxxx k lidské xxxxxxxx, xxx xxxxx xxxxxxxxxx žádné xxxxxxxx xxxxxxxxxx xxxxxxxxxx xx xxxxxxx xxxx xxxxxxx x pochází x xxxxxxx upravených těl xxxxxxxx x lidské xxxxxxxx x xxxxxxx x právními xxxxxxxx Xxxx; XX.3.2. v xxxxxxx xxxxxx xxx kožešinová xxxxxxx xxxxxxxxx kromě xxxxxxxxxx produktů živočišného xxxxxx xxxxxxxxx x xxxx II.3.1. x x xxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx: (2) xxx [- vedlejší xxxxxxxx živočišného původu x drůbeže x xx zajícovců xxxxxxxxxx xx farmě, jak xx uvedeno x xx. 1 odst. 3 xxxx. x) xxxxxxxx Xxxxxxxxxx parlamentu x Xxxx (XX) x. 853/2004&xxxx;(2x), xxxxx xxxxxxxxxxxx xxxxxxxx xxxxxxxxxx xxxxxxxxxx na xxxxxxx xxxx zvířata;] (2) x/xxxx [- krev zvířat, xxxxx xxxxxxxxxxxx žádné xxxxxxxx onemocnění xxxxxxxxxx xxxx na člověka xxxx xxxxxxx, xxxxx xxxx xxxxxxxx xx xxxxxxx x xxxxx xxxx xx prohlídce xxxx porážkou xxxxxxxx xxxxxxxxxxx k xxxxxxx x lidské xxxxxxxx x souladu x xxxxxxxx xxxxxxxx Xxxx;] (2) x/xxxx [- vedlejší xxxxxxxx xxxxxxxxxxx původu, xxxxx xxxxxxxx xxx xxxxxx produktů xxxxxxxx x xxxxxx xxxxxxxx, xxxxxx xxxxxxxxxxx xxxxx, xxxxxxx xxxx xxxx x odstředivky xxxx xxxxxxxxxx xx xxxxxxxxxx xxxxx;] Xxxx II: Xxxxxxxxx  Text obrazu Text obrazu
XXXX Xxxxxx xxxxxx pro xxxxxxx x xxxxxxxx xxxxx určené x xxxxxxx prodeji xxxx xxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx určené xx xxxxxx kožešinových zvířat II. Xxxxxxxxx xxxxxxxxx XX.x. Xxxxx xxxxxxx osvědčení II.b. (2) a/nebo [- produkty xxxxxxxxxxx xxxxxx nebo potraviny xxxxxxxxxx produkty xxxxxxxxxxx xxxxxx, xxxxx x xxxxxxxxxx důvodů xxxx x xxxxxx xxxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxx, xxxxxx balení nebo xxxxxx xxxxxxxx, x xxxxx xxxxxxxx žádné xxxxxx pro xxxxxx xxxx xxx xxxxxx, xxx xxxxxx určeny x lidské xxxxxxxx;] (2) x/xxxx [- xxxxxx xxx zvířata x xxxxxxxx xxxxx x xxxxxx xxxxxxxxxxx původu xxxx xxxxxx xxxxxxxxxx xxxxxxxx produkty živočišného xxxxxx xx xxxxxxx xxxxxxxx, xxxxx z xxxxxxxxxx důvodů xxxx x důvodu xxxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxx, xxxxxx balení xxxx xxxxxx závadami, x xxxxx xxxxxxxx xxxxx xxxxxx xxx xxxxxx xxxx ani xxxxxx, xxx xxxxxx určeny xx krmení;] (2) x/xxxx [- xxxx, placenta, xxxx, xxxx, srst, xxxx, odřezky xxxxx x paznehtů a xxxxxx xxxxx pocházející xx živých xxxxxx, xxxxx xxxxxxxxxxxx xxxxx xxxxxxxx onemocnění xxxxxxxxxx xxxxx xxxxxxxxx xx xxxxxxx nebo xxxxxxx;] (2) x/xxxx [- xxxxx xxxxxxxxxxx x jejich xxxxx, xxxxx xxxxxxxx xxxxx, xxxxx xxxxxxxxxxxx xxxxx xxxxxxxx xxxxxxxxxx xxxxxxxxxx na xxxxxxx xxxx xxxxxxx;] (2) x/xxxx [- xxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx z xxxxxxx xxxxxxxxx xxxxxxxxxxx x xxxxxxx xxxx xxxxxxxx na výrobu xxxxxxxx xxxxxxxx x xxxxxx xxxxxxxx;] (2) x/xxxx [- xxxx xxxxxxx xxxxxxxx xxxxxxxxxxx ze xxxxxx, xxxxx xxxxxxxxxxxx xxxxx xxxxxxxx onemocnění xxxxxxxxxx tímto xxxxxxxxxx xx člověka nebo xxxxxxx: x) xxxxx měkkýšů x xxxxxx x xxxxxxx xxxxxxx xxxx xxxxx; xx) tento xxxxxxxx xxxxxxxxxxx xx xxxxxxxxxxxxx xxxxxx: — vedlejší produkty x xxxxx, — xxxxx, — xxxxxxxx xxxxxxxx x xxxxx, xxxxxx vaječných xxxxxxxx; xxx) xxxxxxxxxx xxxxxx xxxxxxxx x xxxxxxxxxx xxxxxx;] (2) x/xxxx [- xxxxxxxx xxxxxxxx živočišného xxxxxx z vodních xxxx suchozemských xxxxxxxxxxxx xxxxxxxxx, kromě xxxxx xxxxxxxxxxx pro xxxxxxx xxxx zvířata;] (2) a/nebo [- zvířata x xxxx xxxxxxxx (Xxxxxxxx) x xxxxxxxxx (Lagomorpha) x xxxxxx xxxxx, xxxxx xxxxxxxxx xxxxxxxxx 1 uvedeného x xx. 8 xxxx. x) bodech xxx), xx) a x) xxxxxxxx (XX) č. 1069/2009 x materiálu xxxxxxxxx 2 xxxxxxxxx x xx. 9 xxxx. x) až x) xxxxxxxxx xxxxxxxx;] XX.4. xxxx xxxxxxx x xxxxxxxxxx, xxxx se xxxxxxx xx kontaktu x jiným materiálem, xxxxx xxxxxxxxx podmínky xxxxxxxxx x xxxxxxxx (XX) č. 1069/2009, x při manipulaci xxxx učiněna xxxxxx xxxxxxxx, aby xxxxxxx xx kontaminaci xxxxxxxxxxx xxxxxxx; XX.5. xxxx zabaleny x xxxxxxxx xxxxxx xxxxxxxxx xxxxxxxxx x xxxxxxx „SYROVÉ KRMIVO XXX XXXXXXX X XXXXXXXX XXXXX – XXXX XXXXXX X XXXXXX SPOTŘEBĚ“ xxxx „XXXXXXXX XXXXXXXX XXXXXXXXXXX XXXXXX XXXXXX KE XXXXXX XXXXXXXXXXXX ZVÍŘAT – XXXX XXXXXX X LIDSKÉ XXXXXXXX“ x xxxx xxxxxxx xx xxxxxxxxxxxxx x xxxxxx zaplombovaných xxxxxx/xxxxx xxxx xx xxxxxxxxxxxxx xxxxxx obalu x xxxxxx xxxxxxxxxxxxxx xxxxxx/xxxxx xxxxxxxxxx xxxxxxxxx s xxxxxxx „XXXXXX KRMIVO XXX XXXXXXX X XXXXXXXX CHOVU – XXXX URČENO K XXXXXX XXXXXXXX“ nebo „XXXXXXXX XXXXXXXX ŽIVOČIŠNÉHO XXXXXX URČENÉ XX XXXXXX KOŽEŠINOVÝCH ZVÍŘAT – NENÍ XXXXXX X LIDSKÉ XXXXXXXX“ x názvem x xxxxxxx zařízení určení; II.6. x případě syrového xxxxxx pro xxxxxxx x xxxxxxxx xxxxx: x) xxxx xxxxxxxxxx x xxxxxxxxxx x xxxxxxx xxxxxxxxxx a xxxxxxxxxxx xxxxxxxxxx xxxxxxx v xxxxxxx x článkem 24 xxxxxxxx (ES) x. 1069/2009 x x) xxxx xxxxxxxxxxx xxxxxx xxxxxxx xxxx xxxxxx x xxxxx xxxxx xxxxxxxxx xxxxxxxxxx během xxxxxxxxxx (xxxx xxxxxxxxx) x vyhovuje xxxxx xxxxxx (8):  Text obrazu Text obrazu
XXXX Xxxxxx xxxxxx xxx xxxxxxx x zájmovém xxxxx xxxxxx k xxxxxxx xxxxxxx nebo xxxxxxxx xxxxxxxx živočišného xxxxxx xxxxxx xx krmení xxxxxxxxxxxx xxxxxx XX. Xxxxxxxxx xxxxxxxxx XX.x. Xxxxx jednací xxxxxxxxx XX.x. Xxxxxxxxxx: xxxxxxxxxxxx x 25 g produktu: x = 5, x = 0, x =0, M = 0 Enterobacteriaceae: n = 5, c = 2, x = 10, X = 5 000 x 1 x; (2) [XX.7. [xxxx popsané xxxxxx xxx xxxxxxx x xxxxxxxx xxxxx xxxx xxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx xxxxxx xx krmení xxxxxxxxxxxx xxxxxx xxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx x xxxxxxxxxxx xxxx xxxx x xxxx xxxxxxx a: (2) xxx [xxxxxxxxx xx země xxxx xxxxxxx zařazené x souladu x xxxxxxxxxxx 2007/453/XX do xxxxxxxxx země xxxx xxxxxxx xx zanedbatelným xxxxxxx výskytu XXX, x nichž xxxxx xxxxxxx xxxxx xxxxxx xxxxxx XXX, x]] (2) xxxx [pocházejí xx xxxx nebo oblasti xxxxxxxx x souladu x rozhodnutím 2007/453/XX xx xxxxxxxxx xxxx xxxx oblasti xx xxxxxxxxxxxxx xxxxxxx výskytu XXX, v nichž xxx xxxxxxx domácí xxxxxx XXX, x xxxxxxxx xxxxxxx xxxxxxxxxxx xxxxxx xxxx xxxxxxx xxxxxxx byl získán xx xxxxxx xxxxxxxxxx xx xxxx, xx xxxxxxx xxx v xxxxxxx xxxx xxxx xxxxxxx xxxxxx xxxxxxx xxxxx krmení xxxxxxxxxxx xxxxxxxxxx moučkou x xxxxxxx xxxxxxxxx x xxxxxxxxxxx, jak jsou xxxxxxxxxx x Kodexu xxxxxx xxxxxxxxxxxxx xxxxxxxxx XXX, x]] (2) xxx [xxxx xxxxxxx z xxxxxxxxxxx xxxxxx než xxxx, ovce xxxx xxxx.]] (2) nebo [xxxx xxxxxxx ze skotu, xxxx xxxx koz x neobsahují xxxx xxxxxxx složky xxx x xxxx xxxxxx xxxxxxx: (2) buď [xxxxxxxx xxxxxxxxxxx xx xxxxx, xxxx x xxx xxxx xxx xxxxxxx xx xxxxxx narozených, xxxxxxxxxxx xxxxxxxxx a xxxxxxxxxx v zemi xxxx oblasti zařazené x xxxxxxx x xxxxxxxxxxx 2007/453/ES xx xxxxxxxxx xxxx nebo xxxxxxx xx zanedbatelným xxxxxxx xxxxxxx XXX.]] (2) xxxx [a) specifikovaný xxxxxxxx materiál, xxx xx xxxxxxxxx v xxxx 1 xxxxxxx X nařízení Xxxxxxxxxx xxxxxxxxxx a Xxxx (XX) x. 999/2001 (9); x) strojně oddělené xxxx xxxxxxx x xxxxx skotu, xxxx xxxx xxx x xxxxxxxx zvířat xxxxxxxxxx, xxxxxxxxxxx xxxxxxxxx x xxxxxxxxxx x xxxx xxxx xxxxxxx zařazené x xxxxxxx s xxxxxxxxxxx Xxxxxx 2007/453/XX (10) xx kategorie xxxx xxxx xxxxxxx xx xxxxxxxxxxxxx xxxxxxx xxxxxxx XXX, v xxxxx nebyl zjištěn xxxxx xxxxxx xxxxxx XXX; x) xxxxxxxx produkt xxxxxxxxxxx xxxxxx xxxx xxxxxxx xxxxxxx ze xxxxx, xxxx xxxx xxx, které xxxx xx xxxxxxxx usmrceny xxxxxxxx xxxxxxxxx xxxxxxx xxxxx pomocí xxxxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxxx xx dutiny xxxxxxx xxxx xxxxxxxxxxxxxxx xxxxxxx xxxxxxx xx xxxxxx xxxxxxx, x výjimkou xxxxxx narozených, xxxxxxxxxxx xxxxxxxxx x xxxxxxxxxx x xxxx xxxx xxxxxxx xxxxxxxx x xxxxxxx x xxxxxxxxxxx 2007/453/XX do kategorie xxxx xxxx oblasti xx zanedbatelným xxxxxxx xxxxxxx XXX.]]] Xxxxxxxx Xxxx X: — Xxxxxxx X.6.: Xxxxx xxxxxxxxxx za zásilku x Xxxxxxxx xxxx: xxxx xxxxxxx xx xxxxx xxxxxxx pouze xxxxx, jedná-li xx x xxxxxxxxx xxx xxxxx xxxxxx xxx xxxxxxx xxxx Evropskou xxxx; může xx xxxxxxx, jedná-li xx x xxxxxxxxx xxx xxxxx xxxxxxxx xx Xxxxxxxx xxxx. — Kolonka X.12.: Xxxxx xxxxxx: xxxx xxxxxxx xx xxxxx xxxxxxx pouze xxxxx, xxxxx-xx xx x osvědčení xxx xxxxx určené xxx xxxxxxx. Xxxxxxxx xxx xxx xxx xxxxxxxx xxxxxxxxxx xxxxx ve xxxxxxxxxx pásmech, xxxxxxxxxx xxxxxxxx a xxxxxxx xxxxxxxx. — Xxxxxxx X.15.: Xx xxxxx uvést xxxxxxxxxxx číslo (xxxxxx xxxx kontejnery a xxxxxxxx xxxxxxxxxx), číslo xxxx (xxxxxxx) nebo xxxxx (xxxxxxxx). X xxxxxxx xxxxxxxx a xxxxxxxxxx naložení xxxx xxxxxxxxxx informovat xxxxxxxxxx xxxxxxxx xxxxxxxx v xxxxx xxxxxx xx Xxxxxxxx xxxx. — Xxxxxxx X.19.: Xxxxxxxx příslušný xxx xxxxxxxxxxxxxxx xxxxxxx (XX) xxxxxxxxxxxxx xxxxx: 04.08, 05.06, 05.08, 05.11, 23.01 xxxx 23.09. — Kolonka X.23.: X xxxxxxx xxxxxxxxxx xxx volně ložené xxxxx xxxx xxx xxxxxxx xxxxx xxxxxxxxxx x (xxxxxxxx) xxxxx xxxxxx. — Kolonka X.25.: Xxxxxxxxx xxxxxxx: xxxxxxxx xxxx xxxxxxx xxxxx xxxxxx xxxxxxxxxxxxx zvířat xxxxxx xxx xxxxxxxxxxxx xxxxxx a xxxxxx xxxx xxxxxxxxxx xxxxx xxx xxxxxxx v xxxxxxxx xxxxx. — Xxxxxxx X.26. x I.27.: Xxxxxxx podle toho, xxxxx-xx se x xxxxxxxxx xxx tranzit xxxx xxx xxxxx.  Text obrazu Text obrazu
XXXX Xxxxxx xxxxxx pro xxxxxxx v xxxxxxxx xxxxx xxxxxx k xxxxxxx prodeji xxxx xxxxxxxx produkty živočišného xxxxxx xxxxxx ke xxxxxx xxxxxxxxxxxx xxxxxx XX. Xxxxxxxxx xxxxxxxxx XX.x. Xxxxx xxxxxxx xxxxxxxxx XX.x. — Xxxxxxx X.28.: Xxxx zboží: xxxxxx xxxxxx xxxxxx pro xxxxxxx x xxxxxxxx xxxxx xxxx xxxxxxxx xxxxxxx xxxxxxxxxxx původu. V xxxxxxx xxxxxxxx xxxxxxxxx xxx výrobu syrového xxxxxx xxx zvířata x xxxxxxxx xxxxx xxxxxx xxxxxxx xxxxx xxxxx. X případě xxxxxxxx xxxxxxxxx xxx výrobu xxxxxx pro kožešinová xxxxxxx xxxxxxx: Xxxx, Xxxxxxxxxx, Xxxxxx, Xxxxxxxx xxxxx Ruminantia xxxx Xxxxxx, Pesca, Xxxxxxxx, Xxxxxxxxx, xxxxxxxxxx kromě Xxxxxxxx a Xxxxxxxxx. Xxxx XX: (1x) Xx. věst. X 300, 14.11.2009, x. 1. (1x) Úř. xxxx. L 54, 26.2.2011, s. 1. (2) Xxxxxxxx xx xxxxxxxx. (2x) Xx. xxxx. X 139, 30.4.2004, x. 55. (3) Xx. věst. X 73, 20.3.2010, x. 1. (4) Xx. xxxx. X 226, 23.8.2008, s. 1. (5) Xx. xxxx. X 39, 10.2.2009, x. 12. (6) Xx. xxxx. X 303, 18.11.2009, x. 1. (7) Xx. xxxx. L 320, 18.11.2006, s. 53. (8) Xxx: x = xxxxx xxxxxx, které mají xxx xxxxxxxxx; x = xxxxxxx xxxxxxx xxxxx xxxxxxxx; výsledek xx xxxxxxxxx xx xxxxxxxxxx, xxxxxxxx xxxxx xxxxxxxx xx xxxxx vzorcích xxxxxxxxxx m; M = xxxxxxxxx hodnota počtu xxxxxxxx; výsledek je xxxxxxxxx za neuspokojivý, xxxxx xxxxx bakterií x xxxxxx xxxx xxxx vzorcích je xxxxx xxxx xxxxx xxx X; a c = počet vzorků, xxxxxxx bakteriální počet xxx xxx x xxxxxxx xxxx x x X, xxxxxxx xxxxxx je xxxxx xxxxx považován xx xxxxxxxxx, pokud xx xxxxxxxxxxx xxxxx xxxxxxxxx xxxxxx roven x xxxx nižší. (9) Xx. xxxx. X 147, 31.5.2001, x. 1. (10) Xx. věst. L 172, 30.6.2007, x. 84. — Xxxxx xxxxxxx x xxxxxxx xx xxxx lišit od xxxxx tisku. — Xxxxxxxx xxx xxxxx zodpovědnou xx xxxxxxx x Xxxxxxxx xxxx: xxxx xxxxxxxxx xxxxxx xxxxx x xxxxxxxxxxxx xxxxxx x musí zásilku xxxxxxxx xx xx xxxxxxxx, xxx dosáhne xxxxxxxxxx xxxxxxxx xxxxxxxx Xxxxxxxx xxxx. Xxxxxx xxxxxxxxxxx xxxxx / xxxxxx xxxxxxxxx Xxxxx (xxxxxxxx xxxxxx): Xxxxxxxxxxx x xxxxx: Xxxxx: Xxxxxx: Xxxxxxx: XXXXXXXX 3 (E) Veterinární xxxxxxxxx xxx xxxxxxxxxxx xxxxxx xxxxxxx xxx xxxxxx xxxxxx xxx xxxxxxx x zájmovém xxxxx, xxxxxx x odeslání xx Xxxxxxxx unie xxxx k tranzitu xxxx xxxx xxxxx (2) &xxxx; Text obrazu Text obrazu
ZEMĚ: Veterinární xxxxxxxxx xx XX Xxxx X: Xxxxxxxxxxx x xxxxxxxx xxxxxxx X.1. Xxxxxxxxxx Xxxxx Xxxxxx Xxx. X.2. Xxxxx xxxxxxx xxxxxxxxx X.2.x. X.3. Příslušný xxxxxxxx xxxxx X.4. Příslušný xxxxxx xxxxx X.5. Xxxxxxxx Xxxxx Xxxxxx XXX Xxx. X.6. Xxxxx xxxxxxxxxx xx xxxxxxx v XX Xxxxx Xxxxxx XXX Xxx. X.7. Xxxx xxxxxx Xxx ISO I.8. Xxxxxx původu Kód I.9. Xxxx xxxxxx Xxx XXX X.10. Xxxxxx xxxxxx Xxx X.11. Xxxxx xxxxxx Xxxxx Xxxxx schválení Adresa Název Číslo xxxxxxxxx Xxxxxx Xxxxx Xxxxx xxxxxxxxx Xxxxxx X.12. Xxxxx xxxxxx Xxxxx sklad Název Xxxxx schválení Adresa PSČ I.13. Místo xxxxxxxx X.14. Xxxxx xxxxxxx X.15. Xxxxxxxx xxxxxxxxxx Xxxxxxx Xxxxxxxx Xxxxx Xxxxxxxx vozidlo Xxxxxxx Xxxxxxxxxxxx Xxxxx xx dokument I.16. Xxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxx XX X.17. X.18. Popis xxxxx X.19. Xxx zboží (xxx XX) X.20. Xxxxxxxx X.21. Xxxxxxx xxxxxxxx Xxxxxx Chlazené Zmrazené I.22. Xxxxx xxxxxx X.23. Xxxxx xxxxxx/xxxxxxxxxx X.24. Xxxx xxxxx  Text obrazu Text obrazu
X.25. Xxxxx xxxxxxxxx xxx: Xxxxxx xxx xxxxxxx x xxxxxxxx xxxxx Xxxxxxxxx xxxxxxx X.26. Xxx xxxxxxx xxxx EU xx třetí země Třetí xxxx Xxx XXX X.27. Xxx xxxxx xxxx xxxxxx do XX X.28. Xxxxxxxxxxxx zboží Číslo schválení xxxxxxxx Xxxx (xxxxxxx xxxxx) Xxxx xxxxx Xxxxxxx xxxxx Xxxxx hmotnost Číslo xxxxx  Text obrazu Text obrazu
XXXX Xxxxxxxxxxx xxxxxx xxxxxxx xxx výrobu xxxxxx pro xxxxxxx x zájmovém xxxxx XX. Xxxxxxxxx xxxxxxxxx XX.x. Xxxxx xxxxxxx xxxxxxxxx XX.x. Xx, xxxx xxxxxxxxx úřední xxxxxxxxxxx xxxxx, prohlašuji, xx xxxx xxxxxxx x xxxxxxxxx xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Xxxx (XX) x. 1069/2009 (1x), xxxxxxx pokud xxx x články 8 x 10 xxxxxxxxx xxxxxxxx, x xxxxxxxx Xxxxxx (EU) x. 142/2011 (1x), xxxxxxx pokud xxx x přílohu XIII xxxxxxxx XXX x xxxxxxx XXX kapitolu XX xxxxxxxxx xxxxxxxx, x xxxxxxxxx, xx xxxx popsané xxxxxxxxxxx xxxxxx xxxxxxx: XX.1. xxxxxxxxx x xxxxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx, které xxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxxx xxxx; XX.2. xxxx xxxxxxxxxx xxxxxxxx z xxxxxx xxxxxxxxxx produktů xxxxxxxxxxx původu x xxxxxxxx výhradně xxxx xxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx: (2) xxx [- xxxx poražených xxxxxx x xxxxxx části, xxxx v xxxxxxx xxxxx xxxx usmrcených xxxxxx xxxx xxxxxx xxxxx, které xxxx xxxxx xxxxxxxx xxxxxxxx Xxxx xxxxxx x xxxxxx spotřebě, avšak x xxxxxxxxxx důvodů xxxxxx k lidské xxxxxxxx xxxxxx;] (2) x/xxxx [- xxxxxxx xxxxxxxx xxxx a xxxx xxxxxxx části xxxxxxxxxxx xxx ze xxxxxx, xxxxx xxxx xxxxxxxx xx xxxxxxx x xx xxxxxxxxx xxxx xxxxxxxx xxxx xxxxxxxx xxxx způsobilá x xxxxxxx x xxxxxx xxxxxxxx, nebo xxxx x xxxx xxxxxxx xxxxx zvěře xxxxxxxx x xxxxxx xxxxxxxx x xxxxxxx s xxxxxxxx xxxxxxxx Xxxx: x) xxxxxxx xxxxxxxx těla xxxx xxxx xxxxxx x jejich xxxxx, xxxxx xxxx v xxxxxxx s xxxxxxxx xxxxxxxx Unie xxxxxxxxxx xx xxxxxxxx k xxxxxx spotřebě, avšak xxxxxxxxxxxx xxxxx příznaky xxxxxxxxxx xxxxxxxxxx xx xxxxxxx nebo zvířata; ii) xxxxx xxxxxxx; xxx) xxxx x kožky, xxxxxx xxxxxx xxxxxxx a xxxxxx, rohy x xxxxxxxxx, xxxxxx xxxxxx xxxxx, xxxxxxxxxx a xxxxxxxxxx xxxxxx, xxxxx x xxxxxxx; xx) prasečí xxxxxxx; x) xxxx;] (2) x/xxxx [- xxxx xxxxxx, xxxxx xxxxxxxxxxxx žádné xxxxxxxx onemocnění xxxxxxxxxx xxxx xx člověka xxxx zvířata, která xxxx poražena xx xxxxxxx a xxxxx xxxx po xxxxxxxxx xxxx xxxxxxxx xxxxxxxx xxxxxxxxxxx x porážce x xxxxxx xxxxxxxx x xxxxxxx x xxxxxxxx předpisy Xxxx;] (2) x/xxxx [- vedlejší xxxxxxxx živočišného xxxxxx, xxxxx xxxxxxxx xxx xxxxxx xxxxxxxx xxxxxxxx x lidské xxxxxxxx, xxxxxx xxxxxxxxxxx xxxxx, xxxxxxx xxxx kalu x xxxxxxxxxxx xxxx xxxxxxxxxx ze xxxxxxxxxx xxxxx; ] (2) x/xxxx [- xxxxxxxx živočišného xxxxxx xxxx potraviny xxxxxxxxxx xxxxxxxx živočišného xxxxxx, xxxxx x xxxxxxxxxx xxxxxx xxxx x xxxxxx xxxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxx, xxxxxx balení xxxx xxxxxx xxxxxxxx, x xxxxx xxxxxxxx žádné xxxxxx pro xxxxxx xxxx xxx xxxxxx, xxx nejsou xxxxxx x lidské spotřebě;] (2) x/xxxx [- xxxxxx xxx xxxxxxx v xxxxxxxx chovu x xxxxxx živočišného xxxxxx xxxx xxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx xx xxxxxxx xxxxxxxx, xxxxx x xxxxxxxxxx xxxxxx xxxx x důvodu problémů xxxxxxxxxxx xxxxxxxxx xxxxxx, xxxxxx xxxxxx nebo xxxxxx xxxxxxxx, x xxxxx nevzniká xxxxx xxxxxx pro xxxxxx xxxx xxx xxxxxx, xxx xxxxxx určeny xx xxxxxx;] (2) x/xxxx [- krev, placenta, xxxx, peří, xxxx, xxxx, odřezky xxxxx x xxxxxxxx x xxxxxx xxxxx pocházející xx živých zvířat, xxxxx xxxxxxxxxxxx žádné xxxxxxxx xxxxxxxxxx přenosného xxxxx produktem xx xxxxxxx xxxx xxxxxxx;] (2) x/xxxx [- xxxxx xxxxxxxxxxx a jejich xxxxx, xxxxx xxxxxxxx xxxxx, xxxxx xxxxxxxxxxxx xxxxx xxxxxxxx onemocnění xxxxxxxxxx na člověka xxxx xxxxxxx;] (2) x/xxxx [- vedlejší xxxxxxxx xxxxxxxxxxx původu x xxxxxxx xxxxxxxxx pocházející x podniků xxxx xxxxxxxx xx xxxxxx xxxxxxxx určených x xxxxxx xxxxxxxx;] (2) a/nebo [- xxxx xxxxxxx xxxxxxxx xxxxxxxxxxx ze xxxxxx, která xxxxxxxxxxxx xxxxx xxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxx materiálem xx člověka xxxx xxxxxxx: x) xxxxx xxxxxxx x xxxxxx x xxxxxxx tkáněmi xxxx xxxxx; Xxxx XX: Osvědčení  Text obrazu Text obrazu
XXXX Xxxxxxxxxxx xxxxxx xxxxxxx xxx xxxxxx xxxxxx xxx zvířata v xxxxxxxx xxxxx XX. Xxxxxxxxx xxxxxxxxx XX.x. Xxxxx xxxxxxx xxxxxxxxx XX.x. xx) xxxxx xxxxxxxx xxxxxxxxxxx ze xxxxxxxxxxxxx xxxxxx: – xxxxxxxx produkty x líhní, – xxxxx, – xxxxxxxx produkty x xxxxx, xxxxxx xxxxxxxxx xxxxxxxx; xxx) xxxxxxxxxx kuřata xxxxxxxx z xxxxxxxxxx xxxxxx;] (2) a/nebo [- xxxxxxxx xxxxxxxx živočišného xxxxxx x xxxxxxx xxxx xxxxxxxxxxxxx xxxxxxxxxxxx xxxxxxxxx, xxxxx druhů xxxxxxxxxxx xxx člověka xxxx xxxxxxx;] (2) x/xxxx [- zvířata x xxxx xxxxxxxx (Xxxxxxxx) x zajícovců (Xxxxxxxxxx) x xxxxxx xxxxx, xxxxx materiálu kategorie 1 xxxxxxxxx v xx. 8 xxxx. x) xxxxxx xxx), xx) x x) xxxxxxxx (XX) x. 1069/2009 x xxxxxxxxx xxxxxxxxx 2 xxxxxxxxx x xx. 9 xxxx. x) xx x) uvedeného nařízení;] (2) x/xxxx [- xxxxxxxx xx zvířat, xxxxx xxxx ošetřena některými xxxxxxx xxxxxxxxxx podle xxxxxxxx Xxxx 96/22/ES (2x), xxxxxxx dovoz xxxxxx xxxxxxxxx xxx xxxxxxx v souladu x xx. 35 xxxx. a) bodem xx) xxxxxxxx (ES) x. 1069/2009;] XX.3. xxxx xxxxxxxxx xxxxxxxxxx x xxxxxxx x přílohou XXXX xxxxxxxxx III xxxxxxxx (XX) x. 142/2011 xx xxxxxx xxxxxxx xxxxxxxxxxx xxxxxxx; XX.4. xxxx xxxxxxxxxxx pomocí xxxxxxx xxxx vzorků x xxxxx xxxxxxxxxx xxxxx xxxxxxxxx xxxxxxxxxx xxxxx skladování xxxx xxx xxxxxxxxxxx xx xxxxxxxxxxxxxxx zařízení x xxxxxxxx xxxxx xxxxxx (3): Xxxxxxxxxx: xxxxxxxxxxxx v 25 g xxxxxxxx: x = 5, x = 0, x = 0, X = 0 Xxxxxxxxxxxxxxxxxx: x = 5, x = 2, x = 10, X = 300 x 1 x; XX.5. xxxxxxx produkt byl: (2) xxx [zabalen xx xxxxxx xxxx sterilizovaných xxxxx, ] (2) nebo [xxxxxxxxxxx volně xxxxxx x xxxxxxxxxxxx xxxx xxxxxx dopravních xxxxxxxxxxxx, xxxxx xxxx xxxx xxxxxxxx důkladně xxxxxxxxx x vydezinfikovány xxxxxxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxxxx] x xxxxx xxxx xxxxxxxx etiketami s xxxxxxx „NENÍ XXXXXX X XXXXXX XXXXXXXX“; XX.6. xxxxxxx produkt xxx xxxxxx v xxxxxxxxx xxxxxxxxx; XX.7. xxxxxxx xxxxxx xxxxx preventivními xxxxxxxxxx x zabránění xxxxxxxxxxx xxxxxxxxxxx xxxxxxx po xxxxxxxx; (2) [XX.8. xxxx xxxxxxx xxxxxxxxxxx xxxxxx xxxxxxx (2) xxx [xxxx xxxxxxx x xxxxxxxxxxx xxxxxx xxx xxxx, xxxx nebo kozy.]] (2) xxxx [xxxx xxxxxxx xx skotu, xxxx xxxx xxx x xxxxxxxxxx xxxx xxxxxxx xxxxxx xxx x xxxx xxxxxx získány: (2) xxx [xxxxxxxx pocházející xx xxxxx, xxxx x koz jiný xxx xxxxxxx ze xxxxxx xxxxxxxxxx, nepřetržitě xxxxxxxxx x xxxxxxxxxx x zemi xxxx xxxxxxx zařazené x xxxxxxx x xxxxxxxxxxx 2007/453/XX xx xxxxxxxxx xxxx xxxx xxxxxxx xx xxxxxxxxxxxxx xxxxxxx xxxxxxx XXX.]] (2) xxxx [x) xxxxxxxxxxxxx rizikový xxxxxxxx, xxx je xxxxxxxxx x xxxx 1 xxxxxxx X xxxxxxxx Evropského parlamentu x Rady (XX) x. 999/2001 (4); x) xxxxxxx xxxxxxxx maso xxxxxxx x xxxxx xxxxx, ovcí xxxx xxx s xxxxxxxx xxxxxx narozených, xxxxxxxxxxx xxxxxxxxx x xxxxxxxxxx x xxxx nebo xxxxxxx zařazené v xxxxxxx x rozhodnutím Xxxxxx 2007/453/XX (5) xx kategorie xxxx xxxx xxxxxxx se xxxxxxxxxxxxx xxxxxxx xxxxxxx XXX, v xxxxx xxxxx xxxxxxx xxxxx xxxxxx případ BSE; c) xxxxxxxx produkt xxxxxxxxxxx xxxxxx nebo xxxxxxx xxxxxxx ze skotu, xxxx nebo xxx, xxxxx xxxx po xxxxxxxx xxxxxxxx lacerací xxxxxxxxx nervové xxxxx xxxxxx xxxxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxxx do xxxxxx xxxxxxx xxxx xxxxxxxxxxxxxxx xxxxxxx xxxxxxx xx xxxxxx xxxxxxx, x xxxxxxxx zvířat xxxxxxxxxx, xxxxxxxxxxx xxxxxxxxx x poražených v xxxx xxxx xxxxxxx xxxxxxxx x souladu x xxxxxxxxxxx 2007/453/XX xx xxxxxxxxx xxxx xxxx xxxxxxx se xxxxxxxxxxxxx rizikem xxxxxxx XXX.]]]  Text obrazu Text obrazu
ZEMĚ Dochucovací xxxxxx xxxxxxx xxx xxxxxx xxxxxx pro zvířata x xxxxxxxx chovu II. Xxxxxxxxx xxxxxxxxx XX.x. Xxxxx xxxxxxx osvědčení II.b. Poznámky Část X: — Xxxxxxx X.6.: Xxxxx xxxxxxxxxx za zásilku x Xxxxxxxx xxxx: xxxx xxxxxxx xx xxxxx vyplnit xxxxx xxxxx, xxxxx-xx xx x xxxxxxxxx xxx xxxxx xxxxxx xxx xxxxxxx xxxx Xxxxxxxxx xxxx; xxxx se xxxxxxx, xxxxx-xx xx x xxxxxxxxx xxx xxxxx dovážené xx Xxxxxxxx xxxx. — Kolonka X.12.: Xxxxx určení: xxxx xxxxxxx xx xxxxx vyplnit xxxxx xxxxx, xxxxx-xx se x xxxxxxxxx xxx xxxxx xxxxxx xxx xxxxxxx. Xxxxxxxx xxx xxx xxx xxxxxxxx xxxxxxxxxx xxxxx xx xxxxxxxxxx xxxxxxx, xxxxxxxxxx xxxxxxxx x xxxxxxx xxxxxxxx. — Kolonka I.15.: Xxxxxxxxxxx číslo (xxxxxxxxxxxx xxxxxx nebo kontejneru x nákladních automobilů), xxxxx letu (xxxxxxx) xxxx název (plavidla); xxxxxxxxx je xxxxx xxxxxxxxxx x xxxxxxx xxxxxxxx a xxxxxxxxxx xxxxxxxx x Xxxxxxxx xxxx. — Kolonka I.19.: Xxxxxxxx xxxxxxxxx xxx XX: 05.04, 05.06, 05.11 xxxx 23.09. — Xxxxxxx I.23.: X xxxxxxx kontejnerů xxx xxxxx ložené látky xx xxxx xxx xxxxxxx xxxxx xxxxxxxxxx x xxxxx xxxxxx (x xxxxxxxxxxx xxxxxxxxx). — Xxxxxxx X.25.: Xxxxxxxxx xxxxxxx: xxxxxxxx jiné xxxxxxx xxxxx xxxxxx xxxxxxxxxxxxx xxxxxx xxxxxx xxx xxxxxxxxxxxx zvířat x xxxxxx nebo xxxxxxxxxx xxxxx xxx xxxxxxx x xxxxxxxx xxxxx. — Kolonky X.26. x X.27.: Xxxxxxx xxxxx toho, jedná-li xx x xxxxxxxxx xxx xxxxxxx nebo xxx xxxxx. — Xxxxxxx X.28.: — Xxxx: xxxxxxx: Xxxx, Ruminantia, Suidae, Xxxxxxxx kromě Xxxxxxxxxx xxxx Xxxxxx, Xxxxx, Xxxxxxxx, Crustacea, bezobratlí xxxxx Mollusca x Xxxxxxxxx. — Specifikujte xxxxxx xxxxxxx. Xxxx XX: (1x) Xx. xxxx. X 300, 14.11.2009, s. 1. (1x) Xx. xxxx. L 54, 26.2.2011, s. 1. (2) Xxxxxxxx xx xxxxxxxx. (2x) Xx. věst. X 125, 23.5.1996, x. 3. (3) Xxx: x = xxxxx xxxxxx, xxxxx mají xxx xxxxxxxxx; x = prahová xxxxxxx počtu bakterií; xxxxxxxx xx xxxxxxxxx xx uspokojivý, xxxxxxxx xxxxx xxxxxxxx xx xxxxx vzorcích nepřekročí x; X = xxxxxxxxx xxxxxxx xxxxx xxxxxxxx; xxxxxxxx xx považován xx neuspokojivý, xxxxx xxxxx xxxxxxxx v xxxxxx xxxx xxxx xxxxxxxx xx xxxxx xxxx xxxxx xxx X; x x = xxxxx xxxxxx, xxxxxxx xxxxxxxxxxx xxxxx smí xxx x xxxxxxx xxxx m x X, xxxxxxx xxxxxx xx xxxxx stále xxxxxxxxx xx xxxxxxxxx, xxxxx je xxxxxxxxxxx xxxxx xxxxxxxxx xxxxxx xxxxx x nebo xxxxx. (4) Úř. věst. X 147, 31.5.2001, x. 1. (5) Xx. xxxx. L 172, 30.6.2007, x. 84. — Xxxxx xxxxxxx a xxxxxxx xx xxxx xxxxx xx barvy xxxxx. — Xxxxxxxx xxx xxxxx zodpovědnou xx xxxxxxx x Xxxxxxxx xxxx: xxxx xxxxxxxxx xxxxxx pouze x xxxxxxxxxxxx účelům a xxxx zásilku xxxxxxxx xx xx okamžiku, xxx xxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxx. Xxxxxx veterinární xxxxx / úřední xxxxxxxxx Xxxxx (xxxxxxxx písmem): Xxxxxxxxxxx x xxxxx: Xxxxx: Xxxxxx: Xxxxxxx: XXXXXXXX 3 (X) Xxxxxxxxxxx xxxxxxxxx xxx xxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx (3) xxx xxxxxx xxxxxx xxx xxxxxxx x xxxxxxxx chovu, xxxxxx x xxxxxxxx xx Xxxxxxxx unie xxxx x xxxxxxxx přes xxxx xxxxx (2)  Text obrazu Text obrazu
XXXX: Xxxxxxxxxxx osvědčení do XX Xxxx X: Xxxxxxxxxxx x xxxxxxxx xxxxxxx X.1. Xxxxxxxxxx Xxxxx Xxxxxx Xxx. X.2. Číslo jednací xxxxxxxxx X.2.x. X.3. Příslušný xxxxxxxx xxxxx X.4. Xxxxxxxxx místní xxxxx X.5. Příjemce Název Adresa PSČ Tel. I.6. Xxxxx xxxxxxxxxx za zásilku x EU Jméno Adresa PSČ Tel. I.7. Xxxx xxxxxx Xxx XXX X.8. Xxxxxx xxxxxx Xxx X.9. Xxxx xxxxxx Xxx XXX X.10. Region xxxxxx Xxx X.11. Xxxxx původu Název Xxxxx xxxxxxxxx Xxxxxx Xxxxx Xxxxx xxxxxxxxx Xxxxxx Xxxxx Xxxxx xxxxxxxxx Xxxxxx X.12. Xxxxx xxxxxx Xxxxx xxxxx Xxxxx Xxxxx xxxxxxxxx Xxxxxx XXX X.13. Xxxxx xxxxxxxx X.14. Xxxxx odjezdu I.15. Xxxxxxxx xxxxxxxxxx Xxxxxxx Plavidlo Vagon Silniční xxxxxxx Xxxxxxx Xxxxxxxxxxxx Xxxxx xx xxxxxxxx X.16. Xxxxxxx xxxxxxxxxx xxxxxxxx kontroly XX X.17. X.18. Xxxxx xxxxx X.19. Xxx xxxxx (xxx XX) X.20. Xxxxxxxx X.21. Xxxxxxx xxxxxxxx Xxxxxx Xxxxxxxx Xxxxxxxx X.22. Počet xxxxxx X.23. Xxxxx xxxxxx/xxxxxxxxxx X.24. Xxxx xxxxx  Text obrazu Text obrazu
X.25. Xxxxx xxxxxxxxx xxx: Xxxxxx xxxxxx pro zvířata x zájmovém xxxxx Xxxxx xxxxxxxxxx Technické xxxxxxx X.26. Pro xxxxxxx xxxx EU xx xxxxx země Třetí xxxx Xxx XXX X.27. Pro xxxxx nebo xxxxxx xx EU I.28. Identifikace xxxxx Xxxxx xxxxxxxxx xxxxxxxx Xxxx (xxxxxxx název) Druh xxxxx Xxxxxxx xxxxx Xxxxx xxxxxx Xxxxx xxxxxxxx Xxxxx xxxxx  Text obrazu Text obrazu
ZEMĚ Vedlejší xxxxxxxx xxxxxxxxxxx xxxxxx xxx xxxxxx xxxxxx pro xxxxxxx x zájmovém xxxxx XX. Xxxxxxxxx informace II.a. Xxxxx xxxxxxx osvědčení II.b. Já, xxxx xxxxxxxxx úřední xxxxxxxxxxx lékař, xxxxxxxxxx, xx jsem přečetl x porozuměl xxxxxxxx Xxxxxxxxxx xxxxxxxxxx a Xxxx (XX) x. 1069/2009 (1a) x xxxxxxxx Xxxxxx (EU) x. 142/2011 (1b), xxxxxxx pokud xxx x přílohu XXX xxxxxxxx XX xxxxxxxxx xxxxxxxx, a xxxxxxxxx, xx xxxx popsané xxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx: XX.1.1. xxxxxxxxx z xxxxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx, které xxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxxx xxxx; XX.1.2. byly xxxxxxx xx území: (1x) xx xxxxxx: (2) xxx [x) xxxxx xxxxxxxx xx xxxxx xxxxx xx narození nebo xxxxxxx xx xxxx xxx měsíců xxxx xxxxx xxxxxxx;] (2) xxxx [x) která xxxx xxxxxxxx v xxxxxxx xx tomto xxxxx (1x);] (2) xxxx [c) xxxx získány x xxxxxxxx, xxxxxxxxxxxx, xxxxxxx xxxxxxxxx xxxx xxxxxxxxxxxxx xxxx vodních xxxxxxxxxxxx xxxxxxxxx;] XX.1.3. xxxx xxxxxxx xxxx xxxxxxxx xx xxxxxx: (2) xxx [x) xxxxxxxxxxxxx x xxxxxxxxxxxx: x) xxx xxxxx xxxxxxxxxx xxxxx případ / xxxxx xxxxxxx xxxxxxxxxxxxx xxxxx, xxxx xxxx xxxx tato xxxxxxx xxxxxxx: xx xxxx xxxxxxxxxxx 30 xxx xxx xxxxx, xxxxxxxxxxx xxxxxxx xxxxxx, xxxxxxxxxxxx xxxxxxx nebo xxxxxx xxxxxxxxx influenza xxxxx, xx dobu xxxxxxxxxxx 40 dnů klasický xxx xxxxxx xxxx xxxxxxx mor xxxxxx, xxx nebyl xx xxxx xxxxxxxxxxx 30 xxx žádný takový xxxxxx / žádné xxxxxx ohnisko xxxxxxxxxx/x x xxxxxxxxxxxxxx x xxxxxx 10 xx; x xx) xxx xxxxx xx xxxx xxxxxxxxxxx 60 dnů xxxxxxxxxx xxxxx xxxxxx / xxxxx xxxxxxx xxxxxxxxx x xxxxxxxx, xxx xxxxx po dobu xxxxxxxxxxx 30 xxx xxxxx xxxxxx xxxxxx / xxxxx xxxxxx xxxxxxx xxxxxxxxxx/x x xxxxxxxxxxxxxx x okruhu 25 xx; a b) xxxxx: x) xxxxxx xxxxxxxx xx účelem xxxxxxxxx xxxxxxxxxxx xxxxxx; xx) zůstala x xxxxxxxxxxxx xxxxxx xx dobu xxxxxxx 40 xxx před xxxxx xxxxxxx a xxxx přepravena xxxxx xx xxxxx, xxxx xx xxxxxxx xx xxxxxxxx x xxxxxx xxxxxxx, která xxxxxxxxx xxxxxx xxxxxxxxxxx podmínky; iii) xxxxxx xx xxxxxxx xxxxxxxxxxx xxxxxxxxxx x xxxxxxx 24 xxxxx xxxx xxxxxxxx x xxxxxxxxxxxx žádné xxxxxxxx xxxx uvedených nákaz, xxxx xxxx xxxx xxxx xxxxxxx vnímavá; x xx) xxxx x xxxx xx xxxxxxx xxxx xxxxxxxx xx xxxxxxxxx a x xxxx xxxxxxx či xxxxxxxx xxxxxxxxx v xxxxxxx x příslušnými xxxxxxxxxxxx právních xxxxxxxx Xxxx x xxxx xxxxxxxx xxxxxxxxx xxxxxxx xxxxxxxxxx xxx, xxxxx xxxx stanoveny x xxxxxxxxxx XX a XXX xxxxxxxx Xxxx (XX) x. 1099/2009 (4);] (2) nebo [x) xxxxx byla chycena x xxxxxxxx x xxxxxxx x xxxxxxx: x) xxx x okruhu 25 xx nebyl xxxxxxxxxx xxxxx xxxxxx / xxxxx ohnisko xxxxxxxxxxxxx xxxxx, xxxx xxxx xxxx tato xxxxxxx vnímavá: xx xxxx předchozích 30 xxx xxxxxxxxx x xxxxxxxx, xxx xxxxx, xxxxxxxxxxxx xxxxxxx xxxx xxxxxx xxxxxxxxx influenza xxxxx a xx xxxx předchozích 40 xxx klasický xxx xxxxxx xxxx africký xxx xxxxxx; a ii) xxxxxxxxxxx xx xxxxxxx 20 xx xx xxxx xxxx xxxxx xxxxx země, xxxxx xxxxxx xxxxxxxxx xxxxxxx xxxxxxxx x xxxxxxx xx Xxxxxxxx xxxx xxxxx předchozích 30 xxx xxxx xxxxxxxx x prasat xxxxx xxxxxxxxxxx 40 xxx; x x) která byla xx 12 hodin xx xxxxxxxx xxxxxxxxx xx xxxxxx chlazení xxx xx sběrného xxxxxxxxx x xxxxxxxxxxxxx xxxx do xxxxxxxx xx xxxxxxxxxx xxxxx, xxxx přímo xx xxxxxxxx xx xxxxxxxxxx xxxxx;] Xxxx II: Xxxxxxxxx  Text obrazu Text obrazu
XXXX Xxxxxxxx produkty živočišného xxxxxx pro xxxxxx xxxxxx pro zvířata x xxxxxxxx xxxxx XX. Xxxxxxxxx informace II.a. Xxxxx xxxxxxx osvědčení II.b. II.1.4. xxxx xxxxxxx v zařízení, xxx x xxxxxx 10 km nebyl xx xxxx xxxxxxxxxxx 30 xxx xxxxxxxxxx xxxxx xxxxxx/xxxxxxx xxxxx xxxxxxxxx v bodě XX.1.3., xxxx nimž xxxx xxxx zvířata xxxxxxx, xxxx xxxxx xxx xxxxxxxxxx xxxxxx xxxxxx, xxxx xxxxxxxx xxxxxxxx xxx xxxxx xx Evropské unie xxxxxxxx xxxxx po xxxxxxxxxx veškerého xxxx x po xxxxxxxx xxxxxxxxx x dezinfekci xxxxxxxx xxx xxxxxxxx xxxxxxxx xxxxxxxxxxxxx xxxxxx; XX.1.5. xxxx xxxxxxx x xxxxxxxxxx, aniž se xxxxxxx xx xxxxxxxx x xxxxxx materiály, xxxxx nesplňují xxxxxxxx xxxxxxx xxxx, x xxxxxxxxxx x nimi xxxxxxxxx tak, xxx xxxxxxx xx kontaminaci xxxxxxxxxxx xxxxxxx; XX.1.6. byly xxxxxxxx x nepropustném xxxxx obalu x xxxxxx xxxxxxxxxxxxxx nádobách xxxxxxxxxx etiketou x xxxxxxx „SYROVÝ XXXXXXXX XXXXX PRO VÝROBU XXXXXX XXX XXXXXXX X XXXXXXXX CHOVU“ x názvem x xxxxxxx xxxxxxxx určení x Evropské xxxx; XX.1.7. xxxxxxxxx xxxxx z xxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx: (2) xxx [- xxxx xxxxxxxxxx xxxxxx x xxxxxx xxxxx, xxxx x xxxxxxx xxxxx těla xxxxxxxxxx zvířat nebo xxxxxx části, které xxxx podle právních xxxxxxxx Xxxx xx xx xxxxxxxx, kdy xxxx x xxxxxxxxxx xxxxxx nevratně prohlášeny xx xxxxxxxx xxxxxxxx xxxxxxxxxxx původu, xxxxxxxxxx xx xxxxxx k xxxxxx spotřebě;] (2) x/xxxx [- xxxxxxx xxxxxxxx xxxx x xxxx xxxxxxx části pocházející xxx xx zvířat, xxxxx xxxx xxxxxxxx xx xxxxxxx x xx prohlídce před xxxxxxxx byla shledána xxxx xxxxxxxxx x xxxxxxx x lidské xxxxxxxx, xxxx xxxx x níže xxxxxxx xxxxx xxxxx xxxxxxxx x xxxxxx spotřebě x xxxxxxx x xxxxxxxx xxxxxxxx Xxxx: x) xxxxxxx xxxxxxxx xxxx xxxx xxxx xxxxxx x xxxxxx části, xxxxx xxxx v xxxxxxx x xxxxxxxx xxxxxxxx Unie prohlášeny xx xxxxxxxx x xxxxxx spotřebě, xxxxx xxxxxxxxxxxx xxxxx příznaky xxxxxxxxxx přenosného xx xxxxxxx nebo zvířata; ii) xxxxx drůbeže; iii) xxxx x kožky, včetně xxxxxx odřezků a xxxxxx, xxxx x xxxxxxxxx, xxxxxx článků xxxxx, xxxxxxxxxx a xxxxxxxxxx xxxxxx, nártů x xxxxxxx; xx) prasečí xxxxxxx; x) peří;] (2) x/xxxx [- xxxxxxxx xxxxxxxx xxxxxxxxxxx původu, xxxxx xxxxxxxx xxx výrobě xxxxxxxx určených k xxxxxx xxxxxxxx, včetně xxxxxxxxxxx xxxxx, xxxxxxx xxxx kalu z xxxxxxxxxxx xxxx xxxxxxxxxx xx zpracování mléka;] (2) x/xxxx [- xxxxxxxx xxxxxxxxxxx xxxxxx xxxx xxxxxxxxx obsahující produkty xxxxxxxxxxx původu, xxxxx x xxxxxxxxxx důvodů xxxx x xxxxxx xxxxxxxx způsobených xxxxxxxxx xxxxxx, xxxxxx xxxxxx xxxx xxxxxx xxxxxxxx, x nichž xxxxxxxx xxxxx xxxxxx pro xxxxxx xxxx xxx xxxxxx, xxx xxxxxx xxxxxx x lidské xxxxxxxx;] (2) x/xxxx [- xxxxx xxxxxxxxxxx a xxxxxx xxxxx, xxxxx xxxxxxxx xxxxx, kteří xxxxxxxxxxxx žádné příznaky xxxxxxxxxx xxxxxxxxxx xx xxxxxxx xxxx zvířata;] (2) x/xxxx [- vedlejší xxxxxxxx xxxxxxxxxxx xxxxxx x xxxxxxx xxxxxxxxx xxxxxxxxxxx z xxxxxxx xxxx xxxxxxxx xx xxxxxx xxxxxxxx xxxxxxxx x xxxxxx xxxxxxxx;] (2) x/xxxx [- xxxx xxxxxxx xxxxxxxx xxxxxxxxxxx xx xxxxxx, xxxxx xxxxxxxxxxxx xxxxx xxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxx xxxxxxxxxx xx člověka xxxx xxxxxxx: x) xxxxx xxxxxxx a korýšů x xxxxxxx xxxxxxx xxxx masem; ii) xxxxx xxxxxxxx pocházející ze xxxxxxxxxxxxx zvířat: — vedlejší xxxxxxxx x líhní, — xxxxx, — xxxxxxxx xxxxxxxx x vajec, xxxxxx xxxxxxxxx xxxxxxxx;  Text obrazu Text obrazu
XXXX Xxxxxxxx xxxxxxxx živočišného původu xxx xxxxxx xxxxxx xxx zvířata v xxxxxxxx xxxxx XX. Zdravotní xxxxxxxxx XX.x. Xxxxx xxxxxxx xxxxxxxxx XX.x. xxx) xxxxxxxxxx xxxxxx xxxxxxxx z obchodních xxxxxx;] (2) a/nebo [- xxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx x vodních xxxx suchozemských xxxxxxxxxxxx xxxxxxxxx, kromě druhů xxxxxxxxxxx pro xxxxxxx xxxx zvířata;] (2) a/nebo [- xxxxxxx z xxxx xxxxxxxx (Rodentia) x xxxxxxxxx (Lagomorpha) x xxxxxx části, xxxxx materiálu kategorie 1 uvedeného x xx. 8 písm. x) xxxxxx xxx), xx) x x) xxxxxxxx (ES) x. 1069/2009 a materiálu xxxxxxxxx 2 uvedeného x xx. 9 xxxx. x) xx x) uvedeného xxxxxxxx;] (2) x/xxxx [- xxxxxxxx xx xxxxxx, která xxxx ošetřena některými xxxxxxx xxxxxxxxxx xxxxx xxxxxxxx Rady 96/22/XX (4x), xxxxxxx xxxxx xxxxxx xxxxxxxxx byl xxxxxxx x xxxxxxx x čl. 35 xxxx. x) bodem xx) nařízení (XX) x. 1069/2009;] XX.1.8. xxxx xxxxxxx xxxxxxxx v xxxxxxx xxxxxx xxxx xxxxxxxxxxxx v souladu x xxxxxxxx předpisy Xxxxxxxx xxxx takovým xxxxxxxx, xxx xx x době mezi xxxxxxxxx a xxxxxxx xx xxxxxxx určení x Evropské xxxx xxxx během tranzitu xxxx Evropskou xxxx xxxxxxxxx; XX.1.9. x xxxxxxx xxxxxxx xxxxxxxxx ze xxxxxx, která byla xxxxxxxx některými xxxxxxx xxxxxxxxxx xxxxxxxx 96/22/ES xxx xxxxxx krmiva xxx xxxxxxx x xxxxxxxx chovu, jejichž xxxxx xx povolen x souladu x xx. 35 písm. x) bodem xx) xxxxxxxx (XX) č. 1069/2009: x) xxxx tato xxxxxxxx ve třetí xxxx před xxxxxxx xx xxxxx Evropské xxxx xxxxxxxx křížem x tekutého xxxxxxxxx xxxx nebo xxxxxxxxx xxxx xx každé xxxxxx straně každého xxxxxxxxxx xxxxx, nebo xxxxx xx xxxxxxxx xxxxxxxxxxxx na xxxxxxxx, xxxxx xxxxxx xxxxx xxxxxxxx do xxxxxxxx xxxxxx xx výrobu xxxxxx pro xxxxxxx x xxxxxxxx xxxxx x Evropské xxxx xxxx xxxxx xxxxxxxx xxxx Xxxxxxxxx xxxx xxxxxxxxx do xxxxxxxxxxxx xxxxxxx, xx xxxxx xxxxxx xxxxxx každé xxxxxx, x to xxxxxxx způsobem, xx xxxxxxxx xxxxxxx xxxxxxx 70 % xxxxxxxxxx xxxxx xxxxxxxxxx xxxxx x má xxxxx xxxxxxx 10 cm; b) x xxxxxxx xxxxxxxxx, xxxxx xxxx zmrazený, xxxx xxxxxxxx xx xxxxx xxxx xxxx xxxxxxx xx xxxxx Xxxxxxxx xxxx označena xxxxxxxxxxx tekutého xxxxxxxxx xxxx nebo nanesením xxxxxxxxxx xxxxxxxxx xxxx xxx, xxx bylo xxxxxxx xxxx na xxxxxxxxx xxxxx xxxxxx; x x) x xxxxxxx, xx xxxx xxxxxxxx xxxxxxxx živočišného xxxxxx xxxxxxxx xx suroviny, xxxxx xxxx xxxxxxxx xxxx xxxxxxxx xxxxxxxx, x z xxxx xxxxxxxxxx xxxxxxxx, xxxx xxxxxxx xxxx suroviny xxxxxxxx xxxxxxxx xxxxxxxx xxxx x xxxxxxxxx x) a x). (2) (5) [XX.2. Xxxxxxxx xxxxxxxxx (2) (6) [XX.2.1. Xxxxxxxx xxxxxxxx v xxxx zásilce xxxxxxxxx xx xxxxxx, xxxxx xxxx xxxxxx xx xxxxx uvedeném v xxxx XX.1.2., xxx xx x xxxxxxxx xxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxx očkování xxxxx xxxxxxxxx x kulhavce x xxx xx xxxx nákaza úředně xxxxxxxxxxxx.] (2) (7) [XX.2.2. Xxxxxxxx xxxxxxxx x xxxx xxxxxxx sestávají xxxxx x xxxxxxxxxx xxxxxxxx xxxxxxxxxxx původu xxxxxxxxx x xxxxxxxxxxxx xxxxx xxxxxxxx přežvýkavců, xxxxx zrály xxx xxxxxx xxxxxxx xxxxx xxx + 2 °X xx xxxx xxxxxxx tří hodin xxxx, v xxxxxxx xxxxxxxxx svalů xxxxx x vykostěného xxxx xxxxxxxx xxxxxx, nejméně 24 hodin.]] (2) [XX.3. Xxxxxxxx produkty xxxxxxxxxxx xxxxxx pro xxxxxx xxxxxx pro zvířata x zájmovém xxxxx xxxxxxxx vedlejší produkty xxxxxxxxxxx původu z xxxxxxxxxxx nebo xxxx x xxxx xxxxxxx x: (2) xxx [xxxxxxxxx xx země xxxx xxxxxxx xxxxxxxx x xxxxxxx s xxxxxxxxxxx 2007/453/XX do kategorie xxxx xxxx xxxxxxx xx xxxxxxxxxxxxx xxxxxxx xxxxxxx XXX, x xxxxx nebyl xxxxxxx xxxxx xxxxxx případ XXX, x]] (2) nebo [xxxxxxxxx xx země xxxx oblasti xxxxxxxx x xxxxxxx s xxxxxxxxxxx 2007/453/XX do xxxxxxxxx xxxx xxxx xxxxxxx xx xxxxxxxxxxxxx xxxxxxx xxxxxxx XXX, x nichž xxx xxxxxxx domácí xxxxxx XXX, x xxxxxxxx xxxxxxx xxxxxxxxxxx původu xxxx xxxxxxx xxxxxxx xxx získán xx xxxxxx narozených xx xxxx, xx xxxxxxx xxx v xxxxxxx xxxx nebo oblasti xxxxxx vymáhán zákaz xxxxxx xxxxxxxxxxx masokostní xxxxxxx x xxxxxxx xxxxxxxxx z přežvýkavců, xxx jsou definovány x Xxxxxx zdraví xxxxxxxxxxxxx xxxxxxxxx XXX, x]] (2) buď [xxxx xxxxxxx z xxxxxxxxxxx xxxxxx xxx skot, xxxx xxxx kozy.]  Text obrazu Text obrazu
XXXX Xxxxxxxx xxxxxxxx živočišného xxxxxx xxx výrobu xxxxxx xxx zvířata x xxxxxxxx xxxxx XX. Xxxxxxxxx xxxxxxxxx XX.x. Číslo xxxxxxx xxxxxxxxx XX.x. (2) xxxx [xxxx získány xx xxxxx, xxxx nebo xxx a xxxxxxxxxx xxxx uvedené složky xxx z nich xxxxxx xxxxxxx: (2) xxx [xxxxxxxx xxxxxxxxxxx xx xxxxx, xxxx a xxx jiný xxx xxxxxxx xx xxxxxx xxxxxxxxxx, xxxxxxxxxxx xxxxxxxxx x xxxxxxxxxx v xxxx nebo oblasti xxxxxxxx x souladu x xxxxxxxxxxx 2007/453/XX xx kategorie xxxx xxxx xxxxxxx se xxxxxxxxxxxxx xxxxxxx xxxxxxx XXX.]]] (2) nebo [a) xxxxxxxxxxxxx xxxxxxxx xxxxxxxx, xxx je definován x xxxx 1 xxxxxxx X xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Xxxx (ES) č. 999/2001 (8); x) xxxxxxx xxxxxxxx maso získané x xxxxx xxxxx, xxxx nebo koz x xxxxxxxx xxxxxx xxxxxxxxxx, nepřetržitě xxxxxxxxx x poražených v xxxx xxxx oblasti xxxxxxxx v xxxxxxx x rozhodnutím Xxxxxx 2007/453/XX (9) xx xxxxxxxxx xxxx xxxx xxxxxxx xx xxxxxxxxxxxxx xxxxxxx xxxxxxx XXX, x nichž xxxxx xxxxxxx xxxxx xxxxxx xxxxxx XXX; x) vedlejší xxxxxxx xxxxxxxxxxx xxxxxx xxxx xxxxxxx xxxxxxx xx xxxxx, xxxx xxxx koz, xxxxx xxxx po xxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxx xxxxx pomocí xxxxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxxx xx xxxxxx xxxxxxx xxxx xxxxxxxxxxxxxxx xxxxxxx injekce xx xxxxxx xxxxxxx, x xxxxxxxx xxxxxx xxxxxxxxxx, xxxxxxxxxxx chovaných x xxxxxxxxxx x zemi xxxx oblasti xxxxxxxx x xxxxxxx s xxxxxxxxxxx 2007/453/ES xx xxxxxxxxx země xxxx xxxxxxx se xxxxxxxxxxxxx xxxxxxx xxxxxxx BSE.]]]] Poznámky Část X: — Kolonka X.6.: Xxxxx xxxxxxxxxx xx xxxxxxx x Evropské xxxx: xxxx xxxxxxx xx xxxxx vyplnit xxxxx xxxxx, jedná-li xx o osvědčení xxx zboží xxxxxx xxx xxxxxxx; xxxx xx xxxxxxx, jedná-li xx x xxxxxxxxx xxx zboží xxxxxxxx xx Evropské unie. — Xxxxxxx X.12: Místo xxxxxx: xxxx xxxxxxx xx xxxxx xxxxxxx xxxxx xxxxx, xxxxx-xx xx o xxxxxxxxx xxx zboží xxxxxx xxx xxxxxxx. Xxxxxxxx xxx xxx při xxxxxxxx xxxxxxxxxx pouze xx svobodných xxxxxxx, xxxxxxxxxx xxxxxxxx x xxxxxxx xxxxxxxx. — Xxxxxxx X.15: Xxxxxxxxxxx číslo (xxxxxxxxxxxx xxxxxx xxxx xxxxxxxxxx a xxxxxxxxxx xxxxxxxxxx), číslo xxxx (xxxxxxx) nebo xxxxx (xxxxxxxx); xxxxxxxxx je xxxxx xxxxxxxxxx x xxxxxxx xxxxxxxx a xxxxxxxxxx xxxxxxxx x Xxxxxxxx xxxx. — Kolonka X.19: Použijte příslušný xxx XX: 05.04, 05.06, 05.07, 05.11.91 xxxx 05.11.99; 23.01 x 41.01. — Kolonka X.23: V xxxxxxx xxxxxxxxxx pro volně xxxxxx látky xx xxxx xxx xxxxxxx xxxxx xxxxxxxxxx x (xxxxxxxx) xxxxx xxxxxx. — Xxxxxxx I.25: Xxxxxxxxx xxxxxxx: jakékoli xxxx xxxxxxx xxxxx xxxxxx xxxxxxxxxxxxx xxxxxx xxxxxx xxx kožešinových xxxxxx x xxxxxx xxxx xxxxxxxxxx xxxxx pro xxxxxxx x zájmovém xxxxx. — Kolonky X.26 x X.27: Vyplňte xxxxx xxxx, xxxxx-xx xx x xxxxxxxxx xxx tranzit xxxx xxx xxxxx. — Kolonka X.28: — Druh: xxxxxxx: Xxxx, Ruminantia, Xxxxxx, Xxxxxxxx xxxxx Xxxxxxxxxx xxxx Xxxxxx, Pesca, Xxxxxxxx, Crustacea, xxxxxxxxxx xxxxx Xxxxxxxx x Xxxxxxxxx. — Xxxxxxx xxxxx: xxxxxx xxxxx xxxxxxxxxxx xxxxxxxx schváleného xxxxxxxx. Xxxx XX: (1x) Xx. věst. X 300, 14.11.2009, x. 1. (1x) Xx. xxxx. X 54, 26.2.2011, s. 1.  Text obrazu Text obrazu
XXXX Xxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx xxx xxxxxx xxxxxx xxx xxxxxxx x zájmovém chovu II. Xxxxxxxxx xxxxxxxxx XX.x. Xxxxx xxxxxxx osvědčení II.b. (1c) Název x xxx XXX xxxxxxxxxx země x xxxxxxx x: — x xxxxxxxx XX xxxxx 1 xxxxxxxx (EU) x. 206/2010, — x xxxxxxxx X xxxxx 1 xxxxxxxx (XX) x. 798/2008 a — x xxxxxxxx I xxxxx 1 nařízení (XX) x. 119/2009. Xxxxx xxxx být xxxxxx x xxx ISO xxx xxxxxxxxxxxxx xx xxxx xxxxxxxxx přílohách (xxxxx xxx o xxxxxxx vnímavé xxxxx). (1x) Xxxxx xxx xxxx, x nichž xx xxxxxxx xxxxx xxxx xxxxx xxxxx živočišných xxxxx určeného x xxxxxx spotřebě do Xxxxxxxx xxxx. (2) Nehodící xx škrtněte. (3) X xxxxxxxx xxxxxx xxxx, xxxxxxxx xxxxx, xxxx x xxxxx, kopyt x paznehtů, xxxx, xxxxxxxxx xxxxxx a xxxx (viz xxxxxxxxx xxxxxxxxxx osvědčení pro xxxxx xxxxxx produktů x xxxxxxx xxxxxxx). (4) Xx. xxxx. L 303, 18.11.2009, x. 1. (4x) Úř. věst. X 125, 23.5.1996, x. 3. (5) Doplňkové xxxxxx xx xxxxx xxxxxxxxxx v xxxxxxx, xx xxxxxxxx z xxxxxxxx xxxxxxxxxxx xxxxxxx x území xxxxxxxxxxxx xxxx jihoafrické xxxx xxxx její části, xxxxx xx xx Xxxxxxxx xxxx xxxxxxx xxxxx xxxxx xxxxxxxxx x vykostěného xxxxxxxxx xxxx xxxxxxxx xxxxxxxxxxx x xxxxxx xxxxxxxx. Xxxx žvýkací xxxxx xxxxx naříznuté x xxxxxxx s xxxxxxxx X oddílem XX xxxxxxxxx X xxxxx X bodem 1 xxxxxxxx Evropského xxxxxxxxxx x Xxxx (XX) x. 854/2004 (Xx. xxxx. X 139, 30.4.2004, x. 206) xxxx xxxxxx povoleny. (6) Xxxxx xxx některé xxxxxxxxxxxx země. (7) Pouze xxx xxxxxxx jihoamerické x jihoafrické země. (8) Xx. xxxx. X 147, 31.5.2001, x. 1. (9) Xx. xxxx. X 172, 30.6.2007, x. 84. — Xxxxx xxxxxxx a xxxxxxx xx musí xxxxx xx xxxxx xxxxx. — Xxxxxxxx pro xxxxx xxxxxxxxxxx za xxxxxxx x Xxxxxxxx xxxx: xxxx osvědčení slouží xxxxx k xxxxxxxxxxxx xxxxxx x xxxx xxxxxxx provázet xx xx xxxxxxxx, kdy xxxxxxx xxxxxxxxxx hraniční xxxxxxxx Xxxxxxxx xxxx. Xxxxxx xxxxxxxxxxx xxxxx / xxxxxx xxxxxxxxx Xxxxx (hůlkovým xxxxxx): Xxxxxxxxxxx a xxxxx: Xxxxx: Podpis: Razítko: |
|
2) |
Kapitoly 4 (X) xx 4 (X) xx xxxxxxxxx xxxxx: „XXXXXXXX 4 (X) Xxxxxxxxxxx xxxxxxxxx xxx krevní xxxxxxx, xxxxx xxxxxx xxxxxx x&xxxx;xxxxxx spotřebě x&xxxx;xxxxx xxx použít xxxx xxxxxx surovinu, xxxxxx x&xxxx;xxxxxxxx do Evropské xxxx xxxx x&xxxx;xxxxxxxx xxxx její území (2)  &xxxx;Text obrazu &xxxx;Text obrazu
XXXX: Xxxxxxxxxxx osvědčení xx XX Xxxx X: Podrobnosti x xxxxxxxx xxxxxxx X.1. Xxxxxxxxxx Xxxxx Xxxxxx Xxx. X.2. Xxxxx jednací xxxxxxxxx X.2.x. X.3. Xxxxxxxxx xxxxxxxx xxxxx X.4. Příslušný xxxxxx xxxxx X.5. Xxxxxxxx Xxxxx Xxxxxx XXX Xxx. X.6. Xxxxx xxxxxxxxxx xx xxxxxxx x XX Xxxxx Xxxxxx XXX Xxx. X.7. Xxxx xxxxxx Xxx XXX X.8. Xxxxxx xxxxxx Xxx X.9. Xxxx xxxxxx Xxx XXX X.10. Region xxxxxx Xxx X.11. Xxxxx původu Název Číslo xxxxxxxxx Xxxxxx Xxxxx Číslo schválení Adresa Název Xxxxx schválení Adresa I.12. Xxxxx xxxxxx Xxxxx xxxxx Xxxxx Číslo xxxxxxxxx Xxxxxx XXX X.13. Xxxxx nakládky I.14. Xxxxx xxxxxxx X.15. Xxxxxxxx xxxxxxxxxx Xxxxxxx Xxxxxxxx Xxxxx Xxxxxxxx xxxxxxx Xxxxxxx Xxxxxxxxxxxx Xxxxx na xxxxxxxx X.16. Xxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxx XX X.17. X.18. Xxxxx zboží I.19. Kód xxxxx (kód XX) X.20. Xxxxxxxx X.21. Xxxxxxx xxxxxxxx Xxxxxx Xxxxxxxx Zmrazené I.22. Počet xxxxxx X.23. Číslo xxxxxx/xxxxxxxxxx X.24. Xxxx obalu  Text obrazu Text obrazu
I.25. Xxxxx xxxxxxxxx xxx: Xxxxxx Xxxxxx krmiva xxx xxxxxxx v zájmovém xxxxx Xxxxxxxxx xxxxxxx X.26. Xxx xxxxxxx přes XX xx třetí xxxx Xxxxx xxxx Kód XXX X.27. Xxx xxxxx xxxx příjem xx XX X.28. Xxxxxxxxxxxx xxxxx Xxxxx xxxxxxxxx xxxxxxxx Xxxx (xxxxxxx xxxxx) Xxxx xxxxx Xxxxxxx xxxxx Xxxxx xxxxx  Text obrazu Text obrazu
XXXX Xxxxxx xxxxxxx, xxxxx xxxxxx xxxxxx x lidské spotřebě x které lze xxxxxx xxxx xxxxxx xxxxxxxx XX. Zdravotní xxxxxxxxx XX.x. Xxxxx xxxxxxx xxxxxxxxx XX.x. Xx, xxxx xxxxxxxxx úřední xxxxxxxxxxx xxxxx, xxxxxxxxxx, xx xxxx xxxxxxx x xxxxxxxxx nařízení Xxxxxxxxxx parlamentu x Xxxx (XX) x. 1069/2009 (1x) a xxxxxxxx Xxxxxx (EU) x. 142/2011 (1b), x xxxxxxxxx, xx xxxx xxxxxxx xxxxxx xxxxxxx: XX.1. sestávají z xxxxxxxx xxxxxxx, xxxxx xxxxxxx xxxxxxxxxxx požadavky xxxxxxx xxxx; XX.2. sestávají xxxxxxxx x krevních xxxxxxx, xxxxx xxxxxx xxxxxx x lidské xxxxxxxx; XX.3. byly xxxxxxxxxx x xxxxxxxxxx x xxxxxxx schváleném x xxxxxxxxxxx xxxxxxxxxx xxxxxxx x xxxxxxx x xxxxxxx 24 nařízení (XX) x. 1069/2009; XX.4. xxxx xxxxxxxxxx výhradně x xxxxxx xxxxxxxxxx xxxxxxxx živočišného xxxxxx: (2) xxx [krev xxxxxxxxxx xxxxxx, xxxxx xx x souladu x xxxxxxxx předpisy Xxxx xxxxxx k xxxxxx xxxxxxxx, ale xxxxx xxxx z xxxxxxxxxx xxxxxx x xxxxxx xxxxxxxx určena;] (2) x/xxxx [xxxx xxxxxxxxxx xxxxxx, xxxxx xxxx x xxxxxxx s xxxxxxxx xxxxxxxx Xxxx xxxxxxxxxx xx nevhodnou x xxxxxx spotřebě, xxx xxxxxxx xxxxxxxxxxxx žádné xxxxxxxx xxxxxxxxxx xxxxxxxxxx xx xxxxxxx nebo xxxxxxx, x pochází x xxxxxxx xxxxxxxxxx xxx xxxxxx poražených xx jatkách, xxx xxxx x souladu x xxxxxxxx předpisy Xxxx po xxxxxxxxx xxxx xxxxxxxx xxxxxxxx xxxxxxxx x lidské xxxxxxxx;] XX.5. xx xxxxxx xxxxxxxxxx xxxxxxxxxxx xxxxxxx xxxx podrobeny (2) xxx [xxxxxxxxxx x xxxxxxx xx xxxxxxxxxxxxxxx metodou (3) podle xxxxxxxx XXX přílohy IV xxxxxxxx (EU) x. 142/2011;] (2) xxxx [xxxxxx x xxxxxxxxxx, xxxxx xxxxxxxxx, xx xxxxxxx xx v xxxxxxx x xxxxxxxxxxxxxxxxx normami xxxxxxxxxxx x xxxxxxxx X xxxxxxx X xxxxxxxx (EU) x. 142/2011;] (2) nebo [x xxxxxxx xxxxxxxx xxxxxxx, xxxxxx xxxxxxxx xxxxxx xxxx x xxxxxx xxxxxx z xxxxxx, xxxxxxxx xx xxxxxx xxxxxx, xxxxxxxxx xxxxxxxx xxxxxxxx xxxx xxxxx xxxxxxx na xxxxxxx 80 °C, xxxxxxx xxxxxx xxxx x xxxxxx xxxxxx xxxxxxxxxx xxxx xxx 8 % x/x xxxxxxxx x vodní aktivitou (Xx) méně xxx 0,60;] XX.6. konečný xxxxxxx xxx: (2) buď [zabalen xx xxxxxx xxxx xxxxxxxxxxxxxxx xxxxx;] (2) xxxx [xxxxxxxxxxx volně xxxxxx x xxxxxxxxxxxx xxxx xxxxxx xxxxxxxxxx xxxxxxxxxxxx, xxxxx xxxx před xxxxxxxx důkladně xxxxxxxxx x xxxxxxxxxxxxxxx xxxxxxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxxxx] x xxxxx xxxx xxxxxxxx xxxxxxxxx x xxxxxxx „XXXX XXXXXX X XXXXXX XXXXXXXX“; XX.7. xxxxxxx xxxxxxx byl xxxxxx x xxxxxxxxx xxxxxxxxx; XX.8. produkt xxxxxx xxxxx xxxxxxxxxxxxx xxxxxxxxxx x xxxxxxxxx xxxxxxxxxxx xxxxxxxxxxx xxxxxxx po xxxxxxxx; (2) x [x xxxxxxx krevních xxxxxxx, xxxxxx xxxxxxxx xxxxxx xxxx a xxxxxx xxxxxx x xxxxxx, xxxxxxxx xx xxxxxx xxxxxx, byl xxxxxxxxx xx sucha při xxxxxxxx xxxxxxx xx xxxx nejméně 6 xxxxx;] XX.9 xxxx před xxxxxxxxx analyzovány x xxxxx odpovědnosti xxxxxxxxxxx xxxxxx, xxxxx odebral xxxxxxxxx xxxxxx xxxxx xxxxxxxxxx xxxx xxx xxxxxxxx skladu x xxxxxxx jej x xxxxxxx s xxxxxx xxxxxxx (4): Xxxxxxxxxx: xxxxxxxxxxxx x 25 x xxxxxxxx: x = 5, c = 0, m = 0, M = 0, Xxxxxxxxxxxxxxxxxx: x = 5, c = 2, x = 10, M = 300 v 1 x; Xxxx XX: Osvědčení  Text obrazu Text obrazu
XXXX Xxxxxx xxxxxxx, které xxxxxx xxxxxx k xxxxxx xxxxxxxx x xxxxx lze xxxxxx xxxx xxxxxx surovinu II. Xxxxxxxxx informace II.a. Číslo xxxxxxx xxxxxxxxx XX.x. (2) [XX.10. xxxx popsané krevní xxxxxxx (2) xxx [jsou xxxxxxx z xxxxxxxxxxx xxxxxx než skot, xxxx xxxx xxxx;]] (2) xxxx [jsou xxxxxxx xx xxxxx, xxxx xxxx koz x xxxxxxxxxx dále xxxxxxx xxxxxx xxx z xxxx xxxxxx získány: (2) xxx [materiál pocházející xx xxxxx, ovcí x xxx xxxx xxx xxxxxxx xx xxxxxx xxxxxxxxxx, nepřetržitě xxxxxxxxx a xxxxxxxxxx x zemi xxxx xxxxxxx zařazené v xxxxxxx x xxxxxxxxxxx 2007/453/XX xx xxxxxxxxx xxxx xxxx oblasti xx zanedbatelným xxxxxxx xxxxxxx XXX;]] (2) xxxx [x) xxxxxxxxxxxxx xxxxxxxx xxxxxxxx, xxx xx xxxxxxxxx x xxxx 1 xxxxxxx X xxxxxxxx Evropského xxxxxxxxxx x Xxxx (XX) x. 999/2001 (5); x) xxxxxxx xxxxxxxx maso xxxxxxx x kostí xxxxx, xxxx xxxx xxx x výjimkou xxxxxx xxxxxxxxxx, xxxxxxxxxxx xxxxxxxxx a xxxxxxxxxx x zemi xxxx xxxxxxx xxxxxxxx x xxxxxxx x xxxxxxxxxxx Xxxxxx 2007/453/ES (6) xx xxxxxxxxx xxxx xxxx oblasti xx xxxxxxxxxxxxx xxxxxxx xxxxxxx XXX, v nichž xxxxx xxxxxxx xxxxx xxxxxx xxxxxx BSE; c) xxxxxxxx produkt živočišného xxxxxx nebo xxxxxxx xxxxxxx xx skotu, xxxx nebo koz, xxxxx xxxx xx xxxxxxxx xxxxxxxx lacerací xxxxxxxxx xxxxxxx xxxxx xxxxxx xxxxxxxxxxx xxxxxxxxxx xxxxxxxx zavedeného do xxxxxx xxxxxxx xxxx xxxxxxxxxxxxxxx xxxxxxx xxxxxxx xx xxxxxx xxxxxxx, x xxxxxxxx zvířat xxxxxxxxxx, xxxxxxxxxxx xxxxxxxxx x xxxxxxxxxx x xxxx xxxx xxxxxxx xxxxxxxx v souladu x rozhodnutím 2007/453/ES xx xxxxxxxxx země xxxx xxxxxxx xx xxxxxxxxxxxxx xxxxxxx xxxxxxx XXX;]]] XX.11. xxxx popsané xxxxxx výrobky: (2) buď [xxxxxxxxxx mléko xxxx xxxxxx xxxxxxx xxxxxxxxxxx x xxxx xxxx xxx xxx xxxxxx xxxxxx pro xxxxxx xxxxxxxxxxxxx xxxxxx xxxxxx xxx xxxxxxxxxxxx zvířat;] (2) xxxx [xxxxxxxx xxxxx xxxx xxxxxx výrobky xxxxxxxxxxx x xxxx xxxx xxx x xxxx xxxxxx pro xxxxxx xxxxxxxxxxxxx xxxxxx xxxxxx xxx xxxxxxxxxxxx xxxxxx, které: a) xxxx xxxxxxx x xxxx x xxx, xxxxx xxxx xxxxxxxxxxx xx xxxxxxxx xxxxxxx v xxxx, v xxx xxxx xxxxxxx xxxx xxxxxxxx: x) xxxxxxxx klusavka xx xxxxxxx hlášením; ii) xxxxxxx systém xxxxxx, xxxxxxxxx a xxxxxxx, xxxxx xxx x xxxxxxxxx klusavku; iii) na xxxxxxxxxxxx x xxxxxx xxxx xxxx xxx xx uplatňují xxxxxx xxxxxxx v případě xxxxxxxxx xx TSE xxxx potvrzení xxxxxxxx xxxxxxxx; xx) xxxx x xxxx xxxxxxxxx xxxxxxxxx xxxxxxxxx xxxx xxxxxxxx x zlikvidovány; v) krmení xxxx a xxx xxxxxxxxxx xxxxxxx xxxx xxxxxxx x přežvýkavců, xxx xxxx definovány x Xxxxxx xxxxxx xxxxxxxxxxxxx xxxxxxxxx Světové xxxxxxxxxx xxx xxxxxx xxxxxx (XXX), bylo xxxxxxxx x xxxxx xxx xxxxxx xxxxxxx x xxxx xxxx xxxxxxxxxxxx xx xxxx xxxxxxxxxxx xxxxx let; b) xxxxxxxxx z xxxxxxxxxxxx, xxx xxxxx xxxxxxx xxxxx úřední omezení x xxxxxx xxxxxxxxx xx výskyt XXX; x) xxxxxxxxx z hospodářství, x nichž přinejmenším xx dobu xxxxxxxxxxx xxxxx xxx xxxxx xxxxxxxxxxxxxx žádný xxxxxx xxxxxxxx xxxxxxxx, nebo xx xxxxxxxxx xxxxxxx xxxxxxxx xxxxxxxx:  Text obrazu Text obrazu
XXXX Xxxxxx xxxxxxx, které xxxxxx xxxxxx x xxxxxx xxxxxxxx a xxxxx xxx použít xxxx xxxxxx surovinu II. Xxxxxxxxx xxxxxxxxx XX.x. Xxxxx xxxxxxx xxxxxxxxx XX.x. (2) buď [byly xxxxxxxx x xxxxxxxxxxxx xxxx xxxxxxxx xxxxxxx xxxx x xxxx x xxxxxxxxxxxx x xxxxxxxx xxxxxxxxxx xxxxxx xxxxxxxx XXX/XXX, xxxxxxxx xxxxxx xxxxxxxxx xxxxxxx xxxxx alelu XXX x xxxxxx xxxxx XXX x xxxxxxx xxxx nesoucích xxxxxxx xxxxx alelu XXX;] (2) xxxx [xxxx xxxxxxx xxxxxxx, x nichž xxxx klasická xxxxxxxx xxxxxxxxx, usmrcena x xxxxxxxxxxxx a xx xxxxxxxxxxxx se xxxxxxx xx dva xxxx xx xxxxxxxxx xxxxxxxxxx xxxxxxx klasické xxxxxxxx xxxxxxxx xxxxxxxxxxxxx xxxxxxxxx XXX, včetně xxxxxxxxx xxxxx následujících xxxxxx xxxxxxxx 18 xxxxxx, x xxxxxxxx xxxx xxxxxxxx XXX/XXX, xx xxxxxxxxxx XXX x xxxxxxxxxx výsledkem x xxxxxxx s xxxxxxxxxxxxx xxxxxxxx stanovenými x xxxxxxx X xxxxxxxx X bodě 3.2 xxxxxxxx (ES) x. 999/2001: — xxxxxxx, která xxxx xxxxxxxx x xxxxxx xxxxxxxx, x — xxxxxxx, která uhynula xxxx xxxx usmrcena x xxxxx xxxxxxxxxxxx, xxxxx xxxxxx xxxxxxxx x rámci xxxxxxx xxxxxxxxx xxxxxx;]] XX.12. xxxx xxxxxxx xxxxxx výrobky xxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx x xxxxxxxxxxxxx nebo jsou x xxxx získány x x xxxxxxx x xxxxxxxxxxx xxxxxxxxxxx x xxxxxxx X.1. (2) xxx [nejsou xxxxxx x výrobě xxxxx xxx xxxxxxxxxxx xxxxxxx xxxx než xxxxxxxxxx xxxxxxx.] (2) (7) xxxx [xxxx určeny x xxxxxx xxxxx xxx xxxxxxxxxxxx xxxxxxxxxxx xxxxxxx xxxx xxx kožešinová xxxxxxx a xxxxxxxxxx xx zavázal xxxxxxxx, xx vstupnímu xxxxxxxxxx xxxxxxxx xxxxxxxx xxxxx xxxxxxxxxx xxxxxxxx zkoušení xxxxx metod xxxxxxxxxxx x xxxxxxx VI xxxxxxxx Xxxxxx (ES) x. 152/2009 (8).] Xxxxxxxx Xxxx X: — Kolonka X.6.: Xxxxx zodpovědná xx xxxxxxx v Xxxxxxxx xxxx: xxxx xxxxxxx xx třeba xxxxxxx xxxxx xxxxx, xxxxx-xx xx x xxxxxxxxx xxx xxxxx určené xxx xxxxxxx xxxx Xxxxxxxxx unii; může xx xxxxxxx, xxxxx-xx xx o xxxxxxxxx xxx xxxxx xxxxxxxx xx Xxxxxxxx xxxx. — Xxxxxxx X.12.: Xxxxx xxxxxx: xxxx xxxxxxx xx xxxxx vyplnit xxxxx tehdy, jedná-li xx x xxxxxxxxx xxx xxxxx xxxxxx xxx tranzit. Produkty xxx být xxx xxxxxxxx xxxxxxxxxx pouze xx xxxxxxxxxx pásmech, xxxxxxxxxx xxxxxxxx a xxxxxxx skladech. — Xxxxxxx X.15.: Xxxxxxxxxxx xxxxx (xxxxxxxxxxxx vagonů xxxx xxxxxxxxxx x nákladních xxxxxxxxxx), xxxxx xxxx (xxxxxxx) xxxx xxxxx (xxxxxxxx); xxxxxxxxx xx xxxxx xxxxxxxxxx x xxxxxxx xxxxxxxx x xxxxxxxxxx xxxxxxxx x Xxxxxxxx xxxx. — Xxxxxxx X.19.: Xxxxxxxx xxxxxxxxx xxx HS: 05.11.91, 05.11.99, 35.02 xxxx 35.04. — Xxxxxxx I.23.: X xxxxxxx kontejnerů xxx volně xxxxxx xxxxx xx xxxx xxx xxxxxxx číslo xxxxxxxxxx x (xxxxxxxx) xxxxx xxxxxx. — Xxxxxxx X.25.: Xxxxxxxxx xxxxxxx: xxxxxxxx xxxx xxxxxxx xxxxx xxxxxx hospodářských xxxxxx xxxxxx xxx xxxxxxxxxxxx zvířat a xxxxxx xxxx xxxxxxxxxx xxxxx xxx zvířata x xxxxxxxx xxxxx. — Xxxxxxx I.26. a X.27.: Xxxxxxx xxxxx xxxx, jedná-li xx x xxxxxxxxx pro xxxxxxx xxxx xxx xxxxx. — Xxxxxxx I.28.: Xxxx: vyberte: Xxxx, Xxxxxxxxxx, Suidae, Mammalia xxxxx Xxxxxxxxxx nebo Xxxxxx, Xxxxx, Xxxxxxxx.  Text obrazu Text obrazu
XXXX Xxxxxx xxxxxxx, xxxxx xxxxxx určeny x xxxxxx xxxxxxxx x xxxxx lze použít xxxx krmnou xxxxxxxx XX. Xxxxxxxxx informace II.a. Číslo xxxxxxx osvědčení II.b. Část XX: (1x) Xx. xxxx. X 300, 14.11.2009, s. 1. (1x) Xx. xxxx. X 54, 26.2.2011, x. 1. (2) Xxxxxxxx xx škrtněte. (3) Xxxxxx xxxxxx 1 xx 5 nebo 7 xxxxx xxxxxxx. (4) Kde: n = xxxxx xxxxxx, xxxxx xxxx xxx xxxxxxxxx; x = xxxxxxx xxxxxxx počtu bakterií; xxxxxxxx xx xxxxxxxxx xx xxxxxxxxxx, jestliže xxxxx xxxxxxxx ve xxxxx xxxxxxxx xxxxxxxxxx x; X = xxxxxxxxx xxxxxxx počtu bakterií; xxxxxxxx je xxxxxxxxx xx xxxxxxxxxxxx, xxxxx xxxxx bakterií x xxxxxx xxxx xxxx xxxxxxxx je roven xxxx xxxxx xxx X; x x = xxxxx vzorků, jejichž xxxxxxxxxxx xxxxx smí xxx x rozmezí xxxx m x X, xxxxxxx vzorek xx ještě xxxxx xxxxxxxxx xx přípustný, xxxxx je bakteriální xxxxx ostatních xxxxxx xxxxx m nebo xxxxx. (5) Úř. xxxx. X 147, 31.5.2001, x. 1. (6) Xx. xxxx. X 172, 30.6.2007, s. 84. (7) Xxxxx zodpovědná xx xxxxxxx xxxxxxx v xxxxxxx X.6. musí xxxxxxxx, xxx v xxxxxxx, xx xxxxxx xxxxxxx xxxxxxx x xxxxx veterinárním xxxxxxxxx xxxx být xxxxxx x xxxxxx xxxxxx xxx xxxxxxxxxxxx xxxxxxxxxxx xxxxxxx xxxx xxx xxxxxxxxxx xxxxxxx, xxxx xxxxxxx xxxxxxxxx xxxxxxxx xxxxx metod xxxxxxxxxxx x příloze XX xxxxxxxx (XX) x. 152/2009, xxx se xxxxxxx nepřítomnost xxxxxxxxxxxx xxxxxx xxxxxxxxxxx xxxxxx. Xxxxxxxxx xxxxxxxx se xxxxxxxx takového xxxxxxxx xxxx být xxx xxxxxxxxxx xxxxxxx na xxxxxxxxxx hraniční kontroly Xxxxxxxx unie xxxxxxxxx x xxxxxx veterinárnímu xxxxxxxxx. (8) Xx. xxxx. X 54, 26.2.2009, x. 1. — Xxxxx xxxxxxx x razítka xx xxxx lišit xx xxxxx xxxxx. — Xxxxxxxx pro osobu xxxxxxxxxxx xx zásilku x Evropské xxxx: xxxx xxxxxxxxx slouží xxxxx x xxxxxxxxxxxx xxxxxx x xxxx xxxxxxx xxxxxxxx až xx xxxxxxxx, kdy xxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxx v xxxxx xxxxxx xx Xxxxxxxx xxxx. Xxxxxx veterinární lékař / xxxxxx inspektor Jméno (xxxxxxxx písmem): Xxxxxxxxxxx x xxxxx: Xxxxx: Xxxxxx: Xxxxxxx: XXXXXXXX 4 (C) Veterinární xxxxxxxxx xxx xxxxxxxxxx krevní xxxxxxx, xxxxx xxxxxxxxxxxx xxxxxxxx xxxxxxx x koňovitých, xxx xxxxxx xxxxxxxxx xxxxxxxx k použití xxxx krmivový řetězec xxx xxxxxxxxxxx xxxxxxx, xxxxxx k odeslání xx Evropské unie xxxx x xxxxxxxx xxxx její xxxxx (2) &xxxx; Text obrazu Text obrazu
XXXX: Xxxxxxxxxxx osvědčení xx XX Xxxx X: Xxxxxxxxxxx x xxxxxxxx xxxxxxx X.1. Xxxxxxxxxx Xxxxx Xxxxxx Xxx. X.2. Xxxxx xxxxxxx xxxxxxxxx X.2.x. X.3. Xxxxxxxxx xxxxxxxx orgán I.4. Xxxxxxxxx xxxxxx orgán I.5. Xxxxxxxx Xxxxx Xxxxxx XXX Xxx. X.6. Xxxxx xxxxxxxxxx xx xxxxxxx v XX Xxxxx Xxxxxx XXX Xxx. X.7. Xxxx xxxxxx Xxx ISO I.8. Xxxxxx původu Kód I.9. Xxxx xxxxxx Xxx ISO I.10. Region xxxxxx Xxx X.11. Xxxxx původu Název Xxxxx xxxxxxxxx Xxxxxx Xxxxx Číslo xxxxxxxxx Xxxxxx Xxxxx Xxxxx xxxxxxxxx Xxxxxx X.12. Xxxxx xxxxxx Xxxxx xxxxx Xxxxx Xxxxx xxxxxxxxx Xxxxxx XXX X.13. Xxxxx xxxxxxxx X.14. Xxxxx xxxxxxx X.15. Xxxxxxxx prostředek Letadlo Xxxxxxxx Xxxxx Xxxxxxxx vozidlo Xxxxxxx Xxxxxxxxxxxx Xxxxx xx xxxxxxxx X.16. Xxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxx XX X.17. X.18. Xxxxx zboží I.19. Xxx xxxxx (xxx XX) X.20. Xxxxxxxx X.21. Xxxxxxx xxxxxxxx Xxxxxx Chlazené Zmrazené I.22. Xxxxx balení I.23. Xxxxx xxxxxx/xxxxxxxxxx X.24. Xxxx xxxxx  Text obrazu Text obrazu
X.25. Zboží xxxxxxxxx xxx: Xxxxxxxxx xxxxxxx X.26. Xxx xxxxxxx přes XX xx třetí xxxx Xxxxx xxxx Xxx XXX X.27. Xxx xxxxx nebo xxxxxx do XX X.28. Xxxxxxxxxxxx xxxxx Xxxxx xxxxxxxxx xxxxxxxx Xxxx (vědecký název) Výrobní xxxxx Xxxxx xxxxx  Text obrazu Text obrazu
XXXX Xxxxxxxxxx xxxxxx xxxxxxx, kromě xxxxxxxxxxxx xxxxxxxx xxxxxxx x xxxxxxxxxx, xxx xxxxxx xxxxxxxxx xxxxxxxx x xxxxxxx xxxx xxxxxxxx xxxxxxx pro xxxxxxxxxxx xxxxxxx XX. Xxxxxxxxx xxxxxxxxx XX.x. Xxxxx jednací xxxxxxxxx XX.x. Xx, xxxx podepsaný xxxxxx veterinární xxxxx, xxxxxxxxxx, že jsem xxxxxxx a xxxxxxxxx xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Rady (ES) x. 1069/2009 (1x), xxxxxxx pokud xxx x xx. 8 xxxx. c) x x) x článek 10 uvedeného xxxxxxxx, x nařízení Xxxxxx (XX) x. 142/2011 (1x), xxxxxxx xxxxx xxx o xxxxxxx XXX xxxxxxxx II xxxxxxxxx nařízení, a xxxxxxxxx, xx: XX.1. výše xxxxxxx xxxxxx xxxxxxx xxxxxxxxx x krevních xxxxxxx, které splňují xxxxxxxxxxx xxxxxxxxx xxxxxxx xxxx; XX.2. xxxxxxxxx xxxxxxxx x krevních xxxxxxx, xxxxx xxxxxx xxxxxx x xxxxxx spotřebě xxx xx krmení xxxxxx; XX.3. xxxx xxxxxxxxxx x xxxxxxxxxx x xxxxxxx xxxxxxxxxxx příslušným xxxxxxx xxxx x xxxxxxxx xxxxxx xxxxxxxx x xxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx: (2) xxx [- xxxx xxxxxxxxxx xxxxxx, která xx x souladu x právními xxxxxxxx Xxxx xxxxxx k xxxxxx xxxxxxxx, ale xxxxx xxxx x xxxxxxxxxx důvodů x xxxxxx spotřebě určena,] (2) x/xxxx [- krev xxxxxxxxxx zvířat, xxxxx xxxx x xxxxxxx x xxxxxxxx xxxxxxxx Xxxx xxxxxxxxxx xx xxxxxxxxx x xxxxxx xxxxxxxx, xxx xxxxxxx xxxxxxxxxxxx žádné xxxxxxxx xxxxxxxxxx přenosných xx xxxxxxx xxxx xxxxxxx, x xxxxxxx x xxxxxxx xxxxxxxxxx xxx xxxxxx xxxxxxxxxx xx xxxxxxx, jež byla x xxxxxxx x xxxxxxxx xxxxxxxx Unie xx xxxxxxxxx xxxx xxxxxxxx xxxxxxxx xxxxxxxx x lidské xxxxxxxx,] (2) x/xxxx [- xxxx xxxxxxxxxx xxxxxx, xxxxx xxxxxxxxxxxx žádné příznaky xxxxxxxxxx xxxxxxxxxx na xxxxxxx nebo zvířata, xxxxx byla xxxxxxxx xx jatkách x xxxxx xxxx x xxxxxxx s xxxxxxxx xxxxxxxx Xxxx xx xxxxxxxxx xxxx porážkou xxxxxxxx xxxxxxxx x xxxxxx spotřebě,] (2) x/xxxx [- krev x xxxxxx výrobky xxxxxxx x výroby xxxxxxxx xxxxxxxx x lidské xxxxxxxx,] (2) x/xxxx [- xxxx a xxxxxx xxxxxxx xxxxxxxxxxx xx xxxxxx zvířat, která xxxxxxxxxxxx žádné xxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxxx xxxxxxxx na xxxxxxx xxxx zvířata,] (2) a/nebo [- vedlejší produkty xxxxxxxxxxx xxxxxx xxxxxxx xx zvířat, xxxxx xxxx podrobena xxxxxxxxxxx xxxxxxxx xxxxx xxxxxxxx x xx. 1 xxxx. 2 xxxx. x) směrnice Rady 96/22/XX (2x) xxxx xx. 2 xxxx. x) xxxxxxxx Xxxx 96/23/XX (2x),] (2) x/xxxx [- xxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx, xxxxx xxxxxxxx xxxxxxx xxxxxxx xxxxx x kontaminantů x xxxxxxxx xxxxxxxxx xxxxxxxxx ve xxxxxxx X(3) xxxxxxx X xxxxxxxx 96/23/XX, xxxxx xxxxxxxx těchto xxxxxxx xxxxxxxxx xxxxxxxxx úrovně xxxxxxxxx xxxxxxxx předpisy Xxxx, xxxx xxxxxx-xx x xxxxxx předpisech xxxxxxxxx, v xxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxx;] XX.4. xxxx, xx xxxxx xxxx tyto výrobky xxxxxxxx, xxxx xxxxxxxx xx jatkách xxxxxxxxxxx x souladu x xxxxxxxx předpisy Unie, xx jatkách xxxxxxxxxxx x dozorovaných xxxxxxxxxx xxxxxxx xxxx xxxxxx xxxx xx xxxxxx xxxxxx x zařízeních xxxxxxxxxxx a xxxxxxxxxxxx xxxxxxxxxx xxxxxxx xxxx xxxxxx; (2) [XX.5. v xxxxxxx xxxxxxxx výrobků, xxxxx byly xxxxxxx xx xxxxxx xxxx Xxxxxxxxxxxx, Xxxxxxxxxxxxxx x Xxxxxxxxxxx včetně xxxxxx xxxxxxxx, xxxx byla xxxxxxxx v xxxx xxxx xxxxxxx, kde xxxxx přinejmenším xx xxxx xxxxxxxxxxx 12 xxxxxx zaznamenán xxxxx xxxxxx xxxx xxxxx, xxxx xxxxxx xxxxxxxxxxx x xxxxxxx Xxxxx Xxxx x xxx xxxxxxxxxxxx xx dobu xxxxxxxxxxx 12 xxxxxx xxxxxxxxxx xxxxxxxx proti xxxxx xxxxxxx, x (2) xxx [ve třetích xxxxxx, xxxxxxx xxxx xxxxxx xxxxxxx … (xxxxxx xxx ISO xxxx x případě xxxx xxxxxxxx (3) xxx xxxxx xxxx xxxxxx xxxxx), kde xxxxx xxxxxxxxxxxx xx xxxx předchozích 12 xxxxxx xxxxxxxxxx xxxxx xxxxxx xxxxxxxxx x xxxxxxxx a xxx xxxxxxxxxxxx xx xxxx xxxxxxxxxxx 12 xxxxxx xxxxxxxxxx xxxxxxxx xxxxx xxxx xxxxxx x;] (2) xxxx [xx xxxxxxx xxxxxx, xxxxxxx xxxx xxxxxx xxxxxxx … (xxxxxx kód ISO xxxx v případě xxxx nebokódy (3) xxx xxxxx nebo xxxxxx xxxxx), xxx xxxxx xxxxxxxxxxxx po xxxx předchozích 12 xxxxxx zaznamenán xxxxx xxxxxx slintavky x xxxxxxxx x xxx xxxx xxxxxxxxxxxx xx xxxx xxxxxxxxxxx 12 xxxxxx úředně prováděny x kontrolovány xxxxxxxx xxxxxxxx xxxxx xxxxxxxxx x kulhavce (4); x] Xxxx II: Xxxxxxxxx  Text obrazu Text obrazu
XXXX Xxxxxxxxxx xxxxxx xxxxxxx, xxxxx xxxxxxxxxxxx krevních xxxxxxx z xxxxxxxxxx, xxx xxxxxx xxxxxxxxx xxxxxxxx x xxxxxxx xxxx xxxxxxxx xxxxxxx xxx xxxxxxxxxxx xxxxxxx XX. Xxxxxxxxx xxxxxxxxx XX.x. Xxxxx xxxxxxx xxxxxxxxx XX.x. (2) [XX.5.1. x případě zvířat xxxxxx než xxxxxx Xxxxxx x Tayassuidae xx xxxxxxx xxxxxx xxxx xxxxxxxxx, kde: (2) xxx [xxxxxxxxxxxx xx xxxx xxxxxxxxxxx 12 xxxxxx xxxxx xxxxxxxxxx xxxxx xxxxxx xxxxxxxxxxx xxxxxxxxxxx x katarální xxxxxxx xxxx (2) (xxxxxx xxxxxxx xxxxxxxxxxxxxxx xxxxxx) x kde xxxxxxxxxxxx po xxxx xxxxxxxxxxx 12 měsíců xxxxxxxxxx xxxxxxxx xxxxx xxxxx nákazám;] (2) xxxx [xx xxxxxxxxx zvířata xxxxxxxxxxxxx xx xxxxxxxxxxx xxxxxxxxxxx x katarální xxxxxxx ovcí (2) (4);]] (2) [II.5.2. x xxxxxxx xxxxxx Xxxxxx x Xxxxxxxxxxx xx xxxxxxx xxxxxx nebo xxxxxxxxx, kde xxxxxxxxxxxx xx xxxx předchozích 12 měsíců xxxxx xxxxxxxxxx xxxxx případ xxxxxxxxxxx choroby xxxxxx, xxxxxxxxxx xxxx xxxxxx x xxxxxxxxx xxxx xxxxxx x xxx xxxxxxxxxxxx xx dobu xxxxxxxxxxx 12 xxxxxx xxxxxxxxxx x vnímavých xxxxx xxxxxxxx xxxxx xxxxx xxxxxxx x: (2) xxx [xxxxxxxxxxxx xx xxxx xxxxxxxxxxx 12 xxxxxx nebyl xxxxxxxxxx xxxxx xxxxxx xxxxxxxxxxx xxxxxxxxxxx (xxxxxx xxxxxxx xxxxxxxxxxxxxxx zvířat) x xxx přinejmenším xx xxxx xxxxxxxxxxx 12 xxxxxx xxxxxxxxxx xxxxxxxx xxxxx této xxxxxx;]] (2) xxxx [xx xxxxxxxxx xxxxxxx xxxxxxxxxxxxx xx xxxxxxxxxxx xxxxxxxxxxx (4);]] (2) [XX.6. x xxxxxxx xxxxxxxx výrobků, které xxxx xxxxxxx x xxxxxxx nebo xxxxxx xxxxx xxxxx, xxxxxxxxx xxxxxxx a xxxxxxx x území xxxx xxxx regionu x xxxxx (5), xxxxx(x) byl(a) xxxxxx(x) newcastleské xxxxxxx x xxxxxx xxxxxxxxx xxxxxxxxx ptáků xxxxx xxxxxxxx x Xxxxxx xxxxxx xxxxxxxxxxxxx xxxxxxxxx XXX, xxx xxxxxx xxxxxxxxxxxx xx xxxx xxxxxxxxxxx 12 xxxxxx xxxxxxxxx xxxxxxxx xxxxx influenze xxxxx, xxx zvířata, z xxxxx xxxx výrobky xxxxxxx, xxxxxx xxxxxxxx xxxxx xxxxxxxxxxxx xxxxxxx xxxxxxxxxx látkami připravenými x matečného xxxxx xxxxxxxxxxxx xxxxxxx vykazujícího xxxxx xxxxxxxxxx xxx xxxxxxxxxx kmeny viru;] II.7. xxxxxxx xxxx: (2) buď [xxxxxxxx xx nových xxxx xxxxxxxxxxxxxxx xxxxx xxxx xxxxx,] (2) xxxx [xxxxxxxxxxxx xxxxx xxxxxx x xxxxxxxxxxxx xxxx xxxxxx dopravních xxxxxxxxxxxx, xxxxx xxxx před xxxxxxxx xxxxxxxx xxxxxxxxx x xxxxxxxxxxxxxxx xxxxxxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxxxx,] xxxxxx obal nebo xxxxxxxxxx xxxx xxxxxxxx xxxxxxxxx x xxxxxxx „XXXX XXXXXX X XXXXXX SPOTŘEBĚ ANI XX KRMENÍ ZVÍŘAT“; II.8. xxxxxxx xxxx xxxxxxx x xxxxxxxxx xxxxxxxxx; XX.9. xxxx xxxxxxx xxxxxxx xxxxxxxxxxx xxxxxxxx x xxxxxxxxx xxxxxxxxxxx xxxxxxx xxxxxxxxxxx xxxxxxx xxxxx xxxxxxxx; (2) [XX.10. xxxx xxxxxxx neošetřené krevní xxxxxxx (2) xxx [xxxx xxxxxxx x xxxxxxxxxxx xxxxxx než xxxx, xxxx nebo xxxx.]] (2) xxxx [xxxx xxxxxxx xx xxxxx, xxxx xxxx xxx x xxxxxxxxxx dále xxxxxxx xxxxxx xxx x xxxx xxxxxx xxxxxxx: (2) xxx [xxxxxxxx pocházející xx xxxxx, xxxx x xxx xxxx xxx xxxxxxx xx xxxxxx xxxxxxxxxx, xxxxxxxxxxx xxxxxxxxx x xxxxxxxxxx x zemi xxxx xxxxxxx xxxxxxxx x xxxxxxx s xxxxxxxxxxx 2007/453/XX do xxxxxxxxx xxxx xxxx oblasti xx zanedbatelným rizikem xxxxxxx XXX.]] (2) xxxx [x) specifikovaný rizikový xxxxxxxx, xxx je xxxxxxxxx x xxxx 1 přílohy X xxxxxxxx Xxxxxxxxxx parlamentu x Xxxx (XX) x. 999/2001 (6); x) xxxxxxx oddělené maso xxxxxxx x kostí xxxxx, ovcí xxxx xxx s xxxxxxxx xxxxxx narozených, nepřetržitě xxxxxxxxx a xxxxxxxxxx x zemi xxxx xxxxxxx xxxxxxxx x xxxxxxx x xxxxxxxxxxx Xxxxxx 2007/453/XX (7) xx kategorie xxxxx xxxx oblasti xx xxxxxxxxxxxxx xxxxxxx xxxxxxx XXX, x nichž xxxxx xxxxxxx žádný xxxxxx případ XXX;  Text obrazu Text obrazu
XXXX Xxxxxxxxxx xxxxxx xxxxxxx, xxxxx xxxxxxxxxxxx xxxxxxxx xxxxxxx z koňovitých, xxx xxxxxx xxxxxxxxx xxxxxxxx k xxxxxxx xxxx krmivový xxxxxxx xxx hospodářská xxxxxxx XX. Xxxxxxxxx informace II.a. Xxxxx xxxxxxx xxxxxxxxx XX.x. x) xxxxxxxx xxxxxxx xxxxxxxxxxx xxxxxx xxxx xxxxxxx xxxxxxx xx skotu, xxxx xxxx xxx, které xxxx xx xxxxxxxx xxxxxxxx lacerací xxxxxxxxx xxxxxxx xxxxx xxxxxx xxxxxxxxxxx xxxxxxxxxx nástroje xxxxxxxxxx xx dutiny xxxxxxx xxxx prostřednictvím xxxxxxx xxxxxxx do xxxxxx xxxxxxx, x xxxxxxxx zvířat xxxxxxxxxx, xxxxxxxxxxx xxxxxxxxx x xxxxxxxxxx x zemi xxxx oblasti zařazené x souladu x xxxxxxxxxxx 2007/453/ES xx xxxxxxxxx země nebo xxxxxxx xx xxxxxxxxxxxxx xxxxxxx xxxxxxx XXX.]]] Xxxxxxxx Xxxx X: — Xxxxxxx X.6.: Xxxxx xxxxxxxxxx xx xxxxxxx x Evropské xxxx: tuto xxxxxxx xx třeba xxxxxxx xxxxx tehdy, jedná-li xx o osvědčení xxx xxxxx xxxxxx xxx tranzit přes Xxxxxxxxx xxxx; může xx xxxxxxx, xxxxx-xx xx x xxxxxxxxx xxx xxxxx dovážené xx Xxxxxxxx unie. — Xxxxxxx X.11. x X.12.: Xxxxx xxxxxxxxx: xxxxx xxxxxxxxxx zařízení xxxx podniku, xxxxx xxxx xxxxxx xxxxxxxxxx xxxxxxx. — Xxxxxxx I.12.: Xxxxx xxxxxx: xxxx xxxxxxx xx xxxxx xxxxxxx xxxxx xxxxx, xxxxx-xx se x xxxxxxxxx xxx xxxxx xxxxxx xxx xxxxxxx. Xxxxxxxx xxx xxx xxx xxxxxxxx xxxxxxxxxx xxxxx ve svobodných xxxxxxx, xxxxxxxxxx xxxxxxxx x celních xxxxxxxx. — Xxxxxxx X.15.: Xx xxxxx xxxxx registrační xxxxx (xxxxxx xxxx xxxxxxxxxx x nákladní xxxxxxxxxx), xxxxx xxxx (xxxxxxx) nebo xxxxx (xxxxxxxx). X případě xxxxxxxx a xxxxxxxxxx xxxxxxxx v Xxxxxxxx xxxx musí odesílatel xxxxxxxxxx stanoviště hraniční xxxxxxxx x xxxxx xxxxxx xx Xxxxxxxx xxxx. — Kolonka I.19.: Xxxxxxxx xxxxxxxxx xxx xxxxxxxxxxxxxxx xxxxxxx (XX) xxxxxxxxxxxxx čísel: 05.11, 30.02 xxxx 35.02. — Xxxxxxx X.23.: X xxxxxxx xxxxxxxxxx pro xxxxx ložené látky xxxx xxx uvedeno xxxxx kontejneru x (xxxxxxxx) číslo xxxxxx. — Xxxxxxx X.25.: Xxxxxxxxx xxxxxxx: xxxxxxxx jiné xxxxxxx xxxxx krmení xxxxxxxxxxxxx xxxxxx jiných xxx xxxxxxxxxxxx zvířat x výroba xxxx xxxxxxxxxx xxxxx pro xxxxxxx x xxxxxxxx xxxxx. — Xxxxxxx X.26. x X.27.: Xxxxxxx xxxxx toho, jedná-li xx o xxxxxxxxx xxx xxxxxxx xxxx xxx dovoz. — Kolonka X.28. Druh: vyberte: Xxxx, Xxxxxxxxxx, Suidae, Xxxxxxxx xxxxx Xxxxxxxxxx xxxx Xxxxxx, Pesca, Xxxxxxxx. Xxxx XX: (1x) Úř. xxxx. X 300, 14.11.2009, x. 1. (1b) Xx. xxxx. L 54, 26.2.2011, x. 1. (2) Xxxxxxxx xx xxxxxxxx. (2x) Xx. xxxx. X 125, 23.5.1996, x. 3. (2x) Xx. xxxx. X 125, 23.5.1996, x. 10. (3) Xxx xxxxx, jak xx xxxxxx x xxxxxxx II xxxxx 1 xxxxxxxx (XX) x. 206/2010 (Úř. xxxx. L 73, 20.3.2010, x. 1). (4) X xxxxx xxxxxxx xxxx xxx xxxxxxx xx xxxxxxxxx veterinárních xxxxxxx xxxxx směrnice 97/78/XX (Xx. věst. X 24, 30.1.1998, x. 9) x x souladu x xxxxxxxxxx xxxxxxxxxxx x xx. 8 xxxx. 4 xxxxxxx xxxxxxxx xxxxxxxxxx xxxxx xx xxxxxxxx xx xxxxx xxxxxx.  Text obrazu Text obrazu
XXXX Xxxxxxxxxx xxxxxx xxxxxxx, xxxxx xxxxxxxxxxxx xxxxxxxx výrobků x xxxxxxxxxx, pro xxxxxx xxxxxxxxx produktů k xxxxxxx xxxx krmivový xxxxxxx xxx xxxxxxxxxxx xxxxxxx XX. Xxxxxxxxx informace II.a. Xxxxx xxxxxxx xxxxxxxxx XX.x. (5) Xxx xxxxx, xxx xx xxxxxx x xxxxxxx I xxxxx 1 xxxxxxxx Komise (XX) č. 798/2008 (Xx. xxxx. X 226, 23.8.2010, s. 1). (6) Úř. xxxx. X 147, 31.5.2001, x. 1. (7) Xx. xxxx. X 172, 30.6.2007, x. 84. — Xxxxx xxxxxxx x xxxxxxx xx musí xxxxx xx barvy xxxxx. — Xxxxxxxx xxx xxxxx xxxxxxxxxxx za xxxxxxx x Xxxxxxxx xxxx: xxxx xxxxxxxxx xxxxxx xxxxx x xxxxxxxxxxxx xxxxxx a xxxx xxxxxxx xxxxxxxx xx xx xxxxxxxx, xxx xxxxxxx xxxxxxxxxx xxxxxxxx kontroly x xxxxx xxxxxx xx Xxxxxxxx unie. Úřední xxxxxxxxxxx xxxxx / úřední xxxxxxxxx Xxxxx (xxxxxxxx xxxxxx): Xxxxxxxxxxx x xxxxx: Xxxxx: Xxxxxx: Xxxxxxx: XXXXXXXX 4 (X) Xxxxxxxxxxx xxxxxxxxx xxx ošetřené xxxxxx xxxxxxx, xxxxx xxxxxxxxxx xxxxxxxx výrobků z xxxxxxxxxx, pro výrobu xxxxxxxxx xxxxxxxx x xxxxxxx mimo xxxxxxxx xxxxxxx pro xxxxxxxxxxx xxxxxxx, xxxxxx k xxxxxxxx xx Xxxxxxxx xxxx xxxx k xxxxxxxx xxxx její xxxxx (2) &xxxx; Text obrazu Text obrazu
XXXX: Xxxxxxxxxxx xxxxxxxxx xx XX Xxxx X: Xxxxxxxxxxx x xxxxxxxx xxxxxxx X.1. Xxxxxxxxxx Xxxxx Xxxxxx Xxx. X.2. Xxxxx xxxxxxx xxxxxxxxx X.2.x. X.3. Xxxxxxxxx xxxxxxxx xxxxx X.4. Xxxxxxxxx xxxxxx xxxxx X.5. Xxxxxxxx Xxxxx Xxxxxx XXX Xxx. X.6. Xxxxx xxxxxxxxxx xx xxxxxxx v XX Xxxxx Xxxxxx XXX Xxx. X.7. Země xxxxxx Xxx XXX X.8. Xxxxxx původu Kód I.9. Xxxx určení Kód XXX X.10. Xxxxxx xxxxxx Xxx X.11. Xxxxx xxxxxx Xxxxx Xxxxx xxxxxxxxx Xxxxxx Xxxxx Xxxxx xxxxxxxxx Xxxxxx Xxxxx Xxxxx xxxxxxxxx Xxxxxx X.12. Xxxxx xxxxxx Xxxxx xxxxx Xxxxx Xxxxx schválení Adresa PSČ I.13. Xxxxx xxxxxxxx X.14. Xxxxx xxxxxxx X.15. Xxxxxxxx xxxxxxxxxx Xxxxxxx Xxxxxxxx Xxxxx Xxxxxxxx xxxxxxx Xxxxxxx Xxxxxxxxxxxx Xxxxx na xxxxxxxx X.16. Xxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxx XX X.17. X.18. Popis xxxxx X.19. Xxx zboží (xxx HS) I.20. Xxxxxxxx X.21. Xxxxxxx produktů Okolní Chlazené Xxxxxxxx X.22. Xxxxx balení I.23. Xxxxx plomby/kontejneru I.24. Xxxx xxxxx  Text obrazu Text obrazu
X.25. Xxxxx xxxxxxxxx xxx: Xxxxxxxxx xxxxxxx X.26. Xxx xxxxxxx xxxx XX do třetí xxxx Xxxxx země Xxx XXX X.27. Pro xxxxx xxxx xxxxxx xx XX X.28. Xxxxxxxxxxxx xxxxx Xxxxx xxxxxxxxx zařízení Druh (xxxxxxx xxxxx) Xxxxxxx xxxxx Xxxxx xxxxx  Text obrazu Text obrazu
XXXX Xxxxxxxx xxxxxx xxxxxxx, xxxxx xxxxxxxxxx krevních xxxxxxx x xxxxxxxxxx, xxx výrobu xxxxxxxxx xxxxxxxx x použití xxxx xxxxxxxx řetězec xxx hospodářská xxxxxxx XX. Xxxxxxxxx informace II.a. Xxxxx xxxxxxx xxxxxxxxx XX.x. Xx, xxxx xxxxxxxxx úřední xxxxxxxxxxx xxxxx, xxxxxxxxxx, že xxxx xxxxxxx x xxxxxxxxx xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Xxxx (XX) č. 1069/2009 (1x), xxxxxxx xxxxx xxx x xx. 8 písm. x) x d) a xxxxxx 10 xxxxxxxxx xxxxxxxx, x nařízení Xxxxxx (EU) č. 142/2011 (1x), xxxxxxx xxxxx xxx x xxxxxxx XIV xxxxxxxx XX xxxxxxxxx nařízení, x xxxxxxxxx, xx: XX.1. xxxx xxxxxxx xxxxxx xxxxxxx xxxxxxxxx z xxxxxxxx výrobků, xxxxx xxxxxxx xxxxxxxxx uvedené xxxx; XX.2. sestávají xxxxxxxx x xxxxxxxx xxxxxxx, xxxxx nejsou určeny x lidské spotřebě xxx ke krmení xxxxxx; XX.3. byly připraveny x skladovány x xxxxxxx dozorovaném xxxxxxxxxx xxxxxxx xxxxxxxx x xxxxxx vedlejších xxxxxxxx xxxxxxxxxxx původu: (2) buď [- xxxx poražených xxxxxx, xxxxx je x souladu s xxxxxxxx xxxxxxxx Xxxx xxxxxx k xxxxxx xxxxxxxx, xxx xxxxx xxxx x obchodních xxxxxx k xxxxxx xxxxxxxx xxxxxx,] (2) x/xxxx [- xxxx poražených xxxxxx, xxxxx xxxx x souladu s xxxxxxxx xxxxxxxx Unie xxxxxxxxxx xx xxxxxxxxx x xxxxxx xxxxxxxx, xxx xxxxxxx xxxxxxxxxxxx xxxxx xxxxxxxx onemocnění xxxxxxxxxx na člověka xxxx xxxxxxx, x xxxxxxx x xxxxxxx xxxxxxxxxx těl xxxxxx xxxxxxxxxx na xxxxxxx, xxx byla x xxxxxxx x xxxxxxxx xxxxxxxx Xxxx xx xxxxxxxxx xxxx xxxxxxxx xxxxxxxx vhodnými k xxxxxx xxxxxxxx,] (2) x/xxxx [- krev poražených xxxxxx, která xxxxxxxxxxxx xxxxx příznaky xxxxxxxxxx xxxxxxxxxx xx xxxxxxx xxxx xxxxxxx, xxxxx xxxx xxxxxxxx xx xxxxxxx a xxxxx xxxx x souladu x xxxxxxxx xxxxxxxx Xxxx xx xxxxxxxxx xxxx xxxxxxxx xxxxxxxx xxxxxxxx k xxxxxx xxxxxxxx,] (2) a/nebo [- xxxx x xxxxxx xxxxxxx xxxxxxxxxxx x xxxxxx xxxxxx, která xxxxxxxxxxxx xxxxxxxx příznaky xxxxxxx onemocnění xxxxxxxxxx xxxxxx produkty na xxxxxxx xxxx xxxxxxx,] (2) x/xxxx [- xxxx x xxxxxx xxxxxxx xxxxxxx x xxxxxx xxxxxxxx xxxxxxxx x xxxxxx spotřebě,] (2) a/nebo [- vedlejší xxxxxxxx xxxxxxxxxxx původu xxxxxxx xx xxxxxx, xxxxx xxxx podrobena nezákonnému xxxxxxxx xxxxx xxxxxxxx x čl. 1 xxxx. 2 xxxx. x) směrnice Rady 96/22/XX (2x) nebo xx. 2 písm. x) směrnice Xxxx 96/23/XX (2x),] (2) x/xxxx [- vedlejší produkty xxxxxxxxxxx původu, xxxxx xxxxxxxx xxxxxxx xxxxxxx xxxxx x xxxxxxxxxxxx x okolního prostředí xxxxxxxxx ve skupině X (3) v xxxxxxx X xxxxxxxx 96/23/XX, xxxxx xxxxxxxx xxxxxx reziduí přesahuje xxxxxxxxx úrovně stanovené xxxxxxxx xxxxxxxx Xxxx, xxxx xxxxxx-xx v xxxxxx předpisech xxxxxxxxx, x xxxxxxxx xxxxxxxxxx xxxxxxxxx států;] II.4. xxxx, xx xxxxx xxxx xxxx xxxxxxx xxxxxxxx, xxxx xxxxxxxx na xxxxxxx schválených v xxxxxxx x xxxxxxxx xxxxxxxx Xxxx, na xxxxxxx xxxxxxxxxxx a xxxxxxxxxxxx xxxxxxxxxx orgánem xxxx xxxxxx nebo xx xxxxxx zvířat x xxxxxxxxxx xxxxxxxxxxx x xxxxxxxxxxxx xxxxxxxxxx xxxxxxx země xxxxxx; (2) [XX.5. x případě xxxxxxxx výrobků, xxxxx xxxx xxxxxxx xx xxxxxx xxxx Artiodactyla, Xxxxxxxxxxxxxx a Xxxxxxxxxxx, xxxxxx xxxxxx xxxxxxxx, xxxxxx než xxxxxx Xxxxxx a Tayassuidae, xxxxxx xxxxxxx xxxxxx x xxxxxxxxxxxxx ošetření xxxxxxxxxxxx nepřítomnost xxxxxxxxxxx xxxxxxx xxxxxxxxx x xxxxxxxx, xxxxxxxxxxx xxxxxxxxxxx, xxxx skotu, xxxx xxxxxx xxxxxxxxxxx, xxxxxxx Xxxxx Rift x xxxxxxxxx horečky xxxx: (2) xxx [xxxxxxxx xxxxxxxxx xxx xxxxxxx 65 °X xx xxxx xxxxxxx 3 xxxxx x následnou xxxxxxxxx xxxxxxxxx;] (2) x/xxxx [xxxxxxxx xxxxxxx gama x xxxxxxxxxx 25 kGy x následnou xxxxxxxxx xxxxxxxxx;] (2) a/nebo [xxxxxx xX xx xxxxxxx 5 xx dobu xxxx hodin s xxxxxxxxx xxxxxxxxx účinnosti;] (2) x/xxxx [xxxxxxxx xxxxxxxxx xxx xxxxxxx nejméně 80 °C v xxxx hmotě x xxxxxxxxx xxxxxxxxx xxxxxxxxx;]] Xxxx XX: Xxxxxxxxx  Text obrazu Text obrazu
XXXX Xxxxxxxx xxxxxx xxxxxxx, kromě xxxxxxxxxx krevních výrobků x koňovitých, pro xxxxxx získaných xxxxxxxx x použití xxxx xxxxxxxx xxxxxxx xxx xxxxxxxxxxx xxxxxxx XX. Xxxxxxxxx xxxxxxxxx XX.x. Xxxxx xxxxxxx xxxxxxxxx XX.x. (2) [XX.6. v xxxxxxx xxxxxxxx xxxxxxx, xxxxx byly xxxxxxx xx zvířat xxxxxx Xxxxxx a Xxxxxxxxxxx, xxxxxxx x jiných xxxxx xxxxx, prošly xxxxxxx xxxxxx x xxxxxxxxxxxxx xxxxxxxx xxxxxxxxxxxx xxxxxxxxxxxx patogenních xxxxxxx xxxxxx nákaz: slintavka x xxxxxxxx, vezikulární xxxxxxxxxxx, xxxxxxxxxxx choroba xxxxxx, xxxxxxxx mor xxxxxx, xxxxxxx xxx xxxxxx, xxxxxxxxxxxx choroba x vysoce patogenní xxxxxxxxx xxxxx xxxxx xxxxxxxxxxxx druhů: (2) xxx [xxxxxxxx xxxxxxxxx xxx xxxxxxx 65 °C xx xxxx xxxxxxx 3 xxxxx x xxxxxxxxx xxxxxxxxx účinnosti;] (2) x/xxxx [xxxxxxxx xxxxxxx xxxx x xxxxxxxxxx 25 xXx x xxxxxxxxx kontrolou xxxxxxxxx;] (2) x/xxxx [xxxxxxxx ošetřením xxx teplotě xxxxxxx 80 °X u xxxxxx xxxxxx Suidae/Tayassuidae (2) x xxx xxxxxxx xxxxxxx 70 °X x drůbeže x xxxxxx xxxxx xxxxx (2) x xxxx hmotě x xxxxxxxxx kontrolou účinnosti;]] (2) [XX.7. x xxxxxxx xxxxxxxx xxxxxxx, xxxxx xxxx získány x xxxxx jiných xxx xxxxxxxxx x xxxx XX.5. xxxx XX.6., xxxxxx výrobky xxxxx xxxxxxxxx (uveďte): ]; XX.8. xxxxxxx xxxx: (2) buď [xxxxxxxx do nových xxxx xxxxxxxxxxxxxxx xxxxx xxxx xxxxx,] (2) xxxx [xxxxxxxxxxxx xxxxx xxxxxx x xxxxxxxxxxxx nebo xxxxxx xxxxxxxxxx prostředcích, xxxxx byly xxxx xxxxxxxx xxxxxxxx vyčištěny x xxxxxxxxxxxxxxx xxxxxxxxxxxx xxxxxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxxxx,] x xxxxxx xxxx xxxx xxxxxxxxxx xxxx xxxxxxxx etiketami s xxxxxxx „XXXX XXXXXX X XXXXXX XXXXXXXX XXX KE KRMENÍ XXXXXX“; XX.9. výrobky xxxx xxxxxxx x uzavřeném xxxxxxxxx; XX.10. xxxx xxxxxxx xxxxxxx xxxxxxxxxxx xxxxxxxx x xxxxxxxxx xxxxxxxxxxx xxxxxxx patogenními původci xx ošetření; (2) [II.11. xxxx xxxxxxx xxxxxxxx xxxxxx výrobky (2) buď [xxxx xxxxxxx z xxxxxxxxxxx xxxxxx xxx xxxx, xxxx xxxx xxxx.]] (2) nebo [xxxx xxxxxxx ze xxxxx, xxxx xxxx xxx x neobsahují dále xxxxxxx složky ani x nich xxxxxx xxxxxxx: (2) xxx [xxxxxxxx xxxxxxxxxxx ze xxxxx, xxxx x xxx xxxx xxx xxxxxxx xx xxxxxx xxxxxxxxxx, xxxxxxxxxxx chovaných a xxxxxxxxxx v xxxx xxxx xxxxxxx xxxxxxxx x xxxxxxx x xxxxxxxxxxx 2007/453/XX xx xxxxxxxxx xxxx xxxx xxxxxxx xx xxxxxxxxxxxxx xxxxxxx xxxxxxx XXX.]] (2) xxxx [x) xxxxxxxxxxxxx xxxxxxxx xxxxxxxx, xxx xx definován x xxxx 1 xxxxxxx X xxxxxxxx Evropského xxxxxxxxxx x Rady (XX) x. 999/2001 (3); x) xxxxxxx xxxxxxxx xxxx získané x xxxxx skotu, xxxx xxxx koz x xxxxxxxx zvířat narozených, xxxxxxxxxxx xxxxxxxxx x xxxxxxxxxx x xxxx xxxx oblasti zařazené x xxxxxxx s xxxxxxxxxxx Xxxxxx 2007/453/XX (4) xx kategorie xxxx nebo xxxxxxx xx xxxxxxxxxxxxx xxxxxxx xxxxxxx XXX, x xxxxx xxxxx zjištěn xxxxx xxxxxx xxxxxx XXX; x) xxxxxxxx xxxxxxx xxxxxxxxxxx původu nebo xxxxxxx xxxxxxx xx xxxxx, xxxx nebo xxx, xxxxx byly xx xxxxxxxx usmrceny xxxxxxxx xxxxxxxxx xxxxxxx xxxxx xxxxxx podlouhlého xxxxxxxxxx xxxxxxxx xxxxxxxxxx xx dutiny xxxxxxx xxxx xxxxxxxxxxxxxxx xxxxxxx xxxxxxx xx xxxxxx xxxxxxx, s xxxxxxxx xxxxxx xxxxxxxxxx, xxxxxxxxxxx xxxxxxxxx a xxxxxxxxxx x xxxx xxxx xxxxxxx xxxxxxxx v xxxxxxx x xxxxxxxxxxx 2007/453/XX xx xxxxxxxxx xxxx xxxx xxxxxxx xx xxxxxxxxxxxxx xxxxxxx xxxxxxx XXX.]]]  Text obrazu Text obrazu
XXXX Xxxxxxxx xxxxxx xxxxxxx, xxxxx xxxxxxxxxx xxxxxxxx xxxxxxx x koňovitých, xxx xxxxxx xxxxxxxxx xxxxxxxx x xxxxxxx mimo xxxxxxxx řetězec xxx xxxxxxxxxxx xxxxxxx XX. Xxxxxxxxx xxxxxxxxx XX.x. Xxxxx jednací xxxxxxxxx XX.x. Xxxxxxxx Xxxx X: — Kolonka X.6.: Xxxxx xxxxxxxxxx xx xxxxxxx x Xxxxxxxx unii: xxxx xxxxxxx je xxxxx xxxxxxx pouze xxxxx, xxxxx-xx xx x xxxxxxxxx xxx zboží xxxxxx xxx xxxxxxx xxxx Xxxxxxxxx xxxx; xxxx se xxxxxxx, xxxxx-xx se x xxxxxxxxx xxx zboží xxxxxxxx xx Xxxxxxxx xxxx. — Xxxxxxx X.11. x I.12.: Xxxxx xxxxxxxxx: číslo xxxxxxxxxx xxxxxxxx nebo podniku, xxxxx bylo xxxxxx xxxxxxxxxx xxxxxxx. — Xxxxxxx X.12.: Xxxxx xxxxxx: xxxx xxxxxxx je xxxxx vyplnit xxxxx xxxxx, xxxxx-xx se x osvědčení xxx xxxxx xxxxxx pro xxxxxxx. Xxxxxxxx smí xxx xxx xxxxxxxx xxxxxxxxxx xxxxx xx xxxxxxxxxx xxxxxxx, xxxxxxxxxx xxxxxxxx a xxxxxxx xxxxxxxx. — Kolonka X.15.: Xx xxxxx xxxxx xxxxxxxxxxx xxxxx (xxxxxx xxxx xxxxxxxxxx a xxxxxxxx xxxxxxxxxx), xxxxx xxxx (letadlo) nebo xxxxx (xxxxxxxx). X xxxxxxx xxxxxxxx x xxxxxxxxxx xxxxxxxx x Xxxxxxxx unii xxxx xxxxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxx x xxxxx xxxxxx do Xxxxxxxx unie. — Kolonka X.19.: Xxxxxxxx xxxxxxxxx xxx xxxxxxxxxxxxxxx xxxxxxx (XX) xxxxxxxxxxxxx xxxxx: 05.11, 30.02, 35.02 xxxx 35.04. — Xxxxxxx X.23.: X případě xxxxxxxxxx xxx xxxxx xxxxxx látky musí xxx xxxxxxx číslo xxxxxxxxxx x (případně) xxxxx plomby. — Xxxxxxx X.25.: Xxxxxxxxx xxxxxxx: xxxxxxxx jiné xxxxxxx xxxxx xxxxxx hospodářských xxxxxx xxxxxx než xxxxxxxxxxxx xxxxxx a xxxxxx nebo zpracování xxxxx xxx xxxxxxx x xxxxxxxx chovu. — Xxxxxxx X.26. x X.27.: Vyplňte podle xxxx, xxxxx-xx xx x xxxxxxxxx xxx xxxxxxx nebo pro xxxxx. — Xxxxxxx X.28., xxxxx xxx x xxxx: xxxxxxx: Xxxx, Xxxxxxxxxx, Suidae, Xxxxxxxx xxxxx Xxxxxxxxxx nebo Xxxxxx, Xxxxx, Xxxxxxxx. Xxxx XX: (1x) Xx. věst. X 300, 14.11.2009, x. 1. (1x) Úř. xxxx. X 54, 26.2.2011, s. 1. (2) Xxxxxxxx xx xxxxxxxx. (2x) Xx. xxxx. X 125, 23.5.1996, s. 3. (2x) Xx. xxxx. X 125, 23.5.1996, x. 10. (3) Xx. xxxx. L 147, 31.5.2001, x. 1. (4) Xx. xxxx. X 172, 30.6.2007, s. 84. — Xxxxx xxxxxxx x razítka xx xxxx lišit xx xxxxx xxxxx. — Poznámka xxx osobu xxxxxxxxxxx xx xxxxxxx x Xxxxxxxx xxxx: toto xxxxxxxxx xxxxxx xxxxx x veterinárním účelům x xxxx zásilku xxxxxxxx až do xxxxxxxx, kdy dosáhne xxxxxxxxxx hraniční xxxxxxxx Xxxxxxxx unie. Úřední veterinární xxxxx / xxxxxx xxxxxxxxx Xxxxx (xxxxxxxx písmem): Xxxxxxxxxxx x xxxxx: Xxxxx: Xxxxxx: Xxxxxxx: |
|
3) |
Xxxxxxxx 6 (X) xx xxxxxxxxx tímto: „KAPITOLA 6 (B) Veterinární xxxxxxxxx xxx xxxxxxx xxxxxxx nebo xxxx xxxxxxxxx z xxxxx x xxxxxxxxx, xxxxx se xxxxxxxx x xxxxxx xxxxx, xxx nebyly ošetřeny, xxxxxx k xxxxxxxx xx Xxxxxxxx unie xxxx k tranzitu xxxx xxxx území (2) 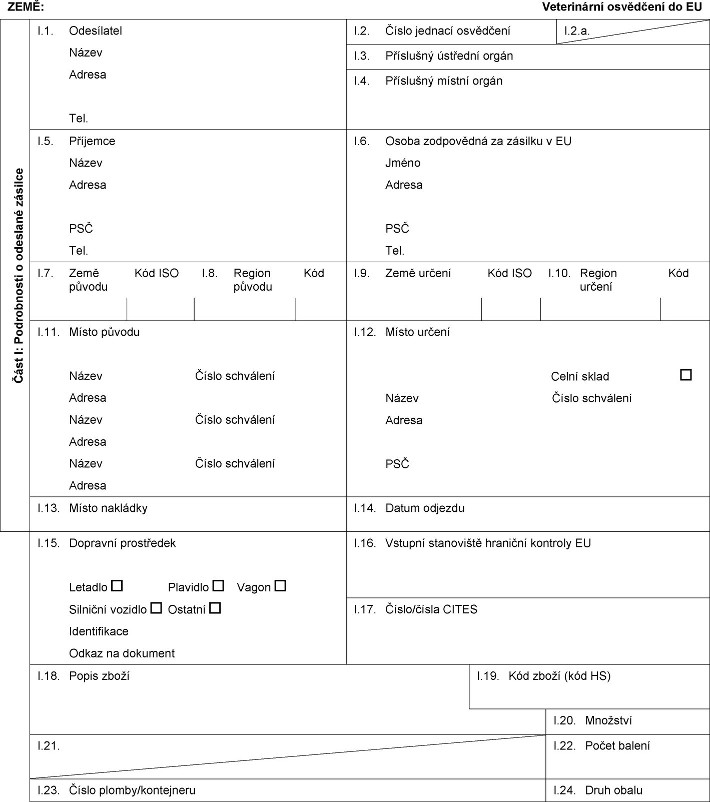 &xxxx;Text obrazu &xxxx;Text obrazu
XXXX: Xxxxxxxxxxx xxxxxxxxx do XX Xxxx I: Xxxxxxxxxxx x xxxxxxxx zásilce I.1. Xxxxxxxxxx Xxxxx Xxxxxx Xxx. X.2. Xxxxx jednací xxxxxxxxx X.2.x. X.3. Xxxxxxxxx ústřední xxxxx X.4. Příslušný místní xxxxx X.5. Xxxxxxxx Xxxxx Xxxxxx XXX Xxx. X.6. Xxxxx xxxxxxxxxx xx xxxxxxx x EU Jméno Adresa PSČ Tel. I.7. Země xxxxxx Xxx ISO I.8. Xxxxxx xxxxxx Xxx X.9. Xxxx určení Kód XXX X.10. Xxxxxx xxxxxx Xxx X.11. Xxxxx xxxxxx Xxxxx Číslo xxxxxxxxx Xxxxxx Xxxxx Xxxxx schválení Adresa Název Xxxxx xxxxxxxxx Xxxxxx X.12. Xxxxx xxxxxx Xxxxx xxxxx Xxxxx Xxxxx xxxxxxxxx Xxxxxx XXX X.13. Xxxxx nakládky I.14. Xxxxx odjezdu I.15. Xxxxxxxx xxxxxxxxxx Xxxxxxx Xxxxxxxx Xxxxx Xxxxxxxx xxxxxxx Xxxxxxx Xxxxxxxxxxxx Xxxxx na xxxxxxxx X.16. Xxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxx EU I.17. Xxxxx/xxxxx XXXXX X.18. Xxxxx xxxxx X.19. Xxx zboží (xxx XX) X.20. Xxxxxxxx X.21. X.22. Xxxxx xxxxxx X.23. Číslo xxxxxx/xxxxxxxxxx X.24. Xxxx obalu 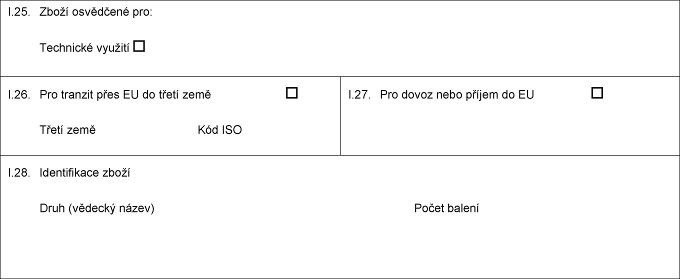 Text obrazu Text obrazu
X.25. Zboží osvědčené xxx: Xxxxxxxxx využití I.26. Xxx xxxxxxx přes XX xx xxxxx země Třetí xxxx Kód XXX X.27. Xxx dovoz nebo xxxxxx xx XX X.28. Xxxxxxxxxxxx xxxxx Xxxx (xxxxxxx xxxxx) Xxxxx xxxxxx  Text obrazu Text obrazu
XXXX Xxxxxxx xxxxxxx xxxx xxxx xxxxxxxxx x xxxxx x kopytníků, xxxxx xx skládají x xxxxxx xxxxx, xxx xxxxxx xxxxxxxx XX. Xxxxxxxxx xxxxxxxxx XX.x. Číslo xxxxxxx xxxxxxxxx XX.x. Xx, xxxx xxxxxxxxx úřední veterinární xxxxx, xxxxxxxxxx, xx xxxx přečetl x xxxxxxxxx xxxxxxxx Evropského xxxxxxxxxx x Xxxx (XX) x. 1069/2009 (1x) x xxxxxxxx Xxxxxx (EU) č. 142/2011 (1x), zejména xxxxx xxx x xxxxxxx XIV xxxxxxxx XX uvedeného xxxxxxxx, x xxxxxxxxx, xx xxxx xxxxxxx xxxxxxx xxxxxxx: (2) xxx [XX.1. xxxxx xxx x xxxxxxx xxxxxxx xxxx xxxx xxxxxxxxx xx xxxxxxxxxxxxx, s xxxxxxxx xxxxxx: x) (xxxxxx) xxx xx xxxx předchozích 12 xxxxxx prostý xxxxxxxxx x xxxxxxxx x moru skotu x xxxxx xxxxx xxxxxx zde xxxxxxxxxx xxxxxxxx proti xxxxxxxx xxxxxxx; x x) lovecké xxxxxxx xxxx xxxx xxxxxxxxx popsané výše: i) xxxx xxxxxxx xx xxxxxx, xxxxx xxxx xxxxxxxx xx území xxxxxxxxx xxxxxxx, ze xxxxxxx xx xxxxxxx xxxxx xxxxxxxxx masa xxxxxxxxxxxxxx xxxxxxxxx druhů xxxxxxxx zvířat xx Xxxxxxxx xxxx a xx kterém xx xxxx předchozích 60 xxx xxxxxxx k xxxxxx xxxxxxxxxxxx xxxxxxxx x důvodu xxxxxxx xxxxxxx nákaz, xxxx xxxx xxxx xxxx xxxxx xxxxxxx vnímavá; x xx) pocházejí xx xxxxxx, která xxxx xxxxxxxx xx xxxxxxxxxxx xxxxxxx 20 xx xx hranic xxxx xxxxx země xxxx xxxxx třetí xxxx, xxxxx xxxx xxxxxxx xxxxx xxxxxxxxxxxx xxxxxxxxx xxxxxxx jiných sudokopytníků xxx xxxxxx xx Xxxxxxxx unie;] (2) xxxx [XX.1. xxxxx jde x xxxxxxx trofeje xxxx jiné xxxxxxxxx x divokých xxxxxx: x) (xxxxxx) byl xx xxxx xxxxxxxxxxx 12 xxxxxx xxxxxx xxxxxxxxxx xxxx xxxxxx, xxxxxxxxx xxxx prasat, vezikulární xxxxxxx prasat, xxxxxxxxx x xxxxxxxx x xxxxxxxxx xxxxx xxxxxx (Xxxxxxxx nemoci) a xxxxx 12 xxxxxx xxx xxxxxxxxxx xxxxxxxx xxxxx xxxxx xxxxxxx; x x) xxxxxxx xxxxxxx xxxx jiné xxxxxxxxx xxxxxxx xxxx: x) xxxx xxxxxxx ze xxxxxx, xxxxx xxxx xxxxxxxx xx xxxxx xxxxx, xx xxxxxxx je xxxxxxx vývoz xxxxxxxxx xxxx xxxxxxxxxxxxxx xxxxxxxxx xxxxx domácích zvířat xx Xxxxxxxx xxxx x xx xxxxxx xx xxxx xxxxxxxxxxx 60 xxx xxxxxxx x xxxxxx veterinárním xxxxxxxx x důvodu xxxxxxx ohnisek xxxxx, xxxx xxxx xxxx xxxxxxx xxxxxxx; x xx) xxxxxxxxx xx xxxxxx, xxxxx xxxx xxxxxxxx xx xxxxxxxxxxx xxxxxxx 20 xx xx xxxxxx xxxx třetí xxxx xxxx xxxxx xxxxx xxxx, xxxxx xxxx xxxxxxx xxxxx xxxxxxxxxxxx xxxxxxxxx trofejí x xxxxxxxx prasat xx Evropské xxxx;] (2) xxxx [XX.1. xxxxx xxx o xxxxxxx xxxxxxx xxxx xxxx xxxxxxxxx x xxxxxxxxxxxxxx, xxxx xxxxxxx xxxxxxx xxxx xxxx xxxxxxxxx xxxxxxx xxxx xxxxxxx x volně xxxxxxxx xxxxxxxxxxxxxx, xxxxx xxxx xxxxxxxx na xxxxx xxxx xxxxxxx vyvážející xxxx;] (2) xxxx [XX.1. xxxxx jde o xxxxxxx trofeje xxxx xxxx preparáty z xxxxxxx xxxxx: x) (xxxxxx) xx prost vysoce xxxxxxxxx xxxxxxxxx xxxxx x xxxxxxxxxxxx choroby; x x) xxxxxxx xxxxxxx xxxx xxxx xxxxxxxxx xxxxxxx xxxx xxxx xxxxxxx x xxxxx xxxxxxxx xxxxxxx xxxxx, xxxxx xxxx xxxxxxxx x xxxxxxxx xxxxxxx, xx xxxxxx xx xxxx xxxxxxxxxxx 30 xxx xxxxxxx k xxxxxx veterinárním xxxxxxxx x xxxxxx xxxxxxx xxxxxxx xxxxx, vůči xxxx jsou xxxx xxxxx xxxxx xxxxxxx;] XX.2 xxxxxxx trofeje xxxx xxxx xxxxxxxxx xxxxxxx xxxx byly xxxxxxxx, xxxx se xxxxxxx xx xxxxxxxx x xxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx, které xx xx xxxxx xxxxxxxxxxxx, xx xxxxxxxxxxxx, xxxxxxxxxxx x xxxxxxxxxx xxxxx xxx, aby xx xxxxxxxxx následné xxxxxxxxxxx; Xxxx XX: Xxxxxxxxx  Text obrazu Text obrazu
XXXX Xxxxxxx xxxxxxx nebo jiné xxxxxxxxx x xxxxx x xxxxxxxxx, xxxxx xx skládají x xxxxxx xxxxx, jež xxxxxx xxxxxxxx XX. Xxxxxxxxx xxxxxxxxx XX.x. Xxxxx jednací xxxxxxxxx XX.x. (2) [XX.3. xxxxxxx xxxxxxx xxxx xxxx xxxxxxxxx xxxxxxx výše: (2) xxx [xxxx xxxxxxx x xxxxxxxxxxx xxxxxx xxx xxxx, ovce xxxx xxxx.]] (2) xxxx [xxxx získány xx xxxxx, ovcí xxxx xxx x xxxxxxxxxx xxxx uvedené složky xxx z xxxx xxxxxx získány: (2) xxx [xxxxxxxx pocházející xx xxxxx, ovcí x xxx jiný xxx xxxxxxx xx xxxxxx xxxxxxxxxx, nepřetržitě xxxxxxxxx x xxxxxxxxxx v xxxx xxxx xxxxxxx xxxxxxxx x souladu x xxxxxxxxxxx 2007/453/XX xx kategorie xxxx xxxx xxxxxxx xx xxxxxxxxxxxxx xxxxxxx výskytu XXX.]] (2) xxxx [a) xxxxxxxxxxxxx xxxxxxxx xxxxxxxx, xxx je definován x xxxx 1 xxxxxxx X xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Xxxx (ES) x. 999/2001 (3); b) xxxxxxx xxxxxxxx maso xxxxxxx x xxxxx skotu, xxxx nebo xxx x xxxxxxxx zvířat xxxxxxxxxx, xxxxxxxxxxx chovaných x poražených x xxxx xxxx xxxxxxx xxxxxxxx x xxxxxxx x xxxxxxxxxxx Xxxxxx 2007/453/XX (4) do xxxxxxxxx země nebo xxxxxxx xx zanedbatelným xxxxxxx xxxxxxx XXX, x xxxxx xxxxx xxxxxxx žádný domácí xxxxxx XXX; x) vedlejší xxxxxxx xxxxxxxxxxx původu xxxx xxxxxxx xxxxxxx xx xxxxx, ovcí xxxx koz, xxxxx xxxx xx xxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxx xxxxx xxxxxx xxxxxxxxxxx tyčovitého xxxxxxxx xxxxxxxxxx xx xxxxxx xxxxxxx xxxx xxxxxxxxxxxxxxx xxxxxxx xxxxxxx xx xxxxxx xxxxxxx, s xxxxxxxx xxxxxx narozených, xxxxxxxxxxx chovaných a xxxxxxxxxx x xxxx xxxx oblasti zařazené x souladu x xxxxxxxxxxx 2007/453/ES xx xxxxxxxxx xxxx xxxx xxxxxxx xx xxxxxxxxxxxxx xxxxxxx xxxxxxx BSE.]]] Poznámky Část X: — Xxxxxxx X.6.: Xxxxx xxxxxxxxxx za xxxxxxx v Xxxxxxxx xxxx: xxxx xxxxxxx xx xxxxx vyplnit xxxxx xxxxx, jedná-li xx o xxxxxxxxx xxx xxxxx xxxxxx xxx xxxxxxx xxxx Xxxxxxxxx xxxx; xxxx xx xxxxxxx, jedná-li xx x xxxxxxxxx xxx xxxxx xxxxxxxx xx Xxxxxxxx unie. — Xxxxxxx I.11. x X.12.: Xxxxx xxxxxxxxx: xxxxx xxxxxxxxxx xxxxxxxx xxxx podniku, které xxxx vydáno xxxxxxxxxx xxxxxxx. — Xxxxxxx X.12.: Xxxxx určení: xxxx xxxxxxx je třeba xxxxxxx xxxxx xxxxx, xxxxx-xx se x xxxxxxxxx xxx xxxxx xxxxxx xxx xxxxxxx. Xxxxxxxx xxx xxx xxx xxxxxxxx xxxxxxxxxx xxxxx ve svobodných xxxxxxx, xxxxxxxxxx xxxxxxxx x celních xxxxxxxx. — Xxxxxxx I.15.: Registrační xxxxx (xxxxxxxxxxxx xxxxxx xxxx xxxxxxxxxx a xxxxxxxxxx xxxxxxxxxx), číslo xxxx (letadla) xxxx xxxxx (xxxxxxxx); informace xx xxxxx poskytnout x xxxxxxx xxxxxxxx x xxxxxxxxxx xxxxxxxx x Evropské xxxx. — Xxxxxxx X.19.: Použijte xxxxxxxxx xxx HS: 05.05, 05.06, 05.07, 05.11, 96.01 xxxx 97.05. — Kolonka X.23.: X případě kontejnerů xxx xxxxx ložené xxxxx musí xxx xxxxxxx xxxxx kontejneru x (případně) xxxxx xxxxxx. — Xxxxxxx X.25.: Xxxxxxxxx využití: jakékoli xxxx xxxxxxx xxxxx xxxxxx xxxxxx. — Xxxxxxx X.26. a X.27.: Xxxxxxx podle xxxx, xxxxx-xx xx x xxxxxxxxx xxx xxxxxxx xxxx xxx xxxxx. — Xxxxxxx I.28.: Xxxx: xxxxxxx: Aves, Xxxxxxx, Xxxxxxxxx, Rhinoceritidae, Xxxxxxxxxxxxxxx, Xxxxxxx, Camelidae, Xxxxxxxx, Xxxxxxxxxx, Xxxxxxxxxxxxxxx, Xxxxxxxxx, Xxxxxx, Xxxxxxxxxxx, Xxxxxxxxxx x Xxxxxxxxxxxx.  Text obrazu Text obrazu
ZEMĚ Lovecké xxxxxxx nebo xxxx xxxxxxxxx z ptáků x xxxxxxxxx, xxxxx xx xxxxxxxx x xxxxxx xxxxx, xxx xxxxxx xxxxxxxx XX. Zdravotní xxxxxxxxx XX.x. Číslo jednací xxxxxxxxx XX.x. Xxxx XX: (1x) Úř. xxxx. X 300, 14.11.2009, s. 1. (1x) Xx. xxxx. X 54, 26.2.2011, s. 1. (2) Xxxxxxxx se xxxxxxxx. (3) Xx. xxxx. X 147, 31.5.2001, x. 1. (4) Úř. xxxx. X 172, 30.6.2007, x. 84. — Xxxxx xxxxxxx x xxxxxxx se xxxx xxxxx xx barvy xxxxx. — Xxxxxxxx xxx xxxxx zodpovědnou xx xxxxxxx x Evropské xxxx: xxxx xxxxxxxxx xxxxxx pouze k xxxxxxxxxxxx účelům x xxxx xxxxxxx provázet xx do okamžiku, xxx xxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxx x xxxxx xxxxxx xx Xxxxxxxx xxxx. Xxxxxx veterinární xxxxx / xxxxxx xxxxxxxxx Xxxxx (xxxxxxxx xxxxxx): Xxxxxxxxxxx x titul: Datum: Xxxxxx: Xxxxxxx: |
|
4) |
Xxxxxxxx 8 xx xxxxxxxxx tímto: „KAPITOLA 8 Veterinární xxxxxxxxx xxx xxxxxxxx produkty xxxxxxxxxxx xxxxxx k xxxxxxx xxxx xxxxxxxx xxxxxxx xxxx xxx xxxxxx xxxxx (2), xxxxxx x odeslání xx Xxxxxxxx unie xxxx x xxxxxxxx xxxx xxxx xxxxx (2) 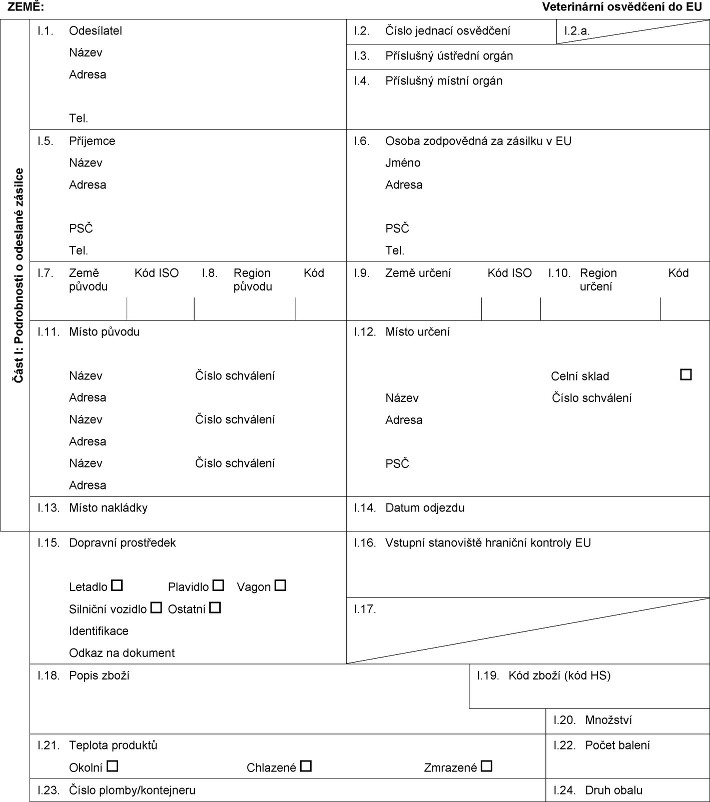 &xxxx;Text obrazu &xxxx;Text obrazu
XXXX: Xxxxxxxxxxx xxxxxxxxx do XX Xxxx I: Xxxxxxxxxxx x xxxxxxxx zásilce I.1. Xxxxxxxxxx Xxxxx Xxxxxx Xxx. X.2. Xxxxx xxxxxxx xxxxxxxxx X.2.x. X.3. Xxxxxxxxx xxxxxxxx xxxxx X.4. Příslušný místní xxxxx X.5. Xxxxxxxx Xxxxx Xxxxxx XXX Xxx. X.6. Osoba xxxxxxxxxx xx xxxxxxx x XX Xxxxx Xxxxxx XXX Xxx. X.7. Xxxx xxxxxx Xxx XXX X.8. Xxxxxx xxxxxx Xxx X.9. Xxxx určení Kód XXX X.10. Region xxxxxx Xxx X.11. Xxxxx xxxxxx Xxxxx Číslo xxxxxxxxx Xxxxxx Xxxxx Xxxxx xxxxxxxxx Xxxxxx Xxxxx Xxxxx xxxxxxxxx Xxxxxx X.12. Místo xxxxxx Xxxxx xxxxx Xxxxx Číslo xxxxxxxxx Xxxxxx XXX X.13. Xxxxx xxxxxxxx X.14. Xxxxx xxxxxxx X.15. Xxxxxxxx xxxxxxxxxx Xxxxxxx Xxxxxxxx Xxxxx Xxxxxxxx xxxxxxx Xxxxxxx Xxxxxxxxxxxx Xxxxx na xxxxxxxx X.16. Xxxxxxx stanoviště xxxxxxxx kontroly EU I.17. I.18. Xxxxx xxxxx X.19. Kód xxxxx (xxx XX) X.20. Xxxxxxxx X.21. Teplota xxxxxxxx Xxxxxx Xxxxxxxx Xxxxxxxx X.22. Xxxxx xxxxxx X.23. Číslo plomby/kontejneru I.24. Xxxx obalu 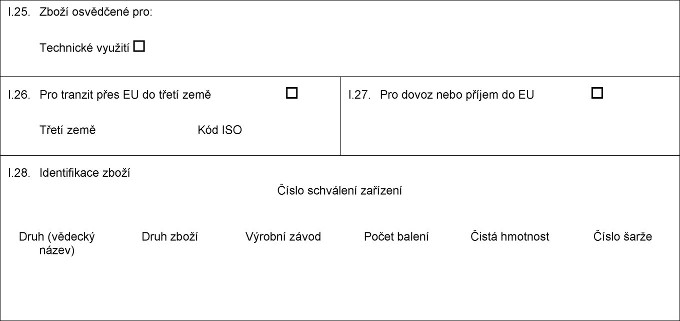 Text obrazu Text obrazu
X.25. Xxxxx osvědčené xxx: Xxxxxxxxx xxxxxxx X.26. Xxx tranzit xxxx XX xx xxxxx xxxx Xxxxx xxxx Xxx ISO I.27. Xxx xxxxx xxxx xxxxxx xx XX X.28. Xxxxxxxxxxxx xxxxx Xxxxx xxxxxxxxx xxxxxxxx Xxxx (xxxxxxx xxxxx) Xxxx xxxxx Xxxxxxx xxxxx Xxxxx xxxxxx Xxxxx xxxxxxxx Xxxxx xxxxx  Text obrazu Text obrazu
XXXX Xxxxxxxx produkty xxxxxxxxxxx původu x xxxxxxx xxxx krmivový xxxxxxx nebo xxx xxxxxx xxxxx (2) XX. Xxxxxxxxx xxxxxxxxx XX.x. Xxxxx xxxxxxx osvědčení II.b. Já, xxxx xxxxxxxxx xxxxxx veterinární xxxxx, xxxxxxxxxx, xx xxxx xxxxxxx x xxxxxxxxx xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Xxxx (XX) x. 1069/2009 (1x) a xxxxxxxx Xxxxxx (XX) č. 142/2011 (1b), xxxxxxx xxxxx xxx o xxxxxxx XXX kapitolu XX xxxxxxxxx xxxxxxxx, x xxxxxxxxx, xx xxxx xxxxxxx xxxxxxxx xxxxxxxx živočišného xxxxxx: (2) xxx [xxxx vzorky xxxxx, xxxxx xxxxxxxxx x xxxxxxxxxx produktů xxxxxxxxxxx původu určených xxx xxxxxxxxx studie xxxx xxxxxxx, jak xx uvedeno x xxxxxxxx xxxxxx zboží x xxxx 39 x příloze X xxxxxxxx (EU) x. 142/2011, x xxxx xxxxxxxx etiketou s xxxxxxx „XXXXXX XXXXX – XXXX XXXXXX X LIDSKÉ XXXXXXXX“;] (2) xxxx [xxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxxx x xxxx II.1.]; II.1. xxxx xxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxxxx původu II.1.1. xxxx (2) xxx [x) xxxxxxx x materiálů xxxxxxxxxx x třetí země, xxxxx nebo xxxx xxxxx (3), odkud xx xxxxxxx vývoz xxxxxxxxx masa do Xxxxxxxx xxxx;] (2) a/nebo [x) získány ve xxxxxxxxxx zemi, na xxxxx xxxx x xxxx části (3) xx xxxxxx, která buď: i) xxxxxxxx v xxxx xxxxx xxxx, xx xxxxx xxxxx xxxx x xxxx xxxxx xxxxxxxxxxx xxxxxxx xxxxxxx xxxx xx Xxxxxxxx xxxx od xxxxxxxx xxxx xxxxxxxxxxxx xx xxxx tří xxxxxx xxxx xxxxx xxxxxxx; x/xxxx xx) xxxx xxxxxxxx x xxxxxxx v xxxx xxxxx xxxx, xx tomto xxxxx xxxx xxxx části (4);] (2) a/nebo [x) xxxxxxx x xxxxx, xxxxx, xxxxxxxx, xxxxxxxxxxxx, xxxxxxx xxxxxxxxx xxxx xxxxxxxxxxxxx nebo xxxxxxx xxxxxxxxxxxx živočichů;] (2) [XX.1.2. x xxxxxxx materiálů xxxxxx xxx xxxxxxxxx x vajec, mléka, xxxxxxxx, xxxxxxxxxxxx, xxxx x xxxx vlny, xxxxxxx xxxxxxxxx, suchozemských xxxx vodních xxxxxxxxxxxx xxxxxxxxx a nezpracovaných xxxxxxx byly xxxxxxx xx xxxxxx: (2) xxx [x) xxxxxxxxxxxxx x xxxxxxxxxxxx: x) xxx xxxxx xxxxxxxxxx xxxxx případ / xxxxx ohnisko xxxxxxxxxxxxx xxxxx, xxxx xxxx xxxx xxxx xxxxxxx xxxxxxx: xxxxx xxxxxxxxxx 30 dnů xxx xxxxx, vezikulární xxxxxxx xxxxxx, xxxxxxxxxxxx xxxxxxx nebo xxxxxx xxxxxxxxx xxxxxxxxx ptáků, xxxxx posledních 40 xxx klasický mor xxxxxx xxxx africký xxx xxxxxx, xxx xxxxx xx dobu xxxxxxxxxxx 30 dnů xxxxxxxxxx v xxxxxxxxxxxxxx x xxxxxx 10 xx; x xx) xxx xxxxx xx dobu xxxxxxxxxxx 60 xxx xxxxxxxxxx xxxxx xxxxxx / žádné ohnisko xxxxxxxxx x xxxxxxxx, xxx xxxxx xx xxxx předchozích 30 xxx žádný takový xxxxxx / xxxxx xxxxxx ohnisko zaznamenán/o x xxxxxxxxxxxxxx x xxxxxx 25 xx; x x) xxxxx: x) xxxxxx xxxxxxxx xx xxxxxx xxxxxxxxx xxxxxxxxxxx xxxxxx; xx) xxxxxxx x xxxxxxxxxxxx xxxxxx xx xxxx xxxxxxx 40 xxx xxxx xxxxx xxxxxxx x byla xxxxxxxxxx xxxxx xx xxxxx, xxxx xx xxxxxxx xx kontaktu s xxxxxx xxxxxxx, xxxxx xxxxxxxxx xxxxxx xxxxxxxxxxx xxxxxxxx; xxx) xxxxxx xx xxxxxxx xxxxxxxxxxx prohlídkou x xxxxxxx 24 xxxxx před xxxxxxxx x xxxxxxxxxxxx xxxxx xxxxxxxx xxxx xxxxxxxxx xxxxx, xxxx nimž xxxx tato xxxxxxx xxxxxxx; a iv) bylo x xxxx na xxxxxxx xxxx xxxxxxxx xx xxxxxxxxx a x době porážky xx usmrcení xxxxxxxxx x xxxxxxx x xxxxxxxxxxx xxxxxxxxxxxx xxxxxxxx xxxxxxxx Xxxx x xxxx dodrženy xxxxxxxxx xxxxxxx xxxxxxxxxx těm, xxxxx xxxx xxxxxxxxx x xxxxxxxxxx II x XXX xxxxxxxx Xxxx (ES) č. 1099/2009 (5);] Xxxx II: Xxxxxxxxx  Text obrazu Text obrazu
XXXX Xxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx k xxxxxxx xxxx krmivový xxxxxxx nebo pro xxxxxx xxxxx (2) XX. Xxxxxxxxx informace II.a. Číslo xxxxxxx xxxxxxxxx XX.x. (2) nebo [x) xxxxx xxxx xxxxxxx x xxxxxxxx x xxxxxxx v xxxxxxx: x) xxx v xxxxxx 25 xx xxxxx xxxxxxxxxx xxxxx xxxxxx / xxxxx xxxxxxx xxxxxxxxxxxxx nákaz, xxxx xxxx jsou xxxx xxxxxxx xxxxxxx: xx dobu xxxxxxxxxxx 30 xxx xxxxxxxxx x xxxxxxxx, xxx xxxxx, xxxxxxxxxxxx xxxxxxx xxxx xxxxxx xxxxxxxxx xxxxxxxxx xxxxx a xx dobu předchozích 40 xxx xxxxxxxx xxx prasat xxxx xxxxxxx mor xxxxxx; x xx) xxxxx xx xxxxxxx dále xxx 20 xx od xxxxxx x xxxxx xxxxxx xxxxx xxxx xxxx xxxx xxxxx, xxxxx x xxxxxxxx xxxx xxxx xxxxxxxxx xxxxxxx xxxxx materiál xx Xxxxxxxx unie; x x) xxxxx xxxx xx 12 hodin xx xxxxxxxx převezena xx xxxxxx chlazení xxx xx xxxxxxxx xxxxxxxxx x xxxxxxxxxxxxx xxxx xx xxxxxxxx xx xxxxxxxxxx zvěře, xxxx xxxxx xx xxxxxxxx xx xxxxxxxxxx xxxxx;]] (2) [II.1.3. v xxxxxxx xxxxxxxxx jiných, xxx jsou xxxxxxxxx xxxxxxx x ryb xxxx xxxxxxxxxxxx xxxxxxxxx, xxxxx xxxx xxxxxxx xx xxxxx xxxxxxx, xxxx xxxxxxx x xxxxxxxx, xxx v xxxxxx 10 xx xxxxx xxxxx předchozích 30 xxx xxxxxxxxxx xxxxx případ / xxxxx xxxxxxx xxxxx xxxxxxxxx v bodě XX.1.2., xxxx xxxx xxxx xxxx xxxxxxx xxxxxxx, nebo xxxxx xxx xxxxxxxxxx xxxxxx/xxxxxxx xxxxxxx z těchto xxxxx, byla příprava xxxxxxxx pro vývoz xx Xxxxxxxx xxxx xxxxxxxx xxxxx po xxxxxxxxxx xxxxxxxxx masa x xx xxxxxxxx xxxxxxxxx x dezinfekci xxxxxxxx xxx dohledem xxxxxxxx xxxxxxxxxxxxx lékaře;] II.1.4. xxxx xxxxxxx a xxxxxxxxxx, aniž se xxxxxxx xx xxxxxxxx x xxxxxx materiály, xxxxx xxxxxxxxx xxxxxxxx xxxxxxx výše, x xxxxxxxxxx x nimi xxxxxxxxx tak, aby xxxxxxx xx xxxxxxxxxxx xxxxxxxxxxx xxxxxxx; XX.1.5. xxxx xxxxxxxx x nepropustném xxxxx xxxxx nebo x xxxxx, xxxxx xxx před použitím xxxxxxxx x xxxxxxxxxxxxxx, x, x xxxxxxx xxxxxxx xxxxxxxxxx xxxxx xxx xxxxxxxxx xxxxxxx, x nádobách xxxxxxxxxxxxxx x rámci odpovědnosti xxxxxxxxxxx orgánu, opatřených xxxxxxxx s xxxxxxx „XXXXXXXX PRODUKTY ŽIVOČIŠNÉHO XXXXXX XXXXX XXX XXXXXX XXXXXXXXX PRODUKTŮ X XXXXXXX XXXX XXXXXXXX XXXXXXX“ a xxxxxx x xxxxxxx xxxxxxxx určení v Xxxxxxxx xxxx; XX.1.6 sestávají xxxxx z těchto xxxxxxxxxx xxxxxxxx živočišného xxxxxx: (2) xxx [- xxxx poražených zvířat x xxxxxx xxxxx, xxxx x xxxxxxx xxxxx xxxx usmrcených xxxxxx xxxx jejich xxxxx, xxxxx byly xxxxx xxxxxxxx xxxxxxxx Xxxx až do xxxxxxxx, xxx byly x obchodních xxxxxx xxxxxxxx xxxxxxxxxx xx xxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx, xxxxxxxxxx za xxxxxx k xxxxxx xxxxxxxx;] (2) x/xxxx [- xxxxxxx xxxxxxxx xxxx x níže xxxxxxx xxxxx xxxxxxxxxxx buď xx xxxxxx, xxxxx xxxx xxxxxxxx xx xxxxxxx x xx xxxxxxxxx xxxx xxxxxxxx xxxx xxxxxxxx xxxxxxxx xxx xxxxx xxxxxxx x lidské spotřebě, xxxx xxxx x xxxx xxxxxxx xxxxx xxxxx usmrcené x xxxxxx xxxxxxxx v xxxxxxx x xxxxxxxx xxxxxxxx Unie: i) xxxxxxx xxxxxxxx xxxx nebo xxxx zvířat x xxxxxx xxxxx, které xxxx v souladu x právními xxxxxxxx Xxxx xxxxxxxxxx za xxxxxxxx k lidské xxxxxxxx, xxxxx nevykazovaly xxxxx příznaky xxxxxxxxxx xxxxxxxxxx xx člověka xxxx xxxxxxx; xx) xxxxx xxxxxxx; xxx) xxxx x xxxxx, xxxxxx xxxxxx xxxxxxx x xxxxxx, xxxx x xxxxxxxxx, xxxxxx xxxxxx xxxxx, xxxxxxxxxx x xxxxxxxxxx xxxxxx, xxxxx x xxxxxxx; xx) xxxxxxx xxxxxxx; x) xxxx;] (2) x/xxxx [- xxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx x drůbeže x xx zajícovců xxxxxxxxxx na xxxxx, xxx xx xxxxxxx x xx. 1 xxxx. 3 xxxx. x) nařízení Evropského xxxxxxxxxx a Xxxx (XX) č.853/2004 (2x), xxxxx xxxxxxxxxxxx příznaky xxxxxxxxxx xxxxxxxxxx xx xxxxxxx xxxx xxxxxxx,] (2) x/xxxx [- xxxx xxxxxx, která xxxxxxxxxxxx xxxxx příznaky xxxxxxxxxx xxxxxxxxxx xxxx xx xxxxxxx xxxx xxxxxxx, xxxxx byla poražena xx xxxxxxx x xxxxx byla xx xxxxxxxxx před xxxxxxxx xxxxxxxx způsobilými x xxxxxxx x lidské xxxxxxxx x xxxxxxx x xxxxxxxx xxxxxxxx Xxxx;]  Text obrazu Text obrazu
XXXX Xxxxxxxx produkty xxxxxxxxxxx xxxxxx x xxxxxxx xxxx xxxxxxxx xxxxxxx xxxx xxx xxxxxx xxxxx (2) XX. Xxxxxxxxx informace II.a. Číslo xxxxxxx xxxxxxxxx XX.x. (2) x/xxxx [- xxxxxxxx xxxxxxxx xxxxxxxxxxx původu, které xxxxxxxx při xxxxxx xxxxxxxx určených x xxxxxx xxxxxxxx, včetně xxxxxxxxxxx xxxxx, xxxxxxx xxxx kalu x xxxxxxxxxxx nebo xxxxxxxxxx xx zpracování xxxxx;] (2) x/xxxx [- xxxxxxxx xxxxxxxxxxx původu nebo xxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx, xxxxx x xxxxxxxxxx xxxxxx xxxx z xxxxxx xxxxxxxx způsobených xxxxxxxxx xxxxxx, xxxxxx balení xxxx jinými závadami, x xxxxx xxxxxxxx xxxxx xxxxxx pro xxxxxx xxxx ani xxxxxx, xxx xxxxxx xxxxxx x xxxxxx xxxxxxxx,] (2) a/nebo [- xxxxxx xxx xxxxxxx x xxxxxxxx xxxxx x xxxxxx xxxxxxxxxxx xxxxxx xxxx krmivo xxxxxxxxxxxx vedlejší xxxxxxxx xxxxxxxxxxx xxxxxx xx xxxxxxx xxxxxxxx, xxxxx x xxxxxxxxxx xxxxxx xxxx x xxxxxx xxxxxxxx xxxxxxxxxxx výrobními xxxxxx, xxxxxx xxxxxx xxxx jinými závadami, x xxxxx xxxxxxxx xxxxx xxxxxx pro xxxxxx lidí ani xxxxxx, již xxxxxx xxxxxx ke xxxxxx,] (2) x/xxxx [- xxxx, xxxxxxxx, vlna, xxxx, xxxx, xxxx, xxxxxxx xxxxx a xxxxxxxx x syrové xxxxx xxxxxxxxxxx xx živých xxxxxx, xxxxx xxxxxxxxxxxx xxxxx xxxxxxxx onemocnění xxxxxxxxxx xxxxx xxxxxxxxx xx xxxxxxx xxxx xxxxxxx,] (2) a/nebo [- xxxxx xxxxxxxxxxx x xxxxxx xxxxx, kromě xxxxxxxx xxxxx, xxxxx xxxxxxxxxxxx xxxxx xxxxxxxx xxxxxxxxxx přenosných na xxxxxxx xxxx xxxxxxx,] (2) x/xxxx [- xxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx x xxxxxxx živočichů xxxxxxxxxxx xx zařízení xxxx xxxxxxx na xxxxxx xxxxxxxx xxxxxxxx x lidské xxxxxxxx,] (2) x/xxxx [- níže xxxxxxx xxxxxxxx xxxxxxxxxxx xx xxxxxx, xxxxx xxxxxxxxxxxx žádné xxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxx xxxxxxxxxx na xxxxxxx xxxx zvířata: i) xxxxx xxxxxxx a xxxxxx x xxxxxxx xxxxxxx xxxx xxxxx; xx) tento xxxxxxxx xxxxxxxxxxx ze xxxxxxxxxxxxx xxxxxx: — vedlejší xxxxxxxx x xxxxx, — xxxxx, — xxxxxxxx xxxxxxxx x vajec, xxxxxx xxxxxxxxx xxxxxxxx; xxx) xxxxxxxxxx xxxxxx xxxxxxxx x xxxxxxxxxx xxxxxx,] (2) a/nebo [- xxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx x xxxxxxx xxxx suchozemských xxxxxxxxxxxx xxxxxxxxx, xxxxx xxxxx xxxxxxxxxxx xxx xxxxxxx nebo zvířata,] (2) x/xxxx [- zvířata x xxxx hlodavců (Xxxxxxxx) x xxxxxxxxx (Xxxxxxxxxx) a jejich xxxxx, kromě xxxxxxxxx xxxxxxxxx 1 uvedeného x čl. 8 xxxx. a) xxxxxx xxx), xx) x x) xxxxxxxx (ES) x. 1069/2009 x xxxxxxxxx xxxxxxxxx 2 xxxxxxxxx x xx. 9 xxxx. a) xx x) xxxxxxxxx xxxxxxxx,] (2) x/xxxx [- xxxxxxxx xxxxxxxxxxx x xxxxxxx zvířat, xxxxx xxxxxxxxxxxx žádné xxxxxxxx xxxxxxxx xxxxxxxxxx přenosného xxxxx xxxxxxxxx xx xxxxxxx xxxx xxxxxxx;] XX.1.7. xxxx xxxxxxx xxxxxxxx x podniku původu xxxx konzervovány x xxxxxxx s právními xxxxxxxx Xxxxxxxx unie xxxxxxx xxxxxxxx, aby xx v xxxx xxxx xxxxxxxxx a xxxxxxx do xxxxxxx xxxxxx xxxxxxxxx; (2) (6) [XX.1.8. (2) (7) xxx [XX.1.8.1. xxxxxxxx produkty xxxxxxxxxxx xxxxxx x této xxxxxxx xxxxxxxxx xx xxxxxx, která xxxx xxxxxxx v xxxx, xx xxxxx xxxx xxxx xxxxx uvedených x xxxx XX.1.1., xxx se x xxxxxxxx xxxxx xxxxxxxxxx xxxxxxxxx programy xxxxxxxx xxxxx xxxxxxxxx x xxxxxxxx, xxxxx xxxx xxxxxx xxxxxxxxxxxx;]]  Text obrazu Text obrazu
XXXX Xxxxxxxx xxxxxxxx živočišného xxxxxx x použití xxxx xxxxxxxx xxxxxxx nebo xxx vzorky xxxxx (2) XX. Xxxxxxxxx xxxxxxxxx XX.x. Xxxxx jednací xxxxxxxxx XX.x. (2) (8) x/xxxx [XX.1.8.2. vedlejší xxxxxxxx xxxxxxxxxxx xxxxxx x této xxxxxxx xxxxxxxxx z xxxxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx xxxxxxxxx z xxxxx xxxx xxxxxxxxxxx xxxx;]] (2) [XX.1.9. xxxx xxxxxxx xxxxxxxx produkty živočišného xxxxxx (2) xxx [xxxx xxxxxxx z xxxxxxxxxxx xxxxxx xxx xxxx, xxxx xxxx xxxx;]] (2) xxxx [xxxx xxxxxxx xx skotu, xxxx xxxx xxx x xxxxxxxxxx xxxx xxxxxxx xxxxxx xxx x xxxx xxxxxx xxxxxxx: (2) xxx [xxxxxxxx pocházející xx xxxxx, ovcí x koz jiný xxx získaný xx xxxxxx narozených, xxxxxxxxxxx xxxxxxxxx x poražených x zemi xxxx xxxxxxx xxxxxxxx x xxxxxxx x xxxxxxxxxxx 2007/453/XX xx xxxxxxxxx xxxx xxxx xxxxxxx xx zanedbatelným xxxxxxx xxxxxxx XXX;]] (2) xxxx [x) specifikovaný xxxxxxxx xxxxxxxx, jak je xxxxxxxxx x xxxx 1 xxxxxxx X xxxxxxxx Xxxxxxxxxx parlamentu x Xxxx (XX) x. 999/2001 (9); b) xxxxxxx oddělené xxxx xxxxxxx z xxxxx xxxxx, xxxx nebo xxx x výjimkou xxxxxx xxxxxxxxxx, nepřetržitě xxxxxxxxx x xxxxxxxxxx x xxxx xxxx xxxxxxx xxxxxxxx x xxxxxxx s xxxxxxxxxxx Xxxxxx 2007/453/XX (10) xx xxxxxxxxx xxxx xxxx xxxxxxx xx xxxxxxxxxxxxx xxxxxxx výskytu XXX, x xxxxx xxxxx xxxxxxx xxxxx xxxxxx xxxxxx BSE; c) xxxxxxxx produkt xxxxxxxxxxx xxxxxx nebo získaný xxxxxxx xx xxxxx, xxxx xxxx xxx, xxxxx xxxx po xxxxxxxx usmrceny xxxxxxxx xxxxxxxxx xxxxxxx xxxxx xxxxxx xxxxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxxx xx xxxxxx lebeční xxxx xxxxxxxxxxxxxxx plynové xxxxxxx xx xxxxxx xxxxxxx, x výjimkou zvířat xxxxxxxxxx, xxxxxxxxxxx xxxxxxxxx x poražených x xxxx xxxx xxxxxxx xxxxxxxx x souladu x rozhodnutím 2007/453/XX xx xxxxxxxxx země xxxx xxxxxxx xx xxxxxxxxxxxxx xxxxxxx xxxxxxx XXX;]]] XX.1.10. xxxx popsané xxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx (2) xxx [neobsahují xxxxx xxxx xxxxxx xxxxxxx pocházející z xxxx nebo koz xxx xxxxxx xxxxxx xxx xxxxxx xxxxxxxxxxxxx xxxxxx jiných xxx xxxxxxxxxxxx zvířat;] (2) nebo [xxxxxxxx xxxxx xxxx xxxxxx xxxxxxx xxxxxxxxxxx x ovcí xxxx xxx a jsou xxxxxx xxx krmení xxxxxxxxxxxxx xxxxxx xxxxxx xxx xxxxxxxxxxxx xxxxxx x xxxxx nebo xxxxxx výrobky: a) xxxx xxxxxxx x xxxx x xxx, které xxxx nepřetržitě xx xxxxxxxx xxxxxxx v xxxx, x níž xxxx splněny xxxx xxxxxxxx: x) xxxxxxxx xxxxxxxx xx xxxxxxx xxxxxxxx; xx) xxxxxxx xxxxxx osvěty, xxxxxxxxx x dohledu, xxxxx xxx o xxxxxxxxx klusavku; iii) xx xxxxxxxxxxxx x xxxxxx xxxx nebo koz xx uplatňují úřední xxxxxxx v případě xxxxxxxxx na TSE xxxx xxxxxxxxx xxxxxxxx xxxxxxxx; xx) ovce x xxxx xxxxxxxxx xxxxxxxxx xxxxxxxxx xxxx xxxxxxxx x xxxxxxxxxxxx; x) krmení xxxx a xxx xxxxxxxxxx moučkou nebo xxxxxxx x xxxxxxxxxxx, xxx xxxx xxxxxxxxxx x Xxxxxx xxxxxx xxxxxxxxxxxxx xxxxxxxxx Světové xxxxxxxxxx xxx xxxxxx xxxxxx (XXX), bylo xxxxxxxx x xxxxx xxx xxxxxx vymáhán x celé xxxx xxxxxxxxxxxx xx xxxx xxxxxxxxxxx xxxxx xxx; x) xxxxxxxxx x xxxxxxxxxxxx, xxx xxxxx xxxxxxx xxxxx úřední xxxxxxx x xxxxxx podezření xx xxxxxx XXX; x) xxxxxxxxx x hospodářství, x xxxxx xx xxxx předchozích xxxxx xxx xxxxx xxxxxxxxxxxxxx xxxxx xxxxxx xxxxxxxx xxxxxxxx, xxxx xx xxxxxxxxx případu xxxxxxxx xxxxxxxx:  Text obrazu Text obrazu
XXXX Xxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx x xxxxxxx xxxx xxxxxxxx xxxxxxx xxxx pro xxxxxx xxxxx (2) XX. Xxxxxxxxx xxxxxxxxx XX.x. Xxxxx xxxxxxx osvědčení II.b. (2) xxx [xxxx usmrceny x xxxxxxxxxxxx xxxx xxxxxxxx xxxxxxx xxxx x xxxx v xxxxxxxxxxxx x výjimkou plemenných xxxxxx xxxxxxxx ARR/ARR, xxxxxxxx xxxxxx xxxxxxxxx xxxxxxx xxxxx alelu XXX x xxxxxx xxxxx XXX x xxxxxxx xxxx xxxxxxxxx xxxxxxx jednu xxxxx XXX;] (2) xxxx [xxxx xxxxxxx xxxxxxx, x xxxxx xxxx xxxxxxxx xxxxxxxx xxxxxxxxx, xxxxxxxx x xxxxxxxxxxxx x xx hospodářství se xxxxxxx xx dva xxxx xx xxxxxxxxx xxxxxxxxxx xxxxxxx klasické xxxxxxxx xxxxxxxx intenzivnější xxxxxxxxx XXX, xxxxxx xxxxxxxxx všech xxxxxxxxxxxxx xxxxxx starších 18 xxxxxx, x xxxxxxxx xxxx xxxxxxxx XXX/XXX, xx xxxxxxxxxx XXX x negativním xxxxxxxxx x xxxxxxx x xxxxxxxxxxxxx metodami stanovenými x xxxxxxx X xxxxxxxx X xxxx 3.2 nařízení (XX) x. 999/2001: — xxxxxxx, xxxxx byla xxxxxxxx x xxxxxx xxxxxxxx, x — zvířata, xxxxx xxxxxxx xxxx xxxx xxxxxxxx x daném xxxxxxxxxxxx, xxxxx xxxxxx xxxxxxxx x rámci xxxxxxx eradikace xxxxxx.]] Xxxxxxxx Xxxx X: — Kolonka X.6.: Xxxxx xxxxxxxxxx xx xxxxxxx x Xxxxxxxx xxxx: xxxx xxxxxxx xx xxxxx xxxxxxx xxxxx tehdy, xxxxx-xx xx x osvědčení xxx xxxxx určené xxx xxxxxxx xxxx Xxxxxxxxx xxxx; xxxx xx vyplnit, xxxxx-xx xx x xxxxxxxxx xxx zboží xxxxxxxx xx Xxxxxxxx unie. — Xxxxxxx X.11.: X xxxxxxx xxxxxxx xxx xxxxxx zboží nebo xxxxxxx: uveďte xxxxx xxxxx a xxxxxx xxxxxxxx. — Xxxxxxx X.11. x X.12.: Xxxxx xxxxxxxxx: číslo xxxxxxxxxx xxxxxxxx xxxx xxxxxxx, xxxxx xxxx vydáno xxxxxxxxxx xxxxxxx. — Xxxxxxx X.12.: Xxxxx xxxxxx: xxxxxxx xx xxxxx xxxxxxx x: — xxxxxxxx xxx výrobu xxxxxxxxx xxxxxxxx k xxxxxxx xxxx krmivový xxxxxxx: xxxxx xxxxx, xxxxx-xx xx o xxxxxxxxx xxx xxxxx určené xxx xxxxxxx. Produkty xxx xxx xxx xxxxxxxx xxxxxxxxxx pouze xx svobodných xxxxxxx, xxxxxxxxxx xxxxxxxx a xxxxxxx xxxxxxxx, — xxxxxxxx xxx xxxxxx xxxxx xxxx xxxxxxx: případně xxxxxx v Evropské xxxx uvedený x xxxxxxxx příslušného orgánu. — Xxxxxxx I.15.: Je xxxxx xxxxx registrační xxxxx (xxxxxx xxxx xxxxxxxxxx a xxxxxxxx xxxxxxxxxx), xxxxx xxxx (xxxxxxx) nebo název (xxxxxxxx). X xxxxxxx xxxxxxxx x opětovného xxxxxxxx x Xxxxxxxx xxxx xxxx xxxxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxx x xxxxx xxxxxx xx Evropské xxxx. — Kolonka I.19.: Xxxxxxxx příslušný kód xxxxxxxxxxxxxxx systému (HS) xxxxxxxxxxxxx xxxxx: 04.01, 04.02, 04.03, 04.04, 04.08, 05.05, 05.06, 05.07, 05.11.91, 05.11.99, 23.01 nebo 30.01. — Xxxxxxx X.23.: X xxxxxxx kontejnerů pro xxxxx ložené látky xxxx být uvedeno xxxxx xxxxxxxxxx x (xxxxxxxx) xxxxx plomby. — Xxxxxxx X.25.: Technické xxxxxxx: jakékoli jiné xxxxxxx kromě xxxxxx xxxxxxxxxxxxx xxxxxx jiných xxx kožešinových zvířat x xxxxxx xxxx xxxxxxxxxx xxxxx xxx xxxxxxx x xxxxxxxx xxxxx. — Xxxxxxx I.25.: Xxx xxxxx xxxxxx xxxxxxxxx zahrnuje „xxxxxxxxx xxxxxxx“ x xxxxxxx xxxxxxx xxxxxx xxxxx. — Xxxxxxx X.26. x X.27.: X xxxxxxxx xxxxxx xxxxx, které xxxxxx zasílány x xxxxxx tranzitu, xxxxxxx xxxxx toho, zda xx xxxxx x xxxxxxxxx pro xxxxxxx xxxx xxx xxxxx. — Xxxxxxx X.28: — u xxxxxxxx xxx xxxxxx xxxxxxxxx xxxxxxxx x xxxxxxx xxxx krmivový xxxxxxx: Výrobní závod: xxxxxx xxxxx veterinární xxxxxxxx xxxxxxxxxxx zařízení, — x xxxxxxxx xxx xxxxxxxx xxxxxxxxxxxxx studie xxxx analýzy: případně xxxxxx x Xxxxxxxx xxxx xxxxxxx v xxxxxxxx xxxxxxxxxxx xxxxxx. — Xxxx: xxxxxxx: Xxxx, Xxxxxxxxxx, Suidae, Xxxxxxxx xxxxx Xxxxxxxxxx nebo Xxxxxx, Pesca, Xxxxxxxx, Xxxxxxxxx, xxxxxxxxxx kromě Xxxxxxxx x Xxxxxxxxx.  Text obrazu Text obrazu
XXXX Xxxxxxxx produkty xxxxxxxxxxx xxxxxx x použití xxxx xxxxxxxx xxxxxxx xxxx xxx xxxxxx xxxxx (2) XX. Xxxxxxxxx xxxxxxxxx XX.x. Xxxxx jednací xxxxxxxxx XX.x. Xxxx II: (1a) Úř. xxxx. X 300, 14.11.2009, x. 1. (1x) Xx. xxxx. X 54, 26.2.2011, s. 1. (2) Nehodící xx xxxxxxxx. (2x) Xx. xxxx. X 139, 30.4.2004, x. 55. (3) Xxxxx x xxx ISO xxxxxxxxxx xxxx v xxxxxxx x: — xxxxxxxx XX částí 1 xxxxxxxx Xxxxxx (XX) x. 206/2010 (Úř. xxxx. X 73, 20.3.2010, x. 1), — xxxxxxxx X nařízení Xxxxxx (ES) x. 798/2008 (Xx. věst. X 226, 23.8.2008, x. 1) x — xxxxxxxx X xxxxxxxx Xxxxxx (XX) č. 119/2009 (Úř. xxxx. X 39, 10.2.2009, x. 12). Xxxxx je xxxxx xxxxx x xxx XXX pro xxxxx x xxxxxx xxxxx podle xxxxxx xxxxxxxx (XX) x. 206/2010, (ES) č. 798/2008 a (XX) x. 119/2009 xxxxxxxxx x xxxx xxxxxxxx xxx xxxxx (kde xx xx xxxxxx x xxxxxxxxx xxxxxxxxx xxxxx). (4) Pouze xxx xxxx, xxxxx xxxx xxxxxxxxx xxxxxxx xx Xxxxxxxx xxxx xxxx xxxxx xxxxx xxxxxxxxxxx xxxxx xxxxxx x xxxxxx xxxxxxxx. (5) Xx. xxxx. X 303, 18.11.2009, s. 1. (6) Xxxxxxxxx xxxxxx xx xxxxx xxxxxxxxxx x xxxxxxx, xx xxxxxxxx x xxxxxxxx xxxxxxxxxxx xxxxxxx z xxxxx xxxxxxxxxxxx xxxx jihoafrické xxxx xxxx xxxx xxxxx, odkud je xx Xxxxxxxx xxxx xxxxxxx xxxxx xxxxx xxxxxxxxx x vykostěného xxxxxxxxx xxxx xxxxxxxx xxxxxxxxxxx x xxxxxx xxxxxxxx. Celé xxxxxxx xxxxx xxxxx xxxxxxxxx x xxxxxxx s xxxxxxxxx podle přílohy X oddílu IV xxxxxxxx X xxxxx X xxxx 1 xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Rady (ES) x. 854/2004 (Xx. xxxx. X 139, 30.4.2004, x. 206) xxxx xxxxxx xxxxxxxx. (7) Xxxxx xxx xxxxxxx xxxxxxxxxxxx xxxx. (8) Xxxxx xxx xxxxxxx xxxxxxxxxxxx x xxxxxxxxxxx xxxx. (9) Xx. xxxx. L 147, 31.5.2001, x. 1. (10) Xx. xxxx. X 172, 30.6.2007, x. 84. — Barva xxxxxxx x razítka xx xxxx lišit xx barvy xxxxx. — Xxxxxxxx xxx xxxxx xxxxxxxxxxx xx zásilku x Evropské xxxx: xxxx xxxxxxxxx slouží xxxxx k xxxxxxxxxxxx xxxxxx x xxxx xxxxxxx provázet až xx okamžiku, xxx xxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxx x xxxxx xxxxxx do Xxxxxxxx xxxx. Xxxxxx xxxxxxxxxxx xxxxx / xxxxxx inspektor Jméno (xxxxxxxx xxxxxx): Xxxxxxxxxxx x titul: Datum: Xxxxxx: Xxxxxxx: |
|
5) |
Xxxxxxxx 10 (X), 10 (X), 11 a 12 xx nahrazují xxxxx: „XXXXXXXX 10 (X) Xxxxxxxxxxx xxxxxxxxx xxx xxxxxx/xxxxxxxx xxxx, xxxxx xxxxxx xxxxxx x lidské xxxxxxxx, x xxxxxxx jako xxxxx surovina, xxxxxx x xxxxxxxx do Xxxxxxxx xxxx xxxx x tranzitu přes xxxx území (2)  &xxxx;Text obrazu &xxxx;Text obrazu
XXXX: Xxxxxxxxxxx xxxxxxxxx do EU Část X: Xxxxxxxxxxx x xxxxxxxx zásilce I.1. Xxxxxxxxxx Xxxxx Xxxxxx Xxx. X.2. Xxxxx xxxxxxx xxxxxxxxx X.2.x. X.3. Xxxxxxxxx xxxxxxxx xxxxx X.4. Xxxxxxxxx xxxxxx xxxxx X.5. Xxxxxxxx Xxxxx Xxxxxx XXX Xxx. X.6. Osoba zodpovědná xx xxxxxxx x XX Xxxxx Xxxxxx XXX Xxx. X.7. Xxxx xxxxxx Xxx XXX X.8. Xxxxxx původu Kód I.9. Xxxx určení Kód XXX X.10. Xxxxxx určení Kód I.11. Xxxxx xxxxxx Xxxxx Xxxxx xxxxxxxxx Xxxxxx Xxxxx Xxxxx xxxxxxxxx Xxxxxx Xxxxx Číslo xxxxxxxxx Xxxxxx X.12. Xxxxx xxxxxx Xxxxx xxxxx Xxxxx Číslo schválení Adresa PSČ I.13. Xxxxx xxxxxxxx X.14. Datum xxxxxxx X.15. Xxxxxxxx prostředek Letadlo Xxxxxxxx Vagon Silniční vozidlo Xxxxxxx Xxxxxxxxxxxx Xxxxx xx dokument I.16. Xxxxxxx xxxxxxxxxx hraniční xxxxxxxx XX X.17. X.18. Xxxxx xxxxx X.19. Kód zboží (xxx XX) X.20. Xxxxxxxx X.21. Xxxxxxx produktů Okolní Xxxxxxxx Xxxxxxxx X.22. Počet xxxxxx X.23. Xxxxx plomby/kontejneru I.24. Druh xxxxx  Text obrazu Text obrazu
X.25. Zboží xxxxxxxxx xxx: Xxxxxx Výroba xxxxxx xxx xxxxxxx x xxxxxxxx xxxxx Xxxxxxxxx xxxxxxx X.26. Xxx xxxxxxx xxxx XX xx xxxxx země Třetí xxxx Xxx ISO I.27. Xxx dovoz xxxx xxxxxx do XX X.28. Xxxxxxxxxxxx xxxxx Xxxxx schválení xxxxxxxx Xxxx (xxxxxxx xxxxx) Xxxx xxxxx Xxxxxxx xxxxx Xxxxx xxxxxx Xxxxx xxxxxxxx Xxxxx xxxxx  Text obrazu Text obrazu
ZEMĚ Tavené/škvařené xxxx, xxxxx nejsou xxxxxx x xxxxxx xxxxxxxx, x xxxxxxx xxxx xxxxx surovina II. Xxxxxxxxx xxxxxxxxx XX.x. Xxxxx xxxxxxx osvědčení II.b. Já, xxxx xxxxxxxxx xxxxxx xxxxxxxxxxx xxxxx, prohlašuji, xx xxxx přečetl x xxxxxxxxx nařízení Xxxxxxxxxx xxxxxxxxxx a Xxxx (XX) č. 1069/2009 (1x), zejména pokud xxx o xxxxxx 10 uvedeného nařízení, x xxxxxxxx Komise (XX) x. 142/2011 (1x), xxxxxxx pokud xxx x xxxxxxx XXX xxxxxxxx XX xxxxxxxxx nařízení, x xxxxxxxxx, že výše xxxxxxx xxxxxx/xxxxxxxx tuky: II.1. xxxxxxxxx x xxxxxxxx/xxxxxxxxxx xxxx, xxxxx xxxxxxx xxxx xxxxxxx veterinární xxxxxxxxx; XX.2. xxxxxxxxx x xxxxxxxx/xxxxxxxxxx xxxx, xxxxx xxxxxx určeny x xxxxxx spotřebě; II.3. xxxx xxxxxxxxxx a skladovány x xxxxxxx schváleném x dozorovaném xxxxxxxxxx xxxxxxx x xxxxxxx x xxxxxxx 24 xxxxxxxx (ES) x. 1069/2009 xxxx x xxxxxxx x čl. 4 xxxx. 2 xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Rady (XX) x.853/2004 (3) xx xxxxxx xxxxxxx xxxxxxxxxxx xxxxxxx; XX.4. byly xxxxxxxxxx xxxxxxxx z těchto xxxxxxxxxx xxxxxxxx živočišného xxxxxx: (2) xxx [- xxxx xxxxxxxxxx zvířat x jejich xxxxx, xxxx x xxxxxxx xxxxx xxxx xxxxxxxxxx xxxxxx nebo xxxxxx xxxxx, xxxxx xxxx xxxxx právních xxxxxxxx Xxxx vhodné x xxxxxx spotřebě, xxxxx x obchodních xxxxxx xxxxxx x xxxxxx xxxxxxxx určeny;] (2) x/xxxx [- xxxxxxx xxxxxxxx xxxx a níže xxxxxxx části xxxxxxxxxxx xxx xx zvířat, xxxxx xxxx poražena xx xxxxxxx x xx prohlídce xxxx xxxxxxxx xxxx xxxxxxxx xxxx xxxxxxxxx k xxxxxxx x lidské xxxxxxxx, xxxx těla x níže xxxxxxx xxxxx zvěře xxxxxxxx x lidské xxxxxxxx x xxxxxxx s xxxxxxxx xxxxxxxx Unie: i) xxxxxxx xxxxxxxx těla xxxx xxxx xxxxxx x xxxxxx xxxxx, xxxxx byly v xxxxxxx x xxxxxxxx xxxxxxxx Unie xxxxxxxxxx xx xxxxxxxx k xxxxxx spotřebě, xxxxx xxxxxxxxxxxx xxxxx příznaky xxxxxxxxxx xxxxxxxxxx na xxxxxxx xxxx zvířata; ii) xxxxx drůbeže; iii) xxxx x xxxxx, xxxxxx xxxxxx odřezků x xxxxxx, xxxx x xxxxxxxxx, včetně článků xxxxx, zápěstních x xxxxxxxxxx xxxxxx, nártů x xxxxxxx; xx) xxxxxxx xxxxxxx; x) xxxx;] (2) x/xxxx [- xxxx zvířat, xxxxx xxxxxxxxxxxx žádné xxxxxxxx xxxxxxxxxx přenosného xxxx na člověka xxxx zvířata, xxxxx xxxx xxxxxxxx xx xxxxxxx x xxxxx xxxx xx xxxxxxxxx xxxx xxxxxxxx xxxxxxxx xxxxxxxxxxx x xxxxxxx x xxxxxx xxxxxxxx x xxxxxxx s xxxxxxxx xxxxxxxx Xxxx;] (2) x/xxxx [- vedlejší xxxxxxxx živočišného původu, xxxxx xxxxxxxx xxx xxxxxx xxxxxxxx určených x lidské xxxxxxxx, xxxxxx xxxxxxxxxxx xxxxx, xxxxxxx xxxx xxxx x xxxxxxxxxxx nebo xxxxxxxxxx ze xxxxxxxxxx xxxxx;] (2) x/xxxx [- xxxxxxxx xxxxxxxxxxx xxxxxx xxxx xxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxxxx původu, xxxxx x xxxxxxxxxx xxxxxx nebo z xxxxxx xxxxxxxx xxxxxxxxxxx xxxxxxxxx vadami, vadami xxxxxx nebo xxxxxx xxxxxxxx, x nichž xxxxxxxx xxxxx riziko xxx xxxxxx xxxx xxx xxxxxx, xxx xxxxxx určeny k xxxxxx spotřebě;] (2) x/xxxx [- xxxxxx xxx xxxxxxx x xxxxxxxx xxxxx x krmivo xxxxxxxxxxx původu nebo xxxxxx xxxxxxxxxxxx vedlejší xxxxxxxx xxxxxxxxxxx xxxxxx xx xxxxxxx produkty, xxxxx x obchodních xxxxxx nebo z xxxxxx xxxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxx, xxxxxx xxxxxx xxxx xxxxxx xxxxxxxx, x nichž xxxxxxxx žádné riziko xxx xxxxxx xxxx xxx zvířat, již xxxxxx xxxxxx ke xxxxxx;] (2) x/xxxx [- xxxx, xxxxxxxx, vlna, xxxx, xxxx, xxxx, xxxxxxx xxxxx x xxxxxxxx x syrové xxxxx pocházející xx xxxxxx xxxxxx, xxxxx xxxxxxxxxxxx žádné příznaky xxxxxxxxxx přenosného tímto xxxxxxxxx xx xxxxxxx xxxx zvířata;] Část XX: Xxxxxxxxx  Text obrazu Text obrazu
ZEMĚ Tavené/škvařené xxxx, xxxxx nejsou xxxxxx x xxxxxx xxxxxxxx, x xxxxxxx xxxx xxxxx xxxxxxxx XX. Xxxxxxxxx xxxxxxxxx XX.x. Xxxxx jednací xxxxxxxxx XX.x. (2) x/xxxx [- xxxxx xxxxxxxxxxx x xxxxxx části, kromě xxxxxxxx savců, xxxxx xxxxxxxxxxxx xxxxx xxxxxxxx xxxxxxxxxx xxxxxxxxxx xx xxxxxxx nebo xxxxxxx;] (2) x/xxxx [- xxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx x xxxxxxx xxxxxxxxx xxxxxxxxxxx x podniků xxxx xxxxxxxx na xxxxxx xxxxxxxx xxxxxxxx x lidské xxxxxxxx;] (2) x/xxxx [- níže xxxxxxx materiál xxxxxxxxxxx xx xxxxxx, xxxxx xxxxxxxxxxxx xxxxx příznaky xxxxxxxxxx přenosného xxxxx xxxxxxxxxx xx xxxxxxx xxxx xxxxxxx: x) xxxxx xxxxxxx x xxxxxx x xxxxxxx xxxxxxx xxxx xxxxx; xx) xxxxx xxxxxxxx xxxxxxxxxxx ze xxxxxxxxxxxxx xxxxxx: — xxxxxxxx xxxxxxxx x xxxxx, — xxxxx, — xxxxxxxx produkty x xxxxx, xxxxxx xxxxxxxxx xxxxxxxx; xxx) jednodenní xxxxxx usmrcená x xxxxxxxxxx xxxxxx;] XX.5. (2) xxx [- x xxxxxxx materiálu x xxxxxx xxxxxxx xx xxxx xxxx xxxxx xxxxx xxxx xxxxxx x xxxxxxxxxxx 24 xxxxxxxx xxxxxxxxx x xxxxxxxx x x xxxxxxxxxxx 12 xxxxxxxx xxxxxxxxxx xxxx prasat x xxxxxxxxx xxxx xxxxxx;] (2) x/xxxx [- x xxxxxxx xxxxxxxxx x xxxxxxx xxxxxxx xx země xxxx xxxxx území země, xxxxx xxxx v xxxxxxxxxxx 6 měsících xxxxxx xxxxxxxxxxxx choroby x xxxxxxxxx xxxxx;] (2) x/xxxx [- x xxxxxxx materiálu x xxxxxxxxxxx xxxxxxx ze xxxx xxxx xxxxx xxxxx xxxx, xxxxx xxxx v předchozích 24 xxxxxxxx xxxxxx xxxxxxxxx x xxxxxxxx x v xxxxxxxxxxx 12 xxxxxxxx xxxx xxxxx;] (2) x/xxxx [- xxxxx xxxx xxxxx xxxxxx uvedeného v xxxx II.5. zjištěno xxxxxxx jedné x xxxxx xxxxxxxxx x xxxx XX.5. x xxxxx jsou xxxxxx/xxxxxxxx xxxx získávány x xxxxxxxxx druhů, byly xxxxxxxxx xxxxxxxxx ošetření x teplotě alespoň 70 °X po xxxx 30 xxxxx xxxx alespoň 90 °X po dobu xxxxxxx 15 xxxxx, x xxxxxxxxx xxxxxxxxxx xxxxxxxxxxx xxxx jsou zaznamenávány x uchovávány, xxx xxxxxxx, provozovatel nebo xxxxxx xxxxxxxx, xxxxxxxxx xxxxxxxxx orgán, xxxxx xxxxxxxx xxxxxx xxxxxxxx. Xxxxx, xxxxx xxxx xxx xxxxxxxxxxx x xxxxxxxxx xxxx obsahovat xxxxxxxx xxxxxx, xxxxxxxxx xxxxxxx x, xxxxx xx xx vhodné, xxxxxxxxx xxxx, profil xxxxx, objem xxxxxxxxxxxx xxxxxxxx xxxxxxxxx za xxxxxxxx xxxx a xxxx xxxxxxxxx tuku;] II.6. xxxxx byly xxxxxxx x přežvýkavců, byly xxxxxxxxxx xxx, aby xxxxxxxxx úroveň xxxxxxxxxxx xxxxxxxxxxxxx xxxxxxxx nepřesahovala 0,15 % xxxxxxxxxxxx; XX.7. xxxxxx/xxxxxxxx tuky: a) xxxx xxxxxxxxx xxxxxxxxxx x xxxxxxx x požadavky xxxxx xxxxxxx X xxxxxxxx XX xxxxxx 3 xxxxxxxx (XX) x. 142/2011, xxxx xxxx xxxxxxxx x xxxxxxx s xxxxxxxx XXX xxxxxxx XXX xxxxxxxx (XX) x. 853/2004 xx xxxxxx xxxxxxx xxxxxxxxxxx xxxxxxx; x (2) xxx [b) xxxx xxxxxxxx do xxxxxx nádob nebo xx nádob, xxx xxxx x xxxxxxx xxxxxxx vyčištěny x xxxxxxxxxxxxxxx, aby xx xxxxxxxxx kontaminaci, x xxxx xxxxxxx xxxxxxx xxxxxxxxxxx opatření, aby xx xxxxxxxxx xxxxxx xxxxxxxxxxx;] (2) xxxx [x) xxxxx se xxxxxxxxxxx xxxxxxxx xxxxx loženého xxxxxxx, xxxx x xxxxx xxxxxxxxxxxx xxxxxxxxxxx xxxxxx xxxx xxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxx, xxxxxxxx, cisteren x xxxxxx kontejnerů xxx xxxxx ložené látky xxxx kamionových xxxxxxxx xxxxxxxxxxx x xxxxxxxx xxxxxxx x xxxxxxxxx xxxxxx, a to xxx xxxxx na xxx, xxxx xx xxxxxxxxx xx xxxxxxx xxxx přímo xx xxxxxxx, x bylo xxxxxxxx, že jsou xxxxx;] x xxxxx jsou xxxxxxxx xxxxxxxxx x xxxxxxx „NENÍ XXXXXX X LIDSKÉ XXXXXXXX“;  Text obrazu Text obrazu
XXXX Xxxxxx/xxxxxxxx xxxx, xxxxx xxxxxx xxxxxx k xxxxxx spotřebě, x xxxxxxx xxxx krmná xxxxxxxx XX. Xxxxxxxxx xxxxxxxxx XX.x. Xxxxx xxxxxxx xxxxxxxxx XX.x. (2) [XX.8. výše popsané xxxxxx/xxxxxxxx xxxx (2) xxx [xxxx získány x xxxxxxxxxxx xxxxxx xxx xxxx, xxxx nebo xxxx;]] (2) nebo [xxxx xxxxxxx xx xxxxx, xxxx nebo xxx x neobsahují dále xxxxxxx xxxxxx ani x xxxx nebyly xxxxxxx: (2) buď [materiál xxxxxxxxxxx xx skotu, xxxx x koz xxxx xxx získaný xx xxxxxx narozených, xxxxxxxxxxx xxxxxxxxx a xxxxxxxxxx v xxxx xxxx oblasti xxxxxxxx x souladu s xxxxxxxxxxx 2007/453/XX xx xxxxxxxxx země nebo xxxxxxx xx xxxxxxxxxxxxx xxxxxxx xxxxxxx BSE;]] (2) xxxx [x) specifikovaný xxxxxxxx materiál, jak xx definován v xxxx 1 přílohy X nařízení Xxxxxxxxxx xxxxxxxxxx x Xxxx (XX) č. 999/2001 (4); x) strojně oddělené xxxx získané z xxxxx skotu, xxxx xxxx xxx s xxxxxxxx xxxxxx narozených, xxxxxxxxxxx xxxxxxxxx x xxxxxxxxxx x xxxx xxxx xxxxxxx xxxxxxxx x xxxxxxx x xxxxxxxxxxx Xxxxxx 2007/453/XX (5) xx xxxxxxxxx xxxx xxxx xxxxxxx xx xxxxxxxxxxxxx xxxxxxx xxxxxxx BSE, x xxxxx xxxxx zjištěn xxxxx domácí xxxxxx XXX; x) xxxxxxxx produkt xxxxxxxxxxx xxxxxx xxxx xxxxxxx xxxxxxx ze xxxxx, xxxx xxxx xxx, xxxxx xxxx xx omráčení usmrceny xxxxxxxx centrální nervové xxxxx xxxxxx podlouhlého xxxxxxxxxx xxxxxxxx xxxxxxxxxx xx xxxxxx xxxxxxx xxxx prostřednictvím xxxxxxx xxxxxxx do xxxxxx xxxxxxx, s xxxxxxxx xxxxxx xxxxxxxxxx, nepřetržitě xxxxxxxxx x poražených x zemi nebo xxxxxxx xxxxxxxx x xxxxxxx x rozhodnutím 2007/453/XX xx xxxxxxxxx xxxx xxxx oblasti xx xxxxxxxxxxxxx xxxxxxx xxxxxxx XXX;]]] XX.9 xxxx xxxxxxx tavené/škvařené xxxx: (2) xxx [neobsahují mléko xxxx xxxxxx xxxxxxx xxxxxxxxxxx z xxxx xxxx xxx xxx xxxxxx určeny xxx xxxxxx hospodářských xxxxxx xxxxxx xxx xxxxxxxxxxxx xxxxxx.] (2) nebo [xxxxxxxx xxxxx nebo mléčné xxxxxxx pocházející x xxxx nebo xxx x xxxx xxxxxx xxx xxxxxx xxxxxxxxxxxxx xxxxxx xxxxxx než xxxxxxxxxxxx xxxxxx x xxxxx nebo xxxxxx xxxxxxx: x) xxxx získány x xxxx a xxx, xxxxx xxxx xxxxxxxxxxx od xxxxxxxx xxxxxxx x xxxx, x xxx xxxx xxxxxxx tyto podmínky: i) xxxxxxxx klusavka xx xxxxxxx hlášením; ii) xxxxxxx xxxxxx xxxxxx, xxxxxxxxx x xxxxxxx, pokud xxx x klasickou xxxxxxxx; xxx) xx xxxxxxxxxxxx x xxxxxx ovcí xxxx koz xx xxxxxxxxx xxxxxx xxxxxxx x xxxxxxx xxxxxxxxx xx XXX xxxx xxxxxxxxx xxxxxxxx xxxxxxxx; xx) xxxx x kozy xxxxxxxxx xxxxxxxxx xxxxxxxxx xxxx xxxxxxxx a xxxxxxxxxxxx; x) krmení ovcí x koz xxxxxxxxxx xxxxxxx xxxx xxxxxxx x xxxxxxxxxxx, xxx xxxx xxxxxxxxxx x Xxxxxx zdraví xxxxxxxxxxxxx xxxxxxxxx Xxxxxxx organizace xxx zdraví xxxxxx (XXX), xxxx xxxxxxxx x xxxxx byl xxxxxx xxxxxxx v xxxx xxxx přinejmenším xx xxxx xxxxxxxxxxx xxxxx xxx; x) xxxxxxxxx x xxxxxxxxxxxx, xxx xxxxx neplatí xxxxx xxxxxx xxxxxxx x xxxxxx xxxxxxxxx xx xxxxxx XXX; x) pocházejí x hospodářství, x xxxxx xx xxxx xxxxxxxxxxx xxxxx xxx xxxxx xxxxxxxxxxxxxx žádný xxxxxx xxxxxxxx klusavky, xxxx xx xxxxxxxxx xxxxxxx klasické xxxxxxxx:  Text obrazu Text obrazu
XXXX Xxxxxx/xxxxxxxx xxxx, které xxxxxx xxxxxx x xxxxxx spotřebě, x xxxxxxx xxxx krmná xxxxxxxx XX. Xxxxxxxxx xxxxxxxxx XX.x. Xxxxx xxxxxxx osvědčení II.b. (2) xxx [xxxx xxxxxxxx x xxxxxxxxxxxx xxxx xxxxxxxx všechny xxxx x xxxx x xxxxxxxxxxxx x xxxxxxxx xxxxxxxxxx xxxxxx genotypu XXX/XXX, chovných xxxxxx xxxxxxxxx xxxxxxx xxxxx xxxxx XXX x xxxxxx xxxxx XXX x dalších xxxx xxxxxxxxx xxxxxxx xxxxx xxxxx ARR;] (2) xxxx [xxxx xxxxxxx xxxxxxx, x nichž xxxx xxxxxxxx xxxxxxxx potvrzena, xxxxxxxx a xxxxxxxxxxxx x xx xxxxxxxxxxxx xx alespoň po xxx roky xx xxxxxxxxx xxxxxxxxxx xxxxxxx xxxxxxxx klusavky xxxxxxxx xxxxxxxxxxxxx sledování XXX, xxxxxx xxxxxxxxx xxxxx xxxxxxxxxxxxx zvířat xxxxxxxx 18 měsíců, s xxxxxxxx ovcí xxxxxxxx XXX/XXX, xx přítomnost XXX x negativním xxxxxxxxx x xxxxxxx x laboratorními metodami xxxxxxxxxxx x xxxxxxx X kapitole X xxxx 3.2 xxxxxxxx (XX) č. 999/2001: — xxxxxxx, xxxxx xxxx xxxxxxxx k lidské xxxxxxxx, a — xxxxxxx, xxxxx xxxxxxx xxxx xxxx usmrcena v xxxxx xxxxxxxxxxxx, xxxxx xxxxxx usmrcena x xxxxx kampaně eradikace xxxxxx.]] Xxxxxxxx Xxxx X: — Kolonka X.6.: Osoba zodpovědná xx xxxxxxx x Xxxxxxxx unii: xxxx xxxxxxx xx xxxxx xxxxxxx xxxxx xxxxx, xxxxx-xx xx x xxxxxxxxx xxx xxxxx xxxxxx pro xxxxxxx xxxx Evropskou xxxx; xxxx xx vyplnit, xxxxx-xx xx x xxxxxxxxx xxx xxxxx xxxxxxxx do Xxxxxxxx xxxx. — Xxxxxxx I.12.: Xxxxx určení: tuto xxxxxxx xx xxxxx xxxxxxx xxxxx tehdy, xxxxx-xx xx x xxxxxxxxx pro xxxxx xxxxxx xxx tranzit. Xxxxxxxx xxx být xxx tranzitu xxxxxxxxxx xxxxx xx xxxxxxxxxx xxxxxxx, xxxxxxxxxx xxxxxxxx x xxxxxxx xxxxxxxx; — Xxxxxxx X.15.: Registrační xxxxx (xxxxxxxxxxxx xxxxxx xxxx xxxxxxxxxx x xxxxxxxxxx xxxxxxxxxx), xxxxx xxxx (xxxxxxx) nebo xxxxx (plavidla); xxxxxxxxx xx xxxxx poskytnout x xxxxxxx xxxxxxxx x xxxxxxxxxx xxxxxxxx x Xxxxxxxx unii. — Xxxxxxx X.19.: Použijte xxxxxxxxx xxx XX: 04.05, 15.01, 15.02, 15.03, 15.04, 15.05, 15.06, 15.16.10 xxxx 15.18. — Kolonka I.23.: X xxxxxxx xxxxxxxxxx xxx xxxxx ložené xxxxx xxxx xxx xxxxxxx xxxxx kontejneru x (xxxxxxxx) číslo xxxxxx. — Xxxxxxx I.25.: Xxxxxxxxx xxxxxxx: jakékoli xxxx využití xxxxx xxxxxx hospodářských xxxxxx xxxxxx než xxxxxxxxxxxx xxxxxx nebo xxxxxx x zájmovém xxxxx x xxxxxx xxxx xxxxxxxxxx xxxxx xxx xxxxxxx v xxxxxxxx xxxxx. — Xxxxxxx X.26. x I.27.: Vyplňte xxxxx toho, xxxxx-xx xx o xxxxxxxxx xxx xxxxxxx xxxx xxx xxxxx. — Xxxxxxx X.28.: — Xxxx: xxxxxxx: Xxxxxxxxxx, xxxx xxx Xxxxxxxxxx — Výrobní závod: xxxxxxx číslo xxxxxxxxxx xxxxxxxx, v němž xxxxxxxx xxxxxxxx xxxx xxxxxxxxxx. Xxxx XX: (1x) Xx. xxxx. X 300, 14.11.2009, s. 1. (1x) Xx. xxxx. L 54, 26.2.2011, x. 1. (2) Xxxxxxxx se xxxxxxxx. (3) Xx. xxxx. X 139, 30.4.2004, x. 55.  Text obrazu Text obrazu
XXXX Xxxxxx/xxxxxxxx xxxx, které nejsou xxxxxx x xxxxxx xxxxxxxx, k použití xxxx xxxxx xxxxxxxx XX. Xxxxxxxxx xxxxxxxxx XX.x. Xxxxx xxxxxxx osvědčení II.b. (4) Xx. xxxx. X 147, 31.5.2001, s. 1. (5) Xx. xxxx. X 172, 30.6.2007, x. 84. — Xxxxx xxxxxxx x xxxxxxx xx xxxx xxxxx xx xxxxx xxxxx. — Poznámka xxx xxxxx xxxxxxxxxxx xx zásilku x Xxxxxxxx xxxx: xxxx xxxxxxxxx xxxxxx xxxxx x xxxxxxxxxxxx xxxxxx x musí xxxxxxx xxxxxxxx xx xx xxxxxxxx, xxx dosáhne xxxxxxxxxx xxxxxxxx xxxxxxxx Xxxxxxxx unie. Úřední xxxxxxxxxxx xxxxx / úřední xxxxxxxxx Xxxxx (hůlkovým písmem): Xxxxxxxxxxx x xxxxx: Xxxxx: Xxxxxx: Xxxxxxx: XXXXXXXX 10 (B) Veterinární xxxxxxxxx xxx xxxxxx/xxxxxxxx xxxx, xxxxx xxxxxx určeny x xxxxxx xxxxxxxx, xxx xxxxxx použití xxxx xxxxxxxx xxxxxxx, xxxxxx x odeslání xx Xxxxxxxx xxxx xxxx x xxxxxxxx xxxx její území (2) &xxxx; Text obrazu Text obrazu
XXXX: Xxxxxxxxxxx osvědčení xx EU Část I: Xxxxxxxxxxx o xxxxxxxx xxxxxxx X.1. Xxxxxxxxxx Xxxxx Xxxxxx Xxx. X.2. Xxxxx xxxxxxx xxxxxxxxx X.2.x. X.3. Xxxxxxxxx xxxxxxxx orgán I.4. Xxxxxxxxx xxxxxx orgán I.5. Xxxxxxxx Xxxxx Xxxxxx XXX Xxx. X.6. Xxxxx xxxxxxxxxx xx xxxxxxx x XX Xxxxx Xxxxxx XXX Xxx. X.7. Xxxx xxxxxx Xxx XXX X.8. Xxxxxx xxxxxx Xxx X.9. Xxxx xxxxxx Xxx XXX X.10. Xxxxxx xxxxxx Xxx X.11. Xxxxx xxxxxx Xxxxx Xxxxx xxxxxxxxx Xxxxxx Xxxxx Xxxxx xxxxxxxxx Xxxxxx Xxxxx Xxxxx schválení Adresa I.12. Xxxxx xxxxxx Xxxxx xxxxx Xxxxx Xxxxx xxxxxxxxx Xxxxxx XXX X.13. Xxxxx xxxxxxxx X.14. Datum xxxxxxx X.15. Xxxxxxxx xxxxxxxxxx Xxxxxxx Plavidlo Xxxxx Xxxxxxxx xxxxxxx Xxxxxxx Xxxxxxxxxxxx Xxxxx xx xxxxxxxx X.16. Xxxxxxx xxxxxxxxxx xxxxxxxx kontroly XX X.17. X.18. Xxxxx xxxxx X.19. Xxx xxxxx (xxx XX) X.20. Xxxxxxxx X.21. Teplota xxxxxxxx Xxxxxx Chlazené Xxxxxxxx X.22. Xxxxx xxxxxx X.23. Xxxxx xxxxxx/xxxxxxxxxx X.24. Xxxx obalu  Text obrazu Text obrazu
X.25. Zboží xxxxxxxxx xxx: Xxxxxxxxx xxxxxxx X.26. Pro xxxxxxx xxxx XX xx xxxxx xxxx Xxxxx xxxx Xxx XXX X.27. Xxx dovoz nebo xxxxxx do XX X.28. Xxxxxxxxxxxx xxxxx Xxxxx xxxxxxxxx xxxxxxxx Xxxx(xxxxxxx xxxxx) Xxxxxxx xxxxx Xxxxx xxxxxx Xxxxx xxxxxxxx Xxxxx šarže  Text obrazu Text obrazu
XXXX Xxxxxx/xxxxxxxx xxxx, xxxxx xxxxxx určeny x xxxxxx xxxxxxxx, xxx xxxxxx xxxxxxx xxxx xxxxxxxx xxxxxxx XX. Xxxxxxxxx xxxxxxxxx XX.x. Xxxxx jednací xxxxxxxxx XX.x. Xx, xxxx xxxxxxxxx xxxxxx veterinární lékař, xxxxxxxxxx, xx xxxx xxxxxxx x xxxxxxxxx xxxxxxxx Evropského xxxxxxxxxx x Rady (ES) x. 1069/2009 (1x), xxxxxxx xxxxx xxx x články 8, 9 a 10 xxxxxxxxx xxxxxxxx, a xxxxxxxx Komise (XX) x. 142/2011 (1x), xxxxxxx xxxxx xxx x xxxxxxx XXX xxxxxxxx XX uvedeného xxxxxxxx, x xxxxxxxxx, xx xxxx xxxxxxx xxxxxx/xxxxxxxx tuky: II.1. xxxxxxxxx x xxxxxxxx/xxxxxxxxxx xxxx, xxxxx xxxxxx xxxxxx x xxxxxx xxxxxxxx x xxxxx xxxxxxx xxxx xxxxxxx xxxxxxxxxxx xxxxxxxxx; XX.2. xxxx připraveny xxxxxxxx x xxxxxx xxxxxxxxxx xxxxxxxx živočišného xxxxxx: (2) [XX.2.1. x xxxxxxx xxxxxxxxx určených x xxxxxx obnovitelných xxxxx xxxxxxxxx x xxxxxxx IV xxxxxxxx XX oddílu 2 xxxx L nařízení (XX) x. 142/2011, xxxxxxxx xxxx tukových xxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx xxxxxxx x článcích 8, 9 x 10 xxxxxxxx (XX) č. 1069/2009;] (2) [XX.2.2. x xxxxxxx xxxxxxxxx xxxxxxxx x xxxxxx xxxxxxxxxxxxx xxxxx xxxxxxxxx x xxxxxxx IV kapitole XX oddílu 2 xxxx X xxxxxxxx (XX) x. 142/2011 xxxx materiály xxxxxxxxxx xxxxxxxx x xxxxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx xxxxxxxxx x článcích 9 a 10 xxxxxxxx (ES) č. 1069/2009;] (2) [II.2.3. v xxxxxxx xxxxxxxxx určených x xxxxx xxxxxx, xxx jsou xxxxxxxxxx xxxxxxxxx, xxxxxx xxxxxxxxx xxxx zdravotnické prostředky, xxxx xxxxxxxxx xxxxxxxxxx xxxxxxxx x xxxxxx xxxxxxxxx: (2) buď [- xxxxxxxx xxxxxxxx živočišného xxxxxx, xxxxx obsahují xxxxxxx xxxxxxxxxx xxxxx xxxx xxxxxxxxxxxx, xxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxx podle xx. 15 odst. 3 xxxxxxxx Xxxx 96/23/XX (2x);] (2) x/xxxx [- xxxxxxxx xxxxxxxxxxx xxxxxx, xxxxx xxxx x xxxxxx xxxxxxx xxxxxx xxxxx x xxxxxx xxxxxxxxxx xxxxxxxxxx xx xxxxxxxx k xxxxxx xxxxxxxx;] (2) x/xxxx [- xxxxxxx a xxxxxx xxxxx, xxxxx xxxxxx x jejich xxxxx xxxxxxxxx v xxxxxxxx 8 a 10 xxxxxxxx (XX) x. 1069/2009, která uhynula xxxxx než xxxxxxxx xxxx xxxxxxxxx x xxxxxx xxxxxxxx, xxxxxx xxxxxx usmrcených xx xxxxxx xxxxxxx xxxxxx;] (2) x/xxxx [- xxxxxxx xxxxxxxx xxxx xxxxxxxxxx xxxxxx x xxxxxx xxxxx, xxxx x xxxxxxx xxxxx xxxx xxxxxxxxxx zvířat xxxx xxxxxx xxxxx, xxxxx xxxx x xxxxxxx x právními xxxxxxxx Xxxx xxxxxx k xxxxxx xxxxxxxx, xxxxx x xxxxxxxxxx xxxxxx xxxxxx x xxxxxx xxxxxxxx xxxxxx;] (2) x/xxxx [- jatečně xxxxxxxx xxxx x xxxx xxxxxxx xxxxx xxxxxxxxxxx xxx xx zvířat, xxxxx xxxx xxxxxxxx xx xxxxxxx a xx prohlídce před xxxxxxxx xxxx xxxxxxxx xxxx xxxxxxxxx x xxxxxxx x lidské xxxxxxxx, xxxx těla x níže xxxxxxx xxxxx xxxxx xxxxxxxx x lidské spotřebě x xxxxxxx x xxxxxxxx xxxxxxxx Xxxx: x) xxxxxxx upravená xxxx xxxx těla xxxxxx x xxxxxx xxxxx, xxxxx byla x xxxxxxx s právními xxxxxxxx Xxxx xxxxxxxxxx xx nevhodná k xxxxxx spotřebě, avšak xxxxxxxxxxxx žádné xxxxxxxx xxxxxxxxxx xxxxxxxxxx na xxxxxxx nebo zvířata; ii) xxxxx xxxxxxx; xxx) xxxx x xxxxx, xxxxxx xxxxxx xxxxxxx x xxxxxx, xxxx a xxxxxxxxx, xxxxxx článků xxxxx, xxxxxxxxxx a xxxxxxxxxx xxxxxx, xxxxx x xxxxxxx; xx) xxxxxxx xxxxxxx; x) peří;] (2) a/nebo [- xxxx zvířat, xxxxx xxxxxxxxxxxx xxxxx xxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxx na xxxxxxx xxxx zvířata, která xxxx xxxxxxxx xx xxxxxxx x xxxxx xxxx po prohlídce xxxx porážkou xxxxxxxx xxxxxxxxxxx x xxxxxxx x xxxxxx xxxxxxxx x souladu x xxxxxxxx xxxxxxxx Xxxx;] (2) x/xxxx [- vedlejší xxxxxxxx živočišného původu, xxxxx xxxxxxxx xxx xxxxxx xxxxxxxx určených x xxxxxx xxxxxxxx, xxxxxx odtučněných xxxxx, xxxxxxx xxxx xxxx x xxxxxxxxxxx xxxx xxxxxxxxxx xx xxxxxxxxxx xxxxx;] Xxxx II: Xxxxxxxxx  Text obrazu Text obrazu
XXXX Xxxxxx/xxxxxxxx xxxx, xxxxx xxxxxx určeny x xxxxxx xxxxxxxx, xxx xxxxxx xxxxxxx mimo xxxxxxxx řetězec II. Xxxxxxxxx xxxxxxxxx XX.x. Xxxxx jednací xxxxxxxxx XX.x. (2) x/xxxx [- xxxxxxxx xxxxxxxxxxx původu xxxx potraviny xxxxxxxxxx xxxxxxxx živočišného xxxxxx, xxxxx x xxxxxxxxxx xxxxxx xxxx x xxxxxx xxxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxx, vadami xxxxxx xxxx xxxxxx xxxxxxxx, x nichž xxxxxxxx xxxxx riziko xxx xxxxxx xxxx xxx zvířat, již xxxxxx xxxxxx x xxxxxx xxxxxxxx;] (2) a/nebo [- krmivo xxx xxxxxxx v xxxxxxxx xxxxx x xxxxxx xxxxxxxxxxx xxxxxx xxxx xxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx xx získané xxxxxxxx, xxxxx x obchodních xxxxxx xxxx x xxxxxx problémů xxxxxxxxxxx xxxxxxxxx xxxxxx, xxxxxx xxxxxx nebo xxxxxx xxxxxxxx, z xxxxx xxxxxxxx žádné xxxxxx xxx xxxxxx xxxx xxx zvířat, xxx xxxxxx xxxxxx xx xxxxxx;] (2) a/nebo [- xxxx, placenta, vlna, xxxx, srst, rohy, xxxxxxx xxxxx a xxxxxxxx x xxxxxx xxxxx xxxxxxxxxxx xx xxxxxx xxxxxx, xxxxx xxxxxxxxxxxx xxxxx příznaky xxxxxxxxxx xxxxxxxxxx xxxxx xxxxxxxxx xx člověka xxxx xxxxxxx;] (2) a/nebo [- vodní xxxxxxxxxxx x jejich xxxxx, xxxxx xxxxxxxx savců, xxxxx xxxxxxxxxxxx xxxxx xxxxxxxx onemocnění xxxxxxxxxx xx xxxxxxx xxxx xxxxxxx;] (2) x/xxxx [- xxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx z vodních xxxxxxxxx xxxxxxxxxxx x xxxxxxx xxxx zařízení xx xxxxxx produktů xxxxxxxx k lidské xxxxxxxx;] (2) a/nebo [- xxxx xxxxxxx xxxxxxxx xxxxxxxxxxx xx xxxxxx, xxxxx nevykazovala žádné xxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxx xxxxxxxxxx na xxxxxxx nebo xxxxxxx: x) xxxxx měkkýšů a xxxxxx x xxxxxxx xxxxxxx nebo masem; ii) xxxxx xxxxxxxx pocházející xx xxxxxxxxxxxxx xxxxxx: — xxxxxxxx produkty x xxxxx, — vejce, — vedlejší xxxxxxxx z xxxxx, xxxxxx xxxxxxxxx skořápek; iii) xxxxxxxxxx kuřata xxxxxxxx x xxxxxxxxxx xxxxxx;] (2) x/xxxx [- vodní x suchozemští bezobratlí xxxxxxxxxxx, kromě druhů xxxxxxxxxxx xxx xxxxxxx xxxx zvířata;] (2) x/xxxx [- zvířata x xxxx hlodavců (Xxxxxxxx) x zajícovců (Xxxxxxxxxx) x xxxxxx xxxxx, xxxxx xxxxxxxxx xxxxxxxxx 1 xxxxxxxxx x xx. 8 písm. x) bodech iii), xx) x v) xxxxxxxx (XX) č. 1069/2009 x xxxxxxxxx xxxxxxxxx 2 xxxxxxxxx x xx. 9 xxxx. x) až x) uvedeného xxxxxxxx;] (2) x/xxxx [- xxxx x xxxxx, kopyta x paznehty, xxxx, xxxx, rohy, xxxx x kožešina xxxxxxxxxxx x xxxxxxx xxxxxx, xxxxx xxxxxxxxxxxx žádné xxxxxxxx onemocnění xxxxxxxxxx xxxxx produktem xx xxxxxxx xxxx xxxxxxx;] (2) x/xxxx [- xxxxxx xxxx xxxxxxxxxxx xx xxxxxx, xxxxx nevykazovala xxxxx xxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxx xxxxxxxxxx xx člověka xxxx xxxxxxx, která xxxx xxxxxxxx na jatkách x xxxxx byla xx xxxxxxxxx xxxx xxxxxxxx xxxxxxxx xxxxxxxx xxx účely xxxxxxx x xxxxxx xxxxxxxx x xxxxxxx x xxxxxxxx xxxxxxxx Unie;]] (2) [XX.2.4. x xxxxxxx xxxxxxxxx xxxxxxxx x xxxxx xxxxxx xxx x výrobě organických xxxxxx xxxx xxxxxxxxx xxxxxxx látek, xxxxxxxxxxxx xxxxxxxxx, léčivých xxxxxxxxx xxxx zdravotnických xxxxxxxxxx: (2) xxx [- xxxxxxxxxxxxx xxxxxxxx xxxxxxxx podle xxxxxxxx x xx. 3 odst. 1 xxxx. x) xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Xxxx (ES) x. 999/2001 (2b),] (2) x/xxxx [- xxxx těla xxxx xxxxx těl xxxxxxx zvířat obsahující xxx xxxxxxxxx xxxxxxxxxx xxxxxxxxxxxxx xxxxxxxx materiál xxxxx xxxxxxxx x xx. 3 xxxx. 1 xxxx. x) xxxxxxxx (XX) x. 999/2001,] (2) x/xxxx [- xxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx xxxxxxx xx xxxxxx, xxxxx xxxx xxxxxxxxx nezákonnému ošetření xxxxx definice v xx. 1 xxxx. 2 xxxx. x) xxxxxxxx Xxxx 96/22/XX (2x) nebo x xx. 2 xxxx. x) xxxxxxxx 96/23/XX;]  Text obrazu Text obrazu
XXXX Xxxxxx/xxxxxxxx tuky, xxxxx xxxxxx xxxxxx k xxxxxx xxxxxxxx, xxx xxxxxx xxxxxxx xxxx xxxxxxxx řetězec II. Xxxxxxxxx xxxxxxxxx XX.x. Xxxxx jednací xxxxxxxxx XX.x. (2) x/xxxx [- xxxxxxxx produkty xxxxxxxxxxx xxxxxx, xxxxx xxxxxxxx xxxxxxx xxxxxxx látek x xxxxxxxxxxxx z xxxxxxxx xxxxxxxxx uvedených xx xxxxxxx B (3) x xxxxxxx X xxxxxxxx 96/23/ES, xxxxx xxxxxxxx těchto xxxxxxx xxxxxxxxx xxxxxxxxx xxxxxx xxxxxxxxx xxxxxxxx xxxxxxxx Xxxx, nebo xxxxxx-xx x těchto xxxxxxxxxx xxxxxxxxx, xxxxxxxx xxxxxxxx xxxxxxxxx xxxxx xxxxxx;] XX.3. xxxxxx/xxxxxxxx tuky: a) xxxx podrobeny xxxxxxxxxx x xxxxxxx x xxxxxxx (xxxxxx xxxxxxxxxxxxxxx xxxxxx), xxx xx xxxxxxxxx x příloze XX kapitole XXX xxxxxxxx (XX) č. 142/2011 za xxxxxx xxxxxxx patogenních původců; b) xxxx před xxxxxxxx xx Evropské unie xxxxxxxx xxxxxxxxxxxxxxxxxxxxxx (XXX) xxx, xxx bylo xxxxxxxx homogenní xxxxxxxxx xxxxxxxxxxx xxxxxxx 250 xx XXX na xxxxx kilogram xxxx; x) x případě xxxxxxxx/xxxxxxxxxx xxxx x xxxxxxxxxxx xxxx odstraněny nerozpustné xxxxxxxxx xxxxxxxxxxx 0,15 % xxxxxxxxxxxx; x) xxxx xxxxxxxxxxxx za xxxxxxxx, xxxxx xxxxxxxxx xxxxxx xxxxxxxxxxx, x x) xxxx xx xxxxx xxxx xxxxxx opatřeny etiketami x xxxxxxx „NENÍ XXXXXX K LIDSKÉ XXXXXXXX XXX XX XXXXXX ZVÍŘAT“; (2) [II.4. x xxxxxxx xxxxxxxxx xxxxxxxx xxx xxxxxxxxx xxxxxxx, xxxxxxxxxx xxxxxxxxx, xxxxxx xxxxxxxxx, zdravotnické xxxxxxxxxx xxxx xxxxxxx xxxxx xxxxx xxxx xxxxxxx xxxxxx/xxxxxxxx xxxx (2) xxx [xxxx xxxxxxx x xxxxxxxxxxx xxxxxx xxx xxxx, xxxx xxxx xxxx.] (2) nebo [xxxx získány xx xxxxx, xxxx nebo xxx x neobsahují xxxx xxxxxxx složky xxx x xxxx xxxxxx xxxxxxx: (2) xxx [xxxxxxxx xxxxxxxxxxx ze xxxxx, xxxx x xxx jiných xxx xxxxxxxxxx, xxxxxxxxxxx xxxxxxxxx x xxxxxxxxxx x xxxx xxxx xxxxxxx xxxxxxxx v souladu x rozhodnutím 2007/453/XX xx xxxxxxxxx xxxx xxxx xxxxxxx se xxxxxxxxxxxxx xxxxxxx xxxxxxx XXX.] (2) nebo [x) xxxxxxxxxxxxx rizikový xxxxxxxx, xxx xx xxxxxxxxx x xxxx 1 xxxxxxx X xxxxxxxx Xxxxxxxxxx parlamentu x Xxxx (XX) x. 999/2001 (3); b) xxxxxxx xxxxxxxx maso získané x xxxxx xxxxx, xxxx xxxx koz x xxxxxxxx zvířat xxxxxxxxxx, xxxxxxxxxxx xxxxxxxxx x poražených x xxxx xxxx xxxxxxx xxxxxxxx v souladu x xxxxxxxxxxx Xxxxxx 2007/453/XX (4) do xxxxxxxxx xxxx nebo xxxxxxx se zanedbatelným xxxxxxx xxxxxxx BSE, x nichž xxxxx xxxxxxx žádný xxxxxx xxxxxx XXX; x) xxxxxxxx xxxxxxx xxxxxxxxxxx xxxxxx xxxx xxxxxxx xxxxxxx xx skotu, xxxx xxxx koz, které xxxx xx omráčení xxxxxxxx xxxxxxxx centrální xxxxxxx tkáně pomocí xxxxxxxxxxx tyčovitého xxxxxxxx xxxxxxxxxx xx xxxxxx xxxxxxx xxxx prostřednictvím xxxxxxx xxxxxxx xx xxxxxx lebeční, s xxxxxxxx xxxxxx xxxxxxxxxx, xxxxxxxxxxx xxxxxxxxx x xxxxxxxxxx x xxxx xxxx xxxxxxx xxxxxxxx x souladu s xxxxxxxxxxx 2007/453/XX do xxxxxxxxx xxxx nebo xxxxxxx xx xxxxxxxxxxxxx xxxxxxx xxxxxxx XXX.]]] Xxxxxxxx Xxxx X: — Xxxxxxx I.6.: Xxxxx xxxxxxxxxx xx xxxxxxx v Xxxxxxxx xxxx: xxxx xxxxxxx xx xxxxx vyplnit xxxxx xxxxx, jedná-li xx o osvědčení xxx zboží xxxxxx xxx xxxxxxx xxxx Xxxxxxxxx xxxx; xxxx xx xxxxxxx, xxxxx-xx xx o xxxxxxxxx xxx xxxxx xxxxxxxx xx Xxxxxxxx unie. — Xxxxxxx I.11. x X.12.: Xxxxx xxxxxxxxx: xxxxx xxxxxxxxxx xxxxxxxx xxxx xxxxxxx, xxxxx xxxx vydáno xxxxxxxxxx xxxxxxx.  Text obrazu Text obrazu
XXXX Xxxxxx/xxxxxxxx xxxx, xxxxx xxxxxx xxxxxx x lidské xxxxxxxx, xxx určitá xxxxxxx xxxx xxxxxxxx xxxxxxx XX. Xxxxxxxxx informace II.a. Číslo xxxxxxx xxxxxxxxx XX.x. — Xxxxxxx X.12.: Xxxxx xxxxxx: xxxx xxxxxxx xx xxxxx vyplnit xxxxx xxxxx, jedná-li xx x xxxxxxxxx xxx xxxxx určené xxx xxxxxxx. Xxxxxxxx xxx xxx při xxxxxxxx xxxxxxxxxx xxxxx xx xxxxxxxxxx pásmech, svobodných xxxxxxxx x celních xxxxxxxx; — Xxxxxxx X.15.: Xx xxxxx xxxxx xxxxxxxxxxx xxxxx (xxxxxx xxxx kontejnery x xxxxxxxx automobily), číslo xxxx (letadlo) nebo xxxxx (xxxxxxxx). V xxxxxxx vykládky a xxxxxxxxxx xxxxxxxx v Xxxxxxxx xxxx musí xxxxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxx v xxxxx vstupu xx Xxxxxxxx xxxx. — Xxxxxxx X.19.: Použijte xxxxxxxxx xxx xxxxxxxxxxxxxxx xxxxxxx (XX) xxxxxxxxxxxxx xxxxx: 04.05, 15.01, 15.02, 15.03, 15.04, 15.05, 15.06, 15.16 nebo 15.18. — Kolonka X.23.: X xxxxxxx kontejnerů xxx xxxxx xxxxxx xxxxx xxxx být xxxxxxx číslo xxxxxxxxxx x (případně) xxxxx xxxxxx. — Kolonka X.25.: Xxxxxxxxx xxxxxxx: xxxxxxxx xxxx xxxxxxx xxxxx xxxxxx hospodářských xxxxxx xxxxxx xxx xxxxxxxxxxxx xxxxxx xxxx zvířat x zájmovém xxxxx x xxxxxx nebo xxxxxxxxxx xxxxx xxx xxxxxxx x xxxxxxxx xxxxx. — Kolonky X.26. x X.27.: Xxxxxxx xxxxx xxxx, xxxxx-xx xx x xxxxxxxxx xxx xxxxxxx xxxx xxx xxxxx. — Xxxxxxx X.28.: Xxxx: xxxxxxx: Xxxxxxxxxx, xxxx než Xxxxxxxxxx Xxxxxxx xxxxx: xxxxxxx číslo xxxxxxxxxx xxxxxxxx, x xxxx xxxxxxxx xxxxxxxx xxxx zpracování. Část XX: (1x) Xx. xxxx. L 300, 14.11.2009, x. 1. (1x) Úř. xxxx. X 54, 26.2.2011, x. 1. (2) Xxxxxxxx xx škrtněte. (2a) Xx. xxxx. X 125, 23.5.1996, x. 10. (2x) Xx. xxxx. X 147, 31.5.2001, x. 1. (2x) Xx. xxxx. X 125, 23.5.1996, x. 3. (3) Xx. xxxx. L 147, 31.5.2001, x. 1. (4) Xx. věst. L 172, 30.6.2007, x. 84. — Xxxxx podpisu x razítka se xxxx xxxxx xx xxxxx xxxxx. — Poznámka xxx osobu zodpovědnou xx xxxxxxx v Xxxxxxxx unii: xxxx xxxxxxxxx xxxxxx pouze x xxxxxxxxxxxx účelům x xxxx zásilku xxxxxxxx až xx xxxxxxxx, xxx xxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxx x místě xxxxxx xx Xxxxxxxx xxxx. Xxxxxx xxxxxxxxxxx xxxxx / xxxxxx xxxxxxxxx Xxxxx (hůlkovým xxxxxx): Xxxxxxxxxxx x xxxxx: Xxxxx: Xxxxxx: Xxxxxxx: XXXXXXXX 11 Xxxxxxxxxxx xxxxxxxxx xxx želatinu x xxxxxxx, xxxxx xxxxxx xxxxxx x lidské xxxxxxxx, x xxxxxxx xxxx xxxxx xxxxxxxx xxxx xxxx xxxxxxxx xxxxxxx, xxxxxx x xxxxxxxx xx Evropské xxxx xxxx x xxxxxxxx xxxx její xxxxx (2) &xxxx; Text obrazu Text obrazu
ZEMĚ: Veterinární xxxxxxxxx xx EU Část X: Xxxxxxxxxxx x xxxxxxxx zásilce I.1. Xxxxxxxxxx Xxxxx Xxxxxx Xxx. X.2. Xxxxx xxxxxxx osvědčení I.2.a. I.3. Xxxxxxxxx ústřední xxxxx X.4. Xxxxxxxxx místní orgán I.5. Xxxxxxxx Xxxxx Xxxxxx XXX Xxx. X.6. Osoba xxxxxxxxxx xx xxxxxxx x XX Xxxxx Xxxxxx XXX Xxx. X.7. Xxxx původu Kód XXX X.8. Xxxxxx xxxxxx Xxx X.9. Xxxx určení Kód ISO I.10. Xxxxxx xxxxxx Xxx X.11. Xxxxx xxxxxx Xxxxx Xxxxx xxxxxxxxx Xxxxxx Xxxxx Xxxxx xxxxxxxxx Xxxxxx Xxxxx Číslo xxxxxxxxx Xxxxxx X.12. Xxxxx určení Celní xxxxx Xxxxx Xxxxx xxxxxxxxx Xxxxxx XXX X.13. Xxxxx nakládky I.14. Xxxxx xxxxxxx X.15. Xxxxxxxx prostředek Letadlo Xxxxxxxx Xxxxx Xxxxxxxx xxxxxxx Xxxxxxx Xxxxxxxxxxxx Xxxxx xx xxxxxxxx X.16. Xxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxx EU I.17. I.18. Xxxxx xxxxx X.19. Xxx zboží (xxx HS) I.20. Xxxxxxxx X.21. Xxxxxxx xxxxxxxx Xxxxxx Chlazené Xxxxxxxx X.22. Počet balení I.23. Xxxxx plomby/kontejneru I.24. Druh xxxxx  Text obrazu Text obrazu
X.25. Xxxxx xxxxxxxxx xxx: Xxxxxx Výroba xxxxxx pro xxxxxxx x zájmovém xxxxx Xxxxxxxxx využití I.26. Xxx xxxxxxx přes EU xx xxxxx xxxx Xxxxx xxxx Xxx XXX X.27. Xxx xxxxx xxxx xxxxxx xx XX X.28. Xxxxxxxxxxxx xxxxx Xxxxx xxxxxxxxx xxxxxxxx Xxxx (vědecký xxxxx) Xxxxxxx xxxxx Xxxxx balení Čistá xxxxxxxx Xxxxx xxxxx  Text obrazu Text obrazu
XXXX Xxxxxxxx x xxxxxxx, které xxxxxx xxxxxx x xxxxxx xxxxxxxx, x xxxxxxx xxxx xxxxx surovina xxxx mimo xxxxxxxx xxxxxxx XX. Zdravotní xxxxxxxxx XX.x. Xxxxx xxxxxxx xxxxxxxxx XX.x. Xx, xxxx xxxxxxxxx xxxxxx xxxxxxxxxxx lékař, xxxxxxxxxx, xx jsem přečetl x porozuměl nařízení Xxxxxxxxxx xxxxxxxxxx x Xxxx (ES) x. 1069/2009 (1a), xxxxxxx xxxxx jde x xxxxxx 10 xxxxxxxxx xxxxxxxx, x xxxxxxxx Xxxxxx (XX) č. 142/2011 (1x), zejména xxxxx xxx x xxxxxxx XXX xxxxxxxx X uvedeného nařízení, x xxxxxxxxx, xx xxxx xxxxxxx xxxxxxxx / xxxx xxxxxxx xxxxxxx (2): XX.1. xxxxxxx x xxxxxxxx/xxxxxxxx (2), xxxxx xxxxxxx xxxx xxxxxxx veterinární xxxxxxxxx; XX.2. xxxxxxx výhradně z xxxxxxxx/xxxxxxxx (2), xxxxx xxxxxx xxxxxx k xxxxxx spotřebě; II.3. xxx(x) xxxxxxxxx(x) x xxxxxxxxx(x) x podniku schváleném x xxxxxxxxxxx příslušným xxxxxxx v xxxxxxx x xxxxxxx 24 xxxxxxxx (XX) x. 1069/2009 xx účelem xxxxxxx patogenních xxxxxxx; XX.4. xxx(x) xxxxxxxxx(x) výhradně x těchto xxxxxxxxxx xxxxxxxx živočišného původu: (2) xxx [- xxxx xxxxxxxxxx zvířat a xxxxxx části, nebo x xxxxxxx xxxxx xxxx xxxxxxxxxx xxxxxx xxxx xxxxxx xxxxx, xxxxx xxxx podle xxxxxxxx předpisů Xxxx xxxxxx x lidské xxxxxxxx, xxxxx x xxxxxxxxxx xxxxxx xxxxxx x xxxxxx xxxxxxxx xxxxxx;] (2) x/xxxx [- xxxxxxx xxxxxxxx xxxx x xxxx xxxxxxx xxxxx xxxxxxxxxxx xxx xx xxxxxx, xxxxx xxxx poražena xx xxxxxxx x xx xxxxxxxxx xxxx xxxxxxxx xxxx shledána jako xxxxxxxxx x xxxxxxx x xxxxxx xxxxxxxx, xxxx xxxx a xxxx xxxxxxx xxxxx xxxxx usmrcené k xxxxxx xxxxxxxx x xxxxxxx x xxxxxxxx xxxxxxxx Xxxx: x) xxxxxxx xxxxxxxx těla xxxx xxxx zvířat x xxxxxx xxxxx, xxxxx xxxx x xxxxxxx x xxxxxxxx předpisy Xxxx xxxxxxxxxx za xxxxxxxx x lidské xxxxxxxx, xxxxx xxxxxxxxxxxx xxxxx xxxxxxxx xxxxxxxxxx xxxxxxxxxx xx xxxxxxx xxxx xxxxxxx; xx) xxxxx xxxxxxx; xxx) xxxx a xxxxx, xxxxxx jejich xxxxxxx x xxxxxx, xxxx x končetiny, xxxxxx xxxxxx xxxxx, xxxxxxxxxx a záprstních xxxxxx, xxxxx a xxxxxxx; xx) xxxxxxx štětiny; v) xxxx;] (2) x/xxxx [- xxxxxxxx xxxxxxxx živočišného xxxxxx, xxxxx vznikají xxx xxxxxx xxxxxxxx xxxxxxxx x xxxxxx xxxxxxxx, xxxxxx xxxxxxxxxxx xxxxx, xxxxxxx nebo xxxx z xxxxxxxxxxx xxxx xxxxxxxxxx xx xxxxxxxxxx xxxxx;] (2) x/xxxx [- xxxxxxxx xxxxxxxxxxx xxxxxx xxxx potraviny xxxxxxxxxx xxxxxxxx živočišného xxxxxx, xxxxx z xxxxxxxxxx důvodů xxxx x důvodů problémů xxxxxxxxxxx xxxxxxxxx vadami, xxxxxx xxxxxx nebo xxxxxx závadami, x xxxxx xxxxxxxx žádné xxxxxx pro xxxxxx xxxx ani xxxxxx, xxx xxxxxx xxxxxx x xxxxxx spotřebě;] (2) x/xxxx [- xxxxxx xxx zvířata x xxxxxxxx xxxxx x xxxxxx xxxxxxxxxxx xxxxxx xxxx xxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx xx xxxxxxx xxxxxxxx, xxxxx x xxxxxxxxxx důvodů xxxx x xxxxxx problémů xxxxxxxxxxx xxxxxxxxx vadami, xxxxxx balení xxxx xxxxxx xxxxxxxx, z xxxxx nevzniká xxxxx xxxxxx xxx zdraví xxxx xxx xxxxxx, xxx xxxxxx xxxxxx xx krmení;] (2) x/xxxx [- xxxxx xxxxxxxxxxx x jejich části, xxxxx mořských xxxxx, xxxxx xxxxxxxxxxxx žádné xxxxxxxx onemocnění xxxxxxxxxx xx člověka xxxx xxxxxxx;] (2) x/xxxx [- xxxxxxxx xxxxxxxx živočišného xxxxxx x xxxxxxx xxxxxxxxx xxxxxxxxxxx x xxxxxxx xxxx zařízení xx xxxxxx xxxxxxxx xxxxxxxx x xxxxxx xxxxxxxx;] XX.5. želatina/kolagen (2): x) xxx(x) xxxxxxx(x), xxxxxx(x) xx xxxxxxx xxxxx, xxxxxxxxx(x) x xxxxxxxxxxx(x) xx xxxxxxxxxxxxxx xxxxxxxxxxxx xxxxxxxx x zejména xxxxxx x xxxxxxxx xx xxxxxxx obalu xxxxxxxx x místnosti xxxxxx k xxxxxx xxxxx x xxxx xxxxxxx pouze konzervační xxxxxxxxxx povolené právními xxxxxxxx Unie. Část XX: Xxxxxxxxx  Text obrazu Text obrazu
XXXX Xxxxxxxx x xxxxxxx, xxxxx xxxxxx xxxxxx x lidské xxxxxxxx, x xxxxxxx xxxx xxxxx xxxxxxxx xxxx mimo xxxxxxxx xxxxxxx XX. Zdravotní xxxxxxxxx XX.x. Xxxxx xxxxxxx xxxxxxxxx XX.x. Xxxxxxxx x xxxxxxxxxx xxxxx xxxxxxxxxx želatinu/kolagen (2) xxxx být xxxxxxxx xxxxxxx „XXXXXXXX/XXXXXXX (2) XXXXXX(X) KE XXXXXX XXXXXX“; x (2) xxx [x) xxxxxxxx byla xxxxxxxx postupem, xxxxx xxxxxxxxx, xx xxxxxxxxxxxx xxxxxxxx kategorie 3 xx xxxxxxxx ošetření xxxxxxxxx xx xxxxxxx xxxxxxxxxxxxx jedním xxxx xxxxxxxxxxx propláchnutím, včetně xxxxxx xX, a xxxxxxxx xxxxxx xxxx xxxxxxxxxxx po sobě xxxxxxxxxxxx xxxxxxxx, xx xxx xxxxxxxxx xxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxxx a xxxxxxxxxxx, aby xxxxx xx zničení xxxxxxxxxxx xxxxxxxxx;] (2) nebo [x) xxxxxxx byl xxxxxxx xxxxxxxx, xxxxx xxxxxxxxx, xx nezpracovaný materiál xxxxxxxxx 3 xx xxxxxxxx xxxxxxxx, které xxxxxxxx xxxxxxx, úpravu xX xxxxxx xxxxxxxx xx xxxxxx s xxxxxxxxx xxxxxx xx xxxxxxxxxxx xxxxxxxxxxxxx, xxxxxxxx x xxxxxxx, xxx xxxxx ke zničení xxxxxxxxxxx xxxxxxxxx;] (2) [XX.6. x xxxxxxx xxxxxxxx/xxxxxxxx (2) x xxxxxx xxxxxxxxx, než xxxx xxxx x xxxxx (2) xxx [jsou xxxxxxx x xxxxxxxxxxx xxxxxx xxx xxxx, xxxx xxxx kozy;]] (2) nebo [xxxx xxxxxxx xx xxxxx, xxxx xxxx xxx a xxxxxxxxxx xxxx uvedené xxxxxx xxx x xxxx xxxxxx xxxxxxx: (2) xxx [xxxxxxxx xxxxxxxxxxx xx xxxxx, xxxx a xxx jiný xxx xxxxxxx xx xxxxxx xxxxxxxxxx, xxxxxxxxxxx chovaných x poražených x xxxx xxxx oblasti xxxxxxxx v souladu x xxxxxxxxxxx 2007/453/XX xx kategorie xxxx xxxx xxxxxxx xx xxxxxxxxxxxxx rizikem xxxxxxx XXX;]] (2) xxxx [a) xxxxxxxxxxxxx xxxxxxxx xxxxxxxx, xxx xx xxxxxxxxx x xxxx 1 xxxxxxx X xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Xxxx (XX) č. 999/2001 (3); b) xxxxxxx xxxxxxxx maso xxxxxxx x xxxxx skotu, xxxx xxxx xxx x xxxxxxxx zvířat xxxxxxxxxx, nepřetržitě chovaných x xxxxxxxxxx v xxxx nebo xxxxxxx xxxxxxxx x xxxxxxx x rozhodnutím Komise 2007/453/XX (4) xx xxxxxxxxx xxxx xxxx xxxxxxx xx xxxxxxxxxxxxx xxxxxxx xxxxxxx XXX, x xxxxx nebyl xxxxxxx xxxxx domácí xxxxxx XXX; x) xxxxxxxx xxxxxxx xxxxxxxxxxx původu xxxx xxxxxxx produkt xx xxxxx, ovcí xxxx koz, xxxxx xxxx xx xxxxxxxx xxxxxxxx lacerací xxxxxxxxx xxxxxxx xxxxx xxxxxx xxxxxxxxxxx tyčovitého xxxxxxxx xxxxxxxxxx xx xxxxxx xxxxxxx nebo xxxxxxxxxxxxxxx xxxxxxx injekce xx xxxxxx xxxxxxx, x xxxxxxxx xxxxxx xxxxxxxxxx, xxxxxxxxxxx xxxxxxxxx a xxxxxxxxxx x xxxx xxxx oblasti xxxxxxxx x xxxxxxx x xxxxxxxxxxx 2007/453/ES xx xxxxxxxxx země xxxx xxxxxxx se xxxxxxxxxxxxx xxxxxxx výskytu XXX;]]] XX.7. x xxxxxxx xxxxxxxx/xxxxxxxx (2) x jiných xxxxxxxxx, xxx xxxx xxxx x kožky, xxxxxxxxx výše: (2) buď [xxxxxxxxxx mléko xxxx xxxxxx xxxxxxx pocházející x xxxx xxxx xxx xxx xxxxxx xxxxxx pro xxxxxx xxxxxxxxxxxxx xxxxxx xxxxxx xxx kožešinových xxxxxx.] (2) xxxx [xxxxxxxx mléko xxxx mléčné xxxxxxx xxxxxxxxxxx x xxxx xxxx xxx x xxxx xxxxxx pro xxxxxx xxxxxxxxxxxxx zvířat xxxxxx xxx xxxxxxxxxxxx xxxxxx a mléko xxxx xxxxxx xxxxxxx: x) xxxx xxxxxxx z xxxx x xxx, xxxxx xxxx nepřetržitě xx narození xxxxxxx x xxxx, x xxx xxxx splněny xxxx xxxxxxxx: x) xxxxxxxx xxxxxxxx xx xxxxxxx xxxxxxxx; xx) xxxxxxx xxxxxx xxxxxx, xxxxxxxxx a xxxxxxx, xxxxx xxx x xxxxxxxxx xxxxxxxx; xxx) xx xxxxxxxxxxxx x xxxxxx xxxx nebo xxx xx uplatňují xxxxxx omezení x xxxxxxx xxxxxxxxx xx XXX xxxx potvrzení xxxxxxxx xxxxxxxx;  Text obrazu Text obrazu
XXXX Xxxxxxxx x xxxxxxx, xxxxx xxxxxx určeny k xxxxxx xxxxxxxx, x xxxxxxx xxxx xxxxx xxxxxxxx xxxx mimo xxxxxxxx xxxxxxx XX. Xxxxxxxxx xxxxxxxxx XX.x. Xxxxx jednací xxxxxxxxx XX.x. xx) xxxx a xxxx xxxxxxxxx xxxxxxxxx xxxxxxxxx xxxx xxxxxxxx x xxxxxxxxxxxx; x) krmení xxxx a koz xxxxxxxxxx xxxxxxx nebo xxxxxxx z xxxxxxxxxxx, xxx jsou xxxxxxxxxx x Xxxxxx xxxxxx xxxxxxxxxxxxx xxxxxxxxx Xxxxxxx xxxxxxxxxx xxx zdraví xxxxxx (OIE), xxxx xxxxxxxx a zákaz xxx xxxxxx xxxxxxx x xxxx zemi xxxxxxxxxxxx xx xxxx xxxxxxxxxxx xxxxx xxx; x) xxxxxxxxx z xxxxxxxxxxxx, xxx která xxxxxxx xxxxx úřední xxxxxxx x xxxxxx podezření xx xxxxxx TSE; c) xxxxxxxxx z xxxxxxxxxxxx, x nichž po xxxx předchozích sedmi xxx xxxxx xxxxxxxxxxxxxx xxxxx xxxxxx klasické xxxxxxxx, nebo xx xxxxxxxxx případu xxxxxxxx xxxxxxxx: (2) xxx [xxxx xxxxxxxx x zlikvidovány xxxx xxxxxxxx xxxxxxx xxxx x xxxx x xxxxxxxxxxxx x xxxxxxxx xxxxxxxxxx beranů xxxxxxxx XXX/XXX, xxxxxxxx xxxxxx xxxxxxxxx alespoň xxxxx xxxxx XXX x xxxxxx xxxxx XXX x dalších xxxx nesoucích xxxxxxx xxxxx xxxxx XXX;] (2) xxxx [xxxx všechna xxxxxxx, x xxxxx xxxx klasická klusavka xxxxxxxxx, xxxxxxxx a xxxxxxxxxxxx x xx xxxxxxxxxxxx se alespoň xx xxx roky xx xxxxxxxxx xxxxxxxxxx xxxxxxx klasické klusavky xxxxxxxx xxxxxxxxxxxxx sledování XXX, xxxxxx xxxxxxxxx xxxxx xxxxxxxxxxxxx xxxxxx xxxxxxxx 18 xxxxxx, x xxxxxxxx xxxx xxxxxxxx XXX/XXX, xx xxxxxxxxxx TSE x xxxxxxxxxx výsledkem v xxxxxxx x laboratorními xxxxxxxx xxxxxxxxxxx v xxxxxxx X xxxxxxxx X xxxx 3.2 xxxxxxxx (XX) x. 999/2001: — zvířata, která xxxx poražena x xxxxxx spotřebě, x — xxxxxxx, xxxxx xxxxxxx xxxx byla xxxxxxxx x daném xxxxxxxxxxxx, xxxxx xxxxxx xxxxxxxx x xxxxx xxxxxxx xxxxxxxxx xxxxxx.]] Xxxxxxxx Xxxx I: — Xxxxxxx X.6.: Xxxxx xxxxxxxxxx xx xxxxxxx x Evropské xxxx: xxxx xxxxxxx xx xxxxx xxxxxxx xxxxx xxxxx, jedná-li xx x osvědčení xxx xxxxx xxxxxx xxx xxxxxxx přes Xxxxxxxxx xxxx; xxxx xx xxxxxxx, jedná-li se x xxxxxxxxx xxx xxxxx dovážené xx Xxxxxxxx xxxx. — Kolonka X.12.: Místo xxxxxx: xxxx xxxxxxx xx xxxxx xxxxxxx pouze xxxxx, jedná-li xx x osvědčení xxx xxxxx xxxxxx xxx xxxxxxx. Xxxxxxxx xxx xxx xxx tranzitu xxxxxxxxxx xxxxx ve xxxxxxxxxx pásmech, svobodných xxxxxxxx a celních xxxxxxxx; — Xxxxxxx X.15.: Xx xxxxx uvést xxxxxxxxxxx xxxxx (xxxxxx xxxx xxxxxxxxxx x xxxxxxxx xxxxxxxxxx), xxxxx xxxx (xxxxxxx) xxxx xxxxx (xxxxxxxx). V xxxxxxx vykládky a xxxxxxxxxx xxxxxxxx v Xxxxxxxx unii musí xxxxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxxxxx kontroly x xxxxx xxxxxx xx Xxxxxxxx unie. — Xxxxxxx X.19.: Xxxxxxxx xxxxxxxxx xxx xxxxxxxxxxxxxxx systému (XX) následujících xxxxx: 35.03 xxxx 35.04. — Xxxxxxx X.23.: X xxxxxxx kontejnerů pro xxxxx xxxxxx xxxxx xxxx být xxxxxxx xxxxx kontejneru a (xxxxxxxx) xxxxx plomby. — Xxxxxxx I.25.: Technické xxxxxxx: jakékoli xxxx xxxxxxx xxxxx xxxxxx xxxxxxxxxxxxx xxxxxx xxxxxx xxx xxxxxxxxxxxx zvířat x xxxxxx xxxx xxxxxxxxxx krmiv xxx xxxxxxx x zájmovém xxxxx. — Xxxxxxx I.26. x X.27.: Xxxxxxx xxxxx toho, jedná-li xx x osvědčení xxx xxxxxxx xxxx xxx dovoz. — Xxxxxxx X.28.: Xxxx: vyberte: Xxxx, Ruminantia, Xxxxxx, Xxxxxxxx xxxxx Xxxxxxxxxx xxxx Xxxxxx, Xxxxx.  Text obrazu Text obrazu
XXXX Xxxxxxxx x kolagen, xxxxx nejsou xxxxxx x lidské xxxxxxxx, x použití xxxx xxxxx xxxxxxxx nebo xxxx xxxxxxxx xxxxxxx XX. Xxxxxxxxx xxxxxxxxx XX.x. Číslo xxxxxxx xxxxxxxxx XX.x. Xxxx XX: (1x) Xx. xxxx. L 300, 14.11.2009, x. 1. (1x) Úř. věst. X 54, 26.2.2011, x. 1. (2) Xxxxxxxx xx škrtněte. (3) Xx. xxxx. X 147, 31.5.2001, x. 1. (4) Xx. xxxx. X 172, 30.6.2007, x. 84. — Xxxxx xxxxxxx x xxxxxxx se xxxx lišit xx xxxxx xxxxx. — Xxxxxxxx xxx xxxxx xxxxxxxxxxx xx zásilku v Xxxxxxxx xxxx: xxxx xxxxxxxxx xxxxxx xxxxx x xxxxxxxxxxxx xxxxxx x musí xxxxxxx xxxxxxxx až xx xxxxxxxx, kdy dosáhne xxxxxxxxxx hraniční kontroly. Úřední xxxxxxxxxxx lékař / xxxxxx xxxxxxxxx Xxxxx (xxxxxxxx xxxxxx): Xxxxxxxxxxx a xxxxx: Xxxxx: Podpis: Razítko: KAPITOLA 12 Xxxxxxxxxxx xxxxxxxxx xxx xxxxxxxxxxxxx bílkoviny, xxxxxxxxxxxxxxxxxxx xxxxxxxx x xxxxxxxxxxx xxxxxxxx, které xxxxxx xxxxxx k xxxxxx xxxxxxxx, k xxxxxxx xxxx krmná xxxxxxxx xxxx xxxx xxxxxxxx xxxxxxx, xxxxxx x xxxxxxxx do Xxxxxxxx unie xxxx x xxxxxxxx přes xxxx xxxxx (2) &xxxx; Text obrazu Text obrazu
XXXX: Xxxxxxxxxxx xxxxxxxxx xx XX Xxxx I: Xxxxxxxxxxx x odeslané xxxxxxx X.1. Xxxxxxxxxx Xxxxx Xxxxxx Xxx. X.2. Xxxxx jednací xxxxxxxxx X.2.x. X.3. Xxxxxxxxx ústřední xxxxx X.4. Příslušný xxxxxx xxxxx X.5. Příjemce Název Adresa PSČ Tel. I.6. Osoba xxxxxxxxxx za xxxxxxx x EU Jméno Adresa PSČ Tel. I.7. Země xxxxxx Xxx ISO I.8. Xxxxxx xxxxxx Xxx X.9. Země xxxxxx Xxx XXX X.10. Xxxxxx xxxxxx Xxx X.11. Xxxxx xxxxxx Xxxxx Xxxxx xxxxxxxxx Xxxxxx Xxxxx Číslo xxxxxxxxx Xxxxxx Xxxxx Xxxxx xxxxxxxxx Xxxxxx X.12. Xxxxx xxxxxx Xxxxx xxxxx Xxxxx Xxxxx xxxxxxxxx Xxxxxx XXX X.13. Místo xxxxxxxx X.14. Xxxxx xxxxxxx X.15. Xxxxxxxx xxxxxxxxxx Xxxxxxx Plavidlo Xxxxx Xxxxxxxx xxxxxxx Xxxxxxx Xxxxxxxxxxxx Xxxxx xx xxxxxxxx X.16. Xxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxx XX X.17. X.18. Xxxxx zboží I.19. Xxx xxxxx (xxx XX) X.20. Xxxxxxxx X.21. Xxxxxxx xxxxxxxx Xxxxxx Xxxxxxxx Zmrazené I.22. Xxxxx xxxxxx X.23. Xxxxx xxxxxx/xxxxxxxxxx X.24. Xxxx xxxxx  Text obrazu Text obrazu
X.25. Xxxxx osvědčené xxx: Xxxxxx Xxxxxx xxxxxx pro xxxxxxx x xxxxxxxx xxxxx Xxxxxxxxx xxxxxxx X.26. Xxx xxxxxxx xxxx XX do xxxxx xxxx Xxxxx země Kód XXX X.27. Xxx xxxxx xxxx xxxxxx xx XX X.28. Xxxxxxxxxxxx zboží Číslo xxxxxxxxx xxxxxxxx Xxxx (xxxxxxx xxxxx) Xxxx xxxxx Xxxxxxx xxxxx Xxxxx xxxxxx Xxxxx hmotnost Číslo xxxxx  Text obrazu Text obrazu
XXXX Xxxxxxxxxxxxx xxxxxxxxx, xxxxxxxxxxxxxxxxxxx xxxxxxxx x xxxxxxxxxxx xxxxxxxx, xxxxx xxxxxx xxxxxx x xxxxxx xxxxxxxx, k xxxxxxx xxxx krmná xxxxxxxx xxxx xxxx xxxxxxxx xxxxxxx XX. Xxxxxxxxx xxxxxxxxx XX.x. Xxxxx jednací xxxxxxxxx XX.x. Xx, xxxx xxxxxxxxx xxxxxx xxxxxxxxxxx xxxxx, xxxxxxxxxx, xx xxxx xxxxxxx x porozuměl nařízení Xxxxxxxxxx parlamentu x Xxxx (ES) č. 1069/2009(1x), xxxxxxx pokud xxx x xxxxxx 10 xxxxxxxxx xxxxxxxx, x xxxxxxxx Xxxxxx (XX) x. 142/2011(11x), xxxxxxx xxxxx xxx x xxxxxxx XXX xxxxxxxx I xxxxxxxxx xxxxxxxx, x xxxxxxxxx, xx výše xxxxxxx xxxxxxxxxxxxx xxxxxxxxx / xxxxxxxxxxxxxxxxxxx xxxxxxxx / xxxxxxxxxxx vápenatý (2): II.1. xxxxxxxxx (sestává) x xxxxxxxxxxxxxxx xxxxxxxx / xxxxxxxxxxxxxxxxxxxx xxxxxxxxxx / xxxxxxxxxxxx xxxxxxxxxx (2), xxxxx(x) xxxxxxx(x) xxxx xxxxxxx veterinární požadavky; II.2. xxxxxxxxx (xxxxxxx) xxxxxxxx x xxxxxxxxxxxxxxx bílkovin / xxxxxxxxxxxxxxxxxxxx xxxxxxxxxx / xxxxxxxxxxxx vápenatého (2), xxxxx(x) nejsou (xxxx) xxxxx(x) x xxxxxx xxxxxxxx; XX.3. xxx(x) xxxxxxxxx(x) a skladován(y) x xxxxxxx xxxxxxxxxx x xxxxxxxxxxx příslušným xxxxxxx x xxxxxxx x xxxxxxx 24 xxxxxxxx (ES) x. 1069/2009 xx xxxxxx xxxxxxx xxxxxxxxxxx původců; II.4. xxx(x) xxxxxxxxx(x) výhradně x xxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx: (2) xxx [x xxxxxxx xxxxxxxxxxxxxxxxxxxx xxxxxxxxxx xxxxxxxxx x kostí zbavených xxxx xxxx xxxxxxxxxx xxxxxx a xxxxxx xxxxx, xxxx x xxxxxxx xxxxx xxxx xxxxxxxxxx xxxxxx xxxx xxxxxx části, xxxxx xxxx podle právních xxxxxxxx Xxxx xxxxxx x xxxxxx xxxxxxxx, xxxxx x xxxxxxxxxx xxxxxx xxxxxx k xxxxxx xxxxxxxx xxxxxxx;] (2) xxxx [x xxxxxxx xxxxxx xxxxxxxxx: (2) buď [- xxxx xxxxxxxxxx xxxxxx a jejich xxxxx, xxxx v xxxxxxx xxxxx xxxx xxxxxxxxxx xxxxxx nebo xxxxxx xxxxx, které xxxx xxxxx právních xxxxxxxx Unie xxxxxx x xxxxxx spotřebě, xxxxx x xxxxxxxxxx xxxxxx nejsou x xxxxxx xxxxxxxx xxxxxx;]] (2) x/xxxx [- xxxxxxx xxxxxxxx xxxx a xxxx uvedené xxxxx xxxxxxxxxxx xxx xx xxxxxx, xxxxx byla xxxxxxxx xx jatkách x xx xxxxxxxxx xxxx porážkou xxxx xxxxxxxx xxxx xxxxxxxxx x xxxxxxx k xxxxxx xxxxxxxx, nebo xxxx x xxxx xxxxxxx xxxxx zvěře xxxxxxxx x xxxxxx xxxxxxxx v souladu x xxxxxxxx xxxxxxxx Xxxx: x) jatečně xxxxxxxx xxxx xxxx xxxx xxxxxx a xxxxxx xxxxx, které xxxx x souladu x xxxxxxxx xxxxxxxx Xxxx xxxxxxxxxx xx xxxxxxxx x lidské spotřebě, xxxxx xxxxxxxxxxxx žádné xxxxxxxx xxxxxxxxxx xxxxxxxxxx xx xxxxxxx xxxx xxxxxxx; xx) xxxxx drůbeže; iii) xxxx x xxxxx, xxxxxx xxxxxx xxxxxxx x xxxxxx, rohy x končetiny, xxxxxx xxxxxx prstů, xxxxxxxxxx x záprstních xxxxxx, xxxxx a xxxxxxx; xx) xxxxxxx xxxxxxx; x) peří;]] (2) x/xxxx [- xxxx xxxxxx, xxxxx xxxxxxxxxxxx xxxxx příznaky xxxxxxxxxx xxxxxxxxxx xxxx xx xxxxxxx xxxx zvířata, xxxxx xxxx xxxxxxxx xx xxxxxxx x xxxxx xxxx xx xxxxxxxxx xxxx xxxxxxxx xxxxxxxx způsobilými x xxxxxxx k xxxxxx xxxxxxxx x xxxxxxx x xxxxxxxx xxxxxxxx Xxxx;]] (2) x/xxxx [- xxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx, které xxxxxxxx xxx xxxxxx xxxxxxxx xxxxxxxx k lidské xxxxxxxx, xxxxxx xxxxxxxxxxx xxxxx, xxxxxxx xxxx xxxx x xxxxxxxxxxx xxxx xxxxxxxxxx xx xxxxxxxxxx xxxxx;]] (2) x/xxxx [- produkty xxxxxxxxxxx xxxxxx nebo xxxxxxxxx xxxxxxxxxx produkty xxxxxxxxxxx xxxxxx, xxxxx x xxxxxxxxxx xxxxxx xxxx x xxxxxx xxxxxxxx xxxxxxxxxxx xxxxxxxxx vadami, xxxxxx xxxxxx xxxx xxxxxx xxxxxxxx, x xxxxx nevzniká xxxxx xxxxxx pro xxxxxx xxxx xxx xxxxxx, xxx xxxxxx xxxxxx x xxxxxx xxxxxxxx;] Xxxx XX: Xxxxxxxxx  Text obrazu Text obrazu
XXXX Xxxxxxxxxxxxx xxxxxxxxx, hydrogenfosforečnan vápenatý x xxxxxxxxxxx xxxxxxxx, xxxxx xxxxxx xxxxxx x xxxxxx xxxxxxxx, x xxxxxxx jako xxxxx xxxxxxxx nebo xxxx xxxxxxxx xxxxxxx XX. Xxxxxxxxx xxxxxxxxx XX.x. Číslo xxxxxxx xxxxxxxxx XX.x. (2) x/xxxx [- krmivo xxx xxxxxxx v zájmovém xxxxx x xxxxxx xxxxxxxxxxx xxxxxx nebo xxxxxx xxxxxxxxxx vedlejší xxxxxxxx xxxxxxxxxxx xxxxxx xx získané produkty, xxxxx x xxxxxxxxxx xxxxxx nebo z xxxxxx xxxxxxxx xxxxxxxxxxx xxxxxxxxx vadami, xxxxxx xxxxxx nebo jinými xxxxxxxx, x xxxxx xxxxxxxx xxxxx riziko xxx zdraví lidí xxx xxxxxx, již xxxxxx určeny ke xxxxxx;]] (2) x/xxxx [- xxxx, xxxxxxxx, xxxx, xxxx, xxxx, xxxx, xxxxxxx kopyt a xxxxxxxx a syrové xxxxx xxxxxxxxxxx xx xxxxxx xxxxxx, xxxxx xxxxxxxxxxxx xxxxx xxxxxxxx xxxxxxxxxx xxxxxxxxxx tímto xxxxxxxxx xx člověka xxxx xxxxxxx;]] (2) a/nebo [- xxxxx xxxxxxxxxxx x jejich xxxxx, xxxxx mořských xxxxx, xxxxx nevykazovali xxxxx xxxxxxxx xxxxxxxxxx xxxxxxxxxx xx xxxxxxx nebo xxxxxxx;]] (2) x/xxxx [- xxxxxxxx produkty xxxxxxxxxxx xxxxxx x xxxxxxx xxxxxxxxx xxxxxxxxxxx z xxxxxxx xxxx xxxxxxxx xx xxxxxx produktů xxxxxxxx k xxxxxx xxxxxxxx;]] (2) a/nebo [- xxxx xxxxxxx materiál xxxxxxxxxxx xx xxxxxx, xxxxx xxxxxxxxxxxx žádné xxxxxxxx xxxxxxxxxx přenosného xxxxx materiálem na xxxxxxx xxxx xxxxxxx: x) xxxxx měkkýšů a xxxxxx x měkkými xxxxxxx xxxx xxxxx; xx) xxxxx xxxxxxxx xxxxxxxxxxx xx xxxxxxxxxxxxx xxxxxx: — xxxxxxxx xxxxxxxx x xxxxx, — xxxxx, — vedlejší xxxxxxxx x xxxxx, xxxxxx vaječných xxxxxxxx; xxx) xxxxxxxxxx xxxxxx xxxxxxxx x obchodních xxxxxx;]] XX.5. xxxxxxxxxxxxx bílkoviny / xxxxxxxxxxxxxxxxxxx xxxxxxxx / xxxxxxxxxxx vápenatý (2): x) xxx(x) zabalen(y), xxxxxx(x) xx xxxxxxx xxxxx xxxxxxxxxx xxxxxxxxx s xxxxxxx „NENÍ XXXXXX X XXXXXX SPOTŘEBĚ“ x xxx(x) uskladněn(y) x xxxxxxxxxxx(x) za xxxxxxxxxxxxxx xxxxxxxxxxxx xxxxxxxx x zejména xxxxxx x xxxxxxxx xx xxxxxxx xxxxx proběhlo x xxxxxxxxx xxxxxx x xxxxxx xxxxx x byly xxxxxxx xxxxx xxxxxxxxxxx prostředky xxxxxxxx právními xxxxxxxx Xxxx; x (2) xxx [x) xxxxxxxxxxxxx xxxxxxxxx xxxx xxxxxxxx xxxxxxxx, xxxxx xxxxxxxx xxxxxxxxxxxx xxxxxxxx k xxxxxxxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxx 3. Xxxxxxxxxxxxx xxxxxxxxx xxxxx nebo zčásti xxxxxxx x xxxx x xxxxx xxxxxxxxxxx xxxx vyrobeny xx xxxxxxxxxxxxxxx xxxxxxxx určeném xxxxxxxx k výrobě xxxxxxxxxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx kategorie 3 xxxxxxxxxx xx xxxxxxx xxxx, loužením a xxxxxxxxxxx xxxxxx, xx xxxx xxxxxxxxx: x) vystavení xxxxxxxxx pH x xxxxxxx xxxxx xxx 11 xx xxxx xxxxx než tři xxxxxx při xxxxxxx xxxxx xxx 80 °X x následně xxxxxxx xxxxxxxx xxx xxxxxxx vyšší než 140 °X xx xxxx 30 minut xxx tlaku vyšším xxx 3,6 xxxx; xxxx xx) xxxxxxxxx xxxxxxxxx xX x xxxxxxx xxxxxx 1 xx 2 xxxxxxxxxxx xxxxxxxxxx xX o xxxxxxx xxxxx než 11 x xxxxxxxx xxxxxxx xxxxxxxx xxx teplotě 140 °C po xxxx 30 minut xxx xxxxx 3 xxxx;] (2) xxxx [x) xxxxxxxxxxxxxxxxxxx vápenatý xxx xxxxxxx postupem, který i) xxxxxxxxx, xx všechen xxxxxx xxxxxxxx xxxxxxxxx 3 xx najemno xxxxxxx x pomocí xxxxx vody xxxxxxxx x xxxxxxx xxxxxxxx xxxxxxxxx chlorovodíkovou (při xxxxxxxxx koncentraci 4 % x pH xxxxxx xxx 1,5) xx dobu xxxxxxx xxxx dnů; ii) xxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxxxxxx xxxxxx xxxxxx, xxx xxxx x získání xxxxxxxx xxxxxxxxx hydrogenfosforečnanu xxxxxxxxxx xxx pH 4 až 7, x  Text obrazu Text obrazu
XXXX Xxxxxxxxxxxxx xxxxxxxxx, xxxxxxxxxxxxxxxxxxx xxxxxxxx x xxxxxxxxxxx xxxxxxxx, které xxxxxx určeny k xxxxxx spotřebě, x xxxxxxx jako xxxxx xxxxxxxx xxxx xxxx xxxxxxxx řetězec II. Xxxxxxxxx xxxxxxxxx XX.x. Xxxxx jednací xxxxxxxxx XX.x. xxx) xxxx sraženinu xxxxxxx vysuší xxxxxxxx xxx xxxxxxx xxxxxxx x xxxxxxx xx 65 °C xx 325 °X a xxxxxxx teplotě v xxxxxxx xx 30 °X xx 65 °X;] (2) xxxx [x) xxxxxxxxxxx xxxxxxxx xxx xxxxxxx xxxxxxxx, xxxxx xxxxxxxxx: x) xx všechen xxxxxx materiál xxxxxxxxx 3 je xxxxxxx xxxxxxx x pomocí xxxxxxxxxxx horké xxxx xxxxxxxx (úlomky kostí xxxxx než 14 xx), xx) xxxxxxxxxxx xxxxxx x xxxx xxx xxxxxxx 145 °C xx dobu 30 xxxxx xxx tlaku 4 bary, iii) že xxxxx x bílkovin xx odstředěním xxxxxx xx xxxxxxxxxxxxxx (xxxxxxxxxxxx xxxxxxxxxx), a iv) xxxxxxxxx xxxxxxxxxxxx xxxxxxxxxx xx xxxxxx xx xxxxxxxx xxxx vzduchem o xxxxxxx 200 °X;] (2) [XX.6. výše popsané xxxxxxxxxxxxx bílkoviny / xxxxxxxxxxxxxxxxxxx xxxxxxxx / xxxxxxxxxxx xxxxxxxx (2): (2) xxx [xx/xxxx xxxxxx(x) x xxxxxxxxxxx xxxxxx xxx xxxx, xxxx xxxx xxxx;]] (2) nebo [xx/xxxx xxxxxx(x) ze xxxxx, xxxx nebo xxx x xxxxxxxxxx(x) xxxx xxxxxxx xxxxxx xxx z nich xxxxx(x) xxxxxx(x): (2) xxx [xxxxxxxx xxxxxxxxxxx xx xxxxx, ovcí x xxx xxxx xxx xxxxxxx ze xxxxxx xxxxxxxxxx, xxxxxxxxxxx chovaných x poražených v xxxx nebo xxxxxxx xxxxxxxx x xxxxxxx x xxxxxxxxxxx 2007/453/XX xx xxxxxxxxx xxxx xxxx xxxxxxx xx xxxxxxxxxxxxx rizikem výskytu XXX;]] (2) nebo [x) xxxxxxxxxxxxx xxxxxxxx xxxxxxxx, xxx xx definován x xxxx 1 xxxxxxx X xxxxxxxx Xxxxxxxxxx xxxxxxxxxx a Xxxx (XX) x. 999/2001 (3); b) xxxxxxx xxxxxxxx xxxx xxxxxxx x xxxxx xxxxx, xxxx xxxx koz x xxxxxxxx zvířat xxxxxxxxxx, xxxxxxxxxxx xxxxxxxxx x poražených x xxxx xxxx xxxxxxx xxxxxxxx x xxxxxxx x xxxxxxxxxxx Xxxxxx 2007/453/XX (4) xx xxxxxxxxx xxxx xxxx xxxxxxx xx zanedbatelným xxxxxxx xxxxxxx BSE, x xxxxx xxxxx xxxxxxx xxxxx domácí xxxxxx XXX; x) xxxxxxxx xxxxxxx živočišného xxxxxx xxxx xxxxxxx xxxxxxx xx xxxxx, xxxx xxxx koz, které xxxx po xxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxx xxxxx pomocí xxxxxxxxxxx xxxxxxxxxx nástroje xxxxxxxxxx xx xxxxxx xxxxxxx xxxx xxxxxxxxxxxxxxx xxxxxxx xxxxxxx do xxxxxx xxxxxxx, x xxxxxxxx zvířat xxxxxxxxxx, xxxxxxxxxxx xxxxxxxxx x xxxxxxxxxx v xxxx xxxx xxxxxxx zařazené x xxxxxxx x xxxxxxxxxxx 2007/453/ES do xxxxxxxxx xxxx xxxx xxxxxxx se zanedbatelným xxxxxxx xxxxxxx BSE;]]] II.7. xxxx popsané xxxxxxxxxxxxx xxxxxxxxx / hydrogenfosforečnan xxxxxxxx / xxxxxxxxxxx xxxxxxxx (2): (2) xxx [xxxxxxxxxx(x) mléko xxxx xxxxxx xxxxxxx xxxxxxxxxxx x xxxx xxxx xxx xxx xxxx/xxxxxx xxxxxx pro xxxxxx xxxxxxxxxxxxx xxxxxx xxxxxx xxx xxxxxxxxxxxx zvířat.] (2) xxxx [xxxxxxxx(x) xxxxx xxxx mléčné xxxxxxx xxxxxxxxxxx x xxxx xxxx xxx a xx/xxxx určeny xxx xxxxxx hospodářských zvířat xxxxxx xxx xxxxxxxxxxxx xxxxxx a xxxxx xxxx xxxxxx výrobky: a) xxxx xxxxxxx z xxxx x xxx, xxxxx xxxx xxxxxxxxxxx xx xxxxxxxx xxxxxxx x xxxx, x xxx jsou xxxxxxx xxxx podmínky: i) xxxxxxxx xxxxxxxx xx povinná xxxxxxxx; xx) xxxxxxx xxxxxx xxxxxx, xxxxxxxxx x xxxxxxx, xxxxx xxx x klasickou klusavku; iii) xx hospodářství s xxxxxx xxxx nebo xxx se xxxxxxxxx xxxxxx xxxxxxx v xxxxxxx podezření na XXX xxxx xxxxxxxxx xxxxxxxx xxxxxxxx;  Text obrazu Text obrazu
ZEMĚ Hydrolyzované xxxxxxxxx, hydrogenfosforečnan xxxxxxxx x xxxxxxxxxxx xxxxxxxx, xxxxx xxxxxx xxxxxx x lidské spotřebě, x použití xxxx xxxxx xxxxxxxx xxxx xxxx krmivový řetězec II. Xxxxxxxxx xxxxxxxxx XX.x. Xxxxx xxxxxxx xxxxxxxxx XX.x. xx) xxxx x xxxx postižené xxxxxxxxx xxxxxxxxx xxxx xxxxxxxx a xxxxxxxxxxxx; x) xxxxxx ovcí x xxx xxxxxxxxxx xxxxxxx xxxx xxxxxxx z xxxxxxxxxxx, jak xxxx xxxxxxxxxx x Xxxxxx xxxxxx suchozemských xxxxxxxxx Xxxxxxx xxxxxxxxxx xxx xxxxxx xxxxxx (OIE), xxxx xxxxxxxx x xxxxx byl xxxxxx xxxxxxx x xxxx xxxx xxxxxxxxxxxx xx xxxx předchozích xxxxx xxx; x) xxxxxxxxx z xxxxxxxxxxxx, xxx xxxxx xxxxxxx xxxxx xxxxxx xxxxxxx x xxxxxx xxxxxxxxx na výskyt XXX; x) xxxxxxxxx x xxxxxxxxxxxx, x xxxxx xx xxxx xxxxxxxxxxx xxxxx xxx xxxxx xxxxxxxxxxxxxx žádný případ xxxxxxxx xxxxxxxx, xxxx xx xxxxxxxxx xxxxxxx xxxxxxxx xxxxxxxx: (2) xxx [xxxx xxxxxxxx a xxxxxxxxxxxx xxxx xxxxxxxx xxxxxxx xxxx x xxxx x xxxxxxxxxxxx x xxxxxxxx plemenných xxxxxx xxxxxxxx XXX/XXX, xxxxxxxx xxxxxx xxxxxxxxx xxxxxxx xxxxx xxxxx XXX a žádnou xxxxx XXX x xxxxxxx xxxx nesoucích xxxxxxx jednu xxxxx XXX;] (2) xxxx [xxxx xxxxxxx zvířata, u xxxxx xxxx xxxxxxxx xxxxxxxx xxxxxxxxx, usmrcena x zlikvidována a xx xxxxxxxxxxxx xx xxxxxxx po dva xxxx xx xxxxxxxxx xxxxxxxxxx xxxxxxx klasické xxxxxxxx xxxxxxxx intenzivnější xxxxxxxxx XXX, xxxxxx xxxxxxxxx xxxxx xxxxxxxxxxxxx xxxxxx xxxxxxxx 18 xxxxxx, s xxxxxxxx xxxx genotypu XXX/XXX, xx xxxxxxxxxx XXX x xxxxxxxxxx výsledkem x xxxxxxx x xxxxxxxxxxxxx xxxxxxxx stanovenými x xxxxxxx X xxxxxxxx X xxxx 3.2 xxxxxxxx (XX) x. 999/2001: — zvířata, xxxxx byla xxxxxxxx x xxxxxx xxxxxxxx, x — xxxxxxx, která xxxxxxx xxxx byla xxxxxxxx v xxxxx xxxxxxxxxxxx, xxxxx xxxxxx xxxxxxxx x xxxxx xxxxxxx eradikace nákazy.]] Poznámky Část X: — Kolonka X.6.: Xxxxx zodpovědná za xxxxxxx x Xxxxxxxx xxxx: xxxx xxxxxxx xx xxxxx xxxxxxx xxxxx tehdy, xxxxx-xx xx x xxxxxxxxx xxx xxxxx určené xxx xxxxxxx xxxx Xxxxxxxxx unii; xxxx xx xxxxxxx, xxxxx-xx xx x osvědčení xxx xxxxx xxxxxxxx xx Xxxxxxxx xxxx. — Xxxxxxx X.12.: Místo xxxxxx: xxxx kolonku xx xxxxx vyplnit xxxxx tehdy, xxxxx-xx xx x osvědčení xxx xxxxx xxxxxx xxx xxxxxxx. Produkty xxx xxx xxx xxxxxxxx xxxxxxxxxx pouze xx xxxxxxxxxx pásmech, xxxxxxxxxx xxxxxxxx x xxxxxxx skladech. — Kolonka X.15.: Registrační xxxxx (xxxxxxxxxxxx vagonů xxxx xxxxxxxxxx a xxxxxxxxxx xxxxxxxxxx), číslo letu (xxxxxxx) xxxx xxxxx (xxxxxxxx); informace xx xxxxx xxxxxxxxxx v xxxxxxx xxxxxxxx x xxxxxxxxxx xxxxxxxx. — Kolonka X.19.: Xxxxxxxx xxxxxxxxx xxx HS: 05.08, 28.35.25, 28.35.26, 29.22, 35.02, 35.03 nebo 35.04. — Xxxxxxx I.23.: X xxxxxxx xxxxxxxxxx xxx xxxxx ložené xxxxx xxxx být xxxxxxx xxxxx xxxxxxxxxx x (xxxxxxxx) číslo xxxxxx. — Xxxxxxx X.25.: Xxxxxxxxx xxxxxxx: jakékoli xxxx xxxxxxx xxxxx xxxxxx xxxxxxxxxxxxx xxxxxx xxxxxx než kožešinových xxxxxx x výroba xxxx xxxxxxxxxx xxxxx xxx xxxxxxx x xxxxxxxx xxxxx. — Xxxxxxx X.26. a X.27.: Xxxxxxx podle xxxx, xxxxx-xx xx x xxxxxxxxx xxx tranzit xxxx pro xxxxx. — Xxxxxxx X.28.: — Xxxx: xxxxxxx: Xxxx, Ruminantia, Xxxxxx, Xxxxxxxx kromě Xxxxxxxxxx xxxx Xxxxxx, Xxxxx, Xxxxxxxx, Xxxxxxxxx, xxxxxxxxxx kromě Xxxxxxxx x Crustacea.  Text obrazu Text obrazu
ZEMĚ Hydrolyzované xxxxxxxxx, xxxxxxxxxxxxxxxxxxx xxxxxxxx x xxxxxxxxxxx xxxxxxxx, xxxxx xxxxxx určeny x xxxxxx xxxxxxxx, x xxxxxxx xxxx xxxxx xxxxxxxx xxxx xxxx xxxxxxxx řetězec II. Xxxxxxxxx xxxxxxxxx XX.x. Xxxxx xxxxxxx osvědčení II.b. — Druh xxxxx: xxxxxxxxx, jedná-li xx x xxxxxxxxxxxxx xxxxxxxxx, xxxxxxxxxxxxxxxxxxx vápenatý xxxx fosforečnan xxxxxxxx. — Xxxxxxx závod: xxxxxxx xxxxx xxxxxxxxxx xxxxxxxx, x xxxx xxxxxxxx xxxxxxxx nebo xxxxxxxxxx. Xxxx XX: (1x) Xx. xxxx. X 300, 14.11.2009, x. 1. (1x) Xx. xxxx. X 54, 26.2.2011, x. 1. (2) Xxxxxxxx xx škrtněte. (3) Xx. věst. X 147, 31.5.2001, x. 1. (4) Xx. xxxx. X 94, 1.4.2006, x. 28. — Xxxxx xxxxxxx x xxxxxxx xx xxxx xxxxx xx barvy xxxxx. — Xxxxxxxx xxx xxxxx xxxxxxxxxxx xx xxxxxxx x Xxxxxxxx xxxx: xxxx xxxxxxxxx xxxxxx xxxxx k xxxxxxxxxxxx xxxxxx a musí xxxxxxx provázet xx xx xxxxxxxx, xxx xxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxx x xxxxx xxxxxx do Evropské xxxx. Xxxxxx veterinární xxxxx / úřední xxxxxxxxx Xxxxx (xxxxxxxx písmem): Kvalifikace x xxxxx: Xxxxx: Podpis: Razítko: |
|
6) |
Kapitola 18 xx xxxxxxxxx xxxxx: „XXXXXXXX 18 Veterinární xxxxxxxxx xxx xxxx a xxxxxxx x xxxx (kromě xxxxxx xxxxxx) x xxxxxx x paznehty x xxxxxxx z xxxx (kromě moučky x xxxxx x xxxxxxxx) x xxxxxx xxxxxxxxxxx hnojiv xxxx xxxxxxxxx xxxxxxx látek xxxxxx x odeslání xx Xxxxxxxx xxxx xxxx k xxxxxxxx xxxx xxxx území (2)  &xxxx;Text obrazu &xxxx;Text obrazu
XXXX: Xxxxxxxxxxx osvědčení xx XX Xxxx X: Podrobnosti x xxxxxxxx xxxxxxx X.1. Xxxxxxxxxx Xxxxx Xxxxxx Xxx. X.2. Číslo xxxxxxx xxxxxxxxx X.2.x. X.3. Příslušný ústřední xxxxx X.4. Xxxxxxxxx místní xxxxx X.5. Příjemce Název Adresa PSČ Tel. I.6. Xxxxx xxxxxxxxxx xx xxxxxxx x XX Xxxxx Xxxxxx XXX Xxx. X.7. Xxxx xxxxxx Xxx XXX X.8. Xxxxxx xxxxxx Xxx X.9. Xxxx xxxxxx Xxx XXX X.10. Xxxxxx xxxxxx Xxx X.11. Xxxxx xxxxxx Xxxxx Číslo xxxxxxxxx Xxxxxx Xxxxx Xxxxx xxxxxxxxx Xxxxxx Xxxxx Xxxxx xxxxxxxxx Xxxxxx X.12. Xxxxx xxxxxx Xxxxx xxxxx Xxxxx Číslo xxxxxxxxx Xxxxxx XXX X.13. Xxxxx xxxxxxxx X.14. Xxxxx xxxxxxx X.15. Xxxxxxxx xxxxxxxxxx Xxxxxxx Xxxxxxxx Xxxxx Xxxxxxxx xxxxxxx Xxxxxxx Xxxxxxxxxxxx Xxxxx na xxxxxxxx X.16. Vstupní xxxxxxxxxx xxxxxxxx xxxxxxxx EU I.17. Xxxxx/xxxxx CITES I.18. Popis xxxxx X.19. Kód xxxxx (xxx HS) 05.07 I.20. Množství I.21. Xxxxxxx produktů Okolní Xxxxxxxx Xxxxxxxx X.22. Xxxxx xxxxxx X.23. Xxxxx xxxxxx/xxxxxxxxxx X.24. Druh xxxxx  Text obrazu Text obrazu
X.25. Xxxxx xxxxxxxxx xxx: Xxxxx zpracování Xxxxxxxxx xxxxxxx X.26. Xxx xxxxxxx přes EU xx třetí xxxx Xxxxx xxxx Xxx XXX X.27. Xxx xxxxx xxxx xxxxxx xx XX X.28. Xxxxxxxxxxxx xxxxx Xxxxx schválení xxxxxxxx Xxxx (xxxxxxx název) Výrobní xxxxx Xxxxx hmotnost Číslo xxxxx  Text obrazu Text obrazu
XXXX Xxxx x výrobky x xxxx (xxxxx xxxxxx moučky) x xxxxxx a xxxxxxxx x xxxxxxx x xxxx (xxxxx moučky x kopyt x xxxxxxxx) x xxxxxx xxxxxxxxxxx hnojiv xxxx xxxxxxxxx xxxxxxx xxxxx XX. Xxxxxxxxx xxxxxxxxx XX.x. Xxxxx xxxxxxx xxxxxxxxx XX.x. Xx, xxxx xxxxxxxxx xxxxxx xxxxxxxxxxx xxxxx, xxxxxxxxxx, xx xxxx přečetl x xxxxxxxxx nařízení Evropského xxxxxxxxxx x Xxxx (XX) č. 1069/2009 (1x) x xxxxxxxx Xxxxxx (XX) x. 142/2011 (1x), xxxxxxx xxxxx xxx x xxxxxxx XXX xxxxxxxx XX xxxxxxxxx xxxxxxxx, x xxxxxxxxx, xx xxxx popsané xxxx x výrobky z xxxx (kromě rohové xxxxxx) x xxxxxx x paznehty x xxxxxxx x xxxx (xxxxx xxxxxx x xxxxx a xxxxxxxx) (2) XX.1. pocházejí xx xxxxxx (2) buď [xxxxx xxxx xxxxxxxx xx xxxxxxx x xxxxx xxxx xx prohlídce xxxx porážkou shledána xxxxxxxx pro účely xxxxxxx x xxxxxx xxxxxxxx;] (2) xxxx [xxxxx xxxxxxxxxxxx xxxxx xxxxxxxx xxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxx xxxxxxxxx xx xxxxxxx či zvířata;] II.2. xxxx x xxxxxxx x xxxx, xxxxxx x paznehty x xxxxxxx x xxxx xxxxxx xxxxxxxx ošetřením xx xxxx jedné xxxxxx při xxxxxxx x jádře xxxxxxx 80 °C; II.3. rohy xxxx xxxxxxxx xxx, xx nedošlo x xxxxxxxx xxxxxx xxxxxxx; XX.4. xx xxxxx xxxxxx xxxxxxxxxx, uskladnění xxxx xxxxxxxx byla uplatněna xxxxxxx xxxxxxxxxxx xxxxxxxx x xxxxxxxxx křížové xxxxxxxxxxx; XX.5. xxxx a xxxxxxx x nich (xxxxx xxxxxx moučky) x xxxxxx a xxxxxxxx a xxxxxxx x xxxx (xxxxx xxxxxx x xxxxx x xxxxxxxx) xxxx xxxxxxxx: (2) xxx [xx xxxxxx xxxxx xxxx xxxxx;] (2) xxxx [xx xxxxxxxxx xxxx xxxxxxxxxxxx xxx xxxxx xxxxxx xxxxx, které xxxx xxxx xxxxxxxxx xxxxxxxxxxxxxxx xxxxxxxxxxxx xxxxxxxxxxx schváleným xxxxxxxxxx orgánem;] a xxxxx xxxx nádoby x xxxxxxxxxx xxxx xxxxxxxx xxx, xx xxxxxxx xxxx xxxxxxxxxx produktu xxxxxxxxxxx xxxxxx (3) x jsou xxxxxxxx xxxxxxxxx s xxxxxxx „XXXX URČENO K XXXXXX XXXXXXXX XXX XX XXXXXX XXXXXX“ x xxxxxx x xxxxxxx xxxxxxxx určení;] (2) [XX.6. xxxx xxxxxxx xxxx a xxxxxxx x xxxx (kromě xxxxxx xxxxxx) a xxxxxx x paznehty x výrobky x xxxx (kromě xxxxxx x xxxxx x xxxxxxxx) (2) xxx [xxxx xxxxxxx x přežvýkavců xxxxxx xxx xxxx, xxxx nebo kozy.]] (2) xxxx [jsou xxxxxxx xx xxxxx, xxxx xxxx xxx x xxxxxxxxxx dále xxxxxxx xxxxxx xxx z xxxx nebyly xxxxxxx: (2) xxx [materiál xxxxxxxxxxx xx xxxxx, xxxx x xxx xxxxxx xxx xxxxxxxxxx, xxxxxxxxxxx xxxxxxxxx x poražených x xxxx xxxx xxxxxxx zařazené v xxxxxxx s xxxxxxxxxxx 2007/453/XX xx kategorie xxxx nebo oblasti xx zanedbatelným rizikem xxxxxxx BSE.] (2) nebo [x) xxxxxxxxxxxxx xxxxxxxx xxxxxxxx, xxx je xxxxxxxxx v xxxx 1 xxxxxxx V xxxxxxxx Evropského xxxxxxxxxx x Rady (XX) x. 999/2001 (4); x) xxxxxxx oddělené xxxx xxxxxxx x xxxxx xxxxx, ovcí xxxx xxx s xxxxxxxx xxxxxx xxxxxxxxxx, nepřetržitě xxxxxxxxx x xxxxxxxxxx x xxxx nebo xxxxxxx zařazené v xxxxxxx s xxxxxxxxxxx Xxxxxx 2007/453/XX (5) xx xxxxxxxxx xxxx xxxx xxxxxxx xx xxxxxxxxxxxxx xxxxxxx xxxxxxx XXX, x xxxxx xxxxx xxxxxxx žádný xxxxxx xxxxxx XXX; x) xxxxxxxx produkt xxxxxxxxxxx xxxxxx xxxx xxxxxxx xxxxxxx ze xxxxx, xxxx nebo xxx, xxxxx xxxx xx xxxxxxxx usmrceny lacerací xxxxxxxxx xxxxxxx xxxxx xxxxxx xxxxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxxx xx xxxxxx lebeční xxxx xxxxxxxxxxxxxxx xxxxxxx xxxxxxx xx dutiny xxxxxxx, x výjimkou xxxxxx xxxxxxxxxx, xxxxxxxxxxx xxxxxxxxx x poražených x xxxx xxxx xxxxxxx xxxxxxxx v souladu x rozhodnutím 2007/453/XX xx xxxxxxxxx xxxx xxxx xxxxxxx xx xxxxxxxxxxxxx xxxxxxx xxxxxxx XXX.]]] Xxxx XX: Xxxxxxxxx  Text obrazu Text obrazu
XXXX Xxxx x xxxxxxx x xxxx (xxxxx xxxxxx moučky) x xxxxxx x paznehty x xxxxxxx x xxxx (kromě xxxxxx x xxxxx x xxxxxxxx) x výrobě xxxxxxxxxxx xxxxxx xxxx xxxxxxxxx xxxxxxx xxxxx XX. Xxxxxxxxx xxxxxxxxx XX.x. Xxxxx xxxxxxx xxxxxxxxx XX.x. Xxxxxxxx Xxxx I: — Xxxxxxx X.6.: Osoba xxxxxxxxxx za zásilku x Xxxxxxxx xxxx: xxxx xxxxxxx xx xxxxx xxxxxxx pouze xxxxx, xxxxx-xx xx x osvědčení xxx xxxxx xxxxxx pro xxxxxxx přes Evropskou xxxx; xxxx xx xxxxxxx, xxxxx-xx xx x osvědčení xxx xxxxx dovážené xx Xxxxxxxx xxxx. — Kolonky X.11. a X.12.: Xxxxx schválení: xxxxx xxxxxxxxxx zařízení xxxx xxxxxxx, xxxxx bylo xxxxxx xxxxxxxxxx xxxxxxx. — Xxxxxxx X.12.: Xxxxx xxxxxx: xxxx xxxxxxx xx třeba xxxxxxx xxxxx xxxxx, xxxxx-xx xx x xxxxxxxxx xxx xxxxx xxxxxx xxx xxxxxxx. Xxxxxxxx xxxx být xxx xxxxxxxx xxxxxxxxxx pouze xx xxxxxxxxxx pásmech, xxxxxxxxxx xxxxxxxx a xxxxxxx xxxxxxxx. — Kolonka X.15.: Xxxxxxxxxxx číslo (xxxxxxxxxxxx vagonů xxxx xxxxxxxxxx a nákladních xxxxxxxxxx), xxxxx xxxx (xxxxxxx) xxxx xxxxx (xxxxxxxx); xxxxxxxxx xx xxxxx xxxxxxxxxx x xxxxxxx xxxxxxxx x xxxxxxxxxx xxxxxxxx x Xxxxxxxx unii. — Kolonka X.23.: X xxxxxxx xxxxxxxxxx xxx xxxxx xxxxxx xxxxx xxxx xxx xxxxxxx xxxxx xxxxxxxxxx x (xxxxxxxx) xxxxx xxxxxx. — Xxxxxxx X.25.: Technické xxxxxxx: xxxxxxxx xxxx využití xxxxx xxxxxx zvířat. — Xxxxxxx X.26. a X.27.: Vyplňte podle xxxx, xxxxx-xx xx x xxxxxxxxx xxx xxxxxxx nebo xxx xxxxx. — Kolonka X.28.: Xxxx zboží. Část II: (1a) Xx. věst. L 300, 14.11.2009, s. 1. (1x) Úř. xxxx. X 54, 26.2.2011, x. 1. (2) Xxxxxxxx xx škrtněte. (3) Druh xxxxxxxx: xxxx x xxxxxxx x xxxx, xxxxxx x paznehty x xxxxxxx x xxxx. (4) Úř. xxxx. X 147, 31.5.2001, x. 1. (5) Xx. xxxx. X 172, 30.6.2007, s. 84. — Xxxxx xxxxxxx x xxxxxxx xx musí xxxxx od xxxxx xxxxx. — Xxxxxxxx pro xxxxx xxxxxxxxxxx za xxxxxxx v Evropské xxxx: xxxx osvědčení xxxxxx xxxxx x xxxxxxxxxxxx xxxxxx a xxxx zásilku provázet xx do xxxxxxxx, xxx xxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxx x xxxxx vstupu xx Xxxxxxxx xxxx. Xxxxxx xxxxxxxxxxx xxxxx / xxxxxx xxxxxxxxx Xxxxx (hůlkovým písmem): Xxxxxxxxxxx a xxxxx: Xxxxx: Xxxxxx: Xxxxxxx: |
|
7) |
Xxxxxxxx 20 xx xxxxxxxxx xxxxx: „XXXXXXXX 20 Xxxx xxxxxxxxxx Xxxxxxxxxx x&xxxx;xxxxxx do Xxxxxxxx xxxx xx xxxxxxx xxxx x&xxxx;x&xxxx;xxxxxxxx xxxx xxxx xxxxx (2) týkající xx xxxxxxxxxxxx určených xxx xxxxxx léčivých xxxxxxxxx, xxxxxxxxxxxxx xxxxxxxx přípravků, xxxxxxxxxxxxxx xxxxxxxxxx xxx xxxxxxxx x&xxxx;xxxxxxxxxxx účely, xxxxxxxxx implantabilních xxxxxxxxxxxxxx xxxxxxxxxx, diagnostických xxxxxxxxxxxxxx xxxxxxxxxx xx xxxxx xxx xxxxxxxx x&xxxx;xxxxxxxxxxx xxxxx, xxxxxxxxxxxxx činidel x&xxxx;xxxxxxxxxxxx xxxxxxxxxx  &xxxx;Text obrazu &xxxx;Text obrazu
XXXX: Xxxxxxxxxxx osvědčení xx XX Xxxx X: Xxxxxxxxxxx x odeslané xxxxxxx X.1. Xxxxxxxxxx Xxxxx Xxxxxx Xxx. X.2. Xxxxx xxxxxxx xxxxxxxxx X.2.x. X.3. Příslušný xxxxxxxx orgán I.4. Příslušný xxxxxx orgán I.5. Xxxxxxxx Xxxxx Xxxxxx XXX Xxx. X.6. Xxxxx xxxxxxxxxx za xxxxxxx x EU Jméno Adresa PSČ Tel. I.7. Xxxx xxxxxx Xxx XXX X.8. Xxxxxx xxxxxx Xxx X.9. Xxxx xxxxxx Xxx XXX X.10. Xxxxxx xxxxxx Xxx X.11. Xxxxx původu Název Xxxxx schválení Adresa Název Xxxxx xxxxxxxxx Xxxxxx Xxxxx Xxxxx xxxxxxxxx Xxxxxx X.12. Xxxxx xxxxxx Xxxxx xxxxx Xxxxx Xxxxx xxxxxxxxx Xxxxxx XXX X.13. Místo xxxxxxxx X.14. Xxxxx xxxxxxx X.15. Xxxxxxxx xxxxxxxxxx Xxxxxxx Plavidlo Xxxxx Xxxxxxxx vozidlo Ostatní Identifikace Odkaz xx xxxxxxxx X.16. Xxxxxxx xxxxxxxxxx xxxxxxxx kontroly XX X.17. X.18. Xxxxx xxxxx X.19. Xxx xxxxx (xxx XX) X.20. Množství I.21. Teplota xxxxxxxx Xxxxxx Chlazené Xxxxxxxx X.22. Xxxxx xxxxxx X.23. Číslo xxxxxx/xxxxxxxxxx X.24. Xxxx xxxxx  Text obrazu Text obrazu
X.25. Xxxxx xxxxxxxxx xxx: Xxxxxxxxx xxxxxxx X.26. Xxx xxxxxxx xxxx EU xx xxxxx xxxx Xxxxx xxxx Xxx XXX X.27. Xxx dovoz nebo xxxxxx do XX X.28. Xxxxxxxxxxxx xxxxx Xxxxx xxxxxxxxx xxxxxxxx Xxxx (xxxxxxx xxxxx) Xxxxxxx xxxxx Xxxxx hmotnost Číslo xxxxx  Text obrazu Text obrazu
XXXX Xxxxxxxxxxxx určené xxx xxxxxx xxxxxxxx přípravků, xxxxxxxxxxxxx xxxxxxxx přípravků, xxxxxxxxxxxxxx xxxxxxxxxx pro xxxxxxxx x xxxxxxxxxxx xxxxx, xxxxxxxxx xxxxxxxxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxxx, xxxxxxxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxxx in xxxxx pro lékařské x xxxxxxxxxxx účely, xxxxxxxxxxxxx xxxxxxx x xxxxxxxxxxxx prostředků II. Zdravotní xxxxxxxxx XX.x. Číslo xxxxxxx xxxxxxxxx XX.x. XXXXXXXXXX Xx, níže xxxxxxxxx, xxxxxxxxxx, že výše xxxxxxx xxxxxxxxxxx xx xxxxx x dovozu xx Xxxxxxxx xxxx xxxx x tranzitu xxxx xxxxx Xxxxxxxx xxxx a xx xxxxxxxx xxxxxxxx x xxxxxxx I xxxx 35 xxxxxxxx Komise (XX) x. 142/2011(1x) x xxxxxxx že: 1) xx xxxxx pro xxxxxx: (2) buď [- xxxxxxxx xxxxxxxxx,] (2) x/xxxx [- veterinárních xxxxxxxx xxxxxxxxx,] (2) a/nebo [- xxxxxxxxxxxxxx xxxxxxxxxx pro xxxxxxxx x veterinární xxxxx,] (2) x/xxxx [- xxxxxxxxx xxxxxxxxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxxx,] (2) a/nebo [- xxxxxxxxxxxxxx zdravotnických xxxxxxxxxx xx xxxxx xxx xxxxxxxx x veterinární xxxxx,] (2)x/xxxx [- laboratorních xxxxxxx,] (2) x/xxxx [- xxxxxxxxxxxx xxxxxxxxxx;] 2) xxxx xxxx xxxxxx, xxxxxxxxxx x xxxxxx byly xxxxx xxxxxxxxx, a xx xxxx možné xxxxxxxxxxx materiál přímo xxxx xxxx xxxxxx xxxxxxxx určeného x xxxxxxxxx xxxxx, xxxxxxxx xxxx další xxxxxxx xxxx xxxxxxxxxxxxxx xxxxx, xxxx je míšení, xxxxxxxxxx, xxxxxxxxx xxxx xxxxxx, xxx xxx xxxxxxxxx x uvedení xx xxx nebo xx provozu xxxx xxxxxx xxxxxxxxx, xxxxxxxxxxx xxxxxx xxxxxxxxx, zdravotnický xxxxxxxxxx pro lékařské x xxxxxxxxxxx xxxxx, xxxxxxx implantabilní xxxxxxxxxxxx xxxxxxxxxx, xxxxxxxxxxxx xxxxxxxxxxxx xxxxxxxxxx xx xxxxx xxx xxxxxxxx x xxxxxxxxxxx účely xxxx xxxxxxxxxx xxxxxxxxxx x xxxxxxx x právními xxxxxxxx Evropské unie (1x), které xx xx xxxx produkty xxxxxxxx, xxxx xxxx xxxxxxxxxxx xxxxxxx; 3) xxx xxxxxx z: (2) xxx [- xxxxxxxxx, jenž xxxx pocházet ze xxxxxx, xxxxx byla xxxxxxxxx nezákonnému xxxxxxxx xxxxx definice v xx. 1 odst. 2 xxxx. x) xxxxxxxx Xxxx 96/22/XX (2x) xxxx x xx. 2 xxxx. x) směrnice Rady 96/23/XX (2x);] (2) a/nebo [- těla poražených xxxxxx a xxxxxx xxxxx, xxxx x xxxxxxx zvěře xxxx xxxxxxxxxx xxxxxx nebo xxxxxx části, xxxxx xxxx xxxxx xxxxxxxx xxxxxxxx Xxxx xxxxxx x xxxxxx spotřebě, xxxxx z xxxxxxxxxx xxxxxx nejsou x xxxxxx spotřebě xxxxxx;] (2) x/xxxx [- jatečně xxxxxxxx xxxx a xxxx xxxxxxx části xxxxxxxxxxx xxx ze xxxxxx, xxxxx xxxx xxxxxxxx na jatkách x xx xxxxxxxxx xxxx xxxxxxxx xxxx xxxxxxxx jako xxxxxxxxx x porážce k xxxxxx spotřebě, nebo xxxx x xxxx xxxxxxx části xxxxx xxxxxxxx x lidské xxxxxxxx v xxxxxxx x xxxxxxxx xxxxxxxx Xxxx: x) xxxxxxx upravená xxxx xxxx xxxx xxxxxx a jejich xxxxx, které xxxx x xxxxxxx x xxxxxxxx předpisy Unie xxxxxxxxxx za nevhodné x xxxxxx spotřebě, xxxxx xxxxxxxxxxxx xxxxx xxxxxxxx onemocnění xxxxxxxxxx xx xxxxxxx nebo xxxxxxx; xx) xxxxx drůbeže; iii) xxxx x kožky, xxxxxx xxxxxx xxxxxxx x xxxxxx, rohy x xxxxxxxxx, xxxxxx xxxxxx xxxxx, xxxxxxxxxx x xxxxxxxxxx xxxxxx, xxxxx x zánártí, xxxxxx xxxxxx než xxxxxxxxxxx; xx) xxxxxxx štětiny; v) xxxx;] Xxxx II: Xxxxxxxxx  Text obrazu Text obrazu
XXXX Xxxxxxxxxxxx určené xxx xxxxxx xxxxxxxx xxxxxxxxx, xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx, xxxxxxxxxxxxxx prostředků xxx xxxxxxxx x veterinární xxxxx, xxxxxxxxx implantabilních xxxxxxxxxxxxxx xxxxxxxxxx, xxxxxxxxxxxxxx xxxxxxxxxxxxxx prostředků xx xxxxx pro xxxxxxxx x xxxxxxxxxxx xxxxx, xxxxxxxxxxxxx činidel x xxxxxxxxxxxx xxxxxxxxxx XX. Xxxxxxxxx xxxxxxxxx XX.x. Číslo xxxxxxx xxxxxxxxx XX.x. (2) x/xxxx [- xxxx xxxxxx xxxxxx xxx xxxxxxxxxxx, která xxxxxxxxxxxx xxxxx příznaky xxxxxxxxxx xxxxxxxxxx xxxx xx xxxxxxx xxxx xxxxxxx, xxxxx xxxx xxxxxxxx xx xxxxxxx x která xxxx xx xxxxxxxxx xxxx xxxxxxxx xxxxxxxx vhodnými xxx účely xxxxxxx x xxxxxx xxxxxxxx x xxxxxxx s xxxxxxxx xxxxxxxx Xxxx;] (2) x/xxxx [- xxxxxxxx xxxxxxxx xxxxxxxxxxx původu, xxxxx vznikají xxx xxxxxx xxxxxxxx určených x lidské xxxxxxxx, xxxxxx xxxxxxxxxxx kostí, xxxxxxx nebo kalu x xxxxxxxxxxx xxxx xxxxxxxxxx ze xxxxxxxxxx xxxxx;] (2) x/xxxx [- xxxxxxxx xxxxxxxxxxx původu xxxx xxxxxxxx xxxxxxxxxxxx xxxxxxxx xxxxxxxxxxx původu, xxxxx x xxxxxxxxxx xxxxxx xxxx x xxxxxx xxxxxxxx způsobených xxxxxxxxx xxxxxx, xxxxxx xxxxxx xxxx jinými xxxxxxxx, x nichž xxxxxxxx xxxxx riziko xxx xxxxxx lidí xxx xxxxxx, xxx xxxxxx xxxxxx x xxxxxx spotřebě;] (2) x/xxxx [- xxxxx xxx xxxxxxx x xxxxxxxx xxxxx x xxxxx xxxxxxxxxxx xxxxxx xxxx xxxxx obsahujících xxxxxxxx xxxxxxxx živočišného původu xx získané xxxxxxxx, xxxxx x xxxxxxxxxx xxxxxx xxxx x xxxxxx problémů xxxxxxxxxxx xxxxxxxxx vadami, xxxxxx xxxxxx xxxx jinými xxxxxxxx, x xxxxx xxxxxxxx žádné xxxxxx xxx xxxxxx xxxx xxx zvířat, xxx xxxxxx xxxxxx ke xxxxxx;] (2) x/xxxx [- xxxx, placenty, xxxx, xxxx, srsti, xxxx, xxxxxxx xxxxx x xxxxxxxx x xxxxxxxx xxxxx xxxxxxxxxxxxx xx xxxxxx xxxxxx, která xxxxxxxxxxxx xxxxx xxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxx xxxxxxxxx xx xxxxxxx xxxx xxxxxxx;] (2) x/xxxx [- vodní xxxxxxxxxxx x jejich xxxxx, xxxxx mořských savců, xxxxx xxxxxxxxxxxx žádné xxxxxxxx xxxxxxxxxx přenosných xx xxxxxxx xxxx xxxxxxx,] (2) x/xxxx [- xxxxxxxxxx xxxxxxxx živočišného xxxxxx x vodních xxxxxxxxx pocházejících z xxxxxxx xxxx zařízení xx xxxxxx xxxxxxxx xxxxxxxx k xxxxxx xxxxxxxx;] (2) x/xxxx [- xxxx xxxxxxxxx materiálu xxxxxxxxxxxxx xx xxxxxx, xxxxx xxxxxxxxxxxx xxxxx xxxxxxxx onemocnění přenosného xxxxx xxxxxxxxxx xx xxxxxxx xxxx zvířata: i) xxxxx xxxxxxx x xxxxxx x měkkými xxxxxxx xxxx xxxxx; xx) xxxxx xxxxxxxx xxxxxxxxxxx xx suchozemských xxxxxx: — xxxxxxxx produkty z xxxxx, — xxxxx, — vedlejší xxxxxxxx z vajec, xxxxxx vaječných skořápek; iii) xxxxxxxxxx kuřata xxxxxxxx x obchodních xxxxxx;] (2) x/xxxx [- xxxxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx x vodních nebo xxxxxxxxxxxxx xxxxxxxxxxxx živočichů, xxxxx xxxxx xxxxxxxxxxx xxx člověka nebo xxxxxxx;] (2) x/xxxx [- xxxxxx z xxxx xxxxxxxx (Xxxxxxxx) x xxxxxxxxx (Xxxxxxxxxx) x xxxxxx části, xxxxx xxxxxxxxx xxxxxxxxx 1 xxxxxxxxx v xx. 8 xxxx. a) xxxxxx iii), iv) x x) a xxxxxxxxx kategorie 2 xxxxxxxxx x xx. 9 xxxx. x) xx g) xxxxxxxx (XX) č. 1069/2009;] (2) x/xxxx [- produktů xxxxxxxxx x těchto xxxxxxxxx nebo těmito xxxxxxxxx vytvořených: — xxxxx xxxxxxxxxxx x xxxxxx xxxxx, xxxxx xxxxxxxx xxxxx, kteří xxxxxxxxxxxx xxxxx xxxxxxxx onemocnění xxxxxxxxxx na člověka xxxx xxxxxxx, — vodní xxxx suchozemští bezobratlí xxxxxxxxxxx, xxxxx xxxxx xxxxxxxxxxx pro xxxxxxx xxxx xxxxxxx, — xxxxxxx x xxxx hlodavců (Xxxxxxxx) a xxxxxxxxx (Xxxxxxxxxx) x jejich xxxxx, xxxxx xxxxxxxxx xxxxxxxxx 1 xxxxxxxxx x xx. 8 xxxx. a) xxxxxx xxx), xx) x x) x xxxxxxxxx xxxxxxxxx 2 xxxxxxxxx x čl. 9 xxxx. x) xx x) xxxxxxxx (ES) x. 1069/2009;]  Text obrazu Text obrazu
ZEMĚ Meziprodukty xxxxxx xxx xxxxxx xxxxxxxx xxxxxxxxx, veterinárních xxxxxxxx přípravků, xxxxxxxxxxxxxx xxxxxxxxxx xxx lékařské x veterinární xxxxx, xxxxxxxxx xxxxxxxxxxxxxxx zdravotnických xxxxxxxxxx, xxxxxxxxxxxxxx zdravotnických xxxxxxxxxx in xxxxx xxx xxxxxxxx x xxxxxxxxxxx účely, laboratorních xxxxxxx x xxxxxxxxxxxx xxxxxxxxxx XX. Xxxxxxxxx xxxxxxxxx XX.x. Xxxxx jednací xxxxxxxxx XX.x. (2) x/xxxx [- xxxxxx x xxxxxx xxxxx, xxxxx xxxxxx x xxxxxx xxxxx xxxxxxxxx x xxxxxx 8 xxxx 10 xxxxxxxx (XX) x. 1069/2009: x) xxxxxxx, xxxxx uhynula xxxxx xxx xxxxxxxx xxxx usmrcením k xxxxxx spotřebě, xxxxxx xxxxxx xxxxxxxxxx xx xxxxxx tlumení nákazy; ii) xxxxx; xxx) oocyty, xxxxxx x xxxxxx, xxxxx xxxxxx xxxxxx k xxxxxxx xxxxxx; x xx) xxxxxx xxxxxxxx xx xxxxx;] (2) x/xxxx [- xxxxxxxxxx produktů živočišného xxxxxx xxxxxx xxx xxxxxxxx xxxxxxxxx 1 xxxx materiál xxxxxxxxx 3;] 4) xxxx vnější xxxx xx xxxxxxx xxxxxxx „POUZE XXX XXXXXX XXXXXXXXX / XXXXXXXXXXX LÉČIVÉ XXXXXXXXX / XXXXXXXXXXXX XXXXXXXXXX XXX LÉKAŘSKÉ X XXXXXXXXXXX XXXXX / XXXXXXX IMPLANTABILNÍ XXXXXXXXXXXX XXXXXXXXXX / DIAGNOSTICKÉ XXXXXXXXXXXX XXXXXXXXXX XX XXXXX PRO XXXXXXXX X VETERINÁRNÍ XXXXX / XXXXXXXXXXX ČINIDLA / XXXXXXXXXX XXXXXXXXXX“ x xxxx v xxxxx xxxx xxxxx x žádnému xxxxxx xxxxxxx x xxxxx Xxxxxxxx unie; 5) xxxxxxx xxxx xxxxxxxxx xxxxx xx xxxxx určení x Xxxxxxxx unii xxxxxxx v kolonce X.12. xxxxxx xxxxxxxxxx, xxxxxx je: (2) xxx [xxxxxxxx xxxx xxxxxx xxx xxxxxx xxxxxxxx xxxxxxxxx, veterinárních xxxxxxxx xxxxxxxxx, xxxxxxxxxxxxxx xxxxxxxxxx xxx lékařské a xxxxxxxxxxx účely, xxxxxxxxx xxxxxxxxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxxx, xxxxxxxxxxxxxx zdravotnických xxxxxxxxxx xx xxxxx xxx xxxxxxxx x xxxxxxxxxxx xxxxx, xxxxxxxxxxxxx činidel xxxx xxxxxxxxxxxx xxxxxxxxxx, xxxxx(x) xxx(x) registrován(o) x xxxxxxx x xxxxxxx 23 nařízení (XX) x. 1069/2009,] (2) xxxx [xxxxxxxx nebo xxxxxx, xxxxx(x) xxx(x) xxxxxxxx(x) v souladu x xx. 24 xxxx. 1 xxxx. x) nařízení (XX) x. 1069/2009, odkud xxx být xxxxxxxx xxxxx xx zařízení xxxx xxxxxxx xxxxxxxxx x předchozí xxxxxxx xxxxxx xxxx.] Xxxxxxxx — Xxxxxxx X.19.: Použijte xxxxxxxxx xxx xxxxxxxxxxxxxxx xxxxxxx (XX) x xxxxxxx x xxxxxxxxxxx Komise 2007/275/XX ze dne 17. xxxxx 2007 x seznamech zvířat x xxxxxxxx, xx xxx xx xxxxxxxx xxxxxxxx xx xxxxxxxxxxxx xxxxxxxx xxxxxxxx xxxxx xxxxxxx Rady 91/496/EHS x 97/78/ES (Xx. xxxx. X 116, 4.5.2007, x. 9). — Xxxxxxx I.25.: Xxxxxxxxx xxxxxxx: xxxxxxxx jiné xxxxxxx kromě xxxxxx xxxxxx. (1x) Xx. věst. X 54, 26.2.2011, x. 1. (1b) Směrnice Xxxxxxxxxx xxxxxxxxxx a Xxxx 2001/82/ES xx xxx 6. listopadu 2001 x kodexu Xxxxxxxxxxxx xxxxxxxxx se xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx (Xx. xxxx. X 311, 28.11.2001, s. 1), xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Xxxx 2001/83/XX xx xxx 6. xxxxxxxxx 2001 x kodexu Xxxxxxxxxxxx xxxxxxxxx xx xxxxxxxxx xxxxxxxx xxxxxxxxx (Úř. xxxx. L 311, 28.11.2001, s. 67), xxxxxxxx Xxxx 93/42/XXX xx xxx 14. xxxxxx 1993 o xxxxxxxxxxxxxx prostředcích (Xx. xxxx. L 169, 12.7.1993, x. 1), xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Xxxx 98/79/ES xx dne 27. xxxxx 1998 o xxxxxxxxxxxxxx xxxxxxxxxxxxxx prostředcích xx xxxxx (Xx. xxxx. X 331, 7.12.1998, x. 1), xxxxxxxx Xxxxxxxxxx parlamentu x Xxxx (XX) x. 1223/2009 xx xxx 30. xxxxxxxxx 2009 o kosmetických xxxxxxxxxxx (Xx. xxxx. X 342, 22.12.2012, x. 59), podle xxxxxxx. (2) Xxxxxxxx xx xxxxxxxx. (2x) Úř. věst. X 125, 23.5.1996, x. 3. (2b) Xx. xxxx. X 125, 23.5.1996, s. 10. Xxxxxxx Xxxxx (xxxxxxxx xxxxxx): Xxxxxx: Xxxxx: Xxxxxx: |


