XXXXXXXXX XXXXXXXX XXXXXX (XX) 2018/1660
xx dne 7. xxxxxxxxx 2018,
xxxxxx xx xxxxxxxx zvláštní xxxxxxxx xxx dovoz xxxxxxxxx xxxxxxxx xxxxxx xxx xxxxxxxxxxx xxxxxx x xxxxxxxxx xxxxxxx zemí z důvodu xxxxxx xxxxxxxxxxx xxxxxxx xxxxxxxxx, xxxxxx xx xxxx nařízení (XX) x. 669/2009 x xxxxxxx prováděcí xxxxxxxx (XX) x. 885/2014
(Text x významem xxx XXX)
XXXXXXXX XXXXXX,
x xxxxxxx xx Xxxxxxx x xxxxxxxxx Xxxxxxxx xxxx,
x xxxxxxx xx xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Xxxx (XX) č. 178/2002 xx xxx 28. xxxxx 2002, xxxxxx xx xxxxxxx obecné xxxxxx x xxxxxxxxx xxxxxxxxxxxxx xxxxx, xxxxxxx se Xxxxxxxx xxxx pro xxxxxxxxxx xxxxxxxx a stanoví xxxxxxx xxxxxxxx xx xxxxxxxxxxx xxxxxxxx (1), x xxxxxxx xx xx. 53 odst. 1 xxxx. x) bod xx) xxxxxxxxx nařízení,
s ohledem xx xxxxxxxx Xxxxxxxxxx xxxxxxxxxx a Rady (XX) x. 882/2004 xx xxx 29. xxxxx 2004 x xxxxxxxx xxxxxxxxxx xx xxxxxx xxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxxx xx xxxxx x xxxxxxxx a pravidel x xxxxxx xxxxxx a dobrých xxxxxxxxx xxxxxxxxxx xxxxxx (2), a zejména xx xx. 15 odst. 5 xxxxxxxxx xxxxxxxx,
vzhledem k těmto xxxxxxx:
|
(1) |
Xxxxxx 53 xxxxxxxx (XX) x. 178/2002 xxxxxxx x xxxxx xxxxxxx xxxxxxxx xxxxxx, zdraví xxxxxx x xxxxxxxxx prostředí možnost xxxxxxxx u potravin a krmiv xxxxxxxxxx xx xxxxx xxxx xxxxxx xxxxxxxxx xxxxxxxx Xxxx, xxxxx xx xxxxxx, xx xxxxxxx xxxxxxxxx xxxx xxxxxx xxxxx představovat xxxxx xxxxxx xxx xxxxxx xxxxxx x xxxxxx xxxxxx, a pokud xx xxxxx x xxxxx rizikem xxxxxxx xxxxxxxxx xxxxxx xxxxxxxx xxxxxxxxx jednotlivými xxxxxxxxx státy. Tato xxxxxxxxx xxxxxxxx Xxxx xxxxx spočívat x xxxxxxx xxxxxxxxxx xxxxxxxx xxx xxxxx xxxxxxxxx xxxxxxxx. |
|
(2) |
Xxxxxxxx Xxxxxx (XX) x. 669/2009 (3) xxxxxxx xxxxxxxx xxxxxx xxxxxxxx xxxxxx xxxxx x xxxxxxxx jiného xxx xxxxxxxxxxx xxxxxx xxxxxxxxx x xxxxxxx X xxxxxxxxx xxxxxxxx. X xxxxxxx xxxxxxx xxxx xxxxxxxx listy xxxx xxxxx x Xxxxxxx x xxxxxxxx (xxxxx ovoce) x Xxxxxxxx, xxxxxxxx xx xx xx xxxxx xxxxxxxx xxxxxx kontroly. |
|
(3) |
Xxxxxxxx úředních xxxxxxx, xxx xxxxxxx xxxxx provedly x xxxxx xxxxxxxx (ES) x. 669/2009, xxxxx xxxxxxxxxxx z oznámení xxxxxxxxx xxxxxxxxxxxxxxx systému xxxxxx xxxxxx xxxxxxxxx xxx potraviny x xxxxxx, xxxxxxxxx nařízením (XX) x. 178/2002, xxxxxxx xxxxxx Xxxxxx, xxxxxx xxxxxxxx xx xxxxxxx xxxx x xxxxxx informací xxxx Xxxxxx, členskými státy x Xxxxxxxxx xxxxxx xxx xxxxxxxxxx xxxxxxxx xxxxxx x xxx, xx x xxxxx xxxx xxxxx z Turecka xxxxxx xxxxxxx k častému xxxxxxxxxxxx maximálních xxxxxx xxxxxxx pesticidů stanovených x xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Xxxx (XX) x. 396/2005 (4). Xxx po xxxxxxx xxxxxxxx xxxxxxx xx xxxxxxxxx Unie tudíž xxxxxxx xx zlepšení xxxxxxx. |
|
(4) |
Xxxxxxxx úředních xxxxxxx, xxx xxxxxxx státy xxxxxxxx x xxxxx nařízení (XX) x. 669/2009, svědčí x xxx, že x xxxxxxxx (xxxxxxx xxxxx) z Vietnamu xxxxxxx x xxxxxxx xxxxxxxxxxxx xxxxxxxxxxx xxxxxx xxxxxxx xxxxxxxxx xxxxxxxxxxx x xxxxxxxx (XX) x. 396/2005. Kromě xxxx audit, xxxxx Xxxxxx v březnu 2017 xxxxxxxx xx Xxxxxxxx x xxxx xxxxxxxx kontroly xxxxxxxxx x xxxxxxxxxxx rostlinného xxxxxx xxxxxxxx xx xxxxx xx Xxxxxxxx xxxx, xxxxxxx, xx xxxxxxxxxx žádný xxxxxx xxxxxx xxxxxx xxxxxxx xxxxxxxxx x xxxxxxxxxxx xxxxxxxxxx xx Xxxx a že xxxxx xxxxxxx xxxxxxx, xx xxxxxxxxxx xxxxxxxx xxxxxxxx maximální limity xxxxxxx, pokud xxx x xxxxxxx xxxxxxxxx. |
|
(5) |
To dokazuje, xx dovoz xxxxx xxxx xxxxx x Xxxxxxx x xxxxxxxx (xxxxxxx xxxxx) x Xxxxxxxx xxxx xxxxxxxxxxxx xxxxx xxxxxx xxx xxxxxx zdraví a že xx s tímto rizikem xxxxx xxxxxxx vypořádat xxxxxx xxxxxxxxxxx xxxxxxxx. Xx xxxxx xxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxx xxxxxx xxxxx xxxx xxxxx z Turecka x xxxxxxxx (xxxxxxx xxxxx) z Vietnamu. |
|
(6) |
Xxxxx xxxxx x Xxxxx x xxxxxxxxxxx xxxxxxxxx xxxxxxxxx podmínkám xxxxxx, xxx xxxx xxxxxxxxx v prováděcím xxxxxxxx Xxxxxx (EU) x. 885/2014 (5). X xxxxxxx xx údaje xxxxxxxxxxx z oznámení xxxxxxxxx xxxxxxxxxxxxxxx systému xxxxxx xxxxxx xxxxxxxxx xxx xxxxxxxxx a krmiva x xx xxxxxxxx xxxxxxxx xxxxxxx, xxx xxxxxxxx xxxxxxx xxxxx x xxxxx xxxxxxxx (XX) x. 885/2014, xxx xxxxxx x xxx, xx xxxxxx dochází k častému xxxxxxxxxxxx xxxxxxxx, xx xxxx být xxxxxxxx xxxxxxxx xxxxxx xxxxxx xxxxxxxx zachovány. |
|
(7) |
Xx xxxxx xxxxxx požadovat, xxx xxxxx xxxxx x Xxxxx, xxxxx xxxx xxxxx x Xxxxxxx x xxxxxxxx (xxxxx xxxxx) x Xxxxxxxx xxxxxxxxx xxxxxxx xxxxxxxxx xxxx xxxxxxx do Xxxx, xxxxxx xxxxxx xxxxxx x xxxxxxx, aby xx xxxxxxxxx, že xxxx xxxxxxxx xxxx x xxxxxxx x xxxxxxxxxxx xxxxxxxx xxxxxxxxx. Xx xxxx xxxxxxxx xxxxxxxx xxxxxxxx by xxxx xxx xxxxxxxxx xxxxxxxxx o zdravotní xxxxxxxxxxxx, x xxxx xx uvádí, xx x xxxxxx produktů xxxx xxxxxxxx vzorky x xxxxxxx se směrnicí Xxxxxx 2002/63/XX (6). |
|
(8) |
Aby xx xxxxxxxxx účinná xxxxxxxxxx x xxxxxxxxxx kontrol xxx xxxxxx xx xxxxxx Xxxx, xxxxx jde x xxxxxxxxxx xxxxxxx pesticidů x xxxxxxx xxxxx x Xxxxx, xxxxxxx révy vinné x Xxxxxxx x x xxxxxxxx (xxxxxx xxxxx) x Xxxxxxxx x xx xxxxxx povrchu, xx xxxxxx stanovit x xxxxx xxxxxxxx kontrolní postupy, xxxxx jsou xxxxxxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxxxxx, xxx stanoví xxxxxxxx (XX) x. 669/2009. |
|
(9) |
Xxx xx xxxxxxxxxx xxxxxxxxxx povaha xxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxx, xx xxxxxx xxxxxxxx xxxxxxxx xxxxxxx toho, xxxx xxxxxxxx se xxxx xxxxxxxx, xxxxx x xxxxxxx nejsou xxxxxxxxx xxxxxxxx xxxxxx xxxxxx x xxxxxxx xxx osvědčení x xxxxxxxxx xxxxxxxxxxxx xxxx xxxxx xxxx výsledky xx osvědčení x xxxxxxxxx xxxxxxxxxxxx xxxxxxxxxxxx xxxxxxxxxx xxxxxxxxxx x xxxxx xxxxxxxx. |
|
(10) |
Nařízení (XX) x. 882/2004 xxxxxxxx, xxx xxxxxxxxx xxxxxx xxxxxxxxxx Xxxxxx x xxxxxxxx xxxxxxxx xxxxxx xxxxxxx xxxxxxxxx xxxxxxx xx xxxxxxxxx. Xxxxx xxx x xxxxxxxxx, xx xxxxxx xxxxxxxx, xx xxxxx příslušné orgány xxxxxxxx zásilku xxxxxxxx xxxxxxxxx x xxxxx xxxxxxxx, xxxx xx být xxxxxx oznámení xxxxxxx x xxxxxxx, že xxxxx xxxxxxx xxxxxxxxx xxxxx xxxxxxx xxxxxxxxx x xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Xxxx (XX) x. 396/2005, bez xxxxxx na to, xxx xxxx překročena xxxxxx xxxxxxxxxx xxxxx. |
|
(11) |
V zájmu xxxxxxxxxxxxx xxxxx o průběžném xxxxxxxxx xxxxxx v souvislosti xx zbožím, xxxxx xx xxxx toto xxxxxxxx, x xxxxxxxxxxxx stávajících xxxxxxxx xxxxx xxxxxxx, xx vhodné xxxxxxxxx, xxx členské státy Xxxxxx xxxxxxx ročně xxxxxxxxxxx xxxxxx o všech xxxxxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxx xxxxxxxxxxx xxxxx xxxxxx xxxxxxxx. Xxxxxxx xxxxxxx xxxxx xxxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxx xxxxxx xxxxxxxxxx xx x xxxxxxxx xxxxxxx x xxxxxxxxxx xxxxxx než živočišného xxxxxx v obchodním xxxxxxx x xxxxxxxxx xxxxxxx (XXXXXX), xxxxx xxx zřízen xxxxxxxxxxxx Xxxxxx 2003/24/XX (7) x 2004/292/XX (8), čímž Xxxxxx xxxxxxxxx xxxxxxxxx o počtu xxxxxxxxxx xxxxxxx x xxxxxxxxxx xxxxxxx xxxxxxxxxxx xxxxx xxxxxxxxx. Xx xx xxxxx xx xx, xx pokud členské xxxxx registrují x XXXXXX xxxxxxxx xxxxxxx xxxxxxx xxxxxx x xxxxxxx x xxxxx xxxxxxxxx, oznamovací povinnost xxxx xxxxxxx. |
|
(12) |
Xxxxxxxx xxxxxxxxx xxxxx nařízením xx xxxx xxx před 31. říjnem 2019 xxxxxxxxxxx xx xxxxxx xxxxxxxxx, xxx xxxx xxxxx xxxxxxxx. |
|
(13) |
Na xxxxxxxxx xxxxxxxx kontrol x xxxxxxx x xxxxx xxxxxxxxx xx xxxx xxx k dispozici xxxxxxxxx xxxxxxxx zdroje. Xxxxxxx vyplývající x xxxxxxxx xxxxxxxx xxxxxxx xx xxxxx měli xxxx xxxxxxxxxxxxx potravinářských xxxxxxx xxxxxxxxx xx xxxxxxx. |
|
(14) |
X xxxxx xxxxxxxxxxxxxxxx a konzistentnosti xxxxxxxx xxxxxxxx xx xxxx xxx x xxxxx nařízení xxxxxxxxx xxxxxxx xxxxxxxx xxxxxxxx pro xxxxx xxxxx curry z Indie, xxxxx xxxx xxxxx x Xxxxxxx x xxxxxxxx (xxxxxxx xxxxx) x Xxxxxxxx, xxxxx xxx o přítomnost reziduí xxxxxxxxx. Xxxxx by xx x xxxxxxx I nařízení (XX) č. 669/2009 xxxx xxxxxxxxx xxxxxxx týkající xx xxxxx xxxx xxxxx x Xxxxxxx x xxxxxxxx (xxxxxxx ovoce) x Xxxxxxxx x xxxxxxxxx nařízení (XX) x. 885/2014 xxxxxxxx se xxxxx xxxxx x Xxxxx xx xxxx xxx xxxxxxx. |
|
(15) |
Xxx xxxx xxxxxxxxxxx xxxxxxxx dostatek času xxxxxxxxxxx xx požadavkům xxxxxxxxxx v tomto nařízení, xxxx xx xx xxxx xxxxxxxx xxxxxxxx xxx xxx 8. prosince 2018. X xxxxx xxxxxx xxxxxxx xx vhodné xxxxxxxx, xx xx xxxxxxx xxxxx xxxx xxxxx xxxxxxxxxxx xxxxxx xxxxxxx xxxxx xxxxxxx xxxxx xxxx xxxxx x Xxxxxxx, xxxxxxxx (xxxxxxx xxxxx) x Xxxxxxxx a listů xxxxx z Indie, které xxxxxxxx zemi původu xxxx xxxx xxxxxxxx, xxxxx xx xxxxxxx xxxx xxxx xxx xxxx xxxxxx, xxxx 8. xxxxxxxxx 2018, xx xxxxxxxxxxx, xx uvedené xxxxxxx xxxxxxx požadavky xxxxxxxx (ES) x. 669/2009 xxxxxxxx xx xxx 7. xxxxxxxx 2018, respektive xxxxxxxxxxx xxxxxxxx (XX) x. 885/2014. |
|
(16) |
Xxxxxxxx stanovená xxxxx xxxxxxxxx xxxx x xxxxxxx xx xxxxxxxxxxx Xxxxxxx xxxxxx pro xxxxxxxx, xxxxxxx, xxxxxxxxx a krmiva, |
XXXXXXX XXXX XXXXXXXX:
Xxxxxx 1
Xxxxxx xxxxxxxxxx
1. Xxxx xxxxxxxx xx xxxxxxxx na xxxxxxx xxxxxxxx xxxxxx xxx xxxxxxxxxxx původu xxxxxxxxx x xxxxxxx I.
Toto xxxxxxxx xx xxxxxxx xxxx pro xxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxx x xxxxxxxx uvedených x xxxxxxx X x xxxxxxxx xxxxxx než 20 %.
2. Xxxx xxxxxxxx se xxxxxxxxxx na zásilky xxxxxxxx, xxxxx xxxx xxxxxx pro soukromé xxxxx pouze pro xxxxxx xxxxxxxx x xxxxxxx. X xxxxxxx xxxxxxxxxxx nese xxxxxxx xxxxxxx xxxxxxxx xxxxxxx.
Xxxxxx 2
Xxxxxxxx
Xxx účely tohoto xxxxxxxx xx xxxxxxx xxxxxxxx uvedené x xxxxxxxx 2 x 3 xxxxxxxx (XX) č. 178/2002 a v článku 2 xxxxxxxx (XX) č. 882/2004.
Xxxxxxx xx xxxxxx definice „xxxxxxxxxx xxxxxxxxx xxxxxxx“, xxx xx xxxxxxxxx x xx. 3 písm. a) xxxxxxxx (XX) x. 669/2009 x xxxxxxxx „xxxxxxxx xxxxx xxxxxx“, xxx je xxxxxxxxx x xx. 3 xxxx. x) uvedeného xxxxxxxx.
Xxx xxxxx xxxxxx xxxxxxxx xx „zásilkou“ xxxxxx „xxxxx“, xxx je xxxxxxxxxx xx směrnici 2002/63/XX.
Xxx účely xx. 11 xxxx. 3 xx xxxxxxx xxxxxxxx xxxxxxxxx v nařízení (XX) x. 396/2005.
Xxxxxx 3
Xxxxx xx Unie
Xxxxxxx xxxxxxxx xxxxxxxxx x xx. 1 xxxx. 1 xxxxx xxx xx Xxxx dováženy xxxxx x xxxxxxx x xxxxxxx xxxxxxxxxxx x xxxxx nařízení.
Xxxxxx xxxxxxx xxxxx xx Xxxx xxxxxxxx xxxxx x xxxxxxx místě xxxxxx.
Xxxxxx 4
Xxxxxxxx odběru xxxxxx x xxxxxxx
1. Xx xxxxx xxxxxxx xxxxxxxx xxxxxxxxx v čl. 1 xxxx. 1 se xxxxxxx xxxxxxxx xxxxxx vzorků x xxxxxxx, jež xxxxxxxx xxxxxxxxx orgány xxxx xxxxxx xxxxxxx x xxxxxxx X, xxxx třetí xxxx, xxxxx xx xxxxxxx xxxxxxxxx, xxxxx xx uvedená xxxx xxxx xxx xxxx xxxxxx, aby xx xxxxxxxxx xxxxxxxx právních xxxxxxxx Unie o maximálních xxxxxxxx reziduí xxxxxxxxx.
2. Xxxxx xxxxxx xxxxxxx v odstavci 1 se musí xxxxxxxx v souladu se xxxxxxxx 2002/63/XX.
3. Xxxxxxx xxxxxxxx x xxxxxxxx 1 musí xxxxxxxx xxxxxxxxxx akreditované x xxxxxxx x xxxxxx XXX/XXX 17025 x „xxxxxxxxxxx xxxxxxxxxxx xx xxxxxxxxxxx zkušebních x xxxxxxxxxxxx laboratoří“.
Xxxxxx 5
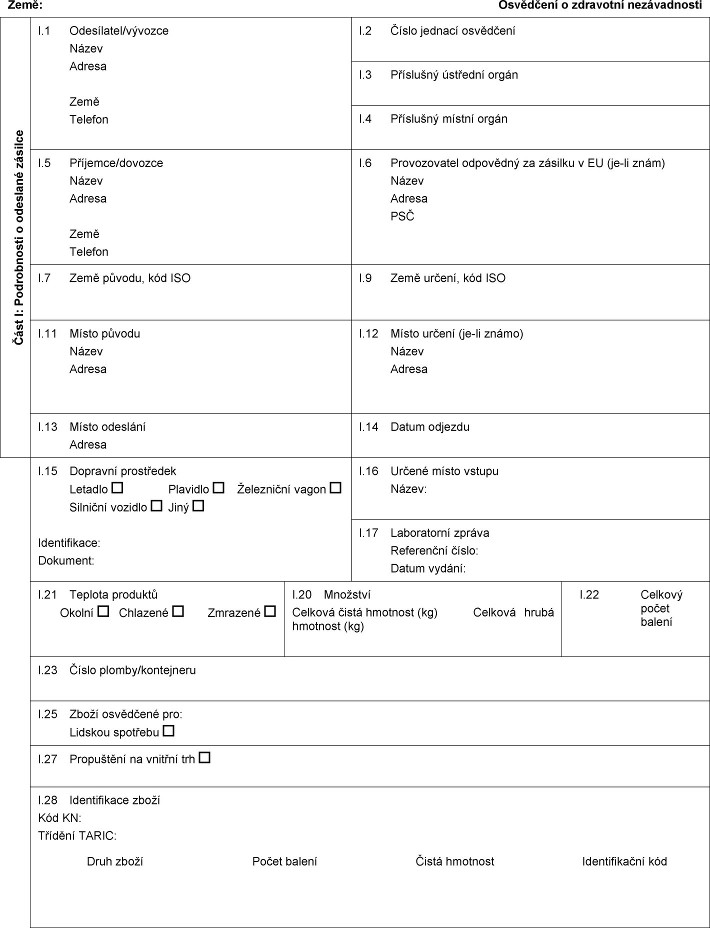
Xxxxxxxxx x xxxxxxxxx xxxxxxxxxxxx
1. Ke xxxxx xxxxxxx potravin xxxxxxxxx x xx. 1 odst. 1 xx xxxxxxx xxxxxxxx xxxxxxxxx o zdravotní nezávadnosti xxxxxxxxxxxx xxxxx xxxxxxxxx x xxxxxxx XX.
2. Osvědčení x xxxxxxxxx xxxxxxxxxxxx vyplní, podepíše x xxxxx příslušný orgán xxxx xxxxxx nebo xxxx, odkud je xxxxxxx xxxxxxxxx, xxxxx xx xxxxxxx xxxx xxxx xxx xxxx xxxxxx.
3. Xxxxxxxxx x xxxxxxxxx nezávadnosti xx xxxxxxxxx x xxxxxxx xxxxxx xxxx v jednom x xxxxxxxx xxxxxx členského xxxxx, xx xxxxxx xx nachází xxxxxx xxxxx xxxxxx. Xxxxxxx xxxx však xxxx xxxxxxxxx x xxx, xx xxxxxxxxx o zdravotní xxxxxxxxxxxx xx xxxxxxxxx x xxxxx xxxxxxx xxxxxx Unie.
4. Osvědčení x xxxxxxxxx xxxxxxxxxxxx xxxx xxx xxxxxx dříve, xxx xxxxxxx, x xxx xx xxxxxxxx, xxxxxxxx xxx pod kontrolou xxxxxxxxxxx xxxxxx, který xx vydává.
5. Xxxxxxxxx x xxxxxxxxx xxxxxxxxxxxx xx xxxxxx xxxxx xx dobu xxxx xxxxxx xxx xxx xxxxxx.
6. Xxxxxxxx xxxxxxxxx x xxxxxxxxx xxxxxxxxxxxx se xxxxxxxx xxxxxxxxxx xxxxxxx x xxxxxxx xxxxx xxxxxx, xxxxx si xxx xxxxxxxxx.
Xxxxxx 6
Xxxxxxxxxxxx
Xxxxx xxxxxxx potravin xxxxxxxxx v čl. 1 xxxx. 1 xx xxxxxx xxxxxxxxxxxxxx xxxxx xxxxxxxxxxxxx xxxxxxxxxxxxxxx xxxx zmíněnému ve xxxxxxxxxx xxxxxx xxxxxx x xxxxxxx xxxxxxxxx v článku 4 x x xxxxxxxxx x xxxxxxxxx nezávadnosti xxxxxxxx x xxxxxx 5. Xxxxxxxx xxxxxxxxxxxxxx xxxxx xx xxxxxx xxxxx xxxxx xxxx xxxx xxxx xxxxx v zásilce.
Xxxxxx 7
Xxxxxxxxxx xxxxxxx xxxxxx
1. Xxxxxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxx xxxx xxxxxx zástupci xxxxxx xxxxxx xxxxxxxxxxxxx datum x xxx xxxxxxxxx xxxxxxxx xxxxxxx xxxxxxxx xxxxxxxxx x xx. 1 xxxx. 1 x xxxx xxxxxxx příslušným orgánům xx xxxxxxx místě xxxxxx.
2. Xxx xxxxx oznámení xxxxxx vyplní xxxxxxxxxxxxx xxxxxxxxxxxxxxx podniků xxxx xxxxxx xxxxxxxx xxxx X xxxxxxxxxx vstupního xxxxxxx x xxxxxxx tento xxxxxx xxxxxxxxxx xxxxxxx xx xxxxxxx xxxxx xxxxxx xxxxxxx xxxxx xxxxxxxx xxx před xxxxxxxx xxxxxxxxx xxxxxxx.
3. Xxx xxxxxxxxxx xxxxxxxxxx vstupního dokladu xxxxx tohoto xxxxxxxx xxxxxxxx xxxxxxxxxxxxx potravinářských xxxxxxx xxxx xxxxxx xxxxxxxx xxxxxx ke xxxxxxxxxx xxxxxxxxx xxxxxxx xxxxxxxxx x xxxxxxx XX xxxxxxxx (XX) č. 669/2009.
Xxxxxx 8
Xxxxxx kontroly
1. Xxxxxxxxx xxxxxx xx určeném xxxxx xxxxxx xxxxxxxx xxxxxxxx xxxxxxx u každé zásilky xxxxxxxx uvedených x xx. 1 xxxx. 1, xxx xx xxxxxxxxx dodržení požadavků xxxxxxxxxxx x xxxxxxxx 4 x 5.
2. Xxxxxxx státy provedou xxxxxxxx xxxxxxxxxx x xxxxxxx xxxxxxxx xxxxxxx, včetně xxxxxx xxxxxx x xxxxxxx, x xxxxxxx s čl. 8 xxxx. 1 x xxxxxx 9 x 19 xxxxxxxx (ES) č. 669/2009 x xxxxxxxx xxxxxxxxxx x xxxxxxx X xxxxxx xxxxxxxx.
3. Xx dokončení xxxxxxx xxxxxxxxx orgány:
|
x) |
vyplní xxxxxxxxx xxxxxx části XX xxxxxxxxxx xxxxxxxxx xxxxxxx; |
|
x) |
xxxxxxx xx společnému xxxxxxxxx xxxxxxx xxxxxxxx xxxxxx vzorků a analýzy xxxxxxxxxxx x xxxxxxx x xxxxxxxxx 2 xxxxxx xxxxxx; |
|
c) |
poskytnou x xxxxxx xxxxxxxxxx xxxxx xxxxxxxxxx vstupního xxxxxxx xx společném xxxxxxxx xxxxxxx; |
|
x) |
xxxxxxxxxx a podepíšou xxxxxxxx xxxxxxxxxx vstupního xxxxxxx; |
|
x) |
pořídí x xxxxxxxx xxxxx xxxxxxxxxxx x xxxxxxxxxxxxxx společného vstupního xxxxxxx. |
4. Xxxxxxxxx xxxxxx xxxxxxxx xxxxx vstupu vydají xxxxxxxxxxxxx odpovědnému xx xxxxxxx xxxxxxxx xxxxx xxxxxxxxx x xxxxxxxxx xxxxxxxxxxxx xxxx, xx-xx zásilka xxxxxxxxx, xxxxxxxxxx xxxxxxx xxxxx xxxxxxxx xxxxxxxxx.
5. Xxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxx xxxx doprovázet zásilku xxxxx její přepravy xx xx jejího xxxxxxxxxx xx xxxxxxx xxxxx.
Xxxxxx 9
Xxxxxxxxx zásilky
1. Xxxxxxx xx xxxxx rozdělit, xxxxx xxxxxx xxxxxxxxx xxxxxxx xxxxxx xxxxxxxx x xxxxx xxxxxxxxx orgány xxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxx xxxxxx, xxx stanoví xxxxxx 8.
2. X xxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxx xxxx xxxxxx xxxx zásilky xxxxx xxxx xxxxxxxx až xx jejího xxxxxxxxxx xx xxxxxxx xxxxx xxxxxxxxxx xxxxxxx kopie xxxxxxxxxx xxxxxxxxx xxxxxxx.
Xxxxxx 10
Xxxxxxxxxx xx xxxxxxx xxxxx
Xxxxxxx mohou xxx xxxxxxxxxx xx volného xxxxx xxxxx tehdy, xxxxx xxxxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxx nebo xxxx xxxxxxxx xxxxxxxx xxxxxx xxxxxxx xxxxxxxx xxxxxxx xxxxxx, xxxxx xxxxxxxxx xxxxx xxxxx vyplnil xxxx, xx xxxx xxxxxxxxx xxxxxxx xxxxxx xxxxxxxx. Xxxxx xxxxxx xxxxxxxx xxxxxxx do xxxxxxx xxxxx xxxxx xxxxx, xxxxxxxx je x xxxxxxx XX.14 xxxxxxxxxx xxxxxxxxx dokladu xxxxxxx xxxxxxxx xxxxxxxxxx příslušného xxxxxx a jestliže xx xxxxxxxx vstupní xxxxxx x xxxxxxx XX.21 podepsán.
Xxxxxx 11
Xxxxxxxxxx xxxxxxxxx
1. Pokud se xx xxxxxxx úředních xxxxxxx provedených x xxxxxxx x xxxxxxx 8 xxxxxx, xx xxxxxxxxx xxxxxx přepisy Xxxx, včetně xxxxxx xxxxxxxx, xxxxxx dodrženy, xxxxxx xxxxxxxxx xxxxx xxxx XXX xxxxxxxxxx xxxxxxxxx xxxxxxx x xxxxxxx xx opatření xxxxx xxxxxx 19, 20 a 21 xxxxxxxx (XX) č. 882/2004.
2. Pokud x xxxxxxx xxxxxx přiloženy xxxxxxxx xxxxxx xxxxxx x xxxxxxx uvedených x xxxxxx 4 xxx xxxxxxxxx x xxxxxxxxx xxxxxxxxxxxx uvedené v článku 5 xxxx pokud xxxx xxxxxxxx xxxx xxxxxxxxx x xxxxxxxxx nezávadnosti xxxxxx x xxxxxxx s požadavky xxxxxxxxxxx x xxxxx nařízení, nesmí xxx zásilka xxxxxxxx xx Xxxx x xxxxxx xx zpět mimo Xxxx xxxx xx xxxxx.
3. Xxxxx xxxxxxxxx orgán xx určeném místě xxxxxx nepovolí xxxxx xxxxxxx xxxxxxxx uvedených x xx. 1 xxxx. 1 x xxxxxx xxxxxxxxxx maximálního xxxxxx xxxxxxx stanoveného x xxxxxxxx (XX) x. 396/2005, neprodleně xxxx odmítnutí zásilky xx xxxxxxxxx oznámí x xxxxxxx s čl. 19 odst. 3 xxxxxxxx (ES) x. 882/2004.
Xxxxxx 12
Xxxxxx
1. Xxxxxxx státy Xxxxxx xxxxxxx xxxxx, do xxxxx xxxxxx xxxxxxxxxxxxx xx xxxxxx xxxxxxxx, xxxxxxxx zprávu x xxxxx xxxxxxxxxxxx výsledcích úředních xxxxxxx xxxxxxxxxxx u zásilek xxxxxxxx xxxxx tohoto xxxxxxxx.
Xxxxxxx xxxxxx obsahuje xxxx xxxxxxxxx:
|
a) |
xxxxx dovezených xxxxxxx; |
|
x) |
xxxxx zásilek, x xxxxxxx xxx proveden xxxxx xxxxxx pro analýzu; |
|
x) |
xxxxxxxx xxxxxxx xxxxxxxxxxx x xx. 8 xxxx. 2. |
2. Xx xx xx xx, xx xxxxx xxxxxxx xxxxx xxxxxxxxxx x XXXXXX xxxxxxxx xxxxxxx xxxxxxx vydané xxxxxx xxxxxxxxxxx orgány v souladu x xxxxx xxxxxxxxx, oznamovací xxxxxxxxxx stanovené x xxxxxxxx 1 byly xxxxxxx.
Xxxxxx 13
Xxxxxxx
Xxxx nařízení se xxxxxxxxx xxxx 31. xxxxxx 2019.
Xxxxxx 14
Xxxxxxx
Xxxxxxx xxxxxxx xxxxxxxxxxx x xxxxxxxx kontrol, xxxxxx xxxxxx xxxxxx, xxxxxxx, xxxxxxxxxx x xxxxxxxxxx xxxxxxxx xxxxxxxxx v návaznosti xx xxxxxxxxxx xxxxxxxxx, nese xxxxxxxxxxxx potravinářského podniku xxxxxxxxx xx xxxxxxx.
Xxxxxx 15
Xxxxx xxxxxxxx (XX) x. 669/2009
Xxxxxxx X xxxxxxxx (XX) x. 669/2009 se mění xxxxx:
|
x) |
x xxxxxxxxx xxx Xxxxxxx xx zrušuje xxxxxxx xxxxxxxxxx na „xxxxx xxxx vinné“; |
|
x) |
v položkách pro Xxxxxxx se xxxxxxx xxxxxxx odkazující xx „xxxxxxxx (dračí xxxxx)“. |
Xxxxxx 16
Xxxxxxx
Xxxxxxxxx xxxxxxxx (XX) x. 885/2014 xx xxxxxxx.
Xxxxxx 17
Xxxxxxxxx opatření
Xx xxxx xxx měsíců xx xxxx xxxxxx tohoto xxxxxxxx v platnost xxxxxx xxxxxxx xxxxx xxxxxx xxxxx zásilek xxxxx xxxxx pocházejících z Indie, xxxxx xxxxxxxx zemi xxxxxx nebo xxxx xxxxxxxx, xxxxx xx xxxxxxx země xxxx xxx xxxx původu, xxxx 8. xxxxxxxxx 2018, xx xxxxxxxxxxx, xx xxxxxxx xxxxxxx splňují xxxxxxxxx xxxxxxxxxxx xxxxxxxx (XX) x. 885/2014.
Xx xxxx xxx xxxxxx xx xxxx xxxxxx xxxxxx xxxxxxxx x xxxxxxxx povolí xxxxxxx xxxxx xxxxxx xxxxx zásilek listů xxxx xxxxx xxxxxxxxxxxxx x Xxxxxxx x xxxxxxxx (dračího xxxxx) xxxxxxxxxxxxx x Xxxxxxxx, xxxxx opustily zemi xxxxxx xxxx xxxx xxxxxxxx, pokud xx xxxxxxx xxxx xxxx xxx země xxxxxx, xxxx 8. xxxxxxxxx 2018, xx xxxxxxxxxxx, že xxxxxxx zásilky xxxxxxx xxxxxxxxx xxxxxxxx (XX) x. 669/2009 xxxxxxxx xx xxx 7. xxxxxxxx 2018.
Xxxxxx 18
Xxxxx v platnost x xxxxxxxxxxxx
Xxxx xxxxxxxx xxxxxxxx x xxxxxxxx xxxxxxxx xxxx xx xxxxxxxxx v Úředním věstníku Xxxxxxxx xxxx.
Xxxxxxx xx xxx xxx 8. xxxxxxxx 2018.
Xxxx xxxxxxxx xx xxxxxxx x xxxxx xxxxxxx x xxxxx xxxxxxxxxx xx xxxxx členských státech.
V Bruselu xxx 7. listopadu 2018.
Xx Xxxxxx
xxxxxxxx
Xxxx-Xxxxxx JUNCKER
(1)&xxxx;&xxxx;Xx.&xxxx;xxxx.&xxxx;X&xxxx;31, 1.2.2002, s. 1.
(2)&xxxx;&xxxx;Xx.&xxxx;xxxx.&xxxx;X&xxxx;165, 30.4.2004, s. 1.
(3)&xxxx;&xxxx;Xxxxxxxx Xxxxxx (XX) x.&xxxx;669/2009 xx dne 24.&xxxx;xxxxxxxx&xxxx;2009, xxxxxx se xxxxxxx xxxxxxxx Xxxxxxxxxx xxxxxxxxxx a Rady (ES) x.&xxxx;882/2004, xxxxx xxx x&xxxx;xxxxxxxx xxxxxx kontroly xxxxxx xxxxxxxxx xxxxx x&xxxx;xxxxxxxx xxxxxx než xxxxxxxxxxx xxxxxx, a kterým xx xxxx rozhodnutí 2006/504/XX (Xx.&xxxx;xxxx.&xxxx;X&xxxx;194, 25.7.2009, x.&xxxx;11).
(4)&xxxx;&xxxx;Xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x&xxxx;Xxxx (ES) x.&xxxx;396/2005 xx dne 23.&xxxx;xxxxx&xxxx;2005 x&xxxx;xxxxxxxxxxx xxxxxxxx reziduí xxxxxxxxx x&xxxx;xxxxxxxxxxx a krmivech xxxxxxxxxxx x&xxxx;xxxxxxxxxxx xxxxxx x&xxxx;xx xxxxxx povrchu x&xxxx;x&xxxx;xxxxx xxxxxxxx Xxxx 91/414/XXX (Xx.&xxxx;xxxx.&xxxx;X&xxxx;70, 16.3.2005, x.&xxxx;1).
(5) Prováděcí xxxxxxxx Komise (XX) č. 885/2014 xx xxx 13. srpna 2014, kterým xx xxxxxxx xxxxxxxx xxxxxxxx xxx xxxxx xxxx x&xxxx;xxxxx curry x&xxxx;Xxxxx a zrušuje prováděcí xxxxxxxx (EU) č. 91/2013 (Xx.&xxxx;xxxx.&xxxx;X&xxxx;242, 14.8.2014, x.&xxxx;20).
(6) Směrnice Xxxxxx 2002/63/XX xx xxx 11. července 2002, xxxxxx xx stanoví xxxxxx Xxxxxxxxxxxx xxx xxxxx xxxxxx xxxxxxxx x&xxxx;xxxxxx kontrole xxxxxxx xxxxxxxxx x&xxxx;xxxxxxxxxx rostlinného x&xxxx;xxxxxxxxxxx xxxxxx x&xxxx;xx xxxxxx povrchu x&xxxx;xxxxxx xx xxxxxxx xxxxxxxx 79/700/XXX (Xx.&xxxx;xxxx.&xxxx;X&xxxx;187, 16.7.2002, x.&xxxx;30).
(7) Rozhodnutí Komise 2003/24/XX xx dne 30.&xxxx;xxxxxxxx&xxxx;2002 x&xxxx;xxxxxx xxxxxxxxxxxxx xxxxxxxxxxxx xxxxxxxxxxxxx xxxxxxx (Xx.&xxxx;xxxx.&xxxx;X&xxxx;8, 14.1.2003, x.&xxxx;44).
(8)&xxxx;&xxxx;Xxxxxxxxxx Xxxxxx 2004/292/ES xx xxx 30. března 2004 x&xxxx;xxxxxxxx xxxxxxx Xxxxxx x&xxxx;x&xxxx;xxxxx xxxxxxxxxx 92/486/XXX (Xx.&xxxx;xxxx.&xxxx;X&xxxx;94, 31.3.2004, s. 63).
XXXXXXX X
Xxxxxxxxx xxxxxx xxx živočišného xxxxxx xxxxxxxxxxx zvláštním xxxxxxxxx, xxxxx xxx x&xxxx;xxxxxx xxxxx do Xxxxxxxx xxxx
|
Xxxxxxxxx (zamýšlené xxxxxxx) |
Xxx XX&xxxx;(1) |
Xxxxxxx XXXXX |
Xxxx xxxxxx |
Xxxxxx (xxxxxx) |
Xxxxxxx fyzických xxxxxxx x xxxxxxx xxxxxxxxxx (%) xxx dovozu |
|
Pitahaya (xxxxx xxxxx) (Xxxxxxxxx – xxxxxxx xxxx xxxxxxxx) |
xx&xxxx;0810&xxxx;90&xxxx;20 |
10 |
Xxxxxxx (XX) |
Xxxxxxx pesticidů xxxxxxxxx v xxxxxxxxxx xxxxxxxx xxxxxxxx x xxxxxxx s čl. 29 odst. 2 nařízení (XX) x.&xxxx;396/2005 (xxxxxxxxx, xxxxx xxxx být kontrolovány xxxxx v xxxxxxxxxx xxxxxxxxxxx původu xxxx xx xxxxxx povrchu) (2) x xxxxxxx xxxxxxxxxxxxxxx&xxxx;(3) (xxxxxxxxxxxxxxx, xxxxxxxxx xxxx XX2, xxxxxx xxxxxx&xxxx;(3), xxxxxxxxx&xxxx;(3), xxxxxxxx&xxxx;(3), xxxxxxxxx&xxxx;(3), xxxxxxx&xxxx;(3) x xxxxxx&xxxx;(3)), xxxxxxxxx&xxxx;(2) x xxxxxxxxxx&xxxx;(2). |
10 |
|
Xxxxx xxxxx (Xxxxxxx/Xxxxxxx xxxxxxxx) (Xxxxxxxxx – čerstvé, xxxxxxxx, xxxxxxxx xxxx sušené) |
xx&xxxx;1211&xxxx;90&xxxx;86 |
10 |
Xxxxx (IN) |
Rezidua xxxxxxxxx xxxxxxxxx x kontrolním xxxxxxxx xxxxxxxx x xxxxxxx s čl. 29 xxxx. 2 nařízení (ES) x.&xxxx;396/2005 (pesticidy, xxxxx xxxx xxx xxxxxxxxxxxx xxxxx v produktech xxxxxxxxxxx xxxxxx nebo xx xxxxxx povrchu) (2) x rezidua xxxxxxx&xxxx;(2). |
20 |
|
Xxxxx xxxx vinné (Potraviny) |
xx&xxxx;2008&xxxx;99&xxxx;99 |
11 , 19 |
Xxxxxxx (XX) |
Xxxxxxx xxxxxxxxx xxxxxxxxx v xxxxxxxxxx xxxxxxxx přijatém x xxxxxxx x&xxxx;xx.&xxxx;29 xxxx. 2 xxxxxxxx (XX) č. 396/2005 (xxxxxxxxx, xxxxx xxxx xxx xxxxxxxxxxxx pouze v xxxxxxxxxx xxxxxxxxxxx xxxxxx xxxx xx xxxxxx xxxxxxx)&xxxx;(2) x rezidua xxxxxxxxxxxxxxx&xxxx;(3) (dithiokarbamáty, xxxxxxxxx xxxx XX2, xxxxxx xxxxxx&xxxx;(3), mankozebu (3), metiramu (3), xxxxxxxxx&xxxx;(3), xxxxxxx&xxxx;(3) x xxxxxx&xxxx;(3)) x xxxxxxxxxxx&xxxx;(2). |
20 |
(1)&xxxx;&xxxx;X xxxxxxx, xx xx x xxxxxx xxxx XX xxxxxxxx vyšetření xxx x xxxxxxxxx xxxxxxxx a xxxxxxxxxxxx xxxxx neuvádí x xxxxx kódu xxxxx xxxxxxxxxxx položky, xxxxxxxx xx kód KN xxxxxxxxx „ex“.
(2) Rezidua xxxxxxxxx xxxxxxxx xxxxxxxxxxxxxxxxx xxxxxxxx xxxxxxxxxx na XX-XX x XX-XX.
(3)&xxxx;&xxxx;Xxxxxxx pesticidů xxxxxxxx metodami x xxxxxxxxx jediného xxxxxxx.