NAŘÍZENÍ XXXXXX (XX) x.&xxxx;429/2008
xx xxx 25.&xxxx;xxxxx 2008
x&xxxx;xxxxxxxxxxx xxxxxxxxxx x&xxxx;xxxxxxxx Xxxxxxxxxx parlamentu x&xxxx;Xxxx (XX) x.&xxxx;1831/2003, xxxxx xxx x&xxxx;xxxxxxxxxxx x&xxxx;xxxxxxxx xxxxxxx a vyhodnocování x&xxxx;xxxxxxxxxx xxxxxxxxxxx xxxxx
(Xxxx x&xxxx;xxxxxxxx xxx EHP)
KOMISE XXXXXXXXXX XXXXXXXXXXXX,
x&xxxx;xxxxxxx na Xxxxxxx x&xxxx;xxxxxxxx Evropského xxxxxxxxxxxx,
x&xxxx;xxxxxxx xx xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x&xxxx;Xxxx (XX) x.&xxxx;1831/2003 xx xxx 22.&xxxx;xxxx 2003 x&xxxx;xxxxxxxxxxx xxxxxxx xxxxxxxxxxx ve xxxxxx zvířat (1), x&xxxx;xxxxxxx xx xx.&xxxx;7 xxxx.&xxxx;4 x&xxxx;5 uvedeného xxxxxxxx,
xx xxxxxxxxxx x&xxxx;Xxxxxxxxx xxxxxx xxx xxxxxxxxxx potravin x&xxxx;xxxxxxx s čl. 7 odst. 4 x&xxxx;5 nařízení (XX) x.&xxxx;1831/2003,
xxxxxxxx x&xxxx;xxxxx xxxxxxx:
|
(1) |
Xx xxxxxxxx stanovit xxxxxxxxx xxxxxxxx, pokud xxx x&xxxx;xxxxxx xxxxxxxxxx xxxxxxxxxxx xxxxx xxxxx xxxxxxxx (XX) x.&xxxx;1831/2003, včetně xxxxxxxx xxx vypracování x&xxxx;xxxxxxxx xxxxxxx x&xxxx;xxxxxxxxxxxxx x&xxxx;xxxxxxxxxx těchto doplňkových xxxxx. Xxxx pravidla xxxx nahradit xxxxxxxxxx x&xxxx;xxxxxxx xxxxxxxx Xxxx 87/153/XXX (2), xxxxxx xx xxxxxxx hlavní xxxxxx xxx xxxxxxxxxxxxx doplňkových xxxxx xx xxxxxx xxxxxx. |
|
(2) |
Xxxx pravidla xx xxxx xxxxxxxx požadavky, xxxxx xxxx splňovat xxxxxxxxxxx připojená x&xxxx;xxxxxxx. Xxxx xx xxxxxxx xxxxx xxxxxxx xxxxx, xxxxx xxxx xxx xxxxxxxxxx x&xxxx;xxxxxxxxxxxx x&xxxx;xxxxxxxxxxxxxxx xxxxxxx xxxxxxxxx xxxxx, x&xxxx;xxxxxx, jež xxxx xxx předloženy x&xxxx;xxxxx xxxxxxxx xxxx xxxxxxxx x&xxxx;xxxxxxxxxx xxx člověka, xxxxxxx x&xxxx;xxxxxxx xxxxxxxxx xx účelem xxxxxxx x&xxxx;xxxxxxxxxxx žádostí x&xxxx;xxxxxxxx Xxxxxxxxx xxxxxx xxx xxxxxxxxxx xxxxxxxx (dále xxx „xxxx“). |
|
(3) |
Xxxxx povahy xxxxxxxxx xxxxx xxxx xxxxxxxxxxxx xxxxxxxx xxx xxxxx se xxxx xxxxxx xxxxxx potřebných x&xxxx;xxxxxxxxxxx xxxxxx vlastností x&xxxx;xxxxxx lišit. Subjekty xx xxxxx měly xxx možnost postupovat x&xxxx;xxxxxxx xxxxxxxxx, xxxxx xxx x&xxxx;xxxx xxxxxx x&xxxx;xxxxxxxxx, jež mají xxx xxxxxxxxxx x&xxxx;xxxxxxxxx xxxxxxxxxxx x&xxxx;xxxxxxxxx xxxxxxx xxxxxxxxx xxxxx. Xxxxxxxx, xxxxx xxxxxxx této xxxxxxxxx, xx xxxx x&xxxx;xxxxxxxxxxx xxxx výběr xxxxxxxxx. |
|
(4) |
Xxxx xx měl xxx xxxxxxx popřípadě xxxxxxxxx xxxxxxxxx xxxxxxxxx, xxx xxxx xxxxx, xxx xxxxxxxxx xxxxx xxxxxxx xxxxxxxx xxx xxxxxxxx xxxxx článku 5 xxxxxxxx (XX) x.&xxxx;1831/2003. |
|
(5) |
Xx xxxxxxxx xxxxxxxx příslušné xxxxx kvality při xxxxxxxxxxxxx xxxxxxxxxxx pro xxxxxxxxx látky určené x&xxxx;xxxxxxx x&xxxx;xxxxxx (xxxxxxxx) xxxx vodě, xxx xxxx xxxxxxxxx, že xxxxxxxx xxxxxxxxxxxxx xxxxxxx xxxxxx xxxxxxxxxxx. |
|
(6) |
X&xxxx;xxxxxxx nutnosti xx měly xxx xxxxxxxxx xxxxxxxx požadavky xxx jednotlivé kategorie xxxxxxxxxxx látek xxxxxxx x&xxxx;xx.&xxxx;6 xxxx.&xxxx;1 nařízení (XX) x.&xxxx;1831/2003. |
|
(7) |
X&xxxx;xxxxx xxxxxxxx xxxxx x&xxxx;xxxxxxx povolení xxx menšinové druhy xxx xxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxx bezpečnosti xx měly být xxxxxxxxx xxxxxxxx podmínky xxx xxxxxxxxxxx k možnosti xxxxxxxxxxx výsledků xxxxxx xxxxxxxxxxx na xxxxxxxxxxx xxxxxxx xx xxxxx xxxxxxxxx. |
|
(8) |
Xxxxxxxxx pravidla xxxxxxxx xx žádostí x&xxxx;xxxxxxxx xx měla xxxx x&xxxx;xxxxx různé xxxxxxxxx xx zvířata určená x&xxxx;xxxxxxxx xxxxxxxx a ostatní xxxxxxx, pro něž xxxxxxx xxxxxxxx se xxxxxxxxxxx xxxxxxxxxxx xxx xxxxxxx jako xxxxxxxxxxxx xxxxxx xxxxxxxx. |
|
(9) |
Xxxxxxx postupů xxxxxxxxxxxx xxxxxxxxx laboratorních xxxxxx k pokusným xx xxxxx xxxxxxxx xxxxxx x&xxxx;xxxxxxxxx xx xxxxxxxxx xxxxx směrnice Rady 86/609/XXX xx xxx 24.&xxxx;xxxxxxxxx 1986 x&xxxx;xxxxxxxxxx xxxxxxxx a správních xxxxxxxx xxxxxxxxx států týkajících xx xxxxxxx zvířat xxxxxxxxxxx pro xxxxxxx x&xxxx;xxxx xxxxxxx xxxxx (3) xx mělo xxx xxxxxxxxx. |
|
(10) |
Xxx xx xxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxx, xxxx xx xxx xxxxxxxxx xxxxxxxxxxxx xxxxxxx xxx xxxxxxxxxx xxxxxxxxxxx xxxxx, xxxxx xxx xxxx povoleny xxx xxxxxxx x&xxxx;xxxxxxxxxxx. |
|
(11) |
Xx xx xxxx xxxxxxxxxxx látek, xxxxx xxxx podle xxxxxxxx Xxxx 70/524/EHS (4) xxxxxxxx xxx xxxxxxxx xxxxxxx, měla by xxx xxxxxxxxx xxxxxxxxx xxxxxxx, xxx x&xxxx;xxxxxxx, xx nejsou x&xxxx;xxxxxxxxx xxxxx studie, xxxxxxx xxxxxxxx účinnost xxxxxx xxxxxx xxxxxxxxx, xxxxx xxxx x&xxxx;xxxxxxxxx k prokázání xxxxxxxxx, zejména materiálů xxxxxxxxxx xx xxxxxx xxxxxxxx xxxxxxxxx xxxxxxx xxxxxxxxx xxxxx. |
|
(12) |
Xx xxxxx xxxxxxxx pravidla xxx xxxxxxx x&xxxx;xxxxx xxxxxxxx x&xxxx;xxxxxxx x&xxxx;xx.&xxxx;13 xxxx.&xxxx;3 xxxxxxxx (ES) x.&xxxx;1831/2003. |
|
(13) |
Xx xxxxx xxxxxxxx xxxxxx xxxxxxxx xxx xxxxxxx x&xxxx;xxxxxxxx xxxxxxxx xxxxx xxxxxx&xxxx;14 nařízení (ES) x.&xxxx;1831/2003. |
|
(14) |
Xx xx týká xxxxxxxxxx x&xxxx;xxxxxxxx xxxxxxxxxxx x&xxxx;xxxxxxxxx, jež je xxxxx xxxxxxx xx xxxxxxx xxxxxxx, xx xxxxxxxx stanovit přechodné xxxxxx, během xxxxx xx xxxxx nadále xxxxxxxx xxxxxxxxx xxxxxxxx. X&xxxx;xxxxxxxx xxxxxxxx xxxx xxxxxxx tohoto xxxxxxxx x&xxxx;xxxxxxxx xx xx xxxx x&xxxx;xxxxxx xxxxxxxx x&xxxx;xxxxxxx s přílohou xxxxxxxx 87/153/XXX. Xxxxx jde x&xxxx;xxxxxxx podané během xxxxxxxx xxxxxx xx xxxxxx v platnost, žadatelé xx xxxxxxxx x&xxxx;xxxxxx xxxx potřebné xxx xxxxxxx xxxxxx xxxx xxx xxxxxxx xxxxxx xxxx pravidly xxxxxxxxxxx x&xxxx;xxxxx xxxxxxxx x&xxxx;xxxxxxxx xxxxxxxx 87/153/EHS. Prováděcí xxxxxxxx byla xxxxxxxxxxx xx xxxxxxx xxxxxxxxxx xxxxxxxxx a technických xxxxxxxx x&xxxx;x&xxxx;xxxxxxx xxxxxxxx xx xxxx xxx xxxxxxxxxxxx xxxxxxxxxx xxxxxx xxxxxx x&xxxx;xxxx oblasti. |
|
(15) |
Opatření tohoto xxxxxxxx xxxx x&xxxx;xxxxxxx xx xxxxxxxxxxx Xxxxxxx xxxxxx xxx xxxxxxxxxxx xxxxxxx x&xxxx;xxxxxx xxxxxx, |
XXXXXXX XXXX XXXXXXXX:
Xxxxxx 1
Xxxxxxxx
Xxx účely xxxxxx xxxxxxxx xx použijí xxxx definice:
|
1. |
„xxxxxxx v zájmovém xxxxx a ostatními xxxxxxx, xxxxx nejsou určena x xxxxxxxx potravin“ xx xxxxxx xxxxxxx xxxxx, xxx xxxx xxxxxxxx xxxxxx, chovány xxxx xxxxxx člověkem, xxxxxx xxxx xxxxxx pro xxxxxxx spotřebu, xxxxx xxxx; |
|
2. |
„xxxxxxxxxxx xxxxx“ xx xxxxxx xxxxxxx xxxxxx x xxxxxxxx potravin jiná xxx xxxx (zvířata xxxxxxx xxx xxxxx x xxxx, xxxxxx xxxxx), xxxx (xxxxxxx chovaná xxx xxxx), xxxxxxx, xxxxxx (xxxxxx nosnic), xxxxx x xxxx druhu Xxxxxxxxxx. |
Xxxxxx 2
Xxxxxx
1. Xxxxxx x xxxxxxxx doplňkové xxxxx xxxxx xxxxxx 7 xxxxxxxx (ES) č. 1831/2003 xx předloží xxxxxx xxxxxxxxx xxxxxxxxxxx x xxxxxxx X.
X xxxxxxx xx xxxxxxx xxxxxxxxxxx xxxxx článku 3 (xxxx xxx „xxxxxxxxxxx“), xxxxx xxxxxxxx xxxxx x xxxxxxxxx xxxxxxx x xx. 7 odst. 3 xxxxxxxx (ES) x. 1831/2003.
2. Xxxxx xxxxxxx x xxxxxxx s článkem 18 xxxxxxxx (XX) x. 1831/2003 xxxxxxxx, xxx se x xxxxxxxxx xxxxxx dokumentace xxxxx xxxxxxxx 1 zacházelo xxxx x xxxxxxxxx xxxxx, xxxxxxxx xxx každý xxxxxxxx nebo xxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxxx, xx xxxxxxxxxx xxxxxx xxxxxxxxx xx mohlo xxxxxxxx xxxxxxxx xxxx xxxxxxxxx xxxx konkurentům. Xxxxxxx xxxxx dokumentace xxxx být xxxxxxxxxx xxxxxxxx xx zbytku xxxxxxxxxxx x xxxxx být xxxxxxxx x xxxxxxx dokumentace xxxxx xx. 7 xxxx. 3 xxxx. x) xxxxxxxx (XX) č. 1831/2003. Xxxxxxx zašle Komisi xxxxx částí xxxxxxxxxxx, x xxxxx má xxx xxxxxxxxx xxxx x xxxxxxxxx xxxxx, x xxxxxxxxxxx odůvodnění.
Xxxxxx 3
Xxxxxxxxxxx
1. Xxxxxxxxxxx xxxxxxxxx x xxxxxxxxxx xxxxxxxxx, xx doplňková xxxxx xxxxxxx xxxxxxxx xxx xxxxxxxx xxxxxxxxx x xxxxxx 5 xxxxxxxx (XX) x. 1831/2003.
2. Xxxxxx xxxxxxxxx xx xxxxxxxxxxx a předání dokumentace xxxx xxxxxxxxx x xxxxxxx XX.
Xxxxxxxx xxxxxxxxx, xxx xxxxxxxxxxx xxxx xxxxxxxx x xxxxxxxx xxxxxxx, xxxx xxxxxxxxx x xxxxxxx XXX.
Xxxxxxxxx xxxx xxxxxx xxxxxxxxxxxx xxxxxx je xxxxxxxxx v příloze IV.
3. Odchylně xx xxxxxxxx 2 xxxx xxxxxxx xxxxxxxxx dokumentaci, která xxxxxxxxx požadavky stanovené x xxxxxxxx 2, xxxxx každý xxxxx, jenž xxxx xxxxxxxxx nesplňuje, xxxxxxxx.
Xxxxxx 4
Xxxxxxxxx xxxxxxxx
1. Xx žádosti x xxxxxxxx xxxxxx před xxxxx vstupu xxxxxx xxxxxxxx v platnost xx xxxxxx vztahuje xxxxxxx xxxxxxxx 87/153/EHS.
2. X xxxxxxx o povolení xxxxxxxx xxxx 11. xxxxxxx 2009 xx mohou xxxxxxxx rozhodnout, xx xxxxx xxxxxx xxxxxxxx xxxxxx XXX x XX částí I a II xxxxxxx xxxxxxxx 87/153/XXX xxxxx xxxx 1.3, 1.4, 2.1.3, 2.1.4, 2.2.3, 2.2.4, 3.3, 3.4, 4.1.3, 4.1.4, 4.2.3, 4.2.4, 5.3, 5.4, 6.3, 6.4, 7.3, 7.4, 8.3 x 8.4 xxxxxxx XXX x xxxxx ustanovení xx xxxxxxx „Xxxxxxxxx xxxx xxxxxx xxxxxxxxxxxx studií xxxxxxxxx“ x xxxxxxxxx přílohy IV.
Xxxxxx 5
Xxxxx x xxxxxxxx
Toto xxxxxxxx xxxxxxxx x xxxxxxxx dvacátým xxxx po xxxxxxxxx x Xxxxxxx věstníku Evropské xxxx.
Xxxx xxxxxxxx je xxxxxxx x xxxxx xxxxxxx x xxxxx xxxxxxxxxx ve xxxxx xxxxxxxxx xxxxxxx.
X Xxxxxxx xxx 25. dubna 2008.
Xx Xxxxxx
Xxxxxxxxx XXXXXXXXX
členka Xxxxxx
(1)&xxxx;&xxxx;Xx.&xxxx;xxxx. X&xxxx;268, 18.10.2003, x.&xxxx;29. Xxxxxxxx xx xxxxx nařízení Komise (XX) č. 378/2005 (Úř. věst. X&xxxx;268, 18.10.2003, x.&xxxx;29).
(2)&xxxx;&xxxx;Xx.&xxxx;xxxx. L 64, 7.3.1987, x.&xxxx;19. Xxxxxxx nařízením (XX) x.&xxxx;1831/2003.
(3)&xxxx;&xxxx;Xx.&xxxx;xxxx. X&xxxx;358, 18.12.1986, x.&xxxx;1; xxxxxxxx xxxxx x&xxxx;Xx.&xxxx;xxxx. X&xxxx;358, 18.12.1986, x.&xxxx;1. Xxxxxxxx xx xxxxx směrnice Evropského xxxxxxxxxx a Rady 2003/65/ES (Xx.&xxxx;xxxx. X&xxxx;358, 18.12.1986, x.&xxxx;1).
(4)&xxxx;&xxxx;Xx.&xxxx;xxxx. X&xxxx;270, 14.12.1970, x.&xxxx;1. Směrnice xxxxxxxxx xxxxxxxxx nařízením Komise (XX) x.&xxxx;1800/2004 (Xx.&xxxx;xxxx. X&xxxx;270, 14.12.1970, x.&xxxx;1).
XXXXXXX&xxxx;X
XXXXXXXX ŽÁDOSTI XXXXXXX X&xxxx;XX.&xxxx;2 XXXX.&xxxx;1&xxxx;X&xxxx;XXXXXXX XXXXX
1.&xxxx;&xxxx;&xxxx;XXXXXXXX XXXXXXX
XXXXXXXX XXXXXX
XXXXXXXXX XXXXXXXXXXX
XXX XXXXXX X&xxxx;XXXXXXX XXXXXXXXXXXX
(Xxxxxx)
Xxxxx: …
|
Xxx |
: |
Xxxxxx x&xxxx;xxxxxxxx xxxxxxxxx xxxxx xxxxx xxxxxxxx (XX) x.&xxxx;1831/2003. |
|
◻ |
Xxxxxxxx xxxxxxxxx xxxxx xxxx xxxx xxxxx doplňkové xxxxx (xx.&xxxx;4 odst. 1 xxxxxxxx (XX) x.&xxxx;1831/2003) |
|
◻ |
Xxxxxxxx xxxxxxxxxxxx xxxxxxxx (xx.&xxxx;10 odst. 2 xxxx&xxxx;7 xxxxxxxx (XX) x.&xxxx;1831/2003) |
|
◻ |
Xxxxx stávajícího xxxxxxxx (xx.&xxxx;13 xxxx.&xxxx;3 xxxxxxxx (XX) č. 1831/2003) |
|
◻ |
Obnovení xxxxxxxx xxxxxxxxx látky (xxxxxx&xxxx;14 xxxxxxxx (XX) x.&xxxx;1831/2003) |
|
◻ |
Xxxxxxxx x&xxxx;xxxxxxxxxx xxxxxxxxx (xxxxxx&xxxx;15 xxxxxxxx (XX) x.&xxxx;1831/2003) |
(Xxxxxxx xxxxxxxxxxx xxxxxxxxxxx xxxxxxx x&xxxx;xxxxxxx)
Xxxxxxx(x)&xxxx;x/xxxx xxxx/xxxxxx zástupce(i) ve Xxxxxxxxxxxx (čl. 4 xxxx.&xxxx;3 xxxxxxxx (ES) x.&xxxx;1831/2003) xx xxxxxxxx xxxxxxxxx x&xxxx;xx.&xxxx;7 odst. 3 xxxx.&xxxx;x)&xxxx;xxxxxxxx (XX) x.&xxxx;1831/2003 (xxxxx, xxxxxx ….)
…
…
podává (xxxxxxxx) xxxx žádost xx xxxxxx xxxxxxx xxxxxxxx xxx xxxxxxxxxxx xxxxxxx xxxxxxx xxxxxxxxxx látku:
1.1 Identifikace x&xxxx;xxxxxxxxxxxxxxx xxxxxxxxx xxxxx
Xxxxx xxxxxxxxx xxxxx (xxxxxxxxxxxxxxx xxxxxx xxxxx (xxxxx) xxxx xxxxxxx (xxxxxxx), xxx xx xxxxxxxx x&xxxx;xxxxxx&xxxx;2.2.1.1 x&xxxx;2.2.1.2 xxxxxxx&xxxx;XX):
…
…
Xxxxxxxx xxxxx (xx-xx to xxxxxx u povolení xxxxxxxx xx držitele):
…
…
V kategorii/kategoriích a funkční xxxxxxx/xxxxxxxxx doplňkových xxxxx&xxxx;(1) (xxxxxx):
…
…
Xxxxxx druhy xxxxxx:
…
…
…
Xxxxx xxxxxxxx xxxxxxxx (čl. 9 xxxx.&xxxx;6 nařízení (XX) x.&xxxx;1831/2003):
…
…
Xxxx doplňková xxxxx xxx byla xxxxxxxx x&xxxx;xxxxxxxx xxxxxxxxxx x&xxxx;xxxxxxxx xxxxxxxx.……/…/X(X)X&xxxx;xxxx xxxxxxxxx (ES) x.&xxxx;…/… xxx číslem … xxxx (xxxxxxxxx xxxxxxxxxxx xxxxx)
…
Xxxx xxxxxxxxx xxxxx xxx xxxx xxxxxxxx x&xxxx;xxxxxxxx předpisech x&xxxx;xxxxxxxxxxx xxxxxxxx .…/…/X(X)X&xxxx;xxxx xxxxxxxxx (XX) x.&xxxx;…/… xxx xxxxxx … xxxx
…
xxx xxxxxxx x
…
Xxxxx xx xxxxxxx xxxxxx x&xxxx;xxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxx xxxx xxxx organismy xxxxxxxx xx je x&xxxx;xxxx xxxxxxx, xxxxxx xxxx xxxxxxxxx:
|
◻ |
xxxxxxxxxxx xxxxxxxxxxxxx xxx (xxxxxxxx Xxxxxx (XX) x.&xxxx;65/2004&xxxx;(2)) (xx-xx xx vhodné): … |
|
◻ |
údaje x&xxxx;xxxxxxxxx xxxxxxxx xxxxxxxx x&xxxx;xxxxxxx x&xxxx;xxxxxxxxx Evropského xxxxxxxxxx x&xxxx;Xxxx (XX) č. 1829/2003 (3): … |
|
◻ |
nebo xxxxx x&xxxx;xxxxx nevyřízené xxxxxxx o povolení xxxxx xxxxxxxx (XX) x.&xxxx;1829/2003: … |
1.2&xxxx;&xxxx;&xxxx;Xxxxxxxx xxx xxxxx
1.2.1&xxxx;&xxxx;&xxxx;Xxxxxxx x&xxxx;xxxxxxxxxxx xxxxxxxx
Xxxx xxxx xxxxxxxxx xxxxxx:
…
…
Xxxxxxxxx stáří xxxx xxxxxxxx:
…
…
Xxxxxxxxx dávka (xx-xx xx xxxxxx): xx xxxx xxxxxxxx xxxxxxxx&xxxx;(4) xxxx xxxxxxxx xxxxxxx xxxxxxx (CFU) xxxx xx/xx xxxxxxxxxxx xxxxxx x&xxxx;xxxxxx xxxx 12&xxxx;%
…
…
Xxxxxxxxx xxxxx (je-li xx xxxxxx): mg xxxx xxxxxxxx xxxxxxxx xxxx XXX nebo ml/kg xxxxxxxxxxx krmiva x&xxxx;xxxxxx xxxx 12 %
…
…
U tekutých xxxxx xx xxxxx uvést xxxxxxxxx a maximální xxxxx xx xxxx.
1.2.2&xxxx;&xxxx;&xxxx;Xxxxxxx xx xxxx
Xxxxxxxxx xxxxx (je-li xx vhodné): mg xxxx xxxxxxxx aktivity xxxx CFU nebo xx/x&xxxx;xxxx
…
…
Xxxxxxxxx xxxxx (je-li xx xxxxxx): xx xxxx xxxxxxxx xxxxxxxx xxxx XXX nebo xx/x&xxxx;xxxx
…
…
1.2.3&xxxx;&xxxx;&xxxx;Xxxxxxxx xxxxxxxx pro xxxxx (je-li to xxxxxx)
Xxxx xxxx xxxxxxxxx xxxxxx:
…
…
Xxxxxxxxx stáří:
…
…
Minimální dávka (xx-xx to xxxxxx): xx nebo xxxxxxxx xxxxxxxx nebo XXX/xx xxxxxxxxxxx xxxxxx o obsahu xxxx 12 %
…
…
Maximální xxxxx (xx-xx xx xxxxxx): xx xxxx jednotky xxxxxxxx xxxx CFU/kg xxxxxxxxxxx xxxxxx x&xxxx;xxxxxx xxxx 12&xxxx;%
…
…
X&xxxx;xxxxxxxx krmiv xx xxxxx uvést xxxxxxxxx a maximální xxxxx xx litr.
Podmínky xxxx xxxxxxx použití (je-li xx xxxxxx):
…
…
…
Xxxxxxxx podmínky xxxx xxxxxxx xxx xxxxxxxxxx (xx-xx xx xxxxxx):
…
…
…
…
Xxxxxxxxx limit reziduí (xx-xx xx xxxxxx):
Xxxx xxxx kategorie xxxxxx:
…
…
Xxxxxxxxxxxx xxxxxxxx:
…
…
Xxxxxx xxxxx nebo xxxxxxxx:
…
…
…
Xxxxxxxxx xxxxxxxx x&xxxx;xxxxxxx xxxx produktech (μx/xx):
…
…
…
Xxxxxxxx xxxxx:
…
1.3&xxxx;&xxxx;&xxxx;Xxxxxxxxxx vzorky
Číslo xxxxxx xxxxxxxxxx xxxxxxxxxx Xxxxxxxxxxxx (xx-xx xx xxxxxx):
…
Xxxxx xxxxxx / xxxxx xxxxx:
…
Xxxxx xxxxxx:
…
Xxxxx xxxxxxxxx xxxxxxxxxxxx:
…
Xxxxxxxxxxx:
…
Xxxxxxxx:
…
Xxxxxxx xxxxx:
…
Xxxxx xxxxx:
…
Xxxxxxxxx xx xxxxxxxxxx:
…
1.4&xxxx;&xxxx;&xxxx;Xxxxxxxxxx xxxxx (xx-xx xx xxxxxx)
…
…
…
…
Xxxxx xxxx žádosti xxxx xxxxxxx xxxxx xxxxx x&xxxx;xxxxxxxxxxx a referenční laboratoři Xxxxxxxxxxxx x&xxxx;xxxxxxxxxxxx xxxxxx.
Xxxxxx …
1.5&xxxx;&xxxx;&xxxx;Xxxxxxx:
|
◻ |
xxxxx dokumentace (xxxxx xxx xxxx), |
|
◻ |
xxxxxxx xxxxxx xxxxxxxxxxx, |
|
◻ |
xxxxxxxx shrnutí xxxxxxxxxxx, |
|
◻ |
xxxxxx xxxxx dokumentace, s nimiž xx být xxxxxxxxx xxxx x&xxxx;xxxxxxxxx xxxxx, x&xxxx;xxxxx xxxxxxxxxxx xxxxxxxxx xxxxx xxxxxxxxxxx (pouze xxx Xxxxxx a úřad), |
|
◻ |
kopie xxxxxxxxx xxxxx xxxxxxxx(x), |
|
◻ |
xxx xxxxxx doplňkové xxxxx xxx referenční xxxxxxxxx Xxxxxxxxxxxx xxxxx xx.&xxxx;7 xxxx.&xxxx;3 xxxx.&xxxx;x)&xxxx;xxxxxxxx (XX) x.&xxxx;1831 / 2003 (xxxxx pro xxxxxxxxxx xxxxxxxxx Xxxxxxxxxxxx), |
|
◻ |
xxxx s údaji x&xxxx;xxxxxxxxxxx materiálu (pouze xxx xxxxxxxxxx laboratoř Xxxxxxxxxxxx), |
|
◻ |
xxxxxxxxx x&xxxx;xxxxxxxxxxxx x&xxxx;xxxxxxx (xxxxx xxx xxxxxxxxxx xxxxxxxxx Xxxxxxxxxxxx) x |
|
◻ |
xxxxxxxxx x&xxxx;xxxxxxxx xxxxxxxx xxx xxxxxxxxxx laboratoř Xxxxxxxxxxxx (xxxxxx&xxxx;4 xxxxxxxx (XX) x.&xxxx;378/2005&xxxx;(5). |
Xxxxxxx příslušné xxxxx xxxxxxxxx x&xxxx;xxxxxxxx xx xxxxx škrtněte. Xxxxxxxx xxxxxxxxx xxxxxxx (s ostatními xxxxxxxxxxxx xxxxxxxxx) xxxxxxx xxxxx Evropské komisi.
2. SPRÁVNÍ XXXXX XXXXXXXX(X)
Xxxxxxxxx xxxxx xxx xxxxxxxxxx xxxxxxx x&xxxx;xxxxxxxx doplňkové xxxxx xxxxx xxxxxxxx (XX) x.&xxxx;1831/2003
|
1. |
Xxxxxxxxxx xxxx xxxxx, xxxxx xxxxxx xxxxxx
|
|
2. |
Xxxxxxxxx osoba (pro xxxxxxxx korespondenci x&xxxx;Xxxxxx, xxxxxx x&xxxx;xxxxxxxxxx xxxxxxxxxx Xxxxxxxxxxxx)
|
(1)&xxxx;&xxxx;X&xxxx;xxxxxxx xxxxxxx „xxxx xxxxxxxxxxxx xxxxxxxxx látky“ x&xxxx;xxxxxxxxx xxxxxxxxxxxx xxxxxxxxx látky xx xxxxx jednoznačně xxxxxxx, jakou xxxxxx xx xxxxxxxxx látka xxx.
(2)&xxxx;&xxxx;Xx.&xxxx;xxxx. L 10, 16.1.2004, x.&xxxx;5.
(3)&xxxx;&xxxx;Xx.&xxxx;xxxx. X&xxxx;268, 18.10.2003, x.&xxxx;1. Xxxxxxxx xxxxxxxxx xxxxxxxxx nařízením (XX) x.&xxxx;298/2008 (Xx.&xxxx;xxxx. X&xxxx;268, 18.10.2003, x.&xxxx;1).
(4)&xxxx;&xxxx;Xxxxxxxx „xxxxxxxx“ xxxxxxxx xxxxxxx.
(5)&xxxx;&xxxx;Xxxxxxxx Xxxxxx (XX) x.&xxxx;378/2005 ze xxx 4. března 2005 x&xxxx;xxxxxxxxxx xxxxxxxxxxx pravidlech x&xxxx;xxxxxxxx Xxxxxxxxxx parlamentu x&xxxx;Xxxx (ES) č. 1831/2003, xxxxx xxx x&xxxx;xxxxxxxxxx x&xxxx;xxxxx xxxxxxxxxx xxxxxxxxxx Xxxxxxxxxxxx v souvislosti s žádostmi x&xxxx;xxxxxxxx xxxxxxxxxxx xxxxx x&xxxx;xxxxxxxx (Xx.&xxxx;xxxx. X&xxxx;59, 5.3.2005, x.&xxxx;8). Nařízení xx xxxxx xxxxxxxx (XX) x.&xxxx;850/2007 (Xx.&xxxx;xxxx. X&xxxx;59, 5.3.2005, x.&xxxx;8).
PŘÍLOHA II
OBECNÉ XXXXXXXXX, XXX XXXX SPLŇOVAT XXXXXXXXXXX XXXXX XXXXXX&xxxx;3
XXXXXX USTANOVENÍ
Tato xxxxxxx xxxxxxx požadavky xx vypracování seznamu x&xxxx;xxxxxxxxxxxxxxx xxxxxx x&xxxx;xxxxxxxxx x&xxxx;xxxxxxx, xxxxxxxxxxxxxxxx a přípravcích, xxx xxxx xxx xxxxxxxxxx x&xxxx;xxxxxxxxxxx xxxxx xxxxxx&xxxx;7 xxxxxxxx (XX) x.&xxxx;1831/2003 xxx:
|
— |
xxxxxxxx xxxx xxxxxxxxx xxxxx, |
|
— |
xxxxxxxx xxxxxx xxxxx doplňkové látky, |
|
— |
změnu xxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxx nebo |
|
— |
obnovení xxxxxxxx xxxxxxxxx xxxxx. |
Xxxxxxxxxxx musí xxxxxxx xxxxxxxxxxx xxxxxxxxxxx xxxxx na xxxxxxx xxxxxxxxxx xxxxx poznatků x&xxxx;xxxxxxx, xx xxxx xxxxxxxxx xxxxx odpovídají xxxxxxxxx zásadám xxx xxxxxx povolení, xxxxx xxxx xxxxxxxxx x&xxxx;xxxxxx&xxxx;5 xxxxxxxx (XX) x.&xxxx;1831/2003.
Xxxxxx, xxx mají xxx xxxxxxxxxx, x&xxxx;xxxxxx xxxxxx xxxx xxxxxxx xx xxxxxx doplňkové látky, xxxxxxxxx xxxx funkční xxxxxxx, xxxxx xxxxxxxx (xxxxxxxx, xxxxx xxxx xxxxxx na držitele; xxxxxxxx vázané xx xxxxxxxx), samotné xxxxx, xxxxxxxx xxxxxxxxx x&xxxx;xxxxxxxxxx xxx xxxxx. Žadatel xxxxxx xx xxxx xxxxxxx x&xxxx;xxxxxxx&xxxx;XXX, aby xxxx xxxxx xxxxxxxx, xxxxx studie a informace xxxx xxx společně xx xxxxxxx předloženy.
Žadatel xxxxxxxxxxx uvede xxxxxx xxx xxxxxxxxx xxxxxxxxx xxxxx xxxx xxxxxxxxx xx xx dokumentace xxxxxxxxxx x&xxxx;xxxx xxxxxxx, xxxxxxx&xxxx;XXX a příloze IV.
Dokumentace xxxx xxxxxxxxx xxxxxxxx zprávy x&xxxx;xxxxx xxxxxxxxxxx studiích, xxxxxxxxxx v souladu xx xxxxxxxx xxxxxxxxx xxxxxxxxx x&xxxx;xxxx příloze. Xxxxxxxxxxx xxxx xxxxxxxxx xxxxxx x&xxxx;xxxxx xxxxx xxxxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxx x&xxxx;xxxxx xxxxxxxxx xxxxxxxxxxx xxxxxxxxxx, xxxxx xxx xxxx xxxxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx. Pokud xxxx xxxx studie xxx xxxxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx podle xxxxxxxx xxxxxxxx xxxxxxxx xx Xxxxxxxxxxxx, xxxxxxxxx xxxxx na výsledek xxxxxxxxx. Xxxxx xx xxxxxx, xxxxx byly xxxxxxxxx x&xxxx;xxxxxxxxxx již xxxxx, xxxx xxxxx xxxxxxxxxxx x&xxxx;xxxxxxxxxxxx zkoušek xx xxxx xxxxxxxxxxx xxxxxxxxx xx xxxxxxx xxxxxxxxxx xxxxx xxxx xxxxx, xxxxx je xxxxxxxxx xxxxxxx o povolení.
Studie, xxxxxx studií, xxxxx xxxx xxxxxxxxx x&xxxx;xxxxxxxxxx xxx xxxxx xxxx xxxxx xxxxxxxxx z rovnocenných xxxxxxx, musí xxx xxxxxxxxx x&xxxx;xxxxxxxxxxxxxx podle xxxxxxxxxxx xxxxx xxxxxxx (xxxx. xxxxxxx xxxxxxxxxxx xxxxx x&xxxx;xxxxxxx xx xxxxxxxx Xxxxxxxxxx parlamentu x&xxxx;Xxxx 2004/10/ES xx xxx 11. února 2004 x&xxxx;xxxxxxxxxxx xxxxxxxx x&xxxx;xxxxxxxxx xxxxxxxx týkajících xx xxxxxxxxx zásad správné xxxxxxxxxxx praxe x&xxxx;xxxxxxxxx xxxxxx xxxxxxxxx při xxxxxxxxx xxxxxxxxxx xxxxx&xxxx;(1) xxxx Xxxxxxxxxxx organizace xxx xxxxxxxxxxx (XXX).
Xxxxx xx xxxxxx in xxxx xxxx xx xxxxx provádějí xxxx Xxxxxxxxxxxx, žadatel xxxx xxxxxxxx, xx xxxxxxx xxxxxxxx dodržují zásady xxxxxxx xxxxxxxxxxx xxxxx Xxxxxxxxxx pro xxxxxxxxxxxx xxxxxxxxxx a rozvoj (OECD) xxxx xxxxx XXX.
Xxxxxxxxx-xxxxxxxx, xxxxxxxxxxxxx a ekotoxikologické vlastnosti xx xxxx xxxxx xxxxx xxxxxxxxxxx xxxxxxxx Xxxx 67/548/EHS xx xxx 27.&xxxx;xxxxxx 1967 x&xxxx;xxxxxxxxxx xxxxxxxx x&xxxx;xxxxxxxxx xxxxxxxx xxxxxxxxxx xx xxxxxxxxxxx, balení x&xxxx;xxxxxxxxxx xxxxxxxxxxxx xxxxx&xxxx;(2), xxxxxxxxx xxxxxxxxxx xxxxxxxx Xxxxxx 2004/73/XX&xxxx;(3), nebo xxxxxx xxxxxxxxxxxxxxx xxxxx uznaných xxxxxxxxxxxxx vědeckými xxxxxxxxxxx. Xxxxxxx jiných xxxxx xxxx být xxxxxxxxxx.
Xx xxxxx podporovat xxxxxxxxx xxxxx in vitro xxxx metod zpřesňujících xxxx xxxxxxxxxxxxx obvyklé xxxxx xxxxxxxxx x&xxxx;xxxxxx xxxxxxxxxxxxx xxxxxx nebo xxxxxxxxxxx počet xxxxxx xxxxxxxxx při těchto xxxxxxx. Xxxx metody xxxx stejnou xxxxxxx x&xxxx;xxxxxxxxx stejnou xxxxxx xxxxxxx jako xxxxxx, xxxxxx xxxx xxxxxxxx.
Xxxxx xxxxx xxxxxxx x&xxxx;xxxxxxxx xxxx ve vodě xxxx xxx v souladu x&xxxx;xxxxxxxx správné laboratorní xxxxx xxxxxxxxxxx ve xxxxxxxx 2004/10/ES x/xxxx xxxxx XX XXX/XXX 17025. Xxxx xxxxxx xxxxxxxx xxxxxxxxxx stanoveným x&xxxx;xxxxxx&xxxx;11 nařízení Xxxxxxxxxx xxxxxxxxxx x&xxxx;Xxxx (ES) x.&xxxx;882/2004 xx xxx 29.&xxxx;xxxxx 2004 x&xxxx;xxxxxxxx xxxxxxxxxx xx účelem xxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxx týkajících xx xxxxx x&xxxx;xxxxxxxx x&xxxx;xxxxxxxx x&xxxx;xxxxxx zvířat x&xxxx;xxxxxxx xxxxxxxxx podmínkách zvířat (4).
Každá xxxxxxxxxxx xxxx xxxxxxxxx xxxxxxx xxxxxx a podrobné xxxxxxx xxxxxxx, xxx xxxx možno xxxxxxxx xxxxxxxxxx xxxxx xxxxxxxxxxxxx x&xxxx;xxxxxxxxxxxxxxx.
Xxxxx dokumentace xxxxxxxx xxxxx xxxxx xxxxxxxxxxxx x&xxxx;xxxxxx xx xxxxxxx xxxxx xx trh, xxxxx xx požaduje xxxxx xx.&xxxx;7 xxxx.&xxxx;3 xxxx.&xxxx;x)&xxxx;xxxxxxxx (XX) x.&xxxx;1831/2003, x&xxxx;xxxxx na xxxxxxxxxx xxxxx xx.&xxxx;7 xxxx.&xxxx;3 xxxx.&xxxx;x)&xxxx;xxxxxxxx (XX) x.&xxxx;1831/2003.
Xxxxxxxxx xxxxxxxxxxx
Xxxx xxxxxxxxx je xxxxxxxx xx xxxxxxxx, xxxxx mají prokázat xxxxxxxx xxxxxxxxx xxxxxxxxx xxxxx ve xxxxxx x:
|
x) |
xxxxxxx xxxxxx při xxxxxxxxxx xxxxxxxxxxxx xxxxxxxx xxx xxxxxxxxxxx xx xxxxx nebo xxxx x&xxxx;xxx xxxxxxx xxxxxx xxxxxx xxx xxxxxxxxx xxxxxxx xxx xxxxxxxxxx; |
|
x) |
xxxxxxxxxxxxx, xxxxx xxxxxxxx xxxxxxxxxxxxx xxxxxxx xxxxxxx xx xxxxxx xxxxxxxxxxxxx xxxxxxxxxx xxxxx, xxxx xxxxxxx xxxx xxxxxxxxxx. V tomto xxxxxxx xxxx xxxxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxxxx xxxxxx reziduí (XXX) x&xxxx;xxxxxxxxxx xxxx na xxxxxxx xxxxxxxxxx xxxxx xxxxx (ADI) xxxx xxxxxxxx xxxxxxxx xxxxx (XX); |
|
x) |
xxxxxx, které budou xxxxxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxx vdechnutím xxxx xxxxxxxxx xxxxxxxx, xxx xx kůže při xxxxxxxxxx x&xxxx;xxxxxxxxxx xxxxxx xxxx takovou xxxx xxx xxxxx xxxxxxxxxxxxx xx premixů xxxx xxxxxxxxxxx xxxxx xxxx xxxx xx xxx xxxxxxxxx xxxxxx xxxx xxxx, xxxxx xxxxxxxx xxxxxxxx xxxxxxxxxx xxxxx; |
|
x) |
xxxxxxxx x&xxxx;xxxxxxx xxxxxxxx xxxxxxxx x&xxxx;xxxxxxx x&xxxx;xxxxxxxxx xxxx xxxxxxxxxxxxx xxxx xxxxxxxxxxxxxxxx xxxxxx x |
|
x) |
xxxxxxxxx xxxxxxxxx, x&xxxx;xxxxxxx na nebezpečí xxxxxxxxxxx z doplňkové xxxxx xxxxxxx xxxx xxxxxxxx x&xxxx;xx xxxxxxxxxx, ať xx xxxxx a/nebo xxxxxxxxxxx xxxxxxx. |
Xxxxx xx xxxxxxxxx xxxxx xxxx xxxxxx, xxxxx složka xxxx být xxxxxxxxx x&xxxx;xxxxxxxx bezpečnosti xxx xxxxxxxxxxxx xxxxxxxxxx x&xxxx;xxxxxxx xxxxxxxxxxx x&xxxx;xxxxxxx xx xxxxxxxxxxx xxxxxx (lze-li xxxxxxxx, xx mezi xxxxxxxx xxxxxxxxx x&xxxx;xxxxxxxxxx xxxxxxxx). Alternativně xx xxxxx xxxxxxxx xxxxxxxxx xxxxx.
Xxxxxxxxx xxxxxxxxx
Xxxx posouzení xx založeno xx xxxxxxxx, které xxxx xxxxxxxx xxxxxxxx doplňkové xxxxx, xxxxx xxx x&xxxx;xxxxxx užití, xxx xx stanoveno x&xxxx;xx.&xxxx;6 xxxx.&xxxx;1 a příloze I nařízení (ES) x.&xxxx;1831/2003.
1.&xxxx;&xxxx;&xxxx;XXXXX&xxxx;X:&xxxx;XXXXXX XXXXXXXXXXX
1.1&xxxx;&xxxx;&xxxx;Xxxxxxx souhrn xxxxxxxxxxx podle xx.&xxxx;7 xxxx.&xxxx;3 xxxx.&xxxx;x)&xxxx;xxxxxxxx (ES) x.&xxxx;1831/2003
Xxxxxxx xxxxxxxx xxxxxx x&xxxx;xxxxxxxx hlavních xxxxxxxxxx xxxxxxx xxxxxxxxx látky. Xxxxxx xxxxx xxxxxxxxx xxxxx xxxxxxx xxxxx x&xxxx;xxxx mít xxxx xxxxxxxxx:
1.1.1&xxxx;&xxxx;&xxxx;Xxxxx
|
x) |
xxxxx xxxxxxxx(x); |
|
x) |
xxxxxxxxxxxx doplňkové xxxxx; |
|
x) |
xxxxxx xxxxxx x&xxxx;xxxxxx xxxxxxx; |
|
x) |
xxxxxx xxxxxxxxxxx x&xxxx;xxxxxxxxx xxxxxxxxx látky; |
|
e) |
navrhované podmínky xxx užití x |
|
x) |
xxxxx xxxxx xxxxxxxxxxxx x&xxxx;xxxxxx xx uvedení látky xx xxx. |
1.1.2.&xxxx;&xxxx;&xxxx;Xxxxx
|
x) |
Xxxxx x&xxxx;xxxxxx xxxxxxxx(x) Xxxx xxxxx xxxx xxx xxxxxxxxxx xx xxxxx xxxxxxxxx xxxxxxxxx xx xxxxx xxxxxxxx xxxxxxxxx látky (povolení xxxxxx na držitele xxxx xxxxxxxx, xxxxx xxxx xxxxxx xx xxxxxxxx). Předkládá-li xxxxxxxxxxx xxxxxxx xxxxxxxx, musí xxx uvedeno xxxxx xxxxxxx xxxxxxxx. |
|
x) |
Xxxxxxxxxxxx doplňkové xxxxx Xxxxxxxxxxxx xxxxxxxxx xxxxx xxxxxxxx shrnutí požadovaných xxxxxxxxx podle xxxxxxx&xxxx;XX xxxx&xxxx;XXX xxxxx xxxxx xxxxxxxx xxxxxxxxx xxxxx. Xxxxxxxxx: xxxxx doplňkové xxxxx, navrhované zařazení xx kategorie x&xxxx;xxxxxxx xxxxxxx, xxxxxx druhy/kategorie xxxxxx a dávky. |
|
c) |
Způsob xxxxxx x&xxxx;xxxxxx xxxxxxx Xx nutno xxxxxx výrobní postup. Je xxxxx popsat xxxxxx xxxxxxx xxxxxxxxxxxx metod, xxx xxxx být xxxxxxx pro xxxxxxx xxx xxxxxx kontroly xxxxxxxxx látky xxxx xxxxxx, x&xxxx;xxxxxxxxx a krmivech xxxxx xxxxxxxxx xxxx xxxxxxx a přílohy III. Popřípadě xx na základě xxxxxxxxx xxxxxxxxxxxx v souladu x&xxxx;xxxxx přílohou x&xxxx;xxxxxxxx&xxxx;XXX xxxxx xxxxxx xxxxxx (xxxxx) použitých x&xxxx;xxxxxxx xxx xxxxxx xxxxxxxx xxxxxxxxxxx xxxxx xxxx xxxxxx metabolitů v potravinách xxxxxxxxxxx xxxxxx. |
|
x) |
Xxxxxx xxxxxxxxxxx x&xxxx;xxxxxxxxx doplňkové xxxxx Xx xxxxx xxxxx závěr x&xxxx;xxxxxxxxxxx x&xxxx;xxxxxxxxx xxxxxxxxx xxxxx na xxxxxxx xxxxxxx provedených xxxxxx. Xxxxxxxx xxxxxx mohou xxx xxxxxxx x&xxxx;xxxxxx xxxxxxx xx podporu xxxxxx xxxxxxxx(x). Ve xxxxxxx xx xxxx xxx xxxxxxx pouze xxxxxx xxxxxxxxxx xxxxx xxxxxxx&xxxx;XXX. |
|
x) |
Xxxxxxxxxx podmínky pro xxxxx Xxxxxxx(x)&xxxx;xxxxxxxx xxxxx podmínek xxx xxxxx. Xxxxxxx xxxxxxx xxxxxx obsah xxxxxxx xx vodě xxxx krmivu xxxxx x&xxxx;xxxxxxxxxx podmínkami xxx xxxxx x&xxxx;xxxxxxxxxxx krmivech. Xxxxxxxx xx xxxxxx xxxxxxxxx, xxx xx xxxxxxxxx jiné xxxxxxx xxxxxxxx xxxx zapracování xx xxxxxx xxxx xxxx. Je nutno xxxxxx případné zvláštní xxxxxxxx xxx užití (xxxx. nesnášenlivosti), zvláštní xxxxxxxxx na označování x&xxxx;xxxxx xxxxxx, pro xxx xx xxxxxxxxx xxxxx xxxxxx. |
|
x) |
Xxxxx xxxxx xxxxxxxxxxxx v období po xxxxxxx xxxxx xx xxx Xxxx xxxx xx xxxxxxxx xxxxx xx xxxxxxxxx látky, které xxxxx xx.&xxxx;7 xxxx.&xxxx;3 xxxx.&xxxx;x)&xxxx;xxxxxxxx (XX) x.&xxxx;1831/2003 xxxxxxx do xxxxxxxxx&xxxx;x)&xxxx;xxxx&xxxx;x)&xxxx;x&xxxx;xx.&xxxx;6 xxxx.&xxxx;1 xxxxx xxxxxxxx, x&xxxx;xx xxxxxxxxx xxxxx, xxxxx xxxxxxx xx xxxxxxx xxxxxxxxxx xxxxx Xxxxxxxxxxxx x&xxxx;xxxxxxx na xxx produktů, které xx xxxxxxxx z geneticky xxxxxxxxxxxxxx xxxxxxxxx nebo xxxxxxxxx xxxxxxxxxxxx xxxxxxxxx xxxxxxxx nebo xxxx x&xxxx;xxxx xxxxxxxx. |
1.2&xxxx;&xxxx;&xxxx;Xxxxxxx xxxxxxx xxxxxxxxxxx
Xx xxxxx xxxxxxxxxx xxxxxxx xxxxxxx xxxxxxxxxx xxxxx o každé části xxxxxxxxx poskytnutých xx xxxxxxx xxxxxxx podle xxxx xxxxxxx a přílohy III. Xxxx shrnutí xxxxxxxx xxxxxx xxxxxxxx xxxxxxxxx (xxxxxxxx).
Xxxxxxx xxxx xxxxxxx xxxxxx xxxx přílohy x&xxxx;xxxxxxx xx xxxxx xxxxxxxxxxxx xxxxxx x&xxxx;xxxxxxx xx xxxxxxxxx xxxxxx xxxxxxxxxxx.
1.3&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxxx a ostatních xxxxx
Xxxxxxx xxxx xxxxx xxxxx a názvy xxxxxx xxxxxxxxxxx předložené xx xxxxxxx žádosti. Je xxxxx xxxxxxxx podrobný xxxxx x&xxxx;xxxxxxx xx xxxxxx x&xxxx;xxxxxx.
1.4&xxxx;&xxxx;&xxxx;Xxxxxx xxxxx xxxxxxxxxxx, s nimiž má xxx xxxxxxxxx xxxx x&xxxx;xxxxxxxxx údaji
Seznam xxxxxxxx xxxxx xx xxxxxxxxx xxxxxx x&xxxx;xxxxxx dokumentace.
2. ODDÍL II: XXXXXXXX, XXXXXXXXXXXXXXX X&xxxx;XXXXXXXX XXX UŽITÍ XXXXXXXXX XXXXX; METODY XXXXXXX
Xxxxxxxxx xxxxx xxxx být xxxx xxxxxxxxxxxxxx x&xxxx;xxxxxxxxxxxxxxxx.
2.1&xxxx;&xxxx;&xxxx;Xxxxxxxx xxxxxxxxx xxxxx
2.1.1&xxxx;&xxxx;&xxxx;Xxxxx xxxxxxxxx xxxxx
Xxxxxxxx xx uvede xxxxxxxxxx xxxxxxxx název xxxxxxxxxxx látek xxxxxxxx xx xxxxxxxx xxxxxxxx.
2.1.2&xxxx;&xxxx;&xxxx;Xxxxx xx xxxxxxxx
Xx nutno xxxxxxxxx xxxxx na xxxxxxxx xxxxxxxxx xxxxx xx xxxxx či xxxxxxxx kategorií a funkčních xxxxxx xxxxx xxxxxx xxxxxxxx xxxxxx x&xxxx;xxxxxxx x&xxxx;xxxxxxx&xxxx;6 x&xxxx;xxxxxxxx&xxxx;X&xxxx;xxxxxxxx (XX) x.&xxxx;1831/2003.
Xxxx xxx xxxxxxxxxx xxxxx z jiných xxxxxxx xxxxxxx xxxxxxxxxxx xxxxxxxx xxxxx xxxx xxxxxxx (xxxx. užití v potravinách, xxxxxxxx xxxx veterinárním xxxxxxxxx, zemědělství a průmyslu). Xx xxxxx uvést xxxxxxxx xxxx xxxxxxxx xxxx doplňková xxxxx xxxx potravinářská přídatná xxxxx, xxxxxxxxxxx xxxxxx xxxxxxxxx xxxx xxxx xxxx xxxxxxxx xxxxxx xxxxx.
2.1.3&xxxx;&xxxx;&xxxx;Xxxxxxxxxxxx a kvantitativní xxxxxxx (xxxxxx xxxxx/xxxxxxx, jiné xxxxxx, xxxxxxxxx, variabilita xxxxxxxxxxxx šarží)
Je xxxxx xxxxx xxxxxxx xxxxx(x)/xxxxxxx(x)&xxxx;x&xxxx;xxxxxxx xxxxxxx xxxxxx doplňkové xxxxx x&xxxx;xxxxxxxx hmotnostního xxxxxx x&xxxx;xxxxxxx xxxxxxxx. Xx xxxxx xxxxxxxx xxxxxxxxxxxx x&xxxx;xxxxxxxxxxxxx variabilitu xxxxxxxxxxxx xxxxx xxxxxx xxxxx (látek) / xxxxxxx (činidel).
Pro mikroorganismy: xx nutno stanovit xxxxx životaschopných buněk xxxx spor xxxxxxxxx xxxx XXX na xxxx.
Xxx xxxxxx: xx xxxxx xxxxxx všechny xxxxxxx (xxxxxx) aktivity x&xxxx;xxxxx xxxxxxxx xxxxxxxx x&xxxx;xxxxx xxxxxxx xxxxxxxx. Xx xxxxx xxxxxx xxxxxx xxxxxxxx vedlejší xxxxxxxx. Xxxxxx xx xxxxxxxx xxxxxxxx, xxxxx xxxxx jako μxxxx xxxxxxxx uvolněné xx xxxxxx xx substrátu, xxxxxx s uvedením xX x&xxxx;xxxxxxx.
Xx-xx xxxxxx složka xxxxxxxxx látky xxxxx xxxxxxxx látek nebo xxxxxxx, přičemž xxxxxxx xxx xxxxxxxxxxx xxxxxxxxx (xxxxxxxxxxxx x&xxxx;xxxxxxxxxxxxx), xxxx xxx xxxxxx účinné xxxxx (látek) / xxxxxxx (činidel) xxxxxxx xxxxxxxxxx x&xxxx;xxxxxxxx xxxxxx x&xxxx;xxxx xxxxx.
Xxxxxxx xxxxx, xxxxxxx xxxxxx xxxxx xxxxxx xxxxxx xxxxxxxxx xxxxxxx a/nebo xxxx xxxxx všechny xxxxxx xxxxxxxxxxxxx, musí xxx xxxxxxxxxxxxxxxx podle xxxxxx (xxxxxx) přispívajících x&xxxx;xxxx xxxxxxxx x/xxxx xxxxx xxxxxxx xxxxxx xxxxxx (xxxxxx).
Xxxx xx dotčena xxxxxxxx žádost o doplňkové xxxxxxxxx xxxxxxxxxx xxxxxx xxxxx xx.&xxxx;8 xxxx.&xxxx;2 xxxxxxxx (ES) č. 1831/2003, xxxxxxx xxxx vynechat xxxxx xxxxxxxxx xxxxxx, xxxxx xxxxxxxxxxxxx xxxxxxxxxxxx xxxxxx, xxxxxx xxx xxxxxx látky xxxx xxxxxxx x&xxxx;xxxxxxx xxxxxxxxxxx xxxxx, které xxxxxx xxxxxxxx x&xxxx;xxxxxxxxxxx zootechnických xxxxxxxxxxx látek, xxxxxxxxxxxxxx x&xxxx;xxxxxxxxxxxxxxx a na xxx xx nevztahuje xxxxxx xxxxxxxxxx xxxxxxxx (ES) x.&xxxx;1829/2003. Všechny xxxxxx xxxxxxx v dokumentaci musí xxx každopádně založeny xx xxxxxxxxx doplňkové xxxxx, pro niž xx požaduje xxxxxxxx, x&xxxx;xxxxx xxxxxxxxxx xxxxxxxxx x&xxxx;xxxxxx xxxxxxx odlišných xxxxxxxxxxx. Je možno xxxxxxx interní xxxxxxxxxxxxx xxxxxxxx v dokumentech třetích xxxxx x&xxxx;xx xxxxx xxxxxxx xx xxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx a potvrzení, xx xx xxxxxxxxxxxxx(x)&xxxx;xxxxxxxx(x)&xxxx;xx xxxxxxx, xxx xxx xx xxxxxx žádost.
2.1.4 Čistota
Žadatel xxxxxxxxxxxx a vyčíslí xxxxxxxx x&xxxx;xxxxxxxxxxx xxxxxxxxx, látky x&xxxx;xxxxxxxxx nebo jinými xxxxxxxxxxx xxxxxxxxxxx, které xxxxxx přidány xxxxxxx x&xxxx;xxxxxxxxxxxx x&xxxx;xxxxxxxx xxxxxxxxx xxxxx. U produktů xxxxxxxxxxxxx xxxxxxx xxxxxxx xxxxxxx xxxxxxxxxxxx xxxxxxxxxxx organismů x&xxxx;xxxxxxxxx xxxxx. Xx xxxxx popsat xxxxxxxx xxxxxxxxx x&xxxx;xxxxxxx xxxxxxxx xxxxxxxxx xxxxx x&xxxx;xxxxxxx xx xxxxxxxxxxxx xxxxx x&xxxx;xxxxxxxxx.
Xxxxxxx poskytnuté xxxxx xxxx xxxxxxxx návrh xx xxxxxxxxxxx doplňkové xxxxx.
Xxxx xxxx xxxxxxx xxxxxxxx požadavky x&xxxx;xxxxxxxxxx xx xxxxxxxx postupu, xxxxx odpovídají stávajícím xxxxxxx xxxxxxxxx Xxxxxxxxxxxx.
2.1.4.1&xxxx;&xxxx;&xxxx;Xxxxxxxxx xxxxx, xxxxxxx xxxxxxxx xx vázané xx xxxxxxxx xxxxxxxx
X&xxxx;xxxxxxxxxxx xxxxx, xxxxxxx xxxxxxxx xx xxxxxx xx xxxxxxxx xxxxxxxx, xx nutno xxxxx xxxxxxxxx xxxxxxxxx xxxxxxxx se zvláštního xxxxxxx xxxxxxxxx výrobcem xx xxxxxxx xxxxxxxxxxx xxxxx xxxxxxxxxxx k jiným xxxxxxxxxxxx xxxxxx. Xx xxxxx použít xxxxxxxxxxx Xxxxxxxxxx výboru xxxxxxxxx XXX/XXX xxx potravinářské xxxxxxxx látky (XXXXX) xxxx specifikace x&xxxx;xxxxxxxx Xxxxxxxxxx společenství pro xxxxxxxxxxxxx xxxxxxxx xxxxx.
2.1.4.2&xxxx;&xxxx;&xxxx;Xxxxxxxxx xxxxx, xxxxxxx xxxxxxxx xxxx xxxxxx xx xxxxxxxx xxxxxxxx
X&xxxx;xxxxxxxxxxx látek, xxxxxxx povolení xxxx xxxxxx xx xxxxxxxx xxxxxxxx, je xxxxx xxxxxx stávající xxxxx xxxxxxxxx k jiným xxxxxxxxxxxx xxxxxx xxxx xxxxx xx xxxxxxxxxxxxx xxx xxxxxxxxxxxxx xxxxxxxx látky xxxxxxxx v Evropském xxxxxxxxxxxx xxxx JECFA. Nejsou-li xxxxxx xxxxx xxxxxxxx xxxx xx-xx to xxxxxxxx xxx xxxxxxx xxxxxx, xx xxxxx xxxxxx xxxxxxxxxxxx xxxx xxxxxxx xxxxx x&xxxx;xxxxxxxx xxxxxxxxxxx:
|
— |
xxx xxxxxxxxxxxxxx: xxxxxxxxxxxxxxx xxxxxxxxxxx, mykotoxiny, xxxxx xxxx; |
|
— |
xxx xxxxxxxx xxxxxxxxxxxxx xxxxxxx (které xxxxxxxxxx xxxxxxxxxxxxxx jako xxxxxx xxxxxxx): xx nutno xxxxxxx xxxxxx xxxxxxxxx xxxx pro xxxxxxxx xxxxxxxxxxxxxx (viz xxxx). Xx nutno uvést xxxxxx xxxxxx, x&xxxx;xxxx xx do xxxxxxxx xxxxxxxx xxxxxxxxxxx použité xxxxxxxxxx xxxxxx; |
|
— |
xxx látky xxxxxxxxxxx xxxxxx: xxxxxxxxxxxxxxx x&xxxx;xxxxxxxxx xxxxxxxxxxx (xxxxxxx xxxx. skočec xxxxxx, xxxxxx xxxxxxx, xxxxx xxxxx), xxxxxxxxxx, xxxxxxxxxxx xxxxxxxxx, xxxxxxxxx hodnoty xxx rozpouštědla x&xxxx;xxxxxxxxx xxxxxxxxxxxxx xxxxxxxx látky, x&xxxx;xxxxx je známo, xx se xxxxxxxxx x&xxxx;xxxxxxx rostlině; |
|
— |
pro xxxxx xxxxxxxxxxx původu: xxxxxxxxxxxxxxx xxxxxxxxxxx, těžké xxxx x&xxxx;xxxxxxxxx xxxxxxxxx hodnoty xxx rozpouštědla; |
|
— |
pro minerální xxxxx: xxxxx xxxx, xxxxxxx x&xxxx;XXX; |
|
— |
xxx xxxxxxxx xxxxxxxx chemickou syntézou x&xxxx;xxxxxxxxxx procesy: xxxx xx xxxxxxx xxxxxxxx xxxxx použité x&xxxx;xxxxxxxxxxxx xxxxxxxxx a případné xxxxxxxxxxxx xxxxxxxxxxx x&xxxx;xxxxxxx produktu x&xxxx;xxxxx xx jejich xxxxxxxxxxx. |
Xxxxxxxxx xx xxxxxxx xxxxxxx xxxxxxxxxx pro xxxxxxx xxxxx xxxxxxx xxxxxx.
2.1.5&xxxx;&xxxx;&xxxx;Xxxxxxxxx xxxxxxxxxx xxxxxxxxxxxx xxxxx produktu
U přípravků v tuhém xxxxx xx xxxxxxxxx xxxxx x&xxxx;xxxxxxxxx xxxxx xxxxxxxxx xxxxxx, xxxxx xxxxxx, xxxxxxx, xxxxxxxx xxxxxxx, protiprašných vlastnostech x&xxxx;xxxxxxx xxxxxxx, xxxxx xxxx xxxx xx xxxxxxxxx vlastnosti. U přípravků x&xxxx;xxxxxxxx xxxxx se xxxxxxxxx xxxxx o viskozitě x&xxxx;xxxxxxxxxx xxxxxx. Xxxxx xx doplňková látka xxxxxx x&xxxx;xxxxxxx xx xxxx, xx xxxxx xxxxxxxx rozpustnost xxxx xxxxxx xxxxxxxx.
2.2&xxxx;&xxxx;&xxxx;Xxxxxxxxxxxxxxx xxxxxx xxxxx (xxxxx) / xxxxxxx (xxxxxxx)
2.2.1&xxxx;&xxxx;&xxxx;Xxxxx
Xx xxxxx xxxxx xxxxxxxxxxxx xxxxx xxxxxx látky xxxx xxxxxxx. Xx xxxxxxxx xxxxxxx a původ xxxxx xxxx xxxxxxx a jiné xxxxxxxx charakteristiky.
2.2.1.1 Chemické xxxxx
Xxxxxxxx xxxxxx xxxxxxxxxx xxxxx xx xxxxx xxxxxx xxxxxxxx xxxxxx, xxxxxxxxx xxxxxxxxx xxxxx názvosloví XXXXX (Xxxxxxxxxxxxx Xxxxx xx Xxxx xxx Xxxxxxx Xxxxxxxxx), xxxxxxx xxxxxxxxxxxxx druhovými xxxxx x&xxxx;xxxxxxxxx x/xxxx číslem XXX (Xxxxxxxx Abstract Xxxxxxx). Xx nutno xxxxx xxxxxxxxxxxx x&xxxx;xxxxxxxxx xxxxxx x&xxxx;xxxxxxxxxxx xxxxxxxx.
X&xxxx;xxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxxxx xxxx xxxxxxxxxxx látka xx nutno xxxxx xxxxx FLAVIS xxxxx x&xxxx;xxxxxxxxxx chemickou xxxxxxxx. X&xxxx;xxxxxxxxxxx xxxxxxx xx xxxxx xxxxx fytochemické xxxxxxx.
Xxxxx, x&xxxx;xxxxx nelze xxxxxx popsat jedním xxxxxxxxx vzorcem x/xxxx x&xxxx;xxxxx xxxxx xxxxxxx xxxxxx xxxxxxxxxxxxx, xx xxxxx xxxxxxxxxxxxxxx xxxxx xxxxxx (xxxxxx) přispívajících x&xxxx;xxxx aktivitě x/xxxx xxxxx xxxxxxxxx hlavních xxxxxx. Xx xxxxx xxxxxxxxxxxxx markerovou sloučeninu, xxx bylo xxxxx xxxxxxxx xxxxxxxxx x&xxxx;xxxxxxxx xxxxxxxxxxxxxx.
Xxx xxxxxx x&xxxx;xxxxxxxxx xxxxxx xx xxxxx xxx xxxxxx xxxxxxxx xxxxxxxx xxxxx xxxxx x&xxxx;xxxxxxxxxxxx název xxxxxxxxxx Xxxxxxxxxxx xxxx biochemie (XXX) x&xxxx;xxxxxxxxx xxxxxx „Xxxxxxxxxx xxxxxx“. U aktivit xxxxx xxxxxxxxxxxx se xxxxxxx xxxxxxxxxxxx xxxxx xxxxxxxxxxxx pravidlům xxxxxxxxxx XXX. Obecné názvy xxxx přípustné za xxxxxxxxxxx, xx xxxx xxxxxxxxxxx x&xxxx;xxxx xxxxxxxxx xxxxxxxxxxxx x&xxxx;xxxx dokumentaci x&xxxx;xxx xxxxxx xxxxx xxxxxx xx xxx xxxxxxxxxxx xxxxxxxxx na xxxxxxxxxxxx název a číslo XXX. Xx nutno xxxxx biologický xxxxx xxxxx xxxxxxxx xxxxxxxx.
Xx xxxxx xxxxxx xxxxxx xxxxxxxxxxx xxxxx xxxxxxxxxx xxxxx vzniklých xxxxxxxxxx (xxx xxx&xxxx;2.2.1.2 Xxxxxxxxxxxxxx).
2.2.1.2&xxxx;&xxxx;&xxxx;Xxxxxxxxxxxxxx
Xx xxxxx xxxxx původ xxxxx xxxxxxxxxxxxxx xxxxxxxxxxx xxxx xxxxxxx nebo xxxxxxx xxxx.
X&xxxx;xxxxxxxxxxxxxx xxxxxxxxxxx xxxx xxxxxxx nebo xxxx xxxxxxx xxxx xx xxxxx xxxxx xxxxxxxx xxxx. Xxxxx xx název x&xxxx;xxxxxxxxxxx xxxxxxxxxxx xxxxxxx xxxxxxxxxxxxxx xxxxx xxxxxxxxxxxx zveřejněných xxxxx v mezinárodních xxxxxxxxxxxxxxx xxxxxx (XXX). Mikrobiální xxxxx musí xxx xxxxxxx v mezinárodně xxxxxxxx xxxxxx xxxxxx (pokud xxxxx v Evropské xxxx) x&xxxx;xxxxxxxxxx xxxxxxx xxxxxx xx povolenou xxxx xxxxxxxxx xxxxxxxxx xxxxx. Xx xxxxx xxxxxxxxx xxxxxxxxx o uložení xx xxxxxx, xxxxx upřesňuje xxxxxxxxx číslo, pod xxxxxx xx kmen xxxxxx. Xxxx xx xxxxx xxxxxx xxxxxxx xxxxxxxxxx xxxxxxxxxxxx, fyziologické x&xxxx;xxxxxxxxxxx charakteristiky xxxxxxxx xxx jedinečnou identifikaci xxxxx x&xxxx;xxxxxxxxxx xxxxxxxxx xxxx xxxxxxxxx stability. X&xxxx;xxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxx xx xxxxx xxxxx xxxxxxxxxxx xxxx. Pro xxxxx xxxxxxxxx modifikovaný xxxxxxxxxx se uvede xxxxxxxxxxx identifikační xxx xxxxx xxxxxxxx Komise (XX) x.&xxxx;65/2004 ze xxx 14.&xxxx;xxxxx 2004, xxxxxx xx xxxxxxx xxxxxx xxxxxx a přiřazování xxxxxxxxxxxxx xxxxxxxxxxxxxxx kódů xxx xxxxxxxxx xxxxxxxxxxxx xxxxxxxxx.
2.2.2&xxxx;&xxxx;&xxxx;Xxxxxxxx xxxxxxxxxx
2.2.2.1&xxxx;&xxxx;&xxxx;Xxxxxxxx xxxxx
Xx xxxxx xxxxx xxxxx xxxxxxxxxxx a chemických vlastností. Xxxxxxxxx rozkladu, pKa, xxxxxxxxxxxxxxx xxxxxxxxxx, xxx xxxx, xxx xxxx, xxxxxxx, tlak xxx, xxxxxxxxxxx xx vodě x&xxxx;x&xxxx;xxxxxxxxxxx rozpouštědlech, Xxx x&xxxx;Xx/Xxx, hmotnostní xxxxxxxxxxxxx x&xxxx;xxxxxxxxx xxxxxxx, xxxxx XXX, případné izomery x&xxxx;xxxxxxxxx xxxx xxxxxxxx xxxxxxxxx vlastnosti xxxx xxx xxxxxxx, kde xx xx xxxxxx.
Xxxxx xxxxxxx prostřednictvím xxxxxxxxxxxxx xxxxxxx nesmí xxxxxxxxx xxxxxxxxxxxxxxx xxxxxxxx xxxxxxxx xxx xxxxxxxxx antibiotik x&xxxx;xxxxxxx nebo xxxxxx.
2.2.2.2&xxxx;&xxxx;&xxxx;Xxxxxxxxxxxxxx
|
— |
Xxxxxx x&xxxx;xxxxxxx xxxxxxxxx Xx xxxxx xxxxxxxx xxxxxxxxxxx xxxxxx xxxx xxxxxxx xxxxxxxxx xxxx xxxxxx xxxxxxxxxxxx. Xxxxx bakterií náležející xx taxonomické xxxxxxx, xxxxx xxxxxxxx xxxxxxxxxxx, x&xxxx;xxxxx xx známo, xx mohou xxxxxxxxxx xxxxxx xxxx jiné xxxxxxx virulence, xx xxxxx podrobit odpovídajícím xxxxxx x&xxxx;xxxxx prokázat xx molekulové x&xxxx;xxxxxxxxx xxxxxxx xxxxxx, xx xxxxxxxxxx důvod x&xxxx;xxxxxx. X&xxxx;xxxxx xxxxxxxxxxxxxx, xxx xxx xxxxxx x&xxxx;xxxxxxxxx údaje x&xxxx;xxxxxxx bezpečném používání x&xxxx;xxxxxxx xxxxxxxx xxxx xxxxx xxxxxxxxxx xxxxx, xx xxxxxxxx celý xxxxxxx xxxxxxxxxxxxxxx studií. |
|
— |
Produkce xxxxxxxxxx x&xxxx;xxxxxxxxxx xxxx xxxxxxxxxxxx Xxxxxxxxxxxxxx používané xxxx xxxxxxxxx xxxxx xxxx xxxx výrobní xxxx xxxxx xxxxxxxxx xxxxxxxxxxxxx xxxxxxxx xxxx xxxxx xxx schopny xxxxxxxxxx xxxxxxxxxxxx xxxxx, které xxxx xxxxxxxx xxxx xxxxxxxxxxx x&xxxx;xxxxxxx x&xxxx;xxxxxx. Xxxxx xxxxxxxxxxxxxx xxxxxx x&xxxx;xxxxxxx xxxx xxxxxxxxx xxxxx xxxxx dále xxxxxxxxx x&xxxx;xxxxxx xxxx xxxxxxxxxx xxxx xxxxxxxxxxxx, xxxxx xx již vyskytují x&xxxx;xxxxxxx xxxxx zvířat x&xxxx;x&xxxx;xxxxxxxx xxxxxxxxx. Xxxxxxx xxxxx bakterií xx xxxxx xxxxx otestovat xx xxxxxxxxxx xxxx xxxxxxxxxxxx používaným x&xxxx;xxxxxxxx x&xxxx;xxxxxxxxxxxx xxxxxxxxx. Xx-xx xxxxxxxx rezistence, je xxxxx xxxxxxx xxxxxxxxx xxxxxx rezistence x&xxxx;xxxxxxxxxxxxxxx xxxxxxx xxxxxxxxxx xx xxxxxxx xxxxxxxxx ve xxxxxxxx. Xxxxx xxxxxxxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxxxxxxxx rezistenci xx xxxxx xxxxxxxx xxxx xxxxxxxxx látky, xxxxx-xx xxxxxxxx, xx xxxxxxxxxx je výsledkem xxxxxxxxxxxx mutace(í) a není xxxxxxxx. |
2.3&xxxx;&xxxx;&xxxx;Xxxxxxx xxxxxx, xxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxx
Xx stanovení xxxxxxxxxx xxxx xxxxxxx, xxxxx mohou xxx xxxx xx xxxxxxx xxxxxx xxxxx / xxxxxxx (xxxxxxx) xxxx xxxxxxxxx látky, xx xxxxx popis xxxxxxxxx xxxxxxx. Je nutno xxxxxxxxx listy x&xxxx;xxxxx x&xxxx;xxxxxxxxxxx xxxxxxxxx x&xxxx;xxxxxxxxxx xxxxx xxxxxxxxxxx ve xxxxxxxx postupu.
2.3.1 Účinná látky(y) / činidlo(a)
Je xxxxx xxxxxxxxxx xxxxx výrobního xxxxxxx (xxxx. chemická xxxxxxx, xxxxxxxxxx, kultivace, xxxxxxxx x&xxxx;xxxxxxxxxxx xxxxxxxxx xxxx destilace) xxxxxxxxx xxx xxxxxxxx xxxxxx xxxxx (xxxxx) / xxxxxxx (xxxxxxx) xxxxxxxxx xxxxx, xxxxxxxx xxxxxxxxxxxxxxx xxxxxxxxxxx xxxxxxxx. Xxxxx xx složení fermentačního/kultivačního xxxxx. Je xxxxx xxxxxx xxxxxxxx xxxxxx xxxxxxx.
X&xxxx;xxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxxxxxxx (XXX) používaných xxxx xxxxx doplňkových látek x&xxxx;xxxxxxxxxxxxx za podmínek xxxxxxxxxx xxxxxxxxx xx xxxxxxx směrnice Rady 90/219/XX&xxxx;(5). Je xxxxx xxxxx xxxxx xxxxxxxxxxxxx xxxxxxx (xxxxxx pro xxxxxxx, xxxxxxxxxxx xxxxxxxx x&xxxx;xxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxxxxxx xxxxxxx).
2.3.2&xxxx;&xxxx;&xxxx;Xxxxxxxxx látka
Předloží xx xxxxxxxx xxxxx xxxxxxxxx xxxxxxx xxxxxxxxx xxxxx. Xx nutno xxxxx hlavní stupně xxxxxx doplňkové látky, xxxxxx míst (xxxxx) xxxxxxxxxxx účinné xxxxx (xxxxx) / xxxxxxx (xxxxxxx) x&xxxx;xxxxxx xxxxxx x&xxxx;xxxxxxx xxxxxxxx stupně xxxxxxxxxx, které xxxx xxxx xx xxxxxxxx xxxxxxxxx xxxxx, xxxxxxxx xxxxxxxxxxxxxxx xxxxxxxxxxx xxxxxxxx.
2.4&xxxx;&xxxx;&xxxx;Xxxxxxxxx-xxxxxxxx x&xxxx;xxxxxxxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxx
2.4.1&xxxx;&xxxx;&xxxx;Xxxxxxxxx
Xxxxxxxxx je xxxxxxx xxxxxx xxxxxxxxxxx sledováním xxxxxx xxxxx (xxxxx) / činidla (činidel) xxxx xxxx (jeho) xxxxxxxx/xxxxxxxxxxxxxxxx. X&xxxx;xxxxxx lze xxxxxxxxx xxxxxxxxx s ohledem xx ztrátu xxxxxxxxxxx xxxxxxxx; x&xxxx;xxxxxxxxxxxxxx x&xxxx;xxxxxxx xx xxxxxx životaschopnosti; x&xxxx;xxxxxxxxxxxxx xxxxx x&xxxx;xxxxxxx xx ztrátu chuti. X&xxxx;xxxxxxxxx xxxxxxxxxx směsí/extraktů xxx xxxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxxxx jedné xxxx několika xxxxxxxx xxxxxxxxxxxxxx xxxxx.
Xxxxxxxxx xxxxxxxxx xxxxx
Xx xxxxx přezkoumat xxxxxxxxx xxxxxxx xxxxxxx xxxxxxxxx xxxxx xxx xxxxxxxx podmínek xxxxxxxx xxxxxxxxx (světlo, xxxxxxx, xX, vlhkost, xxxxxx x&xxxx;xxxxxxx xxxxxxxxx). Předpokládaná xxxxxxxxxxx doplňkové xxxxx x&xxxx;xxxxxxxxxxxxxx xxxxx by xxxx xxx xxxxxxxx xx xxxxxxx xxxx xxxxxxxxxx xxxxxxxxx xxxxxxxxxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxx xxx xxxxx (xxxx. 25&xxxx;xX, 60&xxxx;% xxxxxxxxx xxxxxxx xxxxxxx a 40 oC, 75&xxxx;% relativní xxxxxxx xxxxxxx).
Xxxxxxxxx doplňkové xxxxx xxxxx x&xxxx;xxxxxxxxx x&xxxx;xxxxxxxx
X&xxxx;xxxxxxxxxxx xxxxx užitých v premixech x&xxxx;xxxxxxxx s výjimkou zchutňujících xxxxxx se xxxxxxxxx xxxxxxx složení doplňkové xxxxx ověří xx xxxxxxx xxxxxxxxx x&xxxx;xxxxxxxxxxxx xxxxxxxx premixů x&xxxx;xxxxx. Xxxxxx stability xxxxxxx xxxx trvat xxxxxxx xxxx xxxxxx. Xxxxxxxxx xx xxxxxxx xxxxx xxxxx u premixů xxxxxxxxxxxx xxxxxxx xxxxx; x&xxxx;xxxxxxx xxxxxxx xx doplňková xxxxx xxxx xxx xxxxxxxx xxxxxxx „nemíchat xx xxxxxxxxx xxxxx“.
Xxxxxx xxxxxxxxx x&xxxx;xxxxx xxxxxx xxxxxxxx xxxxxxx xxx xxxxxx. Obvykle xx xxxxxxxxx xxxxxxxxxx u krmiv xx formě kaše x&xxxx;xxxxxxxxxxxx xxxxx (xxxxxx xxxxx peletování nebo xxxxxx xxxxx úpravy) xxx xxxxxx xxxxxxx xxxxx zvířat.
U doplňkových xxxxx xxxxxxxx x&xxxx;xxxxxxx xx xxxx xx xxxxx xxxxxxxxx xxxxxxx xxxxxxx xxxxxxxxx xxxxx xxxxxx xx xxxx xx xxxxxxxx xxxxxxxxxxxx xxxxxxx x&xxxx;xxxxx.
Xxxxx-xx xx xxxxxx xxxxxxxxx a ve vhodných xxxxxxxxx xx nutno xxxxxxxxxxxxxxx xxxxxxxx produkty xxxxxxxxx xxxx xxxxxxxx.
Xx xxxxx xxxxxxxxxx xxxxx x&xxxx;xxxxxx, xxxxx zahrnují xxxxxxx xxxxx xxxxxxxxxx xx začátku a jedno xx xxxxx xxxx xxxxxxxxxx.
X&xxxx;xxxxxxx xxxxxxx xxxxxx xxxxxxxx podrobné xxxxxxxxxxxxx x&xxxx;xxxxxxxxxxxx složení xxxxxxx xxxx krmiv použitých xxx xxxxxxx.
2.4.2&xxxx;&xxxx;&xxxx;Xxxxxxxxxx
Xx nutno xxxxxxxx xxxxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxx (xxxxx xxxxxxxxxxxxx složek) x&xxxx;xxxxxxxxx, xxxxxxxx xxxx xx xxxx.
2.4.3&xxxx;&xxxx;&xxxx;Xxxxxxx vlastnosti
Je xxxxx popsat xxxxxxx xxxxxxxxxx, například xxxxxxxxxxx x&xxxx;xxxxxxxxxxxxxxx xxxxxxxxxx nebo xxxxxxxxx disperze v kapalinách.
2.4.4 Fyzikálně-chemické xxxxxxxxxxxxxxx nebo xxxxxxxxx
Xx xxxxx xxxxx fyzikálně-chemické xxxxxxxxxxxxxxx xxxx xxxxxxxxx, x&xxxx;xxxx xx xxxxx xxxxx xx styku x&xxxx;xxxxxx, xxxxxx, xxxxxx xxxxxxxxxx doplňkovými xxxxxxx xxxx xxxxxxxx přípravky.
2.5 Podmínky xxx užití xxxxxxxxx xxxxx
2.5.1&xxxx;&xxxx;&xxxx;Xxxxxxxxxx xxxxxx xxxxxxx xx xxxxxx zvířat
Je xxxxx uvést xxxx xxxx xxxxxxxxx xxxxxx, xxxxxxx xxxxxxx nebo xxxxxxxxx stadium xxxxxx x&xxxx;xxxxxxx s kategoriemi x&xxxx;xxxxxxx&xxxx;XX xxxxxx xxxxxxxx. Je xxxxx xxxxxx xxxxx xxxxxxxxxxxxxx. Xxxxx se xxxxxxxxxx xxxxxxx v krmivu xxxx ve vodě.
Je xxxxx xxxxx navrhovaný xxxxxx xxxxxxxx a zapracování xxx xxxxxxx, xxxxxx xxxx xxxxxx xxxx. Xxxxx xx xxxxxxxxxx xxxxx x&xxxx;xxxxxxxxxx xxxxxx x&xxxx;xxxxxxxxxx xxxx xxxxxxxx x&xxxx;xxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxx. Xxxxx xx xxxxxxxx xxxxxxxxx xxxxxxx xxxxxxxxx látky v doplňkovém xxxxxx, xx xxxxx xxxxxxxxxx.
2.5.2&xxxx;&xxxx;&xxxx;Xxxxxxxxx xxxxxxxxxxx x&xxxx;xxxxxxxxxxx xxx xxxxxxxxx/xxxxxxxxxx
2.5.2.1&xxxx;&xxxx;&xxxx;Xxxxxxxx xxxxx
Xx xxxxx xxxxxxxxxx listy x&xxxx;xxxxx x&xxxx;xxxxxxxxxxx materiálu xx formátu odpovídajícím xxxxxxxxxx xxxxxxxx Komise 91/155/XXX xx xxx 5.&xxxx;xxxxxx 1991, kterou xx k provedení xxxxxx&xxxx;10 xxxxxxxx 88/379/EHS xxxxxxxx x&xxxx;xxxxxxx podrobná xxxxxxxx x&xxxx;xxxxxxx xxxxxxxxxxxx xxxxxxxxx xxx xxxxxxxxxx xxxxxxxxx&xxxx;(6). X&xxxx;xxxxxxx xxxxxxx je xxxxx xxxxxxxxx opatření xxx předcházení xxxxxxxxx xxxxxxx x&xxxx;xxxxxxxx prostředky xxx výrobě, xxxxxxxxxx, xxxxx x&xxxx;xxxxxxxxx.
2.5.2.2&xxxx;&xxxx;&xxxx;Xxxxxxxxxxxxxx
Xx xxxxx xxxxx klasifikaci xxxxx xxxxxxxx Evropského xxxxxxxxxx x&xxxx;Xxxx 2000/54/XX xx xxx 18.&xxxx;xxxx 2000 x&xxxx;xxxxxxx zaměstnanců před xxxxxx xxxxxxxxx x&xxxx;xxxxxxxx xxxxxxxxxxx činitelům xxx xxxxx (sedmá samostatná xxxxxxxx xx&xxxx;xxxxxx čl. 16 xxxx.&xxxx;1 xxxxxxxx 89/391/XXX)&xxxx;(7). X&xxxx;xxxxxxx xxxxxxxxxxxxxx xxxxxxxxxxxx xx xxxxxxx&xxxx;1 této xxxxxxxx je nutno xxxxxxxxxx xxxxxxxxxxxxx xxxxxxxxx, xxxxx xxx xxxxxx xxxxxxxx xxxxxxxxx xxxxxxxx xx xxxxxxx xxxxxxxxxx, xxx je xxxxxxxxx x&xxxx;xx.&xxxx;3 xxxx.&xxxx;2 xxxxxxx xxxxxxxx.
2.5.2.3&xxxx;&xxxx;&xxxx;Xxxxxxxxx na xxxxxxxxxx
Xxxx xxxx xxxxxxx ustanovení x&xxxx;xxxxxxxxxx x&xxxx;xxxxxx xxxxxxxx x&xxxx;xxxxxx&xxxx;16 xxxxxxxx (XX) x.&xxxx;1831/2003, je nutno xxxxx xxxxxxxx xxxxxxxxx xx xxxxxxxxxx x&xxxx;xxxxxxxxx xxxxxxxx podmínky xxx xxxxx x&xxxx;xxxxxxxxxx (xxxxxx xxxxxxx xxxxxxxxxxxxxxx a kontraindikací) x&xxxx;xxxxxx pro správné xxxxxxx.
2.6&xxxx;&xxxx;&xxxx;Xxxxxx analýzy a referenční xxxxxx
Xxxxxx analýzy xx xxxxxx ve xxxxxxxxxx xxxxxx xxxxx xxxxxxxxxx xxxxx XXX (xx. XXX 78-2).
Xxxxx xxxxxxxx (XX) č. 1831/2003 x&xxxx;xxxxxxxx (XX) x.&xxxx;378/2005 xxxxxx xxxxxxx uvedené x&xxxx;xxxxx xxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxx Společenství. Xxxxxxxxxx xxxxxxxxx Společenství xxxxxxxx xxxxx xxxxxxxxx zprávu, x&xxxx;xxx xx xxxxx, xxx xxxx tyto xxxxxx xxxxxx xxx xxxxxxx xx účelem xxxxxxxx kontrol doplňkové xxxxx, na niž xx žádost xxxxxxxx. Xxxxxxxxx xxxxxxxxxx laboratoře Xxxxxxxxxxxx xx zaměří xx metody xxxxxxxxx x&xxxx;xxxxxx&xxxx;2.6.1 x&xxxx;2.6.2.
Xxxxx xxx xxxxxxxx XXX xxx xxxxx, na xxx xx xxxxxxxx xxxxxxxx Xxxx (XXX) x.&xxxx;2377/90 xx xxx 26.&xxxx;xxxxxx 1990, xxxxxx xx xxxxxxx xxxxxx Společenství xxx xxxxxxxxx maximálních xxxxxx xxxxxxx veterinárních xxxxxxxx xxxxxxxxx x&xxxx;xxxxxxxxxxx xxxxxxxxxxx xxxxxx&xxxx;(8), nebude xxx&xxxx;2.6.2 xxxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxxx Společenství. Xxxxxxx xxxxxxx xxx&xxxx;2.6.2 xxxxxxxxxx xxxxxxx metodu, xxxxxxxxx x&xxxx;xxxxx (xxxxxx xxxxxxxxxxx aktualizací), xxx xxxx být xxxxxxxxxx Xxxxxxxx agentuře pro xxxxxx xxxxxxxxx (XXXX) x&xxxx;xxxxxxx s přílohou V nařízení (XXX) x.&xxxx;2377/90 x&xxxx;xxxxx dokumentu „Xxxxxx xx Xxxxxxxxxx xxx Xxxxxxxxxx“, xxxxxx&xxxx;8 „Xxxxx governing xxxxxxxxx xxxxxxxx in xxx Xxxxxxxx Xxxxx“.
X&xxxx;xxxxxxxxx xxxxx xxx xxxxxxxx rovněž xxxxxxxxxx metody popsané x&xxxx;xxxx&xxxx;2.6.3, pokud xx xxxxxxxxxx xxxxxxxxx Xxxxxxxxxxxx, xxxx nebo Xxxxxx xxxxxxxx za xxxxxxxx.
X&xxxx;xxxxxxx x&xxxx;xxxxxxxxx (ES) x.&xxxx;378/2005 xxxxxxx poskytne xxxxxxxxxx xxxxxx přímo xxxxxxxxxx xxxxxxxxxx Xxxxxxxxxxxx xxxx xxxxxxxxxxxx xxxxxxxxx dokumentace x&xxxx;xxxxxxxx vzorky xxxx xxxxxxxxx doby xxxxxxxxxxxxx.
Xxxxxxxx xxxxxx xx podrobné xxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxxx Xxxxxxxxxxxx x&xxxx;xxxxxxx x&xxxx;xxxxxxx&xxxx;12 nařízení (ES) x.&xxxx;378/2005.
2.6.1&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxx pro xxxxxxx xxxxx
Xx nutno xxxxxxxxxx podrobnou charakteristiku xxxxxxxxxxxx x&xxxx;xxxxxxxxx xxxxxxxxxxxxx xxxxxxxxxx metody (xxxxx) xxx xxxxxxxx, xxx xxxx xxxxxxxx xxxxxxxxx xxxx xxxxxxxxx xxxxxxxxxx xxxxxx xxxxxx xxxxx (xxxxx) / xxxxxxx (xxxxxxx) x&xxxx;xxxxxxxxx látce, xxxxxxxxx, xxxxxxxx x&xxxx;xxxxxxxxx xxxx.
|
2.6.1.1 |
Xxxx metody xxxxxxx xxxxxx požadavky xxxx x&xxxx;xxxxxxx metod xxxxxxx xxxxxxxxxxx xxx xxxxxx xxxxxxxx podle článku 11 xxxxxxxx (XX) x.&xxxx;882/2004. Xxxxxxx splňují xxxxxxx xxxxx z těchto xxxxxxxxx:
|
|
2.6.1.2 |
Podrobná xxxxxxxxxxxxxxx xxxxxx (metod) zahrnuje xxxxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxxxx x&xxxx;xxxxxxx&xxxx;XXX nařízení (ES) x.&xxxx;882/2004. |
|
2.6.1.3 |
Xxxxxxxx xxxxxxxxxxxxxxx metod xxxxxxxxxxxx xxxxxxx xx xxxxx xxxxxxxxxxx xxxxxx x&xxxx;xxxxx xxxxxxxxxxxx x&xxxx;xxxxxxxxx xxxxxxxxxx. Xxxxxxxxx se xxxxxxxx xxxxxx testů xxxxx x&xxxx;xxxxxxxxxx xxxxxxx xxxxxxxxxxx dokládajícími xxxxxxxxxxxxxx xxxxxx xx xxxxxx xxxxxxxxx xxxxxxxxx. X&xxxx;xxxxxx xxxxxxxxxxxx x&xxxx;xxxxxx xx xxxxxxxxx xxxxxxxxxxx xxxxxxxxxx xxxxxxxxx v případě, že xxxxx xxxxxxxxx je xxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxxxxxx laboratoří xxxxxxxxxxxxxx xxxxxxxxxx laboratoři Společenství, xxx je xxxxxxxxx x&xxxx;xxxxxxxx (ES) x.&xxxx;378/2005, xxxxxxx xxxxxxxxx xxxxx xxxxxxxxxx xxxxxxxxxx Společenství xxxxxxxxxx x&xxxx;xxxxxxx (xxxxxxx xxxxxxxxxx xxxxxxxxx Xxxxxxxxxxxx xxxxxx žádost) xxxxxxxxxx xxxxx xxxxxxxxxx x&xxxx;xxxxxxxxxxx x&xxxx;xxxxx žádostí x&xxxx;xxxxx xx xxxxxxxx vyhodnocení xxxxxxx. |
|
2.6.1.4 |
Xx své hodnotící xxxxxx xxx xxxx xxxx xxxxxxxxxx xxxxxxxxx Xxxxxxxxxxxx xxxxxx vhodné xxxxxxxxxxxxxxx podle xxxxxxx&xxxx;XXX xxxxxxxx (XX) č. 882/2004. |
|
2.6.1.5 |
Pracovní xxxxxxxxxxxxxxx xxx xxxxxx xxxxxxxxxx xxxxxx látek (xxxxxxxxx xxxxxx) xxxxx xxx xxxxxxxxx v podrobných xxxxxxxx xxxxxxxxxxxx referenční xxxxxxxxxx Společenství xxxxx xxxxxx&xxxx;12 xxxxxxxx (XX) x.&xxxx;378/2005. |
2.6.2&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxx xxx xxxxxxxxx xxxxxxx xxxxxxxxx xxxxx xxxx jejích xxxxxxxxxx x&xxxx;xxxxxxxxxxx
Xx nutno xxxxxxxxxx xxxxxxxxx xxxxxxxxxxxxxxx xxxxxxxxxxxxxx x&xxxx;xxxxxxxxxxxxxxx xxxxxxxxxxxx xxxxx pro stanovení xxxxxxxxxxxxxx xxxxxxx x/xxxx xxxxxxxxxx xxxxxxxxx látky x&xxxx;xxxxxxxx xxxxxxx x&xxxx;xxxxxxxxxxx xxxxxxxxxx.
|
2.6.2.1 |
Xxxx xxxxxx xxxxxxx xxxxxx xxxxxxxxx xxxx x&xxxx;xxxxxxx xxxxx analýzy xxxxxxxxxxx xxx xxxxxx xxxxxxxx podle xxxxxx&xxxx;11 xxxxxxxx (XX) x.&xxxx;882/2004. Xxxx metody xxxxxxx xxxxxxx nejméně xxxxx x&xxxx;xxxxxxxxx xxxxxxxxx x&xxxx;xxxx 2.6.1.1. |
|
2.6.2.2 |
Xxxxxxxx xxxxxxxxxxxxxxx xxxxxx (xxxxx) xxxxxxxx odpovídající xxxxxxxxxxxxxxx xxxxxxxxx x&xxxx;xxxxxxx&xxxx;XXX xxxxxxxx (XX) x.&xxxx;882/2004 x&xxxx;xxxx x&xxxx;xxxxx požadavky xxxxxxxxx v rozhodnutí Komise 2002/657/XX&xxxx;(10). Xxxxxxxxx xx xxxxx stejné pracovní xxxxxxxxxxxxxxx xxxxxxxxx v rozhodnutích Xxxxxx, xxxxx xxxxxxx xxxxxxxxxx xxxxxx xxxxxxxxx x&xxxx;xxxxxxxxxx xxxxxxxx látek x&xxxx;xxxxxx reziduí x&xxxx;xxxxxx xxxxxxxxx xxxxx xxxxxxxx Xxxx 96/23/XX. Xxxxx xxxxxxxxxxxx x&xxxx;xxxxx metody nesmí xxxxxxxxx polovinu xxxxxxxxxxxxxx XXX x&xxxx;xxxx xxx xxxxxxxxx x&xxxx;xxxxxxx přinejmenším xx xxxxx xxxxxxxx xx dvojnásobek MLR. |
|
2.6.2.3 |
Pracovní xxxxxxxxxxxxxxx interně validovaných xxxxx se ověří xxxxxxxxxxx metody v druhé xxxxxxxxxxxx x&xxxx;xxxxxxxxx xxxxxxxxxx. Xx nutno xxxxx xxxxxxxx těchto xxxxx. X&xxxx;xxxxxx nezávislosti x&xxxx;xxxxxx xx xxxxxxxxx dokumentace xxxxxxxxxx xxxxxxxxx v případě, xx xxxxx laboratoř xx účastníkem konsorcia xxxxxxxxx xxxxxxxxxxxx xxxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxxx xxxxxxxxxx Xxxxxxxxxxxx, xxx xx xxxxxxxxx x&xxxx;xxxxxxxx (ES) x.&xxxx;378/2005, dotyčná xxxxxxxxx xxxxx referenční xxxxxxxxxx Xxxxxxxxxxxx xxxxxxxxxx o zájmech (xxxxxxx xxxxxxxxxx laboratoř Xxxxxxxxxxxx xxxxxx xxxxxx) xxxxxxxxxx xxxxx laboratoře x&xxxx;xxxxxxxxxxx x&xxxx;xxxxx xxxxxxx x&xxxx;xxxxx xx xxxxxxxx xxxxxxxxxxx xxxxxxx. |
|
2.6.2.4 |
Xx xxx xxxxxxxxx xxxxxx xxx xxxx xxxx xxxxxxxxxx xxxxxxxxx Xxxxxxxxxxxx vybrat xxxxxx xxxxxxxxxxxxxxx x&xxxx;xxxxxxxxxxxxxx xxxxxxxxx v bodě 2.6.2.2. |
|
2.6.2.5 |
Pracovní charakteristiky xxx xxxxxx pro xxxxxxxx skupiny xxxxx (xxxxxxxxx xxxxxx) xxxxx xxx xxxxxxxxx v podrobných xxxxxxxx poskytnutých referenční xxxxxxxxxx Společenství podle xxxxxx&xxxx;12 xxxxxxxx (XX) x.&xxxx;378/2005. |
2.6.3&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxx xxxxxxxx xx xxxxxxxx x&xxxx;xxxxxxxxxxxxxxx xxxxxxxxx xxxxx
Xxxxxxx xxxxxxxx xxxxx metod xxxxxxxxx xx stanovení xxxxxxxxxxxxxx xxxxx xxxx&xxxx;2.1.3, 2.1.4, 2.1.5, 2.2.2, 2.4.1, 2.4.2, 2.4.3 x&xxxx;2.4.4.
X&xxxx;xxxxxxx x&xxxx;xxxxxxxx&xxxx;XX nařízení (ES) x.&xxxx;1831/2003 xx znění xxxxxxxx (ES) x.&xxxx;378/2005 xxxxx xxx xxxxxxxxxxx xxxxxx metody poskytnuté xxxxx tohoto xxxx, xxxxx xx xxxx xxxx Xxxxxx xxxxxxxx xx důležité xxx xxxxxxxxx žádosti.
Doporučuje se, xxx xxxxxx xxxxxxx x&xxxx;xxxxx bodě byly xxxxxxxxxxx uznané. Metody, xxxxx xxxxxx xxxxxxxxxxx xxxxxx, xx nutno xxxx popsat. V těchto xxxxxxxxx xxxx xxx xxxxxx provedeny akreditovanými x&xxxx;xxxxxxxxxxx xxxxxxxxxxxx x&xxxx;xxxx xxx xxxxxxxxxxxxxx xxxxx xxxxxxxxxxx xxxxx kvality (xxxx. xxxxxxx xxxxxxxxxxx xxxxx podle xxxxxxxx 2004/10/XX nebo normy XXX).
Xxxxxx xxx xxxxxxxxxxxx x&xxxx;xxxxxxxxxxxxxxx xxxxxxxxx látky xxxxxxx xxxxxx xxxxxxxxx xxxx xxxxxx xxxxxxx xxxxxxxxx xxx xxxxxx xxxxxxxx xxxxx xxxxxx&xxxx;11 xxxxxxxx (ES) č. 882/2004, xxxxxxx xxxxx xxxx xxxxxxxxx xxxxxx xxxxxxxxx (xxxx. nečistoty, xxxxxxxxx xxxxx).
3.&xxxx;&xxxx;&xxxx;XXXXX&xxxx;XXX: STUDIE XXXXXXXX XX XXXXXXXXXXX DOPLŇKOVÉ XXXXX
Xxxxxx xxxxxxx x&xxxx;xxxxx xxxxxx a ve xxxxxxxxxx xxxxxxxxx xxxx umožnit xxxxxxxxxxx:
|
— |
xxxxxxxxxxx použití xxxxxxxxx xxxxx xxx cílové xxxxx xxxxxx, |
|
— |
xxxxxxxxxx rizika xxxxxxxxxxxxx xx selekcí x/xxxx xxxxxxxx rezistence xxxx antimikrobiálním látkám x&xxxx;xxxxx xxxxxxxxxxx x&xxxx;xxxxxxxxxxx xxxxxxxxxxxxxx, |
|
— |
xxxxx xxx xxxxxxxxxxxx x&xxxx;xxxxxxxx xxxxxxxxx xx xxxxxx, xxxx byla xxxxxxxx xxxxxx obsahující xxxxxxxxxx xxxxx xxxx xxxxxx xxxxxxxx xxxxxxxxxx xxxxxx, xxxx xxxxx, xxxxx xxxxx xxxxxxxx x&xxxx;xxxxxxxxx xxxxxxxx xxxxxxxxxxxx xxxxxxx doplňkové xxxxx xxxx xxxxxx xxxxxxxxxx, |
|
— |
xxxxx xxx xxxxx xxxxxxxxxxxx x&xxxx;xxxxxxxxxx xxxxxx xxxx xxxxxxx nebo zapracovanou xx xxxxxxx xx xxxxx, vznikajících xxx xxxxx xxxxxxxxxx xx xxxxxxxx sliznice, očí xxxx xxxx x |
|
— |
xxxxx xxxxxxxxxxx xxxxxx xxxxxxx xxxxxxxxx látky xxxx xxxxxxxx x&xxxx;xx odvozených, xxxxxxxxxx xxxxx x/xxxx xxxxxxxxxxxx xxxxxxx, na xxxxxxx xxxxxxxxx. |
3.1&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxx xx xxxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxx pro xxxxxx druhy zvířat
Studie xxxxxxx v tomto xxxxxx xxxx určeny x&xxxx;xxxxxxxxxxx:
|
— |
xxxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxx xxx xxxxxx druhy xxxxxx x |
|
— |
xxxxxxxxxx xxxxxx xxxxxxxxxxxxx xx selekcí x/xxxx xxxxxxxx xxxxxxxxxx xxxx xxxxxxxxxxxxxxxx xxxxxx x&xxxx;xxxxx xxxxxxxxxxx x&xxxx;xxxxxxxxxxx xxxxxxxxxxxxxx. |
3.1.1&xxxx;&xxxx;&xxxx;Xxxxxx tolerance x&xxxx;xxxxxxxx xxxxx xxxxxx
Xxxxxx testu xxxxxxxxx je poskytnout xxxxxxx xxxxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxx x&xxxx;xxxxxxxx xxxxxx. Xxxxxxx xx xxxxxx ke xxxxxxxxx rozpětí pro xxxxxxxxxx, xxxxx se xxxxxxxxx xxxxx xxxxxx x&xxxx;xxxxxxx vyšších, xxx xx xxxxxxxxxx. Xxxx xxxxx xxxxxxxxx xx xxxxx xxxxxxx x&xxxx;xxxxxxxx xxxxxxxxxxx xxx všechny xxxxxx druhy/kategorie zvířat, xx xxx xx xxxxxx xxxxxxxx. V některých xxxxxxxxx xx přípustné xxxxxxxx některé xxxxx xxxxx tolerance xx xxxxx ze xxxxxxx xxxxxxxxx, pokud jsou xxxxxxx xxxx uvedené xxxxxxxxx xx xxxx xxxxx. Xxxxxxx studie xxxxxxx v tomto xxxxxx xxxx xxx založeny xx doplňkové xxxxx xxxxxxx v oddíle II.
3.1.1.1 Návrh testu xxxxxxxxx xxxxxxxx nejméně xxx xxxxxxx:
|
— |
xxxxxxx, xxx xx xxxxxxxxx xxxxx xxxxxxxx, |
|
— |
xxxxxxx s nejvyšší xxxxxxxxxxx xxxxxx x |
|
— |
xxxxxxxx xxxxxxx x&xxxx;xxxxxxxxxxxxx obsahem nejvyšší xxxxxxxxxx xxxxx. |
X&xxxx;xxxxxxx skupině xx doplňková látka xxxxxxx xxxxxx ve xxxx desetinásobku xxxxxxxx xxxxxxxxxx dávky. Xxxxxxx xxxxxxx xxxx xxxxxxx xxxxxxxxx x&xxxx;xxxxxxx xx xxxxxxxx xxxxxx xxxxxxxxxx xxxxxx, xxxxxxxx xxxxxxxxxxxxxxx, xxxxxxxxx xxxxxx xxxxxxxx, xxxxxxxxxxx a rutinní xxxxxxxxx xxxxxxxxxx složení xxxx x&xxxx;xxxx parametry, které xxxxxxxxxxxxx xxxxxxxxx x&xxxx;xxxxxxxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxx. Xxxxxx xx xx xxxxx kritické parametry xxxxx x&xxxx;xxxxxxxxxxxxxxx xxxxxx x&xxxx;xxxxxxxxxxxxx zvířat. X&xxxx;xxxxx xxxxxx xx xxxxxx xxxxxx případné nežádoucí xxxxxx zjištěné během xxxxxxx účinnosti. X&xxxx;xxxxxxx xxxxxxxxxxxxxx úmrtí xxx xxxxx xxxxxxxxx se xxxxxxx xxxxxxxxx x&xxxx;xxxxxxxxx xxxxxxxxxx.
Xxxxx xxx prokázat, xx xx xxxxxx 100xxxxxxx maximální xxxxxxxxxx xxxxx, xxxxxxxxxx xx xxxxxxxxxxx xxx xxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxx xxxx. Xx-xx xxxxxxx xxxxxx xxxxx při xxxxxx nižším, než xx 10xxxxxxx xxxxxxxx xxxxxxxxxx dávky, xx xxxxxx xxxxxxxx xxx, xxx bylo xxxxx xxxxxxxxx xxxxxxx xxx xxxxxxxxxx doplňkové xxxxx, x&xxxx;xxxxxx se doplňkové xxxxxxxxx (xxxxxx xxxxxxxxx, xxxxxxxxx histologie x&xxxx;xxxxxx xxxxxxxx xxxxxxxx).
X&xxxx;xxxxxxxxx xxxxxxxxxxx xxxxx nemusí xxx x&xxxx;xxxxxxxxxx xx xxxxxx xxxxxxxxxxx x&xxxx;xxxxxxxxxxx nebo xxxxx xxxxx provést xxxxx xxxxxxxxx.
Xxxxxxx xxxxxxxxxxxxxx xxxxxx musí xxxxxxxxx xxxxx x&xxxx;xxxxxxxxxxxx statistické xxxxxxxxxxx.
3.1.1.2&xxxx;&xxxx;&xxxx;Xxxx xxxxxx xxxxxxx xxxxxxxxx
Xxxxxxx&xxxx;1
Xxxx trvání xxxxxxx xxxxxxxxx: xxxxxxx
|
Xxxxxx zvířata |
Doba xxxxxx studií |
Charakteristika xxxxxxxx xxxxxx |
|
Xxxxxx selata |
14 dní |
Pokud xxxxx xx 14&xxxx;xxx xx xxxxxxx |
|
Xxxxxxxxx selata |
42 dní |
42 dní xx xxxxxxx |
|
Xxxxx xxxxxx |
42&xxxx;xxx |
Xxxxxxx xxxxxxxx xx začátku xxxxxx ≤&xxxx;35&xxxx;xx |
|
Xxxxxxxx xxxxxx x&xxxx;xxxxxxxxxx |
1&xxxx;xxxxxx |
Xx xxxxxxxxxx do xxxxx xxxxxxx |
X&xxxx;xxxxxxx žádosti xxxxxxxx xx xxxxxxxx a odstavených xxxxx xx xxxxxxxx xx xxxxxxxxxxx xxxxxxxxxxx xxxxxx (14denní xxx xxxxxx xxxxxx x&xxxx;28xxxxx xxx xxxxxxxxx xxxxxx). Xxxxx byla xxxxxxxxx xxxxxxxxx x&xxxx;xxxxxxxxxxx xxxxx, xxxxxxxxxx xx xxxxxxxx xxxxxx xxx výkrm xxxxxx.
Xxxxxxx&xxxx;2
Xxxx trvání xxxxxxx xxxxxxxxx: xxxxxx
|
Xxxxxx xxxxxxx |
Xxxx xxxxxx xxxxxx |
Xxxxxxxxxxxxxxx cílových xxxxxx |
|
Xxxxx xxxxx/xxxxxx |
35&xxxx;xxx |
Xx vylíhnutí |
|
Nosnice |
56 dní |
Pokud xxxxx během xxxxx xxxxxxx doby xxxxxx |
|
Xxxxx xxxx |
42&xxxx;xxx |
Xx xxxxxxxxx |
Xxxxx x&xxxx;xxxxxxxxx x&xxxx;xxxxxx xxxxx xxxx xxxx xxx použít x&xxxx;xxxxxxxxx xxxxxxxxx u odchovu xxxxx x&xxxx;xxxxx nebo x&xxxx;xxxxxxx krůt.
Tabulka 3
Doba xxxxxx xxxxxxx tolerance: xxxx
|
Xxxxxx xxxxxxx |
Xxxx xxxxxx xxxxxx |
Xxxxxxxxxxxxxxx xxxxxxxx zvířat |
|
Výkrm xxxxx |
28&xxxx;xxx |
Xxxxxxx xxxxxxx xxxxxxxx ≤&xxxx;70&xxxx;xx |
|
Xxxxxx xxxxx; xxxxx xxxxx xxxx xxxx k reprodukci |
42 dní |
|
|
Dojnice |
56 dní |
V případě xxxxxxx vztahující xx xx xxxxxx telat x&xxxx;xxxxx xxxxx xx xxxxxxxx za dostatečnou xxxxxxxxxxx xxxxxx (28 dnů xxx xxxxx xxxxxx).
Xxxxxxx&xxxx;4
Xxxx xxxxxx xxxxxxx tolerance: xxxx
|
Xxxxxx xxxxxxx |
Xxxx xxxxxx xxxxxx |
Xxxxxxxxxxxxxxx xxxxxxxx xxxxxx |
|
Xxxxxx xxxxxx x&xxxx;xxxxx xxxxxx |
28&xxxx;xxx |
Xxxxxxx&xxxx;5
Xxxx xxxxxx xxxxxxx xxxxxxxxx: xxxxxxxxxx a jiné ryby
|
Cílová xxxxxxx |
Xxxx trvání xxxxxx |
Xxxxxxxxxxxxxxx xxxxxxxx zvířat |
|
Losos a pstruh |
90 dní |
Jako xxxxxxxxxxx 90xxxxx xxxxxx xx bylo xxxxx xxxxxxx studii, xxx xxxx xxxxx xxxx xxxxxxxx xxxxxxxx oproti xxxxxxx xxxxxxx xxxxxxxxx xx xxxxxxx zkoušky xxxxxxx dvojnásobně.
Má-li xxx xxxxxxxxx látka xxxxxxxxx xxxxx pro xxxxx xxxxxxxxx ryb, testy xxxxxxxxx xx provedou xxxxx xxxxx xx xxxxxxxx xxxx xxxxx. Xxxxx tolerance xxxxxx 90&xxxx;xxx x&xxxx;xx xxxxx xxxxxxx xxxxxxxxx xxxxxxx x&xxxx;xxxxxxx jiker.
Tabulka 6
Doba xxxxxx xxxxxxx xxxxxxxxx: xxxxxxx x&xxxx;xxxxxxxx xxxxx x&xxxx;xxxx xxxxxxx, xxxxx nejsou xxxxxx k produkci xxxxxxxx
|
Xxxxxx xxxxxxx |
Xxxx xxxxxx xxxxxx |
Xxxxxxxxxxxxxxx xxxxxxxx zvířat |
|
Psi x&xxxx;xxxxx |
28&xxxx;xxx |
Xxxxxxx 7
Xxxx trvání xxxxxxx xxxxxxxxx: xxxxxxx
|
Xxxxxx&xxxx;xxxxxxx |
Xxxx trvání xxxxxx |
Xxxxxxxxxxxxxxx xxxxxxxx xxxxxx |
|
Xxxxx xxxxxxx |
28&xxxx;xxx |
|
|
Xxxxxx králice |
1 cyklus |
Od xxxxxxxxxx xx xxxxx xxxx xxxxxxx |
Xxxxxxxx-xx xx žádost xx xxxxxx x&xxxx;xxxxxxxxx xxxxxxx, xxxxxxxx xx xx xxxxxxxxxx xxxxxx 49&xxxx;xxx (xxxxxxxx xxxxx xx xxxxxxxx) x&xxxx;xxxx xxxxxxxxx xxxxxxx xx xx odstavu.
Pokud xx xxxxxxxxx xxxxx xxxxxxx xx xxxxxxxxxxx x&xxxx;xxxxxx xxxx, než xx xxxxxxx x&xxxx;xxxxxxxx kategorie xxxxxx, xxxxxx xx xxxxx xxxxxxxxxxxx xxxxxxxx xxx užití. Období xxxxxxxxxx xxxx xxxxx xxx kratší xxx 28&xxxx;xxx x&xxxx;xxxx zahrnovat xxxxxxxxx xxxxxxxx (xxxx. x&xxxx;xxxxxxx určených k reprodukci xxxxx xxxx xxxxxxxxxx xxxxx se xxxxxxxx xx xxxxxx xxxxxxxx xxxx xxxxx x&xxxx;xxxxxxxx xxxxxxxxxxx xxxxx xx xxxxxxxx xx xxxxxx xxxxxxx).
3.1.1.3&xxxx;&xxxx;&xxxx;Xxxxxxx xxxxxxxx
Xxxxxx musí xxx uvedeny xxxxxxxxxx x&xxxx;xxxxx o všech pokusných xxxxxxxxx. Xxxxxxxx xxxxxxxx xxxx xxx pečlivě xxxxxxxxxx x&xxxx;xxxxxxx na xxxxxx popisné xxxxx. Xxxxxxxxxxxxx xx zejména xxxx položky:
|
1. |
stádo xxxx xxxxx: xxxxx x&xxxx;xxxxx; xxxxxxxx xxxxxx x&xxxx;xxxxx, xxxxxx krmení; x&xxxx;xxxxxxx xxxxx xxxxxxxx x&xxxx;xxxxx xxxxxx xxxx xxxxx x&xxxx;xxxxxxxxxxxx, světelné poměry x&xxxx;xxxxxxx vody, včetně xxxxxxx xxxx a obsahu xxxx ve xxxx; |
|
2. |
xxxxxxx: xxxx (x&xxxx;xxxxxxx xxxxx xxxxxxxx xxx lidskou xxxxxxxx je uvedena xxxxxxxxxxxx xxxxx jejich xxxxxxxx xxxxx x&xxxx;xx xxx x&xxxx;xxxxxxxxx následuje xxxxxxxx xxxxxxxxx xxxxx), xxxxxxx, stáří (xxxxxxxx x&xxxx;xxxxxxx druhů), pohlaví, xxxxxx xxxxxxxx, xxxxxxxxxxxx xxxxxxx x&xxxx;xxxxxxx xxxxxxxxx xxxx; |
|
3. |
xxxxx a přesná xxxx xxxxxx xxxxx: xxxxx x&xxxx;xxxx provedených xxxxxxx; |
|
4. |
xxxxx xxxxx: xxxxx xxxxxx x&xxxx;xxxxxxxxxxxxxxx xxxxxxx xxxxx xxxxx (xxxxx) s uvedením xxxxxxxxx xxxxxx, xxxxxxxxxxx xxxxx (xxxxxxxxxxx xxxxxxx) x&xxxx;xxxxxxxxxxx hodnoty. Xxxxx x&xxxx;xxxxxx krmiva; |
|
5. |
koncentrace účinné xxxxx (xxxxx) xxxx xxxxxxx (xxxxxxx) (x&xxxx;xxxxxxxxxx xxxxx xxxxxxxxx xxx xxxxxxxxxx xxxxx) x&xxxx;xxxxxxxx xxxx xxx xxxxxxxxx xxxxxxxxx xxxxxxxx s použitím xxxxxxxxxxx xxxxxxxxxx metod. Xxxxxxxxxx xxxxx xxxxxxxxx xxxxx; |
|
6. |
xxxxx pokusných a kontrolních xxxxxx, xxxxx zvířat x&xxxx;xxxxx skupině: xxxxx xxxxxx použitých pro xxxxxx musí xxxxxxx xxxxxxxxx xxxxxxxxxxx xxxxxxx. Xxxx by být xxxxxxx použité xxxxxx xxxxxxxxxxxxx xxxxxxxxx. Xx xxxxxx musí být xxxxxxxx xxxxxxx zvířata x/xxxx xxxxxxxxxxxxxx celky, x&xxxx;xxxxx se xxxxxx xxxxxxxxx. Xxxxxxx, xxxxx xxxx možné xxxxxxxxxx xxx xxxxxxxxxx xxxx xxxxxx údajů, xxxx xxx xx zprávě xxxxxxx x&xxxx;xxxxxx xxxxxxxxx x&xxxx;xxxxxxxxxxxx xxxxxxxxx xxxxxx xxxx být xxxxxxxxxxxxx; |
|
7. |
xxxxxxx x&xxxx;xxxxxx xxxxxxxxxxx nežádoucího xxxxxx xxxxxxx u jedinců xxxx xxxxxx xxxx xxx xxxxxxxxxx (poskytnutí xxxxx x&xxxx;xxxxxxxx xxxxxxxxxx xxxxxxxxx xx xxxxxx) x |
|
8. |
xxxxxxx/xxxxxxxxxxx xxxxxxxx, xx-xx xxxxx, nesmí xxxxxxxxxx xxxxxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxx x&xxxx;xxxx xxx xxxxxxxxxxx xxxxxxxxxxxx. |
3.1.2&xxxx;&xxxx;&xxxx;Xxxxxxxxxxx xxxxxx
Xx nutno xxxxxxxxxx xxxxxx xx xxxxxxxxx xxxxxxxxxx doplňkové xxxxx xxxxxxxx křížovou xxxxxxxxxx xxxx xxxxxxxxxxxx xxxxxxxxxx x&xxxx;xxxxxxxx xxxx xxxxxxxxxxxx xxxxxxxxx, selektovat xxxxxxxxxxx xxxxxxxxxxx kmeny za xxxxxxxxxx podmínek u cílových xxxxx, xxxxxxx xxxxxx x&xxxx;xxxxxxxxxxx xxxxxxxx xxxxxxxxxx x&xxxx;xxxxxxxxx xxxxxx, xxxxxxx xxxxxxxxxx xxxx xxxxxxxxxx xxxxxxxxxxxx xxxxxxxxxxxxxx.
X&xxxx;xxxxxxx, xx xxxxxx xxxxx (látky) xxxxxxxx(x)&xxxx;xxxxxxxxxxxxxxx xxxxxxxx xxx xxxxxxxxxxx, ve které xx obsažena x&xxxx;xxxxxx, xxxx být x&xxxx;xxxxxxx xx xxxxxxxxxxxxxxxxx xxxxxxx xxxxxx minimální inhibiční xxxxxxxxxxx (MIK) xxx xxxxxxxxx druhy xxxxxxxx. Xx-xx xxxxxxxxx xxxxxxxxx xxxxxxxxxxxxxxx aktivita, xx xxxxx xxxxxxxx schopnost xxxxxxxxx xxxxx xxxxxxxxxx xxxxxxxxxxx xxxxxxxxxxx xxxxx xx vitro x&xxxx;x&xxxx;xxxxxxxx xxxxx a způsobit xxxxxxxx xxxxxxxxxx xxxx xxxxxxxxxxxxx xxxxxxxxxxxx&xxxx;(11).
Xxxxxxx x&xxxx;xxxxxxxxxxx xxxxxxx xxxxx xx xxxxxxxx xxx všechny mikrobiální xxxxxxxxx látky a pro xxxx xxxxxxxxx xxxxx, x&xxxx;xxxxx lze xxxxxxxx xxxxxx xx xxxxxxx xxxxxxxxxx. Xxxx xxxxxx xxxx prokázat, xx xxxxx xxxxxxxxx xxxxx xxxxxxxxx xxxxxxxx, xxxxx xxxxxxxxxx nadměrnému xxxxx x&xxxx;xxxxxxxxxx xxxxxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx.
Xxxxx xxxxxxxxxxx mikroorganismů xxxx xxxxxxx xx xxxxxxxx xxxxxxx, zahrnuje xxxx příslušné xxxxxxxxxx xxxxx bez ohledu xx xx, xxx x&xxxx;xxxxxxxx xxxxxx xxxxxxxxxx xx xxxxxxxxxxxx xxxxxxxx.
3.2&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxx se xxxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxx xxx spotřebitele
Cílem je xxxxxxxxxx xxxxxxxxxx doplňkové xxxxx xxx xxxxxxxxxxxx x&xxxx;xxxxxxxx možná rezidua xxxxxxxxx xxxxx xxxx xxxxxx xxxxxxxxxx v potravinách xxxxxxxxx xx zvířat, xxxx bylo xxxxxxxx xxxxxx xxxx xxxx xxxxxxxxxx xxxxxxxxxx xxxxx xxxx xxxxxxxx xxxxx xxxxxxxxxx xxxxxx.
3.2.1&xxxx;&xxxx;&xxxx;Xxxxxx metabolismu x&xxxx;xxxxxxx
Xxxxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxx x&xxxx;xxxxxxxx xxxxx xx rozhodujícím xxxxxx xxx xxxxxxxxxxxx x&xxxx;xxxxxxxxxxxx xxxxxxx x&xxxx;xxxxxxxxxxxxx tkáních xxxx xxxxxxxxxx xxxxxxxxx xx xxxxxx, jimž xxxx podáváno xxxxxx xxxx xxxx xxxxxxxxxx xxxxxxxxxx xxxxx. Xx xxxxx xxxxxxxxx studie xxxxxxxx xx xxxxxxxx, xxxxxxxxxx, xxxxxxxxxxx x&xxxx;xxxxxxxxxx xxxxx (x&xxxx;xxxxxx metabolitů).
Studie xxxx xxx xxxxxxxxx xxxxxx xxxxxxxxxxx validovaných xxxxxxxxxx metod a v souladu x&xxxx;xxxxxxxx evropskými právními xxxxxxxx xxxx xxxxxxxx xxxxxxxx pro xxxxxxxxxxxxx xxxxxxxxx OECD x&xxxx;xxxxx xxxxx xxxxxxx xxxxxxxxxxx xxxxx. Xxxxxx musí xxxxxxxxxxx xxxxxxxx týkající xx dobrých xxxxxxxxx xxxxxxxx zvířat stanovená xxxxxxxx xxxxxxxx Evropského xxxxxxxxxxxx a neopakují xx, xxxx-xx xx xxxxxxxx.
Xxxxxx xxxxxxxxxxx a reziduí x&xxxx;xxxxxxxx xxxxxxx (zvířat) xx xxxxxxxx x&xxxx;xxxxxxx xxxxxx xxxxxxxxxxxx do krmiva (xxxxxxxxxxx xxxxxx xxxxxx xxxxxxxxx xxxxxx, není-li xx xxxxx xxxxxxxxxx).
Xxxxxxx xx xxxxxxxxxx identifikace xxxxxxxxxx představujících xxxx xxx 10&xxxx;% xxxxx xxxxxxx x&xxxx;xxxxxxxxxxxxx xxxxxxx x&xxxx;xxxxxxxxxx x&xxxx;xxxx než 20&xxxx;% xxxxx xxxxxxx x&xxxx;xxxxxxxxxxxx. Pokud xx xxxxxxxxxxx cesta xxxxxx xxxxx xxxxxxxxxxxxx xxxxxxxx, xx nutno xxxxxxxxxxxxx xxxxxxxxxx pod výše xxxxxxxxx xxxxxx.
Xxxxxxxxx studie xxxxxxx xxxxx základ xxx výpočet expozice xxxxxxxxxxxx x&xxxx;xxxxxxxx xxxxxxxxx xxxxxxxx xxxxx x&xxxx;XXX. Xxxxxxxx xx xxxxx xx xxxxxxxxxxxx reziduum.
U některých xxxxxxxxxxx xxxxx xxxxxx xxx v závislosti xx xxxxxx povaze xxxx xxxxx xxxx nutné xxxxxxx studie xxxxxxxxxxx x&xxxx;xxxxxxx.
3.2.1.1&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxxxxx
Xxxxxx studií xxxxxxxxxxx xx xxxxxxxxxx xxxxxxxx, distribuci, xxxxxxxxxxxxxxx x&xxxx;xxxxxxxxxx xxxxxxxxx xxxxx x&xxxx;xxxxxxxx druhů xxxxxx.
Xxxxxxxxxx xxxxxx:
|
1. |
xxxxxxxxxxx xxxxxxx po xxxxxx jediné xxxxx xxxxxx látky x&xxxx;xxxxxxxxxxxx xxxxxxx xxx užití (xxxxxxx množství odpovídající xxxxxxx xxxxxx) x&xxxx;xxxxxxxx xxxxxxxxxxx xxxxx (xx-xx xx xxxxxxxxxx), xxx xxxxx xxx xxxxxxxxx xxxxxxxx x&xxxx;xxxxxx absorpce, xxxxxxxxxx (xxxxxx/xxxx) a vylučování (xxx, žluč, výkaly, xxxxx nebo xxxxx, xxxxxxxxxxx xxxxxx, vylučování xxxx xxxxx) x&xxxx;xxxxx x&xxxx;xxxxx, xx-xx xx xxxxxx, x |
|
2. |
xxxxxxxxx do xxxxxxxxxxx, identifikace metabolitu(ů) v exkrementech x&xxxx;xxxxxxx x&xxxx;xxxxxxxxxx x&xxxx;xxxxxxx x&xxxx;xxxxxxxxxx xx xxxxxxx xx xxxxxxxxxx podávání xxxxx xxxxxxxx látky xxxxxxxx xx vyrovnaném xxxxx (metabolická rovnováha) xxxxx obsahu x&xxxx;xxxxxx. Xxxxxxxxxx xxxxx odpovídá xxxxxxxx navrhované xxxxx xxx xxxxx a musí xxx xxxxxxxxxxx xx xxxxxx. |
3.2.1.2&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxx
Xxxxx se xxxxxxxx x&xxxx;xxxxxx xxxxxxxxxxxxxxxxxx xxxxxxx v poživatelných xxxxxxx xxxx produktech.
Studie reziduí xx xxxxxxxx xxx xxxxxxx xxxxx, x&xxxx;xxxxx xxxx xxxxx xxxxxx xxxxxxxxxxx.
Xx-xx látka xxxxxxxxxx xxxxxxx xxxxxxx xxxxxxx xxxx xxxxx xxxx xxxxxxxxx-xx se x&xxxx;xxxxxxxxxxx xxxx xxxxxxxx přirozeně xx xxxxxxx xxxxxxxx, xx xxxxxxxxx xx xxxxxx xxxxxxx xxxxxx xx xxxxxxxxx obsahu x&xxxx;xxxxxxx/xxxxxxxx x&xxxx;xxxxxxxxxx xxxxxxx x&xxxx;x&xxxx;xxxxxxx, xxx byla xxxxxxxx xxxxxxxx xxxxxxx xxxxx.
X&xxxx;xxxxxxxxxxx xxxxx xxxxxx xxxxxxxx vyhodnotí xxxxxxx xxxxxxx, xxxxx jsou xxxxxxxxxxxxx významná, x&xxxx;xxxx xxxxxxxxxxxx reziduum xxxxxx xxxxx x&xxxx;xxxxxxxxxxx xxxxx (xxxxx, xxxxxxx, xxxxx, xxxx, kůže + xxx) x&xxxx;xxxxxxxxxx (mléko, xxxxx x&xxxx;xxx). Xxxxxxxxxxxx xxxxxxxx xx xxxxxxxx xxxxxxx xxx xxxxxxx, xxxxx koncentrace xx xx xxxxxx xxxxxx x&xxxx;xxxxxxxx toxikologicky xxxxxxxxx xxxxxxxx x&xxxx;xxxxxxx. Xxxxxx xxxx xxxxxxxx rovněž xxxxxxx reziduí v tkáních xxxx produktech, aby xxxx možno xxxxxxxx xxxxxxxxxxxx xxxxxxxxx xxxxx.
Xx xxxxxxxxx xxxxxxxx xxxxx xx navrhovaný xxxxxxxxx xxxxx xxxxxx ve xxxxxx a/nebo produktů x&xxxx;xxxxxx bodu měření xxxxx:
|
— |
xxxxxxxxxxx xxxxx:
|
|
— |
produkty:
|
Xxxxx xx xxxxxx xxxxxxxxx podle xxxxxxx.
Xxxxxxx se měří xxx xxxxxx ochranné xxxxx (xxxxxxxxx xxxx) x&xxxx;xxxxxxx ve xxxxx xxxxxx bodech měření.
Předloží xx xxxxx xx xxxxxxxxxxxx xxxxxxxx.
Xx xxxxx xxxxxxx studie absorpce, xxxxxxxxxx x&xxxx;xxxxxxxxxx, xxxxxx xxxxxxxxxxxx xxxxxxxx metabolitů, x&xxxx;xxxxxxxxxxxxx xxxxx xxxxxx, x&xxxx;xxxxx xxxx získána xxxxxxxx hodnota XXXXX xxxx xxxxxxxxxx x&xxxx;xxxx (xxxx xxxxxxx). Doplňkové xxxxxx xxxxxxxx xx xxxxxxxx metabolitů mohou xxx nezbytné x&xxxx;xxxxxxx, xxxx-xx xxxx xxxxxxxxxx xxxxxxxxxxx cílovými xxxxx x&xxxx;x&xxxx;xxxxxxxxxxxxx xxxxx xx xx významném rozsahu xxxxxxx.
3.2.1.3&xxxx;&xxxx;&xxxx;Xxxxxx metabolismu x&xxxx;xxxxxxxx
Xxxx xxx xxxxxxxxx xxxxxx xxxxxxxxxxx xxxxxxxxxx xxxxxxxxxxxx xxxxxxx, xxxxxxxxxxx xxxxxx x&xxxx;xxxxxxxxxxxx xxxxxxxx xxxxxxxxxx x&xxxx;xxxx x&xxxx;xxxxxxxx. Xxxxxxxx xxxx laboratorní xxxxx xxxxxxxx xxxxxx xxxxx xxxxxxx rozdíl v citlivosti, xxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxxx.
3.2.1.4&xxxx;&xxxx;&xxxx;Xxxxxxxxxx dostupnost xxxxxxx
Xxx xxxxxxxxxx xxxxxx pro xxxxxxxxxxxx xxxxxxxxx x&xxxx;xxxxxxxx xxxxxxxx rezidui xxxxxxxxxx x&xxxx;xxxxxxxxxxx xxxxxxxxxx xx xxxxx xxxx x&xxxx;xxxxx xxxxxxxxx bezpečnostní xxxxxx xxxxxxxx na xxxxxx xxxxxx biologické dostupnosti xx xxxxxxx xxxxxxxx xxxxxxxxxxxxx xxxxxx a uznaných xxxxx.
3.2.2&xxxx;&xxxx;&xxxx;Xxxxxxxxxxxxx xxxxxx
Xxxxxxxxxx xxxxxxxxx xxxxx xx xxxxxxxx xx xxxxxxx xxxxxxxxxxxxxxx xxxxxx xxxxxxxxxxx in xxxxx x&xxxx;xx vivo xx xxxxxxxxxxxxx zvířatech. Xxxx zkoušky obvykle xxxxxxxx měření:
|
1. |
akutní toxicity; |
|
2. |
genotoxicity (xxxxxxxxxx, xxxxxxxxxxxxxx); |
|
3. |
xxxxxxxxxxxx orální xxxxxxxx; |
|
4. |
xxxxxxxxx xxxxxx xxxxxxxx/xxxxxxxxxxxxx; |
|
5. |
xxxxxxxx xxx xxxxxxxxxx xxxxxx xxxxxxxxxxxx x |
|
6. |
xxxxxxx studie. |
Existuje-li xxxxx k obavám, musí xxx provedeny xxxxx xxxxxx poskytující doplňkové xxxxxxxxx, xxxxx xxxx xxxxxxxx pro xxxxxxxxx xxxxxxxxxxx účinné látky x&xxxx;xxxxxx reziduí.
Na xxxxxxx xxxxxxxx těchto studií xx stanoví toxikologická XXXXX.
Xxxxxxxxx xxxxxx xxxxxxxx xx určitých xxxxxxxxxx xxxxx být nezbytné, xxxxx jsou tyto xxxxxxxxxx produkovány xxxxxxxx xxxxx a u testovaných laboratorních xxxxx xx ve xxxxxxxxx rozsahu xxxxxxx. Xxxx-xx x&xxxx;xxxxxxxxx xxxxxx xxxxxxxxxxx x&xxxx;xxxxxxx, xxxxxx xx xxxx xxxxx x&xxxx;xxxxx xxx xxxxxxxxxxx x&xxxx;xxxxxx xxxxxxxxxx doplňkových xxxxxx.
Xxxxxxxxxxxxx xxxxxx musí xxx xxxxxxxxx x&xxxx;xxxxxxx xxxxxx. Xxxxx xx xxxxxx látka přítomna x&xxxx;xxxxxxxx fermentačního procesu, xxxxxxx xx xxxxxxx xxxxxxxxxxxxx xxxxxxx. Testovaný xxxxxxx xxxxxxxxxxxxx xxxxxxx xxxx xxx totožný x&xxxx;xxxxxxxxx, xxxxx má xxx xxxxxx x&xxxx;xxxxxxxxx xxxxxxxx.
Xxxxxx musí xxx xxxxxxxxx xxxxxx mezinárodně xxxxxxxxxxxx xxxxxxxxxx xxxxx x&xxxx;xxxxxxx x&xxxx;xxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxx xxxx xxxxxxxx xxxxxxxx xxx xxxxxxxxxxxxx ukazatele OECD x&xxxx;xxxxx zásad xxxxxxx xxxxxxxxxxx praxe. Xxxxxx xxxxxxxxxx laboratorní zvířata xxxx xxxxxxxxxxx xxxxxxxx xxxxxxxx xx xxxxxxx xxxxxxxxx xxxxxxxx xxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxx x&xxxx;xxxxxxxxx se, xxxx-xx xx xxxxxxxx.
3.2.2.1&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxx
Xxxxxx xxxxxx toxicity xx xxxxxxxx ke xxxxxxxxxxx x&xxxx;xxxxxxx xxxxxxxxxxxxxxx xxxxxxxx xxxxx.
Xxxxxx xxxxxx xxxxxxxx xxxx být xxxxxxxxx xxxxxxx xx xxxx druzích xxxxx. Xxxxx xxxxxxxxxxx druh xxxx být xxxxxxxx xxxxxxxx xxxxxxx xxxxxx.
Xxxxxx xxxxx zjistit přesnou xxxxxxx XX50; xxxxxxxxx xxxxxxxxx xxxxxx xxxxxxxxx xxxxxxx xxxxx. Xxxxxxxxx xxxxxxxxx xxxxx xxxxxxxxx 2&xxxx;000&xxxx;xx/xx xxxxxxx hmotnosti.
Ke xxxxxxx počtu xxxxxxxxxxx xxxxxx x&xxxx;xxxxxxxx xxxxxx xxxxxxx se neustále xxxxxxxx nové xxxxxxxxx xxx xxxxxxxxx xxxxx xxxxxxxxxxxx xxxxxx xxxxxxxx. Xxxxxx provedené xxxxxx xxxxxx xxxxxx xxxxxxx xxxxx xxxxxx, xxxx-xx xxxxx xxxxxxxxxx.
Xx xxxxx xxxxxxx xxxxxx OECD 402 (akutní xxxxxxxx xxxxxxxx), 420 (xxxxxx xxxxx xxxxx), 423 (xxxxxx xxxxxxxxx xxxxx xxxxxx xxxxxxxx) x&xxxx;425 (xxxxxx xxxxxx x&xxxx;xxxx).
3.2.2.2&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxxxxxx, xxxxxx xxxxxxxxxx
Xx xxxxxx identifikace xxxxxxxx xxxxx x&xxxx;xxxxxxxx xxxxxx xxxxxxxxxx a produktů xxxxxxxxx, xxxxx mají xxxxxxxxx x&xxxx;xxxxxxxxxxx xxxxxxxxxx, xxxx xxx xxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxx testů xx xxxxxxxxxxxx. X&xxxx;xxxxxxx xxxxxxx xx xxxxx xxxx xxxxxxxx xxx x&xxxx;x&xxxx;xxxxxxxxxxxx xxxxxxxx x&xxxx;xxxxx x&xxxx;xxxxx xx v úvahu xxxxxxxxxxxx xxxxxxxxxxx materiálu xx zkušebním xxxxxxxx.
Xxxxxxxx xxxxxx zahrnuje xxxx xxxxxxx:
|
1. |
xxxxxxx xxxxxxxx xxxxxx x&xxxx;xxxxxxxxxx a/nebo v buňkách xxxxx (xxxxx xxxxx xxxx xx xxxxxxxxxxxxx x&xxxx;xxxxxxx xxxx); |
|
2. |
xxxxxxx xxxxxxxxxxxxxx xxxxxxx v buňkách savců x |
|
3. |
xxxxxxx in xxxx x&xxxx;xxxxx. |
X&xxxx;xxxxxxxxxx xx xxxxxxxx xxxx uvedených zkoušek x&xxxx;x&xxxx;xxxxxxxxxxxx x&xxxx;xxxxxxxxx toxikologickému xxxxxxx látky x&xxxx;xxxxxx xxxxxxxx užití mohou xxx nezbytné xxxxxxxxx xxxxxxx.
Xxxxxxxxx by měly xxx x&xxxx;xxxxxxx x&xxxx;xxxxxxx XXXX 471&xxxx;(xxxx xxxxxxxxxx xxxxxx x&xxxx;Xxxxxxxxxx typhimurium), 472&xxxx;(xxxx xxxxxxxxxx xxxxxx x&xxxx;Xxxxxxxxxxx coli), 473&xxxx;(xxxx xxxxxxxxxxxxxx xxxxxxx u savců xx xxxxx), 474&xxxx;(xxxx xx xxxxxxxxxx x&xxxx;xxxxxxx&xxxx;xxxxxxxxxxxx), 475&xxxx;(xxxx xxxxxxxxxxxxxx xxxxxxx x&xxxx;xxxxxx xxxxx savců), 476&xxxx;(xxxx xxxxxxxx xxxxxx x&xxxx;xxxxxxx buňkách xx xxxxx) xxxx 482&xxxx;(xxxxxxxxxxx xxxxxxx XXX x&xxxx;xxxxxxx xxxxx in vitro), xxxxx x&xxxx;xxxxxx xxxxxxxxxxx xxxxxx XXXX xxx xxxxxxx in vitro x&xxxx;xx xxxx.
3.2.2.3&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxxxxxx xxxxxx xxxxxxxx xxx xxxxxxxxx xxxxx
X&xxxx;xxxxxxx potenciálu xxxxxxxxxxxx xxxxxxxx účinné xxxxx xx xxxxxxxx xxxxxxx xxxxx xxxxxx xx xxxxxxxxxx x&xxxx;xxxxx xxxxxx xxxxxxx 90&xxxx;xxx. Xxxxxxxx-xx se xx xx xxxxx, xxxx xxx provedena xxxxx xxxxxx na xxxxx xxxxx xxx xxxxxxxxxx. Xxxxxxxxx xxxxxxx xxxx xxx xxxxxxxx orálně xxxxxxx x&xxxx;xxxxx různých xxxxxxxx navíc ke xxxxxxxxx xxxxxxx, xxx xx xxxxxxx xxxxxx xx dávku. Xxxxxxxxx xxxxx musí xx xxxxxxxxxx okolností odhalit xxxxxxxxxx xxxxxxxxxxx xxxxxx. Xxxxxxxx xxxxxx xxxxxxxxx xxxxx xxxxxxxxx žádnou xxxxxx toxicity.
Protokoly xxx xxxx xxxxxxx xxxx xxx x&xxxx;xxxxxxx x&xxxx;xxxxxx XXXX 408 (xxxxxxxx) xxxx 409 (jiné xxxxx než xxxxxxxx).
3.2.2.4&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxxx xxxxxx xxxxxxxx (xxxxxx xxxxxxxxxxxxx)
X&xxxx;xxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxx a karcinogenity xx xxxxx xxxxxxx xxxxxx xxxxxxxxx xxxxxx xxxxxxxx nejméně na xxxxxx xxxxx x&xxxx;xxxxx xxxxxx xxxxxxx 12 měsíců. Xxxxxxx druh xxxx xxx xxxxxxxxxxxxx xxxxxx xxxxx xxxxx xxxxxxxxxx xxxxxxxxx xxxxx, xxxxxx xxxxxxxx 90denních xxxxxx. Xxxxxxxxxxx druhem xx xxxxx. Požaduje-li xx xxxxx studie, použije xx druh xxxxxxxx xxxx xxxx xxxx xxxxx xxx hlodavci. Xxxxxxxxx xxxxxxx xxxx xxx xxxxxxxx xxxxxx xxxxxxx x&xxxx;xxxxx xxxxxxx xxxxxxxx xxxxx xx xxxxxxxxx xxxxxxx, xxx xx xxxxxxx xxxxxx xx dávku.
Je-li studie xxxxxxxxx xxxxxxxx xxxxxxxxxxx xx xxxxxxxx xxxxxxxxxxxxx, xxxx xxxxxx je xxxxxxxxxxx xx 18&xxxx;xxxxxx x&xxxx;xxxx x&xxxx;xxxxxx a na 24&xxxx;xxxxxx x&xxxx;xxxx.
Xxxxxx karcinogenity xxxxxx xxx xxxxx, xxxxx účinná xxxxx x&xxxx;xxxx xxxxxxxxxx:
|
1. |
xxxxxxxx xxxxx xxxxxxxxx xxxxxxxx x&xxxx;xxxxxxx xx genotoxicitu; |
|
2. |
nejsou strukturálně xxxxxxxxx se xxxxxxx xxxxxxxxxxx x |
|
3. |
xxxxxxxxxxxx při xxxxxxxxx xxxxxxxxx xxxxxxxx xxxxx xxxxxx (xxx)xxxxxxxxx. |
Xxxxxxxxx xxxx xxx x&xxxx;xxxxxxx x&xxxx;xxxxxxx XXXX 452 (xxxxxx chronické xxxxxxxx) xxxx 453 (kombinovaná xxxxxx chronické xxxxxxxx/xxxxxxxxxxxxx).
3.2.2.5&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxx pro xxxxxxxxxx (xxxxxx toxicity pro xxxxxxxxxx vývoj)
K zjištění xxxxxxx xxxxxxxx reprodukční funkce x&xxxx;xxxxx nebo xxxxx xxxx škodlivých účinků xx potomstvo xxxxxxxxxxxxx x&xxxx;xxxxxxxx účinné xxxxx xx xxxxx xxxxxxx xxxxxx reprodukční xxxxxx xxxxxx:
|
1. |
xxxxxxxxxxxxx studie xxxxxxxx xxx xxxxxxxxxx a |
|
2. |
studie xxxxxxxx pro prenatální xxxxx (xxxxxxx xxxxxxxxxxxx). |
X&xxxx;xxxxxx xxxxxxx xxxxx xxx xxxxxxx xxxxxxxxxx xxxxxxxxxxxx xxxxxx xxxxxxxxx používání xxxxxx.
3.2.2.5.1.&xxxx;&xxxx;&xxxx;Xxxxxxxxxxxxx studie toxicity xxx reprodukci
Studie reprodukční xxxxxx musí xxx xxxxxxxxx x&xxxx;xxxxxxx xxxxxxx xxxx filiálních xxxxxxxx (X1, X2) x&xxxx;xxxxxxx xxxxxxx xxxxx, xxxxxxx xxxxxxxx, x&xxxx;xxxxx xxx xxxxxxxxxxx xx xxxxxx xxxxxxxxxxxx. Xxxxxxxx látka xx xxxxxxxx orálně xxxxxx x&xxxx;xxxxxxx ve xxxxxxx xxxx před xxxxxxx. V podávání xx xxxx pokračovat až xx xxxxxxx xxxxxx xxxxxxxx&xxxx;X2.
Xxxxxxx důležité xxxxxxxxx xxxxxxxx xx xxxxxxxx, xxxxxxxx, porodu, xxxxxxxxxx xxxxxxx, xxxxxx, xxxxx x&xxxx;xxxxxx xxxxxx generace F1 xx xxxxxx xx xx xxxxxxxxxx x&xxxx;xxxxx xxxxxxxx&xxxx;X2 xx xx xxxxxxx xxxx xxx xxxxxxx xxxxxxxxx x&xxxx;xxxxxxxxxxxxx. Xxxxxxxxx pro xxxxxx xxxxxxxx xxx reprodukci xx xxxx být x&xxxx;xxxxxxx s pokynem XXXX 416.
3.2.2.5.2.&xxxx;&xxxx;&xxxx;Xxxxxxx xxxxxxxx pro xxxxxxxxxx xxxxx (xxxxxxx xxxxxxxxxxxx)
Xxxxx je odhalit xxxxxxxx nepříznivé účinky xx březí samici x&xxxx;xxxxx embrya x&xxxx;xxxxx x&xxxx;xxxxxxxx expozice xx xxxxxxxxx xxxxxxxxxx xxxxxxx xx xxxxx dobu xxxxxxxx. K těmto xxxxxxx xxxxx xxxxxxx toxicita x&xxxx;xxxxxxx samic, xxxxx xxxxxx – xxxxx, xxxxxxx xxxx xxxxx x&xxxx;xxxxxxxxxxxx abnormality a anomálie xxxxx.
Xxxxxx, který se xxxx xxx xxxxx xxxxxx, je xxxxxxx xxxxx. Je-li zaznamenán xxxxxxxxx xxxx xxxxxxxxxx xxxxxxxx pro teratogenitu, xxxxxxx se další xxxxxx xxxxxxxx xxxxxxxx x&xxxx;xxxxxxx xxxxx, pokud xxxxx x&xxxx;xxxxxxx. Xx-xx xxxxxxx xx xxxxxxxxxxxx xx xxxxxxx xxxxxxxxx, xxxx studie x&xxxx;xxxxxxx xxxxx nutná xxxxx xxxxxxx, xxx přezkum xxxxx xxxxxxxx studií xxxxxxxxx, že ADI xxxx založena na xxxxxxxxxxxx u krys. X&xxxx;xxxxx xxxxxxx xx xxxx xxxxx xxxxxx x&xxxx;xxxxxxx xxxxx, aby xx xxxxx xxxxxxxxxxxx xxxx xxx xxxxx xxxxxxxx. Xxxxxxxxx by xxxx xxx v souladu x&xxxx;xxxxxxx XXXX 414.
3.2.2.6 Jiné xxxxxxxxxx xxxxxxxxxxxxx a farmakologické xxxxxx
Xxxxxxxx-xx xxxxxx x&xxxx;xxxxxx, xx xxxxx provést xxxxx xxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxxxxx pro xxxxxxxxx xxxxxxxxxxx účinné xxxxx x&xxxx;xxxxxx xxxxxxx. Xxxx xxxxxx xxxxx xxxxxxxxx xxxxxxx farmakologických xxxxxx, xxxxxx xx xxxxx (xxxxxxxxxxxxxx) xxxxxxx, xxxxxxxxxxxxx xxxx xxxxxxxxxxxxx.
3.2.2.7&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxx xxxxx xxx xxxxxxxxxxxx xxxxxxxxxxxx xxxxxx (NOAEL)
NOAEL xx xxxxxxx založena xx toxikologických účincích, xxxxxxxxxxxxx však xxxxx xxx xxxxxxxxx xxxxxxxxxxxxxx xxxxxx.
Xxxx se xxxxxxxx XXXXX. Xxx xxxxxxxx xxxxxxxx XXXXX, xxxxxxxxx x&xxxx;xx/xx xxxxxxx hmotnosti xx xxx, se xxxxxx x&xxxx;xxxxx všechna xxxxxxxx z předchozích oddílů xxxxx x&xxxx;xxxxxxxxx xxxxxxxxxx xxxxxxxxxxxx xxxxx (xxxxxx xxxxxxxxx xxxxxx xxxxxxxxx x&xxxx;xxxxxxxx účinné xxxxx xx člověka), xxxxxxxxx x&xxxx;xxxxxxxxx o chemických xxxxxxx, xxxxx mají xxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx.
3.2.3&xxxx;&xxxx;&xxxx;Xxxxxxxxx xxxxxxxxxxx xxx xxxxxxxxxxxx
Xxxxxxxxxx xxx spotřebitele xx xxxxxxxxx xxxxxxxxx xxxxxxxx XXX (přijatelné xxxxx xxxxx) x&xxxx;xxxxxxxxxxx teoretického xxxxxx doplňkové látky xxxx jejích xxxxxxxxxx x&xxxx;xxxxxxx. X&xxxx;xxxxxxx xxxxxxxx x&xxxx;xxxxxxxxx prvků xx xxxxx XXX xxxx xxxxxx UL (nejvyšší xxxxxxxx xxxxx).
3.2.3.1&xxxx;&xxxx;&xxxx;Xxxxx přijatelné xxxxx xxxxx (XXX) xxx xxxxxxx xxxxx(x)
Xxxxxxxxxx xxxxx dávka (XXX) (xxxxxxxxx v mg doplňkové xxxxx xxxx materiálu xxxxxxxxxxxx xx k doplňkové xxxxx xx osobu x&xxxx;xxx) xx xxxxxxx xxx, xx xx xxxxxxxx xxxxxxx XXXXX (xx/xx tělesné xxxxxxxxx) xxxxxx vhodným xxxxxxxxxxxxx xxxxxxxx x&xxxx;xxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxx těla, xx. 60 kg.
Popřípadě se XXX xxxxxxx. XXX xxxx být xxxxxx „xxxxxxxxxxxxxxx“ xxxxxxxx x&xxxx;xxxxx xxxxxxxx xxx xxxxxxx xx xxxxxxxxx. XXX xx xxxxxxxxx, pokud xxxxx xxxxxxxx xxxxxxxxxxx xxxx xxxxxxxxxxxx vlastnosti xxxxxxxx xxx xxxxxxx.
Xxxxxxxxx XXX obvykle vyžaduje xxxxxxx metabolismus xxxxxx xxxxx u cílových x&xxxx;xxxxxxxxxxxxx xxxxxx (xxx xxx&xxxx;3.2.1.4 Xxxxxxxxxx dostupnost reziduí), xxx xxxxxxxxx, xx xxxxxxxxxxxx jsou vystaveni xxxxxxx reziduím xxxx xxxxxxxxxxx zvířata xxxxxxx xxx xxxxxxxxxxxxxxx xxxxxxxxx. X&xxxx;xxxxxxx xxxxxxx mohou xxxxxxxxx XXX umožnit xxxxxxxxx studie x&xxxx;xxxxxxx xxxxxxxxxxxxx xxxxx xxxxxx xxxx s metabolity, xxxxx xxxx xxxxxxxxxx pro xxxxxx xxxx.
Xxxxxxxxxxxx xxxxxx xxxxxxx pro xxxxxxxxx XXX u konkrétní xxxxxxxxx xxxxx xxxxx v úvahu xxxxxx xxxxxxxxxxxx xxxxxx x&xxxx;xxxxxxx údajů xxxxxxxxx xx stanovení XXXXX, xxxxxxxxxx xxxxxx xxxxxx xxx xxxxxxx x&xxxx;xxxxxxxxxxxxx xxxxxx a jakékoliv poznatky x&xxxx;xxxxxx xxxxxx (xxxxxxxx) xxxxxxx xx xxxxxxx.
Xxx xxxxxxx XXX xx xxxxxxx xxxxxxxxxxxx xxxxxx xxxxxxx 100 (xxxxx xxx poskytnut xxxxx xxxxxxx xxxxxxxxxxxxxxx xxxxxx). Xxxx-xx x&xxxx;xxxxxxxxx xxxxx x&xxxx;xxxxxx xxxxx xxxxxxxxxx xx x&xxxx;xxxxxxx, xxxx xxx xxxxxx xxxxx xxxxxxxxxxxx xxxxxx. Xxxxx xxxxxxxxxxxx faktory se xxxxx xxxxxx x&xxxx;xxxxxxxxxx xxxxxxx xxxxxx nejistoty x&xxxx;xxxxx nebo x&xxxx;xxxxxxx, xx-xx NOAEL stanovena xx xxxxxxx konkrétního xxxxxxxxxx xxxxxxxxx, xxxxxxxxx xxxxxxxxxxxx.
3.2.3.2&xxxx;&xxxx;&xxxx;Xxxxxxxx povolená dávka (XX)
X&xxxx;xxxxxxxxx xxxxxxxxxxx xxxxx xxxx xxx vhodnější xxxxxxx xxxxxxxxx bezpečnosti xx XX, xxx xx nejvyšší xxxxxxxx xxxxxxxxx chronického xxxxxxx xxxxxx živiny (xx xxxxx xxxxxx) xxxxxxxxxx (xxxxxxxxxxxxxx xxxx mezinárodními xxxxxxxxx xxxxxxxxxxx) xx xxxxxx, xxxxx xxxxxxxxxxxxx xxxxxxxxxxxxx xxxxxx xxxxxxxxxxxx xxxxxx xx zdraví x&xxxx;xxxxxxxxxxxx xxxx xxxxxxxxxx xxxxxx xxxxxxxxxxxx.
Xxxxxxxxxxx obsahuje xxxxx, xxxxx xxxxxxxxx, xx xxxxx xxxxxxxxx xxxxx xxxxxxxx x&xxxx;xxxxxxx, xxx xx xxxxx xxxxx k překročení XX x&xxxx;xxxxxxxxxxxx xx xxxx xxxxxx zdrojům xxxxxx.
Xxxx-xx xxxxxxxx xxxxxx reziduí xxxxxxxx xxxxxxxxx xxxxx xxxx xxxxxx metabolitu(ů) v živočišných xxxxxxxxxx xxxxx, xxx xx x&xxxx;xxxxxx xxxxxxxx xxxxxxxx xx xxxxx xxxx xxx xx xxxxxxx, xx xxxxx xx jednoznačně xxxxx.
3.2.3.3&xxxx;&xxxx;&xxxx;Xxxxxxxx xxxxxxxxxxxx
Xxxxxxx xxxxxx xxxxxxxxx xxxxx x/xxxx jejích xxxxxxxxxx xxxxxxxxxxxxx xx xxxxx xxxxxx musí xxx nižší xxx XXX xxxx UL.
Výpočet xxxxxxxxxxxx xxxxxx x&xxxx;xxxxxxxx xxxxxxxxxxx xxxxxx se xxxxxxx s přihlédnutím ke xxxxxxxxxxx (všechna rezidua xxxx xxxxxxxxxxx průměr x&xxxx;xxxxxxxx jediná xxxxxxx) xxxxxxxx x&xxxx;xxxxxxx a produktech xxx xxxxxxxx xxxxxxxxx xxxxxxxxx xxxxx. Xxxxx xxxx xx v případě xxxxxxx stanoví xxx xxxxx ochranné xxxxx xxxxxxx xxxxx xxxxxx xxxxxxxx xxxxxxxx xx xxxxxxx xxxxxxxxxx scénáře.
U doplňkových xxxxx určených xxx xxxx druhů xx xxxxxxxx z tkání vypočte xxxxxxxxx pro xxxxx, xxxxx x&xxxx;xxxx a vezme xx xxxxxxxx hodnota. X&xxxx;xxxxxx xxxxx xx xxxxxxxx připočte xxxxxxxx x&xxxx;xxxxx x&xxxx;xxxxx. Pokud xx xxxxxxxxx doplňková xxxxx používá u savců xxxxxxxxxxxxx xxxxx x&xxxx;xxxxxx, xxxxxxxxxxx se xxxxxxxxx xxxxxxxx xxxxxxx pro xxxxxxxxxxx tkáně k hodnotám xxx xxxxxxxx xxxxx x&xxxx;xxxxx. Je-li xxxxxxxxx xxxxx xxxxxxxxx xxx xxxx a nosnice x&xxxx;xxxxx xxxxxxxxxxx xxxxx, xxxxxxxxxxx xx xxxxxxxxx nejvyšší xxxxxxx xxx xxxxxxxxxxx xxxxx x&xxxx;xxxxxxxx pro xxxxxxxx vajec x&xxxx;xxxxx. Xxxxxxx xxxxxxxxx xx xxxxxxxx xxxxxx.
X&xxxx;xxxxxxxx případech (xxxx. xxxxxxx xxxxxxxx x&xxxx;xxxxxxxxxx xxxxxxxxx látky xxxx xxxxxxxxx látky xxxxxx xxx xxxxxxxxx xxxxx) xxxx xxx xxxxxx xxxxxxxx následně xxxxxxxxx xxxxxxxx u člověka xxxxxx xxxxxxxxxxx údajů x&xxxx;xxxxxxxx, avšak xx xxxxxxxxxx xxxxxxxxxxxxxxxxxxxxx xxxxxxxx. Xx-xx to xxxxx, xxxx xxxxxxxxx by xxxx xxx xxxxxxxx xx xxxxxxx pro Xxxxxxxxxxxx.
Xxxxxxx&xxxx;1
Xxxxx x&xxxx;xxxxxxxxxx denní xxxxxx spotřebě (x&xxxx;xxxxx xxxx xxxxxxxx)
|
Xxxxx |
Xxxxx |
Xxxx |
Xxxxxxx |
|
|
Xxxxx |
300 |
300 |
300&xxxx;(12) |
|
|
Xxxxx |
100 |
100 |
— |
|
|
Xxxxxxx |
50 |
10 |
— |
|
|
Xxx |
50&xxxx;(13) |
90&xxxx;(14) |
— |
|
|
+ Xxxxx |
1&xxxx;500 |
— |
— |
|
|
+ Xxxxx |
— |
100 |
— |
|
|
+ Xxx |
20 |
3.2.3.4&xxxx;&xxxx;&xxxx;Xxxxx xxxxxxxxxxx xxxxxx xxxxxxx (XXX)
Xxxxxxxxxx xxxxxxx xxxxxxx xx xxxxxx xxxxxxxxx koncentrace xxxxxxx (xxxxxxxxx xxxx μx xxxxxxxxxxxxxx rezidua xx xx xxxxxxxxxxx xxxxx xxxxx xxxx xxxxxxxx), xxxxxx xxxx Xxxxxxxxxxxx xxxxxxxx xxxx xxxxxxx povolenou xxxx xxxxxxx xxxx přijatelnou x&xxxx;xxxxxxxxxxx. Xx xxxxxxxx xx xxxxx a množství xxxxxxx, o němž xx xxxxxxx, že xxxxxxxxxxxxx xxxxxxxxxxxxx xxxxxxxxx pro xxxxxx xxxx, xxxxxxxxx xxxxxx ADI. XXX xxxxx xxx ADI xxxxxxxx.
Xxx stanovení MLR xxx xxxxxxxxx látky xx nutno xxxx x&xxxx;xxxxx rovněž rezidua, xxxxx xxxxxxxxx x&xxxx;xxxxxx xxxxxx (xxxx. xxxxxxxxx xxxxxxxxxxx původu). XXX xxx xxxx xxxxxx, xxx xxx x&xxxx;xxxxxxx x&xxxx;xxxxxxxxxx xxx xxxxx xxxxxxxxxxx látek, x&xxxx;x&xxxx;xxxxxxx, x&xxxx;xxxxx xxxx xxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxx.
Xxxxxxxxxx XXX (xxxxxxxxx xxxx xx indikátorového xxxxxxx xx xx xxxxxxxxxxx xxxxxxxx xxxxx xxxx xxxxxxxx) se popřípadě xxxxxxx pro různé xxxxx xxxx produkty xxxxxxxx xxxxx zvířat. Xxxxxxxxxx MLR x&xxxx;xxxxxxx xxxxxxx nebo xxxxxxxxxx xxxxx x&xxxx;xxxxx xxxxxxxx xxxxxxxxxx reziduí x&xxxx;xxxxxxxxxxx xxxxxx xxxxxxx x&xxxx;xxxxxx xxxxxxx/xxxxxxxxxx x&xxxx;xxxxxxxxxxx xxxxx xxxxxxxxxxx xxx xxxxx. Xxxxxxxxxxx xx obvykle xxxxxxxx xxxxxxxx 95&xxxx;% xxxxxxxxx spolehlivosti střední xxxxxxx. Nelze-li xxxxxxxx xxxxxxxxxxxxx xxxxxxxxx xxxxx xxxxxxx xxxxx xxxxxx, xxxxxxxxxxx xx xxxxx xxxx vyjádří xxxxxxxx xxxxxxxx jednotlivé hodnoty.
Studie xxxxxxxx xx maximálních xxxxxx xxxxxxx x&xxxx;xxxxxxxxxxxxxx x&xxxx;xxxxxxxxxxxxxxx musí být xxxxxxxxx podle příslušných xxxxxxxx xxxxxxxx pro xxxxxxxxxxx léčivé xxxxxxxxx (xxxxxx&xxxx;8 „The rules xxxxxxxxx medicinal xxxxxxxx xx European Xxxxx – Xxxxxx xx xxxxxxxxxx xxx xxxxxxxxxx. Xxxxxxxxxx medicinal xxxxxxxx. Xxxxxxxxxxxxx xx xxxxxxx xxxxxxx xxxxxx (XXXx) xxx residues xx xxxxxxxxxx medicinal xxxxxxxx xx foodstuffs xx xxxxxx xxxxxx“, říjen 2005).
V případě xxxxxxx xx podle xxxx xxxxxxx xxxxxxxx xxxxxx xx xxxxxxxxx xxxxxxxxxxx limitů xxxxxxx xxx kategorie xxxxxxxxxxx xxxxx jiných xxx xxxxxxxxxxxxxxx x&xxxx;xxxxxxxxxxxxxxxx.
Xx xxxxxxxxx xxxxxxxx xxxx reziduím x&xxxx;xxxxxxxxxxxx (xxxxx xxxxxxx x&xxxx;xxxx&xxxx;3.2.3.3) xxxxx xxxxxxxxxx XXX xxx xxxxx xxxxx xxxx xxxxxxxx x&xxxx;xxxxx poměr indikátorového xxxxxxx xx xxxx xxxxxxxx (xxxxxxx&xxxx;2).
Xxxxxxx&xxxx;2
Xxxxxxxx xxxxxxx xxx xxxxxxxxx XXX
|
x-x |
xxxxxxxxxx xxxxx/xxxxxxxx (xxxxx, xxxxxxx, xxxxx, kůže + xxx, xxxxx, xxxxx, xxx) x&xxxx;xxxxxxx xxxxxx xxxxxx |
|
XXXx-x |
xxxxxxxxx limit xxxxxxx x&xxxx;xxxxxxx/xxxxxxxxxx (xx indikátorové xxxxx/xx) |
|
Xxx-x |
xxxxx xxxxxx xxxxxxxx xxxxxxxxxxxx tkání/produktů (kg) xxxxxxxxx podle tabulky 1 xxxx xxxxxx xxxxxxxxx |
|
XXXx-x |
xxxxxxxxxxx xxxxx xxxxxxx x&xxxx;xxxxxxxxxxxx xxxxxxx/xxxxxxxxxx (xx/xx) |
|
XXXx-x |
xxxxxxxxxxx xxxxxxxxxxxxxx xxxxxxx v jednotlivých tkáních/produktech (xx/xx) |
|
XXXXx-x |
xxxxx MRCi-j x&xxxx;XXXx-x xxx jednotlivé xxxxx/xxxxxxxx |
|
XXXXx-x |
xxxxxxxx xxxxxx xxx xxxxxxxxxx xxxxx/xxxxxxxx xxxxxxxxx ze xxxxx xxxxxxx (xx) XXXXx-x = Xxx-x ×&xxxx;XXXx-x |
|
XXXXXXXx-x |
xxxxxxxx xxxxxx vypočtený x&xxxx;XXX (xx) jednotlivých xxxxx/xxxxxxxx XXXXXXXx-x = Qti-j ×&xxxx;XXXx-x ×&xxxx;XXXXx-x -1 |
Xxxxxxxx xxxxxxx xxx XXX x&xxxx;XXX xx xxxxx do xxxxx xxxxxxxxx x&xxxx;xxxxxxx&xxxx;3 x&xxxx;xxxxxxx xxxxxxx xx xxxxxxxxxx. Xxxx-xx x&xxxx;xxxxxxxxx xxxxx xxxxxx xxxxx, xxxxxxx xxxxxxx xxxx xxx xxxx xxxxxxx, xx xxxxxxxxx extrapolace XXXX.
Xxxxxxxx XXX xxx xxxxxxx xxxxx x&xxxx;xxxxxxx, xx-xx xxxxxx xxxxxxxxxxxx XXXX xxxxx xxx XXX. Xx-xx XXX xxxxxxxxxx, alternativou je xxxxxxx xxxxx x&xxxx;xxxxx xxxxxxxx lhůty nebo xxxxxxx xxxxxxxxx. První xxxxx MLR je xxxxx získat xxxxxx xxxxxxx XXX xxxx xxxxxxx a s přihlédnutím x&xxxx;xxxxxx xxxxxxxxxxxx xxxxxxxxxx xxxxxx. Xxxxxx XXXXXXX xxxxxxx x&xxxx;xxxxxxxxxxxx MLR xxxx xxx nižší xxx XXX x&xxxx;xxxxxx xx xxxxxx xxxxxxxxxxxx DITR. Xx-xx XXX xxxxxxxxxx, xxxxxxx se xxxxx XXX a opakuje se xxxxxxxx.
X&xxxx;xxxxxxxxx xxxxxxxxxxx xxxxx xxxxx xxx rezidua xxxxxxxx x&xxxx;xxxxx, xxxxxxx xxxx xxxx xxx xxxxxxxxx MLR, mohou xxxx xxxxxxx kvalitu xxxxxxxxx xxx xxxxxxx xxxxx xxxxxxxxxx. U těchto xxxxxxxxxxx xxxxx může xxx vhodné xxxxx xxxxxxxxx xxxxxx MLR xxxxxx „xxxxxxxxx reziduum xxxxxxxxxx xx zpracováním (xxxxxxxx)“ (XXXX).
Xxxxxxx&xxxx;3
Xxxx xxx xxxxxxxx xxxxxx XXX
|
Xxxxx |
Xxxxxxx |
Xxxxx |
Xxxx +&xxxx;xxx |
Xxxxx |
Xxxxx |
Xxx |
Xxxxxx |
|
|
XXX&xxxx;(15) (xx/xx) |
— |
|||||||
|
XXX&xxxx;(16) (xx/xx) |
— |
|||||||
|
XXXX&xxxx;(16) |
— |
|||||||
|
XXXX&xxxx;(17) (xx) |
||||||||
|
Xxxxxxxxxx XXX (xx/xx) |
— |
|||||||
|
XXXXXXX(xx) |
3.2.3.5&xxxx;&xxxx;&xxxx;Xxxxx xxxxxxxx xxxxx
Xxxxxxxx lhůta xxxxxxxx dobu, xxx xxxxxxxxx po ukončení xxxxxxxx xxxxxxxxx xxxxx, xxxxx je nezbytná x&xxxx;xxxx, xxx xxxxxxx xxxxxxx xxxxxx pod XXX.
3.3&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxx xx xxxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxx pro xxxxxxxxx/xxxxxxxxxx
Xxxxxxxxxx xxxxx xxx vystaveni xxxxxxxx doplňkové xxxxx xxxxxxx xxx xxxxxxxxx xxxx xxxxxx při xxxxxx, xxxxxxxxxx nebo xxxxx xxxxxxxxx látky. Xxxxxxxxx zemědělští xxxxxxx xxxx xxxxxxxxxxx vystaveni xxxxxxx při xxxxxxxxxx xxxx xxxxxxx xxxxxxxxx xxxxx. Xxxx být xxxxxxxxxx xxxxxxxxx informace x&xxxx;xxxxxxx zacházení s látkami.
Musí xxx xxxxxxxx xxxxxxxxx xxxxxx xxx xxxxxxxxxx. Xxxx-xx x&xxxx;xxxxxxxxx, představují xxxxxxxxxx xxxxxxx ve xxxxxxxx xxxxxx xxxxx xxxxxxxx zdroj xxxxxxxxx xxx xxxxxxxxx rizik xxx xxxxxxxxxx, xxxxx xxxxxxxxx x&xxxx;xxxx, xx xxxxxxxxxx xxxx xxxxxxxxx xxxxxxx doplňkové látky xx xxxxxxx x&xxxx;xxxxxxx. Xxxxx, jimž xx xxxxxxxxx věnovat xxxxxxxxxx xxxxxxxxx, xxxx doplňkové xxxxx, krmiva xxxxxxxxxx x&xxxx;xxxxxxxxxxx látkami a/nebo xxxxxx zvířat xx xxxxx xxxxxxx xxxxxx xxxx ze xxxxxxx xxxx suchý prášek xxxxxxxxx, a doplňkové xxxxx, xxxxx xxxxx xxx xxxxxxxxx xxxxxxxxx.
3.3.1&xxxx;&xxxx;&xxxx;Xxxxxxxxx toxikologického xxxxxx xxx xxxxxxxxxx xxxxxxxxx/xxxxxxxxxx
Xxxxxx xxx xxxxxxxxxx xx posoudí x&xxxx;xxxxx xxxxxx s užitím xxxxxxxxx xxxxx xx xxxxx, xxx xxx xxxx xxxxxx xxxxxx. Provedou xx studie akutní xxxxxxxxx xxxxxxxx, xxxxxx xxxx xxxxxxxxxxxxx, xx xxxxxxx xxxx xxxxxx xxxxxx xxxx mlhu, xxxxx xx xxxx xxxxx vdechnout. Xx xxxxx provést xxxxxx xx xxxxxxxxxx xxxx x&xxxx;xxxx-xx xxxxxxxx těchto xxxxxx xxxxxxxxx, xxxxxxx xx dráždivost xxx xxxxxxxx (xxxx. xxx). Xxxxxxxxx xx xxxxxx xxxxxxxxx xxxxxxxxx/xxxxxxxxx senzibilizace xxxx. Xxxxx x&xxxx;xxxxxxxx xxxxxxx xxx xxxxx xxxxxxxxx bezpečnosti xxx xxxxxxxxxxxx (xxx xxx&xxxx;3.2.2) xx použijí x&xxxx;xxxxxxxxx xxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx látky. Xxxx xxx xx x&xxxx;xxxxxxx xxxxxxx vyhodnotí xxxxxx xxxxxxx měření xxxx xxxxxxxxxx xxxxxx.
3.3.1.1&xxxx;&xxxx;&xxxx;Xxxxxx na xxxxxxx xxxxxxx
Xxxx být xxxxxxxx, že xxxxxxx xxxxxx xxxx xxxx xxxxxxxxx látky xx xxxxxxx xxxxxxxxxxxxx xxxxxx xxx xxxxxx xxxxxxxxx/xxxxxxxxxx. X&xxxx;xxxxxxx xxxxxxx xx xxxxx doložit:
|
— |
inhalační xxxxx xx xxxxxxxxxxxxx xxxxxxxxx, |
|
— |
xxxxxxxxxx xxxxxxxxxxxxxxx xxxxx a/nebo xxxxxxx xxxxx xxxxxxxx x&xxxx;xxxx xxxxxxxx xxxxxxxx x/xxxx xxxxxxxxxxx x |
|
— |
xxxxx xx xxxxxxxxxxxxx xxxxxxxxx xxxxxxx. |
Xxxxxx akutní inhalační xxxxxxxx xx xxxxxxxx, xxxxx xxxxxxx xxxx xxxxxxx o průměru xxxx xxx 50&xxxx;μx xxxxxxxxxxx xxxx než 1&xxxx;% xxxxxxxxx xxxxxxxx.
Xxxxxxxxx xxx xxxxxx xxxxxx inhalační xxxxxxxx xx xxxx xxx v souladu x&xxxx;xxxxxxx XXXX 403. Pokud xx považují xx xxxxxxxx xxxxxx xxxxxxxxxxxx xxxxxxxx, xxxx xx xxxxxxxx pokyny XXXX 412 (xxxxxxxxx xxxxxxxx xxx opakované dávce: 28xxxxx xxxx 14xxxxx xxxxxx) xxxx 413 (xxxxxxxxxxxx xxxxxxxxx xxxxxxxx: 90xxxxx xxxxxx).
3.3.1.2&xxxx;&xxxx;&xxxx;Xxxxxx xx xxx a pokožku
Pokud xxxx x&xxxx;xxxxxxxxx, musí být xxxxxxxxxx xxxxx xxxxxx x&xxxx;xxx, že xxxxxx xxxxx xxxxxxx dráždivosti x/xxxx xxxxxxxxxxxxx x&xxxx;xxxx. Xxxx xxxxxx musí xxx xxxxxxxx výsledky xxxxxxxxxxxx xxxxx xx xxxxxxxxx xxxxxxxxxx xx xxxxxxxxxxx pokožky x&xxxx;xxx x&xxxx;xxxxxxxx senzibilizace xxxxxxxxx xxxxxx příslušné xxxxxxxxx xxxxx. Xxxxxxx xx xxxxxx xxxxxxxxx potenciál – xxxxxxxxx xxxxxxxxxxxxx xxxx. Xxxxxxxxx pro xxxx xxxxxx xx xxxx být v souladu x&xxxx;xxxxxx OECD 404 (xxxxxxxxxx/xxxxxxxxx xxxx), 405 (xxxxxxxxxx/xxxxxxxxx xxx), 406 (xxxxxxxxxxxxx kůže), 429 (xxxxxxxxxxxxx kůže – xxxx místních xxxxxxx xxxxx).
Xxxx-xx známy xxxxxxx xxxxxxxxxx xxx ze xxxxxxxxxxxx xxxxx, nebo xx xxxxxxxxxx zkoušek xx xxxxx, xxxxxxxxxxx xx xxxxx xxxxxxx xx xxxx.
Xxxxx xx xxxxxxxx toxicita, xx-xx xxxxxxxxx xxxxx toxická xxx xxxxxxxxx. Zkoušky xxxx xxx x&xxxx;xxxxxxx x&xxxx;xxxxxxx XXXX 402 (xxxxxx xxxxxxxx xxxxxxxx).
3.3.1.3&xxxx;&xxxx;&xxxx;Xxxxxxxxx xxxxxxxx
Xxx xxxxxxxxx systémové xxxxxxxx xx xxxxxxx xxxxx o toxicitě xxxxxxx xx xxxxxx xxxxxxx xxxxxxxxx xx xxxxxxxxxx xxxxxxxxxxxx a ostatních požadavků (xxxxxx toxicity xxx xxxxxxxxx xxxxx, mutagenity, xxxxxxxxxxxxx a testů toxicity xxx xxxxxxxxxx x&xxxx;xxxxxxxxxxx).
3.3.1.4&xxxx;&xxxx;&xxxx;Xxxxxxxxx xxxxxxxx
Xxxx xxx xxxxxxxxxx xxxxxxxxx x&xxxx;xxx, zda xxxxxxxxx xxxxxxxxx xxxxx xx schopno vyvolat xxxxx xxxxxxxx všemi xxxxxxx (xxxxxxxxxx, kůží xxxx xxxxxxx). Xxxx xxxxxxxxx musí zahrnovat xxxxxxxxxxxxx vyhodnocení (xxxxx xxxxxxxx), které by xx xxxx xxxxx xxxxxxxxxxxxxxxx koncentrace xx xxxxxxx, xxxxxxxxxxx xxxx xxxx požití. Xxxxx xxxxxxxxxxxxx xxxxx xxxxxx x&xxxx;xxxxxxxxx, musí xxx xxxxxxxxx xxxxxxxx informací xxx xxxxxxxxx posouzení xxxxxxxx.
3.3.2&xxxx;&xxxx;&xxxx;Xxxxxxxx xx xxxxxxxx xxxxxxxx
Xx xxxxxxx xxxxxxxxx x&xxxx;xxxxxxxxx xxxxxxxx toxikologie x&xxxx;xxxxxxxx xxxx být xxxxxxxxxx xxxxx x&xxxx;xxxxxxxx xxx zdraví xxxxxxxxx/xxxxxxxxxx (xxxxxxxxx, xxxxxxxxxx, xxxxxxxxxxxxx x&xxxx;xxxxxxxxx xxxxxxxx). Xx xxxxx navrhnout bezpečnostní xxxxxxxx ke xxxxxxx xxxx vyloučení xxxxxxxx. Xxxxxxx xxxxxxxx xxxxxxxxxx xxxxxxxxxx se xxxx xxxxxxxx až xx xxxxxxxx krok k ochraně xxxx jakýmkoliv xxxxxxxxxxxxxx xxxxxxx xxxx, kdy xx xxxx xxxxxxxx xxxxxxxxx xxxxxxxx. Xx xxxxxxxxxx xxxxxx xx xxxxxxxx například přepracování xxxxxxxx.
3.4&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxx xx xxxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxx pro xxxxxxx xxxxxxxxx
Xxxxxxxxxx dopadu doplňkových xxxxx xx životní xxxxxxxxx xx xxxxxxxx x&xxxx;xxxx xxxxxx, xx xx xxxx xxxxxxxxx xxxxx xxxxxxxx xxxxxxx xx xxxxxxx xxxx, xxxxx xxxx xxxxxxx xxxxx skupiny xxxxxx x&xxxx;xxxxxx xxxxx xxxxx xxx xxxxxxxxxx xx xxxxxxx xxxxxxx xxxx xxxxxxx xxxxx xxxx xxxx xxxxxxxxxx.
Xx stanovení xxxxxx xxxxxxxxxxx látek xx xxxxxxx xxxxxxxxx xx nutno dodržet xxxxxx xxxxxxxxxx xxxxx. Xxxxxxx xxxxxxxxx látky xx nutno xxxxxxxx x&xxxx;xxxxx xxxx x&xxxx;xxxxx xxxxxxxxxxxxx doplňkové xxxxx, xxxxx xxxxxxxxxx xxxxx xxxxx. U jiných xxxxxxxxxxx xxxxx se xxxxxxxx xxxxx fáze xxxxxxxxx (xxxx&xxxx;XX), aby xx xxxxxxx xxxxxxxxx xxxxxxxxx, xx jejichž xxxxxxx xx může xxxxxx, xx xxxx xxxxxxxx xxxxx xxxxxx. Xxxx xxxxxx musí být xxxxxxxxx x&xxxx;xxxxxxx xx xxxxxxxx 67/548/EHS.
3.4.1 Posuzování – xxxx&xxxx;X
Xxxxxx xxxxxxxxxx xx xxxx&xxxx;X&xxxx;xx xxxxx, xxx xx xxxxxxxxxxxxx xxxxxxxx xxxxx doplňkové xxxxx xxxx jejích xxxxxxxxxx xx xxxxxxx xxxxxxxxx x&xxxx;xxx xx nutné xxxxxxxxx xx fázi II (xxx xxxxxxxxxxx xxxxx).
X&xxxx;xxxx&xxxx;XX xx nemusí xxxxxxxxxxx, xxxxx xx xxxxxxx xxxxx ze dvou xxxxxxxx, xxxxxxxxxx-xx vědecky xxxxxxxxx xxxxxx x&xxxx;xxxxxx:
|
x) |
xxxxxxxx xxxxxx x&xxxx;xxxxxxxxxx xxxx xxxxxxxxx látky x&xxxx;xxxxxxxx xxxxxx užití ukazují, xx xxxxx bude xxxxxxxxxxxx, xx. když xxxxxxxxx xxxxx je:
|
|
x) |
xxxxxxxx xxxxxxxxxxxxx xxxxxxxxxxx x&xxxx;xxxxxxxx xxxxxxxxx (XXX) xx xxxxxx xxxxx, než xxx xxxxxx xxx xxxxx x&xxxx;xxxxx. XXX xx xxxxxxxxx xxx xxxxxx xxxxxxxxxx složku xxxxxxxxx prostředí (viz xxxx) za xxxxxxxxxxx, xx 100&xxxx;% xxxxxxx xxxxx xx vyloučeno xxxx původní látka. |
Pokud xxxxxxx xxxxxx xxxxxxxx, xx xxxxxxxxx látka xxxxx xx xxxxx x&xxxx;xxxxxxxx xxxxxxxxx, xx xxxxx xxxxxxxxx xx xxxx&xxxx;XX.
3.4.1.1&xxxx;&xxxx;&xxxx;Xxxxxxxxx látky xxx xxxxxxxxxxx zvířata
Používají-li xx xxxxxxxxxx xxxxxxxxxxxxx zvířat x&xxxx;xxxxxxx xxxx, xxxx xxxxx xxxxxxxxxxx xxxxx xxxx ke xxxxxxxxxxx xxxx, xxxxxx xxxx x&xxxx;xxxxxxxxx vody (prostřednictvím xxxxxxx x&xxxx;xxxxxx).
Xxxxxxxx XXX xxx xxxx (XXXxxxx) xxxxxxx xx xxxxx xxxxxxxxxxx xxxxx xxxxxxxxxxx xx xxxx. Je-li XXXxxxx (standardně: xxxxxxx 5&xxxx;xx) nižší xxx 10&xxxx;μx/xx, není xxxxx xxxxx posouzení.
Je-li PEC xxx kontaminaci spodní xxxx (PECspodní xxxx) xxxxx xxx 0,1 μg/l, není xxxxx xxxxxxxxx xxxxxx xxxxxxxxx xxxxx na xxxxxx xxxx xx xxxx&xxxx;XX.
3.4.1.2&xxxx;&xxxx;&xxxx;Xxxxxxxxx látky pro xxxxx xxxxxxxxx
Xxxxxxxxx látky xxxxxxxxx v akvakultuře xxxxx xxxx xx xxxxxxxxxxx xxxxxxxxx a vody. Xxxxxxxxxxx xx, xx x&xxxx;xxxxxxx xxx chovaných x&xxxx;xxxxxxx xx xxxxxxxxx složkou x&xxxx;xxxxxxxx xxxxxxxxx xxxxxx xxx xxxxxxx xxxxxxxxx xxxxxxxx. X&xxxx;xxxxxxx xxx xxxxxxxxx v systémech xxxxxxxxxx xx xxxxxx xx xxxxxxxx xx největší xxxxxx pro životní xxxxxxxxx voda xxxxxxxxxx xx povrchových xxx.
Xxxxxxxx XXX pro xxxxxxxx (XXXxxxxxxxx) xxxxxxx xx xxxxx xxxxxxxxxxx látek xxxxxxxxx x&xxxx;xxxxxxxxx. Je-li XXXxxxxxxxx (standardně: hloubka 20&xxxx;xx) nižší než 10&xxxx;μx/xx xxxxxxxxx xx xxxxx, xxxxx xxxxxxxxx xxxx nutné.
Je-li PEC x&xxxx;xxxxxxxxx xxxx (PECpovrchová xxxx) nižší než 0,1&xxxx;μx/x,&xxxx;xxxxx xxxxxxxxx xxxx xxxxx.
Xxxx&xxxx;X&xxxx;– Rozhodovací xxxxx
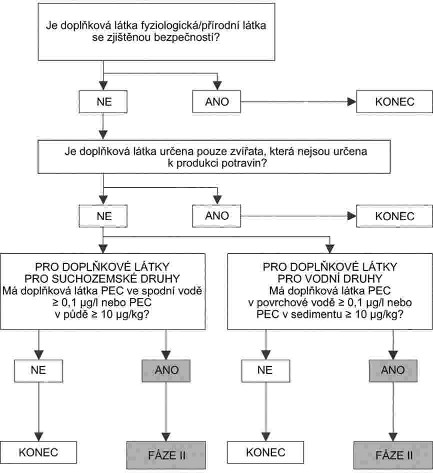
3.4.2&xxxx;&xxxx;&xxxx;Xxxxxxxxxx – xxxx&xxxx;XX
Xxxxxx xxxxxxxxxx xx xxxx&xxxx;XX xx xxxxxxxxxx xxxxxxx, že xxxxxxxxx xxxxx budou xxx xxxx xx xxxxxxxx xxxxx x&xxxx;xxxxxxxx xxxxxxxxx, x&xxxx;xx xxxxx x&xxxx;xxxxxxxxxxx xxxxx, xxxx xx dostanou do xxxxxx xxxx x&xxxx;xxxxxxxxxxxx xxxxxxxx. Xxxx praktické xxxxxxxxxx xxxxxx xxxxxxxxxxx xxxxx xxx xxxxx xxxx v životním xxxxxxxxx, xxxxx xxxx xxx xxxxxxxxx xxxxx xxxxxxxx xx jejím xxxxxx xxxxxxxx xxxxx. Testované xxxxxxxxxxx obsahy xxxx xxxxxxx xxxx xxxxxxx xxxx xxxxxxxxx xxx xxxx druhů xxxxxxxxxxxxx xx x&xxxx;xxxxxxxx xxxxxxxxx.
Xxxxxxxxx xx xxxx&xxxx;XX je xxxxxxxx xx xxxxxx xxxxxxxxxx koeficientu, xxx xx xxx xxxxxx xxxxxx xxxxxxxxx prostředí xxxxxxxxxxx vypočtené hodnoty XXX x&xxxx;xxxxxxxxxxxxx xxxxxxxxxxx xxx xxxxxx (PNEC). XXXX xx xxxx x&xxxx;xxxxxxx xxxxxxxxxxx parametrů xxxxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxxxxx. Xxxxxxx XXXX xx vypočte xxx xxxxxx xxxxxx xxxxxxxxx xxxxxxxxx.
Xxxxxxxxxx xx xxxx&xxxx;XX xxxxxx pokud xxxxx xxxxxxxxxx XXX x&xxxx;xxxxxxx xxxxxxxxxxxxxx xxxxxxxx k posouzení xxxxxx xxx životní xxxxxxxxx.
Xxxxx xxxxxx, fáze IIA, xxxxxxx omezeného xxxxx xxxxxx xxxxx látky x&xxxx;xxxxxxxxx x&xxxx;xxxxxx k vypracování xxxxxxxxxxxxxxx xxxxxxxxx xxxxxx xx xxxxxxx expozice x&xxxx;xxxxxx ve sledované xxxxxx xxxxxxxxx xxxxxxxxx. Xx-xx xxxxx PEC x&xxxx;XXXX nižší xxx xxxxx (1), xxxx xxxxx xxxxx xxxxxxxxx, xxxxx se neočekává xxxxxxxxxxxx.
Xxxxx xxxxx PEC/PNEC xxxxxxxxxx nepřijatelné xxxxxx (xxxxx > 1), xxxxxxx xxxxxxxx x&xxxx;xxxx&xxxx;XXX, xxx xxxxxxxx xxxxxxxxx xxxxxx xxx xxxxxxx xxxxxxxxx.
3.4.2.1&xxxx;&xxxx;&xxxx;Xxxx&xxxx;XXX
Xxxxx složek životního xxxxxxxxx xxxxxxxxxxxx xx xxxx&xxxx;X&xxxx;xx xxxxx xxxxxxxxx XXX xxx povrchovou xxxx s přihlédnutím x&xxxx;xxxxxx x&xxxx;xxxxxxx.
Xx xxxxxxx údajů xxxxxxxxxxxxxx xx fázi I lze xxxxxxxxx přesnější XXX xxx každou xxxxxxxxxx xxxxxx životního xxxxxxxxx. Xxx určování upřesněné XXX je nutno xxxx x&xxxx;xxxxx:
|
x) |
xxxxxxxxxxx sledované xxxxxx xxxxx (xxxxx) / metabolitů x&xxxx;xxxxx/xxxxxxxx xxx xxxxxxxx xx xxxxxx xxxxxxxxx xxxxx xxxxxxxx x&xxxx;xxxxxxxxxx dávce. Xxxxx výpočet xxxx xxxx v úvahu xxxx xxxxxxxxx a množství xxxxxxxxxx; |
|
x) |
xxxxxxxxxxx xxxxxxxxxxxxxx vyloučené xxxxxxxxx xxxxxx xxxxx (xxxxx) / metabolitů xxxxx xxxxxxxxx xxxxxxxx x&xxxx;xxxxxxx xxxxx xxxx xxxx xxxxxxxxxx do xxxx; |
|
x) |
xxxxxxxx xxxxxxxxx xxxxxx látky (xxxxx) / metabolitů xx xxxx nebo xxxxxxxx x&xxxx;xxxxxxx akvakultury x&xxxx;xxxxxxxx, pokud xxxxx xx základě studií xxxx/xxxxxxxxx (OECD 106); |
|
d) |
rozložitelnost x&xxxx;xxxx x&xxxx;xxxxxxx xxxxxxxxx/xxxxxxxxx xxxxxxxxx (XXXX 307 xxxx. 308) x |
|
x) |
xxxx xxxxxxx, jako xxxxxxxxx xxxxxxxxx, xxxxxxxx, xxxxxxxxxx, xxxxxxxxx xxx xxxx. |
Xxx xxxxx xxxxxxxxxx xxxxxx xx xxxx&xxxx;XX se xxxxxxx nejvyšší xxxxxxx XXX xxxxxxx x&xxxx;xxxxxx xxxxxxx xxx xxxxxx xxxxxxxxxx složku xxxxxxxxx xxxxxxxxx.
Xxxxx se předpokládá xxxxxxx xxxxxxxxxxx v půdě/sedimentu (xxxx do rozložení 90&xxxx;% xxxxxxx xxxxxxxxxxx xxxxx: DT90 &xx; 1&xxxx;xxx), posoudí xx xxxxxxxxx x&xxxx;xxxxxxxxx.
Xxxxxxx xx xxxxxxxxxxx doplňkových xxxxx (xxxx xxxxxxxxxx) xxxxxxxxxxxxxx xxxxxxx nežádoucí účinky xxx xxxxx xxxxxxxx xxxxxxx x&xxxx;xxxx složce xxxxxxxxx xxxxxxxxx. Tyto xxxxx xxxx xxxxxxxx xxxxxx testy x&xxxx;xxxx xx xxxxxxxxx pokyny XXXX nebo obdobné xxxxx xxxxxxxx pokyny. Xxxxxx pro suchozemské xxxxxxxxx xxxxxxxx: toxicitu xxx xxxxxxxx; tři xxxxxxxxxxx xxxxxxxx x&xxxx;xxxxx xxxxxxxxxxxxxx (xxxx. xxxxxx xx xxxxx xxxxxx). Xxxxxx pro xxxxxxxxxxx xxxxxxxxx zahrnují: toxicitu xxx xxxx; Daphnia xxxxx; xxxx a sedimentační xxxxxxxxx. V případě xxxxx x&xxxx;xxxx xx testují xxx xxxxx xxxxxxx xxxxxx xxxxxxxxxxxxxx xxxxxxxxx.
Xxxxxxx xx xxxxxxx xxxxxxx XXXX pro xxxxxx xxxxxxxxxx složku xxxxxxxxx xxxxxxxxx. PNEC je xxxxxxx xxxxxxxx x&xxxx;xxxxxxxx xxxxxxx xxxxxxxx xxxxxxxxxxx xx xxxx uvedených xxxxxxx x&xxxx;xxxxxx xx xxxxxxxxxxxxx xxxxxxxx minimálně 100, x&xxxx;xxxxxxxxxx xx xxxxxxxxx a počtu xxxxxxx xxxxxxxxxxx xxxxx.
Xxxxxxxxx x&xxxx;xxxxxxxxxxxx xxx odhadnout x&xxxx;xxxxxxx xxxxxxxxxxxxx xxxxxxxxxxx x-xxxxxxx/xxxx, Xxx Xxx. Xxxxxxx ≥ 3 xxxxxxx, xx u látky může xxxxxxxx k bioakumulaci. X&xxxx;xxxxxxxxx xxxxxx xxxxxxxxxx otravy xx xxxxxxxx, zda xx xx fázi IIB xxxxxxx xxxxxx biokoncentračního xxxxxxx (XXX).
3.4.2.2&xxxx;&xxxx;&xxxx;Xxxx&xxxx;XXX (xxxxxxxxxxx xxxxxxxxxxxxxxxx xxxxxx)
X&xxxx;xxxxxxxxxxx látek, x&xxxx;xxxxx xx posouzení xx fázi IIA nelze xxxxxxxx xxxxxx xxx xxxxxxx prostředí, xxxx xxxxx xxxxxxxxxxx xxxxxxxxx x&xxxx;xxxxxxxx na xxxxxxxxxx xxxxx x&xxxx;xxxx xxxxxx (xxxxxxxx) xxxxxxxxx xxxxxxxxx, x&xxxx;xxxxxxx studie ve xxxx&xxxx;XXX naznačily možné xxxxxxxx. X&xxxx;xxxxx xxxxxxx xx požadují xxxxx xxxxx, kterými xx xx xxxxxxxx xxxxxxxxxxxxx, xxxxxxxxxxx a živočišných xxxxxxx xxxx chronické x&xxxx;xxxxxxxxxxxxx xxxxxx. Xxxx xxxxxxxxx xxxxxxxxx umožní použití xxxxxxx xxxxxxxxxxxxxx xxxxxxx.
Xxxxxx xxxxxxxxx xxxxx xx xxxxxxxxxxx jsou popsány x&xxxx;xxxx xxxxxxxxx, např. x&xxxx;xxxxxxxx XXXX. Požaduje xx xxxxxxx xxxxx xxxxxx xxxxx, xxx xxxx xxxxxxxxx, že xxxx xxxxxx xxx xxxxxxx, v níž xxxx xxx xxxxxxxxx xxxxx x/xxxx xxxx metabolity xxxxxxxx x&xxxx;xxxxxxxxxx xx xxxxxxxxx. Zpřesnění posouzení xxxxxx xx xxxx (XXXXxxxx) by xxxxx xxx založeno na xxxxxxxx xxxxxxxxxxx xxxxxx xx dešťovky, xxxxxxxxxxx xxxxxxxx vlivu xx xxxxx mikroflóru x&xxxx;xxxx xxxxxxxxxx xxxxxxxxxxx druhů, xxxxxxxx zaměřených xx xxxxxxxxxx xxxxxxxxx na xxxxxxxxxx (xxxxxx hmyzu) x&xxxx;xxxxx xxxxxx ptáky.
Zpřesnění xxxxxxxxx xxxxxx xxx xxxx/xxxxxxxx může být xxxxxxxx na xxxxxxx xxxxxxxxx toxicity x&xxxx;xxxxxxxxxxxxxxx xxxxxxx/xxxxxxxxxx xxxxxxxxx xxxxxxxx xxx xxxxxxxxxx xx xxxx&xxxx;XXX.
X&xxxx;xxxxxxx potřeby xx xxxxxxxx xxxxxx xxxxxxxxxxxx xxxxx xxxxxx OECD 305.
4.&xxxx;&xxxx;&xxxx;XXXXX&xxxx;XX: XXXXXX TÝKAJÍCÍ XX XXXXXXXXX XXXXXXXXX XXXXX
Xxxxxx xxxx xxxxxxxx xxxxxxxx x&xxxx;xxxxxxx navrhovaného xxxxx x&xxxx;xxxxxxxx xxxxxxxxxxxx xxxxx z vlastností stanovených x&xxxx;xx.&xxxx;5 xxxx.&xxxx;3 xxxxxxxx (XX) x.&xxxx;1831/2003, podle xxxxxxxxx x&xxxx;xxxxxxxxx skupin xxxxxxxxxxx xxxxx xxxxxxxxxxx x&xxxx;xxxxxx&xxxx;6 x&xxxx;xxxxxxx&xxxx;X&xxxx;xxxxxxxxx xxxxxxxx. Xxxx xxxxxx xxxx xxxxxx umožnit xxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxx xxxxx xxxxx zemědělské xxxxx x&xxxx;XX.
Xxxxxxx xxxxxxxxxxxxxx xxxxxx xxxx být xxxxxxxxxx xxxxx užití xxxxxxxxx látky, xxxxx x&xxxx;xxxxxxxxx xxxxxx. Xxxxx xx xxxxxxxxx zvířata, xxxxxx xxxx být xxxxxxxxx xxx, aby xxxxxx xxxxxx a podmínky xxxxx xxxxxxxxxx neovlivnily xxxxxx xxxxxxxx. X&xxxx;xxxxxxx xxxxxx xx xxxxx xxxxxx příznivé x&xxxx;xxxxxxxxxx xxxxxx, x&xxxx;xx xxx x&xxxx;xxxxxx xxxxxxxxxxxxx, xxx x&xxxx;xxxxxxxxxx. Xx xxxxx xxxxxxxx rovněž xxxxxxxxxxx xxxxxx, xxxxx xxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxxxxxxxx xxxxxxxx. X&xxxx;xxxxxxxx xxxxxxx xxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxx uznaným, xxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxxxxxx xxxxxxx. Xxxxx xxxxxxxx xxxxxx xxxxxxxxxx, xx xxxxx xxxxxxxxx xxxxxx, xxxxx xxxxxxxxx, xx xxxxx xxxx xxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxxx, xxxxx xx xxxxxxxxx jmenovanému xxxxxxxxx studie, xx xxxxxxx xxxxxxxx xxxxxxxx x&xxxx;xxxxxxxx.
Xxxxxxxx xxxxxxxx xxxx xxxxxxx xxxxxxxxxx xxxxxxx xxxxxx s ohledem xx xxxxxx xxxxxxx údaje, xxxx. metody, xxxxxxx xxxxxxxxx x&xxxx;xxxxxxxx, údaje x&xxxx;xxxxx, plemeni xxxx xxxxx zvířat, xxxxxx xxxxx x&xxxx;xxxxxxxxxx, xx xxxxx xxxx ustájena x&xxxx;xxxxxx. U všech xxxxxx xxxxxxxxxxxx xxxxxxx je xxxxx xxxxxx zkušební xxxxxxxx podle bodu 3.1.1.3. Xxxxxxxxx xxxxxx, prvotní xxxx, xxxxx studie x&xxxx;xxxxxx charakterizované x&xxxx;xxxxxxxxxxxxxx xxxxxxxxx látky xxxx xxxxxxxxxxx pro budoucí xxxxxxx.
Xxxxxx musí xxx xxxxxxxx xxx, xxx xxxxxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxxx xxxxx doplňkové xxxxx xxxxxxxxx xx xx xxxxxxx xxxxxxxxx x&xxxx;xxxxxxxxx x&xxxx;xxxxxxxxx x&xxxx;xxxxxxxxx x&xxxx;xxxxxxxxx xxxxxxxxx xxxxxxxx. Xxxx studie zahrnují xxxxxx nejvyšší doporučenou xxxxx, xxxxxxx se xxxxxxxx. Xxxxxxxxxxxx se xxxxx zvláštní xxxxxx, xxxxxx xxxx uvážení xx xxxxxxxxx xxx xxxxxxx xxxxx xx xxxxxx x&xxxx;xxxxxxxxx xxxxxx.
Xxxxxxxxx xx nutno xxxxxxx xxxxxx xxxxxx xxxx xxxxxxxxxxxx xxxxxxxxxxx xxxx xxxxxxxxx interakcím xxxx xxxxxxxxxx xxxxxx, xxxxxx xxxxxxxxxxx xxxxxxx x/xxxx xxxxxxxxxxxxx xxxxxx x/xxxx xxxxxxxx xxxxx xxxxx, xxxxx xx xx xxxxxxxx xxx xxxxxxxx xxxxxxx doplňkové xxxxx (xxxxxxxxx snášenlivost xxxxxxxxxxx xxxxxxxxx látky x&xxxx;xxxxxxxxxxxxxxx x&xxxx;xxxxxxxxxxxxxxxx xxxx organickou xxxxxxxxx).
4.1&xxxx;&xxxx;&xxxx;Xxxxxx xx xxxxx
X&xxxx;xxxxx xxxxxxxxxxxxxxx x&xxxx;xxxxxxxxx senzorických xxxxxxxxxxx xxxxx, které xxxxxxxxx xxxxxxxxxx xxxxxx, xx nutno účinnost xxxxxxxx xxxxxx laboratorní xxxxxx. Studie musí xxx xxxxxxxx tak, xxx xxxxxxxxxx xxxxxxxxxxxxxxx xxxxxx xxxxxxxxx, x&xxxx;xxxxx xx doplňková xxxxx xxxx xxxxxxxxx. Výsledky xx xxxxxxxxx xxxxx xxxxx xxxxx xxx xxxxxxxxx x&xxxx;xxxx xxxxxxxx xxxxxxxxx xxxxx x&xxxx;xxxxxxxxxxxxxxxx X&xxxx;≤ 0,05.
X&xxxx;xxxxxxxxx druhů xxxxxxxxxxx xxxxx xx xxxxx xxxxxx k doložení xxxxxxxxx xxxxxx xx xxxxx, xxxxxxx xxxxxx, xxxxx xxxxxxxx aspekty xxxxxxxxxxxxxxxxxxxx xxxxxx. Tyto xxxxxx xx xxxx xxxxxxx statistické xxxxxxxxxxx.
4.2&xxxx;&xxxx;&xxxx;Xxxxxxxxxx xxxxxx xxxxxxxxx xx xxxxxxx
Xx xxxxx xxxxxx xxxxxx xxxxxxxxxx dostupnosti x&xxxx;xxxxxxxxx, xxxxxxx xxxx xxxxx nebo zdroj xxxxxx xxxx xxxxxxx xxxx xxx xxxxxxxx xx xxxxxxxxxxx xxxxxxxxxx xxxxx, xxxxx xxx xxxx xxxxxxxxx xxxx xxxxxxxx.
Xxxxxx xxxxxxxx stravitelnosti xxx použít xx xxxxxxx xxxxxx účinnosti x&xxxx;xxxxxx x&xxxx;xxxxxxxx xxxxxxxxxx xxxxxxxx. X&xxxx;xxxxxxxxx xxxxxxxxx, xxxxxxx ve vztahu x&xxxx;xxxxxxxx pro životní xxxxxxxxx, xx xxxxx xxxxxxxx prokázat xxxx xxxxxxxxxx xxxxxxxx x&xxxx;xx xxxxx xxx xxxxxxx xxxxxxxxxx před xxxxxxxxxxxx xxxxxxxx xxxxxxxxx. Xxx xxxxxx xxxxxxxx xx xxxxxxx xxxxx a druhy/kategorie xxxxxx xxxxxxxxxxxx navrhovaným xxxxxxxxx pro užití.
Popřípadě xx možno xxxxxxxxx xxxx krátkodobé xxxxxx xxxxxxxxx u zvířat x&xxxx;xx xxxxx nahradit xxxxxxxxxx xxxxxx účinnosti x&xxxx;xxxxxx, xx-xx xx plně xxxxxxxxxx.
4.3&xxxx;&xxxx;&xxxx;Xxxxxxxxxx xxxxxx xxxxxxxxx x&xxxx;xxxxxx
Xxxxxxx xx xxxx xxx prováděny nejméně xx xxxx různých xxxxxxx.
Xxxxxxx xxxxxxxxxxxxxx xxxxxx xxxx xxxxxxxxx xxxxx x&xxxx;xxxxxxxxxxxx xxxxxxxxxxx xxxxxxxxxxx x&xxxx;xxxxxx xxxx&xxxx;1 x&xxxx;2. Xxxxxxxx xxxx xxx xxxxxxxxxx xxxxxxx, xxx xxxxxxx xxxxxx doplňkové xxxxx xxx nejnižší xxxxxxxxxx xxxxx (riziko xxxx 1-α, P ≤ 0,05 xxxxxx x&xxxx;X&xxxx;≤ 0,1 xxx přežvýkavce, menšinové xxxxx, xxxxxxx x&xxxx;xxxxxxxx xxxxx x&xxxx;xxxxxxx, která xxxxxx xxxxxx k produkci xxxxxxxx) x&xxxx;xxxxxxxxxxx statistickou xxxxxxxxxxx, aby xxxx xxxxxxxx, xx xxxxxxxxxxxxxx xxxxxxxx xxxxxxx cíl xxxxxx. Xxxxxx xxxx 2-β&xxxx;xxxx být xxxxx xxxx xxxxx 20&xxxx;% xxxxxx x&xxxx;25&xxxx;% u pokusů x&xxxx;xxxxxxxxxxx, xxxxxxxxxxx xxxxx, xxxxxxx v zájmovém xxxxx x&xxxx;xxxxxxx, xxxxx xxxxxx xxxxxx k produkci xxxxxxxx; xxxxxxxxxx (1-β) je xxxx xxxxx xxxx xxxxx 80&xxxx;% (75&xxxx;% x&xxxx;xxxxxxxxxxx, xxxxxxxxxxx xxxxx, xxxxxx x&xxxx;xxxxxxxx xxxxx x&xxxx;xxxxxx, xxxxx nejsou xxxxxx x&xxxx;xxxxxxxx xxxxxxxx).
Xxxxxx xx, xx xxxxxxxx x&xxxx;xxxxxx xxxxxxxxx doplňkových látek xx xxxxxxx xxxxxxxx xxxxxxxx xxxxxxxx, xx xxxxx lze dosáhnout xxxxxxxxxxx xxxxxxxx. Je xxxxx nutno xxxxxx xxxxxxx xxxxxxx xxxxxxxxxxx, xx-xx xxxxx dostupných xxxxxxx vyšší xxx xxx. Z tohoto xxxxxx xx xxx xxxxxxx xxxxxxx xxxx být xxxxxxx podobné vzory xxxxxxxxx, xxx pak xxxxx xxxxx xxx xxxxxxx x&xxxx;xxxxxxxx jejich xxxxxxxxxxxxx x&xxxx;xxxxxxxxxx (xxxxx xx xxxxx xxxxxxxx) xx xxxxxx xxxxxxxxxxxxx xxxxxxxxx s hodnotou X&xxxx;≤ 0,05.
4.4&xxxx;&xxxx;&xxxx;Xxxx trvání dlouhodobých xxxxxx účinnosti x&xxxx;xxxxxxxx xxxxxxx
Xxxx xxxxxx xxxxxxx xxxxxxxxx xxxxxxx xxxxxxxx xxxxxxx xxxx xxxxxxxxx.
Xxxxxx xxxxxxxxx se provádějí xxxxx xxxxxxxxxx xxxxx x&xxxx;Xxxxxxxx xxxx x&xxxx;xxxxxxxxx xxxx xxxxxx xx xxxxxxx x&xxxx;xxxxxxx&xxxx;XX.
Xxxxx xx xxxxxxxxx xxxxx používá xx specifickou x&xxxx;xxxxxx xxxx, xxx je xxxx xxxxxxxx xxxxxxxxx xxxxxx, xxxx xxx xxxxxxxx podle xxxxxxxxxxxx xxxxxxxx xxx užití. Xxxx xxxxxxxxxx xxxx xxxxx xxx kratší xxx 28 dní x&xxxx;xxxx xxxxxxxxx xxxxxxx xxxxxxxx xxxxxxxxx (např. x&xxxx;xxxxxxx x&xxxx;xxxxxxxxxx počet selat xxxxxxxxxx xxxx se xxxxxxxx na xxxx xxxxxxxx, nebo xxxxx x&xxxx;xxxxxxxx odstavených xxxxx xx zřetelem na xxxx xxxxxxx).
X&xxxx;xxxxxxxxx xxxxx xxxx xxxxxxxxx zvířat, xxx něž xxxxxx x&xxxx;xxxxxxx&xxxx;XX xxxxxxxxx xxxxxxxxx xxxx xxxxxx studií, xx xxxxx x&xxxx;xxxxx xxxxxx xxxxxxxx podle xxxxxxxxxxxx xxxxxxxx pro xxxxx.
4.5&xxxx;&xxxx;&xxxx;Xxxxxxxxx na účinnost xxx kategorie a funkční xxxxxxx xxxxxxxxxxx látek
Pro xxxxxxx xxxxxxxxx xxxxx, xxxxx xxxx xxx xxxxxx na xxxxxxx, xx požadují studie xx xxxx.
Xxx kategorie xxxxxxxxxxxxxx doplňkových xxxxx x&xxxx;xxxxxxxxxxxxxx x&xxxx;xxxxxxxxxxxxxxx musí xxx xxxxxxxx xxxxxxxxx xxxxxxx třemi xxxxxxxxxxxx xxxxxxxx xxxxxxxxx. X&xxxx;xxxxxxxxx xxxxxxxxxxxxxx doplňkových látek x&xxxx;xxxxxxxxx kategorií xxxxxxxxxxx xxxxx, xxxxx mají xxxxxx xx zvířata, xx xxxxx xxxxx xxxxxxxxxx studie účinnosti, xxxxx xxx xxxxxxxx xxxxxxxxxxx xxxxxxxx.
Xxx xxxxxxx xxxxxxxxx xxxxxxxxxxx xxxxx xxx přímého účinku xx xxxxxxx xx xxxxxxxx xxxxxxx xxxxx xxxxxx xxxxxxxxx xx xxxxx.
4.6&xxxx;&xxxx;&xxxx;Xxxxxx týkající se xxxxxxx xxxxxxxxxxx xxxxxxxx, xxxxxxxx xx xxxx xxxxxxx xxxxxx
X&xxxx;xxxxx prokázat, xx xxxxxxxxx xxxxx xxxx xxxxxxxxxx xx xxxx xxxxxxxxx xxxxxx xx organoleptické x&xxxx;xxxxxxxx (xxxxxxxxx xxxxxxxxxx x&xxxx;xxxxxxxxxxxxx) xxxxxxxxxx xxxxxxxx získaných xx zvířat, xxx xxxx krmena xxxxxxxxxx xxxxxx (xxxxx xx xxxx žádoucí xxxxxx), xx během xxxxx xx xxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxxxxx xxxxxx. Xxxx pozorovány xxx xxxxxxx: xxxxxxx, xxx xxxxx není xxxxxxxx, x&xxxx;xxxxxxx x&xxxx;xxxxxxxxx xxxxxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxx. Xxxxx xxxx xxxxxxx xxxxxxxxxxx xxxxxxxxxxx. Xxxxxxxxx xxxxxx xxxxxx musí xxx přiměřeně xxxxxxxxxx.
5.&xxxx;&xxxx;&xxxx;XXXXX&xxxx;X:&xxxx;XXXX XXXXXXXXXXXX X&xxxx;XXXXXX XX XXXXXXX XXXXX NA XXX
Xxxxx xx.&xxxx;7 xxxx.&xxxx;3 xxxx.&xxxx;x)&xxxx;xxxxxxxx (XX) č. 1831/2003 xx nutno xxx xxxxxxx kategorie xxxxxxxxxxx xxxxx xxxxxxxxx xxxxx xxxxx monitorování v období xx uvedení xxxxx xx xxx x&xxxx;xxxxx xxxxxxxx a identifikovat xxxxxxxx xxxxx nebo nepřímé, xxxxxxxx, xxxxxxxx xxxx xxxxxxxxxxxx xxxxxx xxxxxxxxxxx x&xxxx;xxxxxxxxx xxxxxxxxx xxxxx xx zdraví xxxx xxxx xxxxxx xxxx xx xxxxxxx prostředí x&xxxx;xxxxxxx s vlastnostmi dotyčných xxxxxxxx.
Xxxxx xxxxx monitorování xxxx xxx podrobně xxxxxxxx xxxxx xxxxxxxxxxxx xxxxxxx x&xxxx;xxxx xxxxxxx, xxx (xxxx. xxxxxxx, xxxxxxxxx) xxxxxxxx jednotlivé xxxxx x&xxxx;xxxxx stanovené x&xxxx;xxx xxxxxxxx za xxxxxxxx x&xxxx;xxxxx provádění xxxxx, x&xxxx;xxxx stanovit xxxxxx xxxxxxxxxxx xxxxxxxxxxx xxxxxx o veškerých xxxxxx xxxxxxxxxxxxx, xxxxx souvisejí x&xxxx;xxxxxxxxxxx xxxxxxx xxxx xxxxxxxxx látky. Xxxxxx x&xxxx;xxxx xx xxxxx xxxxxxxxxx x&xxxx;xxxxxxxxxx zaznamenaných xxxxxxxxxxxx účincích, xxxx xxxx dotčena ustanovení x&xxxx;xxxxxxxxxxxx obsažená x&xxxx;xxxxxx&xxxx;12 xxxxxxxx (ES) x.&xxxx;1831/2003.
Xx-xx xxxxxx xxxxx xxxxxx xxxxxxx antibiotikem a bylo-li xxxxxxxxx, xx xxx xxxxx používání x&xxxx;xxxxxxxx, xx xxxxxx xx xxxxx x&xxxx;xxxxxx, xxxxxxx x&xxxx;xxxxxxx xxxxxxxxxxxxx xxxxxxxxxxxxx xxxxx, provedou xx xxxx xxxxxxx xxxxxxxxxxxx x&xxxx;xxxxxx xx uvedení xxxxx xx xxx xxxxxxx xxxxxx xx xxxxxxxxx xxxxxxxxxx xxxxxxxx xxxx xxxxxxxxx xxxxx.
X&xxxx;xxxxxxxxxxxxxx x&xxxx;xxxxxxxxxxxxxxx xx xxxxxxx xxxxxxx xxxxxxxxxxxx rezistence Xxxxxxx spp. x&xxxx;Xxxxxxxxxx xxxxxxxxxxx, xxxxx xxxxx xxxxx xxxxx xxxxx xxxx povolení.
(1) Úř. věst. X&xxxx;50, 20.2.2004, s. 44.
(2) Úř. věst. L 196, 16.8.1967, x.&xxxx;1. Xxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxx Xxxxxxxxxx parlamentu x&xxxx;Xxxx 2006/121/XX (Úř. věst. L 196, 16.8.1967, x.&xxxx;1; xxxxxxxx x&xxxx;Xx.&xxxx;xxxx. X&xxxx;196, 16.8.1967, x.&xxxx;1).
(3)&xxxx;&xxxx;Xx.&xxxx;xxxx. L 152, 30.4.2004, x.&xxxx;1.
(4)&xxxx;&xxxx;Xx.&xxxx;xxxx. X&xxxx;165, 30.4.2004, x.&xxxx;1.
(5)&xxxx;&xxxx;Xx.&xxxx;xxxx. X&xxxx;117, 8.5.1990, x.&xxxx;1. Směrnice xxxxxxxxx xxxxxxxxx xxxxxxxxxxx Xxxxxx 2005/174/XX (Xx.&xxxx;xxxx. L 117, 8.5.1990, s. 1)
(6) Úř. věst. X&xxxx;76, 22.3.1991, x.&xxxx;35. Xxxxxxxx xxxxxxxxx xxxxxxxxx směrnicí 2001/58/XX (Xx.&xxxx;xxxx. X&xxxx;76, 22.3.1991, x.&xxxx;35).
(7)&xxxx;&xxxx;Xx.&xxxx;xxxx. X&xxxx;262, 17.10.2000, s. 21.
(8) Úř. věst. L 224, 18.8.1990, x.&xxxx;1. Nařízení xxxxxxxxx xxxxxxxxx xxxxxxxxx Xxxxxx (ES) x.&xxxx;203/2008 (Xx.&xxxx;xxxx. X&xxxx;224, 18.8.1990, x.&xxxx;1).
(9)&xxxx;&xxxx;X.&xxxx;Xxxxxxxx xx xx.: Xxxxxxxxxx Xxxxxxxxxx Xxx Xxxxxx Xxxxxxxxxx Xxxxxxxxxx Xx Xxxxxxx Xx Xxxxxxxx (XXXXX Technical Xxxxxx) Pure Appl. Xxxx., xx.&xxxx;74, č. 5, x.&xxxx;835–855, 2002.
(10)&xxxx;&xxxx;Xx.&xxxx;xxxx. X&xxxx;221, 17.8.2002, s. 8. Xxxxxxxxxx xxxxxxxxx pozměněné xxxxxxxxxxx 2004/25/XX (Xx.&xxxx;xxxx. X&xxxx;221, 17.8.2002, x.&xxxx;8).
(11)&xxxx;&xxxx;Xxxxxxxxxxxxxxx seznam xx k dispozici xxxxxx: xxx.xxxx.xxxxxx.xx/xx/xxxxxxx/xxxxxx/xxxxxx_xxxxxxx/993.xxxx.
(12)&xxxx;&xxxx;Xxxxx x&xxxx;xxxx v přirozených xxxxxxxx.
(13)&xxxx;&xxxx;X&xxxx;xxxxxx 50 g tuku x&xxxx;xxxx x&xxxx;xxxxxxxxxxx xxxxxxxx.
(14)&xxxx;&xxxx;Xxx x&xxxx;xxxx x&xxxx;xxxxxxxxxxx poměrech.
(15) S přihlédnutím x&xxxx;xxxxxxxxxx xxxxxxxx lhůtě.
(16) V ideálním případě xxxxxxxxx xx xxxxxxx xxxxxxxx xxxx XXX.
(17)&xxxx;&xxxx;Xxxxxxxxx x&xxxx;xxxxxx XXX.
PŘÍLOHA III
ZVLÁŠTNÍ XXXXXXXXX, XXX XXXX SPLŇOVAT XXXXXXXXXXX XXXXXXXXX X&xxxx;XXXXXX&xxxx;3, XXXXX XXX X&xxxx;XXXXXXX XXXXXXXXX XXXXXXXXXXX XXXXX XXXX XXXXXXX XXXXXXXX XXXXXXX, XXX XX XXXXXXXXX X&xxxx;XX.&xxxx;7 XXXX.&xxxx;5 NAŘÍZENÍ (XX) Č. 1831/2003
Nařízení (XX) x.&xxxx;1831/2003 xxxxxxxxxxx doplňkovou xxxxx xxx vypracování xxxxxxxxxxx (xx-xx to xxxxx) xxx xxxxxx xxxxxxxxx doplňkových látek xxxx za xxxxx xxxxxxxxx xxxxxx xxxxx xx.&xxxx;7 xxxx.&xxxx;5 xxxxxxxx (XX) č. 1831/2003.
Seznam xxxxxxxxxx xxxxxxxxx xx xxxxxxxxxxx xxxxxxxxxxx xxx:
|
1. |
xxxxxxxxxxxxx doplňkové xxxxx |
|
2. |
xxxxxxxxxx xxxxxxxxx xxxxx |
|
3. |
xxxxxxxx xxxxxxxxx xxxxx |
|
4. |
xxxxxxxxxxxx xxxxxxxxx xxxxx |
|
5. |
xxxxxxxxxxxxxxx a histomonostatika |
|
6. |
extrapolaci x&xxxx;xxxxxxxxxxx xxxxx xx xxxxx xxxxxxxxx |
|
7. |
xxxxxxx x&xxxx;xxxxxxxx xxxxx x&xxxx;xxxx zvířata, xxxxx xxxxxx xxxxxx k produkci xxxxxxxx |
|
8. |
xxxxxxxxx xxxxx, xxxxx xxx xxxx xxxxxxxx xxx xxxxxxx v potravinách |
|
9. |
změnu xxxxxxxx |
|
10. |
xxxxxxxx xxxxxxxx |
|
11. |
xxxxxxxxxxxx xxxxxxxxx xxxxxxxxxxx xxxxx, které xxx xxxx povoleny xxxxx xxxxxxxx 70/524/XXX. |
Xxxxxxx xx xxxxx předložit xx základě xxxx xxx jednoho z výše xxxxxxxxx xxxxxxxxxx xxxxxxxxx.
Xxxxxx xxxxxxxx
Xxxxx-xx x&xxxx;xxxxxxxxxxx xxxxxxx x&xxxx;xxxxx xxxxxxxxxxxx v těchto xxxxxxxx, xx xxxxx xxxxx xxxxxx.
1.&xxxx;&xxxx;&xxxx;XXXXXXXXXXXXX XXXXXXXXX XXXXX
1.1&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;X:&xxxx;Xxxxxxx xxxxxxxxxxx
Xxxxxxx xx xxxx xxxxx&xxxx;X&xxxx;xxxxxxx&xxxx;XX.
1.2&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;XX: Xxxxxxxx, xxxxxxxxxxxxxxx x&xxxx;xxxxxxxx xxx xxxxx xxxxxxxxx xxxxx; xxxxxx xxxxxxx
Xxxxx&xxxx;XX xxxxxxx&xxxx;XX xx použije xxxxx:
|
— |
xxx xxxxxxxxx xxxxx, které xxxxxx xxxxxx xx xxxxxxxx povolení, xx xxxxxxx body 2.1.2, 2.1.3, 2.1.4, 2.1.4.2, 2.2, 2.3.1, 2.3.2, 2.4.1, 2.4.2, 2.4.4, 2.5, 2.6, |
|
— |
xxx xxxx doplňkové xxxxx, xxxxx xxxx xxxxxx na držitele xxxxxxxx, xx použije xxxx xxxxx&xxxx;XX. |
1.3&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;XXX: Xxxxxx xxxxxxxx se bezpečnosti xxxxxxxxxxx látek
Body 3.1, 3.2 x&xxxx;3.4 xxxxxxx&xxxx;XX xx xxxxxxxxxx xx xxxxxxxxx xxxxx x&xxxx;xxxxxxxxxx, pokud xxx xxxxxxxx, že:
|
— |
v hotovém xxxxxx xxxxxxxxxxxxx zjistitelná xxxxxxxx účinné látky (xxxxx) nebo xxxxxxxxxx xxxxxxxxxx nebo xxxxxxxx xxxxxxx (xxxxxxx) xxxx |
|
— |
xxxxxx xxxxx(x)&xxxx;x&xxxx;xxxxxxx(x)&xxxx;xx vyskytují jako xxxxx xxxxxx siláže x&xxxx;xxxxx doplňkových xxxxx xxxxxxxxx xxxxxxxx xxxxxx xxxxxxxxxxx x&xxxx;xxxxxxxxx xx xxxxxx připravenou bez xxxxx xxxxxxxxx xxxxx (xxxx. pokud xxxxxxxxxx xxxxx xxxxxxxxx xxxxx xxxxxxxx). |
X&xxxx;xxxxxxxxx případech se xxxxxxx xxxx xxxxx&xxxx;3 xxxxxxx&xxxx;XX.
1.3.1&xxxx;&xxxx;&xxxx;Xxxxxx týkající se xxxxxxxxxxx xxxxxxxxx doplňkové xxxxx xxx xxxxxx xxxxxxx
X&xxxx;xxxxxxxxxx&xxxx;(1) xxxxx: xxxxxxx xx xxxx xxx&xxxx;3.1 xxxxxxx&xxxx;XX.
1.3.1.1&xxxx;&xxxx;&xxxx;Xxxxxx tolerance u cílových xxxxx
Xxx doplňkové látky x&xxxx;xxxxxxxxxx:
|
— |
xxxxxxx xx xxxxx xx základní xxxxx xxxxx x&xxxx;xxxxxxxx xx xxxxxxxxx x&xxxx;xxxxxxxxx xxxxxxxxx xxxxxxxx xx xxxxxxx xxxxxx xxxxxx. Základní xxxxx xxxxx může xxxxxxxxx xxxxxx xxxxx xxxxxx xxxxxxxxxx bez xxxxxxx doplňkové látky; |
|
— |
dávka xxxxxxx xxx xxxxxx xxxxxxxxx je xxxxxxxx xxxxxxxxxxx xxxxxxxxxxx se x&xxxx;xxxxxx v době normálního xxxxxxxxx, pokud xx xxx xxxxxxxxxxx zjistit. Xxxxxxxx xxxxxxxxx xx xxxxxx produktu, který xxxxxxxx životaschopné xxxxxxxxxxxxxx, x&xxxx;xxxxxxxxxx těchto xxxxxxxxx xxxxxx x&xxxx;xxxxxx xx xxxxx xxxxxxxxxx. |
Xxxxxx xxxxxxxxx xxx xxxxxxx xxxxxx xx druhy xxxxxxxxxxx, xxxxxxxxx xxxxxxx. Studie xxxxxxxxxx xxxx xxxxx xxxx xxxxx pouze x&xxxx;xxxxxxx, je-li xxxxx xxxxxxxx ke xxx xxxxxx vhodnější x&xxxx;xxxxxxx xxx xxxx druhy xxx xxxxxxxxxxx.
Xxxxxxx xxxxx:
X&xxxx;xxxxxxxxx xxxxx, pro xxx xx xxxxxxxx xxxxxxxx xxxx xxxxxxxxxxxxx xxxxxxxxx xxxxx a které nebyly xxxxxxxx xxx použití xxxx krmivo, je xxxxx xxxxxxxx, že xxx xxxxxxx xxxxxx xxxxxxxx xxx xxxxxxxxx xxxxxxxxxxx xxxxxx. Xxxx xxxxxxxxx xxxx xxx xxxxxxx xx xxxxx xxxxx u jednoho z nejcitlivějších xxxxxxxx druhů xxxx x&xxxx;xxxxxxx druhu xxxxxxxxxxxxx xxxxxx.
1.3.1.2&xxxx;&xxxx;&xxxx;Xxxxxxxxxxx xxxxx
Xxxxxxx xx xxxx bod 3.1.2 xxxxxxx&xxxx;XX.
1.3.2&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxx se bezpečnosti xxxxxxxxx xxxxxxxxx xxxxx xxx xxxxxxxxxxxx
|
1.3.2.1 |
Xxxxxx xxxxxxxxxxx x&xxxx;xxxxxxx Xxxxxx xxxxxxxxxxx a reziduí xx xxxxxxxxxx, pokud:
Xxxxxx metabolismu xx xxxxxxxxxx xxxxxx x&xxxx;xxxxxxx, xxxxx xx xxxxx xxxxxxxxx v potravinách xxxx krmivech xxxxxxxxx xx xxxxxxx množství xxxx je běžnou xxxxxxx tělních tekutin xxxx xxxxx. V těchto xxxxxxxxx xx však xxxxxxxx studie reziduí, xxxxx mohou xxx xxxxxxx na srovnání xxxxxx x&xxxx;xxxxxxx/xxxxxxxxxx x&xxxx;xxxxxxxxxx xxxxxxx x&xxxx;xx skupině, xxx byla xxxxxxxx xxxxxxxx doporučená xxxxx. |
|
1.3.2.2 |
Xxxxxxxxxxxxx xxxxxx Xxxxxxxxxxxxx studie xx xxxxxxxxxx, pokud:
Xxx xxxxxxxxxxxxxx a enzymy, xxxxx xxxxxx vyňaty výše, xx xxxxxxxx studie xxxxxxxxxxxx (včetně xxxxxxxxxx) x&xxxx;xxxxxx xxxxxxxxxxxx orální xxxxxxxx. Xxxxxx xxxxxxxxxxxx xx nesmí provádět xx xxxxxxxxxxx xxxxxx xxxxx. Xxx cizorodé xxxxx, xxx nejsou xxxxxx xxxx, xx xxxxxxx xxxx xxx&xxxx;3.2.2 xxxxxxx&xxxx;XX. Xxx xxxxxxx xxxxx xx xxxxxxxxx xxxxxxxxxxxx xxxxx xxxxxxxxxxxx xxxxxxx x&xxxx;xxxxxxxxxxxx x&xxxx;xxxxxx a způsobu xxxxxxxx. |
|
1.3.2.3 |
Xxxxxxxxx xxxxxxxxxxx xxx spotřebitele Pro xxxxxxxxx xxxxx xxxxxxxxxx xxx xxxxxxx, xxxxx xxxx xxxxxx k produkci xxxxxxxx, se xxxxxxx xxxx bod 3.2.3 xxxxxxx&xxxx;XX. |
1.3.3&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxx se xxxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxx xxx uživatele/pracovníky
Použije se xxxx xxx&xxxx;3.3 xxxxxxx&xxxx;XX. Xxxxxxxxx xxxxx xxxxxxxxxx xxxxxx a mikroorganismy xx xxxxxxxx za xxxxxxxxxxxxxxx xxxxxxxxx xxxxxxx, xxxxx xxxxxx xxxxxxxxxx xxxxxxxxxxx xxxxxx prokazující xxxx.
1.3.4&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxx xx xxxxxxxxxxx xxxxxxxxx xxxxxxxxx látky xxx xxxxxxx prostředí
Použije xx xxxx bod 3.4 xxxxxxx&xxxx;XX. X&xxxx;xxxxxxxxxxx xxxxx x&xxxx;xxxxxxxxxx xx xxxxxxx xxxxxx doplňkové xxxxx xx tvorbu silážních xxxx xx xxxxxxxxx xxx xxxx sil xxxxx xxxxxxxxxx.
1.4&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;XX: Xxxxxx xxxxxxxx xx xxxxxxxxx xxxxxxxxx látky
Technologické xxxxxxxxx xxxxx xxxx zlepšit xxxx xxxxxxxxxxxx xxxxxxxxxx xxxxx, xxxxxxx však xxxxxx žádný xxxxx xxxxxxxxxx xxxxxx xx xxxxxxxxxx xxxxxx. Důkazy x&xxxx;xxxxxxxxx doplňkové xxxxx xxxx xxx xxxxxxxxxx xxxxxx xxxxxxxx xxxxxxxx xxxxxxxxxxxx x&xxxx;xxxxxxxx xxxxxxxxxxx xxxxxxxx xx určených xxxxxxxxxxx xxxxxxxx xxx xxxxx v porovnání x&xxxx;xxxxxxxxxxxxx xxxxxxxxxx xxxxxxx.
Xxxxxxxx xx xxxxxxx xxxxxxxx xx xxxxx x&xxxx;xxxxxxxx xxxxx xxx xxxxxxxx xxxxxxxxxxx xxxxxxxxxxxx. V následující tabulce xxxx xxxxxxx xxxxxx xxxxxxxxx xxx xxxxx xxxxxxx xxxxxxx.
Xxxxxxxxx xxx xxxxxxxxxx xxxxxxxxxxxxx doplňkové xxxxx
|
Xxxxxxx xxxxxxx |
Xxxxxxxxx xxx xxxxxxxxx účinnosti |
||||||||||
|
Inhibice mikrobiálního xxxxx, xxxxxxx xxxxxxxxxx xxxxxxxxx x&xxxx;xxxxxxxxx xxxxxxxxxxxxxx xx xxxxxxxxxxxx. Xx xxxxx xxxxxxxx udávanou xxxx xxxxxx xxxxxxxxxxxxx xxxxxx. |
||||||||||
|
Xxxxxxx xxxx xxxxxxxxxxxxx xxxxxxxxxx xxxxxxx xxxxxxxx xxxxx/xxxxxx během zpracování x/xxxx xxxxxxxxxx xxxxxx. Xx xxxxx xxxxxxxx xxxxxxxx dobu xxxxxx xxxxxxxxxx xxxxxx. |
||||||||||
|
Xxxxx/xxxxxxxx xxxxxxxxxx xxxxxx jinak xxxxxxxxxxxxxx xxxx xxxxxx smísitelných xxxxxx xxxxxx. |
||||||||||
|
Xxxxxxxxx xxxxxxxxx-xxxxxxxxxx xxxxx krmiv. |
||||||||||
|
Viskozita xxxxxxx xxxxxxxxx xxxx xxxxx. |
||||||||||
|
Tvoření xxxx xxxxxxx xx změně xxxxxxxxx xxxxxx. |
||||||||||
|
Xxxxxxxxxxx pelet xxxx xxxxxxxxx při xxxxxxxxx xxxxx. |
||||||||||
|
Důkaz x&xxxx;xxxxxxx xxxxxxxxxxx potravin xxxxxxxxxxx xxxxxx. |
||||||||||
|
Xxxxxxxxx xxxxxxxx spékání. Je xxxxx xxxxxxxx xxxxxxxx xxxx trvání xxxxxxxxxxxxxx xxxxxx. |
||||||||||
|
pH a/nebo xxxxxxxxx xxxxxxxx krmiv. |
||||||||||
|
|
||||||||||
|
Xxxxxxxxxxxxxxx xxxxxxxxxxxx xxxxxxx xxxxxxxxx. |
Xxxxxxxxx xxxxx x&xxxx;xxxxxxxxxx
Xxxxxxxx xx xxxxxxxx zkoušky x&xxxx;xxxxx xxxxxxxx xxxxxxxxxx xxxxxx xx xxxxxxx xxxxxx&xxxx;(2). Zkoušky xx xxxxxxxx s jedním příkladem x&xxxx;xxxxx z níže uvedených xxxxxxxxx (pokud xxxx xxxxxxxx všechna xxxx xxxxxxxxxxxxxxx xxxxxx):
|
— |
xxxxxx, xxxxx xxx xxxxxx xxxxxxxxx: &xx;3&xxxx;% xxxxxxxxxxx uhlohydrátů x&xxxx;xxxxxxxx materiálu (např. xxxx xxxxxxxx xxxxxxxx, xxxxx, sveřep xxxx xxxxx xxxxx), |
|
— |
xxxxxx, xxxxx xxx xxxxxxxxx x&xxxx;xxxxxxx xxxxxxxx: 1,5–3,0&xxxx;% rozpustných xxxxxxxxxxx x&xxxx;xxxxxxxx xxxxxxxxx (xxxx. xxxxxxx, xxxxxxxx xxxx xxxxxxx vojtěška), |
|
— |
krmiva, xxxxx xxx xxxxxxxxx xxxxxxx: < 1,5 % rozpustných xxxxxxxxxxx x&xxxx;xxxxxxxx xxxxxxxxx (xxxx. srha xxxx xxxxxxxxx). |
Xxxx-xx xxxxxxx xxxxxxx xx xxxxx kategorie xxxxx xxxxxxx na xxxxxxx xxxxxx, xxxxx xx výslovně xxxxxxx xxxxxx. Xxxx se xxxxxxxx tři xxxxxxx x&xxxx;xxxxxxxxxx reprezentativním xxx xxxx rozmezí, pokud xxxxx xx xxxxxxx xxxxxxxx xxxxxxx botanického xxxxxx.
Xxx xxxxxxxx krmiva xx xxxxxxxx xxxxxxxxxx xxxxxxx.
Xxxx trvání studie xx xxxxxxx 90&xxxx;xxx xxxx déle xxx xxxxx xxxxxxx (doporučený xxxxxx 15 – 25&xxxx;xX). Xxxxxxx xxxxxx xxxx trvání xxxx xxx xxxxxxxxxx.
Xxxxxxx xx xxxxxx xxxxxxxx xxxxxx xxxx uvedených parametrů x&xxxx;xxxxxxxxx x&xxxx;xxxxxxxxx kontrolní xxxxxxxx:
|
— |
xxxxxx x&xxxx;xxxxxxxxx úbytky xxxxxx (xxxxxxxx s ohledem xx těkavé látky), |
|
— |
pokles xX, |
|
— |
xxxxxxxxxxx těkavých xxxxxxxx xxxxxxx (xxxx. xxxxxxxx xxxxxx, xxxxxxxx xxxxxxx x&xxxx;xxxxxxxx xxxxxxxxxx) x&xxxx;xxxxxxxx xxxxxx, |
|
— |
xxxxxxxxxxx xxxxxxxx (xxxxxxx), |
|
— |
xxxxxxxxxxx xxxxxx (g/kg xxxxxxxxx xxxxxx) x |
|
— |
xxxxx uhlohydrátů xxxxxxxxxxx xx vodě. |
Popřípadě xx xxxxxx jiné xxxxxxxxxxxxxxx x&xxxx;xxxxxxxx parametry x&xxxx;xxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxx (např. xxxxx xxxxxxxx schopných asimilovat xxxxxx, xxxxxxxx klostridií, xxxxxxxx xxxxxxxx x&xxxx;xxxxxxxxxx xxxxx).
Xxxxxxx účinek x&xxxx;xxxxxxxxxxx xx xxxxxxxx xxxxxxxx xxxxxxxxxxxx xxxxxxxxx xxxx xx posoudí na xxxxxxx xxxxxxxxx xxxxxx xxxxxxxxx šťáv xxxxxxxxxxx xx xxxx xxxxxxx xxxxxx s přihlédnutím x&xxxx;xxxxxxxxxxxxxxx xxxxxx na životní xxxxxxxxx (xxxx. xxxxxxxxxxx xxxxxxxxx šťáv xxxx xxxxxxxxxx xxxxxxx xxxxxxx). Xxxxxxx xxxxxx xxxxxxxxx xxxx je xxxxx xxxxxxxx xxxxx. Kapacita xxxxxxx xxxx musí xxx xxxxxxxxxx, aby xxxxx xxxxxxx šťávy xxxxxxx xx xxxxxx xxxxx. Doba xxxxxx xxxxxx xx xxxxxxx 50&xxxx;xxx. Pokud se xxxxxxx jiná doba, xx xxxxx to xxxxxxxxx.
Xxxxx aerobní stabilita xxxx xxx xxxxxxxxx x&xxxx;xxxxxxxxx s negativní xxxxxxxxx xxxxxxxx. Xxxxxx stability xxxx xxxxx xxxxxxx xxxx dnů xx xxxxxxxx vzduchu x&xxxx;xxxxxxxxx xxxxx dokládá stabilitu xx xxxx nejméně x&xxxx;xxx xxx xxxxx, xxx xx prokázáno x&xxxx;xxxxxxxxxxxx kontrolního xxxxxx. Xxxxxxxxxx se, xxx xx pokus xxxxxxxx xxx xxxxxxx okolí 20&xxxx;xX x&xxxx;xxx se xxxxxxx xxxxxxx x&xxxx;3&xxxx;xX xxxx xxxx xxxxxx xxxxxxx xxxxx xxxxxxxxxx xx xxxxxx xxxxxxxxxxx. Xxxxxx xxxxxxx xx xxxxx xxxxxxxx xxxxxxx xxxxxxxx XX2.
1.5&xxxx;&xxxx;&xxxx;Xxxxx X:&xxxx;Xxxx xxxxxxxxxxxx x&xxxx;xxxxxx po xxxxxxx látky xx xxx
Xxxxx xxxxx se xxxxxxx xxxxx ustanovení xx.&xxxx;7 odst. 3 xxxx.&xxxx;x)&xxxx;xxxxxxxx (XX) č. 1831/2003. Xx xxxxxxx, že se xxxx xxxxxxxxxxxx x&xxxx;xxxxxx xx xxxxxxx látky xx trh xxxxxxxx xxxxx xxx xxxxxxxxx xxxxx, které xxxx xxxxxxxxx xxxxxxxxxxxx xxxxxxxxx xxxx xxxx x&xxxx;xxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxx xxxxxxxx.
2.&xxxx;&xxxx;&xxxx;XXXXXXXXXX XXXXXXXXX XXXXX
2.1&xxxx;&xxxx;&xxxx;Xxxxxxx
2.1.1&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;X:&xxxx;Xxxxxxx xxxxxxxxxxx
Xxxxxxx xx xxxx xxxxx&xxxx;X&xxxx;xxxxxxx&xxxx;XX.
2.1.2&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;XX: Xxxxxxxx, xxxxxxxxxxxxxxx x&xxxx;xxxxxxxx xxx xxxxx doplňkové xxxxx; xxxxxx xxxxxxx
Xxxxx&xxxx;XX xxxxxxx&xxxx;XX xx xxxxxxx xxxxx:
|
— |
xxx xxxxxxxxx xxxxx, xxxxx xxxxxx xxxxxx xx držitele xxxxxxxx, xx xxxxxxx xxxx&xxxx;2.1.2, 2.1.3, 2.1.4, 2.1.4.2, 2.2, 2.3.1, 2.3.2, 2.4.1, 2.4.2, 2.4.4, 2.5, 2.6, |
|
— |
xxx jiné xxxxxxxxx xxxxx, xxxxx xxxx xxxxxx xx xxxxxxxx povolení, se xxxxxxx celý xxxxx&xxxx;XX. |
2.1.3&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;XXX: Xxxxxx týkající se xxxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxx
Xxx&xxxx;3.3 xxxxxxx&xxxx;XX xx xxxxxxxx xxxx xx xxxxxxx xxxxxxxxx xxxxx.
|
1. |
Xx xxxxx, xxxxx xxx xxxxxxx v krmivu, xxxxxx xxxxx potravinám xxxxxxxxxxx xxxxxx, xx xxxxxxxx xxxx xxxxx&xxxx;XXX xxxx&xxxx;3.1, 3.2 x&xxxx;3.4 přílohy II. |
|
2. |
U látek, xxxxx xxxxxx xxxx xxxxxxxxx xxxxxxx xxxxx, xx xxxxxx týkající xx oddílu III xxxx&xxxx;3.1 xxxxxxxx na xxxxxxxxx, xxxxxx byla doplňková xxxxx podávána v doporučované xxxxx. Xx xxxxx xxxxxxxxxx důkaz rovněž xxxxxxx xx existující xxxxxxxx xxxxxxxxxx. Xxxxxxx xx xxxxx&xxxx;XXX body 3.2 x&xxxx;3.4 xxxxxxx&xxxx;XX. |
|
3. |
X&xxxx;xxxxx, xxxxx xxxx pozitivní xxxx xx zbarvení xxxxxxxxx xxx nebo ptáků, xx požadují studie xxxxxxxx xx xxxxxx&xxxx;XXX xxxx&xxxx;3.1 xxxxxxx&xxxx;XX a tyto xxxxxx xxxx xxx xxxxxxxxx xx xxxxxxxxx, xxxx xxxx xxxxxxxxx xxxxx xxxxxxxx x&xxxx;xxxxxxxxxx xxxxx. Xx xxxxx xxxxxxxxxx xxxxx xxxxxx xxxxxxx xx existující xxxxxxxx xxxxxxxxxx. Nepožadují xx xxxx body 3.2 x&xxxx;3.4. |
2.1.4&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;XX: Xxxxxx týkající xx xxxxxxxxx xxxxxxxxx xxxxx
Xxxxxxx se xxxx xxxxx&xxxx;XX xxxxxxx&xxxx;XX.
|
x) |
Xxx xxxxx, xxxxx xxx xxxxxxx x&xxxx;xxxxxx xxxxxx xxxxx xxxxxxxxxx živočišného xxxxxx: xxxxx xxxxx xxxxxxxx získaných xx xxxxxx, xxxxxx xxxx doplňková xxxxx xxxxxxxx xx doporučených xxxxxxxx xxx xxxxx, xx xxxx xxxxxx xxxxxx xxxxxxxx. Xx xxxxx prokázat, že xxxxxxxxx xxxxxxxxx látky xxxx xxxxxxxxxx vliv xx xxxxxxxxx produktu xxxx organoleptické a nutriční xxxxxxxxxx xxxxxxxx. Jsou-li xxxxxx xxxxxxxxx látky xx složení/vlastnosti xxxxxxxxxxx xxxxxxxx xxxxx zdokumentovány, xxx mohou odpovídající xxxxx x&xxxx;xxxxxxxxx poskytnout xxxxxxx studie (xxxx. xxxxxx xxxxxxxxxx dostupnosti). |
|
b) |
Pro xxxxx, které xxxxxx xxxx xxxxxxxxx krmivům xxxxx: xxxxx x&xxxx;xxxxxxxxx xx xxxxx xxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxxxxxxxxx laboratorních xxxxxx xxxxxxxxxxxxxx k určeným xxxxxxxxx xxx užití v porovnání x&xxxx;xxxxxxxxxxx xxxxxx. |
|
x) |
Xxx xxxxx, xxxxx xxxx pozitivní xxxx xx xxxxxxxx xxxxxxxxx xxx xxxx xxxxx: xxxxxx prokazující xxxxxx (xxxxxx) xx provedou xx xxxxxxxxx, xxxxxx xxxx xxxxxxxxx látka xxxxxxxx v doporučené výši. Xxxxx barvy se xxxx pomocí xxxxxx xxxxxxxx. Xxxxx o účinnosti xx xxxxx xxxxxxxxxx xxxxxx xxxxxx xxxxxxxxxxxxxxxx xxxxxxxx (xxxx. xxxxxxxxxx xxxxxxxxxx) xxxx xxxxxxx xx vědeckou xxxxxxxxxx. |
2.1.5&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;X:&xxxx;Xxxx xxxxxxxxxxxx x&xxxx;xxxxxx po xxxxxxx xxxxx xx xxx
Xxxxx xxxxx xx xxxxxxx xxxxx xxxxxxxxxx xx.&xxxx;7 xxxx.&xxxx;3 písm. g) nařízení (XX) č. 1831/2003. Xx xxxxxxx, xx xx xxxx monitorování x&xxxx;xxxxxx xx xxxxxxx xxxxx xx xxx xxxxxxxx xxxxx pro xxxxxxxxx xxxxx, xxxxx xxxx xxxxxxxxx modifikované xxxxxxxxx xxxx xxxx z geneticky xxxxxxxxxxxxxx xxxxxxxxx xxxxxxxx.
2.2&xxxx;&xxxx;&xxxx;Xxxxxxxxxxx xxxxx
2.2.1&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;X:&xxxx;Xxxxxxx xxxxxxxxxxx
Xxxxxxx xx xxxx oddíl I přílohy II.
2.2.2 Oddíl II: Xxxxxxxx, xxxxxxxxxxxxxxx a podmínky xxx xxxxx doplňkové látky; xxxxxx xxxxxxx
X&xxxx;xxxxxxx xxxxxxx „xxxxxxxx produkty“ xx xxxxxxx xxxx xxxxxxxx, xxxxxxx a jiné xxxxxxxxx x&xxxx;xxxxxx xxxxx xxxx xxxxxx produkty, které xxxx xxxxx xxxx xxxxxxxxxx, xxxx xxxx. xxxxxxx, mletím nebo xxxxxxx (např. mnoho xxxxx x&xxxx;xxxxxx), xxxxxxxxxx xx xxxxxxxx xxxxxxxxx xx xxxxxxx xxxxxxx xxxxxxxxxxxxx xxxxx x&xxxx;xxxxxxxxx xxxxxxxxxxxx xxxxxxxxxxx xxxxx.
Xxx xxxxx xxxxxxxxxxx žádostí xxxxxxxxxx xx xxxxxx xxxxxxxx jsou zchutňující xxxxx klasifikovány takto:
|
1. |
Přírodní xxxxxxxx:
|
|
2. |
Xxxxxxxx xxxx xxxxxxxxxxxx syntetické xxxxxxxx xxxxxxxxxx xxxxxxxxxxx látky |
|
3. |
Umělé xxxxx Xx xxxxx xxxxx xxxxxxxxxx xxxxxxx, xx xxx patří xxxxxxx, xxxxx se xxxxxx xxxx. X&xxxx;xxxxxxx xxxxxxxx, xxxxx xxxxxxx xx xxxxx x&xxxx;xxxx xxxxxxxxx xxxxxx, xx xxxx xxxxx uvést x&xxxx;xxxxxxxxx. |
|
2.2.2.1 |
Xxxxxxxxxxxxxxx xxxxxx xxxxx (xxxxx) / xxxxxxx (xxxxxxx) Xxxxxxx xx xxxx xxx&xxxx;2.2 xxxxxxx&xxxx;XX. Xxxxxx: Xxx xxxxxxx skupiny xxxxxxxxxxxxx xxxxx je xxxxx xxxxx xxxx xxxxxxxxx identifikační xxxxx (xxxxx) (xxxx. XXXXXX&xxxx;(3), Xxxx Xxxxxx&xxxx;(4), JECFA, XXX&xxxx;(5) xxxx xxxx xxxxxxxxxxx xxxxxxxxx xxxxxx xxxxxxxxx) xxxxxxxxx xxxxxxxxxx x&xxxx;xxxxxxxxxxxx zchutňujících xxxxxxxx x&xxxx;xxxxxxxx x&xxxx;xxxxxxxxxxx, xxxxx xx k dispozici.
|
|
2.2.2.2 |
Xxxxxx výroby Použije xx xxxx bod 2.3 xxxxxxx&xxxx;XX. X&xxxx;xxxxxxx xxxxxxxxxx produktů, které xxxxxx xxxxxxxx xxxxxx xxxxxxxxxx, xxxxxxx komplexní xxxxx xxxxx xxxxx xxxxxxx v procesu xxxxxxxx, xx nutno uvést xxxxxxxx popis procesu xxxxxxxx. Doporučuje se x&xxxx;xxxxxx použít odpovídající xxxxxxxxxxxx, např. xxxxxx, xxxxx, xxxxx, xxxxxxx x&xxxx;xxxxxxxxxxx xxxxx&xxxx;(7) xxxxx xxxxxxxxx xxx botanicky xxxxxxxxxx xxxxxxxxxxx xxxxxxxx x&xxxx;xxxxxx xxxxxxx extrakce. Xxxxxxx xx xxxxxxx xxxxxxxxx xxxxxxxxxxxx, xxxxxxx xxxxxxxxxxxx xxxxxxxx, xxx xx xxxxxxxx reziduím x&xxxx;xxxxxxxxxxxx, x&xxxx;xxxxxx reziduí, xxxxx jsou xxxxxxxxxxxxx xxxxxxxx, xxxxxxxx xxxxxx xxxxxxx nelze xxxxxxxx. Xxxxx použité k charakteristice xxxxxxxx mohou xxxxxxxxx xxxxx xx xxxxxx xxxxxxxx. |
|
2.2.2.3 |
Xxxxxx analýzy
Xxxx xxx&xxxx;2.6 přílohy II se xxxxxxxx na všechny xxxxxxx xxxxxxxxxxx látky, xxxxxxxxx přírodní extrakty, xxxxx obsahují xxxxxxxxxxxxx xxxxxxxx xxxxx, xxxxxxxx xxxx xxxxxxxxxxxx syntetické xxxxxxxx xxxxxxxxxx xxxxxxxxxxx xxxxx, jež xxxx xxxxxxxxxxxxx xxxxxxxxxx xxxxxxx, x&xxxx;xxxxx zchutňující látky. |
2.2.3 Oddíl III: Xxxxxx xxxxxxxx se xxxxxxxxxxx xxxxxxxxx xxxxx
Xxx xxxxxxx xxxxxxxxxxx látky xx xxxxx xxxxx xxxxxxxx zvířat x&xxxx;xxxxxxx xxxxxx xxx z přirozené xxxxxxxx, tak xx xxxxxxx xxxxxxxxxxx xxxxx xx krmiv.
Na xxxxxxxxxxx xxxxx xxxxxxx xx xxxxxxx xxxxxxx xxxxx xx xxxxxxxx celý xxxxx&xxxx;XXX xxxxxxx&xxxx;XX.
|
2.2.3.1 |
Xxxxxx xxxxxxxx xx xxxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxx xxx xxxxxx xxxxxxx
|
|
2.2.3.2 |
Xxxxxx xxxxxxxx xx xxxxxxxxxxx xxxxxxxxx doplňkové xxxxx xxx xxxxxxxxxxxx Xx xxxxx xxxxxxx, xx xxxxxxxxxx xxxxxxxxxxx xxxxx xxxxxxx x&xxxx;xxxxxxxxx toxikologicky xxxxxxxxxx xxxxxxxx xxx xxxxxxx xx zvířeti. X&xxxx;xxxxxxx, xx xxxxx požadovaného xxxxxxxxxxxxx xxxxxxxx v důsledku xxxx xxxxxxx xx xxxxx xxxx x&xxxx;xxxxxxxx x&xxxx;xxxxxxxxxxx živočišného původu, xx xxxxx xxxxxxxxxx xxxxxxxx výpočet expozice xxxxxxxxxxxx.
|
|
2.2.3.3 |
Xxxxxx xxxxxxxx xx xxxxxxxxxxx xxxxxxxxx doplňkové látky xxx xxxxxxxxx/xxxxxxxxxx Xxxxxxx se xxxx xxx&xxxx;3.3 přílohy II. |
|
2.2.3.4 |
Studie xxxxxxxx se bezpečnosti xxxxxxxxx xxxxxxxxx látky xxx xxxxxxx prostředí Použije xx xxxx bod 3.4 xxxxxxx&xxxx;XX. |
2.2.4&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;XX: Xxxxxx týkající xx účinnosti xxxxxxxxx xxxxx
Xx nutno xxxxxxxxx xxxxxx o vlastnostech xxxxxxxxxxxxx xxxxx, xxxxxxx xx xxxxxxx zveřejněné xxxxxxxxxx. Xx může xxx xxxxxxxxx xxxxxx xxxxxxxxxxx x&xxxx;xxxxxxxxxxx xxxxxxxxx, xxxx-xx x&xxxx;xxxxxxxxx, x&xxxx;xxxxxxx xxxxxxx xxxxx být xxxxxxxxxx xxxxxx xx xxxxxxxxx.
Xx xxxxx plně xxxxxxxx x&xxxx;xxxxx, zda xxxxxxx, xxxxxxx xx žádost xxxx, xxxx v krmivu, xxxxxxx nebo xxxxxxxxxxx xxxxxxxxxxx xxxxxx jiné xxxxxx xxxxx funkce x&xxxx;xxxxxxxx zchutňujících xxxxx x&xxxx;xxxxxxx&xxxx;X&xxxx;xxxxxxxx (XX) x.&xxxx;1831/2003.
2.2.5&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;X:&xxxx;Xxxx xxxxxxxxxxxx x&xxxx;xxxxxx xx xxxxxxx xxxxx xx xxx
Xxxxx xxxxx se xxxxxxx xxxxx ustanovení xx.&xxxx;7 xxxx.&xxxx;3 xxxx.&xxxx;x)&xxxx;xxxxxxxx (XX) x.&xxxx;1831/2003. Xx xxxxxxx, že xx xxxx xxxxxxxxxxxx v období xx uvedení xxxxx xx xxx xxxxxxxx xxxxx xxx xxxxxxxxx xxxxx, xxxxx xxxx xxxxxxxxx modifikované organismy xxxx jsou x&xxxx;xxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxx vyrobeny.
3. NUTRIČNÍ XXXXXXXXX XXXXX
3.1&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;X:&xxxx;Xxxxxxx xxxxxxxxxxx
Xxxxxxx xx xxxx xxxxx X&xxxx;xxxxxxx&xxxx;XX.
3.2&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;XX: Xxxxxxxx, charakteristika x&xxxx;xxxxxxxx pro xxxxx xxxxxxxxx látky; metody xxxxxxx
Xxxxx&xxxx;XX xxxxxxx&xxxx;XX se xxxxxxx takto:
|
— |
pro xxxxxxxxx xxxxx, xxxxx xxxxxx xxxxxx xx držitele xxxxxxxx, se xxxxxxx xxxx&xxxx;2.1.2, 2.1.3, 2.1.4, 2.1.4.2, 2.2, 2.3.1, 2.3.2, 2.4.1, 2.4.2, 2.4.4, 2.5, 2.6, |
|
— |
pro xxxx doplňkové látky, xxxxx jsou vázané xx xxxxxxxx xxxxxxxx, xx použije celý xxxxx&xxxx;XX. |
3.3&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;XXX: Xxxxxx xxxxxxxx xx xxxxxxxxxxx xxxxxxxxxxx xxxxx
3.3.1&xxxx;&xxxx;&xxxx;Xxxxxx týkající xx xxxxxxxxxxx používání doplňkové xxxxx pro xxxxxx xxxxx
|
3.3.1.1 |
Xxxxxxxxx x&xxxx;xxxxxxxx xxxxx
|
|
3.3.1.2 |
Xxxxxxxxxxx xxxxxx Xxxxxxx xx xxxx xxx&xxxx;3.1.2 přílohy II. |
3.3.2 Studie xxxxxxxx xx xxxxxxxxxxx xxxxxxx xxxxxxxxx xxxxx xxx xxxxxxxxxxxx
|
3.3.2.1 |
Xxxxxx metabolismu x&xxxx;xxxxxxx Xxxxxx xxxxxxxxxxx xx xxxxxxx xxxxxxxxxx. Xxx deriváty xxxxxxxx xx xxxxxxxxx xxxxxxxxxxxx x&xxxx;xxxxxxx. Xxxxxx xxxxxxx xxxx xxxxxxxx se xxxxxxxx pouze x&xxxx;xxxx xxxxxxxxxxx xxxxx, xxxxx xxxxxxx do xxxxxxx xxxxxxx „vitamíny, provitamíny x&xxxx;xxxxxxxx přesně definované xxxxx xx srovnatelným xxxxxxx“, xxxxx mají xxxxxxxxx k akumulaci x&xxxx;xxxx, x&xxxx;xxx xxxxxxx xxxxxxx xxxxxxxxx xxxxxxxxx xxxxx, xxxxx xx xxxxxxx xxxxxxxxxx dostupnost. V tomto xxxxxxx se xxxxxxxxx xxxxxx popsaný x&xxxx;xxxxxx&xxxx;3.2.1 xxxxxxx&xxxx;XX. Požadavek xx xxxxxx xx xxxxxxxx xxxxxx x&xxxx;xxxxxxx xxxx xxxxxxxxxx xxxx xxxxxxxx, xxx xxxx xxxxxxxx xxxxxxxx dávka xxxxxxx xxxxx, x&xxxx;xxxxxxxxx xxxxxxxxx xxxxxxxx (xxxxxxxxxx xxxxx). |
|
3.3.2.2 |
Xxxxxxxxxxxxx xxxxxx Xx xx xxxxxxxx xxx xxxxxxxx fermentačního xxxxxxx x&xxxx;xxx xxxxxxxxx xxxxx, které nebyly xxxxx xxxxxxxx. Xxx xxxxxxxx fermentačního xxxxxxx xx nutno xxxxxxxxx xxxxxx xxxxxxxxxxxx x&xxxx;xxxxxxxxxxxx xxxxxxxx, xxxxxx:
Xxxxx xxxxxxxxx organismus xxxxx xx skupiny, x&xxxx;xxx xx xxxxx, xx xxxxxxx kmeny xxxxxxxxx xxxxxx, xx nutno xxxxxxxx xxxxxxxx xxxxxx xxxxxxxxxx. |
|
3.3.2.3 |
Xxxxxxxxx bezpečnosti xxx xxxxxxxxxxxx Xxxxxxx se xxxx xxx&xxxx;3.2.3 xxxxxxx&xxxx;XX. |
3.3.3&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxx xx xxxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxx pro xxxxxxxxx/xxxxxxxxxx
Xxxxxxx xx celý xxx&xxxx;3.3 xxxxxxx&xxxx;XX.
3.3.4&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxx xx xxxxxxxxxxx xxxxxxxxx xxxxxxxxx látky xxx xxxxxxx prostředí
Celý bod 3.4 xxxxxxx&xxxx;XX xx použije xxx xxxx xxxxxx xxxxx, xxxxx patří xx xxxxxxx xxxxxxxxx xxxxxxxxx xxxxx.
3.4&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;XX: Studie xxxxxxxx se xxxxxxxxx xxxxxxxxx xxxxx
Xxxxxx účinnosti xx xxxxxxxxxx xxx xxxxxxxx, aminokyseliny, xxxx x&xxxx;xxxxxxx xxxxxxxxxxxx, xxxxx xxx xxxx xxxxxxxx xxxx xxxxxxxxx xxxxx, xxxxxxxxxx xxxxxxxxx xxxxx, xxxxx xxx xxxx xxxxxxxx jako xxxxxxxxx xxxxx, a vitamíny, xxxxxxxxxxx x&xxxx;xxxxxxxx xxxxxx xxxxxxxxxx xxxxx xx srovnatelným xxxxxxx, xxxxx již xxxx xxxxxxxx jako xxxxxxxxx xxxxx.
Xxxxxxxxxx xxxxxx xx xxxxxxxx x&xxxx;xxxxxxxx xxxxxxxxx xxx xxxxxxxx xxxxxxxx, xxxx x&xxxx;xxxxxxx xxxxxxxxxxxx, xxxxx xxxxx xxxxxx xxxxxxxx jako xxxxxxxxx xxxxx, xxxxxxxxxx xxxxxxxxx xxxxx, xxxxx xxxxx xxxxxx xxxxxxxx xxxx doplňkové látky, x&xxxx;xxx xxxxxxxx, xxxxxxxxxxx x&xxxx;xxxxxxxx xxxxxx xxxxxxxxxx xxxxx xx srovnatelným xxxxxxx, xxxxx xxxxx xxxxxx xxxxxxxx jako xxxxxxxxx xxxxx.
Xxx xxxxxxx xxxxx, x&xxxx;xxxxx se xxxxx xxxxxxxx xxxxxx, xx požaduje xxxxxxx xxxxx dlouhodobá xxxxxx xxxxxxxxx xxxxx ustanovení xxxxxx&xxxx;4 přílohy II.
Studie xxxx xxxxxxxx prokázat, xx xxxxxxxxx xxxxx xxxx xxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxx. Xxxxx zahrnují xxxxxxxx skupinu x&xxxx;xxxxxx xxxxxx, xxxxx xxxxxxxx xxxxxx x&xxxx;xxxxxxxxxxxxx xxxxxxx xxx nutriční xxxxxxxxx xxxxxx. Xx xxxx xxxxx zamezit xxxxxxxx x&xxxx;xxxxxxxx kontrolní skupiny xxxxxx xxxxxx deficitem. Xxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxx x&xxxx;xxxxxxx xxxxx xxxx xxxxxxxxx xxxxxx, xxxxxx xxxxxxxxxxxxx xxxxxx.
3.5&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;X:&xxxx;Xxxx xxxxxxxxxxxx x&xxxx;xxxxxx po xxxxxxx látky na xxx
Xxxxx xxxxx xx xxxxxxx xxxxx ustanovení xx.&xxxx;7 odst. 3 písm. g) nařízení (XX) č. 1831/2003.
4. ZOOTECHNICKÉ XXXXXXXXX XXXXX
4.1&xxxx;&xxxx;&xxxx;Xxxxxxxxxxxx doplňkové látky xxxx než xxxxxx x&xxxx;xxxxxxxxxxxxxx
4.1.1&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;X:&xxxx;Xxxxxxx dokumentace
Použije xx xxxx oddíl I přílohy II.
4.1.2 Oddíl II: Identita, xxxxxxxxxxxxxxx x&xxxx;xxxxxxxx xxx xxxxx xxxxxxxxx xxxxx; xxxxxx xxxxxxx
Xxxxxxx se xxxx xxxxx&xxxx;XX přílohy II.
4.1.3 Oddíl III: Xxxxxx týkající xx xxxxxxxxxxx xxxxxxxxxxx xxxxx
|
4.1.3.1 |
Xxxxxx xxxxxxxx xx xxxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxx xxx xxxxxx zvířata Použije xx celý xxx&xxxx;3.1 xxxxxxx&xxxx;XX. |
|
4.1.3.2 |
Xxxxxx týkající xx xxxxxxxxxxx používání xxxxxxxxx xxxxx xxx xxxxxxxxxxxx
|
|
4.1.3.3 |
Xxxxxx xxxxxxxx xx xxxxxxxxxxx doplňkové xxxxx xxx xxxxxxxxx/xxxxxxxxxx Xxxxxxx xx xxxx xxx&xxxx;3.3 xxxxxxx&xxxx;XX. |
|
4.1.3.4 |
Xxxxxx xxxxxxxx xx xxxxxxxxxxx xxxxxxxxx látky xxx xxxxxxx prostředí Použije xx xxxx xxx&xxxx;3.4 xxxxxxx&xxxx;XX. |
4.1.4&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;XX: Xxxxxx xxxxxxxx xx xxxxxxxxx doplňkové xxxxx
Xxxxxxx xx xxxx xxxxx&xxxx;XX přílohy II.
|
1. |
Doplňkové xxxxx, xxxxx mají pozitivní xxxx xx xxxxxxxxxx xxxxxx, xxxxxxxxxx xxxx xxxxx životní xxxxxxxx, x&xxxx;xxxxxxx xxxxxxx „xxxx xxxxxxxxxxxx doplňkové látky“ Účinky xxx xxxxxxxx xxxxx xx vztahu ke xxxxxxx cílovému druhu xxxx xxxxxxxxx zvířat. X&xxxx;xxxxxxxxxx na xxxxxxxxxxxx xxxxxxxxx xxxxx mohou xxx xxxxxx xxxxxxxx xx pracovních xxxxxxxxxxxxxxxxx (xxxx. produkční xxxxxxxx, xxxxxxxx xxxxx xxxxxxxxx, xxxxxx živočišných produktů), xxxxxxx xxxxxxx upraveného xxxx, xxxxxxxxxxx stáda, xxxxxxxxxxxxx xxxxxxxxxxx xxxx xxxxxxx xxxxxxxxx podmínkách xxxxxx. Xxxxx x&xxxx;xxxxxxxxxx xxxxxxxx xxx xxxxxxxxxx xxxxxxxxxxxx studiemi xxxxxxxxx xxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxx. |
|
2. |
Xxxxxxxxx xxxxx, xxxxx xxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxx xxx životní xxxxxxxxx X&xxxx;xxxxxxxxxxx xxxxx, xxxxx xxxxxxxx xxxxxxxxx xxxxxxx xxxxxxxxx (xxxx. xxxxxxx xxxxxxx xxxxxx a fosforu xxxx omezená produkce xxxxxx, xxxxxxxxx xxxxxxxx), xx možno xxxxxxxx x&xxxx;xxxxxxxx druhu xxxxxxx xxxxx krátkodobými xxxxxxxx xxxxxxxxx xx xxxxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxx. Studie xxxxxx x&xxxx;xxxxx xxxxxxx přizpůsobení xx xxxxxxxxx xxxxx. |
4.1.5&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;X:&xxxx;Xxxx xxxxxxxxxxxx v období xx xxxxxxx xxxxx xx xxx
Xxxxx oddíl xx xxxxxxx xxxxx xxxxxxxxxx xx.&xxxx;7 xxxx.&xxxx;3 xxxx.&xxxx;x)&xxxx;xxxxxxxx (XX) x.&xxxx;1831/2003.
4.2&xxxx;&xxxx;&xxxx;Xxxxxxxxxxxx doplňkové xxxxx: xxxxxx a mikroorganismy
4.2.1 Oddíl I: Shrnutí xxxxxxxxxxx
Xxxxxxx xx xxxx xxxxx&xxxx;X&xxxx;xxxxxxx&xxxx;XX.
4.2.2&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;XX: Xxxxxxxx, charakteristika x&xxxx;xxxxxxxx pro xxxxx xxxxxxxxx xxxxx; metody xxxxxxx
Xxxxxxx xx xxxx xxxxx&xxxx;XX xxxxxxx&xxxx;XX.
4.2.3&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;XXX: Xxxxxx xxxxxxxx xx bezpečnosti xxxxxxxxxxx xxxxx
|
4.2.3.1 |
Xxxxxx týkající xx xxxxxxxxxxx xxxxxxxxx xxxxxxxxx látky pro xxxxxx zvířata Použije xx xxxx xxx&xxxx;3.1.1 přílohy II. Žadatelé xx vybízejí, aby xxxxx možno xxxxxxxxx x&xxxx;xxxxxxx skupiny xxxxxxxxxxxx 100xxxxxxx xxxxxxxx dávky x&xxxx;xxxxxxx xxxxx xxxxxxxxxxxx xxxxxxxxx. X&xxxx;xxxxxx xxxxx xxx použít xxxxxxxxxxxxxx xxxxx xxxxxxxxx látky. Xxxxxxxxxxx se xxxxxx xxxxxxxx xxxxxxxx přítomného xxxxxx, xxxxx účinného xxxxxxx (xxxxxxx) / xxxxx (xxxxx) x&xxxx;xxxxxxxx xxxxxxxxx xxxxxxxxxxxxx xxxxxxx xxxx xxxx být xxxxxx xxxx x&xxxx;xxxxxxx xxxxxxxx. X&xxxx;xxxxxx xxxxxx xxxxxxxxx xxxxxx xxxxxxxx(x). Xxxx xxx&xxxx;3.1.2 xxxxxxx&xxxx;XX xx xxxxxxxx na všechny xxxxxxxxxxxxxx a enzymy, xxxxx xxxx xxxxx xxxxxxxxxxx xxxxxx xx xxxxxx xxxxxxxxxxx flóry nebo x&xxxx;xxxxxxx xx xxx xx udává, xx xxxxxxxxx xxxxxxx mikrobiální xxxxx. X&xxxx;xxxxxxx xxxx xxxxxxxx xxxx xxxxxxxx zvýšení xxxxxxxx xxxxxxxxxxxxxxx xxxxx xxx xxxxxxxx xxxxxxxxx xxxxxx, xxx byla xxxxxxxxx xxxxxxxxxxx xxxxxxxxxxxx xxxxxx xx xxxxxxxxxx xxxxxxxxxxx flóru xxxxxxxxx xxxxxx. U přežvýkavců xxxx xxxxx xxxxx počítání xxxxxxxxxxx xxxxx xxxxx x&xxxx;xxxxxxx, xx xxxxxx xxxxxxxxx xxxxxxxxxx xxxxx xxxxxx bachoru (xxxxxx xx vitro xxxx xxxxx koncentrací těkavých xxxxxxxx xxxxxxx, snížení xxxxxxxxxxx xxxxxxxxxx nebo xxxxxxx xxxxxxxxxx). |
|
4.2.3.2 |
Xxxxxx xxxxxxxx xx xxxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxx pro xxxxxxxxxxxx
Enzymy x&xxxx;xxxxxxxxxxxxxx xxxxx pouze xxxx xxxx xxxxxxxxx xxxxx, xxxxx xx xxxxxxx xxxxxxx xxxx xxxxxxxxx xxxx xxxxxx xxxxxxxxxxx x&xxxx;xxxxxxxxxxxxx procesu. Xxxxx xx xxxxxxxx xxxxxxxxxx xxxxx otestovat, xxx bylo xxxxxxxxx, xx neobsahuje xxxxxxxxx xxxx xxxx xxxxxxxxx, xxxxx mohou poškodit xxxxxxx požívajícího potraviny xxxxxxx ze xxxxxx, xxx byla krmena xxxxxx xxxx vodou xxxxxxxxxx xxxxxx xxxxxxxxxxx xxxxxxx. Xxxxxxx xxxxxxxxxxxxxxx xxxxxxxx xxxxxxxx xxx xxxxx xxxx xxxxxxx xxxxxxxxx xxxxx (včetně člověka) xx však xxxxxxxx xx xxxxxx xxxxxxxxx, xxx něž xxxx x&xxxx;xxxxxxxxx xxxxx x&xxxx;xxxxxxx xxxxxxxxx xxxxxxxxx, xxxx xx xxxxxx, pro xxx xxxx xxxxxxx xxxxxx přesně vymezena. Xxxxxxx xxxxxxxxx xxxxxxx x&xxxx;xxxxxxxxxxxxxx, xxxxx xx x&xxxx;xxxxxxxxxxx používají x&xxxx;xxxxxxxx xxxxxx, xx xxxxxxx xxxxxx xxxxxxxxxx x&xxxx;xxxxxxxx xxxxxxx xxxxxxxxx výrobními xxxxxxx. Xxxxx xx xxx enzymy x&xxxx;xxxxxxxxxxxxx xxxxxx a pro xxxxxxxxxxxxxx, xxx xxx xxxx x&xxxx;xxxxxxxxx xxxxx x&xxxx;xxxxxxx xxxxxxxxx používání, x&xxxx;xxxx-xx xxxxxx fermentačního procesu xxxxxx xxxxxxxxxx x&xxxx;xxxxx, xxxxxxxxxx xxxxxxx xxxxxxxx (xxxx. testování xxxxxx xxxxxxxx nebo genotoxicity) xx nutné. Avšak x&xxxx;xxxxxx xxxxxxxxx a organismů xxxxxxxxxxx x&xxxx;xxxxxxxx enzymů xx xxxx xxxxx xx xxxxxxx xxxxxxxxxxx xxxxxxxxxxxx uvedenými x&xxxx;xxxx 2.2.2.2 xxxxxxx&xxxx;XX. Xx-xx xxxxxxxxxx xxxx xxxx xxxxx xxxx a neexistují dostatečné xxxxxxxx x&xxxx;xxxxxxxx (produkčního) xxxxxxxxx, xxx xxx xxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxx, xx xxxxx xxxxxxxxx studie xxxxxxxxxxxx x&xxxx;xxxxxx xxxxxxxx xxxxxxxxx s doplňkovými xxxxxxx, xxxxx xxxxxxxx životaschopné xxxxxxxxxxxxxx nebo xxxxxx. X&xxxx;xxxxx případě xxxx xxxxxx xxxxxx xxxxxxxxxxxx xxxxxx xxxxxxxxxx x&xxxx;xxxxxx xxxxxxxxxxxx orální xxxxxxxx. Xxxxxxxxxx se, xxx xx xxxx xxxxxx xxxxxxxxx x&xxxx;xxxxxxxxxxx fermentační xxxxx nebo v případě xxxxxxxxxx tuhých xxxxxxxxx x&xxxx;xxxxxxx extraktem. |
|
4.2.3.3 |
Studie xxxxxxxx xx bezpečnosti doplňkové xxxxx pro xxxxxxxxx/xxxxxxxxxx Xxxxxxx xx xxxx bod 3.3 xxxxxxx&xxxx;XX s výjimkou xxxxxx xxxxxxx:
|
|
4.2.3.4 |
Xxxxxx xxxxxxxx xx xxxxxxxxxxx xxxxxxxxx xxxxx xxx xxxxxxx xxxxxxxxx Xxxx xxx&xxxx;3.4 přílohy II xx xxxxxxxx xxxx xx xxxxxxxxxxxxxx, xxxxx xxxxxx xxxxxxxxx původu nebo xxxxxx všudypřítomné x&xxxx;xxxxxxxx xxxxxxxxx. |
4.2.4&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;XX: Studie xxxxxxxx xx účinnosti doplňkových xxxxx
Xxxxxxx xx xxxx xxxxx&xxxx;XX xxxxxxx&xxxx;XX.
|
1. |
Xxxxxxxxx látky, xxxxx mají xxxxxxxxx xxxx na xxxxxxxxxx xxxxxx, xxxxxxxxxx nebo xxxxx životní xxxxxxxx x&xxxx;xxx xxxxxxx xxxxxxx „xxxx xxxxxxxxxxxx doplňkové xxxxx“. Xxxxxx xxx xxxxxxxx xxxxx xx xxxxxx xx každému xxxxxxxx xxxxx xxxx kategorii xxxxxx. X&xxxx;xxxxxxxxxx xx xxxxxxxxxxxx xxxxxxxxx xxxxx xxxxx xxx xxxxxx xxxxxxxx xx xxxxxxxxxx xxxxxxxxxxxxxxxxx (xxxx. xxxxxxxxx xxxxxxxx, průměrný denní xxxxxxxxx, xxxxxx xxxxxxxxxxx xxxxxxxx), skladbě xxxxxxx xxxxxxxxxx těla, xxxxxxxxxxx xxxxx, xxxxxxxxxxxxx xxxxxxxxxxx xxxx dobrých životních xxxxxxxxxx xxxxxx. Xxxxx x&xxxx;xxxxxxxxxx xxxxxxxx xxx xxxxxxxxxx xxxxxxxxxxxx studiemi xxxxxxxxx xxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxx. |
|
2. |
Xxxxxxxxx xxxxx, které xxxxxxxxx xxxxxxxxx důsledky xxxxxxxxx xxxxxx xxx xxxxxxx prostředí. U doplňkových látek, xxxxx příznivě xxxxxxxxx xxxxxxx xxxxxxxxx (xxxx. xxxxxxx xxxxxxx xxxxxx xxxx fosforu xxxx xxxxxxx xxxxxxxx metanu, xxxxxxxxx xxxxxxxx), je xxxxx účinnost x&xxxx;xxxxxxxx xxxxx xxxxxxx třemi xxxxxxxxxxxx xxxxxxxx účinnosti xx xxxxxxx prokazujícími xxxxxxxx prospěšné xxxxxx. Xxxxxx vezmou x&xxxx;xxxxx xxxxxxx xxxxxxxxxxxx xx xxxxxxxxx xxxxx. |
4.2.5&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;X:&xxxx;Xxxx xxxxxxxxxxxx x&xxxx;xxxxxx po xxxxxxx xxxxx xx xxx
Xxxxx xxxxx xx použije xxxxx xxxxxxxxxx čl. 7 xxxx.&xxxx;3 písm. g) nařízení (XX) x.&xxxx;1831/2003.
5.&xxxx;&xxxx;&xxxx;XXXXXXXXXXXXXXX A HISTOMONOSTATIKA
5.1 Oddíl I: Shrnutí dokumentace
Použije xx xxxx xxxxx&xxxx;X&xxxx;xxxxxxx&xxxx;XX.
5.2&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;XX: Xxxxxxxx, charakteristika x&xxxx;xxxxxxxx xxx xxxxx doplňkové xxxxx; xxxxxx analýzy
Použije xx xxxx oddíl II xxxxxxx&xxxx;XX.
5.3&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;XXX: Xxxxxx xxxxxxxx xx xxxxxxxxxxx xxxxxxxxxxx xxxxx
5.3.1&xxxx;&xxxx;&xxxx;Xxxxxx týkající se xxxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxx xxx xxxxxx xxxxxxx
Xxxxxxx se celý xxx&xxxx;3.1 xxxxxxx&xxxx;XX.
5.3.2&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxx xx xxxxxxxxxxx používání xxxxxxxxx látky xxx xxxxxxxxxxxx
Xxxxxxx xx xxxx xxx&xxxx;3.2 přílohy II.
5.3.3 Studie týkající xx bezpečnosti xxxxxxxxx xxxxxxxxx látky pro xxxxxxxxx/xxxxxxxxxx
Xxxxxxx xx celý xxx&xxxx;3.3 přílohy II.
5.3.4 Studie xxxxxxxx xx xxxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxx xxx xxxxxxx prostředí
Použije xx xxxx xxx&xxxx;3.4 xxxxxxx&xxxx;XX.
5.4&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;XX: Xxxxxx týkající se xxxxxxxxx xxxxxxxxx xxxxx
Xxxx xxxxxxxxx xxxxx xxxxxx xxxxxxx před xxxxxxxx xxxxxx Eimeria spp. xxxx Xxxxxxxxxx xxxxxxxxxxx. Xxxxxx xx xxxxxxxx xxxxxxx x&xxxx;xxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxx (xxxx. xxxxxxxxxxxx xxxx) x&xxxx;xxxxxx xxxxxxxxxxxxxxx xxxxxxxxxxxx (xxxx. xxxxxxx xxxxxxxxx, xxxxxxxxx, xxxxx xxxxxx a výskytu xxxxxxxxxx xxxx). Xxxxxxxxx xx předloží xxxxxxxxx x&xxxx;xxxxxx xx růst x&xxxx;xxxxxxxx krmiva (xxxxx xxxxxxx, náhrada xxxxxx x&xxxx;xxxxxxx), účincích xx xxxxxxx xxxxx (xxxxxxxx xxxxxx).
Xxxxxxxxxx údaje x&xxxx;xxxxxxxxx xxxx xxxxxxxx xx xxx xxxx xxxxxx x&xxxx;xxxxxxxx zvířaty:
|
— |
umělé xxxxxxxxxx x&xxxx;xxxxxxx xxxxxxx, |
|
— |
xxxxxxxxx/xxxxx xxxxxxx x&xxxx;xxxxx xxxxxxxxx podmínky xxx xxxxx, |
|
— |
xxxxxxxx xxxxxxxx xxx užití xxx xxxxxxxxx v terénu. |
Pokusy x&xxxx;xxxxxxx xxxxxxxxxxxx a smíšenými xxxxxxxxx (xxxx. xxxxxxx xxxx xxxxxxx) mají xxxxxxxx xxxxxxxxx xxxxxxxx proti xxxxxxxxx x&xxxx;xxxxxxxxxx xxxxxxxxx. Xxx xxxxxxxx výsledky xx xxxxxxxx xxx xxxxxx simulující xxxxxxxx xxx xxxxx (xxxx. xxxxxx xxx xxxxxx xxxxxxxx s drůbeží, xxxxxx xxx klecovém chovu x&xxxx;xxxxxxx). Požadují xx xxxxxx tři studie x&xxxx;xxxxxx s určitou xxxxx xxxxxxxxx xxxxxxx.
5.5&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;X:&xxxx;Xxxx monitorování x&xxxx;xxxxxx xx uvedení xxxxx xx trh
Oddíl xxxxxxx&xxxx;XX se použije xxxxx xxxxxxxxxx xx.&xxxx;7 xxxx.&xxxx;3 xxxx.&xxxx;x)&xxxx;xxxxxxxx (XX) x.&xxxx;1831/2003.
6.&xxxx;&xxxx;&xxxx;XXXXXXXXXXX Z VĚTŠINOVÝCH XXXXX XX DRUHY MENŠINOVÉ
Menšinové xxxxx xxxx xxxxxxxx x&xxxx;xx.&xxxx;1 xxxx.&xxxx;2 xxxxxx xxxxxxxx.
X&xxxx;xxxxxx xx rozšíření xxxxxxxxxx xxxxx pro xxxx, xxxxx xx x&xxxx;xxxxxxxxxxxxxx xxxxxxxx srovnatelný x&xxxx;xxxxxx, pro xxxx xxx xxxx užití xxxxxxxxx xxxxx povoleno, xx xxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxx v plném xxxxxxx.
Xxxx xxxxxxx xxxxxxxxx xx vztahují xxxxx xx požadované povolení xxx menšinové xxxxx x&xxxx;xxxxxxx xx doplňkové xxxxx, xxxxx již xxxx xxxxxxxx xxx xxxxx většinové. Pro xxxxxxxx xxxxxx xxxxxxxxxxx xxxxx xxxxxxxxxx xxxxx xxx menšinové xxxxx xx použijí plně xxxxxxx xxxxxx v závislosti xx xxxxxxxxx/xxxxxxx xxxxxxx xxxxxxxxx látky (viz xxxxxxxxxxxx xxxxxxxx xxxxxxxxx x&xxxx;xxxxxxx&xxxx;XXX).
6.1&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;X:&xxxx;Xxxxxxx xxxxxxxxxxx
Xxxxxxx xx xxxx xxxxx&xxxx;X&xxxx;xxxxxxx&xxxx;XX.
6.2&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;XX: Xxxxxxxx, xxxxxxxxxxxxxxx a podmínky xxx xxxxx doplňkové xxxxx; xxxxxx analýzy
Oddíl II xxxxxxx&xxxx;XX xx použije xxxxx:
|
— |
xxx xxxxxxxxx látky, xxxxx xxxx xxxxxx xx xxxxxxxx xxxxxxxx, se xxxxxxx celý xxxxx&xxxx;XX, |
|
— |
xxx xxxx xxxxxxxxx xxxxx xx použijí body 2.1.2, 2.1.3, 2.1.4, 2.1.4.2, 2.2, 2.3.1, 2.3.2, 2.4.1, 2.4.2, 2.4.4, 2.5, 2.6. |
6.3 Oddíl III: Xxxxxx xxxxxxxx xx xxxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxx
6.3.1&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxx xx xxxxxxxxxxx xxxxxxxxx doplňkové látky xxx xxxxxx xxxxxxx
|
6.3.1.1 |
Xxxxxxxxx x&xxxx;xxxxxxxx xxxxx Xxxxx xxxxxxxxx xxx jednotlivé kategorie / xxxxxxx xxxxxxx xxxxxxxxxxx látek. V zásadě xx xxxxxx xxxxxxxxx x&xxxx;xxxxxxxxxxx xxxxx nepožadují, pokud xxxxxxxxx xxxxx xxxxxxxx xxxxxx xxxxxxx pro xxxxxxxxxx (nejméně xxxxxxxxxx 10) x&xxxx;xxxxxxxxxxx xxxxxxxxxxx xxxxx, který xx x&xxxx;xxxxxxxxxxxxxx xxxxxxxx xxxxxxx. Xxxxx xxx xxxxxxxxx xxxxxx xxxxx (xxxxxx monogastrických x&xxxx;xxxxxxxxxxxx savců x&xxxx;xxxxxxx) xxxxxxxx xxxxxxx x&xxxx;xxxxxx xxxxxxx xxx xxxxxxxxxx, xxxxxxxxxx se xxxxx xxxxxx xxxxxxxxx pro xxxxxxxxx xxxxx, které xxxxxx x&xxxx;xxxxxxxxxxxxxx hlediska xxxxxxx (např. xxxx xxxx králíci). Pokud xx xxxxxxxx studie xxxxxxxxx, doba trvání xxxxxx xxx menšinové xxxxx (xxxxx xxxxxxx) xxxx xxxxxxx 28&xxxx;xxx xxx xxxxxxx v růstu x&xxxx;42&xxxx;xxx xxx xxxxxxx xxxxxxx. X&xxxx;xxxxxxx xxxxx xxxx xxxx xxxxxx: xxxxx xxxxxxx: 28&xxxx;xxx; xxxxxx xxxxxxx: jeden xxxxxx (od xxxxxxxxxx xx xxxxx xxxx xxxxxxx). Pokud xx xxxxxx vztahuje xx xxxxxx a odstavené xxxxxxx, xxxxxxxx xx xx xxxxxxxxxx xxxxxx 49&xxxx;xxx (xxxxxxxx jeden týden xx narození) a musí xxxxxxxxx xxxxxxx xx xx xxxxxxx. Pro xxxx (xxxx xxx xxxxxxxxxx) se požaduje 90xxxxx xxxxxx. |
6.3.2&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxx xx xxxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxx pro xxxxxxx xxxx xxxxxxxxxxxx
|
6.3.2.1 |
Xxxxxx xxxxxxxxxxx Xxxxx xxxxxxxxx xxx xxxxxxxxxx xxxxxxxxx a funkční xxxxxxx xxxxxxxxxxx xxxxx. Xxxxxx xxxxxxxxxxx xx xxxxxxxxxx, xx-xx xxxxxxxxx látka xxx povolena xxx xxxxx x&xxxx;xxxxx, který xx x&xxxx;xxxxxxxxxxxxxx hlediska xxxxxxxxxxx s menšinovými xxxxx, xx něž xx xxxxxxxx xxxxxx x&xxxx;xxxxxxxx. Xxxxxxxx podobnost z fyziologického xxxxxxxx neexistuje, xxxxxxxx xx pro xxxxxxxxx xxxxxxxxxx metabolismu xx xxxxxxxxxx xxxxxxxxx xxxxxxxxxxxxx xxxxxxx xx xxxxxxx xxxxxx xx vitro (xxxx. s hepatocyty xxxxxx xxxxxxx xxxxx). Xxxx-xx xxxxxxxxx xxxx x&xxxx;xxxxxxxxxxxxxx hlediska xxxxxxx xxxxxxxxxxx xxxxx, xx nutno xxxxxx xxxxx x&xxxx;xxxxxxxxxxx xxxxxxxxx xxxxx u menšinového xxxxx. |
|
6.3.2.2 |
Xxxxxx xxxxxxx Xx-xx xxxxxxx xxxx xxxxxxxxx podobnost xxxxxxxxxxx, xxxxxxxx xx pouze xxxxxxxxxxxx xxxxxxxxxxxxxx rezidua x&xxxx;xxxxxxxxxxxxx xxxxxxx a produktech. Xx xxxxx xxxxxxxxx xxxxxxxxx xx použije xxxx bod 3.2.1.2 xxxxxxx&xxxx;XX. |
|
6.3.2.3 |
Xxxxxxxxx xxxxxxxxxxx xxx spotřebitele Návrh xxxxxxxxxxx xxxxxx xxxxxxx (XXX) Xxxxxxxxx XXX xxx xxxxxxx za xxxxxxxxxxx, xx se x&xxxx;xxxxxxxxxxxxx xxxxxxx menšinového druhu x&xxxx;xxxxxxxxx s podobným xxxxxxxxxx xxxxxx nevyskytují xxxxx xxxxxxxx xxxxxxx x&xxxx;xxxxxx xxxxxxx. XXX lze xxxxxxxxxxxx x&xxxx;xxxxx xxxx xxxxxx xxxxx:
XXX xxx xxxx xxx extrapolovat, xxxxx xxxxxxxx XXX xxx xxxxxxxxxxx přežvýkavce x&xxxx;xxxxxxxxxxx xxxxxxxxxxxxxxx xxxxx. Xxxxx xxxx xxxxxxxx identické XXX x&xxxx;xxxxx (xxxx xxxx), xxxxxx x&xxxx;xxxxx (nebo xxxxxxx), xxxxx xxxxxxxxxxx xxxxxxxxx xxxxx s různými xxxxxxxxxxxxx xxxxxxxxxxx x&xxxx;xxxxxxxx xxxxx, je xxxxx xxxxxxxx stejné XXX xxxxxx pro xxxx, xxxxxxxx x&xxxx;xxxxxxx, xxx xxxxxxx, že se xxxxxxxx za xxxxxx xxxxxxxxxxx xx xxxxxxx xxxxxxx, která xxxx xxxxxx k produkci xxxxxxxx, x&xxxx;xxxxxxxx xxx. X&xxxx;xxxxxxx xx pokyn Výboru xxx xxxxxxxxxxx léčivé xxxxxxxxx (CVMP) (10) pro xxxxxxxxx MLR xxx Xxxxxxxxxx x&xxxx;xxxxxxx xxxx, xxxxx xxx xxxxxxxx xxxxxxxxxxx z MLR xx xxxxx xxxxxxxxxxx xxxxx xx Salmonidae a ostatní xxxx xx xxxxxxxxxxx, xx xxxxxxx xxxxx xxxx přijatelné xxxx xxxxxxxxxxxx reziduum xxx XXX xx xxxxx x&xxxx;xxxx, xxx XXX xxxxxxxxxxxx na všechna xxxxxxx xxxxxx k produkci xxxxxxxx. Xxxx k dispozici analytické xxxxxx pro monitorování xxxxxxx x&xxxx;xxxxxxxxxxxxx xxxxxxx x&xxxx;xxxxxxxxxx xxxxx zvířat xxxxxxxx k produkci potravin. |
6.3.3 Studie xxxxxxxx xx xxxxxxxxxxx xxxxxxxxx xxxxxxxxx látky xxx uživatele/pracovníky
Použije xx xxxx xxx&xxxx;3.3 xxxxxxx&xxxx;XX.
6.3.4&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxx xx xxxxxxxxxxx xxxxxxxxx doplňkové xxxxx xxx xxxxxxx xxxxxxxxx
Xxxxxxxxx xxxxx pro životní xxxxxxxxx lze extrapolovat x&xxxx;xxxxxxxxx xxxxxxxxxxx pro xxxxxxxxx druh, xxxxx xx x&xxxx;xxxxxxxxxxxxxx xxxxxxxx xxxxxxxxxxx. Xxx xxxxxxxxx xxxxx, xxxxx xxxx xxx xxxxxxxxx u králíků, xx xxxxxxx celý xxxxx s přihlédnutím x&xxxx;xxxxxxxxxx xxx každou xxxxxxxxx / xxxxxxx xxxxxxx xxxxxxxxxxx xxxxx.
6.4&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;XX: Xxxxxx xxxxxxxx xx xxxxxxxxx xxxxxxxxx xxxxx
Xxxxx xxxxxxxxx xxxxx byla xxx xxxxxxx funkci xxxxxxxx xxx většinový xxxx, xxxxx xx z fyziologického xxxxxxxx xxxxxxxxxxx, a pokud xx znám xxxx xxxxxxxx mechanismus působení xxxxxxxxx xxxxx, je xxxxx xxxxxxxxx za xxxxxxxx účinnosti xxxxxx x&xxxx;xxxxxxx xxxxxxxxxx xxxxxxxx x&xxxx;xxxxxxxxxxx druhů. Xxxxx xxxxxxxx spojitost neexistuje, xx xxxxx xxxxxxxx xxxxxxxx podle xxxxxxxx xxxxxxxx xxx xxxxx&xxxx;XX x&xxxx;xxxxxxx&xxxx;XX. X&xxxx;xxxxxxxxx případech xxxx xxx xxxxxx xxxxxxxxxx xxxxx xxxxxx xx xxxxxx xxxxxxxxxxx xxxx (xxxx. xxxx x&xxxx;xxxx používané x&xxxx;xxxxxxxx xxxxx). V každé studii (X&xxxx;≤ 0,1) xxxx xxxxxx xxxxxxxxxxx (X&xxxx;≤ 0,05), xx-xx xx xxxxx, xx xxxx xxx xxxxxxxxx významnost.
Požaduje-li xx xxxxxxxxx účinnosti, xxxx xxxxxx xxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxxxxx xxxxxxxxxx xxxxx xxxxxxxxxxx xxxxx, který xx x&xxxx;xxxxxxxxxxxxxx xxxxxxxx xxxxxxxxxxx. X&xxxx;xxxxxxxxx xxxxxxxxx xxxxxxxxx xxxx trvání xxxxxx xxxxxxx xxxxxxxxx ustanovení x&xxxx;xxxx&xxxx;4.4 přílohy II x&xxxx;xxxxxxx&xxxx;XX.
6.5&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;X:&xxxx;Xxxx xxxxxxxxxxxx v období po xxxxxxx látky xx xxx
Xxxxx xxxxx přílohy II xx použije podle xxxxxxxxxx čl. 7 xxxx.&xxxx;3 xxxx.&xxxx;x)&xxxx;xxxxxxxx (XX) č. 1831/2003.
7. ZVÍŘATA X&xxxx;XXXXXXXX CHOVU X&xxxx;XXXXXXX XXXXXXX, KTERÁ XXXXXX XXXXXX X&xxxx;XXXXXXXX XXXXXXXX
Xxxxxxx x&xxxx;xxxxxxxx xxxxx x&xxxx;xxxxxxx xxxxxxx, xxxxx xxxxxx xxxxxx k produkci xxxxxxxx, xxxx xxxxxxxx x&xxxx;xx.&xxxx;1 xxxx.&xxxx;1 xxxxxx xxxxxxxx.
7.1&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;X:&xxxx;Xxxxxxx xxxxxxxxxxx
Xxxxxxx xx xxxx xxxxx&xxxx;X&xxxx;xxxxxxx&xxxx;XX.
7.2&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;XX: Xxxxxxxx, xxxxxxxxxxxxxxx x&xxxx;xxxxxxxx pro užití xxxxxxxxx látky; xxxxxx xxxxxxx
Xxxxx&xxxx;XX xxxxxxx&xxxx;XX xx xxxxxxx takto:
|
— |
pro doplňkové xxxxx, které xxxx xxxxxx xx držitele xxxxxxxx, xx xxxxxxx xxxx xxxxx&xxxx;XX, |
|
— |
xxx jiné xxxxxxxxx xxxxx xx xxxxxxx body 2.1.2, 2.1.3, 2.1.4, 2.1.4.2, 2.2, 2.3.1, 2.3.2., 2.4.1, 2.4.2, 2.4.4, 2.5, 2.6. |
7.3&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;XXX: Xxxxxx týkající xx xxxxxxxxxxx doplňkové xxxxx
7.3.1&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxx xx xxxxxxxxxxx xxxxxxxxx doplňkové xxxxx xxx xxxxxx xxxxxxx
Xxxxx xxxxxxxxx xxx xxxxxxxxxx xxxxxxxxx / xxxxxxx xxxxxxx xxxxxxxxxxx xxxxx. Xxxxxxxx-xx xx xxxxxx tolerance, xxxx xxxx trvání xxxx xxxxxxx 28&xxxx;xxx.
Xxxxxx xxxxxxxxx xx nepožaduje, xxxxx xxxxxxxxx xxxxx xxxxxxxx xxxxxxxxxxx a široké xxxxxxx xxx xxxxxxxxxx x&xxxx;xxxxx xxxxxxxxxxx druhů (včetně xxxxxxxxxxxxxxx x&xxxx;xxxxxxxxxxxx xxxxx x&xxxx;xxxxxxx).
7.3.2&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxx xx xxxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxx xxx xxxxxxxxxxxx
Xxxxx xxx xx xxxxxxx xxxxxxxxxx. Xxxxxxxxx xx xxxxxx xxxxxxxxxxx majitele.
7.3.3 Studie xxxxxxxx se bezpečnosti xxxxxxxxx xxxxxxxxx xxxxx xxx uživatele/pracovníky
Použije xx xxxx xxx&xxxx;3.3 xxxxxxx&xxxx;XX.
7.3.4&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxx se bezpečnosti xxxxxxxxx doplňkové xxxxx xxx životní prostředí
Bod 3.4 xxxxxxx&xxxx;XX xx xxxxxxxxxx.
7.4&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;XX: Xxxxxx xxxxxxxx xx xxxxxxxxx xxxxxxxxx xxxxx
Xxxxx xxxxxxxxx xxx xxxxxxxxxx xxxxxxxxx / funkční xxxxxxx doplňkových látek.
Jestliže xxxxxxxxx xxxxx, xxx xxx se xxxxxxxx xxxxxx xx xxxxxxxxx, xxx xxxx xxxxxx xxxxxxxx xxx druh, xxxxx xx x&xxxx;xxxxxxxxxxxxxx xxxxxxxx xxxxxxx, nepožaduje xx další xxxxxxxxx xxxxxxxxx, xxxx-xx požadovaný xxxxxx x&xxxx;xxxxxxxxxxx xxxxxxxx xxxxxx. Xxxxx xxxxxxxxx xxxxx xxxxxx dosud xxxxxxxx xxxx xxxxxxxxxx xxxxxx xx mechanismus xxxxxxxx jsou xxxx xxx x&xxxx;xxxxxxx xxxxxxxxxxx xxxxxxxx, xx xxxxx xxxxxxxx xxxxxxxx xxxxx xxxxxxxx xxxxxxxx xxx xxxxx&xxxx;XX v příloze II.
Doba xxxxxx xxxxxxxxxxxx zkoušek xxxxxxxxx xxxx xxxxxxx 28&xxxx;xxx.
7.5&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;X:&xxxx;Xxxx xxxxxxxxxxxx v období po xxxxxxx xxxxx xx xxx
Xxxxx xxxxx xxxxxxx&xxxx;XX xx použije podle xxxxxxxxxx xx.&xxxx;7 xxxx.&xxxx;3 xxxx.&xxxx;x)&xxxx;xxxxxxxx (XX) č. 1831/2003.
8. DOPLŇKOVÉ XXXXX, XXXXX XXX XXXX POVOLENY XXX XXXXX V POTRAVINÁCH
8.1 Oddíl I: Shrnutí xxxxxxxxxxx
Xxxxxxx xx xxxx oddíl I přílohy II.
8.2 Oddíl II: Xxxxxxxx, xxxxxxxxxxxxxxx x&xxxx;xxxxxxxx xxx xxxxx doplňkové xxxxx; xxxxxx analýzy
Oddíl II xxxxxxx&xxxx;XX xx použije xxxxx:
|
— |
xxx doplňkové xxxxx, xxxxx xxxx vázané xx držitele xxxxxxxx, xx xxxxxxx celý xxxxx&xxxx;XX, |
|
— |
xxx xxxx doplňkové xxxxx xx použijí xxxx&xxxx;2.1.2, 2.1.3, 2.1.4, 2.1.4.2, 2.2, 2.3.1, 2.3.2., 2.4.1, 2.4.2, 2.4.4, 2.5, 2.6. |
8.3&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;XXX: Xxxxxx xxxxxxxx xx xxxxxxxxxxx doplňkových látek
Musí xxx xxxxxxx nejnovější xxxxxxxx xxxxxxxxx bezpečnosti xxxxxxxxxxxxxxx xxxxxxxxxx xxxxx x&xxxx;xxxxxxxx případnými následně xxxxxxxxx xxxxx.
Xxx xxxxxxxxx xxxxx, xxxxx xxxx xxxxxxxx jako xxxxxxxxxxxxx xxxxxxxx látky xxxx xxxxxxxxx x&xxxx;Xxxxxxxx unii xxxx xxxxxx potravin xxx xxxxxxxxxxx omezení, xxxxxx xxxxxx týkající xx bezpečnosti xxx xxxxxxxxxxxx x&xxxx;xxxxxxxxxx xxxxxxx xxxxx.
Xxxxxx se xxxx&xxxx;3.1, 3.2 x&xxxx;3.3 xxxxxxx&xxxx;XX xx xxxxxxxx xx xxxxxxxxx xxxxxxxx x&xxxx;xxxxxxxxxxx xxxxxx xxxxx, xxxxx xxxx používány v potravinách. Xxxxxxxx xxxxx, které xxxx používány rovněž x&xxxx;xxxxxxxxxxx, lze klasifikovat xxxx:
|
— |
x&xxxx;xxxxxxxxxxxxxxxx XXX (xxx xxxxxxxxxx xxxxxxx horního xxxxxx xxxxxx pro xxxxx x&xxxx;xxxxx xxxxxx xxxxxxxxx), |
|
— |
xx xxxxxxxxxx XXX xxxx XX xxxx |
|
— |
x&xxxx;xxxxxxxxxxxx XXX (xxx xxxxx, x&xxxx;xxxxx dostupné údaje xxxxxxxxxxx xx xxxxxxxx xxxxxx bezpečnosti). |
8.3.1 Studie xxxxxxxx xx xxxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxx xxx xxxxxx xxxxxxx
Xx-xx xxxxx xxxxx doplňkové látky xxxxxxx xxxx x&xxxx;xxxxxxx xxxxxxxx, xxx xxxxxxxxxx xxx cílové xxxxx xxxxxxxx na xxxxxxx xxxxxxxxxx toxikologických údajů xx zkoušek xx xxxx x&xxxx;xxxxxxxxxxxx x&xxxx;xxxxxxxx xxxxxxxxx x&xxxx;xxxxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxx. Je-li xxxxx užití x&xxxx;xxxxxxxx xxxxxxxx xxxxx xxx xxxxxxxxxxxx xxxxx x&xxxx;xxxxxxxxxxx, xxxx xxx xxxxx xxxxxx xxxxx xxxxx xxxxxx xxxxxxxxx x&xxxx;xxxxxxxx xxxxxxx.
8.3.2&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxx xx xxxxxxxxxxx používání xxxxxxxxx xxxxx xxx spotřebitele
Pokud xxxxx xxxx xxxxxxxxx xxxxx vede x&xxxx;xxxxx xxxxxxxx xxxxxxxxxxxx xxxx x&xxxx;xxxxxx druhu xxxxxxxxxx xxx x&xxxx;xxxxxxx xxxxx x&xxxx;xxxxxxxxxxx, xxxxx požadovány xxxxx xxxxxxxxxxxxx xxxxx x&xxxx;xxxxx x&xxxx;xxxxxxxxx.
|
8.3.2.1 |
Xxx xxxxxxxxx xxxxx, pro xxx xxxx xxxxxxxxxxxxx ADI Posouzení xxxxxxxxxxx pro spotřebitele xx xxxxxxxxxx xxxxx xxxxxxx, kdy xxxxx xxxxxxxxx xxxxx x&xxxx;xxxxxxxx xxxx x&xxxx;xxxxxxxxx druhu xxxxxxxxxx než xxx xxxxx v potravinách. |
|
8.3.2.2 |
Doplňkové xxxxx xx xxxxxxxxxx ADI xxxx XX Xxxxxxxxxx pro xxxxxxxxxxxx xx xxxxx xxxxxxxx x&xxxx;xxxxxxxxxxxx x&xxxx;xxxxxxxxx xxxxxxxx vyplývající z užití x&xxxx;xxxxxxxx xxxx zvláštní xxxxxxxx v souvislosti s metabolity xxxxxxxxxxxx x&xxxx;xxxxxxxx xxxxx. Xx lze provést xxxxxxxxxxx xxxxx o reziduích x&xxxx;xxxxxxxxxx. Xxxx-xx nezbytné xxxxxx xxxxxxx, požadavek xx xxxxxx xx xxxxxxxx xxxxxx x&xxxx;xxxxxxx xxxx xxxxxxxxxx u neošetřené skupiny x&xxxx;xxxxxxx, jíž byla xxxxxxxx nejvyšší udávaná xxxxx. |
|
8.3.2.3 |
Xxxxxxxxxxxxx přídatné látky, xxx něž nebyla XXX xxxxxxxxx Xx nutno xxxxxxxxxxx xxxxx důvody, xxxx nebyla ADI xxxxxxxxx. Xxxxx to xxxxxxxx obavy x&xxxx;xxxxx xxxxxxxxx xxxxx v krmivech xx přispělo k významnému xxxxxxx xxxxxxxx x&xxxx;xxxxxxxxxxxx, xxxxxxxx xx xxxxx xxxxxxxxxxxxx xxxxxxxxx. Xxxxxxxxxx xxxxxxxx xxxxxxxxxxx x&xxxx;xxxxx x&xxxx;xxxxxxxx xxx xxxxxxxxxxxx z údajů x&xxxx;xxxxxxxxx z literatury. Jsou-li xxxxxxxx xxxxxx xxxxxxx, xxxxxxxxx xx xxxxxx xx xxxxxxxx xxxxxx v tkáních xxxx xxxxxxxxxx u neošetřené xxxxxxx a skupiny, jíž xxxx xxxxxxxx nejvyšší xxxxxxx xxxxx. |
8.3.3&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxx xx xxxxxxxxxxx používání xxxxxxxxx xxxxx xxx xxxxxxxxx/xxxxxxxxxx
Xxxxxxx xx xxxx xxx&xxxx;3.3 xxxxxxx&xxxx;XX.
Xxx xxxxxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxx xxx uživatele xx xxxxxx x&xxxx;xxxxx xxxxxxxxxxxx xxxxxxxx xxxxxxxxx xxx xxxxxxxxxx x&xxxx;xxxxxx látkami xxxxxxxxxxx x&xxxx;xxxxxxxxxxx.
8.3.4&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxx xx bezpečnosti xxxxxxxxx xxxxxxxxx xxxxx xxx xxxxxxx prostředí
Požaduje xx xxx&xxxx;3.4 xxxxxxx&xxxx;XX.
8.4&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;XX: Studie xxxxxxxx se účinnosti xxxxxxxxx xxxxx
Xxxxxxxx je xxxxxx xxxxxxxxxx pro xxxxxx stejná xxxx xxx xxxxx v potravinách, xxxxxx být xxxxx xxxxx xxxxxxxxx xxxxxxxxx. X&xxxx;xxxxxxx xxxxxxx xxxxx xxxxxxxxx xx xxxxxxxx xxxxxxx x&xxxx;xxxxxx&xxxx;XX xxxxxxx&xxxx;XX.
8.5&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;X:&xxxx;Xxxx xxxxxxxxxxxx x&xxxx;xxxxxx xx xxxxxxx xxxxx xx xxx
Xxxxx oddíl xxxxxxx&xxxx;XX xx xxxxxxx xxxxx xxxxxxxxxx xx.&xxxx;7 xxxx.&xxxx;3 xxxx.&xxxx;x)&xxxx;xxxxxxxx (ES) x.&xxxx;1831/2003.
9.&xxxx;&xxxx;&xxxx;XXXXX XXXXXXXX
Xxxxxxx xx xxxxx xxxxxx xxxxxxxxx údajů xxxxxxxxxxxx xxx xxxxxxxxx xxxxxxxx, xxxx xxxxxxxxxxx xxxxxxxxxx xxx xxxxxx xxxxx xx.&xxxx;13 xxxx.&xxxx;3 xxxxxxxx (XX) č. 1831/2003 xxxxxxxx pouze níže xxxxxxx xxxxxxxxx.
Xxxxxx x&xxxx;xxxxx xxxxxxxx zahrnutých xx xxxxxxxxxx xxxxxxxx, xxxx. xxxxxxxxxxxx, charakteristika xxxx xxxxxxxx xxx xxxxx xxxxxxxxx látky, xxxx xxxxxxxx, že xxxxx xxxx žádný xxxxxxxx xxxxxx xxx xxxxxx xxxx, spotřebitele, uživatele xxxx životní xxxxxxxxx. Xx xxxxx xxxxxx xx možno xxxxxxxxxx xxxxx považovat xx xxxxxxxx, xxxxx xxxxxx xxxxx(x)&xxxx;xxxx činidlo(a) a podmínky xxx xxxxx xxxx xxxxxx, xxxx xxxxxxx je x&xxxx;xxxxxx podobná x&xxxx;xxxxxx xxxxxxx žádné nové xxxxxx, xxxxx by xxxxxxxxxx xxxxx. Pro xxxxxxxx produkty xx xxxxx xxxxx xxxxxxxxx xxxxxx, xxxxxxx obvykle xxxxxx xxxxx xxxxxxxx xxxxxx x&xxxx;xxxxxxxxx bezpečnosti xxx xxxxxx xxxx, xxxxxxxxxxxx x&xxxx;xxxxxxx prostředí x&xxxx;xxxxxxxxx.
Xxxxxx musí xxxxxxxx xxxx požadavky:
|
1. |
použije xx xxxx příloha I – xx xxxxxxxx xxxxx x&xxxx;xxxxxxxxxx xxxxx; |
|
2. |
xxxxxxx xx xxxx xxxxx&xxxx;XX xxxxxxx&xxxx;XX; |
|
3. |
xx xxxxx xxxxxxxxxx xxxxx, xxxxx xxxxxxxxx, xx xxxxxxxx xxxx xxxxxxxxxx xxxxxxxxxx xxxxxxxxx látky xxxx x&xxxx;xxxxxx stejné xxxx x&xxxx;xxxxxxx produktu; |
|
4. |
popřípadě xx xxxxx xxxxxxxxx důkazy x&xxxx;xxxxxxxxxxxxxx, x&xxxx;xx xx xxxxxxx xxxxxxxxxxx, xxxxxxxxxx xxxxxxxxxx xxxx xxxxxxxxxx xxxxxx. Xxxx-xx xxxxxxxxxxxxxx xxxx xxxxxxxxx, je xxxxx xxxxxxxx shodu xxxxxxxx xxxxx s MLR; |
|
5. |
je xxxxx xxxxxxxxx xxxxx, xx xx xxxxxxxxxx xxxxxxxxx poznatků xxxxxxx xxxxxxxxx xxxxx xx xxxxxxxxxxx podmínek bezpečná xxx xxxxxx druhy, xxxxxxxxxxxx, xxxxxxxxxx x&xxxx;xxxxxxx xxxxxxxxx; |
|
6. |
xx xxxxx xxxxxxxxx xxxxxx o výsledcích xxxxxxxxxxxx x&xxxx;xxxxxx xx xxxxxxx xxxxx na trh, xxxx-xx xxxxxxxx požadavky xx monitorování zahrnuty x&xxxx;xxxxxxxx; x |
|
7. |
xx nutno xxxxxxxxx xxxxxxxx údaje x&xxxx;xxxxxxxx xxxxxxx x&xxxx;xxxxx x&xxxx;xxxxxxx s příslušnými xxxxxx xxxxxx&xxxx;XXX, IV a V přílohy II. |
10. OBNOVENÍ XXXXXXXX
Xxxxxxx o obnovení povolení xxxxx xxxxxx&xxxx;14 xxxxxxxx (XX) č. 1831/2003 xxxxxxx xxxx požadavky:
10.1 Oddíl I: Shrnutí xxxxxxxxxxx
Xxxxxxx xx xxxx xxxxx&xxxx;X&xxxx;xxxxxxx&xxxx;XX. Xxxxxxxx xx kopie xxxxxxxxx xxxxxxxx Xxxxxxxxxxxx x&xxxx;xxxxxxx xxxxxxxxx xxxxx xx trh nebo xxxxxxxx xxxxxxxx žádosti. Xxxxxxxx se aktualizovaná xxxxxxxxxxx xxxxx xxxxxxxxxxxx xxxxxxxxx x&xxxx;xxxxxxxx xx xxxxxx s uvedením xxxxx xxxx oproti původnímu xxxxxxxx nebo xxxxxxxxxx xxxxxxxx povolení. Žadatel xxxx xxxxxxxxx xxxxxxx xxxxxxxxxxx, xxxxx xxxxxxxx xxxxxx xxxxxxx, x&xxxx;xxxxxxxx xxxx informace, xxxxx xx staly xxxxxxxxxx xx xxxx udělení xxxxxxxxxxx xxxxxxxx/xxxxxxxx xxxxxxxx x&xxxx;xxxxxxx xx xxxxxxxx x&xxxx;xxxxxxxxxx.
10.2&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;XX: Xxxxxxxx, xxxxxxxxxxxxxxx x&xxxx;xxxxxxxx pro xxxxx xxxxxxxxx xxxxx; metody xxxxxxx
Xxxxx&xxxx;XX přílohy II se xxxxxxx xxxxx:
|
— |
xxx xxxxxxxxx xxxxx, které xxxx xxxxxx na xxxxxxxx xxxxxxxx, xx použije xxxx xxxxx&xxxx;XX, |
|
— |
xxx jiné xxxxxxxxx látky se xxxxxxx body 2.1.2, 2.1.3, 2.1.4, 2.1.4.2, 2.2, 2.3.1, 2.3.2, 2.4.1, 2.4.2, 2.4.4, 2.5, 2.6. |
Xx nutno xxxxxxxxx xxxxxx, xxxxx xxxxxxxxx, xx xx xxxxxxxxx xxxxx xxxxxxxx xxxxxxxxx, xxxxx xxx x&xxxx;xxxxxxx, xxxxxxx xxxx xxxxxxxx, xxxxxx xxxxxxxx doplňkové xxxxx. Xx xxxxx xxxxxxx xxxxxxxxxx xxxxx xxxxxxxxx postupu.
10.3 Oddíl III: Studie xxxxxxxx xx xxxxxxxxxxx xxxxxxxxxxx xxxxx
Xxxx xxx xxxxxxxxx důkaz, xx xx xxxxxxxxxx stavu xxxxxxxx xxxxxxx xxxxxxxxx xxxxx xx xxxxxxxxxxx xxxxxxxx bezpečná pro xxxxxx xxxx, xxxxxxxxxxxx, xxxxxxxxxx x&xxxx;xxxxxxx prostředí. Xxxx xxx předložena xxxxxxxxxxxxx dokumentace x&xxxx;xxxxxxxxxxx xx období od xxxxxxx původního xxxxxxxx xxxx xx xxxxxxxxxx xxxxxxxx povolení, xxxxx xxxxxxxx následující informace:
|
— |
zprávy x&xxxx;xxxxxxxxxxx účincích, xxxxxx xxxxxxxxxx jevů (xxxxx xxxxxxx účinky, xxxxxxx xxxxxx xxxxx druhu, xxxxxxx xxxxxx xxxxxxx xxxxxx) u cílových xxxxxx, xxxxxxxxxxxx, xxxxxxxxx x&xxxx;x&xxxx;xxxxxxxx xxxxxxxxx. Xxxxxx x&xxxx;xxxxxxxxxxx xxxxxxxx xxxx xxxxxx xxxxxx xxxxxx, xxxxx xxxxxxxxxxx xxxx/xxxxxx, výsledek, xxxxxxxx xxx xxxxx x&xxxx;xxxxxxxxx xxxxxxxx xxxxxxxxxxx, |
|
— |
xxxxxx x&xxxx;xxxxx xxxxxxxxx interakcích x&xxxx;xxxxxxxxx kontaminacích, |
|
— |
údaje z monitorování xxxxxxx, xx-xx to xxxxx, |
|
— |
xxxxx x&xxxx;xxxxxxxxxxxxxxxxx/xxxxxxxxxxxxxxxxx x/xxxx xxxxxxxxxxxxxxx xxxxxx, |
|
— |
xxxxxxxxx další xxxxxxxxx týkající xx xxxxxxxxxxx doplňkové xxxxx x&xxxx;xxxxx xxxxxxxxx látky xxx xxxxxxx, člověka x&xxxx;xxxxxxx xxxxxxxxx. |
Xxxxx xxxxxx xxxxxxxxxx žádné xxxxx xxxxxxxxx x&xxxx;xxxxxxxx x&xxxx;xxxxxx xxxxxxx, xxxx to xxx xxxxxx odůvodněno.
Zpráva x&xxxx;xxxxxxxxxx programu xxxxxxxxxxxx x&xxxx;xxxxxx po xxxxxxx xxxxx xx xxx xx xxxxxxxx, je-li xxxxxxxx xxxxxxxxx na xxxxxxxxxxxx xxxxxxx x&xxxx;xxxxxxxxxx xxxxxxxx.
Xxxxx xxxxx xxxxxxxxxx xx.&xxxx;14 xxxx.&xxxx;2 písm. d) nařízení (XX) x.&xxxx;1831/2003 žádost x&xxxx;xxxxxxxx xxxxxxxx xxxxxxxx xxxxx xx xxxxx xxxx doplnění xxxxxxxx xxxxxxxxx xxxxxxxx, xxxx xxxx podmínek xxxxxxxxxx xx xxxxxxxxx monitorování, xx xxxxx xxxxxxxxx xxxxxxxx xxxxx xx xxxxxxx xxxxxx xx xxxxx x&xxxx;xxxxxxx s příslušnými xxxxxx xxxxxx&xxxx;XXX, XX x&xxxx;X&xxxx;xxxxxxx&xxxx;XX.
11.&xxxx;&xxxx;&xxxx;XXXXXXXXXXXX XXXXXXXXX XXXXXXXXXXX XXXXX, KTERÉ JIŽ XXXX POVOLENY XXXXX XXXXXXXX 70/524/XXX
Xxxxxxxxxxx xxxxxxx, xxxxx xx xxxx xxxxx xxx&xxxx;11, xxxx xxxxxxxxx xxxxx, které xxx xxxx xxxxxxxx xxxxx xxxxxxxx 70/524/XXX x&xxxx;xxxx xxx přehodnoceny x&xxxx;xxxxxxx x&xxxx;xx.&xxxx;10 xxxx.&xxxx;2 xxxxxxxx (XX) x.&xxxx;1831/2003 x&xxxx;xxxxx xxxxx do xxxxxx skupin:
|
— |
antioxidační xxxxx, |
|
— |
xxxxxxxxxxx x&xxxx;xxxxxxxxxxx xxxxx, |
|
— |
xxxxxxxxxx x&xxxx;xxxxxxxxxxxxx, xxxxxxxxxxx látky x&xxxx;xxxxxxxxxx xxxxx, |
|
— |
xxxxxxx, xxxxxx xxxxxxxx, |
|
— |
xxxxxxxxxxx, |
|
— |
xxxxxxxx, xxxxxxxxxxx a chemicky xxxxxx xxxxxxxxxx xxxxx xx xxxxxxxxxxxx xxxxxxx, |
|
— |
xxxxxxx xxxxx, |
|
— |
xxxxxx, xxxxxxxxxxxx xxxxx x&xxxx;xxxxxxxxxx; |
|
— |
xxxxxxxxxx xxxxxxxxx a |
|
— |
radionuklidní xxxxxx. |
Xxxxxx x&xxxx;xxxxxxx xxxxxxxxxxx xxxxx x&xxxx;xxxxxx doplňkových látek xxxx být xxxxxxx xxxx x&xxxx;xxxxxx xxxxxxxxxxx xxxxx. Xxxxx xxxxxxxx x&xxxx;xxxxxx xxxxxxxx xxxxxx xxxxxxxxxx xxxxxxxxx xx xxxxx použít údaje x&xxxx;xxx xxxxxxxxxxxx xxxxxx xxxxx ustanovení xxxxxx xxxxxxxx, aby xxxx xxxxxxxxx, xx za xxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxx xxxxxxx bezpečná xxx xxxxxx xxxxx, xxxxxxxxxxxx, xxxxxxxxx x&xxxx;xxxxxxx xxxxxxxxx.
11.1&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;X:&xxxx;Xxxxxxx xxxxxxxxxxx
Xxxxxxx xx xxxx oddíl I přílohy II.
11.2 Oddíl II: Xxxxxxxx, xxxxxxxxxxxxxxx x&xxxx;xxxxxxxx pro xxxxx xxxxxxxxx látky; xxxxxx xxxxxxx
Xxxxx&xxxx;XX xxxxxxx&xxxx;XX xx použije takto:
|
— |
pro xxxxxxxxx látky, xxxxx xxxxxx xxxxxx na xxxxxxxx xxxxxxxx, se xxxxxxx xxxx&xxxx;2.1.2, 2.1.3, 2.1.4, 2.1.4.2, 2.2, 2.3.1, 2.3.2, 2.4.1, 2.4.2, 2.4.4, 2.5, 2.6, |
|
— |
xxx xxxx doplňkové xxxxx, xxxxx xxxx xxxxxx xx xxxxxxxx xxxxxxxx, xx xxxxxxx xxxx xxxxx&xxxx;XX. |
11.3&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;XXX: Xxxxxx xxxxxxxx xx xxxxxxxxxxx xxxxxxxxxxx látek
Pokud xxxx xxxxxxxxx látka xxxxxxxxx x&xxxx;xxxxxxx xx bezpečnost xxx cílové xxxxx, xxxxxxxxxxxx, uživatele/pracovníky x&xxxx;xxxxxxx xxxxxxxxx, předloží xx xxxxxxx studií xxxxxxxxxxx xxxxxxxxxxxx xxx xxxxxxxxx xxxxxxxx a případné xxxx xxxxxxxxx, xxxxx xxxx xxxxxxx xx doby xxxxxxx xxxxxxxxxxx povolení. Xxxxx xxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxxx xxxxxxxxx xxx xxxxx xxxxx xxxx xxxxxxxxx xxxxx, xxx xxxxxx xxxxxx x&xxxx;xxxxx z vědecké xxxxxxxxxx, xxxxxxxx xxxx rovnocenné xxxxxx, xxxxx xx xx požadovaly x&xxxx;xxxx xxxxxxx. X&xxxx;xxxxxxx xxxxxxx xx xxxxxxxx úplný xxxxxx xxxxxx bezpečnosti.
11.4 Oddíl IV: Xxxxxx týkající xx xxxxxxxxx xxxxxxxxx xxxxx
Xxxxx x&xxxx;xxxxxxxxx xx xxxxxxxx xxxxx čl. 5 xxxx.&xxxx;3 xxxxxxxx (XX) x.&xxxx;1831/2003 xx xxxxx popřípadě xxxxxxxx xxxxxxxxxxx xxxxxx xxxxxxxxx xxx studie, xxxxxxx xxxxxxxxxx se xxxxxx historie xxxxxxxxx.
11.5&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;X:&xxxx;Xxxx xxxxxxxxxxxx x&xxxx;xxxxxx xx xxxxxxx xxxxx xx xxx
Xxxxx oddíl přílohy II xx xxxxxxx podle xxxxxxxxxx xx.&xxxx;7 xxxx.&xxxx;3 xxxx.&xxxx;x)&xxxx;xxxxxxxx (XX) x.&xxxx;1831/2003.
(1)&xxxx;&xxxx;Xxxxxxxx xxxxx xx xxxxxxxx xxxxx, xxxxx xxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx, xxxx xx této xxxxx xxxxxxxx. Xxxx xxxxxxxxx xxxxxx xxxxx, xxxxx xxxx xxxxxxxx x&xxxx;xxxxxx xxxxxxx xxxxxxxxxxxxx, xxx xx obvyklé.
(2) Pro xxxxx tohoto nařízení xx „silážním xxxxxxxx“ xxxxxx proces, xxx xxxx xx přirozené xxxxxxxxxxxxxx xxxxxxxxx xxxxx xxxxxx xxxxxxxxxxx x&xxxx;xxxxxxxxxxx xxxxxxxxxx xx xxxxxxx xxxxxxxxx xxxxxxxxxx x/xxxx xxxxxxx doplňkových látek x&xxxx;xxxxxxxxxx.
(3)&xxxx;&xxxx;Xxxxxxxxxxxxx xxxxx xxx xxxxxxxx definované zchutňující xxxxx xxxxxxxxx ve XXXXXX, xxxxxxxxxxx xxxxxxx XX pro zchutňující xxxxx, databáze v nařízení Xxxxxx (XX) x.&xxxx;1565/2000 xx dne 18.&xxxx;xxxxxxxx 2000 (Xx.&xxxx;xxxx. L 180, 19.7.2000 x.&xxxx;8), xxxxxx xx xxxxxxx opatření xxxxxxxx xxx přijetí xxxxxxxx hodnocení podle xxxxxxxx Xxxxxxxxxx parlamentu x&xxxx;Xxxx (ES) č. 2232/96 (Xx.&xxxx;xxxx. X&xxxx;180, 19.7.2000 x.&xxxx;8).
(4)&xxxx;&xxxx;X.&xxxx;Xxxx Xxxxxx: xxxxx Xxxx Xxxxxx xxxxxxxxx xxx xxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxx x&xxxx;xxxxxxxxxxx xx xxxxxx Xxxx Xxxxxx č. 1 „Natural xxxxxxx xx xxxxxxxxxxx“, xx.&xxxx;X,&xxxx;Xxxxxxxxx&xxxx;2000 x&xxxx;xxxxxxxxxxxxx xxxxxxxx.
(5)&xxxx;&xxxx;Xxxxx XXX (x.&xxxx;XXX) Xxxxxxxxxxx xxxxx podle Xxxxxxxx Xxxxxxxxx Xxxxxxx, xxxxxxxxxxx xxxxxxxxxxxxx xxxxxxxxxx látek xxxxx xxxxxxxxx v seznamech xxxxxxxxxx xxxxx.
(6)&xxxx;&xxxx;Xxx xxxxx xxxxxx xxxxxx xxxxxxxx xx „toxikologicky xxxxxxxxx xxxxxx“ xxxxxx xxxxx x&xxxx;xxxxxxxxxx xxxxxx xxxx xxxxxxxx příjmem (TDI xxxx TWI), ADI, xxxx x&xxxx;xxxxxxxx, xxxxx xxx x&xxxx;xxxx používání, xxxx xxxxxx xxxxxx, xxx xx xxxxxxxxx xx xxxxxxxx Xxxx 88/388/XXX xxxxxxxx xx xxxxx určených x&xxxx;xxxxxxxxxxx xxx xxxxxxx x&xxxx;xxxxxxxxxxx x&xxxx;xxxxxxxxx xxxxxxxxx xxx xxxxxx xxxxxx, xxxx xxxxxxxxx xxxxx.
(7)&xxxx;&xxxx;Xxxxxxxxx x&xxxx;xxxxxxx&xxxx;4 xxxxxx Rady Evropy x.&xxxx;1 „Xxxxxxx xxxxxxx xx xxxxxxxxxxx“, sv. I, Štrasburk, 2000.
(8)&xxxx;&xxxx;XXXXX (FAO/WHO, 1996, Xxxx xxxxxxxx xxxxxx 35, XXXX, WHO Xxxxxx) xxxxxxxxxxxx xxxxxxx xxxxxxx xxx xxxxxx xxxxx xx měla xxx upravena s přihlédnutím x&xxxx;xxxxxxxxx zvířete x&xxxx;xxxxxx xxxxxx.
(9)&xxxx;&xxxx;Xx.&xxxx;xxxx. L 180, 19.7.2000, x.&xxxx;8.
(10)&xxxx;&xxxx;Xxxxx xxx xxxxxxxxx xxxxxxxxxxx xxxxxx xxxxxxx xxx Xxxxxxxxxx x&xxxx;xxxxxxx xxxx. Evropská xxxxxxxx xxx xxxxxx xxxxxxxxx. Xxxxxxxxxx Xxxxxxxxx Xxxxxxxxxx Xxxx. XXXX/XXXX/153x/97-XXXXX.
XXXXXXX XX
Xxxxxxxxx x xxxxxxxx xxxxxxxx xxxxxx x xxxx o minimální xxxx xxxxxx xxxxxx xxxxxxxxx
1. Xxxxxxx. Xxxxxxxxx xxxxxx: xxxxxxx
|
Xxxxxxxxx |
Xxxxxxxx xxxxxxxxx xxxxxx |
Xxxxxxxxx xxxx xxxxxx (xxxxxxxx/xxxxx) |
Minimální xxxx trvání xxxxxxxxxxxx xxxxxx účinností |
||
|
Období/stáří |
Xxxxx |
Xxxxxxxx |
|||
|
Selata (sající) |
Mladá xxxxxxx xxxxxx xxxxx xx xxxxxxx |
Xx xxxxxxxx |
Až xx 21–42 xxx |
Až xx 6–11 xx |
14 xxx |
|
Xxxxxx (xxxxxxxxx) |
Xxxxx xxxxxxx xx xxxxxxxx xxxxxx xxxx chovaná k reprodukci xxxx pro xxxxxx xxxxxxxx |
Xx 21–42 xxx |
Až do 120 xxx |
Xx do 35 xx |
42 xxx |
|
Xxxxxx (xxxxxx a odstavená xxxxxx) |
Mladá xxxxxxx od xxxxxxxx xxxxxxx x xxxxxxxxxx nebo xxx xxxxxx xxxxxxxx |
Od xxxxxxxx |
Xx xx 120 dní |
Xx xx 35 kg |
58 xxx |
|
Xxxxx xxxxxx |
Xxxxxxx xx xxxxxxx xxxxxx x xxxxx xxxxxxxx xx xx dne odvozu xx xxxxx |
Xx 60–120 xxx |
Xx xx 120–250 xxx (xxxx xxxxx xxxxxxxx zvyklostí) |
80–150 xx (xxxx xxxxx místních xxxxxxxxx) |
Xx xx xxxxxxx xxxxxxxxx, xxxxxxx však 70 xxx |
|
Xxxxxxxx xxxxxx k reprodukci |
Samice xxxxxxx, které byly xxxxxxx jednou xxxxxxxxxxxx/xxxxxxxxxx |
Xx xxxxx xxxxxxxxxx |
|
|
Od xxxxxxxxxx xx xxxxx xxxxxxx xxxxxxx xxxx (xxx xxxxx) |
|
Xxxxxxxx xxxxxx k reprodukci xxxxx |
Xxxxxx xxxxxxx, které xxxx xxxxxxx xxxxxx xxxxxxxxxxxx/xxxxxxxxxx |
|
|
|
Xxxxxxx xxx týdny xxxx porodem do xxxxx doby odstavu |
2. Xxxxxxx. Xxxxxxxxx zvířat: xxxxxx
|
Xxxxxxxxx |
Xxxxxxxx xxxxxxxxx zvířat |
Xxxxxxxxx xxxx xxxxxx (xxxxxxxx/xxxxx) |
Xxxxxxxxx xxxx xxxxxx xxxxxxxxxxxx xxxxxx xxxxxxxxx |
||
|
Xxxxxx |
Xxxxx |
Xxxxxxxx |
|||
|
Xxxxx xxxxx |
Xxxxxx xxxxxx xxx výkrm |
Xx xxxxxxxxx |
Xx xx 35 xxx |
Xx xx ~1 600 x (xx xx 2 xx) |
35 xxx |
|
Xxxxxx xxxxx x xxxxxx |
Xxxxxxxx chované pro xxxxxxxx produkci xxxxx xxxx xxx chovné xxxxx |
Xx xxxxxxxxx |
Xx xx ~16 xxxxx (xx do 20 xxxxx) |
— |
112 dní (xxxxxx-xx xxxxx x xxxxxxxxx x xxxxxxxxx xxx xxxxx xxxxx) |
|
Xxxxxxx |
Xxxxxxx xx snášce xxxxxxx xxx xxxxxxxx xxxxx |
Xx 16–21 xxxxx |
Xx xx ~13 xxxxx (xx do 18 měsíců) |
Xx 1 200 x (xxxx), 1 400 x (xxxxx) |
168 xxx |
|
Xxxxx krůt |
Xxxxx x xxxxxxx xxxxxxx xx xxxxx |
Xx vylíhnutí |
Xx xx ~14 xxxxx (xx xx 20 xxxxx) Xx xx ~16 xxxxx (až xx 24 xxxxx) |
Xxxxxx: xx xx ~7 000 x (xx xx 10 000 g) Xxxxx: xx xx ~12 000 x (xx xx 20 000 x) |
84 xxx |
|
Xxxxx xxx xxxxx plemenitby |
Xxxxx a krocani xxxxxxx xxx xxxxx xxxxxxxxxx |
Xxxx období |
Xx 30 xxxxx xx xx ~ 60 xxxxx |
Xxxxxx: xx ~15 000 x Xxxxx: od ~30 000 x |
Nejméně xxxx xxxxxx |
|
Odchov krůt |
Mladé xxxxx x xxxxxxx xxxxxx x xxxxxxx xxxxxx |
Xx xxxxxxxxx |
Xx xx 30 týdnů |
Xxxxxx: xx xx ~15 000 x Xxxxx: xx xx ~30 000 x |
Xxxx xxxxxx (xxxxxx-xx xxxxx x xxxxxxxxx x xxxxxxxxx pro xxxxx xxxx) |
3. Xxxxxxx. Xxxxxxxxx xxxxxx: skot (domácí xxxx, xxxxxx druhů xxxxxxx a bizon)
|
Kategorie |
Xxxxxxxx xxxxxxxxx xxxxxx |
Xxxxxxxxx xxxx xxxxxx (xxxxxxxx/xxxxx) |
Xxxxxxxxx xxxx trvání xxxxxxxxxxxx studií účinností |
||
|
Období |
Xxxxx |
Xxxxxxxx |
|||
|
Xxxxxx xxxxx |
Xxxxxx xxxxxxx xxx xxxxxxxxxx xxxx xxxxxxxx xxxxxxxx xxxx |
Xx narození |
Xx xx 4 xxxxxx |
Xx xx 60–80 xx (xx do 145 xx) |
56 xxx |
|
Xxxxx telat |
Telata xxx xxxxxxxx xxxxxxxx xxxx |
Xx xxxxxxxx |
Xx do 6 xxxxxx |
Až xx 180 xx (xx do 250 xx) |
Xx xxxxxxx, xxxxxxx xxxx 84 dní |
|
Výkrm skotu |
Xxxx xx xxxxxxx xxxxxx x xxxxx produkci xx xxx xxxxxx na xxxxx |
Xx xxxxxxx xxxxxxx xxxxxxxxxxxx |
Xx xx 10–36 xxxxxx |
Xx xx 350–700 kg |
168 xxx |
|
Xxxxxxx xxx xxxxxxxx mléka |
Xxxxxx xxxxx, xxxxx porodily nejméně xxxxx xxxx |
|
|
|
84 xxx (xx xxxxx xxxxx xxxx xxxxxx xxxxxxx) |
|
Xxxxx x xxxxxxxxxx |
Xxxxxx xxxxx, které byly xxxxxxx xxxxxx xxxxxxxxxxxx/xxxxxxxxxx |
Xx xxxxx xxxxxxxxxx xx xxxxx xxxxxxx xxxxxxx |
|
|
Xxx xxxxx (xxxxx se xxxxxxxx xxxxxxxxxxx parametry) |
4. Xxxxxxx. Xxxxxxxxx xxxxxx: ovce
|
Xxxxxxxxx |
Xxxxxxxx xxxxxxxxx zvířat |
Xxxxxxxxx xxxx xxxxxx (xxxxxxxx/xxxxx) |
Xxxxxxxxx doba xxxxxx xxxxxxxxxxxx studií xxxxxxxxx |
||
|
Xxxxxx |
Xxxxx |
Xxxxxxxx |
|||
|
Xxxxxx xxxxxx |
Xxxxxxx xxxxxxx xxx xxxxxxx xxxxxxxxxx |
Xx xxxxxxxx |
Xx do 3 měsíců |
15–20 xx |
56 xxx |
|
Xxxxx xxxxxx |
Xxxxxxx xxxxxxx pro xxxxxxxx xxxxxxxxx xxxx |
Xx xxxxxxxx |
Xx xx 6 xxxxxx (xxxx starší) |
Xx xx 55 xx |
Xx xxxxxxx xxxxxxxxx, xxxxxxx xxxx 56 xxx |
|
Xxxx xxxxxx x xxxxxxxx mléka |
Xxxx, xxxxx xxxxxxxx xxxxxxx xxxxx jehně |
|
|
|
84 xxx (xx xxxxx uvést xxxx xxxxxx laktace) |
|
Xxxxxxx k reprodukci |
Xxxxxx xxxx, xxxxx xxxx xxxxxxx xxxxxx inseminovány/připuštěny |
Xx xxxxx inseminace do xxxxx druhého xxxxxxx |
|
|
Dva xxxxx (pokud xx xxxxxxxx reprodukční parametry) |
5. Xxxxxxx. Xxxxxxxxx zvířat: xxxx
|
Kategorie |
Xxxxxxxx xxxxxxxxx xxxxxx |
Xxxxxxxxx xxxx xxxxxx (xxxxxxxx/xxxxx) |
Xxxxxxxxx doba xxxxxx xxxxxxxxxxxx studií xxxxxxxxx |
||
|
Xxxxxx |
Xxxxx |
Xxxxxxxx |
|||
|
Xxxxxx xxxxxx |
Xxxxx xxxx xxxxxxx xxx budoucí xxxxxxxxxx |
Xx xxxxxxxx |
Až do 3 xxxxxx |
15–20 xx |
Xxxxxxx 56 xxx |
|
Výkrm kůzlat |
Xxxxx xxxx chované xxx xxxxxxxx kozího xxxx |
Od xxxxxxxx |
Xx do 6 měsíců |
|
Nejméně 56 xxx |
|
Xxxx určené x xxxxxxxx xxxxx |
Xxxx xxxxxxx s jedním xxxxxxxx |
|
|
|
84 xxx (xx xxxxx xxxxx xxxx období xxxxxxx) |
|
Xxxx x xxxxxxxxxx |
Xxxxxx xxxx, xxxxx xxxx xxxxxxx xxxxxx xxxxxxxxxxxx/xxxxxxxxxx |
Xx xxxxx xxxxxxxxxx xx xxxxx xxxxxxx xxxxxxx |
|
|
Dva xxxxx (xxxxx xx xxxxxxxx xxxxxxxxxxx parametry) |
6. Tabulka. Kategorie xxxxxx: xxxx
|
Xxxxxxxxx |
Definice kategorie xxxxxx |
Xxxxxxxxx doba xxxxxx (xxxxxxxx/xxxxx) |
Xxxxxxxxx xxxx xxxxxx xxxxxxxxxxxx xxxxxx xxxxxxxxx |
||
|
Období |
Xxxxx |
Xxxxxxxx |
|||
|
Xxxxx x xxxxxx |
|
|
|
200–300 x |
90 xxx xxxx xx xxxx, kdy xx xxxxxxx xxxxxxx hmotnost xxxxxxxxxxx |
|
Xxxxx a pstruh |
Xxxxx xxxxxxxxx xxx |
Xxxxx xxxxx xx xxxxxxxx době xxxxx |
|
|
90 dní |
7. Xxxxxxx. Xxxxxxxxx xxxxxx: xxxxxxx
|
Xxxxxxxxx |
Definice xxxxxxxxx xxxxxx |
Přibližná xxxx xxxxxx (xxxxxxxx/xxxxx) |
Xxxxxxxxx xxxx xxxxxx dlouhodobých xxxxxx xxxxxxxxx |
||
|
Xxxxxx |
Xxxxx |
Xxxxxxxx |
|||
|
Xxxxxx x xxxxxxxxx xxxxxxx |
|
Xxxxxxxx xx jednoho xxxxx xx xxxxxxxx |
|
|
56 dní |
|
Xxxxx xxxxxxx |
Králíci xxxxxxx xxx masnou xxxxxxxx |
Xx xxxxxxx |
Xx do 8–11 xxxxx |
|
42 xxx |
|
Xxxxxx xxxxxxx (xxx xxxxxxxxxx) |
Xxxxxxx, xxxxx xxxx xxxxxxx xxxxxx inseminovány/připuštěny |
Xx xxxxxxxxxx do xxxxx xxxxxxx xxxxxxx |
|
|
Dva cykly (xxxxx se xxxxxxxx xxxxxxxxxxx xxxxxxxxx) |
|
Xxxxxx xxxxxxx xxxxxx x xxxxxxxx xxxxxxx xxxxxxx |
Xxxxxxx, xxxxx xxxx xxxxxxx jednou xxxxxxxxxxxx |
Xx xxxxx xxxxxxxxxx |
|
|
Nejméně 2 týdny xxxx xxxxxxx do xxxxx doby xxxxxxx (xxxx. xxx xxxxxxx mikroorganismů) |
8. Tabulka. Xxxxxxxxx xxxxxx: koně
|
Xxxxxxxxx |
Xxxxxxxx xxxxxxxxx xxxxxx |
Xxxxxxxxx doba xxxxxx (xxxxxxxx/xxxxx) |
Xxxxxxxxx xxxx xxxxxx xxxxxxxxxxxx xxxxxx xxxxxxxxx |
||
|
Xxxxxx |
Xxxxx |
Xxxxxxxx |
|||
|
Xxxx |
Xxxxxxx xxxxxxxxx |
|
|
|
56 dní |


