XXXXXXXX XXXXXX (XX) 2015/566
xx xxx 8. xxxxx 2015,
xxxxxx xx xxxxxxx směrnice 2004/23/XX, xxxxx xxx o postupy xxx xxxxxxxxx xxxxxxxxxxxx xxxxxxxxxx x xxxxxxxxxxxxxx norem xxx dovážené tkáně x xxxxx
(Xxxx x xxxxxxxx xxx XXX)
XXXXXXXX XXXXXX,
s ohledem xx Xxxxxxx o fungování Xxxxxxxx xxxx,
x xxxxxxx xx xxxxxxxx Xxxxxxxxxx parlamentu x Xxxx 2004/23/ES xx xxx 31. xxxxxx 2004 x xxxxxxxxx jakostních x xxxxxxxxxxxxxx norem xxx xxxxxxxx, xxxxx, vyšetřování, xxxxxxxxxx, xxxxxxxxxx, xxxxxxxxxx x xxxxxxxxxx xxxxxxxx tkání x xxxxx (1), x xxxxxxx xx xx. 9 xxxx. 4 xxxxxxx xxxxxxxx,
xxxxxxxx k těmto xxxxxxx:
|
(1) |
Xxxxxxxx 2004/23/XX xxxxxxx x xxxxx xxxxxxxxx vysoké xxxxxx xxxxxxx xxxxxxxx zdraví x Xxxx xxxxxxxx x xxxxxxxxxxxx xxxxx xxx darování, xxxxx, xxxxxxxxxxx, xxxxxxxxxx, xxxxxxxxxx, xxxxxxxxxx x xxxxxxxxxx xxxxx xxxxxxxx xxxxx x xxxxx xxxxxxxx k použití x xxxxxxx x xxx xxxxxxxx, xxxxx x xxxxxxxxxxx lidských xxxxx x xxxxx obsažených x xxxxxxxxxxx xxxxxxxx k použití x xxxxxxx, xxxxx xx xx tyto xxxxxxxxx xxxxxxxx jiné právní xxxxxxxx Xxxx. |
|
(2) |
X xxxxxxxxxxx výměně xxxxx x xxxxx xxxxxxx xx xxxxx větším xxxxxxx, x xxxxxxxx 2004/23/XX xxxxx xxxxxxxx, xxx xxxxx tkání x xxxxx xxxxxxxxxxx tkáňová zařízení, xxxxx pro xxxxx xxxx xxxxxxxxxxxx či xxxxxxxxx xxxxxxx státy xxxx xxx xxxxxxx xxxxxxxxx xx xxxxxxxx. Xxxxxxx x xxxxxxxxx xxxxxxxxx xxxx xxxxxxxxx v čl. 9 xxxx. 3 xxxxxxxx 2004/23/XX, xxxxx xxxxxxxx xxxxxxxxxx xxxxxxx, xxx přímo xxxxxxxx dovoz xxxxxxxx xxxxx x xxxxx za xxxxxxxx stanovených x xxxxxx 6 xxxxxxxx Xxxxxx 2006/17/XX (2) xxxx x xxxxxxxxx případě. Xxxx xxxxxxx xxxx xxxxxxxxx xxxxxxxxxx, xxxx xxxx, při povolování xxxxxx xxxxxxxxxxxx xxxxxxxxx xxxxx x xxxxxx xxxxx, xxxxxxxxx xxxx xxxx xxxxxxxxxxx xxxx, které xxxx xxxxxxxxx při xxxxx xxxx xxxxxxxxxx xxxxxxxxxxxx xxxxxx život. |
|
(3) |
Xxxxxxxx 2004/23/XX xxxx xxxxxxxx, xxx xxxxxxx státy x xxxxxxxxxx xxxxxxx xxxxxxxx xxxxxxxxx, xx xxxxx xxxxx x xxxxx xxxxxxx xxxxxxxx x xxxxxxxxxxxx normy xxxxxxxxxx normám, xxxxx xxxx xxxxxxxxx xx xxxxxxxx 2004/23/XX, a vyzývá xx zřízení xxxxxxx xxx ověřování rovnocennosti xxxxxxxxxx x xxxxxxxxxxxxxx norem xxx xxxxx xxxxx x xxxxx. Xxxx xxxxxxx xx xxxx být xxxxxxxxx x xxxx xxxxxxxx, xxxx jsou dotčeny xxxxxx xxxxxxxx Xxxx x xxxxxxx cel. |
|
(4) |
Xxxxxxx xx xxxxxx xxxxxxxx programy xxxxxxxxxxx x xxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxx xxxxxxxx xxx činnosti související x xxxxxxx a buňkami xxxxxxxxx x Xxxx. Xxxx xx xxxxxx stanovit xxxxxxx, xxxxx musí xxxxxxxxx xxxxxxxxxx xxxxxxx xxxxxxxx xx vztahu k dodavatelům xx třetích xxxx. |
|
(5) |
X xxxxxxxx xxxxxx, který xxxxx xxxxxxxx xxxxxxxxx xxxxxx xxxxx čl. 9 odst. 3 xxxxxxxx 2004/23/XX, xxxx xxxxxxx xxxxx tkání x xxxxx xx třetích xxxx xxxxxxxx xxxxxxxxxx xxxxxxx xxxxxxxx. V případech, xxx xxxxxxxxx xxxxxx xxxxx povolí xxxxx xxxxx xx. 9 odst. 3 xxxxxxxx 2004/23/XX, xxxx xxxxxxxxx orgány xxxxxxxx, xxx xxxxxxx xxxxx xxxxxxxx xxxxxxxx x xxxxxxxxxxxx xxxxx rovnocenné xxxxxx xxxxxxxxxx x xxxxxxx směrnici. |
|
(6) |
Tkáně x xxxxx xx xxxx xxx xx normálních xxxxxxxxx xxxxxxxx xxxxxxx xxxxx nebo nemocničními xxxxxxxxxx, xxxxx jsou xxxxxxxxxxxx xx jmenovány xxxx jim xxxx xxxxxxx oprávnění xx xxxxxxxx coby xxxxxxxxxxx xxxxxxxx zařízením xxx xxxxx xxxxxx. Xxxxx xxxxx xxxx xxxxxxxxxx xxxxxxxx xx xxxx xxx xxxxxxxxxx xx xxxxxxxxxx xxxxxxx xxxxxxxx, xxxxx xxxx xxxxxxx xxxxxxxxx xxxxxxxx x xxxxxxxxxxx xx xxxxx xxxx xx xxxxx xxxxx x xxxxx. Jestliže xx xxxxxxx smluvního ujednání x xxxxxxxxxxx xx xxxxx xxxx xxxxxxx nabízející xxxxxxxxxxxxxxxxxxx služby x xxxxx xxxxxxxx xxxxx tkání x xxxxx, avšak xxxxxx xxx xxxxxxx xxxxx, xxxxx by být xxxxxxxxx za dovážející xxxxxxx xxxxxxxx. Členské xxxxx mohou xxxx xxxxxx xxxxxxxxx mimo xxxxxx xxxxxxxxxx xxxx xxxxxxxx. |
|
(7) |
Xxxx-xx xxxxxxx xxxxxxxxx xxxxxxxx xx dovoz xxxxx x xxxxx x xxxxxxxxxxx xx třetí xxxx xxxx xxxxxxxx, xxxx xxxxxxxxx organizace xxxxxxxxx xx xxxxxxx x xxxxxxx, xxxxxxx xxxxxxxx xxxxxxxxx xxx xxxxxxx xxxxxxx, xxxxxx x xxxxxxxxx nebo xxxxxxxxxxx, xxxx xx xxx považovány xx xxxxxxxxxx tkáňové xxxxxxxx. Xxxx subjekty xxxx xxxxxxxx požadavky xxxx xxxxxxxx x xxxxxx xxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxx 2004/23/XX x xxxxxx příslušné xxxxxx xx musí xxxxxxxxxxx xx xxxxxxxx xxxx xxx xxxx xxxxxx xxxxxxxxx xx xxxxxxxx xxxx dovážejícím xxxxxxxx zařízením pro xxxxx dovozu. Xxxxxxxx x xxxxxxxxxx na xxxxx xxxx xxxxxxxx xxxx xxxxxxxxx vyšetřování, zpracování, xxxxxxxxxx, xxxxxxxxxx nebo xxxxxxxxxx dovážených tkání x xxxxx, xxxx xxx xxxxxx xxxxxxxxxxxx xx xxxxxxxxx xxxx jim xxxx být uděleno xxxxxxxxx nebo xxxxxxxx xxx xxxxx xxxxxx xxxxxxxx xxxxxx příslušnými xxxxxx; xxxx xxxx xxxxxxxx xxxxxxxxx xxxxxxxx 2004/23/XX. Xxxxx toho xxxx mohou xxxxxx xxxxx x xxxxx pocházející xx xxxxxxx zemí xx bank tkání xxxx xxxxxxxxxxxx xxxxxxxx x Xxxx, xxxxx xxxx xxxxxxxxxxxx xx jmenovány xxxx xxx xxxx xxxxxxx xxxxxxxxx či xxxxxxxx xxxx xxxxxxxxxxx xxxxxxxx zařízením xxxxxx xxxxxxxxxxx xxxxxx. |
|
(8) |
Xxxxxxxx xxxx xxxxxxxxxx xxxxxxx xxxxxxxx xxxxxx xxxxxxxxxxxx xx xxxxxxxxx nebo xxx xxxx xxxxxxx xxxxxxxxx xx xxxxxxxx coby xxxxxxxx xxxxxxxxx pro xxxxxxxx, které xxxxxxxxxx x Xxxx, xxxxx xxxxxxx xxxxx přizpůsobit xxx xxxxxxx xxx xxxxxxxxx xxxxxxxxx, xxxxxxxx a podávání xxxxx, jestliže budou xxxxxxxx xxxxxxx stanovené x xxxx xxxxxxxx. |
|
(9) |
V zájmu xxxxxx xxxxxxxxxx xxxxxxxxxx xxxxx x xxxxx v Unii, včetně xxxxxxx přeshraniční xxxxxxxxxx, xx xxxxxxxxx xxxxx xxxx orgány xxxx xxxxx osvědčení o akreditaci, xxxxxxxxx, oprávnění nebo xxxxxxxx dovážejícího xxxxxxxxx xxxxxxxx. |
|
(10) |
Xxxxxxxxx xxxxx xxx xxxxxxxxx, xxx xxxxxxxx xxxxx x xxxxx xxxxxxx xxxxxxxx x xxxxxxxxxxxx xxxxx, xxxxx xxxx xxxxxxxxxx xxxxxx xxxxxxxxxx xx xxxxxxxx 2004/23/ES, xxxxx xxxxxxxx. Xxxxxxx xxxxx xx xxxxx xxxxxxxx, xxx x xxxxxxxxxxx xxxxxxxxx xxxxxx prováděly xxxxxxxx x xxxxxxxxxx xx xxxxxxx xxxx a aby spolupracovaly x xxxxxxxxx xxxxxxxxx státy, xx xxxxx mohou xxx xxxxxxxx xxxxx x xxxxx xxxxxxxxxxxxx. Xxxxxxxxxxx xx přijetí xxxxxxxxxxxxxx xxxxxxxx x xxxxxxxxxx, zda xx třeba x xxxxxxxxxx xx třetích xxxx xxxxxxxx xxxxxxxx xx xxxxx, náleží xxxxxxxx xxxxxx, x xxxxx xxxx xxxxxxxx dovážející tkáňová xxxxxxxx. |
|
(11) |
Xxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxx se xxxxxxxx xxx příslušné xxxxxx (Operational Manual xxx Competent Authorities xx xxxxxxxxxxx), která xxxx zahrnuje inspekce xxxxxxxxxxxx tkáňových zařízení x xxxxxx xxxxxxxxxx xx xxxxxxx zemí; xxx xxxxxxxxx inspekcí může xxxx příručka xxxxxxxx xxxxxx posloužit xxxx xxxxxxxxxx xxxxxxxx. |
|
(12) |
Xxxxxxxxxx tkáňová xxxxxxxx by xxxx xxxxxx, že xxxxx x xxxxx, jež xxxxxxxx xx Unie, xxxxxxx xxxxxxxx a bezpečnostní xxxxx, xxxxx xxxx xxxxxxxxxx xxxxxxxxx x xxxxxxxxxxxxx xxxxxx xxxxxxxxxx ve směrnici 2004/23/XX. Xxxxxxx prvky xxx xxxxxxxxx, xxx xxxxxx xxxxxxxxx proběhlo, x xxxxxxx zajištění sledovatelnosti xx x xxxxx x xxxxxxxx, xxx xxxx xxxxxxxx xxxxxx xxxxxxxxxxxx x xxxxxxxxxxx xxxxxxxx v souladu xx xxxxxxxx 2004/23/XX, představují xxxxxxx xxxxxx s dodavateli xx xxxxxxx xxxx x xxxxxxxxxxx, která xx xxx xxxxxx a poskytnuta xxxxxxxxxx orgánům. Xxxxxxxxxx xxxxxxx xxxxxxxx xx xxxxxx vyzývají, aby x xxxxx dodavatelů xx xxxxxxx zemí xxxx xxxxxxx xxxxxx xxxxxxxxxxx xxxxxxx prováděly audit. |
|
(13) |
Dovážející xxxxxxx xxxxxxxx by xxxx zajistit, xx xx xx xxxxxxxx xxxxx a buňky x xxxxxxx xx xxxxxxxx Xxxxxx 2006/86/XX (3) xxxxxxxxxx jednotný xxxxxxxx xxx, x xx xxx xxx, xx xxxx xxxxxxxxx xxxxx xxxx, xxxx xx xxxxxx xxxxxxxxxx xx xxxxxxx xxxx xxxx xxxxxxx podmínek xxxxxxx xxxxxx, xxxxxx s nimi xxxxxxxx. |
|
(14) |
Xxxxxxx státy by xxxx xxx xxxxxxx xxxxxx x xxxxxxx xxxxxxxxxxxxx xxxxxx xxxxxxx x xxxxxxxxx xxxxxxxxxxx x xxxx xxxxxxxx, xxxxx jde o dokumentaci x xxxxxxx dohody. Xxxxxx xxxxxxxxxxx xxxxx by xxxxxxx xxxx xxxxxxxx xxxxxxxxxx tkáňová xxxxxxxx, xxx byla xxxxxxxxxxxx xx xxxxxxxxx nebo xxxx bylo xxxxxxx xxxxxxxxx xx xxxxxxxx, x xxxxxx xx k němu xxxxxx xxxxxxxx xxxxxxxxxx xxxx xxxxxxxxx xx xxxxxxxx dodavatele ze xxxxx xxxx. Xxxx xxxxxxx by měly xxx xxxxxxx xx xxxxxxx, xxx určitá xxxxx (nebo osoby) xx nebo xxxx xxx xxxxx xxxxxxx xxxxxxx xx xxxxx xxxx xxxxxxxxxx xxxxx xxxx xxxxx – xxxxx xx xxxxxxx x xxxxxxx darování xxxxxxxxxxxxx xxxxx mezi xxxxxxxx, xxxxxxxx určené k autolognímu xxxxxxx xxxx xxxxxxxx xxxxxx xxxxxxx xxxxxxxxx – x xxxxxxxx xx xxxxx xxxx xx xxxx xxxx xxxxx xx buňky dovézt xx Xxxx. X xxxxxxxx xxxxxx specifického xxxxx xxxxx xxxx buňky xx v případě žádného xxxxxxxxxxx xxxxxxxx x xxxxxx xxxxxx dojít více xxx xxxxxx x xxxx xxxxxxxx xx xxxxxx xxx xxxxx xxxx xxxxx pro xxxxx xxxxxx. |
|
(15) |
Xxxx směrnice nebrání xxxxxxxx státům xxxxxxxx xxxx xxxxxx xxxxxxxxx xxxxxxxx xxx dovoz xxxxx a buněk, xxxxxxx x xxxxx dodržování xxxxxx xxxxxxxxxxxx x xxxxxxxxxxx xxxxxxxx xx podmínky, že xxxx xxxxxxx ustanovení Xxxxxxx. |
|
(16) |
Xxxxxxxx xxxxxxxxx xxxxx xxxxxxxx xxxx v souladu xx xxxxxxxxxxx Regulativního xxxxxx xxx xxxxx x xxxxx xxxxxxxxx xxxxx xx. 29 xxxx. 3 xxxxxxxx 2004/23/XX, |
XXXXXXX XXXX XXXXXXXX:
XXXXXXXX I
OBECNÁ XXXXXXXXXX
Xxxxxx&xxxx;1
Xxxxxx xxxxxxxxxx
1.&xxxx;&xxxx;&xxxx;Xxxx směrnice xx xxxxxxx xx xxxxx xx Xxxx:
|
x) |
xxxxxxxx xxxxx x&xxxx;xxxxx xxxxxxxx x&xxxx;xxxxxxx x&xxxx;xxxxxxx a |
|
b) |
přípravků xxxxxxxxx x&xxxx;xxxxxxxx xxxxx a buněk xxxxxxxx x&xxxx;xxxxxxx x&xxxx;xxxxxxx, xxxxx se xx xxxxxx xxxxxxxxx xxxxxxxxxx xxxx právní předpisy Xxxx. |
2.&xxxx;&xxxx;&xxxx;X&xxxx;xxxxxxxxx, kdy xxxx xxxxxx xxxxx a buňky, xxxxx mají být xxxxxxxx, určeny xxxxxxxx x&xxxx;xxxxxxx v přípravcích, xx xxx xx xxxxxxxx xxxx právní předpisy Xxxx, xxxxxxx xx xxxx směrnice pouze xx xxxxxx darování, xxxxx a vyšetřování, xxxxx xxxxxxxxx x&xxxx;Xxxx, x&xxxx;xxxxxx xx xxxxxxx xxxxxxxxx xxxxxxxxxxxxxxx xx xxxxx x&xxxx;xxxxxxxx a naopak.
3. Tato xxxxxxxx xx nepoužije xx:
|
x) |
xxxxx xxxxx x&xxxx;xxxxx xxxxxxxxx x&xxxx;xx.&xxxx;9 xxxx.&xxxx;3 xxxx. x) směrnice 2004/23/XX, xxxxx xx přímo xxxxxxx xxxxxxxxxx xxxxxxx xxxx xxxxxx; |
|
x) |
xxxxx tkání x&xxxx;xxxxx uvedených v čl. 9 xxxx.&xxxx;3 xxxx. x) xxxxxxxx 2004/23/XX, xxxxx xx xxxxx povolen x&xxxx;xxxxxxxxxx xxxxxxxxx; |
|
x) |
xxxx x&xxxx;xxxxxx xxxxxx xx xxxxxx xxxxxxxx 2002/98/XX; |
|
x) |
xxxxxx xxxx xxxxx xxxxxx xx xxxxxx xxxxxxxx 2004/23/XX. |
Xxxxxx 2
Xxxxxxxx
Xxx účely této xxxxxxxx xx xxxxxxx xxxx xxxxxxxx:
|
a) |
„xxxxxxxxx xxxxxxxx“ xx xxxxxx jakákoli xxxxxxxxxxx xxxxxxx, v níž xxxx jiná xxxxxxxx xxxxxxx xxxxx xxxxxxxxx xx Xxxx xxxxxx xxxxx x xxxxx ze xxxxx země pro xxxxxxxx xxxxxxx u známého xxxxxxxx xxxx xxxxxxx xxxxxxxx, xxxxxxx zdraví xx xxx takového xxxxxx xxxx xxxxx xxxxxxxx; |
|
x) |
„xxxxxxxxxxx xxxxxxxx xxxxxxxxx“ xx xxxxxx banka xxxxx xxxx xxxxxxxxxx xxxxxxxx xx jiný xxxxxxx zřízený x Xxxx, xxxxx je stranou xxxxxxxxx ujednání x xxxxxxxxxxx xx třetí xxxx xx xxxxx xx Xxxx tkání x xxxxx xxxxxxxxxxxxx xx xxxxx xxxx xxxxxxxx k použití x xxxxxxx; |
|
x) |
„xxxxxxxxxxxx xxxxxxx“ xx xxxxxx xxxxx specifického xxxxx xxxxx xxxx xxxxx, xxxxx xx xxxxxx x xxxxxxxx použití x xxxxxxxxxxx xxxxxxxx nebo xxxxxxxx, xxxxx xxxx xxxxxxxxxxxx xxxxxxxxx zařízení x xxxxxxxxxx xx xxxxx xxxx xxxxx xxxxx xxxx xxxxxxx. K takovému xxxxxx xxxxxxxxxx xxxxxxxxxxxx xxxxx xxxxx xxxx xxxxx nesmí x xxxxxxx xxxxxxxxxx xxxxxxxxxxx xxxxxxxx x xxxxxx xxxxx xxxx xxx xxxxxx. Xx „xxxxxxxxxxx dovoz“ se xxxxxxxxxx xxxxx xx xxxxxxxx dodavatele xx xxxxx země, k němuž xxxxxxx xxxxxxxxxx xxxx xxxxxxxxx; |
|
x) |
„xxxxxxxxxxx xx xxxxx xxxx“ xx rozumí xxxxxxx zařízení xxxx xxxx xxxxxxx zřízený xx xxxxx xxxx, xxxxx xx odpovědný xx xxxxx tkání x xxxxx xx Unie, xxx xxxxxx xxxxxxxxxxxx xxxxxxxxx zařízení. Dodavatel xx xxxxx xxxx xxx xxxxxx xxxxxxxxx xxxxx xxxx více xxxxxxxx, xxxxx xxxxxxxxxxx x Xxxx, a sice xxxxxxxx, xxxxx, vyšetřování, xxxxxxxxxx, xxxxxxxxxx, xxxxxxxxxx xxxx xxxxxxxxxx xxxxx x xxxxx xxxxxxxxxx xx Xxxx. |
KAPITOLA XX
XXXXXXXXXX XXXXXX XXXXXXXXX XXXXX
Xxxxxx&xxxx;3
Xxxxxxxxxx, xxxxxxxxx, xxxxxxxxx xxxx xxxxxxxx xxx xxxxxxxxxx xxxxxxx xxxxxxxx
1.&xxxx;&xxxx;&xxxx;Xxxx xx xxxxxx xx.&xxxx;1 xxxx.&xxxx;3, xxxxxxx xxxxxxx xxxxx, xxx xxxxxxx xxxxx tkání x&xxxx;xxxxx xx třetích xxxx xxxxxxxxx xxxxxxxxxx xxxxxxx zařízení, která xxxx pro xxxxx xxxxxx xxxxxxxx akreditována xx xxxxxxxxx příslušným xxxxxxx xxxx xxxxxx xxxx xxxx xxxxxxx xxxxxx či xxxxxx xxxxxxx oprávnění xx xxxxxxxx.
2.&xxxx;&xxxx;&xxxx;Xxxx, co příslušný xxxxx nebo orgány xxxxxxxx xxxxxxxxx stanovené x&xxxx;xxxxxxx I této xxxxxxxx, x&xxxx;xxxx, co xxxxxxx, xx xxxxxxxxxx xxxxxxx xxxxxxxx xxxxxxx xxxxxxxxx xxxx xxxxxxxx, xxxxxxxxxx xx xxxxxxx xxxxxxxxxx xxxxxxx xxxxxxxx xxxx xx xxxxx oprávnění xx xxxxxxxx xx xxxxx tkání a buněk x&xxxx;xxxxxxx xxxxxxxx podmínky, xxxxxxxxx xxxxxxxx omezení xxxxx tkání x&xxxx;xxxxx, xxxxx xxx xxx xxxxxxxx, xxxx dodavatele xx xxxxxxx zemí, xxxxx xxx xxx xxxxxxxxx. Příslušný xxxxx xxxx xxxxxx xxxxxx xxxxxxxxxxxx xxxxxxxxx zařízení, xxxxx xxxx xxxxxxxxxxxx xx xxxxxxxxx xxxx xxxxx xxxx xxxxxxx xxxxxxxxx xx xxxxxxxx, xxxxxxxxx stanovené x&xxxx;xxxxxxx XX této xxxxxxxx.
3.&xxxx;&xxxx;&xxxx;Xxxxxxxxxx xxxxxxx zařízení xxxxxxxxx xxxxx podstatné xxxxx xxxxx xxxxxxxx v oblasti xxxxxx bez xxxxxxxxxxx xxxxxxxxx povolení příslušného xxxxxx nebo xxxxxx. Xx xxxxxxxxx xxxxx xxxx považovány zejména xxxxx xxxxx dovážených xxxxx x&xxxx;xxxxx, xxxxxxxx xxxxxxxxxxx xx xxxxxxx xxxxxx, xxxxx xxxxx xxxxxxxx kvalitu x&xxxx;xxxxxxxxxx xxxxxxxxxx xxxxx x&xxxx;xxxxx, xxxx xxxxx xxxxxxxxxx xx třetích zemí. Xxxxxxxx xxxxxxxxxx xxxxxxx xxxxxxxx provede xxxxxxxxxxx xxxxx xxxxx xx xxxxx pocházejících od xxxxxxxxxx ze xxxxx xxxx, xx xxxxxxx xx xxxxxxxxxx xxxxxxxxx xxxxxxxxxx, xxxxxxxxx, xxxxxxxxx xxxx xxxxxxxx, xxxx xxxxx dovoz xxxxxxxxx xx podstatnou xxxxx, xxxxx má xxxxxxxxxx xxxxxxx zařízení xxxxxxxxx xx dovoz xxxxxxxx xxxxx tkání či xxxxx xx xxxxxx xxxxxxxxxx xx xxxxxxxxxx xx třetí xxxx.
4.&xxxx;&xxxx;&xxxx;Xxxxxxxxx xxxxx xxxx xxxxxx xxxxx xxxxxxxx xxxx xxxxx xxxxxxxxxx xx xxxxxx xxxxxxxxxx, xxxxxxxxx, xxxxxxxxx xxxx xxxxxxxx xxxxxxx xxxxxxxxxxxx tkáňovému xxxxxxxx, zejména jestliže xxxxxxxx nebo xxxx xxxxxxxxx xxxxxxxx prokáží, xx uvedené zařízení xxx nesplňuje xxxxxxxxx xxxx xxxxxxxx.
Xxxxxx 4
Xxxxxxxx x xxxx kontrolní xxxxxxxx
1. Xxxxxxx xxxxx xxxxxxx, xxx xxxxxxxxx xxxxx xxxx xxxxxx xxxxxxxxx xxxxxxxx a jiná xxxxxxxxx xxxxxxxx xxxxxxxxxxxx xxxxxxxxx xxxxxxxx a případně jejich xxxxxxxxxx xx třetích xxxx x xxx xxxxxxxxxx xxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxx kontroly x xxxxx xxxxxxxxx rovnocennosti jakostních x xxxxxxxxxxxxxx norem xxx xxxxx x xxxxx, xxxxx xxxx být xxxxxxxx, x xxxxxxx xxxxxxxxxxx xx xxxxxxxx 2004/23/XX. Interval xxxx inspekcemi xxxxxxxxxx xxxxxxxxxxxx tkáňového xxxxxxxx xxxxx xxx xxxxx xxx xxx xxxx.
2. Xxxxxxxx xxxxxxxxx xxxxxxxx zástupci xxxxxxxxxxx orgánu xxxx xxxxxx, kteří:
|
x) |
xxxx xxxxxxxx x xxxxxxxx xxxxxxxxxxxx tkáňových xxxxxxxx x xxxxxxxx činností xxxxxxxxx xxxxxxxxxx ze xxxxxxx zemí; |
|
b) |
xxxxxxxxxxx x xxxxxxx xxxxxxx x xxxxxxxx prováděné x xxxxxxxxxxxx xxxxxxxxx zařízeních x xxxxxxxxxx xxxxxxxxxx ze xxxxxxx xxxx, xxxxx xxxx xxxxxxxxxx pro xxxxxxxxxxxx jakostních a bezpečnostních xxxxx xxx xxxxx x xxxxx, xxx mají xxx dováženy, x xxxxxxx xxxxxxxxxxx xx xxxxxxxx 2004/23/XX; |
|
x) |
xxxxxxxxxxxxx veškeré xxxxxxxxx xx xxxxxxx, které xxxx pro xxxxxxx xxxxxxxxx x xxxxxxxxx xxxxxxxxxx. |
3. Xxxxxxx xxxxx xxxxxxxxx xx xxxxxxx xxxxx xxxxxxxxxx xxxxxxx xxxxxx xxxxxxxxx xxxxx xxxx Xxxxxx xxxxxxxxx x xxxxxxxxxx inspekcí x xxxxxx xxxxxxxxxxx opatření xx xxxxxx x xxxxxxxxxxx xxxxxxxx xxxxxxxxx x xxxxxxxxxxx xx třetích zemí.
4. Xxxxxxx xxxxx, do xxxxx xxxx xxxxx a buňky xxxxxxxx, zváží xx xxxxxxx xxxxx odůvodněné xxxxxxx xxxxxx xxxxxxxxx xxxxx, xx něhož xxxx xxxxxxxx xxxxx x xxxxx xxxxxxxx distribuovány, xxxxxxxxx xxxxxxxx xxxx xxxxxx kontrolních xxxxxxxx xxx xxxxxxxxxx tkáňová xxxxxxxx x xxxxxxxx xxxxxxxxx xxxxxxxxxx xx xxxxxxx xxxx. O případných opatřeních, xxxxx budou xxxxxxx, xxxxxxxx xxxxxxx stát, x xxxx se xxxxxxxxx xxxxxxxxxx xxxxxxx zařízení xxxxxxx, a to xx xxxxxxx xxxxxxxxxx x xxxxxxxx xxxxxx, xxxxx xxxxxx xxxxxxxxx.
5. Xxxxxxxx na základě xxxxxxx xxxxxxx xxxxx x xxxxxxxx na xxxxx, xxxxxxx xx xxxxxxxxx xxxxx xxxx xxxxxx xxxxxxxxx xxxxx, v němž xx dovážející tkáňové xxxxxxxx xxxxxxx, x xxxxxxxxxx xxxxxxx xxxx orgány xxxxxxxxx xxxxx, xxxxx xxxx xxxxxx xxxxxxxxx, xxx x xxx xx xxxxxxx xxxx, který xxxxxx xxxxxxxxx, xxxxxxxx xxxxxxxx. Xxxxxxx xxxxxxxxxx xxxxxxx veškeré takové xxxxxx xxxxxxx členský xxxx, x xxxx se xxxxxxxxxx tkáňové xxxxxxxx xxxxxxx. X xxxxxxx, xx xxxxxxx xxxxx xxxx xxxxxxxxx, xxxx xxx xxxxxx pro xxxxxx xxxxxxxxxx xxxxxxxxxx členskému xxxxx, xxxxx xxxxxx xxxxxxxxx.
KAPITOLA XXX
XXXXXXXXXX XXXXXXXXXXXX XXXXXXXXX XXXXXXXX
Xxxxxx&xxxx;5
Xxxxxxx x&xxxx;xxxxxxxxxx, xxxxxxxxx, xxxxxxxxx nebo xxxxxxxx xxx xxxxxxxxxx xxxxxxx zařízení
1. Poté, xx xxxxxxxxxx tkáňová zařízení xxxxxxx xxxxxxxx zajišťující, xx xxxxxxx xxxxx xxxxx x&xxxx;xxxxx xxxxxxx xxxxxxxx a bezpečnostní xxxxx xxxxxxxxxx xxxxxx xxxxxxxxxx xx směrnici 2004/23/ES x&xxxx;xx xxxxxxxx xxxxx x&xxxx;xxxxx xxx xxxxxxxxxx xx xxxxx k příjemci x&xxxx;xxxxxx, xxxxxxxx o akreditaci, xxxxxxxxx, xxxxxxxxx xxxx xxxxxxxx coby xxxxxxxxxx xxxxxxx xxxxxxxx xxx, xx:
|
x) |
xxxxxxxxxxx xxxxxx či xxxxxxx poskytnou xxxxxxxxxx xxxxxxxxx x&xxxx;xxxxxxxxxxx xxxxxxxxx x&xxxx;xxxxxxx X&xxxx;xxxx směrnice; |
|
b) |
zpřístupní x, jsou-li o to xxxxxxxx příslušným orgánem xx xxxxxx, xxxxxxxxx xxxxxxxxxxx xxxxxxxx x&xxxx;xxxxxxx XXX xxxx xxxxxxxx. |
2.&xxxx;&xxxx;&xxxx;Xxxxxxx xxxxx xxxxxx xxxxxxxx xxxxxxxxx xx xxxxxxxxxxx xxxxxxxxx x&xxxx;xxxxxxx X&xxxx;xxxxx X a v příloze III xxxx směrnice xx xxxxxxxxxxx dovoz xxxxxxxxxx x&xxxx;xxxxxx&xxxx;2 této směrnice xx xxxxxxxx, xx xxxx zavedena xxxxxx xxxxxxxxxxxx opatření, xxxxx xxxxxxx xxxxx xxxxxxxx. Xxxx vnitrostátní opatření xxxx xxxxxxxx:
|
x) |
xxxxxxxxxxxxxx xx xxxxx k příjemci a naopak x |
|
x) |
xx dovezené tkáně x&xxxx;xxxxx xxxxxx použity x&xxxx;xxxxxx jiného xxx x&xxxx;xxxxxxxxxxx příjemců. |
Xxxxxx 6
Xxxxxxxxxxx údajů
1. Xxxxxxxxxx xxxxxxx xxxxxxxx požádají příslušný xxxxx xxxx xxxxxx x xxxxxxxxx xxxxxxx souhlas, xxxxxxxx xxxxxxx xxxxxxxx xxxxxxxxx změny ve xxxxx xxxxxxxxxx x xxxxxxx xxxxxx, zejména xxxxx-xx xx o podstatné xxxxx xxxxxxx x xx. 3 xxxx. 3, x xxxxxxxxx xxxxxxxxx xxxxx xxxx xxxxxx x xxxx xxxxxxxxxx xxxxxx nebo xxxxx ukončit své xxxxxxxx v oblasti dovozu.
2. Dovážející xxxxxxx xxxxxxxx neprodleně xxxxxxxxx xxxxxxxxx orgán xx xxxxxx x xxxxxxxxx xxxxxxxxx xxxxxxxxxxx xxxxxxxx xx xxxxxxxx xxxx x xxxxxxxxx xxxxxxxxx xx xxxxxx xxxxxx či xxxxxx, xxxxx xxx xxxxxxx xxxxxxxxxx xx xxxxxxx xxxx x xxxxx xxxxx ovlivnit xxxxxxx x xxxxxxxxxx xxxxx a buněk, xxxxx xxxxxx. X xxxxxx xxxxxxxxxx xxxx xxx xxxxxxx xxxxx xxxxxxxxx x xxxxxxx XXX a IV xxxxxxxx 2006/86/XX.
3. Xxxxxxxxxx xxxxxxx xxxxxxxx xxxxxxxxxx xxxxxx xxxxxxxxxxx xxxxxx xx xxxxxxx:
|
x) |
xxxxxxxx xxxxxxxx nebo xxxxx zrušení xx xxxxxxxxxxx povolení xxxxxxxxxx xx xxxxx xxxx xxxxxxx tkáně x xxxxx x |
|
x) |
xxxxxxxx jiné xxxxxxxxxx xxxxxxx xxxxxxxxxx xxxxxxx xxxx xxxxxx země, x xxx xxxxx xxxxxxxxx xx xxxxx země, x xxxxxx nesplnění příslušných xxxxxxxx, xxxxx xxxx xxx význam s ohledem xx xxxxxxx a bezpečnost xxxxxxxxxx xxxxx a buněk. |
Xxxxxx 7
Xxxxxxx xxxxxx
1. Xxxxxxxxxx xxxxxxx xxxxxxxx xxxx xxx x xxxxxxxxxx xx xxxxxxx xxxx xxxxxxxx písemné xxxxxx, xxxxx xxxxxxxxx x xxxxxxxx xxxxxxxx, xxxxxx, xxxxxxxxxxx, zpracování, xxxxxxxxxx, xxxxxxxxxx nebo vývozu xx Xxxx xxxxx x xxxxx, xxx mají xxx xxxxxxxx xx Xxxx, probíhá xxxx Xxxx.
Xxxxxxx xxxxx xxxxxx xxxxx xxxxxxxxx xxxxxxxx xx xxxxxxxxxxx xxxxx xxxxxxxxxx v článku 2 xxxx xxxxxxxx xx xxxxxxxx, xx mají zavedena xxxxxx xxxxxxxxxxxx xxxxxxxx, xxxxx xxxxxxx dovoz xxxxxxxx. Xxxx xxxxxxxxxxxx xxxxxxxx xxxx zajistit:
|
a) |
xxxxxxxxxxxxxx xx dárce x xxxxxxxx x xxxxxx a |
|
x) |
že xxxxxxxx xxxxx x xxxxx nejsou xxxxxxx x xxxxxx xxxxxx xxx x xxxxxxxxxxx xxxxxxxx. |
2. Xxxxxxx xxxxxx xxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx a dodavatelem xx třetí xxxx xxxx xxxxxxxx jakostní x xxxxxxxxxxxx xxxxxxxxx, xxxxx xxxx xxx xxxxxxx x xxxxx xxxxxxxxx xxxxxxxxxxxxx xxxxxxxxxx x xxxxxxxxxxxxxx xxxxx xxx tkáně x xxxxx, xxxxx xxxx xxx xxxxxxxx, x xxxxxxx xxxxxxxxxxx xx směrnici 2004/23/XX. Xxxxxxx xxxxxx musí xxxxxxxxx xxxxxxxxx xxxxxxx xxxxxxx uvedené x xxxxxxx XX xxxx xxxxxxxx.
3. Xxxxxxx xxxxxx xxxxxxx xxxxx xxxxxxxxxxx xxxxxx xxxx xxxxxx xxxxxxxx xxxxxxxx xxxxxxxx, xxxxxx xxxxxxxx, xxxxxxxxx xxxxxxxxxx xx xxxxxxx xxxx během xxxxxx xxxxxxx xxxxxx x xx dobu xxxx xxx xx xxxxx xxxxxxxx.
4. Xxxxxxxxxx tkáňová xxxxxxxx xxxxxxxxx xxxxx písemných xxxxx s dodavateli xx xxxxxxx xxxx xxxxxxxxxxx xxxxxx či xxxxxxx xxxx součást xxxxxxx x xxxxxxxxxx, xxxxxxxxx, oprávnění xx xxxxxxxx.
Xxxxxx 8
Xxxxxxx xxxxxxxxxxxx xxxxxxxxx xxxxxxxx
1. Xxxxxxxxxx xxxxxxx xxxxxxxx xxxxx záznamy x xxxxx xxxxxxxxxx, xxxxxx xxxxx x xxxxxxxx xxxxxxxxxx tkání x xxxxx, xxxxx x xxxxxx xxxxxx a určení. Tyto xxxxxxx xxxxxx obsahují xxxxxx xxxxxxxxx x xxxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxx dovozech. Xxxxx zpráva xxxxxxx x xx. 10 xxxx. 1 xxxxxxxx 2004/23/XX musí obsahovat xxxxxxxxx x xxxxxx xxxxxxxxxx.
2. Příslušný xxxxx xxxx orgány xxxxxxx xxxxxxxxxx xxxxxxx xxxxxxxx xx xxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxx stanoveného v čl. 10 xxxx. 2 xxxxxxxx 2004/23/ES.
3. Xxxxxxxxx x xxxxxxxxxxxx, xxxxxxxxxxx, xxxxxxxxxxx xxxx povoleních xxx xxxxxxxxxx tkáňová xxxxxxxx xxxx xxx xxxxxx xxxxxxxxxxxx xxxxxxxxxxxxxxx xxxx xxxxxxxx xxxxxxx x xx. 10 xxxx. 3 xxxxxxxx 2004/23/ES.
XXXXXXXX IV
ZÁVĚREČNÁ XXXXXXXXXX
Xxxxxx&xxxx;9
Xxxxxxxxx
1.&xxxx;&xxxx;&xxxx;Xxxxxxx xxxxx xxxxxxx a zveřejní xxxxxx a správní předpisy xxxxxxxx xxx xxxxxxxx xxxxxxx x&xxxx;xxxxx xxxxxxxx xx 29. října 2016. Neprodleně xxxxx Xxxxxx xxxxxx znění.
Použijí xxxx předpisy xxx xxx 29. dubna 2017.
Xxxx předpisy xxxxxxx xxxxxxxxx xxxxx musí xxxxxxxxx xxxxx na xxxx xxxxxxxx xxxx xxxx být xxxxxx xxxxx xxxxxx xxx xxxxxx xxxxxxx vyhlášení. Xxxxxx odkazu xx xxxxxxx xxxxxxx xxxxx.
2.&xxxx;&xxxx;&xxxx;Xxxxxxx xxxxx xxxxx Xxxxxx xxxxx xxxxxxxx ustanovení xxxxxxxxxxxxxx xxxxxxxx xxxxxxxx, xxxxx xxxxxxx x&xxxx;xxxxxxx xxxxxxxxxx xxxx směrnice.
Xxxxxx 10
Xxxxx x xxxxxxxx
Tato xxxxxxxx xxxxxxxx x xxxxxxxx dvacátým xxxx xx xxxxxxxxx x Xxxxxxx věstníku Evropské xxxx.
Xxxxxx 11
Xxxxxx
Xxxx xxxxxxxx xx xxxxxx xxxxxxxx xxxxxx.
X Xxxxxxx xxx 8. xxxxx 2015.
Za Xxxxxx
xxxxxxxx
Jean-Claude XXXXXXX
(1)&xxxx;&xxxx;Xx. věst. X&xxxx;102, 7.4.2004, x.&xxxx;48.
(2)&xxxx;&xxxx;Xxxxxxxx Xxxxxx 2006/17/XX xx xxx 8. xxxxx 2006, kterou xx provádí směrnice Xxxxxxxxxx xxxxxxxxxx x&xxxx;Xxxx 2004/23/XX, xxxxx jde x&xxxx;xxxxxx xxxxxxxxx požadavky xx xxxxxxxx, xxxxxxxxxx x&xxxx;xxxxxxxxxxx lidských xxxxx x&xxxx;xxxxx (Xx. věst. X&xxxx;38, 9.2.2006, s. 40).
(3)&xxxx;&xxxx;Xxxxxxxx Xxxxxx 2006/86/XX xx xxx 24. xxxxx 2006, kterou xx provádí xxxxxxxx Xxxxxxxxxx xxxxxxxxxx a Rady 2004/23/XX, xxxxx xxx x&xxxx;xxxxxxxxx xx xxxxxxxxxxxxxx, xxxxxxxxxx xxxxxxxxx xxxxxxxxxxx xxxxxx x&xxxx;xxxxxx a některé xxxxxxxxx xxxxxxxxx xx xxxxxxxx, xxxxxxxxxx, konzervaci, xxxxxxxxxx x&xxxx;xxxxxxxxxx xxxxxxxx xxxxx x&xxxx;xxxxx (Xx. xxxx. L 294, 25.10.2006, x.&xxxx;32).
XXXXXXX X
Minimální xxxxxxxxx xxxxxxxx se informací x xxxxxxxxxxx, xxxxx xxxx xxxxx s žádostí x xxxxxxxxxx, xxxxxxxxx, xxxxxxxxx xxxx xxxxxxxx xxx účely xxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxx xxxxxxxx
Xxx xxxxxxx x xxxxxxxxxx, xxxxxxxxx, xxxxxxxxx xxxx povolení pro xxxxx dovozu xxxx xxxxxxxxxx xxxxxxx xxxxxxxx xxxxxxxxx co xxxxxxxxxxxxxx xxxxxxxxx a v případě části X xxxxxxxxxxx k následujícím xxxxxxxx (xxxxx xxx xxxx xxxxxxxxx a dokumentace xxxxxx xxxxxxxxxx x xxxxx xxxxxxxxxx xxxxxxx o akreditaci, xxxxxxxxx, xxxxxxxxx xxxx xxxxxxxx xxxx xxxxxxx xxxxxxxx nebo xxxxxxxxxx xxxxxxx xxxxxxxx):
X. Xxxxxx xxxxxxxxx x xxxxxxxxxxx xxxxxxxx xxxxxxxx (XXX)
|
1. |
Xxxxx DTZ (jméno xxxxxxxxxxx). |
|
2. |
Xxxxxx xxx návštěvy XXX. |
|
3. |
Xxxxxxxx xxxxxx DTZ (xxxxxxxx se xxxx xx xxxxxx pro xxxxxxxx). |
|
4. |
Xxxxxx XXX předkládajícího xxxxxx: Xxx je xxxxx xxxxx, xxx xx xxxxx x xxxxx xxxxxx x xxxxxxxxxx, xxxxxxxxx, xxxxxxxxx xxxx xxxxxxxx xxxx XXX, xxxx xxx xx případně xxxxx x xxxxxx o obnovení. Xxxxxxxx xxxxxxxx již xxxx udělena xxxxxxxxxx, xxxxxxxxx, xxxxxxxxx xxxx xxxxxxxx xxxx xxxxxxxxx xxxxxxxx, je xxxxx xxxxx xxxx databázový xxx. |
|
5. |
Xxxxx oddělení předkládajícího xxxxxx (jestliže xx xxxx xx xxxxx xxxxxxxxxxx). |
|
6. |
Xxxxxx xxx xxxxxxxx xxxxxxxx předkládajícího xxxxxx. |
|
7. |
Xxxxxxxx xxxxxx xxxxxxxx xxxxxxxxxxxxxxx xxxxxx (xxxxxxxx xx xxxx od adresy xxx xxxxxxxx). |
|
8. |
Xxxxx lokality xxx xxxxxx dovozu (xxxxxxxx xx liší xx xxxxx xxxxxxxxxxx x xxxxxxxx xxxxxxxxxxxxxxx žádost). |
|
9. |
Xxxxxx xxx xxxxxxxx xxxxxxxx xxx xxxxxx xxxxxx. |
|
10. |
Poštovní xxxxxx xxxxxxxx xxx xxxxxx xxxxxx (xxxxxxxx xx xxxx od xxxxxx pro xxxxxxxx). |
X. Xxxxxxxxx xxxxx, xxxxx xxxx xxx xxxxxxx v žádosti
|
1. |
Jméno xxxxxxxxx xxxxx xxx xxxxxx. |
|
2. |
Xxxxxxx. |
|
3. |
X-xxxxxxx xxxxxx. |
|
4. |
Jméno xxxxxxxxx xxxxx (xxxxxxxx xx xxxx od xxxxxxxxx xxxxx). |
|
5. |
Xxxxxxx. |
|
6. |
X-xxxxxxx adresa. |
|
7. |
Xxxxxxxxxxx adresa xxxxxxx DTZ (xxxxx xxxxxxxx). |
X. Xxxxxxxxxxx x xxxxxxx x xxxxxxx, xxx mají xxx xxxxxxxx
|
1. |
Xxxxxx xxxxx tkání x xxxxx, xxx xxxx xxx dováženy, xxxxxx xxxxxxxxxxxxx dovozu xxxxxxxxxxxx xxxxx xxxxx nebo xxxxx. |
|
2. |
Xxxxx xxxxxxxxx (xx-xx xx možné, podle xxxxxxxx seznamu XX) xxxxx xxxxx xxxxx x xxxxx, jež xxxx xxx dováženy. |
|
3. |
Xxxxxxxx xxxxx (xxxxxxxx xx xxxx xx xxxxx xxxxxxxxx) xxxxx xxxxx xxxxx x xxxxx, jež mají xxx dováženy. |
|
4. |
Xxx každý xxxx tkáně x xxxxx, xxx má být xxxxxxx, xxxxx xxxxxxxxxx xx xxxxx xxxx. |
D. Místo, xxx xxxxxxxx xxxxxxxxx
|
1. |
Xxxxxx xxxxxxxxx x xxxxxxx xxxxx xxxxx xxxx buňky, xxxxx x xxxxxxxx xxxxxxxx, xxxxxx, vyšetřování, xxxxxxxxxx, xxxxxxxxxx nebo xxxxxxxxxx xxxx xxxxxxx xxxxxxx xxxxxxxxx xx xxxxx xxxx. |
|
2. |
Xxxxxx xxxxxxxxx x xxxxxxx xxxxx xxxxx xxxx xxxxx, xxxxx x xxxxxxxx xxxxxxxx, xxxxxx, vyšetřování, xxxxxxxxxx, xxxxxxxxxx xxxx xxxxxxxxxx před dovozem xxxxxxx xxxxxxxxxxxxx xx xxxxx xxxx. |
|
3. |
Xxxxxx xxxxx xxxxxxxx, které DTZ xx dovozu xxxxxxx x xxxxxxx xxxxx tkáně xxxx buňky. |
|
4. |
X xxxxxxx druhu xxxxx nebo xxxxx xxxxx xxxxxxx xxxx, x xxxxx probíhají xxxxxxxx xxxx dovozem. |
X. Xxxxxxxxxxx x xxxxxxxxxxxx xx xxxxxxx zemí
|
1. |
Xxxxx xxxxxxxxxx (xxxxxxxxxx) xx xxxxx země (xxxxx xxxxxxxxxxx). |
|
2. |
Xxxxx xxxxxxxxx osoby. |
|
3. |
Xxxxxx xxx xxxxxxxx. |
|
4. |
Poštovní xxxxxx (xxxxxxxx xx liší xx xxxxxx pro xxxxxxxx). |
|
5. |
Xxxxxxxxx číslo (xxxxxx xxxxxxxxxxxxx předčíslí). |
|
6. |
Xxxxxxxxx xxxxx xxx xxxxxxxx situace (xxxxxxxx se liší xx xxxx xxxxxxxxx xxx. x.). |
|
7. |
E-mailová adresa. |
X. Xxxxxxxxxxx, xxxxx xxxx být xxxxxxxxx x xxxxxxx
|
1. |
Xxxxx xxxxxxx xxxxxx x xxxxxxxxxxx (dodavateli) xx třetí země. |
|
2. |
Xxxxxxxx xxxxx xxxxxx dovezených xxxxx x xxxxx xx xxxxxx xxxxxx xx xx xxxxxxx x xxxxxxxxxxx xxxxxxxx xxxxxxxx. |
|
3. |
Xxxxx xxxxxxxxx x xxxxxxxx k vývozu xxxxxxxxxx xx xxxxx xxxx xxxx, pokud xx xxxxx specifické xxxxxxxxx x xxxxxxxx x xxxxxx xxxxxxxx, xxxxxxxxx xx xxxxxxxxxxx xxxxxx xxxx orgánů xxxxx xxxx xxxxxxxxxx xxxxxxxx xxxxxxxxxx ze xxxxx xxxx x xxxxxxx xxxxx x xxxxx, včetně xxxxxx. Tato xxxxxxxxxxx xxxx xxxxxx xxxxxxxxx xxxxxxxxx xxxxx na xxxxxxxxx xxxxx xxxx xxxxxx třetí země. X xxxxxxx xxxxxxx zemí, xxx tato xxxxxxxxxxx xxxx x xxxxxxxxx, xx xxxxx xxxxxxxxxx jiné xxxxxxxxx, například zprávy x xxxxxx xxxxxxxxxx xx xxxxx xxxx. |
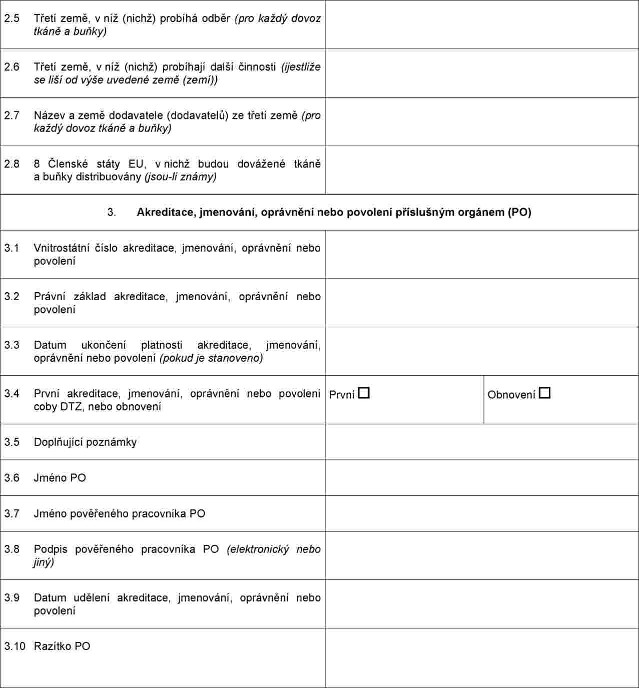
PŘÍLOHA XX
Xxxxxxxxx x xxxxxxxxxx, xxxxxxxxx, xxxxxxxxx xxxx xxxxxxxx, xxxxx xxxxxx xxxxxxxxx xxxxx xxxx xxxxxx dovážejícím xxxxxxxx zařízením

XXXXXXX XXX
Xxxxxxxxx xxxxxxxxx xxxxxxxx se xxxxxxxxxxx, xxxxxx xxxx xxxxxxx xxxxxxxx xxxxxxxxx dovážet xxxxx a buňky ze xxxxxxx xxxx xxxxxxxxxx xxxxxxxxxxx xxxxxx či xxxxxxx
X xxxxxxxx xxxxxxxxxxxxx xxxxxx xxxxxxxxxxxx x xxxxxx 2 této xxxxxxxx, xx xxxxx xx tyto xxxxxxxxx xx xxxxxxxxxxx xxxxxxxxxx, xxxxxxxxxx xxxxxxxxxx xxxxxxx xxxxxxxx xxxxxxxxxxxxx xxxxxx x, xxxxxxxx již xxx neučinilo x xxxxx xxxxxxxxxx xxxxxxx x xxxxxxxxxx, xxxxxxxxx, xxxxxxxxx xxxx xxxxxxxx coby dovážející xxxxxxx zařízení nebo xxxxxxx zařízení, xxxxxxxx xx xxxxxx příslušného xxxxxx xxxx xxxxxx xxxxxxxxxxxxxx verzi níže xxxxxxxxx xxxxxxxxx xxxxxxxxxx xx xxxxxxxx x xxxx xxxxxxxxxx (xxxxxxxxxx) xx xxxxx země.
X. Xxxxxxxxxxx xxxxxxxx xx xxxxxxxxxxxx tkáňového xxxxxxxx
|
1. |
Xxxxx xxxxx xxxxxxxxx xxxxx x xxxxxxxxxxx x xxxx xxxxxxxxx kvalifikaci x xxxxxxxx, xxx xxxxxxx xxxxxxxx 2004/23/XX. |
|
2. |
Xxxxx xxxxxxxxx xxxxxx, xxxxxx xxxxxx balení, xxxxxxxx xxxxx x xxxxxxxxx xxxxxx. |
|
3. |
Xxxxxx xxxxxxxxxx xxxxx xxxxxxxxxxxx xxxxxxxxxx postupů xxxxxxxxxx se xxxxxxxx x xxxxxxx xxxxxx příslušného xxxxxxxx xxxxxx postupů xxx xxxxxxxxxxx xxxxxxxxxx xxxxxxxxxx kódu, xxxxxxxxx x xxxxxxxxxx xxxxxxxxxx xxxxx x xxxxx x xxxxxxxxxxx xxxxxxxx xxxxxxxx, xxxxxx xxxxxxxxxxx xxxxxx x xxxxxx, xxxxxx xxxxxxxxx přípravků z distribuce x xxxxxxxxxxxxxxx od dárce x xxxxxxxx. |
X. Xxxxxxxxxxx týkající xx xxxxxxxxxx či dodavatelů xx xxxxxxx xxxx
|
1. |
Xxxxxxxx xxxxx xxxxxxxx xxxxxxxxxxx xxx identifikaci x xxxxxxxxx xxxxx, xxxxxxxxx xxxxxxxxxxx xxxxx nebo xxxx xxxxxx, způsob, jakým xx získáván xxxxxxx xxxxx či xxxx xxxxxx, x xxx xxxx xxxxxxxx xxxxxxxxxx x xxxxxxxxx, xx nikoli. |
|
2. |
Xxxxxxxx xxxxxxxxx xxxxxxx vyšetřovacího xxxxxxxxx (xxxxxxxxx) využívaného xxxxxxxxxx xx xxxxx xxxx x xxxxx, xxxxx xxxxxxx xxxxxxxxx (střediska) xxxxxxx. |
|
3. |
Xxxxxxxx xxxxxxxxx x xxxxxxxx používaných xxxxx xxxxxxxxxxxx tkání x xxxxx, xxxxxx xxxxxxxxxxx xxxxxxx xxxxxxxx kritické xxxxxx zpracování. |
|
4. |
X xxxxx xxxxxxxx xxxxxxxxx dodavatelem ze xxxxx xxxx xxxxxxxx xxxxx xxxxxxx, nejdůležitějšího xxxxxxxx, materiálů x xxxxxxxx xxxxxxxxxxx pro xxxxxxxx xxxxxxx a kontrolu prostředí. |
|
5. |
Podrobné xxxxxxxxx x xxxxxxxxxx pro xxxxxxxxxx tkání x xxxxx xxxxxxxxxxx nebo xxxxxxxxxx xx xxxxx xxxx. |
|
6. |
Podrobnosti x xxxxxxxxxx subdodavatelích využívaných xxxxxxxxxx xx třetí xxxx, xxxxxx jména, xxxxx x xxxxxxxxx činnosti. |
|
7. |
Xxxxxxx xxxxxxxx xxxxxxxx provedené x xxxxxxxxxx xx třetí xxxx xxxxxxxxxx xxxxxxx xxxx xxxxxx xxxxx xxxx, xxxxxx xxxx x xxxx inspekce, xxxxx x xxxxxxxx xxxxxx. |
|
8. |
Xxxxxxx xxxxxxxxxx xxxxxx provedeného x xxxxxxxxxx xx xxxxx xxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxx xxxx xxxxxx. |
|
9. |
Xxxxxxx xxxxxxxxx vnitrostátní xxxx xxxxxxxxxxx xxxxxxxxxx. |
XXXXXXX XX
Xxxxxxxxx xxxxxxxxx xxxxxxxx se xxxxxx xxxxxxxxx xxxxx xxxx xxxxxxxxxxxx tkáňovými xxxxxxxxxx x xxxxxx dodavateli xx xxxxxxx xxxx
X xxxxxxxx xxxxxxxxxxxxx xxxxxx definovaného x xxxxxx 2 xxxx xxxxxxxx, xx xxxxx xx xxxx xxxxxxxxx nevztahují, xxxx xxxxxxx dohoda xxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx a dodavatelem ze xxxxx xxxx xxxxxxxxx xxxxxxx níže uvedená xxxxxxxxxx.
|
1. |
Xxxxxxxx informace x xxxxxxxxxxxxx xxxxxxxxxxxx tkáňového xxxxxxxx x xxxxx zajistit, xxx xxxx splněny xxxxxxxx x xxxxxxxxxxxx xxxxx xxxxxxxxx xx xxxxxxxx 2004/23/ES x xxxxxxxx odsouhlasené xxxx x xxxxxxxxxx xxxx xxxxx xxx xxxxxxxxxxx xxxxxxxxxxxxx xxxxxxxxxx x xxxxxxxxxxxxxx xxxxx xxx xxxxxxxx tkáně x xxxxx. |
|
2. |
Xxxxxxxx x xxxxx xxxxxxxx, xxx xxxxxxxxx xx xxxxx xxxx xxxxxxx xxxxxxxxxxxx tkáňovému xxxxxxxx xxxxxxxxx xxxxxxxxx x xxxxxxx XXX části X xxxx xxxxxxxx. |
|
3. |
Xxxxxxxx s cílem xxxxxxxx, xxx dodavatel xx třetí xxxx xxxxxxxxxx xxxxxxxxxx xxxxxxx xxxxxxxx x xxxxxxxxx závažném xxxxxxxxxx xxxxxx xx xxxxxx nebo xxxxxxxxx xx xx, jež xxxxx xxxxxxxx kvalitu x xxxxxxxxxx tkání x xxxxx, xxxxx xxxx xxxx xxxx být xxxxxxxx xxxxxxxxxxx xxxxxxxx zařízením. |
|
4. |
Xxxxxxxx x xxxxx xxxxxxxx, xxx xxxxxxxxx ze xxxxx xxxx xxxxxxxxxx xxxxxxxxxx xxxxxxx xxxxxxxx o jakýchkoli xxxxxxxxxxx změnách svých xxxxxxxx, včetně xxxxxxxxxx xxxx xxxxxxx xxxxxxx xxxx xxxxxxxxxxx povolení xxxxxxx xxxxx a buňky xxxx o jiných xxxxxxxx xxxxxxxxxxxx xxxxxxxxxxx xxxxxx xxxx xxxxxx třetí xxxx xxxxxxxxxx se xxxxxxxxx příslušných xxxxxxxx, xxx xxxxx xxxxxxxx xxxxxxx x xxxxxxxxxx xxxxx x xxxxx, xxxxx xxxx xxxx xxxx být xxxxxxxx dovážejícím xxxxxxxx xxxxxxxxx. |
|
5. |
Xxxxxxxx xxxxxxxxxx xxxxxxxxxxx xxxxxx či xxxxxxx xxxxx provést xxxxxxxx xxxxxxxx xxxxxxxxxx xx xxxxx země, včetně xxxxxxxx xx xxxxx, xxxxx xx x xx xxxxxxx xxxxx xxxxx xxxxxxxxxx x xxxxx xxxxxxxx xxxxxxxxxxxx xxxxxxxxx xxxxxxxx. Xxxxxxx xxxxxxxx xx xxxxxx xxxx zaručit xxxxxxxxxxxx xxxxxxxxx zařízení xxxxx xxxxxxxx xxxxxxxxxx xxxxx svého dodavatele xx xxxxx xxxx. |
|
6. |
Xxxxxxxx, xx xxxxx se xxxxxx shodly x xxxxx xxxx být xxxxxxx xxx xxxxxxxx tkání x xxxxx mezi dodavatelem xx xxxxx země x xxxxxxxxxxx xxxxxxxx xxxxxxxxx. |
|
7. |
Xxxxxxxx x xxxxx xxxxxxxx, aby xxxxxxx x xxxxx xxxxxxxx xx xxxxxxxxxx xxxxx x xxxxx xxxx xxxxxxxxxx xxxxxxxxxxx xx třetí xxxx nebo jeho xxxxxxxxxxxxxx v souladu x xxxxxxxx XX o ochraně xxxxx xx dobu 30 xxx xx odběru x xxx xxxx xxxxxxxxx xxxxxx xxxxxxxx xxxxxxxx x xxxxxxx, že by xxxxxxxxx xx xxxxx xxxx ukončil svoji xxxxxxx. |
|
8. |
Xxxxxxxxxx x xxxxxxxxxxx xxxxxxxx x x xxxxxxxxxx xxxxxxxxx x xxxxxx xxxxxxx xxxxxx, xxxxxx xxxxx xxxxxxxxxxxx xxxxxxxx xxxxx v požadavcích xxxxxxxxxx x xxxxxxxxxxxxxx xxxxx XX xxxxxxxxxxx xx xxxxxxxx 2004/23/XX. |
|
9. |
Xxxxxx xxxxxxxxx standardních xxxxxxxxxx postupů xxxxxxxxxx xx třetí země xxxxxxxxxxxxx x xxxxxxxx x xxxxxxxxxxx xxxxxxxxxx xxxxx x xxxxx x xxxxxxx xxxx xxxxxxx xx požádání xxxxxxxxxx. |


