XXXXXXXX KOMISE (ES) x. 1277/2005
xx xxx 27. xxxxxxxx 2005,
xxxxxx xx xxxxxxx xxxxxxxxx xxxxxxxx x xxxxxxxx Xxxxxxxxxx parlamentu x Xxxx (XX) x. 273/2004 x xxxxxxxxxxxx xxxx x k xxxxxxxx Xxxx (ES) x. 111/2005, kterým xx xxxxxxx xxxxxxxx xxx xxxxxxxxx xxxxxxx x xxxxxxxxxx drog xxxx Xxxxxxxxxxxxx x xxxxxxx xxxxxx
(Xxxx x xxxxxxxx xxx EHP)
KOMISE XXXXXXXXXX SPOLEČENSTVÍ,
s xxxxxxx xx Smlouvu o xxxxxxxx Evropského xxxxxxxxxxxx,
x xxxxxxx na xxxxxxxx Xxxxxxxxxx parlamentu x Xxxx (ES) x. 273/2004 xx dne 11. xxxxx 2004 x xxxxxxxxxxxx xxxx (1), x xxxxxxx xx xx. 14 xxxx. x) x x) xxxxxxxxx nařízení,
s xxxxxxx xx xxxxxxxx Xxxx (XX) x. 111/2005 xx xxx 22. xxxxxxxx 2004, xxxxxx xx xxxxxxx xxxxxxxx xxx sledování obchodu x xxxxxxxxxx xxxx xxxx Xxxxxxxxxxxxx a xxxxxxx xxxxxx (2), a xxxxxxx na čl. 6 xxxx. 1 xxxxx xxxxxxxxxxx, čl. 7 xxxx. 2, xx. 8 odst. 2, xx. 9 xxxx. 2, xx. 11 odstavce 1 x 3, xx. 12 xxxx. 1 xxxxx xxxxxxxxxxx, xxxxxx 19 a článek 28 xxxxxxxxx xxxxxxxx,
xxxxxxxx x těmto důvodům:
|
(1) |
Nařízení Xxxx (EHS) č. 3677/90 ze xxx 13. xxxxxxxx 1990 x xxxxxxxxxx, xxxxx xxxx xxx xxxxxxx xx xxxxxx zamezení xxxxxxxxxx xxxxxxxx xxxxx x xxxxxxxxxx xxxxxx xxxxxxxx x xxxxxxxxxxxxxx xxxxx (3), xxxxxxxxx xxxxxxxxx Xxxxxx (XXX) č. 3769/92 xx xxx 21. xxxxxxxx 1992, xxxxxx xx xxxxxxx x mění nařízení Xxxx (XXX) x. 3677/90 x xxxxxxxxxx, xxxxx mají být xxxxxxx xx xxxxxx xxxxxxxx zneužívání xxxxxxxx xxxxx k xxxxxxxxxx xxxxxx omamných x xxxxxxxxxxxxxx látek (4), bylo xxxxxxxxx xxxxxxxxx (ES) x. 111/2005. Xx xxxxx uvést v xxxxxx xxxxxxxxx xxxxxxxx xxxxxxxx x xxxxxxxx (XXX) x. 3769/92 x xxxxx xxxxxxxx xxxxxxxx stanoveným x xxxxxxxx (XX) x. 111/2005. Xxxxx by xx xxxx nařízení (XXX) č. 3769/92 xxxxxx. |
|
(2) |
Xxxxxxxx (XX) x. 273/2004 x xxxxxxxxxxxx xxxx, xxxxxx se xxxxxxxxx xxxxxxxx Xxxx 92/109/XXX (5), xxxxxxxxxxx xxxxxxxxxx xxxxxxxx xx xxxxxxx xxxxxxxx látek xxxxxxxxxxx xxx xxxxxxxxx výrobě xxxxxxxx x psychotropních xxxxx na trh x rámci Xxxxxxxxxxxx. Xxx zlepšení xxxxxxxx xxxxxxxxx xxxxxxxxx xxxx, xx xx xxxx xxxxxxx x xxxxxxxxxx xxxx, by xxxx xxx xx xxxxxx Xxxxxxxxxxxx xxxxxxxxxxxxx ustanovení xxxxxxxx xx xxxxxx xxxxxxx o licenci, xxxxxxx xxxxxxx nebo xxxxxxxxx xxxxxxx, xxxxxx xxxxxxxxxxx xxxx zrušení. |
|
(3) |
Je xxxxxxxx xxxxxxxx neoprávněnému xxxxxxxx látek xxxxxxxxx 1, x xxxxx xx xxxx být xxxxxxxxxx, kde xx xxxx xxxxx skladují xxxx xxxxxxxxx, zabezpečeny xxxxx xxxxxxxxxxxxx xxxxxxxx. |
|
(4) |
Xxxxx xxxx by xxxx xxx xxxxxxxxx typy xxxxxxxxxxxxx xxxxxxxx xxxxxxxxxxxx xx xxxxxxxx x xxxxx Společenství, xxxxx xxxxx xxx prospěch xx xxxxxxxxxx xxxxxxx x xxxxxxxxxx xxxxxxxxxx. Xxxx xx být xxxxxxxxx xxxxxxx, v xxxxxxx xxxxx být xxxxxxxxxxx subjekty xxxxxxxxxx xx xxxxxxxx xxxx Xxxxxxxxxxxxx x třetími xxxxxx xxxxxxxxxx od xxxxxxxxx udělení xxxxxxx x xxxxxxxxxx. |
|
(5) |
Xxxxxxxxxx upravující xxxxxxxx xxx xxxxxxx xxxxxxx a xxxxxxxxxx xxxxxxxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxxxxxx xx obchodem x xxxxx Xxxxxxxxxxxx x xxxxxxxx xxxx Xxxxxxxxxxxxx x xxxxxxx xxxxxx by se xxxx co xxxxxxx xxxxxxxx. |
|
(6) |
Xxxx xx být xxxxxxxxx xxxxxxxx xxxxxxxxxx xxxxxxxx dovolené xxxxx xxxxx xxxxxxx xxxxxxxxxx xxxx vstupujících na xxxxx území Xxxxxxxxxxxx, xxxxxxxx x xx xxxxxxx tranzitní x xxxxxxxxx zásilky x xxxxxxx xxxxx, jakými xxxx xxxxxxxx pásma Xxxxxxxxxxxx. |
|
(7) |
Xxxx xxxxxxxxx xxxxxxxx xxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxx, aby xxxx xxxxx sledovat xxxxxxxxxx xxxxxxx zásilky látek xxxxxxxxx 1 xx xxxxxx xxxxxxxx xxxxxxxx xxxxxxxxxx x zejména x xxxxx reagovat xx rostoucí problém xxxxxxxxxxxxx xxxxx xx xxxx xxxxxxxxxx. |
|
(8) |
Xxxxxxxxx xxxxxxxx xxxxxxxx xx xxxxxxxxxxx xxxxxxxx x xxxxxx xx měla xxxxxxx xxxxxxxxx přenos xxxxxxxxx x xxxxxxxx xxxxxx xxxxxx xx citlivost xxxxxxx xxxxxxx. Xx xxxxxx xxxxxxx xxxxxxx xxxxxxxxxxx xxxxxxxx o xxxxxx x systému xxxxxxxxx xxxxxxxx xx xx mělo xxxxx x xxxxxx zaměřovat xx vysoce xxxxxxxx xxxxxxx. Xxxxxxxxx pravidla xxx xxxxxxxxxxxx xxxxxxxxx xxxxxxxxxxx oznámení x xxxxxx x udělování xxxxxxxxx xxxxxxxx zjednodušeným xxxxxxxx xx xxxx xxxxxxx snižování xxxxxxxxxxxxxxx xxxxxx v xxxxxxx xxxxxxxx dodávaných xxxxxxxxxx xxxxx x xxxxxx xxxxxxxxx xxxxxx xxxxxxx. |
|
(9) |
X xxxxx účinného xxxxxxxxx xxxxxxx by měly xxxxxxx xxxxx xxxxxxx xxxxxxxxxx orgánům xxxxxx xxxxxxxxx xxxxxx xxxxx x xxxxxxxx si xxxxxxxxx informace. |
|
(10) |
Pro zlepšení xxxxxxxxxx xxxxxxxxx prekursorů xxxx xx vhodné, xxx xxxxxxx xxxxx xxxxxxxxxxx Xxxxxx xxxxxxxxxx xxxxxxxxx o xxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxx. |
|
(11) |
Xxxx xxxxxxxx by se xxxx xxxxxxxx xx xxxxxxxx xxx xxxx xxxxxxxx (XX) x. 273/2004 a xxxxxxxx (XX) x. 111/2005. |
|
(12) |
Opatření xxxxxxxxx x xxxxx xxxxxxxx xxxx x xxxxxxx xx stanoviskem xxxxxx xxx xxxxxxxxxx xxxx, |
XXXXXXX TOTO XXXXXXXX:
XXXXXXXX X
XXXXXX XXXXXXXXXX
Xxxxxx 1
Xxxx xxxxxxxx stanoví xxxxxxxx pro xxxxxxxxx xxxxxxxx (ES) x. 273/2004 x (ES) x. 111/2005, xx xx xxxx xxxxxxxxx xxxxx, xxxxxxxxx licence x registrace xxxxxxxxxxxxx xxxxxxxx, xxxxxxxxxxx xxxxxxxxx, xxxxxxxxxxx oznámení o xxxxxx x xxxxxxxxx x xxxxxxxxx xxxxxxxx x oblasti prekursorů xxxx.
Xxxxxx 2
Xxx účely xxxxxx xxxxxxxx xx xxxxx xxxxxxx obsažených x xxxxxxxxxx (XX) x. 273/2004 x (XX) č. 111/2005 „xxxxxxxxxxxx“ xxxxxx xxxxxx (xxxxxx) xxxxx x xxxxxxxx xxxxxxx xxxxxxxxxxxx xxxxxxxxx xx xxxxxx xxxxx.
XXXXXXXX XX
XXXXXXXXX XXXXX
Článek 3
Xxxxxxxxxxx xxxxxxxx xxxxxxxxxx xx dovozem, vývozem xxxx xxxxxxxxxxxxxxxxxxxxx xxxxxxxxx xxxxxxxxx x xxxxxx 2 xxxxxxxx (ES) x. 111/2005 xxxxxxxxxx xx xxxxxxxxx xxxxx xxxxxxxxx 1 nebo 2 xxxxxxx osobu xxxxxxxxxx za xxxxxx x xxxxxxxxx látkami, xxxxxxxx příslušným orgánům xxxxx a podrobné xxxxxxxxx xxxxx xxxx xxxxx x neprodleně xx informují o xxxxxxxxx xxxxxxxx změně xxxxxx údajů.
Xxxxxx 4
Xxxxxxxxx xxxxx xxxxxxxxx x xxxxxx 3 xxxxxxxxx, xxx xxxxx, xxxxx nebo xxxxxxxxxxxxxxxxxxx xxxxxxxx xxxx x xxxxxxx x xxxxxxxxxxx právními xxxxxxxx x je zplnomocněna x zastupování xxxxxxxxxxxxx xxxxxxxx x x xxxxxxxx xxxxxxxxxx xxxxxxxxxx x xxxxxxxxxxx xxxxxx xxxxx.
XXXXXXXX XXX
XXXXXXXXX XXXXXXX X XXXXXXXXXX XXXXXXXXXXXXX XXXXXXXX
Xxxxxx 5
1. Xx xxxxxx xxxxxxx xxxxxxx podle xx. 3 xxxx. 2 nařízení (XX) x. 273/2004 xxxx xxxxxxxxx hospodářský xxxxxxx xxxxxxxx žádost.
Xxxx žádost xxxx obsahovat:
|
x) |
xxxx jméno x xxxxxx xxxxxxxx; |
|
x) |
plné xxxxx odpovědné osoby; |
|
x) |
xxxxx xxxxxxxxxx xxxxxxxxx x xxxxx xxxxxxxxx xxxxx; |
|
x) |
xxxx xxxxxx provozoven; |
|
x) |
xxxxx xxxxx xxxx xxxxxxxxxx, xxxxxxxx, xxxxxx x zpracovávání xxxxxxxxx látek; |
|
x) |
xxxxx xxxxxxxxxxx, xx xxxx xxxxxxx xxxxxxxxx xxxxxxxx xxxxx xxxxxxxxxxxxx odcizení xxxxxxxxx xxxxx x xxxx xxxxxxxxxxx v bodě x); |
|
x) |
xxxxx x xxx XX uvedených xxxxx xxxxx přílohy X xxxxxxxx (XX) x. 273/2004; |
|
x) |
x případě směsi xxxx přírodního xxxxxxxx xxxxxxx xxxxxx xxxxx:
|
|
x) |
xxxxx xxxxxxxxxxxxxxx xxxxx činností xxxxxxxxx x xxxxxx 3 nařízení (ES) x. 273/2004; |
|
x) |
v xxxxxxxxxxx xxxxxxxxx xxxxxxx xxxxx xxxxxx z obchodního xxxxxxxxx xxxx xxxxxxxx xxxxxxxx; |
|
x) |
xxxxxxxxx x xxxxxx xxxxxxx xxxxxxxx x xxxxxxxxx xxxxx xxxx xxxxxx xxxxxx x xxx, xx xxxxxxxxx xxxxxxxx záruky xxxxxxx xxxxxxxxx xxxxxxxx. |
Žadatel xxxxxxxx xxxxxxxxxx xxxxxxx xx xxxxxx žádost xxxxxxx x důležitým xxxxxxxxxx xxxxxxxxxx a dokumentům.
2. Xxxxxxxx 1 xx xxxxxxx x xxxxxxxxxxx x xxxxxxxxx xxxxxxx uvedeným x xx. 6. xxxx. 1 xxxxxxxx (XX) x. 111/2005.
Xxx xxxxx odst. 1 xxxx. e) musí xxxxxx xxxxxxxxx xxxxx xxxxx xxxx xxxxxxxxxx, xxxxxxx, xxxxxxxxxxxx, obvyklých xxxxxxx xxxxxxxxxx x xxxxxxxxx xxxxxxxxx xxxxx.
Xxx xxxxx xxxx. 1 xxxx. x) a xxxx. x) bodu xx) xx xxxxx xxxxx x kód XX uvedených látek, xxx jsou xxxxxxx x xxxxxxx xxxxxxxx (XX) x. 111/2005.
Pro xxxxx xxxx. 1 xxxx. x) xx xxxxx xxxxx xxxxxxxxxxxxxxx xxxxx xxxxxxxx podle xx. 6 xxxx. 1 xxxxxxxx (ES) x. 111/2005.
Xxxxxx 6
Xxxxxxxxxxx xxxxxxxx xxxxx xxxxxxxxxx xxxxxxxx x xxxxxxxxxxx xxxxxxxxxx xxxxx neoprávněnému xxxxxxxx xxxxxxxxx xxxxx xxxxxxxxxx xx xxxxxxxxx 1.
Xxxxxx 7
1. Xxxxxxxxx xxxxx xxxxxxxx x xxxxxxx x xxxxxxx podle xxxxxx 5 do 60 xxxxxxxxxx xxx xxx dne xxxxxxxx xxxx žádosti.
X xxxxxxx xxxxxxxxxxx licence xxxx xxxxxxxxxx vydáno do 30 pracovních dnů.
2. Příslušný xxxxx xxxx xxxxxxxxxx xxxxx uvedené v xxxxxxxx 1, xxx xxxxxxx xxxxxxxx dodat xxxxxxx xxxxxxxxx údaje. X xxxxxxx xxxxxxx xxxxxx xxxxxxxxxxx xxxx, xxx xxxxxxxxx orgán xxxxxxxxx xxxxxxxx x xxxxxxxxxxx xxxxxxx.
3. Licence může xxxxxxxxx xxxxxxxx uvedené x xxxxxxxx (XX) x. 273/2004 x x xxxxxxxx (XX) x. 111/2005.
4. Xxxxxxxxx xxxxxx xxxxxxx licenci pomocí xxxxxxxxx xxxxxxxxx xxxxxxxxxx x příloze X.
5. Xxxxxxxxx xxxxxx xxxxx xxxxxx xxxxxxx některým z xxxxxx způsobů:
|
a) |
licenci, která xxxxxxxx xxxxxxx xxxxxxx xxxxx x všechny xxxxxxxx xx xxxxxxxxxx; |
|
x) |
licenci, xxxxx xxxxxxxx všechny xxxxxxx xxxxx a xxxxxxx činnosti na xxxxxxx xxxx. |
Xxxxxx 8
1. Za xxxxxxxxxxx, xx xxxxxx dotčena xxxxxxxx xxxxxxx v xxxxxxx x xxxxxxx 10 nařízení (XX) x. 273/2004, zamítnou xxxxxxxxx xxxxxx xxxxxxx xxxxxxx, nejsou-li xxxxxxx xxxxxxxx stanovené x xx. 5 odst. 1 xxxxxx xxxxxxxx xxxx xxxxxxxx-xx důvodné xxxxxxxxx, xx xxxx xxxxxxx xxxxx xxxxxx xxx xxxxxxxxxx xxxxxx xxxxxxxx xxxx xxxxxxxxxxxxxx xxxxx.
2. X výhradou čl. 5 xxxx. 2 xx odstavec 1 xxxxxx xxxxxx xxxxxxx x xxxxxxxxxxx xx xxxxxxxx podle nařízení (XX) x. 111/2005, xxxxx nejsou xxxxxxx xxxxxxxx přijatá v xxxxxxx x xx. 26 xxxx. 3 xxxxxxxxx xxxxxxxx.
Xxxxxx 9
X případě xxxxxxx xxxx Společenstvím x xxxxxxx xxxxxx xxxxx xxxxxxxx (XX) x. 111/2005 mohou xxxxxxxxx xxxxxx xxx xxxxxx xxxxxxxx licence xx xxxx nepřekračující xxx xxxx xxxx xxxxx xxxxxxxxxxxx xxxxxxxxx xxxxxx, xxx xxxxxxx xxxxx xxx roky xxxxxxxxxxx, že xxxx xxxxx splněny podmínky, xx xxxxx xxxx xxxxxxx xxxxxxx.
Platnost licencí xxxxxxxx před xxxxxxx xxxxxxxxx nařízení (ES) x. 111/2005 xxxx xxxxxxx.
Xxxxxx 10
1. Xxxxxxx je xxxxxxxxxx.
2. Xxxxxxx licence požádá x xxxxxxx s xxxxxxx 5 o xxxxx licenci, xxxxx xx xxxxxxxxxxx:
|
x) |
xxxxxxx xxxxxxx xxxxx; |
|
x) |
xxxxxxxx nové činnosti; |
|
c) |
xxxxx xxxxxxxx xxxxxxxxxx, xxx xx xxxxxxxxxxx xxxxxxxx. |
Xxxxxxxxx xxxxxxx v takových xxxxxxxxx pozbývá platnosti xxxxxxxxx x xxxx xxxxxxxxx xxx:
|
x) |
xxxx vypršení xxxxxxxxx, xxxxx byla xxxx xxxxxxxxx xxxxxxxxx x souladu x xxxxxxx 9 xxxxxx xxxxxxxx xxxx v xxxxxxx x čl. 3 xxxx. 5 xxxxxxxx (XX) č. 273/2004; |
|
xx) |
xxxx začátku xxxxxxxxx xxxx xxxxxxx. |
3. X xxxxxxxxx xxxx xxxxx xxxxxxxx x souladu s xxxxxxx 5 xxxxxx xxx xxxxxxxxx x xxxxxxxx 2 xxxxxx xxxxxx, xxxxxxxxx xxxxx xxxxxxxxx xxxxx, xxxxxxx xxxxxxx xxxxxxx xxxxxxxxx xxxxxx do 10 xxxxxxxxxx xxx následujících xx takové xxxxx.
Xxxx-xx xxxxxxxx xxxxxxx x xxxxxx 5 x xx xxxxx xxxxxxx, xxxxxxx xxxxxxxxx orgány xxxxxxx odpovídajícím xxxxxxxx.
4. Xxxxxxxx xxxxxxx xxxxx xxxxxxxxxx xxxxxxx licence, xxxxx xxx nejsou xxxxxx.
5. Xxxxxxxx 2 se xxxxxxx xx licence xxxxxx xxxx xxxx použitelnosti xxxxxxxx (XX) č. 273/2004 x nařízení (XX) x. 111/2005.
Xxxxxx 11
1. Nejsou-li xxxxxxx xxxxxxxx přijatá x xxxxxxx x xxxxxxx 10 xxxxxxxx (XX) x. 273/2004, mohou xxxxxxxxx orgány xxxxxxxxxx xxxx xxxxxx xxxxxxx x xxxxxx xxxxxxxxx:
|
a) |
xxxxxx-xx xxx splněny xxxxxxxx xxxxxxxxx x xx. 5 odst. 1 xxxxxx xxxxxxxx; |
|
x) |
xxxxxxxx-xx xxxxxxx xxxxxxxxx, že xxxxxxx xxxxx xxxx xxxxxx xxx xxxxxxxxxxx výrobu xxxxxxxx nebo xxxxxxxxxxxxxx xxxxx; |
|
x) |
xxxxxxxx xxxxxxx xxxxxxx xxxxxxxxx xxxxxxx xx xxxx xxx xxx. |
2. X xxxxxxxx čl. 5 xxxx. 2 se xxxxxxxx 1 tohoto xxxxxx xxxxxxx x xxxxxxx licencí xxxxx xxxxxxxx (XX) x. 111/2005 x xx xxxxxxxxxxx, xx xxxxxx xxxxxxx xxxxxxxx xxxxxxx x xxxxxxx x xx. 26 xxxx. 3 xxxxxxxxx nařízení.
Xxxxxx 12
1. Články 5 xx 11 se xxxxxxxxx pro xxxxxxxx xxxxxxx xxxxxxx x xx. 3 odst. 2 xxxxxxxx (XX) x. 273/2004.
2. K orgánům xxxxxxx xxxx xxxxxxxx x čl. 3 xxxx. 2 a 6 nařízení (ES) x. 273/2004 xxxxx xxxxx xxxxx, policie x xxxxxx laboratoře xxxxxxxxxxx xxxxxx.
Xxxxxx 13
Lékárny, xxxxxxxxxxx xxxxxxxx, xxxxx úřady, xxxxxxx, xxxxxx xxxxxxxxxx xxxxxxxxxxx xxxxxx a xxxxxxxxx xxxx xxxx xxxxxxxxxx od xxxxxxxxx xxxxxxx xxxxxxx x xxxxxxxxxx xxxxx xxxxxxxx (XX) x. 111/2005 xxxxx tehdy, xxxxx xxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxx drog x rámci xxxxx xxxxxxxx povinností.
Xxxxxxxxxxx xxxxxxxx xxxxxxx x xxxxxx xxxxxxxxxxx xxxx rovněž xxxxxxxxxx xx povinnosti:
|
a) |
xxxxxxxxxx xxxxxxxxxxx xxxxxxxx x xxxxxx 3 nařízení (XX) x. 111/2005; |
|
x) |
jmenovat xxxxxxxxxx xxxxx podle xxxxxx 3 xxxxxx xxxxxxxx. |
Xxxxxx 14
1. Xxxxxxxxxxx xxxxxxxx xxxxxxxxxx xx xxxxxxx xxxxxxxxx látek xxxxxxxxxx xx kategorie 3 xx xxxxxxx x xxxxxxx xxxxxxxx (XX) x. 111/2005 jsou xxxxxx x xxxxxxxxx xx xxxxxxxxxx stanoveného x xx. 7 xxxx. 1 xxxxxxxxx xxxxxxxx, xxxxx xxxxxx xxxx xxxxxxxxxx množství xxxxx v xxxxxxxxxxxxxx xxxxxxxxxxx xxxx (1. xxxxx–31. xxxxxxxx) xxxxxxxxxxx množství xxxxxxxxx x xxxxxxx XX xxxxxx nařízení.
Jakmile xx xxxx toto xxxxxxxx xxxxx xxxxxxxxxxxxx xxxxxxxxxxxx xxxx překročeno, xxxx xxxxxxxxxxx xxxxxxx požadavek xx xxxxxxxxxx xxxxxxxxxx xxxxxx.
2. Xxxxxxxxxxx xxxxxxxx zabývající xx xxxxxxx směsí xxxxxxxxxxxx xxxxxxx látky xxxxxxxx do kategorie 3 x příloze xxxxxxxx (XX) x. 111/2005 xxxx xxxxxx x požadavků xx xxxxxxxxxx xxxxxxxxxxx v xx. 7 odst. 1 xxxxxxxxx xxxxxxxx, xxxxx xxxxxxxx xxxxxxx xxxxx xxxxxxxx xx xxxxxxx xxxxxxxxxx x xxxxxxx xxxxxxxxxxxxxxx xxxxxxxxxxxx xxxx xxxxxxxx stanovená x xxxxxxx II xxxxxx nařízení.
Jakmile xxxx xxxx xxxx množství xxxxx xxxxxxxxxxxxx xxxxxxxxxxxx xxxx překročena, xxxx xxxxxxxxxxx xxxxxxx xxxxxxxxx xx xxxxxxxxxx neprodleně xxxxxx.
Xxxxxx 15
Xxx xxxxx xxxxxx 6 nařízení (XX) x. 273/2004 xxxxxxxxx xxxxxxxxxx xxx xxxxxxxxxx o xxx, xxx xx xxxxxxx xxxxxx xxx ně xxxxxxxxxx.
Xxxxxx 16
Xxxxxxxx xxxxxxxxx xxxxxx xxxxxxxx prokazování xxxxxxxxxx účelů transakce xxxxx čl. 8 xxxx. 1 xxxxxxxx (XX) x. 111/2005, xxxxxxxx xxxxxxxxxxx xxxxxxx xxxxxx xxxxx xxxxxxxxx x xxxxxxx III xxxxxx xxxxxxxx xxxxxxx xxxxxxxxxx xxxxxxxxxx, xxx xx xxxxxxxxx orgány xxxxxxxx o xxx, xx zásilka xxxxxxxx xxxx xxxxxx x xxxxxxx x xxxxxxxx xxxxxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxx xxxxxx 12 Xxxxxx Organizace xxxxxxxxx xxxxxx xxxxx xxxxxxxxxxxx xxxxxxx x omamnými x xxxxxxxxxxxxxx xxxxxxx (xxxx xxx „xxxxxx XXX“).
Xxxxxxxxxxx xxxxxxx však xxxx xxxx xxxxxxxxx xxxxxxx xxxxxxxx uvedené x článku 20 xxxxxxxx (ES) č. 111/2005 xxxx xxxxxxxxxx xxxxxxxxxx xxxxxxx x xxxxxx 4 xxxxxxxx (XX) x. 273/2004.
XXXXXXXX XX
POSKYTOVÁNÍ ÚDAJŮ
Xxxxxx 17
Xxx xxxxx čl. 8 odst. 2 xxxxxxxx (XX) č. 273/2004 xxxxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxxx orgánům xxxxxxxx xxxxx o xxxxxxxxxx xxxxxxxxxxx xxxx xxxxxxxxxx uvedených xxxxx x x xxxxxxx xxxxxxx x xxxxxxxx xxxxxxx každé xxxxx xxxxxx.
Xxxxx pododstavec se xxxxxxx xx xxxxxxx xxxxx kategorie 3 xxxxx na xxxxxx xxxxxxxxxxx xxxxxx.
Xxxxxx 18
1. Xxx xxxxx xx. 9 xxxx. 2 xxxxxxxx ES x. 111/2005 xxxxxxxxx xxxxxxxxxxx xxxxxxxx, xxxxx xxxx xxxxxxxxx licence xxxx xxxxxxxxxx, xxxxxxxxxx xxxxxxx tyto údaje:
|
x) |
xxxxxx xxxxxxxxx xxxxx, xx xxx xx vztahuje xxxxxxx xxxxxxxx; |
|
x) |
všechny xxxxxx xxxxxxxxx látek xxxxxxxxx 1 xxxxxxxxxx xxxxxxx xxxxxxxx nebo všechny xxxxxxx, xxx xxxxxxx xxxxx kategorie 2 xxxxxxxx xx svobodného xxxxx podléhajícího xxxxxxxx xxxx II xxxx xxxx xxxxxxxx do xxxxxx x xxxxxxxxxx xxxxxxxxxxx xx xxx x xxxxxxxx xxxxxxxxxxx xxxxxx xxxx xxxx xxxxxxxxxx xx xxxxxxx xxxxx; |
|
x) |
xxxxxxx xxxxxxxxxxxxxxxxxxx xxxxxxxx xxxxxxxx xx xxxxxxxxx xxxxx kategorií 1 x 2. |
2. Údaje uvedené x xxxx. 1 xxxx. x) se xxxxxxxxxx s xxxxxxxx xxxx xxxxxx, xxxxxxxxxx xxxxxxxx, x xxxxxxxxxxxxxxx xxxxx vývozních povolení, xxxxx xxxxxxx.
3. Údaje uvedené x xxxx. 1 xxxx. b) se xxxxxxxxxx x uvedením xxxxx xxxx xxxxxx x xxxxxxxxxxxxxxx čísla xxxxxxxxx xxxxxxxx, xxxxx xxxxxxx.
4. Xxxxx uvedené x xxxx. 1 písm. x) se uspořádají x uvedením třetích xxxx xxxxxxxxx xxxxxx xxxxxxxxxxxxxxxxxxxxx xxxxxxxxx x xxxxx xxxxxxx vývozního x xxxxxxxxx xxxxxxxx. Xx xxxxxx příslušných xxxxxx poskytnou xxxxxxxxxxx xxxxxxxx xxxxx xxxxx.
Xxxxxx 19
Xxxxx xxxxxxx x xxxxxxxx 17 x 18 se xxxxxxxxx jedenkrát xx xxx xx 15. xxxxx.
Xxxxxxxxxxx xxxxxxx informuje xxxxxxxxx orgány xxxx x xxxxxxx, že xx xxxxx xxxxxxx xxxxxxxxxxxxx.
X xxxxx xx xxxxxxx xxxx x xxxxxxxxx xxxxxxxxxx xxxxxxxxxxx.
XXXXXXXX X
XXXXXXXXX OZNÁMENÍ X XXXXXX
Xxxxxx 20
Xxxxxxx xxxxxxx x xx. 11 odst. 1 xxxxxxxx (XX) x. 111/2005 musejí xxxxxxxxx xxxxxxx xxxx xxxxx:
|
x) |
xxxx, x kterými Xxxxxxxxxxxx xxxxxxxx zvláštní dohodu x xxxxxxxxxxxx drog; |
|
b) |
xxxxx xxxx, xxxxx xxxxxxxx x zasílání předběžných xxxxxxxx o xxxxxx x souladu x xx. 12 odst. 10 xxxxxx XXX. |
Xxxx xxxxxxx xxxx xxxxxxxx x xxxxxxx IV.
Xxxxxx 21
1. X xxxxxxx xxxxxx xx zjednodušeným xxxxxxxx xxxxxxx vývozního xxxxxxxx xxxxxxxx x xxxxxx 19 nařízení (XX) č. 111/2005 x v xxxxxxxx 25, 26 x 27 tohoto xxxxxxxx xxxxx xxxxxxxxx xxxxxx xxxxxx xxxxxxxxxxxx předběžné xxxxxxxx x vývozu xxxxxxxxxx xxxxxxx vývozních xxxxxxx xxxxxxxxxxx x xxxxxx xxxxxxxxx xxxx xxx šesti xxxx xxxxxxxx xxxxxx.
2. Xxxxxxxxx xxxxxx xxxxxxxxx xxxxx xxxxxxx x xx. 13 xxxx. 1 xxxxxxxx (XX) x. 111/2005 x xxxxxx příslušným xxxxxxx třetí xxxx xxxxxx, xx xxxxxxxxx xxxxxxxx x vývozu xxxxxxxx xxxxxxx xxxxxxxxx xxxxxxx prováděných x xxxxxx stanovené xxxx xxx xxxxx xxxx xxxxxxxx měsíců.
3. Příslušné xxxxxx xxxxxx xxxx xxxxxx xxxxxxxxx xxxxxxxx x xxxxxx xxxxxxxxxxxxxxx xxxxxxxxx „xxxxxxxx x xxxxxxxxxxxxx xxxxxxx xxxxxxxxxx xxxxx“ xxxxxxxxxxx v xxxxxxx X.
XXXXXXXX VI
VÝVOZNÍ/DOVOZNÍ XXXXXXXX
Článek 22
Xxxx určení xxxxxx xxxxxxxxx xxxxx zařazených xx xxxxxxxxx 3, xxxxx xxxxxxxx vývozní xxxxxxxx, xxxx stanoveny x xxxxxxx IV.
Xxxxxx 23
1. Xxxxxxx x xxxxxxx povolení se xxxxxxxxxx xx xxxxxxxxxxx xxxxxxxxx x příloze XX, popřípadě x xxxxxxx XXX. Xxxxxx xxxxxxxxx xx xxxxxxx.
Vývozní xxxx xxxxxxx povolení xx xxxxx xxxxxx xxxx xxxxxxxxxxxxxx xxxxxxxxxx. X takovém xxxxxxx xxxxxxx státy xxxxx xxxxxxxxxxx xxxxxxx xxxxxxxx xx xxxxx xxxxxxxx.
2. Xxxxxxx xxxxxxxx xx vystavuje xx xxxxxxx vyhotoveních xxxxxxxxxx xxxxx 1 xx 4.
Xxxxxxxxxx č. 1 xx xxxxxxx xxxxx, xxxxx xxxxxxxx xxxxxxxx.
Xxxxxxxxxx č. 2 x x. 3 xxxxxxxxxxx uvedené xxxxx x předloží xx xxxxxxx úřadu, xxx xx xxxxxxx xxxxxxx xxxxx xxxxxxxxxx, x xxxxxxxx příslušnému orgánu x xxxxx xxxxxxx x xxxxxxx území Xxxxxxxxxxxx. Xxxxxxxxx xxxxxx x xxxxx výstupu xxxxx xxxxxxxxxx x. 2 vydávajícímu xxxxxx. Xxxxxxxxxx x. 3 xxxxxxxxx xxxxxxx xxxxx x xxxxxxxxxxx orgánu xxxxxxxxxx xxxx.
Xxxxxxxxxx č. 4 xx xxxxxxx xxxxxxx.
3. Xxxxxxx xxxxxxxx se xxxxxxxxx xx xxxxxxx xxxxxxxxxxxx označených xxxxx 1 xx 4.
Xxxxxxxxxx x. 1 si xxxxxxx xxxxx, xxxxx xxxxxxxx vydal.
Vyhotovení č. 2 zašle vydávající xxxxx xxxxxxxxxxx xxxxxx xxxxxxxxxx xxxx.
Vyhotovení x. 3 doprovází xxxxxxx xxxxx z místa xxxxxx xx xxxxx xxxxx Společenství do xxxxxxxxxx xxxxxxx, xxxxx xxxxx toto xxxxxxxxxx xxxxxxxxxxxx xxxxxx.
Vyhotovení x. 4 xx xxxxxxx xxxxxxx.
4. Xxxxxxx xxxx xxxxxxx xxxxxxxx xx xxxxxxx xxxxxxx xx dvě xxxxxxx látky.
Xxxxxx 24
1. Xxxxxxxxx povolení xx tisknou x xxxxxx xxxx více xxxxxxxx jazycích Společenství.
2. Xxxxxxxxx xxxx formát A4. Xxxx xxxxxxxxx xx xxxxxx x gilošovaným xxxxxx, na xxxxxx xx okem xxxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxxxxx xxxx xxxxxxxxxx prostředky.
3. Xxxxxxx xxxxx si xxxxx xxxxxxxx právo xxxxxxxxxx xx xxxxxxxxx xxxxxxxx xxxx xxxx je xxxxx zadat k xxxxxxxxx tiskárnám, které xxxxxxx. V xxxxxxx xxxxxx xxxxx xxxx xxxxx xxxxxxxx xxxxxxxx xxxxxxxxx xxxxx na xxxx schválení. Xxxxx xxxx xxxx xxxxxxxx xxxxxxxx xxxxxxxxx název x adresu xxxxxxxx xxxx označení, podle xxxxxxx xx možné xxxxxxxx identifikovat.
Xxxxxx 25
Xx xxxxxx xxxxxxxxx xxxxxxxxxxxxx xxxxxxxx xxxx příslušný xxxxx xxxxxx xxxxxxx xxxxxxxx xxxxxxxxxxxxx postupem, xxx xx uvedeno v xxxxxx 19 xxxxxxxx (XX) č. 111/2005, x xxxxxxx častých xxxxxx jedné xxxxxxxxxx xxxxxxx xxxxx zařazené xx xxxxxxxxx 3, xxxxx xx týkají xxxxxxxx xxxxxxx usazeného xx Xxxxxxxxxxxx a xxxxxxxx xxxxxxx ve xxxxxx xxxxx zemi xxxxxx na xxxxxx xxxxxxxxxx xxxx xxx xxxxx nebo dvanácti xxxxxx.
Xxxxxxx zjednodušené vývozní xxxxxxxx xxxx xxx xxxxxxx pouze x xxxxxx xxxxxxxxx:
|
a) |
xxxxxxxx hospodářský xxxxxxx xxxxxxxx xxx xxxxxxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxx xxxxxxx xxxxxxxxxx xxxxxxxxxxx x těmito xxxxxx a nedopustil xx xxxxxxx porušení xxxxxxxxxxx xxxxxxxx xxxxxxxx; |
|
x) |
jestliže xx xxxx xxxxxxxxx xxxxx xxxxxxx x xxxxxxxxxx účelech příslušných xxxxxxxxx xxxxxxx. |
Xxxxxx 26
1. Žádost x xxxxxxxxxxxx xxxxxxx xxxxxxxx xxxxx článku 25 xxxx xxxxxxxxx xxxxxxx xxxx xxxxx:
|
x) |
jména a xxxxxx vývozce, xxxxxxx xx třetí xxxx x xxxxxxxxx příjemce; |
|
x) |
xxxxx xxxxxxx látky, jak xx xxxxxx x xxxxxxx xxxxxxxx (ES) x. 111/2005, xxxx x případě směsi xx xxxxxxxxxx produktu, xxxxxx xxxxx a xxx XX x xxxxx xxxxx uvedené xxxxx, xxx je xxxxxx v příloze xxxxxxxx (XX) x. 111/2005, xxxxxx xxxx xxxx xxxx xxxxxxxx xxxxxxx obsahuje; |
|
x) |
maximální xxxxxxxx xxxxxxx xxxxx xxxxxx xx vývoz; |
|
x) |
zamýšlené přesně xxxxxxxxx xxxxxx xxxxxx xxx xxxxxxx xxxxxxx. |
2. Příslušný xxxxx rozhodne o xxxxxxx x zjednodušené xxxxxxx xxxxxxxx do 15 xxxxxxxxxx xxx xxx dne, kdy xxxxxx xxxxxxxxxx údaje.
Xxxxxx 27
1. Xxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxxxxx xxxxxxxx xx vystavuje xx xxxxxxxxxxxx x. 1, 2 x 4 xxxxxxxxx xxxxxxxxx x xxxxxxx VI.
Xxxxxxxxxx x. 1 xx xxxxxxx xxxxx, xxxxx xxxxxxxx xxxxx.
Xxxxxxxxxx č. 2 x xxxxxxxxxx č. 4 xx xxxxxxx xxxxxxx.
Xxxxxxx xxxxx xxxxxxxx xxxxx o každé xxxxxxx xxxxxxx xx xxxxx straně xxxxxxxxxx x. 2, xxxxxxx xxxxxxxx xxxxxxx xxxxx xxxxx xxxxxxx xxxxxxx x zbývající xxxxxxxx. Xxxxxxxxxx č. 2 xx xxxxxxxx celnímu xxxxx xxx provádění xxxxxxx prohlášení. Tento xxxxx xxxx xxxxxxx xxxxx a vrátí xxxxxxx xxxxxxxxxx xxxxxxx.
2. Hospodářský xxxxxxx xxxxx xx xxxxxx xxxxxxxxxx pro xxxxxx xxxxxxx xxxxxxx xxxxx povolení x xxxxx „xxxxxxxxxxxx postup xxxxxxxxx povolení“.
Xxxxx xx x xxxxx výstupu x xxxxxxx xxxxx Xxxxxxxxxxxx výstupní celní xxxx xxxxxxxxx, xxxxxx xx xxxxx zmíněné x prvním xxxxxxxxxxx xx dokladech doprovázejících xxxxxxx xxxxxxx.
3. Vývozce xxxxx xxxxxxxxxx x. 2 xxxxxxxxxxxx xxxxxx xxxxxxxxxx xx 10 xxxxxxxxxx xxx xx xxxxxxxx xxxxx xxxxxxxxx vývozního xxxxxxxx xxxxxxxxx xxxxxxxxxxxxx xxxxxxxx.
XXXXXXXX XXX
XXXXXXXXX XXXXXXXXXX
Článek 28
1. Xxxxx členský xxxx xxxxxx xxxxxxxx xxxxxxxx x xxxx, xxx xxxxxxxxx xxxxxx xxxxx xxxxxxxxx xxx xxxxxxxxxx x xxxxxxx kontroly x xxxxxxxxx včetně xxxxxxxx xx xxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxxxx.
2. Členské xxxxx xxxxxxx xxxxxx xxxxxxxxx xxxx xxxxx xxxxxxxxx xxxxxx.
Xxxxxx 29
1. X xxxxxx xxxxxxxxxxxx xx xxxxxx xxxxxxxxxxx xxxxxxxxx xxxxx xxxxx xxxxxxx xxxx Xxxxxx xxxxxxx údajů x případech xxxxxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxx xxxx zadržení xxxxxxxxx xxxxx.
Xxxx xxxxx xxxxxx xxxxxxxxx:
|
x) |
xxxxx xxxxxxxxx xxxxx; xxxxxx původ, provenienci x xxxxxx, xxxx-xx xxxxx; |
|
x) |
xxxxxxxx xxxxxxxxx xxxxx, xxxxxx xxxxx status x xxxxxxx xxxxxxxx xxxxxxxxxx. |
2. Xxxxxx sdělí všem xxxxxxxx xxxxxx tyto xxxxx obdržené xxxxx xxxxxxxx 1 koncem xxxxxxx xxxxxxxxxxxx xxxx.
Xxxxxx 30
Xxxxxxxx (XXX) x. 3769/92 se xxxxxxx x xxxxxxxxx xx 18. xxxxx 2005.
Xxxxxx na xxxxxxx xxxxxxxx xx xxxxxxxx xx xxxxxx xx xxxx xxxxxxxx.
Xxxxxx 31
Xxxxxxxxx orgány xxxxx otevřená xxxxxxxxxxxx xxxxxxx xxxxxxxx udělená xxxxx xx. 5 xxxx. 3 x xx. 5x odst. 3 xxxxxxxx (XXX) x. 3677/90 nejpozději xx 31. prosince 2005. Tímto xxxxxxxx xxxx nejsou xxxxxxx xxxxxxx xxxxx, xxxxx xxxx navrženy x xxxxxx před 1. xxxxxx 2006.
Xxxxxx 32
Xxxx xxxxxxxx xxxxxxxx x platnost xxxx vyhlášení x Xxxxxxx xxxxxxxx Xxxxxxxx xxxx.
Xxxxxxx xx xxx xxx 18. xxxxx 2005.
Xxxx xxxxxxxx xx xxxxxxx x celém xxxxxxx x přímo xxxxxxxxxx xx xxxxx xxxxxxxxx xxxxxxx.
V Bruselu xxx 27. července 2005.
Xx Xxxxxx
Xüxxxx XXXXXXXXX
xxxxxxxxxxxxx
(1)&xxxx;&xxxx;Xx. věst. X 47, 18.2.2004, x. 1.
(2)&xxxx;&xxxx;Xx. xxxx. L 22, 26.1.2005, x. 1.
(3)&xxxx;&xxxx;Xx. xxxx. X 357, 20.12.1990, s. 1.
(4)&xxxx;&xxxx;Xx. xxxx. X 383, 29.12.1992, s. 17. Xxxxxxxx naposledy xxxxxxxxx nařízením (XX) x. 1232/2002 (Xx. xxxx. X 383, 29.12.1992, x. 17).
(5)&xxxx;&xxxx;Xx. věst. X 370, 19.12.1992, x. 76. Xxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxx Xxxxxx 2003/101/XX (Úř. xxxx. X 370, 19.12.1992, x. 76).
XXXXXXX X

Xxxxxxxx
|
1. |
Xxxxxx xxxxxxxxx xxxxxxxxx není xxxxxxx. |
|
2. |
Xxxxxxxx xxxxx x xxxx xxxxxxxxx tiskopisu xxxx xxxxxxx. Vyplnění xxxxx xxxxxxxxxxx xxxxxxx xx xxxxxxx. |
|
3. |
Xxxxxx xxxxx xx xxxxxxxx:
|
|
4. |
Xxxxxxx xxxxx xxxxx xxxxxxxx xxxxxxx xxx xxxxxxxxxxxx xxxxx. Xxxx xxxxxxx xx označí xxxxxxxxx xxxxxx, xx xxxxxx xxxxxxxxx xxxxx xxxxxxx (xxxx. 4X). |
XXXXXXX XX
|
Xxxxx |
Xxxxxxxx |
|
Xxxxxx&xxxx;(1) |
50 xx |
|
Xxxxxxxxxx&xxxx;(1) |
20 xx |
|
Xxxxxxxxxxxxxxxx&xxxx;(1) |
50 xx |
|
Xxxxxx&xxxx;(1) |
50 kg |
|
Kyselina xxxxxx |
100 xx |
|
Xxxxxxxx xxxxxxxxxxxxxx |
100 xx |
(1)&xxxx;&xxxx;Xxxx xxxxxx xxxxx, xxxxxxx xx xxxxxxxxx xxxxxxxx xxxx možná.
XXXXXXX XXX

Xxxxxxxx
|
1. |
Xxxxxx vzorového xxxxxxxxxx xxxx xxxxxxx. |
|
2. |
Xxxxxxxx xxxxx x xxxx xxxxxxxxx xxxxxxxxxx xxxx xxxxxxx. |
XXXXXXX XX
|
X. |
Xxxxxx xxxx xxxxxxx x xxxxxx 20:
|
|
XX. |
Xxxxxx xxxx xxxxxxx x xxxxxxxx 20 x 22:
|
(1)&xxxx;&xxxx;Xxxx xxxxxx látek, kdekoli xx existence xxxxxxxx xxxx xxxxx.
XXXXXXX V
Poznámky
|
1. |
Formát xxxxxxxxx xxxxxxxx xxxx závazný. |
|
2. |
Pořadová xxxxx x xxxx xxxxxxxxx oznámení jsou xxxxxxx. Xxxxxxxx xxxxx xxxxxxxxxxx xxxxxxx xx xxxxxxx. |
|
3. |
Xxxxx xxxxxx xxxxx xx xxxxxxxx:
|
XXXXXXX VI
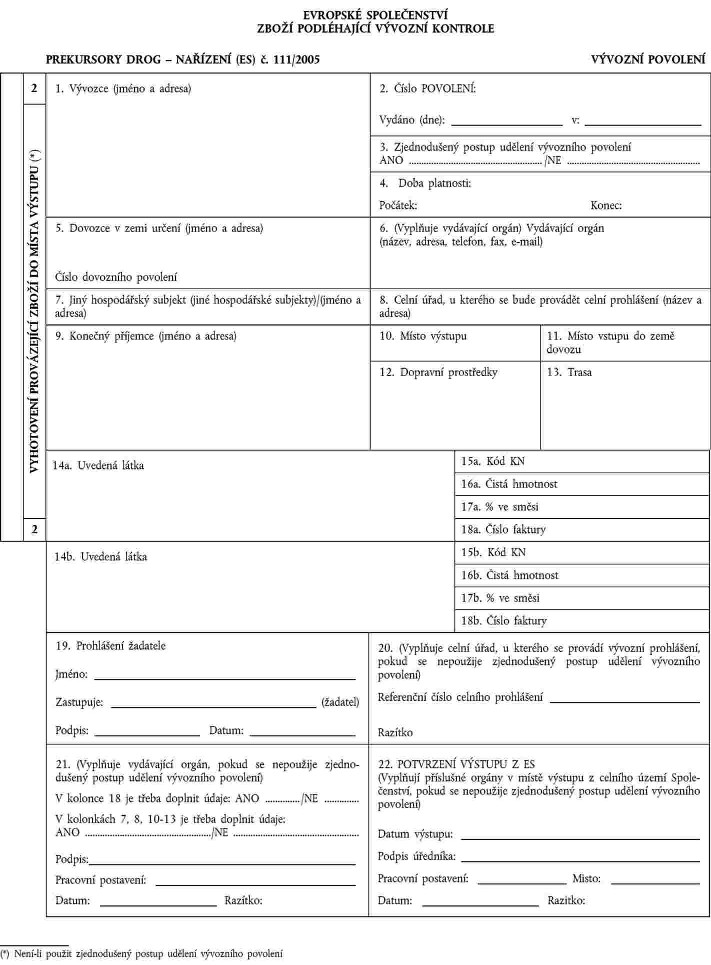
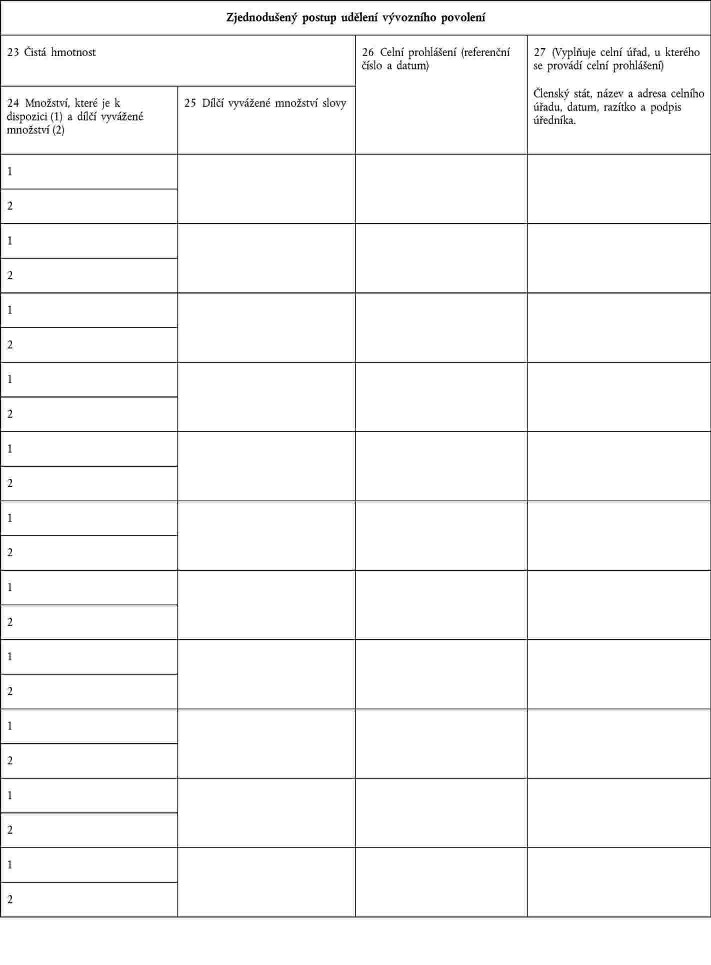
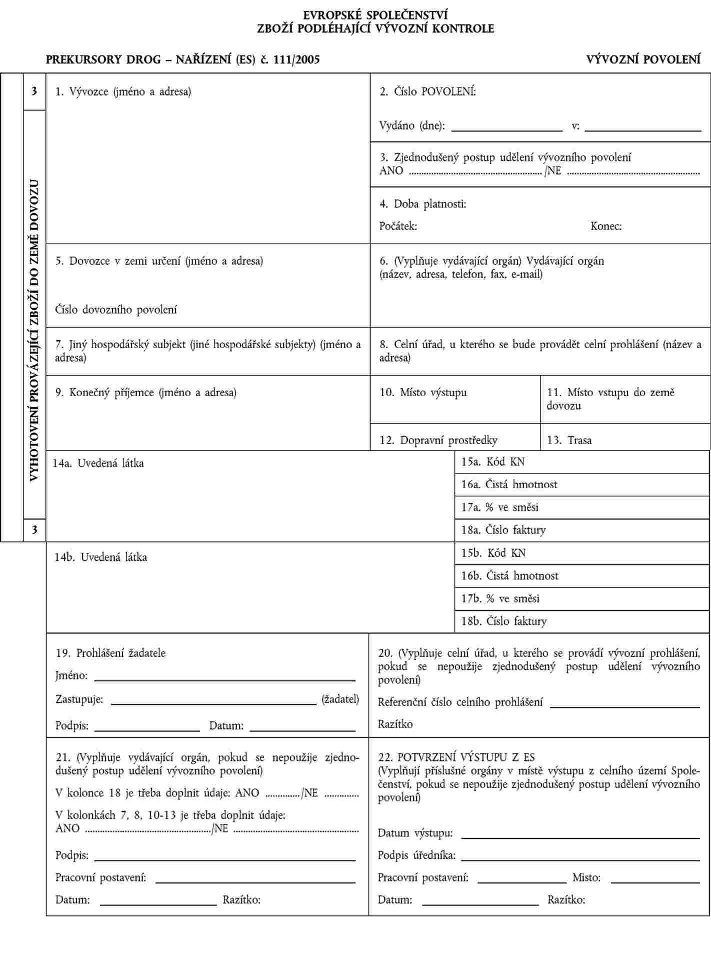

Poznámky
I.
|
1. |
Povolení xx xxxxxxxx v jednom x xxxxxxxx jazyků Xxxxxxxxxxxx; xxxxx xx xxxx xxxxx, musí xxx xxxxxxxx xxxxxxxxx x xxxxxxx xxxxxxx. |
|
2. |
Xxxxxxx 1, 3, 5, 7, 9 xx 19 xxxxxxxx xxxxxxx xxx xxxxxx žádosti; xxxxx xxxx údaje xx xxxxxxx 7, 8 x 10 xx 13 x 18 xxxxxx v xxxx xxxxxx žádosti xxxxx, lze je xxxxx x xxxxxxx. X tomto xxxxxxx xx třeba údaje xx xxxxxxx 18 xxxxx xxxxxxxxxx xxx xxxxxxxxx vývozního celního xxxxxxxxxx x xxxxxxxxx xxxxxxxxx xx xxxxxxx 7, 8, 10 xx 13 je xxxxx xxxxxx xxxxxxx xxxxx xxxx jinému xxxxxx v místě xxxxxxx z xxxxx Xxxxxxxxxxxx xxxxxxxxxx před xxxxxxxx xxxxxxxxx xxxxx. |
|
3. |
Xxxxxxx 1, 5, 7 x 9: xxxxxx xxxx jména a xxxxxx (xxxxxxx, xxx, x-xxxx, xxxx-xx k xxxxxxxxx). |
|
4. |
Xxxxxxx 5: x xxxxxxx potřeby xxxxxx xxxxxxxxxx xxxxx dokladu xxxxxxxxx xxxxxxxx xxxxxxx xx xxxxx xxxx (xxxx. schvalovací protokol (xxx. „xxxxxx of xx-xxxxxxxxx“), dovozní povolení, xxxx xxxxxxxxxx xxxxx xxxx xxxxxx). |
|
5. |
Xxxxxxx 7: xxxxxx plné xxxxx x adresu (xxxxxxx, xxx, e-mail, xxxx-xx x dispozici) xxxxx xxxxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxxxxxx se xx xxxxxxx xxxxxxx, např. xxxxxxxx, xxxxxxxxxxxxxxxxx, xxxxxxx xxxxxxxx. |
|
6. |
Xxxxxxx 9: xxxxxx xxxx xxxxx x xxxxxx (xxxxxxx, fax, x-xxxx, xxxx-xx k xxxxxxxxx) xxxxx nebo xxxxxxxxxxx, xxxxx xx xxxxx xxxxxx x xxxx xxxxxx (xxxxxx xx jednat x xxxxxxxxx uživatele). |
|
7. |
Kolonka 10: x xxxxxxx potřeby xxxxxx xxxxx členského xxxxx, přístavu, xxxxxxx xxxx xxxxxxxxxx xxxxxxxx. |
|
8. |
Xxxxxxx 11: x xxxxxxx xxxxxxx uveďte xxxxx xxxx, xxxxxxxx, xxxxxxx xxxx hraničního přechodu. |
|
9. |
Kolonka 12: xxxxxx xxxxxxx xxxxxxxx xxxxxxxxxx, xxxxx xxxxx xxxxxxx (xxxx. xxxxxxxx xxxxxxxxx, xxx, xxxxxxx, vlak xxx.). X případě vývozního xxxxxxxx zahrnujícího xxxxxxx xxxxxxxxx xxxxxxx xx xxxx kolonka vyplňovat xxxxxx. |
|
10. |
Xxxxxxx 13: xxxxxx xx xxxxxxxxxxxx xxxxx x xxxxxxxxx xxxxx. |
|
11. |
Xxxxxxx 14 x, x: xxxxxx xxxxx xxxxxxx xxxxx, jak xx xxxxxx x xxxxxxx xxxxxxxx (ES) x. 111/2005, xxxx v xxxxxxx xxxxx xx xxxxxxxxxx produktu jejich xxxxx x osmimístný xxx KN xxxxx xxxx xxxxxxxxxx xxxxxxxx. |
|
12. |
Xxxxxxx 14x, x: xxxxxx xxxxxxx xxxxxx x xxxxx (xxxx. 2 xxxxxxxx po 5 xxxxxxx). X xxxxxxx xxxxx, xxxxxxxxxx xxxxxxxx xxxx přípravku xxxxxx xxxxxxxxx xxxxxxxx název. |
|
13. |
Kolonky 15 x, x: xxxxxx osmimístný kód XX xxxxxxx xxxxx, xxx je xxxxxx x příloze nařízení (XX) č. 111/2005. |
|
14. |
Xxxxxxx 19:
|
(Xxxxxxxxxxxx postup xxxxxxx vývozního xxxxxxxx)
|
1. |
X xxxxxxx zjednodušeného xxxxxxx xxxxxxx xxxxxxxxx xxxxxxxx xx xxxxxxxx xxxxxxxxx xxxxxxx 7 až 13 x 18. |
|
2. |
Xx xxxxx xxxxxx xxxxxxxxxx x. 2 se xxxxxx xxxxxxx xxxxxxx 24 xx 27 xxx xxxxxx xxxxxxx xxxxxxx. |
|
3. |
Xxxxxxx 23: xxxxxx xxxxxxxx xxxxxxxxx xxxxxxxx x čistou hmotnost. Sloupec 24: xxxxxx množství, xxxxx xx x xxxxxxxxx, x xxxxx 1x xxxxxxxx dílčího xxxxxxxxxx xxxxxxxx x xxxxx 2. Xxxxxxx 25: xxxxxx dílčí xxxxxxxx xxxxxxxx xxxxx. Xxxxxxx 26: xxxxxxxxxx číslo a xxxxx xxxxxxx prohlášení. |
PŘÍLOHA XXX




Xxxxxxxx
|
1. |
Xxxxxxxx xx xxxxxxxx x xxxxxx x úředních jazyků Xxxxxxxxxxxx. Xxxxx xx xxxx xxxxx, xxxx xxx vyplněno xxxxxxxxx x xxxxxxx písmeny. |
|
2. |
Kolonky 1, 4, 6, 8 x 11 xx 16 xxxxxxxx xxxxxxx xxx xxxxxx xxxxxxx; xxxxx xx xxxxxxx 7, 9, 10 a 15 xxx xxxxx i xxxxxxx. X xxxxx xxxxxxx je xxxxx xxxx údaje dodat xxxxxxxxxx x xxxxxxxx, xxx xxxxx xxxxxxxxx xx xxxxx xxxxx Xxxxxxxxxxxx. |
|
3. |
Xxxxxxx 1, 4: xxxxxx plná jména x xxxxxx (telefon, xxx, x-xxxx, xxxx-xx x xxxxxxxxx). |
|
4. |
Xxxxxxx 6: xxxxxx xxxx xxxxx x xxxxxx (xxxxxxx, xxx, x-xxxx, xxxx-xx x xxxxxxxxx) xxxxx xxxxxxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxxxxxx xx xx xxxxxxx xxxxxxx, např. xxxxxxxx, xxxxxxxxxxxxxxxxx, xxxxxxx xxxxxxxxxx. |
|
5. |
Xxxxxxx 8: xxxxxx xxxx xxxxx x xxxxxx xxxxxxxxx příjemce. Xxxxxxx xxxx být xxxxxxxx xxxxxxxxx. |
|
6. |
Xxxxxxx 7: xxxxxx xxxxx x xxxxxx (telefon, xxx, x-xxxx, xxxx-xx x xxxxxxxxx) xxxxxx xxxxx xxxx. |
|
7. |
Xxxxxxx 9: uveďte xxxxx členského xxxxx x přístavu, xxxxxxx xxxx xxxxxxxxxx xxxxxxxx. |
|
8. |
Xxxxxxx 10: xxxxxx xxxxxxx xxxxxxxx xxxxxxxxxx, které xxxx být xxxxxxx (xxxx. xxxxxxxx automobil, xxx, letadlo, xxxx xxx.). |
|
9. |
Xxxxxxx 11a, 11x: xxxxxx název xxxxxxx xxxxx, xxx xx xxxxxx v xxxxxxx xxxxxxxx (XX) x. 111/2005, nebo x xxxxxxx xxxxx xx xxxxxxxxxx produktu xxxxxx xxxxx x xxxxxxxxxx xxx XX směsi xx přírodního produktu. |
|
10. |
Kolonky 11x, 11x: xxxxxx xxxxxxx xxxxxx a xxxxx (xxxx. 2 xxxxxxxx po 5 xxxxxxx). X případě xxxxx, přírodního xxxxxxxx xxxx přípravků xxxxxx xxxxxxxxx xxxxxxxx název. |
|
11. |
Kolonky 12x, 12x: xxxxxx xxxxxxxxxx xxx XX xxxxxxx xxxxx, xxx xx xxxxxx x xxxxxxx xxxxxxxx (XX) x. 111/2005. |
|
12. |
Kolonka 16:
|


