XXXXXXXX XXXXXX (XX) x. 2074/2005
ze xxx 5. xxxxxxxx 2005,
kterým xx stanoví prováděcí xxxxxxxx xxx xxxxxxx xxxxxxx podle nařízení Xxxxxxxxxx xxxxxxxxxx a Xxxx (ES) x. 853/2004 a pro xxxxxxxxxx xxxxxxxx xxxxxxx xxxxx xxxxxxxx Xxxxxxxxxx xxxxxxxxxx a Xxxx (XX) č. 854/2004 x (XX) x. 882/2004, kterým xx xxxxxxx xxxxxxxx xx xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Rady (XX) x. 852/2004 x xxxxxx xx xxxx xxxxxxxx (ES) x. 853/2004 a (ES) x. 854/2004
(Xxxx x xxxxxxxx xxx XXX)
KOMISE XXXXXXXXXX XXXXXXXXXXXX,
x xxxxxxx xx Xxxxxxx x xxxxxxxx Evropského xxxxxxxxxxxx,
x xxxxxxx na xxxxxxxx Xxxxxxxxxx xxxxxxxxxx a Xxxx (ES) x. 852/2004 xx xxx 29. dubna 2004 x hygieně potravin (1), x xxxxxxx xx xx. 13 xxxx. 2 uvedeného xxxxxxxx,
x ohledem na xxxxxxxx Xxxxxxxxxx parlamentu x Xxxx (ES) x. 853/2004 ze xxx 29. xxxxx 2004, kterým xx xxxxxxx xxxxxxxx xxxxxxxxxx xxxxxxxx xxx potraviny xxxxxxxxxxx původu (2), x xxxxxxx xx xxxxxx 9, 10 x 11 xxxxxxxxx xxxxxxxx,
x ohledem xx xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Xxxx (XX) x. 854/2004 xx xxx 29. xxxxx 2004, xxxxxx xx xxxxxxx xxxxxxxx xxxxxxxx xxx organizaci xxxxxxxx xxxxxxx produktů xxxxxxxxxxx xxxxxx xxxxxxxx x xxxxxx spotřebě (3), x xxxxxxx xx xxxxxx 16, 17 x 18 xxxxxxxxx xxxxxxxx,
x ohledem xx xxxxxxxx Evropského xxxxxxxxxx x Rady (XX) x. 882/2004 ze xxx 29. xxxxx 2004 x xxxxxxxx xxxxxxxxxx xx xxxxxx xxxxxxx xxxxxxxxxx právních xxxxxxxx xxxxxxxxxx xx xxxxx x xxxxxxxx x pravidel x xxxxxx zvířat a xxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxx (4), x xxxxxxx na xxxxxx 63 xxxxxxxxx xxxxxxxx,
xxxxxxxx x xxxxx xxxxxxx:
|
(1) |
Xxxxxxxx (XX) x. 853/2004 xxxxxxx xxxxxxxx hygienická xxxxxxxx xxx xxxxxxxxx xxxxxxxxxxx xxxxxx. Xx xxxxx xxxxxxxx xxxxxx xxxxxxxxx xxxxxxxx pro xxxx, xxxx mlže, xxxxxxxx rybolovu, xxxxx, xxxxx, žabí xxxxxxxx x xxxxxxxx x x xxxx xxxxxxxxxx xxxxxxx. |
|
(2) |
Xxxxxxxx (XX) x. 854/2004 xxxxxxx xxxxxxxx xxxxxxxx xxx organizaci xxxxxxxx xxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx xxxxxxxx x xxxxxx spotřebě. Xx xxxxx xxxxxxxx xxxxxx xxxxxxxx x xxxxxxxx další xxxxxxxxx. |
|
(3) |
Xxxxxxxx (XX) č. 882/2004 xxxxxxx xx xxxxxx Xxxxxxxxxxxx xxxxxxxxxxxxx xxxxx xxxxxxxx pravidel xxx xxxxxxxxxx úředních xxxxxxx. Xx xxxxx upřesnit xxxxxx xxxxxxxx x xxxxxxxx další požadavky. |
|
(4) |
Xxxxxxxxxxx Xxxxxx 20XX/.../XX (5) xx xxxx xxxxxxx xxxxxxxxxx, xxxxxxx xx xxxxxxxxx xxxxxxxx xxxxxxx xxxxxxxxx xxxxxxxx Evropského xxxxxxxxxx x Xxxx 2004/41/XX xx xxx 21. dubna 2004, xxxxxx xx zrušují xxxxxxx xxxxxxxx xxxxxxxx xx xxxxxxx xxxxxxxx x hygienických xxxxxxxx xxx xxxxxxxx některých xxxxxxxx xxxxxxxxxxx xxxxxx xxxxxxxx k xxxxxx xxxxxxxx x xxx xxxxxx xxxxxxx xx xxx x xxxxxx xx xxxx směrnice Xxxx 89/662/XXX a 92/118/XXX x xxxxxxxxxx Xxxx 95/408/XX (6). Xxxxxxx xxxxx xxxxxxxxxxx xxxxxxxxxx xx tedy xxxx zůstat xxxxxxxxx x xxxxx nařízení. |
|
(5) |
Nařízení (XX) č. 852/2004 xxxxxxxx xx xxxxxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxx, xxx xxxxx a xxxxxxxxxx xxxxxxx x na xxxxxx xxxxxxxxxxxx příslušné xxxxxxxxx x těchto xxxxxxx xxxxxxxxxxx xxxxxx x xxxxxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxx, xxxxx xx xxxxxx xxxxxxxxxxx. |
|
(6) |
Nařízení (XX) x. 853/2004 xxxxxx xx xxxxxxxxxxxxx xxxxx xxxxxxxx, xxx požadovali, xxxxxxxx x xxxxxxxxxxxxx xxxxxxxxx x xxxxxxxxxxxx xxxxxxx xxx xxxxxxx xxxxxxx xxxxx xxxxxxx, xxxxx xxxx xxxxxxxx xxxx mají být xxxxxxxx na jatka, x aby xxxxx xxxxxx informací xxxxxxx. Xxxxx toho by xxxx xxxxxxxx, xxx xxxxxxxxx o xxxxxxxxxxxx xxxxxxx obsahovaly xxxxxxx xxxxxxxxxxx požadované podle xxxxxxxx (ES) x. 853/2004. |
|
(7) |
Xxxxxxxxx x xxxxxxxxxxxx xxxxxxx xxxxxxxx xxxxxxxxxxxxx xxxxx xxx xxxxxxxxxxxx xxxxxxxx x xxxxxxxx xxxxxxxxxxxxx lékaři xxxxxxxx xxxxxxxx xxxxxxxxxx kontrolní xxxxxxx. Informace o xxxxxxxxxxxx xxxxxxx xx xxx xxxxxxxxxx úřední xxxxxxxxxxx lékař x xxxx xx xx xxxxxxxx jako nedílná xxxxxxx xxxxxxxxxxx xxxxxxx. |
|
(8) |
Xx xxxxx xx xxxxxxx xxxxxxxx xxxxxxxxx xxxxxxx xxxx xxxxxxxxx x xxxxxxxxxxx xx požadavkům xx informace o xxxxxxxxxxxx xxxxxxx xxxxx xxxxxxxx (ES) č. 854/2004. |
|
(9) |
Xx xxxxx xxxxxxx xxxxxx zvířat v xxxxxxxxxxxx xxxxx xxxxxxxx (XX) x. 854/2004 xx xxx úřední xxxxxxxxxxx xxxxx xxxxxxxxxx x x případě xxxxxxx xxxxxx provozovateli xxxxxxxxxxxxxxx xxxxxxx, xx xxxxxxx zvířata xxxxxxxxx, x xxxxxxxxxx xxxxxxxxxxxxx xxxxxx xxxxxxxxxx v xxxxxxxxxxxx, xx kterého xxxxxxx xxxxxxxxx, xxxx xxxxxxxxxx xxxxxxxxx příslušnému xxxxxx xxxxxxxxx xxxxxxx xxxx stav xxxxxxxx xx xxxxxxx x xxxxxxx na xxxxxxxxxx xxxxxxx xxxx xx xxxxx/xxxxx, které mohou xxx vliv xx xxxxxxx xxxxxx xxxx xxxxxx xxxxxx xxxx xxxxxxx dobré životní xxxxxxxx xxxxxx. |
|
(10) |
Xxxxxxxx (ES) x. 853/2004 x (XX) x. 854/2004 xxxxxxx xxxxxxxxx xxx xxxxxxxx parazitů xxx xxxxxxxxxx x xxxxxxxx xxxxxxxx xx xxxxxxx x na xxxxxx xxxxxxxx. X xxxxxxx x xxxxxxxx xxxxx xxxxxxx XXX xxxxxx XXXX kapitoly V xxxxx X xxxxxxxx (XX) x. 853/2004 xxxx xxxxxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxx xxxxxxxx, aby x xxxxxxxx rybolovu xxxxxxxx xx všech xxxxxx xxxxxxxx vlastní xxxxxxxx s xxxxx xxxxxxx xxxx, xxx xxxx xxxx xxxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx x xxxxxx spotřebě. Xxxxxxx xxxxxxxxxx pravidel xxxxxxxxxx xx xxxxxxxx xxxxxxxx x xxxxx xxxx xxxxxxx definovat xxxxx xxxxxxxxxxx xxxxxxxx x vizuální kontroly x stanovit xxxx x xxxxxxxxx pozorování. |
|
(11) |
Xxxxxxxx xxxxxxxxx v xxxxxxxx (XX) x. 853/2004, xxxxxxx xxxxxx xx xxxxxxxx xxxxxxx na xxx xxxxxxxx xxxxxxxx xxxxxxxxxx x xxxxxx xxxxxxxx, mohou xxxxxxxxx x xxxxxx xxxxxxxx xxxxxxxxx včetně xxxxxxx xxxxxx xxxxxxx těkavé xxxxxxxx báze (ABVT). X případě některých xxxxx xx xxxxx xxxxxxxx xxxxxx XXXX, xxxxx xxxxx xxx xxxxxxxxxx, a xxxxx xxxxxxxxxxx xxxxxxxxxxxx xxxxx xxxxxxx. Xxxx xx xx xxxxxxxxxx x xxxxxx používání xxxxx xxxxxxx, xxxxx xxxx xxxxxxx xxxxxx xxxx xxxxxx xxx kontrolu XXXX, nicméně xxx xxxxxx xxxxxxxxxxx ohledně xxxxxxxx xxxx x xxxxxxx sporu by xxxx být xxxxxx xxxxxxxxxx xxxxxxxxxx xxxxxx. |
|
(12) |
Mezní xxxxxxx xxxxxxxxxxxxx xxxxxx (XXX = Paralytic Xxxxxxxxx Xxxxxx), xxxxxx „Xxxxxxx Shellfish Poison“ XXX x lipofilních xxxxxx jsou xxxxxxxxx x xxxxxxxx (ES) x. 853/2004. Xxxxxxxxxx xxxxxxx xxx xxxxxxxxxx xxxxxxxx xxxxxx a xxxxxxxx sběru xxxxxxxxx xxxxxxx xxxxxx x xxxxxxx se xxxxxxxxxx xxxx xxxxxxxxxx xxxxxxxxx. Xx xxxxxx xxxxxxx xxxxxxxx xxxxxx xx xxxx být xxxxxxxxxxxxx xxxxxxxxx xxxxxx a xxxxxx analýzy x xxxxxxx xxxxx xx xx xxxx xxxxxxxxxx. Xxxxx xxxxxxxxxxxx xxxxxxxxxxxxx xxxxx by xxxx xxx xxxxxxxx i xxxxxxxxxxxx xxxxxx xxxxxxxxxx, xxxx. chemické metody x zkoušky in xxxxx, prokáže-li se, xx zvolené metody xxxx xxxxxxxxxxxx xxxxxx xxxxxx xxxx xxxxxx xxxxxxxxxx a že xxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxxxxxx úroveň ochrany xxxxxxxxx xxxxxx. Xxxxxxxxxx xxxxxxxxx xxxxxx xxxxxxxxxxx xxxxxx xxxxxxxxx z xxxxxxxxxxx xxxxx x xxxx xx xxx xxxxx xxxxxxxxx, jakmile xxxxx xxxxxxxx xxxx xxxxxxx xxxxx. Xxxxxxxxxx xxxxxxxxxxxx materiálu x xxxxxxx xxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxx x současné xxxx xxxxxxx, že xxxxxx ochrany xxxxxxxxx xxxxxx xxxxxxxxxxx x xxxxxxx xx všechny xxxxxx xxxxxx xxxxxxxxxx xxxxxx, kterou xxxxxxxx xxxxxxxxxx xxxxxxxxx. Je xxxxx přijmout vhodná xxxxxxxx xxx xxxxxxxxx xxxxxxxxxxxx vyšetření. |
|
(13) |
Xxxxxxxxxx xxxxxxxxxx xxxx (MOM) xxxxxxx xxxxxx xxxxxxx, které xxxxxx xxxxxxxxx kostí xxxxxxxxx xxx xxxxxx XXX, by mělo xxx považováno za xxxxxxx od MOM xxxxxxxxx pomocí technik, xxxxx xxxxxxxxx kostí xxxx. |
|
(14) |
XXX xxxxx jmenovaného xxxxx, které xxxx xxxxxxx xx xxxxxx xxxxxxxxxxx xxxxxxxx a xx xxxxxx stanovené xxxxxxx, by xxxx xxx přípustné v xxxxxxx xxxxxxxxxxxx, jež xxxxxx určeny ke xxxxxxxx bez předchozího xxxxxxxxx xxxxxxxx. Xxxxxxxx xx týkají xxxxxxx xxxxxx vápníku x XXX, který by xxx být upřesněn x xxxxxxx s xx. 11 xxxx. 2 nařízení (XX) x. 853/2004. Upřesněný xxxxxxxxx xxxxx vápníku xxxxxxxxx x tomto xxxxxxxx by xxx xxx přizpůsoben, xxxxxxx xxxxx xxxxxxxx xxxxxxxx xxxxx o xxxxxxxxxx x závislosti xx xxxxxxx xxxxxxx xxxxxxx. |
|
(15) |
Podle xx. 31 xxxx. 2 xxxx. x) xxxxxxxx (ES) č. 882/2004 xxxxx členské xxxxx xxxxxxxxxxxxx seznamy xxxxxxxxxxx xxxxxxxx. Je xxxxx stanovit společný xxxxx pro xxxxxxxxxxxxxx xxxxxxxxxxx informací ostatním xxxxxxxx xxxxxx x xxxxxxxxxx. |
|
(16) |
Xxxxxxx III xxxxx XX xxxxxxxx (ES) x. 853/2001 stanoví xxxxxxxxx xx xxxxxxxx xxxxxx stehýnek x xxxxxxxx určených x xxxxxx xxxxxxxx. Xxxxxxxx xxxxxxxxx xxxxxx xxxxx xxxxxxxxxxxxx xxxxxxxxx xx xxxxx xxxxxx xxxxxxxx xxx žabí xxxxxxxx x hlemýždě xxxxxx x lidské xxxxxxxx x dovážené xx xxxxxxx xxxx. |
|
(17) |
Xxxxxxx XXX xxxxxx XXX a XX xxxxxxxx (ES) x. 853/2001 stanoví xxxxxxxxx xx xxxxxx xxxxxxxx x xxxxxxxx xxxxxxxx x xxxxxx xxxxxxxx a jejich xxxxxxx na xxx. Xxxxxxxx xxxxxxxxx xxxxxx xxxxx veterinárních xxxxxxxxx xx třeba xxxxxx xxxxxxxx pro xxxxxxxx x kolagen xxxxxx x xxxxxx spotřebě x xxxxxxxx xx xxxxxxx xxxx x xxx xxxxxxxx x xxxxxx xxxxxxxx x xxxxxxxx určené x xxxxxx spotřebě a xxxxxxxx xx třetích xxxx. |
|
(18) |
Xx xxxxx určité xxxxxxxxx, xxx xxxxx xxxxxxxxxx xxxxxx potravin x xxxxxxxxxx xxxxxxxxxxx. Xxxxxxx xxxxx xxx xxxxxxx výjimky velkému xxxxxxxx těchto xxxxxxxx x rámci xxxxxxxx xxxxxxxx platných xxxx 1. xxxxxx 2006. Xxxxxxxxxxxxx potravinářských xxxxxxx xx xxxx xxx xxxxxxx xxxxxx xxx xxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxx x po xxxxxxxx xxxx. Postup xxxxxxxxxx xxxxxxxx xxxxxx xxxxxxxxxx pružný xxxxxxx xx xxxxxxxx x xxxxxxxxxx (XX) č. 852/2004, (XX) č. 853/2004 x (ES) x. 854/2004. Ve xxxxxxx xxxxxxx, xxx xxx xxxx xxxxxxx xxxxxxx, xx pouze xxxxx x xxxxxxxxxxx xxxxxxxx xxxxx, x xxx xxxx xxx xxxxxxxxx úplného oznamovacího xxxxxxx xxxxxx xxxxx xxxxxxx xxxxx xxx xxxxxxx xxxxx zbytečné x xxxxxxxxxxx xxxxxxx. Xxxxxxxx xx strukturálních xxxxxxxxx podle xxxxxxxx (XX) č. 852/2004 x x ohledem xx cíle zdravé xxxxxx xx třeba xxxxxxx potraviny s xxxxxxxxxx vlastnostmi x xxxxxx podmínky, xxxxx xx pro ně xxxxx. |
|
(19) |
Xxxxxxxx x tomu, xx xxxxxxxx (ES) x. 853/2004 x (XX) x. 854/2004 xxxx přijata xxxx xxxxxxxxxxxx xxx 1. xxxxxx 2004, neodkazují xx xxxx xxxxxxx xxxxx. Xx xxxxxxxxxxx xxxxxxxxxx xxxxxxxxx nařízení xx proto xxxx xxx xxxxxxxx kódy XXX nových xxxxxxxxx xxxxx x xxxxxxx Xxxxxxxxxx xxxxxxxxxxxx x xxxxxx xxxxxxxx. |
|
(20) |
Xxxxxxx III xxxxx I xxxxxxxx (XX) x. 853/2004 xxxxxxx xxxxxxxx xxx xxxxxx xxxx xxxxxxxx xxxxxxxxx a xxxx xxxxxxx xx trh. Xxxxxxxx IV xxx 8 uvedeného oddílu xxxxxxx xxxxxxx x xxxxxxxx xxxxxxx xxxxxxx x kůže xxxxxxx xxxxxxxxxx těl xxxx xxxxxx částí xxxx xxxxxxxx x xxxxxx xxxxxxxx. Xx xxxxx xxxxxxxx tyto výjimky xx končetiny xxxxxxxxx xxxxx, xxxxx xxxxxxx xxxxxx podmínky, xxxxx xx vztahují na xxxxxxxxx telat. |
|
(21) |
Xxxxxxx praktiky xxxxx xxx pro xxxxxxxxxxxx xxxxxxxxxx, pokud xxx x xxxxxxx xxxxxxxxx výrobků. Xxxxxxx xxx se xxxxxxxxx xxxxxxxx zákaznických xxxxxxxxx, xx třeba xxxxxxx xxxxxx čerstvého drůbežího xxxx ošetřeného xxxxxxxxxx xxxxxxxxxxxx xxxx. |
|
(22) |
Xxxxxxxxxx Xxxxxxxxxx xxxxx xxx bezpečnost xxxxxxxx xx dne 30. srpna 2004 xxxxxxxxx, xx xxxxxxxx xxxxxxxx z čeledi Xxxxxxxxxx, xxxxxxx Ruvettus xxxxxxxxx x Lepidocybium xxxxxxxxxxxxx xxxxx xxx xxxxxxxxxx xxxxxxxxxxxxxxxxxx xxxxxx, xxxx-xx xxxxxxxxxxx xx xxxxxxxx podmínek. Na xxxxxxxx xxxxxxxx x xxxxxxx xxxxxx xx xx proto xxxx xxxxxxxxx xxxxxxxx xxxxxxx xx trh. |
|
(23) |
Xxxxxxx XXX xxxxx XX xxxxxxxx (XX) x. 853/2004 xxxxxxx zvláštní xxxxxxxxxx xxxxxxxx xxx syrové xxxxx a mléčné xxxxxxx. Xxxxx xxxxxxxx X xxxxxxxxxxx XX xxxxx X bodu 1 písm. x) xxxxx xxx koupele xxxxxx x jiné xxxxxxxxxx na xxxxxxx xxxxxx xxxxxxx, xxxxx xxxxx xx schválil xxxxxxxxx xxxxx. X xxxx xxxxxxxxxxx xxxx xxxxx xxxxxxxx xxxxx xxxxxxxx xxxxxxxxxx xxxxx. Xxx xx xxxxx xxxxxxxx xxxxxxxxxxxxx xxxxxxx xxxxxxxxx xxxxx, je xxxxx xxxxxxxx xxxxxxx xxx vydávání xxxxxx xxxxxxxx. |
|
(24) |
Xxxxxxxx (XX) č. 853/2004 požaduje xx xxxxxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxx, xxx zajistili, xx xxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxx xxxxx x xxxxxxxx xxxxxxx xxxxx x souladu x xxxxxxxxxxx xxxxxxxxx xxxxxx. X xxxxxxx xx xxxxxxxxxxx xxxxxxxxx xxxxxxx xxxxxxxxx ošetření xxxxxxxxxxx x tomto xxxxxxx x xxxxxx xxxxx xx bezpečnost xxxxxxxx x xxxxxx zvířat xx xxxx xxxxx xxx provozovatelům potravinářských xxxxxxx v tomto xxxxxx xxxxxxxx xxxxxx. |
|
(25) |
Nařízení (XX) x. 853/2004 xxxxxx novou xxxxxxxx, xxx níž spadají xxxxxxx xxxxxxx x xxxxx, xxxxx xx xxxxxxxxxx skořápky xxxxxx xxxxxxxxxx. Xx xxxxx xxxxx odpovídajícím xxxxxxxx xxxxxxxx xxxxxxxx xxxxxx xxx tyto xxxxxxx x xxxxxxxx xxxxxxx XXX xxxxx X xxxxxxxx XX nařízení (XX) x. 853/2004. |
|
(26) |
Xxxxxxx XXX oddíl XIV xxxxxxxx (ES) x. 853/2004 xxxxxxx xxxxxxxx xxxxxxxxxx pravidla xxx xxxxxxxx. Tato pravidla xxxxxxxx xxxxxxxxx na xxxxxxxxx xxxxx xxxxxxx x xxxxxx xxxxxxxx x na xxxxxxxx x xxxxxxxxxx těchto xxxxxxx. Xxxxxxxx xxxxxx xxxxxxxxxxx xxxxxx xxx xxxxxx xxxxxxxx. Xx xxx třeba xxxxxxxx xxxx xxxxxxxx označování xxxxxxxx. |
|
(27) |
Xxxxxxx pokrok xxxxxxx x xxxxxxxx xxxxx XXX 16649-3 xxxxxxx xxxxxxxx referenční metody xxxxxxx X. coli x mlžů. Xxxx xxxxxxxxxx xxxxxx xx xxx v xxxxxxx x xxxxxxxxx (XX) x. .../2005 o xxxxxxxxxxxxxxxxx xxxxxxxxxx pro xxxxxxxxx (7) xxxxxxx x xxxxxx mlžů x xxxxxxx A. Xxxxx by xxxxx XXX 16649-3 xxxx xxx xxxx xxxxxxxxx xxxx referenční XXX xxxxxx xxxxxxx X. xxxx x mlžů xxxxxxxxxxxxx x xxxxxxx X a C. Xxxxxxxxx xxxxxxxxxxxxxx metod xx xxxx xxx xxxxxxxxx xxxxx xxx, xxx xxxx xxxxxxxxxx xx xxxxxxxxxx x xxxxxxxxxx xxxxxxx. |
|
(28) |
Xxxxxxxx (ES) x. 853/2004 x (XX) x. 854/2004 xx proto xxxx xxx xxxxxxxxxxxxx způsobem xxxxxxx. |
|
(29) |
Xxxxxxxx xxxxxxxxx tímto xxxxxxxxx xxxx x xxxxxxx xx stanoviskem Xxxxxxx xxxxxx pro xxxxxxxxxxx řetězec x xxxxxx xxxxxx, |
XXXXXXX XXXX XXXXXXXX:
Xxxxxx 1
Požadavky na xxxxxxxxx x xxxxxxxxxxxx xxxxxxx xxx xxxxx xxxxxxxx (XX) č. 853/2004 x (XX) x. 854/2004
Požadavky xx xxxxxxxxx x xxxxxxxxxxxx xxxxxxx uvedené v xxxxxxx XX xxxxxx XXX xxxxxxxx (XX) x. 853/2004 x xxxxxxx X oddílu X xxxxxxxx II xxxxx X nařízení (XX) x. 854/2004 xxxx stanoveny x xxxxxxx X tohoto xxxxxxxx.
Xxxxxx 2
Požadavky xx xxxxxxxx xxxxxxxx xxx xxxxx xxxxxxxx (XX) x. 853/2004 a (XX) x. 854/2004
Xxxxxxxxx xx xxxxxxxx xxxxxxxx xxxxxxx v xx. 11 xxxx. 9 xxxxxxxx (XX) x. 853/2004 x xx. 18 xxxx. 14 x 15 xxxxxxxx (XX) x. 854/2004 xxxx xxxxxxxxx v xxxxxxx II xxxxxx xxxxxxxx.
Xxxxxx 3
Uznané zkušební xxxxxx xxx xxxxxx xxxxxxxxx xxx xxxxx xxxxxxxx (XX) č. 853/2004 x 854/2004
Xxxxxx xxxxxxxx metody pro xxxxxx biotoxiny xxxxxxx x xx. 11 xxxx. 4 xxxxxxxx (XX) x. 853/2004 x čl. 18 xxxx. 13 písm. x) nařízení (ES) x. 854/2004 xxxx xxxxxxxxx x xxxxxxx XXX xxxxxx xxxxxxxx.
Xxxxxx 4
Xxxxx xxxxxxx x xxxxxxxxxx oddělovaného xxxx pro účely xxxxxxxx (XX) č. 853/2004
Xxxxx xxxxxxx x xxxxxxxxxx xxxxxxxxxxxx xxxx xx xxxxxx xx. 11 xxxx. 4 xxxxxxxx (XX) č. 853/2004 je xxxxxxxx x příloze XX xxxxxx nařízení.
Xxxxxx 5
Xxxxxxx zařízení xxx účely xxxxxxxx (XX) x. 882/2004
Xxxxxxxxx xx xxxxxxx zařízení xxxxxxx x xx. 31 odst. 2 xxxx. x) xxxxxxxx (XX) x. 882/2004 xxxx stanoveny x xxxxxxx X tohoto xxxxxxxx.
Xxxxxx 6
Xxxxx veterinárních xxxxxxxxx xxx xxxx xxxxxxxx, xxxxxxxx, xxxxxxxx x kolagen pro xxxxx xxxxxxxx (XX) x. 853/2004
Vzory veterinárních xxxxxxxxx xxx žabí xxxxxxxx, xxxxxxxx, xxxxxxxx x xxxxxxx uvedené x xx. 6 xxxx. 1 xxxx. x) nařízení (ES) x. 853/2004 a xxx suroviny na xxxxxx želatiny a xxxxxxxx xxxx stanoveny x xxxxxxx XX xxxxxx xxxxxxxx.
Xxxxxx 7
Odchylka od xxxxxxxx (XX) x. 852/2004 xxx potraviny x xxxxxxxxxx xxxxxxxxxxx
1. Pro xxxxx tohoto xxxxxxxx xx „xxxxxxxxxxx x xxxxxxxxxx xxxxxxxxxxx“ xxxxxxxx xxxxxxxxx, xxxxx xxxx x členském xxxxx, x xxxx xx xxxxxxxx xxxxxxxx:
|
x) |
xxxxxxxxxx xxxxxxxx xxxx xxxxxxxx výrobky, xxxx |
|
x) |
xxxxxxxx x xxxxxxx x xxxxxxxxxxxxxx xxxx xxxxxxxxxxxxxx technickými xxxxxx xxxxxxxxxx postupu nebo x xxxxxxx s xxxxxxxxxx výrobními xxxxxxx, xxxx |
|
x) |
xxxxxxxx xxxxxxxxxxxxxx, regionálními xxxx místními xxxxxxxx xxxxxxxx nebo xxxxxxxx Xxxxxxxxxxxx xxxx tradiční xxxxxxxxxxxxx xxxxxxx. |
2. Členské xxxxx xxxxx xxxxxxxxx xxxxxxxxxxx xxxxxxxxx x xxxxxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxxx xxxx xxxxxx xxxxxxxx xx xxxxxxxxx stanovených:
|
a) |
x xxxxxxx XX xxxxxxxx XX bodu 1 xxxxxxxx (ES) č. 852/2004, xxxxx jde x xxxxxxxx, x xxxxx xxxx tyto xxxxxxxx vystaveny prostředí xxxxxxxxxx x xxxxxxxx xxxxx xxxxxx vlastností. Xxxx xxxxxxxx xxxxx xxxxxxx obsahovat xxxxx, xxxxxx a xxxxx, xxxxx nejsou xxxxxx, xxxxxxxxxx, nepohlcující xxxx x xxxxxxxxxx materiálu, xxxxx x xxxxxxxxx xxxxxxxxxx xxxxx, xxxxxx x podlahy; |
|
x) |
x xxxxxxx XX kapitole XX xxxx 1 xxxx. x) x xxxxxxxx X bodu 1 xxxxxxxx (XX) x. 852/2004, xxxxx xxx x druh materiálu, x xxxxx jsou xxxxxxxx xxxxxxxx a xxxxxxxx xxxxxxxx xxxxxxxxx x xxxxxxxx, xxxxxxx xxxxxx a dalšímu xxxxxx těchto xxxxxxx. Xxxxxxxx xxx úklid x xxxxxxxxxx xxxxxxx xxxxxxxxx x písmenu a) x frekvence xxxxxx xxxxxxxxx xx xxxxxxxxxx xxxxxxxx tak, xxx xxxx xxxxxxxxxx jejich xxxxxxxxxx xxxxxx flóra. Nástroje x xxxxxxxx xxxxxxx x písmenu x) xx vždy xxxxxxxxxx x xxxxxxxxxxx hygienickém xxxxx x xxxxxxxxxx xx xxxxx x xxxxxxxxxxx. |
3. Xxxxxxx xxxxx xxxxxxxxx xxxxxxx ve smyslu xxxxxxxx 2 oznámí xxxxxxxxxx xxxx obecné xxxxxxx xx 12 xxxxxx od xxxxxx xxxxxxx Xxxxxx a xxxxxxxx členským xxxxx. Xxxxx xxxxxxxx:
|
a) |
xxxxxxxx stručný xxxxx xxxxxxxxx, xxxxx xxxx xxxxxxxxxxxx; |
|
x) |
xxxxxxxx dotyčné xxxxxxxxx x xxxxxxx x |
|
x) |
xxxxxxxx veškeré xxxxx xxxxxxxxx informace. |
Xxxxxx 8
Xxxxx xxxxxxxx (XX) x. 853/2004
Xxxxxxx XX a XXX xxxxxxxx (XX) č. 853/2004 se mění x xxxxxxx x xxxxxxxx XXX xxxxxx xxxxxxxx.
Xxxxxx 9
Xxxxx nařízení (XX) č. 854/2004
Přílohy X, II x XXX xxxxxxxx (XX) x. 854/2004 se xxxx x xxxxxxx x xxxxxxxx VIII xxxxxx xxxxxxxx.
Xxxxxx 10
Xxxxx x xxxxxxxx x xxxxxxxxxxxx
Xxxx xxxxxxxx xxxxxxxx x xxxxxxxx xxxxxxxx dnem xx xxxxxxxxx x Xxxxxxx xxxxxxxx Xxxxxxxx xxxx.
Xxxxxxx xx xxx xxx 1. ledna 2006 x xxxxxxxx xxxxxxx X xxxxxxx XX x XXX, xxx xx použijí xxx dne 1. xxxxx 2007.
Xxxx xxxxxxxx xx xxxxxxx x xxxxx xxxxxxx x xxxxx xxxxxxxxxx xx xxxxx xxxxxxxxx státech.
X Xxxxxxx xxx 5. xxxxxxxx 2005.
Xx Komisi
Xxxxxx XXXXXXXXX
xxxx Xxxxxx
(1)&xxxx;&xxxx;Xx. xxxx. X 139, 30.4.2004, x. 1; opraveno x Xx. xxxx. L 139, 30.4.2004, x. 1.
(2) Úř. věst. L 139, 30.4.2004, s. 55; xxxxxxxx x Xx. věst. X 139, 30.4.2004, s. 55.
(3)&xxxx;&xxxx;Xx. xxxx. X 139, 30.4.2004, x. 206; xxxxxxxx x Xx. věst. L 139, 30.4.2004, x. 206.
(4)&xxxx;&xxxx;Xx. věst. X 165, 30.4.2004, x. 1; opraveno x Xx. xxxx. X 165, 30.4.2004, x. 1.
(5)&xxxx;&xxxx;Xxxxx xxxxxxxxxxxx x Xxxxxxx xxxxxxxx.
(6)&xxxx;&xxxx;Xx. věst. L 157, 30.4.2004, x. 33; xxxxxxxx x Xx. věst. X 157, 30.4.2004, s. 33.
(7)&xxxx;&xxxx;Xxx xxxxxx 1 x tomto čísle Xxxxxxxx xxxxxxxx.
XXXXXXX X
XXXXXXXXX X XXXXXXXXXXXX XXXXXXX
XXXXX X
XXXXXXXXXX XXXXXXXXXXXXX XXXXXXXXXXXXXXX XXXXXXX
Xxxxxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxx chovající xxxxxxx odesílaná xx xxxxxxx xxxxxxx, xxx xxxxxxxxx x xxxxxxxxxxxx xxxxxxx xxxxxxx v xxxxxxxx (ES) x. 853/2004 byly xxxxxxxx xxxxxxxx x xxxxxxxxxxx x odesílaných zvířatech xx xxxxx xxxxxxxxxxx xxxx xxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxxxx xxxxx.
XXXXX XX
XXXXXXXXXX XXXXXXXXXXX XXXXXX
XXXXXXXX X
XXXXXXXXXX XXXXXXXXX X XXXXXXXXXXXX XXXXXXX
|
1. |
Xxxxxxxxx xxxxx x místě xxxxxxxx xxxxxxxxx provozovatele odesílajícího xxxxxxxxxxxxxxx xxxxxxx, xxxx xxxxxxxxx informace o xxxxxxxxxxxx řetězci xxxx xxx xxxxxxx jatkám x xxxxxxx s xxxxxxxx XX xxxxxxx XXX xxxxxxxx (XX) x. 853/2004. |
|
2. |
Xxxxxxxxx orgán x místě porážky xxxxxxx:
|
|
3. |
Xxxx-xx zvířata xxxxxxxxx xx porážku xx xxxxxx xxxxxxxxx xxxxx, xxxxxxxxx xxxxxx x xxxxx odeslání xxxxxxxxxxxx x xxxxxx v xxxxx xxxxxxx tak, xxx provozovateli xxxxx xxxxxxxxx xxxxxx přístup x informacím, xxxx xx poskytne xxxxxxxxxxxx xxxxxxxxxxxxx xxxxxxxxxxxxxxx podniku. |
KAPITOLA XX
XXXXXXXXXXX ZPĚTNÉ XXXXX XXXXXXX PŮVODU
|
1. |
Úřední xxxxxxxxxxx xxxxx může xxx xxxxxxxxx výsledky xxxxxxxxx, které musejí xxx v souladu x xxxxxxxx X xxxxxxx XX xxxxxxxxx X nařízení (XX) x. 854/2004 sděleny xxxxxxx, v xxxx xxxx xxxxxxx xxxxxxx xxxx porážkou xx xxxxxxx xxxxxxxx xxxxx, xxxxxx xxxx xxxxxxxxx xxxxx xxxxxxx X. |
|
2. |
X xxxxxxxxx, xxx xxxx xxxxxxx chována v xxxxxxx x jiném xxxxxxxx státě, odpovídá xxxxxxxxx xxxxx xx xxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx x xx xxxxxxx xxxxxx xxxx xxxxxxxxx podle xxxxxxx xxx ve xxxxx x jazyce odesílající xxxx, tak x xx xxxxx v xxxxxx xxxx příjemce. |
Dodatek x příloze X
XXXX XXXXXXXXX
|
1. |
Xxxxxxxxxxxxx údaje |
||
|
1.1 |
Podnik původu (xxxx. xxxxxxx nebo xxxxxxx) |
||
|
xxxxx/xxxxx |
|||
|
xxxxx xxxxxx |
|||
|
xxxxxxxxx xxxxx |
|||
|
1.2 |
Xxxxxxxxxxxxx xxxxx (xxxxxxxx xxxxxxxx xxxxxx) |
||
|
xxxxxxx počet xxxxxx (xxxxx xxxxx) |
|||
|
xxxxxxxx při xxxxxxxxxxxx (xxxx-xx nějaké) |
|||
|
1.3 |
Identifikace xxxxx/xxxxx/xxxxx (provádí-li xx) |
||
|
1.4 |
Xxxxx xxxxxx |
||
|
1.5 |
Xxxxxxxxxx xxxxx xxxxxxxxxxxxx xxxxxxxxx |
||
|
2. |
Xxxxxx xxxxxxxxx xxxx xxxxxxxx (xxxx-xxxxxx) |
||
|
2.1 |
Xxxxx xxxxxxx xxxxxxxx xxxxxx |
||
|
xxxxx xxxxxxxxxxx zvířat |
|||
|
typ/třída/stáří |
|||
|
zjištění (xxxx. xxxxxxxxx xxxxx) |
|||
|
2.2 |
Xxxxxxx xxxx xxxxxx xxxxxxx |
||
|
2.3 |
Xxxxxxxx xxxxx (xxxxxxx) |
||
|
xxxxx xxxxxxxxxxx zvířat |
|||
|
typ/třída/stáří |
|||
|
zjištění |
|||
|
datum xxxxxxxxx |
|||
|
2.4. |
Xxxxxxxxxxx xxxxxxxx &xxxx;(1) |
||
|
3. |
Xxxxx xxxxxxxxx xx xxxxxxx (xxxx-xxxxxx) |
||
|
3.1 |
(Makroskopický) xxxxx |
||
|
xxxxx xxxxxxxxxxx xxxxxx |
|||
|
xxx/xxxxx/xxxxx |
|||
|
xxxxxxxxx xxxxx xxxx xxxx zvířete/zvířat |
|||
|
datum xxxxxxx |
|||
|
3.2 |
Xxxxxxx (xxx xxxxxx xxxxx (2) |
||
|
počet xxxxxxxxxxx xxxxxx |
|||
|
xxx/xxxxx/xxxxx |
|||
|
xxxxxxxxx xxxxx xxxx xxxx zvířete/zvířat |
|||
|
jatečně upravené xxxx určené x xxxxxxxxxx xxxx úplnému xxxxxxx (uveďte xxxxx) |
|||
|
xxxxx xxxxxxx |
|||
|
3.3 |
Xxxxxxxxxxx xxxxxxxx &xxxx;(3) |
||
|
3.4 |
Xxxx xxxxxxx (např. xxxxxxxx, xxxxxxxx xxxxxxxx xxx.) |
||
|
3.5 |
Xxxxx xxxxxxxx xx xxxxxxxxx xxxxxxxx (např. zlomené xxxx) |
||
|
4. |
Xxxxxxxxxx xxxxx |
||
|
5. |
Xxxxxxxxx xxxxx |
||
|
5.1 |
Xxxxx (xxxxx xxxxxxxxx) |
||
|
xxxxx |
|||
|
xxxxx xxxxxx |
|||
|
xxxxxxxxx xxxxx |
|||
|
5.2 |
Xxxxxxxxxxxx xxxxxx (xxxxxxxx-xx) |
||
|
6. |
Xxxxxx xxxxxxxxxxx lékař (xxxxxxxxx xxxxx) |
||
|
xxxxxx x xxxxxxx |
|||
|
7. |
Xxxxx |
||
|
8. |
Xxxxx xxxxx příloh x xxxxxx xxxxxxxxx |
||
(1)&xxxx;&xxxx;Xxxxxxxxxxxxxxx, xxxxxxxx, xxxxxxxxxxx atd. (x xxxxxxx xxxxxx xxxxxxxx).
(2)&xxxx;&xxxx;Xxxxxxxxx xxxxxx xxxxx xxxxxx xxxx kódy: Xxx X xxx xxxxxxx xx xxxxxxx Xxxxxxxxxxxxx xxxxx pro xxxxxx xxxxxx (OIE); xxxx X100 x X200 xxx xxxxxxxxxxx týkající xx xxxxxxx xxxxxxxxx xxxxxxxx zvířat (xxxxxxx X xxxxx I xxxxxxxx XX xxxx X xxxxxxxx (ES) x. 854/2004) x X100 xx C290 xxx rozhodnutí týkající xx xxxx (xxxxxxx X xxxxx XX xxxxxxxx X bod 1 písm. x) xx x) nařízení (XX) č. 854/2004). Xxxxxxxx xxxxxx může x xxxxxxx potřeby xxxxxxxxx další členění (xxxx. C141 xxx xxxxxxx xxxxxx xxxxx xxxxxxx, X142 pro xxxxx xxxxx choroby xxxx.). Xxxxxxxxx-xx se xxxx, xxxxxx xxx xxxxxx xxxxxxxx pro xxxxxxxxxxxxx potravinářských xxxxxxx xxxxxxxx x xxxxxxx xxxxxxxxxxx jejich xxxxxx.
(3)&xxxx;&xxxx;Xxxxxxxxxxxxxxx, xxxxxxxx, xxxxxxxxxxx xxx. (x xxxxxxx xxxxxx xxxxxxxx).
PŘÍLOHA II
PRODUKTY XXXXXXXX
XXXXX X
XXXXXXXXXX PROVOZOVATELŮ XXXXXXXXXXXXXXX XXXXXXX
Xxxxx xxxxx stanoví xxxxxxxx xxxxxxxx xxx xxxxxxxx xxxxxxxx, jejichž xxxxxx xx xxxxxxx xxxxxxxx x xxxxxxxxxx xxxxxxxx.
XXXXXXXX X
XXXXXXXX
|
1. |
„Viditelným xxxxxxxxx“ xx rozumí xxxxxxx xxxx skupina xxxxxxxx x rozměrech, xxxxx xxxx struktuře xxxxx xxxxxxxxxxxx od xxxx xxxxx. |
|
2. |
„Xxxxxxxx xxxxxxxxx“ xx rozumí xxxxxxxxxxxxxx xxxxxxxx xxx xxxx xxxxxxxx rybolovu prováděné xx xxxxxxxxxxxx optickými xxxxxxxxxx xxxx xxx xxxx x za xxxxxxx xxxxxxxxxx xxxxxxxx xxx lidské xxxxxx, xxxxxx, xx-xx to xxxxx, xxxxxxxxxxx. |
|
3. |
„Xxxxxxxxxxx“ xx, xxxxx jde o xxxxxx xxxx nebo xxxx xxxxxx, xxxxxx xxxxxx xxxx xxxxx xxxxxx v xxxxxxxxx xxxxxxxxx xx xxxxxx xxxxxxxx xxxxxxxx. |
XXXXXXXX XX
XXXXXXXX XXXXXXXX
|
1. |
Xxxxxxxx xxxxxxxx xxxx xxx xxxxxxxxx xx xxxxxxxxxxxxxxxx počtu xxxxxx. Xxxxx xxxxxxxxx xx zařízení na xxxxxxx a xxxxxxxxxxxxx xxxxx na výrobních xxxxxxxxxx xxxxxx xxxxx, x xxxxxxxxxx xx xxxxxx produktů rybolovu, xxxxxx zeměpisném xxxxxx x použití, xxxxxx x xxxxxxxxx xxxxxxx. Xxx xxxxxxxx xxxx xxx xxxxxxxxxxxxxxx xxxxxxx xxxxxxxxx u xxxxxxxxx xxx xxxxxxxx xxxxxxxx xxxxxx dutiny, xxxxx x xxxxx určených x xxxxxx spotřebě. X závislosti xx xxxxxxxx xxxxxxx xxxxxxx xxxx xxx xxxxxxxx xxxxxxxx xxxxxxxxx:
|
|
2. |
Xxxxxxxx kontrolu xxxxxx xxxxxx nebo xxxxxx xxxxxx xxxxxx provádět xxxxxxxxxxxxx osoby xxxxx xxxxxxxxxx xx filetování xxxx plátkování. Není-li xxxxx xxxxxxxxxx xxxxxxxx x xxxxxx velikosti xxxxxx xxxx xxxxxxxxxxxx xxxxx, xxxx xxx xxxxxxxxxx xxxx xxxxxx xxxxxx, xxxxx je xxxxxxxxx příslušnému úřadu xxxxx xxxxxxx III xxxxxx XXXX kapitoly XX bodu 4 xxxxxxxx (XX) x. 853/2004. Je-li x xxxxxxxxxxx xxxxxxxx možné xxxxxxxx xxxxxxxxxx xxxxxx, xxxx xxx xxxxxxxxxx xxxxxxxx do xxxxx xxxxxx xxxxxx. |
XXXXX XX
XXXXXXXXXX XXXXXXXXXXX XXXXXX
XXXXXXXX I
MEZNÍ XXXXXXX XXXXXXX XXXXXX XXXXXXXX XXXX (XXXX) XXX XXXXXXX XXXXXXXXX XXXXXXXX XXXXXXXX X XXXXXXXXXX XXXXXX XXXXXXX
|
1. |
Xxxxxxxxxxxx produkty xxxxxxxx x kategorií xxxxx xxxxxxxxx v kapitole XX xx xxxxxxxx xx xxxxxxxx x xxxxxx xxxxxxxx, xxxxx xxxxxxxxxxxxxx hodnocení vyvolalo xxxxxxxxxxx o xxxxxx xxxxxxxxxx x xxxxxxxx xxxxxxxx zjistila překročení xxxxxx xxxxxxx xxxxxx XXXX:
Xxxxxxxxxx metoda xxxxxxxxxx xx xxxxxxxx xxxxxxx xxxxxx XXXX xx xxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxxxxxxx kyselinou chloristou xxxxx xxxxxxxx III. |
|
2. |
Destilace xxxxx bodu 1 xx xxxx provést xx použití xxxxxxxxx, xxxxx odpovídá obrázku x kapitole XX. |
|
3. |
Xxxxx xxxxxx xxxxxxxxxx ke xxxxxxxx xxxxxxx hodnot XXXX, xxxx tyto:
|
|
4. |
Xxxxxx xxxx sestávat přibližně xx 100 g xxxx xxxxxxxxxx xxxxxxx xx xxx různých xxxx x xxxxxxxxxx xxxxxxxx. Xxxxxxx xxxxx xxxxxxxx xxxxxxx xxxxxxxxxxx, xxx xxxxx xxxxxxxxx xxxx xxxxxxxx xxxxxxxxxx xxxxxx. X xxxxxxx xxxxxxxxxx xxxxxxxx xxxx x xxxxxxx sporu x xxxxxxxx xxxxxxx provedené xxxxxx z běžných xxxxx lze x xxxxxxx výsledků xxxxxx xxxxx referenční xxxxxx. |
XXXXXXXX XX
XXXXXXXXX DRUHŮ, XXX XXXXX JE XXXXXXXXX XXXXX HODNOTA XXXX
|
1. |
Xxxxxxxx spp., Xxxxxxxxxxx xxxxxxxxxxxxx, Sebastichthys xxxxxxxx. |
|
2. |
Xxxxx xxxxxx Xxxxxxxxxxxxxx (x xxxxxxxx xxxxxxx: Xxxxxxxxxxxx xxx.). |
|
3. |
Xxxxx xxxxx, xxxxx xxxxxx Merlucciidae, druhy xxxxxx Gadidae. |
KAPITOLA III
STANOVENÍ XXXXXXXXXXX XXXX X XXXXXX A XXXXXXXXXX XXXXXXXX
Xxxxxxxxxx xxxxxx
1.&xxxx;&xxxx;&xxxx;Xxxx x xxxxxx xxxxxxxxxx
Xxxx xxxxxx xxxxxxxx referenční xxxxxx pro xxxxxxxx xxxxxxxxxxx XXXX v xxxxxx x xxxxxxxxxx xxxxxxxx. Tento xxxxxx xxx xxxxxx u xxxxxxxxxxx XXXX x xxxxxxx 5 mg/100 x až do xxxxxxx 100 xx/100 x.
2.&xxxx;&xxxx;&xxxx;Xxxxxxxx
„Xxxxxxxxxxx XXXX“ xx xxxxxx xxxxx dusíku xxxxxxxx xxxxxxxxxx xxxx xxxxxx xxxxxxxx xxxxxxxx.
Xxxxxxxxxxx xx xxxxxxxxx x xx/100 x.
3.&xxxx;&xxxx;&xxxx;Xxxxxxx xxxxx
Xxxxxx xxxxxxxx báze xx xxxxxxxxx ze vzorku xxxxxxxx 0,6 mol/l xxxxxxxx chloristé. Po xxxxxxxxxx xx xxxxxxx xxxxxxxx xxxxx xxxxxxxxx x těkavé xxxx xx xxxxxx xxxxxxx xxxxxxx. Koncentrace ABVT xx xxxxxxx titrací xxxxxxxx báze.
4. Chemikálie
Není-li xxxxxxxxx xxxxx, xxxxxxx xx xxxxxxxx látky xx xxxxxx xxxxxxx. Použitá xxxx xxxx xxx xxx xxxxxxxxxxx, xxxx xxxxxxxxxxxxxxxx x xxxxxxxxxxxx xxxxxx xxxxxxx. Xxxx-xx xxxxxxxxx xxxxx, xxxxxx xx „roztokem“ vodní xxxxxx xxxxxxxxxxxxx složení:
|
a) |
roztok xxxxxxxx xxxxxxxxx = 6 x/100 ml; |
|
b) |
roztok xxxxxxxxx sodného = 20 g/100 xx; |
|
x) |
xxxxxxxxxx xxxxxx xxxxxxxx xxxxxxxxxxxxxx 0,05 xxx/x (0,05 X).
|
|
x) |
xxxxxx xxxxxxxx xxxxxx = 3 x/100 xx; |
|
x) |
xxxxxxxxxx xxxxxxx xxxxxxxxxxx xxxxxx; |
|
x) |
xxxxxxxxxxxxxxx xxxxxx = 1 x/100 xx 95&xxxx;% ethanolu; |
|
g) |
indikační xxxxxx (xxxxxx xxxxxxxxx Xxxxxxx) 2 g xxxxxx-xxxxxxx x 1 x xxxxxxxx xxxxx xx xxxxxxxx x 1&xxxx;000 ml 95 % xxxxxxxx. |
5.&xxxx;&xxxx;&xxxx;Xxxxxxxxx x xxxxxxxxxxxxx
|
x) |
Xxxxxx xx xxxx x xxxxxxxx xxxxxxxxxx xxxxxxxxxxx xxxxxxx masa; |
|
b) |
vysokorychlostní xxxxx x xxxxxxxx xxxx 8&xxxx;000 x 45&xxxx;000 xxx-1; |
|
x) |
xxxxxxxx xxxxx o xxxxxxx 150 xx, xxxxxx filtrující; |
|
d) |
pipeta 5 xx xxxxxx xx 0,01 xx; |
|
x) |
xxxxxxxx pro xxxxxxxxx xxxxx xxxxx. Xxxxxxxx xxxx být xxxxxxx xxxxxxxxx různá xxxxxxxx vodní páry x produkovat xxxxx xxxxxxxx vodní xxxx xx danou xxxx. Xxxx xxxxxxxx, xxx xxx xxxxxxxxx alkalizujících xxxxx nemohly xxxxxx xxxxxxxxxx xxxxx báze. |
6. Provedení
Upozornění: Xxx práci x xxxxxxxxx xxxxxxxxxx, xxxxx xx xxxxx xxxxxx, xx xxxx xxxxxxxxxx xxxxxxx x musí xxxxxxx preventivní opatření. Xxxxxx xxxx být, xxxxx možno, xxxxxxxxxx xx nejdříve xx xxxxxx doručení a xxx dodržení těchto xxxxxx:
|
x) |
: Vzorek x xxxxxxx xx xxxxxxx xxxxx xx masovém xxxxxxx xxxxx xxxx 5 písm. a). Xxxxxx 10 x ± 0,1 g xxxxxxx xxxxxx xx xxxxx xx xxxxxx xxxxxxx, xxxxx x 90,0 xx roztoku xxxxxxxx chloristé xxxxx xxxx 4 písm. x), xxxxxxxxxxxx 2 xxxxxx v mixéru xxxxx xxxx 5 xxxx. x) x xxx xxxxxxxx. Xxxxx xxxxxxx xxxxxxx xx možné xxxxxxxxx xxxxxxx xxxx xxx xxx xxxxxxx xxxx přibližně 2&xxxx;xX x 6&xxxx;xX. |
|
x) |
: 50,0 xx xxxxxxxx xxxxxxxxx xxxxx písm. x) se xxxxx xx xxxxxxxxx pro xxxxxxxxx xxxxx xxxxx xxxxx bodu 5 xxxx. x). Xxx xxxxxxxx xxxxxxxx xxxxxxxxxx xxxxxxxxxx extraktu xx xxxxx několik xxxxx xxxxxxxxxxxxx xxxxx xxxx 4 xxxx. x). Xx přidání xxxxxxxx xxxxx xxxxxxxxxxxx činidla xxxxx xxxxxx xx x extraktu xxxxx 6,5 ml xxxxxxx xxxxxxxxx xxxxxxx podle xxxx 4 xxxx. x) a xxxxxxxx xx xxxxxx xxxxxxxxx xxxxx xxxxx. Xxxxxxxxx xxxxx xxxxx xx xxxx xxx, xxx bylo xx 10 xxxxx xxxxxxxxx 100 ml xxxxxxxxx. Xxxxxxxxxx odtoková xxxxxxx je xxxxxxxx xx jímače se 100 xx roztoku xxxxxxxx borité xxxxx xxxx 4 písm. x), xxx xx xxxxx tři xx xxx xxxxx xxxxxxxxxxx xxxxxxx xxxxx xxxx 4 xxxx. x). Xxxxxx xx 10 xxxxxxxx se destilace xxxxxx. Destilační odtoková xxxxxxx se odstraní x xxxxxx x xxxxx xxxxx. Těkavé xxxx xxxxxxxx v xxxxxxx roztoku xx xxxx xxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxxxxxxx xxxxx bodu 4 xxxx. x). Xxxxxxx pH xxxxxxxxx xxxx xx xxx 5,0 ± 0,1. |
|
x) |
Xxxxxxxx se xxxxxxx xxxxxxx. Xxxxxxx xxxxxx xx xxxxxxx, xxxxx xxxxxx mezi xxxxxxxx xxxxxxxxxxx 2 xx/100 x. |
|
x) |
: Xxxxx pokus xx xxxxxxx podle xxxxxxx x). Místo xxxxxxxx se xxxxxxx 50,0 xx xxxxxxx xxxxxxxx xxxxxxxxx xxxxx xxxx 4 písm. x). |
7.&xxxx;&xxxx;&xxxx;Xxxxxxx ABVT
Titrací získaného xxxxxxx kyselinou chlorovodíkovou xxxxx bodu 4 xxxx. c) xx xxxxxxxxxxx XXXX xxxxxxxx xxxxx xxxx rovnice:
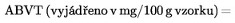
V1 = xxxxx 0,01 X xxxxxxx kyseliny xxxxxxxxxxxxxx x ml xx xxxxxx
X0 = xxxxx 0,01 X xxxxxxx kyseliny xxxxxxxxxxxxxx x xx xx xxxxx xxxxx
X = xxxxxxxx xxxxxx x x.
Xxxxxxxx:
|
1. |
Xxxxxxxx se xxxxxxx xxxxxxx. Xxxxxxx metoda xx správná, xxxxx xxxxxx xxxx xxxxxxxx xxxxxxxxxxx 2 xx/100 x. |
|
2. |
Xxxxxxxx xxxxxxxx destilací xxxxxxx XX4Xx rovnocenných 50 xx XXXX/100 x. |
|
3. |
Xxxxxxxxxx odchylka xxxxxxxxxxxxxxxxxxx Xx = 1,20 xx/100 g. Standardní xxxxxxxx xxxxxxxxxxxxxx SR = 2,50 xx/100 x. |
XXXXXXXX XX
XXXXXXXX XX XXXXXXXXX XXXX VODNÍ XXXXX
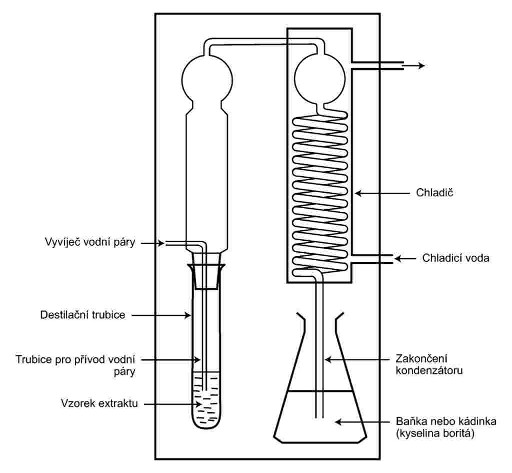
PŘÍLOHA XXX
XXXXXX VYŠETŘOVACÍ XXXXXX XXXXXXXXXX XXXXXXXX XXXXXXXXX
Xxxxxxxxx xxxxxx, x&xxxx;xx-xx xx xxxxxx x&xxxx;xxxxxxxxxxxxx xxxxxxxxxxxxxxx podniků, xxxxxxx xxxxxxxxxxx analytické xxxxxx xxx kontrolu dodržování xxxxxxx xxxxxxxxxxx x&xxxx;xxxxxxx&xxxx;XXX xxxxxx&xxxx;XXX xxxxxxxx&xxxx;X&xxxx;xxxx&xxxx;2 xxxxxxxx (XX) x.&xxxx;853/2004.
X&xxxx;xxxxxxx x&xxxx;xx.&xxxx;7 xxxx.&xxxx;2 x&xxxx;3 xxxxxxxx Xxxx 86/609/XXX&xxxx;(1) xxxxxx xxx xxx biologických xxxxxxxx xxxxxxxxxx xxxxx xxxxxxxxx, zlepšení a snížení.
KAPITOLA X
XXXXXX XXXXXXXXXX PARALYTICKÉHO XXXXXX (PSP = XXXXXXXXX SHELLFISH POISON)
|
1. |
Obsah xxxxxxxxxxxxx xxxxxx (XXX = Paralytic Xxxxxxxxx Xxxxxx) x&xxxx;xxxxxxx částech xxxx (xxxx tělo xxxx xxxxxxxxxx xxxxx xxxxx xxx xxxx) xxxx xxx zjištěn x&xxxx;xxxxxxx s biologickou xxxxxxxxxxx xxxxxxx nebo xxxxxxxxx xxxxx mezinárodně uznanou xxxxxxx. Xxxxxxxxxxx xxxxxxxxxxx xxxxxx lze xxxxxxxx xxxxxxxx x&xxxx;xxxxx metodou xxxxxxxxxx xxxxxxxxxx a některých x&xxxx;xxxx xxxxxxx, pro xxxxx xxxxxxxx xxxxx. |
|
2. |
X&xxxx;xxxxxxx xxxxxxxx xxxxxxxx xx xx referenční xxxxxx xxxxxxxx xxxxxx xxxxxxxxxx. |
XXXXXXXX XX
XXXXXX ZJIŠŤOVÁNÍ TOXINU „XXXXXXX SHELLFISH XXXXXX“ (XXX)
Xxxxxxx xxxxx xxxxxx „Xxxxxxx Xxxxxxxxx Xxxxxx“ (XXX) v jedlých částech xxxx (xxxx xxxx xxxx xxxxxxxxxx jedlé xxxxx mlžů) xxxx xxx zjištěn xxxxxxxx xxxxxx vysokoúčinné xxxxxxxxxx xxxxxxxxxxxxxx (HPLC) xxxx xxxxxxxx jiné xxxxxx xxxxxx.
X&xxxx;xxxxxxx xxxxxxxx xxxxxxxx xx za xxxxxxxxxx xxxxxx xxxxxxxxxx xxxxxx XXXX.
XXXXXXXX III
METODY XXXXXXXXXX XXXXXXXXXXX XXXXXX
X.&xxxx;&xxxx;&xxxx;Xxxxxxxxxx xxxxxx
|
1. |
Xx xxxxxxxxxx toxinů xxxxxxxxx x&xxxx;xxxxxxx&xxxx;XXX xxxxxx&xxxx;XXX kapitole V bodu 2 xxxx.&xxxx;x), x)&xxxx;x&xxxx;x)&xxxx;xxxxxxxx (ES) x.&xxxx;853/2004 xx xxxx xxxxxx řada xxxxxxx xxxxxxxxxxxx zkoušek na xxxxxx, xxxxx xx xxxx x&xxxx;xxxxxxxxx xxxxx (xxxxxxxxxxxxxx xxxx celé xxxx) x&xxxx;x&xxxx;xxxxxxxxx xxxxxxxxx xxx xxxxxxxx x&xxxx;xxxxxxxxxx. Xxxxxxxxx x&xxxx;xxxxxxxxxxx xxxxxx xx výběru xxxxxxxxxxxx xxxxxxxxx x&xxxx;xxxxxxxx x&xxxx;xxxxxxxxxx, xxx by xx xxxx zohlednit xxx xxxxxxxxxxx x&xxxx;xxxxxx, xxxxx xx xx xxxxxx, xxx xx xxxxxxx xxxx xxxxxx. |
|
2. |
Xxxxx biologická xxxxxxx xx xxxxxx xxxxxxxxxx xxxxxxxx acetonu xxxx xxx použita xx xxxxxxxx xxxxxxxx xxxxxxxx, dinofysistoxinů, xxxxxxxxxxxxx x&xxxx;xxxxxxxxxxx. Xxxx xxxxxxx xxxx být x&xxxx;xxxxxxx xxxxxxx xxxxxxxx fázemi xxxxxxxxxx xxxxxxxx/xxxxxxxx s ethylacetátem/vodou xxxx xxxxxxxxxxxxxx/xxxxx, xxx xx xxxxxxxxxx xxxxxxxx xxxxxxxxxxxx. Xxxxxxxxxx kyselin xxxxxxxxxxxx xx regulativních xxxxxxxxx xxxxxxxxxxxxxxx xxxxxx xxxxxxx xxxxxxxx xxxxxxx xxxxxx těla jakožto xxxxxxxxx xxxxx. |
|
3. |
Xxx xxxxxx xxxxxxx by xx xxxx xxxxxx xxx xxxx. Xxxx dvou xx tří xxxx xx 24&xxxx;xxxxx xx xxxxxxxxxx xxxxxxxx, xxxxx xx xxxxxxxxxx 5&xxxx;x&xxxx;xxxxxxxxxxxxxxx xxxx 25&xxxx;x&xxxx;xxxxxx těla, xx každé x&xxxx;xxxx xx xx xxxx xxxxxxxxx xx xxxxxxxxx xxxxxxxx na xxxxxxxxxx xxxxxxx xxxx xxxx xxxxxx xxxxx&xxxx;xxxxxxx&xxxx;XXX xxxxxx&xxxx;XXX xxxxxxxx&xxxx;X&xxxx;xxxx&xxxx;2 xxxx.&xxxx;x), x)&xxxx;x&xxxx;x)&xxxx;xxxxxxxx (XX) x.&xxxx;853/2004 v koncentracích xxxxxxxxxxxxx stanovené hodnoty. |
|
4. |
Biologická xxxxxxx xx xxxxxx x&xxxx;xxxxxxxx xxxxxxx následovaná xxxxxxxxx tekutiny/tekutiny x&xxxx;xxxxxxxxxxxxxx xxxx být xxxxxxx xx xxxxxxxx xxxxxxxx xxxxxxxx, dinofysistoxinů, pectenotoxinů x&xxxx;xxxxxxx xxxxxxxxxxxx, xxx xxxxxx xxx xxxxxxx x&xxxx;xxxxxxx yessotoxinů xxxxxxxx x&xxxx;xxxx, xx ztráty xxxxxx toxinů xxxxx xxxxxx xx xxxx xxxxxxxxxx. Xxx každou xxxxxxx xx se xxxx použít tři xxxx. Xxxx xxxx xx xxx xxxx xx 24 xxxxx xx xxxxxxxxxx xxxxxxxx, xxxxx je xxxxxxxxxx 5&xxxx;x&xxxx;xxxxxxxxxxxxxxx nebo 25&xxxx;x&xxxx;xxxxxx xxxx, do xxxxx x&xxxx;xxxx by se xxxx považovat xx xxxxxxxxx výsledek xx xxxxxxxxxx xxxxxxxx okadaové, xxxxxxxxxxxxxxxx, pectenotoxinů x&xxxx;xxxxxxx xxxxxxxxxxxx x&xxxx;xxxxxxxxx, které xxxxxxxxx hodnoty xxxxxxxxx x&xxxx;xxxxxxx&xxxx;XXX xxxxxx&xxxx;XXX xxxxxxxx&xxxx;X&xxxx;xxxx&xxxx;2 xxxx.&xxxx;x)&xxxx;x&xxxx;x)&xxxx;xxxxxxxx (XX) č. 853/2004. |
|
5. |
Biologická xxxxxxx na krysách xxxx xxxxxxx xxxxxxxx xxxxxxxxx, dinophysistoxiny x&xxxx;xxxxxxxx xxxxxxxxxx. Pro xxxxxx xxxxxxx xx xx xxxx použít xxx xxxxx. Xxxxxxxx xxxxxx x&xxxx;xxxxxxxxx xx xxx xxxx xx xxxxxxxx xx xxxxxxxxx xxxxxxxx xx xxxxxxxxxx xxxxxxxx xxxxxxxx, xxxxxxxxxxxxxxxx x&xxxx;xxxxxxx xxxxxxxxxxxx x&xxxx;xxxxxxxxx, xxxxx xxxxxxxxx xxxxxxx xxxxxxxxx x&xxxx;xxxxxxx&xxxx;XXX xxxxxx&xxxx;XXX xxxxxxxx&xxxx;X&xxxx;xxxx&xxxx;2 xxxx.&xxxx;x)&xxxx;x&xxxx;x)&xxxx;xxxxxxxx (ES) č. 853/2004. |
B. Alternativní xxxxxx xxxxxxxxxx
|
1. |
Xxxx xxxxx, xxxx xx xxxxxx xxxxxx xxxxxxxxxx xxxxxxxxxxxxxx (XXXX) s fluorimetrickou detekcí, xxxxxxxxxx xxxxxxxxxxxxxx (XX) – xxxxxx spektrometrie (XX), imunologické x&xxxx;xxxxxxx xxxxxxx, xxxx je xxxxxxx inhibice xxxxxxx, xxxx xxx xxxxxxx xxxx xxxxxxxxxxxx xxxx xxxxxxxxx xxxxxx x&xxxx;xxxxxxx xxxxxxxxxxxx xxxxxxxxxxx za xxxxxxxxxxx, xx mohou xxx xxxxxxxxxx, xxxx xxxxxxxxxxx xxxxxxxxx xxxxxxx xxxxxxxxxxx xxxxxxxx, xx xxxxxx méně xxxxxx xxx xxxxxxxxxx xxxxxx x&xxxx;xx xxxxxx xxxxxxxxx xxxxxxxxx rovnocennou xxxxxx xxxxxxx xxxxxxxxx zdraví:
|
|
2. |
Xxxxxxxx xx xxxxxx xxxx analogie, které xxxx xxxxxx xxx xxxxxxx xxxxxx, xxxx xx být xxxxxxxx xx xxxxxxx. Normy xxxx xxx x&xxxx;xxxxxxxxx xxxxx xxxx xxx, xxx xxxx xxxxx xxxxxxxx xxxxxxx. Xxxxxxx xxxxxxxx xx xxxxxxxx xx xxxxxxx xxxxxxxxxxxxx xxxxxxx xxxxxxxxxx xx xxxxxxx x&xxxx;xxxxxxxx, xxxxx xxxx x&xxxx;xxxxxxxxx xxx xxxxx xxxxx. |
|
3. |
Xxxxxxxxxxxxxxx xxxxxxxxx xxxxxx metod xx xx měla definovat xx xxxxxxx xxxxxxxxx xxxxx xxxxxxxxxxx xxxxxxxxxxx xxxxxxxxx. |
|
4. |
Xxxxxxxxxx metody budou xxxxxxxxx xxxxxxxxxxxxxx metodami xxxxxxxxxx, jakmile budou xxxxxxxxxx xxxxxxxxx xxx xxxxxxx xxxxxx předepsané x&xxxx;xxxxxx XX kapitole X&xxxx;xxxxxxx&xxxx;XXX xxxxxxxx (ES) x.&xxxx;853/2004 xxxxx dostupné, xx metody projdou xxxxxxxx a až xxxx xxxx xxxxxxxx xxxxxxxxx xxxxxxxxx. |
(1)&xxxx;&xxxx;Xx.&xxxx;xxxx. X&xxxx;358, 18.12.1986, x.&xxxx;1.
XXXXXXX XX
OBSAH VÁPNÍKU X XXXXXXXXXX XXXXXXXXXXX MASE
Obsah xxxxxxx x XXX xxxxx xxxxxxxx (XX) x. 853/2004:
|
1. |
xxxxxxxxxx 0,1 % (= 100 xx/100 x xxxx 1 000 xxx) x xxxxxxxx xxxxxxxx; |
|
2. |
xx stanoví xxxxxxxxxxx xxxxxxxxxxxxxxxx xxxxxxx. |
XXXXXXX X
XXXXXXX XXXXXXXXXXX XXXXXXXXXXXXXXX XXXXXXXX
XXXXXXXX I
PŘÍSTUP X&xxxx;XXXXXXXX XXXXXXXXXXX XXXXXXXXXXXXXXX XXXXXXXX
Xx xxxxx xxxxxxx xxxxxxxx xxxxxx xxx xxxxxxxxxxx xxxxxxxxxx xxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxxx zařízení xxxxxxxxxx jiným členským xxxxxx x&xxxx;xxxxxxxxxx Komise xxxxxxxxx internetovou xxxxxxx, xx kterou xxxxx xxxxxxx xxxx xxxxxx xxxxx na své xxxxxxxxxxxx xxxxxxxxxxx stránky.
KAPITOLA XX
XXXXXX XXX XXXXXXXXXXXX XXXXXXXXXXX XXXXXXX
X.&xxxx;&xxxx;&xxxx;Xxxxxxx xxxxxxx
|
1. |
Xxxxx xxxxxxx xxxx xxxxxxxx Xxxxxx xxxxxx xxxxxx xx xxxxx vnitrostátní xxxxxxxxxxxx xxxxxxx, xxxxx xxxxxxxx xxxxxxx xxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxxx zařízení xxx xxxxxxxx xxxxxxxxxxx xxxxxx ve smyslu xxxxxxx&xxxx;X&xxxx;xxxx&xxxx;8.1 xxxxxxxx (XX) x.&xxxx;853/2004. |
|
2. |
Xxxxxxx xxxxxxx xxxxxxx x&xxxx;xxxx&xxxx;1 xxxxxxx x&xxxx;xxxxx xxxxxxx x&xxxx;xxxxxxxxx xx x&xxxx;xxxxxx nebo více xxxxxxxx xxxxxxxx Xxxxxxxxxxxx. |
X.&xxxx;&xxxx;&xxxx;Xxxxxxxx xxxxxx
|
1. |
Xxxxxxxxxxxx xxxxxxx, xxxxx xxxxxxxx xxxxxxx seznamů, xxxxxxxx xxxxxxxxx xxxxx, xxxxxxxxx xxxxx x&xxxx;xxxxxxxxxxx xxxxxx uvedených v článku 4 xxxxxxxx (ES) x.&xxxx;882/2004. |
|
2. |
Xxxxxxx xxxxxxx obsahuje odkazy xx:
|
XXXXXXXX XXX
XXXXXXXXX A KÓDY XXX XXXXXXX XXXXXXXXXXX XXXXXXXX
Xxx&xxxx;xxxxxxxxx široké xxxxxxxxxxx xxxxxxxxx o schválených xxxxxxxxxxxxxxx xxxxxxxxxx x&xxxx;xxx&xxxx;xxxxx xxxxxxxxx xxxxxx xxxxxxx se xxxxxxx struktury, xxxxxx xxxxxxxxxxx xxxxx a kódů.
KAPITOLA XX
XXXXXXXXX SPECIFIKACE
Úkoly x&xxxx;xxxxxxxx xxxxxxx v kapitolách II x&xxxx;XXX xx xxxxxxxxxx v souladu x&xxxx;xxxxxxxxxxx xxxxxxxxxxxxx zveřejněnými Xxxxxx.
PŘÍLOHA VI
VZOR VETERINÁRNÍCH XXXXXXXXX XXX XXXXX XXXXXX STEHÝNEK, HLEMÝŽDŮ, XXXXXXXX X&xxxx;XXXXXXXX
XXXXX I
ŽABÍ XXXXXXXX X&xxxx;XXXXXXXX
Xxxxxxxxxxx xxxxxxxxx xxx xxxxx xxxxxx xxxxxxxx x&xxxx;xxxxxxxx xxxxx xx.&xxxx;6&xxxx;xxxx.&xxxx;1 xxxx.&xxxx;x)&xxxx;xxxxxxxx (ES) x.&xxxx;853/2004 xxxx xxxxxxxxx xxxxxx stanoveným x&xxxx;xxxxxxx&xxxx;X&xxxx;xxxxx X,&xxxx;xxxxxxxxxx části B této xxxxxxx.
XXXXX XX
XXXXXXXX
Xxxx xxxx xxxxxxx xxxx xxxxxxxx xxxxxx xxxxxxxx Xxxxxxxxxxxx, mezi xxx patří xxxxxxxxxxxx, xxx xxxxxx xxxxx xxxxxxxx o přenosných spongiformních xxxxxxxxxxxxxxx x&xxxx;xxxxxxxxx, xxxx xxxxxxxxxxx xxxxxxxxx xxx xxxxx xxxxxxxx x&xxxx;xxxxxxx x&xxxx;xxxxxx želatiny podle xx.&xxxx;6 xxxx.&xxxx;1 xxxx.&xxxx;x)&xxxx;xxxxxxxx (XX) x.&xxxx;853/2004 xxxxxxxxx xxxxxx stanoveným x&xxxx;xxxxxxx&xxxx;XX xxxxx X,&xxxx;xxxxxxxxxx v části B této xxxxxxx.
XXXXX XXX
XXXXXXX
Xxxx xxxx xxxxxxx jiné zvláštní xxxxxx xxxxxxxx Xxxxxxxxxxxx, xxxx něž patří xxxxxxxxxxxx, ale xxxxxx xxxxx xxxxxxxx x&xxxx;xxxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxxxxxxxx x&xxxx;xxxxxxxxx, xxxx xxxxxxxxxxx osvědčení xxx dovoz xxxxxxxx x&xxxx;xxxxxxx x&xxxx;xxxxxx xxxxxxxx xx xxxxxx xx.&xxxx;6 xxxx.&xxxx;1 písm. d) nařízení (XX) x.&xxxx;853/2004 odpovídat xxxxxx xxxxxxxxxx v dodatku III xxxxx X,&xxxx;xxxxxxxxxx x&xxxx;xxxxx&xxxx;X&xxxx;xxxx xxxxxxx.
Xxxxxxx X xxxxxxx XX
Xxxx X
XXXX VETERINÁRNÍHO OSVĚDČENÍ XXX XXXXX XXXXXXXXXX, XXXXXXXXX XXXX PŘIPRAVENÝCH XXXXXX XXXXXXXX URČENÝCH X LIDSKÉ XXXXXXXX


Xxxx X
XXXX XXXXXXXXXXXXX XXXXXXXXX XXX XXXXX XXXXX XXXXXXXX X LIDSKÉ XXXXXXXX XXXXXXXXX ZE XXXXXXXX, XXXXXXXX, XXXXXXXXXXXX XXXX XXXXXXXXXXXXXX


Xxxxxxx XX x xxxxxxx XX
Xxxx X
XXXX VETERINÁRNÍHO XXXXXXXXX XXX XXXXX XXXXXXXX XXXXXX X XXXXXX XXXXXXXX


Xxxx B
VZOR XXXXXXXXXXXXX XXXXXXXXX XXX XXXXX XXXXXXXX K VÝROBĚ XXXXXXXX XXXXXX X XXXXXX SPOTŘEBĚ


Dodatek III x&xxxx;xxxxxxx&xxxx;XX
Xxxx X
XXXX VETERINÁRNÍHO XXXXXXXXX PRO XXXXX XXXXXXXX XXXXXXXX X&xxxx;XXXXXX XXXXXXXX


Xxxx B
VZOR XXXXXXXXXXXXX XXXXXXXXX XXX XXXXX XXXXXXXX X&xxxx;XXXXXX XXXXXXXX XXXXXXXX X&xxxx;XXXXXX SPOTŘEBĚ


XXXXXXX XXX
XXXXX XXXXXXXX (XX) x.&xxxx;853/2004
X&xxxx;xxxxxxxx (XX) x.&xxxx;853/2004 xx přílohy II x&xxxx;XXX xxxx xxxxx:
|
1. |
X&xxxx;xxxxxxx&xxxx;XX xx xxxxx&xxxx;X&xxxx;xxxx&xxxx;X&xxxx;xxxx takto:
|
|
2. |
Xxxxxxx&xxxx;XXX se mění xxxxx:
|
(1)&xxxx;&xxxx;Xx.&xxxx;xxxx. X&xxxx;123, 24.4.1998, x.&xxxx;1.“
XXXXXXX XXXX
ZMĚNY NAŘÍZENÍ (XX) x. 854/2004
X xxxxxxxx (ES) x. 854/2004 se xxxxxxx X, XX x XXX xxxx xxxxx:
|
1. |
X xxxxxxx X xxxxxx X xxxxxxxx XXX xx xxx 3 xxxx xxxxx:
|
|
2. |
X xxxxxxx XX kapitole II xxxxx X xx xxxx 4 x 5 xxxxxxxxx tímto:
|
|
3. |
X xxxxxxx XXX xxxxxxxx XX xxxxx X xx xxx 1 xxxxxxxxx xxxxx:
|


