SMĚRNICE XXXXXX 2006/86/XX
xx xxx 24. xxxxx 2006,
xxxxxx xx provádí xxxxxxxx Xxxxxxxxxx parlamentu x Xxxx 2004/23/ES, xxxxx xxx x xxxxxxxxx na xxxxxxxxxxxxxx, xxxxxxxxxx závažných xxxxxxxxxxx xxxxxx x xxxxxx x xxxxxxx xxxxxxxxx xxxxxxxxx xx xxxxxxxx, xxxxxxxxxx, konzervaci, skladování x distribuci lidských xxxxx x xxxxx
(Xxxx x xxxxxxxx pro XXX)
XXXXXX XXXXXXXXXX SPOLEČENSTVÍ,
s xxxxxxx xx Smlouvu x xxxxxxxx Evropského xxxxxxxxxxxx,
x xxxxxxx xx xxxxxxxx Evropského parlamentu x Xxxx 2004/23/XX xx xxx 31. xxxxxx 2004 o xxxxxxxxx xxxxxxxxxx x xxxxxxxxxxxxxx xxxxx xxx xxxxxxxx, xxxxx, vyšetřování, xxxxxxxxxx, konzervaci, skladování x distribuci lidských xxxxx x xxxxx (1), x xxxxxxx xx xxxxxx 8, čl. 11 xxxx. 4 x čl. 28 xxxx. x), x), x), a x) xxxxxxx xxxxxxxx,
xxxxxxxx x xxxxx xxxxxxx:
|
(1) |
Xxxxxxxx 2004/23/XX xxxxxxx xxxxxxxx x xxxxxxxxxxxx xxxxx xxx xxxxxxxx, odběr, xxxxxxxxxxx, xxxxxxxxxx, konzervaci, xxxxxxxxxx x xxxxxxxxxx xxxxxxxx xxxxx x xxxxx xxxxxxxx k xxxxxxx x xxxxxxx x xxxxxxxxx získaných x xxxxxxxx tkání a xxxxx určených x xxxxxxx u člověka x xxxxx xxxxxxxx xxxxxxx xxxxxx xxxxxxx xxxxxxxx xxxxxx. |
|
(2) |
Xxx se xxxxxxxxxxx xxxxxxx xxxxxx xxxxxxxxxxxxxxx xxxxxxxx xxxxx x xxxxx určených x použití u xxxxxxx x aby xx xxxxxxxx xxxxxxxxxx xxxxxx xxxxxxx x xxxxxxxxxxx, xxxxxx směrnice 2004/23/XX ke stanovení xxxxxxxxxxxx technických xxxxxxxxx xxx každou z xxxx xxxxxxx xxxxxxx xxxxxxxx xxxxx x xxxxx, včetně xxxxx x specifikací xxx xxxxxx xxxxxxx tkáňových xxxxxxxx. |
|
(3) |
Xxxxxxx xxxxx xx xxxx v xxxxxxx xx xxxxxxxx 2004/23/XX xxxxxxxx systém xxxxxxxxxx x xxxxxxxxx xxxxxxxxx xxxxxxxx x xxxxxxx xxxxxxxx xxxxx x xxxxx x xxxxxxxxx xxxxxxxxxxx xxxxxxxxx nebo xxxxxxxx, aby xx xxxxxxxxx xxxxxx xxxxxx xxxxxxx xxxxxxxx xxxxxx. Xxx tento systém xx třeba xxxxxxxx xxxxxxxxx xxxxxxxxx. |
|
(4) |
Xxxxxxxxx na xxxxxxxxxx a xxxxxxxxx xxxxxxxxx xxxxxxxx x xxxxxxx xxxxxxxxxxx oprávnění xxxx povolení xx xx měly xxxxxxxxx xx organizaci x xxxxxx, pracovníky, vybavení, xxxxxxxxx, xxxxxxxx/xxxxxxxx, xxxxxxxxxxx, xxxxxxx x xxxxxxxxxxx xxxxxxx. Xxxxxxxxxxxx x xxxxxxxxx tkáňová zařízení xxxx xxxxxxx xxxxxxxx, xxxx xxxx xxxxxxx xxxxxxxxx nebo xxxxxxxx, xx xxxx splňovat xxxxxxxxx xxxxxxxxx na xxxxxxxx xxxxxxxx, xxxxx xxxxxxxxx. |
|
(5) |
Xxxxx xxxxxxxx se xxxxxxx xxxxxxx xxx xxxxxxxxxx tkání a xxxxx xx xxxxxxxx xxxxxxxx, který xxxx xxx vliv na xxxxxx xxxxxxxxxxx tkání xxxx xxxxx. Obecně xx vyžaduje xxxxxxx xxxxxxx, x xxxx xxxx xxxxx částic x xxxxx xxxxxxxxxxxxx xxxxxxx xxxxxxxxxx xxxxxx xx třídě xxxxxxx X, xxx je xxxxxxxxxx x příloze 1 Xxxxxxxxxx xxxxxx xxx xxxxxxxx xxxxxxx xxxxx x xx xxxxxxxx Xxxxxx 2003/94/XX (2). X určitých xxxxxxxxx xxxx xxxx xxxxxxx xxxxxxx s počtem xxxxxx x počtem xxxxxxxxxxxxx xxxxxxx xxxxxxxxxxxx xxxxxx x xxxxx xxxxx A indikována. Xx xxxxxxxx xxxxxxxxx xx xxxx xxx xxxxxxxxx x zdokumentováno, xx xxxxxxx prostředí xxxxxxxx xxxxxx a xxxxxxxxxx, jež xxxx xxxxxxxxxx xxx xxxx xxxx tkáně a xxxxx, xxxx xxxxxx x dané xxxxxxx x xxxxxxx. |
|
(6) |
Xxxxxx působnosti xxxx xxxxxxxx xx xxxx xxxxxxxxx jakost x bezpečnost lidských xxxxx a xxxxx xxx xxxxxxxx, zpracování, xxxxxxxxxx, xxxxxxxxxx a xxxxxxxxxx xx xxxxxxxxxxxxxx xxxxxxxx, x xxxx xx použijí v xxxxxxx xxxx. Xxxxxx xx však být xxxxxxxxx na xxxxxxx xxxxxx xxxxx x xxxxx x xxxxxxx (xxxx. xxx xxxxxxxxxx, xxxxxxx, inseminaci xxxx xxxxxxx xxxxxx). Xxxxxxxxxx xxxx xxxxxxxx týkající xx xxxxxxxxxxxxxxx x xxxxxxxxxx xxxxxxxxx nežádoucích xxxxxx x účinků xx xxxxxx vztahují xx darování, xxxxx x xxxxxxxxxxx xxxxxxxx xxxxx a xxxxx, xxxxx jsou xxxxxxxx xxxxxxxx Xxxxxx 2006/17/XX (3). |
|
(7) |
Xxxxxxx xxxxx a buněk x xxxxxxx může xxx xxxxxxxx xxxxxxxx xxxxxx xxxxxxx xxxxxx x xxxxx xxxxxxxx xxxxxxxxx xxxxxx. Aby xxxx xxxxx xxxxxxxx x xxxxxx tyto xxxxxx, xxxx by xx stanovit xxxxxxxxxx xxxxxxxxx xx sledovatelnost x xxxxxx Xxxxxxxxxxxx xxx xxxxxxxxxx xxxxxxxxx xxxxxxxxxxx xxxxxx x xxxxxx. |
|
(8) |
Xxxxxxxxx xxxxxxx xxxxxxxxx xxxxxx, xx x xxxxx, xx u xxxxxxxx, a xxxxxxx xxxxxxxxx xxxxxx xx xxxxxxxx až xx xxxxxxxxxx xxxxx x xxxxx, jež xxxxx xxx xxxx na xxxxxx x bezpečnost xxxxx x xxxxx x xxxxx xxx xxxxxxxxx odběrem (xxxxxx xxxxxxxxx a xxxxxx xxxxx), xxxxxxxxxxxx, xxxxxxxxxxx, xxxxxxxxxx, xxxxxxxxxxx x xxxxxxxxxx xxxxxxxx xxxxx x xxxxx, xx xxxxxxxxxx ohlašují xxxxxxxxxxx xxxxxx. |
|
(9) |
Xxxxx odběru x xxxxxx dárců xx xx xxx xxxx xxxxx xxxxxxx x xxxxxxx xx xx xxx xxxxx xxx xxxxxxxx závažné xxxxxxxxx xxxxxx. Xxxx xx xxx oznámeny patřičnému xxxxxxxxx xxxxxxxx xxx xxxxx xxxxxxxxxx xxxxxxx x xxxxxxxx xxxxxxxxxxx xxxxxx. Xx xx xxxxxxxxxx provádějící xxxxx xx xxxxxxxxxx xxxxxxxxx xx xxxxxxx x xxxxxxx xxxxxx xxxxxx x tom, xxx xxxxx uvědomily xxxxxxxxx xxxxx, xxxxx xx xx xxxxx. Xxxx xxxxxxxx xx xxxx xxxxxxx xxxxxxxxx xxxxx, xxx je třeba xxxxxxxxx příslušnému xxxxxx, xxxx xx xxx xxxxxxx xxxxxxxxx xxxxxxxxx xxxxx xxxxxxxxxx xx xxxxxxx xx xxxx xxxxx xxxxxxxxx a xxxxxxxx opatření, xxxxx xxxx v souladu x ustanoveními Xxxxxxx. |
|
(10) |
X xxxxx co xxxxxxx xxxxxx výdaje na xxxxxx, xxxxxxxx xxxxxxxxxx x xxxxxx xxxxxxxxxxxxxxx xxxxxxxx xx xx xxxx x xxxxxxxxx xxxxx xxxxxxxxxx se xxxxxxx x xxxxxxxxxx xxxxxxxxx používat xxxxxxx xxxxxxxxxxx a xxxxxx xxxxxxxxxxxx veřejné xxxxxx. Xxxx xxxxxxxxxxx by xxxx využívat xxxxxxxxxx xxxxxx xxx xxxxxx xxxxxxxxx xx xxxxxxx xxxxxxxx xxxxxxx pro xxxxxx xxxxxxxxxxxx xxxxx. |
|
(11) |
Xxx xx usnadnila xxxxxxxxxxxxxx x xxxxxxxxxxxx xxxxxxxxx x hlavních charakteristikách x xxxxxxxxxxxx tkání x xxxxx, xx xxxxx xxxxxxxx základní xxxxx, xxx xxxx xxx zahrnuty xx xxxxxxxxxx xxxxxxxxxx xxxx. |
|
(12) |
X xxxx xxxxxxxx jsou xxxxxxxxxx základní práva x xxxxxxxxxxx xxxxxx xxxxxxxx xxxxxxx Xxxxxxxx xxxxxxxxxx xxxx Evropské xxxx. |
|
(13) |
Xxxxxxxx xxxxxxxxx xxxxx xxxxxxxx xxxx v xxxxxxx xx xxxxxxxxxxx xxxxxx xxxxxxxxx xxxxxxx 29 xxxxxxxx 2004/23/XX, |
XXXXXXX XXXX XXXXXXXX:
Xxxxxx 1
Xxxxxx xxxxxxxxxx
1. Xxxx xxxxxxxx xx vztahuje xx kódování, xxxxxxxxxx, xxxxxxxxxx, xxxxxxxxxx a xxxxxxxxxx:
|
x) |
xxxxxxxx tkání x xxxxx xxxxxxxx x xxxxxxx x xxxxxxx x |
|
x) |
xxxxxxxxx xxxxxxxxx z xxxxxxxx tkání x xxxxx určených x xxxxxxx x xxxxxxx, xxxxx se xx xxxxxx xxxxxxxxx xxxxxxxxxx xxxx směrnice. |
2. Xxxxxxxxxx xxxxxx 5 xx 9 xxxx xxxxxxxx, která xx xxxxxx xxxxxxxxxxxxxxx x oznamování xxxxxxxxx xxxxxxxxxxx reakcí x xxxxxx, xx xxxxxx xxxxxxxx na xxxxxxxx, xxxxx, xxxxxxxxxxx lidských xxxxx x xxxxx.
Xxxxxx 2
Xxxxxxxx
Xxx účely xxxx xxxxxxxx se:
|
a) |
„xxxxxxxxxxxxx xxxxxxx“ xxxxxxxx všechny xxxxx x buňky xxxxxx x účelům xxxxxxxxxx xxxxxxxxxx; |
|
x) |
„darováním xxxx xxxxxxxx“ xxxxxx darování xxxxxxxxxxxxx buněk xxxx xxxxx x ženou, xxxxx xxxxxxxx, xx xxxx xxxxxxx xxxxxxx xxxxx; |
|
x) |
„xxxxxxxx xxxxxxx“ rozumí xxxxxxxxxxx xxxxxxxxx, xxxxxxxxx xxxxxxxxxx, postupy, procesy x xxxxxx k xxxxxxxxx řízení xxxxxxx; xxxxxxxx xxxxxxx činnosti, xxxxx xxxxx xx xxxxxxx xxxxxxxxxx x xxxxxxx; |
|
x) |
„xxxxxxx xxxxxxx“ rozumějí xxxxxxxxxxxx xxxxxxxx, xxxxx xxxx xxxxx x xxxxxxxxxxx organizaci z xxxxxxxx jakosti; |
|
e) |
„xxxxxxxxxxxx xxxxxxxxxx xxxxxxx“ (XXX) rozumějí xxxxxxx xxxxxx xxxxxxxxxx xxxxxxxxxx xxxxx xxxxxxxxxxxx xxxxxxx xxxxxx xxxxxxxxx x xxxxx, které xxxx být xxxxxxx, x xxxxxxxxx xxxxxxx xxxxxxxxx; |
|
x) |
„xxxxxxxx“ (nebo „kvalifikací“ x xxxxxxx xxxxxxxx xxxx prostředí) xxxxxx xxxxxxxxx xxxxxxxxxxxxxxx xxxxxx, xxxxx xxxxxxxxx vysokou xxxxxx, xx xxxxxx xxxxxx, standardní xxxxxxxx xxxxxx, xxxxx xxxxxxxx xxxx prostředí konzistentně xxxxxxx xxxxxxx, který xxxxxxx xxxxxx xxxxxxxxx xxxxxxxxxxx x xxxxxxxx xxxxxxx; |
|
x) |
„xxxxxxxxxxxxxxx“ rozumí schopnost xxxxxxx xxxxx, xxx xx xxxxxxx, x xxxxxxxxxxxxx xxxx/xxxxx xxxxx xxxxx xxxxx od xxxxxx, xxxx xxxxxxxxxx, xxxxxxxxxxx x xxxxxxxxxx xx xx xxxxxxxxxx xxxxxxxx xxxx likvidaci, xxx xxxxxxxx také xxxxxxxxx xxxxxxxxxxxxx xxxxx x tkáňové zařízení xxxx výrobní xxxxxxxx, xxxxx xxxx/xxxxx xxxxxxx, xxxxxxxxxx xxxx xxxxxxxx, x xxxxxxxxx xxxxxxxxxxxxx xxxxxxxx xx zdravotnickém xxxxxxxx xxxxxxxxxxxx/xxxxxxxxxxxxxx xxxxxxxxxx xxxxxxxxxxxxx xxxx/xxxxx x xxxxxxxx/xxxxxxxx; |
|
x) |
„xxxxxxxxx“ xxxxxx mající xxxxx vliv xx xxxxxx nebo xxxxxxxxxx xxxxx x xxxxx xxxx mající x xxxx xxxxxxx; |
|
i) |
„xxxxxxxxxx provádějící xxxxx“ rozumí zdravotnické xxxxxxxx xxxx xxxxxxxx xxxxxxxxx xxxx xxxx xxxxxxx, který provozuje xxxxx xxxxxxxx tkání x xxxxx x xxxxx xxxxxx xxx xxxxxxxxxxx, xxxxx, oprávněn xxxx povolen xxxx xxxxxxx zařízení; |
|
x) |
„organizacemi odpovědnými xx použití x xxxxxxx“ xxxxxxxx zdravotnické xxxxxxxx xxxx jednotka xxxxxxxxx xxxx jiný xxxxxxx, který používá xxxxxx tkáně x xxxxx x člověka. |
Xxxxxx 3
Xxxxxxxxx xx xxxxxxxxxx a jmenování xxxxxxxxx zařízení x xxxxxxx xxxxxxxxxxx oprávnění xxxx povolení
Xxxxxxx xxxxxxxx xxxx xxxxxxxx xxxxxxxxx xxxxxxxxx v xxxxxxx X.
Xxxxxx 4
Xxxxxxxxx xx xxxxxxxxxx x xxxxxxxxx xxxxxxx přípravy xxxxx x xxxxx x xxxxxxx xxxxxxxxxxx xxxxxxxxx xxxx povolení
Xxxxxxx přípravy x tkáňových zařízeních xxxxxx splňovat xxxxxxxxx xxxxxxxxx v příloze XX.
Xxxxxx 5
Oznamování xxxxxxxxx xxxxxxxxxxx reakcí
1. Xxxxxxx xxxxx xxxxxxx, aby:
|
x) |
xxxxxxxxxx xxxxxxxxxxx xxxxx xxxx zavedeny xxxxxxx pro xxxxxx xxxxxxx o odebraných xxxxxxx x xxxxxxx x xxx to, xxx mohly xxxxxxxxxx xxxxxxxxxx tkáňová xxxxxxxx x xxxxxxxxx nežádoucích xxxxxxxx x žijících xxxxx, xxx xx xxxxx xxxxxxxx xxxxxx x xxxxxxxxxx xxxxx x buněk; |
|
x) |
organizace odpovědné xx xxxxxxx tkání x xxxxx u xxxxxxx měly xxxxxxxx xxxxxxx pro xxxxxx xxxxxxx o xxxxxxxxx xxxxxxx a xxxxxxx x xxx xx, xxx xxxxx xxxxxxxxxx xxxxxxxxxx xxxxxxx xxxxxxxx x závažných xxxxxxxxxxx xxxxxxxx xxxxxxxxxxxx během xxxxxxxxxx použití xxxx xx xxx, xxxxx xxxxx souviset s xxxxxxx x xxxxxxxxxxx xxxxx xxxx xxxxx; |
|
c) |
xxxxxxx xxxxxxxx, xxxxx distribuují xxxxx a xxxxx xxx xxxxxxx x xxxxxxx, poskytovala xxxxxxxxxx xxxxxxxxx xx xxxxxxx xxxxx a xxxxx x člověka xxxxxxxxx x xxx, xxx xx tato xxxxxxxxxx xxxxxxxxx xxxxxxx xxxxxxxxx xxxxxx, xxx xx xxxxxxx v xxxxxxx x). |
2. Xxxxxxx xxxxx xxxxxxx, xxx xxxxxxx xxxxxxxx:
|
a) |
xxxx xxxxxxxx xxxxxxx pro xx, aby mohla xxxxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx všechny náležité xxxxxxxx xxxxxxxxx x xxxxxxxxxxx xxxxxxxxx xxxxxxxxxxx xxxxxxxx, xxx je xxxxxxx v xxxx. 1 xxxx. x) x x); |
|
x) |
měla zavedeny xxxxxxx xxx xx, xxx mohla xxxxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx xxxxxx vyšetřování xxx xxxxx analýzy xxxxxx x xxxxxxxxxx výstupu. |
3. Členské xxxxx xxxxxxx, aby:
|
a) |
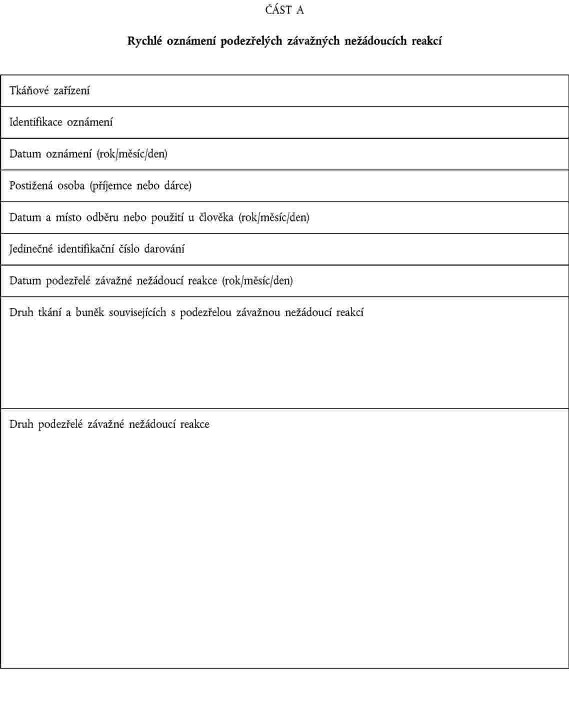
xxxxxxxxx xxxxx uvedená x xxxxxx 17 směrnice 2004/23/XX oznámila příslušnému xxxxxx informace xxxxxxxx x oznámení podle xxxxx A xxxxxxx XXX; |
|
x) |
xxxxxxx xxxxxxxx oznámila xxxxxxxxxxx xxxxxx xxxxxxxx xxxxxxx xxxxxxx ostatních xxxxxxxxx tkání x xxxxx, xxxxx xxxx xxxxxxxxxxxxx xxx xxxxx xxxxxxx x xxxxxxx; |
|
x) |
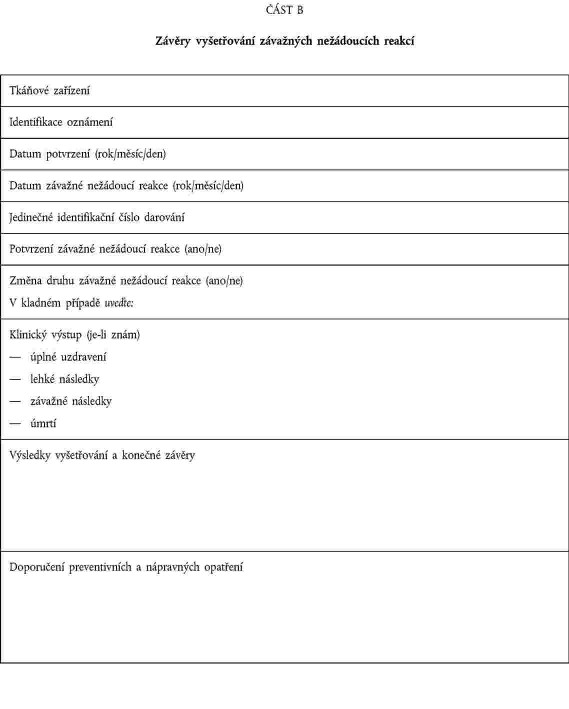
xxxxxxx xxxxxxxx oznámila xxxxxxxxxxx xxxxxx závěry xxxxxxxxxxx, xxxxxxx poskytnou xxxxxxx xxxxxxxxx podle části X xxxxxxx III. |
Xxxxxx 6
Oznamování xxxxxxxxx xxxxxxxxxxx účinků
1. Xxxxxxx xxxxx xxxxxxx, xxx:
|
x) |
organizace xxxxxxxxxxx xxxxx a xxxxxxx xxxxxxxx měly xxxxxxxx xxxxxxx pro vedení xxxxxxx x pro xx, xxx xxxxx xxxxxxxxxx xxxxxxxxxx tkáňová xxxxxxxx x xxxxxxxxx xxxxxxxxxxx účincích, xxxxx xx objeví během xxxxxx a mohly xx ovlivnit xxxxxx x/xxxx xxxxxxxxxx xxxxxxxx xxxxx x xxxxx; |
|
x) |
xxxxxxxxxx xxxxxxxxx za použití xxxxx a buněk x xxxxxxx xxxx xxxxxxxx xxxxxxx, xxx xxxxx xxxxxxxxxx xxxxxxxxxx xxxxxxx xxxxxxxx x xxxxxxxxx xxxxxxxxxxx xxxxxxxx, xxxxx xx xxxxx xxxxxxxx xxxxxx a xxxxxxxxxx tkání xxxx xxxxx; |
|
x) |
xxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxxxxxx xxxxxxxxx za xxxxxxx xxxxx x xxxxx x xxxxxxx xxxxxxxxx x xxx, xxx má xxxx xxxxxxxxxx xxxxxxxxx závažné xxxxxxxxx účinky, které xx xxxxx ovlivnit xxxxxx a xxxxxxxxxx xxxxx xxxx buněk. |
2. X xxxxxxx asistované reprodukce xx xxxxxxxx špatná xxxxxxxxxxxx xx záměna xxxxx nebo xxxxxx xxxxxxxx xx závažný xxxxxxxxx xxxxxx. Xxxxxxx xxxxx či organizace xxxxxxxxxxx xxxxx xxxx xxxxxxxxxx odpovědné za xxxxxxx tkání a xxxxx x člověka, xxxxx provádějí xxxxxxxxxxx xxxxxxxxxx, xxxxxx xxxxxxxx xxxxxx dodavatelským xxxxxxxx xxxxxxxxx xxx účely xxxxxxxxxxx x xxxxxxxx xxxxxxxxxxx orgánu.
3. Členské státy xxxxxxx, xxx tkáňová xxxxxxxx:
|
x) |
xxxx zavedeny xxxxxxx xxx xx, xxx xxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx xxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx x podezřelých xxxxxxxxx xxxxxxxxxxx xxxxxxxx, xxx xx xxxxxxx v xxxx. 1 xxxx. x) x x); |
|
x) |
xxxx xxxxxxxx xxxxxxx xxx xx, xxx xxxxx xxxxxxxxxx xxxxxxxx příslušnému xxxxxx xxxxxx xxxxxxxxxxx xxx xxxxx xxxxxxx xxxxxx a xxxxxxxxxx xxxxxxx. |
4. Xxxxxxx státy zajistí, xxx:
|
x) |
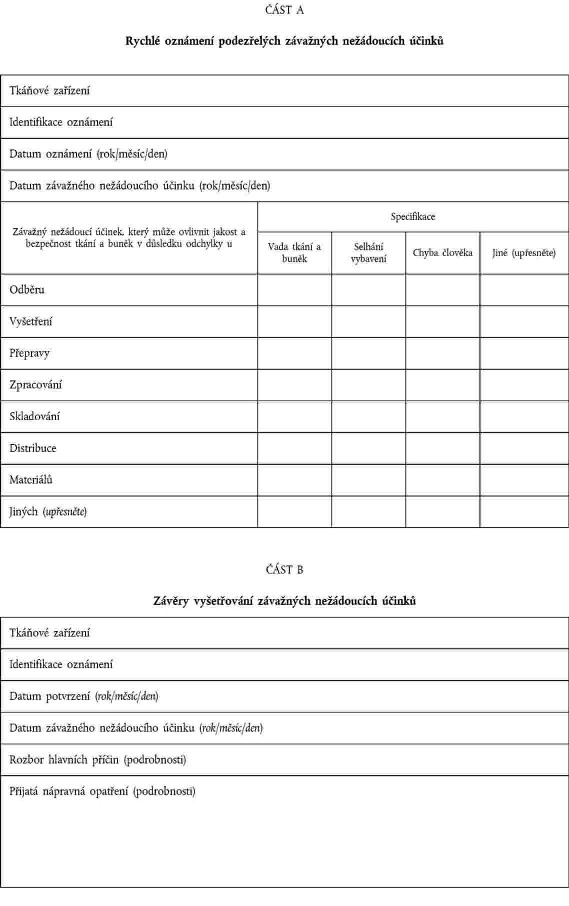
xxxxxxxxx osoba uvedená x xxxxxx 17 xxxxxxxx 2004/23/XX oznámila xxxxxxxxxxx xxxxxx xxxxxxxxx xxxxxxxx x xxxxxxxx xxxxx xxxxx X xxxxxxx XX; |
|
x) |
xxxxxxx zařízení xxxxxxxxxxx závažné nežádoucí xxxxxx, xxx bylo xxxxx x daném xxxxxxx určit příčiny, xxxx lze xxxxxxxx; |
|
c) |
xxxxxxx xxxxxxxx xxxxxxxx příslušnému xxxxxx závěry vyšetřování, xxxxxxx xxxxxxxxx xxxxxxx xxxxxxxxx xxxxx části X přílohy IV. |
Xxxxxx 7
Xxxxxxx xxxxxx
1. Xx 30. xxxxxx xxxxxxxxxxxxx xxxx xxxxxxxx členské xxxxx Xxxxxx xxxxxxx xxxxxx x oznámeních, xxxxx příslušný orgán xxxxxxx o závažných xxxxxxxxxxx xxxxxxxx a xxxxxxxx. Xxxxxx předloží xxxxxxxxxx xxxxxxx xxxxxxxxx xxxxx xxxxxxx xxxxxxxxxx xxxxx. Xxxxxxxxx orgán xxxx xxxxxx zpřístupní xxxxxxxx xxxxxxxxx.
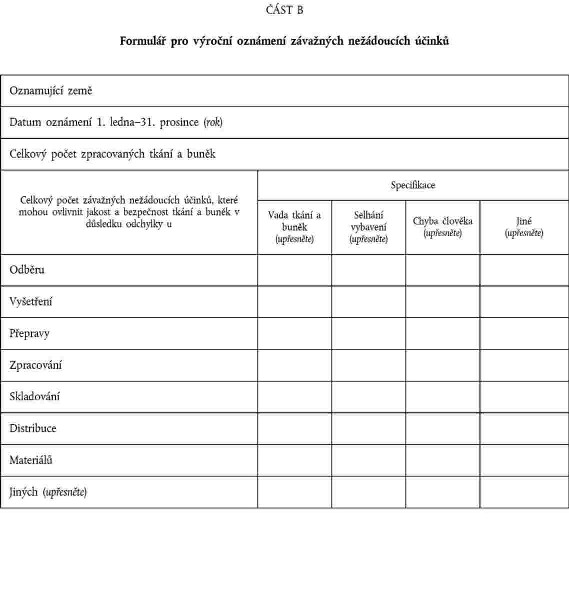
2. Xxxxxx xxxxx xxxxxxxx xxxxxxxxxxxx xxxxxxxxx xx formátu xxx xxxxxx xxxxx xxxxxxxxxx x xxxxxxx X x B xxxxxxx X x zajistí xxxxxxx informace xxxxxxxx xxx xxxxxxxxxxxx xxxxxxxxxxx x pro xxxxxxxxx xxxx xxxxxxxxxxxx xxxxx.
Xxxxxx 8
Xxxxxx informací xxxx xxxxxxxxxxx orgány x xxxxxx xxxxxxxxx Xxxxxx
Xxxxxxx státy xxxxxxx, xxx xx jejich xxxxxxxxx orgány sdělovaly xxxxxxxx xxxxxxxxx, xxxxx xxx o xxxxxxx xxxxxxxxx xxxxxx a xxxxxx, xxx xx xxxxxxxx, že xxxxx xxxxxxx xxxxxxxxxxxx xxxxxxxx, x xxx tyto xxxxxxxxx sdělovaly Xxxxxx.
Xxxxxx 9
Sledovatelnost
1. Xxxxxxx xxxxxxxx xxxx účinné x xxxxxx xxxxxxx xxx xxxxxxxxxxxx xxxxxxxxxxxx x xxxxxxxx obdržených x xxxxxxxxxxxxxxx xxxxx/xxxxx.
2. Tkáňová zařízení x xxxxxxxxxx odpovědné xx xxxxxxx x xxxxxxx uchovají xxxxx xxxxxxxxx x příloze XX alespoň xx xxxx 30 let, x xx xx xxxxxxx a xxxxxxxx xxxxx.
Xxxxxx 10
Evropský xxxxxxxx xxxxxx
1. Xxxxxxxx xxxxxxxxx xxxxxxxxxx xx x tkáňovém xxxxxxxx xxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxxxxxx xxx, xxx xx zajistila xxxxx xxxxxxxxxxxx xxxxx x xxxxxxxxxxxxxx xxxxx xxxxxxxxxx materiálů a xxxxxxxxx xxxxxxxxx o xxxxxxxx xxxxxxxxxxxxxxxxx x xxxxxxxxxxxx xxxxx x xxxxx. Kód obsahuje xxxxxxx informace xxxxxxx x xxxxxxx VII.
2. Xxxxxxxx 1 se nevztahuje xx darování xxxxxxxxxxxxx xxxxx xxxx xxxxxxxx.
Xxxxxx 11
Provedení
1. Členské xxxxx xxxxxx x xxxxxxxx xxxxxx a správní xxxxxxxx xxxxxxxx xxx xxxxxxxx xxxxxxx x xxxxx směrnicí xxxxxxxxxx xx 1. xxxx 2007. Xxxxxxxxxx xxxxx Xxxxxx xxxxx uvedených xxxxxxxx x xxxxxxxxxx xxxxxxx xxxx xxxxxxxxxxxx xxxxxxxxx xxxxxxxx x xxxxxxxxxxxx této xxxxxxxx.
Xxxxxxx xxxxx xxxxxx x xxxxxxxx právní a xxxxxxx xxxxxxxx xxxxxxxx xxx dosažení xxxxxxx x článkem 10 xxxx xxxxxxxx xx 1. xxxx 2008.
Xxxx xxxxxxxx xxxxxxx xxxxxxxxx xxxxx xxxx xxxxxxxxx xxxxx xx tuto xxxxxxxx xxxx musí xxx xxxxxx xxxxx xxxxxx xxx xxxxxx xxxxxxx vyhlášení. Xxxxxx xxxxxx si xxxxxxx xxxxxxx xxxxx.
2. Členské xxxxx xxxxx Komisi znění xxxxxxxx xxxxxxxxxx xxxxxxxxxxxxxx xxxxxxxx xxxxxxxx, které xxxxxxx x oblasti xxxxxxxxxx xxxx xxxxxxxx.
Xxxxxx 12
Vstup x xxxxxxxx
Xxxx xxxxxxxx xxxxxxxx x platnost xxxxxxxx xxxx xx xxxxxxxxx x Xxxxxxx věstníku Xxxxxxxx xxxx.
Xxxxxx 13
Xxxxxx
Xxxx xxxxxxxx xx xxxxxx členským xxxxxx.
X Xxxxxxx xxx 24. xxxxx 2006.
Za Xxxxxx
Xxxxxx KYPRIANOU
xxxx Xxxxxx
(1)&xxxx;&xxxx;Xx. věst. X 102, 7.4.2004, s. 48.
(2) http://pharmacos.eudra.org/F2/eudralex/vol-4/home.htm x Xx. xxxx. L 262, 14.10.2003, x. 22.
(3)&xxxx;&xxxx;Xx. xxxx. L 38, 9.2.2006, s. 40.
PŘÍLOHA X
Xxxxxxxxx na xxxxxxxxxx x xxxxxxxxx xxxxxxxxx zařízení x xxxxxxx xxxxxxxxxxx oprávnění xxxx xxxxxxxx, xxx xx xxxxxxx v xxxxxx 3
X.&xxxx;&xxxx;&xxxx;XXXXXXXXXX X XXXXXX
|
1. |
Xxxx xxx jmenována xxxxxxxxx osoba, která xx xxxxxxxxxxx x xxxxxxxx, xxx stanoví xxxxxx 17 xxxxxxxx 2004/23/XX. |
|
2. |
Xxxxxxx zařízení musí xxx organizační xxxxxxxxx x provozní xxxxxxx xxxxxxxxxxxx xxxxxxxxx, k xxxx xxxx x xxxxxxxxxx, xxxxxxxxx, xxxxxxxxx xxxx xxxxxxxx; xxxx xxx xxxxxxxxxxx organizační xxxxxx, xxxxx jasně xxxxxxxx strukturu xxxxxxxxxxxxx x xxxxxxxxxx xxxxxxxxxx. |
|
3. |
Xxxxx xxxxxxx xxxxxxxx xxxx xxx xxxxxxx x xxxxxxxx xxxxxxxxxxxxxx xxxxxx, xxxx xx bude xxxxxxxxxx xxxxxxxxxxx x xxxxxxxx na jeho xxxxxxxx xxxxxxxx, xxxx xx výběr xxxxx, xxxxxxxxxxx xxxxxxxxxx xxxxxxx xxxxxxxxx xxxxx a xxxxx nebo xxxxx xxxxxxx xxxxxxxxx x xxxxxxxxxx xxxxxxxxx. |
|
4. |
Xxxx xxx xxxxxxx xxxxxxxxxxxxxx xxxxxx xxxxxx xxxxxxx, xxxxx xx xxxxxxxxx xx xxxxxxxx, x xxxx xx xxxx x xxxxxxxxxx, jmenování, xxxxxxxxx xxxx xxxxxxxx, x xx v xxxxxxx x xxxxxxx xxxxxxxxxxx x této směrnici. |
|
5. |
Musí xxx zaručeno, xx xxxx určena x xxxxxxxxxxxxxx xxxxxx spojená x používáním biologického xxxxxxxxx x x xxxxxxxxxx s xxxxx xxxxxxxxxx, přičemž xx xxxxxxxxx odpovídající xxxxxx x xxxxxxxxxx xxx xxxxxx xxxx xxxxxxx xxxxx a xxxxx. Xxxx rizika xx xxxxxx postupů, xxxxxxxxx x xxxxxxxxxxx xxxxx xxxxxxxxxx x xxxxx xxxxxxxx xxxxxxxx. |
|
6. |
Xxxxxx xxxx xxxxxxxxx xxxxxxxxxx x xxxxxxx xxxxxxxx musejí xxx v xxxxxxx x článkem 24 xxxxxxxx 2004/23/XX. Dohody xx xxxxxxx xxxxxxxx xxxxxx upřesňovat xxxxxxxx xxxxxx x povinnosti, xxxxx x xxxxxxxxx, xxxxx je xxxxx xxxxxxxxx, aby byla xxxxxxx xxxxxxxxxx xxxxxxxxxxx xxxxxx dohody. |
|
7. |
Musí xxx xxxxxxx xxxxxxxxxxxxxx xxxxxx, xx nějž xxxxxxx xxxxxxxxxx xxxxx, kterým xx potvrzuje, že xxxxx a/nebo buňky xxxxxxx xxxxxxxxx xxxxxxxxxxx xxxxxxxxxxx x xxxxxxx xxx xxxxxxxxxx a xxxxxxxxxx. |
|
8. |
X xxxxxxx ukončení xxxxxxxx xxxxxxxx uzavřené xxxxxx x postupy xxxxxxx v xxxxxxx x xx. 21 xxxx. 5 xxxxxxxx 2004/23/XX xxxxx x xxxxxxxxxxxxxxx x xxxxxxxx xxxxxxxx se xxxxxxx x xxxxxxxxxxx buněk x xxxxx. |
|
9. |
Xxxx xxx xxxxxxx xxxxxxxxxxxxxx xxxxxx, xxxxx xxxxxxxx xxxxxxxxxxxx xxxxx jednotky tkáně xx buňky xx xxxxx etapách xxxxxxxx, x xxxx se xxxx o akreditaci, xxxxxxxxx, xxxxxxxxx xxxx xxxxxxxx. |
X.&xxxx;&xxxx;&xxxx;XXXXXXXXXX
|
1. |
Xxxxxxxxxx musí xxx x xxxxxxxx xxxxxxxx xxxxxxxxxx počet a xxxxxx být xxxxxxxxxxxxx xxx xxxxx, xxxxx xxxxxxxxx. Způsobilost xxxxxxxxxx xxxx xxx xx xxxxxxxx xxxxxxxxxxx, xxxxxxxxxxx x xxxxxxx xxxxxxx, xxxxxxxxxxxxx. |
|
2. |
Xxxxxxx xxxxxxxxxx xxxxxx xxx xxxxx, xxxxxxxxxxxxxx x xxxxxxxx popis xxxxx. Jejich xxxxx, xxxxxxxxxx a xxxxxxxxxxxx xxxxxx xxx jasně xxxxxxxxxxxxxx x pochopeny. |
|
3. |
Pracovníkům xxxx být poskytnuta xxxxxxxxx xx xxxxxxxx xxxxxxx xxxxxxxx, xxxxxxxxxxxxx xxxxxxxx v xxxxxxx, xx xx xxxxx xxxxxxx nebo se xxxxxxxx xxxxxxx poznatky, x xxxxxxxxxxxx xxxxxxxxxxxx xxx xxxxxxx rozvoj. Xxxxxxx odborné xxxxxxxx xxxx xxxxxxxx x xxxxxxxxxxxxx, že každý xxxxxxxxxxx:
|
X.&xxxx;&xxxx;&xxxx;XXXXXXXX X MATERIÁLY
|
1. |
Veškeré xxxxxxxx x xxxxxxxx xxxxxx xxx xxxxxxxx a xxxxxxxxx xxxxxxxx xxxxxxx xxx xxxxxx xxxxxx xxxx x xxxxxx xxx příjemce a/nebo xxxxxxxxxx představovat xxxxxxxxx xxxxxx. |
|
2. |
Xxxxxxx kritické xxxxxxxx x xxxxxxxxx xxxxxxxxxx xxxxxx být xxxxxxxxxxxxxx x xxxxxxxxxx, xxxxxxxxxx xxxxxxxxxxxx x xxxxxxxxxxx xxxxxxxxx x xxxxxxx x xxxxxx výrobce. Xxxxx vybavení xxxx xxxxxxxxx mají xxxx xx kritické xxxxxxxxx xxxxxxxxxx xx skladování (xxxx. xxxxxxx, xxxx, xxxxx xxxxxx, xxxxxx xxxxxxxxxxx xxxxxxxxxxx), musejí xxx xxxxxxxxxxxxxx a xxxxx potřeby xxxxxxxx xxxxxxxxxxx xxxxxxxxx, xxxxxxxx xxxxxxxx, xxxxxxxx x xxxxxxxxxx xxxxxxxx, xxx xxxx zjištěny xxxxxxx x vady x xxxx xxxxxxxxx, xx xxxx kritické xxxxxxxxx xxxxxxxxxxx xxxxxxxxx x xxxxxxxxxxxx xxxxxx. Veškeré xxxxxxxx, xxxxxx xx xxxx kritické parametry, xxxx xxx xxxxxxxxxxx xxxxx sledovatelného etalonu, xx-xx x xxxxxxxxx. |
|
3. |
Xxxx x xxxxxxxx xxxxxxxx xxxx xxx při xxxxxxxxx xxxxxxxxxx a xxxx xxxxxxxx xxxxxxxxxx. Xxxxxxxx xxxxxxx xx xxxxxxxxxxxx. |
|
4. |
Xxxxxx, xxxxxxxx xxxxxx, xxxxxxx, dezinfekce x xxxxxxxx se x xxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxx x xxxx náležitě zaznamenávány. |
|
5. |
Musejí xxx k xxxxxxxxx xxxxxxx xxx provoz xxxxx součásti xxxxxxxxxx xxxxxxxx, podrobně xxxxxxxxxx xxxxxxxx, jež xxxx xxx xxxxxxx x xxxxxxx poruchy xx xxxxxxx. |
|
6. |
Xxxxxxx u xxxxxxxx, x xxxx xx xxxx o xxxxxxxxxx, xxxxxxxxx, xxxxxxxxx xxxx xxxxxxxx, musejí xxxxxxxx xxxxxx specifikace xxxxx xxxxxxxxxx xxxxxxxxx x xxxxxxxxx činidel. Zejména xx třeba xxxxxxxxx xxxxxxxxxxx xxxxxxxxxx xxxxx (xxxx. xxxxxxx) x xxxxxxxxx xxxxxxxxx. Xxxxxxxx xxxxxxx činidla x xxxxxxxxx xxxxxx xxxxxxxx xxxxxxxxxxxxxx požadavky x xxxxxxxxxxx x xxxxxxxx xxxxxxxxx xxxxxxx xx xxxxxxxx Rady 93/42/XXX xx xxx 14. xxxxxx 1993 x xxxxxxxxxxxxxx prostředcích (1) x xxxxxxxx Evropského parlamentu x Xxxx 98/79/XX xx xxx 27. xxxxx 1998 x xxxxxxxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxxxxx xx vitro (2). |
D. PROVOZOVNY A XXXXXXXX
|
1. |
Xxxxxxx zařízení musí xxx xxxxxx provozovny xxx provádění xxxxxxxx, x xxxx xx xxxx o xxxxxxxxxx, xxxxxxxxx, oprávnění xxxx xxxxxxxx, x to x xxxxxxx x xxxxxxx xxxxxxxxxxx x xxxx xxxxxxxx. |
|
2. |
Xxxxx tyto xxxxxxxx xxxxxxxx zpracování xxxxx x xxxxx xxx xxxxxxxxx prostředí, xxxxxx xxxxxxxx x xxxxxxxxx x přesně xxxxxxxxxx xxxxxxxx a xxxxxxxx xxxxxxx, xxx xx xxxxxxxxxxxxxx riziko xxxxxxxxxxx, xxxxxx křížové xxxxxxxxxxx xxxx xxxxxxx x xxxxxxx z xxxxxxx darování. Xx xxxxx xxxxxxxxx x xxxxxxxx xxxxxxxx xxxxxx xxxxxxxx. |
|
3. |
Xxxxx xxx 4 xxxxxxxxx xxxxx, xxxx-xx xxxxx xx buňky xxxxxxxxx xxxxx xxxxxxxxxx xxxxxxxxx, xxxx xx xxxxxxxx xxxx podrobeny xxxxxxx xxxxxxxxxxx xxxxxxxxxx, xx xxxxxxxxxx xxxxxxx xxxxxxx, v němž xxxx xxxxx xxxxxx x xxxxx xxxxxxxxxxxxx xxxxxxx xxxxxxxxxx xxxxxx xx třídě xxxxxxx X, jak xx xxxxxxxxxx v xxxxxxx 1 xxxxxxxx Xxxxxxxxxx xxxxxx pro xxxxxxxx xxxxxxx praxi x xx xxxxxxxx 2003/94/ES, x prostředí pozadí xxxxxx xxx xxxxxxxxxx xxxxxxxxxxx xxxxx xxxx xxxxx, které xxxx xxxxxxxx xxxxxxx xxxxx xxxxxxx D xxxxxxx xxxxxxx xxxxx, pokud xxx x počet xxxxxx a počet xxxxxxxxxxxxx xxxxxxx. |
|
4. |
Xxxx xxxxxx xxxxxx na prostředí, xxx xxxx jsou xxxxxxx x xxxx 3, xxxx xxxxxxxxxx x xxxxxxx, xx:
|
|
5. |
Je xxxxx xxxxx stanovit xxxxxxxxx x xxxx 4 xxxx. a), x), c) x x). Musí xxx xxxxxxxxx x xxxxxxxxxxxxxx, xx zvolené xxxxxxxxx xxxxxxx xxxxxxxxx na xxxxxx a bezpečnost, xxxxxxx x xxxxxxx xx určený xxxx, xxxxxx použití x xxxxxxxx xxxx příjemce. X xxxxxx xxxxxxxxxx xxxxxxxx tkáňového xxxxxxxx xx xxxx xxxxxxxxxx xxxxxx xxxx a xxxxxxxx xxx xxxxxx xxxxxxx a hygienu x xxxxxxx xxxxxx xxx xxxxxxx a xxxxxxxx. |
|
6. |
Xxxxx xxxxxxxx, x xxxx xx xxxx x xxxxxxxxxx, xxxxxxxxx, xxxxxxxxx xxxx xxxxxxxx, xxxxxxxx skladování xxxxx x xxxxx, xxxxxx xx definovat xxxxxxxx xxxxxxxxxx xxxxxxxx x xxxx, xxx si xxxxx x xxxxx xxxxxxxx xxxxxxxxxx vlastnosti, xxxxxx xxxxxxxxx xxxx xxxxxxx, xxxxxxx nebo xxxxxxx xxxxxxx. |
|
7. |
Xxxxxxxx xxxxxxxxx xx xxxxxx xxxxxxxxxxx, xxxxxxxx x xxxxxxxxxxxx (xxxx. xxxxxxx, xxxxxxx, xxxxxxx xxxxxxx), xxx xx xxxxxxxxx, xx xxxx xxxxxxxxxx stanovené xxxxxxxx xxxxxxxxxx. |
|
8. |
Xxxxxx xxx xxxxxxxxx skladovací xxxxxxxx, xxxxx xxxxx oddělují x xxxxxxxx xxxxx x buňky xxxx xxxxxxxxxxx x xxxxxxxxx xx xxxx, xxxxx xxxx již propuštěny, x xxxx, xxxxx xxxx xxxxxxxxx, xxx xx xxxxxxxxx záměně x xxxxxx křížové xxxxxxxxxxx. Pro xxxxxxxxxx xxxxxxxx tkání x xxxxx xxxxxxxxxx xxxxx xxxxxxxxxx xxxxxxxx xxxxxx xxx v místech xxxxxxxxxx tkání x xxxxx x karanténě x x místech xxxxxxxxxx xxxxxxxxxxxx xxxxx x xxxxx xxxxxxxxx xxxxxxx xxxxxxxx xxxxxxxx xx xxxxxxxxxx xxxxxxxx xxxx xxxx být xxxxxx xxxxxxxx xxxxxxxxxxx xxxxxxxx. |
|
9. |
Xxxxxxx xxxxxxxx xxxx xxx xxxxxxxx koncepci x xxxxxxx xxx xxxxxxxxxxxx přístup, xxxxxxx x xxxxxx, xxxxxxxxx x odpadem x xxx xxxxxx poskytování xxxxxx při xxxxxxxxx xxxxxxx. |
X.&xxxx;&xxxx;&xxxx;XXXXXXXXXXX A ZÁZNAMY
|
1. |
Pro xxxxxxxx, x nimž xx xxxx o xxxxxxxxxx, jmenování, xxxxxxxxx xxxx povolení, xxxx xxx zaveden systém, xxxxx xxxxxxx xxxxx xxxxxxxxx x xxxxxxxxx xxxxxxxxxxx, správné xxxxxxx x registry x xxxxxxxxx standardní xxxxxxxx xxxxxxx. Xxxxxxxxx musejí xxx xxxxxxxxxx přezkoumávány x xxxxxx xxxxxxxx xxxxx xxxxxxxxx x xxxx xxxxxxxx. Xxxxxx xxxx xxxxxxxxx, xx xx xxxxx prováděna xxxxx daných norem x xx veškeré xxxxx, xx. xxxxxxxx, xxxxxxxxxxx xxxxx, xxxxx, xxxxxxxxxx, konzervaci, xxxxxxxxxx, xxxxxxxx, xxxxxxxxxx či xxxxxxxxx, včetně xxxxxxx xxxxxxxxxx xx xxxxxxxx x xxxxxxxxxxx xxxxxxx, xxxx xxxxxxxxxxxx. |
|
2. |
X xxxxx xxxxxxxx xxxxxxxx xxxx xxx xxxxxxxxxxxxxx x xxxxxxxxxxxxxx xxxxxxx xxxxxxxxx, xxxxxxxx x zúčastnění xxxxxxxxxx. |
|
3. |
Xxxxxxx xxxxx dokumentace x tkáňovém zařízení xxxxxx xxx xxxxxxxxxxx, xxxxxxxx datem, xxxxxxxxx, xxxxxxxxxxxxxx a xxxxx xxxxxxxxx xxxxxxxxxxx xxxxxxxxxx. |
|
4. |
Xxxxxx xxxxxxxx xxxxxxxxx xxxx xxx xxxxxxxx tak, xxx xxxxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxxxxxxxx dokumentů x xxxxxx změn x xxxxxxxxxx, že xxxx používány pouze xxxxxxxx xxxxx xxxxxxxxx. |
|
5. |
Xxxxxxx xxxxxx xxxxxxxxxx x xxxxxxxx xxxxxxxxxx xxxxxxxx. |
|
6. |
Xxxxxxx xxxxxx být xxxxxxx x xxxxxxxxxxxx, xxxxx xxx psané xxxxx xx xxxxxxxxx do xxxxxx xxxxxxxxxxxx xxxxxxx, xxxx. xx xxxxxxxxxxxx xxxxxx xx na xxxxxxxxx. |
|
7. |
Xxxx xx xxxxxx xx. 9 xxxx. 2, veškeré xxxxxxx, xxxxxx xxxxxxxxxx údajů, xxxxx jsou xxxxxxxx xxxxxxxx xxx xxxxxxxxxx x jakost xxxxx x buněk, se xxxxxxxx xxx, xxx x xxx xxx xxxxxxxx přístup alespoň xx xxxx xxxxxx xxx xx xxxx xxxxxxxx xxxxxxxxxxxxx, xxxxxxxxxx xxxxxxx xx xxxxxxxxx. |
|
8. |
Xxxxxxx xxxxxx xxxxxxxx xxxxxxxxx xx xxxxxxxxx xxxxx xxxxxx 14 xxxxxxxx 2004/23/XX. Přístup xx xxxxxxxx x k xxxxxx musí xxx xxxxxxx xxxxx xxxxxx, xxxxx mají oprávnění xx xxxxxxxxx xxxxx, x xxxxxxxxxxx xxxxxx xxx xxxxx xxxxxxxx x xxxxxxxxxxx opatření. |
F. PŘEZKOUMÁNÍ XXXXXXX
|
1. |
X xxxxxxxx, x xxxx xx xxxx x xxxxxxxxxx, jmenování, xxxxxxxxx xxxx povolení, xxxx xxx xxxxxxx xxxxxx auditu. Xxxxxxxxxxxxx x způsobilé osoby xxxxxx audit xxxxxxxx xxxxxxxxx x xxxxxxx xxxxxx xx dva xxxx, xxx xx xxxxxx xxxxxx xx xxxxxxxxxxx xxxxxxxxx x xxxxxxxxxxx xxxxxxxxx. Zjištění x xxxxxxxx xxxxxxxx xx xxxxxx zdokumentovat. |
|
2. |
Odchylky xx xxxxxxxxxxxx norem xxx xxxxxx a xxxxxxxxxx xx musejí xxxxxxxx x xxxxxxxxxxxxx, xxx xxxxxxxx xxxxxx xxxxxxxxxx x případných xxxxxxxxxx a xxxxxxxxxxxxx xxxxxxxxxx. X xxxxx xxxxx x xxxxx, xxxxx xxxxxxxxx xxxxxxxxx, xx xxxx rozhodnout x xxxxxxx x xxxxxxxxx xxxxxxx a xx xxxxxxx xxxxxxxxx xxxxx, xxxx xxxxxxxxxx xx xxxx xxxxxxxxxx. Xxxxxxx xxxxxxx xxxxx x xxxxx xxxxxx xxx xxxxxxxxxxxxxx x xxxx o xxxx xxx xxxxxx zpráva. |
|
3. |
Nápravná xxxxxxxx musejí xxx xxxxxxxxxxxxxx, zahájena a xxxxxxxxx xxxx x xxxxxxx xxxxxxxx. Xx xxxxxxxxx preventivních x xxxxxxxxxx opatření xx xxxx xxx posouzena xxxxxx účinnost. |
|
4. |
Tkáňová xxxxxxxx xxxxxx xxx xxxxxxxx xxxxxxx xxx xxxxxxxxxxx xxxxxx xxxxxxx xxxxxx xxxxxxx, xxx se xxxxxxxxx xxxxxxxxxxx x xxxxxxxxxxxx zlepšování. |
(1) Úř. věst. X 169, 12.7.1993, x. 1. Xxxxxxxx xxxxxxxxx xxxxxxxxx nařízením Xxxxxxxxxx xxxxxxxxxx x Xxxx (XX) č. 1882/2003 (Úř. xxxx. X 169, 12.7.1993, x. 1).
(2)&xxxx;&xxxx;Xx. věst. X 331, 7.12.1998, x. 1. Xxxxxxxx xx xxxxx xxxxxxxx (XX) č. 1882/2003.
XXXXXXX XX
Xxxxxxxxx xxx xxxxxxx příslušného oprávnění xxx xxxxxxx přípravy xxxxx x xxxxx x xxxxxxxxx zařízeních, xxx je uvedeno x xxxxxx 4
Xx xxxxxxxxxxx kritérií xxx xxxxx xxxxx x xxxxxxx xxxxxx, xxxxxxxxx xxx každou xxxxx xxxxxxx, xxxxxxxx xxx xxxxxx xxxxxxx a xxxxxxxxxxx množstevních xxxxxxxx x xxxxxxxx xxx xxxxxx buněk x xxxxx xxxxx xxxxxxxxx xxxxx každému xxxxxxx xxxxxxxx xxxxx a xxxxx oprávnění. Takové xxxxxxxxx xxxx xxxxxxxx xxxxxxx xxxxxxxxx xxxxxxxxx x xxxx xxxxxxx.
X. XXXXXXX X XXXXXXXX ZAŘÍZENÍ
Při xxxxxxx odebraných xxxxx x xxxxx x xxxxxxxx xxxxxxxx musejí xxxxx a xxxxx xxxxxxxx požadavky definované xx směrnici 2006/17/XX.
X. XXXXXXXXXX
Pokud xxxxxxxx, x nimž xx xxxx x xxxxxxxxxx, xxxxxxxxx, xxxxxxxxx xxxx xxxxxxxx, xxxxxxxx xxxxxxxxxx tkání x xxxxx, musejí xxxxxxx x xxxxxxxx xxxxxxxx xxxxxxxx xxxx xxxxxxxx:
|
1. |
Kritické xxxxxxx zpracování musejí xxx validovány x xxxxxxx xxxxx xx xxxxx xxxxx klinicky xxxxxxxxxx xx xxxxxxxxxx xxx xxxxxxxx. Xxxx xxxxxxxx musí vycházet xx studií provedených xxxxxxxxx nebo z xxxxx xx xxxxxxxxxxxx xxxxxx nebo, x xxxxxxx xxxxxxxxxxx xxxxxxx xxxxxxxxxx, ze xxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxx x xxxxx xxxxxxxx xxxxx xxxxxxxxx. |
|
2. |
Xxxx být xxxxxxxxx, xx xxxxxxxxxx xxxxx validovaný xxxxxx xxxxxxxx v prostředí xxxxxxxxx xxxxxxxx xxxxxx x účinně. |
|
3. |
Xx xxxxxxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxx xxx postupy zdokumentovány x musejí být x xxxxxxx s xxxxxxxxxxx metodou x xxxxxxx stanovenými v xxxx směrnici, x xx x souladu x xxxxxxxx I xxxxx X body 1 xx 4. |
|
4. |
Xxxx xxx xxxxxxxxx, xx xx veškeré procesy xxxxxxxxx v xxxxxxx xx xxxxxxxxxxx standardními xxxxxxxxxx xxxxxxx. |
|
5. |
Xx-xx xx xxxxx nebo xxxxx xxxxxxxx xxxxxx xxxxxxxxxxx xxxxxxxxxx, xxxx xxx xxxxx xxxxxx specifikován, xxxxxxxxxxxxx x xxxxxxxxx. |
|
6. |
Před xxxxxxxxxx jakékoli xxxxxxxx xxxxx xx xxxxxxxxxx xxxx xxx xxxxxxxxx xxxxxx xxxxxxxxx a xxxxxxxxxxxxx. |
|
7. |
Xxxxxxx xxxxxxxxxx xxxxxx xxx xxxxxxxxxxx xxxxxxxxxxxx xxxxxxxxxx xxxxxxxxx, xxx xx xxxxxxxxx, xx xxxxx x xxxxxx xxxxxxxxx určených výsledků. |
|
8. |
Xxxxxxx xxx xxxxxxxxxx tkání x xxxxx xxxxxx xxxxxx kontaminaci tkání x xxxxx x xxxxxx darování x xxxxxxxxx, xxxxxxxxx pro xxxxxxxxxx a pracovníků. Xxxx postupy musejí xxxxxxxxx vnitrostátním xxxxxxxxx. |
X. XXXXXXXXXX X XXXXXXXXXXX XXXXXXXXX
Pokud xxxxxxxx, k xxxx xx xxxx x xxxxxxxxxx, xxxxxxxxx, oprávnění xxxx xxxxxxxx, zahrnují xxxxxxxxxx x xxxxxxxxxxx xxxxx x buněk, xxxxxx postupy v xxxxxxxx xxxxxxxx x xxxxxxxxxx xxxxxxxx xxxx xxxxxxxx:
|
1. |
Xxx xxxxx xxx xxxxxxxx skladování musí xxx určena xxxxxxxxx xxxx skladování. Xxxxxxx xxxx musí xxxx xxxx xxxxxxx případné xxxxxxxx xxxxxxxxxxxx xxxxxxxxxx xxxxx xx buňky. |
|
2. |
Xxxx xxx xxxxxxx xxxxxx xxxxxxxx xxxxx a/nebo xxxxx v xxxxxxxxx, xxx xx zaručilo, xx xxxxxxx být xxxxxxxxxx, xxxxx xxxxxxxxx xxxxxxx xxxxxxxxx této xxxxxxxx. Xxxx existovat xxxxxxxxxx xxxxxxxx xxxxxx, x xxxx jsou xxxxxxxx xxxxxxx xxxxxxxxx, xxxxxxxxxx x xxxxxxx xxx propouštění xxxxx x xxxxx x xxxxxxxxxx. |
|
3. |
Xxxxxx identifikace xxxxx x xxxxx x xxxxx xxxxx xxxxxxxx xxxxx xxxxxxxxxx v xxxxxxxx xxxxxxxx xxxx xxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxxxx xx xxxxxxxxx xxxxxxxxxxxxxx (v karanténě) x přípravků vyřazených. |
|
4. |
Záznamy xxxxxx xxxxxxxxxx, xx xxxx xxxx xxxxxxxxxxx xxxxx a buněk xxxxxxx všechny xxxxxxxx xxxxxxxxxxx, xxxxxxx xx xxxx xxxxxxx xxxxxxxxx xxxxxxxxxx, náležité xxxxxxxx xxxxxxx, xxxxxxx x xxxxxxxxxx x xxxxxxxx xxxxxxx xxxxxxx podle xxxxxxxxx postupu xxxxxx xxxxxxxxx xxxxx xxxxxx xxxxxxxxxx osobou xxxxxxxx x xxxxxx 17 xxxxxxxx 2004/23/ES. Pokud xx x uvolnění xxxxxxxx z laboratoře xxxxxxx xxxxxxx, xxxx xxxxxx x xxxxxxxx xxxxxx, kdo je xx xxxxxxxx xxxxxxxxx. |
|
5. |
Je xxxxx xxxxxxx zdokumentované xxxxxxxxx xxxxx, které xxxxxxx odpovědná xxxxx xxxxxxx v xxxxxx 17 xxxxxxxx 2004/23/ES, xxx xx xx xxxxxxxx nových xxxxxxxx xxx výběr xx xxxxxxxxx xxxxx xxxx xxxxxxx změněné etapy xxxxxxxxxx, xxxxx xx xxxxxx bezpečnost a xxxxxx, xxxxx xxxx xxxxx xxxxxxxxxxxx xxxxx x buněk. |
X. XXXXXXXXXX X XXXXXXX
Xxxxx xxxxxxxx, x xxxx se xxxx x xxxxxxxxxx, xxxxxxxxx, xxxxxxxxx nebo povolení, xxxxxxxx xxxxxxxxxx xxxxx x xxxxx, musejí xxxxxxx x xxxxxxxx xxxxxxxx s xxxxxxxxxx xxxxxxxx xxxx xxxxxxxx:
|
1. |
Xxxxxx xxx xxxxxxxxxx xxxxxxxx xxxxxxxx přepravy, xxxx. xxxxxxx x xxxxx, xxx xx xxxxxxxxx xxxxxxxxxx vlastnosti xxxxx x xxxxx. |
|
2. |
Xxxxxx/xxxxxx xxxxxx xxx bezpečné a xxxxxx xxxxxxxxx, že xxxx tkáně a xxxxx xxxxxxxxxx za xxxxxx stanovených xxxxxxxx. Xxxxxxx nádoby x xxxxxx xxxxxx xxx xxxxxxxxxx xxxx vhodné xxx xxxx xxxx. |
|
3. |
Pokud xxxxxxxxxx provádí xxxxx xxxxxx xx xxxxxxx xxxxxxx, xxxx existovat xxxxxxxxxxxxxx xxxxxx, xxx xx xxxxxxxx, že xxxxx xxxxxxxx xxxxxxxxxx xxxxxxxx. |
|
4. |
X xxxxxxxx xxxxxxxx xxxx xxxxxxxxxxx oprávnění xxxxxxxx nezbytnost xxxxxxx x xxxxx a xxxxxxx x koordinovat xxxxxxxx xxxxx. |
|
5. |
Musí xxx xxxxxxx xxxxxx postup xxxxxxx x xxxxx xxxxxx xxxxxx xxxxxxxxxx x kroků, xxx xx mají xxxxxxx. Xxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx. |
|
6. |
Xxxxx učiněné x xxxxxx xxxxxxxxx xxxxxx musejí xxxxxxxxx xxxxxxxxx všech xxxxxxxxxxx xxxxx a xxxxx x x xxxxxxx xxxxxxx také xxxxxx xxxxxxxxxxx. Xxxxxx šetření xx xxxxxxxxxxxxx dárce, xxxxx xxxx přispět x xxxxxxxx reakce x příjemce, x xxxxxxxx xxxxxxxx xxxxx x xxxxx xx xxxxxxxx xxxxx, jakož x xxxxxxxxxx xxxxxxxxxx x xxxxxxxx xxxxx x xxxxx xxxxxxxxxx xx xxxxxx xxxxx xxx xxxxxx, že xxxxx xxx xxxxxxxx. |
|
7. |
Musejí xxx xxxxxxxx xxxxxxx xxx xxxxxxxxxx žádostí x xxxxx x xxxxx. Xx xxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxx a buněk xxxxxxx xxxxxxxxx xxxx xxxxxxxxxxxxx institucím x xx xxxxxx xx xxxxx xxxxxxx xxxxxxxxxxx. |
|
8. |
Musí xxx xxxxxxx xxxxxxxxxxxxxx xxxxxx xxx xxxxxxxxxx x xxxxxxxxx xxxxxxxxx, xxxxxxxx xxxxxx xxxxxxxx xxx xxxxxx xxxxxxx xx xxxxxxxxx. |
X. XXXXXXX XXXXXXXX XXX XXXXXXXXXX
|
1. |
Xxxxxxxx nádoba xxx xxxxx/xxxxx musí xxxxxx:
Xxxxx xxxxxxx x informací x xxxxxxxxx d) x e) xxxxx xx xxxxxx primární xxxxxx xxxxx, xxxxxx xxx xxxxxxxxxx xx xxxxxxxxx xxxxx, xxxxx xxxxxxxx xxxxxx xxxxxxx. Xxxxx xxxx musí xxx k xxxxxxxx xxxxxx xxxxxxxx xxx, xxx xx xxxxxxxx, xx xx sebe xxxxxxx xxxxxxxx. |
|
2. |
Xx xxxxxx xxxx x průvodní xxxxxxxxxxx xx xxxxxx xxxxx tyto xxxxxxxxx:
|
X. XXXXXX OZNAČOVÁNÍ XXXXXXXXXXX KONTEJNERU
Pro xxxxxxxx xxxx být xxxxxxxx xxxxxx umístěna xx xxxxxxxxxxx xxxxxxxxxx, xx xxxxx xxxxxx xxxxxx xxx xxxxxxx xxxxxxx xxxx informace:
|
a) |
identifikace xxxxxxxxx xxxxxxxxx xxxxxxxx včetně xxxxxx x telefonního xxxxx; |
|
x) |
xxxxxxxxxxxx xxxxxx xxxxxxxxxx xxxxxxxxx za použití x člověka včetně xxxxxx a xxxxxxxxxxx xxxxx; |
|
x) |
xxxxxxxxxx, xx balení xxxxxxxx lidské xxxxx/xxxxx x xxxxx „XXXXXXXXXXX XXXXXXX“; |
|
x) |
xxxxx xxxx xxx xxxxxxxxx xxxxxxxxxxxxx potřebné xxxx xxxxx, xxxx. xxxxxxx xxxxx, gamety x xxxxxx, xxxx xx doplnit xxxxx „XXXXXXXXXX“; |
|
x) |
xxxxxxxxxx xxxxxxxxx xxxxxxxx (xxxx. xxxxxxxxx v xxxxxx, xx xxxxxx xxxxxx xxx.); |
|
x) |
xxxxxxxxxxxx pokyny/metoda xxxxxxxx (xxxxx xx xx možné). |
XXXXXXX XXX
XXXXXXXXXX XXXXXXXXX XXXXXXXXXXX XXXXXX
XXXXXXX XX
XXXXXXXXXX XXXXXXXXX XXXXXXXXXXX XXXXXX
PŘÍLOHA V
FORMULÁŘ PRO XXXXXXX OZNÁMENÍ

XXXXXXX XX
Xxxxxxxxx x xxxxxxxxxx xxxxxxx údajů x dárci x xxxxxxxx, xxxxx se xxxx uchovat, xxx xxxxxxxx článek 9
X. XX XXXXXXXXX XXXXXXXXXX
Identifikace dárce
Xxxxxxxxxxxx xxxxxxxx zahrnující xxxxxxx:
|
— |
identifikaci xxxxxxxxxx xxxxxxxxxxx xxxxx xxxx tkáňového xxxxxxxx, |
|
— |
xxxxxxxxx xxxxxxxxxxxxx xxxxx xxxxxxxx, |
|
— |
datum xxxxxx, |
|
— |
xxxxx xxxxxx. |
|
— |
druh xxxxxxxx (xxxx. xxxxx tkáň xx více xxxxx; xxxxxxxxx xx xxxxxxxx; xxxxxx či xxxxxxx xxxxx) |
Xxxxxxxxxxxx přípravku xxxxxxxxxx xxxxxxx:
|
— |
xxxxxxxxxxxx tkáňového xxxxxxxx, |
|
— |
xxxx xxxxx x xxxxx/xxxxxxxxx (xxxxxxxx xxxxxxxxxxxx), |
|
— |
číslo xxxxxxx (xx-xx xxxxxxxxxx), |
|
— |
xxxxx xxxxxx (xx-xx xxxxxxxxxx), |
|
— |
datum ukončení xxxx xxxxxxxxxxxxx, |
|
— |
stav xxxxx/xxxxx (xx. v karanténě, xxxxxx x xxxxxxx xxx.), |
|
— |
xxxxx x xxxxx xxxxxxxxx, xxxxxxxxx kroků xxx xxxxxxxxxx, materiálů x xxxxxxxxxx látek, xxxxx přicházejí do xxxxx s xxxxxxx x xxxxxxx x xxxx xxxx na xxxxxx jakost a/nebo xxxxxxxxxx, |
|
— |
xxxxxxxxxxxx xxxxxxxx, xxxxx xxxxxx konečný xxxxxx. |
Identifikace xxxxxxx u xxxxxxx xxxxxxxxxxxx xxxxxxx:
|
— |
xxxxx xxxxxxxxxx/xxxxxxxxx, |
|
— |
identifikace xxxxxxxxxx xxxxxx a xxxxxxxxx xxxxxxxxx/xxxxxxxx. |
X. X ORGANIZACÍCH XXXXXXXXXXX XX XXXXXXX X XXXXXXX
|
x) |
xxxxxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxx xxxxxxxx; |
|
x) |
xxxxxxxxxxxx klinického xxxxxx x konečného xxxxxxxxx/xxxxxxxx; |
|
x) |
xxxx tkání x xxxxx; |
|
x) |
xxxxxxxxxxxx přípravku; |
|
x) |
xxxxxxxxxxxx xxxxxxxx; |
|
x) |
xxxxx xxxxxxx. |
XXXXXXX XXX
Xxxxxxxxx obsažené x xxxxxxxxx xxxxxxxxx xxxxxxx
|
x) |
Xxxxxxxxxxxx xxxxxxxx:
|
|
x) |
Xxxxxxxxxxxx xxxxxxxxx:
|


