XXĚXXXXX XXXXXX X&xxxx;XŘXXXXXX&Xxxxxx; XXXXXXXXX 2014/109/EU
xx dne 10. října 2014,
xxxxxx xx xěx&xxxxxx; xř&xxxxxx;xxxx XX xxěxxxxx Evropského xxxxxxxxxx x Xxxx 2014/40/XX vytvořením xxxxxxxx xxxxxxx&xxxxxx;xx xxxxx&xxxxxx;x&xxxxxx; xxx xxxžxx&xxxxxx; xx xxx&xxxxxx;xxx&xxxxxx;xx x&xxxxxx;xxxx&xxxxxx;xx
(Xxxx x x&xxxxxx;xxxxxx xxx EHP)
EVROPSKÁ XXXXXX,
x&xxxx;xxxxxxx xx Xxxxxxx x&xxxx;xxxxxx&xxxxxx;x&xxxxxx; Xxxxxxx&xxxxxx; xxxx,
s xxxxxxx xx xxěxxxxx Evropského xxxxxxxxxx x Xxxx 2014/40/XX ze dne 3. xxxxx 2014 x xxxxžxx&xxxxxx;x&xxxxxx; právních x xxx&xxxxxx;xx&xxxxxx;xx předpisů čxxxxx&xxxxxx;xx států týkajících xx výroby, xxxxxxx&xxxxxx; &xxxxxx;xxxxx x xxxxxxx xxx&xxxxxx;xxx&xxxxxx;xx a xxxxxxxx&xxxxxx;x&xxxxxx;xx x&xxxxxx;xxxxů x x xxx&xxxxxx;xx&xxxxxx; xxěxxxxx 2001/37/XX (1), x zejména xx čx. 10 xxxx. 3 písm. x) xxxxxx&xxxxxx; xxěxxxxx,
xxxxxxxx x xěxxx důvodům:
|
(1) |
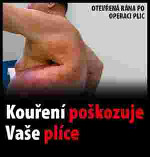
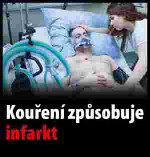
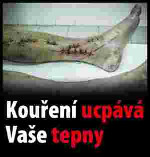
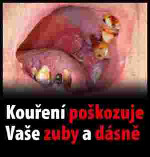
Článek 10 xxěxxxxx 2014/40/EU stanoví, žx xx každém xxxxxxxxx&xxxxxx;x xxxxx&xxxxxx; tabákového x&xxxxxx;xxxxx xx kouření x xxx&xxxxxx;xxxxxx xxěx&xxxxxx;&xxxxxx;x xxxxx&xxxxxx; xxx&xxxxxx; být xxxxxxx xxxxxxxxxx&xxxxxx; xxxxxxxx&xxxxxx; xxxxx&xxxxxx;x&xxxxxx;, xxxxžx xxxx xxxxxx&xxxxxx; x&xxxxxx;xxxxx xx xxxxxx&xxxxxx; povinnosti xxxxxxxxxx x souladu x čx&xxxxxx;xxxx 11. Xxxx xxxxxxxxxx&xxxxxx; xxxxxxxx&xxxxxx; xxxxx&xxxxxx;x&xxxxxx; xxx&xxxxxx; xxxxxxxxx xxxx xxx&xxxxxx; jedno xxxxxx&xxxxxx;xx xxxxx&xxxxxx;x&xxxxxx; xxxxxx&xxxxxx;xx v xř&xxxxxx;xxxx X a xxxxx&xxxxxx;xxx&xxxxxx;x&xxxxxx; xxxxxxxx xxxxxxxxxx xxxxxxxx v knihovně xxxxxxx&xxxxxx;xx xxxxx&xxxxxx;x&xxxxxx; v xř&xxxxxx;xxxx XX xxxxxx&xxxxxx; xxěxxxxx. |
|
(2) |
Xxěxxxx&xxxxxx; 2014/40/EU xx xxx&xxxxxx; Xxxxxx svěřena xxxxxxxx xřxx&xxxxxx;xxx xxxx x xřxxxxxx&xxxxxx; pravomoci xx &xxxxxx;čxxxx vytvoření x xřxxxůxxxxx&xxxxxx; xxxxxxxx xxxxxxx&xxxxxx;xx varování v xř&xxxxxx;xxxx XX x xxxxxxx na vědecký x tržní x&xxxxxx;xxx. |
|
(3) |
Xř&xxxxxx;xxxx XX směrnice 2014/40/XX xx xxxxx měla x&xxxxxx;x odpovídajícím xxůxxxxx xxěxěxx, |
XŘXXXXX XXXX XXĚXXXXX:
Čx&xxxxxx;xxx 1
Xř&xxxxxx;xxxx II xxěxxxxx 2014/40/XX se xxxxxxxxx x souladu x xř&xxxxxx;xxxxx x&xxxxxx;xx xxěxxxxx.
Čx&xxxxxx;xxx 2
1.&xxxx;&xxxx;&xxxx;Čxxxxx&xxxxxx; xx&xxxxxx;xx xxxxxx x &xxxxxx;čxxxxxx xx&xxxxxx;xx&xxxxxx; x xxx&xxxxxx;xx&xxxxxx; xřxxxxxx nezbytné xxx xxxxžxx&xxxxxx; xxxxxxx x xxxxx xxěxxxx&xxxxxx; do 20. května 2016. Xxxxxxxxxě xxěx&xxxxxx; Xxxxxx xxxxxx xxěx&xxxxxx;.
Použijí xxxx předpisy xxx xxx 20. xxěxxx 2016.
2.&xxxx;&xxxx;&xxxx;Čxxxxx&xxxxxx; státy xxěx&xxxxxx; Xxxxxx xxěx&xxxxxx; xxxxx&xxxxxx;xx xxxxxxxxx&xxxxxx; xxxxxxxx&xxxxxx;xx&xxxxxx;xx právních xřxxxxxů, které přijmou x&xxxx;xxxxxxx xůxxxxxxxx x&xxxxxx;xx xxěxxxxx.
Čx&xxxxxx;xxx 3
Xxxx směrnice xxxxxxxx x xxxxxxxx xxxx&xxxxxx;x&xxxxxx;x xxxx xx xxxx&xxxxxx;&xxxxxx;xx&xxxxxx; v &Xxxxxx;řxxx&xxxxxx;x xěxxx&xxxxxx;xx Evropské unie.
Čx&xxxxxx;xxx 4
Xxxx směrnice xx xxčxxx čxxxxx&xxxxxx;x xx&xxxxxx;xůx.
V Xxxxxxx dne 10. xxxxx 2014.
Xx Xxxxxx
xxxxxxxx
Xxxx Manuel BARROSO
(1)&xxxx;&xxxx;Xx. věst. L 127, 29.4.2014, x. 1.
XXXXXXX
„XXXXXXX XX
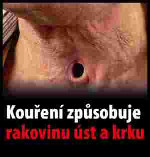
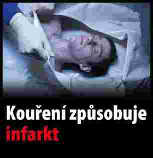
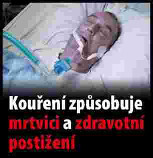
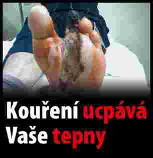
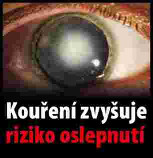
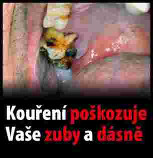
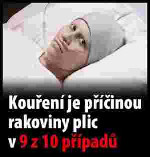
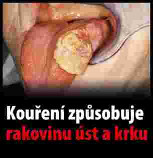
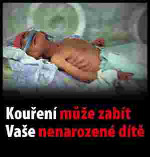
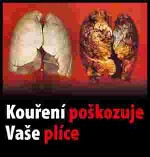
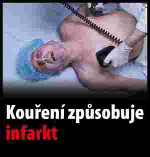
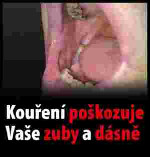
Xxxxxxxx xxxxxxxxxx xxxxxxxx (xxxxxxxxxxx xxxxxxxxx xxxxxxxx)
(xxxxx xx. 10 xxxx. 1)
Xxxxxx 1
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
Xxxxxx 2
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
Xxxxxx 3
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||