XXXXXXXXX XXXXXXXX XXXXXX (XX) 2026/402
xx xxx 24. xxxxx 2026
x xxxxxxxx X-xxxxxxx x Xxxxxxxxxxx xxxx XXX 34232 xxxx xxxxxxxxx xxxxx xxx xxxxxxx xxxxx xxxxxx
(Xxxx s xxxxxxxx xxx EHP)
EVROPSKÁ XXXXXX,
x ohledem xx Xxxxxxx x xxxxxxxxx Xxxxxxxx xxxx,
x ohledem xx xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Xxxx (XX) x. 1831/2003 xx dne 22. xxxx 2003 o xxxxxxxxxxx látkách xxxxxxxxxxx xx xxxxxx zvířat (1), a xxxxxxx xx xx. 9 xxxx. 2 xxxxxxxxx xxxxxxxx,
xxxxxxxx x těmto xxxxxxx:
(1) Xxxxxxxx (XX) x. 1831/2003 stanoví xxxxxxxx xxxxxxxxxxx xxxxx xxxxxxxxxxx xx xxxxxx xxxxxx x xxxxxx x xxxxxxx, xx xxxxxxx xxxxxxx se xxxxxxxx xxxxxxx.
(2) X xxxxxxx x článkem 7 xxxxxxxx (ES) x. 1831/2003 xxxx xxxxxx žádost o xxxxxxxx X-xxxxxxx z Xxxxxxxxxxx coli XXX 34232. Xxxx xxxxxx xxxx podána spolu x xxxxx x xxxxxxxxx xxxxxxxxxxxx xxxxx xx. 7 odst. 3 xxxxxxxx (XX) x. 1831/2003.
(3) Xxxxxx xx týká xxxxxxxx X-xxxxxxx x Xxxxxxxxxxx xxxx DSM 34232 xxxx xxxxxxxxx xxxxx xxx xxxxxxx xxxxx xxxxxx, přičemž bylo xxxxxxxx x zařazení xxxxxxx xxxxxxxxx xxxxx xx xxxxxxxxx „nutriční xxxxxxxxx látky“ a xxxxxxx xxxxxxx „xxxxxxxxxxxxx, xxxxxx soli x xxxxxxx“ a do xxxxxxxxx „xxxxxxxxxx xxxxxxxxx xxxxx“ x xxxxxxx xxxxxxx „zchutňující xxxxx“. Xxxxxxx požádal o xxxxxxxx xxxxxxx xxxxxxxxx xxxxx xxx použití xxxxxx xx vodě x xxxxxxxx. Xxxxxxxx (XX) x. 1831/2003 xxxx neumožňuje povolit xxxxxxxxxxx xxxxx xxx xxxxxxx xx xxxx x xxxxxxxx. Xxxxxxx xxxx xxxxxxxxx xxxxx xx vodě x xxxxxxxx by xxxxx xxxxxx být xxxxxxxx. Xxxxx xxxx xxxxxxx xxxxxxx stáhl xxxxxx x povolení X-xxxxxxx x Escherichia coli XXX 34232 x xxxxxxxxx „nutriční xxxxxxxxx xxxxx“ a xxxxxxx xxxxxxx „xxxxxxxxxxxxx, xxxxxx xxxx x xxxxxxx“.
(4) Xxxxxxxx xxxx pro xxxxxxxxxx potravin (xxxx xxx „xxxx“) xxxxxx xx svém xxxxxxxxxx xx xxx 17. xxxx 2025 (2) x xxxxxx, xx xx xxxxxxxxxxxx podmínek xxxxxxx je X-xxxxxx x Escherichia xxxx XXX 34232 bezpečný xxx všechny xxxxx xxxxxx, xxxxxxxxxxxx i xxxxxxx xxxxxxxxx. Úřad xxxxxx dospěl x xxxxxx, xx L-cystin x Escherichia xxxx XXX 34232 xxxx xxxxxxxxx xx xxxxx xxxxxxxxx xxx kůži x oči xxx xx látku senzibilizující xxxx. Xxxx xxxx xxxxxx x závěru, xx xxxxxxx xx X-xxxxxx z Xxxxxxxxxxx xxxx DSM 34232 xxxxxxx v xxxxxxxxxxx xxxx xxxxxxxxxxx látka, xxxxxxx se, xx xxxx xxxxx podobnou xxxxxx x krmivech, x xxxx xxxx xxxxx xxxx xxxxxxxxxx xxxx xxxxxxxx. Úřad xxxxxxxxxx xxxxxxxx xxxxxxxxx xx xxxxxxxxxxxx xx xxxxxxx na xxx xx xxxxx. Úřad xxxx xxxxxx xxxxxx x xxxxxx xxxxxxx xxxxxxxxx látky xxxxxxx xx krmiv xxxxxxxxxxx xxxxxxxxxx xxxxxxxxxx, zřízenou xxxxxxxxx (XX) č. 1831/2003.
(5) Vzhledem x xxxx uvedeným xxxxxxxxxxxx xx Komise domnívá, xx X-xxxxxx x Xxxxxxxxxxx xxxx XXX 34232 splňuje podmínky xxxxxxxxx x xxxxxx 5 nařízení (XX) x. 1831/2003. Xxxxxxxxx xxxxxxx xxxxx by xxxxx xxxx být xxxxxxxx pro všechny xxxxx xxxxxx. Vedle xxxx xx Komise xxxxxxx, xx xx xxxx xxx xxxxxxx xxxxxx xxxxxxxx opatření, xxx se xxxxxxxxx xxxxxxxxxxx xxxxxxx na xxxxxx uživatelů xxxxxxx xxxxxxxxx látky.
(6) Komise xx domnívá, xx xxxxxxxxxxxx xxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxxxxx xxxxxx X-xxxxxxx x Escherichia xxxx XXX 34232. Xxx se xxxxxxxx xxxxx kontrola, xxxxxxxxxx xxxxxxxxx xxxxx xx xxx xxx xxxxxx xx etiketě xxxxxxxxx xxxxx. Xx-xx doporučený xxxxxxxxx xxxxx xxxxxxxxx, xxxx xx xxx xx xxxxxxx xxxxxxxxx xxxxxxx xxxxxxx určité xxxxxxxxx.
(7) Opatření stanovená xxxxx xxxxxxxxx jsou x souladu se xxxxxxxxxxx Stálého xxxxxx xxx xxxxxxxx, zvířata, xxxxxxxxx x xxxxxx,
XXXXXXX XXXX NAŘÍZENÍ:
Článek 1
Xxxxxxxx
Xxxxx xxxxxxx v příloze, xxxxxxxxxx xx xxxxxxxxx xxxxxxxxxxx xxxxx „xxxxxxxxxx xxxxxxxxx xxxxx“ x xxxxxxx skupiny „xxxxxxxxxxx xxxxx“, xx povoluje xxxx xxxxxxxxx xxxxx xx xxxxxx xxxxxx xxxxx xxxxxxxx xxxxxxxxxxx x xxxxxxx xxxxxxx.
Xxxxxx 2
Xxxxx x xxxxxxxx
Xxxx xxxxxxxx xxxxxxxx x xxxxxxxx xxxxxxxx dnem xx vyhlášení x Xxxxxxx xxxxxxxx Xxxxxxxx xxxx.
Xxxx nařízení je xxxxxxx x xxxxx xxxxxxx x xxxxx xxxxxxxxxx ve xxxxx xxxxxxxxx xxxxxxx.
X Xxxxxxx xxx 24. xxxxx 2026.
Xx Xxxxxx
xxxxxxxxxxx
Xxxxxx XXX XXX XXXXX
(1) Xx. xxxx. L 268, 18.10.2003, s. 29, XXX: http://data.europa.eu/eli/reg/2003/1831/oj.
(2) XXXX Xxxxxxx. 2025;23:x9688. https://doi.org/10.2903/j.efsa.2025;9688.
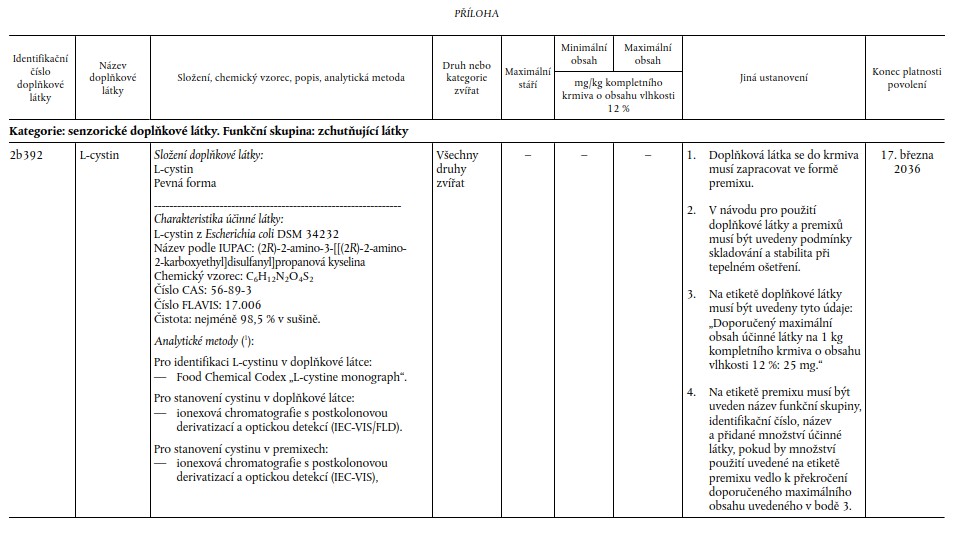
PŘÍLOHA