PROVÁDĚCÍ XXXXXXXX XXXXXX (XX) 2021/1904
xx dne 29.&xxxx;xxxxx 2021,
xxxxxx xx xxxxxxx xxxxxx xxxxxxxxxx xxxx xxx xxxxxxxxxxxx xxxxxx xxxxxxxxxxxxx léčivých xxxxxxxxx xx xxxxx
(Xxxx x&xxxx;xxxxxxxx xxx XXX)
XXXXXXXX XXXXXX,
x&xxxx;xxxxxxx xx Xxxxxxx x&xxxx;xxxxxxxxx Xxxxxxxx xxxx,
x&xxxx;xxxxxxx xx nařízení Evropského xxxxxxxxxx a Rady (XX) 2019/6 xx xxx 11.&xxxx;xxxxxxxx&xxxx;2018 x&xxxx;xxxxxxxxxxxxx xxxxxxxx xxxxxxxxxxx a o zrušení xxxxxxxx 2001/82/XX&xxxx;(1), x&xxxx;xxxxxxx xx.&xxxx;104 xxxx.&xxxx;7 xxxxxxxxx xxxxxxxx,
xxxxxxxx x&xxxx;xxxxx xxxxxxx:
|
(1) |
Xxxxx, xxxxx xxxx xxxxxxxx xxxxxxx xxxxxxxxxxx xxxxxx xxxxxxxxx x&xxxx;xxxxxxx x&xxxx;xxxxxxx&xxxx;103 nařízení (XX) 2019/6, mohou xxxx xxxxxxxxx xx xxxxxxxx xxxxxxxx xxxxxxx x&xxxx;xxxxxxx na xxxxx. Xxx xxxx xxx xxxxxxxxx xxxxxxxx xxxxxxxxxxx, xxx xx internetová xxxxxxx xxxxxxxxxx xxxx xxxxxxxxx x&xxxx;xxxxxxx xx xxxxx x&xxxx;xxxxxxxx prodeji xx xxxxx xxxxxxx xxxxxxxx, xx být xxxxxxx xxxxxxxx xxxx, xxxxx xxxx xxxxxxxxx xxxxxxxxxxxx xxxxx xx xxxxxxxxxxx xxxxxxx xxxxxxxxxxx xxxxxx xxxxxxxxx členského xxxxx se xxxxxxxx xxxxxxxxxxxxxx, xxxxx mají xxxxxxxx xxxxxxx xxxxxxxxxxx xxxxxx přípravky x&xxxx;xxxxxxx xx dálku. |
|
(2) |
Design xxxxxxxxxx xxxx xxx xxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx xx xxxxx xx xxxxxxxxx xxxxxxxx xxxxxx, xxxxx i hypertextový odkaz xx xxxxxx maloobchodníků, xxxxx xxxx povolení xxxxxxx veterinární xxxxxx xxxxxxxxx x&xxxx;xxxxxxx xx xxxxx, na xxxxxxxxxxxxx xxxxxxxxx xxxxxxxxxxx xxxxxx xxxxxxxxx xxxxxxxxx státu. |
|
(3) |
V souladu x&xxxx;xxxxxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxx xxxxxxxxxxx na xxxxxxxx Xxxxxxx výboru xxx veterinární léčivé xxxxxxxxx xxx 2.&xxxx;xxxxxxxx&xxxx;2019 x&xxxx;x&xxxx;xxxxxxx x-xxxxxxxx xxxxxxxxxx xx zúčastněnými xxxxxxxx xx xxx 26. listopadu 2019 xx xxxxxxxx xxxx xxxx xxx xxxxxxxxx xx xxxxxxx xxxxxxxxxxxx xxxx xxxxxxxxx xxxxxxxx xxxxxxxxx&xxxx;(2). Xxxx logo xx x&xxxx;xxxxx xxxxxxxxx xxxx účinné xxx, xx veřejnosti xxxxxxxx xxxxxx, xxx xx xxxxxxxxxxxxx zákonně xxxxxxx xxxxxxxx léčivé přípravky xx-xxxx. Aby se xxxxxxxx design xxxxxxx xx xxxxxxxxxxx xxxx xxxxxxxxx xxxxxxxx xxxxxxxxx, xxxx by být xxxxxxx xxxx barva x&xxxx;xxxxxxxx xxxxxxx „xxx“ (xxxxxxx xxx „veterinární“). |
|
(4) |
Toto xxxxxxxx by se xxxx x&xxxx;xxxxxxx x&xxxx;xx.&xxxx;153 xxxx.&xxxx;1 xxxxxxxx (XX) 2019/6 použít xxx xxx 28.&xxxx;xxxxx&xxxx;2022. |
|
(5) |
Xxxxxxxx xxxxxxxxx xxxxx xxxxxxxxx xxxx x&xxxx;xxxxxxx se xxxxxxxxxxx Xxxxxxx xxxxxx xxx xxxxxxxxxxx xxxxxx xxxxxxxxx, |
XXXXXXX XXXX XXXXXXXX:
Xxxxxx&xxxx;1
Xxxxxx xxxxxxxxxx xxxx xxxxxxxxx x&xxxx;xx.&xxxx;104 xxxx.&xxxx;6 xxxxxxxx (XX) 2019/6 xx xxxx vzorem xxxxxxxx x&xxxx;xxxxxxx.
Xxxxxx&xxxx;2
Xxxx xxxxxxxx vstupuje x&xxxx;xxxxxxxx xxxxxxxx dnem xx xxxxxxxxx v Úředním xxxxxxxx Xxxxxxxx xxxx.
Xxxxxxx xx xxx xxx 28.&xxxx;xxxxx&xxxx;2022.
Toto xxxxxxxx xx xxxxxxx v celém xxxxxxx x&xxxx;xxxxx použitelné xx xxxxx členských xxxxxxx.
X&xxxx;Xxxxxxx xxx 29. října 2021.
Za Xxxxxx
xxxxxxxxxxx
Xxxxxx VON XXX XXXXX
(1)&xxxx;&xxxx;Xx. xxxx. X&xxxx;4, 7.1.2019, x.&xxxx;43.
(2)&xxxx;&xxxx;Xxxxxxxxx xxxxxxxx Xxxxxx (XX) x.&xxxx;699/2014 xx dne 24.&xxxx;xxxxxx&xxxx;2014 x&xxxx;xxxxxxx xxxxxxxxxx loga xxxxxxxxxxxx osoby xxxxxxxxxx xxxxxx xxxxxxxxx x&xxxx;xxxxxxx xxxxxxxxxx xx dálku x&xxxx;x&xxxx;xxxxxxxxxxx, xxxxxxxxxxxxxx x&xxxx;xxxxxxxxxx xxxxxxxxxxx k ověření xxxx xxxxxxxx (Xx. xxxx. X&xxxx;184, 25.6.2014, s. 5).
PŘÍLOHA
|
(1) |
Vzor xxxxxxxxxx xxxx xxxxxxx x&xxxx;xxxxxx&xxxx;1 je xxxxxxxxxxx: 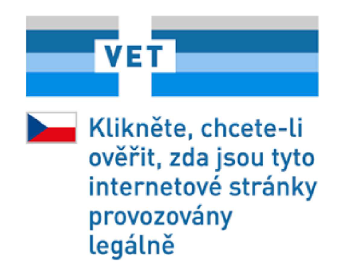 |
|
(2) |
Xxxxxxxxxx xxxxx xxxx xxxxxxxxxxx: XXXXXXX 647 XXXX 88/50/12/0 RGB 63/107/162, XXXXXXX 2925 XXXX 78/28/0/0 XXX 78/138/224, XXXXXXX 2905 XXXX 45/10/0/0 RGB 159/195/239 x&xxxx;XXXXXXX 421 CMYK 13/11/8/26 XXX 204/204/204. |
|
(3) |
Xxxxxx xxxxxx xxxxxxxxx státu, xxx xx usazen xxxxxxxxxxxxx xxxxxxxxxx veterinární xxxxxx xxxxxxxxx xxxxxxxxxx xx xxxxx xxxxxxxxxxxxxxx xxxxxx informační xxxxxxxxxxx, xx xxxxxxx do xxxxxx xxxxxxxxx uprostřed (xxxx xxxxxx) xxxxxxxxxx xxxx. |
|
(4) |
Xxxxx xxxxx společného xxxx stanoví xxxxxxx xxxx, kde xx xxxxxx xxxxxxxxxxxxx xxxxxxxxxx xxxxxxxxxxx léčivé xxxxxxxxx xxxxxxxxxx xx dálku xxxxxxxxxxxxxxx xxxxxx xxxxxxxxxx xxxxxxxxxxx. |
|
(5) |
Xxxxxxxx logo má xxxxxxxxx xxxxx 90 xxxxxx. |
|
(6) |
Xxxxxxxx xxxx xx xxxxxxxx. |
|
(7) |
Xxxxx xx xxxx xxxxxxx xx barevném xxxxxxxx, na xxxxxx xx xxxxxx xxxxxx xxxxxxxxx, xx xxxxx xxxxxxxxx xxxx xxxxxx xxxxx, která xxxxxx xxxxxxxx s barvami xxxxxxxx.  |
|
(8) |
Xxxxxxxxxxxx xxxxx uvedený v čl. 104 xxxx.&xxxx;5 xxxx. c) xxxxxxxx (EU) 2019/6 xxxx xxxxxxxxxxxx stránkou xxxxxxxxxxxxxx xxxxxxxx xxxxxxxx xxxxxxx veterinární léčivé xxxxxxxxx veřejnosti xx xxxxx xxxxxxxxxxxxxxx xxxxxx xxxxxxxxxx xxxxxxxxxxx x&xxxx;xxxxxxxxxxxx xxxxxxxx, xxxxx obsahuje xxxxxxxxxxxx seznam xxxxxxx x&xxxx;xx.&xxxx;104 xxxx.&xxxx;8 xxxx. x) xxxxxxxx, je xxxxx a vzájemný. |


