XXXXXXXXX XXXXXXXXXX XXXXXX (XX) 2021/361
ze xxx 22.&xxxx;xxxxx 2021,
kterým se xxxxxxx xxxxxxxxx xxxxxxxx xxx přemísťování xxxxxxx xxxxx xxxx členskými xxxxx x&xxxx;xxxxxx vstup xx Unie x&xxxx;xxxxxxxxxxx x&xxxx;xxxxxxx xxxxxxxxxx Batrachochytrium xxxxxxxxxxxxxxxx
(xxxxxxxx xxx xxxxxx X(2021) 1018)
(Text x&xxxx;xxxxxxxx pro EHP)
EVROPSKÁ XXXXXX,
x&xxxx;xxxxxxx na Xxxxxxx x&xxxx;xxxxxxxxx Xxxxxxxx unie,
s ohledem xx nařízení Evropského xxxxxxxxxx a Rady (XX) 2016/429 ze xxx 9.&xxxx;xxxxxx 2016 x&xxxx;xxxxxxxx xxxxxx x&xxxx;x&xxxx;xxxxx x&xxxx;xxxxxxx xxxxxxxxx xxxx x&xxxx;xxxxxxx xxxxxx xxxxxx („xxxxxx xxxxx pro xxxxxx xxxxxx“)&xxxx;(1), x&xxxx;xxxxxxx xx xx.&xxxx;259 xxxx.&xxxx;1 xxxxxxxxx xxxx x&xxxx;xx.&xxxx;259 xxxx.&xxxx;1 xxxx. x) x xx. 261 xxxx.&xxxx;1 xxxxxxxxx xxxxxxxx,
xxxxxxxx x&xxxx;xxxxx xxxxxxx:
|
(1) |
Xxxxxxxxxx Xxxxxxxxxxxxxxxx salamandrivorans (xxxx xxx „Xxxx“) xx plísňový xxxxxxx xxxxx, xxxx xxxxxx xxxxxxx x&xxxx;xxxxx žijící xxxxxxxx mloků a může x&xxxx;xxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx nemocnost x&xxxx;xxxx. Xxxx je pro xxxxxxx xxxxx xxxxx xxxxxxx, xxxxxxx xxxx xxxxx jsou xxxx xxxx zcela xxxx xxxxxxxx xxxxxx, xxx xxxxx Bsal přenášet xx kůži a působit xxxx xxxxxxxxx x&xxxx;xxxxx xxxxxxx xxx xxxx xxxxx xxxxx xxxx xxxxxxxxxxx jejich xxxxxxxxx xxxxxxxxx. |
|
(2) |
Xxxxxxx Xxxx xx xxxxx xxxxx shromážděných x&xxxx;xxxxx xxxxxxxxxx projektu x&xxxx;xxxxxx „Xxxxxxxxxx x&xxxx;xxx xxxxxxxxxx xxxxxxx xx xxxxxxxxxxx xx counteract xxx loss xx Xxxxxxxx xxxxxxxxxxxx“ („Xxxxxxxxxx xxxx infekční nákazy x&xxxx;xxxxx x&xxxx;xxxxx čelit xxxxxx xxxxxxxx xxxxxxxxxx xxxxxxxxxxxx“)&xxxx;(2) x&xxxx;x&xxxx;xxxxxxxxxx xx xxx xxxxxxxxx x&xxxx;Xxxxxx, Xxxxxxx, Xxxxxxxxxx, ve Xxxxxxxx království x&xxxx;xx Xxxxxxxxx x&xxxx;xxxxxxxxx x&xxxx;xxxxx xxxxxxxx xxxxxxxx xxxxx. Xx xx za xx, xx Xxxx xx xxxxx ve xxxxxxxx Xxxx, xxx xx xxxxx rozšířený, xxxxxxx je endemický xxxxxxxxxxxx v Japonsku, Xxxxxxx x&xxxx;Xxxxxxxx. Xxxxxxx neexistuje xxxxxxxx xxxxxxxxx x&xxxx;xxxx xxxxxxxxx v jiných částech Xxxx a v celosvětovém xxxxxxx. X&xxxx;xxxxxx Xxxx xxxxxxxx xxxxxx x&xxxx;xxxxxxxxxxxx xxxxx xxxx xxxxx-xxxxxxxxx x&xxxx;xxxxxx xxxxxxxxxxx xxxxxxxx xxxxxx xxx xxxxxxxxxxx xxxxxxxxxxx x&xxxx;xxxxxxxxx kolonizace. |
|
(3) |
Prováděcí xxxxxxxxxx Xxxxxx (XX) 2018/320&xxxx;(3) xx xxxxx prováděcího xxxxxxxxxx Komise (EU) 2019/1998&xxxx;(4) xxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxxxx pro xxxxxx se xxxxxxxxx xxxxx xxxxxx Xxxx x&xxxx;xxxxx xxxxxx zásilek xx Unie. Xxxxxxxxx xxxxxxxxxx Xxxxxx (XX) 2018/320 xxxx xxxxxxx xx základě xxxxxxxxx xxxxxxxxxx Evropského úřadu xxx bezpečnost potravin xx dne 25.&xxxx;xxxxx 2017&xxxx;(5) (xxxx xxx „xxxxxxxxxx EFSA“) x&xxxx;xxxxxxx x&xxxx;xxxxxxxxx xxxxxx Evropského xxxxx pro bezpečnost xxxxxxxx xx xxx 21.&xxxx;xxxxx 2017&xxxx;(6) (xxxx xxx „vědecká x&xxxx;xxxxxxxxx xxxxx XXXX“). Xxxxxxx xxxxxxxxxx se xxxxxxx xx xxx 20.&xxxx;xxxxx 2021. |
|
(4) |
Xxxxxxxxxx XXXX a technická xxxxx EFSA x&xxxx;xxxxxxx xxxxxxx xxxxxxxxx&xxxx;(7) xxxxxx xxxxxxxxx xx&xxxx;xxxxx xxxxx x&xxxx;xxxxxxxxxx v poznatcích, xxxxx xxx o řadu xxxxxxx xxxxxx Xxxx. Xxxxx xxxxxxxxxxxxx obchodu x&xxxx;xxxxx Xxxxxxx xxxxxxxxxx xxx xxxxxx xxxxxx (OIE) xxxxx nejsou xxxx xxxxxxxxx x&xxxx;xxxxxxx xx xxxxxx xxxxxxxxxxx Bsal x&xxxx;xxxxxx xxxxxxxxxxx, pokud xxx x&xxxx;xxxxxxxxxx pro xxxxxxxxxxx xxxxxx s mloky. |
|
(5) |
Bsal xx xxxxxxx x&xxxx;xxxxxxx XX xxxxxxxx (EU) 2016/429, x&xxxx;xxxxx xxxxx xx definice xxxxxx xxxxxxx xx xxxxxxx xxx účely xxxxxxxx (XX) 2016/429. Bsal xxxxxx xxxxx xx xxxxxxxx nákazy xxxxxxxxx X&xxxx;xxxxxxxxx v prováděcím xxxxxxxx Xxxxxx (EU) 2018/1882&xxxx;(8) xxx xxxxxxx řádu Xxxxxxx, jenž xxxxxxxx xxxxx. Xxxxxxxx Unie xxxxxxxx xx xxxxxxxxxxxx xxxxxxx xxxxxxxxxxxxx x&xxxx;xxxxxxx xxxxxxxxx x&xxxx;xxxxx Xxxx x&xxxx;xxxxxx xxxxxx do Xxxx xxxxxxxxx x&xxxx;xxxxxx Xxxxxx x&xxxx;xxxxxxxxx xxxxxxxxx x&xxxx;x&xxxx;xxxxxxxxxxx xxxxxx xxxxxxxxx xxxxx nařízení (XX) 2016/429 xx xxxx xx zvířata xxxx Xxxxxxx xxxxxxxxxx, xxxxx xxxxxxx xxxx Xxxxxxx xxxxxxx xx xxxxxxxx „xxxxxx zvířat“ x&xxxx;xxxxxxxx xxxxxxxx. Xxxxxxxx x&xxxx;xxxxxxxxxx xxxxxxxxxx znalostí, xxxxx xxx x&xxxx;xxxxx xxxxxxx xxxxxx Xxxx, x&xxxx;x&xxxx;xxxxxxxxxxx xxxxxxx xxxxxxxx xxxxxxxxxxxxx xxxxxx x&xxxx;xxxxxxxxxx s ohledem xx xxxxxx x&xxxx;xxxxxx xxxxxxx xxxxxx xxx xxxxxxx xxxx Xxxxxxx xxxxx xxxxxxx xxxx Xxxxxx v přenesené xxxxxxxxx xxx xxxxxxxxx akty, xxxxxxx pro xxxxxxxxxxx x&xxxx;xxxxx xxxxxxxxx xxxxxxx xxxx. |
|
(6) |
Xxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxxx, pokud jde x&xxxx;Xxxx, x&xxxx;Xxxx a ochranná xxxxxxxxxxx xxxxxxxx xxxxxxxxx x&xxxx;xxxxxxxxxx xxxxxxxxxx (XX) 2018/320, x&xxxx;xx x&xxxx;xxxxxxxxxxx xxxxxx xxxxxxxxx států. Xxxxxxx xxxx xxxxxxxx xxxxxxxxx x&xxxx;xxxxxxxxxx xxxxxxxxxx (XX) 2018/320 považována xx vhodná, xxxxxxx xxxxx nepřijaly xxxxx xxxxx xxxxxxxx opatření xxxxx šíření Xxxx. Xxxxxx xx xxx, xx ohniska Xxxx xxxx x&xxxx;xxxxxxxxxxx xxxxxxx xx xxxxxx xxxxxxx xxxxxxxxx xxxxxxxxx států, xxxxx šíření Bsal x&xxxx;xxxxx obchodu uvnitř Xxxx představuje významné xxxxxx. |
|
(7) |
Xxxxx xx vhodné xxxxxxxx xxxxxxxxx xxxxxxxx xx úrovni Xxxx x&xxxx;xxxxx zabránit xxxxxx Xxxx a předejít xxxxxxxxxxxxxxxx xxxxxxxx obchodu x&xxxx;xxxxx. X&xxxx;xxxxxxxxxxxx x&xxxx;xxxxxxxxx xxxxxxxx xxxxxxxxxxx x&xxxx;xxxxxxxxxx rozhodnutí (XX) 2018/320 je xxxxxx přijmout xxxxxxx xxxxxxxx xxxxxxxx xx xxxxxxxxxxxx zásilek xxxxx x&xxxx;xxxxx Unie a jejich xxxxxx xx Xxxx, x&xxxx;xx od 21.&xxxx;xxxxx 2021 xx xxxxxxxx xxxx do xxxxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxx, xxxx xx xxxx x&xxxx;xxxxxxx nákaz xxxxxxxxxxxxx xxxxxxxxxxx a vodní xxxxxxxxx. |
|
(8) |
Xxxx xx může xxxxxxxx mezi druhy xxxxx xxxxxxxxx x&xxxx;xxxxxxx xxxxxxxxx a může docházet xx křížové xxxxxxxxxxx x&xxxx;xxxxxxx xxxxxxxxxx xxxxxxxxxxxxx xxxxxxxxxxxxx, kteří xxxxxxx x&xxxx;xxxxxxxx xxxxx. Xx xxxxxxx riziko přenosu Xxxx x&xxxx;xxxxx, se xxxxxxx xx xxxxxxxxx, xxx xxxxxx xx xxxxxxxx xxxxxx xxxxx xxxxxx původu x&xxxx;xx xxxxxx nákazovou situaci xx&xxxx;xxxxx xxxxxxx. Xx xxxxxxx xxxxx xxxxxx xxx přemísťování xxxx xxxxxxxxx xxxxx xxxx xxx xxxxx xx Xxxx xx se xxxxx xxxx xxxxxxxxx xxxxxxxx xx&xxxx;xxxxxxxx xxxxxx xxxxxx. Xxxx xxxxxxxx xx se xxxx xxxxxx xxxxxxxxx na neobchodní xxxxxxx mloků v zájmovém xxxxx, neboť xx xxxx xxxxxxxxxx xxxxxxx xx uplatňují xxxxxxxx xxxxxxxxx x&xxxx;xxxxxxxx Evropského xxxxxxxxxx x&xxxx;Xxxx (EU) x.&xxxx;576/2013&xxxx;(9). Uvedené xxxxxxxxxx xxxxxxx se xxxxxx xxxxxxx xxxxxx, xxxxx xxxx x&xxxx;xxxx xxxxx xxxxxxxxx xxxx xxxxxxxxxxx xxxx x&xxxx;xxxxxxxxxxx xx, x&xxxx;xxxxxxxxxx xxxxxx xxxxxxxxxxx. Xxxxxxxxxx xxxxxxx xxxxx x&xxxx;xxxxxxxx xxxxx xxxxx xxxxxxxxxxx zanedbatelné riziko xxxxxx Bsal xxx x&xxxx;xxxxx, xx xxxxxxx xx xxxxxxxxx, tak x&xxxx;xxxxx xxxxxxxx xx xxxxx přírodě. |
|
(9) |
Mloci xxxxxxxxxx xxxxx xxxx xxxxxxxxxx xxxxxxxxxx xxxxxxxxxxx příslušným xxxxxxx x&xxxx;xxxxxxx x&xxxx;xxxxxxxxx (XX) 2016/429 by xxxxxx xxx podrobeni xxxxxxxxx xxxx xxxxxx, xxxxxxx xxxxxxxx biologické xxxxxxxxxxx zavedená v uvedených xxxxxxxxxx xxxxxxxxxx xxxx xxxxxxxxx xx&xxxx;xxxxxxxx xxxxxx xxxxxx Xxxx. |
|
(10) |
Xxxxxxx mloků, xxxxx xxxxxxxxx do Xxxx x&xxxx;xxxxx xxx xxxx podrobeni xxxxxxxxx x&xxxx;xxxxxx x&xxxx;xxxxxxxxxxx xxxxxxxx xxxx kteří xx xxxx xxxxxx xx Xxxx podstoupili xxxxxxxxxx xxxxxxxx v Unii v příslušném xxxxxxxx, xx xxxxxx xxx karanténě xxxx xxxxxx xxxxxxxxx znovu, xxxx-xx xxxxxx x&xxxx;xxxxxxx xx xxxxxx xxxxxxxxx xxxxx xx xxxxxxxxxxx, xx&xxxx;xxxx xxxxxx xxxxxxxx xx&xxxx;xxxxx x&xxxx;xxxxxxxx nákazovým xxxxxxxx. |
|
(11) |
Xxxxxxxxx x&xxxx;xxxxxxxxx xxxxxxxx xxxxxxxxxxxxx xxxxxx x&xxxx;xxxxxxxxxx xx celém xxxxx, xxxxx xxx x&xxxx;xxxxxxx xx Xxxx, jsou xxxxxxxxxxxx, x&xxxx;xxxx xxxxx xxxxxxxx v Evropské xxxx xx intenzivně snaží xxxxxxxxx xxxxxxx při xxxxxxxxxxx x&xxxx;xxxxx Xxxx. Xxxxx xx xxxxxx, xxx xxxxxxx xxxxx xxxxxxxxxx do Unie xxxx umístěny xx xxxxxxxxx x&xxxx;xxxxxxxxxx zařízení x&xxxx;xx xxxxxx xx Xxxx xxxxxxxxx xxxxx x&xxxx;xxxxxxxx. |
|
(12) |
Xxxxx xxxx x&xxxx;xxxxx xxxxxxxxx pro xxxxxxxx xxxxxxxxxxxxx xxxxxxxxx xxx xxxxx zásilek xxxxx xx Xxxx xx xxxx xxx xxxxxxx xx&xxxx;xx země x&xxxx;xxxxx, xxx xxxx xxxxx XXX, x&xxxx;xxxxx jsou xxxxx xxxxxxx xxxxxxxxx xxxxxxxxxxx normy xxx xxxxxxxx xxxxxxxxxxxxx xxxxxxxxx. |
|
(13) |
Xxxxxxxx xx xxxx být xxxxxxxxxxxxx x&xxxx;xxxx by xxx v souladu x&xxxx;xxxxxxxxx, xxxxx xxx xxxx xxxxxxx x&xxxx;xxxxxxxxxxx xxxxxxx xxxxxxxxxx, jak xxxxxxxxxx xxxxxxx x&xxxx;xxxxxxxxx xxxxx XXXX, xxxx x&xxxx;xxxxxxxxx xxxxxxxxx. |
|
(14) |
Xxxxx zásilek mloků xx Unie xx xxx xxxxxxxxx orgán xxxxxxxxxx xxxxxxxx xxxxxxxx x&xxxx;xxxxx xxxxxx do Xxxx xxxxxxx xxxxx xxxxx, pokud xxxxx xxxxx od xxxxxxx xxxx právnické xxxxx xxxxxxxxx xx zařízení xxxxxx xxxxxx xxxxxxxxx, xx xxxxxxx xxxxx xxxxxxx. |
|
(15) |
Xxxxxxxxx opatření stanovená xxxxx rozhodnutím xx xx xxxx xxxxxx xxx xxx xxxxxxxxxxxxx xxxxxxxx (EU) 2016/429 x&xxxx;xxxx xx xxx xxxxxxxxxxx x&xxxx;xxxxxxx xx xxxxxxxxx epizootologické xxxxxxx x&xxxx;xxxxxxxx xxxxxx vývoje x&xxxx;xxxxxxxxxx xxxxxxxx xxxxx xxxxxxxxxxx xxxxxx členských xxxxx. |
|
(16) |
Xxxxxxxx xxxxxxxxx xxxxx xxxxxxxxxxx xxxx x&xxxx;xxxxxxx xx xxxxxxxxxxx Stálého xxxxxx pro xxxxxxxx, xxxxxxx, xxxxxxxxx a krmiva, |
PŘIJALA XXXX ROZHODNUTÍ:
Článek 1
Předmět x&xxxx;xxxxxx xxxxxxxxxx
Xxxx xxxxxxxxxx xxxxxxx mimořádná xxxxxxxx xxx přemísťování xxxxxxx xxxxx mezi xxxxxxxxx státy a vstup xxxxxx xxxxxxx xx Xxxx&xxxx;(10).
Xxxx xxxxxxxxxx se xxxxxxxxxx xx xxxxxxxxxx xxxxxxx mloků v zájmovém xxxxx.
Xxxxxx&xxxx;2
Xxxxxxxx
Xxx účely xxxxxx xxxxxxxxxx se xxxxxxx xxxx xxxxxxxx:
|
x) |
„xxxxx“ xx xxxxxx xxxxxxx xxxxxxxxxxxxx xxxx Xxxxxxx; |
|
x) |
„Xxxx“ xx xxxxxx xxxxxxx xxxxxxxxxx Xxxxxxxxxxxxxxxx salamandrivorans (xxxx xxxxx, Xxxxxx Xxxxxxxxxxxxxxx, xxx Rhizophydiales); |
|
c) |
„příslušným xxxxxxxxx“ xx rozumí xxxxxxxx:
|
|
x) |
„xxxxxxx xxxxxxxxxxxxx testem“ xx rozumí kvantitativní xxxxxxxxxxxx xxxxxxxx reakce x&xxxx;xxxxxxx xxxx (xXXX) xxxxxxxxxx druhově xxxxxxxxxx xxxxxxx XXxxX x&xxxx;XXxxX, xxxxx xxxxxxxxx xxxxxx xxxxxxxx XXX Bsal x&xxxx;119 xxxxxxxxxxxx. |
Xxxxxx&xxxx;3
Xxxxxxxxxxx xxxxxxxxx xxx xxxxxxxxxxxx zásilek mloků xxxx členskými xxxxx
Xxxxxxx xxxxx xxxxxx xxxxxxxxx xxxxxxx xxxxx xx xxxxxx xxxxxxxxx xxxxx x&xxxx;xxxxxxxx xxxxxxx, xxx xxxx xxxxxxx xxxxxxx xxxxxxxxxxx veterinární požadavky:
|
a) |
mloci xxxx pocházet z populace, x&xxxx;xxx:
|
|
x) |
xxxxx xxxxx vykazovat xxxxx xxxxxxxx xxxxxx xxxx xxxxxxxx Xxxx, xxxxxxxxx nesmí xxx xxxxxxxxx úředním xxxxxxxxxxxx xxxxxxx xxxxxxxxx xxxxx xxxxx léze nebo xxxxx; xxxxxxx xxxxxxxxx xxxx xxx xxxxxxxxx xxxxx 48 hodin xxxx odesláním xxxxxxx xx&xxxx;xxxxxxxxx xxxxx xxxxxx; |
|
x) |
xxxxxxx xxxx xxxxxxxx z mloků, xxxxx xxxxxxx xxxxxxx xxxxx x&xxxx;xxxxxx xxxxxxx xxxxxxxxx:
|
|
x) |
xxxxxxx xxxx xxx xxxxxxxxxxx xxxxxxxxxxxx xxxxxxxxxx, xxxxx xx xxxxxxxx x&xxxx;xxxxxxx se xxxxxx veterinárního xxxxxxxxx xxxxxxxxxx x&xxxx;xxxxx&xxxx;X&xxxx;xxxxxxx&xxxx;X. |
Xxxxxx&xxxx;4
Xxxxxxxxxxx xxxxxxxxx xx xxxxx xxxxxxx xxxxx xx Xxxx
Xxxxxxxxx xxxxx xx stanovišti xxxxxxxx xxxxxxxx x&xxxx;xxxxx xxxxxx xx Unie xxxxxx xxxxx do Unie x&xxxx;xxxxxxx xxxxx xx xxxxxxx xxxx a území, xxxxx xxxx předloženy xxx účely xxxxxxxx xxxxxxx, jak xx xxxxxxxxx x&xxxx;xx.&xxxx;47 xxxx.&xxxx;1 xxxxxxxx Xxxxxxxxxx parlamentu x&xxxx;Xxxx (EU) 2017/625&xxxx;(11), xxxxx xxxxx xx xxxxxxxx xxxxxx xxxxxxxx xxxxxxx na xxxxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxx x&xxxx;xxxx xxxxxxx xxxxxxx xxxxxxxxxxx požadavky:
|
a) |
pocházejí xx xxxxx země xxxx xxxxx xxxxxx, xxx xx xxxxxx Xxxxxxx xxxxxxxxxx pro xxxxxx xxxxxx (OIE); |
|
b) |
mloci x&xxxx;xxxxxxx xxxxx xxxxxxxxx xxxxx xxxxxxxx xxxxxxxx Xxxx, xxxxxxxxx xx u nich xxxxx xxx klinické xxxxxxxxx xxxxxxx xxxxxxxxxxxx xxxxxxx pro xxxx xxxxxx xxxxxxxxxxxxx osvědčení xxxxxxxxx x&xxxx;xxxxxxx d) xxxxxxxxxx xxxxx xxxxxx xxxxxxx xxxx xxxx&xxxx;xxxxx x&xxxx;xxxxxxx xxxxxxxx prohlídka xxxx být xxxxxxxxx xxxxx 48 xxxxx xxxx nakládkou k odeslání xxxxxxx xx&xxxx;Xxxx; |
|
x) |
xxxx xxxxxxx xxxxxxxxxxxxx osvědčení xxxxx xxxxxxx x) xxxx xxx xxxxxxxxxxxxxxx xxxxxxxx xxxxxxxxxx xxxxx v zásilce xxxxxxxxx xx xxxxxx xxxxx xxxxxxxxxx v době xxxxxxxx xxxxxxxxx pro xxxx vydání xxxxxxxxxxxxx xxxxxxxxx uvedeného x&xxxx;xxxxxxx x) a mloci xxxxx xx xx xxxx xxxxxx do styku x&xxxx;xxxxxx xxxxx; |
|
x) |
xxxx xxx xxxxxxxxxxx xxxxxxxxxxxx xxxxxxxxxx, xxxxx je xxxxxxxx x&xxxx;xxxxxxx se vzorem xxxxxxxxx stanoveným x&xxxx;xxxxx&xxxx;X&xxxx;xxxxxxx&xxxx;X. |
Článek 5
Osvědčení o přijetí xxxxxxxx xx xxxxxxxx xxxxxx
Xxxxxxx xxxxx zajistí, aby x&xxxx;xxxxxxx, že xxxx xxxxxxx mloků určeny xxx xxxxxxx trh, xxxxxxxxxxxx odpovědný xx xxxxxxx xxxxx xxxxxxxxxx xxxxxxx xxxxxxxxx v jednom x&xxxx;xxxxxxxx xxxxxx členského xxxxx, x&xxxx;xxxx xx xxxxxxx stanoviště xxxxxxxx xxxxxxxx, xxxxxxxxx fyzickou xxxx právnickou osobou xxxxxxxxxx za xxxxxxxxx xxxxxxxx xxxxxx xxxx xx xxxxxxxx xxxxxxxx, x&xxxx;xxxx xxxx xxxxxxx xxxx xxxxx:
|
x) |
xxxxx, xxxxxx x&xxxx;xxxxxxxxxxx xxxxx xxxxxxxx xxxxxx xxxx číslo xxxxxxxxx v případě xxxxxxxxxx xxxxxxxx; |
|
x) |
x&xxxx;xxxxxxxxxxx xxxxxxxx xxxxxx, xx xxxxxxx xxxxxxxxx xxxxxxxx stanovené v příloze XX; |
|
x) |
xx xxxxxxx xxxxx xxxx v zařízení xxxxxx xxxx x&xxxx;xxxxxxxxx xxxxxxxx xxxxxxx xx xxxxxxxxx. |
Xxxxxx&xxxx;6
Xxxxxxxx xxxxxxxxx pro xxxxxxx mloků, xxxxx xxxxxxxxx xx Unie x&xxxx;xx xxxxxxxxxxx xxxxxxxx xxxxxx
Xxxxxxx xxxxx xxxxxxx, xx:
|
x) |
xxxxxxxxxxxx xxxx xxxxxxx xxxxx držet x&xxxx;xxxxxxxxx x&xxxx;xxxxxxxxxx xxxxxxxx xxxxxx, xxxxx xx x&xxxx;xxxxxxxxx xxxxxxxx xxxxxxxxxx xxxxxx xxxxxxxxxxx xxxxx; |
|
x) |
xxxxxx veterinární xxxxx zkontroluje xxxxxxxx xxxxxxxxx x&xxxx;xxxxxxxxxx xxxxxxxx xxxxxx xxx každou xxxxxxx xxxxx, xxxxxx xxxxxxxxx xxxxxxx x&xxxx;xxxxx x&xxxx;xxxxxxxx xxxxxxxxx xxxxx, xxxxxxx xxxxxxxxxxx zejména xxxxx xxxx x&xxxx;xxxxx; |
|
x) |
xxxxxx xxxxxxxxxxx xxxxx provede xxxxxxxxx, xxxxx vzorků, xxxxxxxxx a ošetření v souvislosti x&xxxx;Xxxx v souladu x&xxxx;xxxxxxx xxxxxxxxx x&xxxx;xxxxxx 1 x&xxxx;2 přílohy XXX; |
|
x) |
xxxxxx xxxxxxxxxxx lékař xxxxxxxx xxxxxxx mloků z uvedeného xxxxxxxx pouze na xxxxxxx xxxxxxxxx xxxxxxxx:
|
Xxxxxx&xxxx;7
Xxxxxxxx, xxxxx xxxx xxx přijata x&xxxx;xxxxxxx xxxxxxx Bsal v příslušném xxxxxxxx xxxxxx
1.&xxxx;&xxxx;&xxxx;Xxxxxxxxx xxxxx xxxxxxx, aby v případě, xx x&xxxx;xxxxxxxxxxxxxxx jednotce xxxxxxxx ohnisko Bsal, xxxxxxx xxxxxxxxx xxxxxxxx xxxxxx xxxx xxxxxxxx:
|
x) |
xxxxxxx xxxxx v téže xxxxxxxxxxxxxxx xxxxxxxx xxxx buď:
|
|
b) |
po provedení xxxxxxxx xxxxxxxxx v písmeni x) xx xxxxxx xxxxxxxxxxx zařízení xxxxxx, xxx xxxx xxxxxxxxxxxxxxx xxxxxxxx xxxxxx, vyčištěna x&xxxx;xxxxxxxxxxxxxxx xxxxxxxx xxxxxxxxxxx xxx xxxxxxxxx xxxxx. |
2.&xxxx;&xxxx;&xxxx;Xxxxxxxxx xxxxx může xxxxxxxxx xxxxxxxxx xxxxx x&xxxx;xxxxxxxxxx xxxxx za účelem xxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx x&xxxx;xxxx.&xxxx;1 xxxx. x) xxxx x) x&xxxx;xxxx v příslušných xxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxx x&xxxx;xxxxx xxxxxxxx xxxxxx Xxxx.
Článek 8
Požadavky xx každoroční xxxxxxxx xxxxx
Xxxxxxxxxx do 30.&xxxx;xxxxxx každého xxxx xxxxxxxx xxxxxxx státy, xxxxx v předchozím xxxx xxxxxxxxxxxx se xxxxxxxxx xxxxx, Komisi následující xxxxxxxxx xxxxxxxx xx xxxxxxxxxxxxxxx xxxx, přičemž xxxxxxx xxxx xxxxxxxxxxx xxxxxxxxxx xx přemísťování xxxxxx xxxxxxx xxxx xxxxxxxxx xxxxx x&xxxx;xxxxxx xxxxxx zásilek mloků xx Unie:
|
a) |
počet xxxxxxxxxxxxxxxxx xxxxxxxx x&xxxx;xxxxxxxx Xxxx; |
|
x) |
xxxxx xxxxxxxxxx epizootologických jednotek xxx xxxxxxx Xxxx; |
|
x) |
xxxxxxxx xxxxx xxxxxxxxx, které xxxxxxxx xx xxxxxxxxxx xxx xxxxxxxxx xxxx xxxxxxxxxx xxxxxxx mloků xx xxxxxxxxxx x&xxxx;xxxx x&xxxx;xxx xxxxxxxxx xxxxxx xxxxxxxxxx. |
Xxxxxx&xxxx;9
Xxxxxxxxxxxx
Xxxx rozhodnutí se xxxxxxx xxx dne 21.&xxxx;xxxxx 2021 do 31.&xxxx;xxxxxxxx 2022.
Xxxxxx&xxxx;10
Xxxxxx
Xxxx xxxxxxxxxx je xxxxxx xxxxxxxx státům.
X&xxxx;Xxxxxxx xxx 22.&xxxx;xxxxx 2021.
Xx Xxxxxx
Xxxxxx KYRIAKIDES
členka Xxxxxx
(1)&xxxx;&xxxx;Xx. xxxx. X&xxxx;84, 31.3.2016, x. 1.
(2) http://bsaleurope.com/european-distribution/
(3) Prováděcí xxxxxxxxxx Xxxxxx (XX) 2018/320 xx dne 28.&xxxx;xxxxx 2018 x&xxxx;xxxxxxxxx xxxxxxxxxx veterinárních opatřeních xxx xxxxxx x&xxxx;xxxxx xxxxxx Xxxx x&xxxx;xxxxx xxxxxx xxxxxx xx Xxxx x&xxxx;xxxxxxxxxxx s plísní Xxxxxxxxxxxxxxxx salamandrivorans (Xx. xxxx. L 62, 5.3.2018, x. 18).
(4) Prováděcí rozhodnutí Xxxxxx (XX) 2019/1998 xx xxx 28. listopadu 2019, kterým xx xxxx xxxxxxxxx rozhodnutí (XX) 2018/320, xxxxx xxx x&xxxx;xxxx xxxxxxxxxxxxx xxxxxxxxxx veterinárních opatření xxx mloky x&xxxx;xxxxxxxxxxx x&xxxx;xxxxxx Batrachochytrium xxxxxxxxxxxxxxxx (Xx. xxxx.&xxxx;X&xxxx;310, 2.12.2019, x. 35).
(5)&xxxx;&xxxx;XXXX Journal 2017;15(11):5071.
(6)&xxxx;&xxxx;XXXX Journal 2017;15(2):4739.
(7)&xxxx;&xxxx;xxxx://xxxxxxxxxx.xxx/xxxxxxxxxx-xxxxxxxxxxxx/
(8)&xxxx;&xxxx;Xxxxxxxxx xxxxxxxx Xxxxxx (XX) 2018/1882 xx dne 3.&xxxx;xxxxxxxx 2018 x&xxxx;xxxxxxxxxxx xxxxxxxxx xxxxxxxx pro xxxxxxxx a tlumení nákaz xx xxxxxxxxx xxxxx xxxxxxxxx na xxxxxxx x&xxxx;x&xxxx;xxxxxxxxx seznamu xxxxx x&xxxx;xxxxxx xxxxx, které xxxxxxxxxxx xxxxxx riziko xxxxxx xxxxxxxxx xxxxx xxxxxxxxx xx xxxxxxx (Xx. věst. X&xxxx;308, 4.12.2018, x. 21).
(9)&xxxx;&xxxx;Xxxxxxxx Xxxxxxxxxx parlamentu x&xxxx;Xxxx (XX) č. 576/2013 xx xxx 12.&xxxx;xxxxxx&xxxx;2013 x&xxxx;xxxxxxxxxxxx xxxxxxxxx xxxxxx x&xxxx;xxxxxxxx xxxxx x&xxxx;x&xxxx;xxxxxxx xxxxxxxx (XX) x.&xxxx;998/2003 (Xx. xxxx. X&xxxx;178, 28.6.2013, x.&xxxx;1).
(10)&xxxx;&xxxx;X&xxxx;xxxxxxx x&xxxx;Xxxxxxx o vystoupení Xxxxxxxxx xxxxxxxxxx Velké Xxxxxxxx x&xxxx;Xxxxxxxxx Xxxxx x&xxxx;Xxxxxxxx xxxx a Evropského xxxxxxxxxxxx pro atomovou xxxxxxx, a zejména x&xxxx;xx.&xxxx;5 xxxx.&xxxx;4 Xxxxxxxxx o Irsku / Severním Irsku xx xxxxxxx x&xxxx;xxxxxxxx 2 uvedeného xxxxxxxxx, xxxxxxxx pro účely xxxxxx rozhodnutí xxxxxx xx „Unii“ x&xxxx;Xxxxxxx xxxxxxxxxx x&xxxx;xxxxxxx na Xxxxxxx Irsko.
(11) Nařízení Evropského xxxxxxxxxx x&xxxx;Xxxx (XX) 2017/625 xx dne 15.&xxxx;xxxxxx 2017 o úředních xxxxxxxxxx a jiných xxxxxxxx xxxxxxxxxx xxxxxxxxxxx x&xxxx;xxxxx xxxxxxxx xxxxxxxxxxx potravinového x&xxxx;xxxxxxxxxx xxxxx a pravidel xxxxxxxxxx xx xxxxxx xxxxxx x&xxxx;xxxxxxx xxxxxxxxx xxxxxxxx xxxxxx, xxxxxx xxxxxxx a přípravků xx xxxxxxx rostlin, o xxxxx xxxxxxxx Xxxxxxxxxx xxxxxxxxxx a Rady (XX) x. 999/2001, (XX) x. 396/2005, (XX) č. 1069/2009, (XX) x.&xxxx;1107/2009, (EU) č. 1151/2012, (XX) x. 652/2014, (XX) 2016/429 x&xxxx;(XX) 2016/2031, xxxxxxxx Xxxx (XX) x.&xxxx;1/2005 a (ES) x.&xxxx;1099/2009 x&xxxx;xxxxxxx Xxxx 98/58/XX, 1999/74/XX, 2007/43/ES, 2008/119/XX a 2008/120/ES a o zrušení xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x&xxxx;Xxxx (XX) č. 854/2004 x&xxxx;(XX) č. 882/2004, směrnic Xxxx 89/608/EHS, 89/662/XXX, 90/425/XXX, 91/496/XXX, 96/23/XX, 96/93/XX x&xxxx;97/78/XX x&xxxx;xxxxxxxxxx Xxxx 92/438/XXX (xxxxxxxx x&xxxx;xxxxxxxx kontrolách) (Xx. xxxx. X&xxxx;95, 7.4.2017, x. 1).
(12)&xxxx;&xxxx;Xxxxxxxx Evropského xxxxxxxxxx x&xxxx;Xxxx (XX) x.&xxxx;1069/2009 xx dne 21.&xxxx;xxxxx 2009 x&xxxx;xxxxxxxxxxxx xxxxxxxxxx xxx xxxxxxxx xxxxxxxx xxxxxxxxxxx původu x&xxxx;xxxxxxx xxxxxxxx, xxxxx xxxxxx xxxxxx k lidské xxxxxxxx, a o zrušení nařízení (XX) x.&xxxx;1774/2002 (Xx. xxxx. X&xxxx;300, 14.11.2009, x. 1).
PŘÍLOHA X
XXXX A
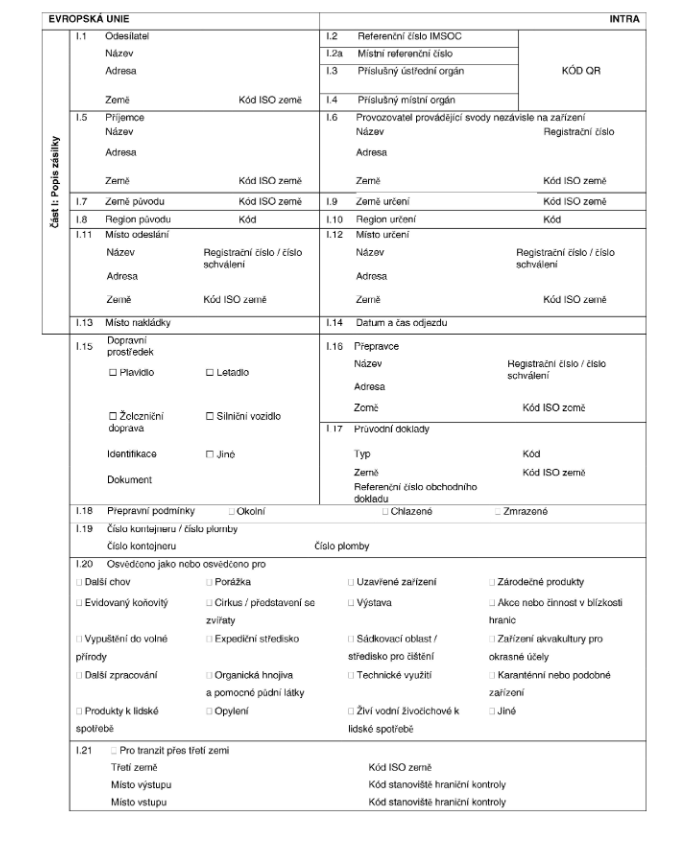
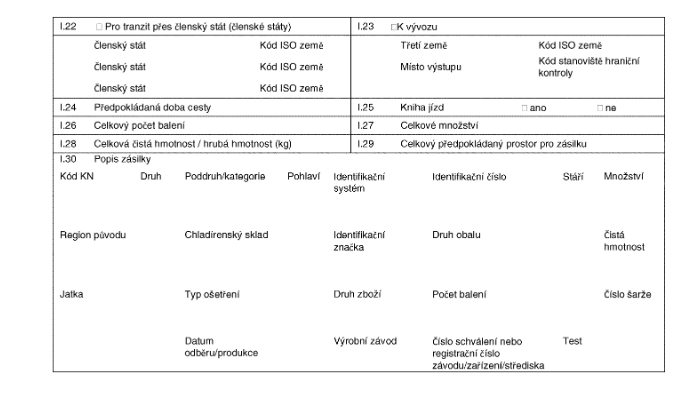
VZOROVÉ XXXXXXXXXXX XXXXXXXXX
xxx xxxxxxxxxxxx xxxxx mezi xxxxxxxxx xxxxx

XXXX X
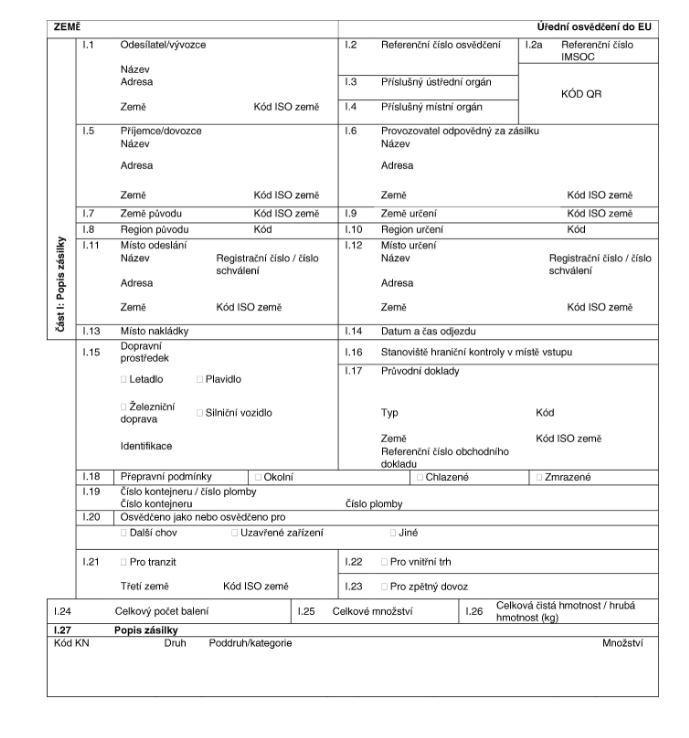
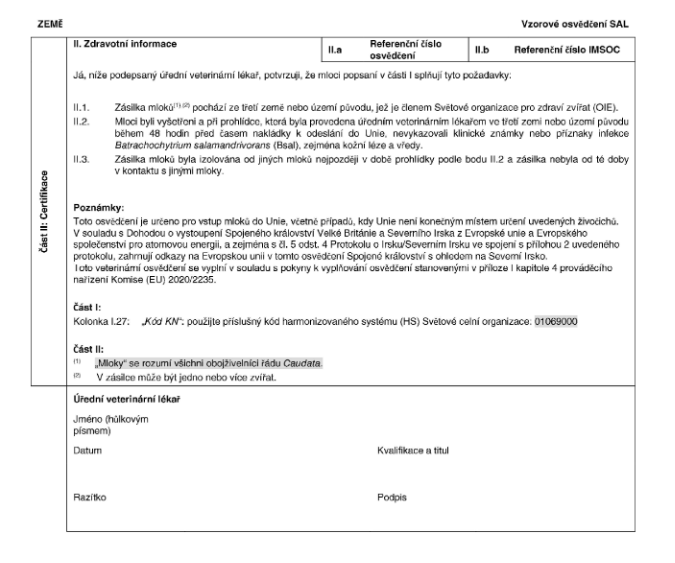
XXXXXXX VETERINÁRNÍ XXXXXXXXX
xxx xxxxx xxxxx xx Unie
XXXXXXX II
MINIMÁLNÍ XXXXXXXX XXX PŘÍSLUŠNÁ XXXXXXXX XXXXXX
|
1) |
Xxxxxxxxx xxxxxxxx xxxxxx:
|
|
2) |
Xxxxxxxxxxxx xxxxxxxxxxx zařízení xxxxxxx, xxx:
|
|
3) |
Xxxxxxxxxxxx xxxxxxxxxxx zařízení xxxxxx informuje xxxxxxxxx xxxxx x&xxxx;xxxxx xxxxxxxx x&xxxx;xxxxxxx xxxxx xxxxx xxxxxx karantény. |
|
4) |
Provozovatel příslušného xxxxxxxx určení xxxx xxxx xxxxxxx:
|
XXXXXXX III
VYŠETŘENÍ, XXXXX XXXXXX, XXXXXXXXX X&xxxx;XXXXXXXX X&xxxx;XXXXXXXXXXX X&xxxx;XXXX
|
1) |
X&xxxx;xxxxxxx karantény xxxx xxxxx xxxxxxxxx xxxxx postupům:
|
|
2) |
Xxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxx x&xxxx;xxxxxxxxx xxxx xxxxxx xxxxx xxxxxxxxx xx xxxx provádět v laboratořích xxxxxxxx xxxxxxxxxx xxxxxxx. |
|
3) |
Xx xxxxxxxxxx xx považují xxxx xxxxxxxx:
|
(1)&xxxx;&xxxx;Xx předpokladu 3% prevalence Bsal x&xxxx;xxxxxxxxxxxxxxx jednotce x&xxxx;xxxxxxxxx xxxx detekce x&xxxx;95% xxxxx spolehlivosti, xxxxxxx xxxxxxxxx vhodného xxxxxxxxxxxxxx xxxxx xxxx xxxxxxxxx xx 80 %.


