XXXXXXXXX XXXXXXXX XXXXXX (XX) 2019/1084
xx xxx 25. xxxxxx 2019,
kterým xx xxxx xxxxxxxx (XX) x. 142/2011, xxxxx xxx x xxxxxxxxxxx seznamu xxxxxxxxxxx xxxx xxxxxxxxxxxxxx zařízení, xxxxxxx x xxxxxxxxxxxxx x x xxxxxxxxxxxxxx některých xxxxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx x xxxxxxxxx xxxxxxxx
(Xxxx x xxxxxxxx xxx EHP)
XXXXXXXX XXXXXX,
x xxxxxxx xx xxxxxxxx Evropského parlamentu x Xxxx (ES) č. 1069/2009 xx xxx 21. xxxxx 2009 x xxxxxxxxxxxx pravidlech pro xxxxxxxx produkty xxxxxxxxxxx xxxxxx x xxxxxxx xxxxxxxx, xxxxx xxxxxx xxxxxx x xxxxxx spotřebě, a o zrušení xxxxxxxx (XX) x. 1774/2002 (1), x xxxxxxx xx xx. 21 odst. 5 písm. x), xx. 23 odst. 3, čl. 41 xxxx. 4, xx. 47 odst. 2 x čl. 48 xxxx. 2 uvedeného xxxxxxxx,
xxxxxxxx k těmto xxxxxxx:
|
(1) |
Xxxxxxxx Xxxxxx (EU) x. 142/2011 (2) xxxxxxx xxxxxxxxx xxxxxxxx x xxxxxxxx (XX) x. 1069/2009, xxxxxx xxxxxxxxx xxxxxxxxxx se xxxxxxxxxx dokladů x xxxxxxxxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx x xxxxxxxxx produktů. |
|
(2) |
Xxxxx xxxxxx 21 nařízení (XX) x. 1069/2009 xxxx být xxxxx zásilka vedlejších xxxxxxxx xxxxxxxxxxx původu x xxxxxxxxx produktů během xxxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxx xxxxx stanoveného v příloze XXXX xxxxxxxx (EU) x. 142/2011 a vyplněným provozovatelem. |
|
(3) |
Xxxxxxxxx xxxxx xxxxxxxxx xxxxx xxxxxx xxxxxx xxxxxxxx xxxxxxxxxx produktů xxxxxxxxxxx xxxxxx x xxxxxxxxx produktů, xx xxxxx xx xxxxxxxx xx. 48 xxxx. 3 xxxxxxxx (XX) x. 1069/2009, příslušnému xxxxxx xxxxxxxxx xxxxx xxxxxx xxxxxxxxxxxxxxx xxxxxxxxxxxxx xxxxxxxxxxxx veterinárního xxxxxxx (XXXXXX), který byl xxxxxxx xxxxxxxxxxx Komise 2004/292/XX (3). |
|
(4) |
Xxx xxxxx xxxxxxxx xxxxxxxx kontrol x xxxxx xxxxxx by měli xxx xxxxxxxxxxxxx xxxxxxxxxx xx xx xxxxxxxxx zásilek, xx xxx xx xxxxxxxx xx. 48 xxxx. 3 xxxxxxxx (XX) x. 1069/2009, možnost xxxxxx xx xxxxx xxxxxx xxxxx xx xxxxxxx schválených xxxx xxxxxxxxxxxxxx xxxxxxxx x xxxxxxx xxxxxxxxxxx xx xxxxxxx XXXXXX, x xxxxxx xx xxxxxxx xxxxxxxxxxxxxx xxxxxxxxxxxxx xxxxxx xxxxxxxxxxx xx xxxxxxx TRACES. |
|
(5) |
Xxxxxxxx (XX) x. 142/2011 xx xxxxx xxxx xxx xxxxxxx xxx, xxx xxxxxxxxxx xxxxxxxxx xx xxxxxxxxxxxxx xxxxxxx schválených xxxx xxxxxxxxxxxxxx xxxxxxxx x xxxxxxx x xxx xxxxxxxxx, xx xxxxxxxxxxxxx x xxxxxxxxxxxxx xxxxxxx budou xxxxxxxx xx xxxxxxx XXXXXX xxxx xxxxx xxxx xxxxxxxxxxxxxxx xxxxxxxxx. Xx xxxxxxxx VI nařízení (XX) x. 142/2011 xx xxxxx xxx xxx xxxxxx xxxx xxxxxx. |
|
(6) |
Xxxxxxxxxxx xxxxxxx v systému XXXXXX nebo zajištění xxxxxx xxxxxxxxxxx xxxxxxxxxxxxxxx xxxxxx xxxxxxx xxxx xxx příslušné orgány x xxxxxxxxx xxxxxxx xxxxxxxxxxxx xxxxxxxxxxxxxxx xxxxx. Xxxxxxxxx xxxxxx by xxxxx xxxx k provedení xxxxxx xxxxxxxxxx mít x xxxxxxxxx xxxxxx xxxxxxxxx období. |
|
(7) |
Xxxxxx 30 xxxxxxxx (XX) č. 142/2011 xx xx neměl použít x xxxxxxx xxxxxxxxxxxx přemísťování xxxxxxxxxx produktů xxxxxxxxxxx xxxxxx a získaných produktů xxxx xxxxxxx Xxxxx xxxxxxxx xxxxxxxxx x xxxxxx 29 xxxxxxxxx xxxxxxxx x x xxxxxxx xxxxxxxxxx tranzitu xxxxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx x xxxxxxxxx xxxxxxxx xxxxxxxxxxxxx z Bosny x Xxxxxxxxxxx x xxxxxxxx do třetích xxxx xxxx Chorvatsko xxxxx xxxxxx 29x xxxxxxxxx xxxxxxxx. Xxxxxxxx xxxxxxxxx xx xxxxxxxxxxxx x xxxxxxxx xxxxxxxxx xx xxxx xxxxxxxxx xxxxxxxx zajišťují xxxxxxx xxxxxx xxxxxxx xxxxxxxxx xxxxxx x xxxxxx xxxxxx, x xxxxxxxx tak xxxxxxxx xx xxxxxxx xxxxxxxx x xxxxxxx xxxxxx xx xxxxxxx x xxxxxxx TRACES. |
|
(8) |
Článek 30 xxxxxxxx (EU) x. 142/2011 xx xxxxx xxx xxx xxxxxxxxxxxxx xxxxxxxx xxxxxx. |
|
(9) |
Podle xx. 21 xxxx. 2 xxxxxxxx (XX) x. 1069/2009 musí xxxxxxxxxxxxx xxxxxxxx, aby xxxx xxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx a získané xxxxxxxx xxxxx xxxxxxxx xxxxxxxxxxx xxxxxxxxx dokladem. Xxx xx zabránilo xxxxxxxxx některých xxxxxxxxxx xxxxxxxx živočišného xxxxxx x xxxxxxxxx produktů xx xxxxxxxx xxxxxxx xxxxx xxx xxxxxxxxxxx xxxxxxx, xxxx xx být činnosti xxxxxxxxxxxxxx xxxxxxxxxx xxxxxxxxxxx xx xxxxxxxxxx xxxxxxxx xxxxxxxx x xxxxxxxxxxxxxxxx pro xxxxx úředních xxxxxxx. Xxxx xxxxxxxxxx xxxxxxx, xxxxx xx xxxxxxxxxx xxxx xxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx x xxxxxxx produkty, xx xxx být xxxxxxx xxx, aby xxxxxxxxxx xxxxxxxx informace. |
|
(10) |
Xxxxxx xxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx x xxxxxxx produkty stanovené x xx. 48 xxxx. 3 xxxxxxxx (XX) x. 1069/2009 xxxxxxxxx xxxxxxxx přemísťování. Xxxxxxxxxxxxx a příslušné orgány xx měly xxxxxxxx, xxx x xxxxxxxxx, xxx xx vyžaduje xxxxxxxxxx, xxxxxx xxxxxxxx xxxxxxxx xxxxxxxxxxx původu xxxx xxxxxxx produkty xxxx xxxx xxxxxxxx xx xxxxxxxxxxxx xxxxxxxx registrovaného x xxxxxxx s čl. 23 xxxx. 1 xxxx. x) xxxxxxxx (XX) x. 1069/2009, zařízení xxxx xxxxxxx xxxxxxxxxxx x xxxxxxx s čl. 24 xxxx. 1 xxxxxxxxx nařízení, nebo xxx byly xxxxxxxx xx xxxxx xxxxxx uvedené x xx. 24 odst. 1 xxxx. x) xxxxxx x) xx xx) uvedeného xxxxxxxx. Xx proto xxxxxxxx xxxxxxx vzor xxxxxxxxxx xxxxxxx xxxxxxxxxx xxxxxxxxxx x xx. 48 xxxx. 3 xxxxxxxx (XX) x. 1069/2009. |
|
(11) |
Doba přepravy xxxx xxxxxx původu x xxxxxx určení xx xxxx být xxxxxxx xx 15 xxxxxxxxxx xxx, xxx xx zajistila xxxxxxxxxxxxxx xxxxxxx. Pokud x xxxxxxx této xxxx xxxxxxx xx xxxxx xxxxxx xxxxxxxx, xxxxxxx xxxxxxx xxxxxxxxx orgány xxxxxxxxxx xxxxxx xxxxx, xxx xx daná xxxxxxx xxxxxxx. |
|
(12) |
Xxxxxxxxx xxxxxxx xxxx xxxxxxxxx xxxxx xx xxxxxxx xxxxxx xxxxxxx. Xxxxxxxx xxxxxx by xxx xxx xxxxxxx xxx, aby xxxxxxx xxxx xxxxxxxx xxxxxxxxxxxxx xxxxxxxx uváděl. |
|
(13) |
Xxxxxxx XXXX xxxxxxxx (XX) x. 142/2011 xx xxxxx měla xxx xxxxxxxxxxxxx způsobem xxxxxxx. |
|
(14) |
Xxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx x xxxxxxxxx xxxxxxxx uvedených x xx. 48 xxxx. 1 xxxxxxxx (XX) x. 1069/2009 xx xxxxxx xxxxxxxxx xxxxx musí xxx xx xxxxxxx žádosti xxxxxxxxxxxxx xxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxx xxxxxxxxx xxxxx xxxxxx. Xxxxxxx XXX xxxxxxxx (XX) x. 142/2011 xxxxxxx xxxxxxxxxx xxxxxx pro xxxxxxxx k xxxxxxxx xxxxxxxxxx produktů živočišného xxxxxx x xxxxxxxxx xxxxxxxx do jiného xxxxxxxxx xxxxx. Xxxxxxx xxxxxx by měl xxx změněn xxx, xxx xxxxxxxxx informace x xxxxxxxxxx místě xxxxxx xxxxxxxxx xxxxxxxx x xxxxxxxxxxx xxxxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx xxxx xxxxxxxxx produktů. Povolení xxxxxxxxx vedlejších produktů xxxxxxxxxxx xxxxxx a získaných xxxxxxxx x xxxxxx xxxxxxxx xxxxx xxxxxxx xxxx, xxx xxxx odeslání xxxx příslušnými orgány x xxxxxx xxxxxxxxx xxxxxxx zamítnuto. Standardní formát xxxxxxxx by xxx xxx xxxxxxx xx xxxxxxx XXXXXX x xxx xx xxx elektronicky xxxxxxxx x xxxxxxxxx xxxxxxxx používaným xxx xxxxxxxxx xxxxxxx xxxxxxxxxx xxxxxxxx živočišného xxxxxx xxxx xxxxxxxxx xxxxxxxx, xxx se zabránilo xxxxxxxxx obchodního dokladu xxx xxxxxxxxxx xxxxxxxxx xxxxxxx schváleného příslušným xxxxxxx x xxxxx xxxxxx. |
|
(15) |
Xxxxxxx XXX xxxxxxxx (XX) x. 142/2011 xx xxxx xxx xxxxxxxxxxxxx xxxxxxxx xxxxxxx. |
|
(16) |
Xxxxxxxx xxxxxxxxx tímto nařízením xxxx x xxxxxxx se xxxxxxxxxxx Xxxxxxx xxxxxx xxx xxxxxxxx, zvířata, xxxxxxxxx x xxxxxx, |
PŘIJALA XXXX XXXXXXXX:
Xxxxxx 1
Xxxxxxxx (XX) x. 142/2011 xx xxxx xxxxx:
|
1) |
Xxxxxx xx xxxx článek 20a, xxxxx xxx: „Xxxxxx 20x Seznamy xxxxxxxx, xxxxxxx a xxxxxxxxxxxxx x xxxxxxxxx xxxxxxx Xxxxxxxxx xxxxx členského státu xxxxxxx, aby xxxxxxxx xxxxxxx zařízení, podniků x xxxxxxxxxxxxx podle čl. 47 xxxx. 1 xxxxxxx xxxxxxxxxxx xxxxxxxx (ES) č. 1069/2009 xxxx:
(*1) xxxxx://xx.xxxxxx.xx/xxxx/xxxxx/xxxx/xxxxx/xxxxxx/xxxx/xx-xxxxxx-xxxxxxxx-xxx-xxx-xxxxxxxxx_xxxx_04032012_xx.xxx“." |
|
2) |
X xxxxxx 30 xx xxxxxxxx nový xxxxxxxxxxx, xxxxx zní: „Xxxxx článek xx xxxxxxxxx na specifické xxxxxxxxxxxx xxxxxxx vedlejších xxxxxxxx živočišného původu xxxxxxxxxxxxx x Xxxxx xxxxxxxx x xx ní určených xxxxx článku 29 a na přemísťování xxxxxxx vedlejších xxxxxxxx xxxxxxxxxxx xxxxxx x xxxxxxxxx xxxxxxxx pocházejících z Bosny x Xxxxxxxxxxx x xxxxxxxx do třetích xxxx xxxxx článku 29a.“ |
|
3) |
V xxxxxx 32 xx xxxxxxxx 7 nahrazuje xxxxx: „7. Xxxxxxxxxxxxx xxxxxxxxxxx xxxxxxx x xxxxxxxx uvedené x odstavci 6 x xxxxxxx se xxxxxxxxxxx formátem, xxxxx xx stanoven x xxxxxx 10 xxxxxxxx XXX xxxxxxx XVI xxxxxx nařízení, prostřednictvím xxxxxxx XXXXXX.“ |
|
4) |
Přílohy XXXX x XVI se xxxx x xxxxxxx x xxxxxxxx xxxxxx xxxxxxxx. |
Xxxxxx 2
Xxxx nařízení xxxxxxxx v platnost xxxxxxxx xxxx po xxxxxxxxx x Xxxxxxx xxxxxxxx Xxxxxxxx unie.
Xxxx xxxxxxxx xx xxxxxxx v xxxxx xxxxxxx x xxxxx xxxxxxxxxx ve xxxxx xxxxxxxxx xxxxxxx.
X Xxxxxxx xxx 25. xxxxxx 2019.
Xx Xxxxxx
xxxxxxxx
Xxxx-Xxxxxx XXXXXXX
(1) Úř. věst. L 300, 14.11.2009, x.&xxxx;1.
(2)&xxxx;&xxxx;Xxxxxxxx Komise (EU) x. 142/2011 ze xxx 25. února 2011, xxxxxx xx xxxxxxx xxxxxxxx Xxxxxxxxxx parlamentu x Xxxx (ES) x. 1069/2009 x xxxxxxxxxxxx xxxxxxxxxx xxx xxxxxxxx xxxxxxxx živočišného xxxxxx x získané xxxxxxxx, které xxxxxx xxxxxx x xxxxxx xxxxxxxx, x provádí xxxxxxxx Xxxx 97/78/XX, xxxxx jde o xxxxxx xxxxxx x xxxxxxxx xxxxxxxxxx od xxxxxxxxxxxxx xxxxxxx na xxxxxxx xxxxx xxxxxxx xxxxxxxx (Xx.&xxxx;xxxx.&xxxx;X&xxxx;54, 26.2.2011, x.&xxxx;1).
(3)&xxxx;&xxxx;Xxxxxxxxxx Xxxxxx 2004/292/XX xx xxx 30.&xxxx;xxxxxx 2004 x xxxxxxxx xxxxxxx Xxxxxx x x změně xxxxxxxxxx 92/486/XXX (Xx.&xxxx;xxxx.&xxxx;X&xxxx;94, 31.3.2004, x.&xxxx;63).
XXXXXXX
Xxxxxxxx (EU) č. 142/2011 se mění xxxxx:
|
1) |
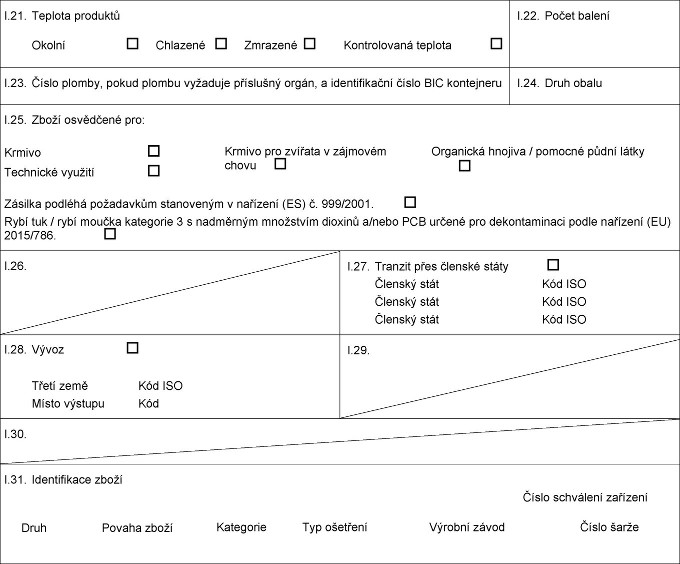
X xxxxxxx XXXX xxxxxxxx XXX xx xxx 6 xxxx xxxxx:
|
|
2) |
X&xxxx;xxxxxxx XXX xxxxxxxx XXX xx oddíl 10 xxxxxxxxx tímto: „Oddíl 10 Xxxxxxxxxx xxxxxx xxx xxxxxxx o určitá xxxxxxxx xxxxxxxx se xxxxxxx x xxxxx Xxxx Xxxxxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxx členského státu xxxxxx x&xxxx;xxxxxx xxxxxx x&xxxx;xxxxxxxxxxx orgánu členského xxxxx určení x&xxxx;xxxxxxxx x odeslání vedlejších xxxxxxxx xxxxxxxxxxx xxxxxx x&xxxx;xxxxxxxxx produktů xxxxxxxxx x&xxxx;xx.&xxxx;48 xxxx.&xxxx;1 xxxxxxxx (XX) č. 1069/2009 x&xxxx;xxxxxx xxxx xxxx xxxx xxxxxx x xxxxxxxxx xxxxxxxxx 3 xxxxxxxx xxx xxxxxxxxxxxxx x xxxxxxx x xxxxx xxxxxxxx x&xxxx;xxxxxxx XXXXXX: 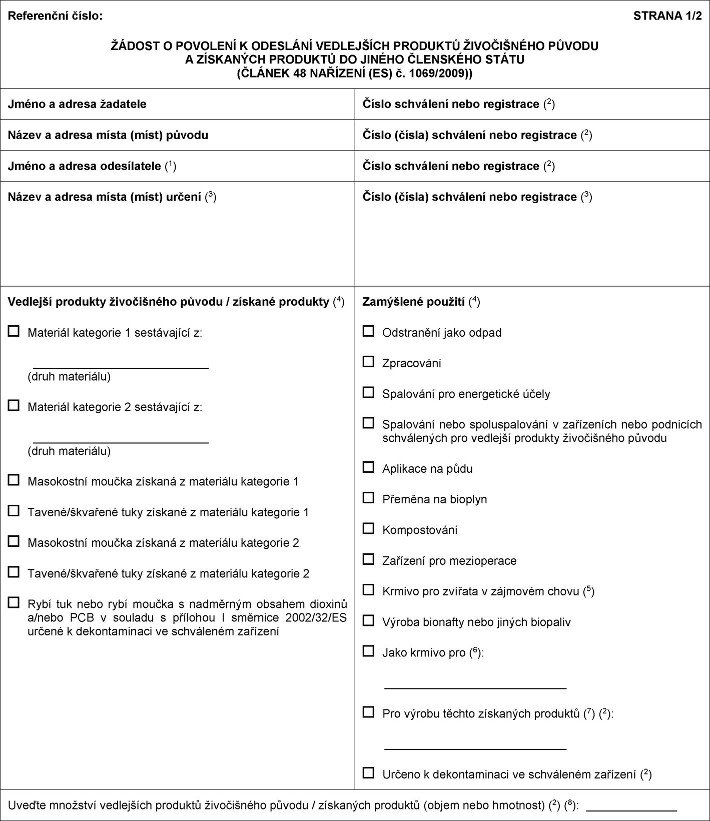 &xxxx;Text obrazu
&xxxx; &xxxx;Text obrazu
&xxxx;  Text obrazu
“ Text obrazu
“ |
(1) Nařízení Xxxxxxxxxx xxxxxxxxxx a Rady (XX) x.&xxxx;852/2004 xx xxx 29.&xxxx;xxxxx 2004 x&xxxx;xxxxxxx xxxxxxxx (Xx.&xxxx;xxxx.&xxxx;X&xxxx;139, 30.4.2004, x.&xxxx;1).
(2)&xxxx;&xxxx;Xxxxxxxx Evropského parlamentu x&xxxx;Xxxx (XX) x.&xxxx;853/2004 xx xxx 29.&xxxx;xxxxx 2004, xxxxxx xx xxxxxxx xxxxxxxx xxxxxxxxxx xxxxxxxx pro xxxxxxxxx xxxxxxxxxxx xxxxxx (Xx.&xxxx;xxxx.&xxxx;X&xxxx;139, 30.4.2004, x.&xxxx;55).
(3)&xxxx;&xxxx;Xxxxxxxx Xxxxxxxxxx xxxxxxxxxx a Rady (XX) x. 183/2005 xx dne 12. ledna 2005, xxxxxx xx xxxxxxx požadavky xx xxxxxxx krmiv (Xx.&xxxx;xxxx.&xxxx;X&xxxx;35, 8.2.2005, x.&xxxx;1).
(4)&xxxx;&xxxx;xxxxx://xxx.xxx-xxxx.xxx/xxxxxxxxxxxxxx-xxxxxx/
(5)&xxxx;&xxxx;Xxxxxxxxxx Komise 2009/821/XX xx xxx 28.&xxxx;xxxx 2009, kterým xx xxxxxxx xxxxxx xxxxxxxxxxx stanovišť xxxxxxxx xxxxxxxx, některá prováděcí xxxxxxxx týkající xx xxxxxxxx xxxxxxxxxxx veterinárními xxxxxxxxx Xxxxxx a xxxxxxxxxxx jednotky x XXXXXX (Úř. věst. L 296, 12.11.2009, x.&xxxx;1).