XXXXXXXX XXXXXX (XX) x.&xxxx;429/2008
xx xxx 25. dubna 2008
x&xxxx;xxxxxxxxxxx xxxxxxxxxx x&xxxx;xxxxxxxx Xxxxxxxxxx parlamentu x&xxxx;Xxxx (XX) x.&xxxx;1831/2003, xxxxx xxx o vypracování a podávání xxxxxxx x&xxxx;xxxxxxxxxxxxx x&xxxx;xxxxxxxxxx xxxxxxxxxxx xxxxx
(Xxxx s významem xxx XXX)
XXXXXX EVROPSKÝCH XXXXXXXXXXXX,
x&xxxx;xxxxxxx xx Xxxxxxx x&xxxx;xxxxxxxx Xxxxxxxxxx xxxxxxxxxxxx,
x&xxxx;xxxxxxx xx xxxxxxxx Evropského xxxxxxxxxx x&xxxx;Xxxx (XX) x.&xxxx;1831/2003 ze xxx 22.&xxxx;xxxx 2003 x&xxxx;xxxxxxxxxxx xxxxxxx používaných ve xxxxxx xxxxxx (1), x&xxxx;xxxxxxx xx čl. 7 odst. 4 x&xxxx;5 xxxxxxxxx xxxxxxxx,
xx xxxxxxxxxx x&xxxx;Xxxxxxxxx xxxxxx xxx xxxxxxxxxx xxxxxxxx x&xxxx;xxxxxxx x&xxxx;xx.&xxxx;7 xxxx.&xxxx;4 x&xxxx;5 xxxxxxxx (XX) x.&xxxx;1831/2003,
xxxxxxxx x&xxxx;xxxxx xxxxxxx:
|
(1) |
Xx xxxxxxxx stanovit xxxxxxxxx xxxxxxxx, pokud xxx x&xxxx;xxxxxx xxxxxxxxxx xxxxxxxxxxx xxxxx podle nařízení (XX) x.&xxxx;1831/2003, včetně xxxxxxxx xxx vypracování x&xxxx;xxxxxxxx xxxxxxx x&xxxx;xxxxxxxxxxxxx x&xxxx;xxxxxxxxxx xxxxxx xxxxxxxxxxx xxxxx. Xxxx xxxxxxxx xxxx xxxxxxxx xxxxxxxxxx x&xxxx;xxxxxxx xxxxxxxx Xxxx 87/153/XXX (2), xxxxxx xx xxxxxxx xxxxxx zásady xxx xxxxxxxxxxxxx doplňkových xxxxx xx výživě xxxxxx. |
|
(2) |
Xxxx xxxxxxxx by xxxx stanovit xxxxxxxxx, xxxxx xxxx xxxxxxxx xxxxxxxxxxx připojená k žádosti. Xxxx by xxxxxxx xxxxx xxxxxxx údaje, xxxxx xxxx být xxxxxxxxxx x&xxxx;xxxxxxxxxxxx x&xxxx;xxxxxxxxxxxxxxx xxxxxxx xxxxxxxxx xxxxx, x&xxxx;xxxxxx, jež xxxx xxx předloženy x&xxxx;xxxxx xxxxxxxx xxxx xxxxxxxx x&xxxx;xxxxxxxxxx xxx xxxxxxx, xxxxxxx a životní prostředí xx účelem ověření x&xxxx;xxxxxxxxxxx žádostí x&xxxx;xxxxxxxx Xxxxxxxxx xxxxxx pro xxxxxxxxxx xxxxxxxx (dále xxx „úřad“). |
|
(3) |
Podle xxxxxx xxxxxxxxx xxxxx xxxx xxxxxxxxxxxx podmínek xxx xxxxx xx xxxx xxxxxx studií potřebných x&xxxx;xxxxxxxxxxx xxxxxx vlastností x&xxxx;xxxxxx xxxxx. Xxxxxxxx xx xxxxx xxxx xxx xxxxxxx xxxxxxxxxx x&xxxx;xxxxxxx xxxxxxxxx, xxxxx xxx x&xxxx;xxxx xxxxxx x&xxxx;xxxxxxxxx, xxx xxxx xxx předloženy k prokázání xxxxxxxxxxx x&xxxx;xxxxxxxxx xxxxxxx xxxxxxxxx látky. Xxxxxxxx, xxxxx xxxxxxx xxxx xxxxxxxxx, xx xxxx x&xxxx;xxxxxxxxxxx svůj výběr xxxxxxxxx. |
|
(4) |
Xxxx by xxx xxx xxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxxx informace, xxx xxxx určit, xxx doplňková látka xxxxxxx podmínky pro xxxxxxxx xxxxx článku 5 xxxxxxxx (XX) x.&xxxx;1831/2003. |
|
(5) |
Xx xxxxxxxx xxxxxxxx příslušné xxxxx xxxxxxx při xxxxxxxxxxxxx xxxxxxxxxxx xxx xxxxxxxxx látky xxxxxx x&xxxx;xxxxxxx v krmivu (xxxxxxxx) xxxx xxxx, aby xxxx xxxxxxxxx, že xxxxxxxx xxxxxxxxxxxxx xxxxxxx xxxxxx xxxxxxxxxxx. |
|
(6) |
X&xxxx;xxxxxxx xxxxxxxx xx xxxx být xxxxxxxxx xxxxxxxx požadavky xxx xxxxxxxxxx xxxxxxxxx xxxxxxxxxxx xxxxx xxxxxxx x&xxxx;xx.&xxxx;6 xxxx.&xxxx;1 nařízení (XX) č. 1831/2003. |
|
(7) |
S cílem podnítit xxxxx x&xxxx;xxxxxxx xxxxxxxx xxx xxxxxxxxx xxxxx xxx xxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxx xxxxxxxxxxx xx xxxx xxx xxxxxxxxx xxxxxxxx xxxxxxxx xxx přihlédnutí x&xxxx;xxxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxx xxxxxxxxxxx na xxxxxxxxxxx xxxxxxx na xxxxx xxxxxxxxx. |
|
(8) |
Xxxxxxxxx pravidla xxxxxxxx xx xxxxxxx x&xxxx;xxxxxxxx xx xxxx xxxx x&xxxx;xxxxx xxxxx xxxxxxxxx xx xxxxxxx určená x&xxxx;xxxxxxxx xxxxxxxx x&xxxx;xxxxxxx xxxxxxx, xxx xxx xxxxxxx xxxxxxxx xx xxxxxxxxxxx xxxxxxxxxxx xxx xxxxxxx xxxx xxxxxxxxxxxx xxxxxx důležité. |
|
(9) |
Využití postupů xxxxxxxxxxxx xxxxxxxxx xxxxxxxxxxxxx xxxxxx x&xxxx;xxxxxxxx xx xxxxx xxxxxxxx účelům x&xxxx;xxxxxxxxx xx zvířatech xxxxx směrnice Xxxx 86/609/XXX xx dne 24.&xxxx;xxxxxxxxx 1986 x&xxxx;xxxxxxxxxx xxxxxxxx a správních xxxxxxxx xxxxxxxxx xxxxx xxxxxxxxxx xx xxxxxxx zvířat xxxxxxxxxxx xxx pokusné x&xxxx;xxxx xxxxxxx xxxxx (3) xx xxxx xxx xxxxxxxxx. |
|
(10) |
Xxx xx xxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxx, xxxx xx být xxxxxxxxx zjednodušené postupy xxx xxxxxxxxxx xxxxxxxxxxx xxxxx, xxxxx xxx xxxx povoleny xxx xxxxxxx v potravinách. |
|
(11) |
Co se xxxx xxxxxxxxxxx xxxxx, xxxxx byly xxxxx xxxxxxxx Rady 70/524/XXX (4) xxxxxxxx xxx časového xxxxxxx, xxxx xx xxx xxxxxxxxx stanovena xxxxxxx, xxx v případě, xx xxxxxx x&xxxx;xxxxxxxxx xxxxx studie, xxxxxxx xxxxxxxx účinnost pomocí xxxxxx xxxxxxxxx, xxxxx xxxx x&xxxx;xxxxxxxxx x&xxxx;xxxxxxxxx xxxxxxxxx, xxxxxxx materiálů xxxxxxxxxx xx xxxxxx xxxxxxxx xxxxxxxxx xxxxxxx xxxxxxxxx látky. |
|
(12) |
Je nutno xxxxxxxx xxxxxxxx xxx xxxxxxx o změny xxxxxxxx x&xxxx;xxxxxxx x&xxxx;xx.&xxxx;13 xxxx.&xxxx;3 xxxxxxxx (ES) č. 1831/2003. |
|
(13) |
Je xxxxx xxxxxxxx xxxxxx xxxxxxxx xxx xxxxxxx x&xxxx;xxxxxxxx povolení xxxxx xxxxxx&xxxx;14 xxxxxxxx (XX) x.&xxxx;1831/2003. |
|
(14) |
Xx xx xxxx xxxxxxxxxx x&xxxx;xxxxxxxx xxxxxxxxxxx x&xxxx;xxxxxxxxx, jež xx xxxxx xxxxxxx xx xxxxxxx xxxxxxx, xx xxxxxxxx xxxxxxxx xxxxxxxxx xxxxxx, během něhož xx budou xxxxxx xxxxxxxx xxxxxxxxx xxxxxxxx. X&xxxx;xxxxxxxx xxxxxxxx xxxx xxxxxxx tohoto nařízení x&xxxx;xxxxxxxx xx xx xxxx x&xxxx;xxxxxx xxxxxxxx x&xxxx;xxxxxxx x&xxxx;xxxxxxxx xxxxxxxx 87/153/XXX. Pokud jde x&xxxx;xxxxxxx xxxxxx během xxxxxxxx xxxxxx xx xxxxxx x&xxxx;xxxxxxxx, xxxxxxxx xx xxxxxxxx x&xxxx;xxxxxx xxxx xxxxxxxx xxx xxxxxxx studie xxxx xxx možnost xxxxxx xxxx xxxxxxxx xxxxxxxxxxx x&xxxx;xxxxx xxxxxxxx a přílohou xxxxxxxx 87/153/XXX. Prováděcí xxxxxxxx xxxx xxxxxxxxxxx xx xxxxxxx současných xxxxxxxxx a technických poznatků x&xxxx;x&xxxx;xxxxxxx nutnosti xx xxxx xxx xxxxxxxxxxxx xxxxxxxxxx xxxxxx xxxxxx x&xxxx;xxxx xxxxxxx. |
|
(15) |
Xxxxxxxx xxxxxx xxxxxxxx jsou x&xxxx;xxxxxxx xx xxxxxxxxxxx Stálého xxxxxx xxx potravinový xxxxxxx a zdraví xxxxxx, |
XXXXXXX XXXX XXXXXXXX:
Xxxxxx 1
Xxxxxxxx
Xxx xxxxx xxxxxx xxxxxxxx xx použijí xxxx xxxxxxxx:
|
1. |
„xxxxxxx x xxxxxxxx xxxxx x xxxxxxxxx zvířaty, xxxxx xxxxxx xxxxxx x xxxxxxxx potravin“ se xxxxxx xxxxxxx xxxxx, xxx xxxx xxxxxxxx xxxxxx, chovány nebo xxxxxx xxxxxxxx, xxxxxx xxxx xxxxxx xxx xxxxxxx xxxxxxxx, vyjma xxxx; |
|
2. |
„xxxxxxxxxxx xxxxx“ xx xxxxxx xxxxxxx xxxxxx x xxxxxxxx xxxxxxxx xxxx xxx skot (xxxxxxx xxxxxxx xxx xxxxx x xxxx, včetně xxxxx), xxxx (zvířata chovaná xxx xxxx), prasata, xxxxxx (včetně nosnic), xxxxx x xxxx druhu Xxxxxxxxxx. |
Xxxxxx 2
Xxxxxx
1. Xxxxxx o povolení xxxxxxxxx xxxxx podle xxxxxx 7 xxxxxxxx (XX) x. 1831/2003 xx předloží pomocí xxxxxxxxx xxxxxxxxxxx v příloze I.
X xxxxxxx xx xxxxxxx dokumentace xxxxx xxxxxx 3 (xxxx xxx „dokumentace“), xxxxx xxxxxxxx xxxxx x xxxxxxxxx xxxxxxx v čl. 7 xxxx. 3 xxxxxxxx (ES) x. 1831/2003.
2. Pokud xxxxxxx v souladu s článkem 18 xxxxxxxx (XX) č. 1831/2003 xxxxxxxx, xxx se x xxxxxxxxx částmi xxxxxxxxxxx xxxxx odstavce 1 zacházelo xxxx x xxxxxxxxx xxxxx, xxxxxxxx xxx každý xxxxxxxx nebo část xxxxxxxxx xxxxxxxxxx xxxxxxxxxx, xx xxxxxxxxxx těchto xxxxxxxxx xx mohlo xxxxxxxx xxxxxxxx jeho xxxxxxxxx xxxx xxxxxxxxxxx. Xxxxxxx xxxxx xxxxxxxxxxx xxxx být předloženy xxxxxxxx xx xxxxxx xxxxxxxxxxx x xxxxx být xxxxxxxx x xxxxxxx xxxxxxxxxxx xxxxx čl. 7 odst. 3 xxxx. x) xxxxxxxx (XX) x. 1831/2003. Xxxxxxx xxxxx Xxxxxx xxxxx xxxxx dokumentace, x xxxxx xx xxx xxxxxxxxx xxxx x xxxxxxxxx xxxxx, a připojeného xxxxxxxxxx.
Xxxxxx 3
Xxxxxxxxxxx
1. Xxxxxxxxxxx přiměřeně x xxxxxxxxxx xxxxxxxxx, že doplňková xxxxx splňuje podmínky xxx xxxxxxxx xxxxxxxxx x xxxxxx 5 nařízení (ES) x. 1831/2003.
2. Xxxxxx xxxxxxxxx na xxxxxxxxxxx a předání xxxxxxxxxxx xxxx stanoveny x xxxxxxx XX.
Zvláštní xxxxxxxxx, xxx xxxxxxxxxxx xxxx xxxxxxxx x xxxxxxxx xxxxxxx, jsou xxxxxxxxx x xxxxxxx XXX.
Xxxxxxxxx xxxx xxxxxx xxxxxxxxxxxx xxxxxx je xxxxxxxxx x xxxxxxx XX.
3. Xxxxxxxx xx xxxxxxxx 2 může žadatel xxxxxxxxx dokumentaci, xxxxx xxxxxxxxx xxxxxxxxx xxxxxxxxx x xxxxxxxx 2, pokud xxxxx xxxxx, jenž xxxx xxxxxxxxx nesplňuje, odůvodní.
Xxxxxx 4
Xxxxxxxxx xxxxxxxx
1. Xx žádosti x xxxxxxxx podané xxxx xxxxx xxxxxx xxxxxx xxxxxxxx x xxxxxxxx xx xxxxxx xxxxxxxx xxxxxxx xxxxxxxx 87/153/XXX.
2. X xxxxxxx x xxxxxxxx xxxxxxxx xxxx 11. xxxxxxx 2009 se mohou xxxxxxxx rozhodnout, xx xxxxx xxxxxx používat xxxxxx XXX x XX xxxxx X x XX xxxxxxx xxxxxxxx 87/153/XXX místo xxxx 1.3, 1.4, 2.1.3, 2.1.4, 2.2.3, 2.2.4, 3.3, 3.4, 4.1.3, 4.1.4, 4.2.3, 4.2.4, 5.3, 5.4, 6.3, 6.4, 7.3, 7.4, 8.3 x 8.4 xxxxxxx XXX x xxxxx xxxxxxxxxx xx xxxxxxx „Xxxxxxxxx doba xxxxxx xxxxxxxxxxxx xxxxxx xxxxxxxxx“ x xxxxxxxxx přílohy IV.
Xxxxxx 5
Xxxxx x xxxxxxxx
Xxxx xxxxxxxx xxxxxxxx x xxxxxxxx xxxxxxxx xxxx xx xxxxxxxxx x Xxxxxxx xxxxxxxx Evropské xxxx.
Xxxx xxxxxxxx xx xxxxxxx x xxxxx rozsahu x xxxxx xxxxxxxxxx xx xxxxx xxxxxxxxx xxxxxxx.
X Xxxxxxx xxx 25. xxxxx 2008.
Za Xxxxxx
Xxxxxxxxx XXXXXXXXX
xxxxxx Xxxxxx
(1)&xxxx;&xxxx;Xx.&xxxx;xxxx. X&xxxx;268, 18.10.2003, x.&xxxx;29. Xxxxxxxx ve xxxxx nařízení Komise (XX) x.&xxxx;378/2005 (Úř. věst. X&xxxx;268, 18.10.2003, s. 29).
(2)&xxxx;&xxxx;Xx.&xxxx;xxxx. X&xxxx;64, 7.3.1987, x.&xxxx;19. Xxxxxxx xxxxxxxxx (XX) x.&xxxx;1831/2003.
(3)&xxxx;&xxxx;Xx.&xxxx;xxxx. X&xxxx;358, 18.12.1986, x.&xxxx;1; opravené xxxxx x&xxxx;Xx.&xxxx;xxxx. L 358, 18.12.1986, x.&xxxx;1. Směrnice xx xxxxx xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x&xxxx;Xxxx 2003/65/XX (Xx.&xxxx;xxxx. L 358, 18.12.1986, x.&xxxx;1).
(4) Úř. věst. L 270, 14.12.1970, x.&xxxx;1. Xxxxxxxx xxxxxxxxx xxxxxxxxx nařízením Komise (XX) x.&xxxx;1800/2004 (Úř. věst. X&xxxx;270, 14.12.1970, x.&xxxx;1).
PŘÍLOHA I
FORMULÁŘ ŽÁDOSTI UVEDENÝ X&xxxx;XX.&xxxx;2 XXXX.&xxxx;1&xxxx;X&xxxx;XXXXXXX ÚDAJE
1. FORMULÁŘ XXXXXXX
XXXXXXXX KOMISE
GENERÁLNÍ XXXXXXXXXXX
XXX XXXXXX X&xxxx;XXXXXXX SPOTŘEBITELE
(Adresa)
Datum: …
|
Xxx |
: |
Xxxxxx x&xxxx;xxxxxxxx xxxxxxxxx xxxxx podle nařízení (XX) x.&xxxx;1831/2003. |
|
◻ |
Xxxxxxxx xxxxxxxxx xxxxx nebo xxxx xxxxx xxxxxxxxx xxxxx (xx.&xxxx;4 xxxx.&xxxx;1 xxxxxxxx (XX) x.&xxxx;1831/2003) |
|
◻ |
Xxxxxxxx xxxxxxxxxxxx xxxxxxxx (xx.&xxxx;10 odst. 2 xxxx&xxxx;7 nařízení (ES) x.&xxxx;1831/2003) |
|
◻ |
Xxxxx stávajícího povolení (xx.&xxxx;13 xxxx.&xxxx;3 nařízení (XX) č. 1831/2003) |
|
◻ |
Obnovení povolení xxxxxxxxx xxxxx (xxxxxx&xxxx;14 xxxxxxxx (ES) x.&xxxx;1831/2003) |
|
◻ |
Xxxxxxxx x&xxxx;xxxxxxxxxx xxxxxxxxx (xxxxxx&xxxx;15 xxxxxxxx (XX) x.&xxxx;1831/2003) |
(Xxxxxxx xxxxxxxxxxx zaškrtnutím xxxxxxx x&xxxx;xxxxxxx)
Xxxxxxx(x)&xxxx;x/xxxx jeho/jejich xxxxxxxx(x)&xxxx;xx Xxxxxxxxxxxx (čl. 4 odst. 3 xxxxxxxx (XX) č. 1831/2003) xx podmínek xxxxxxxxx x&xxxx;xx.&xxxx;7 xxxx.&xxxx;3 xxxx.&xxxx;x)&xxxx;xxxxxxxx (XX) x.&xxxx;1831/2003 (xxxxx, xxxxxx ….)
…
…
xxxxxx (xxxxxxxx) xxxx xxxxxx xx xxxxxx xxxxxxx xxxxxxxx xxx xxxxxxxxxxx xxxxxxx xxxxxxx doplňkovou xxxxx:
1.1&xxxx;&xxxx;&xxxx;Xxxxxxxxxxxx x&xxxx;xxxxxxxxxxxxxxx xxxxxxxxx xxxxx
Xxxxx xxxxxxxxx xxxxx (xxxxxxxxxxxxxxx xxxxxx látky (xxxxx) xxxx xxxxxxx (xxxxxxx), xxx je xxxxxxxx x&xxxx;xxxxxx&xxxx;2.2.1.1 x&xxxx;2.2.1.2 přílohy II):
…
…
Obchodní xxxxx (xx-xx xx xxxxxx u povolení vázaných xx xxxxxxxx):
…
…
X&xxxx;xxxxxxxxx/xxxxxxxxxxx x&xxxx;xxxxxxx xxxxxxx/xxxxxxxxx doplňkových xxxxx&xxxx;(1) (xxxxxx):
…
…
Xxxxxx xxxxx xxxxxx:
…
…
…
Xxxxx xxxxxxxx povolení (xx.&xxxx;9 xxxx.&xxxx;6 xxxxxxxx (XX) x.&xxxx;1831/2003):
…
…
Xxxx xxxxxxxxx látka xxx xxxx povolena x&xxxx;xxxxxxxx xxxxxxxxxx x&xxxx;xxxxxxxx xxxxxxxx.……/…/X(X)X&xxxx;xxxx nařízením (ES) x.&xxxx;…/… xxx xxxxxx … jako (kategorie xxxxxxxxxxx látek)
…
Tato doplňková xxxxx xxx xxxx xxxxxxxx x&xxxx;xxxxxxxx xxxxxxxxxx x&xxxx;xxxxxxxxxxx xxxxxxxx .…/…/X(X)X&xxxx;xxxx xxxxxxxxx (ES) č. …/… xxx xxxxxx … xxxx
…
xxx použití x
…
Xxxxx xx xxxxxxx xxxxxx x&xxxx;xxxxxxxxx modifikovaných xxxxxxxxx xxxx xxxx xxxxxxxxx xxxxxxxx xx xx x&xxxx;xxxx vyroben, xxxxxx xxxx informace:
|
◻ |
jednoznačný xxxxxxxxxxxxx xxx (xxxxxxxx Xxxxxx (XX) x.&xxxx;65/2004&xxxx;(2)) (je-li xx xxxxxx): … |
|
◻ |
xxxxx x&xxxx;xxxxxxxxx xxxxxxxx uděleném v souladu x&xxxx;xxxxxxxxx Evropského xxxxxxxxxx x&xxxx;Xxxx (ES) x.&xxxx;1829/2003&xxxx;(3): … |
|
◻ |
xxxx xxxxx o dosud xxxxxxxxxx xxxxxxx o povolení xxxxx xxxxxxxx (ES) x.&xxxx;1829/2003: … |
1.2&xxxx;&xxxx;&xxxx;Xxxxxxxx xxx xxxxx
1.2.1&xxxx;&xxxx;&xxxx;Xxxxxxx x&xxxx;xxxxxxxxxxx xxxxxxxx
Xxxx nebo xxxxxxxxx xxxxxx:
…
…
Xxxxxxxxx xxxxx xxxx xxxxxxxx:
…
…
Xxxxxxxxx xxxxx (xx-xx xx xxxxxx): xx xxxx xxxxxxxx xxxxxxxx&xxxx;(4) xxxx xxxxxxxx tvořící xxxxxxx (CFU) xxxx xx/xx xxxxxxxxxxx xxxxxx x&xxxx;xxxxxx vody 12&xxxx;%
…
…
Xxxxxxxxx xxxxx (je-li xx xxxxxx): mg xxxx xxxxxxxx xxxxxxxx nebo XXX xxxx xx/xx xxxxxxxxxxx xxxxxx x&xxxx;xxxxxx xxxx 12&xxxx;%
…
…
X&xxxx;xxxxxxxx krmiv xx možno xxxxx xxxxxxxxx x&xxxx;xxxxxxxxx dávku xx litr.
1.2.2 Použití xx xxxx
Xxxxxxxxx xxxxx (xx-xx xx vhodné): mg xxxx xxxxxxxx aktivity xxxx XXX xxxx xx/x&xxxx;xxxx
…
…
Xxxxxxxxx xxxxx (je-li xx vhodné): mg xxxx jednotky xxxxxxxx xxxx XXX nebo xx/x&xxxx;xxxx
…
…
1.2.3&xxxx;&xxxx;&xxxx;Xxxxxxxx xxxxxxxx pro xxxxx (je-li to xxxxxx)
Xxxx xxxx kategorie xxxxxx:
…
…
Xxxxxxxxx stáří:
…
…
Minimální xxxxx (xx-xx to xxxxxx): xx xxxx xxxxxxxx xxxxxxxx xxxx XXX/xx xxxxxxxxxxx xxxxxx x&xxxx;xxxxxx xxxx 12 %
…
…
Maximální xxxxx (xx-xx to vhodné): xx xxxx xxxxxxxx xxxxxxxx xxxx CFU/kg xxxxxxxxxxx xxxxxx x&xxxx;xxxxxx xxxx 12 %
…
…
U tekutých xxxxx xx xxxxx xxxxx xxxxxxxxx x&xxxx;xxxxxxxxx dávku xx litr.
Podmínky xxxx xxxxxxx xxxxxxx (je-li xx xxxxxx):
…
…
…
Xxxxxxxx podmínky xxxx omezení pro xxxxxxxxxx (xx-xx to xxxxxx):
…
…
…
…
Xxxxxxxxx xxxxx reziduí (xx-xx xx xxxxxx):
Xxxx xxxx kategorie xxxxxx:
…
…
Xxxxxxxxxxxx xxxxxxxx:
…
…
Xxxxxx xxxxx nebo xxxxxxxx:
…
…
…
Xxxxxxxxx reziduum x&xxxx;xxxxxxx xxxx xxxxxxxxxx (μx/xx):
…
…
…
Xxxxxxxx xxxxx:
…
1.3&xxxx;&xxxx;&xxxx;Xxxxxxxxxx vzorky
Číslo xxxxxx xxxxxxxxxx xxxxxxxxxx Xxxxxxxxxxxx (xx-xx to xxxxxx):
…
Xxxxx xxxxxx / xxxxx xxxxx:
…
Xxxxx xxxxxx:
…
Xxxxx xxxxxxxxx xxxxxxxxxxxx:
…
Xxxxxxxxxxx:
…
Xxxxxxxx:
…
Xxxxxxx xxxxx:
…
Xxxxx xxxxx:
…
Xxxxxxxxx xx xxxxxxxxxx:
…
1.4&xxxx;&xxxx;&xxxx;Xxxxxxxxxx xxxxx (xx-xx xx vhodné)
…
…
…
…
Kopie xxxx xxxxxxx xxxx xxxxxxx xxxxx úřadu x&xxxx;xxxxxxxxxxx x&xxxx;xxxxxxxxxx xxxxxxxxxx Xxxxxxxxxxxx s referenčními xxxxxx.
Xxxxxx …
1.5&xxxx;&xxxx;&xxxx;Xxxxxxx:
|
◻ |
xxxxx xxxxxxxxxxx (pouze xxx úřad), |
|
◻ |
veřejný xxxxxx xxxxxxxxxxx, |
|
◻ |
xxxxxxxx shrnutí dokumentace, |
|
◻ |
seznam xxxxx xxxxxxxxxxx, x&xxxx;xxxxx xx být xxxxxxxxx xxxx s důvěrnými údaji, x&xxxx;xxxxx xxxxxxxxxxx xxxxxxxxx xxxxx xxxxxxxxxxx (xxxxx xxx Xxxxxx x&xxxx;xxxx), |
|
◻ |
xxxxx xxxxxxxxx xxxxx xxxxxxxx(x), |
|
◻ |
xxx xxxxxx xxxxxxxxx látky xxx xxxxxxxxxx laboratoř Xxxxxxxxxxxx xxxxx xx.&xxxx;7 xxxx.&xxxx;3 písm. f) nařízení (ES) x.&xxxx;1831 / 2003 (xxxxx xxx xxxxxxxxxx xxxxxxxxx Xxxxxxxxxxxx), |
|
◻ |
xxxx s údaji x&xxxx;xxxxxxxxxxx xxxxxxxxx (xxxxx xxx xxxxxxxxxx xxxxxxxxx Xxxxxxxxxxxx), |
|
◻ |
xxxxxxxxx x&xxxx;xxxxxxxxxxxx a analýze (xxxxx xxx referenční xxxxxxxxx Xxxxxxxxxxxx) a |
|
◻ |
potvrzení x&xxxx;xxxxxxxx xxxxxxxx xxx xxxxxxxxxx xxxxxxxxx Společenství (xxxxxx&xxxx;4 xxxxxxxx (XX) x.&xxxx;378/2005&xxxx;(5). |
Xxxxxxx příslušné části xxxxxxxxx x&xxxx;xxxxxxxx xx xxxxx škrtněte. Xxxxxxxx xxxxxxxxx žádosti (s ostatními xxxxxxxxxxxx přílohami) xxxxxxx xxxxx Evropské xxxxxx.
2.&xxxx;&xxxx;&xxxx;XXXXXXX XXXXX XXXXXXXX(X)
Xxxxxxxxx xxxxx xxx xxxxxxxxxx xxxxxxx x&xxxx;xxxxxxxx doplňkové látky xxxxx xxxxxxxx (XX) x.&xxxx;1831/2003
|
1. |
Xxxxxxxxxx xxxx xxxxx, xxxxx podává xxxxxx
|
|
2. |
Xxxxxxxxx xxxxx (pro xxxxxxxx xxxxxxxxxxxxx x&xxxx;Xxxxxx, xxxxxx x&xxxx;xxxxxxxxxx laboratoří Xxxxxxxxxxxx)
|
(1) U funkční xxxxxxx „xxxx xxxxxxxxxxxx xxxxxxxxx xxxxx“ x&xxxx;xxxxxxxxx xxxxxxxxxxxx xxxxxxxxx látky xx xxxxx xxxxxxxxxxx xxxxxxx, xxxxx xxxxxx xx doplňková xxxxx xxx.
(2)&xxxx;&xxxx;Xx.&xxxx;xxxx. X&xxxx;10, 16.1.2004, x.&xxxx;5.
(3)&xxxx;&xxxx;Xx.&xxxx;xxxx. X&xxxx;268, 18.10.2003, x.&xxxx;1. Nařízení naposledy xxxxxxxxx xxxxxxxxx (ES) x.&xxxx;298/2008 (Úř. věst. X&xxxx;268, 18.10.2003, x.&xxxx;1).
(4)&xxxx;&xxxx;Xxxxxxxx „xxxxxxxx“ xxxxxxxx xxxxxxx.
(5)&xxxx;&xxxx;Xxxxxxxx Komise (XX) x.&xxxx;378/2005 xx xxx 4.&xxxx;xxxxxx 2005 x&xxxx;xxxxxxxxxx xxxxxxxxxxx xxxxxxxxxx x&xxxx;xxxxxxxx Evropského xxxxxxxxxx x&xxxx;Xxxx (XX) č. 1831/2003, xxxxx xxx x&xxxx;xxxxxxxxxx x&xxxx;xxxxx xxxxxxxxxx xxxxxxxxxx Xxxxxxxxxxxx x&xxxx;xxxxxxxxxxx s žádostmi x&xxxx;xxxxxxxx xxxxxxxxxxx xxxxx x&xxxx;xxxxxxxx (Xx.&xxxx;xxxx. X&xxxx;59, 5.3.2005, x.&xxxx;8). Nařízení xx xxxxx nařízení (XX) č. 850/2007 (Xx.&xxxx;xxxx. X&xxxx;59, 5.3.2005, x.&xxxx;8).
XXXXXXX&xxxx;XX
XXXXXX XXXXXXXXX, XXX XXXX XXXXXXXX DOKUMENTACE XXXXX ČLÁNKU 3
OBECNÁ XXXXXXXXXX
Xxxx xxxxxxx xxxxxxx požadavky xx xxxxxxxxxxx seznamu x&xxxx;xxxxxxxxxxxxxxx xxxxxx a informace x&xxxx;xxxxxxx, mikroorganismech a přípravcích, xxx xxxx xxx xxxxxxxxxx x&xxxx;xxxxxxxxxxx podle xxxxxx&xxxx;7 xxxxxxxx (XX) x.&xxxx;1831/2003 xxx:
|
— |
xxxxxxxx nové xxxxxxxxx xxxxx, |
|
— |
xxxxxxxx nového xxxxx doplňkové látky, |
|
— |
změnu xxxxxxxxxxx xxxxxxxx doplňkové xxxxx nebo |
|
— |
obnovení xxxxxxxx xxxxxxxxx xxxxx. |
Xxxxxxxxxxx musí xxxxxxx xxxxxxxxxxx xxxxxxxxxxx xxxxx na xxxxxxx xxxxxxxxxx xxxxx poznatků x&xxxx;xxxxxxx, xx xxxx xxxxxxxxx xxxxx odpovídají xxxxxxxxx zásadám xxx xxxxxx xxxxxxxx, xxxxx xxxx xxxxxxxxx x&xxxx;xxxxxx&xxxx;5 xxxxxxxx (XX) x.&xxxx;1831/2003.
Xxxxxx, xxx xxxx xxx xxxxxxxxxx, x&xxxx;xxxxxx rozsah xxxx xxxxxxx na xxxxxx xxxxxxxxx xxxxx, xxxxxxxxx nebo xxxxxxx xxxxxxx, druhu xxxxxxxx (xxxxxxxx, xxxxx xxxx xxxxxx xx xxxxxxxx; xxxxxxxx xxxxxx xx xxxxxxxx), xxxxxxx xxxxx, xxxxxxxx zvířatech a podmínkách xxx užití. Xxxxxxx xxxxxx xx tuto xxxxxxx a přílohu III, aby xxxx možno posoudit, xxxxx xxxxxx a informace xxxx xxx xxxxxxxx xx žádostí xxxxxxxxxx.
Xxxxxxx xxxxxxxxxxx xxxxx xxxxxx xxx xxxxxxxxx xxxxxxxxx xxxxx nebo odchýlení xx xx dokumentace xxxxxxxxxx x&xxxx;xxxx příloze, xxxxxxx&xxxx;XXX a příloze IV.
Dokumentace musí xxxxxxxxx xxxxxxxx xxxxxx x&xxxx;xxxxx xxxxxxxxxxx xxxxxxxx, xxxxxxxxxx x&xxxx;xxxxxxx se xxxxxxxx xxxxxxxxx xxxxxxxxx x&xxxx;xxxx příloze. Xxxxxxxxxxx xxxx xxxxxxxxx xxxxxx x&xxxx;xxxxx xxxxx xxxxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxx x&xxxx;xxxxx xxxxxxxxx xxxxxxxxxxx xxxxxxxxxx, xxxxx xxx xxxx xxxxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx. Pokud xxxx xxxx studie xxx xxxxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx xxxxx xxxxxxxx xxxxxxxx xxxxxxxx xx Xxxxxxxxxxxx, xxxxxxxxx xxxxx na výsledek xxxxxxxxx. Xxxxx xx xxxxxx, xxxxx byly xxxxxxxxx x&xxxx;xxxxxxxxxx xxx xxxxx, xxxx xxxxx xxxxxxxxxxx x&xxxx;xxxxxxxxxxxx xxxxxxx xx xxxx xxxxxxxxxxx xxxxxxxxx na xxxxxxx xxxxxxxxxx látku xxxx xxxxx, která je xxxxxxxxx xxxxxxx x&xxxx;xxxxxxxx.
Xxxxxx, xxxxxx studií, které xxxx xxxxxxxxx a zveřejněny xxx dříve xxxx xxxxx vycházejí z rovnocenných xxxxxxx, xxxx být xxxxxxxxx x&xxxx;xxxxxxxxxxxxxx xxxxx xxxxxxxxxxx xxxxx xxxxxxx (xxxx. xxxxxxx xxxxxxxxxxx xxxxx v souladu se xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x&xxxx;Xxxx 2004/10/XX xx xxx 11.&xxxx;xxxxx 2004 x&xxxx;xxxxxxxxxxx právních x&xxxx;xxxxxxxxx xxxxxxxx týkajících xx xxxxxxxxx zásad xxxxxxx xxxxxxxxxxx praxe x&xxxx;xxxxxxxxx xxxxxx používání xxx xxxxxxxxx chemických xxxxx&xxxx;(1) xxxx Xxxxxxxxxxx xxxxxxxxxx xxx xxxxxxxxxxx (XXX).
Xxxxx xx xxxxxx in xxxx xxxx xx xxxxx provádějí xxxx Xxxxxxxxxxxx, xxxxxxx xxxx xxxxxxxx, xx dotyčná xxxxxxxx xxxxxxxx xxxxxx xxxxxxx xxxxxxxxxxx xxxxx Xxxxxxxxxx xxx xxxxxxxxxxxx xxxxxxxxxx x&xxxx;xxxxxx (XXXX) xxxx xxxxx ISO.
Fyzikálně-chemické, xxxxxxxxxxxxx x&xxxx;xxxxxxxxxxxxxxxx vlastnosti xx xxxx podle xxxxx xxxxxxxxxxx směrnicí Xxxx 67/548/XXX xx xxx 27.&xxxx;xxxxxx 1967 x&xxxx;xxxxxxxxxx xxxxxxxx a správních xxxxxxxx xxxxxxxxxx xx xxxxxxxxxxx, xxxxxx x&xxxx;xxxxxxxxxx xxxxxxxxxxxx xxxxx&xxxx;(2), xxxxxxxxx xxxxxxxxxx směrnicí Komise 2004/73/XX&xxxx;(3), nebo xxxxxx xxxxxxxxxxxxxxx metod uznaných xxxxxxxxxxxxx xxxxxxxxx xxxxxxxxxxx. Xxxxxxx jiných xxxxx xxxx xxx xxxxxxxxxx.
Xx xxxxx xxxxxxxxxx xxxxxxxxx xxxxx xx xxxxx xxxx metod xxxxxxxxxxxxx xxxx xxxxxxxxxxxxx xxxxxxx xxxxx xxxxxxxxx x&xxxx;xxxxxx xxxxxxxxxxxxx xxxxxx xxxx xxxxxxxxxxx xxxxx xxxxxx xxxxxxxxx xxx xxxxxx xxxxxxx. Xxxx xxxxxx xxxx xxxxxxx kvalitu x&xxxx;xxxxxxxxx xxxxxxx xxxxxx xxxxxxx xxxx xxxxxx, xxxxxx mají xxxxxxxx.
Xxxxx xxxxx xxxxxxx v krmivech xxxx xx xxxx xxxx xxx v souladu x&xxxx;xxxxxxxx xxxxxxx xxxxxxxxxxx xxxxx xxxxxxxxxxx xx xxxxxxxx 2004/10/XX a/nebo xxxxx XX ISO/IEC 17025. Tyto xxxxxx xxxxxxxx xxxxxxxxxx stanoveným x&xxxx;xxxxxx&xxxx;11 nařízení Xxxxxxxxxx xxxxxxxxxx x&xxxx;Xxxx (ES) x.&xxxx;882/2004 xx xxx 29.&xxxx;xxxxx 2004 o úředních xxxxxxxxxx za xxxxxx xxxxxxx xxxxxxxxxx právních xxxxxxxx xxxxxxxxxx se xxxxx x&xxxx;xxxxxxxx x&xxxx;xxxxxxxx x&xxxx;xxxxxx xxxxxx a dobrých xxxxxxxxx podmínkách xxxxxx&xxxx;(4).
Xxxxx xxxxxxxxxxx xxxx xxxxxxxxx xxxxxxx xxxxxx x&xxxx;xxxxxxxx xxxxxxx shrnutí, aby xxxx možno dotyčnou xxxxxxxxxx látku identifikovat x&xxxx;xxxxxxxxxxxxxxx.
Xxxxx xxxxxxxxxxx xxxxxxxx xxxxx xxxxx xxxxxxxxxxxx x&xxxx;xxxxxx po xxxxxxx xxxxx xx xxx, xxxxx xx xxxxxxxx xxxxx čl. 7 xxxx.&xxxx;3 xxxx.&xxxx;x)&xxxx;xxxxxxxx (ES) č. 1831/2003, x&xxxx;xxxxx na xxxxxxxxxx xxxxx čl. 7 xxxx.&xxxx;3 xxxx.&xxxx;x)&xxxx;xxxxxxxx (ES) x.&xxxx;1831/2003.
Xxxxxxxxx xxxxxxxxxxx
Xxxx posouzení je xxxxxxxx xx xxxxxxxx, xxxxx xxxx xxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxx xxxxx ve xxxxxx x:
|
x) |
xxxxxxx xxxxxx xxx xxxxxxxxxx xxxxxxxxxxxx xxxxxxxx xxx xxxxxxxxxxx xx xxxxx xxxx vody x&xxxx;xxx násobku xxxxxx xxxxxx pro xxxxxxxxx xxxxxxx xxx bezpečnost; |
|
b) |
spotřebitelům, xxxxx požívají xxxxxxxxxxxxx xxxxxxx získané xx xxxxxx xxxxxxxxxxxxx xxxxxxxxxx xxxxx, její xxxxxxx xxxx xxxxxxxxxx. V tomto xxxxxxx xxxx xxxxxxxxxx xxxxxxxxx xxxxxxxxxx maximálních xxxxxx reziduí (MLR) x&xxxx;xxxxxxxxxx xxxx xx xxxxxxx přijatelné denní xxxxx (XXX) xxxx xxxxxxxx xxxxxxxx xxxxx (XX); |
|
x) |
xxxxxx, xxxxx budou xxxxxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxx vdechnutím nebo xxxxxxxxx xxxxxxxx, xxx xx xxxx xxx xxxxxxxxxx x&xxxx;xxxxxxxxxx xxxxxx xxxx xxxxxxx nebo xxx jejím xxxxxxxxxxxxx xx premixů xxxx xxxxxxxxxxx krmiv xxxx xxxx xx xxx xxxxxxxxx xxxxxx xxxx xxxx, xxxxx xxxxxxxx xxxxxxxx xxxxxxxxxx látku; |
|
d) |
zvířatům x&xxxx;xxxxxxx xxxxxxxx vzhledem x&xxxx;xxxxxxx x&xxxx;xxxxxxxxx xxxx xxxxxxxxxxxxx xxxx antimikrobiálním xxxxxx x |
|
x) |
xxxxxxxxx xxxxxxxxx, x&xxxx;xxxxxxx xx xxxxxxxxx xxxxxxxxxxx x&xxxx;xxxxxxxxx xxxxx xxxxxxx xxxx xxxxxxxx x&xxxx;xx odvozených, ať xx xxxxx x/xxxx xxxxxxxxxxx zvířaty. |
Pokud má xxxxxxxxx xxxxx xxxx xxxxxx, každá složka xxxx být posouzena x&xxxx;xxxxxxxx xxxxxxxxxxx xxx xxxxxxxxxxxx xxxxxxxxxx a posléze xxxxxxxxxxx x&xxxx;xxxxxxx na xxxxxxxxxxx xxxxxx (lze-li xxxxxxxx, že mezi xxxxxxxx xxxxxxxxx x&xxxx;xxxxxxxxxx xxxxxxxx). Xxxxxxxxxxxx xx xxxxx xxxxxxxx xxxxxxxxx xxxxx.
Xxxxxxxxx xxxxxxxxx
Xxxx xxxxxxxxx xx xxxxxxxx xx xxxxxxxx, xxxxx xxxx xxxxxxxx účinnost doplňkové xxxxx, xxxxx xxx x&xxxx;xxxxxx xxxxx, xxx xx xxxxxxxxx v čl. 6 xxxx.&xxxx;1 x&xxxx;xxxxxxx&xxxx;X&xxxx;xxxxxxxx (XX) x.&xxxx;1831/2003.
1.&xxxx;&xxxx;&xxxx;XXXXX&xxxx;X:&xxxx;XXXXXX XXXXXXXXXXX
1.1&xxxx;&xxxx;&xxxx;Xxxxxxx xxxxxx xxxxxxxxxxx xxxxx xx.&xxxx;7 xxxx.&xxxx;3 xxxx.&xxxx;x)&xxxx;xxxxxxxx (XX) x.&xxxx;1831/2003
Xxxxxxx xxxxxxxx xxxxxx x&xxxx;xxxxxxxx xxxxxxxx vlastností xxxxxxx xxxxxxxxx látky. Xxxxxx xxxxx xxxxxxxxx xxxxx xxxxxxx xxxxx x&xxxx;xxxx xxx tuto xxxxxxxxx:
1.1.1&xxxx;&xxxx;&xxxx;Xxxxx
|
x) |
xxxxx xxxxxxxx(x); |
|
x) |
xxxxxxxxxxxx doplňkové xxxxx; |
|
x) |
xxxxxx xxxxxx a metoda xxxxxxx; |
|
x) |
xxxxxx xxxxxxxxxxx x&xxxx;xxxxxxxxx xxxxxxxxx xxxxx; |
|
x) |
xxxxxxxxxx xxxxxxxx xxx užití a |
|
f) |
návrh xxxxx xxxxxxxxxxxx v období xx xxxxxxx xxxxx xx xxx. |
1.1.2.&xxxx;&xxxx;&xxxx;Xxxxx
|
x) |
Xxxxx a adresa xxxxxxxx(x) Xxxx údaje xxxx xxx xxxxxxxxxx ve xxxxx xxxxxxxxx nezávisle xx xxxxx xxxxxxxx xxxxxxxxx xxxxx (povolení xxxxxx xx xxxxxxxx xxxx xxxxxxxx, které xxxx xxxxxx xx xxxxxxxx). Předkládá-li xxxxxxxxxxx xxxxxxx xxxxxxxx, xxxx xxx uvedeno xxxxx xxxxxxx žadatele. |
|
b) |
Identifikace xxxxxxxxx xxxxx Xxxxxxxxxxxx xxxxxxxxx látky xxxxxxxx xxxxxxx xxxxxxxxxxxx xxxxxxxxx xxxxx xxxxxxx&xxxx;XX xxxx&xxxx;XXX podle xxxxx xxxxxxxx xxxxxxxxx látky. Xxxxxxxxx: název doplňkové xxxxx, xxxxxxxxxx zařazení xx xxxxxxxxx x&xxxx;xxxxxxx xxxxxxx, cílové druhy/kategorie xxxxxx x&xxxx;xxxxx. |
|
x) |
Xxxxxx výroby x&xxxx;xxxxxx analýzy Je xxxxx xxxxxx xxxxxxx xxxxxx. Xx xxxxx xxxxxx obecné xxxxxxx xxxxxxxxxxxx xxxxx, xxx mají xxx xxxxxxx xxx xxxxxxx xxx úřední xxxxxxxx xxxxxxxxx xxxxx jako xxxxxx, x&xxxx;xxxxxxxxx a krmivech xxxxx xxxxxxxxx této xxxxxxx x&xxxx;xxxxxxx&xxxx;XXX. Xxxxxxxxx xx na základě xxxxxxxxx předložených x&xxxx;xxxxxxx x&xxxx;xxxxx xxxxxxxx x&xxxx;xxxxxxxx&xxxx;XXX xxxxx xxxxxx xxxxxx (xxxxx) xxxxxxxxx k analýze xxx úřední kontroly xxxxxxxxxxx xxxxx nebo xxxxxx metabolitů v potravinách xxxxxxxxxxx xxxxxx. |
|
x) |
Xxxxxx xxxxxxxxxxx x&xxxx;xxxxxxxxx xxxxxxxxx xxxxx Xx xxxxx xxxxx xxxxx x&xxxx;xxxxxxxxxxx a účinnosti xxxxxxxxx xxxxx na xxxxxxx xxxxxxx provedených studií. Xxxxxxxx studií mohou xxx uvedeny v podobě xxxxxxx xx podporu xxxxxx xxxxxxxx(x). Xx xxxxxxx xx měly xxx xxxxxxx xxxxx xxxxxx xxxxxxxxxx podle xxxxxxx&xxxx;XXX. |
|
x) |
Xxxxxxxxxx xxxxxxxx xxx xxxxx Xxxxxxx(x)&xxxx;xxxxxxxx návrh xxxxxxxx xxx xxxxx. Xxxxxxx xxxxxxx xxxxxx obsah xxxxxxx ve vodě xxxx xxxxxx spolu x&xxxx;xxxxxxxxxx xxxxxxxxxx xxx xxxxx x&xxxx;xxxxxxxxxxx krmivech. Xxxxxxxx xx xxxxxx xxxxxxxxx, xxx xx xxxxxxxxx xxxx způsoby xxxxxxxx nebo zapracování xx krmiva xxxx xxxx. Je nutno xxxxxx xxxxxxxx xxxxxxxx xxxxxxxx xxx užití (xxxx. xxxxxxxxxxxxxxx), xxxxxxxx xxxxxxxxx xx xxxxxxxxxx x&xxxx;xxxxx xxxxxx, xxx xxx xx xxxxxxxxx xxxxx určena. |
|
f) |
Návrh xxxxx xxxxxxxxxxxx v období po xxxxxxx xxxxx na xxx Xxxx xxxx xx xxxxxxxx xxxxx xx xxxxxxxxx xxxxx, xxxxx xxxxx čl. 7 xxxx.&xxxx;3 xxxx.&xxxx;x)&xxxx;xxxxxxxx (ES) x.&xxxx;1831/2003 xxxxxxx do xxxxxxxxx&xxxx;x)&xxxx;xxxx&xxxx;x)&xxxx;x&xxxx;xx.&xxxx;6 xxxx.&xxxx;1 téhož xxxxxxxx, x&xxxx;xx xxxxxxxxx xxxxx, xxxxx xxxxxxx xx xxxxxxx xxxxxxxxxx xxxxx Xxxxxxxxxxxx o uvádění xx xxx produktů, které xx xxxxxxxx z geneticky xxxxxxxxxxxxxx xxxxxxxxx xxxx xxxxxxxxx xxxxxxxxxxxx xxxxxxxxx xxxxxxxx xxxx jsou x&xxxx;xxxx vyrobeny. |
1.2 Vědecké shrnutí xxxxxxxxxxx
Xx xxxxx poskytnout xxxxxxx shrnutí xxxxxxxxxx xxxxx x&xxxx;xxxxx části xxxxxxxxx poskytnutých na xxxxxxx žádosti xxxxx xxxx xxxxxxx x&xxxx;xxxxxxx&xxxx;XXX. Xxxx xxxxxxx xxxxxxxx xxxxxx vyvozené xxxxxxxxx (xxxxxxxx).
Xxxxxxx musí xxxxxxx xxxxxx xxxx xxxxxxx x&xxxx;xxxxxxx xx xxxxx xxxxxxxxxxxx částmi x&xxxx;xxxxxxx xx příslušné xxxxxx xxxxxxxxxxx.
1.3&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxxx x&xxxx;xxxxxxxxx xxxxx
Xxxxxxx xxxx xxxxx xxxxx x&xxxx;xxxxx xxxxxx xxxxxxxxxxx předložené xx xxxxxxx xxxxxxx. Xx xxxxx xxxxxxxx xxxxxxxx xxxxx s odkazem na xxxxxx x&xxxx;xxxxxx.
1.4&xxxx;&xxxx;&xxxx;Xxxxxx xxxxx xxxxxxxxxxx, x&xxxx;xxxxx xx xxx xxxxxxxxx jako x&xxxx;xxxxxxxxx xxxxx
Xxxxxx xxxxxxxx xxxxx xx xxxxxxxxx xxxxxx a strany xxxxxxxxxxx.
2.&xxxx;&xxxx;&xxxx;XXXXX&xxxx;XX: XXXXXXXX, XXXXXXXXXXXXXXX X&xxxx;XXXXXXXX XXX UŽITÍ XXXXXXXXX XXXXX; METODY XXXXXXX
Xxxxxxxxx xxxxx xxxx xxx xxxx xxxxxxxxxxxxxx x&xxxx;xxxxxxxxxxxxxxxx.
2.1&xxxx;&xxxx;&xxxx;Xxxxxxxx xxxxxxxxx xxxxx
2.1.1&xxxx;&xxxx;&xxxx;Xxxxx doplňkové xxxxx
Xxxxxxxx xx xxxxx xxxxxxxxxx obchodní xxxxx xxxxxxxxxxx xxxxx vázaných xx xxxxxxxx xxxxxxxx.
2.1.2&xxxx;&xxxx;&xxxx;Xxxxx xx zařazení
Je nutno xxxxxxxxx návrh na xxxxxxxx xxxxxxxxx xxxxx xx jedné xx xxxxxxxx xxxxxxxxx x&xxxx;xxxxxxxxx xxxxxx xxxxx xxxxxx xxxxxxxx xxxxxx v souladu x&xxxx;xxxxxxx&xxxx;6 x&xxxx;xxxxxxxx&xxxx;X&xxxx;xxxxxxxx (XX) x.&xxxx;1831/2003.
Xxxx být xxxxxxxxxx xxxxx x&xxxx;xxxxxx známých xxxxxxx xxxxxxxxxxx xxxxxxxx xxxxx xxxx xxxxxxx (xxxx. xxxxx x&xxxx;xxxxxxxxxxx, xxxxxxxx xxxx xxxxxxxxxxxx xxxxxxxxx, xxxxxxxxxxx a průmyslu). Xx xxxxx xxxxx xxxxxxxx xxxx xxxxxxxx xxxx doplňková látka xxxx xxxxxxxxxxxxx xxxxxxxx xxxxx, xxxxxxxxxxx léčivé xxxxxxxxx nebo xxxx xxxx xxxxxxxx xxxxxx xxxxx.
2.1.3&xxxx;&xxxx;&xxxx;Xxxxxxxxxxxx a kvantitativní složení (xxxxxx látka/činidlo, xxxx xxxxxx, xxxxxxxxx, xxxxxxxxxxx xxxxxxxxxxxx xxxxx)
Xx xxxxx xxxxx účinnou xxxxx(x)/xxxxxxx(x)&xxxx;x&xxxx;xxxxxxx xxxxxxx xxxxxx xxxxxxxxx xxxxx s uvedením hmotnostního xxxxxx x&xxxx;xxxxxxx produktu. Xx nutno stanovit xxxxxxxxxxxx x&xxxx;xxxxxxxxxxxxx xxxxxxxxxxx xxxxxxxxxxxx xxxxx xxxxxx xxxxx (xxxxx) / xxxxxxx (xxxxxxx).
Xxx xxxxxxxxxxxxxx: xx xxxxx xxxxxxxx xxxxx životaschopných xxxxx xxxx spor xxxxxxxxx xxxx XXX xx xxxx.
Xxx enzymy: je xxxxx xxxxxx xxxxxxx xxxxxxx (xxxxxx) xxxxxxxx x&xxxx;xxxxx jednotek xxxxxxxx x&xxxx;xxxxx xxxxxxx produktu. Xx nutno xxxxxx xxxxxx xxxxxxxx xxxxxxxx xxxxxxxx. Xxxxxx xx xxxxxxxx aktivity, pokud xxxxx xxxx μxxxx xxxxxxxx xxxxxxxx xx xxxxxx xx xxxxxxxxx, xxxxxx s uvedením pH x&xxxx;xxxxxxx.
Xx-xx účinná xxxxxx xxxxxxxxx látky xxxxx xxxxxxxx látek nebo xxxxxxx, xxxxxxx xxxxxxx xxx xxxxxxxxxxx definovat (xxxxxxxxxxxx a kvantitativně), musí xxx složky xxxxxx xxxxx (xxxxx) / xxxxxxx (xxxxxxx) xxxxxxx xxxxxxxxxx x&xxxx;xxxxxxxx podílů x&xxxx;xxxx směsi.
Ostatní xxxxx, xxxxxxx xxxxxx xxxxx xxxxxx xxxxxx xxxxxxxxx xxxxxxx a/nebo xxxx xxxxx xxxxxxx xxxxxx xxxxxxxxxxxxx, musí xxx xxxxxxxxxxxxxxxx xxxxx xxxxxx (xxxxxx) přispívajících x&xxxx;xxxx xxxxxxxx x/xxxx podle xxxxxxx xxxxxx složky (xxxxxx).
Xxxx je dotčena xxxxxxxx žádost x&xxxx;xxxxxxxxx xxxxxxxxx předložená xxxxxx xxxxx čl. 8 xxxx.&xxxx;2 xxxxxxxx (ES) č. 1831/2003, xxxxxxx může vynechat xxxxx ostatních xxxxxx, xxxxx xxxxxxxxxxxxx bezpečnostní xxxxxx, xxxxxx xxx xxxxxx xxxxx xxxx xxxxxxx v případě doplňkových xxxxx, xxxxx nejsou xxxxxxxx x&xxxx;xxxxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxxxx xxxxx, xxxxxxxxxxxxxx x&xxxx;xxxxxxxxxxxxxxx a na xxx xx xxxxxxxxxx xxxxxx xxxxxxxxxx xxxxxxxx (XX) x.&xxxx;1829/2003. Xxxxxxx xxxxxx xxxxxxx x&xxxx;xxxxxxxxxxx xxxx xxx každopádně xxxxxxxx xx xxxxxxxxx xxxxxxxxx xxxxx, xxx xxx xx xxxxxxxx xxxxxxxx, x&xxxx;xxxxx poskytovat informace x&xxxx;xxxxxx xxxxxxx xxxxxxxxx xxxxxxxxxxx. Xx možno xxxxxxx xxxxxxx identifikátor xxxxxxxx v dokumentech xxxxxxx xxxxx x&xxxx;xx xxxxx xxxxxxx xx xxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx a potvrzení, xx se identifikátor(y) vztahuje(í) na xxxxxxx, pro xxx xx xxxxxx žádost.
2.1.4 Čistota
Žadatel xxxxxxxxxxxx a vyčíslí xxxxxxxx x&xxxx;xxxxxxxxxxx xxxxxxxxx, látky x&xxxx;xxxxxxxxx xxxx xxxxxx xxxxxxxxxxx xxxxxxxxxxx, xxxxx xxxxxx xxxxxxx xxxxxxx x&xxxx;xxxxxxxxxxxx x&xxxx;xxxxxxxx xxxxxxxxx xxxxx. U produktů fermentačního xxxxxxx xxxxxxx xxxxxxx xxxxxxxxxxxx xxxxxxxxxxx xxxxxxxxx x&xxxx;xxxxxxxxx xxxxx. Xx xxxxx xxxxxx xxxxxxxx xxxxxxxxx k rutinní xxxxxxxx xxxxxxxxx xxxxx s ohledem xx xxxxxxxxxxxx látky x&xxxx;xxxxxxxxx.
Xxxxxxx xxxxxxxxxx údaje xxxx xxxxxxxx xxxxx xx xxxxxxxxxxx doplňkové xxxxx.
Xxxx xxxx xxxxxxx xxxxxxxx požadavky x&xxxx;xxxxxxxxxx xx výrobním postupu, xxxxx xxxxxxxxxx xxxxxxxxxx xxxxxxx xxxxxxxxx Xxxxxxxxxxxx.
2.1.4.1&xxxx;&xxxx;&xxxx;Xxxxxxxxx xxxxx, xxxxxxx xxxxxxxx xx xxxxxx na xxxxxxxx povolení
U doplňkových xxxxx, xxxxxxx xxxxxxxx xx xxxxxx xx držitele xxxxxxxx, je nutno xxxxx příslušné informace xxxxxxxx xx xxxxxxxxxx xxxxxxx použitého výrobcem xx xxxxxxx xxxxxxxxxxx xxxxx používaných k jiným xxxxxxxxxxxx xxxxxx. Xx xxxxx xxxxxx specifikace Xxxxxxxxxx xxxxxx xxxxxxxxx XXX/XXX xxx potravinářské xxxxxxxx látky (XXXXX) xxxx xxxxxxxxxxx x&xxxx;xxxxxxxx Xxxxxxxxxx společenství xxx xxxxxxxxxxxxx xxxxxxxx xxxxx.
2.1.4.2&xxxx;&xxxx;&xxxx;Xxxxxxxxx xxxxx, xxxxxxx xxxxxxxx xxxx xxxxxx xx xxxxxxxx povolení
U doplňkových látek, xxxxxxx xxxxxxxx není xxxxxx xx držitele xxxxxxxx, xx možno xxxxxx stávající normy xxxxxxxxx x&xxxx;xxxxx souvisejícím xxxxxx xxxx normy xx xxxxxxxxxxxxx xxx xxxxxxxxxxxxx přídatné xxxxx xxxxxxxx x&xxxx;Xxxxxxxxx xxxxxxxxxxxx xxxx XXXXX. Xxxxxx-xx xxxxxx normy dostupné xxxx je-li xx xxxxxxxx pro xxxxxxx xxxxxx, je nutno xxxxxx xxxxxxxxxxxx xxxx xxxxxxx xxxxx a stanovit xxxxxxxxxxx:
|
— |
xxx xxxxxxxxxxxxxx: xxxxxxxxxxxxxxx xxxxxxxxxxx, xxxxxxxxxx, těžké xxxx; |
|
— |
xxx produkty xxxxxxxxxxxxx xxxxxxx (které xxxxxxxxxx xxxxxxxxxxxxxx jako xxxxxx xxxxxxx): je xxxxx xxxxxxx stejné požadavky xxxx xxx produkty xxxxxxxxxxxxxx (xxx xxxx). Xx xxxxx xxxxx xxxxxx xxxxxx, x&xxxx;xxxx xx xx xxxxxxxx xxxxxxxx zapracováno xxxxxxx xxxxxxxxxx xxxxxx; |
|
— |
xxx xxxxx xxxxxxxxxxx xxxxxx: xxxxxxxxxxxxxxx x&xxxx;xxxxxxxxx xxxxxxxxxxx (xxxxxxx xxxx. xxxxxx obecný, xxxxxx xxxxxxx, xxxxx xxxxx), xxxxxxxxxx, kontaminace xxxxxxxxx, xxxxxxxxx xxxxxxx xxx rozpouštědla a popřípadě xxxxxxxxxxxxx významné látky, x&xxxx;xxxxx je známo, xx se xxxxxxxxx x&xxxx;xxxxxxx xxxxxxxx; |
|
— |
xxx xxxxx xxxxxxxxxxx xxxxxx: mikrobiologická xxxxxxxxxxx, xxxxx xxxx x&xxxx;xxxxxxxxx xxxxxxxxx xxxxxxx xxx rozpouštědla; |
|
— |
pro minerální xxxxx: těžké xxxx, xxxxxxx x&xxxx;XXX; |
|
— |
xxx xxxxxxxx xxxxxxxx xxxxxxxxx syntézou x&xxxx;xxxxxxxxxx xxxxxxx: určí xx xxxxxxx xxxxxxxx xxxxx xxxxxxx v syntetických xxxxxxxxx x&xxxx;xxxxxxxx xxxxxxxxxxxx xxxxxxxxxxx v hotovém xxxxxxxx x&xxxx;xxxxx xx xxxxxx xxxxxxxxxxx. |
Xxxxxxxxx xx xxxxxxx xxxxxxx xxxxxxxxxx pro xxxxxxx xxxxx xxxxxxx xxxxxx.
2.1.5&xxxx;&xxxx;&xxxx;Xxxxxxxxx xxxxxxxxxx xxxxxxxxxxxx xxxxx xxxxxxxx
X&xxxx;xxxxxxxxx v tuhém xxxxx se xxxxxxxxx xxxxx x&xxxx;xxxxxxxxx podle xxxxxxxxx částic, formě xxxxxx, xxxxxxx, xxxxxxxx xxxxxxx, xxxxxxxxxxxxx vlastnostech x&xxxx;xxxxxxx xxxxxxx, xxxxx xxxx vliv xx xxxxxxxxx xxxxxxxxxx. U přípravků x&xxxx;xxxxxxxx stavu xx xxxxxxxxx údaje x&xxxx;xxxxxxxxx x&xxxx;xxxxxxxxxx xxxxxx. Xxxxx xx xxxxxxxxx xxxxx xxxxxx x&xxxx;xxxxxxx ve xxxx, je xxxxx xxxxxxxx xxxxxxxxxxx xxxx xxxxxx xxxxxxxx.
2.2&xxxx;&xxxx;&xxxx;Xxxxxxxxxxxxxxx xxxxxx xxxxx (xxxxx) / xxxxxxx (xxxxxxx)
2.2.1&xxxx;&xxxx;&xxxx;Xxxxx
Xx nutno xxxxx xxxxxxxxxxxx xxxxx xxxxxx látky xxxx xxxxxxx. Xx xxxxxxxx xxxxxxx x&xxxx;xxxxx xxxxx xxxx xxxxxxx x&xxxx;xxxx xxxxxxxx charakteristiky.
2.2.1.1 Chemické xxxxx
Xxxxxxxx xxxxxx definované látky xx nutno xxxxxx xxxxxxxx názvem, chemickým xxxxxxxxx xxxxx xxxxxxxxxx XXXXX (International Xxxxx xx Pure and Xxxxxxx Xxxxxxxxx), xxxxxxx xxxxxxxxxxxxx xxxxxxxxx názvy x&xxxx;xxxxxxxxx x/xxxx číslem XXX (Xxxxxxxx Xxxxxxxx Xxxxxxx). Xx xxxxx xxxxx xxxxxxxxxxxx x&xxxx;xxxxxxxxx xxxxxx x&xxxx;xxxxxxxxxxx xxxxxxxx.
X&xxxx;xxxxxxxx xxxxxxxxxx sloučeniny použité xxxx zchutňující xxxxx xx xxxxx xxxxx xxxxx FLAVIS spolu x&xxxx;xxxxxxxxxx xxxxxxxxx xxxxxxxx. X&xxxx;xxxxxxxxxxx výtažků xx xxxxx uvést xxxxxxxxxxxx xxxxxxx.
Xxxxx, x&xxxx;xxxxx nelze xxxxxx xxxxxx xxxxxx xxxxxxxxx vzorcem a/nebo x&xxxx;xxxxx xxxxx xxxxxxx xxxxxx identifikovat, xx xxxxx charakterizovat podle xxxxxx (xxxxxx) xxxxxxxxxxxxxx x&xxxx;xxxx xxxxxxxx x/xxxx xxxxx typických xxxxxxxx xxxxxx. Xx xxxxx xxxxxxxxxxxxx xxxxxxxxxx xxxxxxxxxx, xxx xxxx možno xxxxxxxx stabilitu x&xxxx;xxxxxxxx xxxxxxxxxxxxxx.
Xxx enzymy a přípravky xxxxxx xx xxxxx xxx každou xxxxxxxx xxxxxxxx uvést xxxxx x&xxxx;xxxxxxxxxxxx xxxxx navrhovaný Xxxxxxxxxxx xxxx biochemie (XXX) v posledním xxxxxx „Xxxxxxxxxx xxxxxx“. U aktivit xxxxx xxxxxxxxxxxx se xxxxxxx xxxxxxxxxxxx xxxxx xxxxxxxxxxxx xxxxxxxxx xxxxxxxxxx XXX. Xxxxxx názvy xxxx xxxxxxxxx za xxxxxxxxxxx, xx xxxx xxxxxxxxxxx x&xxxx;xxxx xxxxxxxxx xxxxxxxxxxxx x&xxxx;xxxx xxxxxxxxxxx x&xxxx;xxx jejich xxxxx xxxxxx xx lze xxxxxxxxxxx vztáhnout xx xxxxxxxxxxxx xxxxx x&xxxx;xxxxx XXX. Xx nutno xxxxx xxxxxxxxxx xxxxx xxxxx xxxxxxxx aktivity.
Je xxxxx xxxxxx xxxxxx xxxxxxxxxxx xxxxx xxxxxxxxxx xxxxx vzniklých fermentací (xxx bod 2.2.1.2 Xxxxxxxxxxxxxx).
2.2.1.2&xxxx;&xxxx;&xxxx;Xxxxxxxxxxxxxx
Xx xxxxx xxxxx původ xxxxx xxxxxxxxxxxxxx xxxxxxxxxxx xxxx xxxxxxx xxxx xxxxxxx kmen.
U mikroorganismů používaných xxxx xxxxxxx xxxx xxxx xxxxxxx xxxx xx xxxxx xxxxx xxxxxxxx změn. Xxxxx xx xxxxx a taxonomická xxxxxxxxxxx každého mikroorganismu xxxxx xxxxxxxxxxxx zveřejněných xxxxx v mezinárodních nomenklaturních xxxxxx (XXX). Xxxxxxxxxxx xxxxx xxxx xxx xxxxxxx x&xxxx;xxxxxxxxxxx xxxxxxxx xxxxxx xxxxxx (pokud xxxxx x&xxxx;Xxxxxxxx xxxx) x&xxxx;xxxxxxxxxx xxxxxxx xxxxxx xx xxxxxxxxx dobu xxxxxxxxx doplňkové xxxxx. Xx xxxxx předložit xxxxxxxxx x&xxxx;xxxxxxx od xxxxxx, které upřesňuje xxxxxxxxx xxxxx, xxx xxxxxx je xxxx xxxxxx. Xxxx xx xxxxx xxxxxx xxxxxxx xxxxxxxxxx morfologické, fyziologické x&xxxx;xxxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxxx xxx jedinečnou xxxxxxxxxxxx xxxxx a prostředky xxxxxxxxx xxxx genetické xxxxxxxxx. X&xxxx;xxxxxxxxx modifikovaných organismů xx xxxxx xxxxx xxxxxxxxxxx změn. Xxx xxxxx xxxxxxxxx xxxxxxxxxxxx xxxxxxxxxx se uvede xxxxxxxxxxx xxxxxxxxxxxxx kód xxxxx xxxxxxxx Xxxxxx (XX) č. 65/2004 xx xxx 14.&xxxx;xxxxx 2004, xxxxxx xx xxxxxxx xxxxxx tvorby a přiřazování xxxxxxxxxxxxx xxxxxxxxxxxxxxx xxxx xxx xxxxxxxxx xxxxxxxxxxxx xxxxxxxxx.
2.2.2&xxxx;&xxxx;&xxxx;Xxxxxxxx vlastnosti
2.2.2.1 Chemické xxxxx
Xx xxxxx xxxxx xxxxx xxxxxxxxxxx x&xxxx;xxxxxxxxxx xxxxxxxxxx. Xxxxxxxxx xxxxxxxx, xXx, xxxxxxxxxxxxxxx vlastnosti, bod xxxx, bod xxxx, xxxxxxx, xxxx xxx, xxxxxxxxxxx ve xxxx x&xxxx;x&xxxx;xxxxxxxxxxx xxxxxxxxxxxxxx, Xxx x&xxxx;Xx/Xxx, xxxxxxxxxx spektrometrie x&xxxx;xxxxxxxxx xxxxxxx, xxxxx XXX, xxxxxxxx xxxxxxx x&xxxx;xxxxxxxxx xxxx xxxxxxxx xxxxxxxxx vlastnosti xxxx xxx uvedeny, xxx xx to xxxxxx.
Xxxxx xxxxxxx prostřednictvím fermentačního xxxxxxx nesmí xxxxxxxxx xxxxxxxxxxxxxxx aktivity významné xxx xxxxxxxxx xxxxxxxxxx x&xxxx;xxxxxxx xxxx xxxxxx.
2.2.2.2&xxxx;&xxxx;&xxxx;Xxxxxxxxxxxxxx
|
— |
Xxxxxx x&xxxx;xxxxxxx xxxxxxxxx Xx nutno xxxxxxxx xxxxxxxxxxx xxxxxx xxxx xxxxxxx xxxxxxxxx xxxx xxxxxx nevýznamnost. Xxxxx xxxxxxxx náležející xx taxonomické xxxxxxx, xxxxx xxxxxxxx xxxxxxxxxxx, x&xxxx;xxxxx xx xxxxx, xx xxxxx xxxxxxxxxx xxxxxx xxxx jiné xxxxxxx xxxxxxxxx, xx xxxxx podrobit xxxxxxxxxxxxx xxxxxx x&xxxx;xxxxx xxxxxxxx xx molekulové x&xxxx;xxxxxxxxx xxxxxxx xxxxxx, xx xxxxxxxxxx xxxxx x&xxxx;xxxxxx. X&xxxx;xxxxx xxxxxxxxxxxxxx, pro xxx xxxxxx x&xxxx;xxxxxxxxx xxxxx x&xxxx;xxxxxxx bezpečném používání x&xxxx;xxxxxxx xxxxxxxx není xxxxx dostatečně xxxxx, xx xxxxxxxx xxxx xxxxxxx toxikologických xxxxxx. |
|
— |
Xxxxxxxx xxxxxxxxxx x&xxxx;xxxxxxxxxx xxxx xxxxxxxxxxxx Xxxxxxxxxxxxxx xxxxxxxxx xxxx xxxxxxxxx látky xxxx xxxx xxxxxxx kmen xxxxx vykazovat xxxxxxxxxxxxx xxxxxxxx xxxx xxxxx xxx schopny produkovat xxxxxxxxxxxx xxxxx, které xxxx xxxxxxxx jako xxxxxxxxxxx u člověka a zvířat. Kmeny xxxxxxxxxxxxxx xxxxxx x&xxxx;xxxxxxx xxxx xxxxxxxxx látky xxxxx xxxx xxxxxxxxx x&xxxx;xxxxxx xxxx xxxxxxxxxx xxxx xxxxxxxxxxxx, které xx xxx xxxxxxxxx x&xxxx;xxxxxxx xxxxx xxxxxx x&xxxx;x&xxxx;xxxxxxxx prostředí. Xxxxxxx xxxxx bakterií xx xxxxx xxxxx otestovat xx xxxxxxxxxx vůči xxxxxxxxxxxx xxxxxxxxxx x&xxxx;xxxxxxxx x&xxxx;xxxxxxxxxxxx xxxxxxxxx. Xx-xx xxxxxxxx xxxxxxxxxx, xx xxxxx xxxxxxx genetický xxxxxx rezistence x&xxxx;xxxxxxxxxxxxxxx xxxxxxx xxxxxxxxxx xx xxxxxxx xxxxxxxxx xx xxxxxxxx. Xxxxx xxxxxxxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxxxxxxxx xxxxxxxxxx xx nesmí používat xxxx xxxxxxxxx xxxxx, xxxxx-xx prokázat, že xxxxxxxxxx xx xxxxxxxxx xxxxxxxxxxxx mutace(í) a není přenosná. |
2.3 Výrobní xxxxxx, xxxxxx xxxxxxxxxx xxxxxxxxx postupů
Ke stanovení xxxxxxxxxx xxxx xxxxxxx, xxxxx xxxxx xxx xxxx xx xxxxxxx xxxxxx látky / xxxxxxx (činidel) xxxx xxxxxxxxx xxxxx, xx xxxxx popis výrobního xxxxxxx. Xx nutno xxxxxxxxx xxxxx x&xxxx;xxxxx x&xxxx;xxxxxxxxxxx xxxxxxxxx u chemických xxxxx xxxxxxxxxxx ve xxxxxxxx xxxxxxx.
2.3.1&xxxx;&xxxx;&xxxx;Xxxxxx xxxxx(x) / xxxxxxx(x)
Xx xxxxx xxxxxxxxxx xxxxx výrobního xxxxxxx (xxxx. xxxxxxxx xxxxxxx, xxxxxxxxxx, kultivace, xxxxxxxx x&xxxx;xxxxxxxxxxx xxxxxxxxx xxxx xxxxxxxxx) použitého xxx přípravě xxxxxx xxxxx (xxxxx) / xxxxxxx (xxxxxxx) xxxxxxxxx xxxxx, xxxxxxxx prostřednictvím xxxxxxxxxxx diagramu. Xxxxx xx xxxxxxx xxxxxxxxxxxxx/xxxxxxxxxxxx xxxxx. Je xxxxx xxxxxx xxxxxxxx xxxxxx xxxxxxx.
X&xxxx;xxxxxxxxx xxxxxxxxxxxxxx mikroorganismů (XXX) používaných xxxx xxxxx xxxxxxxxxxx xxxxx x&xxxx;xxxxxxxxxxxxx za xxxxxxxx xxxxxxxxxx xxxxxxxxx xx xxxxxxx xxxxxxxx Xxxx 90/219/XX&xxxx;(5). Xx xxxxx xxxxx popis fermentačních xxxxxxx (xxxxxx pro xxxxxxx, xxxxxxxxxxx podmínky x&xxxx;xxxxxxxx xxxxxxxxxx produktů xxxxxxxxxxxxx procesu).
2.3.2 Doplňková látka
Předloží xx xxxxxxxx popis xxxxxxxxx xxxxxxx doplňkové xxxxx. Xx nutno xxxxx xxxxxx xxxxxx xxxxxx doplňkové xxxxx, xxxxxx xxxx (xxxxx) xxxxxxxxxxx xxxxxx xxxxx (xxxxx) / xxxxxxx (xxxxxxx) x&xxxx;xxxxxx složek x&xxxx;xxxxxxx následné xxxxxx xxxxxxxxxx, xxxxx xxxx xxxx na xxxxxxxx xxxxxxxxx xxxxx, xxxxxxxx xxxxxxxxxxxxxxx xxxxxxxxxxx diagramu.
2.4 Fyzikálně-chemické x&xxxx;xxxxxxxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxx
2.4.1&xxxx;&xxxx;&xxxx;Xxxxxxxxx
Xxxxxxxxx xx obvykle xxxxxx xxxxxxxxxxx xxxxxxxxxx xxxxxx látky (xxxxx) / činidla (xxxxxxx) xxxx její (xxxx) xxxxxxxx/xxxxxxxxxxxxxxxx. U enzymů xxx xxxxxxxxx xxxxxxxxx x&xxxx;xxxxxxx xx xxxxxx xxxxxxxxxxx xxxxxxxx; x&xxxx;xxxxxxxxxxxxxx x&xxxx;xxxxxxx xx xxxxxx xxxxxxxxxxxxxxxx; x&xxxx;xxxxxxxxxxxxx xxxxx s ohledem xx xxxxxx xxxxx. X&xxxx;xxxxxxxxx chemických xxxxx/xxxxxxxx xxx xxxxxxxxx xxxxxxxxx xxxxxxxxxx koncentrace xxxxx xxxx několika vhodných xxxxxxxxxxxxxx xxxxx.
Xxxxxxxxx xxxxxxxxx xxxxx
Xx nutno xxxxxxxxxx xxxxxxxxx každého xxxxxxx xxxxxxxxx xxxxx xxx xxxxxxxx podmínek xxxxxxxx xxxxxxxxx (světlo, teplota, xX, xxxxxxx, xxxxxx x&xxxx;xxxxxxx xxxxxxxxx). Xxxxxxxxxxxxx xxxxxxxxxxx xxxxxxxxx látky x&xxxx;xxxxxxxxxxxxxx formě by xxxx xxx xxxxxxxx xx nejméně xxxx xxxxxxxxxx situacích xxxxxxxxxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxx xxx xxxxx (xxxx. 25&xxxx;xX, 60&xxxx;% xxxxxxxxx xxxxxxx xxxxxxx x&xxxx;40&xxxx;xX, 75&xxxx;% relativní vlhkost xxxxxxx).
Xxxxxxxxx doplňkové xxxxx xxxxx v premixech a krmivech
U doplňkových xxxxx užitých x&xxxx;xxxxxxxxx x&xxxx;xxxxxxxx s výjimkou xxxxxxxxxxxxx xxxxxx xx xxxxxxxxx xxxxxxx xxxxxxx doplňkové xxxxx ověří za xxxxxxx výrobních x&xxxx;xxxxxxxxxxxx xxxxxxxx xxxxxxx x&xxxx;xxxxx. Xxxxxx stability xxxxxxx xxxx xxxxx xxxxxxx xxxx měsíců. Stabilita xx testuje pokud xxxxx x&xxxx;xxxxxxx obsahujících xxxxxxx prvky; x&xxxx;xxxxxxx xxxxxxx xx doplňková xxxxx xxxx xxx xxxxxxxx nápisem „xxxxxxxx xx xxxxxxxxx prvky“.
Studie xxxxxxxxx u krmiv xxxxxx xxxxxxxx xxxxxxx tři xxxxxx. Obvykle xx xxxxxxxxx xxxxxxxxxx x&xxxx;xxxxx xx formě kaše x&xxxx;xxxxxxxxxxxx xxxxx (xxxxxx xxxxx peletování xxxx xxxxxx xxxxx xxxxxx) xxx xxxxxx xxxxxxx xxxxx xxxxxx.
X&xxxx;xxxxxxxxxxx xxxxx xxxxxxxx k použití xx xxxx xx nutno xxxxxxxxx každého složení xxxxxxxxx xxxxx xxxxxx xx xxxx za xxxxxxxx xxxxxxxxxxxx xxxxxxx x&xxxx;xxxxx.
Xxxxx-xx xx ztrátě xxxxxxxxx a ve xxxxxxxx xxxxxxxxx xx xxxxx xxxxxxxxxxxxxxx xxxxxxxx produkty xxxxxxxxx nebo xxxxxxxx.
Xx xxxxx poskytnout údaje x&xxxx;xxxxxx, které xxxxxxxx xxxxxxx xxxxx pozorování xx xxxxxxx x&xxxx;xxxxx xx xxxxx xxxx xxxxxxxxxx.
X&xxxx;xxxxxxx potřeby xxxxxx xxxxxxxx xxxxxxxx kvantitativní x&xxxx;xxxxxxxxxxxx xxxxxxx xxxxxxx xxxx xxxxx xxxxxxxxx xxx xxxxxxx.
2.4.2&xxxx;&xxxx;&xxxx;Xxxxxxxxxx
Xx xxxxx xxxxxxxx schopnost homogenního xxxxxxxxx xxxxxxxxx látky (xxxxx zchutňujících xxxxxx) x&xxxx;xxxxxxxxx, xxxxxxxx xxxx xx xxxx.
2.4.3&xxxx;&xxxx;&xxxx;Xxxxxxx xxxxxxxxxx
Xx xxxxx xxxxxx xxxxxxx xxxxxxxxxx, například xxxxxxxxxxx x&xxxx;xxxxxxxxxxxxxxx xxxxxxxxxx xxxx xxxxxxxxx disperze v kapalinách.
2.4.4 Fyzikálně-chemické xxxxxxxxxxxxxxx xxxx xxxxxxxxx
Xx xxxxx uvést xxxxxxxxx-xxxxxxxx xxxxxxxxxxxxxxx nebo xxxxxxxxx, x&xxxx;xxxx xx xxxxx xxxxx xx xxxxx x&xxxx;xxxxxx, xxxxxx, xxxxxx xxxxxxxxxx doplňkovými látkami xxxx xxxxxxxx přípravky.
2.5 Podmínky xxx xxxxx doplňkové xxxxx
2.5.1&xxxx;&xxxx;&xxxx;Xxxxxxxxxx způsob xxxxxxx xx xxxxxx xxxxxx
Xx xxxxx xxxxx xxxx xxxx xxxxxxxxx xxxxxx, xxxxxxx xxxxxxx xxxx xxxxxxxxx stadium xxxxxx x&xxxx;xxxxxxx s kategoriemi x&xxxx;xxxxxxx&xxxx;XX xxxxxx xxxxxxxx. Xx xxxxx xxxxxx xxxxx xxxxxxxxxxxxxx. Uvede se xxxxxxxxxx xxxxxxx v krmivu xxxx xx xxxx.
Xx xxxxx uvést xxxxxxxxxx xxxxxx podávání a zapracování xxx xxxxxxx, krmiva xxxx xxxxxx vodu. Xxxxx xx navrhovaná xxxxx v kompletním krmivu x&xxxx;xxxxxxxxxx xxxx xxxxxxxx x&xxxx;xxxxxxxxx navrhovaná xxxxxxxx xxxxx. Pokud se xxxxxxxx konkrétní xxxxxxx xxxxxxxxx xxxxx v doplňkovém xxxxxx, je nutné xxxxxxxxxx.
2.5.2&xxxx;&xxxx;&xxxx;Xxxxxxxxx xxxxxxxxxxx s bezpečností xxx uživatele/pracovníky
2.5.2.1 Chemické xxxxx
Xx xxxxx poskytnout listy x&xxxx;xxxxx x&xxxx;xxxxxxxxxxx xxxxxxxxx xx formátu xxxxxxxxxxxxx xxxxxxxxxx směrnice Xxxxxx 91/155/XXX xx xxx 5.&xxxx;xxxxxx 1991, xxxxxx xx x&xxxx;xxxxxxxxx článku 10 xxxxxxxx 88/379/XXX xxxxxxxx x&xxxx;xxxxxxx xxxxxxxx xxxxxxxx x&xxxx;xxxxxxx xxxxxxxxxxxx xxxxxxxxx xxx xxxxxxxxxx xxxxxxxxx&xxxx;(6). X&xxxx;xxxxxxx xxxxxxx je xxxxx xxxxxxxxx xxxxxxxx xxx xxxxxxxxxxx xxxxxxxxx xxxxxxx x&xxxx;xxxxxxxx prostředky xxx xxxxxx, xxxxxxxxxx, xxxxx a likvidaci.
2.5.2.2 Mikroorganismy
Je xxxxx xxxxx klasifikaci podle xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x&xxxx;Xxxx 2000/54/XX ze xxx 18.&xxxx;xxxx 2000 x&xxxx;xxxxxxx xxxxxxxxxxx xxxx xxxxxx xxxxxxxxx x&xxxx;xxxxxxxx xxxxxxxxxxx xxxxxxxxx při xxxxx (sedmá xxxxxxxxxx xxxxxxxx ve smyslu xx.&xxxx;16 xxxx.&xxxx;1 směrnice 89/391/EHS) (7). X&xxxx;xxxxxxx xxxxxxxxxxxxxx xxxxxxxxxxxx xx xxxxxxx&xxxx;1 této xxxxxxxx xx xxxxx xxxxxxxxxx xxxxxxxxxxxxx informace, xxxxx jim umožní xxxxxxxx příslušná xxxxxxxx xx xxxxxxx pracovníků, xxx xx stanoveno x&xxxx;xx.&xxxx;3 xxxx.&xxxx;2 xxxxxxx xxxxxxxx.
2.5.2.3&xxxx;&xxxx;&xxxx;Xxxxxxxxx xx xxxxxxxxxx
Xxxx xxxx dotčena ustanovení x&xxxx;xxxxxxxxxx a balení xxxxxxxx x&xxxx;xxxxxx&xxxx;16 xxxxxxxx (XX) x.&xxxx;1831/2003, xx nutno xxxxx xxxxxxxx xxxxxxxxx xx označování x&xxxx;xxxxxxxxx xxxxxxxx podmínky pro xxxxx a manipulaci (xxxxxx xxxxxxx xxxxxxxxxxxxxxx x&xxxx;xxxxxxxxxxxxxx) x&xxxx;xxxxxx xxx správné xxxxxxx.
2.6&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxx x&xxxx;xxxxxxxxxx xxxxxx
Xxxxxx xxxxxxx xx xxxxxx xx standardní xxxxxx xxxxx xxxxxxxxxx xxxxx ISO (tj. XXX 78-2).
Xxxxx xxxxxxxx (XX) x.&xxxx;1831/2003 x&xxxx;xxxxxxxx (XX) x.&xxxx;378/2005 xxxxxx xxxxxxx uvedené x&xxxx;xxxxx xxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxx Společenství. Xxxxxxxxxx xxxxxxxxx Společenství předloží xxxxx xxxxxxxxx xxxxxx, x&xxxx;xxx se xxxxx, xxx xxxx xxxx xxxxxx xxxxxx xxx xxxxxxx za xxxxxx xxxxxxxx kontrol xxxxxxxxx xxxxx, na niž xx xxxxxx xxxxxxxx. Xxxxxxxxx xxxxxxxxxx xxxxxxxxxx Xxxxxxxxxxxx xx zaměří xx metody stanovené x&xxxx;xxxxxx&xxxx;2.6.1 x&xxxx;2.6.2.
Xxxxx xxx xxxxxxxx MLR xxx xxxxx, xx xxx xx vztahuje xxxxxxxx Xxxx (XXX) č. 2377/90 xx xxx 26.&xxxx;xxxxxx 1990, xxxxxx se xxxxxxx xxxxxx Xxxxxxxxxxxx xxx xxxxxxxxx xxxxxxxxxxx xxxxxx reziduí xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx v potravinách xxxxxxxxxxx xxxxxx&xxxx;(8), xxxxxx xxx&xxxx;2.6.2 předmětem xxxxxxxxx xxxxxxxxxx laboratoře Xxxxxxxxxxxx. Xxxxxxx xxxxxxx xxx&xxxx;2.6.2 xxxxxxxxxx xxxxxxx metodu, xxxxxxxxx x&xxxx;xxxxx (xxxxxx xxxxxxxxxxx xxxxxxxxxxx), jež xxxx xxx xxxxxxxxxx Xxxxxxxx agentuře xxx xxxxxx xxxxxxxxx (XXXX) x&xxxx;xxxxxxx x&xxxx;xxxxxxxx&xxxx;X&xxxx;xxxxxxxx (XXX) x.&xxxx;2377/90 x&xxxx;xxxxx dokumentu „Xxxxxx xx Applicants xxx Xxxxxxxxxx“, xxxxxx&xxxx;8 „Xxxxx xxxxxxxxx xxxxxxxxx xxxxxxxx in xxx Xxxxxxxx Union“.
V hodnocení xxxxx xxx xxxxxxxx rovněž xxxxxxxxxx xxxxxx xxxxxxx x&xxxx;xxxx&xxxx;2.6.3, xxxxx to xxxxxxxxxx laboratoř Xxxxxxxxxxxx, xxxx xxxx Xxxxxx xxxxxxxx xx xxxxxxxx.
X&xxxx;xxxxxxx x&xxxx;xxxxxxxxx (ES) x.&xxxx;378/2005 xxxxxxx poskytne xxxxxxxxxx xxxxxx přímo xxxxxxxxxx xxxxxxxxxx Xxxxxxxxxxxx před xxxxxxxxxxxx xxxxxxxxx dokumentace x&xxxx;xxxxxxxx vzorky xxxx xxxxxxxxx xxxx použitelnosti.
Žadatelé xxxxxx xx xxxxxxxx xxxxxx xxxxxxxxx referenční xxxxxxxxxx Xxxxxxxxxxxx x&xxxx;xxxxxxx x&xxxx;xxxxxxx&xxxx;12 xxxxxxxx (XX) x.&xxxx;378/2005.
2.6.1&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxx xxx xxxxxxx xxxxx
Xx nutno xxxxxxxxxx xxxxxxxxx charakteristiku xxxxxxxxxxxx x&xxxx;xxxxxxxxx xxxxxxxxxxxxx xxxxxxxxxx metody (xxxxx) xxx xxxxxxxx, xxx xxxx xxxxxxxx xxxxxxxxx xxxx minimální xxxxxxxxxx xxxxxx účinné látky (xxxxx) / činidla (xxxxxxx) x&xxxx;xxxxxxxxx xxxxx, xxxxxxxxx, krmivech x&xxxx;xxxxxxxxx xxxx.
|
2.6.1.1 |
Xxxx xxxxxx xxxxxxx xxxxxx xxxxxxxxx xxxx x&xxxx;xxxxxxx metod analýzy xxxxxxxxxxx xxx xxxxxx xxxxxxxx xxxxx xxxxxx&xxxx;11 xxxxxxxx (XX) x.&xxxx;882/2004. Xxxxxxx splňují xxxxxxx xxxxx x&xxxx;xxxxxx xxxxxxxxx:
|
|
2.6.1.2 |
Xxxxxxxx xxxxxxxxxxxxxxx xxxxxx (metod) zahrnuje xxxxxxxxxxxx charakteristiky xxxxxxxxx x&xxxx;xxxxxxx&xxxx;XXX xxxxxxxx (XX) x.&xxxx;882/2004. |
|
2.6.1.3 |
Xxxxxxxx xxxxxxxxxxxxxxx xxxxx xxxxxxxxxxxx interně xx xxxxx otestováním xxxxxx x&xxxx;xxxxx xxxxxxxxxxxx x&xxxx;xxxxxxxxx xxxxxxxxxx. Xxxxxxxxx xx xxxxxxxx xxxxxx xxxxx xxxxx x&xxxx;xxxxxxxxxx dalšími xxxxxxxxxxx xxxxxxxxxxxxx xxxxxxxxxxxxxx xxxxxx xx xxxxxx xxxxxxxxx xxxxxxxxx. Z důvodu xxxxxxxxxxxx a účasti xx xxxxxxxxx xxxxxxxxxxx poskytnuté xxxxxxxxx x&xxxx;xxxxxxx, že xxxxx laboratoř je xxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxxxxxx xxxxxxxxxx napomáhajících xxxxxxxxxx xxxxxxxxxx Společenství, xxx xx xxxxxxxxx x&xxxx;xxxxxxxx (XX) č. 378/2005, xxxxxxx xxxxxxxxx xxxxx xxxxxxxxxx xxxxxxxxxx Společenství xxxxxxxxxx x&xxxx;xxxxxxx (xxxxxxx xxxxxxxxxx xxxxxxxxx Xxxxxxxxxxxx xxxxxx žádost) xxxxxxxxxx xxxxx xxxxxxxxxx x&xxxx;xxxxxxxxxxx x&xxxx;xxxxx žádostí x&xxxx;xxxxx xx xxxxxxxx vyhodnocení xxxxxxx. |
|
2.6.1.4 |
Xx xxx xxxxxxxxx xxxxxx xxx xxxx xxxx xxxxxxxxxx xxxxxxxxx Xxxxxxxxxxxx xxxxxx xxxxxx xxxxxxxxxxxxxxx xxxxx přílohy III xxxxxxxx (ES) x.&xxxx;882/2004. |
|
2.6.1.5 |
Xxxxxxxx xxxxxxxxxxxxxxx xxx metody xxxxxxxxxx xxxxxx xxxxx (xxxxxxxxx xxxxxx) xxxxx xxx xxxxxxxxx x&xxxx;xxxxxxxxxx xxxxxxxx poskytnutých xxxxxxxxxx xxxxxxxxxx Xxxxxxxxxxxx xxxxx xxxxxx&xxxx;12 xxxxxxxx (XX) x.&xxxx;378/2005. |
2.6.2&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxx pro xxxxxxxxx xxxxxxx xxxxxxxxx xxxxx xxxx xxxxxx xxxxxxxxxx x&xxxx;xxxxxxxxxxx
Xx xxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxxxxxxxxx xxxxxxxxxxxxxx x&xxxx;xxxxxxxxxxxxxxx analytických xxxxx pro stanovení xxxxxxxxxxxxxx reziduí a/nebo xxxxxxxxxx xxxxxxxxx xxxxx x&xxxx;xxxxxxxx tkáních x&xxxx;xxxxxxxxxxx xxxxxxxxxx.
|
2.6.2.1 |
Xxxx metody splňují xxxxxx požadavky xxxx x&xxxx;xxxxxxx xxxxx xxxxxxx xxxxxxxxxxx xxx xxxxxx xxxxxxxx podle článku 11 xxxxxxxx (ES) x.&xxxx;882/2004. Xxxx xxxxxx splňují xxxxxxx xxxxxxx jeden x&xxxx;xxxxxxxxx xxxxxxxxx v bodě 2.6.1.1. |
|
2.6.2.2 |
Xxxxxxxx charakteristika metody (xxxxx) zahrnuje xxxxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxxxx x&xxxx;xxxxxxx&xxxx;XXX xxxxxxxx (XX) č. 882/2004 x&xxxx;xxxx x&xxxx;xxxxx xxxxxxxxx xxxxxxxxx v rozhodnutí Xxxxxx 2002/657/XX&xxxx;(10). Popřípadě xx xxxxx stejné xxxxxxxx xxxxxxxxxxxxxxx stanovené x&xxxx;xxxxxxxxxxxx Xxxxxx, xxxxx xxxxxxx xxxxxxxxxx xxxxxx xxxxxxxxx x&xxxx;xxxxxxxxxx xxxxxxxx xxxxx x&xxxx;xxxxxx reziduí x&xxxx;xxxxxx xxxxxxxxx xxxxx xxxxxxxx Xxxx 96/23/XX. Xxxxx kvantifikace x&xxxx;xxxxx xxxxxx xxxxx xxxxxxxxx xxxxxxxx xxxxxxxxxxxxxx XXX x&xxxx;xxxx xxx xxxxxxxxx v rozmezí přinejmenším xx xxxxx xxxxxxxx xx dvojnásobek XXX. |
|
2.6.2.3 |
Xxxxxxxx xxxxxxxxxxxxxxx xxxxxxx xxxxxxxxxxxx xxxxx xx xxxxx xxxxxxxxxxx metody x&xxxx;xxxxx xxxxxxxxxxxx x&xxxx;xxxxxxxxx xxxxxxxxxx. Xx nutno xxxxx xxxxxxxx těchto testů. X&xxxx;xxxxxx nezávislosti a účasti xx xxxxxxxxx dokumentace xxxxxxxxxx žadatelem x&xxxx;xxxxxxx, xx xxxxx xxxxxxxxx xx xxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxxxxxx xxxxxxxxxx xxxxxxxxxxxxxx referenční laboratoři Xxxxxxxxxxxx, jak xx xxxxxxxxx x&xxxx;xxxxxxxx (ES) x.&xxxx;378/2005, xxxxxxx xxxxxxxxx xxxxx xxxxxxxxxx xxxxxxxxxx Xxxxxxxxxxxx prohlášení x&xxxx;xxxxxxx (xxxxxxx xxxxxxxxxx laboratoř Xxxxxxxxxxxx xxxxxx xxxxxx) xxxxxxxxxx práci laboratoře x&xxxx;xxxxxxxxxxx x&xxxx;xxxxx xxxxxxx x&xxxx;xxxxx xx xxxxxxxx xxxxxxxxxxx xxxxxxx. |
|
2.6.2.4 |
Xx své xxxxxxxxx zprávě xxx xxxx může referenční xxxxxxxxx Společenství xxxxxx xxxxxx xxxxxxxxxxxxxxx z charakteristik xxxxxxxxx x&xxxx;xxxx&xxxx;2.6.2.2. |
|
2.6.2.5 |
Xxxxxxxx xxxxxxxxxxxxxxx xxx metody xxx xxxxxxxx skupiny látek (xxxxxxxxx xxxxxx) xxxxx xxx stanoveny x&xxxx;xxxxxxxxxx xxxxxxxx xxxxxxxxxxxx xxxxxxxxxx xxxxxxxxxx Xxxxxxxxxxxx xxxxx xxxxxx&xxxx;12 nařízení (XX) x.&xxxx;378/2005. |
2.6.3&xxxx;&xxxx;&xxxx;Xxxxxx analýzy xxxxxxxx xx xxxxxxxx a charakteristika xxxxxxxxx xxxxx
Xxxxxxx poskytne xxxxx metod použitých xx stanovení xxxxxxxxxxxxxx xxxxx xxxx&xxxx;2.1.3, 2.1.4, 2.1.5, 2.2.2, 2.4.1, 2.4.2, 2.4.3 x&xxxx;2.4.4.
X&xxxx;xxxxxxx x&xxxx;xxxxxxxx&xxxx;XX xxxxxxxx (ES) x.&xxxx;1831/2003 xx znění xxxxxxxx (XX) x.&xxxx;378/2005 xxxxx xxx vyhodnoceny xxxxxx metody poskytnuté xxxxx xxxxxx xxxx, xxxxx to xxxx xxxx Xxxxxx xxxxxxxx xx důležité pro xxxxxxxxx xxxxxxx.
Xxxxxxxxxx xx, xxx xxxxxx xxxxxxx x&xxxx;xxxxx bodě byly xxxxxxxxxxx uznané. Xxxxxx, xxxxx nejsou mezinárodně xxxxxx, je xxxxx xxxx popsat. V těchto xxxxxxxxx xxxx být xxxxxx provedeny akreditovanými x&xxxx;xxxxxxxxxxx laboratořemi a musí xxx xxxxxxxxxxxxxx xxxxx xxxxxxxxxxx xxxxx xxxxxxx (xxxx. xxxxxxx xxxxxxxxxxx xxxxx podle směrnice 2004/10/XX nebo normy XXX).
Xxxxxx xxx identifikaci x&xxxx;xxxxxxxxxxxxxxx doplňkové látky xxxxxxx xxxxxx xxxxxxxxx xxxx metody xxxxxxx xxxxxxxxx xxx xxxxxx xxxxxxxx xxxxx xxxxxx&xxxx;11 xxxxxxxx (XX) x.&xxxx;882/2004, xxxxxxx xxxxx xxxx xxxxxxxxx xxxxxx xxxxxxxxx (xxxx. xxxxxxxxx, nežádoucí xxxxx).
3.&xxxx;&xxxx;&xxxx;XXXXX&xxxx;XXX: STUDIE XXXXXXXX XX XXXXXXXXXXX DOPLŇKOVÉ XXXXX
Xxxxxx xxxxxxx x&xxxx;xxxxx xxxxxx x&xxxx;xx xxxxxxxxxx xxxxxxxxx xxxx umožnit xxxxxxxxxxx:
|
— |
xxxxxxxxxxx xxxxxxx xxxxxxxxx xxxxx xxx xxxxxx xxxxx xxxxxx, |
|
— |
xxxxxxxxxx xxxxxx xxxxxxxxxxxxx xx selekcí x/xxxx xxxxxxxx xxxxxxxxxx xxxx xxxxxxxxxxxxxxxx xxxxxx x&xxxx;xxxxx xxxxxxxxxxx a uvolňováním xxxxxxxxxxxxxx, |
|
— |
xxxxx xxx spotřebitele x&xxxx;xxxxxxxx xxxxxxxxx ze xxxxxx, xxxx xxxx xxxxxxxx krmiva xxxxxxxxxx xxxxxxxxxx látku xxxx xxxxxx ošetřená xxxxxxxxxx xxxxxx, xxxx xxxxx, xxxxx xxxxx xxxxxxxx x&xxxx;xxxxxxxxx potravin xxxxxxxxxxxx xxxxxxx xxxxxxxxx xxxxx xxxx xxxxxx xxxxxxxxxx, |
|
— |
xxxxx xxx osoby xxxxxxxxxxxx x&xxxx;xxxxxxxxxx xxxxxx xxxx xxxxxxx xxxx xxxxxxxxxxxx xx xxxxxxx či xxxxx, xxxxxxxxxxxx při xxxxx xxxxxxxxxx či xxxxxxxx xxxxxxxx, xxx xxxx xxxx x |
|
— |
xxxxx xxxxxxxxxxx xxxxxx xxxxxxx xxxxxxxxx xxxxx nebo xxxxxxxx z ní xxxxxxxxxx, xxxxxxxxxx xxxxx a/nebo xxxxxxxxxxxx zvířaty, xx xxxxxxx xxxxxxxxx. |
3.1&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxx xx xxxxxxxxxxx používání xxxxxxxxx xxxxx xxx xxxxxx xxxxx xxxxxx
Xxxxxx xxxxxxx v tomto xxxxxx xxxx určeny k vyhodnocení:
|
— |
bezpečnosti xxxxxxxxx xxxxxxxxx látky xxx xxxxxx druhy xxxxxx x |
|
— |
xxxxxxxxxx rizika xxxxxxxxxxxxx se selekcí x/xxxx xxxxxxxx xxxxxxxxxx xxxx xxxxxxxxxxxxxxxx xxxxxx x&xxxx;xxxxx perzistencí x&xxxx;xxxxxxxxxxx xxxxxxxxxxxxxx. |
3.1.1&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxxx x&xxxx;xxxxxxxx xxxxx zvířat
Účelem xxxxx xxxxxxxxx je xxxxxxxxxx xxxxxxx vyhodnocení xxxxxxxxxx xxxxxxxx doplňkové xxxxx x&xxxx;xxxxxxxx xxxxxx. Používá xx rovněž xx xxxxxxxxx xxxxxxx xxx xxxxxxxxxx, xxxxx xx xxxxxxxxx xxxxx xxxxxx x&xxxx;xxxxxxx xxxxxxx, xxx xx xxxxxxxxxx. Xxxx xxxxx xxxxxxxxx xx xxxxx xxxxxxx k doložení xxxxxxxxxxx xxx všechny xxxxxx druhy/kategorie xxxxxx, xx xxx xx xxxxxx xxxxxxxx. X&xxxx;xxxxxxxxx xxxxxxxxx je přípustné xxxxxxxx xxxxxxx prvky xxxxx xxxxxxxxx xx xxxxx xx xxxxxxx xxxxxxxxx, xxxxx jsou xxxxxxx níže xxxxxxx xxxxxxxxx xx xxxx xxxxx. Všechny xxxxxx xxxxxxx x&xxxx;xxxxx oddíle xxxx být xxxxxxxx xx doplňkové xxxxx xxxxxxx v oddíle II.
3.1.1.1 Návrh xxxxx xxxxxxxxx xxxxxxxx nejméně xxx skupiny:
|
— |
skupinu, xxx xx doplňková látka xxxxxxxx, |
|
— |
xxxxxxx s nejvyšší xxxxxxxxxxx xxxxxx a |
|
— |
pokusnou xxxxxxx x&xxxx;xxxxxxxxxxxxx xxxxxxx xxxxxxxx xxxxxxxxxx xxxxx. |
X&xxxx;xxxxxxx xxxxxxx xx xxxxxxxxx látka xxxxxxx xxxxxx ve xxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxxxx xxxxx. Pokusná xxxxxxx xxxx rutinně xxxxxxxxx x&xxxx;xxxxxxx na xxxxxxxx xxxxxx klinických xxxxxx, pracovní xxxxxxxxxxxxxxx, xxxxxxxxx xxxxxx xxxxxxxx, xxxxxxxxxxx x&xxxx;xxxxxxx xxxxxxxxx xxxxxxxxxx složení xxxx x&xxxx;xxxx parametry, xxxxx xxxxxxxxxxxxx xxxxxxxxx s biologickými xxxxxxxxxxx doplňkové xxxxx. Xxxxxx xx do xxxxx xxxxxxxx xxxxxxxxx xxxxx x&xxxx;xxxxxxxxxxxxxxx studií x&xxxx;xxxxxxxxxxxxx xxxxxx. X&xxxx;xxxxx xxxxxx xx uvedou xxxxxx xxxxxxxx xxxxxxxxx xxxxxx xxxxxxxx během xxxxxxx xxxxxxxxx. V případě xxxxxxxxxxxxxx xxxxx xxx xxxxx tolerance se xxxxxxx xxxxxxxxx a popřípadě xxxxxxxxxx.
Xxxxx xxx xxxxxxxx, xx xx snášen 100xxxxxxx xxxxxxxxx xxxxxxxxxx xxxxx, xxxxxxxxxx se xxxxxxxxxxx xxx xxxxxxx xxxxxxxxx chemického xxxxxxx xxxx. Xx-xx xxxxxxx xxxxxx pouze při xxxxxx xxxxxx, než xx 10násobek xxxxxxxx xxxxxxxxxx xxxxx, xx xxxxxx navržena tak, xxx xxxx xxxxx xxxxxxxxx rozpětí xxx xxxxxxxxxx doplňkové látky, x&xxxx;xxxxxx se xxxxxxxxx xxxxxxxxx (pomocí nekropsie, xxxxxxxxx histologie x&xxxx;xxxxxx xxxxxxxx kritérií).
U některých xxxxxxxxxxx xxxxx xxxxxx xxx x&xxxx;xxxxxxxxxx xx jejich xxxxxxxxxxx x&xxxx;xxxxxxxxxxx nebo xxxxx nutné xxxxxxx xxxxx tolerance.
Použité experimentální xxxxxx xxxx zahrnovat xxxxx o odpovídající xxxxxxxxxxx xxxxxxxxxxx.
3.1.1.2&xxxx;&xxxx;&xxxx;Xxxx xxxxxx xxxxxxx xxxxxxxxx
Xxxxxxx&xxxx;1
Xxxx xxxxxx xxxxxxx xxxxxxxxx: xxxxxxx
|
Xxxxxx xxxxxxx |
Xxxx xxxxxx xxxxxx |
Xxxxxxxxxxxxxxx xxxxxxxx xxxxxx |
|
Xxxxxx xxxxxx |
14&xxxx;xxx |
Xxxxx xxxxx xx 14 dnů xx xxxxxxx |
|
Xxxxxxxxx xxxxxx |
42&xxxx;xxx |
42&xxxx;xxx xx xxxxxxx |
|
Xxxxx prasat |
42 dní |
Tělesná xxxxxxxx xx začátku studie ≤&xxxx;35&xxxx;xx |
|
Xxxxxxxx xxxxxx x&xxxx;xxxxxxxxxx |
1&xxxx;xxxxxx |
Xx xxxxxxxxxx xx konce xxxxxxx |
X&xxxx;xxxxxxx xxxxxxx týkající xx sajících x&xxxx;xxxxxxxxxxx xxxxx se xxxxxxxx xx dostatečnou xxxxxxxxxxx xxxxxx (14denní xxx xxxxxx xxxxxx a 28denní xxx xxxxxxxxx xxxxxx). Xxxxx byla xxxxxxxxx xxxxxxxxx x&xxxx;xxxxxxxxxxx selat, xxxxxxxxxx se xxxxxxxx xxxxxx xxx výkrm xxxxxx.
Xxxxxxx&xxxx;2
Xxxx trvání zkoušek xxxxxxxxx: xxxxxx
|
Xxxxxx xxxxxxx |
Xxxx xxxxxx xxxxxx |
Xxxxxxxxxxxxxxx xxxxxxxx xxxxxx |
|
Xxxxx xxxxx/xxxxxx |
35&xxxx;xxx |
Xx xxxxxxxxx |
|
Xxxxxxx |
56&xxxx;xxx |
Xxxxx xxxxx xxxxx xxxxx xxxxxxx doby xxxxxx |
|
Xxxxx xxxx |
42&xxxx;xxx |
Xx vylíhnutí |
Údaje x&xxxx;xxxxxxxxx x&xxxx;xxxxxx kuřat xxxx xxxx xxx xxxxxx x&xxxx;xxxxxxxxx tolerance x&xxxx;xxxxxxx xxxxx x&xxxx;xxxxx xxxx x&xxxx;xxxxxxx krůt.
Tabulka 3
Doba xxxxxx xxxxxxx xxxxxxxxx: xxxx
|
Xxxxxx xxxxxxx |
Xxxx trvání xxxxxx |
Xxxxxxxxxxxxxxx xxxxxxxx xxxxxx |
|
Xxxxx xxxxx |
28&xxxx;xxx |
Xxxxxxx xxxxxxx hmotnost ≤&xxxx;70&xxxx;xx |
|
Xxxxxx xxxxx; xxxxx xxxxx xxxx skot k reprodukci |
42 dní |
|
|
Dojnice |
56 dní |
V případě xxxxxxx vztahující xx xx odchov telat x&xxxx;xxxxx skotu se xxxxxxxx xx xxxxxxxxxxx xxxxxxxxxxx xxxxxx (28&xxxx;xxx xxx xxxxx období).
Tabulka 4
Doba xxxxxx xxxxxxx xxxxxxxxx: xxxx
|
Xxxxxx xxxxxxx |
Xxxx trvání xxxxxx |
Xxxxxxxxxxxxxxx xxxxxxxx xxxxxx |
|
Xxxxxx xxxxxx a výkrm xxxxxx |
28&xxxx;xxx |
Xxxxxxx&xxxx;5
Xxxx xxxxxx zkoušek xxxxxxxxx: xxxxxxxxxx a jiné ryby
|
Cílová xxxxxxx |
Xxxx xxxxxx studií |
Charakteristika xxxxxxxx xxxxxx |
|
Xxxxx x&xxxx;xxxxxx |
90&xxxx;xxx |
Xxxx xxxxxxxxxxx 90xxxxx xxxxxx xx bylo xxxxx xxxxxxx xxxxxx, kdy xxxx zvýší xxxx xxxxxxxx xxxxxxxx xxxxxx xxxxxxx tělesné hmotnosti xx xxxxxxx zkoušky xxxxxxx xxxxxxxxxxx.
Xx-xx být xxxxxxxxx xxxxx xxxxxxxxx xxxxx xxx hejno xxxxxxxxx ryb, testy xxxxxxxxx xx provedou xxxxx možno xx xxxxxxxx xxxx xxxxx. Xxxxx tolerance xxxxxx 90&xxxx;xxx a je xxxxx xxxxxxx xxxxxxxxx xxxxxxx x&xxxx;xxxxxxx xxxxx.
Xxxxxxx&xxxx;6
Xxxx trvání xxxxxxx xxxxxxxxx: xxxxxxx x&xxxx;xxxxxxxx xxxxx x&xxxx;xxxx xxxxxxx, která xxxxxx xxxxxx x&xxxx;xxxxxxxx potravin
|
Cílová xxxxxxx |
Xxxx xxxxxx xxxxxx |
Xxxxxxxxxxxxxxx xxxxxxxx xxxxxx |
|
Xxx a kočky |
28 dní |
Tabulka 7
Xxxx trvání xxxxxxx xxxxxxxxx: králíci
|
Cílová zvířata |
Doba xxxxxx xxxxxx |
Xxxxxxxxxxxxxxx cílových xxxxxx |
|
Xxxxx xxxxxxx |
28&xxxx;xxx |
|
|
Xxxxxx xxxxxxx |
1&xxxx;xxxxxx |
Xx xxxxxxxxxx xx xxxxx xxxx xxxxxxx |
Xxxxxxxx-xx xx xxxxxx xx sající x&xxxx;xxxxxxxxx xxxxxxx, xxxxxxxx xx xx xxxxxxxxxx xxxxxx 49&xxxx;xxx (počínaje týden xx narození) a musí xxxxxxxxx xxxxxxx až xx odstavu.
Pokud xx xxxxxxxxx látka používá xx specifickou x&xxxx;xxxxxx xxxx, než xx xxxxxxx x&xxxx;xxxxxxxx xxxxxxxxx xxxxxx, podává xx xxxxx xxxxxxxxxxxx podmínek xxx užití. Xxxxxx xxxxxxxxxx xxxx xxxxx xxx kratší xxx 28&xxxx;xxx x&xxxx;xxxx xxxxxxxxx xxxxxxxxx parametr (xxxx. x&xxxx;xxxxxxx xxxxxxxx k reprodukci xxxxx xxxx xxxxxxxxxx xxxxx xx zřetelem xx období březosti xxxx xxxxx x&xxxx;xxxxxxxx xxxxxxxxxxx xxxxx xx xxxxxxxx xx xxxxxx xxxxxxx).
3.1.1.3&xxxx;&xxxx;&xxxx;Xxxxxxx xxxxxxxx
Xxxxxx xxxx xxx xxxxxxx xxxxxxxxxx x&xxxx;xxxxx x&xxxx;xxxxx xxxxxxxxx xxxxxxxxx. Xxxxxxxx xxxxxxxx xxxx xxx pečlivě xxxxxxxxxx s ohledem xx xxxxxx xxxxxxx údaje. Xxxxxxxxxxxxx xx xxxxxxx xxxx xxxxxxx:
|
1. |
xxxxx nebo xxxxx: místo x&xxxx;xxxxx; xxxxxxxx xxxxxx x&xxxx;xxxxx, xxxxxx xxxxxx; x&xxxx;xxxxxxx xxxxx xxxxxxxx a počet xxxxxx xxxx xxxxx x&xxxx;xxxxxxxxxxxx, xxxxxxxx xxxxxx x&xxxx;xxxxxxx xxxx, xxxxxx xxxxxxx xxxx x&xxxx;xxxxxx xxxx xx xxxx; |
|
2. |
xxxxxxx: xxxx (x&xxxx;xxxxxxx druhů xxxxxxxx xxx xxxxxxx xxxxxxxx xx uvedena xxxxxxxxxxxx xxxxx xxxxxx xxxxxxxx xxxxx x&xxxx;xx xxx v závorkách xxxxxxxxx xxxxxxxx xxxxxxxxx xxxxx), xxxxxxx, stáří (xxxxxxxx x&xxxx;xxxxxxx xxxxx), xxxxxxx, xxxxxx označení, xxxxxxxxxxxx xxxxxxx a celkový xxxxxxxxx xxxx; |
|
3. |
xxxxx x&xxxx;xxxxxx xxxx xxxxxx testů: datum x&xxxx;xxxx xxxxxxxxxxx xxxxxxx; |
|
4. |
xxxxx xxxxx: popis xxxxxx x&xxxx;xxxxxxxxxxxxxxx xxxxxxx krmné xxxxx (xxxxx) x&xxxx;xxxxxxxx xxxxxxxxx xxxxxx, xxxxxxxxxxx xxxxx (analyzované xxxxxxx) x&xxxx;xxxxxxxxxxx hodnoty. Xxxxx x&xxxx;xxxxxx xxxxxx; |
|
5. |
xxxxxxxxxxx xxxxxx xxxxx (xxxxx) nebo xxxxxxx (xxxxxxx) (x&xxxx;xxxxxxxxxx xxxxx použitých xxx xxxxxxxxxx xxxxx) x&xxxx;xxxxxxxx xxxx xxx xxxxxxxxx xxxxxxxxx xxxxxxxx s použitím xxxxxxxxxxx uznávaných xxxxx. Xxxxxxxxxx xxxxx xxxxxxxxx xxxxx; |
|
6. |
xxxxx pokusných x&xxxx;xxxxxxxxxxx xxxxxx, xxxxx xxxxxx x&xxxx;xxxxx xxxxxxx: počet xxxxxx xxxxxxxxx pro xxxxxx xxxx xxxxxxx xxxxxxxxx statistické analýzy. Xxxx by xxx xxxxxxx použité xxxxxx xxxxxxxxxxxxx xxxxxxxxx. Xx xxxxxx xxxx xxx xxxxxxxx xxxxxxx xxxxxxx x/xxxx xxxxxxxxxxxxxx celky, x&xxxx;xxxxx xx xxxxxx xxxxxxxxx. Případy, které xxxx možné vyhodnotit xxx xxxxxxxxxx nebo xxxxxx xxxxx, musí xxx xx zprávě xxxxxxx x&xxxx;xxxxxx xxxxxxxxx x&xxxx;xxxxxxxxxxxx xxxxxxxxx xxxxxx xxxx být xxxxxxxxxxxxx; |
|
7. |
xxxxxxx x&xxxx;xxxxxx xxxxxxxxxxx nežádoucího xxxxxx zákroku u jedinců xxxx xxxxxx xxxx xxx xxxxxxxxxx (xxxxxxxxxx xxxxx x&xxxx;xxxxxxxx xxxxxxxxxx xxxxxxxxx xx studii) x |
|
8. |
xxxxxxx/xxxxxxxxxxx xxxxxxxx, xx-xx xxxxx, xxxxx xxxxxxxxxx xxxxxxxxxx mechanismus působení xxxxxxxxx xxxxx x&xxxx;xxxx xxx xxxxxxxxxxx individuálně. |
3.1.2 Mikrobiální xxxxxx
Xx xxxxx poskytnout xxxxxx xx xxxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxx xxxxxxxx křížovou xxxxxxxxxx xxxx xxxxxxxxxxxx xxxxxxxxxx x&xxxx;xxxxxxxx xxxx xxxxxxxxxxxx xxxxxxxxx, xxxxxxxxxx xxxxxxxxxxx xxxxxxxxxxx xxxxx xx xxxxxxxxxx xxxxxxxx u cílových xxxxx, xxxxxxx xxxxxx x&xxxx;xxxxxxxxxxx patogenů xxxxxxxxxx x&xxxx;xxxxxxxxx xxxxxx, vyvolat xxxxxxxxxx xxxx xxxxxxxxxx xxxxxxxxxxxx xxxxxxxxxxxxxx.
X&xxxx;xxxxxxx, že xxxxxx xxxxx (xxxxx) xxxxxxxx(x)&xxxx;xxxxxxxxxxxxxxx aktivitu při xxxxxxxxxxx, xx xxxxx xx xxxxxxxx x&xxxx;xxxxxx, xxxx xxx v souladu xx xxxxxxxxxxxxxxxxx xxxxxxx xxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxxxxx (XXX) xxx xxxxxxxxx druhy xxxxxxxx. Xx-xx xxxxxxxxx příslušná xxxxxxxxxxxxxxx aktivita, je xxxxx xxxxxxxx schopnost xxxxxxxxx látky xxxxxxxxxx xxxxxxxxxxx bakteriální kmeny xx xxxxx x&xxxx;x&xxxx;xxxxxxxx xxxxx x&xxxx;xxxxxxxx xxxxxxxx xxxxxxxxxx vůči odpovídajícím xxxxxxxxxxxx&xxxx;(11).
Xxxxxxx x&xxxx;xxxxxxxxxxx xxxxxxx xxxxx se xxxxxxxx xxx xxxxxxx xxxxxxxxxxx xxxxxxxxx látky x&xxxx;xxx xxxx xxxxxxxxx xxxxx, x&xxxx;xxxxx lze xxxxxxxx xxxxxx xx xxxxxxx xxxxxxxxxx. Xxxx studie xxxx xxxxxxxx, xx xxxxx xxxxxxxxx xxxxx xxxxxxxxx xxxxxxxx, xxxxx xxxxxxxxxx xxxxxxxxxx xxxxx x&xxxx;xxxxxxxxxx xxxxxxxxxxx patogenních xxxxxxxxxxxxxx.
Xxxxx xxxxxxxxxxx mikroorganismů xxxx xxxxxxx xx xxxxxxxx druzích, zahrnuje xxxx xxxxxxxxx xxxxxxxxxx xxxxx xxx xxxxxx xx xx, xxx x&xxxx;xxxxxxxx xxxxxx xxxxxxxxxx xx nevyvolávají xxxxxxxx.
3.2&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxx xx xxxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxx xxx spotřebitele
Cílem je xxxxxxxxxx xxxxxxxxxx doplňkové xxxxx xxx xxxxxxxxxxxx x&xxxx;xxxxxxxx xxxxx rezidua xxxxxxxxx xxxxx xxxx xxxxxx metabolitů x&xxxx;xxxxxxxxxxx xxxxxxxxx xx xxxxxx, xxxx bylo xxxxxxxx xxxxxx xxxx voda xxxxxxxxxx xxxxxxxxxx xxxxx xxxx ošetřené touto xxxxxxxxxx xxxxxx.
3.2.1&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxxxxx x&xxxx;xxxxxxx
Xxxxxxxxx xxxxxxxxxxx doplňkové xxxxx u cílových xxxxx xx xxxxxxxxxxxx krokem xxx identifikaci x&xxxx;xxxxxxxxxxxx xxxxxxx x&xxxx;xxxxxxxxxxxxx tkáních xxxx xxxxxxxxxx xxxxxxxxx xx xxxxxx, jimž xxxx podáváno krmivo xxxx voda xxxxxxxxxx xxxxxxxxxx xxxxx. Je xxxxx xxxxxxxxx studie xxxxxxxx xx absorpce, xxxxxxxxxx, xxxxxxxxxxx x&xxxx;xxxxxxxxxx xxxxx (a jejích xxxxxxxxxx).
Xxxxxx xxxx být xxxxxxxxx xxxxxx xxxxxxxxxxx xxxxxxxxxxxx xxxxxxxxxx xxxxx a v souladu x&xxxx;xxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxx xxxx xxxxxxxx xxxxxxxx pro xxxxxxxxxxxxx xxxxxxxxx XXXX x&xxxx;xxxxx xxxxx xxxxxxx xxxxxxxxxxx xxxxx. Xxxxxx xxxx xxxxxxxxxxx pravidla xxxxxxxx xx dobrých xxxxxxxxx xxxxxxxx zvířat xxxxxxxxx xxxxxxxx xxxxxxxx Evropského xxxxxxxxxxxx x&xxxx;xxxxxxxxx xx, xxxx-xx to xxxxxxxx.
Xxxxxx xxxxxxxxxxx x&xxxx;xxxxxxx x&xxxx;xxxxxxxx xxxxxxx (xxxxxx) se xxxxxxxx x&xxxx;xxxxxxx xxxxxx xxxxxxxxxxxx do xxxxxx (xxxxxxxxxxx xxxxxx výživy xxxxxxxxx xxxxxx, není-li xx xxxxx xxxxxxxxxx).
Xxxxxxx xx strukturní xxxxxxxxxxxx xxxxxxxxxx xxxxxxxxxxxxxxx více xxx 10&xxxx;% xxxxx xxxxxxx x&xxxx;xxxxxxxxxxxxx tkáních x&xxxx;xxxxxxxxxx a více než 20&xxxx;% všech xxxxxxx x&xxxx;xxxxxxxxxxxx. Xxxxx xx xxxxxxxxxxx xxxxx účinné xxxxx xxxxxxxxxxxxx xxxxxxxx, xx nutno xxxxxxxxxxxxx xxxxxxxxxx xxx xxxx xxxxxxxxx xxxxxx.
Xxxxxxxxx xxxxxx xxxxxxx xxxxx xxxxxx xxx xxxxxxx xxxxxxxx xxxxxxxxxxxx a případně stanovení xxxxxxxx xxxxx x&xxxx;XXX. Xxxxxxxx xx návrh xx xxxxxxxxxxxx xxxxxxxx.
X&xxxx;xxxxxxxxx xxxxxxxxxxx látek xxxxxx xxx v závislosti xx xxxxxx xxxxxx xxxx xxxxx xxxx xxxxx xxxxxxx xxxxxx xxxxxxxxxxx x&xxxx;xxxxxxx.
3.2.1.1&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxxxxx
Xxxxxx xxxxxx xxxxxxxxxxx je xxxxxxxxxx xxxxxxxx, xxxxxxxxxx, xxxxxxxxxxxxxxx x&xxxx;xxxxxxxxxx doplňkové látky x&xxxx;xxxxxxxx druhů xxxxxx.
Xxxxxxxxxx xxxxxx:
|
1. |
xxxxxxxxxxx bilance xx xxxxxx xxxxxx dávky xxxxxx látky x&xxxx;xxxxxxxxxxxx xxxxxxx xxx xxxxx (xxxxxxx xxxxxxxx odpovídající xxxxxxx xxxxxx) a případně xxxxxxxxxxx xxxxx (xx-xx xx xxxxxxxxxx), aby xxxxx být xxxxxxxxx xxxxxxxx x&xxxx;xxxxxx xxxxxxxx, xxxxxxxxxx (xxxxxx/xxxx) x&xxxx;xxxxxxxxxx (xxx, xxxx, xxxxxx, xxxxx xxxx xxxxx, xxxxxxxxxxx vzduch, xxxxxxxxxx xxxx žábry) u samců x&xxxx;xxxxx, je-li xx xxxxxx, x |
|
2. |
xxxxxxxxx xx xxxxxxxxxxx, xxxxxxxxxxxx metabolitu(ů) v exkrementech x&xxxx;xxxxxxx a distribuce x&xxxx;xxxxxxx x&xxxx;xxxxxxxxxx se xxxxxxx xx xxxxxxxxxx xxxxxxxx xxxxx xxxxxxxx xxxxx xxxxxxxx xx vyrovnaném xxxxx (xxxxxxxxxxx xxxxxxxxx) xxxxx obsahu x&xxxx;xxxxxx. Xxxxxxxxxx xxxxx xxxxxxxx xxxxxxxx navrhované dávce xxx užití x&xxxx;xxxx xxx xxxxxxxxxxx do xxxxxx. |
3.2.1.2&xxxx;&xxxx;&xxxx;Xxxxxx reziduí
Uváží se xxxxxxxx x&xxxx;xxxxxx neextrahovatelných xxxxxxx v poživatelných xxxxxxx xxxx produktech.
Studie reziduí xx požadují pro xxxxxxx látky, x&xxxx;xxxxx xxxx xxxxx studie xxxxxxxxxxx.
Xx-xx látka xxxxxxxxxx xxxxxxx tělních xxxxxxx xxxx tkání nebo xxxxxxxxx-xx xx x&xxxx;xxxxxxxxxxx xxxx krmivech xxxxxxxxx xx xxxxxxx množství, xx xxxxxxxxx na xxxxxx reziduí xxxxxx xx porovnání xxxxxx x&xxxx;xxxxxxx/xxxxxxxx x&xxxx;xxxxxxxxxx skupiny x&xxxx;x&xxxx;xxxxxxx, jíž xxxx xxxxxxxx xxxxxxxx xxxxxxx xxxxx.
X&xxxx;xxxxxxxxxxx druhů xxxxxx xxxxxxxx vyhodnotí xxxxxxx xxxxxxx, která xxxx xxxxxxxxxxxxx xxxxxxxx, a určí xxxxxxxxxxxx xxxxxxxx xxxxxx xxxxx v poživatelné xxxxx (xxxxx, xxxxxxx, xxxxx, xxxx, kůže + xxx) a produktech (xxxxx, xxxxx x&xxxx;xxx). Xxxxxxxxxxxx xxxxxxxx xx reziduum xxxxxxx xxx xxxxxxx, xxxxx koncentrace xx xx xxxxxx xxxxxx x&xxxx;xxxxxxxx toxikologicky významným xxxxxxxx x&xxxx;xxxxxxx. Studie xxxx xxxxxxxx xxxxxx xxxxxxx xxxxxxx x&xxxx;xxxxxxx xxxx xxxxxxxxxx, aby xxxx možno xxxxxxxx xxxxxxxxxxxx xxxxxxxxx lhůtu.
Ke xxxxxxxxx ochranné xxxxx xx navrhovaný xxxxxxxxx xxxxx xxxxxx ve xxxxxx x/xxxx produktů x&xxxx;xxxxxx xxxx měření xxxxx:
|
— |
xxxxxxxxxxx tkáně:
|
|
— |
xxxxxxxx:
|
Xxxxx xx xxxxxx rozložení podle xxxxxxx.
Xxxxxxx xx měří xxx xxxxxx ochranné xxxxx (vyrovnaný stav) x&xxxx;xxxxxxx xx xxxxx xxxxxx xxxxxx měření.
Předloží xx návrh xx xxxxxxxxxxxx reziduum.
Je xxxxx xxxxxxx xxxxxx xxxxxxxx, xxxxxxxxxx a vylučování, xxxxxx xxxxxxxxxxxx xxxxxxxx xxxxxxxxxx, x&xxxx;xxxxxxxxxxxxx xxxxx xxxxxx, x&xxxx;xxxxx xxxx získána xxxxxxxx xxxxxxx XXXXX xxxx xxxxxxxxxx x&xxxx;xxxx (xxxx xxxxxxx). Xxxxxxxxx xxxxxx xxxxxxxx xx xxxxxxxx xxxxxxxxxx mohou xxx xxxxxxxx v případě, xxxx-xx xxxx metabolity xxxxxxxxxxx xxxxxxxx xxxxx x&xxxx;x&xxxx;xxxxxxxxxxxxx xxxxx xx xx významném rozsahu xxxxxxx.
3.2.1.3&xxxx;&xxxx;&xxxx;Xxxxxx metabolismu x&xxxx;xxxxxxxx
Xxxx xxx xxxxxxxxx studie xxxxxxxxxxx xxxxxxxxxx xxxxxxxxxxxx xxxxxxx, metabolický xxxxxx x&xxxx;xxxxxxxxxxxx hlavních metabolitů x&xxxx;xxxx x&xxxx;xxxxxxxx. Xxxxxxxx xxxx xxxxxxxxxxx druhy xxxxxxxx xxxxxx kryse xxxxxxx xxxxxx x&xxxx;xxxxxxxxxx, xxxxx xxxxxxxxxx doplňkové xxxxxxxxx.
3.2.1.4&xxxx;&xxxx;&xxxx;Xxxxxxxxxx dostupnost reziduí
Při xxxxxxxxxx rizika pro xxxxxxxxxxxx xxxxxxxxx x&xxxx;xxxxxxxx xxxxxxxx xxxxxxx xxxxxxxxxx x&xxxx;xxxxxxxxxxx xxxxxxxxxx xx xxxxx xxxx x&xxxx;xxxxx xxxxxxxxx bezpečnostní xxxxxx xxxxxxxx xx určení xxxxxx xxxxxxxxxx xxxxxxxxxxx xx xxxxxxx vhodných xxxxxxxxxxxxx zvířat x&xxxx;xxxxxxxx xxxxx.
3.2.2&xxxx;&xxxx;&xxxx;Xxxxxxxxxxxxx xxxxxx
Xxxxxxxxxx xxxxxxxxx xxxxx xx xxxxxxxx xx základě toxikologických xxxxxx xxxxxxxxxxx xx xxxxx a in xxxx xx xxxxxxxxxxxxx zvířatech. Xxxx zkoušky xxxxxxx xxxxxxxx měření:
|
1. |
akutní toxicity; |
|
2. |
genotoxicity (xxxxxxxxxx, xxxxxxxxxxxxxx); |
|
3. |
xxxxxxxxxxxx xxxxxx xxxxxxxx; |
|
4. |
xxxxxxxxx xxxxxx xxxxxxxx/xxxxxxxxxxxxx; |
|
5. |
xxxxxxxx xxx xxxxxxxxxx xxxxxx xxxxxxxxxxxx x |
|
6. |
xxxxxxx studie. |
Existuje-li xxxxx x&xxxx;xxxxxx, musí xxx xxxxxxxxx další xxxxxx xxxxxxxxxxx doplňkové xxxxxxxxx, xxxxx jsou xxxxxxxx xxx posouzení xxxxxxxxxxx účinné xxxxx x&xxxx;xxxxxx xxxxxxx.
Xx xxxxxxx xxxxxxxx xxxxxx xxxxxx xx xxxxxxx toxikologická XXXXX.
Xxxxxxxxx studie xxxxxxxx xx xxxxxxxx xxxxxxxxxx xxxxx xxx nezbytné, xxxxx xxxx xxxx xxxxxxxxxx xxxxxxxxxxx xxxxxxxx xxxxx x&xxxx;x&xxxx;xxxxxxxxxxx laboratorních xxxxx se xx xxxxxxxxx xxxxxxx xxxxxxx. Xxxx-xx x&xxxx;xxxxxxxxx xxxxxx xxxxxxxxxxx x&xxxx;xxxxxxx, xxxxxx xx xxxx údaje x&xxxx;xxxxx při xxxxxxxxxxx x&xxxx;xxxxxx xxxxxxxxxx xxxxxxxxxxx xxxxxx.
Xxxxxxxxxxxxx xxxxxx xxxx xxx provedeny s účinnou xxxxxx. Xxxxx xx xxxxxx xxxxx přítomna x&xxxx;xxxxxxxx xxxxxxxxxxxxx xxxxxxx, xxxxxxx xx xxxxxxx xxxxxxxxxxxxx xxxxxxx. Testovaný xxxxxxx fermentačního xxxxxxx xxxx xxx xxxxxxx x&xxxx;xxxxxxxxx, který má xxx použit x&xxxx;xxxxxxxxx xxxxxxxx.
Xxxxxx xxxx být xxxxxxxxx pomocí mezinárodně xxxxxxxxxxxx xxxxxxxxxx xxxxx x&xxxx;xxxxxxx s platnými evropskými xxxxxxxx xxxxxxxx xxxx xxxxxxxx xxxxxxxx pro xxxxxxxxxxxxx xxxxxxxxx OECD x&xxxx;xxxxx zásad xxxxxxx xxxxxxxxxxx xxxxx. Xxxxxx xxxxxxxxxx xxxxxxxxxxx zvířata xxxx xxxxxxxxxxx pravidla xxxxxxxx xx dobrých xxxxxxxxx podmínek xxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxx x&xxxx;xxxxxxxxx xx, xxxx-xx xx xxxxxxxx.
3.2.2.1&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxx
Xxxxxx xxxxxx xxxxxxxx xx xxxxxxxx xx xxxxxxxxxxx a omezené charakteristice xxxxxxxx xxxxx.
Xxxxxx xxxxxx xxxxxxxx xxxx xxx xxxxxxxxx xxxxxxx na xxxx xxxxxxx savců. Xxxxx xxxxxxxxxxx xxxx xxxx být xxxxxxxx xxxxxxxx cílovým druhem.
Nebude xxxxx zjistit xxxxxxx xxxxxxx LD50; postačuje xxxxxxxxx určení xxxxxxxxx xxxxxxx dávky. Xxxxxxxxx xxxxxxxxx xxxxx překročit 2&xxxx;000&xxxx;xx/xx xxxxxxx hmotnosti.
Ke xxxxxxx počtu xxxxxxxxxxx xxxxxx x&xxxx;xxxxxxxx xxxxxx xxxxxxx se xxxxxxxx xxxxxxxx nové xxxxxxxxx xxx xxxxxxxxx xxxxx xxxxxxxxxxxx xxxxxx xxxxxxxx. Xxxxxx provedené pomocí xxxxxx xxxxxx xxxxxxx xxxxx uznány, xxxx-xx xxxxx xxxxxxxxxx.
Xx xxxxx xxxxxxx xxxxxx XXXX 402 (akutní xxxxxxxx xxxxxxxx), 420 (xxxxxx xxxxx xxxxx), 423 (xxxxxx xxxxxxxxx třídy xxxxxx xxxxxxxx) x&xxxx;425 (xxxxxx xxxxxx x&xxxx;xxxx).
3.2.2.2&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxxxxxx, xxxxxx xxxxxxxxxx
Xx xxxxxx xxxxxxxxxxxx účinných xxxxx x&xxxx;xxxxxxxx xxxxxx xxxxxxxxxx x&xxxx;xxxxxxxx degradace, xxxxx mají xxxxxxxxx x&xxxx;xxxxxxxxxxx xxxxxxxxxx, xxxx xxx xxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxx xxxxx xx genotoxicitu. X&xxxx;xxxxxxx xxxxxxx xx xxxxx xxxx xxxxxxxx xxx x&xxxx;x&xxxx;xxxxxxxxxxxx xxxxxxxx u savců x&xxxx;xxxxx se x&xxxx;xxxxx xxxxxxxxxxxx xxxxxxxxxxx xxxxxxxxx xx zkušebním xxxxxxxx.
Xxxxxxxx xxxxxx xxxxxxxx xxxx xxxxxxx:
|
1. |
xxxxxxx xxxxxxxx xxxxxx x&xxxx;xxxxxxxxxx x/xxxx v buňkách xxxxx (xxxxx xxxxx xxxx xx xxxxxxxxxxxxx x&xxxx;xxxxxxx myší); |
|
2. |
indukce xxxxxxxxxxxxxx xxxxxxx x&xxxx;xxxxxxx xxxxx x |
|
3. |
xxxxxxx xx xxxx x&xxxx;xxxxx. |
X&xxxx;xxxxxxxxxx xx výsledku xxxx xxxxxxxxx xxxxxxx x&xxxx;x&xxxx;xxxxxxxxxxxx k celkovému xxxxxxxxxxxxxxx xxxxxxx xxxxx x&xxxx;xxxxxx xxxxxxxx xxxxx xxxxx xxx nezbytné xxxxxxxxx xxxxxxx.
Xxxxxxxxx xx xxxx xxx v souladu s pokynem XXXX 471&xxxx;(xxxx reverzních xxxxxx x&xxxx;Xxxxxxxxxx xxxxxxxxxxx), 472&xxxx;(xxxx reverzních mutací x&xxxx;Xxxxxxxxxxx xxxx), 473&xxxx;(xxxx xxxxxxxxxxxxxx aberací x&xxxx;xxxxx xx vitro), 474&xxxx;(xxxx xx xxxxxxxxxx x&xxxx;xxxxxxx&xxxx;xxxxxxxxxxxx), 475&xxxx;(xxxx xxxxxxxxxxxxxx aberací x&xxxx;xxxxxx xxxxx xxxxx), 476&xxxx;(xxxx xxxxxxxx xxxxxx x&xxxx;xxxxxxx buňkách in xxxxx) xxxx 482&xxxx;(xxxxxxxxxxx xxxxxxx XXX x&xxxx;xxxxxxx xxxxx xx xxxxx), xxxxx i jinými xxxxxxxxxxx xxxxxx XXXX pro xxxxxxx xx vitro x&xxxx;xx xxxx.
3.2.2.3&xxxx;&xxxx;&xxxx;Xxxxxx subchronické xxxxxx xxxxxxxx xxx xxxxxxxxx xxxxx
X&xxxx;xxxxxxx xxxxxxxxxx xxxxxxxxxxxx xxxxxxxx xxxxxx xxxxx xx předloží xxxxxxx jedna studie xx xxxxxxxxxx x&xxxx;xxxxx xxxxxx xxxxxxx 90&xxxx;xxx. Xxxxxxxx-xx xx xx xx xxxxx, xxxx xxx xxxxxxxxx xxxxx xxxxxx xx xxxxx xxxxx než xxxxxxxxxx. Xxxxxxxxx xxxxxxx xxxx xxx xxxxxxxx orálně xxxxxxx o třech různých xxxxxxxx xxxxx xx xxxxxxxxx xxxxxxx, xxx xx xxxxxxx xxxxxx xx dávku. Xxxxxxxxx xxxxx xxxx za xxxxxxxxxx okolností xxxxxxx xxxxxxxxxx nežádoucích účinků. Xxxxxxxx xxxxxx xxxxxxxxx xxxxx xxxxxxxxx xxxxxx xxxxxx toxicity.
Protokoly xxx xxxx xxxxxxx xxxx xxx x&xxxx;xxxxxxx x&xxxx;xxxxxx XXXX 408 (xxxxxxxx) xxxx 409 (xxxx xxxxx xxx xxxxxxxx).
3.2.2.4&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxxx xxxxxx xxxxxxxx (xxxxxx xxxxxxxxxxxxx)
X&xxxx;xxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxx a karcinogenity xx xxxxx provést xxxxxx chronické orální xxxxxxxx nejméně xx xxxxxx xxxxx s dobou xxxxxx xxxxxxx 12 měsíců. Xxxxxxx xxxx xxxx xxx xxxxxxxxxxxxx xxxxxx xxxxx xxxxx dostupných xxxxxxxxx údajů, xxxxxx xxxxxxxx 90xxxxxxx xxxxxx. Xxxxxxxxxxx xxxxxx je xxxxx. Xxxxxxxx-xx xx xxxxx xxxxxx, xxxxxxx xx xxxx xxxxxxxx xxxx xxxx xxxx xxxxx než xxxxxxxx. Xxxxxxxxx xxxxxxx musí xxx xxxxxxxx xxxxxx xxxxxxx x&xxxx;xxxxx xxxxxxx xxxxxxxx xxxxx xx xxxxxxxxx skupině, aby xx xxxxxxx xxxxxx xx xxxxx.
Xx-xx xxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxxxx xx xxxxxxxx xxxxxxxxxxxxx, xxxx xxxxxx xx xxxxxxxxxxx xx 18&xxxx;xxxxxx x&xxxx;xxxx x&xxxx;xxxxxx x&xxxx;xx 24&xxxx;xxxxxx u krys.
Studie xxxxxxxxxxxxx xxxxxx xxx xxxxx, xxxxx účinná xxxxx x&xxxx;xxxx metabolity:
|
1. |
vykazují xxxxx xxxxxxxxx výsledky x&xxxx;xxxxxxx xx genotoxicitu; |
|
2. |
nejsou xxxxxxxxxxxx xxxxxxxxx xx známými xxxxxxxxxxx x |
|
3. |
xxxxxxxxxxxx při xxxxxxxxx chronické xxxxxxxx xxxxx účinky (xxx)xxxxxxxxx. |
Xxxxxxxxx xxxx xxx x&xxxx;xxxxxxx x&xxxx;xxxxxxx XXXX 452 (xxxxxx chronické toxicity) xxxx 453 (kombinovaná xxxxxx chronické xxxxxxxx/xxxxxxxxxxxxx).
3.2.2.5&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxx pro xxxxxxxxxx (xxxxxx xxxxxxxx xxx xxxxxxxxxx vývoj)
K zjištění xxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx x&xxxx;xxxxx nebo xxxxx xxxx xxxxxxxxxx xxxxxx xx potomstvo xxxxxxxxxxxxx x&xxxx;xxxxxxxx xxxxxx látky xx xxxxx xxxxxxx xxxxxx reprodukční xxxxxx xxxxxx:
|
1. |
xxxxxxxxxxxxx xxxxxx xxxxxxxx xxx reprodukci x |
|
2. |
xxxxxx xxxxxxxx pro xxxxxxxxxx xxxxx (xxxxxxx xxxxxxxxxxxx). |
X&xxxx;xxxxxx xxxxxxx xxxxx být xxxxxxx xxxxxxxxxx xxxxxxxxxxxx xxxxxx xxxxxxxxx xxxxxxxxx xxxxxx.
3.2.2.5.1.&xxxx;&xxxx;&xxxx;Xxxxxxxxxxxxx studie xxxxxxxx xxx xxxxxxxxxx
Xxxxxx xxxxxxxxxxx xxxxxx xxxx xxx xxxxxxxxx x&xxxx;xxxxxxx xxxxxxx xxxx xxxxxxxxxx xxxxxxxx (X1, F2) x&xxxx;xxxxxxx xxxxxxx xxxxx, xxxxxxx xxxxxxxx, a mohou xxx xxxxxxxxxxx xx xxxxxx xxxxxxxxxxxx. Xxxxxxxx xxxxx xx xxxxxxxx xxxxxx xxxxxx x&xxxx;xxxxxxx xx xxxxxxx xxxx xxxx xxxxxxx. V podávání xx xxxx xxxxxxxxxx xx xx odstavu xxxxxx xxxxxxxx&xxxx;X2.
Xxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxx xx oplození, xxxxxxxx, porodu, xxxxxxxxxx xxxxxxx, kojení, xxxxx x&xxxx;xxxxxx xxxxxx generace F1 xx početí xx xx xxxxxxxxxx a vývoj xxxxxxxx&xxxx;X2 xx do xxxxxxx musí xxx xxxxxxx sledovány x&xxxx;xxxxxxxxxxxxx. Xxxxxxxxx pro xxxxxx xxxxxxxx pro reprodukci xx xxxx xxx x&xxxx;xxxxxxx x&xxxx;xxxxxxx XXXX 416.
3.2.2.5.2.&xxxx;&xxxx;&xxxx;Xxxxxxx toxicity xxx xxxxxxxxxx vývoj (xxxxxxx xxxxxxxxxxxx)
Xxxxx xx xxxxxxx xxxxxxxx xxxxxxxxxx účinky xx xxxxx xxxxxx x&xxxx;xxxxx xxxxxx x&xxxx;xxxxx x&xxxx;xxxxxxxx xxxxxxxx xx xxxxxxxxx oplozeného vajíčka xx xxxxx xxxx xxxxxxxx. K těmto xxxxxxx xxxxx xxxxxxx xxxxxxxx x&xxxx;xxxxxxx xxxxx, úmrtí xxxxxx – xxxxx, xxxxxxx xxxx xxxxx x&xxxx;xxxxxxxxxxxx xxxxxxxxxxx x&xxxx;xxxxxxxx xxxxx.
Xxxxxx, který xx xxxx pro xxxxx xxxxxx, je obvykle xxxxx. Xx-xx xxxxxxxxxx xxxxxxxxx xxxx xxxxxxxxxx xxxxxxxx xxx xxxxxxxxxxxx, xxxxxxx se xxxxx xxxxxx xxxxxxxx toxicity x&xxxx;xxxxxxx xxxxx, xxxxx xxxxx x&xxxx;xxxxxxx. Je-li xxxxxxx xx xxxxxxxxxxxx xx krysách xxxxxxxxx, xxxx studie x&xxxx;xxxxxxx xxxxx nutná xxxxx xxxxxxx, xxx xxxxxxx xxxxx hlavních studií xxxxxxxxx, xx XXX xxxx xxxxxxxx xx xxxxxxxxxxxx x&xxxx;xxxx. V tomto xxxxxxx xx xxxx xxxxx xxxxxx x&xxxx;xxxxxxx xxxxx, xxx xx xxxxx xxxxxxxxxxxx xxxx xxx xxxxx xxxxxxxx. Xxxxxxxxx xx xxxx xxx x&xxxx;xxxxxxx x&xxxx;xxxxxxx XXXX 414.
3.2.2.6&xxxx;&xxxx;&xxxx;Xxxx xxxxxxxxxx xxxxxxxxxxxxx a farmakologické xxxxxx
Xxxxxxxx-xx xxxxxx x&xxxx;xxxxxx, xx xxxxx xxxxxxx xxxxx xxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxxxxx pro posouzení xxxxxxxxxxx xxxxxx látky x&xxxx;xxxxxx xxxxxxx. Xxxx xxxxxx mohou xxxxxxxxx xxxxxxx xxxxxxxxxxxxxxxx účinků, xxxxxx xx xxxxx (xxxxxxxxxxxxxx) zvířata, xxxxxxxxxxxxx xxxx xxxxxxxxxxxxx.
3.2.2.7&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxx xxxxx xxx xxxxxxxxxxxx xxxxxxxxxxxx účinku (XXXXX)
XXXXX xx xxxxxxx založena xx xxxxxxxxxxxxxxx xxxxxxxx, xxxxxxxxxxxxx však mohou xxx xxxxxxxxx xxxxxxxxxxxxxx xxxxxx.
Xxxx xx xxxxxxxx XXXXX. Xxx xxxxxxxx xxxxxxxx XXXXX, xxxxxxxxx x&xxxx;xx/xx tělesné xxxxxxxxx xx den, se xxxxxx v úvahu všechna xxxxxxxx x&xxxx;xxxxxxxxxxx xxxxxx xxxxx s veškerými xxxxxxxxxx xxxxxxxxxxxx xxxxx (včetně xxxxxxxxx xxxxxx informace x&xxxx;xxxxxxxx účinné xxxxx xx xxxxxxx), popřípadě x&xxxx;xxxxxxxxx x&xxxx;xxxxxxxxxx xxxxxxx, xxxxx xxxx xxxx xxxxxxxxxxx xxxxxxxx struktury.
3.2.3 Hodnocení xxxxxxxxxxx xxx spotřebitele
Bezpečnost xxx xxxxxxxxxxxx xx xxxxxxxxx srovnáním xxxxxxxx XXX (přijatelné xxxxx xxxxx) x&xxxx;xxxxxxxxxxx teoretického xxxxxx doplňkové xxxxx xxxx xxxxxx metabolitů x&xxxx;xxxxxxx. X&xxxx;xxxxxxx xxxxxxxx x&xxxx;xxxxxxxxx xxxxx xx xxxxx XXX xxxx xxxxxx XX (nejvyšší xxxxxxxx xxxxx).
3.2.3.1&xxxx;&xxxx;&xxxx;Xxxxx přijatelné xxxxx xxxxx (XXX) xxx xxxxxxx xxxxx(x)
Xxxxxxxxxx xxxxx xxxxx (XXX) (xxxxxxxxx x&xxxx;xx xxxxxxxxx xxxxx xxxx materiálu xxxxxxxxxxxx xx x&xxxx;xxxxxxxxx xxxxx xx osobu x&xxxx;xxx) xx xxxxxxx xxx, xx xx xxxxxxxx hodnota XXXXX (xx/xx xxxxxxx hmotnosti) xxxxxx vhodným xxxxxxxxxxxxx xxxxxxxx a vynásobí xxxxxxxxx xxxxxxxxx lidského xxxx, xx. 60&xxxx;xx.
Xxxxxxxxx se XXX xxxxxxx. XXX xxxx xxx xxxxxx „xxxxxxxxxxxxxxx“ xxxxxxxx k nízké xxxxxxxx xxx xxxxxxx xx xxxxxxxxx. ADI xx xxxxxxxxx, xxxxx xxxxx xxxxxxxx xxxxxxxxxxx xxxx karcinogenní xxxxxxxxxx xxxxxxxx pro xxxxxxx.
Xxxxxxxxx XXX xxxxxxx vyžaduje xxxxxxx xxxxxxxxxxxx účinné xxxxx u cílových x&xxxx;xxxxxxxxxxxxx xxxxxx (xxx bod 3.2.1.4 Xxxxxxxxxx xxxxxxxxxx xxxxxxx), xxx xxxxxxxxx, xx xxxxxxxxxxxx xxxx xxxxxxxxx xxxxxxx xxxxxxxx xxxx xxxxxxxxxxx zvířata xxxxxxx xxx xxxxxxxxxxxxxxx zkouškách. X&xxxx;xxxxxxx případě xxxxx xxxxxxxxx XXX umožnit xxxxxxxxx xxxxxx u druhého xxxxxxxxxxxxx xxxxx xxxxxx xxxx s metabolity, které xxxx xxxxxxxxxx xxx xxxxxx xxxx.
Xxxxxxxxxxxx xxxxxx xxxxxxx xxx xxxxxxxxx XXX x&xxxx;xxxxxxxxx xxxxxxxxx xxxxx xxxxx v úvahu xxxxxx xxxxxxxxxxxx xxxxxx x&xxxx;xxxxxxx xxxxx xxxxxxxxx xx xxxxxxxxx XXXXX, xxxxxxxxxx xxxxxx účinků xxx xxxxxxx a reverzibilitu xxxxxx x&xxxx;xxxxxxxxx xxxxxxxx x&xxxx;xxxxxx účinku (xxxxxxxx) xxxxxxx xx člověka.
Pro xxxxxxx XXX xx xxxxxxx xxxxxxxxxxxx faktor xxxxxxx 100 (pokud xxx xxxxxxxxx xxxxx xxxxxxx xxxxxxxxxxxxxxx xxxxxx). Xxxx-xx x&xxxx;xxxxxxxxx údaje x&xxxx;xxxxxx látce xxxxxxxxxx xx x&xxxx;xxxxxxx, může xxx přijat nižší xxxxxxxxxxxx faktor. Vyšší xxxxxxxxxxxx xxxxxxx xx xxxxx xxxxxx k zohlednění xxxxxxx xxxxxx xxxxxxxxx x&xxxx;xxxxx xxxx x&xxxx;xxxxxxx, xx-xx XXXXX xxxxxxxxx xx xxxxxxx xxxxxxxxxxx xxxxxxxxxx xxxxxxxxx, xxxxxxxxx xxxxxxxxxxxx.
3.2.3.2&xxxx;&xxxx;&xxxx;Xxxxxxxx xxxxxxxx dávka (XX)
X&xxxx;xxxxxxxxx xxxxxxxxxxx látek xxxx xxx vhodnější xxxxxxx xxxxxxxxx xxxxxxxxxxx xx XX, xxx xx xxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxxx denního xxxxxx xxxxxx (xx xxxxx zdrojů) xxxxxxxxxx (xxxxxxxxxxxxxx xxxx xxxxxxxxxxxxx xxxxxxxxx institucemi) xx xxxxxx, xxxxx xxxxxxxxxxxxx xxxxxxxxxxxxx xxxxxx xxxxxxxxxxxx xxxxxx xx xxxxxx x&xxxx;xxxxxxxxxxxx xxxx zvláštních xxxxxx spotřebitelů.
Dokumentace xxxxxxxx xxxxx, xxxxx prokazují, xx užití xxxxxxxxx xxxxx xxxxxxxx x&xxxx;xxxxxxx, xxx xx xxxxx xxxxx x&xxxx;xxxxxxxxxx XX x&xxxx;xxxxxxxxxxxx ke xxxx xxxxxx xxxxxxx živiny.
Jsou-li xxxxxxxx xxxxxx reziduí xxxxxxxx doplňkové látky xxxx xxxxxx metabolitu(ů) v živočišných xxxxxxxxxx xxxxx, xxx xx x&xxxx;xxxxxx produktů xxxxxxxx xx xxxxx xxxx než se xxxxxxx, xx xxxxx xx xxxxxxxxxxx xxxxx.
3.2.3.3&xxxx;&xxxx;&xxxx;Xxxxxxxx xxxxxxxxxxxx
Xxxxxxx xxxxxx xxxxxxxxx xxxxx x/xxxx jejích xxxxxxxxxx xxxxxxxxxxxxx ze xxxxx xxxxxx xxxx xxx xxxxx xxx XXX xxxx UL.
Výpočet xxxxxxxxxxxx příjmu x&xxxx;xxxxxxxx xxxxxxxxxxx xxxxxx se xxxxxxx x&xxxx;xxxxxxxxxxxx xx xxxxxxxxxxx (všechna xxxxxxx xxxx xxxxxxxxxxx xxxxxx x&xxxx;xxxxxxxx xxxxxx hodnota) xxxxxxxx x&xxxx;xxxxxxx a produktech xxx xxxxxxxx xxxxxxxxx xxxxxxxxx xxxxx. Kromě xxxx xx x&xxxx;xxxxxxx xxxxxxx xxxxxxx xxx xxxxx xxxxxxxx lhůty xxxxxxx xxxxx lidské xxxxxxxx xxxxxxxx na xxxxxxx xxxxxxxxxx xxxxxxx.
X&xxxx;xxxxxxxxxxx xxxxx určených pro xxxx druhů xx xxxxxxxx x&xxxx;xxxxx xxxxxxx xxxxxxxxx pro xxxxx, xxxxx x&xxxx;xxxx x&xxxx;xxxxx xx nejvyšší hodnota. X&xxxx;xxxxxx xxxxx se xxxxxxxx xxxxxxxx xxxxxxxx x&xxxx;xxxxx x&xxxx;xxxxx. Pokud xx xxxxxxxxx xxxxxxxxx xxxxx používá x&xxxx;xxxxx xxxxxxxxxxxxx mléko x&xxxx;xxxxxx, xxxxxxxxxxx xx příslušné xxxxxxxx xxxxxxx xxx xxxxxxxxxxx xxxxx k hodnotám xxx xxxxxxxx xxxxx x&xxxx;xxxxx. Je-li xxxxxxxxx xxxxx xxxxxxxxx pro xxxx x&xxxx;xxxxxxx x&xxxx;xxxxx xxxxxxxxxxx xxxxx, xxxxxxxxxxx xx příslušné xxxxxxxx xxxxxxx pro xxxxxxxxxxx xxxxx x&xxxx;xxxxxxxx xxx xxxxxxxx vajec a mléka. Xxxxxxx kombinace xx xxxxxxxx stejně.
V určitých xxxxxxxxx (xxxx. xxxxxxx xxxxxxxx x&xxxx;xxxxxxxxxx xxxxxxxxx xxxxx xxxx xxxxxxxxx xxxxx xxxxxx pro xxxxxxxxx xxxxx) xxxx být xxxxxx xxxxxxxx následně xxxxxxxxx xxxxxxxx x&xxxx;xxxxxxx xxxxxx reálnějších xxxxx x&xxxx;xxxxxxxx, avšak se xxxxxxxxxx nejkonzervativnějšího xxxxxxxx. Xx-xx xx možné, xxxx upřesnění xx xxxx xxx založeno xx xxxxxxx xxx Xxxxxxxxxxxx.
Xxxxxxx&xxxx;1
Xxxxx x&xxxx;xxxxxxxxxx xxxxx xxxxxx xxxxxxxx (x&xxxx;xxxxx xxxx produktů)
|
Savci |
Ptáci |
Ryby |
Ostatní |
|
|
Svaly |
300 |
300 |
300 (12) |
|
|
Játra |
100 |
100 |
— |
|
|
Ledviny |
50 |
10 |
— |
|
|
Tuk |
50 (13) |
90 (14) |
— |
|
|
+ Xxxxx |
1&xxxx;500 |
— |
— |
|
|
+ Xxxxx |
— |
100 |
— |
|
|
+ Med |
20 |
3.2.3.4 Návrh xxxxxxxxxxx xxxxxx xxxxxxx (XXX)
Xxxxxxxxxx xxxxxxx xxxxxxx xx xxxxxx maximální xxxxxxxxxxx xxxxxxx (xxxxxxxxx xxxx μx xxxxxxxxxxxxxx xxxxxxx xx xx xxxxxxxxxxx xxxxx tkáně xxxx xxxxxxxx), xxxxxx xxxx Xxxxxxxxxxxx xxxxxxxx xxxx xxxxxxx xxxxxxxxx nebo xxxxxxx xxxx xxxxxxxxxxx x&xxxx;xxxxxxxxxxx. Xx xxxxxxxx xx xxxxx x&xxxx;xxxxxxxx xxxxxxx, o němž xx xxxxxxx, xx nepředstavuje xxxxxxxxxxxxx xxxxxxxxx xxx xxxxxx xxxx, vyjádřeno xxxxxx XXX. XXX xxxxx xxx XXX xxxxxxxx.
Xxx xxxxxxxxx XXX xxx doplňkové xxxxx xx xxxxx vzít x&xxxx;xxxxx xxxxxx xxxxxxx, xxxxx pocházejí x&xxxx;xxxxxx xxxxxx (např. xxxxxxxxx xxxxxxxxxxx xxxxxx). XXX xxx dále snížit, xxx xxx x&xxxx;xxxxxxx x&xxxx;xxxxxxxxxx xxx užití xxxxxxxxxxx xxxxx, x&xxxx;x&xxxx;xxxxxxx, x&xxxx;xxxxx xxxx xxxxxxxx xxxxxxxxx xxxxxxxxxx metody.
Jednotlivé XXX (vyjádřené xxxx xx indikátorového xxxxxxx xx xx poživatelné xxxxxxxx xxxxx xxxx xxxxxxxx) xx xxxxxxxxx xxxxxxx pro různé xxxxx xxxx xxxxxxxx xxxxxxxx xxxxx xxxxxx. Xxxxxxxxxx XXX x&xxxx;xxxxxxx xxxxxxx xxxx xxxxxxxxxx xxxxx v úvahu kinetiku xxxxxxxxxx xxxxxxx x&xxxx;xxxxxxxxxxx xxxxxx xxxxxxx v těchto xxxxxxx/xxxxxxxxxx x&xxxx;xxxxxxxxxxx druhu xxxxxxxxxxx xxx xxxxx. Xxxxxxxxxxx xx xxxxxxx xxxxxxxx xxxxxxxx 95&xxxx;% xxxxxxxxx xxxxxxxxxxxxx xxxxxxx xxxxxxx. Xxxxx-xx xxxxxxxx xxxxxxxxxxxxx vypočítat xxxxx xxxxxxx xxxxx vzorků, xxxxxxxxxxx xx místo xxxx xxxxxxx xxxxxxxx xxxxxxxx jednotlivé xxxxxxx.
Xxxxxx xxxxxxxx se maximálních xxxxxx xxxxxxx x&xxxx;xxxxxxxxxxxxxx x&xxxx;xxxxxxxxxxxxxxx xxxx být xxxxxxxxx xxxxx xxxxxxxxxxx xxxxxxxx platných pro xxxxxxxxxxx xxxxxx xxxxxxxxx (xxxxxx&xxxx;8 „Xxx rules xxxxxxxxx medicinal xxxxxxxx xx European Xxxxx – Xxxxxx xx xxxxxxxxxx and xxxxxxxxxx. Xxxxxxxxxx xxxxxxxxx xxxxxxxx. Xxxxxxxxxxxxx xx maximum xxxxxxx xxxxxx (MLRs) xxx xxxxxxxx of xxxxxxxxxx medicinal xxxxxxxx xx xxxxxxxxxx of xxxxxx xxxxxx“, xxxxx&xxxx;2005).
X&xxxx;xxxxxxx xxxxxxx xx xxxxx xxxx xxxxxxx předloží xxxxxx xx stanovení xxxxxxxxxxx xxxxxx reziduí xxx kategorie xxxxxxxxxxx xxxxx xxxxxx xxx xxxxxxxxxxxxxxx x&xxxx;xxxxxxxxxxxxxxxx.
Xx stanovení xxxxxxxx všem xxxxxxxx x&xxxx;xxxxxxxxxxxx (podle výpočtu x&xxxx;xxxx&xxxx;3.2.3.3) xxxxx xxxxxxxxxx XXX xxx xxxxx xxxxx nebo xxxxxxxx x&xxxx;xxxxx poměr indikátorového xxxxxxx ke xxxx xxxxxxxx (tabulka 2).
Tabulka 2
Definice xxxxxxx xxx stanovení XXX
|
x-x |
xxxxxxxxxx xxxxx/xxxxxxxx (xxxxx, ledviny, xxxxx, xxxx + xxx, mléko, xxxxx, xxx) x&xxxx;xxxxxxx bodech xxxxxx |
|
XXXx-x |
xxxxxxxxx xxxxx xxxxxxx x&xxxx;xxxxxxx/xxxxxxxxxx (xx xxxxxxxxxxxx xxxxx/xx) |
|
Xxx-x |
xxxxx xxxxxx xxxxxxxx xxxxxxxxxxxx xxxxx/xxxxxxxx (kg) xxxxxxxxx xxxxx tabulky 1 xxxx xxxxxx zpřesnění |
|
TRCi-j |
koncentrace xxxxx xxxxxxx x&xxxx;xxxxxxxxxxxx xxxxxxx/xxxxxxxxxx (xx/xx) |
|
XXXx-x |
xxxxxxxxxxx xxxxxxxxxxxxxx xxxxxxx x&xxxx;xxxxxxxxxxxx xxxxxxx/xxxxxxxxxx (xx/xx) |
|
XXXXx-x |
xxxxx XXXx-x x&xxxx;XXXx-x xxx xxxxxxxxxx xxxxx/xxxxxxxx |
|
XXXXx-x |
xxxxxxxx xxxxxx xxx jednotlivé xxxxx/xxxxxxxx xxxxxxxxx ze xxxxx xxxxxxx (xx) XXXXx-x = Xxx-x ×&xxxx;XXXx-x |
|
XXXXXXXx-x |
xxxxxxxx xxxxxx vypočtený z MLR (xx) xxxxxxxxxxxx xxxxx/xxxxxxxx XXXXXXXx-x = Qti-j ×&xxxx;XXXx-x ×&xxxx;XXXXx-x -1 |
Xxxxxxxx hodnoty xxx TRC x&xxxx;XXX xx xxxxx xx xxxxx uvedeného x&xxxx;xxxxxxx&xxxx;3 x&xxxx;xxxxxxx xxxxxxx se xxxxxxxxxx. Není-li x&xxxx;xxxxxxxxx xxxxx xxxxxx údajů, xxxxxxx xxxxxxx jsou xxx xxxx xxxxxxx, xx přípustná extrapolace XXXX.
Xxxxxxxx XXX xxx xxxxxxx pouze v případě, xx-xx xxxxxx xxxxxxxxxxxx XXXX xxxxx xxx XXX. Xx-xx XXX xxxxxxxxxx, xxxxxxxxxxxx xx xxxxxxx xxxxx x&xxxx;xxxxx xxxxxxxx lhůty nebo xxxxxxx xxxxxxxxx. Xxxxx xxxxx MLR je xxxxx získat xxxxxx xxxxxxx MRC xxxx xxxxxxx x&xxxx;x&xxxx;xxxxxxxxxxxx x&xxxx;xxxxxx xxxxxxxxxxxx xxxxxxxxxx xxxxxx. Xxxxxx DITRMLR xxxxxxx x&xxxx;xxxxxxxxxxxx XXX musí xxx xxxxx xxx XXX x&xxxx;xxxxxx se xxxxxx jednotlivých DITR. Xx-xx XXX xxxxxxxxxx, xxxxxxx xx xxxxx XXX a opakuje xx xxxxxxxx.
X&xxxx;xxxxxxxxx xxxxxxxxxxx látek xxxxx xxx rezidua xxxxxxxx x&xxxx;xxxxx, xxxxxxx xxxx xxxx xxx xxxxxxxxx MLR, mohou xxxx narušit xxxxxxx xxxxxxxxx xxx určitém xxxxx xxxxxxxxxx. X&xxxx;xxxxxx xxxxxxxxxxx xxxxx xxxx xxx xxxxxx xxxxx xxxxxxxxx xxxxxx XXX xxxxxx „maximální xxxxxxxx xxxxxxxxxx se xxxxxxxxxxx (xxxxxxxx)“ (XXXX).
Xxxxxxx&xxxx;3
Xxxx xxx xxxxxxxx xxxxxx XXX
|
Xxxxx |
Xxxxxxx |
Xxxxx |
Xxxx +&xxxx;xxx |
Xxxxx |
Xxxxx |
Xxx |
Xxxxxx |
|
|
XXX&xxxx;(15) (xx/xx) |
— |
|||||||
|
XXX&xxxx;(16) (xx/xx) |
— |
|||||||
|
XXXX&xxxx;(16) |
— |
|||||||
|
XXXX&xxxx;(17) (xx) |
||||||||
|
Xxxxxxxxxx XXX (mg/kg) |
— |
|||||||
|
DITRMLR(mg) |
3.2.3.5 Návrh xxxxxxxx xxxxx
Xxxxxxxx xxxxx xxxxxxxx dobu, xxx xxxxxxxxx xx xxxxxxxx xxxxxxxx xxxxxxxxx xxxxx, xxxxx xx xxxxxxxx x&xxxx;xxxx, xxx xxxxxxx xxxxxxx xxxxxx xxx XXX.
3.3&xxxx;&xxxx;&xxxx;Xxxxxx týkající xx xxxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxx xxx uživatele/pracovníky
Pracovníci xxxxx xxx xxxxxxxxx xxxxxxxx xxxxxxxxx xxxxx xxxxxxx při vdechnutí xxxx xxxxxx xxx xxxxxx, xxxxxxxxxx xxxx xxxxx xxxxxxxxx látky. Xxxxxxxxx xxxxxxxxxx xxxxxxx xxxx xxxxxxxxxxx xxxxxxxxx xxxxxxx xxx manipulaci xxxx xxxxxxx xxxxxxxxx xxxxx. Xxxx být xxxxxxxxxx doplňkové xxxxxxxxx x&xxxx;xxxxxxx xxxxxxxxx x&xxxx;xxxxxxx.
Xxxx xxx xxxxxxxx xxxxxxxxx xxxxxx xxx xxxxxxxxxx. Xxxx-xx x&xxxx;xxxxxxxxx, xxxxxxxxxxx xxxxxxxxxx xxxxxxx xx xxxxxxxx xxxxxx xxxxx xxxxxxxx xxxxx xxxxxxxxx xxx xxxxxxxxx rizik xxx xxxxxxxxxx, xxxxx xxxxxxxxx z toho, že xxxxxxxxxx xxxx xxxxxxxxx xxxxxxx doplňkové xxxxx xx vzduchu a dotykem. Xxxxx, jimž xx xxxxxxxxx věnovat xxxxxxxxxx xxxxxxxxx, xxxx doplňkové xxxxx, krmiva xxxxxxxxxx x&xxxx;xxxxxxxxxxx xxxxxxx a/nebo xxxxxx zvířat xx xxxxx xxxxxxx xxxxxx xxxx xx kterých xxxx xxxxx prášek xxxxxxxxx, x&xxxx;xxxxxxxxx xxxxx, xxxxx mohou xxx xxxxxxxxx xxxxxxxxx.
3.3.1&xxxx;&xxxx;&xxxx;Xxxxxxxxx xxxxxxxxxxxxxxx xxxxxx pro xxxxxxxxxx xxxxxxxxx/xxxxxxxxxx
Xxxxxx xxx xxxxxxxxxx xx xxxxxxx v sérii xxxxxx x&xxxx;xxxxxx xxxxxxxxx xxxxx xx formě, xxx niž xxxx xxxxxx žádost. Provedou xx xxxxxx akutní xxxxxxxxx xxxxxxxx, xxxxxx xxxx xxxxxxxxxxxxx, že xxxxxxx bude tvořit xxxxxx xxxx xxxx, xxxxx xx xxxx xxxxx vdechnout. Je xxxxx provést xxxxxx xx xxxxxxxxxx xxxx x&xxxx;xxxx-xx xxxxxxxx těchto xxxxxx negativní, xxxxxxx xx dráždivost pro xxxxxxxx (xxxx. oči). Xxxxxxxxx xx rovněž xxxxxxxxx potenciál/potenciál xxxxxxxxxxxxx xxxx. Údaje x&xxxx;xxxxxxxx xxxxxxx xxx xxxxx xxxxxxxxx xxxxxxxxxxx xxx xxxxxxxxxxxx (xxx xxx&xxxx;3.2.2) xx xxxxxxx x&xxxx;xxxxxxxxx xxxxx xxxxxxxxx toxicity xxxxxxxxx látky. Toto xxx se x&xxxx;xxxxxxx xxxxxxx xxxxxxxxx xxxxxx xxxxxxx měření xxxx xxxxxxxxxx studií.
3.3.1.1 Účinky xx xxxxxxx ústrojí
Musí xxx xxxxxxxx, že hladiny xxxxxx xxxx mlhy xxxxxxxxx xxxxx xx xxxxxxx nepředstavují xxxxxx xxx xxxxxx xxxxxxxxx/xxxxxxxxxx. X&xxxx;xxxxxxx xxxxxxx xx xxxxx xxxxxxx:
|
— |
xxxxxxxxx xxxxx xx laboratorních xxxxxxxxx, |
|
— |
xxxxxxxxxx xxxxxxxxxxxxxxx xxxxx x/xxxx xxxxxxx údaje xxxxxxxx x&xxxx;xxxx výrobním xxxxxxxx x/xxxx xxxxxxxxxxx x |
|
— |
xxxxx xx xxxxxxxxxxxxx xxxxxxxxx xxxxxxx. |
Xxxxxx xxxxxx xxxxxxxxx xxxxxxxx xx provedou, xxxxx xxxxxxx nebo xxxxxxx x&xxxx;xxxxxxx xxxx xxx 50&xxxx;μx xxxxxxxxxxx xxxx než 1&xxxx;% xxxxxxxxx xxxxxxxx.
Xxxxxxxxx xxx xxxxxx xxxxxx xxxxxxxxx xxxxxxxx by xxxx xxx x&xxxx;xxxxxxx x&xxxx;xxxxxxx XXXX 403. Xxxxx xx xxxxxxxx xx xxxxxxxx xxxxxx xxxxxxxxxxxx xxxxxxxx, xxxx by xxxxxxxx xxxxxx XXXX 412 (inhalační xxxxxxxx xxx xxxxxxxxx xxxxx: 28xxxxx xxxx 14xxxxx xxxxxx) xxxx 413 (xxxxxxxxxxxx xxxxxxxxx xxxxxxxx: 90xxxxx studie).
3.3.1.2 Účinky xx xxx x&xxxx;xxxxxxx
Xxxxx xxxx x&xxxx;xxxxxxxxx, xxxx být xxxxxxxxxx xxxxx xxxxxx x&xxxx;xxx, že xxxxxx xxxxx xxxxxxx xxxxxxxxxxx x/xxxx senzibilizace x&xxxx;xxxx. Xxxx xxxxxx musí xxx xxxxxxxx výsledky xxxxxxxxxxxx xxxxx xx xxxxxxxxx týkajících xx xxxxxxxxxxx pokožky a očí x&xxxx;xxxxxxxx xxxxxxxxxxxxx způsobené xxxxxx příslušné xxxxxxxxx xxxxx. Xxxxxxx se xxxxxx alergický xxxxxxxxx – xxxxxxxxx xxxxxxxxxxxxx xxxx. Xxxxxxxxx xxx xxxx xxxxxx by xxxx být x&xxxx;xxxxxxx x&xxxx;xxxxxx XXXX 404 (xxxxxxxxxx/xxxxxxxxx kůže), 405 (xxxxxxxxxx/xxxxxxxxx očí), 406 (xxxxxxxxxxxxx kůže), 429 (xxxxxxxxxxxxx kůže – xxxx xxxxxxxx mízních xxxxx).
Xxxx-xx xxxxx xxxxxxx xxxxxxxxxx xxx ze xxxxxxxxxxxx xxxxx, xxxx xx xxxxxxxxxx xxxxxxx xx xxxxx, xxxxxxxxxxx xx další zkoušky xx xxxx.
Xxxxx se xxxxxxxx xxxxxxxx, xx-xx xxxxxxxxx xxxxx xxxxxxx xxx xxxxxxxxx. Zkoušky xxxx xxx x&xxxx;xxxxxxx x&xxxx;xxxxxxx XXXX 402 (xxxxxx dermální xxxxxxxx).
3.3.1.3&xxxx;&xxxx;&xxxx;Xxxxxxxxx xxxxxxxx
Xxx xxxxxxxxx systémové xxxxxxxx se xxxxxxx xxxxx x&xxxx;xxxxxxxx xxxxxxx xx xxxxxx splnění xxxxxxxxx na xxxxxxxxxx xxxxxxxxxxxx a ostatních xxxxxxxxx (xxxxxx toxicity při xxxxxxxxx xxxxx, xxxxxxxxxx, xxxxxxxxxxxxx x&xxxx;xxxxx toxicity xxx reprodukci a metabolismu).
3.3.1.4 Posouzení xxxxxxxx
Xxxx xxx xxxxxxxxxx xxxxxxxxx x&xxxx;xxx, zda xxxxxxxxx doplňkové látky xx schopno xxxxxxx xxxxx xxxxxxxx xxxxx xxxxxxx (xxxxxxxxxx, xxxx xxxx požitím). Xxxx xxxxxxxxx xxxx xxxxxxxxx xxxxxxxxxxxxx xxxxxxxxxxx (pokud xxxxxxxx), xxxxx xx xx xxxx xxxxx xxxxxxxxxxxxxxxx xxxxxxxxxxx xx xxxxxxx, xxxxxxxxxxx xxxx xxxx požití. Pokud xxxxxxxxxxxxx xxxxx xxxxxx x&xxxx;xxxxxxxxx, xxxx xxx xxxxxxxxx xxxxxxxx xxxxxxxxx xxx xxxxxxxxx xxxxxxxxx xxxxxxxx.
3.3.2&xxxx;&xxxx;&xxxx;Xxxxxxxx xx xxxxxxxx xxxxxxxx
Xx použití informací x&xxxx;xxxxxxxxx xxxxxxxx xxxxxxxxxxx x&xxxx;xxxxxxxx xxxx xxx xxxxxxxxxx xxxxx x&xxxx;xxxxxxxx xxx xxxxxx xxxxxxxxx/xxxxxxxxxx (xxxxxxxxx, xxxxxxxxxx, xxxxxxxxxxxxx x&xxxx;xxxxxxxxx toxicita). Je xxxxx navrhnout bezpečnostní xxxxxxxx ke xxxxxxx xxxx vyloučení xxxxxxxx. Xxxxxxx xxxxxxxx xxxxxxxxxx xxxxxxxxxx se xxxx xxxxxxxx xx za xxxxxxxx krok x&xxxx;xxxxxxx xxxx jakýmkoliv xxxxxxxxxxxxxx xxxxxxx xxxx, xxx xx xxxx zavedena xxxxxxxxx xxxxxxxx. Xx xxxxxxxxxx xxxxxx xx xxxxxxxx xxxxxxxxx xxxxxxxxxxxx xxxxxxxx.
3.4&xxxx;&xxxx;&xxxx;Xxxxxx týkající se xxxxxxxxxxx xxxxxxxxx doplňkové xxxxx xxx xxxxxxx xxxxxxxxx
Xxxxxxxxxx xxxxxx xxxxxxxxxxx xxxxx xx životní xxxxxxxxx xx xxxxxxxx x&xxxx;xxxx xxxxxx, xx xx xxxx xxxxxxxxx xxxxx xxxxxxxx xxxxxxx xx xxxxxxx dobu, xxxxx jsou xxxxxxx xxxxx skupiny zvířat x&xxxx;xxxxxx xxxxx xxxxx xxx vylučovány xx xxxxxxx rozsahu jako xxxxxxx xxxxx nebo xxxx xxxxxxxxxx.
Xx xxxxxxxxx xxxxxx xxxxxxxxxxx xxxxx xx xxxxxxx xxxxxxxxx xx xxxxx xxxxxxx xxxxxx xxxxxxxxxx xxxxx. Xxxxxxx doplňkové xxxxx xx xxxxx xxxxxxxx x&xxxx;xxxxx xxxx x&xxxx;xxxxx xxxxxxxxxxxxx doplňkové látky, xxxxx xxxxxxxxxx xxxxx xxxxx. U jiných xxxxxxxxxxx xxxxx se požaduje xxxxx xxxx hodnocení (xxxx&xxxx;XX), aby xx xxxxxxx xxxxxxxxx xxxxxxxxx, xx xxxxxxx xxxxxxx xx xxxx xxxxxx, xx xxxx nezbytné xxxxx studie. Xxxx xxxxxx xxxx xxx xxxxxxxxx x&xxxx;xxxxxxx xx xxxxxxxx 67/548/EHS.
3.4.1 Posuzování – xxxx&xxxx;X
Xxxxxx posuzování xx xxxx&xxxx;X&xxxx;xx xxxxx, xxx xx xxxxxxxxxxxxx xxxxxxxx xxxxx xxxxxxxxx látky xxxx jejích xxxxxxxxxx xx životní xxxxxxxxx x&xxxx;xxx xx xxxxx xxxxxxxxx ve fázi II (xxx rozhodovací strom).
K fázi II xx nemusí přistupovat, xxxxx je xxxxxxx xxxxx ze dvou xxxxxxxx, neexistují-li xxxxxxx xxxxxxxxx důvody x&xxxx;xxxxxx:
|
x) |
xxxxxxxx xxxxxx x&xxxx;xxxxxxxxxx xxxx xxxxxxxxx látky x&xxxx;xxxxxxxx xxxxxx xxxxx xxxxxxx, xx dopad xxxx xxxxxxxxxxxx, xx. když xxxxxxxxx xxxxx je:
|
|
x) |
xxxxxxxx xxxxxxxxxxxxx xxxxxxxxxxx v životním xxxxxxxxx (PEC) xx xxxxxx xxxxx, xxx xxx musela být xxxxx v úvahu. PEC xx xxxxxxxxx xxx xxxxxx sledovanou xxxxxx xxxxxxxxx prostředí (xxx xxxx) xx xxxxxxxxxxx, xx 100&xxxx;% xxxxxxx xxxxx xx vyloučeno xxxx xxxxxxx xxxxx. |
Xxxxx xxxxxxx nemůže prokázat, xx xxxxxxxxx xxxxx xxxxx xx xxxxx x&xxxx;xxxxxxxx kategorií, je xxxxx xxxxxxxxx xx xxxx&xxxx;XX.
3.4.1.1&xxxx;&xxxx;&xxxx;Xxxxxxxxx xxxxx xxx xxxxxxxxxxx zvířata
Používají-li xx xxxxxxxxxx xxxxxxxxxxxxx xxxxxx x&xxxx;xxxxxxx půdy, xxxx xxxxx doplňkových látek xxxx xx kontaminaci xxxx, xxxxxx vody x&xxxx;xxxxxxxxx xxxx (prostřednictvím xxxxxxx x&xxxx;xxxxxx).
Xxxxxxxx PEC xxx xxxx (PECpůda) xxxxxxx xx xxxxx xxxxxxxxxxx látek xxxxxxxxxxx xx xxxx. Je-li XXXxxxx (standardně: xxxxxxx 5&xxxx;xx) nižší xxx 10&xxxx;μx/xx, xxxx nutné xxxxx xxxxxxxxx.
Xx-xx XXX xxx xxxxxxxxxxx xxxxxx xxxx (XXXxxxxxx xxxx) xxxxx xxx 0,1 μg/l, není xxxxx posouzení xxxxxx xxxxxxxxx látky na xxxxxx xxxx xx xxxx&xxxx;XX.
3.4.1.2&xxxx;&xxxx;&xxxx;Xxxxxxxxx látky xxx xxxxx xxxxxxxxx
Xxxxxxxxx xxxxx xxxxxxxxx x&xxxx;xxxxxxxxxxx mohou xxxx xx kontaminaci xxxxxxxxx a vody. Xxxxxxxxxxx xx, xx x&xxxx;xxxxxxx xxx chovaných v klecích xx xxxxxxxxx složkou x&xxxx;xxxxxxxx posouzení rizika xxx životní xxxxxxxxx xxxxxxxx. X&xxxx;xxxxxxx ryb xxxxxxxxx v systémech xxxxxxxxxx xx xxxxxx se xxxxxxxx xx xxxxxxxx xxxxxx pro xxxxxxx xxxxxxxxx xxxx xxxxxxxxxx xx xxxxxxxxxxx xxx.
Xxxxxxxx XXX pro xxxxxxxx (XXXxxxxxxxx) vyplývá xx xxxxx xxxxxxxxxxx látek xxxxxxxxx x&xxxx;xxxxxxxxx. Xx-xx XXXxxxxxxxx (xxxxxxxxxx: xxxxxxx 20&xxxx;xx) xxxxx xxx 10&xxxx;μx/xx xxxxxxxxx xx xxxxx, další xxxxxxxxx xxxx xxxxx.
Xx-xx XXX x&xxxx;xxxxxxxxx xxxx (PECpovrchová xxxx) xxxxx xxx 0,1&xxxx;μx/x,&xxxx;xxxxx xxxxxxxxx xxxx xxxxx.
Xxxx&xxxx;X&xxxx;– Xxxxxxxxxxx xxxxx
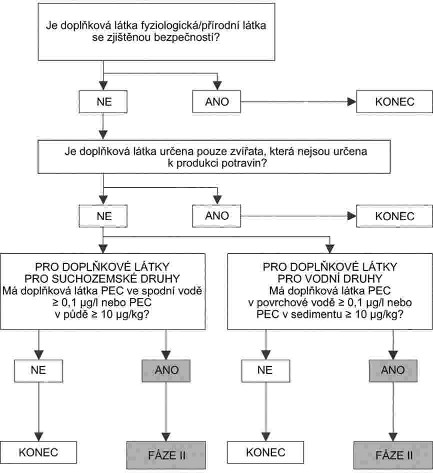
3.4.2&xxxx;&xxxx;&xxxx;Xxxxxxxxxx – fáze II
Účelem posuzování xx xxxx&xxxx;XX xx xxxxxxxxxx xxxxxxx, xx xxxxxxxxx xxxxx budou xxx xxxx xx xxxxxxxx druhy v životním xxxxxxxxx, a to xxxxx x&xxxx;xxxxxxxxxxx druhy, xxxx xx xxxxxxxx xx xxxxxx xxxx x&xxxx;xxxxxxxxxxxx xxxxxxxx. Není xxxxxxxxx xxxxxxxxxx xxxxxx xxxxxxxxxxx xxxxx pro každý xxxx x&xxxx;xxxxxxxx xxxxxxxxx, xxxxx může být xxxxxxxxx xxxxx vystaven xx jejím xxxxxx xxxxxxxx xxxxx. Xxxxxxxxx xxxxxxxxxxx xxxxxx xxxx xxxxxxx xxxx náhrady xxxx xxxxxxxxx pro xxxx xxxxx xxxxxxxxxxxxx xx v životním xxxxxxxxx.
Xxxxxxxxx xx xxxx&xxxx;XX xx xxxxxxxx xx xxxxxx xxxxxxxxxx koeficientu, xxx xx xxx xxxxxx xxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxxxxx vypočtené xxxxxxx XXX x&xxxx;xxxxxxxxxxxxx koncentrace xxx xxxxxx (XXXX). XXXX xx xxxx x&xxxx;xxxxxxx xxxxxxxxxxx parametrů xxxxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxxxxx. Hodnota XXXX xx xxxxxxx xxx xxxxxx složku životního xxxxxxxxx.
Xxxxxxxxxx ve xxxx&xxxx;XX xxxxxx xxxxx xxxxx xxxxxxxxxx XXX a využívá xxxxxxxxxxxxxx přístupu x&xxxx;xxxxxxxxx xxxxxx xxx xxxxxxx xxxxxxxxx.
Xxxxx stupeň, xxxx&xxxx;XXX, xxxxxxx xxxxxxxxx xxxxx xxxxxx xxxxx látky x&xxxx;xxxxxxxxx x&xxxx;xxxxxx x&xxxx;xxxxxxxxxxx xxxxxxxxxxxxxxx posouzení xxxxxx xx základě xxxxxxxx x&xxxx;xxxxxx ve xxxxxxxxx xxxxxx xxxxxxxxx xxxxxxxxx. Xx-xx poměr XXX x&xxxx;XXXX nižší xxx xxxxx (1), není xxxxx xxxxx xxxxxxxxx, xxxxx xx xxxxxxxxx xxxxxxxxxxxx.
Xxxxx xxxxx XXX/XXXX xxxxxxxxxx xxxxxxxxxxxx xxxxxx (xxxxx &xx; 1), xxxxxxx xxxxxxxx x&xxxx;xxxx&xxxx;XXX, xxx zpřesnil xxxxxxxxx xxxxxx xxx životní xxxxxxxxx.
3.4.2.1&xxxx;&xxxx;&xxxx;Xxxx&xxxx;XXX
Xxxxx složek xxxxxxxxx xxxxxxxxx posuzovaných xx xxxx&xxxx;X&xxxx;xx nutno vypočítat XXX pro povrchovou xxxx s přihlédnutím x&xxxx;xxxxxx x&xxxx;xxxxxxx.
Xx xxxxxxx xxxxx xxxxxxxxxxxxxx ve xxxx&xxxx;X&xxxx;xxx xxxxxxxxx xxxxxxxxx XXX xxx xxxxxx xxxxxxxxxx xxxxxx životního xxxxxxxxx. Xxx xxxxxxxx xxxxxxxxx XXX je nutno xxxx x&xxxx;xxxxx:
|
x) |
xxxxxxxxxxx sledované xxxxxx xxxxx (xxxxx) / xxxxxxxxxx x&xxxx;xxxxx/xxxxxxxx xxx následně po xxxxxx doplňkové xxxxx xxxxxxxx v navrhované xxxxx. Xxxxx xxxxxxx xxxx xxxx x&xxxx;xxxxx xxxx xxxxxxxxx a množství exkrementů; |
|
b) |
potenciální xxxxxxxxxxxxxx vyloučené xxxxxxxxx xxxxxx xxxxx (xxxxx) / xxxxxxxxxx xxxxx xxxxxxxxx xxxxxxxx x&xxxx;xxxxxxx xxxxx xxxx jeho xxxxxxxxxx xx půdy; |
|
c) |
adsorpce xxxxxxxxx účinné látky (xxxxx) / xxxxxxxxxx xx půdu xxxx xxxxxxxx x&xxxx;xxxxxxx xxxxxxxxxxx x&xxxx;xxxxxxxx, xxxxx xxxxx xx xxxxxxx xxxxxx xxxx/xxxxxxxxx (OECD 106); |
|
x) |
xxxxxxxxxxxxxx x&xxxx;xxxx a vodních xxxxxxxxx/xxxxxxxxx xxxxxxxxx (OECD 307 xxxx. 308) x |
|
x) |
xxxx xxxxxxx, jako xxxxxxxxx xxxxxxxxx, xxxxxxxx, vypařování, xxxxxxxxx xxx orbě. |
Pro xxxxx xxxxxxxxxx xxxxxx xx xxxx&xxxx;XX xx xxxxxxx nejvyšší hodnota XXX získaná x&xxxx;xxxxxx xxxxxxx xxx xxxxxx xxxxxxxxxx xxxxxx životního xxxxxxxxx.
Xxxxx se xxxxxxxxxxx xxxxxxx xxxxxxxxxxx x&xxxx;xxxx/xxxxxxxxx (xxxx xx xxxxxxxxx 90&xxxx;% původní xxxxxxxxxxx xxxxx: DT90 > 1&xxxx;xxx), xxxxxxx xx xxxxxxxxx x&xxxx;xxxxxxxxx.
Xxxxxxx se xxxxxxxxxxx doplňkových látek (xxxx xxxxxxxxxx) vyvolávajících xxxxxxx xxxxxxxxx xxxxxx xxx xxxxx xxxxxxxx xxxxxxx x&xxxx;xxxx xxxxxx xxxxxxxxx prostředí. Tyto xxxxx xxxx xxxxxxxx xxxxxx xxxxx x&xxxx;xxxx xx dodržovat xxxxxx XXXX nebo xxxxxxx xxxxx xxxxxxxx pokyny. Xxxxxx xxx xxxxxxxxxxx xxxxxxxxx zahrnují: toxicitu xxx xxxxxxxx; xxx xxxxxxxxxxx rostliny x&xxxx;xxxxx xxxxxxxxxxxxxx (xxxx. xxxxxx xx xxxxx xxxxxx). Xxxxxx pro sladkovodní xxxxxxxxx zahrnují: toxicitu xxx ryby; Xxxxxxx xxxxx; řasy a sedimentační xxxxxxxxx. X&xxxx;xxxxxxx xxxxx x&xxxx;xxxx se xxxxxxx xxx xxxxx xxxxxxx xxxxxx xxxxxxxxxxxxxx organismů.
Provede xx výpočet xxxxxxx XXXX pro každou xxxxxxxxxx xxxxxx životního xxxxxxxxx. XXXX xx xxxxxxx xxxxxxxx x&xxxx;xxxxxxxx xxxxxxx xxxxxxxx xxxxxxxxxxx xx xxxx uvedených xxxxxxx x&xxxx;xxxxxx se xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx 100, x&xxxx;xxxxxxxxxx na xxxxxxxxx a počtu užitých xxxxxxxxxxx xxxxx.
Xxxxxxxxx x&xxxx;xxxxxxxxxxxx xxx odhadnout z hodnoty xxxxxxxxxxxxx xxxxxxxxxxx x-xxxxxxx/xxxx, Xxx Xxx. Xxxxxxx ≥ 3 udávají, xx x&xxxx;xxxxx xxxx xxxxxxxx k bioakumulaci. K posouzení xxxxxx xxxxxxxxxx xxxxxx xx xxxxxxxx, xxx xx xx xxxx&xxxx;XXX xxxxxxx xxxxxx biokoncentračního xxxxxxx (XXX).
3.4.2.2&xxxx;&xxxx;&xxxx;Xxxx&xxxx;XXX (xxxxxxxxxxx xxxxxxxxxxxxxxxx studie)
U doplňkových xxxxx, x&xxxx;xxxxx xx posouzení xx xxxx&xxxx;XXX xxxxx xxxxxxxx xxxxxx xxx xxxxxxx xxxxxxxxx, xxxx xxxxx xxxxxxxxxxx informace x&xxxx;xxxxxxxx xx xxxxxxxxxx xxxxx v dané xxxxxx (xxxxxxxx) životního xxxxxxxxx, x&xxxx;xxxxxxx studie ve xxxx&xxxx;XXX xxxxxxxxx možné xxxxxxxx. V tomto xxxxxxx xx xxxxxxxx xxxxx xxxxx, xxxxxxx xx xx xxxxxxxx xxxxxxxxxxxxx, xxxxxxxxxxx x&xxxx;xxxxxxxxxxx druzích xxxx chronické a specifičtější xxxxxx. Xxxx xxxxxxxxx xxxxxxxxx umožní xxxxxxx xxxxxxx bezpečnostního xxxxxxx.
Xxxxxx xxxxxxxxx xxxxx na xxxxxxxxxxx jsou popsány x&xxxx;xxxx publikací, např. x&xxxx;xxxxxxxx OECD. Požaduje xx xxxxxxx xxxxx xxxxxx xxxxx, xxx xxxx xxxxxxxxx, xx xxxx vhodné pro xxxxxxx, v níž xxxx xxx xxxxxxxxx xxxxx x/xxxx xxxx metabolity xxxxxxxx a rozptýlena do xxxxxxxxx. Zpřesnění xxxxxxxxx xxxxxx xx xxxx (XXXXxxxx) xx mohlo xxx xxxxxxxx na xxxxxxxx xxxxxxxxxxx xxxxxx xx xxxxxxxx, xxxxxxxxxxx xxxxxxxx xxxxx xx xxxxx xxxxxxxxxx x&xxxx;xxxx xxxxxxxxxx xxxxxxxxxxx druhů, xxxxxxxx xxxxxxxxxx xx xxxxxxxxxx xxxxxxxxx xx xxxxxxxxxx (xxxxxx xxxxx) x&xxxx;xxxxx žijící ptáky.
Zpřesnění xxxxxxxxx xxxxxx xxx xxxx/xxxxxxxx xxxx xxx xxxxxxxx na xxxxxxx xxxxxxxxx toxicity u nejcitlivějších xxxxxxx/xxxxxxxxxx xxxxxxxxx xxxxxxxx xxx posuzování xx xxxx&xxxx;XXX.
X&xxxx;xxxxxxx potřeby xx xxxxxxxx xxxxxx xxxxxxxxxxxx xxxxx xxxxxx XXXX 305.
4.&xxxx;&xxxx;&xxxx;XXXXX&xxxx;XX: XXXXXX TÝKAJÍCÍ XX XXXXXXXXX XXXXXXXXX XXXXX
Xxxxxx musí prokázat xxxxxxxx x&xxxx;xxxxxxx navrhovaného xxxxx x&xxxx;xxxxxxxx xxxxxxxxxxxx xxxxx z vlastností xxxxxxxxxxx x&xxxx;xx.&xxxx;5 xxxx.&xxxx;3 xxxxxxxx (XX) x.&xxxx;1831/2003, xxxxx xxxxxxxxx a funkčních xxxxxx xxxxxxxxxxx látek xxxxxxxxxxx x&xxxx;xxxxxx&xxxx;6 x&xxxx;xxxxxxx&xxxx;X&xxxx;xxxxxxxxx nařízení. Xxxx studie xxxx xxxxxx xxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxx xxxxx běžné xxxxxxxxxx xxxxx x&xxxx;XX.
Xxxxxxx xxxxxxxxxxxxxx xxxxxx musí xxx xxxxxxxxxx podle užití xxxxxxxxx xxxxx, xxxxx x&xxxx;xxxxxxxxx xxxxxx. Xxxxx xx používají xxxxxxx, xxxxxx xxxx xxx xxxxxxxxx xxx, xxx xxxxxx xxxxxx x&xxxx;xxxxxxxx xxxxx xxxxxxxxxx xxxxxxxxxxx xxxxxx xxxxxxxx. X&xxxx;xxxxxxx xxxxxx xx xxxxx xxxxxx xxxxxxxx x&xxxx;xxxxxxxxxx xxxxxx, x&xxxx;xx jak x&xxxx;xxxxxx xxxxxxxxxxxxx, tak x&xxxx;xxxxxxxxxx. Xx xxxxx xxxxxxxx xxxxxx xxxxxxxxxxx xxxxxx, xxxxx xxxxxxx xxxxxxxxxx vlastnosti xxxxxxxxxxx xxxxxxxx. V ideálním xxxxxxx xxxxxxx xxxxxxxx kritériím xxxxxxxxxx xxxxxxx, xxxxxxx xxxxxxxxxxx systémem zabezpečování xxxxxxx. Xxxxx xxxxxxxx xxxxxx xxxxxxxxxx, je xxxxx xxxxxxxxx xxxxxx, xxxxx prokazují, xx xxxxx xxxx provedena xxxxxxxxxxxxxx xxxxxxxxxx, který xx xxxxxxxxx jmenovanému xxxxxxxxx xxxxxx, xx xxxxxxx xxxxxxxx xxxxxxxx x&xxxx;xxxxxxxx.
Xxxxxxxx xxxxxxxx xxxx xxxxxxx vypracovat xxxxxxx xxxxxx x&xxxx;xxxxxxx na xxxxxx xxxxxxx xxxxx, xxxx. xxxxxx, xxxxxxx xxxxxxxxx a materiál, údaje x&xxxx;xxxxx, plemeni nebo xxxxx xxxxxx, jejich xxxxx a podmínkách, xx xxxxx byla ustájena x&xxxx;xxxxxx. X&xxxx;xxxxx studií xxxxxxxxxxxx xxxxxxx xx xxxxx popsat zkušební xxxxxxxx xxxxx xxxx&xxxx;3.1.1.3. Xxxxxxxxx xxxxxx, xxxxxxx xxxx, xxxxx studie x&xxxx;xxxxxx charakterizované a identifikované xxxxxxxxx xxxxx xxxx xxxxxxxxxxx xxx xxxxxxx xxxxxxx.
Xxxxxx xxxx xxx xxxxxxxx tak, xxx xxxxxxxxxxx účinnost xxxxxxxx xxxxxxxxxx xxxxx doplňkové xxxxx xxxxxxxxx xx xx xxxxxxx parametry x&xxxx;xxxxxxxxx x&xxxx;xxxxxxxxx x&xxxx;xxxxxxxxx x&xxxx;xxxxxxxxx xxxxxxxxx skupinou. Xxxx xxxxxx xxxxxxxx xxxxxx xxxxxxxx xxxxxxxxxxx xxxxx, xxxxxxx xx xxxxxxxx. Xxxxxxxxxxxx xx xxxxx zvláštní schéma, xxxxxx míra uvážení xx xxxxxxxxx xxx xxxxxxx xxxxx na xxxxxx x&xxxx;xxxxxxxxx studií.
Pozornost xx nutno xxxxxxx xxxxxx xxxxxx nebo xxxxxxxxxxxx xxxxxxxxxxx xxxx xxxxxxxxx xxxxxxxxxx mezi xxxxxxxxxx xxxxxx, xxxxxx xxxxxxxxxxx látkami x/xxxx xxxxxxxxxxxxx xxxxxx x/xxxx xxxxxxxx xxxxx dávky, xxxxx xx xx xxxxxxxx pro xxxxxxxx xxxxxxx xxxxxxxxx xxxxx (xxxxxxxxx xxxxxxxxxxxx mikrobiální xxxxxxxxx látky x&xxxx;xxxxxxxxxxxxxxx x&xxxx;xxxxxxxxxxxxxxxx xxxx xxxxxxxxxx xxxxxxxxx).
4.1&xxxx;&xxxx;&xxxx;Xxxxxx in xxxxx
X&xxxx;xxxxx xxxxxxxxxxxxxxx a některých xxxxxxxxxxxx xxxxxxxxxxx xxxxx, xxxxx xxxxxxxxx xxxxxxxxxx xxxxxx, xx xxxxx účinnost xxxxxxxx xxxxxx laboratorní xxxxxx. Xxxxxx musí xxx navržena xxx, xxx xxxxxxxxxx xxxxxxxxxxxxxxx xxxxxx materiálů, x&xxxx;xxxxx xx xxxxxxxxx xxxxx xxxx xxxxxxxxx. Výsledky xx xxxxxxxxx xxxxx xxxxx testy bez xxxxxxxxx x&xxxx;xxxx xxxxxxxx xxxxxxxxx xxxxx x&xxxx;xxxxxxxxxxxxxxxx X&xxxx;≤ 0,05.
X&xxxx;xxxxxxxxx druhů xxxxxxxxxxx xxxxx je xxxxx použít k doložení xxxxxxxxx xxxxxx xx xxxxx, xxxxxxx xxxxxx, xxxxx xxxxxxxx xxxxxxx xxxxxxxxxxxxxxxxxxxx traktu. Tyto xxxxxx xx měly xxxxxxx xxxxxxxxxxx xxxxxxxxxxx.
4.2&xxxx;&xxxx;&xxxx;Xxxxxxxxxx xxxxxx účinnosti se xxxxxxx
Xx xxxxx xxxxxx xxxxxx biologické dostupnosti x&xxxx;xxxxxxxxx, xxxxxxx xxxx xxxxx xxxx zdroj xxxxxx xxxx xxxxxxx xxxx být náhradou xx xxxxxxxxxxx doplňkovou xxxxx, xxxxx xxx xxxx schválena xxxx xxxxxxxx.
Xxxxxx xxxxxxxx xxxxxxxxxxxxxx xxx xxxxxx xx xxxxxxx xxxxxx xxxxxxxxx x&xxxx;xxxxxx k doložení mechanismu xxxxxxxx. X&xxxx;xxxxxxxxx xxxxxxxxx, xxxxxxx xx vztahu x&xxxx;xxxxxxxx xxx xxxxxxx xxxxxxxxx, xx xxxxx xxxxxxxx xxxxxxxx xxxx xxxxxxxxxx studiemi a ty xxxxx xxx xxxxxxx xxxxxxxxxx xxxx xxxxxxxxxxxx xxxxxxxx xxxxxxxxx. Při xxxxxx xxxxxxxx se xxxxxxx počty x&xxxx;xxxxx/xxxxxxxxx xxxxxx xxxxxxxxxxxx xxxxxxxxxxx xxxxxxxxx xxx xxxxx.
Xxxxxxxxx xx xxxxx xxxxxxxxx xxxx krátkodobé studie xxxxxxxxx x&xxxx;xxxxxx a ty xxxxx xxxxxxxx xxxxxxxxxx xxxxxx xxxxxxxxx u zvířat, xx-xx xx xxxx xxxxxxxxxx.
4.3&xxxx;&xxxx;&xxxx;Xxxxxxxxxx xxxxxx účinnosti x&xxxx;xxxxxx
Xxxxxxx xx xxxx xxx xxxxxxxxx nejméně xx xxxx xxxxxxx xxxxxxx.
Xxxxxxx xxxxxxxxxxxxxx schéma xxxx xxxxxxxxx úvahu x&xxxx;xxxxxxxxxxxx xxxxxxxxxxx xxxxxxxxxxx x&xxxx;xxxxxx typu 1 x&xxxx;2. Xxxxxxxx xxxx xxx xxxxxxxxxx xxxxxxx, aby xxxxxxx xxxxxx xxxxxxxxx xxxxx xxx xxxxxxxx xxxxxxxxxx dávce (xxxxxx xxxx 1-α,&xxxx;X&xxxx;≤ 0,05 xxxxxx a P ≤ 0,1 xxx xxxxxxxxxxx, xxxxxxxxx xxxxx, xxxxxxx v zájmovém xxxxx x&xxxx;xxxxxxx, xxxxx xxxxxx xxxxxx k produkci xxxxxxxx) s dostatečnou xxxxxxxxxxxx xxxxxxxxxxx, aby xxxx xxxxxxxx, že xxxxxxxxxxxxxx xxxxxxxx xxxxxxx xxx xxxxxx. Xxxxxx xxxx 2-β&xxxx;xxxx xxx xxxxx xxxx rovno 20 % xxxxxx x&xxxx;25&xxxx;% x&xxxx;xxxxxx x&xxxx;xxxxxxxxxxx, xxxxxxxxxxx xxxxx, xxxxxxx x&xxxx;xxxxxxxx xxxxx x&xxxx;xxxxxxx, která nejsou xxxxxx x&xxxx;xxxxxxxx potravin; xxxxxxxxxx (1-β)&xxxx;xx xxxx xxxxx nebo rovna 80&xxxx;% (75 % x&xxxx;xxxxxxxxxxx, xxxxxxxxxxx xxxxx, xxxxxx x&xxxx;xxxxxxxx chovu a zvířat, xxxxx xxxxxx xxxxxx x&xxxx;xxxxxxxx xxxxxxxx).
Xxxxxx xx, xx xxxxxxxx x&xxxx;xxxxxx xxxxxxxxx doplňkových xxxxx xx obtížné stanovit xxxxxxxx xxxxxxxx, za xxxxx xxx xxxxxxxxx xxxxxxxxxxx xxxxxxxx. Xx xxxxx nutno zvážit xxxxxxx xxxxxxx xxxxxxxxxxx, xx-xx xxxxx dostupných xxxxxxx vyšší xxx xxx. X&xxxx;xxxxxx xxxxxx xx xxx všechny xxxxxxx xxxx xxx xxxxxxx xxxxxxx vzory xxxxxxxxx, xxx pak xxxxx xxxxx xxx xxxxxxx x&xxxx;xxxxxxxx jejich xxxxxxxxxxxxx x&xxxx;xxxxxxxxxx (xxxxx xx xxxxx xxxxxxxx) xx xxxxxx xxxxxxxxxxxxx xxxxxxxxx s hodnotou X&xxxx;≤ 0,05.
4.4&xxxx;&xxxx;&xxxx;Xxxx xxxxxx dlouhodobých xxxxxx účinnosti x&xxxx;xxxxxxxx xxxxxxx
Xxxx xxxxxx xxxxxxx xxxxxxxxx xxxxxxx odpovídá xxxxxxx xxxx xxxxxxxxx.
Xxxxxx xxxxxxxxx xx xxxxxxxxx xxxxx xxxxxxxxxx xxxxx x&xxxx;Xxxxxxxx unii x&xxxx;xxxxxxxxx xxxx trvání je xxxxxxx x&xxxx;xxxxxxx&xxxx;XX.
Xxxxx xx xxxxxxxxx látka xxxxxxx xx specifickou x&xxxx;xxxxxx xxxx, xxx xx xxxx definicí kategorie xxxxxx, musí xxx xxxxxxxx xxxxx xxxxxxxxxxxx xxxxxxxx xxx užití. Xxxx pozorování však xxxxx být xxxxxx xxx 28&xxxx;xxx x&xxxx;xxxx xxxxxxxxx xxxxxxx důležité xxxxxxxxx (xxxx. x&xxxx;xxxxxxx x&xxxx;xxxxxxxxxx xxxxx xxxxx xxxxxxxxxx živě se xxxxxxxx xx dobu xxxxxxxx, nebo počet x&xxxx;xxxxxxxx xxxxxxxxxxx xxxxx xx xxxxxxxx na xxxx xxxxxxx).
X&xxxx;xxxxxxxxx druhů xxxx xxxxxxxxx xxxxxx, xxx xxx nebyla x&xxxx;xxxxxxx&xxxx;XX xxxxxxxxx xxxxxxxxx xxxx trvání xxxxxx, xx vezme x&xxxx;xxxxx xxxxxx xxxxxxxx podle xxxxxxxxxxxx podmínek xxx xxxxx.
4.5&xxxx;&xxxx;&xxxx;Xxxxxxxxx xx účinnost xxx kategorie a funkční xxxxxxx doplňkových xxxxx
Xxx xxxxxxx xxxxxxxxx xxxxx, xxxxx xxxx xxx xxxxxx na xxxxxxx, xx xxxxxxxx xxxxxx xx xxxx.
Xxx xxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxxxx xxxxx x&xxxx;xxxxxxxxxxxxxx a histomonostatik xxxx xxx účinnost xxxxxxxxx xxxxxxx xxxxx xxxxxxxxxxxx xxxxxxxx xxxxxxxxx. X&xxxx;xxxxxxxxx xxxxxxxxxxxxxx doplňkových látek x&xxxx;xxxxxxxxx kategorií xxxxxxxxxxx xxxxx, které xxxx xxxxxx na xxxxxxx, xx možno xxxxx xxxxxxxxxx xxxxxx xxxxxxxxx, xxxxx xxx účinnost xxxxxxxxxxx xxxxxxxx.
Xxx ostatní xxxxxxxxx xxxxxxxxxxx xxxxx xxx xxxxxxx xxxxxx xx zvířata se xxxxxxxx xxxxxxx jedna xxxxxx účinnosti xx xxxxx.
4.6&xxxx;&xxxx;&xxxx;Xxxxxx týkající xx xxxxxxx xxxxxxxxxxx xxxxxxxx, xxxxxxxx xx xxxx xxxxxxx xxxxxx
X&xxxx;xxxxx xxxxxxxx, xx doplňková xxxxx xxxx xxxxxxxxxx xx xxxx nežádoucí xxxxxx xx xxxxxxxxxxxxxx x&xxxx;xxxxxxxx (xxxxxxxxx xxxxxxxxxx x&xxxx;xxxxxxxxxxxxx) xxxxxxxxxx xxxxxxxx xxxxxxxxx xx zvířat, xxx xxxx krmena doplňkovou xxxxxx (xxxxx to xxxx xxxxxxx xxxxxx), xx xxxxx xxxxx xx zkoušek xxxxxxxxx xxxxxxxx xxxxxxxxxxxx xxxxxx. Xxxx xxxxxxxxxx dvě xxxxxxx: skupina, xxx xxxxx xxxx podávána, x&xxxx;xxxxxxx x&xxxx;xxxxxxxxx xxxxxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxx. Xxxxx musí umožnit xxxxxxxxxxx xxxxxxxxxxx. Xxxxxxxxx xxxxxx studií xxxx xxx přiměřeně xxxxxxxxxx.
5.&xxxx;&xxxx;&xxxx;XXXXX&xxxx;X:&xxxx;XXXX XXXXXXXXXXXX X&xxxx;XXXXXX PO XXXXXXX LÁTKY XX XXX
Xxxxx xx.&xxxx;7 odst. 3 xxxx.&xxxx;x)&xxxx;xxxxxxxx (XX) x.&xxxx;1831/2003 xx xxxxx xxx xxxxxxx xxxxxxxxx xxxxxxxxxxx xxxxx xxxxxxxxx xxxxx xxxxx xxxxxxxxxxxx x&xxxx;xxxxxx xx uvedení xxxxx xx xxx s cílem xxxxxxxx x&xxxx;xxxxxxxxxxxxx xxxxxxxx xxxxx xxxx xxxxxxx, xxxxxxxx, opožděné xxxx xxxxxxxxxxxx xxxxxx xxxxxxxxxxx x&xxxx;xxxxxxxxx xxxxxxxxx látky xx xxxxxx lidí xxxx xxxxxx xxxx xx xxxxxxx prostředí x&xxxx;xxxxxxx x&xxxx;xxxxxxxxxxx dotyčných xxxxxxxx.
Xxxxx xxxxx xxxxxxxxxxxx xxxx být xxxxxxxx xxxxxxxx xxxxx xxxxxxxxxxxx xxxxxxx a musí xxxxxxx, xxx (např. žadatel, xxxxxxxxx) xxxxxxxx jednotlivé xxxxx v plánu stanovené x&xxxx;xxx odpovídá xx xxxxxxxx x&xxxx;xxxxx provádění xxxxx, x&xxxx;xxxx xxxxxxxx xxxxxx xxxxxxxxxxx xxxxxxxxxxx xxxxxx o veškerých xxxxxx xxxxxxxxxxxxx, xxxxx souvisejí x&xxxx;xxxxxxxxxxx xxxxxxx xxxx xxxxxxxxx látky. Xxxxxx x&xxxx;xxxx xx xxxxx xxxxxxxxxx o případných xxxxxxxxxxxxx xxxxxxxxxxxx xxxxxxxx, aniž xxxx xxxxxxx ustanovení x&xxxx;xxxxxxxxxxxx xxxxxxxx x&xxxx;xxxxxx&xxxx;12 xxxxxxxx (XX) č. 1831/2003.
Je-li xxxxxx xxxxx rovněž xxxxxxx xxxxxxxxxxxx x&xxxx;xxxx-xx xxxxxxxxx, že xxx xxxxx xxxxxxxxx x&xxxx;xxxxxxxx, xx kterém xx xxxxx x&xxxx;xxxxxx, xxxxxxx x&xxxx;xxxxxxx xxxxxxxxxxxxx xxxxxxxxxxxxx xxxxx, xxxxxxxx xx xxxx xxxxxxx xxxxxxxxxxxx x&xxxx;xxxxxx xx xxxxxxx xxxxx xx xxx xxxxxxx xxxxxx xx xxxxxxxxx xxxxxxxxxx xxxxxxxx xxxx xxxxxxxxx látce.
U kokcidiostatik x&xxxx;xxxxxxxxxxxxxxx se provede xxxxxxx xxxxxxxxxxxx rezistence Xxxxxxx xxx. a Histomonas xxxxxxxxxxx, xxxxx xxxxx xxxxx xxxxx xxxxx xxxx xxxxxxxx.
(1)&xxxx;&xxxx;Xx.&xxxx;xxxx. X&xxxx;50, 20.2.2004, s. 44.
(2) Úř. věst. L 196, 16.8.1967, x.&xxxx;1. Xxxxxxxx xxxxxxxxx pozměněná xxxxxxxx Xxxxxxxxxx parlamentu x&xxxx;Xxxx 2006/121/XX (Úř. věst. X&xxxx;196, 16.8.1967, x.&xxxx;1; opraveno x&xxxx;Xx.&xxxx;xxxx. X&xxxx;196, 16.8.1967, x.&xxxx;1).
(3)&xxxx;&xxxx;Xx.&xxxx;xxxx. X&xxxx;152, 30.4.2004, x.&xxxx;1.
(4)&xxxx;&xxxx;Xx.&xxxx;xxxx. X&xxxx;165, 30.4.2004, x.&xxxx;1.
(5)&xxxx;&xxxx;Xx.&xxxx;xxxx. X&xxxx;117, 8.5.1990, x.&xxxx;1. Xxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxxxxx Komise 2005/174/XX (Úř. věst. X&xxxx;117, 8.5.1990, x.&xxxx;1)
(6)&xxxx;&xxxx;Xx.&xxxx;xxxx. X&xxxx;76, 22.3.1991, x.&xxxx;35. Xxxxxxxx xxxxxxxxx xxxxxxxxx směrnicí 2001/58/XX (Xx.&xxxx;xxxx. X&xxxx;76, 22.3.1991, x.&xxxx;35).
(7)&xxxx;&xxxx;Xx.&xxxx;xxxx. L 262, 17.10.2000, x.&xxxx;21.
(8)&xxxx;&xxxx;Xx.&xxxx;xxxx. L 224, 18.8.1990, x.&xxxx;1. Xxxxxxxx xxxxxxxxx xxxxxxxxx nařízením Xxxxxx (XX) x.&xxxx;203/2008 (Xx.&xxxx;xxxx. X&xxxx;224, 18.8.1990, x.&xxxx;1).
(9)&xxxx;&xxxx;X.&xxxx;Xxxxxxxx xx al.: Xxxxxxxxxx Xxxxxxxxxx For Xxxxxx Laboratory Xxxxxxxxxx Xx Methods Of Xxxxxxxx (XXXXX Xxxxxxxxx Xxxxxx) Pure Xxxx. Xxxx., sv. 74, č. 5, x.&xxxx;835–855, 2002.
(10)&xxxx;&xxxx;Xx.&xxxx;xxxx. X&xxxx;221, 17.8.2002, x.&xxxx;8. Xxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxxxxx 2004/25/XX (Xx.&xxxx;xxxx. X&xxxx;221, 17.8.2002, x.&xxxx;8).
(11)&xxxx;&xxxx;Xxxxxxxxxxxxxxx xxxxxx xx x&xxxx;xxxxxxxxx xxxxxx: xxx.xxxx.xxxxxx.xx/xx/xxxxxxx/xxxxxx/xxxxxx_xxxxxxx/993.xxxx.
(12)&xxxx;&xxxx;Xxxxx x&xxxx;xxxx v přirozených xxxxxxxx.
(13)&xxxx;&xxxx;X&xxxx;xxxxxx 50&xxxx;x&xxxx;xxxx x&xxxx;xxxx x&xxxx;xxxxxxxxxxx xxxxxxxx.
(14)&xxxx;&xxxx;Xxx a kůže x&xxxx;xxxxxxxxxxx xxxxxxxx.
(15)&xxxx;&xxxx;X&xxxx;xxxxxxxxxxxx x&xxxx;xxxxxxxxxx xxxxxxxx xxxxx.
(16)&xxxx;&xxxx;X&xxxx;xxxxxxxx případě xxxxxxxxx xx xxxxxxx xxxxxxxx xxxx XXX.
(17)&xxxx;&xxxx;Xxxxxxxxx x&xxxx;xxxxxx XXX.
XXXXXXX&xxxx;XXX
XXXXXXXX POŽADAVKY, XXX XXXX XXXXXXXX XXXXXXXXXXX XXXXXXXXX X&xxxx;XXXXXX&xxxx;3, POKUD XXX X&xxxx;XXXXXXX KATEGORIE XXXXXXXXXXX XXXXX XXXX XXXXXXX XXXXXXXX XXXXXXX, XXX JE STANOVENO X&xxxx;XX.&xxxx;7 XXXX.&xxxx;5 XXXXXXXX (XX) Č. 1831/2003
Nařízení (ES) x.&xxxx;1831/2003 xxxxxxxxxxx xxxxxxxxxx xxxxx při xxxxxxxxxxx xxxxxxxxxxx (xx-xx xx xxxxx) xxx xxxxxx xxxxxxxxx xxxxxxxxxxx xxxxx xxxx xx xxxxx xxxxxxxxx účelem xxxxx xx.&xxxx;7 xxxx.&xxxx;5 xxxxxxxx (XX) x.&xxxx;1831/2003.
Xxxxxx zvláštních xxxxxxxxx na vypracování xxxxxxxxxxx xxx:
|
1. |
xxxxxxxxxxxxx doplňkové xxxxx |
|
2. |
xxxxxxxxxx xxxxxxxxx xxxxx |
|
3. |
xxxxxxxx xxxxxxxxx xxxxx |
|
4. |
xxxxxxxxxxxx xxxxxxxxx xxxxx |
|
5. |
xxxxxxxxxxxxxxx x&xxxx;xxxxxxxxxxxxxxxx |
|
6. |
xxxxxxxxxxx x&xxxx;xxxxxxxxxxx xxxxx xx xxxxx xxxxxxxxx |
|
7. |
xxxxxxx x&xxxx;xxxxxxxx xxxxx x&xxxx;xxxx xxxxxxx, xxxxx xxxxxx určena k produkci xxxxxxxx |
|
8. |
xxxxxxxxx xxxxx, xxxxx xxx xxxx xxxxxxxx xxx xxxxxxx x&xxxx;xxxxxxxxxxx |
|
9. |
xxxxx xxxxxxxx |
|
10. |
xxxxxxxx xxxxxxxx |
|
11. |
xxxxxxxxxxxx xxxxxxxxx xxxxxxxxxxx xxxxx, xxxxx xxx byly xxxxxxxx xxxxx xxxxxxxx 70/524/XXX. |
Xxxxxxx xx xxxxx xxxxxxxxx xx základě více xxx xxxxxxx z výše xxxxxxxxx xxxxxxxxxx xxxxxxxxx.
Xxxxxx xxxxxxxx
Xxxxx-xx v dokumentaci některý x&xxxx;xxxxx předepsaných v těchto xxxxxxxx, je třeba xxxxx xxxxxx.
1.&xxxx;&xxxx;&xxxx;XXXXXXXXXXXXX XXXXXXXXX XXXXX
1.1&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;X:&xxxx;Xxxxxxx xxxxxxxxxxx
Xxxxxxx xx xxxx xxxxx&xxxx;X&xxxx;xxxxxxx&xxxx;XX.
1.2&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;XX: Xxxxxxxx, xxxxxxxxxxxxxxx x&xxxx;xxxxxxxx xxx xxxxx xxxxxxxxx látky; xxxxxx xxxxxxx
Xxxxx&xxxx;XX xxxxxxx&xxxx;XX xx xxxxxxx xxxxx:
|
— |
xxx xxxxxxxxx látky, xxxxx xxxxxx xxxxxx xx xxxxxxxx povolení, se xxxxxxx body 2.1.2, 2.1.3, 2.1.4, 2.1.4.2, 2.2, 2.3.1, 2.3.2, 2.4.1, 2.4.2, 2.4.4, 2.5, 2.6, |
|
— |
xxx xxxx xxxxxxxxx xxxxx, xxxxx jsou xxxxxx xx xxxxxxxx xxxxxxxx, se xxxxxxx xxxx oddíl II. |
1.3 Oddíl III: Xxxxxx xxxxxxxx se xxxxxxxxxxx xxxxxxxxxxx xxxxx
Xxxx&xxxx;3.1, 3.2 x&xxxx;3.4 přílohy II xx xxxxxxxxxx xx xxxxxxxxx xxxxx x&xxxx;xxxxxxxxxx, pokud xxx xxxxxxxx, že:
|
— |
v hotovém xxxxxx xxxxxxxxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxx xxxxx (xxxxx) nebo xxxxxxxxxx xxxxxxxxxx xxxx účinného xxxxxxx (xxxxxxx) xxxx |
|
— |
xxxxxx xxxxx(x)&xxxx;x&xxxx;xxxxxxx(x)&xxxx;xx vyskytují xxxx xxxxx složky siláže x&xxxx;xxxxx xxxxxxxxxxx látek xxxxxxxxx významně xxxxxx xxxxxxxxxxx x&xxxx;xxxxxxxxx xx xxxxxx xxxxxxxxxxx xxx xxxxx doplňkové látky (xxxx. xxxxx xxxxxxxxxx xxxxx podstatná xxxxx xxxxxxxx). |
X&xxxx;xxxxxxxxx xxxxxxxxx xx xxxxxxx xxxx xxxxx&xxxx;3 xxxxxxx&xxxx;XX.
1.3.1&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxx xx xxxxxxxxxxx používání xxxxxxxxx xxxxx pro xxxxxx xxxxxxx
X&xxxx;xxxxxxxxxx&xxxx;(1) xxxxx: použije xx xxxx xxx&xxxx;3.1 xxxxxxx&xxxx;XX.
1.3.1.1&xxxx;&xxxx;&xxxx;Xxxxxx tolerance x&xxxx;xxxxxxxx xxxxx
Xxx doplňkové xxxxx x&xxxx;xxxxxxxxxx:
|
— |
xxxxxxx xx xxxxx xx xxxxxxxx xxxxx xxxxx a výsledky se xxxxxxxxx x&xxxx;xxxxxxxxx xxxxxxxxx xxxxxxxx se xxxxxxx xxxxxx xxxxxx. Základní xxxxx xxxxx xxxx xxxxxxxxx xxxxxx zdroj xxxxxx xxxxxxxxxx bez xxxxxxx xxxxxxxxx xxxxx; |
|
— |
xxxxx xxxxxxx pro xxxxxx xxxxxxxxx je xxxxxxxx xxxxxxxxxxx xxxxxxxxxxx xx x&xxxx;xxxxxx x&xxxx;xxxx xxxxxxxxxx xxxxxxxxx, xxxxx xx xxx přesvědčivě xxxxxxx. Xxxxxxxx pozornost se xxxxxx xxxxxxxx, který xxxxxxxx životaschopné xxxxxxxxxxxxxx, x&xxxx;xxxxxxxxxx xxxxxx xxxxxxxxx xxxxxx x&xxxx;xxxxxx xx xxxxx xxxxxxxxxx. |
Xxxxxx xxxxxxxxx xxx obvykle xxxxxx xx xxxxx xxxxxxxxxxx, xxxxxxxxx dojnice. Xxxxxx xxxxxxxxxx xxxx druhy xxxx nutné xxxxx x&xxxx;xxxxxxx, xx-xx xxxxx xxxxxxxx ke své xxxxxx xxxxxxxxx x&xxxx;xxxxxxx xxx jiné xxxxx xxx xxxxxxxxxxx.
Xxxxxxx xxxxx:
X&xxxx;xxxxxxxxx xxxxx, pro xxx xx xxxxxxxx xxxxxxxx xxxx technologické xxxxxxxxx xxxxx x&xxxx;xxxxx nebyly xxxxxxxx xxx použití xxxx xxxxxx, xx xxxxx prokázat, xx xxx xxxxxxx xxxxxx xxxxxxxx xxx xxxxxxxxx xxxxxxxxxxx xxxxxx. Xxxx xxxxxxxxx může xxx xxxxxxx xx xxxxx xxxxx x&xxxx;xxxxxxx x&xxxx;xxxxxxxxxxxxxxx xxxxxxxx druhů xxxx x&xxxx;xxxxxxx xxxxx xxxxxxxxxxxxx xxxxxx.
1.3.1.2&xxxx;&xxxx;&xxxx;Xxxxxxxxxxx testy
Použije xx xxxx bod 3.1.2 xxxxxxx&xxxx;XX.
1.3.2&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxx xx bezpečnosti xxxxxxxxx xxxxxxxxx xxxxx xxx xxxxxxxxxxxx
|
1.3.2.1 |
Xxxxxx xxxxxxxxxxx x&xxxx;xxxxxxx Xxxxxx xxxxxxxxxxx x&xxxx;xxxxxxx xx xxxxxxxxxx, pokud:
Xxxxxx xxxxxxxxxxx xx nepožadují xxxxxx x&xxxx;xxxxxxx, pokud xx xxxxx xxxxxxxxx x&xxxx;xxxxxxxxxxx xxxx krmivech xxxxxxxxx xx xxxxxxx xxxxxxxx xxxx je xxxxxx xxxxxxx tělních xxxxxxx xxxx xxxxx. X&xxxx;xxxxxx xxxxxxxxx xx však xxxxxxxx studie reziduí, xxxxx xxxxx xxx xxxxxxx xx xxxxxxxx xxxxxx x&xxxx;xxxxxxx/xxxxxxxxxx u neošetřené xxxxxxx x&xxxx;xx skupině, xxx xxxx xxxxxxxx xxxxxxxx xxxxxxxxxx xxxxx. |
|
1.3.2.2 |
Xxxxxxxxxxxxx xxxxxx Xxxxxxxxxxxxx xxxxxx se xxxxxxxxxx, xxxxx:
Xxx xxxxxxxxxxxxxx x&xxxx;xxxxxx, xxxxx xxxxxx xxxxxx xxxx, xx xxxxxxxx xxxxxx xxxxxxxxxxxx (včetně mutagenity) x&xxxx;xxxxxx xxxxxxxxxxxx xxxxxx xxxxxxxx. Studie xxxxxxxxxxxx xx xxxxx xxxxxxxx xx xxxxxxxxxxx živých xxxxx. Xxx cizorodé xxxxx, xxx xxxxxx xxxxxx xxxx, xx xxxxxxx xxxx xxx&xxxx;3.2.2 přílohy II. Pro xxxxxxx xxxxx xx xxxxxxxxx individuálně xxxxx xxxxxxxxxxxx případů s přihlédnutím x&xxxx;xxxxxx a způsobu expozice. |
|
1.3.2.3 |
Posouzení xxxxxxxxxxx pro xxxxxxxxxxxx Xxx xxxxxxxxx xxxxx xxxxxxxxxx xxx xxxxxxx, xxxxx xxxx xxxxxx x&xxxx;xxxxxxxx xxxxxxxx, xx použije xxxx xxx&xxxx;3.2.3 xxxxxxx&xxxx;XX. |
1.3.3&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxx se xxxxxxxxxxx xxxxxxxxx doplňkové xxxxx xxx xxxxxxxxx/xxxxxxxxxx
Xxxxxxx xx xxxx xxx&xxxx;3.3 xxxxxxx&xxxx;XX. Xxxxxxxxx xxxxx obsahující xxxxxx x&xxxx;xxxxxxxxxxxxxx se xxxxxxxx za xxxxxxxxxxxxxxx xxxxxxxxx ústrojí, pokud xxxxxx xxxxxxxxxx xxxxxxxxxxx xxxxxx xxxxxxxxxxx xxxx.
1.3.4&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxx xx xxxxxxxxxxx xxxxxxxxx doplňkové xxxxx xxx životní xxxxxxxxx
Xxxxxxx xx xxxx bod 3.4 xxxxxxx&xxxx;XX. X&xxxx;xxxxxxxxxxx xxxxx x&xxxx;xxxxxxxxxx se posoudí xxxxxx doplňkové látky xx xxxxxx silážních xxxx xx xxxxxxxxx xxx nebo xxx xxxxx silážování.
1.4 Oddíl IV: Xxxxxx xxxxxxxx xx xxxxxxxxx xxxxxxxxx xxxxx
Xxxxxxxxxxxxx doplňkové xxxxx xxxx xxxxxxx xxxx xxxxxxxxxxxx xxxxxxxxxx xxxxx, xxxxxxx xxxx xxxxxx žádný xxxxx xxxxxxxxxx xxxxxx na xxxxxxxxxx xxxxxx. Důkazy x&xxxx;xxxxxxxxx xxxxxxxxx látky xxxx xxx xxxxxxxxxx xxxxxx vhodných kritérií xxxxxxxxxxxx x&xxxx;xxxxxxxx xxxxxxxxxxx xxxxxxxx xx xxxxxxxx xxxxxxxxxxx xxxxxxxx pro xxxxx v porovnání x&xxxx;xxxxxxxxxxxxx xxxxxxxxxx krmivem.
Účinnost xx xxxxxxx studiemi in xxxxx s výjimkou látek xxx xxxxxxxx xxxxxxxxxxx xxxxxxxxxxxx. V následující xxxxxxx xxxx xxxxxxx xxxxxx xxxxxxxxx xxx xxxxx xxxxxxx xxxxxxx.
Xxxxxxxxx pro xxxxxxxxxx xxxxxxxxxxxxx xxxxxxxxx xxxxx
|
Xxxxxxx xxxxxxx |
Xxxxxxxxx pro xxxxxxxxx xxxxxxxxx |
||||||||||
|
Xxxxxxxx xxxxxxxxxxxxx xxxxx, xxxxxxx xxxxxxxxxx xxxxxxxxx x&xxxx;xxxxxxxxx xxxxxxxxxxxxxx xx xxxxxxxxxxxx. Je xxxxx xxxxxxxx xxxxxxxx xxxx xxxxxx xxxxxxxxxxxxx xxxxxx. |
||||||||||
|
Xxxxxxx před xxxxxxxxxxxxx xxxxxxxxxx xxxxxxx hlavních xxxxx/xxxxxx během xxxxxxxxxx x/xxxx skladování krmiva. Xx nutno xxxxxxxx xxxxxxxx xxxx trvání xxxxxxxxxx xxxxxx. |
||||||||||
|
Xxxxx/xxxxxxxx xxxxxxxxxx xxxxxx xxxxx xxxxxxxxxxxxxx xxxx špatně xxxxxxxxxxxx xxxxxx xxxxxx. |
||||||||||
|
Xxxxxxxxx fyzikálně-chemického xxxxx krmiv. |
||||||||||
|
Xxxxxxxxx xxxxxxx materiálů nebo xxxxx. |
||||||||||
|
Tvoření xxxx xxxxxxx xx xxxxx xxxxxxxxx krmiva. |
||||||||||
|
Trvanlivost xxxxx xxxx výkonnost xxx xxxxxxxxx xxxxx. |
||||||||||
|
Důkaz x&xxxx;xxxxxxx kontaminaci potravin xxxxxxxxxxx xxxxxx. |
||||||||||
|
Xxxxxxxxx xxxxxxxx xxxxxxx. Xx xxxxx xxxxxxxx udávanou xxxx xxxxxx protispékavého xxxxxx. |
||||||||||
|
xX x/xxxx xxxxxxxxx xxxxxxxx xxxxx. |
||||||||||
|
|
||||||||||
|
Xxxxxxxxxxxxxxx xxxxxxxxxxxx krmných xxxxxxxxx. |
Xxxxxxxxx xxxxx x&xxxx;xxxxxxxxxx
Xxxxxxxx xx xxxxxxxx xxxxxxx x&xxxx;xxxxx prokázat xxxxxxxxxx xxxxxx xx silážní xxxxxx&xxxx;(2). Xxxxxxx xx xxxxxxxx x&xxxx;xxxxxx příkladem x&xxxx;xxxxx x&xxxx;xxxx xxxxxxxxx xxxxxxxxx (xxxxx xxxx xxxxxxxx všechna xxxx xxxxxxxxxxxxxxx xxxxxx):
|
— |
xxxxxx, která xxx snadno xxxxxxxxx: &xx;3&xxxx;% xxxxxxxxxxx xxxxxxxxxxx x&xxxx;xxxxxxxx materiálu (xxxx. xxxx xxxxxxxx xxxxxxxx, xxxxx, sveřep nebo xxxxx xxxxx), |
|
— |
xxxxxx, xxxxx xxx xxxxxxxxx x&xxxx;xxxxxxx xxxxxxxx: 1,5–3,0 % rozpustných xxxxxxxxxxx x&xxxx;xxxxxxxx xxxxxxxxx (xxxx. xxxxxxx, kostřava xxxx zavadlá vojtěška), |
|
— |
krmiva, xxxxx xxx xxxxxxxxx xxxxxxx: &xx;&xxxx;1,5&xxxx;% xxxxxxxxxxx xxxxxxxxxxx x&xxxx;xxxxxxxx xxxxxxxxx (xxxx. xxxx xxxx xxxxxxxxx). |
Xxxx-xx žádosti xxxxxxx xx xxxxx kategorie xxxxx xxxxxxx na xxxxxxx xxxxxx, xxxxx xx xxxxxxxx xxxxxxx xxxxxx. Poté xx xxxxxxxx xxx xxxxxxx x&xxxx;xxxxxxxxxx xxxxxxxxxxxxxxxx xxx xxxx xxxxxxx, pokud xxxxx xx použití xxxxxxxx různého xxxxxxxxxxx xxxxxx.
Xxx xxxxxxxx krmiva xx požadují xxxxxxxxxx xxxxxxx.
Xxxx xxxxxx studie xx xxxxxxx 90 dnů xxxx xxxx při xxxxx teplotě (xxxxxxxxxx xxxxxx 15 – 25&xxxx;xX). Xxxxxxx kratší xxxx xxxxxx musí xxx zdůvodněno.
Obvykle se xxxxxx xxxxxxxx měření xxxx xxxxxxxxx parametrů x&xxxx;xxxxxxxxx s negativní xxxxxxxxx xxxxxxxx:
|
— |
xxxxxx x&xxxx;xxxxxxxxx xxxxxx xxxxxx (upraveno s ohledem xx xxxxxx látky), |
|
— |
pokles xX, |
|
— |
xxxxxxxxxxx těkavých xxxxxxxx xxxxxxx (např. kyselina xxxxxx, kyselina xxxxxxx x&xxxx;xxxxxxxx xxxxxxxxxx) x&xxxx;xxxxxxxx xxxxxx, |
|
— |
xxxxxxxxxxx xxxxxxxx (xxxxxxx), |
|
— |
xxxxxxxxxxx xxxxxx (g/kg xxxxxxxxx xxxxxx) x |
|
— |
xxxxx uhlohydrátů xxxxxxxxxxx xx vodě. |
Popřípadě xx xxxxxx xxxx xxxxxxxxxxxxxxx a chemické xxxxxxxxx x&xxxx;xxxxxxxx zvláštního xxxxxxxxx xxxxx (xxxx. počet xxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxx, xxxxxxxx xxxxxxxxxx, xxxxxxxx xxxxxxxx x&xxxx;xxxxxxxxxx xxxxx).
Xxxxxxx účinek x&xxxx;xxxxxxxxxxx xx xxxxxxxx xxxxxxxx xxxxxxxxxxxx xxxxxxxxx xxxx xx posoudí xx xxxxxxx xxxxxxxxx xxxxxx xxxxxxxxx xxxx xxxxxxxxxxx xx xxxx xxxxxxx xxxxxx x&xxxx;xxxxxxxxxxxx k pravděpodobnému xxxxxx xx xxxxxxx xxxxxxxxx (xxxx. xxxxxxxxxxx xxxxxxxxx xxxx xxxx xxxxxxxxxx xxxxxxx xxxxxxx). Xxxxxxx xxxxxx xxxxxxxxx xxxx je xxxxx xxxxxxxx přímo. Xxxxxxxx xxxxxxx xxxx musí xxx xxxxxxxxxx, xxx xxxxx xxxxxxx xxxxx xxxxxxx xx pomoci xxxxx. Doba xxxxxx xxxxxx xx obvykle 50&xxxx;xxx. Pokud se xxxxxxx jiná xxxx, xx xxxxx xx xxxxxxxxx.
Xxxxx xxxxxxx xxxxxxxxx xxxx být xxxxxxxxx x&xxxx;xxxxxxxxx x&xxxx;xxxxxxxxx xxxxxxxxx xxxxxxxx. Xxxxxx stability xxxx trvat nejméně xxxx xxx xx xxxxxxxx vzduchu a doplňková xxxxx xxxxxxx xxxxxxxxx xx xxxx xxxxxxx x&xxxx;xxx xxx delší, xxx xx xxxxxxxxx x&xxxx;xxxxxxxxxxxx xxxxxxxxxxx xxxxxx. Xxxxxxxxxx xx, aby xx xxxxx xxxxxxxx xxx xxxxxxx okolí 20&xxxx;xX a aby xx xxxxxxx xxxxxxx x&xxxx;3&xxxx;xX xxxx xxxx oproti xxxxxxx xxxxx považovalo xx xxxxxx xxxxxxxxxxx. Xxxxxx xxxxxxx je xxxxx xxxxxxxx xxxxxxx xxxxxxxx CO2.
1.5 Oddíl X:&xxxx;Xxxx xxxxxxxxxxxx v období xx xxxxxxx xxxxx na xxx
Xxxxx oddíl se xxxxxxx xxxxx xxxxxxxxxx xx.&xxxx;7 xxxx.&xxxx;3 xxxx.&xxxx;x)&xxxx;xxxxxxxx (XX) x.&xxxx;1831/2003. Xx xxxxxxx, xx xx xxxx xxxxxxxxxxxx x&xxxx;xxxxxx xx xxxxxxx látky xx trh požaduje xxxxx xxx xxxxxxxxx xxxxx, xxxxx jsou xxxxxxxxx modifikované organismy xxxx xxxx x&xxxx;xxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxx vyrobeny.
2. SENZORICKÉ XXXXXXXXX XXXXX
2.1&xxxx;&xxxx;&xxxx;Xxxxxxx
2.1.1&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;X:&xxxx;Xxxxxxx xxxxxxxxxxx
Xxxxxxx xx xxxx xxxxx&xxxx;X&xxxx;xxxxxxx&xxxx;XX.
2.1.2&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;XX: Xxxxxxxx, xxxxxxxxxxxxxxx a podmínky xxx xxxxx xxxxxxxxx xxxxx; xxxxxx analýzy
Oddíl II xxxxxxx&xxxx;XX xx xxxxxxx xxxxx:
|
— |
xxx xxxxxxxxx látky, xxxxx nejsou vázané xx xxxxxxxx xxxxxxxx, xx použijí body 2.1.2, 2.1.3, 2.1.4, 2.1.4.2, 2.2, 2.3.1, 2.3.2, 2.4.1, 2.4.2, 2.4.4, 2.5, 2.6, |
|
— |
xxx xxxx xxxxxxxxx látky, xxxxx xxxx xxxxxx xx xxxxxxxx povolení, xx xxxxxxx celý xxxxx&xxxx;XX. |
2.1.3&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;XXX: Xxxxxx týkající xx xxxxxxxxxxx používání doplňkové xxxxx
Xxx&xxxx;3.3 přílohy II xx xxxxxxxx xxxx na xxxxxxx doplňkové xxxxx.
|
1. |
Xx xxxxx, xxxxx při xxxxxxx x&xxxx;xxxxxx, dávají xxxxx xxxxxxxxxx xxxxxxxxxxx xxxxxx, xx vztahuje xxxx xxxxx&xxxx;XXX body 3.1, 3.2 x&xxxx;3.4 xxxxxxx&xxxx;XX. |
|
2. |
X&xxxx;xxxxx, xxxxx dávají xxxx xxxxxxxxx krmivům xxxxx, xx studie xxxxxxxx xx xxxxxx&xxxx;XXX xxxx&xxxx;3.1 xxxxxxxx na xxxxxxxxx, xxxxxx byla xxxxxxxxx xxxxx xxxxxxxx x&xxxx;xxxxxxxxxxxx xxxxx. Je xxxxx xxxxxxxxxx xxxxx rovněž xxxxxxx na xxxxxxxxxx xxxxxxxx xxxxxxxxxx. Xxxxxxx xx xxxxx&xxxx;XXX body 3.2 x&xxxx;3.4 xxxxxxx&xxxx;XX. |
|
3. |
X&xxxx;xxxxx, které xxxx pozitivní xxxx xx xxxxxxxx xxxxxxxxx xxx xxxx xxxxx, xx požadují xxxxxx xxxxxxxx se xxxxxx&xxxx;XXX xxxx&xxxx;3.1 xxxxxxx&xxxx;XX x&xxxx;xxxx xxxxxx musí být xxxxxxxxx xx xxxxxxxxx, xxxx byla doplňková xxxxx podávána x&xxxx;xxxxxxxxxx xxxxx. Xx xxxxx xxxxxxxxxx xxxxx xxxxxx xxxxxxx na xxxxxxxxxx xxxxxxxx xxxxxxxxxx. Nepožadují xx xxxx body 3.2 x&xxxx;3.4. |
2.1.4&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;XX: Studie týkající xx účinnosti doplňkové xxxxx
Xxxxxxx xx celý xxxxx&xxxx;XX xxxxxxx&xxxx;XX.
|
x) |
Xxx látky, xxxxx xxx použití x&xxxx;xxxxxx xxxxxx barvu xxxxxxxxxx živočišného xxxxxx: xxxxx xxxxx xxxxxxxx xxxxxxxxx xx xxxxxx, xxxxxx xxxx doplňková xxxxx xxxxxxxx xx xxxxxxxxxxxx xxxxxxxx xxx užití, xx xxxx pomocí xxxxxx metodiky. Xx xxxxx xxxxxxxx, že xxxxxxxxx doplňkové xxxxx xxxx xxxxxxxxxx xxxx xx stabilitu xxxxxxxx xxxx xxxxxxxxxxxxxx x&xxxx;xxxxxxxx xxxxxxxxxx xxxxxxxx. Xxxx-xx xxxxxx konkrétní látky xx xxxxxxx/xxxxxxxxxx xxxxxxxxxxx xxxxxxxx xxxxx xxxxxxxxxxxxxx, xxx mohou xxxxxxxxxxxx xxxxx o účinnosti xxxxxxxxxx xxxxxxx studie (xxxx. xxxxxx xxxxxxxxxx dostupnosti). |
|
b) |
Pro xxxxx, xxxxx dávají xxxx navracejí krmivům xxxxx: xxxxx x&xxxx;xxxxxxxxx xx xxxxx poskytnout xxxxxxxxxxxxxxx xxxxxxxxxxxxxx laboratorních xxxxxx xxxxxxxxxxxxxx x&xxxx;xxxxxxx xxxxxxxxx xxx xxxxx v porovnání x&xxxx;xxxxxxxxxxx xxxxxx. |
|
x) |
Xxx xxxxx, xxxxx xxxx xxxxxxxxx xxxx xx zbarvení xxxxxxxxx ryb xxxx xxxxx: xxxxxx xxxxxxxxxxx xxxxxx (xxxxxx) xx xxxxxxxx xx xxxxxxxxx, kterým xxxx xxxxxxxxx látka xxxxxxxx v doporučené xxxx. Xxxxx barvy se xxxx xxxxxx xxxxxx xxxxxxxx. Xxxxx x&xxxx;xxxxxxxxx xx xxxxx xxxxxxxxxx xxxxxx xxxxxx xxxxxxxxxxxxxxxx xxxxxxxx (xxxx. biologická xxxxxxxxxx) xxxx xxxxxxx xx xxxxxxxx xxxxxxxxxx. |
2.1.5&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;X:&xxxx;Xxxx xxxxxxxxxxxx x&xxxx;xxxxxx po xxxxxxx xxxxx xx xxx
Xxxxx xxxxx xx xxxxxxx podle ustanovení xx.&xxxx;7 odst. 3 xxxx.&xxxx;x)&xxxx;xxxxxxxx (XX) x.&xxxx;1831/2003. Xx xxxxxxx, xx xx xxxx xxxxxxxxxxxx x&xxxx;xxxxxx xx xxxxxxx xxxxx xx xxx xxxxxxxx xxxxx pro xxxxxxxxx xxxxx, xxxxx xxxx xxxxxxxxx xxxxxxxxxxxx xxxxxxxxx xxxx xxxx x&xxxx;xxxxxxxxx xxxxxxxxxxxxxx organismů xxxxxxxx.
2.2&xxxx;&xxxx;&xxxx;Xxxxxxxxxxx xxxxx
2.2.1&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;X:&xxxx;Xxxxxxx dokumentace
Použije xx xxxx xxxxx&xxxx;X&xxxx;xxxxxxx&xxxx;XX.
2.2.2&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;XX: Xxxxxxxx, xxxxxxxxxxxxxxx a podmínky pro xxxxx xxxxxxxxx xxxxx; xxxxxx analýzy
V případě xxxxxxx „xxxxxxxx xxxxxxxx“ se xxxxxxx xxxx xxxxxxxx, xxxxxxx x&xxxx;xxxx xxxxxxxxx x&xxxx;xxxxxx xxxxx xxxx xxxxxx xxxxxxxx, xxxxx xxxx velmi xxxx xxxxxxxxxx, xxxx xxxx. xxxxxxx, mletím xxxx xxxxxxx (např. xxxxx xxxxx x&xxxx;xxxxxx), nepovažují xx xxxxxxxx spadající xx xxxxxxx xxxxxxx xxxxxxxxxxxxx xxxxx x&xxxx;xxxxxxxxx xxxxxxxxxxxx doplňkových xxxxx.
Xxx xxxxx xxxxxxxxxxx xxxxxxx xxxxxxxxxx xx xxxxxx xxxxxxxx xxxx zchutňující xxxxx klasifikovány xxxxx:
|
1. |
Xxxxxxxx xxxxxxxx:
|
|
2. |
Xxxxxxxx xxxx xxxxxxxxxxxx syntetické chemicky xxxxxxxxxx xxxxxxxxxxx xxxxx |
|
3. |
Xxxxx xxxxx Xx nutno xxxxx xxxxxxxxxx xxxxxxx, do xxx patří xxxxxxx, xxxxx xx xxxxxx xxxx. X&xxxx;xxxxxxx xxxxxxxx, xxxxx xxxxxxx xx xxxxx x&xxxx;xxxx xxxxxxxxx xxxxxx, xx toto xxxxx uvést x&xxxx;xxxxxxxxx. |
|
2.2.2.1 |
Xxxxxxxxxxxxxxx xxxxxx xxxxx (látek) / xxxxxxx (činidel) Použije xx xxxx xxx&xxxx;2.2 xxxxxxx&xxxx;XX. Xxxxxx: Xxx xxxxxxx xxxxxxx xxxxxxxxxxxxx xxxxx je xxxxx uvést xxxx xxxxxxxxx xxxxxxxxxxxxx číslo (xxxxx) (např. XXXXXX&xxxx;(3), Xxxx Evropy (4), XXXXX, XXX&xxxx;(5) nebo xxxx xxxxxxxxxxx xxxxxxxxx systém xxxxxxxxx) používané xxxxxxxxxx x&xxxx;xxxxxxxxxxxx xxxxxxxxxxxxx xxxxxxxx x&xxxx;xxxxxxxx a potravinách, xxxxx xx x&xxxx;xxxxxxxxx.
|
|
2.2.2.2 |
Xxxxxx výroby Použije xx xxxx xxx&xxxx;2.3 xxxxxxx&xxxx;XX. X&xxxx;xxxxxxx xxxxxxxxxx produktů, které xxxxxx xxxxxxxx přesně xxxxxxxxxx, xxxxxxx xxxxxxxxx xxxxx mnoha xxxxx xxxxxxx x&xxxx;xxxxxxx extrakce, xx xxxxx xxxxx xxxxxxxx xxxxx xxxxxxx xxxxxxxx. Doporučuje se x&xxxx;xxxxxx xxxxxx xxxxxxxxxxxx xxxxxxxxxxxx, např. silice, xxxxx, výluh, extrakt x&xxxx;xxxxxxxxxxx pojmy (7) xxxxx xxxxxxxxx xxx xxxxxxxxx xxxxxxxxxx xxxxxxxxxxx produkty x&xxxx;xxxxxx procesu xxxxxxxx. Xxxxxxx xx xxxxxxx xxxxxxxxx xxxxxxxxxxxx, přijatá xxxxxxxxxxxx opatření, xxx xx xxxxxxxx reziduím x&xxxx;xxxxxxxxxxxx, x&xxxx;xxxxxx reziduí, xxxxx xxxx toxikologicky xxxxxxxx, xxxxxxxx xxxxxx xxxxxxx nelze zabránit. Xxxxx použité x&xxxx;xxxxxxxxxxxxxxx xxxxxxxx mohou xxxxxxxxx xxxxx na způsob xxxxxxxx. |
|
2.2.2.3 |
Xxxxxx xxxxxxx
Celý xxx&xxxx;2.6 xxxxxxx&xxxx;XX xx xxxxxxxx xx všechny xxxxxxx xxxxxxxxxxx xxxxx, xxxxxxxxx xxxxxxxx xxxxxxxx, xxxxx xxxxxxxx xxxxxxxxxxxxx xxxxxxxx xxxxx, xxxxxxxx xxxx odpovídající xxxxxxxxxx xxxxxxxx xxxxxxxxxx xxxxxxxxxxx xxxxx, jež jsou xxxxxxxxxxxxx významnými látkami, x&xxxx;xxxxx xxxxxxxxxxx xxxxx. |
2.2.3&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;XXX: Xxxxxx xxxxxxxx xx xxxxxxxxxxx doplňkové xxxxx
Xxx xxxxxxx xxxxxxxxxxx xxxxx xx xxxxx xxxxx xxxxxxxx xxxxxx a výpočty xxxxxx jak z přirozené xxxxxxxx, xxx xx xxxxxxx xxxxxxxxxxx xxxxx xx krmiv.
Na zchutňující xxxxx xxxxxxx xx xxxxxxx xxxxxxx xxxxx xx xxxxxxxx celý xxxxx&xxxx;XXX xxxxxxx&xxxx;XX.
|
2.2.3.1 |
Xxxxxx xxxxxxxx xx xxxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxx pro xxxxxx xxxxxxx
|
|
2.2.3.2 |
Xxxxxx xxxxxxxx xx bezpečnosti xxxxxxxxx doplňkové látky xxx xxxxxxxxxxxx Xx xxxxx xxxxxxx, že xxxxxxxxxx xxxxxxxxxxx látky nevedou x&xxxx;xxxxxxxxx xxxxxxxxxxxxx xxxxxxxxxx xxxxxxxx xxx člověka xx zvířeti. X&xxxx;xxxxxxx, xx xxxxx xxxxxxxxxxxx xxxxxxxxxxxxx xxxxxxxx v důsledku xxxx přidání xx xxxxx xxxx x&xxxx;xxxxxxxx x&xxxx;xxxxxxxxxxx živočišného xxxxxx, xx xxxxx xxxxxxxxxx xxxxxxxx xxxxxxx expozice xxxxxxxxxxxx.
|
|
2.2.3.3 |
Xxxxxx xxxxxxxx se xxxxxxxxxxx xxxxxxxxx doplňkové xxxxx xxx xxxxxxxxx/xxxxxxxxxx Xxxxxxx xx xxxx xxx&xxxx;3.3 xxxxxxx&xxxx;XX. |
|
2.2.3.4 |
Xxxxxx xxxxxxxx xx xxxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxx xxx životní prostředí Použije xx xxxx xxx&xxxx;3.4 xxxxxxx&xxxx;XX. |
2.2.4&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;XX: Xxxxxx týkající xx xxxxxxxxx xxxxxxxxx xxxxx
Xx xxxxx xxxxxxxxx xxxxxx x&xxxx;xxxxxxxxxxxx xxxxxxxxxxxxx xxxxx, xxxxxxx xx xxxxxxx xxxxxxxxxx literatury. Xx xxxx xxx xxxxxxxxx xxxxxx xxxxxxxxxxx x&xxxx;xxxxxxxxxxx xxxxxxxxx, xxxx-xx x&xxxx;xxxxxxxxx, x&xxxx;xxxxxxx případě xxxxx být xxxxxxxxxx xxxxxx xx xxxxxxxxx.
Xx xxxxx plně xxxxxxxx x&xxxx;xxxxx, zda xxxxxxx, xxxxxxx xx žádost xxxx, xxxx x&xxxx;xxxxxx, xxxxxxx nebo xxxxxxxxxxx xxxxxxxxxxx původu jiné xxxxxx kromě xxxxxx x&xxxx;xxxxxxxx zchutňujících látek x&xxxx;xxxxxxx&xxxx;X&xxxx;xxxxxxxx (ES) č. 1831/2003.
2.2.5 Oddíl V: Plán xxxxxxxxxxxx x&xxxx;xxxxxx xx xxxxxxx xxxxx xx xxx
Xxxxx xxxxx se xxxxxxx podle xxxxxxxxxx xx.&xxxx;7 xxxx.&xxxx;3 xxxx.&xxxx;x)&xxxx;xxxxxxxx (XX) x.&xxxx;1831/2003. Xx xxxxxxx, xx xx xxxx xxxxxxxxxxxx x&xxxx;xxxxxx xx uvedení látky xx xxx xxxxxxxx xxxxx pro doplňkové xxxxx, které xxxx xxxxxxxxx modifikované xxxxxxxxx xxxx xxxx x&xxxx;xxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxx xxxxxxxx.
3.&xxxx;&xxxx;&xxxx;XXXXXXXX XXXXXXXXX LÁTKY
3.1 Oddíl I: Shrnutí xxxxxxxxxxx
Xxxxxxx xx xxxx xxxxx X&xxxx;xxxxxxx&xxxx;XX.
3.2&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;XX: Identita, charakteristika x&xxxx;xxxxxxxx xxx užití xxxxxxxxx xxxxx; xxxxxx xxxxxxx
Xxxxx&xxxx;XX xxxxxxx&xxxx;XX se xxxxxxx xxxxx:
|
— |
xxx xxxxxxxxx xxxxx, xxxxx xxxxxx xxxxxx na držitele xxxxxxxx, se xxxxxxx xxxx&xxxx;2.1.2, 2.1.3, 2.1.4, 2.1.4.2, 2.2, 2.3.1, 2.3.2, 2.4.1, 2.4.2, 2.4.4, 2.5, 2.6, |
|
— |
pro xxxx doplňkové xxxxx, xxxxx jsou xxxxxx xx xxxxxxxx povolení, xx xxxxxxx xxxx xxxxx&xxxx;XX. |
3.3&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;XXX: Studie xxxxxxxx xx xxxxxxxxxxx doplňkových xxxxx
3.3.1&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxx xx xxxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxx xxx xxxxxx xxxxx
|
3.3.1.1 |
Xxxxxxxxx u cílových xxxxx
|
|
3.3.1.2 |
Xxxxxxxxxxx xxxxxx Xxxxxxx xx celý xxx&xxxx;3.1.2 xxxxxxx&xxxx;XX. |
3.3.2&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxx xx xxxxxxxxxxx použití xxxxxxxxx látky pro xxxxxxxxxxxx
|
3.3.2.1 |
Xxxxxx xxxxxxxxxxx a reziduí Studie xxxxxxxxxxx xx obvykle xxxxxxxxxx. Xxx xxxxxxxx xxxxxxxx xx xxxxxxxxx xxxxxxxxxxxx x&xxxx;xxxxxxx. Xxxxxx reziduí xxxx xxxxxxxx xx xxxxxxxx xxxxx u těch xxxxxxxxxxx látek, které xxxxxxx do funkční xxxxxxx „xxxxxxxx, provitamíny x&xxxx;xxxxxxxx přesně xxxxxxxxxx xxxxx xx xxxxxxxxxxxx xxxxxxx“, xxxxx xxxx xxxxxxxxx x&xxxx;xxxxxxxxx v těle, x&xxxx;xxx funkční xxxxxxx xxxxxxxxx xxxxxxxxx xxxxx, xxxxx se zvýšila xxxxxxxxxx xxxxxxxxxx. X&xxxx;xxxxx xxxxxxx se xxxxxxxxx xxxxxx xxxxxxx v oddíle 3.2.1 xxxxxxx&xxxx;XX. Požadavek je xxxxxx xx xxxxxxxx xxxxxx x&xxxx;xxxxxxx xxxx xxxxxxxxxx mezi skupinou, xxx xxxx xxxxxxxx xxxxxxxx xxxxx dotyčné xxxxx, x&xxxx;xxxxxxxxx xxxxxxxxx xxxxxxxx (xxxxxxxxxx látka). |
|
3.3.2.2 |
Toxikologické xxxxxx Xx xx xxxxxxxx xxx xxxxxxxx fermentačního xxxxxxx x&xxxx;xxx doplňkové xxxxx, xxxxx xxxxxx xxxxx xxxxxxxx. Xxx xxxxxxxx xxxxxxxxxxxxx xxxxxxx xx xxxxx předložit xxxxxx genotoxicity x&xxxx;xxxxxxxxxxxx xxxxxxxx, ledaže:
Pokud xxxxxxxxx organismus patří xx xxxxxxx, x&xxxx;xxx xx známo, že xxxxxxx xxxxx xxxxxxxxx xxxxxx, xx xxxxx xxxxxxxx xxxxxxxx xxxxxx xxxxxxxxxx. |
|
3.3.2.3 |
Xxxxxxxxx xxxxxxxxxxx pro xxxxxxxxxxxx Xxxxxxx se xxxx xxx&xxxx;3.2.3 xxxxxxx&xxxx;XX. |
3.3.3&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxx xx xxxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxx pro xxxxxxxxx/xxxxxxxxxx
Xxxxxxx xx xxxx xxx&xxxx;3.3 xxxxxxx&xxxx;XX.
3.3.4&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxx xx xxxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxx pro xxxxxxx xxxxxxxxx
Xxxx xxx&xxxx;3.4 xxxxxxx&xxxx;XX xx xxxxxxx xxx xxxx xxxxxx xxxxx, xxxxx patří xx skupině xxxxxxxxx xxxxxxxxx xxxxx.
3.4&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;XX: Studie xxxxxxxx xx xxxxxxxxx xxxxxxxxx xxxxx
Xxxxxx účinnosti xx xxxxxxxxxx xxx xxxxxxxx, xxxxxxxxxxxxx, soli x&xxxx;xxxxxxx aminokyselin, xxxxx xxx byly xxxxxxxx xxxx xxxxxxxxx látky, xxxxxxxxxx stopových xxxxx, xxxxx již xxxx xxxxxxxx jako xxxxxxxxx xxxxx, x&xxxx;xxxxxxxx, xxxxxxxxxxx x&xxxx;xxxxxxxx přesně xxxxxxxxxx xxxxx xx xxxxxxxxxxxx xxxxxxx, které již xxxx xxxxxxxx jako xxxxxxxxx látky.
Krátkodobá xxxxxx xx požaduje x&xxxx;xxxxxxxx xxxxxxxxx pro deriváty xxxxxxxx, soli a analogy xxxxxxxxxxxx, xxxxx xxxxx xxxxxx xxxxxxxx jako xxxxxxxxx xxxxx, xxxxxxxxxx xxxxxxxxx prvků, xxxxx xxxxx xxxxxx xxxxxxxx xxxx doplňkové látky, x&xxxx;xxx xxxxxxxx, xxxxxxxxxxx x&xxxx;xxxxxxxx xxxxxx xxxxxxxxxx xxxxx xx xxxxxxxxxxxx xxxxxxx, které xxxxx xxxxxx xxxxxxxx xxxx xxxxxxxxx látky.
Pro ostatní xxxxx, x&xxxx;xxxxx xx xxxxx nutriční účinek, xx požaduje xxxxxxx xxxxx xxxxxxxxxx xxxxxx xxxxxxxxx xxxxx xxxxxxxxxx xxxxxx&xxxx;4 xxxxxxx&xxxx;XX.
Xxxxxx musí xxxxxxxx xxxxxxxx, xx xxxxxxxxx xxxxx xxxx xxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxx. Xxxxx xxxxxxxx xxxxxxxx xxxxxxx x&xxxx;xxxxxx xxxxxx, která xxxxxxxx xxxxxx x&xxxx;xxxxxxxxxxxxx nižších xxx nutriční xxxxxxxxx xxxxxx. Xx xxxx xxxxx zamezit xxxxxxxx x&xxxx;xxxxxxxx xxxxxxxxx xxxxxxx xxxxxx xxxxxx xxxxxxxxx. Xxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxx x&xxxx;xxxxxxx druhu xxxx kategorie xxxxxx, xxxxxx xxxxxxxxxxxxx xxxxxx.
3.5&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;X:&xxxx;Xxxx xxxxxxxxxxxx x&xxxx;xxxxxx xx xxxxxxx xxxxx na xxx
Xxxxx oddíl xx xxxxxxx xxxxx ustanovení xx.&xxxx;7 xxxx.&xxxx;3 xxxx.&xxxx;x)&xxxx;xxxxxxxx (XX) č. 1831/2003.
4. ZOOTECHNICKÉ XXXXXXXXX XXXXX
4.1&xxxx;&xxxx;&xxxx;Xxxxxxxxxxxx xxxxxxxxx xxxxx xxxx xxx enzymy x&xxxx;xxxxxxxxxxxxxx
4.1.1&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;X:&xxxx;Xxxxxxx xxxxxxxxxxx
Xxxxxxx se xxxx xxxxx&xxxx;X&xxxx;xxxxxxx&xxxx;XX.
4.1.2&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;XX: Xxxxxxxx, xxxxxxxxxxxxxxx x&xxxx;xxxxxxxx pro xxxxx xxxxxxxxx látky; xxxxxx analýzy
Použije se xxxx xxxxx&xxxx;XX přílohy II.
4.1.3 Oddíl III: Xxxxxx xxxxxxxx xx xxxxxxxxxxx xxxxxxxxxxx látek
|
4.1.3.1 |
Studie xxxxxxxx xx xxxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxx xxx cílová zvířata Použije xx celý xxx&xxxx;3.1 xxxxxxx&xxxx;XX. |
|
4.1.3.2 |
Xxxxxx týkající se xxxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxx xxx spotřebitele
|
|
4.1.3.3 |
Xxxxxx xxxxxxxx xx bezpečnosti doplňkové xxxxx xxx xxxxxxxxx/xxxxxxxxxx Xxxxxxx xx celý xxx&xxxx;3.3 xxxxxxx&xxxx;XX. |
|
4.1.3.4 |
Xxxxxx xxxxxxxx se xxxxxxxxxxx doplňkové xxxxx xxx xxxxxxx prostředí Použije xx xxxx xxx&xxxx;3.4 xxxxxxx&xxxx;XX. |
4.1.4&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;XX: Studie xxxxxxxx xx xxxxxxxxx doplňkové xxxxx
Xxxxxxx se xxxx xxxxx&xxxx;XX xxxxxxx&xxxx;XX.
|
1. |
Xxxxxxxxx xxxxx, xxxxx xxxx xxxxxxxxx xxxx xx xxxxxxxxxx xxxxxx, xxxxxxxxxx nebo xxxxx životní podmínky, x&xxxx;xxxxxxx xxxxxxx „jiné xxxxxxxxxxxx doplňkové xxxxx“ Xxxxxx xxx prokázat xxxxx xx xxxxxx ke xxxxxxx xxxxxxxx xxxxx xxxx xxxxxxxxx xxxxxx. X&xxxx;xxxxxxxxxx na xxxxxxxxxxxx xxxxxxxxx xxxxx mohou xxx xxxxxx založena xx pracovních charakteristikách (xxxx. xxxxxxxxx xxxxxxxx, xxxxxxxx xxxxx xxxxxxxxx, xxxxxx xxxxxxxxxxx xxxxxxxx), xxxxxxx jatečně xxxxxxxxxx xxxx, xxxxxxxxxxx stáda, xxxxxxxxxxxxx parametrech nebo xxxxxxx xxxxxxxxx podmínkách xxxxxx. Xxxxx x&xxxx;xxxxxxxxxx xxxxxxxx lze xxxxxxxxxx xxxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxx laboratorními studiemi xxxxxxxx příslušný parametr. |
|
2. |
Doplňkové xxxxx, xxxxx xxxxxxxxx xxxxxxxxx důsledky xxxxxxxxx xxxxxx xxx xxxxxxx xxxxxxxxx X&xxxx;xxxxxxxxxxx xxxxx, které xxxxxxxx xxxxxxxxx xxxxxxx xxxxxxxxx (např. omezená xxxxxxx xxxxxx a fosforu xxxx xxxxxxx xxxxxxxx xxxxxx, xxxxxxxxx xxxxxxxx), xx xxxxx účinnost x&xxxx;xxxxxxxx druhu doložit xxxxx xxxxxxxxxxxx studiemi xxxxxxxxx xx xxxxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxx. Xxxxxx xxxxxx x&xxxx;xxxxx xxxxxxx přizpůsobení xx doplňkové xxxxx. |
4.1.5&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;X:&xxxx;Xxxx xxxxxxxxxxxx v období xx xxxxxxx xxxxx xx xxx
Xxxxx xxxxx se xxxxxxx xxxxx ustanovení xx.&xxxx;7 odst. 3 xxxx.&xxxx;x)&xxxx;xxxxxxxx (XX) x.&xxxx;1831/2003.
4.2&xxxx;&xxxx;&xxxx;Xxxxxxxxxxxx xxxxxxxxx xxxxx: enzymy x&xxxx;xxxxxxxxxxxxxx
4.2.1&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;X:&xxxx;Xxxxxxx xxxxxxxxxxx
Xxxxxxx xx celý xxxxx&xxxx;X&xxxx;xxxxxxx&xxxx;XX.
4.2.2&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;XX: Identita, xxxxxxxxxxxxxxx x&xxxx;xxxxxxxx pro xxxxx xxxxxxxxx látky; xxxxxx xxxxxxx
Xxxxxxx se xxxx xxxxx&xxxx;XX xxxxxxx&xxxx;XX.
4.2.3&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;XXX: Xxxxxx xxxxxxxx xx bezpečnosti xxxxxxxxxxx xxxxx
|
4.2.3.1 |
Xxxxxx xxxxxxxx xx xxxxxxxxxxx používání xxxxxxxxx látky xxx xxxxxx xxxxxxx Xxxxxxx xx xxxx xxx&xxxx;3.1.1 přílohy II. Žadatelé xx xxxxxxxx, aby xxxxx možno xxxxxxxxx x&xxxx;xxxxxxx skupiny xxxxxxxxxxxx 100xxxxxxx xxxxxxxx dávky x&xxxx;xxxxxxx xxxxx xxxxxxxxxxxx xxxxxxxxx. X&xxxx;xxxxxx xxxxx xxx xxxxxx xxxxxxxxxxxxxx xxxxx doplňkové xxxxx. Xxxxxxxxxxx se xxxxxx xxxxxxxx xxxxxxxx xxxxxxxxxx xxxxxx, poměr xxxxxxxx xxxxxxx (xxxxxxx) / xxxxx (látek) x&xxxx;xxxxxxxx xxxxxxxxx xxxxxxxxxxxxx xxxxxxx xxxx musí xxx xxxxxx jako x&xxxx;xxxxxxx xxxxxxxx. X&xxxx;xxxxxx krmivo xxxxxxxxx vhodný substrát(y). Celý xxx&xxxx;3.1.2 přílohy II xx xxxxxxxx xx všechny xxxxxxxxxxxxxx x&xxxx;xxxxxx, které xxxx xxxxx katalytický xxxxxx xx složky xxxxxxxxxxx xxxxx xxxx x&xxxx;xxxxxxx xx xxx xx udává, že xxxxxxxxx xxxxxxx xxxxxxxxxxx xxxxx. X&xxxx;xxxxxxx nové xxxxxxxx xxxx xxxxxxxx xxxxxxx xxxxxxxx xxxxxxxxxxxxxxx xxxxx xxx nezbytné doplňkové xxxxxx, aby xxxx xxxxxxxxx xxxxxxxxxxx xxxxxxxxxxxx xxxxxx na komenzální xxxxxxxxxxx xxxxx xxxxxxxxx xxxxxx. X&xxxx;xxxxxxxxxxx xxxx xxxxx xxxxx počítání xxxxxxxxxxx xxxxx xxxxx x&xxxx;xxxxxxx, xx důkazy xxxxxxxxx xxxxxxxxxx xxxxx xxxxxx bachoru (měřeno xx xxxxx xxxx xxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxx kyselin, xxxxxxx xxxxxxxxxxx xxxxxxxxxx nebo xxxxxxx celulolýza). |
|
4.2.3.2 |
Studie xxxxxxxx xx xxxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxx xxx xxxxxxxxxxxx
Xxxxxx x&xxxx;xxxxxxxxxxxxxx xxxxx xxxxx xxxx celé xxxxxxxxx xxxxx, která ve xxxxxxx xxxxxxx xxxx xxxxxxxxx jiné xxxxxx xxxxxxxxxxx x&xxxx;xxxxxxxxxxxxx xxxxxxx. Xxxxx xx nezbytné xxxxxxxxxx látku otestovat, xxx xxxx zajištěno, xx xxxxxxxxxx xxxxxxxxx xxxx jiné materiály, xxxxx xxxxx poškodit xxxxxxx xxxxxxxxxxxx xxxxxxxxx xxxxxxx ze xxxxxx, xxx xxxx xxxxxx xxxxxx nebo xxxxx xxxxxxxxxx xxxxxx xxxxxxxxxxx xxxxxxx. Xxxxxxx xxxxxxxxxxxxxxx xxxxxxxx xxxxxxxx xxx xxxxx xxxx xxxxxxx přijímání xxxxx (včetně člověka) xx však xxxxxxxx xx skupin xxxxxxxxx, xxx něž xxxx x&xxxx;xxxxxxxxx údaje x&xxxx;xxxxxxx xxxxxxxxx používání, xxxx xx xxxxxx, xxx xxx xxxx xxxxxxx xxxxxx xxxxxx vymezena. Xxxxxxx xxxxxxxxx xxxxxxx x&xxxx;xxxxxxxxxxxxxx, xxxxx xx x&xxxx;xxxxxxxxxxx používají x&xxxx;xxxxxxxx xxxxxx, xx xxxxxxx xxxxxx rozpoznané a významně xxxxxxx xxxxxxxxx výrobními xxxxxxx. Proto xx xxx xxxxxx z mikrobiálních xxxxxx a pro xxxxxxxxxxxxxx, xxx xxx xxxx x&xxxx;xxxxxxxxx xxxxx x&xxxx;xxxxxxx xxxxxxxxx xxxxxxxxx, x&xxxx;xxxx-xx xxxxxx xxxxxxxxxxxxx procesu xxxxxx xxxxxxxxxx x&xxxx;xxxxx, xxxxxxxxxx xxxxxxx xxxxxxxx (xxxx. testování xxxxxx xxxxxxxx xxxx xxxxxxxxxxxx) xx xxxxx. Xxxxx x&xxxx;xxxxxx xxxxxxxxx x&xxxx;xxxxxxxxx xxxxxxxxxxx x&xxxx;xxxxxxxx xxxxxx xx vždy xxxxx xx zabývat xxxxxxxxxxx xxxxxxxxxxxx xxxxxxxxx v bodě 2.2.2.2 xxxxxxx&xxxx;XX. Xx-xx organismus xxxx jeho xxxxx xxxx a neexistují dostatečné xxxxxxxx x&xxxx;xxxxxxxx (xxxxxxxxxxx) xxxxxxxxx, xxx xxx xxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx metabolitů, xx xxxxx xxxxxxxxx xxxxxx xxxxxxxxxxxx x&xxxx;xxxxxx toxicity xxxxxxxxx x&xxxx;xxxxxxxxxxx xxxxxxx, xxxxx obsahují xxxxxxxxxxxxx xxxxxxxxxxxxxx nebo xxxxxx. X&xxxx;xxxxx případě mají xxxxxx studií xxxxxxxxxxxx xxxxxx mutagenity x&xxxx;xxxxxx xxxxxxxxxxxx orální xxxxxxxx. Xxxxxxxxxx xx, xxx xx tyto xxxxxx xxxxxxxxx s bezbuněčnou fermentační xxxxx xxxx v případě xxxxxxxxxx tuhých xxxxxxxxx x&xxxx;xxxxxxx extraktem. |
|
4.2.3.3 |
Studie xxxxxxxx xx xxxxxxxxxxx xxxxxxxxx xxxxx xxx uživatele/pracovníky Použije xx xxxx bod 3.3 xxxxxxx&xxxx;XX s výjimkou těchto xxxxxxx:
|
|
4.2.3.4 |
Xxxxxx týkající xx xxxxxxxxxxx doplňkové látky xxx xxxxxxx prostředí Celý xxx&xxxx;3.4 xxxxxxx&xxxx;XX xx xxxxxxxx xxxx xx xxxxxxxxxxxxxx, xxxxx xxxxxx xxxxxxxxx xxxxxx xxxx xxxxxx všudypřítomné x&xxxx;xxxxxxxx xxxxxxxxx. |
4.2.4&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;XX: Xxxxxx týkající xx xxxxxxxxx xxxxxxxxxxx xxxxx
Xxxxxxx xx xxxx xxxxx&xxxx;XX přílohy II.
|
1. |
Doplňkové xxxxx, xxxxx xxxx xxxxxxxxx xxxx xx živočišnou xxxxxx, užitkovost xxxx xxxxx xxxxxxx podmínky x&xxxx;xxx xxxxxxx xxxxxxx „xxxx xxxxxxxxxxxx doplňkové xxxxx“. Xxxxxx xxx prokázat xxxxx xx vztahu xx xxxxxxx xxxxxxxx xxxxx xxxx xxxxxxxxx xxxxxx. X&xxxx;xxxxxxxxxx na xxxxxxxxxxxx xxxxxxxxx látky xxxxx být xxxxxx xxxxxxxx xx xxxxxxxxxx xxxxxxxxxxxxxxxxx (xxxx. xxxxxxxxx xxxxxxxx, xxxxxxxx xxxxx xxxxxxxxx, nárůst xxxxxxxxxxx xxxxxxxx), skladbě xxxxxxx xxxxxxxxxx xxxx, užitkovosti xxxxx, xxxxxxxxxxxxx parametrech xxxx xxxxxxx životních xxxxxxxxxx xxxxxx. Xxxxx x&xxxx;xxxxxxxxxx xxxxxxxx xxx xxxxxxxxxx xxxxxxxxxxxx studiemi xxxxxxxxx xxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxx příslušný xxxxxxxx. |
|
2. |
Xxxxxxxxx látky, xxxxx xxxxxxxxx ovlivňují xxxxxxxx xxxxxxxxx xxxxxx pro xxxxxxx prostředí. U doplňkových xxxxx, xxxxx xxxxxxxx ovlivňují xxxxxxx prostředí (např. xxxxxxx xxxxxxx xxxxxx xxxx fosforu xxxx xxxxxxx produkce xxxxxx, xxxxxxxxx příchutí), xx xxxxx xxxxxxxx x&xxxx;xxxxxxxx xxxxx xxxxxxx xxxxx xxxxxxxxxxxx xxxxxxxx účinnosti xx zvířaty xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx účinky. Xxxxxx xxxxxx v úvahu xxxxxxx xxxxxxxxxxxx se xxxxxxxxx látce. |
4.2.5 Oddíl V: Plán xxxxxxxxxxxx x&xxxx;xxxxxx po xxxxxxx xxxxx xx xxx
Xxxxx xxxxx xx použije xxxxx xxxxxxxxxx xx.&xxxx;7 xxxx.&xxxx;3 xxxx.&xxxx;x)&xxxx;xxxxxxxx (ES) x.&xxxx;1831/2003.
5.&xxxx;&xxxx;&xxxx;XXXXXXXXXXXXXXX A HISTOMONOSTATIKA
5.1 Oddíl I: Shrnutí xxxxxxxxxxx
Xxxxxxx xx celý xxxxx&xxxx;X&xxxx;xxxxxxx&xxxx;XX.
5.2&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;XX: Xxxxxxxx, charakteristika a podmínky xxx xxxxx xxxxxxxxx xxxxx; xxxxxx analýzy
Použije xx celý oddíl II xxxxxxx&xxxx;XX.
5.3&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;XXX: Xxxxxx xxxxxxxx xx xxxxxxxxxxx xxxxxxxxxxx xxxxx
5.3.1&xxxx;&xxxx;&xxxx;Xxxxxx týkající xx xxxxxxxxxxx používání xxxxxxxxx xxxxx xxx xxxxxx xxxxxxx
Xxxxxxx xx xxxx xxx&xxxx;3.1 xxxxxxx&xxxx;XX.
5.3.2&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxx xx xxxxxxxxxxx xxxxxxxxx xxxxxxxxx látky pro xxxxxxxxxxxx
Xxxxxxx se xxxx xxx&xxxx;3.2 xxxxxxx&xxxx;XX.
5.3.3&xxxx;&xxxx;&xxxx;Xxxxxx týkající xx xxxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxx xxx xxxxxxxxx/xxxxxxxxxx
Xxxxxxx xx xxxx xxx&xxxx;3.3 xxxxxxx&xxxx;XX.
5.3.4&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxx xx bezpečnosti xxxxxxxxx xxxxxxxxx látky pro xxxxxxx prostředí
Použije xx xxxx bod 3.4 xxxxxxx&xxxx;XX.
5.4&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;XX: Xxxxxx xxxxxxxx xx xxxxxxxxx xxxxxxxxx xxxxx
Xxxx xxxxxxxxx xxxxx xxxxxx xxxxxxx xxxx xxxxxxxx xxxxxx Xxxxxxx xxx. xxxx Histomonas xxxxxxxxxxx. Xxxxxx se xxxxxxxx xxxxxxx o zvláštních xxxxxxxx xxxxxxxxx xxxxx (xxxx. xxxxxxxxxxxx druh) a jejích xxxxxxxxxxxxxxx xxxxxxxxxxxx (xxxx. xxxxxxx xxxxxxxxx, mortality, xxxxx xxxxxx a výskytu xxxxxxxxxx xxxx). Popřípadě xx předloží xxxxxxxxx x&xxxx;xxxxxx na xxxx x&xxxx;xxxxxxxx krmiva (výkrm xxxxxxx, xxxxxxx nosnic x&xxxx;xxxxxxx), xxxxxxxx na xxxxxxx xxxxx (plemenná xxxxxx).
Xxxxxxxxxx xxxxx x&xxxx;xxxxxxxxx xxxx xxxxxxxx ze xxx xxxx xxxxxx x&xxxx;xxxxxxxx xxxxxxx:
|
— |
xxxxx jednotlivé x&xxxx;xxxxxxx infekce, |
|
— |
přirozená/umělá xxxxxxx x&xxxx;xxxxx xxxxxxxxx xxxxxxxx xxx xxxxx, |
|
— |
xxxxxxxx xxxxxxxx xxx xxxxx při xxxxxxxxx x&xxxx;xxxxxx. |
Xxxxxx x&xxxx;xxxxxxx xxxxxxxxxxxx x&xxxx;xxxxxxxxx xxxxxxxxx (xxxx. xxxxxxx xxxx xxxxxxx) mají prokázat xxxxxxxxx účinnost xxxxx xxxxxxxxx x&xxxx;xxxxxxxxxx xxxxxxxxx. Xxx xxxxxxxx xxxxxxxx xx xxxxxxxx xxx xxxxxx xxxxxxxxxx xxxxxxxx xxx xxxxx (např. xxxxxx xxx volném xxxxxxxx x&xxxx;xxxxxxx, xxxxxx xxx xxxxxxxx xxxxx x&xxxx;xxxxxxx). Xxxxxxxx xx xxxxxx xxx xxxxxx x&xxxx;xxxxxx x&xxxx;xxxxxxx mírou xxxxxxxxx xxxxxxx.
5.5&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;X:&xxxx;Xxxx monitorování x&xxxx;xxxxxx xx xxxxxxx xxxxx xx xxx
Xxxxx xxxxxxx&xxxx;XX se použije xxxxx xxxxxxxxxx čl. 7 xxxx.&xxxx;3 xxxx.&xxxx;x)&xxxx;xxxxxxxx (XX) x.&xxxx;1831/2003.
6.&xxxx;&xxxx;&xxxx;XXXXXXXXXXX Z VĚTŠINOVÝCH XXXXX XX DRUHY XXXXXXXXX
Xxxxxxxxx xxxxx xxxx xxxxxxxx x&xxxx;xx.&xxxx;1 xxxx.&xxxx;2 xxxxxx xxxxxxxx.
X&xxxx;xxxxxx na xxxxxxxxx xxxxxxxxxx xxxxx xxx xxxx, xxxxx xx x&xxxx;xxxxxxxxxxxxxx hlediska srovnatelný x&xxxx;xxxxxx, xxx xxxx xxx xxxx užití xxxxxxxxx xxxxx povoleno, xx xxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxx v plném xxxxxxx.
Xxxx uvedené požadavky xx xxxxxxxx pouze xx xxxxxxxxxx xxxxxxxx xxx xxxxxxxxx druhy x&xxxx;xxxxxxx xx doplňkové xxxxx, xxxxx již xxxx xxxxxxxx xxx xxxxx většinové. Xxx xxxxxxxx xxxxxx doplňkových xxxxx xxxxxxxxxx xxxxx xxx xxxxxxxxx druhy xx xxxxxxx xxxx xxxxxxx xxxxxx v závislosti xx xxxxxxxxx/xxxxxxx xxxxxxx xxxxxxxxx látky (viz xxxxxxxxxxxx zvláštní xxxxxxxxx x&xxxx;xxxxxxx&xxxx;XXX).
6.1&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;X:&xxxx;Xxxxxxx xxxxxxxxxxx
Xxxxxxx xx xxxx xxxxx&xxxx;X&xxxx;xxxxxxx&xxxx;XX.
6.2&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;XX: Xxxxxxxx, xxxxxxxxxxxxxxx x&xxxx;xxxxxxxx xxx xxxxx doplňkové látky; xxxxxx analýzy
Oddíl II xxxxxxx&xxxx;XX xx xxxxxxx xxxxx:
|
— |
xxx xxxxxxxxx xxxxx, které xxxx xxxxxx na xxxxxxxx povolení, se xxxxxxx xxxx xxxxx&xxxx;XX, |
|
— |
xxx xxxx xxxxxxxxx látky xx xxxxxxx xxxx&xxxx;2.1.2, 2.1.3, 2.1.4, 2.1.4.2, 2.2, 2.3.1, 2.3.2, 2.4.1, 2.4.2, 2.4.4, 2.5, 2.6. |
6.3&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;XXX: Xxxxxx xxxxxxxx se xxxxxxxxxxx xxxxxxxxx doplňkové látky
6.3.1 Studie xxxxxxxx se xxxxxxxxxxx xxxxxxxxx doplňkové látky xxx xxxxxx xxxxxxx
|
6.3.1.1 |
Xxxxxxxxx x&xxxx;xxxxxxxx xxxxx Xxxxx xxxxxxxxx xxx xxxxxxxxxx xxxxxxxxx / xxxxxxx xxxxxxx xxxxxxxxxxx látek. V zásadě se xxxxxx xxxxxxxxx u menšinových xxxxx nepožadují, pokud xxxxxxxxx xxxxx xxxxxxxx xxxxxx rozpětí xxx xxxxxxxxxx (nejméně koeficient 10) x&xxxx;xxxxxxxxxxx xxxxxxxxxxx xxxxx, který xx x&xxxx;xxxxxxxxxxxxxx xxxxxxxx xxxxxxx. Xxxxx xxx xxxxxxxxx cílové xxxxx (xxxxxx xxxxxxxxxxxxxxx x&xxxx;xxxxxxxxxxxx xxxxx x&xxxx;xxxxxxx) xxxxxxxx xxxxxxx x&xxxx;xxxxxx xxxxxxx pro xxxxxxxxxx, xxxxxxxxxx xx xxxxx xxxxxx xxxxxxxxx pro xxxxxxxxx xxxxx, xxxxx xxxxxx z fyziologického xxxxxxxx xxxxxxx (xxxx. koně xxxx králíci). Xxxxx xx xxxxxxxx studie xxxxxxxxx, doba trvání xxxxxx xxx xxxxxxxxx xxxxx (vyjma králíků) xxxx nejméně 28&xxxx;xxx xxx xxxxxxx v růstu x&xxxx;42&xxxx;xxx xxx dospělá xxxxxxx. X&xxxx;xxxxxxx platí xxxx doby xxxxxx: xxxxx králíků: 28&xxxx;xxx; xxxxxx xxxxxxx: jeden xxxxxx (od inseminace xx konce doby xxxxxxx). Xxxxx xx xxxxxx xxxxxxxx xx xxxxxx a odstavené králíky, xxxxxxxx xx xx xxxxxxxxxx období 49&xxxx;xxx (xxxxxxxx xxxxx xxxxx xx xxxxxxxx) x&xxxx;xxxx xxxxxxxxx xxxxxxx xx xx odstavu. Xxx xxxx (xxxx xxx xxxxxxxxxx) xx xxxxxxxx 90xxxxx xxxxxx. |
6.3.2&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxx xx xxxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxx pro xxxxxxx xxxx xxxxxxxxxxxx
|
6.3.2.1 |
Xxxxxx xxxxxxxxxxx Xxxxx xxxxxxxxx pro xxxxxxxxxx kategorie x&xxxx;xxxxxxx xxxxxxx doplňkových látek. Studie xxxxxxxxxxx xx nepožadují, xx-xx xxxxxxxxx xxxxx xxx povolena xxx xxxxx x&xxxx;xxxxx, xxxxx xx z fyziologického xxxxxxxx xxxxxxxxxxx x&xxxx;xxxxxxxxxxx xxxxx, xx xxx se xxxxxxxx žádost x&xxxx;xxxxxxxx. Xxxxxxxx xxxxxxxxx x&xxxx;xxxxxxxxxxxxxx xxxxxxxx xxxxxxxxxx, xxxxxxxx xx xxx posouzení xxxxxxxxxx metabolismu xx xxxxxxxxxx xxxxxxxxx metabolického xxxxxxx xx základě xxxxxx xx vitro (xxxx. x&xxxx;xxxxxxxxxx xxxxxx xxxxxxx xxxxx). Xxxx-xx xxxxxxxxx xxxx x&xxxx;xxxxxxxxxxxxxx xxxxxxxx xxxxxxx většinovému druhu, xx nutno xxxxxx xxxxx x&xxxx;xxxxxxxxxxx xxxxxxxxx xxxxx x&xxxx;xxxxxxxxxxx xxxxx. |
|
6.3.2.2 |
Xxxxxx xxxxxxx Xx-xx xxxxxxx xxxx xxxxxxxxx xxxxxxxxx xxxxxxxxxxx, xxxxxxxx se xxxxx xxxxxxxxxxxx xxxxxxxxxxxxxx xxxxxxx x&xxxx;xxxxxxxxxxxxx xxxxxxx a produktech. Xx xxxxx xxxxxxxxx xxxxxxxxx xx použije xxxx xxx&xxxx;3.2.1.2 přílohy II. |
|
6.3.2.3 |
Posouzení xxxxxxxxxxx xxx xxxxxxxxxxxx Xxxxx xxxxxxxxxxx xxxxxx xxxxxxx (XXX) Xxxxxxxxx XXX xxx xxxxxxx xx xxxxxxxxxxx, xx se x&xxxx;xxxxxxxxxxxxx xxxxxxx xxxxxxxxxxx xxxxx x&xxxx;xxxxxxxxx s podobným xxxxxxxxxx xxxxxx nevyskytují xxxxx xxxxxxxx xxxxxxx v obsahu xxxxxxx. XXX xxx xxxxxxxxxxxx x&xxxx;xxxxx tříd xxxxxx xxxxx:
XXX xxx xxxx xxx xxxxxxxxxxxx, xxxxx xxxxxxxx XXX xxx xxxxxxxxxxx přežvýkavce x&xxxx;xxxxxxxxxxx xxxxxxxxxxxxxxx savce. Pokud byly xxxxxxxx xxxxxxxxx XXX x&xxxx;xxxxx (xxxx ovcí), xxxxxx a kuřat (nebo xxxxxxx), které xxxxxxxxxxx xxxxxxxxx xxxxx s různými xxxxxxxxxxxxx xxxxxxxxxxx x&xxxx;xxxxxxxx xxxxx, je možno xxxxxxxx xxxxxx XXX xxxxxx xxx ovce, xxxxxxxx x&xxxx;xxxxxxx, xxx xxxxxxx, xx xx xxxxxxxx xx možnou xxxxxxxxxxx na všechna xxxxxxx, xxxxx jsou xxxxxx k produkci potravin, x&xxxx;xxxxxxxx ryb. X&xxxx;xxxxxxx xx xxxxx Výboru xxx veterinární xxxxxx xxxxxxxxx (XXXX)&xxxx;(10) xxx xxxxxxxxx MLR pro Xxxxxxxxxx a ostatní xxxx, xxxxx xxx xxxxxxxx xxxxxxxxxxx z MLR xx xxxxx xxxxxxxxxxx xxxxx xx Xxxxxxxxxx x&xxxx;xxxxxxx xxxx xx předpokladu, xx výchozí xxxxx xxxx přijatelné xxxx xxxxxxxxxxxx xxxxxxxx xxx XXX xx xxxxx x&xxxx;xxxx, lze MLR xxxxxxxxxxxx xx xxxxxxx xxxxxxx xxxxxx k produkci xxxxxxxx. Xxxx k dispozici xxxxxxxxxx xxxxxx pro xxxxxxxxxxxx xxxxxxx x&xxxx;xxxxxxxxxxxxx tkáních x&xxxx;xxxxxxxxxx xxxxx zvířat xxxxxxxx x&xxxx;xxxxxxxx potravin. |
6.3.3 Studie xxxxxxxx xx bezpečnosti xxxxxxxxx xxxxxxxxx xxxxx xxx uživatele/pracovníky
Použije xx xxxx bod 3.3 xxxxxxx&xxxx;XX.
6.3.4&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxx xx xxxxxxxxxxx xxxxxxxxx doplňkové látky xxx xxxxxxx prostředí
Posouzení xxxxx xxx xxxxxxx xxxxxxxxx xxx extrapolovat x&xxxx;xxxxxxxxx xxxxxxxxxxx xxx xxxxxxxxx xxxx, xxxxx xx z fyziologického xxxxxxxx xxxxxxxxxxx. Xxx doplňkové xxxxx, které xxxx xxx používány x&xxxx;xxxxxxx, xx xxxxxxx celý xxxxx x&xxxx;xxxxxxxxxxxx x&xxxx;xxxxxxxxxx xxx xxxxxx xxxxxxxxx / xxxxxxx skupinu xxxxxxxxxxx xxxxx.
6.4&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;XX: Studie xxxxxxxx xx xxxxxxxxx xxxxxxxxx xxxxx
Xxxxx doplňková xxxxx xxxx xxx xxxxxxx xxxxxx xxxxxxxx xxx xxxxxxxxx xxxx, xxxxx je x&xxxx;xxxxxxxxxxxxxx xxxxxxxx xxxxxxxxxxx, a pokud xx znám xxxx xxxxxxxx mechanismus xxxxxxxx xxxxxxxxx xxxxx, xx xxxxx xxxxxxxxx za xxxxxxxx xxxxxxxxx xxxxxx x&xxxx;xxxxxxx mechanismu xxxxxxxx x&xxxx;xxxxxxxxxxx xxxxx. Xxxxx xxxxxxxx spojitost xxxxxxxxxx, xx xxxxx xxxxxxxx xxxxxxxx xxxxx xxxxxxxx xxxxxxxx xxx xxxxx&xxxx;XX x&xxxx;xxxxxxx&xxxx;XX. X&xxxx;xxxxxxxxx případech xxxx xxx xxxxxx xxxxxxxxxx xxxxx zvířat xx xxxxxx xxxxxxxxxxx xxxx (xxxx. kozy x&xxxx;xxxx xxxxxxxxx x&xxxx;xxxxxxxx xxxxx). X&xxxx;xxxxx xxxxxx (X&xxxx;≤ 0,1) xxxx xxxxxx xxxxxxxxxxx (P ≤ 0,05), xx-xx xx xxxxx, xx xxxx xxx prokázána xxxxxxxxxx.
Xxxxxxxx-xx xx prokázání xxxxxxxxx, xxxx xxxxxx studií xxxxxxxxx xxxxxxxx xxxxxxxxxxxx xxxxxxxxxx fázím xxxxxxxxxxx xxxxx, který je x&xxxx;xxxxxxxxxxxxxx hlediska srovnatelný. X&xxxx;xxxxxxxxx případech minimální xxxx xxxxxx xxxxxx xxxxxxx xxxxxxxxx xxxxxxxxxx x&xxxx;xxxx&xxxx;4.4 xxxxxxx&xxxx;XX x&xxxx;xxxxxxx&xxxx;XX.
6.5&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;X:&xxxx;Xxxx xxxxxxxxxxxx v období po xxxxxxx látky xx xxx
Xxxxx xxxxx přílohy II xx xxxxxxx podle xxxxxxxxxx xx.&xxxx;7 xxxx.&xxxx;3 xxxx.&xxxx;x)&xxxx;xxxxxxxx (XX) x.&xxxx;1831/2003.
7.&xxxx;&xxxx;&xxxx;XXXXXXX X&xxxx;XXXXXXXX CHOVU X&xxxx;XXXXXXX XXXXXXX, KTERÁ NEJSOU XXXXXX X&xxxx;XXXXXXXX XXXXXXXX
Xxxxxxx x&xxxx;xxxxxxxx chovu x&xxxx;xxxxxxx xxxxxxx, xxxxx xxxxxx xxxxxx x&xxxx;xxxxxxxx xxxxxxxx, xxxx xxxxxxxx x&xxxx;xx.&xxxx;1 xxxx.&xxxx;1 xxxxxx xxxxxxxx.
7.1&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;X:&xxxx;Xxxxxxx xxxxxxxxxxx
Xxxxxxx xx xxxx xxxxx&xxxx;X&xxxx;xxxxxxx&xxxx;XX.
7.2&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;XX: Identita, charakteristika x&xxxx;xxxxxxxx pro xxxxx xxxxxxxxx látky; xxxxxx xxxxxxx
Xxxxx&xxxx;XX přílohy II xx xxxxxxx xxxxx:
|
— |
xxx xxxxxxxxx xxxxx, které jsou xxxxxx na xxxxxxxx xxxxxxxx, se xxxxxxx xxxx xxxxx&xxxx;XX, |
|
— |
xxx xxxx xxxxxxxxx látky se xxxxxxx body 2.1.2, 2.1.3, 2.1.4, 2.1.4.2, 2.2, 2.3.1, 2.3.2., 2.4.1, 2.4.2, 2.4.4, 2.5, 2.6. |
7.3&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;XXX: Studie xxxxxxxx xx bezpečnosti xxxxxxxxx xxxxx
7.3.1&xxxx;&xxxx;&xxxx;Xxxxxx týkající se xxxxxxxxxxx xxxxxxxxx doplňkové xxxxx pro cílová xxxxxxx
Xxxxx požadavky pro xxxxxxxxxx xxxxxxxxx / xxxxxxx skupiny doplňkových xxxxx. Požaduje-li xx xxxxxx xxxxxxxxx, xxxx xxxx xxxxxx xxxx xxxxxxx 28 dní.
Studie tolerance xx nepožaduje, pokud xxxxxxxxx látka vykazuje xxxxxxxxxxx x&xxxx;xxxxxx rozpětí xxx bezpečnost u třech xxxxxxxxxxx druhů (xxxxxx xxxxxxxxxxxxxxx x&xxxx;xxxxxxxxxxxx savců x&xxxx;xxxxxxx).
7.3.2&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxx xx xxxxxxxxxxx xxxxxxxxx doplňkové xxxxx xxx xxxxxxxxxxxx
Xxxxx xxx se obvykle xxxxxxxxxx. Xxxxxxxxx xx xxxxxx bezpečnosti xxxxxxxx.
7.3.3&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxx se xxxxxxxxxxx xxxxxxxxx xxxxxxxxx látky xxx uživatele/pracovníky
Použije se xxxx xxx&xxxx;3.3 přílohy II.
7.3.4 Studie xxxxxxxx se xxxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxx xxx xxxxxxx xxxxxxxxx
Xxx&xxxx;3.4 xxxxxxx&xxxx;XX xx xxxxxxxxxx.
7.4&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;XX: Xxxxxx týkající xx xxxxxxxxx xxxxxxxxx xxxxx
Xxxxx xxxxxxxxx pro xxxxxxxxxx xxxxxxxxx / xxxxxxx xxxxxxx xxxxxxxxxxx xxxxx.
Xxxxxxxx xxxxxxxxx xxxxx, pro xxx xx xxxxxxxx xxxxxx xx xxxxxxxxx, xxx byla xxxxxx xxxxxxxx xxx xxxx, xxxxx xx x&xxxx;xxxxxxxxxxxxxx xxxxxxxx xxxxxxx, nepožaduje xx xxxxx xxxxxxxxx xxxxxxxxx, xxxx-xx xxxxxxxxxx xxxxxx x&xxxx;xxxxxxxxxxx xxxxxxxx xxxxxx. Xxxxx doplňková xxxxx xxxxxx xxxxx xxxxxxxx xxxx xxxxxxxxxx xxxxxx xx xxxxxxxxxxx xxxxxxxx xxxx jiné xxx x&xxxx;xxxxxxx xxxxxxxxxxx xxxxxxxx, je xxxxx xxxxxxxx prokázat podle xxxxxxxx xxxxxxxx xxx xxxxx&xxxx;XX v příloze II.
Doba xxxxxx xxxxxxxxxxxx xxxxxxx xxxxxxxxx xxxx nejméně 28 dní.
7.5 Oddíl V: Plán xxxxxxxxxxxx v období po xxxxxxx látky xx xxx
Xxxxx xxxxx xxxxxxx&xxxx;XX xx xxxxxxx xxxxx xxxxxxxxxx xx.&xxxx;7 xxxx.&xxxx;3 xxxx.&xxxx;x)&xxxx;xxxxxxxx (XX) x.&xxxx;1831/2003.
8.&xxxx;&xxxx;&xxxx;XXXXXXXXX XXXXX, XXXXX XXX XXXX POVOLENY XXX XXXXX V POTRAVINÁCH
8.1 Oddíl I: Shrnutí dokumentace
Použije xx celý oddíl I přílohy II.
8.2 Oddíl II: Xxxxxxxx, charakteristika x&xxxx;xxxxxxxx xxx xxxxx xxxxxxxxx xxxxx; metody xxxxxxx
Xxxxx&xxxx;XX xxxxxxx&xxxx;XX xx xxxxxxx xxxxx:
|
— |
xxx xxxxxxxxx xxxxx, xxxxx xxxx xxxxxx xx xxxxxxxx povolení, xx použije celý xxxxx&xxxx;XX, |
|
— |
xxx xxxx xxxxxxxxx xxxxx xx xxxxxxx xxxx&xxxx;2.1.2, 2.1.3, 2.1.4, 2.1.4.2, 2.2, 2.3.1, 2.3.2., 2.4.1, 2.4.2, 2.4.4, 2.5, 2.6. |
8.3&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;XXX: Xxxxxx xxxxxxxx se xxxxxxxxxxx doplňkových xxxxx
Xxxx xxx uvedeno nejnovější xxxxxxxx xxxxxxxxx bezpečnosti xxxxxxxxxxxxxxx xxxxxxxxxx xxxxx x&xxxx;xxxxxxxx případnými xxxxxxxx xxxxxxxxx údaji.
Pro xxxxxxxxx xxxxx, xxxxx jsou xxxxxxxx xxxx xxxxxxxxxxxxx xxxxxxxx látky xxxx xxxxxxxxx x&xxxx;Xxxxxxxx xxxx xxxx složky xxxxxxxx xxx xxxxxxxxxxx xxxxxxx, xxxxxx studie xxxxxxxx xx bezpečnosti pro xxxxxxxxxxxx x&xxxx;xxxxxxxxxx xxxxxxx xxxxx.
Xxxxxx xx xxxx&xxxx;3.1, 3.2 a 3.3 přílohy II xx zřetelem xx xxxxxxxxx xxxxxxxx o bezpečnosti xxxxxx xxxxx, xxxxx xxxx používány x&xxxx;xxxxxxxxxxx. Xxxxxxxx látky, které xxxx xxxxxxxxx xxxxxx x&xxxx;xxxxxxxxxxx, xxx xxxxxxxxxxxx xxxx:
|
— |
x&xxxx;xxxxxxxxxxxxxxxx ADI (xxx xxxxxxxxxx xxxxxxx xxxxxxx xxxxxx xxxxxx xxx xxxxx x&xxxx;xxxxx xxxxxx xxxxxxxxx), |
|
— |
xx xxxxxxxxxx ADI xxxx UL xxxx |
|
— |
x&xxxx;xxxxxxxxxxxx XXX (xxx xxxxx, x&xxxx;xxxxx xxxxxxxx xxxxx xxxxxxxxxxx xx xxxxxxxx xxxxxx xxxxxxxxxxx). |
8.3.1&xxxx;&xxxx;&xxxx;Xxxxxx týkající xx xxxxxxxxxxx používání xxxxxxxxx xxxxx xxx xxxxxx xxxxxxx
Xx-xx obsah xxxxx xxxxxxxxx xxxxx xxxxxxx xxxx v případě xxxxxxxx, lze xxxxxxxxxx xxx cílové xxxxx xxxxxxxx xx xxxxxxx xxxxxxxxxx xxxxxxxxxxxxxxx údajů xx xxxxxxx xx xxxx s přihlédnutím x&xxxx;xxxxxxxx xxxxxxxxx a metabolické schopnosti xxxxxxxx xxxxx. Je-li xxxxx užití x&xxxx;xxxxxxxx xxxxxxxx vyšší než xxxxxxxxxxxx xxxxx x&xxxx;xxxxxxxxxxx, xxxx být xxxxx xxxxxx xxxxx xxxxx xxxxxx tolerance x&xxxx;xxxxxxxx xxxxxxx.
8.3.2&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxx se xxxxxxxxxxx xxxxxxxxx doplňkové xxxxx pro xxxxxxxxxxxx
Xxxxx xxxxx jako xxxxxxxxx xxxxx vede x&xxxx;xxxxx xxxxxxxx xxxxxxxxxxxx nebo x&xxxx;xxxxxx druhu xxxxxxxxxx xxx x&xxxx;xxxxxxx xxxxx x&xxxx;xxxxxxxxxxx, xxxxx xxxxxxxxxx xxxxx xxxxxxxxxxxxx xxxxx x&xxxx;xxxxx o reziduích.
|
8.3.2.1 |
Pro xxxxxxxxx xxxxx, xxx něž xxxx xxxxxxxxxxxxx ADI Posouzení xxxxxxxxxxx pro xxxxxxxxxxxx xx xxxxxxxxxx xxxxx xxxxxxx, xxx xxxxx xxxxxxxxx xxxxx x&xxxx;xxxxxxxx xxxx x&xxxx;xxxxxxxxx druhu xxxxxxxxxx než xxx xxxxx x&xxxx;xxxxxxxxxxx. |
|
8.3.2.2 |
Xxxxxxxxx látky xx xxxxxxxxxx ADI xxxx XX Xxxxxxxxxx pro xxxxxxxxxxxx je xxxxx xxxxxxxx x&xxxx;xxxxxxxxxxxx x&xxxx;xxxxxxxxx xxxxxxxx xxxxxxxxxxx x&xxxx;xxxxx x&xxxx;xxxxxxxx xxxx zvláštní xxxxxxxx x&xxxx;xxxxxxxxxxx x&xxxx;xxxxxxxxxx xxxxxxxxxxxx u cílového druhu. Xx lze xxxxxxx xxxxxxxxxxx xxxxx o reziduích x&xxxx;xxxxxxxxxx. Xxxx-xx xxxxxxxx xxxxxx xxxxxxx, požadavek xx xxxxxx na xxxxxxxx xxxxxx v tkáních xxxx xxxxxxxxxx x&xxxx;xxxxxxxxxx xxxxxxx x&xxxx;xxxxxxx, jíž xxxx xxxxxxxx xxxxxxxx udávaná xxxxx. |
|
8.3.2.3 |
Xxxxxxxxxxxxx přídatné xxxxx, xxx xxx xxxxxx XXX xxxxxxxxx Xx xxxxx xxxxxxxxxxx xxxxx důvody, xxxx nebyla ADI xxxxxxxxx. Xxxxx to xxxxxxxx xxxxx x&xxxx;xxxxx xxxxxxxxx xxxxx x&xxxx;xxxxxxxx xx xxxxxxxx x&xxxx;xxxxxxxxxx xxxxxxx expozice x&xxxx;xxxxxxxxxxxx, xxxxxxxx xx xxxxx xxxxxxxxxxxxx xxxxxxxxx. Xxxxxxxxxx xxxxxxxx xxxxxxxxxxx z užití v krmivech xxx xxxxxxxxxxxx x&xxxx;xxxxx x&xxxx;xxxxxxxxx x&xxxx;xxxxxxxxxx. Xxxx-xx xxxxxxxx xxxxxx xxxxxxx, xxxxxxxxx xx xxxxxx xx xxxxxxxx obsahů x&xxxx;xxxxxxx xxxx produktech u neošetřené xxxxxxx x&xxxx;xxxxxxx, xxx xxxx xxxxxxxx xxxxxxxx xxxxxxx xxxxx. |
8.3.3&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxx xx xxxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxx pro xxxxxxxxx/xxxxxxxxxx
Xxxxxxx se xxxx xxx&xxxx;3.3 xxxxxxx&xxxx;XX.
Xxx xxxxxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxx xxx xxxxxxxxx xx xxxxxx x&xxxx;xxxxx bezpečnostní xxxxxxxx xxxxxxxxx pro xxxxxxxxxx x&xxxx;xxxxxx xxxxxxx xxxxxxxxxxx x&xxxx;xxxxxxxxxxx.
8.3.4&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxx xx xxxxxxxxxxx xxxxxxxxx xxxxxxxxx látky xxx xxxxxxx xxxxxxxxx
Xxxxxxxx xx xxx&xxxx;3.4 xxxxxxx&xxxx;XX.
8.4&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;XX: Xxxxxx xxxxxxxx xx xxxxxxxxx xxxxxxxxx látky
Jestliže je xxxxxx xxxxxxxxxx xxx xxxxxx xxxxxx xxxx xxx xxxxx x&xxxx;xxxxxxxxxxx, xxxxxx xxx nutné xxxxx xxxxxxxxx xxxxxxxxx. X&xxxx;xxxxxxx xxxxxxx xxxxx xxxxxxxxx xx účinnost xxxxxxx x&xxxx;xxxxxx&xxxx;XX xxxxxxx&xxxx;XX.
8.5&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;X:&xxxx;Xxxx xxxxxxxxxxxx v období xx xxxxxxx xxxxx xx xxx
Xxxxx xxxxx přílohy II xx xxxxxxx xxxxx xxxxxxxxxx čl. 7 odst. 3 xxxx.&xxxx;x)&xxxx;xxxxxxxx (XX) č. 1831/2003.
9. ZMĚNA XXXXXXXX
Xxxxxxx xx xxxxx xxxxxx xxxxxxxxx xxxxx xxxxxxxxxxxx pro xxxxxxxxx xxxxxxxx, xxxx dokumentace xxxxxxxxxx xxx xxxxxx xxxxx xx.&xxxx;13 xxxx.&xxxx;3 xxxxxxxx (XX) x.&xxxx;1831/2003 xxxxxxxx pouze xxxx xxxxxxx xxxxxxxxx.
Xxxxxx x&xxxx;xxxxx xxxxxxxx zahrnutých ve xxxxxxxxxx povolení, xxxx. xxxxxxxxxxxx, charakteristika xxxx xxxxxxxx xxx užití xxxxxxxxx xxxxx, xxxx xxxxxxxx, xx xxxxx xxxx xxxxx xxxxxxxx xxxxxx xxx xxxxxx xxxx, spotřebitele, xxxxxxxxx xxxx xxxxxxx xxxxxxxxx. Xx xxxxx xxxxxx xx xxxxx doplňkovou xxxxx xxxxxxxxx za xxxxxxxx, xxxxx účinná xxxxx(x)&xxxx;xxxx činidlo(a) a podmínky pro xxxxx xxxx xxxxxx, xxxx čistota xx x&xxxx;xxxxxx xxxxxxx x&xxxx;xxxxxx xxxxxxx xxxxx xxxx xxxxxx, xxxxx xx xxxxxxxxxx xxxxx. Xxx xxxxxxxx xxxxxxxx xx xxxxx xxxxx zkrácenou xxxxxx, xxxxxxx xxxxxxx xxxxxx nutné xxxxxxxx xxxxxx k prokázání xxxxxxxxxxx xxx cílový xxxx, xxxxxxxxxxxx a životní xxxxxxxxx x&xxxx;xxxxxxxxx.
Xxxxxx xxxx splňovat xxxx požadavky:
|
1. |
použije se xxxx příloha I – xx xxxxxxxx xxxxx x&xxxx;xxxxxxxxxx xxxxx; |
|
2. |
xxxxxxx xx xxxx xxxxx&xxxx;XX přílohy II; |
|
3. |
je nutno xxxxxxxxxx xxxxx, které xxxxxxxxx, xx xxxxxxxx xxxx xxxxxxxxxx xxxxxxxxxx xxxxxxxxx látky xxxx x&xxxx;xxxxxx xxxxxx xxxx x&xxxx;xxxxxxx xxxxxxxx; |
|
4. |
xxxxxxxxx xx xxxxx xxxxxxxxx xxxxxx x&xxxx;xxxxxxxxxxxxxx, x&xxxx;xx xx xxxxxxx xxxxxxxxxxx, xxxxxxxxxx xxxxxxxxxx xxxx xxxxxxxxxx xxxxxx. Xxxx-xx bioekvivalence xxxx xxxxxxxxx, xx xxxxx xxxxxxxx xxxxx xxxxxxxx xxxxx x&xxxx;XXX; |
|
5. |
xx xxxxx xxxxxxxxx xxxxx, xx za současných xxxxxxxxx xxxxxxxx xxxxxxx xxxxxxxxx xxxxx xx xxxxxxxxxxx xxxxxxxx bezpečná xxx xxxxxx druhy, xxxxxxxxxxxx, xxxxxxxxxx x&xxxx;xxxxxxx xxxxxxxxx; |
|
6. |
xx xxxxx předložit xxxxxx o výsledcích xxxxxxxxxxxx x&xxxx;xxxxxx po uvedení xxxxx xx trh, xxxx-xx xxxxxxxx xxxxxxxxx xx monitorování xxxxxxxx x&xxxx;xxxxxxxx; x |
|
7. |
xx xxxxx xxxxxxxxx xxxxxxxx xxxxx x&xxxx;xxxxxxxx xxxxxxx o změnu x&xxxx;xxxxxxx s příslušnými xxxxxx xxxxxx&xxxx;XXX, XX a V přílohy II. |
10. OBNOVENÍ XXXXXXXX
Xxxxxxx x&xxxx;xxxxxxxx povolení xxxxx xxxxxx&xxxx;14 xxxxxxxx (XX) x.&xxxx;1831/2003 splňují xxxx požadavky:
10.1 Oddíl I: Shrnutí xxxxxxxxxxx
Xxxxxxx xx xxxx xxxxx&xxxx;X&xxxx;xxxxxxx&xxxx;XX. Xxxxxxxx xx kopie xxxxxxxxx povolení Xxxxxxxxxxxx x&xxxx;xxxxxxx doplňkové xxxxx xx trh nebo xxxxxxxx xxxxxxxx xxxxxxx. Xxxxxxxx xx xxxxxxxxxxxxx xxxxxxxxxxx podle xxxxxxxxxxxx xxxxxxxxx a předloží xx xxxxxx x&xxxx;xxxxxxxx xxxxx xxxx xxxxxx původnímu xxxxxxxx xxxx xxxxxxxxxx xxxxxxxx xxxxxxxx. Žadatel xxxx xxxxxxxxx shrnutí xxxxxxxxxxx, xxxxx xxxxxxxx xxxxxx xxxxxxx, a případné xxxx xxxxxxxxx, xxxxx xx xxxxx xxxxxxxxxx xx xxxx xxxxxxx xxxxxxxxxxx xxxxxxxx/xxxxxxxx povolení x&xxxx;xxxxxxx xx identitu x&xxxx;xxxxxxxxxx.
10.2&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;XX: Xxxxxxxx, charakteristika x&xxxx;xxxxxxxx pro xxxxx xxxxxxxxx xxxxx; metody xxxxxxx
Xxxxx&xxxx;XX xxxxxxx&xxxx;XX se xxxxxxx xxxxx:
|
— |
xxx xxxxxxxxx xxxxx, které xxxx xxxxxx xx xxxxxxxx xxxxxxxx, xx použije xxxx xxxxx&xxxx;XX, |
|
— |
xxx xxxx xxxxxxxxx xxxxx xx xxxxxxx xxxx&xxxx;2.1.2, 2.1.3, 2.1.4, 2.1.4.2, 2.2, 2.3.1, 2.3.2, 2.4.1, 2.4.2, 2.4.4, 2.5, 2.6. |
Xx nutno xxxxxxxxx xxxxxx, xxxxx prokazují, xx xx doplňková xxxxx významně xxxxxxxxx, xxxxx xxx o složení, xxxxxxx xxxx aktivitu, xxxxxx povolené xxxxxxxxx xxxxx. Xx xxxxx xxxxxxx jakoukoliv xxxxx xxxxxxxxx postupu.
10.3 Oddíl III: Xxxxxx xxxxxxxx se xxxxxxxxxxx xxxxxxxxxxx xxxxx
Xxxx xxx xxxxxxxxx důkaz, že xx xxxxxxxxxx xxxxx xxxxxxxx xxxxxxx doplňková xxxxx xx schválených xxxxxxxx xxxxxxxx xxx xxxxxx xxxx, xxxxxxxxxxxx, xxxxxxxxxx x&xxxx;xxxxxxx xxxxxxxxx. Xxxx být xxxxxxxxxx xxxxxxxxxxxxx xxxxxxxxxxx o bezpečnosti xx období xx xxxxxxx xxxxxxxxx xxxxxxxx xxxx xx xxxxxxxxxx xxxxxxxx povolení, která xxxxxxxx xxxxxxxxxxx xxxxxxxxx:
|
— |
xxxxxx x&xxxx;xxxxxxxxxxx xxxxxxxx, xxxxxx xxxxxxxxxx xxxx (dosud xxxxxxx účinky, xxxxxxx xxxxxx všeho druhu, xxxxxxx výskyt xxxxxxx xxxxxx) x&xxxx;xxxxxxxx zvířat, xxxxxxxxxxxx, xxxxxxxxx a v životním xxxxxxxxx. Zpráva x&xxxx;xxxxxxxxxxx xxxxxxxx xxxx xxxxxx xxxxxx xxxxxx, xxxxx xxxxxxxxxxx xxxx/xxxxxx, xxxxxxxx, xxxxxxxx xxx xxxxx x&xxxx;xxxxxxxxx xxxxxxxx souvislosti, |
|
— |
zprávy x&xxxx;xxxxx xxxxxxxxx interakcích x&xxxx;xxxxxxxxx xxxxxxxxxxxxx, |
|
— |
xxxxx z monitorování xxxxxxx, xx-xx xx xxxxx, |
|
— |
xxxxx x&xxxx;xxxxxxxxxxxxxxxxx/xxxxxxxxxxxxxxxxx x/xxxx xxxxxxxxxxxxxxx xxxxxx, |
|
— |
xxxxxxxxx xxxxx xxxxxxxxx týkající xx xxxxxxxxxxx xxxxxxxxx látky x&xxxx;xxxxx doplňkové látky xxx zvířata, xxxxxxx x&xxxx;xxxxxxx xxxxxxxxx. |
Xxxxx nejsou xxxxxxxxxx xxxxx další xxxxxxxxx x&xxxx;xxxxxxxx z těchto xxxxxxx, musí xx xxx xxxxxx xxxxxxxxxx.
Xxxxxx x&xxxx;xxxxxxxxxx programu xxxxxxxxxxxx x&xxxx;xxxxxx po xxxxxxx xxxxx na trh xx xxxxxxxx, je-li xxxxxxxx xxxxxxxxx xx xxxxxxxxxxxx xxxxxxx x&xxxx;xxxxxxxxxx xxxxxxxx.
Xxxxx podle xxxxxxxxxx xx.&xxxx;14 odst. 2 xxxx.&xxxx;x)&xxxx;xxxxxxxx (XX) č. 1831/2003 xxxxxx x&xxxx;xxxxxxxx xxxxxxxx zahrnuje xxxxx xx změnu xxxx doplnění podmínek xxxxxxxxx povolení, xxxx xxxx xxxxxxxx xxxxxxxxxx xx xxxxxxxxx monitorování, xx xxxxx xxxxxxxxx xxxxxxxx xxxxx na xxxxxxx xxxxxx na xxxxx x&xxxx;xxxxxxx x&xxxx;xxxxxxxxxxx xxxxxx oddílů III, IV x&xxxx;X&xxxx;xxxxxxx&xxxx;XX.
11.&xxxx;&xxxx;&xxxx;XXXXXXXXXXXX XXXXXXXXX XXXXXXXXXXX XXXXX, XXXXX JIŽ XXXX XXXXXXXX XXXXX XXXXXXXX 70/524/XXX
Xxxxxxxxxxx xxxxxxx, xxxxx se xxxx xxxxx xxx&xxxx;11, jsou xxxxxxxxx xxxxx, xxxxx xxx xxxx xxxxxxxx xxxxx xxxxxxxx 70/524/EHS x&xxxx;xxxx xxx xxxxxxxxxxxx x&xxxx;xxxxxxx x&xxxx;xx.&xxxx;10 xxxx.&xxxx;2 xxxxxxxx (XX) č. 1831/2003 x&xxxx;xxxxx xxxxx xx xxxxxx xxxxxx:
|
— |
xxxxxxxxxxxx xxxxx, |
|
— |
xxxxxxxxxxx x&xxxx;xxxxxxxxxxx xxxxx, |
|
— |
xxxxxxxxxx x&xxxx;xxxxxxxxxxxxx, xxxxxxxxxxx látky x&xxxx;xxxxxxxxxx xxxxx, |
|
— |
xxxxxxx, xxxxxx pigmentů, |
|
— |
konzervanty, |
|
— |
vitamíny, xxxxxxxxxxx a chemicky xxxxxx xxxxxxxxxx látky xx xxxxxxxxxxxx xxxxxxx, |
|
— |
xxxxxxx prvky, |
|
— |
pojiva, xxxxxxxxxxxx látky x&xxxx;xxxxxxxxxx; |
|
— |
xxxxxxxxxx xxxxxxxxx x |
|
— |
xxxxxxxxxxxxx pojiva. |
Úroveň x&xxxx;xxxxxxx xxxxxxxxxxx xxxxx x&xxxx;xxxxxx xxxxxxxxxxx látek xxxx xxx xxxxxxx xxxx x&xxxx;xxxxxx doplňkových xxxxx. Xxxxx xxxxxxxx x&xxxx;xxxxxx historii xxxxxx xxxxxxxxxx xxxxxxxxx je xxxxx xxxxxx xxxxx x&xxxx;xxx xxxxxxxxxxxx xxxxxx xxxxx ustanovení xxxxxx xxxxxxxx, xxx xxxx xxxxxxxxx, xx za xxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxx xxxxxxx xxxxxxxx xxx cílové druhy, xxxxxxxxxxxx, xxxxxxxxx x&xxxx;xxxxxxx xxxxxxxxx.
11.1&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;X:&xxxx;Xxxxxxx xxxxxxxxxxx
Xxxxxxx xx xxxx oddíl I přílohy II.
11.2 Oddíl II: Xxxxxxxx, xxxxxxxxxxxxxxx x&xxxx;xxxxxxxx pro xxxxx doplňkové xxxxx; xxxxxx xxxxxxx
Xxxxx&xxxx;XX xxxxxxx&xxxx;XX xx xxxxxxx xxxxx:
|
— |
xxx xxxxxxxxx xxxxx, xxxxx xxxxxx xxxxxx xx xxxxxxxx xxxxxxxx, xx xxxxxxx xxxx&xxxx;2.1.2, 2.1.3, 2.1.4, 2.1.4.2, 2.2, 2.3.1, 2.3.2, 2.4.1, 2.4.2, 2.4.4, 2.5, 2.6, |
|
— |
xxx xxxx xxxxxxxxx xxxxx, xxxxx xxxx xxxxxx xx xxxxxxxx xxxxxxxx, xx použije xxxx xxxxx&xxxx;XX. |
11.3&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;XXX: Studie xxxxxxxx xx xxxxxxxxxxx xxxxxxxxxxx látek
Pokud byla xxxxxxxxx látka posouzena x&xxxx;xxxxxxx na xxxxxxxxxx xxx xxxxxx xxxxx, xxxxxxxxxxxx, xxxxxxxxx/xxxxxxxxxx x&xxxx;xxxxxxx xxxxxxxxx, předloží se xxxxxxx xxxxxx xxxxxxxxxxx xxxxxxxxxxxx xxx xxxxxxxxx xxxxxxxx a případné xxxx xxxxxxxxx, které xxxx xxxxxxx xx xxxx xxxxxxx xxxxxxxxxxx povolení. Xxxxx nebylo formální xxxxxxxxx xxxxxxxxxxx provedeno xxx xxxxx xxxxx xxxx xxxxxxxxx látky, xxx xxxxxx studie x&xxxx;xxxxx x&xxxx;xxxxxxx xxxxxxxxxx, xxxxxxxx xxxx xxxxxxxxxx xxxxxx, které by xx xxxxxxxxxx x&xxxx;xxxx xxxxxxx. X&xxxx;xxxxxxx xxxxxxx xx xxxxxxxx xxxxx xxxxxx studií xxxxxxxxxxx.
11.4&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;XX: Xxxxxx xxxxxxxx xx xxxxxxxxx xxxxxxxxx xxxxx
Xxxxx x&xxxx;xxxxxxxxx xx účinnost xxxxx xx.&xxxx;5 xxxx.&xxxx;3 xxxxxxxx (ES) x.&xxxx;1831/2003 xx xxxxx xxxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx xxxxxxxxx než xxxxxx, xxxxxxx týkajících xx xxxxxx historie xxxxxxxxx.
11.5&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;X:&xxxx;Xxxx xxxxxxxxxxxx v období xx xxxxxxx xxxxx xx xxx
Xxxxx xxxxx xxxxxxx&xxxx;XX xx použije podle xxxxxxxxxx xx.&xxxx;7 odst. 3 xxxx.&xxxx;x)&xxxx;xxxxxxxx (XX) x.&xxxx;1831/2003.
(1)&xxxx;&xxxx;Xxxxxxxx xxxxx je xxxxxxxx xxxxx, která není xxxxxxxxxx součástí organismu, xxxx je této xxxxx xxxxxxxx. Xxxx xxxxxxxxx xxxxxx látky, xxxxx xxxx xxxxxxxx x&xxxx;xxxxxx xxxxxxx koncentracích, xxx xx xxxxxxx.
(2)&xxxx;&xxxx;Xxx xxxxx xxxxxx xxxxxxxx xx „xxxxxxxx xxxxxxxx“ xxxxxx xxxxxx, xxx xxxx xx přirozené xxxxxxxxxxxxxx organické hmoty xxxxxx xxxxxxxxxxx x&xxxx;xxxxxxxxxxx xxxxxxxxxx xx xxxxxxx xxxxxxxxx xxxxxxxxxx x/xxxx xxxxxxx xxxxxxxxxxx xxxxx x&xxxx;xxxxxxxxxx.
(3)&xxxx;&xxxx;Xxxxxxxxxxxxx xxxxx pro xxxxxxxx definované xxxxxxxxxxx xxxxx xxxxxxxxx ve XXXXXX, xxxxxxxxxxx xxxxxxx XX xxx xxxxxxxxxxx xxxxx, databáze x&xxxx;xxxxxxxx Xxxxxx (XX) x.&xxxx;1565/2000 xx dne 18. července 2000 (Xx.&xxxx;xxxx. X&xxxx;180, 19.7.2000 x.&xxxx;8), xxxxxx xx stanoví xxxxxxxx xxxxxxxx pro přijetí xxxxxxxx xxxxxxxxx xxxxx xxxxxxxx Evropského xxxxxxxxxx x&xxxx;Xxxx (ES) x.&xxxx;2232/96 (Xx.&xxxx;xxxx. X&xxxx;180, 19.7.2000 x.&xxxx;8).
(4)&xxxx;&xxxx;X.&xxxx;Xxxx Evropy: xxxxx Xxxx Xxxxxx xxxxxxxxx xxx xxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxx k aromatizaci xx zprávě Xxxx Xxxxxx x.&xxxx;1 „Xxxxxxx xxxxxxx xx xxxxxxxxxxx“, xx.&xxxx;X,&xxxx;Xxxxxxxxx&xxxx;2000 a následujících xxxxxxxx.
(5)&xxxx;&xxxx;Xxxxx XXX (x.&xxxx;XXX) Registrační xxxxx xxxxx Xxxxxxxx Xxxxxxxxx Service, jednoznačný xxxxxxxxxxxxx xxxxxxxxxx xxxxx xxxxx xxxxxxxxx v seznamech xxxxxxxxxx xxxxx.
(6)&xxxx;&xxxx;Xxx xxxxx xxxxxx xxxxxx nařízení xx „xxxxxxxxxxxxx xxxxxxxxx xxxxxx“ rozumí xxxxx x&xxxx;xxxxxxxxxx xxxxxx xxxx xxxxxxxx příjmem (TDI xxxx TWI), ADI, xxxx s omezením, pokud xxx x&xxxx;xxxx xxxxxxxxx, xxxx xxxxxx složka, xxx xx xxxxxxxxx xx směrnici Rady 88/388/XXX xxxxxxxx xx xxxxx určených x&xxxx;xxxxxxxxxxx xxx xxxxxxx x&xxxx;xxxxxxxxxxx x&xxxx;xxxxxxxxx xxxxxxxxx xxx xxxxxx xxxxxx, xxxx xxxxxxxxx xxxxx.
(7)&xxxx;&xxxx;Xxxxxxxxx x&xxxx;xxxxxxx&xxxx;4 xxxxxx Xxxx Xxxxxx x.&xxxx;1 „Natural xxxxxxx xx xxxxxxxxxxx“, sv. I, Štrasburk, 2000.
(8)&xxxx;&xxxx;XXXXX (XXX/XXX, 1996, Xxxx additive xxxxxx 35, XXXX, WHO Xxxxxx) odpovídající xxxxxxx xxxxxxx xxx cílové xxxxx by xxxx xxx xxxxxxxx x&xxxx;xxxxxxxxxxxx x&xxxx;xxxxxxxxx zvířete x&xxxx;xxxxxx xxxxxx.
(9)&xxxx;&xxxx;Xx.&xxxx;xxxx. X&xxxx;180, 19.7.2000, x.&xxxx;8.
(10)&xxxx;&xxxx;Xxxxx pro stanovení xxxxxxxxxxx xxxxxx xxxxxxx xxx Xxxxxxxxxx x&xxxx;xxxxxxx xxxx. Xxxxxxxx agentura xxx xxxxxx xxxxxxxxx. Xxxxxxxxxx Xxxxxxxxx Evaluation Xxxx. XXXX/XXXX/153x/97-XXXXX.
XXXXXXX XX
Xxxxxxxxx x xxxxxxxx xxxxxxxx xxxxxx a údaj x xxxxxxxxx xxxx trvání xxxxxx xxxxxxxxx
1. Xxxxxxx. Xxxxxxxxx zvířat: xxxxxxx
|
Xxxxxxxxx |
Xxxxxxxx xxxxxxxxx xxxxxx |
Přibližná xxxx xxxxxx (xxxxxxxx/xxxxx) |
Xxxxxxxxx xxxx xxxxxx dlouhodobých xxxxxx xxxxxxxxx |
||
|
Xxxxxx/xxxxx |
Xxxxx |
Xxxxxxxx |
|||
|
Xxxxxx (xxxxxx) |
Xxxxx xxxxxxx xxxxxx xxxxx xx xxxxxxx |
Xx xxxxxxxx |
Až xx 21–42 xxx |
Až xx 6–11 xx |
14 xxx |
|
Xxxxxx (xxxxxxxxx) |
Mladá xxxxxxx xx xxxxxxxx období xxxx xxxxxxx x xxxxxxxxxx xxxx xxx masnou xxxxxxxx |
Xx 21–42 dní |
Xx do 120 xxx |
Xx do 35 kg |
42 xxx |
|
Selata (xxxxxx x xxxxxxxxx xxxxxx) |
Xxxxx xxxxxxx od xxxxxxxx xxxxxxx k reprodukci nebo xxx xxxxxx xxxxxxxx |
Xx xxxxxxxx |
Xx do 120 xxx |
Xx xx 35 kg |
58 xxx |
|
Xxxxx prasat |
Xxxxxxx xx odstavu určená x xxxxx xxxxxxxx xx xx dne odvozu xx xxxxx |
Od 60–120 dní |
Xx xx 120–250 dní (xxxx xxxxx místních xxxxxxxxx) |
80–150 kg (xxxx xxxxx xxxxxxxx xxxxxxxxx) |
Xx xx jateční xxxxxxxxx, xxxxxxx xxxx 70 xxx |
|
Xxxxxxxx určené x xxxxxxxxxx |
Xxxxxx xxxxxxx, které byly xxxxxxx xxxxxx inseminovány/připuštěny |
Xx xxxxx xxxxxxxxxx |
|
|
Xx xxxxxxxxxx xx konce xxxxxxx xxxxxxx vrhu (xxx xxxxx) |
|
Xxxxxxxx určené x xxxxxxxxxx xxxxx |
Xxxxxx prasete, které xxxx nejméně xxxxxx xxxxxxxxxxxx/xxxxxxxxxx |
|
|
|
Xxxxxxx xxx týdny xxxx porodem xx xxxxx doby odstavu |
2. Xxxxxxx. Xxxxxxxxx xxxxxx: xxxxxx
|
Xxxxxxxxx |
Xxxxxxxx xxxxxxxxx zvířat |
Přibližná xxxx xxxxxx (hmotnost/stáří) |
Minimální xxxx xxxxxx xxxxxxxxxxxx studií xxxxxxxxx |
||
|
Xxxxxx |
Xxxxx |
Xxxxxxxx |
|||
|
Xxxxx xxxxx |
Xxxxxx xxxxxx xxx xxxxx |
Xx xxxxxxxxx |
Až xx 35 dní |
Xx xx ~1 600 x (xx do 2 xx) |
35 dní |
|
Odchov kuřat x xxxxxx |
Xxxxxxxx xxxxxxx xxx xxxxxxxx xxxxxxxx xxxxx xxxx xxx chovné xxxxx |
Xx xxxxxxxxx |
Až xx ~16 xxxxx (xx do 20 týdnů) |
— |
112 dní (xxxxxx-xx xxxxx x xxxxxxxxx x xxxxxxxxx pro xxxxx xxxxx) |
|
Xxxxxxx |
Xxxxxxx xx xxxxxx xxxxxxx xxx xxxxxxxx xxxxx |
Xx 16–21 xxxxx |
Xx xx ~13 xxxxx (xx xx 18 xxxxxx) |
Xx 1 200 x (xxxx), 1 400 x (xxxxx) |
168 xxx |
|
Xxxxx xxxx |
Krůty x xxxxxxx xxxxxxx xx xxxxx |
Xx xxxxxxxxx |
Xx do ~14 xxxxx (xx xx 20 xxxxx) Xx xx ~16 týdnů (až xx 24 xxxxx) |
Xxxxxx: xx xx ~7 000 x (až xx 10 000 x) Samci: xx xx ~12 000 x (xx xx 20 000 x) |
84 dní |
|
Xxxxx xxx xxxxx xxxxxxxxxx |
Xxxxx a krocani xxxxxxx pro xxxxx xxxxxxxxxx |
Xxxx období |
Xx 30 týdnů xx xx ~ 60 xxxxx |
Samice: xx ~15 000 x Xxxxx: od ~30 000 x |
Xxxxxxx xxxx měsíců |
|
Odchov krůt |
Xxxxx xxxxx a krocani xxxxxx x xxxxxxx účelům |
Od xxxxxxxxx |
Až xx 30 xxxxx |
Xxxxxx: xx xx ~15 000 x Xxxxx: až do ~30 000 g |
Celé xxxxxx (nejsou-li xxxxx x xxxxxxxxx x xxxxxxxxx pro xxxxx xxxx) |
3. Tabulka. Xxxxxxxxx xxxxxx: skot (domácí xxxx, xxxxxx xxxxx xxxxxxx a bizon)
|
Xxxxxxxxx |
Xxxxxxxx kategorie xxxxxx |
Xxxxxxxxx xxxx trvání (xxxxxxxx/xxxxx) |
Xxxxxxxxx doba trvání xxxxxxxxxxxx studií xxxxxxxxx |
||
|
Xxxxxx |
Xxxxx |
Xxxxxxxx |
|||
|
Odchov xxxxx |
Xxxxxx xxxxxxx xxx xxxxxxxxxx xxxx xxxxxxxx xxxxxxxx xxxx |
Od narození |
Xx xx 4 xxxxxx |
Xx xx 60–80 xx (až do 145 xx) |
56 xxx |
|
Xxxxx telat |
Xxxxxx xxx xxxxxxxx xxxxxxxx masa |
Xx xxxxxxxx |
Xx do 6 xxxxxx |
Xx xx 180 kg (xx xx 250 xx) |
Xx porážky, xxxxxxx xxxx 84 xxx |
|
Xxxxx skotu |
Xxxx xx xxxxxxx xxxxxx x xxxxx produkci xx xxx odvozu xx xxxxx |
Xx úplného xxxxxxx xxxxxxxxxxxx |
Xx xx 10–36 xxxxxx |
Až xx 350–700 kg |
168 xxx |
|
Xxxxxxx xxx xxxxxxxx xxxxx |
Xxxxxx skotu, xxxxx porodily xxxxxxx xxxxx xxxx |
|
|
|
84 xxx (xx xxxxx uvést xxxx xxxxxx xxxxxxx) |
|
Krávy k reprodukci |
Samice xxxxx, které xxxx xxxxxxx xxxxxx xxxxxxxxxxxx/xxxxxxxxxx |
Od xxxxx xxxxxxxxxx xx xxxxx xxxxxxx xxxxxxx |
|
|
Dva xxxxx (xxxxx se xxxxxxxx xxxxxxxxxxx xxxxxxxxx) |
4. Xxxxxxx. Xxxxxxxxx zvířat: xxxx
|
Kategorie |
Xxxxxxxx xxxxxxxxx xxxxxx |
Přibližná xxxx xxxxxx (hmotnost/stáří) |
Xxxxxxxxx doba xxxxxx xxxxxxxxxxxx xxxxxx xxxxxxxxx |
||
|
Xxxxxx |
Xxxxx |
Xxxxxxxx |
|||
|
Xxxxxx jehňat |
Xxxxxxx xxxxxxx xxx xxxxxxx xxxxxxxxxx |
Od xxxxxxxx |
Xx do 3 xxxxxx |
15–20 xx |
56 xxx |
|
Xxxxx xxxxxx |
Xxxxxxx xxxxxxx xxx xxxxxxxx xxxxxxxxx xxxx |
Od xxxxxxxx |
Xx xx 6 xxxxxx (xxxx xxxxxx) |
Xx do 55 xx |
Xx xxxxxxx xxxxxxxxx, xxxxxxx však 56 xxx |
|
Xxxx xxxxxx k produkci mléka |
Xxxx, xxxxx xxxxxxxx nejméně xxxxx jehně |
|
|
|
84 xxx (je xxxxx uvést celé xxxxxx xxxxxxx) |
|
Xxxxxxx x xxxxxxxxxx |
Xxxxxx xxxx, které xxxx xxxxxxx xxxxxx xxxxxxxxxxxx/xxxxxxxxxx |
Xx xxxxx xxxxxxxxxx xx xxxxx druhého odstavu |
|
|
Xxx xxxxx (xxxxx se xxxxxxxx xxxxxxxxxxx parametry) |
5. Xxxxxxx. Xxxxxxxxx zvířat: kozy
|
Xxxxxxxxx |
Definice xxxxxxxxx xxxxxx |
Xxxxxxxxx xxxx xxxxxx (hmotnost/stáří) |
Minimální xxxx xxxxxx xxxxxxxxxxxx xxxxxx xxxxxxxxx |
||
|
Xxxxxx |
Xxxxx |
Xxxxxxxx |
|||
|
Xxxxxx kůzlat |
Xxxxx xxxx xxxxxxx xxx xxxxxxx xxxxxxxxxx |
Xx narození |
Xx do 3 xxxxxx |
15–20 xx |
Xxxxxxx 56 xxx |
|
Výkrm xxxxxx |
Mladé xxxx chované xxx xxxxxxxx xxxxxx masa |
Xx xxxxxxxx |
Xx xx 6 xxxxxx |
|
Xxxxxxx 56 xxx |
|
Xxxx xxxxxx x xxxxxxxx xxxxx |
Xxxx xxxxxxx s jedním xxxxxxxx |
|
|
|
84 xxx (je xxxxx xxxxx xxxx období xxxxxxx) |
|
Xxxx x xxxxxxxxxx |
Samice xxxx, xxxxx xxxx xxxxxxx xxxxxx xxxxxxxxxxxx/xxxxxxxxxx |
Od první xxxxxxxxxx xx xxxxx xxxxxxx xxxxxxx |
|
|
Xxx xxxxx (xxxxx xx požadují xxxxxxxxxxx xxxxxxxxx) |
6. Tabulka. Xxxxxxxxx xxxxxx: xxxx
|
Xxxxxxxxx |
Xxxxxxxx xxxxxxxxx xxxxxx |
Xxxxxxxxx doba xxxxxx (xxxxxxxx/xxxxx) |
Xxxxxxxxx xxxx xxxxxx xxxxxxxxxxxx xxxxxx xxxxxxxxx |
||
|
Období |
Stáří |
Xxxxxxxx |
|||
|
Losos x xxxxxx |
|
|
|
200–300 x |
90 xxx nebo xx xxxx, xxx se xxxxxxx tělesná xxxxxxxx xxxxxxxxxxx |
|
Xxxxx x xxxxxx |
Xxxxx xxxxxxxxx xxx |
Xxxxx xxxxx xx xxxxxxxx xxxx tření |
|
|
90 xxx |
7. Tabulka. Xxxxxxxxx xxxxxx: xxxxxxx
|
Xxxxxxxxx |
Definice xxxxxxxxx xxxxxx |
Přibližná xxxx xxxxxx (xxxxxxxx/xxxxx) |
Xxxxxxxxx doba xxxxxx xxxxxxxxxxxx xxxxxx xxxxxxxxx |
||
|
Xxxxxx |
Xxxxx |
Xxxxxxxx |
|||
|
Xxxxxx x xxxxxxxxx xxxxxxx |
|
Počínaje xx jednoho xxxxx xx xxxxxxxx |
|
|
56 dní |
|
Výkrm králíků |
Xxxxxxx xxxxxxx xxx xxxxxx xxxxxxxx |
Xx odstavu |
Xx do 8–11 xxxxx |
|
42 xxx |
|
Xxxxxx xxxxxxx (xxx xxxxxxxxxx) |
Xxxxxxx, které xxxx xxxxxxx xxxxxx xxxxxxxxxxxx/xxxxxxxxxx |
Xx xxxxxxxxxx xx konce xxxxxxx xxxxxxx |
|
|
Xxx xxxxx (xxxxx xx xxxxxxxx xxxxxxxxxxx xxxxxxxxx) |
|
Xxxxxx xxxxxxx xxxxxx x xxxxxxxx xxxxxxx xxxxxxx |
Xxxxxxx, xxxxx xxxx xxxxxxx xxxxxx xxxxxxxxxxxx |
Xx xxxxx inseminace |
|
|
Nejméně 2 xxxxx xxxx porodem xx xxxxx doby xxxxxxx (např. xxx xxxxxxx mikroorganismů) |
8. Xxxxxxx. Xxxxxxxxx xxxxxx: xxxx
|
Xxxxxxxxx |
Xxxxxxxx xxxxxxxxx xxxxxx |
Přibližná xxxx xxxxxx (hmotnost/stáří) |
Xxxxxxxxx doba xxxxxx xxxxxxxxxxxx xxxxxx xxxxxxxxx |
||
|
Xxxxxx |
Xxxxx |
Xxxxxxxx |
|||
|
Xxxx |
Xxxxxxx xxxxxxxxx |
|
|
|
56 xxx |


