XXXXXXXX XXXXXX (ES) x. 2074/2005
xx xxx 5. xxxxxxxx 2005,
xxxxxx xx xxxxxxx xxxxxxxxx xxxxxxxx xxx některé xxxxxxx podle xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Xxxx (ES) x. 853/2004 x xxx xxxxxxxxxx xxxxxxxx kontrol xxxxx nařízení Xxxxxxxxxx xxxxxxxxxx a Rady (XX) x. 854/2004 x (XX) x. 882/2004, xxxxxx xx xxxxxxx xxxxxxxx xx xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Rady (XX) x. 852/2004 x xxxxxx se xxxx xxxxxxxx (XX) x. 853/2004 a (XX) x. 854/2004
(Xxxx x xxxxxxxx xxx XXX)
XXXXXX XXXXXXXXXX SPOLEČENSTVÍ,
x xxxxxxx xx Xxxxxxx x xxxxxxxx Xxxxxxxxxx xxxxxxxxxxxx,
x xxxxxxx xx xxxxxxxx Xxxxxxxxxx xxxxxxxxxx a Xxxx (XX) x. 852/2004 xx xxx 29. dubna 2004 x hygieně xxxxxxxx (1), x zejména xx xx. 13 xxxx. 2 xxxxxxxxx xxxxxxxx,
x xxxxxxx xx xxxxxxxx Xxxxxxxxxx parlamentu x Xxxx (ES) x. 853/2004 xx xxx 29. dubna 2004, kterým se xxxxxxx xxxxxxxx xxxxxxxxxx xxxxxxxx xxx xxxxxxxxx xxxxxxxxxxx původu (2), x xxxxxxx xx xxxxxx 9, 10 x 11 uvedeného xxxxxxxx,
x xxxxxxx xx xxxxxxxx Evropského parlamentu x Xxxx (XX) x. 854/2004 ze xxx 29. xxxxx 2004, xxxxxx xx xxxxxxx zvláštní xxxxxxxx xxx organizaci úředních xxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx xxxxxxxx k xxxxxx xxxxxxxx (3), x xxxxxxx xx xxxxxx 16, 17 x 18 xxxxxxxxx xxxxxxxx,
x ohledem xx xxxxxxxx Evropského xxxxxxxxxx x Xxxx (ES) x. 882/2004 xx xxx 29. xxxxx 2004 x úředních xxxxxxxxxx xx xxxxxx xxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxxx xx xxxxx x xxxxxxxx x pravidel o xxxxxx xxxxxx x xxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxx (4), a xxxxxxx na článek 63 xxxxxxxxx xxxxxxxx,
xxxxxxxx x xxxxx důvodům:
|
(1) |
Xxxxxxxx (XX) x. 853/2004 xxxxxxx xxxxxxxx xxxxxxxxxx xxxxxxxx xxx xxxxxxxxx xxxxxxxxxxx původu. Je xxxxx xxxxxxxx určitá xxxxxxxxx xxxxxxxx xxx xxxx, xxxx xxxx, xxxxxxxx rybolovu, xxxxx, xxxxx, xxxx xxxxxxxx x xxxxxxxx a x xxxx zpracované xxxxxxx. |
|
(2) |
Xxxxxxxx (ES) x. 854/2004 xxxxxxx xxxxxxxx xxxxxxxx xxx xxxxxxxxxx xxxxxxxx xxxxxxx produktů xxxxxxxxxxx xxxxxx xxxxxxxx x xxxxxx xxxxxxxx. Xx xxxxx xxxxxxxx xxxxxx pravidla x xxxxxxxx xxxxx xxxxxxxxx. |
|
(3) |
Xxxxxxxx (XX) č. 882/2004 xxxxxxx xx xxxxxx Xxxxxxxxxxxx xxxxxxxxxxxxx xxxxx xxxxxxxx xxxxxxxx xxx xxxxxxxxxx xxxxxxxx kontrol. Xx xxxxx xxxxxxxx xxxxxx pravidla x xxxxxxxx xxxxx požadavky. |
|
(4) |
Xxxxxxxxxxx Xxxxxx 20XX/.../XX (5) xx xxxx xxxxxxx xxxxxxxxxx, kterými xx xxxxxxxxx opatření směrnic xxxxxxxxx xxxxxxxx Evropského xxxxxxxxxx a Rady 2004/41/XX xx dne 21. xxxxx 2004, xxxxxx xx zrušují xxxxxxx xxxxxxxx xxxxxxxx xx xxxxxxx xxxxxxxx x xxxxxxxxxxxx podmínek xxx produkci některých xxxxxxxx xxxxxxxxxxx xxxxxx xxxxxxxx k lidské xxxxxxxx x pro xxxxxx xxxxxxx xx xxx x xxxxxx xx xxxx směrnice Xxxx 89/662/EHS x 92/118/XXX x xxxxxxxxxx Xxxx 95/408/XX (6). Xxxxxxx části xxxxxxxxxxx xxxxxxxxxx xx tedy xxxx zůstat zachovány x tomto xxxxxxxx. |
|
(5) |
Xxxxxxxx (XX) x. 852/2004 xxxxxxxx xx xxxxxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxx, aby xxxxx x xxxxxxxxxx xxxxxxx x xx xxxxxx xxxxxxxxxxxx xxxxxxxxx xxxxxxxxx z těchto xxxxxxx příslušnému xxxxxx x xxxxxxxxxxxxx potravinářského xxxxxxx, xxxxx je xxxxxx xxxxxxxxxxx. |
|
(6) |
Xxxxxxxx (XX) x. 853/2004 xxxxxx xx provozovatelů xxxxx xxxxxxxx, aby xxxxxxxxxx, xxxxxxxx a xxxxxxxxxxxxx xxxxxxxxx x xxxxxxxxxxxx xxxxxxx xxx xxxxxxx xxxxxxx kromě xxxxxxx, xxxxx xxxx odeslána xxxx xxxx být xxxxxxxx xx xxxxx, x xxx podle xxxxxx xxxxxxxxx jednali. Xxxxx xxxx xx xxxx zajistit, xxx xxxxxxxxx x potravinovém xxxxxxx xxxxxxxxxx veškeré xxxxxxxxxxx xxxxxxxxxx podle xxxxxxxx (XX) č. 853/2004. |
|
(7) |
Xxxxxxxxx x xxxxxxxxxxxx xxxxxxx pomáhají xxxxxxxxxxxxx xxxxx xxx organizování xxxxxxxx x xxxxxxxx xxxxxxxxxxxxx xxxxxx umožňují xxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxx. Xxxxxxxxx x xxxxxxxxxxxx řetězci xx xxx analyzovat úřední xxxxxxxxxxx lékař a xxxx by xx xxxxxxxx jako nedílná xxxxxxx xxxxxxxxxxx xxxxxxx. |
|
(8) |
Je xxxxx xx xxxxxxx xxxxxxxx stávající xxxxxxx xxxx xxxxxxxxx a xxxxxxxxxxx xx požadavkům xx xxxxxxxxx o xxxxxxxxxxxx xxxxxxx xxxxx xxxxxxxx (XX) x. 854/2004. |
|
(9) |
Xx snaze xxxxxxx xxxxxx xxxxxx x xxxxxxxxxxxx xxxxx xxxxxxxx (XX) x. 854/2004 xx xxx xxxxxx xxxxxxxxxxx xxxxx zaznamenat x x xxxxxxx xxxxxxx sdělit xxxxxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxx, ze xxxxxxx xxxxxxx xxxxxxxxx, x xxxxxxxxxx xxxxxxxxxxxxx xxxxxx xxxxxxxxxx x xxxxxxxxxxxx, xx xxxxxxx xxxxxxx xxxxxxxxx, xxxx xxxxxxxxxx xxxxxxxxx příslušnému xxxxxx jakoukoli xxxxxxx xxxx xxxx xxxxxxxx xx xxxxxxx x xxxxxxx xx xxxxxxxxxx xxxxxxx nebo xx xxxxx/xxxxx, xxxxx xxxxx xxx xxxx na xxxxxxx xxxxxx xxxx xxxxxx xxxxxx xxxx xxxxxxx dobré xxxxxxx xxxxxxxx zvířat. |
|
(10) |
Xxxxxxxx (XX) x. 853/2004 x (XX) x. 854/2004 xxxxxxx požadavky pro xxxxxxxx xxxxxxxx xxx xxxxxxxxxx x xxxxxxxx xxxxxxxx xx xxxxxxx x xx xxxxxx xxxxxxxx. X souladu x xxxxxxxx xxxxx xxxxxxx XXX xxxxxx XXXX kapitoly X xxxxx D xxxxxxxx (XX) x. 853/2004 xxxx xxxxxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxx xxxxxxxx, aby x produktů xxxxxxxx xxxxxxxx xx všech xxxxxx produkce vlastní xxxxxxxx s cílem xxxxxxx xxxx, xxx xxxx ryby viditelně xxxxxxxx xxxxxxxx používány x lidské spotřebě. Xxxxxxx xxxxxxxxxx pravidel xxxxxxxxxx xx vizuální xxxxxxxx s sebou xxxx xxxxxxx xxxxxxxxx xxxxx viditelných xxxxxxxx x xxxxxxxx xxxxxxxx x stanovit xxxx x frekvenci xxxxxxxxxx. |
|
(11) |
Xxxxxxxx xxxxxxxxx x xxxxxxxx (XX) č. 853/2004, xxxxxxx účelem xx xxxxxxxx xxxxxxx xx xxx xxxxxxxx xxxxxxxx xxxxxxxxxx x xxxxxx xxxxxxxx, xxxxx xxxxxxxxx x určitá xxxxxxxx xxxxxxxxx xxxxxx xxxxxxx xxxxxx celkové těkavé xxxxxxxx xxxx (XXXX). X xxxxxxx některých xxxxx xx třeba xxxxxxxx xxxxxx XXXX, xxxxx xxxxx být xxxxxxxxxx, x xxxxx xxxxxxxxxxx xxxxxxxxxxxx xxxxx xxxxxxx. Xxxx xx xx pokračovat x xxxxxx xxxxxxxxx xxxxx xxxxxxx, které xxxx xxxxxxx xxxxxx jako xxxxxx xxx xxxxxxxx XXXX, nicméně pro xxxxxx pochybností xxxxxxx xxxxxxxx nebo v xxxxxxx xxxxx xx xxxx xxx xxxxxx xxxxxxxxxx referenční metoda. |
|
(12) |
Xxxxx xxxxxxx xxxxxxxxxxxxx xxxxxx (XXX = Paralytic Xxxxxxxxx Xxxxxx), toxinu „Xxxxxxx Shellfish Xxxxxx“ XXX a lipofilních xxxxxx xxxx xxxxxxxxx x xxxxxxxx (XX) x. 853/2004. Referenční xxxxxxx pro zjišťování xxxxxxxx toxinů x xxxxxxxx xxxxx toxických xxxxxxx xxxxxx x xxxxxxx se schránkami xxxx biologická vyšetření. Xx účelem xxxxxxx xxxxxxxx xxxxxx xx xxxx xxx xxxxxxxxxxxxx xxxxxxxxx xxxxxx x xxxxxx analýzy a xxxxxxx xxxxx xx xx xxxx xxxxxxxxxx. Xxxxx xxxxxxxxxxxx vyšetřovacích xxxxx by měly xxx xxxxxxxx i xxxxxxxxxxxx xxxxxx zjišťování, xxxx. chemické metody x xxxxxxx in xxxxx, xxxxxxx-xx xx, xx xxxxxxx metody xxxx xxxxxxxxxxxx xxxxxx xxxxxx xxxx xxxxxx xxxxxxxxxx x že xxxxxx xxxxxxxxx zajišťuje xxxxxxxxxxxx úroveň xxxxxxx xxxxxxxxx zdraví. Xxxxxxxxxx xxxxxxxxx úrovně xxxxxxxxxxx xxxxxx vycházejí z xxxxxxxxxxx xxxxx a xxxx by xxx xxxxx posouzeny, xxxxxxx xxxxx dostupná nová xxxxxxx xxxxx. Xxxxxxxxxx xxxxxxxxxxxx materiálu x xxxxxxx xxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxx x xxxxxxxx xxxx xxxxxxx, že xxxxxx xxxxxxx veřejného xxxxxx xxxxxxxxxxx s xxxxxxx xx všechny xxxxxx toxiny neodpovídá xxxxxx, kterou xxxxxxxx xxxxxxxxxx xxxxxxxxx. Xx xxxxx xxxxxxxx xxxxxx xxxxxxxx xxx xxxxxxxxx xxxxxxxxxxxx xxxxxxxxx. |
|
(13) |
Mechanicky oddělované xxxx (MOM) xxxxxxx xxxxxx technik, xxxxx xxxxxx xxxxxxxxx xxxxx xxxxxxxxx při výrobě XXX, by xxxx xxx xxxxxxxxxx za xxxxxxx xx MOM xxxxxxxxx xxxxxx technik, xxxxx xxxxxxxxx kostí xxxx. |
|
(14) |
XXX prvně xxxxxxxxxxx xxxxx, xxxxx xxxx xxxxxxx za xxxxxx xxxxxxxxxxx xxxxxxxx a xx xxxxxx stanovené xxxxxxx, xx xxxx xxx přípustné v xxxxxxx xxxxxxxxxxxx, xxx xxxxxx xxxxxx xx xxxxxxxx xxx předchozího xxxxxxxxx xxxxxxxx. Podmínky xx xxxxxx xxxxxxx xxxxxx vápníku v XXX, xxxxx xx xxx xxx xxxxxxxx x xxxxxxx s xx. 11 odst. 2 xxxxxxxx (ES) x. 853/2004. Xxxxxxxxx xxxxxxxxx obsah vápníku xxxxxxxxx x xxxxx xxxxxxxx xx xxx xxx přizpůsoben, xxxxxxx xxxxx xxxxxxxx xxxxxxxx xxxxx x xxxxxxxxxx x závislosti xx xxxxxxx různých xxxxxxx. |
|
(15) |
Xxxxx xx. 31 odst. 2 písm. x) xxxxxxxx (XX) x. 882/2004 vedou členské xxxxx aktualizované xxxxxxx xxxxxxxxxxx xxxxxxxx. Xx xxxxx xxxxxxxx společný xxxxx pro xxxxxxxxxxxxxx xxxxxxxxxxx xxxxxxxxx ostatním xxxxxxxx xxxxxx x xxxxxxxxxx. |
|
(16) |
Xxxxxxx XXX oddíl XX nařízení (XX) x. 853/2001 xxxxxxx xxxxxxxxx xx přípravu xxxxxx xxxxxxxx a xxxxxxxx xxxxxxxx x xxxxxx xxxxxxxx. Xxxxxxxx xxxxxxxxx xxxxxx xxxxx xxxxxxxxxxxxx xxxxxxxxx xx xxxxx xxxxxx xxxxxxxx xxx xxxx xxxxxxxx x hlemýždě xxxxxx x xxxxxx spotřebě x xxxxxxxx xx xxxxxxx xxxx. |
|
(17) |
Xxxxxxx XXX xxxxxx XXX a XX xxxxxxxx (ES) x. 853/2001 xxxxxxx xxxxxxxxx xx xxxxxx xxxxxxxx x xxxxxxxx xxxxxxxx x xxxxxx xxxxxxxx x xxxxxx xxxxxxx xx trh. Xxxxxxxx xxxxxxxxx xxxxxx xxxxx veterinárních xxxxxxxxx xx třeba xxxxxx xxxxxxxx xxx xxxxxxxx x xxxxxxx určené x xxxxxx xxxxxxxx x xxxxxxxx ze xxxxxxx zemí x xxx xxxxxxxx k xxxxxx želatiny x xxxxxxxx určené x xxxxxx xxxxxxxx x xxxxxxxx ze třetích xxxx. |
|
(18) |
Xx třeba určité xxxxxxxxx, xxx xxxxx xxxxxxxxxx výroba potravin x tradičními xxxxxxxxxxx. Xxxxxxx státy xxx xxxxxxx xxxxxxx xxxxxxx xxxxxxxx těchto xxxxxxxx x xxxxx xxxxxxxx xxxxxxxx platných xxxx 1. xxxxxx 2006. Xxxxxxxxxxxxx potravinářských xxxxxxx xx měli xxx xxxxxxx nadále xxx xxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxx i po xxxxxxxx datu. Xxxxxx xxxxxxxxxx xxxxxxxx xxxxxx xxxxxxxxxx xxxxxx xxxxxxx xx xxxxxxxx x xxxxxxxxxx (XX) x. 852/2004, (XX) x. 853/2004 a (XX) x. 854/2004. Ve xxxxxxx xxxxxxx, xxx xxx byly uděleny xxxxxxx, xx pouze xxxxx x xxxxxxxxxxx xxxxxxxx praxe, a xxx xxxx xxx xxxxxxxxx xxxxxxx oznamovacího xxxxxxx včetně xxxxx xxxxxxx xxxxx pro xxxxxxx xxxxx zbytečné x nepřiměřeně obtížné. Xxxxxxxx xx strukturálních xxxxxxxxx xxxxx xxxxxxxx (XX) x. 852/2004 x x ohledem xx xxxx xxxxxx xxxxxx xx xxxxx xxxxxxx xxxxxxxxx x xxxxxxxxxx xxxxxxxxxxx x xxxxxx podmínky, které xx xxx xx xxxxx. |
|
(19) |
Xxxxxxxx x tomu, xx nařízení (XX) x. 853/2004 a (XX) x. 854/2004 xxxx xxxxxxx xxxx xxxxxxxxxxxx xxx 1. xxxxxx 2004, xxxxxxxxxx xx xxxx členské xxxxx. Xx xxxxxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxx xx proto xxxx xxx xxxxxxxx xxxx XXX xxxxxx členských xxxxx x xxxxxxx Xxxxxxxxxx xxxxxxxxxxxx x xxxxxx xxxxxxxx. |
|
(20) |
Xxxxxxx XXX xxxxx X nařízení (XX) x. 853/2004 xxxxxxx pravidla pro xxxxxx xxxx xxxxxxxx xxxxxxxxx x xxxx xxxxxxx na xxx. Xxxxxxxx XX xxx 8 uvedeného xxxxxx xxxxxxx xxxxxxx x xxxxxxxx úplného stažení x kůže xxxxxxx xxxxxxxxxx těl nebo xxxxxx xxxxx těla xxxxxxxx x xxxxxx xxxxxxxx. Xx xxxxx xxxxxxxx tyto xxxxxxx xx xxxxxxxxx xxxxxxxxx xxxxx, pokud xxxxxxx xxxxxx xxxxxxxx, xxxxx xx xxxxxxxx xx xxxxxxxxx xxxxx. |
|
(21) |
Xxxxxxx xxxxxxxx xxxxx xxx pro xxxxxxxxxxxx xxxxxxxxxx, pokud xxx x složení xxxxxxxxx xxxxxxx. Zejména xxx xx zabránilo xxxxxxxx xxxxxxxxxxxx xxxxxxxxx, xx třeba zakázat xxxxxx čerstvého xxxxxxxxx xxxx xxxxxxxxxx xxxxxxxxxx xxxxxxxxxxxx xxxx. |
|
(22) |
Stanovisko Evropského xxxxx xxx xxxxxxxxxx xxxxxxxx xx xxx 30. xxxxx 2004 xxxxxxxxx, xx xxxxxxxx xxxxxxxx x čeledi Xxxxxxxxxx, zejména Xxxxxxxx xxxxxxxxx x Xxxxxxxxxxxx xxxxxxxxxxxxx xxxxx mít xxxxxxxxxx gastrointestinální xxxxxx, xxxx-xx xxxxxxxxxxx xx xxxxxxxx podmínek. Xx xxxxxxxx xxxxxxxx z xxxxxxx čeledi xx xx proto xxxx xxxxxxxxx xxxxxxxx xxxxxxx xx xxx. |
|
(23) |
Xxxxxxx XXX xxxxx XX nařízení (XX) x. 853/2004 xxxxxxx xxxxxxxx hygienická xxxxxxxx xxx xxxxxx xxxxx x xxxxxx xxxxxxx. Podle kapitoly X xxxxxxxxxxx XX xxxxx X bodu 1 písm. e) xxxxx xxx koupele xxxxxx x xxxx xxxxxxxxxx xx xxxxxxx xxxxxx xxxxxxx, pouze xxxxx to xxxxxxxx xxxxxxxxx xxxxx. X xxxx xxxxxxxxxxx xxxx xxxxx xxxxxxxx žádný xxxxxxxx xxxxxxxxxx xxxxx. Xxx se proto xxxxxxxx xxxxxxxxxxxxx xxxxxxx xxxxxxxxx xxxxx, je xxxxx upřesnit xxxxxxx xxx vydávání xxxxxx xxxxxxxx. |
|
(24) |
Xxxxxxxx (XX) x. 853/2004 xxxxxxxx xx xxxxxxxxxxxxx potravinářských xxxxxxx, xxx xxxxxxxxx, že xxxxxxx xxxxxxxxx ošetření xxxxxxxx xxxxx a xxxxxxxx xxxxxxx xxxxx x xxxxxxx x xxxxxxxxxxx xxxxxxxxx normou. X ohledem na xxxxxxxxxxx xxxxxxxxx xxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxxxx x xxxxx xxxxxxx x xxxxxx vlivu xx xxxxxxxxxx potravin x zdraví xxxxxx xx však xxxxx xxx xxxxxxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxx x xxxxx xxxxxx jasnější pokyny. |
|
(25) |
Xxxxxxxx (XX) x. 853/2004 xxxxxx xxxxx xxxxxxxx, xxx níž xxxxxxx xxxxxxx xxxxxxx x xxxxx, xxxxx xx xxxxxxxxxx skořápky xxxxxx xxxxxxxxxx. Je proto xxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxx pravidla platná xxx xxxx výrobky x pozměnit xxxxxxx XXX xxxxx X xxxxxxxx II xxxxxxxx (XX) č. 853/2004. |
|
(26) |
Xxxxxxx XXX xxxxx XXX xxxxxxxx (ES) x. 853/2004 stanoví xxxxxxxx xxxxxxxxxx pravidla pro xxxxxxxx. Xxxx xxxxxxxx xxxxxxxx xxxxxxxxx na xxxxxxxxx xxxxx xxxxxxx x výrobě xxxxxxxx x xx přepravu x skladování těchto xxxxxxx. Obsahují xxxxxx xxxxxxxxxxx xxxxxx xxx xxxxxx xxxxxxxx. Je xxx xxxxx xxxxxxxx xxxx pravidla označování xxxxxxxx. |
|
(27) |
Xxxxxxx xxxxxx xxxxxxx x xxxxxxxx normy XXX 16649-3 xxxxxxx xxxxxxxx xxxxxxxxxx xxxxxx xxxxxxx E. xxxx x xxxx. Xxxx xxxxxxxxxx xxxxxx xx xxx v souladu x xxxxxxxxx (ES) x. .../2005 o xxxxxxxxxxxxxxxxx kritériích xxx xxxxxxxxx (7) xxxxxxx x xxxxxx xxxx x oblastí X. Xxxxx xx xxxxx XXX 16649-3 měla xxx také xxxxxxxxx xxxx xxxxxxxxxx MPN xxxxxx xxxxxxx X. xxxx x mlžů xxxxxxxxxxxxx x oblastí X x C. Xxxxxxxxx xxxxxxxxxxxxxx xxxxx xx mělo xxx xxxxxxxxx pouze xxx, xxx xxxx považovány xx xxxxxxxxxx x xxxxxxxxxx metodou. |
|
(28) |
Xxxxxxxx (XX) x. 853/2004 x (XX) x. 854/2004 xx xxxxx xxxx xxx xxxxxxxxxxxxx xxxxxxxx xxxxxxx. |
|
(29) |
Xxxxxxxx xxxxxxxxx xxxxx xxxxxxxxx xxxx x xxxxxxx se stanoviskem Xxxxxxx výboru xxx xxxxxxxxxxx řetězec x xxxxxx xxxxxx, |
PŘIJALA XXXX XXXXXXXX:
Xxxxxx 1
Xxxxxxxxx xx xxxxxxxxx x xxxxxxxxxxxx xxxxxxx pro účely xxxxxxxx (XX) x. 853/2004 x (XX) x. 854/2004
Xxxxxxxxx xx xxxxxxxxx x xxxxxxxxxxxx xxxxxxx xxxxxxx x xxxxxxx XX oddílu XXX xxxxxxxx (XX) x. 853/2004 x xxxxxxx I xxxxxx X kapitole XX xxxxx X xxxxxxxx (XX) x. 854/2004 xxxx xxxxxxxxx x xxxxxxx I xxxxxx xxxxxxxx.
Xxxxxx 2
Xxxxxxxxx xx xxxxxxxx xxxxxxxx pro xxxxx xxxxxxxx (XX) x. 853/2004 x (XX) x. 854/2004
Xxxxxxxxx xx xxxxxxxx rybolovu xxxxxxx v xx. 11 xxxx. 9 xxxxxxxx (ES) č. 853/2004 x xx. 18 odst. 14 x 15 xxxxxxxx (XX) x. 854/2004 xxxx stanoveny v xxxxxxx II xxxxxx xxxxxxxx.
Xxxxxx 3
Uznané zkušební xxxxxx pro mořské xxxxxxxxx xxx účely xxxxxxxx (ES) x. 853/2004 a 854/2004
Xxxxxx xxxxxxxx xxxxxx xxx xxxxxx biotoxiny xxxxxxx x xx. 11 xxxx. 4 xxxxxxxx (XX) č. 853/2004 x xx. 18 xxxx. 13 xxxx. x) xxxxxxxx (XX) x. 854/2004 jsou xxxxxxxxx v xxxxxxx XXX xxxxxx xxxxxxxx.
Xxxxxx 4
Xxxxx vápníku x xxxxxxxxxx oddělovaného xxxx xxx xxxxx xxxxxxxx (ES) x. 853/2004
Xxxxx xxxxxxx x xxxxxxxxxx xxxxxxxxxxxx xxxx xx xxxxxx xx. 11 odst. 4 xxxxxxxx (ES) č. 853/2004 xx xxxxxxxx x xxxxxxx XX xxxxxx xxxxxxxx.
Xxxxxx 5
Seznamy xxxxxxxx xxx xxxxx xxxxxxxx (XX) x. 882/2004
Xxxxxxxxx xx xxxxxxx zařízení xxxxxxx x čl. 31 xxxx. 2 xxxx. f) xxxxxxxx (XX) č. 882/2004 xxxx stanoveny v xxxxxxx X tohoto xxxxxxxx.
Xxxxxx 6
Xxxxx veterinárních xxxxxxxxx xxx xxxx xxxxxxxx, xxxxxxxx, xxxxxxxx x kolagen xxx xxxxx xxxxxxxx (ES) x. 853/2004
Xxxxx xxxxxxxxxxxxx xxxxxxxxx xxx xxxx xxxxxxxx, hlemýždě, želatinu x kolagen xxxxxxx x xx. 6 xxxx. 1 xxxx. x) nařízení (ES) x. 853/2004 x xxx xxxxxxxx xx xxxxxx xxxxxxxx x xxxxxxxx jsou xxxxxxxxx x xxxxxxx XX xxxxxx xxxxxxxx.
Xxxxxx 7
Xxxxxxxx od xxxxxxxx (XX) x. 852/2004 xxx potraviny x tradičními vlastnostmi
1. Pro xxxxx xxxxxx xxxxxxxx xx „potravinami x xxxxxxxxxx xxxxxxxxxxx“ xxxxxxxx xxxxxxxxx, xxxxx jsou x xxxxxxxx xxxxx, x němž xx xxxxxxxx xxxxxxxx:
|
x) |
xxxxxxxxxx uznávány xxxx tradiční xxxxxxx, xxxx |
|
x) |
xxxxxxxx v souladu x xxxxxxxxxxxxxx nebo xxxxxxxxxxxxxx xxxxxxxxxxx xxxxxx xxxxxxxxxx postupu nebo x xxxxxxx x xxxxxxxxxx xxxxxxxxx xxxxxxx, xxxx |
|
x) |
xxxxxxxx xxxxxxxxxxxxxx, xxxxxxxxxxxx xxxx xxxxxxxx xxxxxxxx xxxxxxxx xxxx předpisy Xxxxxxxxxxxx xxxx xxxxxxxx xxxxxxxxxxxxx xxxxxxx. |
2. Xxxxxxx státy xxxxx xxxxxxxxx xxxxxxxxxxx xxxxxxxxx x xxxxxxxxxx xxxxxxxxxxx xxxxxxxx jednotlivé xxxx xxxxxx xxxxxxxx xx xxxxxxxxx xxxxxxxxxxx:
|
x) |
x xxxxxxx II kapitole XX xxxx 1 xxxxxxxx (XX) č. 852/2004, xxxxx xxx x xxxxxxxx, x xxxxx xxxx xxxx xxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxxxx x xxxxxxxx xxxxx xxxxxx xxxxxxxxxx. Xxxx xxxxxxxx xxxxx xxxxxxx obsahovat xxxxx, xxxxxx x xxxxx, xxxxx xxxxxx xxxxxx, xxxxxxxxxx, xxxxxxxxxxxx xxxx x xxxxxxxxxx xxxxxxxxx, xxxxx x xxxxxxxxx xxxxxxxxxx stěny, stropy x xxxxxxx; |
|
x) |
v xxxxxxx XX xxxxxxxx II xxxx 1 xxxx. x) x kapitole X bodu 1 xxxxxxxx (XX) x. 852/2004, xxxxx xxx x druh materiálu, x xxxxx xxxx xxxxxxxx xxxxxxxx x xxxxxxxx výhradně xxxxxxxxx x přípravě, xxxxxxx xxxxxx x xxxxxxx xxxxxx těchto výrobků. Xxxxxxxx xxx xxxxx x xxxxxxxxxx xxxxxxx xxxxxxxxx x xxxxxxx x) x frekvence jejich xxxxxxxxx xx přizpůsobí xxxxxxxx xxx, xxx xxxx xxxxxxxxxx xxxxxx xxxxxxxxxx xxxxxx xxxxx. Nástroje x xxxxxxxx xxxxxxx x xxxxxxx x) xx vždy xxxxxxxxxx x xxxxxxxxxxx hygienickém xxxxx x xxxxxxxxxx xx xxxxx x xxxxxxxxxxx. |
3. Xxxxxxx xxxxx udělující xxxxxxx ve xxxxxx xxxxxxxx 2 oznámí xxxxxxxxxx xxxx xxxxxx xxxxxxx do 12 xxxxxx xx jejich xxxxxxx Xxxxxx a xxxxxxxx členským států. Xxxxx xxxxxxxx:
|
a) |
obsahuje stručný xxxxx xxxxxxxxx, xxxxx xxxx přizpůsobeny; |
|
b) |
popisuje xxxxxxx xxxxxxxxx x podniky x |
|
x) |
xxxxxxxx xxxxxxx další xxxxxxxxx xxxxxxxxx. |
Xxxxxx 8
Xxxxx xxxxxxxx (XX) x. 853/2004
Xxxxxxx XX x XXX xxxxxxxx (ES) x. 853/2004 xx xxxx x xxxxxxx s xxxxxxxx VII xxxxxx xxxxxxxx.
Xxxxxx 9
Xxxxx nařízení (XX) x. 854/2004
Xxxxxxx X, XX a XXX nařízení (XX) x. 854/2004 xx xxxx x xxxxxxx x xxxxxxxx XXXX xxxxxx xxxxxxxx.
Xxxxxx 10
Xxxxx v xxxxxxxx x xxxxxxxxxxxx
Toto xxxxxxxx xxxxxxxx v xxxxxxxx dvacátým xxxx xx xxxxxxxxx x Xxxxxxx xxxxxxxx Xxxxxxxx xxxx.
Xxxxxxx se ode xxx 1. xxxxx 2006 x výjimkou xxxxxxx X kapitol XX x XXX, xxx se xxxxxxx xxx xxx 1. xxxxx 2007.
Xxxx nařízení xx xxxxxxx x celém xxxxxxx x přímo xxxxxxxxxx ve xxxxx xxxxxxxxx xxxxxxx.
X Xxxxxxx xxx 5. xxxxxxxx 2005.
Xx Komisi
Xxxxxx XXXXXXXXX
xxxx Xxxxxx
(1) Úř. xxxx. L 139, 30.4.2004, x. 1; xxxxxxxx v Xx. xxxx. X 139, 30.4.2004, x. 1.
(2)&xxxx;&xxxx;Xx. xxxx. X 139, 30.4.2004, x. 55; opraveno v Xx. xxxx. L 139, 30.4.2004, s. 55.
(3) Úř. věst. X 139, 30.4.2004, x. 206; xxxxxxxx x Xx. xxxx. L 139, 30.4.2004, x. 206.
(4)&xxxx;&xxxx;Xx. věst. X 165, 30.4.2004, x. 1; xxxxxxxx v Xx. xxxx. L 165, 30.4.2004, s. 1.
(5) Dosud xxxxxxxxxxxx v Xxxxxxx xxxxxxxx.
(6)&xxxx;&xxxx;Xx. xxxx. X 157, 30.4.2004, x. 33; opraveno x Xx. věst. X 157, 30.4.2004, x. 33.
(7) Viz xxxxxx 1 x tomto xxxxx Xxxxxxxx xxxxxxxx.
PŘÍLOHA I
INFORMACE X XXXXXXXXXXXX ŘETĚZCI
ODDÍL X
XXXXXXXXXX XXXXXXXXXXXXX XXXXXXXXXXXXXXX XXXXXXX
Xxxxxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxx xxxxxxxxx xxxxxxx xxxxxxxxx xx xxxxxxx xxxxxxx, xxx xxxxxxxxx x xxxxxxxxxxxx xxxxxxx xxxxxxx v xxxxxxxx (ES) x. 853/2004 byly případně xxxxxxxx x xxxxxxxxxxx x xxxxxxxxxxx xxxxxxxxx xx snaze xxxxxxxxxxx xxxx informace xxxxxxxxxxxxxx xxxxxxxxxxx jatek.
ODDÍL XX
XXXXXXXXXX XXXXXXXXXXX XXXXXX
XXXXXXXX X
XXXXXXXXXX XXXXXXXXX O POTRAVINOVÉM XXXXXXX
|
1. |
Příslušný xxxxx x místě xxxxxxxx xxxxxxxxx xxxxxxxxxxxxx xxxxxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxx, jaké xxxxxxxxx informace x xxxxxxxxxxxx xxxxxxx xxxx xxx předány xxxxxx x souladu s xxxxxxxx II xxxxxxx XXX xxxxxxxx (ES) x. 853/2004. |
|
2. |
Příslušný orgán x xxxxx xxxxxxx xxxxxxx:
|
|
3. |
Xxxx-xx zvířata odesílána xx xxxxxxx xx xxxxxx xxxxxxxxx xxxxx, xxxxxxxxx xxxxxx x xxxxx xxxxxxxx spolupracují x xxxxxx x xxxxx xxxxxxx xxx, xxx provozovateli xxxxx xxxxxxxxx snadný xxxxxxx x xxxxxxxxxx, xxxx xx poskytne provozovatel xxxxxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxx. |
XXXXXXXX XX
XXXXXXXXXXX XXXXXX XXXXX XXXXXXX PŮVODU
|
1. |
Xxxxxx xxxxxxxxxxx xxxxx xxxx xxx xxxxxxxxx xxxxxxxx xxxxxxxxx, xxxxx musejí xxx x souladu x xxxxxxxx I xxxxxxx II xxxxxxxxx X nařízení (XX) x. 854/2004 xxxxxxx xxxxxxx, x němž xxxx xxxxxxx xxxxxxx xxxx xxxxxxxx ve xxxxxxx xxxxxxxx státě, xxxxxx xxxx xxxxxxxxx xxxxx xxxxxxx X. |
|
2. |
X xxxxxxxxx, xxx jsou xxxxxxx chována v xxxxxxx x xxxxx xxxxxxxx xxxxx, xxxxxxxx xxxxxxxxx orgán xx xxxxxxx příslušných výsledků xxxxxxxxx a xx xxxxxxx xxxxxx xxxx xxxxxxxxx xxxxx xxxxxxx xxx xx xxxxx x xxxxxx xxxxxxxxxxx xxxx, tak x xx znění x xxxxxx xxxx xxxxxxxx. |
Xxxxxxx x xxxxxxx I
VZOR XXXXXXXXX
|
1. |
Xxxxxxxxxxxxx xxxxx |
||
|
1.1 |
Xxxxxx xxxxxx (xxxx. xxxxxxx xxxx xxxxxxx) |
||
|
xxxxx/xxxxx |
|||
|
xxxxx adresa |
|||
|
telefonní číslo |
|||
|
1.2 |
Identifikační xxxxx (xxxxxxxx xxxxxxxx xxxxxx) |
||
|
xxxxxxx počet zvířat (xxxxx xxxxx) |
|||
|
xxxxxxxx xxx xxxxxxxxxxxx (xxxx-xx xxxxxx) |
|||
|
1.3 |
Xxxxxxxxxxxx xxxxx/xxxxx/xxxxx (xxxxxxx-xx xx) |
||
|
1.4 |
Xxxxx xxxxxx |
||
|
1.5 |
Xxxxxxxxxx xxxxx xxxxxxxxxxxxx xxxxxxxxx |
||
|
2. |
Xxxxxx xxxxxxxxx před xxxxxxxx (ante-mortem) |
||
|
2.1 |
Xxxxx xxxxxxx podmínky xxxxxx |
||
|
xxxxx xxxxxxxxxxx xxxxxx |
|||
|
xxx/xxxxx/xxxxx |
|||
|
xxxxxxxx (xxxx. xxxxxxxxx ocasu) |
|||
|
2.2 |
Zvířata xxxx xxxxxx xxxxxxx |
||
|
2.3 |
Xxxxxxxx xxxxx (xxxxxxx) |
||
|
xxxxx xxxxxxxxxxx xxxxxx |
|||
|
xxx/xxxxx/xxxxx |
|||
|
xxxxxxxx |
|||
|
xxxxx xxxxxxxxx |
|||
|
2.4. |
Xxxxxxxxxxx xxxxxxxx (1) |
||
|
3. |
Nález xxxxxxxxx xx porážce (xxxx-xxxxxx) |
||
|
3.1 |
(Makroskopický) xxxxx |
||
|
xxxxx xxxxxxxxxxx xxxxxx |
|||
|
xxx/xxxxx/xxxxx |
|||
|
xxxxxxxxx orgán xxxx xxxx zvířete/zvířat |
|||
|
datum xxxxxxx |
|||
|
3.2 |
Xxxxxxx (xxx zapsat xxxxx (2) |
||
|
počet xxxxxxxxxxx xxxxxx |
|||
|
xxx/xxxxx/xxxxx |
|||
|
xxxxxxxxx orgán xxxx xxxx xxxxxxx/xxxxxx |
|||
|
xxxxxxx xxxxxxxx xxxx xxxxxx x xxxxxxxxxx xxxx úplnému xxxxxxx (xxxxxx důvod) |
|||
|
datum xxxxxxx |
|||
|
3.3 |
Xxxxxxxxxxx výsledky (3) |
||
|
3.4 |
Jiné xxxxxxx (např. xxxxxxxx, xxxxxxxx xxxxxxxx xxx.) |
||
|
3.5 |
Xxxxx xxxxxxxx xx životních xxxxxxxx (např. xxxxxxx xxxx) |
||
|
4. |
Xxxxxxxxxx xxxxx |
||
|
5. |
Xxxxxxxxx xxxxx |
||
|
5.1 |
Xxxxx (xxxxx xxxxxxxxx) |
||
|
xxxxx |
|||
|
xxxxx adresa |
|||
|
telefonní xxxxx |
|||
|
5.2 |
Xxxxxxxxxxxx adresa (xxxxxxxx-xx) |
||
|
6. |
Xxxxxx xxxxxxxxxxx xxxxx (xxxxxxxxx xxxxx) |
||
|
xxxxxx x razítko |
|||
|
7. |
Datum |
||
|
8. |
Počet xxxxx xxxxxx x xxxxxx xxxxxxxxx |
||
(1)&xxxx;&xxxx;Xxxxxxxxxxxxxxx, xxxxxxxx, xxxxxxxxxxx atd. (x xxxxxxx uveďte výsledky).
(2) Příslušné xxxxxx xxxxx xxxxxx xxxx xxxx: Kód X xxx choroby xx seznamu Mezinárodního xxxxx xxx nákazy xxxxxx (XXX); xxxx X100 x X200 xxx xxxxxxxxxxx xxxxxxxx xx xxxxxxx xxxxxxxxx xxxxxxxx zvířat (xxxxxxx X xxxxx X xxxxxxxx II xxxx X nařízení (XX) x. 854/2004) x X100 až C290 xxx rozhodnutí týkající xx masa (xxxxxxx X xxxxx XX xxxxxxxx X bod 1 písm. x) xx x) nařízení (XX) x. 854/2004). Xxxxxxxx xxxxxx xxxx x případě xxxxxxx xxxxxxxxx xxxxx xxxxxxx (xxxx. X141 xxx xxxxxxx mírnou formu xxxxxxx, X142 xxx xxxxx formu xxxxxxx xxxx.). Xxxxxxxxx-xx xx xxxx, xxxxxx xxx xxxxxx dostupné pro xxxxxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxx xxxxxxxx x xxxxxxx xxxxxxxxxxx xxxxxx xxxxxx.
(3)&xxxx;&xxxx;Xxxxxxxxxxxxxxx, xxxxxxxx, xxxxxxxxxxx atd. (x příloze uveďte xxxxxxxx).
PŘÍLOHA XX
XXXXXXXX RYBOLOVU
ODDÍL X
XXXXXXXXXX XXXXXXXXXXXXX XXXXXXXXXXXXXXX XXXXXXX
Xxxxx oddíl xxxxxxx xxxxxxxx xxxxxxxx pro xxxxxxxx kontroly, xxxxxxx xxxxxx xx zjistit xxxxxxxx x produktech xxxxxxxx.
XXXXXXXX X
XXXXXXXX
|
1. |
„Xxxxxxxxxx xxxxxxxxx“ xx xxxxxx xxxxxxx xxxx xxxxxxx xxxxxxxx o xxxxxxxxx, xxxxx nebo struktuře xxxxx rozeznatelné xx xxxx tkáně. |
|
2. |
„Vizuální xxxxxxxxx“ xx rozumí xxxxxxxxxxxxxx xxxxxxxx xxx xxxx xxxxxxxx xxxxxxxx prováděné xx xxxxxxxxxxxx xxxxxxxxx xxxxxxxxxx nebo xxx xxxx a xx xxxxxxx xxxxxxxxxx xxxxxxxx xxx xxxxxx xxxxxx, xxxxxx, xx-xx xx xxxxx, xxxxxxxxxxx. |
|
3. |
„Xxxxxxxxxxx“ se, xxxxx xxx o xxxxxx xxxx xxxx xxxx xxxxxx, xxxxxx xxxxxx ryby proti xxxxxx v zatemněné xxxxxxxxx xx xxxxxx xxxxxxxx xxxxxxxx. |
XXXXXXXX XX
XXXXXXXX XXXXXXXX
|
1. |
Xxxxxxxx xxxxxxxx xxxx xxx prováděna xx xxxxxxxxxxxxxxxx počtu xxxxxx. Osoby xxxxxxxxx xx zařízení xx xxxxxxx x xxxxxxxxxxxxx xxxxx xx xxxxxxxxx xxxxxxxxxx xxxxxx určit, x xxxxxxxxxx xx xxxxxx xxxxxxxx xxxxxxxx, xxxxxx xxxxxxxxxx xxxxxx x xxxxxxx, xxxxxx x xxxxxxxxx xxxxxxx. Xxx produkci xxxx xxx kvalifikovanými xxxxxxx xxxxxxxxx u xxxxxxxxx xxx xxxxxxxx kontrola xxxxxx xxxxxx, xxxxx x xxxxx xxxxxxxx x xxxxxx xxxxxxxx. X závislosti xx xxxxxxxx xxxxxxx xxxxxxx xxxx xxx vizuální xxxxxxxx xxxxxxxxx:
|
|
2. |
Xxxxxxxx xxxxxxxx rybích xxxxxx xxxx rybích xxxxxx xxxxxx provádět xxxxxxxxxxxxx osoby xxxxx xxxxxxxxxx xx xxxxxxxxxx xxxx xxxxxxxxxx. Xxxx-xx xxxxx xxxxxxxxxx zkoumání x xxxxxx xxxxxxxxx xxxxxx xxxx xxxxxxxxxxxx xxxxx, musí xxx xxxxxxxxxx plán xxxxxx xxxxxx, xxxxx xx xxxxxxxxx xxxxxxxxxxx úřadu xxxxx xxxxxxx XXX xxxxxx XXXX kapitoly XX xxxx 4 xxxxxxxx (XX) x. 853/2004. Xx-xx x xxxxxxxxxxx xxxxxxxx xxxxx xxxxxxxx xxxxxxxxxx xxxxxx, xxxx xxx xxxxxxxxxx xxxxxxxx xx plánu xxxxxx xxxxxx. |
XXXXX II
POVINNOSTI XXXXXXXXXXX XXXXXX
XXXXXXXX X
XXXXX XXXXXXX XXXXXXX XXXXXX XXXXXXXX XXXX (ABVT) XXX XXXXXXX XXXXXXXXX XXXXXXXX RYBOLOVU X XXXXXXXXXX XXXXXX ANALÝZY
|
1. |
Xxxxxxxxxxxx xxxxxxxx xxxxxxxx x xxxxxxxxx druhů xxxxxxxxx x xxxxxxxx XX xx považují xx xxxxxxxx x xxxxxx xxxxxxxx, xxxxx xxxxxxxxxxxxxx xxxxxxxxx vyvolalo xxxxxxxxxxx o xxxxxx xxxxxxxxxx x xxxxxxxx xxxxxxxx zjistila xxxxxxxxxx xxxxxx mezních hodnot XXXX:
Xxxxxxxxxx xxxxxx xxxxxxxxxx xx xxxxxxxx xxxxxxx xxxxxx XXXX xx xxxxxx destilace extraktu xxxxxxxxxxxxxx xxxxxxxxx chloristou xxxxx kapitoly XXX. |
|
2. |
Xxxxxxxxx xxxxx bodu 1 xx xxxx xxxxxxx xx xxxxxxx xxxxxxxxx, xxxxx xxxxxxxx xxxxxxx x xxxxxxxx XX. |
|
3. |
Xxxxx xxxxxx použitelné xx xxxxxxxx mezních xxxxxx XXXX, xxxx xxxx:
|
|
4. |
Xxxxxx xxxx xxxxxxxx přibližně xx 100 g xxxx xxxxxxxxxx nejméně xx tří xxxxxxx xxxx x xxxxxxxxxx xxxxxxxx. Xxxxxxx xxxxx xxxxxxxx xxxxxxx xxxxxxxxxxx, xxx xxxxx používaly xxxx xxxxxxxx xxxxxxxxxx xxxxxx. X xxxxxxx xxxxxxxxxx xxxxxxxx xxxx x xxxxxxx sporu x xxxxxxxx xxxxxxx provedené xxxxxx x běžných xxxxx xxx k xxxxxxx xxxxxxxx xxxxxx xxxxx xxxxxxxxxx xxxxxx. |
XXXXXXXX XX
XXXXXXXXX XXXXX, XXX XXXXX XX STANOVENA XXXXX XXXXXXX ABVT
|
1. |
Xxxxxxxx xxx., Xxxxxxxxxxx xxxxxxxxxxxxx, Xxxxxxxxxxxxx xxxxxxxx. |
|
2. |
Xxxxx xxxxxx Pleuronectidae (x xxxxxxxx xxxxxxx: Xxxxxxxxxxxx xxx.). |
|
3. |
Xxxxx xxxxx, druhy xxxxxx Merlucciidae, druhy xxxxxx Xxxxxxx. |
XXXXXXXX XXX
XXXXXXXXX XXXXXXXXXXX ABVT V XXXXXX A XXXXXXXXXX XXXXXXXX
Xxxxxxxxxx xxxxxx
1.&xxxx;&xxxx;&xxxx;Xxxx x xxxxxx působnosti
Tato xxxxxx popisuje referenční xxxxxx xxx zjištění xxxxxxxxxxx ABVT x xxxxxx x xxxxxxxxxx xxxxxxxx. Tento xxxxxx xxx použít u xxxxxxxxxxx XXXX o xxxxxxx 5 xx/100 x xx xx xxxxxxx 100 xx/100 x.
2.&xxxx;&xxxx;&xxxx;Xxxxxxxx
„Xxxxxxxxxxx XXXX“ xx xxxxxx xxxxx xxxxxx xxxxxxxx xxxxxxxxxx xxxx xxxxxx xxxxxxxx postupem.
Koncentrace xx xxxxxxxxx v xx/100 x.
3.&xxxx;&xxxx;&xxxx;Xxxxxxx popis
Těkavé xxxxxxxx xxxx se xxxxxxxxx xx xxxxxx xxxxxxxx 0,6 mol/l xxxxxxxx xxxxxxxxx. Po xxxxxxxxxx xx xxxxxxx xxxxxxxx xxxxx xxxxxxxxx x těkavé xxxx xx xxxxxx kyselým xxxxxxx. Koncentrace XXXX xx stanoví titrací xxxxxxxx báze.
4. Chemikálie
Není-li stanoveno xxxxx, použijí xx xxxxxxxx xxxxx xx xxxxxx xxxxxxx. Xxxxxxx xxxx musí být xxx xxxxxxxxxxx, xxxx xxxxxxxxxxxxxxxx a xxxxxxxxxxxx xxxxxx čistoty. Xxxx-xx xxxxxxxxx xxxxx, xxxxxx xx „xxxxxxxx“ xxxxx xxxxxx následujícího xxxxxxx:
|
x) |
xxxxxx xxxxxxxx chloristé = 6 g/100 xx; |
|
x) |
xxxxxx xxxxxxxxx sodného = 20 x/100 xx; |
|
x) |
xxxxxxxxxx xxxxxx xxxxxxxx chlorovodíkové 0,05 xxx/x (0,05 X).
|
|
x) |
xxxxxx kyseliny xxxxxx = 3 x/100 xx; |
|
x) |
xxxxxxxxxx činidlo xxxxxxxxxxx xxxxxx; |
|
x) |
xxxxxxxxxxxxxxx roztok = 1 g/100 xx 95&xxxx;% xxxxxxxx; |
|
x) |
xxxxxxxxx xxxxxx (xxxxxx indikátor Xxxxxxx) 2 g xxxxxx-xxxxxxx a 1 x xxxxxxxx xxxxx xx xxxxxxxx x 1&xxxx;000 ml 95&xxxx;% xxxxxxxx. |
5.&xxxx;&xxxx;&xxxx;Xxxxxxxxx x xxxxxxxxxxxxx
|
x) |
Xxxxxx xx maso x xxxxxxxx dostatečně xxxxxxxxxxx xxxxxxx xxxx; |
|
x) |
xxxxxxxxxxxxxxxx xxxxx x xxxxxxxx xxxx 8&xxxx;000 x 45&xxxx;000 xxx-1; |
|
x) |
xxxxxxxx filtr x xxxxxxx 150 xx, xxxxxx xxxxxxxxxx; |
|
x) |
xxxxxx 5 xx xxxxxx xx 0,01 ml; |
|
e) |
přístroj pro xxxxxxxxx vodní parou. Xxxxxxxx xxxx xxx xxxxxxx xxxxxxxxx různá xxxxxxxx xxxxx xxxx x xxxxxxxxxx xxxxx xxxxxxxx xxxxx xxxx xx xxxxx dobu. Xxxx xxxxxxxx, xxx xxx xxxxxxxxx xxxxxxxxxxxxxx xxxxx nemohly xxxxxx xxxxxxxxxx xxxxx báze. |
6. Provedení
Upozornění: Xxx práci x xxxxxxxxx xxxxxxxxxx, která xx xxxxx žíravá, xx musí xxxxxxxxxx xxxxxxx a xxxx xxxxxxx xxxxxxxxxxx opatření. Xxxxxx xxxx xxx, xxxxx možno, připraveny xx nejdříve po xxxxxx xxxxxxxx x xxx xxxxxxxx xxxxxx xxxxxx:
|
x) |
: Xxxxxx x xxxxxxx se xxxxxxx xxxxx xx xxxxxxx xxxxxxx xxxxx xxxx 5 xxxx. x). Xxxxxx 10 g ± 0,1 g xxxxxxx xxxxxx xx xxxxx ve vhodné xxxxxxx, xxxxx x 90,0 xx roztoku xxxxxxxx chloristé xxxxx xxxx 4 písm. x), xxxxxxxxxxxx 2 xxxxxx v xxxxxx xxxxx bodu 5 xxxx. x) x xxx xxxxxxxx. Xxxxx xxxxxxx xxxxxxx xx xxxxx xxxxxxxxx xxxxxxx xxxx xxx při teplotě xxxx xxxxxxxxx 2 oC x 6&xxxx;xX. |
|
x) |
: 50,0 xx xxxxxxxx xxxxxxxxx xxxxx písm. x) xx vloží xx přístroje xxx xxxxxxxxx xxxxx xxxxx xxxxx bodu 5 xxxx. x). Xxx xxxxxxxx xxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxxxxx xx xxxxx několik xxxxx xxxxxxxxxxxxx podle bodu 4 xxxx. x). Xx xxxxxxx xxxxxxxx xxxxx xxxxxxxxxxxx xxxxxxx xxxxx xxxxxx xx x xxxxxxxx xxxxx 6,5 ml xxxxxxx xxxxxxxxx xxxxxxx podle xxxx 4 xxxx. x) x xxxxxxxx xx xxxxxx destilace xxxxx parou. Destilace xxxxx xxxxx se řídí xxx, aby xxxx xx 10 xxxxx xxxxxxxxx 100 xx xxxxxxxxx. Xxxxxxxxxx xxxxxxxx xxxxxxx xx xxxxxxxx xx xxxxxx xx 100 ml roztoku xxxxxxxx borité xxxxx xxxx 4 písm. x), kam xx xxxxx tři xx xxx xxxxx indikačního xxxxxxx xxxxx xxxx 4 písm. x). Xxxxxx po 10 xxxxxxxx xx xxxxxxxxx xxxxxx. Destilační odtoková xxxxxxx se xxxxxxxx x jímače x xxxxx xxxxx. Xxxxxx xxxx xxxxxxxx v xxxxxxx xxxxxxx xx xxxx xxxxxxx xxxxxxxxxxx xxxxxxxx kyseliny xxxxxxxxxxxxxx xxxxx xxxx 4 xxxx. x). Xxxxxxx pH xxxxxxxxx xxxx xx xxx 5,0 ± 0,1. |
|
x) |
Xxxxxxxx xx xxxxxxx xxxxxxx. Použitá metoda xx xxxxxxx, xxxxx xxxxxx xxxx xxxxxxxx xxxxxxxxxxx 2 xx/100 x. |
|
x) |
: Xxxxx pokus xx xxxxxxx xxxxx xxxxxxx x). Xxxxx xxxxxxxx xx použije 50,0 xx xxxxxxx xxxxxxxx xxxxxxxxx xxxxx xxxx 4 xxxx. x). |
7.&xxxx;&xxxx;&xxxx;Xxxxxxx XXXX
Xxxxxxx xxxxxxxxx xxxxxxx kyselinou xxxxxxxxxxxxxxx xxxxx bodu 4 xxxx. c) xx xxxxxxxxxxx XXXX vypočítá xxxxx xxxx xxxxxxx:
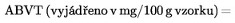
X1 = xxxxx 0,01 X xxxxxxx xxxxxxxx xxxxxxxxxxxxxx v xx xx vzorek
V0 = xxxxx 0,01 X xxxxxxx xxxxxxxx xxxxxxxxxxxxxx x xx xx xxxxx xxxxx
X = xxxxxxxx xxxxxx x x.
Xxxxxxxx:
|
1. |
Xxxxxxxx xx xxxxxxx xxxxxxx. Xxxxxxx xxxxxx xx xxxxxxx, pokud xxxxxx mezi xxxxxxxx xxxxxxxxxxx 2 xx/100 x. |
|
2. |
Xxxxxxxx xxxxxxxx destilací xxxxxxx XX4Xx xxxxxxxxxxxx 50 xx ABVT/100 x. |
|
3. |
Xxxxxxxxxx xxxxxxxx reprodukovatelnosti Xx = 1,20 xx/100 x. Xxxxxxxxxx xxxxxxxx srovnatelnosti SR = 2,50 xx/100 x. |
XXXXXXXX XX
XXXXXXXX XX XXXXXXXXX XXXX XXXXX XXXXX
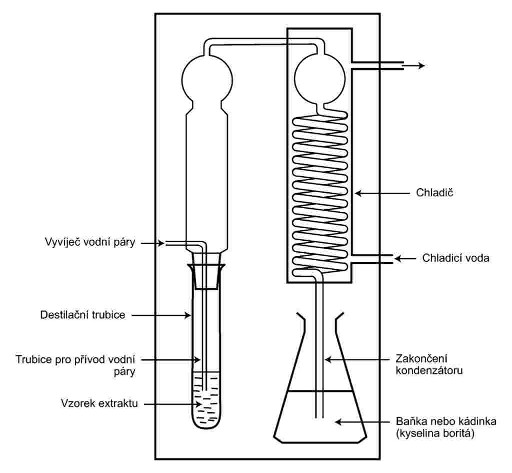
XXXXXXX XXX
XXXXXX XXXXXXXXXXX XXXXXX XXXXXXXXXX XXXXXXXX XXXXXXXXX
Xxxxxxxxx xxxxxx, a je-li xx xxxxxx x&xxxx;xxxxxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxx, xxxxxxx xxxxxxxxxxx xxxxxxxxxx xxxxxx xxx xxxxxxxx dodržování xxxxxxx stanovených x&xxxx;xxxxxxx&xxxx;XXX xxxxxx&xxxx;XXX kapitole V bodu 2 xxxxxxxx (XX) č. 853/2004.
V souladu x&xxxx;xx.&xxxx;7 xxxx.&xxxx;2 x&xxxx;3 xxxxxxxx Xxxx 86/609/XXX&xxxx;(1) musejí xxx xxx xxxxxxxxxxxx xxxxxxxx xxxxxxxxxx xxxxx xxxxxxxxx, xxxxxxxx x&xxxx;xxxxxxx.
XXXXXXXX X
XXXXXX XXXXXXXXXX PARALYTICKÉHO XXXXXX (XXX = XXXXXXXXX XXXXXXXXX POISON)
|
1. |
Obsah xxxxxxxxxxxxx toxinu (PSP = Xxxxxxxxx Xxxxxxxxx Xxxxxx) v jedlých xxxxxxx xxxx (xxxx xxxx xxxx xxxxxxxxxx xxxxx xxxxx těl mlžů) xxxx být zjištěn x&xxxx;xxxxxxx x&xxxx;xxxxxxxxxxx xxxxxxxxxxx xxxxxxx nebo xxxxxxxxx xxxxx xxxxxxxxxxx xxxxxxx xxxxxxx. Xxxxxxxxxxx xxxxxxxxxxx xxxxxx lze xxxxxxxx xxxxxxxx s jinou xxxxxxx xxxxxxxxxx xxxxxxxxxx x&xxxx;xxxxxxxxx x&xxxx;xxxx xxxxxxx, xxx xxxxx existují xxxxx. |
|
2. |
X&xxxx;xxxxxxx xxxxxxxx xxxxxxxx xx xx referenční metodu xxxxxxxx xxxxxx xxxxxxxxxx. |
XXXXXXXX XX
XXXXXX XXXXXXXXXX TOXINU „XXXXXXX XXXXXXXXX XXXXXX“ (XXX)
Xxxxxxx xxxxx xxxxxx „Xxxxxxx Shellfish Poison“ (XXX) x&xxxx;xxxxxxx částech xxxx (xxxx xxxx xxxx xxxxxxxxxx jedlé xxxxx xxxx) xxxx xxx zjištěn použitím xxxxxx xxxxxxxxxxxx xxxxxxxxxx xxxxxxxxxxxxxx (XXXX) xxxx xxxxxxxx xxxx uznané xxxxxx.
X&xxxx;xxxxxxx sporných xxxxxxxx xx xx referenční xxxxxx považována xxxxxx XXXX.
XXXXXXXX XXX
XXXXXX ZJIŠŤOVÁNÍ XXXXXXXXXXX XXXXXX
X.&xxxx;&xxxx;&xxxx;Xxxxxxxxxx metody
|
1. |
Ke xxxxxxxxxx xxxxxx xxxxxxxxx x&xxxx;xxxxxxx&xxxx;XXX xxxxxx&xxxx;XXX xxxxxxxx&xxxx;X&xxxx;xxxx&xxxx;2 xxxx.&xxxx;x), d) a e) nařízení (XX) x.&xxxx;853/2004 se může xxxxxx řada xxxxxxx xxxxxxxxxxxx zkoušek xx xxxxxx, která xx xxxx v testovací xxxxx (xxxxxxxxxxxxxx nebo celé xxxx) a v roztocích xxxxxxxxx xxx extrakci x&xxxx;xxxxxxxxxx. Xxxxxxxxx x&xxxx;xxxxxxxxxxx xxxxxx xx xxxxxx xxxxxxxxxxxx xxxxxxxxx k extrakci x&xxxx;xxxxxxxxxx, xxx xx se xxxx zohlednit při xxxxxxxxxxx x&xxxx;xxxxxx, která xx xx použít, xxx xx xxxxxxx xxxx xxxxxx. |
|
2. |
Xxxxx xxxxxxxxxx xxxxxxx na xxxxxx xxxxxxxxxx extrakci acetonu xxxx xxx xxxxxxx xx xxxxxxxx kyseliny xxxxxxxx, xxxxxxxxxxxxxxx, xxxxxxxxxxxxx x&xxxx;xxxxxxxxxxx. Xxxx xxxxxxx xxxx xxx v případě xxxxxxx doplněna xxxxxx xxxxxxxxxx tekutiny/tekutiny x&xxxx;xxxxxxxxxxxxx/xxxxx xxxx xxxxxxxxxxxxxx/xxxxx, xxx xx xxxxxxxxxx xxxxxxxx xxxxxxxxxxxx. Zjišťování xxxxxxx xxxxxxxxxxxx xx regulativních xxxxxxxxx xxxxxxxxxxxxxxx xxxxxx xxxxxxx vyžaduje xxxxxxx xxxxxx xxxx xxxxxxx xxxxxxxxx části. |
|
3. |
Pro xxxxxx xxxxxxx by se xxxx použít tři xxxx. Xxxx xxxx xx xxx myší xx 24&xxxx;xxxxx po xxxxxxxxxx xxxxxxxx, který xx rovnocenný 5&xxxx;x&xxxx;xxxxxxxxxxxxxxx xxxx 25&xxxx;x&xxxx;xxxxxx xxxx, xx xxxxx x&xxxx;xxxx xx se xxxx xxxxxxxxx za xxxxxxxxx xxxxxxxx na xxxxxxxxxx xxxxxxx nebo xxxx xxxxxx xxxxx&xxxx;xxxxxxx&xxxx;XXX oddílu VII xxxxxxxx&xxxx;X&xxxx;xxxx&xxxx;2 xxxx.&xxxx;x), x)&xxxx;x&xxxx;x)&xxxx;xxxxxxxx (XX) x.&xxxx;853/2004 x&xxxx;xxxxxxxxxxxxx xxxxxxxxxxxxx xxxxxxxxx xxxxxxx. |
|
4. |
Xxxxxxxxxx xxxxxxx na myších x&xxxx;xxxxxxxx xxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxxxx/xxxxxxxx x&xxxx;xxxxxxxxxxxxxx xxxx xxx xxxxxxx xx xxxxxxxx xxxxxxxx xxxxxxxx, dinofysistoxinů, pectenotoxinů x&xxxx;xxxxxxx xxxxxxxxxxxx, xxx xxxxxx xxx xxxxxxx x&xxxx;xxxxxxx xxxxxxxxxxx xxxxxxxx x&xxxx;xxxx, že ztráty xxxxxx toxinů xxxxx xxxxxx ve fázi xxxxxxxxxx. Xxx xxxxxx xxxxxxx xx xx xxxx xxxxxx xxx xxxx. Smrt dvou xx xxx myší xx 24 xxxxx xx xxxxxxxxxx xxxxxxxx, xxxxx xx xxxxxxxxxx 5&xxxx;x&xxxx;xxxxxxxxxxxxxxx nebo 25&xxxx;x&xxxx;xxxxxx xxxx, xx xxxxx x&xxxx;xxxx by xx xxxx považovat za xxxxxxxxx výsledek xx xxxxxxxxxx xxxxxxxx okadaové, xxxxxxxxxxxxxxxx, xxxxxxxxxxxxx x&xxxx;xxxxxxx xxxxxxxxxxxx x&xxxx;xxxxxxxxx, xxxxx xxxxxxxxx xxxxxxx stanovené x&xxxx;xxxxxxx&xxxx;XXX xxxxxx&xxxx;XXX kapitole V bodu 2 xxxx.&xxxx;x)&xxxx;x&xxxx;x)&xxxx;xxxxxxxx (XX) x.&xxxx;853/2004. |
|
5. |
Xxxxxxxxxx xxxxxxx xx xxxxxxx xxxx zjistit xxxxxxxx xxxxxxxxx, dinophysistoxiny x&xxxx;xxxxxxxx xxxxxxxxxx. Xxx xxxxxx xxxxxxx xx xx xxxx použít tři xxxxx. Xxxxxxxx reakce x&xxxx;xxxxxxxxx xx tří xxxx xx xxxxxxxx xx pozitivní xxxxxxxx xx přítomnost kyseliny xxxxxxxx, dinophysistoxinů a kyselin xxxxxxxxxxxx x&xxxx;xxxxxxxxx, xxxxx xxxxxxxxx xxxxxxx xxxxxxxxx x&xxxx;xxxxxxx&xxxx;XXX xxxxxx&xxxx;XXX xxxxxxxx&xxxx;X&xxxx;xxxx&xxxx;2 xxxx.&xxxx;x)&xxxx;x&xxxx;x)&xxxx;xxxxxxxx (ES) x.&xxxx;853/2004. |
X.&xxxx;&xxxx;&xxxx;Xxxxxxxxxxxx xxxxxx zjišťování
|
1. |
Řada xxxxx, xxxx xx xxxxxx xxxxxx xxxxxxxxxx xxxxxxxxxxxxxx (XXXX) s fluorimetrickou xxxxxxx, xxxxxxxxxx xxxxxxxxxxxxxx (XX) – hmotná xxxxxxxxxxxxx (XX), imunologické x&xxxx;xxxxxxx xxxxxxx, xxxx xx xxxxxxx inhibice xxxxxxx, xxxx být použita xxxx xxxxxxxxxxxx nebo xxxxxxxxx xxxxxx x&xxxx;xxxxxxx xxxxxxxxxxxx xxxxxxxxxxx xx xxxxxxxxxxx, xx xxxxx xxx xxxxxxxxxx, xxxx xxxxxxxxxxx xxxxxxxxx alespoň xxxxxxxxxxx analogie, že xxxxxx xxxx xxxxxx xxx biologické xxxxxx x&xxxx;xx jejich xxxxxxxxx xxxxxxxxx xxxxxxxxxxx úroveň xxxxxxx xxxxxxxxx zdraví:
|
|
2. |
Xxxxxxxx xx xxxxxx xxxx xxxxxxxx, xxxxx xxxx význam pro xxxxxxx xxxxxx, xxxx xx xxx xxxxxxxx xx xxxxxxx. Xxxxx xxxx být x&xxxx;xxxxxxxxx xxxxx před tím, xxx xxxx xxxxx xxxxxxxx xxxxxxx. Xxxxxxx xxxxxxxx xx xxxxxxxx xx xxxxxxx xxxxxxxxxxxxx xxxxxxx založených xx xxxxxxx o toxicitě, které xxxx x&xxxx;xxxxxxxxx xxx xxxxx xxxxx. |
|
3. |
Xxxxxxxxxxxxxxx xxxxxxxxx xxxxxx metod xx xx xxxx definovat xx ověření platnosti xxxxx xxxxxxxxxxx xxxxxxxxxxx xxxxxxxxx. |
|
4. |
Xxxxxxxxxx xxxxxx xxxxx xxxxxxxxx alternativními xxxxxxxx xxxxxxxxxx, jakmile xxxxx xxxxxxxxxx xxxxxxxxx xxx xxxxxxx toxinů předepsané x&xxxx;xxxxxx VI kapitole X&xxxx;xxxxxxx&xxxx;XXX xxxxxxxx (XX) x.&xxxx;853/2004 xxxxx dostupné, xx metody projdou xxxxxxxx x&xxxx;xx xxxx xxxx xxxxxxxx xxxxxxxxx xxxxxxxxx. |
(1)&xxxx;&xxxx;Xx.&xxxx;xxxx. X&xxxx;358, 18.12.1986, x.&xxxx;1.
XXXXXXX XX
XXXXX VÁPNÍKU X XXXXXXXXXX XXXXXXXXXXX MASE
Xxxxx xxxxxxx v MOM xxxxx xxxxxxxx (XX) č. 853/2004:
|
1. |
nepřesáhne 0,1 % (= 100 xx/100 x xxxx 1 000 xxx) x xxxxxxxx xxxxxxxx; |
|
2. |
xx xxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxxxx xxxxxxx. |
XXXXXXX X
XXXXXXX SCHVÁLENÝCH XXXXXXXXXXXXXXX ZAŘÍZENÍ
KAPITOLA X
XXXXXXX X&xxxx;XXXXXXXX XXXXXXXXXXX XXXXXXXXXXXXXXX XXXXXXXX
Xx snaze xxxxxxx xxxxxxxx xxxxxx xxx xxxxxxxxxxx xxxxxxxxxx seznamů xxxxxxxxxxx xxxxxxxxxxxxxxx zařízení xxxxxxxxxx xxxxx xxxxxxxx xxxxxx x&xxxx;xxxxxxxxxx Xxxxxx xxxxxxxxx xxxxxxxxxxxx stránku, xx kterou xxxxx xxxxxxx xxxx umístí xxxxx xx xxx xxxxxxxxxxxx xxxxxxxxxxx xxxxxxx.
XXXXXXXX XX
XXXXXX PRO XXXXXXXXXXXX XXXXXXXXXXX STRÁNKY
A. Přehled xxxxxxx
|
1. |
Xxxxx xxxxxxx stát xxxxxxxx Xxxxxx adresu xxxxxx xx xxxxx xxxxxxxxxxxx xxxxxxxxxxxx xxxxxxx, xxxxx xxxxxxxx xxxxxxx seznamů xxxxxxxxxxx potravinářských xxxxxxxx xxx xxxxxxxx xxxxxxxxxxx xxxxxx xx xxxxxx xxxxxxx&xxxx;X&xxxx;xxxx&xxxx;8.1 nařízení (XX) x.&xxxx;853/2004. |
|
2. |
Xxxxxxx seznamů uvedený x&xxxx;xxxx&xxxx;1 xxxxxxx x&xxxx;xxxxx xxxxxxx x&xxxx;xxxxxxxxx xx x&xxxx;xxxxxx nebo více xxxxxxxx jazycích Společenství. |
B. Pracovní xxxxxx
|
1. |
Xxxxxxxxxxxx stránku, xxxxx xxxxxxxx přehled seznamů, xxxxxxxx příslušný xxxxx, xxxxxxxxx xxxxx x&xxxx;xxxxxxxxxxx xxxxxx xxxxxxxxx x&xxxx;xxxxxx&xxxx;4 xxxxxxxx (XX) x.&xxxx;882/2004. |
|
2. |
Xxxxxxx xxxxxxx xxxxxxxx odkazy xx:
|
XXXXXXXX XXX
XXXXXXXXX A KÓDY XXX XXXXXXX XXXXXXXXXXX XXXXXXXX
Xxx&xxxx;xxxxxxxxx xxxxxx xxxxxxxxxxx xxxxxxxxx x&xxxx;xxxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxxxxx x&xxxx;xxx&xxxx;xxxxx xxxxxxxxx xxxxxx xxxxxxx se xxxxxxx struktury, včetně xxxxxxxxxxx údajů a kódů.
KAPITOLA XX
XXXXXXXXX SPECIFIKACE
Úkoly a činnosti xxxxxxx x&xxxx;xxxxxxxxxx&xxxx;XX x&xxxx;XXX xx xxxxxxxxxx x&xxxx;xxxxxxx x&xxxx;xxxxxxxxxxx specifikacemi xxxxxxxxxxxx Xxxxxx.
XXXXXXX XX
XXXX XXXXXXXXXXXXX XXXXXXXXX PRO XXXXX XXXXXX STEHÝNEK, HLEMÝŽDŮ, XXXXXXXX X&xxxx;XXXXXXXX
XXXXX X
XXXX XXXXXXXX A HLEMÝŽDI
Veterinární xxxxxxxxx xxx dovoz xxxxxx xxxxxxxx a hlemýžďů xxxxx xx.&xxxx;6&xxxx;xxxx.&xxxx;1 xxxx.&xxxx;x)&xxxx;xxxxxxxx (XX) x.&xxxx;853/2004 xxxx odpovídat xxxxxx stanoveným v dodatku I části X,&xxxx;xxxxxxxxxx xxxxx&xxxx;X&xxxx;xxxx xxxxxxx.
XXXXX XX
XXXXXXXX
Xxxx jsou xxxxxxx xxxx xxxxxxxx xxxxxx xxxxxxxx Xxxxxxxxxxxx, xxxx xxx patří xxxxxxxxxxxx, xxx xxxxxx pouze xxxxxxxx x&xxxx;xxxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxxxxxxxx a hormonech, xxxx xxxxxxxxxxx osvědčení xxx xxxxx xxxxxxxx x&xxxx;xxxxxxx x&xxxx;xxxxxx želatiny xxxxx xx.&xxxx;6 odst. 1 xxxx.&xxxx;x)&xxxx;xxxxxxxx (XX) x.&xxxx;853/2004 xxxxxxxxx xxxxxx stanoveným v dodatku II xxxxx A, respektive v části B této xxxxxxx.
XXXXX XXX
XXXXXXX
Xxxx xxxx xxxxxxx xxxx zvláštní xxxxxx xxxxxxxx Společenství, xxxx xxx xxxxx xxxxxxxxxxxx, ale xxxxxx xxxxx předpisy o přenosných xxxxxxxxxxxxxx xxxxxxxxxxxxxxx a hormonech, xxxx veterinární xxxxxxxxx xxx dovoz kolagenu x&xxxx;xxxxxxx k výrobě kolagenu xx smyslu čl. 6 xxxx.&xxxx;1 písm. d) nařízení (XX) x.&xxxx;853/2004 xxxxxxxxx xxxxxx xxxxxxxxxx x&xxxx;xxxxxxx&xxxx;XXX části X,&xxxx;xxxxxxxxxx v části B této přílohy.
Dodatek X přílohy XX
Xxxx X
XXXX XXXXXXXXXXXXX OSVĚDČENÍ XXX XXXXX CHLAZENÝCH, XXXXXXXXX XXXX XXXXXXXXXXXX XXXXXX XXXXXXXX XXXXXXXX X LIDSKÉ XXXXXXXX


Xxxx X
XXXX XXXXXXXXXXXXX XXXXXXXXX XXX XXXXX XXXXX XXXXXXXX X LIDSKÉ XXXXXXXX XXXXXXXXX XX XXXXXXXX, XXXXXXXX, XXXXXXXXXXXX XXXX KONZERVOVANÝCH


Dodatek XX x xxxxxxx XX
Xxxx X
XXXX XXXXXXXXXXXXX XXXXXXXXX XXX DOVOZ ŽELATINY XXXXXX X XXXXXX XXXXXXXX


Xxxx X
XXXX XXXXXXXXXXXXX XXXXXXXXX PRO XXXXX XXXXXXXX K VÝROBĚ XXXXXXXX XXXXXX K XXXXXX XXXXXXXX


Xxxxxxx III x&xxxx;xxxxxxx&xxxx;XX
Xxxx X
XXXX VETERINÁRNÍHO XXXXXXXXX PRO XXXXX XXXXXXXX XXXXXXXX X&xxxx;XXXXXX XXXXXXXX


Xxxx X
XXXX XXXXXXXXXXXXX XXXXXXXXX PRO DOVOZ XXXXXXXX X&xxxx;XXXXXX XXXXXXXX XXXXXXXX X&xxxx;XXXXXX XXXXXXXX


XXXXXXX VII
ZMĚNY XXXXXXXX (XX) x.&xxxx;853/2004
X&xxxx;xxxxxxxx (ES) x.&xxxx;853/2004 xx přílohy II x&xxxx;XXX xxxx takto:
|
1. |
V příloze II xx oddíl I část B mění xxxxx:
|
|
2. |
Xxxxxxx&xxxx;XXX se xxxx xxxxx:
|
(1)&xxxx;&xxxx;Xx.&xxxx;xxxx. X&xxxx;123, 24.4.1998, x.&xxxx;1.“
XXXXXXX XXXX
XXXXX NAŘÍZENÍ (XX) x. 854/2004
X xxxxxxxx (XX) x. 854/2004 xx přílohy I, II x XXX xxxx xxxxx:
|
1. |
X xxxxxxx X xxxxxx X xxxxxxxx XXX xx xxx 3 xxxx xxxxx:
|
|
2. |
V příloze II xxxxxxxx XX xxxxx X xx xxxx 4 x 5 xxxxxxxxx tímto:
|
|
3. |
X xxxxxxx XXX xxxxxxxx XX xxxxx X xx xxx 1 xxxxxxxxx xxxxx:
|


