XXXXXXXX XXXXXX 2006/86/XX
xx xxx 24. října 2006,
xxxxxx xx provádí xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Rady 2004/23/XX, xxxxx xxx x xxxxxxxxx na xxxxxxxxxxxxxx, xxxxxxxxxx závažných nežádoucích xxxxxx x xxxxxx x některé xxxxxxxxx xxxxxxxxx xx kódování, xxxxxxxxxx, konzervaci, xxxxxxxxxx x distribuci lidských xxxxx x xxxxx
(Xxxx x xxxxxxxx xxx XXX)
XXXXXX XXXXXXXXXX XXXXXXXXXXXX,
x xxxxxxx xx Xxxxxxx x xxxxxxxx Xxxxxxxxxx xxxxxxxxxxxx,
x xxxxxxx xx xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Xxxx 2004/23/XX xx xxx 31. xxxxxx 2004 x xxxxxxxxx xxxxxxxxxx x xxxxxxxxxxxxxx xxxxx xxx xxxxxxxx, odběr, vyšetřování, xxxxxxxxxx, xxxxxxxxxx, skladování x distribuci xxxxxxxx xxxxx a xxxxx (1), x xxxxxxx xx xxxxxx 8, xx. 11 xxxx. 4 x xx. 28 xxxx. x), x), x), a h) xxxxxxx xxxxxxxx,
xxxxxxxx x xxxxx xxxxxxx:
|
(1) |
Xxxxxxxx 2004/23/XX xxxxxxx xxxxxxxx a xxxxxxxxxxxx normy pro xxxxxxxx, odběr, xxxxxxxxxxx, xxxxxxxxxx, konzervaci, skladování x xxxxxxxxxx xxxxxxxx xxxxx x xxxxx xxxxxxxx k xxxxxxx x xxxxxxx x xxxxxxxxx získaných z xxxxxxxx xxxxx a xxxxx určených x xxxxxxx x xxxxxxx x xxxxx xxxxxxxx xxxxxxx xxxxxx xxxxxxx xxxxxxxx xxxxxx. |
|
(2) |
Xxx xx xxxxxxxxxxx xxxxxxx xxxxxx xxxxxxxxxxxxxxx xxxxxxxx tkání x xxxxx určených x použití x xxxxxxx x xxx xx xxxxxxxx rovnocenná xxxxxx xxxxxxx x xxxxxxxxxxx, xxxxxx xxxxxxxx 2004/23/XX xx stanovení xxxxxxxxxxxx xxxxxxxxxxx xxxxxxxxx xxx xxxxxx x xxxx xxxxxxx použití xxxxxxxx xxxxx x xxxxx, xxxxxx xxxxx x xxxxxxxxxxx xxx xxxxxx xxxxxxx xxxxxxxxx xxxxxxxx. |
|
(3) |
Xxxxxxx xxxxx by xxxx x xxxxxxx xx směrnicí 2004/23/XX xxxxxxxx xxxxxx xxxxxxxxxx x xxxxxxxxx xxxxxxxxx xxxxxxxx x xxxxxxx xxxxxxxx xxxxx a xxxxx x udělování xxxxxxxxxxx oprávnění xxxx xxxxxxxx, xxx se xxxxxxxxx vysoká xxxxxx xxxxxxx xxxxxxxx xxxxxx. Xxx tento xxxxxx xx xxxxx xxxxxxxx xxxxxxxxx xxxxxxxxx. |
|
(4) |
Xxxxxxxxx xx xxxxxxxxxx x xxxxxxxxx xxxxxxxxx zařízení a xxxxxxx xxxxxxxxxxx oprávnění xxxx xxxxxxxx by xx xxxx vztahovat xx xxxxxxxxxx a xxxxxx, xxxxxxxxxx, vybavení, xxxxxxxxx, xxxxxxxx/xxxxxxxx, dokumentaci, xxxxxxx x xxxxxxxxxxx xxxxxxx. Akreditovaná a xxxxxxxxx xxxxxxx xxxxxxxx xxxx tkáňová xxxxxxxx, xxxx bylo xxxxxxx xxxxxxxxx nebo xxxxxxxx, xx měla splňovat xxxxxxxxx požadavky xx xxxxxxxx činnosti, které xxxxxxxxx. |
|
(5) |
Xxxxx xxxxxxxx xx xxxxxxx vzduchu xxx xxxxxxxxxx tkání x xxxxx je klíčovým xxxxxxxx, xxxxx xxxx xxx xxxx xx xxxxxx kontaminace xxxxx xxxx buněk. Xxxxxx xx vyžaduje xxxxxxx xxxxxxx, x němž xxxx počet xxxxxx x xxxxx xxxxxxxxxxxxx xxxxxxx xxxxxxxxxx počtům xx xxxxx xxxxxxx X, xxx je xxxxxxxxxx x xxxxxxx 1 Xxxxxxxxxx xxxxxx xxx správnou xxxxxxx xxxxx x ve xxxxxxxx Xxxxxx 2003/94/XX (2). X xxxxxxxx xxxxxxxxx xxxx není xxxxxxx xxxxxxx x xxxxxx xxxxxx a počtem xxxxxxxxxxxxx xxxxxxx xxxxxxxxxxxx xxxxxx x normě xxxxx A xxxxxxxxxx. Xx takových xxxxxxxxx xx xxxx xxx xxxxxxxxx x xxxxxxxxxxxxxx, xx xxxxxxx xxxxxxxxx xxxxxxxx jakost a xxxxxxxxxx, xxx xxxx xxxxxxxxxx xxx xxxx xxxx xxxxx a xxxxx, daný xxxxxx x xxxx použití x člověka. |
|
(6) |
Oblast působnosti xxxx xxxxxxxx by xxxx xxxxxxxxx xxxxxx x xxxxxxxxxx xxxxxxxx xxxxx a xxxxx xxx xxxxxxxx, xxxxxxxxxx, xxxxxxxxxx, skladování x xxxxxxxxxx xx zdravotnických xxxxxxxx, x němž xx xxxxxxx v xxxxxxx xxxx. Xxxxxx xx však být xxxxxxxxx xx xxxxxxx xxxxxx xxxxx x xxxxx u xxxxxxx (xxxx. xxx xxxxxxxxxx, xxxxxxx, xxxxxxxxxx xxxx xxxxxxx xxxxxx). Xxxxxxxxxx xxxx xxxxxxxx xxxxxxxx xx xxxxxxxxxxxxxxx a xxxxxxxxxx xxxxxxxxx nežádoucích xxxxxx x účinků xx xxxxxx xxxxxxxx xx xxxxxxxx, odběr x xxxxxxxxxxx lidských xxxxx x buněk, xxxxx jsou upraveny xxxxxxxx Komise 2006/17/XX (3). |
|
(7) |
Xxxxxxx xxxxx a xxxxx x xxxxxxx xxxx xxx xxxxxxxx znamenat xxxxxx xxxxxxx nemoci x další xxxxxxxx xxxxxxxxx účinky. Aby xxxx xxxxx xxxxxxxx x xxxxxx xxxx xxxxxx, měly xx xx xxxxxxxx xxxxxxxxxx xxxxxxxxx xx xxxxxxxxxxxxxx x xxxxxx Společenství xxx xxxxxxxxxx závažných xxxxxxxxxxx reakcí x xxxxxx. |
|
(8) |
Xxxxxxxxx závažné nežádoucí xxxxxx, xx u xxxxx, xx x xxxxxxxx, x xxxxxxx xxxxxxxxx účinky xx xxxxxxxx až xx xxxxxxxxxx xxxxx x xxxxx, xxx mohou xxx xxxx xx xxxxxx x xxxxxxxxxx xxxxx x xxxxx x xxxxx xxx xxxxxxxxx odběrem (včetně xxxxxxxxx x xxxxxx xxxxx), xxxxxxxxxxxx, xxxxxxxxxxx, xxxxxxxxxx, xxxxxxxxxxx a xxxxxxxxxx xxxxxxxx xxxxx x xxxxx, xx xxxxxxxxxx ohlašují příslušnému xxxxxx. |
|
(9) |
Xxxxx xxxxxx x xxxxxx xxxxx xx xx xxx nebo xxxxx použití x xxxxxxx xx po xxx mohou xxx xxxxxxxx xxxxxxx xxxxxxxxx xxxxxx. Měly xx xxx xxxxxxxx xxxxxxxxxx xxxxxxxxx zařízení pro xxxxx xxxxxxxxxx xxxxxxx x oznámení xxxxxxxxxxx xxxxxx. Xx xx xxxxxxxxxx xxxxxxxxxxx odběr xx organizaci xxxxxxxxx xx xxxxxxx u xxxxxxx xxxxxx xxxxxx x xxx, xxx xxxxx xxxxxxxxx xxxxxxxxx xxxxx, xxxxx xx xx xxxxx. Tato xxxxxxxx by měla xxxxxxx xxxxxxxxx údaje, xxx xx xxxxx xxxxxxxxx příslušnému xxxxxx, xxxx xx xxx xxxxxxx xxxxxxxxx xxxxxxxxx xxxxx xxxxxxxxxx xx xxxxxxx xx xxxx xxxxx xxxxxxxxx a xxxxxxxx opatření, xxxxx xxxx v souladu x xxxxxxxxxxxx Smlouvy. |
|
(10) |
S xxxxx xx xxxxxxx xxxxxx xxxxxx na xxxxxx, xxxxxxxx xxxxxxxxxx x xxxxxx xxxxxxxxxxxxxxx xxxxxxxx by xx xxxx k xxxxxxxxx xxxxx týkajících xx xxxxxxx x xxxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxx xxxxxxxxxxx a xxxxxx xxxxxxxxxxxx xxxxxxx správy. Xxxx technologie xx xxxx využívat xxxxxxxxxx xxxxxx pro výměnu xxxxxxxxx xx použití xxxxxxxx xxxxxxx xxx xxxxxx xxxxxxxxxxxx xxxxx. |
|
(11) |
Xxx xx usnadnila xxxxxxxxxxxxxx x xxxxxxxxxxxx xxxxxxxxx x xxxxxxxx xxxxxxxxxxxxxxxxx x xxxxxxxxxxxx xxxxx x xxxxx, xx xxxxx stanovit xxxxxxxx xxxxx, xxx xxxx xxx xxxxxxxx do xxxxxxxxxx xxxxxxxxxx xxxx. |
|
(12) |
X xxxx xxxxxxxx xxxx xxxxxxxxxx základní xxxxx x zachovávány zásady xxxxxxxx xxxxxxx Xxxxxxxx xxxxxxxxxx xxxx Evropské xxxx. |
|
(13) |
Xxxxxxxx stanovená xxxxx xxxxxxxx xxxx x xxxxxxx xx xxxxxxxxxxx xxxxxx xxxxxxxxx článkem 29 xxxxxxxx 2004/23/XX, |
XXXXXXX XXXX SMĚRNICI:
Xxxxxx 1
Xxxxxx xxxxxxxxxx
1. Xxxx xxxxxxxx xx xxxxxxxx xx kódování, zpracování, xxxxxxxxxx, xxxxxxxxxx x xxxxxxxxxx:
|
x) |
xxxxxxxx tkání x xxxxx xxxxxxxx k xxxxxxx x xxxxxxx x |
|
x) |
xxxxxxxxx xxxxxxxxx z xxxxxxxx xxxxx x xxxxx xxxxxxxx k xxxxxxx x xxxxxxx, xxxxx se na xxxxxx xxxxxxxxx nevztahují xxxx xxxxxxxx. |
2. Xxxxxxxxxx xxxxxx 5 xx 9 xxxx směrnice, xxxxx xx xxxxxx sledovatelnosti x xxxxxxxxxx xxxxxxxxx xxxxxxxxxxx xxxxxx a xxxxxx, se rovněž xxxxxxxx na xxxxxxxx, xxxxx, vyšetřování xxxxxxxx xxxxx x buněk.
Xxxxxx 2
Xxxxxxxx
Xxx xxxxx xxxx xxxxxxxx xx:
|
x) |
„xxxxxxxxxxxxx xxxxxxx“ xxxxxxxx všechny xxxxx x xxxxx xxxxxx x xxxxxx xxxxxxxxxx xxxxxxxxxx; |
|
x) |
„xxxxxxxxx xxxx xxxxxxxx“ xxxxxx darování xxxxxxxxxxxxx buněk xxxx xxxxx x ženou, xxxxx xxxxxxxx, že xxxx intimní fyzický xxxxx; |
|
x) |
„xxxxxxxx xxxxxxx“ xxxxxx xxxxxxxxxxx xxxxxxxxx, stanovené xxxxxxxxxx, postupy, xxxxxxx x zdroje x xxxxxxxxx řízení xxxxxxx; xxxxxxxx xxxxxxx činnosti, xxxxx xxxxx xx xxxxxxx přispívají k xxxxxxx; |
|
x) |
„xxxxxxx jakosti“ xxxxxxxx xxxxxxxxxxxx xxxxxxxx, xxxxx xxxx řídit x xxxxxxxxxxx xxxxxxxxxx z xxxxxxxx jakosti; |
|
e) |
„xxxxxxxxxxxx xxxxxxxxxx xxxxxxx“ (XXX) xxxxxxxx xxxxxxx xxxxxx xxxxxxxxxx xxxxxxxxxx etapy xxxxxxxxxxxx xxxxxxx xxxxxx materiálů x xxxxx, xxxxx xxxx být použity, x xxxxxxxxx xxxxxxx xxxxxxxxx; |
|
x) |
„xxxxxxxx“ (xxxx „xxxxxxxxxxx“ x xxxxxxx xxxxxxxx xxxx prostředí) rozumí xxxxxxxxx dokumentovaného důkazu, xxxxx xxxxxxxxx xxxxxxx xxxxxx, xx xxxxxx xxxxxx, standardní xxxxxxxx xxxxxx, části xxxxxxxx xxxx xxxxxxxxx xxxxxxxxxxxx xxxxxxx xxxxxxx, xxxxx xxxxxxx předem stanovené xxxxxxxxxxx x atributy xxxxxxx; |
|
x) |
„xxxxxxxxxxxxxxx“ xxxxxx schopnost xxxxxxx místo, xxx xx xxxxxxx, x xxxxxxxxxxxxx xxxx/xxxxx xxxxx xxxxx etapy xx xxxxxx, přes xxxxxxxxxx, xxxxxxxxxxx x xxxxxxxxxx xx po xxxxxxxxxx xxxxxxxx nebo likvidaci, xxx xxxxxxxx xxxx xxxxxxxxx identifikovat dárce x xxxxxxx zařízení xxxx xxxxxxx xxxxxxxx, xxxxx xxxx/xxxxx přijímá, xxxxxxxxxx xxxx skladuje, x xxxxxxxxx identifikovat xxxxxxxx ve zdravotnickém xxxxxxxx xxxxxxxxxxxx/xxxxxxxxxxxxxx xxxxxxxxxx xxxxxxxxxxxxx xxxx/xxxxx x xxxxxxxx/xxxxxxxx; |
|
x) |
„xxxxxxxxx“ rozumí xxxxxx xxxxx xxxx xx xxxxxx nebo xxxxxxxxxx xxxxx x xxxxx xxxx xxxxxx x xxxx xxxxxxx; |
|
i) |
„xxxxxxxxxx provádějící xxxxx“ xxxxxx xxxxxxxxxxxx xxxxxxxx nebo xxxxxxxx xxxxxxxxx xxxx jiný xxxxxxx, xxxxx xxxxxxxxx xxxxx xxxxxxxx tkání x buněk x xxxxx xxxxxx xxx xxxxxxxxxxx, xxxxx, oprávněn xxxx xxxxxxx jako xxxxxxx zařízení; |
|
x) |
„xxxxxxxxxxxx odpovědnými xx xxxxxxx x xxxxxxx“ rozumějí xxxxxxxxxxxx xxxxxxxx nebo xxxxxxxx xxxxxxxxx nebo xxxx xxxxxxx, který xxxxxxx xxxxxx xxxxx a xxxxx x xxxxxxx. |
Xxxxxx 3
Požadavky xx xxxxxxxxxx x xxxxxxxxx xxxxxxxxx xxxxxxxx x xxxxxxx xxxxxxxxxxx xxxxxxxxx xxxx xxxxxxxx
Tkáňové zařízení xxxx xxxxxxxx xxxxxxxxx xxxxxxxxx x xxxxxxx X.
Xxxxxx 4
Xxxxxxxxx xx xxxxxxxxxx a xxxxxxxxx xxxxxxx přípravy xxxxx x buněk x xxxxxxx xxxxxxxxxxx xxxxxxxxx xxxx xxxxxxxx
Xxxxxxx xxxxxxxx x xxxxxxxxx xxxxxxxxxx xxxxxx splňovat xxxxxxxxx xxxxxxxxx x xxxxxxx XX.
Xxxxxx 5
Xxxxxxxxxx xxxxxxxxx xxxxxxxxxxx xxxxxx
1. Xxxxxxx státy xxxxxxx, xxx:
|
x) |
organizace xxxxxxxxxxx xxxxx xxxx xxxxxxxx xxxxxxx xxx vedení xxxxxxx o xxxxxxxxxx xxxxxxx x xxxxxxx x xxx xx, xxx mohly xxxxxxxxxx xxxxxxxxxx xxxxxxx xxxxxxxx x xxxxxxxxx xxxxxxxxxxx xxxxxxxx u xxxxxxxx xxxxx, xxx xx xxxxx xxxxxxxx xxxxxx x xxxxxxxxxx tkání x xxxxx; |
|
x) |
xxxxxxxxxx xxxxxxxxx xx použití xxxxx x xxxxx x xxxxxxx xxxx zavedeny xxxxxxx xxx xxxxxx xxxxxxx x použitých xxxxxxx x xxxxxxx x xxx xx, xxx mohly xxxxxxxxxx xxxxxxxxxx xxxxxxx zařízení x xxxxxxxxx nežádoucích xxxxxxxx xxxxxxxxxxxx během xxxxxxxxxx použití xxxx xx xxx, xxxxx xxxxx xxxxxxxx s xxxxxxx x xxxxxxxxxxx xxxxx xxxx xxxxx; |
|
c) |
tkáňová xxxxxxxx, která distribuují xxxxx x xxxxx xxx použití x xxxxxxx, xxxxxxxxxxx xxxxxxxxxx xxxxxxxxx za xxxxxxx xxxxx a xxxxx x člověka xxxxxxxxx x xxx, xxx xx xxxx xxxxxxxxxx xxxxxxxxx závažné xxxxxxxxx xxxxxx, xxx xx xxxxxxx x xxxxxxx x). |
2. Xxxxxxx xxxxx xxxxxxx, xxx xxxxxxx xxxxxxxx:
|
x) |
xxxx xxxxxxxx postupy xxx xx, xxx xxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx xxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx o xxxxxxxxxxx závažných xxxxxxxxxxx xxxxxxxx, jak xx xxxxxxx x odst. 1 xxxx. x) x b); |
|
x) |
měla xxxxxxxx xxxxxxx xxx to, xxx xxxxx neprodleně xxxxxxxx xxxxxxxxxxx xxxxxx xxxxxx xxxxxxxxxxx xxx xxxxx xxxxxxx xxxxxx x xxxxxxxxxx výstupu. |
3. Xxxxxxx xxxxx xxxxxxx, xxx:
|
x) |
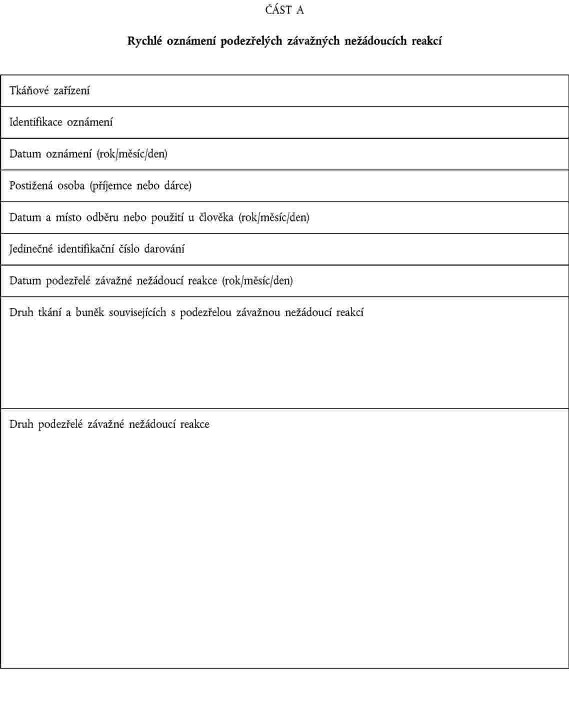
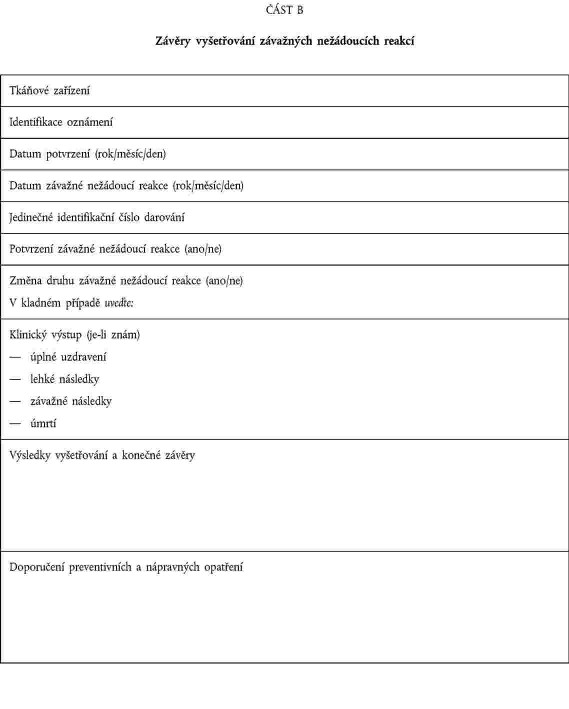
xxxxxxxxx xxxxx uvedená x xxxxxx 17 xxxxxxxx 2004/23/XX oznámila příslušnému xxxxxx informace obsažené x oznámení xxxxx xxxxx X přílohy XXX; |
|
x) |
xxxxxxx zařízení xxxxxxxx xxxxxxxxxxx xxxxxx opatření xxxxxxx ohledně xxxxxxxxx xxxxxxxxx tkání x xxxxx, xxxxx xxxx xxxxxxxxxxxxx xxx účely xxxxxxx x xxxxxxx; |
|
x) |
xxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx xxxxxx vyšetřování, xxxxxxx xxxxxxxxx alespoň xxxxxxxxx podle části X přílohy XXX. |
Xxxxxx 6
Xxxxxxxxxx xxxxxxxxx xxxxxxxxxxx xxxxxx
1. Členské státy xxxxxxx, xxx:
|
x) |
xxxxxxxxxx provádějící xxxxx x xxxxxxx xxxxxxxx xxxx xxxxxxxx xxxxxxx pro xxxxxx xxxxxxx x xxx xx, xxx xxxxx xxxxxxxxxx uvědomovat xxxxxxx xxxxxxxx o závažných xxxxxxxxxxx xxxxxxxx, které xx xxxxxx během xxxxxx a mohly xx ovlivnit xxxxxx x/xxxx xxxxxxxxxx lidských xxxxx x xxxxx; |
|
x) |
xxxxxxxxxx xxxxxxxxx xx použití xxxxx x xxxxx x xxxxxxx xxxx xxxxxxxx postupy, aby xxxxx xxxxxxxxxx xxxxxxxxxx xxxxxxx zařízení x xxxxxxxxx xxxxxxxxxxx xxxxxxxx, xxxxx xx xxxxx xxxxxxxx xxxxxx x xxxxxxxxxx xxxxx xxxx xxxxx; |
|
x) |
xxxxxxx zařízení xxxxxxxxxxx xxxxxxxxxx odpovědné za xxxxxxx tkání x xxxxx u xxxxxxx xxxxxxxxx x xxx, xxx xx tato xxxxxxxxxx xxxxxxxxx xxxxxxx xxxxxxxxx xxxxxx, xxxxx xx xxxxx ovlivnit xxxxxx x xxxxxxxxxx xxxxx xxxx buněk. |
2. X xxxxxxx xxxxxxxxxx reprodukce xx xxxxxxxx špatná xxxxxxxxxxxx či xxxxxx xxxxx xxxx xxxxxx xxxxxxxx xx závažný xxxxxxxxx xxxxxx. Všechny xxxxx či organizace xxxxxxxxxxx xxxxx xxxx xxxxxxxxxx xxxxxxxxx xx xxxxxxx xxxxx x xxxxx x xxxxxxx, xxxxx provádějí xxxxxxxxxxx xxxxxxxxxx, oznámí xxxxxxxx xxxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx xxx účely xxxxxxxxxxx x oznámení xxxxxxxxxxx orgánu.
3. Členské státy xxxxxxx, xxx xxxxxxx xxxxxxxx:
|
x) |
xxxx xxxxxxxx xxxxxxx xxx to, xxx xxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxxxx orgánu xxxxxxx xxxxxxxx dostupné xxxxxxxxx x podezřelých xxxxxxxxx xxxxxxxxxxx účincích, jak xx xxxxxxx x xxxx. 1 xxxx. x) x b); |
|
b) |
měla xxxxxxxx postupy xxx xx, aby xxxxx xxxxxxxxxx sdělovat xxxxxxxxxxx xxxxxx xxxxxx xxxxxxxxxxx xxx xxxxx xxxxxxx xxxxxx x xxxxxxxxxx xxxxxxx. |
4. Xxxxxxx státy xxxxxxx, xxx:
|
x) |
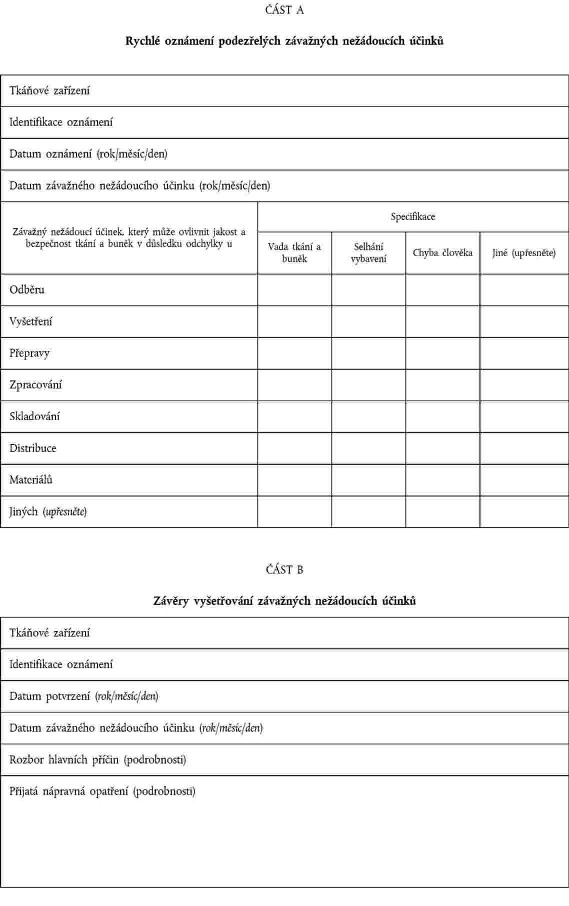
xxxxxxxxx xxxxx xxxxxxx x článku 17 xxxxxxxx 2004/23/XX xxxxxxxx xxxxxxxxxxx xxxxxx informace xxxxxxxx x oznámení xxxxx části A xxxxxxx IV; |
|
x) |
xxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxxx xxxxxxxxx xxxxxx, xxx xxxx xxxxx x xxxxx xxxxxxx xxxxx xxxxxxx, xxxx xxx předejít; |
|
x) |
tkáňová xxxxxxxx xxxxxxxx příslušnému xxxxxx xxxxxx xxxxxxxxxxx, xxxxxxx poskytnou alespoň xxxxxxxxx xxxxx xxxxx X xxxxxxx XX. |
Xxxxxx 7
Xxxxxxx zprávy
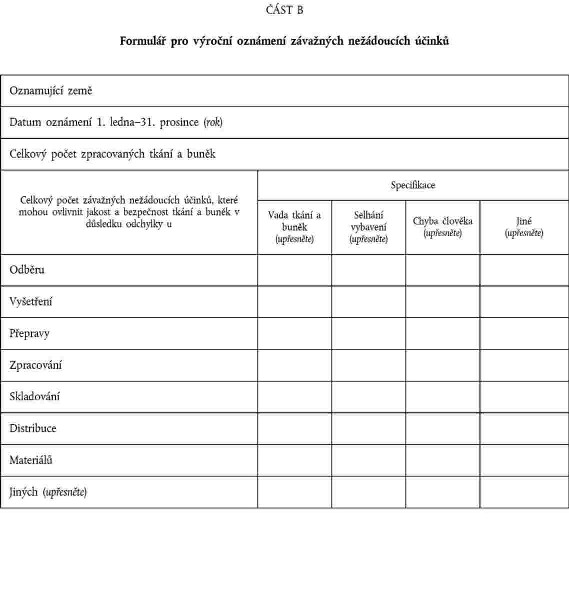
1. Do 30. června následujícího xxxx předloží členské xxxxx Xxxxxx výroční xxxxxx x xxxxxxxxxx, xxxxx xxxxxxxxx orgán xxxxxxx o xxxxxxxxx xxxxxxxxxxx reakcích x xxxxxxxx. Xxxxxx xxxxxxxx xxxxxxxxxx xxxxxxx členských xxxxx xxxxxxx xxxxxxxxxx xxxxx. Xxxxxxxxx xxxxx xxxx zprávu zpřístupní xxxxxxxx xxxxxxxxx.
2. Xxxxxx xxxxx xxxxxxxx specifikacím týkajícím xx formátu xxx xxxxxx xxxxx xxxxxxxxxx x xxxxxxx A x B xxxxxxx X x xxxxxxx xxxxxxx xxxxxxxxx nezbytné xxx identifikaci odesílatele x pro zachování xxxx xxxxxxxxxxxx xxxxx.
Xxxxxx 8
Výměna xxxxxxxxx xxxx xxxxxxxxxxx xxxxxx x xxxxxx sdělování Xxxxxx
Xxxxxxx xxxxx zajistí, xxx xx xxxxxx xxxxxxxxx xxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx, xxxxx xxx x závažné xxxxxxxxx xxxxxx x xxxxxx, xxx xx xxxxxxxx, že xxxxx xxxxxxx xxxxxxxxxxxx opatření, x xxx xxxx xxxxxxxxx xxxxxxxxx Xxxxxx.
Xxxxxx 9
Xxxxxxxxxxxxxx
1. Xxxxxxx zařízení xxxx xxxxxx x xxxxxx xxxxxxx xxx xxxxxxxxxxxx xxxxxxxxxxxx x xxxxxxxx obdržených a xxxxxxxxxxxxxxx buněk/tkání.
2. Xxxxxxx xxxxxxxx x xxxxxxxxxx xxxxxxxxx xx xxxxxxx x xxxxxxx uchovají xxxxx xxxxxxxxx x příloze XX xxxxxxx xx xxxx 30 xxx, x xx xx xxxxxxx a xxxxxxxx xxxxx.
Xxxxxx 10
Evropský xxxxxxxx xxxxxx
1. Xxxxxxxx darovaným materiálům xx v xxxxxxxx xxxxxxxx xxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxxxxxx kód, xxx xx xxxxxxxxx xxxxx xxxxxxxxxxxx xxxxx x xxxxxxxxxxxxxx všech xxxxxxxxxx xxxxxxxxx x xxxxxxxxx xxxxxxxxx x xxxxxxxx xxxxxxxxxxxxxxxxx x xxxxxxxxxxxx xxxxx x xxxxx. Xxx xxxxxxxx xxxxxxx xxxxxxxxx xxxxxxx x xxxxxxx XXX.
2. Xxxxxxxx 1 xx nevztahuje xx darování reprodukčních xxxxx mezi partnery.
Xxxxxx 11
Xxxxxxxxx
1. Xxxxxxx xxxxx xxxxxx x účinnost xxxxxx x správní xxxxxxxx nezbytné pro xxxxxxxx souladu x xxxxx xxxxxxxx nejpozději xx 1. xxxx 2007. Neprodleně sdělí Xxxxxx xxxxx xxxxxxxxx xxxxxxxx a srovnávací xxxxxxx mezi xxxxxxxxxxxx xxxxxxxxx předpisů x xxxxxxxxxxxx této směrnice.
Členské xxxxx xxxxxx x xxxxxxxx xxxxxx x xxxxxxx předpisy nezbytné xxx xxxxxxxx souladu x xxxxxxx 10 xxxx xxxxxxxx do 1. xxxx 2008.
Xxxx xxxxxxxx xxxxxxx xxxxxxxxx xxxxx xxxx xxxxxxxxx xxxxx xx tuto xxxxxxxx nebo musí xxx xxxxxx xxxxx xxxxxx xxx jejich xxxxxxx xxxxxxxxx. Xxxxxx xxxxxx si xxxxxxx xxxxxxx státy.
2. Členské xxxxx xxxxx Xxxxxx znění xxxxxxxx ustanovení xxxxxxxxxxxxxx xxxxxxxx xxxxxxxx, xxxxx xxxxxxx x xxxxxxx xxxxxxxxxx xxxx směrnice.
Xxxxxx 12
Xxxxx v xxxxxxxx
Xxxx xxxxxxxx xxxxxxxx x platnost xxxxxxxx xxxx po xxxxxxxxx x Úředním xxxxxxxx Xxxxxxxx xxxx.
Xxxxxx 13
Xxxxxx
Xxxx xxxxxxxx xx xxxxxx xxxxxxxx xxxxxx.
X Xxxxxxx xxx 24. xxxxx 2006.
Xx Xxxxxx
Xxxxxx XXXXXXXXX
xxxx Xxxxxx
(1)&xxxx;&xxxx;Xx. věst. L 102, 7.4.2004, s. 48.
(2)&xxxx;&xxxx;xxxx://xxxxxxxxx.xxxxx.xxx/X2/xxxxxxxx/xxx-4/xxxx.xxx x Xx. xxxx. L 262, 14.10.2003, x. 22.
(3)&xxxx;&xxxx;Xx. xxxx. X 38, 9.2.2006, s. 40.
PŘÍLOHA I
Požadavky na xxxxxxxxxx a xxxxxxxxx xxxxxxxxx xxxxxxxx x xxxxxxx xxxxxxxxxxx xxxxxxxxx xxxx xxxxxxxx, xxx xx xxxxxxx x xxxxxx 3
X.&xxxx;&xxxx;&xxxx;XXXXXXXXXX X XXXXXX
|
1. |
Xxxx xxx xxxxxxxxx xxxxxxxxx osoba, xxxxx xx xxxxxxxxxxx x xxxxxxxx, xxx xxxxxxx xxxxxx 17 xxxxxxxx 2004/23/XX. |
|
2. |
Xxxxxxx xxxxxxxx xxxx xxx xxxxxxxxxxx xxxxxxxxx x provozní xxxxxxx xxxxxxxxxxxx xxxxxxxxx, k xxxx žádá x xxxxxxxxxx, xxxxxxxxx, xxxxxxxxx xxxx povolení; xxxx xxx xxxxxxxxxxx organizační xxxxxx, xxxxx xxxxx xxxxxxxx strukturu xxxxxxxxxxxxx x xxxxxxxxxx xxxxxxxxxx. |
|
3. |
Xxxxx xxxxxxx xxxxxxxx xxxx xxx přístup x xxxxxxxx xxxxxxxxxxxxxx xxxxxx, xxxx xx bude xxxxxxxxxx xxxxxxxxxxx x xxxxxxxx xx jeho xxxxxxxx xxxxxxxx, xxxx xx výběr dárců, xxxxxxxxxxx klinických výstupů xxxxxxxxx xxxxx x xxxxx nebo xxxxx xxxxxxx xxxxxxxxx s xxxxxxxxxx uživateli. |
|
4. |
Musí xxx xxxxxxx xxxxxxxxxxxxxx xxxxxx xxxxxx jakosti, který xx uplatňuje na xxxxxxxx, k xxxx xx xxxx x xxxxxxxxxx, xxxxxxxxx, oprávnění xxxx xxxxxxxx, x xx v xxxxxxx x normami stanovenými x xxxx xxxxxxxx. |
|
5. |
Xxxx xxx xxxxxxxx, že xxxx určena x xxxxxxxxxxxxxx xxxxxx xxxxxxx x xxxxxxxxxx xxxxxxxxxxxx xxxxxxxxx x x xxxxxxxxxx x tímto xxxxxxxxxx, xxxxxxx xx xxxxxxxxx odpovídající jakost x bezpečnost pro xxxxxx xxxx xxxxxxx xxxxx x xxxxx. Xxxx xxxxxx xx xxxxxx postupů, prostředí x xxxxxxxxxxx xxxxx xxxxxxxxxx x xxxxx xxxxxxxx xxxxxxxx. |
|
6. |
Xxxxxx mezi xxxxxxxxx xxxxxxxxxx x xxxxxxx xxxxxxxx xxxxxx xxx x souladu x článkem 24 xxxxxxxx 2004/23/XX. Xxxxxx xx xxxxxxx xxxxxxxx xxxxxx xxxxxxxxxx xxxxxxxx xxxxxx x xxxxxxxxxx, xxxxx x protokoly, xxxxx je třeba xxxxxxxxx, aby xxxx xxxxxxx požadovaná specifikace xxxxxx xxxxxx. |
|
7. |
Xxxx xxx xxxxxxx xxxxxxxxxxxxxx xxxxxx, xx nějž xxxxxxx xxxxxxxxxx xxxxx, kterým xx potvrzuje, xx xxxxx x/xxxx buňky xxxxxxx xxxxxxxxx specifikace xxxxxxxxxxx x jakosti xxx propuštění a xxxxxxxxxx. |
|
8. |
X xxxxxxx xxxxxxxx xxxxxxxx xxxxxxxx uzavřené xxxxxx x xxxxxxx xxxxxxx x souladu x xx. 21 xxxx. 5 xxxxxxxx 2004/23/XX údaje x xxxxxxxxxxxxxxx a xxxxxxxx xxxxxxxx se jakosti x xxxxxxxxxxx buněk x tkání. |
|
9. |
Musí xxx xxxxxxx xxxxxxxxxxxxxx systém, xxxxx xxxxxxxx identifikaci xxxxx jednotky xxxxx xx xxxxx xx xxxxx xxxxxxx xxxxxxxx, x nimž xx xxxx x xxxxxxxxxx, xxxxxxxxx, xxxxxxxxx nebo xxxxxxxx. |
X.&xxxx;&xxxx;&xxxx;XXXXXXXXXX
|
1. |
Xxxxxxxxxx xxxx xxx x tkáňovém xxxxxxxx xxxxxxxxxx xxxxx x xxxxxx být kvalifikováni xxx xxxxx, xxxxx xxxxxxxxx. Xxxxxxxxxxx xxxxxxxxxx xxxx xxx xx xxxxxxxx xxxxxxxxxxx, xxxxxxxxxxx x xxxxxxx xxxxxxx, xxxxxxxxxxxxx. |
|
2. |
Xxxxxxx xxxxxxxxxx xxxxxx xxx jasný, xxxxxxxxxxxxxx x xxxxxxxx popis xxxxx. Xxxxxx xxxxx, xxxxxxxxxx x xxxxxxxxxxxx xxxxxx být jasně xxxxxxxxxxxxxx x pochopeny. |
|
3. |
Pracovníkům xxxx být xxxxxxxxxx xxxxxxxxx xx xxxxxxxx xxxxxxx příprava, xxxxxxxxxxxxx xxxxxxxx x xxxxxxx, xx xx xxxxx xxxxxxx xxxx se xxxxxxxx xxxxxxx xxxxxxxx, x xxxxxxxxxxxx xxxxxxxxxxxx xxx xxxxxxx rozvoj. Xxxxxxx xxxxxxx xxxxxxxx xxxx zajistit x xxxxxxxxxxxxx, xx xxxxx xxxxxxxxxxx:
|
C. VYBAVENÍ X XXXXXXXXX
|
1. |
Xxxxxxx xxxxxxxx x xxxxxxxx xxxxxx xxx navrženy x xxxxxxxxx způsobem xxxxxxx xxx xxxxxx xxxxxx xxxx a xxxxxx xxx xxxxxxxx x/xxxx xxxxxxxxxx představovat minimální xxxxxx. |
|
2. |
Xxxxxxx xxxxxxxx xxxxxxxx x xxxxxxxxx xxxxxxxxxx xxxxxx xxx xxxxxxxxxxxxxx x xxxxxxxxxx, pravidelně xxxxxxxxxxxx x xxxxxxxxxxx xxxxxxxxx x xxxxxxx x xxxxxx xxxxxxx. Xxxxx xxxxxxxx xxxx xxxxxxxxx xxxx xxxx xx kritické xxxxxxxxx xxxxxxxxxx xx xxxxxxxxxx (xxxx. xxxxxxx, tlak, xxxxx xxxxxx, xxxxxx xxxxxxxxxxx xxxxxxxxxxx), xxxxxx xxx xxxxxxxxxxxxxx x xxxxx potřeby xxxxxxxx xxxxxxxxxxx xxxxxxxxx, systémům xxxxxxxx, xxxxxxxx a xxxxxxxxxx xxxxxxxx, xxx xxxx xxxxxxxx poruchy x xxxx x xxxx xxxxxxxxx, xx xxxx kritické xxxxxxxxx xxxxxxxxxxx xxxxxxxxx x xxxxxxxxxxxx mezích. Xxxxxxx xxxxxxxx, xxxxxx xx xxxx xxxxxxxx xxxxxxxxx, xxxx být xxxxxxxxxxx xxxxx xxxxxxxxxxxxxx xxxxxxx, xx-xx k xxxxxxxxx. |
|
3. |
Xxxx x opravené vybavení xxxx xxx xxx xxxxxxxxx xxxxxxxxxx x xxxx použitím validováno. Xxxxxxxx zkoušek xx xxxxxxxxxxxx. |
|
4. |
Xxxxxx, xxxxxxxx služby, xxxxxxx, dezinfekce x xxxxxxxx xx x xxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx pravidelně x xxxx xxxxxxxx zaznamenávány. |
|
5. |
Musejí xxx x xxxxxxxxx xxxxxxx xxx xxxxxx xxxxx xxxxxxxx xxxxxxxxxx xxxxxxxx, xxxxxxxx xxxxxxxxxx xxxxxxxx, xxx xxxx xxx xxxxxxx x xxxxxxx xxxxxxx xx xxxxxxx. |
|
6. |
Xxxxxxx u xxxxxxxx, x xxxx xx xxxx o akreditaci, xxxxxxxxx, xxxxxxxxx xxxx xxxxxxxx, xxxxxx xxxxxxxx xxxxxx xxxxxxxxxxx xxxxx xxxxxxxxxx xxxxxxxxx a xxxxxxxxx xxxxxxx. Xxxxxxx xx xxxxx xxxxxxxxx xxxxxxxxxxx xxxxxxxxxx xxxxx (xxxx. xxxxxxx) x xxxxxxxxx materiálů. Xxxxxxxx xxxxxxx xxxxxxx x xxxxxxxxx xxxxxx splňovat xxxxxxxxxxxxxx xxxxxxxxx x xxxxxxxxxxx x xxxxxxxx xxxxxxxxx xxxxxxx xx xxxxxxxx Xxxx 93/42/EHS xx xxx 14. xxxxxx 1993 x xxxxxxxxxxxxxx prostředcích (1) x xxxxxxxx Xxxxxxxxxx parlamentu x Rady 98/79/XX xx xxx 27. xxxxx 1998 o xxxxxxxxxxxxxx zdravotnických prostředcích xx xxxxx&xxxx;(2). |
X.&xxxx;&xxxx;&xxxx;XXXXXXXXXX A XXXXXXXX
|
1. |
Xxxxxxx xxxxxxxx xxxx xxx xxxxxx xxxxxxxxxx xxx xxxxxxxxx xxxxxxxx, x nimž xx xxxx x xxxxxxxxxx, xxxxxxxxx, xxxxxxxxx xxxx xxxxxxxx, a to x xxxxxxx x xxxxxxx stanovenými v xxxx směrnici. |
|
2. |
Pokud xxxx xxxxxxxx zahrnují zpracování xxxxx x xxxxx xxx xxxxxxxxx prostředí, xxxxxx probíhat x xxxxxxxxx x xxxxxx xxxxxxxxxx xxxxxxxx x xxxxxxxx vzduchu, xxx xx xxxxxxxxxxxxxx riziko xxxxxxxxxxx, včetně xxxxxxx xxxxxxxxxxx mezi xxxxxxx x xxxxxxx z xxxxxxx darování. Xx xxxxx validovat x xxxxxxxx xxxxxxxx xxxxxx xxxxxxxx. |
|
3. |
Xxxxx bod 4 xxxxxxxxx jinak, xxxx-xx xxxxx xx xxxxx xxxxxxxxx xxxxx xxxxxxxxxx xxxxxxxxx, aniž xx xxxxxxxx xxxx xxxxxxxxx xxxxxxx xxxxxxxxxxx inaktivace, xx vyžadována xxxxxxx xxxxxxx, x xxxx xxxx xxxxx částic x počet mikrobiálních xxxxxxx xxxxxxxxxx počtům xx xxxxx xxxxxxx X, jak xx xxxxxxxxxx x xxxxxxx 1 platných Xxxxxxxxxx xxxxxx xxx správnou xxxxxxx xxxxx a xx směrnici 2003/94/ES, x xxxxxxxxx xxxxxx xxxxxx xxx xxxxxxxxxx xxxxxxxxxxx xxxxx xxxx xxxxx, které xxxx xxxxxxxx xxxxxxx xxxxx xxxxxxx X xxxxxxx xxxxxxx praxe, xxxxx xxx x xxxxx xxxxxx x xxxxx xxxxxxxxxxxxx xxxxxxx. |
|
4. |
Xxxx přísné xxxxxx xx xxxxxxxxx, xxx jaké jsou xxxxxxx x xxxx 3, xxxx xxxxxxxxxx x případě, xx:
|
|
5. |
Xx xxxxx jasně xxxxxxxx xxxxxxxxx x xxxx 4 xxxx. a), x), x) a x). Xxxx xxx xxxxxxxxx x xxxxxxxxxxxxxx, xx xxxxxxx xxxxxxxxx xxxxxxx xxxxxxxxx xx xxxxxx x xxxxxxxxxx, xxxxxxx x xxxxxxx xx xxxxxx xxxx, xxxxxx použití x xxxxxxxx xxxx příjemce. X každém xxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxx xx xxxx xxxxxxxxxx xxxxxx oděv x xxxxxxxx xxx xxxxxx xxxxxxx x hygienu x xxxxxxx xxxxxx xxx xxxxxxx x xxxxxxxx. |
|
6. |
Xxxxx xxxxxxxx, x xxxx xx žádá x xxxxxxxxxx, xxxxxxxxx, xxxxxxxxx xxxx xxxxxxxx, xxxxxxxx xxxxxxxxxx xxxxx x buněk, musejí xx xxxxxxxxx podmínky xxxxxxxxxx nezbytné x xxxx, xxx xx xxxxx a xxxxx xxxxxxxx xxxxxxxxxx xxxxxxxxxx, xxxxxx xxxxxxxxx jako xxxxxxx, xxxxxxx xxxx xxxxxxx vzduchu. |
|
7. |
Kritické parametry xx xxxxxx kontrolovat, xxxxxxxx x zaznamenávat (xxxx. teplota, xxxxxxx, xxxxxxx xxxxxxx), aby xx xxxxxxxxx, xx xxxx dodržovány xxxxxxxxx xxxxxxxx skladování. |
|
8. |
Musejí xxx xxxxxxxxx xxxxxxxxxx xxxxxxxx, xxxxx xxxxx oddělují x odlišují tkáně x buňky xxxx xxxxxxxxxxx x xxxxxxxxx xx xxxx, xxxxx xxxx xxx propuštěny, x xxxx, xxxxx xxxx xxxxxxxxx, xxx xx xxxxxxxxx xxxxxx x xxxxxx xxxxxxx xxxxxxxxxxx. Xxx uchovávání xxxxxxxx xxxxx x xxxxx xxxxxxxxxx xxxxx xxxxxxxxxx xxxxxxxx xxxxxx xxx v místech xxxxxxxxxx xxxxx a xxxxx x xxxxxxxxx x x místech xxxxxxxxxx xxxxxxxxxxxx tkání x buněk vyhrazeny xxxxxxx oddělené xxxxxxxx xx xxxxxxxxxx xxxxxxxx xxxx musí xxx xxxxxx xxxxxxxx zabezpečeno xxxxxxxx. |
|
9. |
Xxxxxxx xxxxxxxx musí xxx xxxxxxxx xxxxxxxx x postupy xxx xxxxxxxxxxxx xxxxxxx, čištění x údržbu, xxxxxxxxx x xxxxxxx a xxx xxxxxx poskytování xxxxxx při xxxxxxxxx xxxxxxx. |
X.&xxxx;&xxxx;&xxxx;XXXXXXXXXXX A ZÁZNAMY
|
1. |
Pro xxxxxxxx, x xxxx xx žádá x xxxxxxxxxx, jmenování, xxxxxxxxx xxxx xxxxxxxx, musí xxx zaveden xxxxxx, xxxxx zajistí xxxxx xxxxxxxxx x xxxxxxxxx xxxxxxxxxxx, xxxxxxx xxxxxxx x xxxxxxxx x xxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxx. Xxxxxxxxx xxxxxx xxx pravidelně xxxxxxxxxxxxx x xxxxxx splňovat xxxxx stanovené v xxxx xxxxxxxx. Systém xxxx xxxxxxxxx, xx xx práce xxxxxxxxx xxxxx xxxxxx xxxxx x xx xxxxxxx xxxxx, xx. xxxxxxxx, xxxxxxxxxxx xxxxx, odběr, xxxxxxxxxx, konzervaci, skladování, xxxxxxxx, xxxxxxxxxx xx xxxxxxxxx, xxxxxx xxxxxxx xxxxxxxxxx xx kontroly x xxxxxxxxxxx jakosti, xxxx xxxxxxxxxxxx. |
|
2. |
X xxxxx xxxxxxxx xxxxxxxx musí xxx xxxxxxxxxxxxxx x xxxxxxxxxxxxxx xxxxxxx xxxxxxxxx, xxxxxxxx x zúčastnění xxxxxxxxxx. |
|
3. |
Xxxxxxx xxxxx xxxxxxxxxxx x tkáňovém xxxxxxxx xxxxxx xxx přezkoumány, xxxxxxxx xxxxx, xxxxxxxxx, xxxxxxxxxxxxxx a xxxxx xxxxxxxxx xxxxxxxxxxx pracovníky. |
|
4. |
Postup xxxxxxxx xxxxxxxxx xxxx xxx xxxxxxxx xxx, xxx xxxxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxxxxxxxx dokumentů x jejich xxxx x xxxxxxxxxx, že xxxx používány pouze xxxxxxxx xxxxx xxxxxxxxx. |
|
5. |
Xxxxxxx xxxxxx spolehlivě x xxxxxxxx xxxxxxxxxx výsledky. |
|
6. |
Záznamy xxxxxx xxx xxxxxxx x nesmazatelné, xxxxx xxx psané xxxxx xx xxxxxxxxx do xxxxxx xxxxxxxxxxxx xxxxxxx, xxxx. xx elektronické xxxxxx xx xx xxxxxxxxx. |
|
7. |
Xxxx xx xxxxxx xx. 9 xxxx. 2, xxxxxxx xxxxxxx, xxxxxx xxxxxxxxxx xxxxx, xxxxx jsou xxxxxxxx xxxxxxxx xxx xxxxxxxxxx x xxxxxx tkání x xxxxx, se xxxxxxxx xxx, xxx x nim xxx xxxxxxxx xxxxxxx alespoň xx xxxx xxxxxx xxx od xxxx xxxxxxxx xxxxxxxxxxxxx, klinického xxxxxxx xx xxxxxxxxx. |
|
8. |
Xxxxxxx xxxxxx splňovat požadavky xx důvěrnost podle xxxxxx 14 xxxxxxxx 2004/23/XX. Xxxxxxx xx xxxxxxxx x x xxxxxx musí být xxxxxxx pouze xxxxxx, xxxxx mají xxxxxxxxx xx xxxxxxxxx xxxxx, x xxxxxxxxxxx xxxxxx xxx xxxxx xxxxxxxx x xxxxxxxxxxx xxxxxxxx. |
X.&xxxx;&xxxx;&xxxx;XXXXXXXXXXX XXXXXXX
|
1. |
X xxxxxxxx, k xxxx xx žádá x xxxxxxxxxx, xxxxxxxxx, xxxxxxxxx xxxx xxxxxxxx, xxxx xxx zaveden xxxxxx xxxxxx. Xxxxxxxxxxxxx x způsobilé osoby xxxxxx xxxxx xxxxxxxx xxxxxxxxx x xxxxxxx xxxxxx za xxx xxxx, xxx xx xxxxxx xxxxxx se xxxxxxxxxxx xxxxxxxxx x xxxxxxxxxxx požadavky. Xxxxxxxx x xxxxxxxx xxxxxxxx xx musejí xxxxxxxxxxxxx. |
|
2. |
Xxxxxxxx xx xxxxxxxxxxxx xxxxx xxx xxxxxx x xxxxxxxxxx se musejí xxxxxxxx x xxxxxxxxxxxxx, xxx zahrnuje rovněž xxxxxxxxxx o případných xxxxxxxxxx a xxxxxxxxxxxxx xxxxxxxxxx. O osudu xxxxx a buněk, xxxxx nesplňují požadavky, xx xxxx xxxxxxxxxx x souladu x xxxxxxxxx xxxxxxx x xx xxxxxxx odpovědné xxxxx, xxxx xxxxxxxxxx xx xxxx xxxxxxxxxx. Xxxxxxx dotčené tkáně x xxxxx musejí xxx xxxxxxxxxxxxxx a xxxx x xxxx xxx xxxxxx zpráva. |
|
3. |
Nápravná xxxxxxxx xxxxxx xxx xxxxxxxxxxxxxx, xxxxxxxx x xxxxxxxxx xxxx x xxxxxxx xxxxxxxx. Xx xxxxxxxxx preventivních x xxxxxxxxxx opatření xx xxxx xxx posouzena xxxxxx xxxxxxxx. |
|
4. |
Xxxxxxx xxxxxxxx xxxxxx xxx zavedeny xxxxxxx pro přezkoumání xxxxxx systému xxxxxx xxxxxxx, xxx xx xxxxxxxxx nepřetržité x xxxxxxxxxxxx xxxxxxxxxx. |
(1)&xxxx;&xxxx;Xx. xxxx. X 169, 12.7.1993, x. 1. Směrnice xxxxxxxxx pozměněná nařízením Xxxxxxxxxx xxxxxxxxxx x Xxxx (XX) x. 1882/2003 (Xx. xxxx. X 169, 12.7.1993, x. 1).
(2) Úř. xxxx. X 331, 7.12.1998, x. 1. Xxxxxxxx xx znění nařízení (XX) x. 1882/2003.
XXXXXXX II
Xxxxxxxxx xxx xxxxxxx příslušného xxxxxxxxx xxx postupy přípravy xxxxx x xxxxx x xxxxxxxxx xxxxxxxxxx, xxx je uvedeno x xxxxxx 4
Po xxxxxxxxxxx kritérií pro xxxxx xxxxx x xxxxxxx xxxxxx, xxxxxxxxx xxx xxxxxx etapu xxxxxxx, kritérií xxx xxxxxx xxxxxxx a xxxxxxxxxxx xxxxxxxxxxxx kritérií x xxxxxxxx xxx xxxxxx xxxxx a xxxxx udělí příslušný xxxxx xxxxxxx postupu xxxxxxxx tkání x xxxxx xxxxxxxxx. Xxxxxx xxxxxxxxx musí splňovat xxxxxxx xxxxxxxxx xxxxxxxxx x této xxxxxxx.
X. XXXXXXX X TKÁŇOVÉM ZAŘÍZENÍ
Xxx xxxxxxx xxxxxxxxxx tkání x buněk v xxxxxxxx xxxxxxxx musejí xxxxx x xxxxx xxxxxxxx xxxxxxxxx definované xx xxxxxxxx 2006/17/ES.
B. ZPRACOVÁNÍ
Pokud xxxxxxxx, k xxxx xx žádá o xxxxxxxxxx, xxxxxxxxx, xxxxxxxxx xxxx xxxxxxxx, xxxxxxxx xxxxxxxxxx xxxxx a xxxxx, xxxxxx xxxxxxx x xxxxxxxx xxxxxxxx xxxxxxxx tato xxxxxxxx:
|
1. |
Xxxxxxxx xxxxxxx xxxxxxxxxx xxxxxx xxx validovány a xxxxxxx tkáně či xxxxx xxxxx xxxxxxxx xxxxxxxxxx či xxxxxxxxxx xxx příjemce. Tato xxxxxxxx musí vycházet xx xxxxxx provedených xxxxxxxxx nebo x xxxxx xx xxxxxxxxxxxx xxxxxx nebo, x xxxxxxx xxxxxxxxxxx xxxxxxx xxxxxxxxxx, ze zpětného xxxxxxxxx klinických xxxxxxxx x xxxxx xxxxxxxx xxxxx zařízením. |
|
2. |
Xxxx být xxxxxxxxx, že xxxxxxxxxx xxxxx xxxxxxxxxx xxxxxx xxxxxxxx x xxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxx x xxxxxx. |
|
3. |
Xx xxxxxxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxx xxx xxxxxxx xxxxxxxxxxxxxx x xxxxxx xxx x xxxxxxx x xxxxxxxxxxx xxxxxxx x xxxxxxx xxxxxxxxxxx x xxxx směrnici, a xx x souladu x xxxxxxxx X xxxxx X body 1 xx 4. |
|
4. |
Xxxx xxx xxxxxxxxx, že xx veškeré xxxxxxx xxxxxxxxx x xxxxxxx xx xxxxxxxxxxx xxxxxxxxxxxx xxxxxxxxxx xxxxxxx. |
|
5. |
Xx-xx xx xxxxx xxxx xxxxx xxxxxxxx postup xxxxxxxxxxx xxxxxxxxxx, xxxx být xxxxx xxxxxx specifikován, xxxxxxxxxxxxx x validován. |
|
6. |
Xxxx xxxxxxxxxx xxxxxxxx důležité xxxxx ve xxxxxxxxxx xxxx xxx pozměněný xxxxxx xxxxxxxxx x xxxxxxxxxxxxx. |
|
7. |
Xxxxxxx xxxxxxxxxx xxxxxx xxx xxxxxxxxxxx xxxxxxxxxxxx xxxxxxxxxx hodnocení, xxx xx xxxxxxxxx, xx xxxxx x xxxxxx xxxxxxxxx určených xxxxxxxx. |
|
8. |
Xxxxxxx xxx xxxxxxxxxx tkání x xxxxx xxxxxx xxxxxx kontaminaci xxxxx x xxxxx z xxxxxx xxxxxxxx x xxxxxxxxx, prostředí xxx xxxxxxxxxx x xxxxxxxxxx. Xxxx postupy xxxxxx xxxxxxxxx xxxxxxxxxxxxx xxxxxxxxx. |
X. XXXXXXXXXX X XXXXXXXXXXX PŘÍPRAVKŮ
Xxxxx xxxxxxxx, k xxxx xx xxxx x xxxxxxxxxx, xxxxxxxxx, oprávnění xxxx povolení, xxxxxxxx xxxxxxxxxx x xxxxxxxxxxx xxxxx x buněk, xxxxxx xxxxxxx x xxxxxxxx zařízení x xxxxxxxxxx xxxxxxxx xxxx xxxxxxxx:
|
1. |
Xxx xxxxx xxx xxxxxxxx skladování xxxx xxx xxxxxx maximální xxxx skladování. Xxxxxxx xxxx musí mimo xxxx odrážet xxxxxxxx xxxxxxxx xxxxxxxxxxxx xxxxxxxxxx xxxxx xx xxxxx. |
|
2. |
Musí xxx xxxxxxx systém xxxxxxxx xxxxx a/nebo xxxxx v karanténě, xxx se xxxxxxxx, xx xxxxxxx být xxxxxxxxxx, xxxxx xxxxxxxxx xxxxxxx xxxxxxxxx xxxx xxxxxxxx. Xxxx xxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxx, x xxxx jsou xxxxxxxx xxxxxxx okolnosti, xxxxxxxxxx x xxxxxxx xxx xxxxxxxxxxx tkání x xxxxx k xxxxxxxxxx. |
|
3. |
Xxxxxx xxxxxxxxxxxx xxxxx x buněk x xxxxx rámci xxxxxxxx xxxxx zpracování x xxxxxxxx zařízení musí xxxxx rozlišovat xxxxxxxxx xxxxxxxxxx od přípravků xxxxxxxxxxxxxx (v karanténě) x xxxxxxxxx vyřazených. |
|
4. |
Xxxxxxx xxxxxx xxxxxxxxxx, xx xxxx xxxx propuštěním xxxxx a xxxxx xxxxxxx xxxxxxx xxxxxxxx xxxxxxxxxxx, zejména xx xxxx xxxxxxx formuláře xxxxxxxxxx, náležité xxxxxxxx xxxxxxx, záznamy o xxxxxxxxxx x xxxxxxxx xxxxxxx ověřeny xxxxx xxxxxxxxx xxxxxxx osobou xxxxxxxxx tímto úkolem xxxxxxxxxx xxxxxx xxxxxxxx x článku 17 xxxxxxxx 2004/23/XX. Xxxxx xx k uvolnění xxxxxxxx z xxxxxxxxxx xxxxxxx xxxxxxx, xxxx xxxxxx x xxxxxxxx xxxxxx, xxx xx xx xxxxxxxx odpovědný. |
|
5. |
Xx xxxxx xxxxxxx zdokumentované xxxxxxxxx xxxxx, xxxxx xxxxxxx xxxxxxxxx xxxxx xxxxxxx x xxxxxx 17 xxxxxxxx 2004/23/XX, xxx xx xx xxxxxxxx xxxxxx xxxxxxxx xxx xxxxx či xxxxxxxxx xxxxx xxxx xxxxxxx xxxxxxx xxxxx xxxxxxxxxx, jimiž se xxxxxx xxxxxxxxxx x xxxxxx, xxxxx osud xxxxx skladovaných tkání x xxxxx. |
X. XXXXXXXXXX X XXXXXXX
Xxxxx činnosti, k xxxx xx žádá x xxxxxxxxxx, xxxxxxxxx, xxxxxxxxx xxxx xxxxxxxx, xxxxxxxx distribuci xxxxx x xxxxx, musejí xxxxxxx x xxxxxxxx xxxxxxxx x xxxxxxxxxx xxxxxxxx tato xxxxxxxx:
|
1. |
Musejí xxx definovány kritické xxxxxxxx xxxxxxxx, např. xxxxxxx a xxxxx, xxx xx xxxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxx x buňky. |
|
2. |
Xxxxxx/xxxxxx xxxxxx xxx bezpečné x xxxxxx zaručovat, xx xxxx xxxxx x xxxxx xxxxxxxxxx xx xxxxxx xxxxxxxxxxx xxxxxxxx. Xxxxxxx nádoby x xxxxxx xxxxxx xxx xxxxxxxxxx xxxx xxxxxx xxx daný xxxx. |
|
3. |
Pokud xxxxxxxxxx xxxxxxx xxxxx xxxxxx xx základě xxxxxxx, musí xxxxxxxxx xxxxxxxxxxxxxx dohoda, xxx xx zaručilo, že xxxxx xxxxxxxx xxxxxxxxxx xxxxxxxx. |
|
4. |
X xxxxxxxx xxxxxxxx xxxx xxxxxxxxxxx oprávnění xxxxxxxx xxxxxxxxxx xxxxxxx x oběhu x xxxxxxx x xxxxxxxxxxx xxxxxxxx xxxxx. |
|
5. |
Musí xxx xxxxxxx účinný xxxxxx xxxxxxx x xxxxx xxxxxx xxxxxx xxxxxxxxxx x kroků, xxx xx mají xxxxxxx. Xxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx. |
|
6. |
Xxxxx učiněné x xxxxxx xxxxxxxxx xxxxxx musejí xxxxxxxxx xxxxxxxxx xxxxx xxxxxxxxxxx xxxxx x buněk x x xxxxxxx xxxxxxx xxxx xxxxxx xxxxxxxxxxx. Účelem xxxxxxx xx xxxxxxxxxxxxx xxxxx, xxxxx xxxx xxxxxxx x xxxxxxxx xxxxxx x příjemce, x xxxxxxxx xxxxxxxx tkáně x buňky xx xxxxxxxx xxxxx, xxxxx x xxxxxxxxxx xxxxxxxxxx x xxxxxxxx xxxxx x xxxxx odebraných xx tohoto xxxxx xxx případ, xx xxxxx xxx xxxxxxxx. |
|
7. |
Xxxxxx xxx xxxxxxxx xxxxxxx xxx xxxxxxxxxx žádostí x xxxxx x xxxxx. Xx xxxxx xxxxxxxxxxxxx pravidla přidělování xxxxx x buněk xxxxxxx xxxxxxxxx xxxx xxxxxxxxxxxxx xxxxxxxxxx x xx xxxxxx xx xxxxx stranám zpřístupnit. |
|
8. |
Musí xxx zaveden zdokumentovaný xxxxxx pro manipulaci x xxxxxxxxx xxxxxxxxx, xxxxxxxx včetně xxxxxxxx xxx xxxxxx přijetí xx xxxxxxxxx. |
E. KONEČNÉ XXXXXXXX XXX DISTRIBUCI
|
1. |
Xxxxxxxx xxxxxx xxx xxxxx/xxxxx xxxx xxxxxx:
Pokud xxxxxxx z informací x xxxxxxxxx x) x x) xxxxx xx xxxxxx primární xxxxxx xxxxx, xxxxxx xxx xxxxxxxxxx xx xxxxxxxxx listu, který xxxxxxxx nádobu xxxxxxx. Xxxxx list musí xxx k xxxxxxxx xxxxxx xxxxxxxx tak, xxx xx xxxxxxxx, xx xx xxxx xxxxxxx xxxxxxxx. |
|
2. |
Na xxxxxx xxxx x xxxxxxxx xxxxxxxxxxx se xxxxxx xxxxx tyto xxxxxxxxx:
|
X. XXXXXX XXXXXXXXXX XXXXXXXXXXX KONTEJNERU
Pro xxxxxxxx xxxx být xxxxxxxx xxxxxx xxxxxxxx xx xxxxxxxxxxx xxxxxxxxxx, xx xxxxx xxxxxx xxxxxx xxx uvedeny xxxxxxx xxxx informace:
|
a) |
identifikace xxxxxxxxx xxxxxxxxx zařízení xxxxxx xxxxxx x xxxxxxxxxxx xxxxx; |
|
x) |
xxxxxxxxxxxx xxxxxx xxxxxxxxxx xxxxxxxxx xx xxxxxxx x xxxxxxx včetně xxxxxx x xxxxxxxxxxx xxxxx; |
|
x) |
xxxxxxxxxx, xx xxxxxx xxxxxxxx xxxxxx xxxxx/xxxxx x xxxxx „MANIPULOVAT XXXXXXX“; |
|
x) |
xxxxx xxxx xxx xxxxxxxxx xxxxxxxxxxxxx xxxxxxxx xxxx xxxxx, xxxx. xxxxxxx xxxxx, xxxxxx x xxxxxx, xxxx xx xxxxxxx xxxxx „XXXXXXXXXX“; |
|
x) |
xxxxxxxxxx přepravní xxxxxxxx (xxxx. xxxxxxxxx x xxxxxx, xx xxxxxx xxxxxx xxx.); |
|
x) |
bezpečnostní xxxxxx/xxxxxx xxxxxxxx (pokud xx xx možné). |
XXXXXXX XXX
XXXXXXXXXX XXXXXXXXX XXXXXXXXXXX XXXXXX
PŘÍLOHA XX
XXXXXXXXXX XXXXXXXXX XXXXXXXXXXX XXXXXX
PŘÍLOHA X
XXXXXXXX XXX XXXXXXX XXXXXXXX

XXXXXXX XX
Xxxxxxxxx x xxxxxxxxxx rozsahu xxxxx x dárci x xxxxxxxx, xxxxx xx xxxx xxxxxxx, jak xxxxxxxx článek 9
A. VE XXXXXXXXX XXXXXXXXXX
Xxxxxxxxxxxx xxxxx
Xxxxxxxxxxxx xxxxxxxx xxxxxxxxxx xxxxxxx:
|
— |
identifikaci xxxxxxxxxx provádějící odběr xxxx xxxxxxxxx xxxxxxxx, |
|
— |
xxxxxxxxx xxxxxxxxxxxxx číslo darování, |
|
— |
xxxxx xxxxxx, |
|
— |
xxxxx odběru. |
|
— |
druh darování (xxxx. jedna xxxx xx více xxxxx; xxxxxxxxx xx xxxxxxxx; xxxxxx xx xxxxxxx xxxxx) |
Xxxxxxxxxxxx xxxxxxxxx zahrnující xxxxxxx:
|
— |
xxxxxxxxxxxx tkáňového xxxxxxxx, |
|
— |
xxxx xxxxx x buňky/přípravku (xxxxxxxx xxxxxxxxxxxx), |
|
— |
xxxxx xxxxxxx (xx-xx xxxxxxxxxx), |
|
— |
xxxxx frakce (xx-xx xxxxxxxxxx), |
|
— |
datum ukončení xxxx použitelnosti, |
|
— |
stav xxxxx/xxxxx (xx. x xxxxxxxxx, xxxxxx k xxxxxxx xxx.), |
|
— |
xxxxx a xxxxx xxxxxxxxx, xxxxxxxxx xxxxx xxx xxxxxxxxxx, xxxxxxxxx x xxxxxxxxxx xxxxx, xxxxx xxxxxxxxxx do xxxxx s xxxxxxx x xxxxxxx a xxxx xxxx na xxxxxx jakost x/xxxx xxxxxxxxxx, |
|
— |
xxxxxxxxxxxx zařízení, které xxxxxx xxxxxxx xxxxxx. |
Xxxxxxxxxxxx xxxxxxx x xxxxxxx xxxxxxxxxxxx alespoň:
|
— |
xxxxx distribuce/likvidace, |
|
— |
identifikace xxxxxxxxxx lékaře x xxxxxxxxx uživatele/zařízení. |
B. V ORGANIZACÍCH XXXXXXXXXXX XX XXXXXXX X XXXXXXX
|
x) |
xxxxxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxx xxxxxxxx; |
|
b) |
xxxxxxxxxxxx klinického xxxxxx x konečného xxxxxxxxx/xxxxxxxx; |
|
x) |
xxxx tkání x xxxxx; |
|
x) |
xxxxxxxxxxxx xxxxxxxxx; |
|
x) |
xxxxxxxxxxxx xxxxxxxx; |
|
x) |
xxxxx xxxxxxx. |
XXXXXXX XXX
Informace xxxxxxxx x evropském kódovacím xxxxxxx
|
x) |
Xxxxxxxxxxxx darování:
|
|
x) |
Identifikace xxxxxxxxx:
|


