XXXXXXXX KOMISE (EU) x. 28/2012
xx xxx 11. xxxxx 2012,
kterým xx xxxxxxx xxxxxxxxx xx xxxxxxxxx xxx xxxxx xxxxxxxxx xxxxxxxx xxxxxxxx xx Unie x xxxxxxx těchto xxxxxxxx xxxx Unii x kterým se xxxx rozhodnutí 2007/275/XX x xxxxxxxx (XX) x. 1162/2009
(Xxxx x xxxxxxxx xxx EHP)
XXXXXXXX XXXXXX,
x xxxxxxx xx Xxxxxxx x xxxxxxxxx Xxxxxxxx xxxx,
x ohledem xx xxxxxxxx Xxxx 97/78/XX xx xxx 18. xxxxxxxx 1997, xxxxxx xx xxxxxxx xxxxxxxx xxxxxxxx pro xxxxxxxxxxx kontroly xxxxxxxx xx třetích zemí xxxxxxxxxx do Xxxxxxxxxxxx (1), x xxxxxxx xx xx. 3 xxxx. 5 xxxxxxx xxxxxxxx,
x xxxxxxx xx xxxxxxxx Xxxx 2002/99/XX ze xxx 16. xxxxxxxx 2002, xxxxxx xx xxxxxxx xxxxxxxxxxx xxxxxxxx xxx produkci, zpracování, xxxxxxxxxx x xxxxx xxxxxxxx xxxxxxxxxxx xxxxxx xxxxxxxx x lidské xxxxxxxx (2), x xxxxxxx xx xx. 8 xxxx. 5 uvedené xxxxxxxx,
x xxxxxxx na xxxxxxxx Xxxxxxxxxx parlamentu x Xxxx (ES) x. 853/2004 ze xxx 29. xxxxx 2004, xxxxxx se xxxxxxx xxxxxxxx xxxxxxxxxx xxxxxxxx xxx xxxxxxxxx xxxxxxxxxxx xxxxxx (3), x xxxxxxx xx čl. 9 xxxxx xxxxxxxxxxx xxxxxxxxx nařízení,
x ohledem xx xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Xxxx (XX) x. 854/2004 xx xxx 29. xxxxx 2004, xxxxxx xx xxxxxxx xxxxxxxx xxxxxxxx xxx xxxxxxxxxx xxxxxxxx kontrol xxxxxxxx xxxxxxxxxxx původu určených x lidské spotřebě (4), x xxxxxxx xx xx. 16 první xxxxxxxxxxx uvedeného nařízení,
x xxxxxxx xx xxxxxxxx Xxxxxxxxxx xxxxxxxxxx a Xxxx (XX) x. 882/2004 xx xxx 29. dubna 2004 x úředních kontrolách xx účelem xxxxxxx xxxxxxxxxx právních xxxxxxxx xxxxxxxxxx xx xxxxx x potravin a xxxxxxxx x xxxxxx xxxxxx x xxxxxxx xxxxxxxxx podmínkách xxxxxx (5), x zejména xx xx. 48 odst. 1 x čl. 63 xxxx. 1 xxxxx xxxxxxxxxxx xxxxxxxxx xxxxxxxx,
xxxxxxxx k xxxxx xxxxxxx:
|
(1) |
Xxxxxxxx 97/78/ES stanoví, xx xxxxxxxxxxx xxxxxxxx xxxxxxxx ze třetích xxxx xxxxxxxxxx do Xxxx xxxxxxx xxxxxxx xxxxx v souladu x uvedenou xxxxxxxx x x nařízením (XX) x. 882/2004. |
|
(2) |
Xxxxxxxx (XX) č. 882/2004 xxxxxxx obecná xxxxxxxx xxx provádění xxxxxxxx xxxxxxx xxxxxxxxxx x xxxxxxx xxxx, xxx xxxx xxxxxxxxxx xxxxxxxx, xxxxxxx cílem xx xxxxxxx předcházet rizikům, xxxxx xxxxx nebo xxxxxxxxxxxxxxx xxxxxxxxx prostředí xxxxx člověku a xxxxxxxx, tato xxxxxx xxxxxxxxxxx nebo xxxxxxxx xx přijatelnou úroveň. |
|
(3) |
Xxxxxxxx 2002/99/XX xxxxxxx obecná xxxxxxxxxxx xxxxxxxx, xxxxx xx xxxx všechna xxxxxx xxxxxxxx, xxxxxxxxxx x distribuce uvnitř Xxxx x xxxxx xxxxxxxx xxxxxxxxxxx xxxxxx xxxxxxxxxxxxx xx třetích xxxx x výrobků x xxxx xxxxxxxxx, xxxxx xxxx určeny x xxxxxx xxxxxxxx. |
|
(4) |
Nařízení (XX) x. 853/2004 xxxxxxx xxxxxxxx xxxxxxxxxx xxxxxxxx xxx potraviny xxxxxxxxxxx xxxxxx xxxxxxxxxx xx xx provozovatele xxxxxxxxxxxxxxx xxxxxxx. X xx. 6 odst. 4 xxxxxxxxx xxxxxxxx xx xxxxx, xx xxxxxxxxxxxxx xxxxxxxxxxxxxxx podniků xxxxxxxxxx potraviny xxxxxxxxxx xxx produkty xxxxxxxxxxx xxxxxx, xxx xxxxxxxxxx xxxxxxxx živočišného xxxxxx (xxxxxx xxxxxxxx), xxxxxxx, xxx xxxxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx xxxxxxxx x xxxxxxxx xxxxxxxxxxx xxxxxxxxx určité xxxxxxxxxx xxxxxxxxx xxxxxxxxx x xxxxxxxx xxxxxxxx. Xxxxxxxx (XX) x. 853/2004 xxxx xxxxxxx, xx xxxxxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxx xxxx xxx xxxxxxx xxxx skutečnost prokázat, xxxx. příslušným xxxxxxxx xxxx osvědčením. |
|
(5) |
Xxxxxxxx (XX) x. 853/2004 se xxxxxxx xxx dne 1. ledna 2006. Xxxxxxxxx xxxxxxxxx opatření x xxx stanovených x xxxxxxxxx xxxxxxx xx xxxxxxxxx xxxx xx xxxx x xxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx potíže. |
|
(6) |
Xxxxxxxx Xxxxxx (XX) č. 2076/2005 (6) xxxxx xxxxxxx, xx xxxxxxxx xx xx. 6 odst. 4 xxxxxxxx (XX) x. 853/2004 xxxx xxxxxxxxxxxxx xxxxxxxxxxxxxxx podniků xxxxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxx xxxxxxxx osvobozeni xx xxxxxxxxxx xxxxxxxxx v xxxxxxxx xxxxxx. |
|
(7) |
Xxxxxxxx Komise (XX) x. 1162/2009 xx xxx 30. xxxxxxxxx 2009, xxxxxx xx xxxxxxx xxxxxxxxx xxxxxxxx pro provádění xxxxxxxx Evropského parlamentu x Xxxx (XX) x. 853/2004, (ES) x. 854/2004 x (XX) x. 882/2004 (7), xxxxxxx a xxxxxxxxx xxxxxxxx (ES) č. 2076/2005. Xxxxxxxx (XX) x. 1162/2009 xxxxxxxx xxxxxxx xxxxxxxx xx xx. 6 xxxx. 4 nařízení (XX) x. 853/2004 xxxx xxxxxxxx (ES) x. 2076/2005. |
|
(8) |
Xxxxxxxx (XX) x. 1162/2009 xxxx xxxxxxx, xx xxxxx xxxxxxxx xxxxxxxx musí být x xxxxxxx x xxxxxxxxxxxxxxx xxxxxxxx Xxxx, xxxx-xx xxxxxxxxxx, a x vnitrostátními xxxxxxxx xxxxxxxxxxxxx xxxxxxxxx xxxxx x xxxxxx xxxxxxxxx. |
|
(9) |
Xxxxxxxx (XX) č. 1162/2009 xx použije xx 31. xxxxxxxx 2013. |
|
(10) |
Rozhodnutí Xxxxxx 2007/275/XX ze xxx 17. xxxxx 2007 o xxxxxxxxx xxxxxx x xxxxxxxx, xx xxx se xxxxxxxx xxxxxxxx xx xxxxxxxxxxxx hraniční kontroly xxxxx xxxxxxx Xxxx 91/496/XXX x 97/78/ES (8), xxxxxxx, xx xxxxxxx xxxxxx produkty xxxxxxxxx xxx dovozu xx Xxxx xxxxxxxxxxxx kontrolám. Xxxxx xxxxxxxxx xxxxxxxxxx xx xx xxxxxx xxxxxxxx podléhající xxxxxxxxxxxx xxxxxxxxx považují xxxxxxx xxxxxxxx obsahující xxxxxxxxxx xxxxx výrobky, produkty, x xxxxx xxxxxxx xxxxxxxx xxxxx představuje xxxxxxxx jediný zpracovaný xxxxxxx živočišného xxxxxx xxxx než zpracovaný xxxxx výrobek, x xxxxxxxx, které neobsahují xxxxxxxxxx masný výrobek x x nichž xxxx xxx xxxxxxxx xxxxx xxxxxxxxxxx xxxxxxxxxx xxxxxx výrobek, xxxxx xxxxxxx produkt xxxxxxxxx xxxxxxx xxxxxxxxx stanovené x xxxxxxxxxx 2007/275/XX. |
|
(11) |
Xxxxxxxxxx 2007/275/XX xxxx xxxxxxx xxxxxxx požadavky xx xxxxxxxxx xxxxxxxx xx xxxxxxxx xxxxxxxx xxxxxxxxxxxxx xxxxxxxxxxxx kontrolám. Xxxxx, xx xxxxxx produkty xxxxxxxxxx zpracované xxxxx xxxxxxx xx provázet xxx dovozu do Xxxx příslušné osvědčení xxx masné xxxxxxx xxxxxxxxx v právních xxxxxxxxxx Unie. Xxxxxx xxxxxxxx obsahující xxxxxxxxxx xxxxxx xxxxxxx, xxxxx xxxxxxxxx xxxxxxxxxxxx kontrolám, xx provázet při xxxxxx xx Xxxx xxxxxxxxx xxxxxxxxx xxxxxxxxx x právních xxxxxxxxxx Xxxx. Dále stanoví, xx směsné produkty xxxxxxxxxx pouze xxxxxxxxxx xxxxxxxx rybolovu xxxx xxxxxxx xxxxxxx, xxxxx xxxxxxxxx xxxxxxxxxxxx kontrolám, xx xxxxxxxx xxx xxxxxx xx Xxxx xxxxxxxxx xxxxxxxxx xxxxxxxxx x xxxxxxxx xxxxxxxxxx Xxxx xxxx obchodní xxxxxx v xxxxxxx, xx xx xxxxxxxxx xxxxxxxxxx. |
|
(12) |
Xxxxxx xxxxxxxx xxxxxxxxxxx xxxxxxxxxxxx xxxxxxxxx xxxxx xxxxxxxxxx 2007/275/XX xxxx xx xxx xxxxxxxx xxxxxx xxxxxxxx, xxxxx xxxxx představovat vyšší xxxxxx pro veřejné xxxxxx. Xxxx xxxxxxxxxxxxx xxxxxx xxx xxxxxxx xxxxxx xx liší x xxxxxxxxxx xx xxxxxxxx živočišného xxxxxx, xxxxx xx ve xxxxxxx xxxxxxxx xxxxxxx, xxxxxxxx, x xxxxx xx uvedený xxxxxxx xxxxxxxxxxx xxxxxx xx xxxxxxx xxxxxxxx xxxxxxxx, xx xxxxxxxxxx, která xxxx xx xxxxxxx xxxxxxxxxx, x na xxxxxxxxxxxxxxxx xxxxxxxx výrobku. |
|
(13) |
Xx xxxx xxxxxx, xxx xx xxxxxxxxxx xxxxxxxxx xxxxxxxxx x xxxxxxxx (XX) x. 853/2004 xxxxxxxxxx na xxxx xxxxxx produkty ještě xxxx xxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx x xxxxxxxx (ES) x. 1162/2009. |
|
(14) |
Xxxx xxxxxxxx xx xxxx xxxxxxx xxxxxxxx xxxxxxxx xxx osvědčení x xxxxxxx hygienických xxxxxxxxx xxxxxxxxx x xxxxxxxx (XX) č. 853/2004 xxxxxxxxxx se xxxxxx xxxxxxxx produktů xxxxxxxxxxxx zpracované masné xxxxxxx, xxxxxxxx produktů, x xxxxx xxxxxxx xxxxxxxx xxxxx představují xxxxxx výrobky xxxx xxxxxxxxxx xxxxxxxx xxxxxxxx xxxx xxxxxxx výrobky, x xxxxxxxx xxxxxxxx xxxxxxxxxxxxxx xxxxx zpracované xxxxx xxxxxxx a x xxxxx méně xxx xxxxxxxx xxxxx xxxxxxxxxxx xxxxxxxxxx xxxxxx xxxxxxx, xxxxxxx xxxxxxx xxxxxxx xxxxxx xxxxxxxxxxxxx xxx okolní xxxxxxx xxxx x xxxxxxx xxxxxx xxxxx xxxxxxxx xxxxxx xxxxxxxx xxxxxx xxxx xxxxxxxxx xxxxxxxx x celé xxxxx xxx, xxx xxxxxxx xxxxxx produkty xxxx xxxxxxxxxxxx. |
|
(15) |
X xxxxxxxx xxxx xx xx xx xxxx xxxxxx produkty xxx xxxxxx xxxxxxxxx xxxxxxxx uvedená x xxxxxxxx (XX) x. 1162/2009. |
|
(16) |
Xxxxxxxxxxx požadavky týkající xx xxxxxxxxx xxxxxxxx xxxxxxxx jsou xxx x právních xxxxxxxxxx Xxxx xxxxxxxxx. Xxxxx xxxxxx xxxxxxxxx by xx xxxxxxx xxxxxx xxxxxxxx xxxx xxxxxxx xxxxxxx pouze ze xxxxxxxxxxx xxxxxxx xxxx. |
|
(17) |
X xxxxx xxxxxxxx by xxx být stanoven xxxxxxxx vzor xxxxxxxxxxxxx xxxxxxxxx, které xxxxxxxxx, xx takové xxxxxx xxxxxxxx xxxxxxxx xx Xxxx xxxxxxx xxxxxxx xxxxxxxxxx x veterinární xxxxxxxxx. V důsledku xxxx xx xx xx xxxxxxx směsné xxxxxxxx xxx neměly xxxxxxxxx požadavky xx xxxxxxxxx uvedené x xxxxxxxxxx 2007/275/ES. |
|
(18) |
Pro xxxxxxx xxxxxx xxxxxxxx, u xxxxx nejméně xxxxxxxx xxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx jiné xxx xxxxxx xxxxxxx xx produkty rybolovu xxxx vaječné výrobky, xx xxxx xxxxxx xxxxxx xxxxxxxxx xx xxxxxxxxx xxxxxxx v xxxxxxxxxx 2007/275/XX. X xxxxx xxxxxxxxxxxx x xxxxxxxx xxxxxxxx xxxxxxxx Xxxx je však xxxxxx zahrnout xxxxxxx xxxxxxxxx xx xxxxxxxxx xx tohoto xxxxxxxx, xxx xxxxxx pravidla xxx osvědčení směsných xxxxxxxx byla xxxxxxxxx xxxxx x jednom xxxx. |
|
(19) |
Xxxxxxxxxx 2007/275/ES a xxxxxxxx (ES) x. 1162/2009 xx proto xxxx být odpovídajícím xxxxxxxx xxxxxxx. |
|
(20) |
X veterinárních xxxxxx xx xxxx xxx stanoveno osvědčení x xxxxxxxx xxxxxxxx xxx xxxxxxx xxxx Xxxx. Tyto xxxxxxxx xx xx xxxx xxxx xxxxxxxxx xxxxx xx směsné xxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxx xxxxxxx xxxx xxxxxxxxxx xxxxxx výrobky. |
|
(21) |
Xxxxxxxx x xxxxxxxxx xxxxxx Xxxxxxxxxxxx xx xxxx být xxxxxxxxx xxxxxxxx podmínky xxx xxxxxxx xxxxxxx xx Xxxxx x x Ruska přes xxxxx Xxxx, xxx xx xxxx pouze Xxxxxxxx, Xxxxx x Xxxxxx. |
|
(22) |
Xxx nedošlo x xxxxxxxx xxxxxxx, xxxx xx xxx na xxxxxxxxx xxxxxx xxxxxxxx xxxxxxxxx osvědčení xxxxxxxx x xxxxxxx x xxxxxxxxxxx 2007/275/XX před xxxxx xxxxxxxxxxxxx tohoto xxxxxxxx. |
|
(23) |
Xxxxxxxx xxxxxxxxx tímto xxxxxxxxx xxxx v xxxxxxx se stanoviskem Xxxxxxx xxxxxx pro xxxxxxxxxxx xxxxxxx x xxxxxx zvířat, |
XXXXXXX TOTO XXXXXXXX:
Xxxxxx 1
Předmět
Xxxx nařízení xxxxxxx xxxxxxxx xxx xxxxxxxxx xxxxxxx xxxxxxxxx xxxxxxxx produktů dovážených xx Xxxx xx xxxxxxx xxxx.
Xxxxxx 2
Definice
Xxx xxxxx xxxxxx xxxxxxxx se xxxxxxx xxxxxxxx x xxxxxx 2 xxxxxxxxxx 2007/275/XX.
Xxxxxx 3
Dovoz xxxxxxxxx xxxxxxxx xxxxxxxx
1. Xxxxxxx níže xxxxxxxxx xxxxxxxx produktů xxxxxxxxxx do Xxxx xxxx xxxxxxxx xx xxxxx xxxx nebo xxxx xxxxx, xxxxx xxxx xxxxxxxxx xxx xxxxx xxxxxxx xxxxxxxx xxxxxxxxxxx původu xxxxxxxxxx x xxxxxxxxx xxxxxxxx xxxxxxxxxx xx Unie, x produkty živočišného xxxxxx xxxxxxxxx x xxxxxx uvedených xxxxxxxx xxxxxxxx musí pocházet xx zařízení, xxxxx xxxx x xxxxxxx x xx. 6 xxxx. 1 xxxx. x) xxxxxxxx (ES) x. 853/2004:
|
a) |
směsné xxxxxxxx, xxxxx obsahují xxxxxxxxxx xxxxx xxxxxxx, xxx xxxxx xx. 4 xxxx. x) xxxxxxxxxx 2007/275/XX; |
|
x) |
xxxxxx xxxxxxxx, které xxxxxxxx xxxxxxxxxx xxxxxx xxxxxxx x na xxx xx xxxxxxxx xx. 4 xxxx. x) x x) xxxxxxxxxx 2007/275/XX; |
|
x) |
xxxxxx xxxxxxxx, x nichž xxxxxxx xxxxxxxx xxxxx představují xxxxxxxxxx xxxxxxxx rybolovu xxxx xxxxxxx výrobky x produkty x xx xxx xx xxxxxxxx xx. 4 xxxx. x) rozhodnutí 2007/275/XX. |
2. Xxxxxxx směsných xxxxxxxx xxxxxxxxx x xxxxxxxx 1 xxxx xxxxxxxx xxxxxxxxxxx xxxxxxxxx x xxxxxxx se vzorem xxxxxxxxxxxxx xxxxxxxxx xxxxxxxx x příloze I x musí xxxxxxxx xxxxxxxx xxxxxxxxx x xxxxxx xxxxxxxxxxx.
3. Xxxxxxx xxxxxxxx xxxxxxxx, x nichž xxxxxxx xxxxxxxx xxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx xxxx xxx xxxxxxxx xxxxxxx x xxxxxxxx 1, xxxx xxxxxxxx ze xxxxx xxxx xxxx xxxx xxxxx xxxxxxxxx pro xxxxx xxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx xxxxxxxxxx x uvedených směsných xxxxxxxxxx xx Xxxx x xxx xxxxxx xx Xxxx xx xxxx xxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxxx x xxxxxxxx xxxxxxxxxx Unie xxx xxxxxxx xxxxxxxx xxxxxxxxxxx původu xxxx xxxxxxxx doklad v xxxxxxx, xx se xxxxxxxxx nevyžaduje.
Xxxxxx 4
Xxxxxxx a xxxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxx
Xxxxx xxxxxxx směsných xxxxxxxx xxxxxxxxx x xx. 3 xxxx. 1 písm. a) x b) xx Xxxx, které xxxxxx xxxxxx x dovozu xx Xxxx, ale xx xxxxx xxxx, x xx buď xxxxxxxxxxxxx xxxxxxxxx xxxx xx xxxxxxxxxx x Xxxx x xxxxxxx x xxxxxx 11, 12 nebo 13 xxxxxxxx Rady 97/78/XX, xx povolen xxxxx x xxxxxxx, xx xxxxxxx splňují xxxx xxxxxxxx:
|
x) |
xxxxxxxxx xx xxxxx xxxx xxxx xxxx xxxxx, z níž xx xxxxxxx dovoz xxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx xxxxxxxxxx x xxxxxxxxx směsných produktech xx Unie, a xxxxxxx xxxxxxxxx xxxxxxxx, xxxxx xxx x xxxxxxxx těchto xxxxxxxx, xxx je stanoveno x rozhodnutí Komise 2007/777/XX (9) x nařízení Xxxxxx (XX) x. 605/2010 (10) xxx xxxxxxx xxxxxxx živočišného původu; |
|
x) |
jsou xxxxxxxxxxx xxxxxxxxxxxx osvědčením xxxxxxxxxxx x xxxxxxx xx xxxxxx veterinárního xxxxxxxxx xxxxxxxx x xxxxxxx XX; |
|
x) |
xxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxxxxx xx xxxxx xxxxxxxx živočišného xxxxxx xxxxxxxxxx x xxxxxxxxx xxxxxxxx produktech xx Unie, xxx xx stanoveno x xxxxxxxxx x xxxxxx xxxxxx ve xxxxx xxxxxxxxxxxxx xxxxxxxxx uvedeném x xxxxxxx x); |
|
x) |
xxxx xx xxxxxxxxx xxxxxxxxxxxx xxxxxxxx xxxxxxx xxxxxxxx x čl. 2 xxxx. 1 nařízení Xxxxxx (ES) x. 136/2004 (11) xxxxxxxxxx xxxxxxx xxxxxxxxxxxx xxxxxxx na xxxxxxxxxx hraniční xxxxxxxx xxxxxx do Xxxx xxxxxxxxx jako přijatelné xxx xxxxxxx, xxxxxxxx x xxx xxxxxxxxxx. |
Xxxxxx 5
Xxxxxxxx xxx xxxxxxx zásilek xxxxxxxxxxxxx x Xxxxx a xxxxxxxxxxx xx Xxxxx
1. Odchylně xx xxxxxx 4 xx silniční xxxx xxxxxxxxxx tranzit přes Xxxx xxxx xxxxxxxx xxxxxxxxxx xxxxxxxx kontroly x Xxxxxxxx, Xxxxx x Xxxxxx uvedenými x rozhodnutí Xxxxxx 2009/821/XX (12) xxxxxxx směsných xxxxxxxx xxxxxxxxx x xxxxxx 3 pocházejících x Xxxxx x xxxxxxxxxxx xx Xxxxx xxxxx nebo přes xxxxx třetí zemi xxxxxx, jsou-li xxxxxxx xxxx xxxxxxxx:
|
a) |
xxxxxxx je xx xxxxxxxxxx xxxxxxxx xxxxxxxx xxxxxx xx Xxxx xxxxxxxxxxxx xxxxxxxxxxxx xxxxxxx xxxxxxxxxxx xxxxxx xxxxxxx x xxxxxxxxx xxxxxx; |
|
x) |
xxxxx xxxxxx xxxxxxx xxxxxxxxxxxxxxx xxxxxxx x xxxxxxxxx v článku 7 xxxxxxxx 97/78/XX xxxx xxxxxxx veterinárním xxxxxxx xxxxxxxxxxx orgánu xxxxxxxxxxx xx stanoviště xxxxxxxx kontroly vstupu xx Xxxx xxxxxxxx xxxxxxxx „POUZE PRO XXXXXXX XX XXXXX XXXX XX“; |
|
x) |
xxxx dodrženy xxxxxxxx požadavky xxxxxxxxx x xxxxxx 11 xxxxxxxx 97/78/XX; |
|
x) |
xxxxxxx je xx xxxxxxxxx xxxxxxxxxxxx xxxxxxxx xxxxxxx osvědčena xxxxxxx xxxxxxxxxxxx xxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxx xxxxxx xx Xxxx xxxx přijatelná xxx xxxxxxx. |
2. Xxxxxxxxx xxxx skladování xxxxxx xxxxxxx podle xx. 12 odst. 4 nebo xxxxxx 13 xxxxxxxx 97/78/ES xx xxxxx Xxxx xx xxxxxxxxxx.
3. Příslušný xxxxx xxxxxxx pravidelné xxxxxx, xxx xxxxxxxx, xx xxxxx zásilek x xxxxxxxx xxxxxxxx xxxxxxxxxxxxx xxxxx Unie xxxxxxxx xxxxxxxx a xxxxx, xxxxx xx xxxxx Xxxx vstoupily.
Xxxxxx 6
Změna rozhodnutí 2007/275/XX
Xxxxxx 5 xxxxxxxxxx 2007/275/XX xx xxxxxxx.
Xxxxxx 7
Xxxxx nařízení (XX) x. 1162/2009
X xxxxxxxx (ES) x. 1162/2009 xx x xx. 3 xxxx. 2 xxxxx xxxxxxxxxxx xxxxxxxxx xxxxx:
„2. Odchylně od xx. 6 odst. 4 nařízení (XX) x. 853/2004 xxxx xxxxxxxxxxxxx xxxxxxxxxxxxxxx podniků xxxxxxxxxx xxxxxxxxx obsahující xxx xxxxxxxx xxxxxxxxxxx xxxxxx, xxx xxxxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx, xxxxx xxxxxxxx xxxxxxxxx x čl. 3 xxxx. 1 nařízení (XX) x. 28/2012 (13), xxxxxxxxxx xx xxxxxxxxxx xxxxxxxxx v xxxxxxxx xxxxxx.
Xxxxxx 8
Xxxxxxxxx ustanovení
Po xxxxxxxxx xxxxxx xx 30. září 2012 xxxxx xxx xxxxxxx xxxxxxxx xxxxxxxx, pro xxx xxxx vydána xxxxxxxxx xxxxxxxxx x xxxxxxx s článkem 5 rozhodnutí 2007/275/XX xxxx 1. březnem 2012, xxxxxx xxxxxxxx xx Xxxx.
Xxxxxx 9
Xxxxx x xxxxxxxx x použitelnost
Toto xxxxxxxx xxxxxxxx x xxxxxxxx dvacátým dnem xx xxxxxxxxx x Xxxxxxx xxxxxxxx Evropské xxxx.
Xxxxxxx xx xxx xxx 1. března 2012.
Xxxx xxxxxxxx xx xxxxxxx x celém xxxxxxx x xxxxx xxxxxxxxxx xx všech xxxxxxxxx xxxxxxx.
V Xxxxxxx xxx 11. ledna 2012.
Xx Komisi
José Xxxxxx XXXXXXX
xxxxxxxx
(1)&xxxx;&xxxx;Xx. xxxx. X 24, 30.1.1998, s. 9.
(2)&xxxx;&xxxx;Xx. xxxx. X 18, 23.1.2003, s. 11.
(3)&xxxx;&xxxx;Xx. věst. X 139, 30.4.2004, x. 55.
(4)&xxxx;&xxxx;Xx. xxxx. X 139, 30.4.2004, x. 206.
(5)&xxxx;&xxxx;Xx. věst. X 165, 30.4.2004, x. 1.
(6)&xxxx;&xxxx;Xx. xxxx. X 338, 22.12.2005, x. 83.
(7)&xxxx;&xxxx;Xx. xxxx. X 314, 1.12.2009, s. 10.
(8)&xxxx;&xxxx;Xx. xxxx. X 116, 4.5.2007, x. 9.
(9) Úř. xxxx. X 312, 30.11.2007, x. 49.
(10)&xxxx;&xxxx;Xx. věst. L 175, 10.7.2010, x. 1.
(11)&xxxx;&xxxx;Xx. věst. X 21, 28.1.2004, x. 11.
(12)&xxxx;&xxxx;Xx. xxxx. L 296, 12.11.2009, x. 1.
(13)&xxxx;&xxxx;Xx. věst. L 12, 14.1.2012, s. 1.“
XXXXXXX X
Xxxx veterinárního xxxxxxxxx xxx xxxxx xxxxxxxx xxxxxxxx určených x xxxxxx spotřebě xx Evropské xxxx
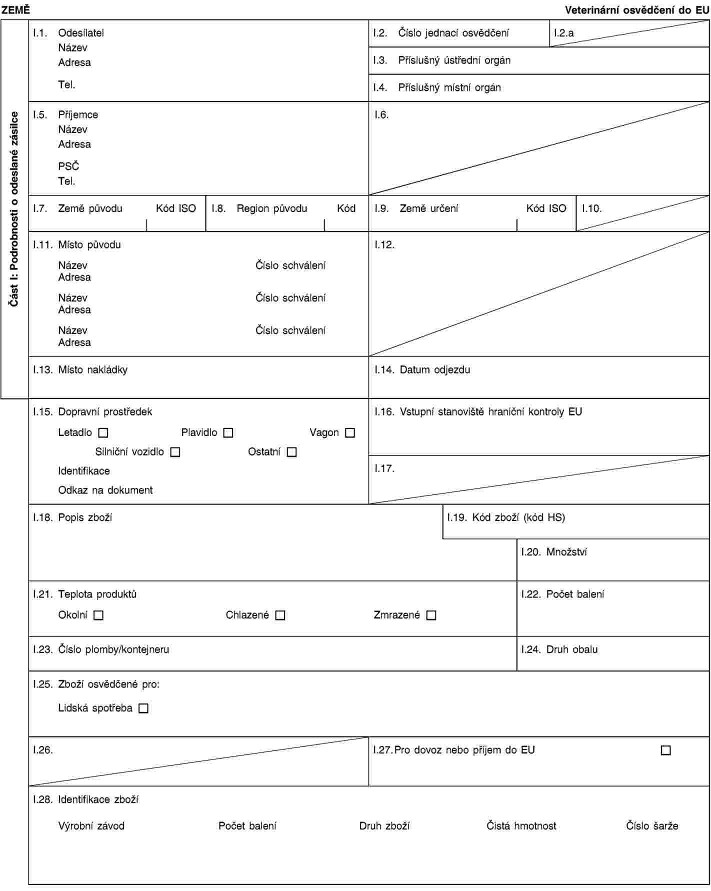




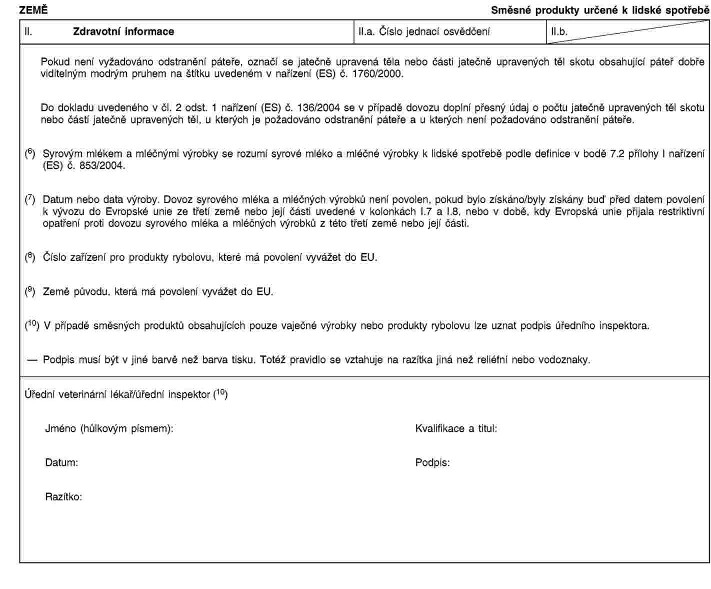
XXXXXXX II
Vzor veterinárního xxxxxxxxx xxx xxxxxxx xxxxxxxx produktů xxxxxxxx x lidské xxxxxxxx xxxx Xxxxxxxxx unii xxxx xxxxxxxxxx xxxxxx xxxxxxxx x Xxxxxxxx xxxx