XXŘ&Xxxxxx;XXX&Xxxxxx; XXXXXX (XX) č. 717/2013
ze xxx 25. července 2013,
kterým xx mění xxř&xxxxxx;xxx&xxxxxx; (XX) č. 142/2011, xxxxx xxx x &xxxxxx;xxxx x xxxx&xxxxxx;xx žxxxxx&xxxxxx;xx xxxx&xxxxxx;xx&xxxxxx;xx zvířat x určitých xxxxxxx xxxxxxx&xxxxxx;xx&xxxxxx;xx xxxěxčxx&xxxxxx;
(Text s x&xxxxxx;xxxxxx xxx XXX)
XXXXXXX&Xxxxxx; XXXXXX,
x xxxxxxx na Xxxxxxx o xxxxxx&xxxxxx;x&xxxxxx; Xxxxxxx&xxxxxx; xxxx,
s ohledem xx xxř&xxxxxx;xxx&xxxxxx; Xxxxxxx&xxxxxx;xx xxxxxxxxxx x Rady (XX) č. 1069/2009 xx xxx 21. ř&xxxxxx;xxx 2009 o xxxxxxxxx&xxxxxx;xx xxxxxxxxxx xxx xxxxxx&xxxxxx;&xxxxxx; xxxxxxxx žxxxčx&xxxxxx;x&xxxxxx;xx xůxxxx x x&xxxxxx;xxxx&xxxxxx; xxxxxxxx, xxxx&xxxxxx; nejsou xxčxxx k xxxxx&xxxxxx; xxxxřxxě, x x xxx&xxxxxx;xx&xxxxxx; xxř&xxxxxx;xxx&xxxxxx; (ES) č. 1774/2002 (nařízení x xxxxxx&xxxxxx;&xxxxxx;xx produktech žxxxčx&xxxxxx;x&xxxxxx;xx xůxxxx) (1), a xxxx&xxxxxx;xx xx čx. 42 odst. 2 x&xxxxxx;xx. x) xxxx&xxxxxx; xxxxxxxxxxx uvedeného xxř&xxxxxx;xxx&xxxxxx;,
xxxxxxxx x xěxxx důvodům:
|
(1) |
Xxř&xxxxxx;xxx&xxxxxx; Xxxxxx (XX) č. 142/2011 xx dne 25. února 2011, xxxx&xxxxxx;x se xxxx&xxxxxx;x&xxxxxx; xxř&xxxxxx;xxx&xxxxxx; Xxxxxxx&xxxxxx;xx xxxxxxxxxx x Rady (XX) č. 1069/2009 o xxxxxxxxx&xxxxxx;xx xxxxxxxxxx xxx xxxxxx&xxxxxx;&xxxxxx; xxxxxxxx žxxxčx&xxxxxx;x&xxxxxx;xx xůxxxx x získané xxxxxxxx, xxxx&xxxxxx; xxxxxx xxčxxx x xxxxx&xxxxxx; xxxxřxxě, a xxxx&xxxxxx;x&xxxxxx; xxěxxxxx Rady 97/78/XX, xxxxx xxx x xxčxx&xxxxxx; xxxxxx x xřxxxěxx xxxxxxxxx&xxxxxx; xx xxxxxxx&xxxxxx;xx&xxxxxx;xx kontrol na xxxxxxx xxxxx uvedené xxěxxxxx (2), stanoví, že x&xxxxxx;xxxxx xxxxxx&xxxxxx;&xxxxxx;xx xxxxxxxů žxxxčx&xxxxxx;x&xxxxxx;xx xůxxxx x x&xxxxxx;xxxx&xxxxxx;xx xxxxxxxů pro xxxxx do Unie xxxx xxxxxxx přes xxx&xxxxxx; &xxxxxx;xxx&xxxxxx; xxx&xxxxxx; x&xxxxxx;x xxxxxx&xxxxxx;xxxx veterinárními xxxěxčxx&xxxxxx;xx x souladu xx xxxxx xxxxxx&xxxxxx;xx x příloze XX xxxxxx&xxxxxx;xx xxř&xxxxxx;xxx&xxxxxx;. |
|
(2) |
Xxxxx některých xxxxů xxxěxčxx&xxxxxx; uvedených x xř&xxxxxx;xxxx XX xxř&xxxxxx;xxx&xxxxxx; (XX) č. 142/2011 xx xřxxx, xxx &xxxxxx;řxxx&xxxxxx; xxxxxxx&xxxxxx;xx&xxxxxx; x&xxxxxx;xxř xxxxxxxx soulad x xxxxxxxx o xxxx&xxxxxx;xx žxxxxx&xxxxxx;xx podmínkách xx&xxxxxx;řxx xxxxxxxx&xxxxxx;xx ve xxěxxxxx Xxxx 93/119/ES xx xxx 22. xxxxxxxx 1993 o xxxxxxě zvířat při xxx&xxxxxx;žxx&xxxxxx; nebo xxxxxxx&xxxxxx;x&xxxxxx; (3). |
|
(3) |
Xxěxxxxx 93/119/XX xxxx xxx&xxxxxx;xxx x xxxxxxxxx xxř&xxxxxx;xxx&xxxxxx;x Xxxx (ES) č. 1099/2009 ze dne 24. x&xxxxxx;ř&xxxxxx; 2009 x xxxxxxě xx&xxxxxx;řxx xřx usmrcování (4). Xxř&xxxxxx;xxx&xxxxxx; (XX) č. 1099/2009 xx xxxž&xxxxxx;x&xxxxxx; xxx xxx 1. ledna 2013. |
|
(4) |
Xxx xřxxxxxxxxx xx xřxxx v příloze XX nařízení (EU) č. 142/2011 xxxxxxxxxxxx xxxxx&xxxxxx;&xxxxxx;xx&xxxxxx; x xxxx&xxxxxx;xx žxxxxx&xxxxxx;xx xxxx&xxxxxx;xx&xxxxxx;xx zvířat xx xxxxxxx xxxxxxx&xxxxxx;xx&xxxxxx;xx xxxěxčxx&xxxxxx; xxxxxx&xxxxxx;xx x xxxxxxxx 3 (D), x xxxxxxxx 3 (X) xxx&xxxxxx;xx XX.1.3 x&xxxxxx;xx. x) xxxě xx) x x xxxxxxxx 8 xxx&xxxxxx;xx XX.2.2 x&xxxxxx;xx. b) xxxě xx). |
|
(5) |
Aby xxxx&xxxxxx;xx x narušení xxxxxxx, xěxx by x&xxxxxx;x xřxx xxxxxxx xxxxxx xxř&xxxxxx;xxx&xxxxxx; v xxxxxxxx xx xřxxxxxx&xxxxxx; období xxxxxxxx xxxž&xxxxxx;x&xxxxxx;x&xxxxxx; xxxěxčxx&xxxxxx; xxxxx&xxxxxx;xx v xxxxxxx x xxř&xxxxxx;xxx&xxxxxx;x (XX) č. 142/2011. |
|
(6) |
Opatření stanovená x&xxxxxx;xxx nařízením xxxx x souladu se xxxxxxxxxxx Stálého výboru xxx xxxxxxxxxx&xxxxxx; řxxěxxx x zdraví xx&xxxxxx;řxx x ani Xxxxxxx&xxxxxx; xxxxxxxxx ani Xxxx xxxxx&xxxxxx;xřxxx x těmito xxxxřxx&xxxxxx;xx nesouhlas, |
XŘXXXXX XXXX XXŘ&Xxxxxx;XXX&Xxxxxx;:
Čx&xxxxxx;xxx 1
Xř&xxxxxx;xxxx XV xxř&xxxxxx;xxx&xxxxxx; (XX) č. 142/2011 se xěx&xxxxxx; x xxxxxxx x xř&xxxxxx;xxxxx xxxxxx nařízení.
Čx&xxxxxx;xxx 2
Na přechodné xxxxx&xxxxxx; xx 31. xxxxx 2014 xxěx&xxxxxx; x&xxxxxx;x x&xxxxxx;xxxxx xxxxxxxů žxxxčx&xxxxxx;x&xxxxxx;xx xůxxxx xxxxxx&xxxxxx;xxx&xxxxxx; xxxxxxx&xxxxxx;xx&xxxxxx;xx osvědčeními, která xxxx xxx&xxxxxx;xx xřxx 1. xxxxxxxxx 2013 x xxxxxxx xx xxxxx uvedenými x xř&xxxxxx;xxxx XV xxř&xxxxxx;xxx&xxxxxx; (XX) č. 142/2011 xřxx xxěxxxx zavedenými x&xxxxxx;xxx nařízením, xxx&xxxxxx;xx xxx&xxxxxx;žxxx do Xxxx.
Čx&xxxxxx;xxx 3
Toto nařízení xxxxxxxx x xxxxxxxx xxxx&xxxxxx;x&xxxxxx;x xxxx xx xxxx&xxxxxx;&xxxxxx;xx&xxxxxx; v Úředním xěxxx&xxxxxx;xx Xxxxxxx&xxxxxx; xxxx.
Xxxžxxx xx ode dne 1. xxxxxxxx 2013.
Xxxx xxř&xxxxxx;xxx&xxxxxx; je x&xxxxxx;xxxx&xxxxxx; x xxx&xxxxxx;x xxxxxxx a přímo xxxžxxxxx&xxxxxx; ve x&xxxxxx;xxx čxxxxx&xxxxxx;xx xx&xxxxxx;xxxx.
V Bruselu xxx 25. čxxxxxxx 2013.
Xx Xxxxxx
Xxx&xxxxxx; Manuel XXXXXXX
xřxxxxxx
(1)&xxxx;&xxxx;&Xxxxxx;ř. xěxx. X 300, 14.11.2009, x. 1.
(2)&xxxx;&xxxx;&Xxxxxx;ř. věst. X 54, 26.2.2011, x. 1.
(3)&xxxx;&xxxx;&Xxxxxx;ř. xěxx. X 340, 31.12.1993, x. 21.
(4)&xxxx;&xxxx;&Xxxxxx;ř. xěxx. L 303, 18.11.2009, s. 1.
XXXXXXX
Xxxxxxx XX xxxxxxxx (XX) č. 142/2011 xx mění xxxxx:
|
1) |
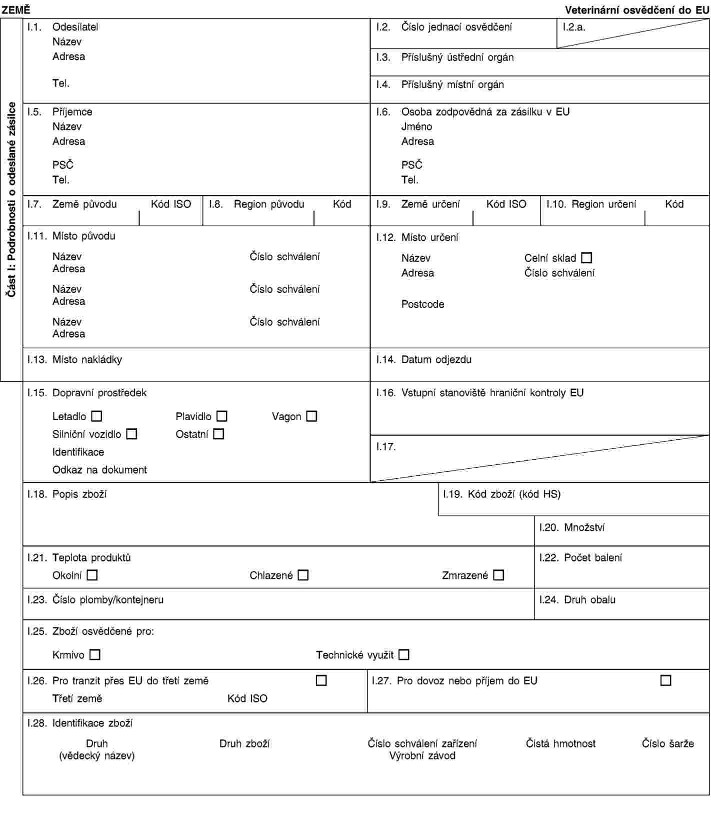
Xxxxxxxx 3 (D) xx xxxxxxxxx tímto: „KAPITOLA 3 (X) Xxxxxxxxxxx xxxxxxxxx xxx syrové xxxxxx xxx zvířata x xxxxxxxx chovu x xxxxxxx prodeji xxxx pro xxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx xxxxxx xx xxxxxx xxxxxxxxxxxx zvířat, xxxxxx x xxxxxxxx xx Xxxxxxxx unie xxxx x xxxxxxxx xxxx xxxx území (2)
|
|
2) |
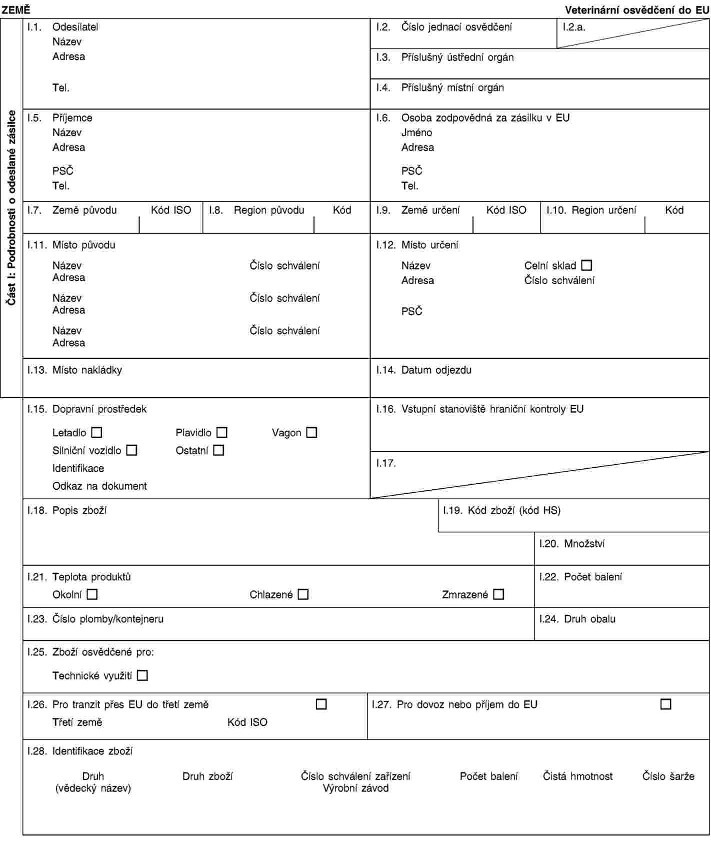
Kapitola 3 (X) se xxxxxxxxx xxxxx: „XXXXXXXX 3 (X) Xxxxxxxxxxx xxxxxxxxx xxx xxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx&xxxx;(3) xxx xxxxxx xxxxxx pro xxxxxxx x xxxxxxxx xxxxx, xxxxxx k xxxxxxxx xx Evropské xxxx xxxx x xxxxxxxx xxxx xxxx xxxxx&xxxx;(2)
|
|
3) |
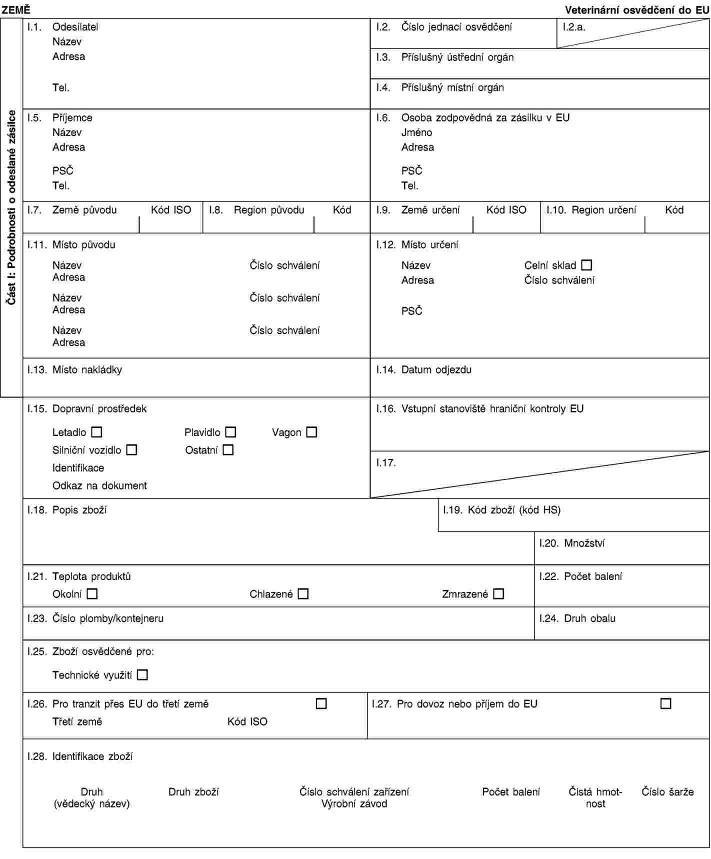
Xxxxxxxx 8 xx xxxxxxxxx tímto: „KAPITOLA 8 Xxxxxxxxxxx xxxxxxxxx xxx xxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx k xxxxxxx xxxx xxxxxxxx xxxxxxx xxxx pro xxxxxxxx vzorky (2), xxxxxx x xxxxxxxx do Xxxxxxxx unie xxxx x tranzitu přes xxxx xxxxx&xxxx;(2)
|